きのこを生体センサーとして用いたきのこ栽培方法
【課題】形態形成の最適移行段階が的確に分かり、良質なきのこが得られるきのこ栽培方法を提供するものである。
【解決手段】きのこに環境刺激を与えた際のきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとに、きのこを栽培することを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【解決手段】きのこに環境刺激を与えた際のきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとに、きのこを栽培することを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、きのこを生体センサーとして用いたきのこ栽培方法に関するものである。
【0002】
従来、きのこの人工栽培方法として、菌床栽培や原木栽培が一般的に採用されている。
【0003】
例えば、マイタケの菌床栽培の場合、オガ粉に米糠等の栄養分を加えた菌床(培地)を殺菌・冷却し、この菌床に種菌を接種し、菌床中に菌糸を蔓延させ、菌糸が蔓延した菌床にマイタケ子実体原基を形成させ、このマイタケ子実体原基からマイタケ子実体を発生・生長させて収穫が行われている。
【0004】
また、このマイタケの人工栽培方法においては、種菌接種から子実体収穫に亙るマイタケの外観変化の観察及び培養日数を指標とする経験的な管理が行われている。
【0005】
ところで、菌糸が蔓延した菌床からの子実体原基の形成や、子実体原基からの子実体の発生・成長等、所謂マイタケの形態形成を良好に進める為には、例えば、菌糸が蔓延した菌床から子実体原基を形成させる場合、適正な時期に光や温度等の適宜な環境刺激を与える必要がある。即ち、菌糸が蔓延した菌床から子実体原基を形成させる場合においては、菌糸(菌体)内に十分に栄養分が貯蔵された時点が上記適正な時期(次の子実体原基形成への最適移行段階)であるといわれ、この最適移行段階にある菌床に光や温度等の適宜な環境刺激を与えると、その後の子実体原基形成が良好に行われ、最終的に形状・大きさが良好な子実体が得られる。
【発明の開示】
【発明が解決しようとする課題】
【0006】
しかしながら、栽培するマイタケが上述した最適移行段階にあるか否かを見極めることは厄介であり、よって栽培マイタケに適切なタイミングで環境刺激を与えることは困難である。
【0007】
何故なら、従来のような外観変化の観察及び培養日数を指標とする経験的な管理手法では、マイタケに外観の変化が認められたときには多くの場合、内生的変化は既に終了した後であると考えられ、最適移行段階にあるマイタケを見極めるのは非常に難しいからである。
【0008】
また、上述した外観変化の観察は目視によって行われることから観察者による差が大きく、最適移行段階にあるか否かを観察者(栽培者)の資質に依存しなければならず、客観的に最適移行段階にあるか否かを見極めることはこの点からも困難である。
【0009】
従って、従来のマイタケの人工栽培方法においては、前記最適移行段階となった状態を適切に見極め、適切なタイミングで環境刺激を与えることは難しく、よって、現実には観察者の所謂勘により環境刺激を与えざるをえないのが現状である。
【0010】
また、実際、マイタケ栽培は同時に多数の子実体形成を行うため、前記最適移行段階の菌体が多い菌床が多数を占めた生産ロットでは、全体として、収穫の初めから終わりまでの日数も短く、収量や品質も良好となるのに対し、前記最適移行段階の菌体が多い菌床が少数であった生産ロットでは、逆に、全体として収穫の初めから終わりまでの日数が長く、収量や品質も悪くなり、生産ロット毎の生産性が不均一となるという問題もある。
【0011】
本発明者らは、形態形成における最適移行段階に至ったきのこを見極め、最も最適なタイミングできのこの形態形成に必要な環境刺激を与えるには、きのこ(菌糸、子実体原基若しくは子実体)内部の変化をいち早く察知することが必要であるという知見に基づき、鋭意研究を重ねた結果、(1)きのこに環境刺激を与えると、きのこに内在する生体電位が変化すること、(2)最適移行段階に至ったきのこと最適移行段階に至っていないきのことは、環境刺激を与えた場合の生体電位の変化が異なり、きのこに環境刺激を与えた際に有意な生体電位の上昇が認められる場合にはきのこの形態形成が良好になる傾向があることから、環境刺激に対する生体電位に有意な上昇が認められる場合にはきのこは最適移行段階に至ったものと考えられ、よって、この場合に環境刺激を与えれば良いこと、の2つを見出し、この事実を利用し、良好なきのこを効率的に栽培する方法を完成させたものである。
【課題を解決するための手段】
【0012】
添付図面を参照して本発明の要旨を説明する。
【0013】
きのこに環境刺激を与えた際のきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとに、きのこを栽培することを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0014】
また、請求項1記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記確知した生体電位の変化をもとに、きのこに環境刺激を与えるか若しくは与えないかを決定して当該きのこを栽培することを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0015】
また、請求項1,2いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記確知する生体電位の変化とは、所定時間におけるきのこの生体電位の傾きであり、この傾きが正ならば前記きのこに環境刺激を与え、負ならば前記きのこに環境刺激を与えないようにすることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0016】
また、請求項3記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記傾きが正である場合、予め設定された上限値以上となるまでは環境刺激を与えず、上限値以上となったら環境刺激を与え、また、前記傾きが負である場合、予め設定された下限値以下になるまでは環境刺激を与え、下限値以下となったら環境刺激を与えないようにすることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0017】
また、請求項1〜4いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激は環境刺激付与装置3により与え、前記生体電位の変化の確知は生体電位計測装置2により行うことを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0018】
また、請求項5記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記生体電位計測装置2は、生体電位を計測する電極部2A及び該電極部2Aにより計測された生体電位を増幅する増幅部2Bを具備するものであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0019】
また、請求項1〜6いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、複数個のきのこを栽培する場合、当該栽培する一部のきのこの生体電位の変化の確知を行うことを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0020】
また、請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置3は、きのこに光を照射する光照射装置3aであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0021】
また、請求項8記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記光は、所定の光質であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0022】
また、請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置3は、きのこを所定の温度に調整する温度制御装置3bであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0023】
また、請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置3は、きのこに所定の湿気を加える加湿装置3cであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0024】
また、請求項1〜7記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置3は、栽培雰囲気中の気体濃度を調整する気体濃度制御装置3dであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【発明の効果】
【0025】
本発明は、きのこに環境刺激を与えた際のきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとに、きのこを栽培するから、形態形成の最適移行段階が的確に分かり、良質なきのこが得られることになる。
【発明を実施するための最良の形態】
【0026】
好適と考える本発明の実施形態を、図面に基づいて本発明の作用を示して簡単に説明する。
【0027】
きのこの栽培に際し、きのこに環境刺激を与え、この環境刺激に対するきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとにきのこを栽培する。
【0028】
本発明におけるきのことは、例えばきのこ栽培工場等、人為的に環境の制御が可能な施設内で栽培されるきのこであり、菌床栽培(袋や瓶を容器とするものも含む)、原木栽培のきのこである。
【0029】
また、本発明におけるきのこの生体電位とは、きのこの細胞膜の内部イオンの濃度差により発生する微小電位(数mV)を指している。
【0030】
また、本発明において生体電位を測定する対象は、子実体,子実体原基若しくは原木や菌床9に蔓延する菌糸である。
【0031】
また、本発明における生体電位計測装置2とは、生体電位を計測する電極部2Aと、この電極部2Aで計測された生体電位を増幅する増幅部2Bとを具備したもので、前記電極部2Aは、正極2a、負極2b及び不関電極2cによりなる構成とし、この正極2a、負極2b及び不関電極2cを夫々前記きのこに挿入して当該きのこの生体電位を計測し、当該きのこの生体電位の変化を確知する。
【0032】
菌糸が蔓延した菌床9から子実体原基の形成や、子実体原基からの子実体の発生・成長等、所謂きのこの形態形成を良好に進める為には、例えば、菌糸が蔓延した菌床9から良好な子実体原基を形成させる為には、適正な時期に光(光を全く与えないという環境刺激も含む。)、温度、湿度、二酸化炭素濃度等、きのこの種類に応じて適宜な環境刺激を与える必要がある。
【0033】
即ち、菌糸が蔓延した菌床9から子実体原基を形成させる場合においては、菌糸(菌体)内に十分に栄養分が貯蔵された時点が適正な時期(次の子実体原基形成への最適移行段階)であるといわれ、この最適移行段階にある菌糸に光、温度、湿度、二酸化炭素濃度等、きのこの種類に応じた適宜な環境刺激を与えると、その後の子実体原基の形成が良好に行われ、最終的に形状・大きさが良好な子実体が得られる。
【0034】
また、本発明者らは、(1)きのこに環境刺激を与えると、きのこに内在する生体電位が変化すること、(2)最適移行段階に至ったきのこと最適移行段階に至っていないきのことは、環境刺激を与えた場合の生体電位の変化が異なり、きのこに環境刺激を与えた際に有意な生体電位の上昇が認められる場合にはきのこの形態形成が良好になる傾向があることから、環境刺激に対する生体電位に有意な上昇が認められる場合にはきのこは最適移行段階に至ったものと考えられ、よって、この場合に環境刺激を与えれば良いこと、の2つを見出し、環境刺激を与えたきのこの所定時間における生体電位の傾きを求め、この傾きが正の所定の傾きならばきのこに環境刺激を与え、負の所定の傾きならばきのこに環境刺激を与えないようにすることで、きのこの形態形成が良好に行われることを確認した。
【0035】
更に、本発明者らは、栽培対象のきのこに光、温度、湿度、二酸化炭素濃度等の環境刺激を与え、このきのこの生体電位の変化を確知した際に、この確知した生体電位の変化(傾き)が予め設定された上限値以上となるまでは環境刺激を与えず、上限値以上となったら環境刺激を与え、下限値以下になるまでこの状態を維持し、下限値以下となったら環境刺激を与えないようにし、その後、上限値以上となるまではこの状態を維持するというように環境刺激を与えること、与えないことを繰り返すと、よりきのこの形態形成が良好に行われることを確認した。
【0036】
従って、本発明は、きのこに環境刺激を与えた際のきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとに、きのこを栽培するから、形態形成の最適移行段階が的確に分かり、良質なきのこが得られることになる。
【実施例】
【0037】
本発明の具体的な実施例について図面に基づいて説明する。
【0038】
本実施例は、マイタケを生体センサーとして用いたマイタケ栽培方法であり、人為的な環境刺激を付与し得る栽培室4内に複数個のマイタケを配置し、この複数個のマイタケのなかの一つを生体センサーに設定し、この生体センサーに設定したマイタケの前記環境刺激に対する生体電位の変化を確知し、この確知した生体電位の変化をもとに、前記複数個のマイタケに環境刺激を与え続けるか若しくは中止するかを決定してマイタケを複数個同時に栽培する場合である。
【0039】
尚、生体電位の変化を確知した後、一旦環境刺激の付与を停止し、その後、この確知した生体電位の変化をもとに環境刺激を与えるか若しくは与えないかを決定する場合も含まれる。
【0040】
マイタケは、図1に図示したとおり、栽培室4内に複数個配置される。
【0041】
前記栽培室4の外部であって環境ブース10内に生体電位計測装置2が配設される。
【0042】
本実施例は、前記簡易環境ブース10内に生体電位計測装置2を設置することで、外部からの干渉を防止して正確な生体電位の計測が可能となる。
【0043】
前記生体電位計測装置2は、増幅器2Bに電極部2Aが接続された構成としている。
【0044】
前記電極部2Aは、前記栽培室4内の複数個のマイタケのなかの生体センサーに設定されたマイタケに挿入される。
【0045】
前記電極部2Aは、正極2a、負極2b及び不関電極2cより構成され、本実施例の場合、前記正極2a、負極2b及び不関電極2cとして、表面に塩化銀膜を生成した約φ0.5mmの銀針電極部2Aを採用することで、分極を防ぎながら生体電位を測定することができる。
【0046】
前記増幅器2Bは、その出力端が、前記簡易環境ブース10の外部に配設されたコンピュータ5とペンレコーダー8に接続される構成としている。
【0047】
従って、本実施例は、前記増幅器2Bにより増幅され出力された生体電位の測定値がこのコンピュータ5及びペンレコーダー8により連続的に記録される。
【0048】
前記コンピュータ5は、前記記録された生体電位の変化、即ち、所定時間の生体電位の変化(傾き)を演算して分析する構成としている。
【0049】
前記環境刺激は、本実施例の場合、光(後述の所定の光質が望ましい。)を付与し得る光照射装置3aを採用する。
【0050】
本実施例の場合、前記光照射装置3aを栽培室4の上部に付設し、マイタケの上部に光が当たるようにしている。尚、前記光照射装置3aの配設位置は、本実施例以外にも適宜設定することができるが、本実施例のように光照射装置3aをマイタケの上部に付設することで、マイタケの菌傘に効率良く光が照射されてマイタケの生体電位の確知や形態形成が良好となる。
【0051】
また、前記栽培室4内には、温度センサー6及び湿度センサー7を設置し、この温度センサー6及び湿度センサー7の出力端子を前記コンピュータ5及びペンレコーダー8に接続し、栽培室4内の温度と湿度とを連続的に記録する構成としている。
【0052】
本実施例の場合、光以外の環境刺激を一定とするため、前記コンピュータ5に予め所定の温度及び湿度を設定しておき、前記栽培室4内の温度センサー6及び湿度センサー7により測定された温度及び湿度が前記設定と異なる場合に、前記コンピュータ5がペルチェ素子3b、超音波加湿器3cを制御してこの栽培室4内の温度と湿度とを略一定状態に調整する構成としている。
【0053】
尚、前記ペルチェ素子3bは電流の制御だけで急速な冷却・加熱ができるため好ましいが、ペルチェ素子3b以外にも適宜な加熱・冷却手段を採用することができる。また、超音波加湿器3c以外にも適宜な加湿手段を採用することができる。
【0054】
更に、本実施例の場合は、前記栽培室4内の酸素、二酸化炭素等の気体濃度を制御する気体濃度制御装置3dを設けた構成としている。
【0055】
具体的には、前記気体濃度制御装置3dとしてエアバッファ3dを採用し、前記栽培室4内の気体濃度組成が等しくなるように、栽培室4内外の空気を一旦エアバッファ3d内に集め、ACファンによりダクトを通して栽培室4内に空気を送り込む構成としている。
【0056】
尚、前記エアバッファ3d内の温度および湿度、酸素濃度、二酸化炭素濃度及び気圧については、前記コンピュータ5にて常時記録する構成としている。
【0057】
以下に本実施例のマイタケを生体センサーとして用いたマイタケ栽培方法について詳しく説明する。
【0058】
本実施例では、以下の工程(1)〜(4)を経て、マイタケの子実体原基が形成されて5日ほど経過した菌床9を、前記栽培室4内に配置する(図1参照)。
【0059】
(1)培地調整及び殺菌
コーンコブ,米糠,広葉樹オガコ等の培地基材,添加物を容積比10:2程度の割合で加水しながら混合し、適当な水分率(65%程度)に調整する。これを一定量ずつ通気用の除菌フィルターのついたポリプロピレン製の耐熱性袋または800〜850ccの栽培瓶に充填する。下方に直径2cm程度の穴を開けて蓋をし、121℃で一定時間高圧殺菌する。
【0060】
(2)種菌接種
殺菌終了後、一昼夜冷却し、培地の温度が20℃以下になってから培養基にマイタケ(Grifola frondosa(Dicks.Fr).S.F.Gray)の種菌を適当量接種する。この際、子実体原基の形成方法が子実体の形成に影響をおよぼす。そのため、子実体原基を形成させる空間を確保する必要がある。空間は通気孔を中心に上面の4分の1程度、高さ5cm程度とする。袋の口を3〜4回折り返し,その両端を合わせてホチキスや輪ゴムなどで止めるのが一般的である。
【0061】
(3)菌糸培養
接種後の培地は湿度60〜70%、温度20〜30℃、暗黒の培養室で培養する。培養時、呼吸による二酸化炭素放出のため換気を行う。
【0062】
(4)子実体原基形成
マイタケは菌糸の生育温度と子実体原基の形成温度が重なっているため「芽出し」までは培養室で行われる。子実体原基が十分に盛り上がり、濃灰色に変色し、その表面が波上に盛り上がるのを確認してから、栽培室4へ移動する。その後、2〜3日して子実体原基が黒色となり水滴が目立たなくなってから、子実体が生育する部分のみ袋をカットする。カットの方法はカッターで5cmほどの十文字に切ったり、通気孔部分を取り外したりする。
【0063】
次に、本実施例は、栽培室4へ移動した前記複数個のうち、生体センサーに設定した子実体原基に、前記生体電位計測装置2の前記電極部2Aを挿入する。
【0064】
具体的には、前記子実体原基に挿入した前記正極2aの約10mm下に負極2bを、子実体原基と菌床9との境界に不関電極2cをそれぞれ深さ約10mmとなる程度に挿入する(尚、図2は子実体原基が子実体に生長した写真である)。
【0065】
尚、本実施例の場合、前記生体電位計測装置2の前記増幅器2Bとして差動型生体電位アンプ(CMMR:約120dB以上、S/N比:約80dB)を使用し、増幅率を50倍に設定する。
【0066】
即ち、前記増幅率は、マイタケの生体電位の変化が概ね40mV〜60mVであることから、サチュレーションを起こさないと考えられる50倍に設定する。更に、前記増幅器2Bの出力バイアス電圧は±0Vとする。
【0067】
次に、栽培室4内のマイタケに対して光照射装置3aによる光刺激の付与を行う。
【0068】
本実施例の場合、前記光照射装置3aとして、発光ダイオードを採用する。
【0069】
具体的には、前記発光ダイオードとして、超高輝度型青色発光ダイオード(中心発光波長470nm、放射束密度6W/m2)を採用し、この青色発光ダイオードを複数個取り付けたパネルを栽培室4の上部に配置する。
【0070】
即ち、本発明者らがこれまでマイタケを生体センサーとしてマイタケの生体電位の変化における光質依存性の検討を行ったところ、波長については、マイタケは青色領域(430〜470nm)付近で生体電位の変化が大きく、緑・黄色領域では徐々に小さくなり、赤色領域ではほぼ変化を示さない結果を得ている(後述する実験例2及び図6参照)。
【0071】
尚、図7に示すように、青色光と赤色光で栽培したマイタケを比較すると、青色光のマイタケの方が形態形成が良好であり、色も濃く、菌傘の広がりが大きいことを確認している。
【0072】
また、光質依存性の検討として更に、波長が青色領域の光の強さ(放射束密度)についても検討を行ったところ、子実体の生体電位応答は光の強度(光量子束密度)に比例することを確認している(後述する実験例3及び図8参照)。
【0073】
尚、2W/m2の青色光と6W/m2の青色光で生育したマイタケを比較すると、6W/m2の青色光で生育したマイタケの方が形態形成が良好であり、色も濃く、菌傘の広がりが大きいことを確認している。
【0074】
この理由は、照射する青色光の光強度が強いとマイタケが有するフラボノイド等の青色領域に特異的な光屈折作用を有する色素の活性が増し、濃い菌傘が形成されることで形態形成が良好となったと推測できる。尚、放射束密度6W/m2は、一般のきのこ栽培工場で使用している光強度の約2.5倍に相当する。
【0075】
本実施例は、前記光刺激の付与と同時に、この光刺激に対する生体センサーに設定したマイタケの生体電位の変化をコンピュータ5により確知する。
【0076】
本実施例における前記生体電位の変化とは、生体センサーとなるマイタケの光刺激に対する60分間の分析区間長の生体電位の計測値(例えば、サンプリングは1分間隔としてデータ数60個)から算出される回帰直線の傾きである。
【0077】
尚、本実施例は、60分間の分析区間長以外に、適宜な分析区間長の生体電位の計測値により生体電位の変化を確知して良い。
【0078】
次に、本実施例の場合、図3に図示したとおり、確知した前記生体電位の変化が正方向の変化であれば、そのままマイタケに光刺激を付与し続け、負方向の変化であれば、マイタケに光刺激を付与するのを中止し、生体電位の変化が正方向となったら、再びマイタケに光刺激を付与するようにする。
【0079】
また、本実施例の場合、前記コンピュータ5に生体電位の変化の正負の閾値(スレッショルドレベル)、即ち、生体電位の変化の上限値及び下限値を入力し、この上限値及び下限値と、本実施例のマイタケから確知された生体電位の変化とを比較して、本実施例のマイタケから確知された生体電位の変化が予め設定された上限値以上となるまでは光刺激を付与せず、上限値以上となったら光刺激を付与し、下限値以下になるまでこの状態を維持し、下限値以下となったら光刺激を付与しないようにし、その後、上限値以上となるまではこの状態を維持する構成とする。
【0080】
ここで、前記上限値と下限値は、予め光刺激を付与しない条件下(暗状態の栽培室4)に所定時間静置した生体センサーマイタケに内在するごく微小な生体電位の変化をもとに適宜設定するか、若しくは、予め光刺激を付与した条件下(明状態の栽培室4)で所定時間静置した生体センサーマイタケの生体電位の変化をもとに適宜設定すると良い。
【0081】
即ち、本実施例においてはごく微小な生体電位の変化がノイズとなって細かな間隔で光刺激付与装置3aの作動・非作動の切り替えが行われることが予想されたため、予め上限値と下限値とを設定している。
【0082】
本実施例の場合、上限値を+0.005とし、下限値を−0.005に設定している。これにより微小なノイズの影響がなくなって、細かな間隔での作動・非作動の切り替えが行われることを防止することができ、よりマイタケの形態形成が良好となる。
【0083】
尚、この上限値及び下限値の設定はマイタケの生長度合いによりその都度変更を行って良く、また、環境刺激の種類によりこの上限値及び下限値の設定を適宜変更して良い。
【0084】
また、本実施例の場合、光以外の環境刺激を一定とするため、前記栽培室4内の温度が16〜22℃となるようにする。
【0085】
特に、栽培室4内の温度が18℃においては、最もマイタケの生体電位の変化が大きく、また、この温度におけるマイタケの形態形成が良好となることを確認している(後述する実験例4及び図9,図10参照。)。
【0086】
また、栽培室4内の湿度は、95%を中心としてプラスマイナス5%の範囲となるようにしている。栽培室4内の湿度を95%を中心としてプラスマイナス5%の範囲とすることで、マイタケの形態形成が良好となることを確認している。
【0087】
また、栽培室4内の酸素は21%,二酸化炭素は600ppm〜700ppmとすることで、マイタケの形態形成が良好となることを確認している(後述する実験例5及び図11,図12参照。)。
【0088】
尚、本実施例において、各マイタケをラボジャッキに載置し、マイタケと前記光照射装置3aとの距離を常に一定(例えば3cm)に調整した場合には、光が常に一定の強度でマイタケに照射されるため、マイタケの生体電位の確知や形態形成が良好となる。
【0089】
栽培室4内の複数個のマイタケの全てを生体センサーに設定するとともに、全てのマイタケ毎に独立した光照射装置3aによる光刺激を付与する構成とし、各マイタケ毎に環境刺激を与え続けるか若しくは中止するかを決定しても良い。
【0090】
また、予め生体センサーに設定したマイタケに環境刺激を与えて栽培し、この際の前記マイタケの生体電位の変化を確知してサンプルデータとして取得しておき、後日、このサンプルデータにもとづき、環境刺激を与えるか若しくは与えないかの制御を自動的に行いながら、生体電位の変化の確知を行わずして複数個のマイタケを栽培しても良い。
【0091】
本実施例はマイタケに適した環境刺激として光を採用したが、前記環境刺激として温度刺激を採用しても良い。具体的には、後述する実験例4の結果を踏まえ、マイタケの形態形成の最適移行段階における生体電位の変化が最も大となる18℃の温度がマイタケに加わるように予め設定された温度制御装置3b(例えば、空調機)を採用すると良い。
【0092】
また、環境刺激として湿気をマイタケに加えるようにしても良い。前記湿気は、予めマイタケの形態形成の最適移行段階における生体電位の変化が最も大となる湿気を把握しておき、このマイタケの生体電位の変化が最も大となる所定の湿気が与えられるように加湿装置3cを調整すると良い。
【0093】
また、環境刺激として栽培室雰囲気中の酸素、二酸化炭素等の気体濃度を調整しても良い。前記気体濃度は、予め、マイタケの形態形成の最適移行段階における生体電位の変化が最も大となる濃度を把握しておき、このマイタケの生体電位の変化が最も大となる所定の気体濃度雰囲気となるように気体濃度制御装置3dを制御すると良い。
【0094】
また、上記光、温度、湿気、気体濃度等の適宜な環境刺激を目的に応じて組み合わせてマイタケに付与しても良く、この場合、複合的な環境条件の中で、マイタケにとって最良の環境刺激を優先的に与えるプログラムを用いると良い。尚、マイタケの生体電位の変化を確知する際の環境刺激と、その後、この確知した生体電位の変化をもとに与える環境刺激とを別種としても良い。
【0095】
きのこの種類毎に適した環境刺激があるため(例えば、ブナシメジの子実体形成時に適した環境刺激は温度である。)ため、マイタケ以外のきのこについても適宜な環境刺激付与装置3による環境刺激を与えて本実施例同様に栽培を行うことができる。
【0096】
本実施例は上述のように構成したから、マイタケの形態形成の最適移行段階が的確に分かり、最も最適なタイミングで環境刺激を与えることができ、よって、良質なきのこが得られるマイタケ栽培方法となる。
【0097】
また、栽培する複数個のマイタケのうちの1つを生体センサーマイタケとするだけであるから、作業は厄介ではない。
【0098】
また、生体電位の変化の確知を行うマイタケと、生体電位の変化の確知を行わないマイタケとを一緒に1ロットとして栽培するから、どの生産ロットも形態形成に要する日数が最短で、収穫の初めから終わりまでの日数も短く、収量や品質も最良で、生産ロット毎の生産性が均一となる。
【0099】
また、本実施例は、光照射装置3aとして発光ダイオードを採用することで、例えば従来の豆電球等に比して低電圧・極小電流で省エネルギーに光の照射を行うことができ、従来の豆電球等に比して長寿命であるため光の照射を低コストに行うことができ、しかも光の照射の際に発熱を伴わないため栽培室4内の温度が上昇せず栽培室4内の温度管理を容易化できる。
【0100】
また、発光ダイオードの光は指向性が高いため、光源の配設位置の設定次第でマイタケに集中的に光を照射することが可能となり、この点においても省エネルギーとなるばかりでなく、マイタケの形態形成を効率良く行うことができる。
【0101】
また、本実施例は光刺激として青色発光ダイオードを採用し、この光の強さを6W/m2に設定することにより、マイタケに大きな生体電位の変化を生じさせることができるため、生体電位の変化の確知が確実且つ容易に行われるとともに、マイタケの形態形成を一層効率良く行うことができる。
【0102】
また、本実施例は、栽培室4内の温度や湿度、ガス濃度を一定状態とすることによっても、マイタケの生体電位の変化の確知と、マイタケの形態形成の促進が良好に行われる。
【0103】
また、本実施例は、マイタケから確知した生体電位の変化を、予め設定した上限値と下限値と比較して環境刺激を与え続けるか否かを決定するから、上限値と下限値に達しない微小な生体電位の変化が確知されて細かな間隔で発光ダイオードの作動・非作動の切り替えが行われるといったことがなく、環境刺激の付与が効率的に行われて、マイタケの形態形成が良好となる。
【0104】
また、最適移行段階にあるきのこに環境刺激を長時間与え続けると、きのこの生体電位の変化が見られなくなって(飽和してしまい)、光の照射エネルギーが無駄になったり、形態形成の促進効果を十分得られない場合があるが、本実施例は、環境刺激をきのこの生体電位の変化に応じて与えるか否かを決定するから、光の照射エネルギーの無駄がなく、効率良く形態形成を行うことができる。
【0105】
(実験例1)
実験例1は、本実施例のマイタケを生体センサーとして用いたマイタケ栽培方法の効果を確認したものである。
【0106】
具体的には、本実施例の青色発光ダイオードを取り付けたパネルを光照射装置3aとして栽培室4上部に配置し、この青色発光ダイオードの作動・非作動をマイタケの生体電位の変化に応じ制御する本実施例の区画(図表中、生体リズム制御と称す。)、前記同様の栽培室4の前記光照射装置3aを12時間作動したのち12時間非作動とする区画(図表中、12L12Dと称す。)、前記同様の栽培室4の前記光照射装置3aを24時間作動させる区画(図表中、24L0Dと称す。)、前記同様の栽培室4の前記光照射装置3aを30分毎に作動・非作動させる区画(図表中、30分ON/OFFと称す。)及び対照として栽培室4に光照射装置3aを設けない暗黒区画(図表中、暗状態と称す。)を設けた。
【0107】
各栽培室4内には子実体原基が形成されて5日ほど経過した菌床9を配置した。また、生体リズム制御区画については上述した本実施例と同様、銀針電極部2Aを挿入する菌床9と同時に、銀針電極部2Aを挿入しない2個の菌床9を連動制御区画(図表中、連動制御と称す。)として配置した。
【0108】
更に、各栽培室4内の室温を18℃に設定すると共に、空気組成が等しくなるように、外気及び内気を一旦エアバッファ3d内に集め、ACファンにより吸気ダクトを通して各栽培室4内に空気を送り込んだ。
【0109】
次いで、2週間の栽培実験を行い、マイタケの生長経過(形態形成)を観察した。
【0110】
子実体の大きさは、長軸方向および短軸方向、菌床9上部からの高さ(図4参照。)について1日おきに測定を行った。また、実験最終日に各マイタケの子実体の大きさ及び新鮮重を測定した。結果は表1に示す。
【0111】
【表1】

【0112】
表1より、生体リズム制御区画及び連動制御区画は、他の区画と比較して子実体の傘が大きく開き、子実体が高く生長するなど、形態形成に違いが見られた。また、収穫時の重量に関しては、表1及び図5に図示したとおり、生体リズム制御区画及び連動制御区画が重くなった。この実験例1と同じ試験を繰り返し行ったところ、再現性が認められた。
【0113】
以上の結果より、マイタケの生体電位の変化に応じて環境刺激を与えた方が、マイタケの生体電位の変化に応じて環境刺激を与えない場合よりも、栽培されたマイタケの形態形成が良好になるといえる。
【0114】
(実験例2)
実験例2は、光の波長がマイタケの形態形成にどのような影響を与えるのかを確認したものである。
【0115】
栽培室4内は室温18℃、湿度95%に調整し、実施例の(1)〜(4)の工程を経て、マイタケの子実体原基が形成されて5日ほど経過した菌床9を配置した。
【0116】
具体的には、光照射装置3aとしてアイショートアーク型のキセノンランプ(300W)を採用した。
【0117】
前記キセノンランプの照射光には可視光線以外の波長が含まれるため、あらかじめ光学フィルタを用いて紫外域(400nm以下)と赤外域(700nm以上)の波長を除去した照射光を用いた。
【0118】
前記照射光を特定の干渉フィルタを透過させることで、単色光(特定波長の光)とし、この前記特定波長の光を集光レンズで集光し、この集光した光を光ファイバでマイタケの上部に照射した。
【0119】
また、光の照射は、波長を400〜680nmの範囲で変化させ、強度を光量子束密度35μmol/m2/sに設定して行い、マイタケの生体電位の変化量を計測した。
【0120】
また、生体電位の計測は、上述した本実施例のマイタケの栽培方法に順じて行った。
【0121】
図6に示すように、マイタケは青色領域(430〜470nm)付近で生体電位の変化が大きく、緑・黄色領域(480〜570nm)付近では徐々に小さくなり、赤色領域(610nm)付近ではほぼ変化を示さない結果を得ている。
【0122】
従って、図7に示すように、青色領域(430〜470nm)下で栽培したマイタケは形態形成が良好となるといえる。
【0123】
(実験例3)
実験例3は、光の強度がマイタケの形態形成にどのような影響を与えるのかを確認したものである。
【0124】
栽培室4内は室温18℃、湿度95%に調整し、実施例の(1)〜(4)の工程を経て、マイタケの子実体原基が形成されて5日ほど経過した菌床9を配置した。
【0125】
また、前記各菌床9はラボジャッキに載置する。
【0126】
具体的には、光照射装置3aとして青色発光ダイオード(放射束密度6W/m2)を採用する。この青色発光ダイオードを複数取り付けたパネルを栽培室の上部に配置する。
【0127】
また、光の強度(放射束密度)の変化は、子実体頂点の光強度が常に所定強度となるよう菌床9の高さと前記光照射装置3aとの距離をラボジャッキを上下動調節することで行う。
【0128】
前記菌床9頂点の光強度が3,4,6,8,10W/m2になるように設定し、光を照射し、マイタケの生体電位の変化量を計測した。
【0129】
また、生体電位の計測は、上述した本実施例のマイタケの栽培方法に順じて行った。
【0130】
図8に示すように、子実体の生体電位応答は光の強度に比例することを確認している。
【0131】
(実験例4)
実験例4は、栽培室4内の温度がマイタケの形態形成にどのような影響を与えるのかを確認したものである。
【0132】
栽培室4内には、実施例の(1)〜(4)の工程を経て、マイタケの子実体原基が形成されて5日ほど経過した菌床9を配置した。
【0133】
光の照射は、上述した本実施例のマイタケの栽培方法に順じて行った。
【0134】
また、栽培室4内の温度は、ペルチェ素子3bにより、一般に生産現場で設定されている温度である16℃〜22℃に変化させた。
【0135】
具体的にはペルチェ素子3bをコンピュータ5により制御して栽培室4内の温度を16℃、18℃、20℃、22℃の順に変化させ、これを1クルーとし、各温度を24〜36時間程度維持して栽培する過程で、マイタケの生体電位の変化を観察した。尚、実験は5個のマイタケに対して行った。
【0136】
また、生体電位の計測は、上述した本実施例のマイタケの栽培方法に順じて行った。
【0137】
【表2】

【0138】
表2及び図9に示すように、光の照射条件が同じ場合には、栽培室4内の温度を18℃に設定した場合に、マイタケの生体電位の変化が最も大きく光刺激に対する生体電位応答がみられることを確認した。
【0139】
また、生体電位の変化が最も大きな18℃で栽培した場合、14℃で栽培した場合夫々のマイタケの栽培終了時の形態形成を図10に示し、夫々の収穫時の重さ(新鮮重)を表3に示す。
【0140】
また、子実体上面の縦幅、横幅について比較したものを表4に示す(表4中、Aは14℃で栽培した場合、Bは18℃で栽培した場合を示す。)。
【0141】
【表3】

【0142】
【表4】

【0143】
従って、本実施例は栽培室4内の温度が18℃の場合に最もマイタケの生体電位の変化が大きく、この温度下のマイタケは形態形成が良好となるといえる。
【0144】
(実験例5)
実験例5は、栽培室4内の二酸化炭素濃度が形態形成にどのような影響を与えるのかを確認したものである。
【0145】
栽培室4内は室温18℃、湿度95%、二酸化炭素濃度500〜800ppmに調整し、実施例の(1)〜(4)の工程を経て、マイタケの子実体原基が形成されて5日ほど経過した菌床9を配置した。
【0146】
前記二酸化炭素濃度は気体濃度制御装置3dで栽培室4内の気体濃度が均一になるように、栽培室4内外の空気を一旦エアバッファ3d内に集め、ACファンによりダクトを通して栽培室4に空気を送りこんで制御する。
【0147】
また、光照射装置3aとして青色発光ダイオード(放射束密度6W/m2)を採用する。この青色発光ダイオードを複数取り付けたパネルを栽培室の上部に配置する。
【0148】
また、光照射は30分ON/OFFを繰り返し行い、マイタケの生体電位を継続して計測した。
【0149】
計測開始から7時間後に、栽培室4の二酸化炭素濃度を5000ppmを超える濃度に上昇させ、この状態を10時間維持し、生体電位を継続して計測した。
【0150】
その後、予め栽培室4の二酸化炭素濃度を500ppmから800ppmになるようにコンピュータ5に設定した状態で、栽培室4の窓を開放することで換気を行い、栽培室4の二酸化炭素濃度が前記設定値になったところで栽培室4の窓を閉じ、生体電位を継続して計測した。
【0151】
また、生体電位の計測は、上述した本実施例のマイタケの栽培方法に順じて行った。
【0152】
その結果、図11に示すように、栽培室4が高濃度の二酸化炭素条件下になることで子実体の生体電位は急激に低下し、一定条件の光刺激に対する生体電位応答は見られなくなることを確認した。
【0153】
またその後、図12に示すように、換気を行うことによって、栽培室の二酸化炭素濃度が前記設定値に低下すると、数時間後に再び光刺激に対する生体電位応答が回復したことを確認している。
【0154】
従って、高濃度の二酸化炭素条件下では子実体の生長が阻害され、子実体の生体電位応答と形態形成との関連性が示唆された。
【図面の簡単な説明】
【0155】
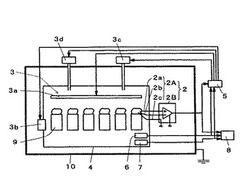
【図1】本実施例の栽培装置の概略説明図である。
【図2】本実施例の電極部を挿入した後、子実体になった状態の写真である。
【図3】本実施例の生体電位の変化に応じた制御のフローチャートである。
【図4】実験例1の説明図である。
【図5】実験例1の結果を示すグラフ図である。
【図6】実験例2の光の波長と生体電位変化量との関係を示すグラフ図である。
【図7】実験例2の光の波長(青色光と赤色光)が形態形成に与える影響を比較したマイタケの写真である。
【図8】実験例3の光の強度と生体電位変化量との関係を示すグラフ図である。
【図9】実験例4の環境温度が生体電位に与える影響を示すグラフ図である。
【図10】実験例4の環境温度(14℃と18℃)が形態形成に与える影響を比較したマイタケの写真である。
【図11】実験例5の二酸化炭素濃度が生体電位応答に与える影響を示すグラフ図である。
【図12】実験例5の換気後の二酸化炭素濃度が生体電位応答に与える影響を示すグラフ図である。
【符号の説明】
【0156】
2 生体電位計測装置
2A 電極部
2B 増幅部
3 環境刺激付与装置
3a 光照射装置
3b 温度制御装置
3c 加湿装置
3d 気体濃度制御装置
【技術分野】
【0001】
本発明は、きのこを生体センサーとして用いたきのこ栽培方法に関するものである。
【0002】
従来、きのこの人工栽培方法として、菌床栽培や原木栽培が一般的に採用されている。
【0003】
例えば、マイタケの菌床栽培の場合、オガ粉に米糠等の栄養分を加えた菌床(培地)を殺菌・冷却し、この菌床に種菌を接種し、菌床中に菌糸を蔓延させ、菌糸が蔓延した菌床にマイタケ子実体原基を形成させ、このマイタケ子実体原基からマイタケ子実体を発生・生長させて収穫が行われている。
【0004】
また、このマイタケの人工栽培方法においては、種菌接種から子実体収穫に亙るマイタケの外観変化の観察及び培養日数を指標とする経験的な管理が行われている。
【0005】
ところで、菌糸が蔓延した菌床からの子実体原基の形成や、子実体原基からの子実体の発生・成長等、所謂マイタケの形態形成を良好に進める為には、例えば、菌糸が蔓延した菌床から子実体原基を形成させる場合、適正な時期に光や温度等の適宜な環境刺激を与える必要がある。即ち、菌糸が蔓延した菌床から子実体原基を形成させる場合においては、菌糸(菌体)内に十分に栄養分が貯蔵された時点が上記適正な時期(次の子実体原基形成への最適移行段階)であるといわれ、この最適移行段階にある菌床に光や温度等の適宜な環境刺激を与えると、その後の子実体原基形成が良好に行われ、最終的に形状・大きさが良好な子実体が得られる。
【発明の開示】
【発明が解決しようとする課題】
【0006】
しかしながら、栽培するマイタケが上述した最適移行段階にあるか否かを見極めることは厄介であり、よって栽培マイタケに適切なタイミングで環境刺激を与えることは困難である。
【0007】
何故なら、従来のような外観変化の観察及び培養日数を指標とする経験的な管理手法では、マイタケに外観の変化が認められたときには多くの場合、内生的変化は既に終了した後であると考えられ、最適移行段階にあるマイタケを見極めるのは非常に難しいからである。
【0008】
また、上述した外観変化の観察は目視によって行われることから観察者による差が大きく、最適移行段階にあるか否かを観察者(栽培者)の資質に依存しなければならず、客観的に最適移行段階にあるか否かを見極めることはこの点からも困難である。
【0009】
従って、従来のマイタケの人工栽培方法においては、前記最適移行段階となった状態を適切に見極め、適切なタイミングで環境刺激を与えることは難しく、よって、現実には観察者の所謂勘により環境刺激を与えざるをえないのが現状である。
【0010】
また、実際、マイタケ栽培は同時に多数の子実体形成を行うため、前記最適移行段階の菌体が多い菌床が多数を占めた生産ロットでは、全体として、収穫の初めから終わりまでの日数も短く、収量や品質も良好となるのに対し、前記最適移行段階の菌体が多い菌床が少数であった生産ロットでは、逆に、全体として収穫の初めから終わりまでの日数が長く、収量や品質も悪くなり、生産ロット毎の生産性が不均一となるという問題もある。
【0011】
本発明者らは、形態形成における最適移行段階に至ったきのこを見極め、最も最適なタイミングできのこの形態形成に必要な環境刺激を与えるには、きのこ(菌糸、子実体原基若しくは子実体)内部の変化をいち早く察知することが必要であるという知見に基づき、鋭意研究を重ねた結果、(1)きのこに環境刺激を与えると、きのこに内在する生体電位が変化すること、(2)最適移行段階に至ったきのこと最適移行段階に至っていないきのことは、環境刺激を与えた場合の生体電位の変化が異なり、きのこに環境刺激を与えた際に有意な生体電位の上昇が認められる場合にはきのこの形態形成が良好になる傾向があることから、環境刺激に対する生体電位に有意な上昇が認められる場合にはきのこは最適移行段階に至ったものと考えられ、よって、この場合に環境刺激を与えれば良いこと、の2つを見出し、この事実を利用し、良好なきのこを効率的に栽培する方法を完成させたものである。
【課題を解決するための手段】
【0012】
添付図面を参照して本発明の要旨を説明する。
【0013】
きのこに環境刺激を与えた際のきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとに、きのこを栽培することを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0014】
また、請求項1記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記確知した生体電位の変化をもとに、きのこに環境刺激を与えるか若しくは与えないかを決定して当該きのこを栽培することを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0015】
また、請求項1,2いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記確知する生体電位の変化とは、所定時間におけるきのこの生体電位の傾きであり、この傾きが正ならば前記きのこに環境刺激を与え、負ならば前記きのこに環境刺激を与えないようにすることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0016】
また、請求項3記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記傾きが正である場合、予め設定された上限値以上となるまでは環境刺激を与えず、上限値以上となったら環境刺激を与え、また、前記傾きが負である場合、予め設定された下限値以下になるまでは環境刺激を与え、下限値以下となったら環境刺激を与えないようにすることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0017】
また、請求項1〜4いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激は環境刺激付与装置3により与え、前記生体電位の変化の確知は生体電位計測装置2により行うことを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0018】
また、請求項5記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記生体電位計測装置2は、生体電位を計測する電極部2A及び該電極部2Aにより計測された生体電位を増幅する増幅部2Bを具備するものであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0019】
また、請求項1〜6いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、複数個のきのこを栽培する場合、当該栽培する一部のきのこの生体電位の変化の確知を行うことを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0020】
また、請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置3は、きのこに光を照射する光照射装置3aであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0021】
また、請求項8記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記光は、所定の光質であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0022】
また、請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置3は、きのこを所定の温度に調整する温度制御装置3bであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0023】
また、請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置3は、きのこに所定の湿気を加える加湿装置3cであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【0024】
また、請求項1〜7記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置3は、栽培雰囲気中の気体濃度を調整する気体濃度制御装置3dであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法に係るものである。
【発明の効果】
【0025】
本発明は、きのこに環境刺激を与えた際のきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとに、きのこを栽培するから、形態形成の最適移行段階が的確に分かり、良質なきのこが得られることになる。
【発明を実施するための最良の形態】
【0026】
好適と考える本発明の実施形態を、図面に基づいて本発明の作用を示して簡単に説明する。
【0027】
きのこの栽培に際し、きのこに環境刺激を与え、この環境刺激に対するきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとにきのこを栽培する。
【0028】
本発明におけるきのことは、例えばきのこ栽培工場等、人為的に環境の制御が可能な施設内で栽培されるきのこであり、菌床栽培(袋や瓶を容器とするものも含む)、原木栽培のきのこである。
【0029】
また、本発明におけるきのこの生体電位とは、きのこの細胞膜の内部イオンの濃度差により発生する微小電位(数mV)を指している。
【0030】
また、本発明において生体電位を測定する対象は、子実体,子実体原基若しくは原木や菌床9に蔓延する菌糸である。
【0031】
また、本発明における生体電位計測装置2とは、生体電位を計測する電極部2Aと、この電極部2Aで計測された生体電位を増幅する増幅部2Bとを具備したもので、前記電極部2Aは、正極2a、負極2b及び不関電極2cによりなる構成とし、この正極2a、負極2b及び不関電極2cを夫々前記きのこに挿入して当該きのこの生体電位を計測し、当該きのこの生体電位の変化を確知する。
【0032】
菌糸が蔓延した菌床9から子実体原基の形成や、子実体原基からの子実体の発生・成長等、所謂きのこの形態形成を良好に進める為には、例えば、菌糸が蔓延した菌床9から良好な子実体原基を形成させる為には、適正な時期に光(光を全く与えないという環境刺激も含む。)、温度、湿度、二酸化炭素濃度等、きのこの種類に応じて適宜な環境刺激を与える必要がある。
【0033】
即ち、菌糸が蔓延した菌床9から子実体原基を形成させる場合においては、菌糸(菌体)内に十分に栄養分が貯蔵された時点が適正な時期(次の子実体原基形成への最適移行段階)であるといわれ、この最適移行段階にある菌糸に光、温度、湿度、二酸化炭素濃度等、きのこの種類に応じた適宜な環境刺激を与えると、その後の子実体原基の形成が良好に行われ、最終的に形状・大きさが良好な子実体が得られる。
【0034】
また、本発明者らは、(1)きのこに環境刺激を与えると、きのこに内在する生体電位が変化すること、(2)最適移行段階に至ったきのこと最適移行段階に至っていないきのことは、環境刺激を与えた場合の生体電位の変化が異なり、きのこに環境刺激を与えた際に有意な生体電位の上昇が認められる場合にはきのこの形態形成が良好になる傾向があることから、環境刺激に対する生体電位に有意な上昇が認められる場合にはきのこは最適移行段階に至ったものと考えられ、よって、この場合に環境刺激を与えれば良いこと、の2つを見出し、環境刺激を与えたきのこの所定時間における生体電位の傾きを求め、この傾きが正の所定の傾きならばきのこに環境刺激を与え、負の所定の傾きならばきのこに環境刺激を与えないようにすることで、きのこの形態形成が良好に行われることを確認した。
【0035】
更に、本発明者らは、栽培対象のきのこに光、温度、湿度、二酸化炭素濃度等の環境刺激を与え、このきのこの生体電位の変化を確知した際に、この確知した生体電位の変化(傾き)が予め設定された上限値以上となるまでは環境刺激を与えず、上限値以上となったら環境刺激を与え、下限値以下になるまでこの状態を維持し、下限値以下となったら環境刺激を与えないようにし、その後、上限値以上となるまではこの状態を維持するというように環境刺激を与えること、与えないことを繰り返すと、よりきのこの形態形成が良好に行われることを確認した。
【0036】
従って、本発明は、きのこに環境刺激を与えた際のきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとに、きのこを栽培するから、形態形成の最適移行段階が的確に分かり、良質なきのこが得られることになる。
【実施例】
【0037】
本発明の具体的な実施例について図面に基づいて説明する。
【0038】
本実施例は、マイタケを生体センサーとして用いたマイタケ栽培方法であり、人為的な環境刺激を付与し得る栽培室4内に複数個のマイタケを配置し、この複数個のマイタケのなかの一つを生体センサーに設定し、この生体センサーに設定したマイタケの前記環境刺激に対する生体電位の変化を確知し、この確知した生体電位の変化をもとに、前記複数個のマイタケに環境刺激を与え続けるか若しくは中止するかを決定してマイタケを複数個同時に栽培する場合である。
【0039】
尚、生体電位の変化を確知した後、一旦環境刺激の付与を停止し、その後、この確知した生体電位の変化をもとに環境刺激を与えるか若しくは与えないかを決定する場合も含まれる。
【0040】
マイタケは、図1に図示したとおり、栽培室4内に複数個配置される。
【0041】
前記栽培室4の外部であって環境ブース10内に生体電位計測装置2が配設される。
【0042】
本実施例は、前記簡易環境ブース10内に生体電位計測装置2を設置することで、外部からの干渉を防止して正確な生体電位の計測が可能となる。
【0043】
前記生体電位計測装置2は、増幅器2Bに電極部2Aが接続された構成としている。
【0044】
前記電極部2Aは、前記栽培室4内の複数個のマイタケのなかの生体センサーに設定されたマイタケに挿入される。
【0045】
前記電極部2Aは、正極2a、負極2b及び不関電極2cより構成され、本実施例の場合、前記正極2a、負極2b及び不関電極2cとして、表面に塩化銀膜を生成した約φ0.5mmの銀針電極部2Aを採用することで、分極を防ぎながら生体電位を測定することができる。
【0046】
前記増幅器2Bは、その出力端が、前記簡易環境ブース10の外部に配設されたコンピュータ5とペンレコーダー8に接続される構成としている。
【0047】
従って、本実施例は、前記増幅器2Bにより増幅され出力された生体電位の測定値がこのコンピュータ5及びペンレコーダー8により連続的に記録される。
【0048】
前記コンピュータ5は、前記記録された生体電位の変化、即ち、所定時間の生体電位の変化(傾き)を演算して分析する構成としている。
【0049】
前記環境刺激は、本実施例の場合、光(後述の所定の光質が望ましい。)を付与し得る光照射装置3aを採用する。
【0050】
本実施例の場合、前記光照射装置3aを栽培室4の上部に付設し、マイタケの上部に光が当たるようにしている。尚、前記光照射装置3aの配設位置は、本実施例以外にも適宜設定することができるが、本実施例のように光照射装置3aをマイタケの上部に付設することで、マイタケの菌傘に効率良く光が照射されてマイタケの生体電位の確知や形態形成が良好となる。
【0051】
また、前記栽培室4内には、温度センサー6及び湿度センサー7を設置し、この温度センサー6及び湿度センサー7の出力端子を前記コンピュータ5及びペンレコーダー8に接続し、栽培室4内の温度と湿度とを連続的に記録する構成としている。
【0052】
本実施例の場合、光以外の環境刺激を一定とするため、前記コンピュータ5に予め所定の温度及び湿度を設定しておき、前記栽培室4内の温度センサー6及び湿度センサー7により測定された温度及び湿度が前記設定と異なる場合に、前記コンピュータ5がペルチェ素子3b、超音波加湿器3cを制御してこの栽培室4内の温度と湿度とを略一定状態に調整する構成としている。
【0053】
尚、前記ペルチェ素子3bは電流の制御だけで急速な冷却・加熱ができるため好ましいが、ペルチェ素子3b以外にも適宜な加熱・冷却手段を採用することができる。また、超音波加湿器3c以外にも適宜な加湿手段を採用することができる。
【0054】
更に、本実施例の場合は、前記栽培室4内の酸素、二酸化炭素等の気体濃度を制御する気体濃度制御装置3dを設けた構成としている。
【0055】
具体的には、前記気体濃度制御装置3dとしてエアバッファ3dを採用し、前記栽培室4内の気体濃度組成が等しくなるように、栽培室4内外の空気を一旦エアバッファ3d内に集め、ACファンによりダクトを通して栽培室4内に空気を送り込む構成としている。
【0056】
尚、前記エアバッファ3d内の温度および湿度、酸素濃度、二酸化炭素濃度及び気圧については、前記コンピュータ5にて常時記録する構成としている。
【0057】
以下に本実施例のマイタケを生体センサーとして用いたマイタケ栽培方法について詳しく説明する。
【0058】
本実施例では、以下の工程(1)〜(4)を経て、マイタケの子実体原基が形成されて5日ほど経過した菌床9を、前記栽培室4内に配置する(図1参照)。
【0059】
(1)培地調整及び殺菌
コーンコブ,米糠,広葉樹オガコ等の培地基材,添加物を容積比10:2程度の割合で加水しながら混合し、適当な水分率(65%程度)に調整する。これを一定量ずつ通気用の除菌フィルターのついたポリプロピレン製の耐熱性袋または800〜850ccの栽培瓶に充填する。下方に直径2cm程度の穴を開けて蓋をし、121℃で一定時間高圧殺菌する。
【0060】
(2)種菌接種
殺菌終了後、一昼夜冷却し、培地の温度が20℃以下になってから培養基にマイタケ(Grifola frondosa(Dicks.Fr).S.F.Gray)の種菌を適当量接種する。この際、子実体原基の形成方法が子実体の形成に影響をおよぼす。そのため、子実体原基を形成させる空間を確保する必要がある。空間は通気孔を中心に上面の4分の1程度、高さ5cm程度とする。袋の口を3〜4回折り返し,その両端を合わせてホチキスや輪ゴムなどで止めるのが一般的である。
【0061】
(3)菌糸培養
接種後の培地は湿度60〜70%、温度20〜30℃、暗黒の培養室で培養する。培養時、呼吸による二酸化炭素放出のため換気を行う。
【0062】
(4)子実体原基形成
マイタケは菌糸の生育温度と子実体原基の形成温度が重なっているため「芽出し」までは培養室で行われる。子実体原基が十分に盛り上がり、濃灰色に変色し、その表面が波上に盛り上がるのを確認してから、栽培室4へ移動する。その後、2〜3日して子実体原基が黒色となり水滴が目立たなくなってから、子実体が生育する部分のみ袋をカットする。カットの方法はカッターで5cmほどの十文字に切ったり、通気孔部分を取り外したりする。
【0063】
次に、本実施例は、栽培室4へ移動した前記複数個のうち、生体センサーに設定した子実体原基に、前記生体電位計測装置2の前記電極部2Aを挿入する。
【0064】
具体的には、前記子実体原基に挿入した前記正極2aの約10mm下に負極2bを、子実体原基と菌床9との境界に不関電極2cをそれぞれ深さ約10mmとなる程度に挿入する(尚、図2は子実体原基が子実体に生長した写真である)。
【0065】
尚、本実施例の場合、前記生体電位計測装置2の前記増幅器2Bとして差動型生体電位アンプ(CMMR:約120dB以上、S/N比:約80dB)を使用し、増幅率を50倍に設定する。
【0066】
即ち、前記増幅率は、マイタケの生体電位の変化が概ね40mV〜60mVであることから、サチュレーションを起こさないと考えられる50倍に設定する。更に、前記増幅器2Bの出力バイアス電圧は±0Vとする。
【0067】
次に、栽培室4内のマイタケに対して光照射装置3aによる光刺激の付与を行う。
【0068】
本実施例の場合、前記光照射装置3aとして、発光ダイオードを採用する。
【0069】
具体的には、前記発光ダイオードとして、超高輝度型青色発光ダイオード(中心発光波長470nm、放射束密度6W/m2)を採用し、この青色発光ダイオードを複数個取り付けたパネルを栽培室4の上部に配置する。
【0070】
即ち、本発明者らがこれまでマイタケを生体センサーとしてマイタケの生体電位の変化における光質依存性の検討を行ったところ、波長については、マイタケは青色領域(430〜470nm)付近で生体電位の変化が大きく、緑・黄色領域では徐々に小さくなり、赤色領域ではほぼ変化を示さない結果を得ている(後述する実験例2及び図6参照)。
【0071】
尚、図7に示すように、青色光と赤色光で栽培したマイタケを比較すると、青色光のマイタケの方が形態形成が良好であり、色も濃く、菌傘の広がりが大きいことを確認している。
【0072】
また、光質依存性の検討として更に、波長が青色領域の光の強さ(放射束密度)についても検討を行ったところ、子実体の生体電位応答は光の強度(光量子束密度)に比例することを確認している(後述する実験例3及び図8参照)。
【0073】
尚、2W/m2の青色光と6W/m2の青色光で生育したマイタケを比較すると、6W/m2の青色光で生育したマイタケの方が形態形成が良好であり、色も濃く、菌傘の広がりが大きいことを確認している。
【0074】
この理由は、照射する青色光の光強度が強いとマイタケが有するフラボノイド等の青色領域に特異的な光屈折作用を有する色素の活性が増し、濃い菌傘が形成されることで形態形成が良好となったと推測できる。尚、放射束密度6W/m2は、一般のきのこ栽培工場で使用している光強度の約2.5倍に相当する。
【0075】
本実施例は、前記光刺激の付与と同時に、この光刺激に対する生体センサーに設定したマイタケの生体電位の変化をコンピュータ5により確知する。
【0076】
本実施例における前記生体電位の変化とは、生体センサーとなるマイタケの光刺激に対する60分間の分析区間長の生体電位の計測値(例えば、サンプリングは1分間隔としてデータ数60個)から算出される回帰直線の傾きである。
【0077】
尚、本実施例は、60分間の分析区間長以外に、適宜な分析区間長の生体電位の計測値により生体電位の変化を確知して良い。
【0078】
次に、本実施例の場合、図3に図示したとおり、確知した前記生体電位の変化が正方向の変化であれば、そのままマイタケに光刺激を付与し続け、負方向の変化であれば、マイタケに光刺激を付与するのを中止し、生体電位の変化が正方向となったら、再びマイタケに光刺激を付与するようにする。
【0079】
また、本実施例の場合、前記コンピュータ5に生体電位の変化の正負の閾値(スレッショルドレベル)、即ち、生体電位の変化の上限値及び下限値を入力し、この上限値及び下限値と、本実施例のマイタケから確知された生体電位の変化とを比較して、本実施例のマイタケから確知された生体電位の変化が予め設定された上限値以上となるまでは光刺激を付与せず、上限値以上となったら光刺激を付与し、下限値以下になるまでこの状態を維持し、下限値以下となったら光刺激を付与しないようにし、その後、上限値以上となるまではこの状態を維持する構成とする。
【0080】
ここで、前記上限値と下限値は、予め光刺激を付与しない条件下(暗状態の栽培室4)に所定時間静置した生体センサーマイタケに内在するごく微小な生体電位の変化をもとに適宜設定するか、若しくは、予め光刺激を付与した条件下(明状態の栽培室4)で所定時間静置した生体センサーマイタケの生体電位の変化をもとに適宜設定すると良い。
【0081】
即ち、本実施例においてはごく微小な生体電位の変化がノイズとなって細かな間隔で光刺激付与装置3aの作動・非作動の切り替えが行われることが予想されたため、予め上限値と下限値とを設定している。
【0082】
本実施例の場合、上限値を+0.005とし、下限値を−0.005に設定している。これにより微小なノイズの影響がなくなって、細かな間隔での作動・非作動の切り替えが行われることを防止することができ、よりマイタケの形態形成が良好となる。
【0083】
尚、この上限値及び下限値の設定はマイタケの生長度合いによりその都度変更を行って良く、また、環境刺激の種類によりこの上限値及び下限値の設定を適宜変更して良い。
【0084】
また、本実施例の場合、光以外の環境刺激を一定とするため、前記栽培室4内の温度が16〜22℃となるようにする。
【0085】
特に、栽培室4内の温度が18℃においては、最もマイタケの生体電位の変化が大きく、また、この温度におけるマイタケの形態形成が良好となることを確認している(後述する実験例4及び図9,図10参照。)。
【0086】
また、栽培室4内の湿度は、95%を中心としてプラスマイナス5%の範囲となるようにしている。栽培室4内の湿度を95%を中心としてプラスマイナス5%の範囲とすることで、マイタケの形態形成が良好となることを確認している。
【0087】
また、栽培室4内の酸素は21%,二酸化炭素は600ppm〜700ppmとすることで、マイタケの形態形成が良好となることを確認している(後述する実験例5及び図11,図12参照。)。
【0088】
尚、本実施例において、各マイタケをラボジャッキに載置し、マイタケと前記光照射装置3aとの距離を常に一定(例えば3cm)に調整した場合には、光が常に一定の強度でマイタケに照射されるため、マイタケの生体電位の確知や形態形成が良好となる。
【0089】
栽培室4内の複数個のマイタケの全てを生体センサーに設定するとともに、全てのマイタケ毎に独立した光照射装置3aによる光刺激を付与する構成とし、各マイタケ毎に環境刺激を与え続けるか若しくは中止するかを決定しても良い。
【0090】
また、予め生体センサーに設定したマイタケに環境刺激を与えて栽培し、この際の前記マイタケの生体電位の変化を確知してサンプルデータとして取得しておき、後日、このサンプルデータにもとづき、環境刺激を与えるか若しくは与えないかの制御を自動的に行いながら、生体電位の変化の確知を行わずして複数個のマイタケを栽培しても良い。
【0091】
本実施例はマイタケに適した環境刺激として光を採用したが、前記環境刺激として温度刺激を採用しても良い。具体的には、後述する実験例4の結果を踏まえ、マイタケの形態形成の最適移行段階における生体電位の変化が最も大となる18℃の温度がマイタケに加わるように予め設定された温度制御装置3b(例えば、空調機)を採用すると良い。
【0092】
また、環境刺激として湿気をマイタケに加えるようにしても良い。前記湿気は、予めマイタケの形態形成の最適移行段階における生体電位の変化が最も大となる湿気を把握しておき、このマイタケの生体電位の変化が最も大となる所定の湿気が与えられるように加湿装置3cを調整すると良い。
【0093】
また、環境刺激として栽培室雰囲気中の酸素、二酸化炭素等の気体濃度を調整しても良い。前記気体濃度は、予め、マイタケの形態形成の最適移行段階における生体電位の変化が最も大となる濃度を把握しておき、このマイタケの生体電位の変化が最も大となる所定の気体濃度雰囲気となるように気体濃度制御装置3dを制御すると良い。
【0094】
また、上記光、温度、湿気、気体濃度等の適宜な環境刺激を目的に応じて組み合わせてマイタケに付与しても良く、この場合、複合的な環境条件の中で、マイタケにとって最良の環境刺激を優先的に与えるプログラムを用いると良い。尚、マイタケの生体電位の変化を確知する際の環境刺激と、その後、この確知した生体電位の変化をもとに与える環境刺激とを別種としても良い。
【0095】
きのこの種類毎に適した環境刺激があるため(例えば、ブナシメジの子実体形成時に適した環境刺激は温度である。)ため、マイタケ以外のきのこについても適宜な環境刺激付与装置3による環境刺激を与えて本実施例同様に栽培を行うことができる。
【0096】
本実施例は上述のように構成したから、マイタケの形態形成の最適移行段階が的確に分かり、最も最適なタイミングで環境刺激を与えることができ、よって、良質なきのこが得られるマイタケ栽培方法となる。
【0097】
また、栽培する複数個のマイタケのうちの1つを生体センサーマイタケとするだけであるから、作業は厄介ではない。
【0098】
また、生体電位の変化の確知を行うマイタケと、生体電位の変化の確知を行わないマイタケとを一緒に1ロットとして栽培するから、どの生産ロットも形態形成に要する日数が最短で、収穫の初めから終わりまでの日数も短く、収量や品質も最良で、生産ロット毎の生産性が均一となる。
【0099】
また、本実施例は、光照射装置3aとして発光ダイオードを採用することで、例えば従来の豆電球等に比して低電圧・極小電流で省エネルギーに光の照射を行うことができ、従来の豆電球等に比して長寿命であるため光の照射を低コストに行うことができ、しかも光の照射の際に発熱を伴わないため栽培室4内の温度が上昇せず栽培室4内の温度管理を容易化できる。
【0100】
また、発光ダイオードの光は指向性が高いため、光源の配設位置の設定次第でマイタケに集中的に光を照射することが可能となり、この点においても省エネルギーとなるばかりでなく、マイタケの形態形成を効率良く行うことができる。
【0101】
また、本実施例は光刺激として青色発光ダイオードを採用し、この光の強さを6W/m2に設定することにより、マイタケに大きな生体電位の変化を生じさせることができるため、生体電位の変化の確知が確実且つ容易に行われるとともに、マイタケの形態形成を一層効率良く行うことができる。
【0102】
また、本実施例は、栽培室4内の温度や湿度、ガス濃度を一定状態とすることによっても、マイタケの生体電位の変化の確知と、マイタケの形態形成の促進が良好に行われる。
【0103】
また、本実施例は、マイタケから確知した生体電位の変化を、予め設定した上限値と下限値と比較して環境刺激を与え続けるか否かを決定するから、上限値と下限値に達しない微小な生体電位の変化が確知されて細かな間隔で発光ダイオードの作動・非作動の切り替えが行われるといったことがなく、環境刺激の付与が効率的に行われて、マイタケの形態形成が良好となる。
【0104】
また、最適移行段階にあるきのこに環境刺激を長時間与え続けると、きのこの生体電位の変化が見られなくなって(飽和してしまい)、光の照射エネルギーが無駄になったり、形態形成の促進効果を十分得られない場合があるが、本実施例は、環境刺激をきのこの生体電位の変化に応じて与えるか否かを決定するから、光の照射エネルギーの無駄がなく、効率良く形態形成を行うことができる。
【0105】
(実験例1)
実験例1は、本実施例のマイタケを生体センサーとして用いたマイタケ栽培方法の効果を確認したものである。
【0106】
具体的には、本実施例の青色発光ダイオードを取り付けたパネルを光照射装置3aとして栽培室4上部に配置し、この青色発光ダイオードの作動・非作動をマイタケの生体電位の変化に応じ制御する本実施例の区画(図表中、生体リズム制御と称す。)、前記同様の栽培室4の前記光照射装置3aを12時間作動したのち12時間非作動とする区画(図表中、12L12Dと称す。)、前記同様の栽培室4の前記光照射装置3aを24時間作動させる区画(図表中、24L0Dと称す。)、前記同様の栽培室4の前記光照射装置3aを30分毎に作動・非作動させる区画(図表中、30分ON/OFFと称す。)及び対照として栽培室4に光照射装置3aを設けない暗黒区画(図表中、暗状態と称す。)を設けた。
【0107】
各栽培室4内には子実体原基が形成されて5日ほど経過した菌床9を配置した。また、生体リズム制御区画については上述した本実施例と同様、銀針電極部2Aを挿入する菌床9と同時に、銀針電極部2Aを挿入しない2個の菌床9を連動制御区画(図表中、連動制御と称す。)として配置した。
【0108】
更に、各栽培室4内の室温を18℃に設定すると共に、空気組成が等しくなるように、外気及び内気を一旦エアバッファ3d内に集め、ACファンにより吸気ダクトを通して各栽培室4内に空気を送り込んだ。
【0109】
次いで、2週間の栽培実験を行い、マイタケの生長経過(形態形成)を観察した。
【0110】
子実体の大きさは、長軸方向および短軸方向、菌床9上部からの高さ(図4参照。)について1日おきに測定を行った。また、実験最終日に各マイタケの子実体の大きさ及び新鮮重を測定した。結果は表1に示す。
【0111】
【表1】

【0112】
表1より、生体リズム制御区画及び連動制御区画は、他の区画と比較して子実体の傘が大きく開き、子実体が高く生長するなど、形態形成に違いが見られた。また、収穫時の重量に関しては、表1及び図5に図示したとおり、生体リズム制御区画及び連動制御区画が重くなった。この実験例1と同じ試験を繰り返し行ったところ、再現性が認められた。
【0113】
以上の結果より、マイタケの生体電位の変化に応じて環境刺激を与えた方が、マイタケの生体電位の変化に応じて環境刺激を与えない場合よりも、栽培されたマイタケの形態形成が良好になるといえる。
【0114】
(実験例2)
実験例2は、光の波長がマイタケの形態形成にどのような影響を与えるのかを確認したものである。
【0115】
栽培室4内は室温18℃、湿度95%に調整し、実施例の(1)〜(4)の工程を経て、マイタケの子実体原基が形成されて5日ほど経過した菌床9を配置した。
【0116】
具体的には、光照射装置3aとしてアイショートアーク型のキセノンランプ(300W)を採用した。
【0117】
前記キセノンランプの照射光には可視光線以外の波長が含まれるため、あらかじめ光学フィルタを用いて紫外域(400nm以下)と赤外域(700nm以上)の波長を除去した照射光を用いた。
【0118】
前記照射光を特定の干渉フィルタを透過させることで、単色光(特定波長の光)とし、この前記特定波長の光を集光レンズで集光し、この集光した光を光ファイバでマイタケの上部に照射した。
【0119】
また、光の照射は、波長を400〜680nmの範囲で変化させ、強度を光量子束密度35μmol/m2/sに設定して行い、マイタケの生体電位の変化量を計測した。
【0120】
また、生体電位の計測は、上述した本実施例のマイタケの栽培方法に順じて行った。
【0121】
図6に示すように、マイタケは青色領域(430〜470nm)付近で生体電位の変化が大きく、緑・黄色領域(480〜570nm)付近では徐々に小さくなり、赤色領域(610nm)付近ではほぼ変化を示さない結果を得ている。
【0122】
従って、図7に示すように、青色領域(430〜470nm)下で栽培したマイタケは形態形成が良好となるといえる。
【0123】
(実験例3)
実験例3は、光の強度がマイタケの形態形成にどのような影響を与えるのかを確認したものである。
【0124】
栽培室4内は室温18℃、湿度95%に調整し、実施例の(1)〜(4)の工程を経て、マイタケの子実体原基が形成されて5日ほど経過した菌床9を配置した。
【0125】
また、前記各菌床9はラボジャッキに載置する。
【0126】
具体的には、光照射装置3aとして青色発光ダイオード(放射束密度6W/m2)を採用する。この青色発光ダイオードを複数取り付けたパネルを栽培室の上部に配置する。
【0127】
また、光の強度(放射束密度)の変化は、子実体頂点の光強度が常に所定強度となるよう菌床9の高さと前記光照射装置3aとの距離をラボジャッキを上下動調節することで行う。
【0128】
前記菌床9頂点の光強度が3,4,6,8,10W/m2になるように設定し、光を照射し、マイタケの生体電位の変化量を計測した。
【0129】
また、生体電位の計測は、上述した本実施例のマイタケの栽培方法に順じて行った。
【0130】
図8に示すように、子実体の生体電位応答は光の強度に比例することを確認している。
【0131】
(実験例4)
実験例4は、栽培室4内の温度がマイタケの形態形成にどのような影響を与えるのかを確認したものである。
【0132】
栽培室4内には、実施例の(1)〜(4)の工程を経て、マイタケの子実体原基が形成されて5日ほど経過した菌床9を配置した。
【0133】
光の照射は、上述した本実施例のマイタケの栽培方法に順じて行った。
【0134】
また、栽培室4内の温度は、ペルチェ素子3bにより、一般に生産現場で設定されている温度である16℃〜22℃に変化させた。
【0135】
具体的にはペルチェ素子3bをコンピュータ5により制御して栽培室4内の温度を16℃、18℃、20℃、22℃の順に変化させ、これを1クルーとし、各温度を24〜36時間程度維持して栽培する過程で、マイタケの生体電位の変化を観察した。尚、実験は5個のマイタケに対して行った。
【0136】
また、生体電位の計測は、上述した本実施例のマイタケの栽培方法に順じて行った。
【0137】
【表2】

【0138】
表2及び図9に示すように、光の照射条件が同じ場合には、栽培室4内の温度を18℃に設定した場合に、マイタケの生体電位の変化が最も大きく光刺激に対する生体電位応答がみられることを確認した。
【0139】
また、生体電位の変化が最も大きな18℃で栽培した場合、14℃で栽培した場合夫々のマイタケの栽培終了時の形態形成を図10に示し、夫々の収穫時の重さ(新鮮重)を表3に示す。
【0140】
また、子実体上面の縦幅、横幅について比較したものを表4に示す(表4中、Aは14℃で栽培した場合、Bは18℃で栽培した場合を示す。)。
【0141】
【表3】

【0142】
【表4】

【0143】
従って、本実施例は栽培室4内の温度が18℃の場合に最もマイタケの生体電位の変化が大きく、この温度下のマイタケは形態形成が良好となるといえる。
【0144】
(実験例5)
実験例5は、栽培室4内の二酸化炭素濃度が形態形成にどのような影響を与えるのかを確認したものである。
【0145】
栽培室4内は室温18℃、湿度95%、二酸化炭素濃度500〜800ppmに調整し、実施例の(1)〜(4)の工程を経て、マイタケの子実体原基が形成されて5日ほど経過した菌床9を配置した。
【0146】
前記二酸化炭素濃度は気体濃度制御装置3dで栽培室4内の気体濃度が均一になるように、栽培室4内外の空気を一旦エアバッファ3d内に集め、ACファンによりダクトを通して栽培室4に空気を送りこんで制御する。
【0147】
また、光照射装置3aとして青色発光ダイオード(放射束密度6W/m2)を採用する。この青色発光ダイオードを複数取り付けたパネルを栽培室の上部に配置する。
【0148】
また、光照射は30分ON/OFFを繰り返し行い、マイタケの生体電位を継続して計測した。
【0149】
計測開始から7時間後に、栽培室4の二酸化炭素濃度を5000ppmを超える濃度に上昇させ、この状態を10時間維持し、生体電位を継続して計測した。
【0150】
その後、予め栽培室4の二酸化炭素濃度を500ppmから800ppmになるようにコンピュータ5に設定した状態で、栽培室4の窓を開放することで換気を行い、栽培室4の二酸化炭素濃度が前記設定値になったところで栽培室4の窓を閉じ、生体電位を継続して計測した。
【0151】
また、生体電位の計測は、上述した本実施例のマイタケの栽培方法に順じて行った。
【0152】
その結果、図11に示すように、栽培室4が高濃度の二酸化炭素条件下になることで子実体の生体電位は急激に低下し、一定条件の光刺激に対する生体電位応答は見られなくなることを確認した。
【0153】
またその後、図12に示すように、換気を行うことによって、栽培室の二酸化炭素濃度が前記設定値に低下すると、数時間後に再び光刺激に対する生体電位応答が回復したことを確認している。
【0154】
従って、高濃度の二酸化炭素条件下では子実体の生長が阻害され、子実体の生体電位応答と形態形成との関連性が示唆された。
【図面の簡単な説明】
【0155】
【図1】本実施例の栽培装置の概略説明図である。
【図2】本実施例の電極部を挿入した後、子実体になった状態の写真である。
【図3】本実施例の生体電位の変化に応じた制御のフローチャートである。
【図4】実験例1の説明図である。
【図5】実験例1の結果を示すグラフ図である。
【図6】実験例2の光の波長と生体電位変化量との関係を示すグラフ図である。
【図7】実験例2の光の波長(青色光と赤色光)が形態形成に与える影響を比較したマイタケの写真である。
【図8】実験例3の光の強度と生体電位変化量との関係を示すグラフ図である。
【図9】実験例4の環境温度が生体電位に与える影響を示すグラフ図である。
【図10】実験例4の環境温度(14℃と18℃)が形態形成に与える影響を比較したマイタケの写真である。
【図11】実験例5の二酸化炭素濃度が生体電位応答に与える影響を示すグラフ図である。
【図12】実験例5の換気後の二酸化炭素濃度が生体電位応答に与える影響を示すグラフ図である。
【符号の説明】
【0156】
2 生体電位計測装置
2A 電極部
2B 増幅部
3 環境刺激付与装置
3a 光照射装置
3b 温度制御装置
3c 加湿装置
3d 気体濃度制御装置
【特許請求の範囲】
【請求項1】
きのこに環境刺激を与えた際のきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとに、きのこを栽培することを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項2】
請求項1記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記確知した生体電位の変化をもとに、きのこに環境刺激を与えるか若しくは与えないかを決定して当該きのこを栽培することを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項3】
請求項1,2いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記確知する生体電位の変化とは、所定時間におけるきのこの生体電位の傾きであり、この傾きが正ならば前記きのこに環境刺激を与え、負ならば前記きのこに環境刺激を与えないようにすることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項4】
請求項3記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記傾きが正である場合、予め設定された上限値以上となるまでは環境刺激を与えず、上限値以上となったら環境刺激を与え、また、前記傾きが負である場合、予め設定された下限値以下になるまでは環境刺激を与え、下限値以下となったら環境刺激を与えないようにすることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項5】
請求項1〜4いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激は環境刺激付与装置により与え、前記生体電位の変化の確知は生体電位計測装置により行うことを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項6】
請求項5記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記生体電位計測装置は、生体電位を計測する電極部及び該電極部により計測された生体電位を増幅する増幅部を具備するものであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項7】
請求項1〜6いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、複数個のきのこを栽培する場合、当該栽培する一部のきのこの生体電位の変化の確知を行うことを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項8】
請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置は、きのこに光を照射する光照射装置であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項9】
請求項8記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記光は、所定の光質であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項10】
請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置は、きのこを所定の温度に調整する温度制御装置であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項11】
請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置は、きのこに所定の湿気を加える加湿装置であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項12】
請求項1〜7記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置は、栽培雰囲気中の気体濃度を調整する気体濃度制御装置であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項1】
きのこに環境刺激を与えた際のきのこの生体電位の変化を確知し、この確知した生体電位の変化をもとに、きのこを栽培することを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項2】
請求項1記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記確知した生体電位の変化をもとに、きのこに環境刺激を与えるか若しくは与えないかを決定して当該きのこを栽培することを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項3】
請求項1,2いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記確知する生体電位の変化とは、所定時間におけるきのこの生体電位の傾きであり、この傾きが正ならば前記きのこに環境刺激を与え、負ならば前記きのこに環境刺激を与えないようにすることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項4】
請求項3記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記傾きが正である場合、予め設定された上限値以上となるまでは環境刺激を与えず、上限値以上となったら環境刺激を与え、また、前記傾きが負である場合、予め設定された下限値以下になるまでは環境刺激を与え、下限値以下となったら環境刺激を与えないようにすることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項5】
請求項1〜4いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激は環境刺激付与装置により与え、前記生体電位の変化の確知は生体電位計測装置により行うことを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項6】
請求項5記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記生体電位計測装置は、生体電位を計測する電極部及び該電極部により計測された生体電位を増幅する増幅部を具備するものであることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項7】
請求項1〜6いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、複数個のきのこを栽培する場合、当該栽培する一部のきのこの生体電位の変化の確知を行うことを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項8】
請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置は、きのこに光を照射する光照射装置であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項9】
請求項8記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記光は、所定の光質であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項10】
請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置は、きのこを所定の温度に調整する温度制御装置であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項11】
請求項1〜7いずれか1項に記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置は、きのこに所定の湿気を加える加湿装置であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【請求項12】
請求項1〜7記載のきのこを生体センサーとして用いたきのこ栽培方法において、前記環境刺激付与装置は、栽培雰囲気中の気体濃度を調整する気体濃度制御装置であることを特徴とするきのこを生体センサーとして用いたきのこ栽培方法。
【図1】


【図3】


【図4】


【図5】


【図6】


【図8】


【図9】


【図11】


【図12】


【図2】


【図7】


【図10】




【図3】


【図4】


【図5】


【図6】


【図8】


【図9】


【図11】


【図12】


【図2】


【図7】


【図10】


【公開番号】特開2007−222164(P2007−222164A)
【公開日】平成19年9月6日(2007.9.6)
【国際特許分類】
【出願番号】特願2007−20135(P2007−20135)
【出願日】平成19年1月30日(2007.1.30)
【出願人】(593084915)株式会社雪国まいたけ (30)
【Fターム(参考)】
【公開日】平成19年9月6日(2007.9.6)
【国際特許分類】
【出願日】平成19年1月30日(2007.1.30)
【出願人】(593084915)株式会社雪国まいたけ (30)
【Fターム(参考)】
[ Back to top ]

