グリシントランスポーター阻害物質
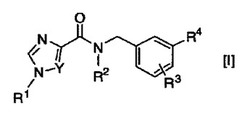
本発明は、グリシン取り込み阻害作用に基づいた統合失調症、アルツハイマー病、認知機能障害、認知症、不安障害(全般性不安障害、パニック障害、強迫性障害、社会不安障害、外傷後ストレス障害、特定の恐怖症、急性ストレス障害等)、うつ病、薬物依存、痙攣、振戦、疼痛、又は睡眠障害等の疾患の予防又は治療に有用な式[I]で表される新規な化合物又はその医薬上許容される塩を提供することを目的とする。
【化1】

【化1】

【発明の詳細な説明】
【技術分野】
【0001】
本発明は、グリシントランスポーター阻害作用を有する化合物に関する。
【背景技術】
【0002】
グルタミン酸受容体の一つであるNMDA受容体は脳内の神経細胞膜上に存在しており、神経の可塑性、認知、注意、記憶など様々な神経生理学的な現象に関わっている。NMDA受容体には複数のアロステリック結合部位が存在し、グリシン結合部位もその一つである(NMDA受容体複合体グリシン結合部位)。NMDA受容体複合体グリシン結合部位はNMDA受容体の活性化に関与していることが報告されている(非特許文献1)。
【0003】
グリシン作動性神経のシナプス前終末に活動電位が到達するとシナプス間隙へのグリシンの放出が開始される。放出されたグリシンはシナプス後部の受容体等と結合した後、トランスポーターによりシナプス間隙から取り除かれる。このことよりグリシンのトランスポーターは細胞外液にあるグリシン量を調節することでNMDA受容体の機能を調節していると考えられている。
【0004】
グリシントランスポーター(GlyT)は細胞外グリシンの細胞内への再取り込みに関わっているタンパクであり、現在までにGlyT1及びGlyT2の二つのサブタイプの存在が明らかとなっている。GlyT1は主に大脳皮質、海馬及び視床等に発現しており、統合失調症、アルツハイマー病、認知機能障害、認知症、不安障害(全般性不安障害、パニック障害、強迫性障害、社会不安障害、外傷後ストレス障害、特定の恐怖症、急性ストレス障害等)、うつ病、薬物依存、痙攣、振戦、疼痛、及び睡眠障害等の疾患との関連が報告されている(非特許文献2〜4)。
【0005】
GlyT1阻害作用を有し、5員環ヘテロアリールアミド構造をもつ化合物は以下の特許文献において報告がされている(特許文献1〜3)。これらの特許文献1〜3及び非特許文献5,6に記載された化合物は、該アミド構造の窒素原子に、窒素含有基が結合していることを特徴とする化合物である。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】WO2005/037216
【特許文献2】WO2006/106425
【特許文献3】WO2008/065500
【非特許文献】
【0007】
【非特許文献1】Molecular Psychiatry (2004) 9, 984-997
【非特許文献2】Current Medicinal Chemistry, 2006, 13, 1017-1044
【非特許文献3】Neuropsychopharmacology (2005), 1-23
【非特許文献4】Expert Opinion on Therapeutic Patents (2004) 14 (2) 201-214
【非特許文献5】Bioorganic & Medicinal Chemistry Letters (2009) 19 2974-2976
【非特許文献6】Bioorganic & Medicinal Chemistry Letters (2010) 20 907-911
【発明の概要】
【発明が解決しようとする課題】
【0008】
本発明は、グリシン取り込み阻害作用に基づいた統合失調症、アルツハイマー病、認知機能障害、認知症、不安障害(全般性不安障害、パニック障害、強迫性障害、社会不安障害、外傷後ストレス障害、特定の恐怖症、急性ストレス障害等)、うつ病、薬物依存、痙攣、振戦、疼痛、又は睡眠障害等の疾患の予防又は治療に有用な新規な化合物又はその医薬上許容される塩を提供することを目的とする。
【課題を解決するための手段】
【0009】
本発明者らはGlyT1に対し阻害作用を有する新規な骨格の化合物につき鋭意検討した結果、下記に示す式で表される化合物が優れたGlyT1阻害物質であることを見出し、本発明を完成するに至った。
【0010】
以下、本発明を詳細に説明する。本発明の態様(以下、「本発明化合物」という)は以下に示すものである。
(1)式[I]
【0011】
【化1】

(式中、
R1は、水素原子、又はC1-6アルキル基を示し、
R2は、C1-6アルキル基、C2-6アルケニル基、C3-6シクロアルキル基、C1-6ハロアルキル基、C1-6ヒドロキシアルキル基、又はC1-6アルコキシC1-6アルキル基を示し、
R3は、水素原子、C1-6アルキル基、C1-6アルコキシ基、C1-6ハロアルキル基、C1-6ハロアルコキシ基、又はハロゲン原子を示し、
R4は、フェニル基を示し、
該フェニル基は、C1-6アルキル基、C1-6アルコキシ基、C1-6ハロアルキル基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、C1-6アルコキシC1-6アルキル基、C2-7アルコキシカルボニル基、シアノ基、及びハロゲン原子から選択される1から3個の置換基で置換されてもよく、
Yは、式CH、又は
窒素原子を示す。)で表される化合物又はその医薬上許容される塩。
(2)R2が分岐C3-6アルキル基、又はC3-6シクロアルキル基である上記(1)に記載の化合物又はその医薬上許容される塩。
(3)Yが式CHである上記(1)又は(2)に記載の化合物又はその医薬上許容される塩。
(4)R3がハロゲン原子である上記(1)〜(3)のいずれか1つに記載の化合物又はその医薬上許容される塩。
(5)R3がフッ素原子である上記(1)〜(3)のいずれか1つに記載の化合物又はその医薬上許容される塩。
(6)R4が、フェニル基、又はC1-6アルコキシ基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、及びハロゲン原子から選択される1〜3個の置換基で置換されたフェニル基である上記(1)〜(5)のいずれか1つに記載の化合物又はその医薬上許容される塩。
(7)
式[I]の化合物が下式:
【化2】

(式中、
R1は、メチル基、又はエチル基を示し、
R4は、フェニル基、又は
C1-6アルコキシ基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、及びハロゲン原子から選択される1から3個の置換基で置換されたフェニル基を示す)で表される上記(1)に記載の化合物又はその医薬上許容される塩。
(8)
化合物が、
N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[6-フルオロ-3'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-[(4',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(3',6-ジフルオロ-4'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(3',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロ-3'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロ-4'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(4'-クロロ-6-フルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',5',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-{[3'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[4'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',5',6-テトラフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、又は
1-エチル-N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド
である上記(1)に記載の化合物又はその医薬上許容される塩。
(9)
化合物が、
N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[6-フルオロ-3'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-[(4',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[3'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[4'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',5',6-テトラフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、又は
1-エチル-N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド
である上記(1)に記載の化合物又はその医薬上許容される塩。
(10)上記(1)〜(9)のいずれか1つに記載の化合物又はその医薬上許容される塩を有効成分として含む医薬。
(11)上記(1)〜(9)のいずれか1つに記載の化合物又はその医薬上許容される塩を有効成分として含む、統合失調症、アルツハイマー病、認知機能障害、認知症、不安障害、うつ病、薬物依存、痙攣、振戦、又は睡眠障害の疾患の予防剤又は治療剤。
【発明の効果】
【0012】
本発明化合物はグリシントランスポーター(GlyT1)阻害活性を有する。また、本発明化合物は、以下の試験例で示すように高い膜透過性を示すため、経口投与する医薬にとって重要である腸管吸収に優れることが期待される。さらに、本発明化合物は、以下の試験例で示すように、薬物の脳移行性を制御している排出トランスポーターであるP−糖タンパク質の基質として認識されないため、良好な脳移行性が期待される。
【発明を実施するための形態】
【0013】
本明細書において用いる「C1-6アルキル基」とは直鎖状又は分岐鎖状の炭素数1〜6個のアルキル基を意味し、例えばメチル、エチル、プロピル、イソプロピル、ブチル、イソブチル、tert−ブチル、ペンチル、イソペンチル、ヘキシルを挙げることができる。
【0014】
本明細書において用いる「C2-6アルケニル基」とは直鎖状又は分岐鎖状の炭素数2〜6個のアルケニル基を意味し、例えばビニル、アリル、ブタ−2−エニル、プロパ−1−エン−2−イルを挙げることができる。
【0015】
本明細書において用いる「C3-6シクロアルキル基」とは炭素数3〜6個のシクロアルキル基を意味し、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基である。
【0016】
本明細書において用いる「C1-6アルコキシ基」とは直鎖状又は分岐鎖状の炭素数1〜6個のアルコキシ基を意味し、例えばメトキシ、エトキシ、プロポキシ、イソプロポキシ、ブトキシ、イソブトキシ、ペンチルオキシ、イソペンチルオキシ、ヘキシルオキシを挙げることができる。
【0017】
本明細書において用いる「C1-6アルコキシC1-6アルキル基」とはC1-6アルコキシ基で置換されたC1-6アルキル基を示し、例えば、メトキシメチル、メトキシエチル、メトキシプロピル、メトキシブチル、メトキシペンチル、メトキシヘキシル、エトキシメチル、エトキシエチル、エトキシプロピル、イソプロポキシメチル、イソプロポキシエチル、イソプロポキシプロピル、1-メトキシエチル、1-エトキシエチル、2-メトキシプロピル、2-エトキシプロピルを挙げることができる。
【0018】
本明細書において用いる「ハロゲン(ハロ)」とは、フッ素原子、塩素原子、臭素原子、ヨウ素原子である。
【0019】
本明細書において用いる「C1-6ハロアルキル基」とはハロゲン原子で置換された直鎖状又は分岐鎖状の炭素数1〜6個のアルキル基を意味し、ハロゲン原子の好ましい置換数は1〜3個であり、例えばフルオロメチル、ジフルオロメチル、トリフルオロメチル、トリクロロメチルを挙げることができる。
【0020】
本明細書において用いる「C1-6ハロアルコキシ基」とはハロゲン原子で置換された直鎖状又は分岐鎖状の炭素数1〜6個のアルコキシ基を意味し、ハロゲン原子の好ましい置換数は1〜3個であり、例えばフルオロメトキシ、ジフルオロメトキシ、トリフルオロメトキシを挙げることができる。
【0021】
本明細書において用いる「C1-6ヒドロキシアルキル基」とはヒドロキシ基で置換された直鎖状又は分岐鎖状の炭素数1〜6個のアルキル基を意味し、例えば、ヒドロキシメチル、2−ヒドロキシエチル、1−ヒドロキシエチル、3−ヒドロキシプロピル、2−ヒドロキシプロピル、1−ヒドロキシプロピルを挙げることができる。
【0022】
本明細書において用いる「C2-7アルコキシカルボニル基」とは、鎖状又は分岐鎖状の炭素数2〜7個のアルコキシカルボニル基を示し、例えば、メトキシカルボニル、エトキシカルボニル、プロポキシカルボニル、イソプロポキシカルボニル、ブトキシカルボニル、イソブトキシカルボニルを挙げることができる。
【0023】
本明細書中における「医薬上許容される塩」とは、薬剤的に許容することのできる酸付加塩を意味し、用いられる酸としては、硫酸、塩酸、臭化水素酸、硝酸及びリン酸等の無機酸、或いは、酢酸、シュウ酸、乳酸、クエン酸、リンゴ酸、グルコン酸、酒石酸、フマール酸、マレイン酸、メタンスルホン酸、エタンスルホン酸、ベンゼンスルホン酸及びp−トルエンスルホン酸等の有機酸を挙げることができる。遊離体から当該塩への変換は従来の方法で行うことができる。
【0024】
本発明化合物において、好ましい態様を以下にあげる。
R2は、好ましくは、分岐C3-6アルキル基、又はC3-6シクロアルキル基であり、より好ましくは、分岐C3-6アルキル基である。
R3は、好ましくはハロゲン原子であり、より好ましくはフッ素原子である。R3の
より好ましい例がフッ素原子である場合、式(I)化合物はより好ましくは下記式によって表される。
【化3】

R1は、好ましくはC1-6アルキル基であり、より好ましくはメチル基又はエチル基であり、さらにより好ましくはメチル基である。
R4は、好ましくは、フェニル基、又はC1-6アルコキシ基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、及びハロゲン原子から選択される1から3個の置換基で置換されたフェニル基である。
【0025】
本発明化合物は複数の不斉中心を含むことができる。従って前記化合物は光学活性体で存在するとともにそのラセミ体でも存在することができ、さらに複数のジアステレオマーも存在することができる。前記の全ての形態は本発明の範囲内に含まれる。個々の異性体は公知の方法、例えば光学活性な出発物質若しくは中間体の使用、中間体若しくは最終生成物の製造における光学選択的な反応又はジアステレオ選択的な反応、或いは中間体又は最終生成物の製造におけるクロマトグラフィーを用いた分離等により得ることが可能である。さらに、本発明化合物が水和物又は溶媒和物を形成する場合、それらも本発明の範囲内に含まれる。同様に、本発明化合物の水和物又は溶媒和物の医薬上許容される塩も本発明の範囲内に含まれる。
【0026】
本発明の他の態様は、以下に示す通りである。
(A)式[I]
【化4】

(式中、
R1は、水素原子、又はC1-6アルキル基を示し、
R2は、C1-6アルキル基、C3-6シクロアルキル基、C1-6ハロアルキル基、又はC1-6アルコキシC1-6アルキル基を示し、
R3は、水素原子、又はハロゲン原子を示し、
R4は、フェニル基を示し、
該フェニル基は、C1-6アルキル基、C1-6アルコキシ基、C1-6ハロアルキル基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、C1-6アルコキシC1-6アルキル基、C2-6アルコキシカルボニル基、シアノ基、及びハロゲン原子から選択される1から3個の置換基で置換されてもよく、
Yは、窒素原子、又は
式CHを示す。)で表される化合物又はその医薬上許容される塩。
(B)R1がC1-6アルキル基であり、
Yが式CHである上記(A)に記載の化合物又はその医薬上許容される塩。
(C)R1がC1-6アルキル基であり、
Yが窒素原子である上記(A)に記載の化合物又はその医薬上許容される塩。
(D)R3がハロゲン原子である上記(A)〜(C)のいずれかに記載の化合物又はその医薬上許容される塩。
(E)R3がフッ素原子である上記(A)〜(C)のいずれかに記載の化合物又はその医薬上許容される塩。
(F)R2が、C1-6アルキル基、又はC3-6シクロアルキル基である上記(A)〜(E)のいずれかに記載の化合物又はその医薬上許容される塩。
(G)R2が、C1-6アルコキシC1-6アルキル基である上記(A)〜(E)のいずれかに記載の化合物又はその医薬上許容される塩。
【0027】
本発明に係る化合物は、経口又は非経口的に投与することができる。その投与剤型は錠剤、カプセル剤、顆粒剤、散剤、粉剤、トローチ剤、軟膏剤、クリーム剤、乳剤、懸濁剤、坐剤、注射剤等であり、いずれも慣用の製剤技術(例えば、第15改正日本薬局方に規定する方法等)によって製造することができる。これらの投与剤型は、患者の症状、年齢及び治療の目的に応じて適宜選択することができる。
これらの製剤は、本発明の化合物を含有する組成物に薬理学的に許容されるキャリヤー、すなわち、賦形剤(例えば、結晶セルロース、デンプン、乳糖、マンニトール)、結合剤(例えば、ヒドロキシプロピルセルロース、ポリビニルピロリドン)、滑沢剤(例えば、ステアリン酸マグネシウム、タルク)、崩壊剤(例えば、カルボキシメチルセルロースカルシウム)、および/またはその他薬理学的に許容される各種添加剤を配合し、製造することができる。
【0028】
また、本発明の化合物を1以上の他の治療薬、種々の抗精神病薬(antipsychotics)、抗うつ薬、例えば、5HT3アンタゴニスト、5HT2アンタゴニスト、セロトニンアゴニスト、NK−1アンタゴニスト、選択的セロトニン再取込阻害薬(SSRI)、セロトニンノルアドレナリン再取込阻害薬(SNRI)、三環系抗うつ薬、ドーパミン作動性抗うつ薬、H3アンタゴニスト、5HT1Aアンタゴニスト、5HT1Bアンタゴニスト、5HT1Dアンタゴニスト、D1アゴニスト、M1アゴニスト、抗けいれん薬、認知機能増強薬、および、その他向精神薬(psychoactive drug)と共に使用してもよい。
【0029】
本発明の化合物と組み合わせて共に使用してもよい他の治療薬とは、例えばオンダンセトロン(ondansetron)、グラニセトロン(granisetron)、メトクロプラミド(metoclopramide)、スマトリプタン(sumatriptan)、ラウオルシン(rauwolscine)、ヨヒムビン(yohimbine)、メトクロプラミド(metoclopramide)、フルオキセチン(fluoxetine)、シタロプラム(citalopram)、エスシタロプラム(escitalopram)、フェモキセチン(femoxetine)、フルボキサミン(fluvoxamine)、パロキセチン(paroxetine)、インダルピン(indalpine)、サートラリン(sertraline)、ジメルジン(zimeldine)、ベンラファキシン(venlafaxine)、レボキセチン(reboxetine)、ミルナシプラン(Milnacipran)、デュロキセチン(duloxetine)、イミプラミン(imipramine)、アミトリプチリン(amitriptiline)、クロミプラミン(chlomipramine)、ノルトリプチリン(nortriptiline)、ブプロピオン(bupropion)、アミネプチン(amineptine)、ジバルプロエクス(divalproex)、カルバマゼピン(carbamazepine)、ジアゼパム(diazepam)、リスペリドン(risperidone)、オランザピン(olanzapine)、ジプラシドン(ziprasidone)、アリピプラゾール(aripiprazole)、クエチアピン(quetiapine)、ペロスピロン(perospirone)、クロザピン(clozapine)ハロペリドール(haloperidol)、ピモジド(pimozide)、ドロペリドール(droperidol)、クロルプロマジン(chlorpromazine)、チオリダジン(thioridazine)、メソリダジン(mesoridazine)、トリフルオペラジン(trifluoperazine)、ペルフェナジン(perphenazine)、フルフェナジン(fluphenazine)、チフルプロマジン(thiflupromazine)、プロクロルペラジン(prochlorperazine)、アセトフェナジン(acetophenazine)、チオチキセン(thiothixene)、クロルプロチキセン(chlorprothixene)、ラモトリジン(lamotrigine)、ロキサピン(loxapine)、モリンドン(molindone)等を挙げることができる。これら組み合わせは、同時に(同一の医薬処方において、または異なる医薬処方において)、別々に、または連続的に投与されればよい。
【0030】
本発明の化合物の組み合わせによる使用および治療方法に関連する特に有利な点には、個々の成分の通常使用される投与量よりも少ない投与量での同等または改善された効果を挙げることができる。また、精神障害の陽性症状および/または陰性症状および/または認知機能障害に対する治療効果のさらなる増強も期待される。本発明の組み合わせによる使用および治療方法は、ある種の神経弛緩薬での治療に十分に応答しない、または該治療に耐性のある患者の治療においても利益を提供しうる。
【0031】
本発明に係る化合物の投与量は、成人を治療する場合で1日1〜2000mgであり、これを1日1回又は数回に分けて投与する。この投与量は、患者の年齢、体重及び症状によって適宜増減することができる。
【0032】
式[I]の化合物は種々の合成方法によって製造することができる。以下の方法は、本発明化合物の製造法の例示であり、これに限定されるものではない。
【0033】
以下の一般的製造法中、「不活性溶媒」とは例えばメタノール、エタノール、イソプロパノール、n−ブタノール、エチレングリコール等のアルコール類、ジエチルエーテル、t−ブチルメチルエーテル、ジイソプロピルエーテル、テトラヒドロフラン、1,4−ジオキサン、1,2−ジメトキシエタン等のエーテル類、ペンタン、ヘキサン、ヘプタン、トルエン、ベンゼン、キシレン等の炭化水素類、酢酸エチル、ギ酸エチル等のエステル類、アセトン、メチルエチルケトン等のケトン類、クロロホルム、ジクロロメタン等のハロゲン化炭素系溶媒、ジメチルホルムアミド、N-メチルピロリドン等のアミド類、アセトニトリル、ジメチルスルホキシド、水又はこれらの混合溶媒等である。
【0034】
「塩基」とは例えば、水素化リチウム、水素化ナトリウム、水素化カリウム、水素化カルシウムなどのアルカリ金属又はアルカリ土類金属の水素化物;リチウムアミド、ナトリウムアミド、リチウムジイソプロピルアミド、リチウムジシクロヘキシルアミド、リチウムヘキサメチルジシラジド、ナトリウムヘキサメチルジシラジド、カリウムヘキサメチルジシラジドなどのアルカリ金属又はアルカリ土類金属のアミド;ナトリウムメトキシド、ナトリウムエトキシド、カリウム tert−ブトキシドなどのアルカリ金属又はアルカリ土類金属の低級アルコキシド;ブチルリチウム、sec−ブチルリチウム、tert−ブチルリチウム、メチルリチウムなどのアルキルリチウム;水酸化ナトリウム、水酸化カリウム、水酸化リチウム、水酸化バリウムなどのアルカリ金属又はアルカリ土類金属の水酸化物;炭酸ナトリウム、炭酸カリウム、炭酸セシウムなどのアルカリ金属又はアルカリ土類金属の炭酸塩;炭酸水素ナトリウム、炭酸水素カリウムなどのアルカリ金属又はアルカリ土類金属の炭酸水素塩;トリエチルアミン、N−メチルモルホリン、N,N−ジイソプロピルエチルアミン、1,8−ジアザビシクロ[5.4.0]ウンデカ−7−エン(DBU)、1,5−ジアザビシクロ[4.3.0]ノン−5−エン(DBN)、N,N−ジメチルアニリンなどのアミン;ピリジン、イミダゾール、2,6−ルチジンなどの塩基性ヘテロ環化合物などである。これらの塩基は当業者に公知である種々の反応条件に応じて適宜選択される。
【0035】
「酸」とは例えば、塩酸、臭化水素酸、硫酸、硝酸、リン酸などの無機酸及びp−トルエンスルホン酸、メタンスルホン酸、トリフルオロ酢酸、ギ酸、酢酸、クエン酸、シュウ酸などの有機酸である。これらの酸は当業者に公知である種々の反応条件に応じて適宜選択される。
「ルイス酸」とは例えば、三フッ化ホウ素、三塩化アルミニウム、四塩化チタン、三塩化鉄、塩化亜鉛、四塩化スズなどをあげることができる。
【0036】
一般的製造法1
【0037】
【化5】

【0038】
式中、X1は、臭素原子、ヨウ素原子、またはトリフルオロメタンスルホニルオキシ基を示し、その他の記号は前記と同義である。
【0039】
工程1:不活性溶媒中、塩基の存在下又は非存在下、パラジウム触媒及び必要に応じてパラジウム触媒の配位子を使用することにより化合物(1)に対して化合物(2)を反応させることにより、本発明化合物(I)を得ることができる。
【0040】
ここで、パラジウム触媒とは、例えば酢酸パラジウム、トリス(ジベンジリデンアセトン)ジパラジウム、テトラキス(トリフェニルホスフィン)パラジウム、ジクロロビス(トリフェニルホスフィン)パラジウム、(1,3−ジイソプロピルイミダゾール−2−イリデン)(3−クロロピリジル)パラジウム(II)二塩化物、[1,3−ビス(2,6−ジイソプロピルフェニル)イミダゾール−2−イリデン](3−クロロピリジル)パラジウム(II)二塩化物、塩化〔1,1’−ビス(ジフェニルホスフィノ)フェロセン〕パラジウム等を挙げることができ、配位子とは例えばトリフェニルホスフィン、2,2−ビス(ジフェニルホスフィノ)−1,1−ビナフチル(BINAP)、2−(ジ−tert−ブチルホスフィノ)ビフェニル、9,9−ジメチル−4,5−ビス(ジフェニルホスフィノ)キサンテン(Xantphos)等を挙げることができ、化合物(2)の例としては、R4MgClなどのGrignard反応剤、R4ZnClなどの亜鉛反応剤、R4とホウ酸又はホウ酸エステルが結合したものなどのホウ素反応剤やR4SnBu3などのスズ反応剤などが挙げられる。
【0041】
一般的製造法2
【0042】
【化6】

【0043】
式中、X2は、ハロゲン原子又はヒドロキシ基を示し、その他の記号は前記と同義である。
【0044】
工程2:不活性溶媒中、塩基存在下又は非存在下、化合物(3)とX2がハロゲン原子である化合物(4)を反応させ、本発明化合物(I)を得ることができる。或いは化合物(3)とX2が水酸基である化合物(4)を当業者に公知である種々のアミド化反応に供することにより、本発明化合物(I)を得ることができる。ここでアミド化反応とは、例えば不活性溶媒中、塩基存在下又は非存在下、O−(7−アザベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウム ヘキサフルオロリン酸(HATU)、O−(ベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウム ヘキサフルオロリン酸(HBTU)、N,N’−ジシクロヘキシルカルボジイミド(DCC)、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩(EDC・HCl)、ジフェニルホスホリルアジド(DPPA)又はカルボニルジイミダゾール(CDI)などの縮合剤を用いたアミド化反応、クロロ炭酸エチル、クロロ炭酸イソブチル又はトリメチルアセチルクロリドなどを用いた混合酸無水物経由のアミド化反応などである。ここで縮合剤を用いたアミド化反応の際、必要に応じて1−ヒドロキシベンゾトリアゾール(HOBt)、ヒドロキシスクシンイミド(HOSu)などの添加剤を使用することができる。
【0045】
一般的製造法3
【0046】
【化7】

【0047】
式中、Lは、ハロゲン原子、メタンスルホニルオキシ基、トリフルオロメタンスルホニルオキシ基又はp−トルエンスルホニルオキシ基などの脱離基を示し、Raは、C1-6アルキル基を示し、その他の記号は前記と同義である。
【0048】
工程3:不活性溶媒中、塩基存在下又は非存在下、化合物(5)と化合物(6)を反応させることにより、本発明化合物(I−1)を得ることができる。
【0049】
一般的製造法4
【0050】
【化8】

【0051】
式中の記号は前記と同義である。
【0052】
工程4:不活性溶媒中、塩基存在下又は非存在下、本発明の化合物(I-2)と化合物(7)を反応させることにより、本発明化合物(I−1)を得ることができる。
【0053】
一般的製造法5
【0054】
【化9】

【0055】
工程5:一般的製造法2の工程2と同様の方法で化合物(8)と化合物(4)から化合物(1)を合成することができる。
【0056】
一般的製造法6
【0057】
【化10】

【0058】
工程6:不活性溶媒中、酸存在下又は非存在下、還元剤を用いて、化合物(9)と化合物(10)を還元的アミノ化反応に供することにより化合物(8)を得ることができる。ここで還元剤とは例えば、水素化トリアセトキシホウ素ナトリウム、水素化シアノホウ素ナトリウム、水素化ホウ素ナトリウムなどである。
【0059】
工程7:一般的製造法1の工程1と同様の方法で化合物(8)と化合物(2)から化合物(3)を合成することができる。
【0060】
工程8:一般的製造法1の工程1と同様の方法で化合物(9)と化合物(2)から化合物(11)を合成することができる。
【0061】
工程9:一般的製造法6の工程6と同様の方法で化合物(11)と化合物(10)から化合物(3)を合成することができる。
【0062】
一般的製造法7
【0063】
【化11】

【0064】
式中、RbおよびRcは、独立して水素原子、C1-6アルキル基、C1-6ハロアルキル基、又はC1-6アルコキシC1-6アルキル基を示し、或いはRbとRcは結合する炭素原子と一緒になってC3-6シクロアルキル環を形成してもよい。
【0065】
工程10:一般的製造法6の工程6と同様の方法で化合物(12)と化合物(13)から化合物(8)を合成することができる。
【0066】
工程11:一般的製造法1の工程1と同様の方法で化合物(8)と化合物(2)から化合物(3)を合成することができる。
【0067】
工程12:一般的製造法1の工程1と同様の方法で化合物(12)と化合物(2)から化合物(14)を合成することができる。
【0068】
工程13:一般的製造法6の工程6と同様の方法で化合物(14)と化合物(13)から化合物(3)を合成することができる。
【0069】
一般的製造法8
【0070】
【化12】

【0071】
工程14:一般的製造法2の工程2と同様の方法で化合物(14)と化合物(4)から化合物(5)を合成することができる。
【0072】
工程15:一般的製造法2の工程2と同様の方法で化合物(12)と化合物(4)から化合物(15)を合成することができる。
【0073】
工程16:一般的製造法1の工程1と同様の方法で化合物(15)と化合物(2)から化合物(5)を合成することができる。
【実施例】
【0074】
次に、製造例、実施例及び試験例により本発明をさらに詳細に説明するが、本発明はこれらの実施例に限定されるものではない。
【0075】
カラムクロマトグラフィーを使用して精製した際の「NHシリカゲルカートリッジ」にはBiotage(登録商標)SNAPCartridge KP−NH、「シリカゲルカートリッジ」にはBiotage(登録商標)SNAPCartridge KP−Silを使用した。
【0076】
製造例及び実施例中記載の各機器データは以下の測定機器で測定した。
【0077】
MSスペクトル:島津LCMS−2010EV又はmicromass Platform LC
NMRスペクトル:[1H-NMR]600MHz:JNM−ECA600(日本電子)、500MHz:JNM−ECA500(日本電子)、300MHz:UNITYNOVA300(Varian Inc.)、200MHz:GEMINI2000/200(Varian Inc.)
【0078】
実施例中で使用したマイクロウエーブ反応装置はInitiator(Biotage AB)である。
【0079】
実施例中の化合物名はACD/Name (ACD/Labs 10.01, Advanced Chemistry Development Inc.)により命名した。
【0080】
製造例1 6−フルオロ−3’−(ヒドロキシメチル)ビフェニル−3−カルバルデヒド
【0081】
【化13】

【0082】
3−ブロモ−4−フルオロ−ベンズアルデヒド(1.00g)、3−(ヒドロキシメチル)フェニルボロン酸(787mg)、テトラキス(トリフェニルホスフィン)パラジウム(569mg)、炭酸カリウム(1.36g)、ジメチルホルムアミド(6mL)とエタノール(3mL)の混合物をマイクロウエーブ反応装置(150℃、20分)で反応を行った。酢酸エチルを加え、セライト(Celite登録商標)ろ過後、酢酸エチル溶液を水で洗浄した。無水硫酸ナトリウムで酢酸エチル層を乾燥した。乾燥剤をろ別後、酢酸エチル層を減圧濃縮した。得られた残渣をカラムクロマトグラフィー(シリカゲルカートリッジ、ヘキサン:酢酸エチル=80:20〜65:35)で精製し、標題化合物(1.10g)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.74 - 1.81 (m, 1 H) 4.74 - 4.82 (m, 2 H) 7.28 - 7.62 (m, 5 H) 7.85 - 7.91 (m, 1 H) 7.97 - 8.04 (m, 1 H) 10.0 (s, 1 H)
【0083】
製造例2 {5’−[(シクロブチルアミノ)メチル]−2’−フルオロビフェニル−3−イル}メタノール
【0084】
【化14】

【0085】
シクロブチルアミン(370mg)、6−フルオロ−3’−(ヒドロキシメチル)ビフェニル−3−カルバルデヒド(1.00g)とクロロホルム(10mL)の混合物を室温で30分撹拌した。これに水素化トリアセトキシホウ素ナトリウム(1.29g)を加え、1.5日撹拌した。反応液を1M水酸化ナトリウム水溶液で洗浄した後、無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(シリカゲルカートリッジ、ヘキサン:酢酸エチル=75:25〜15:85)で精製し、標題化合物(1.16g)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.59 - 1.79 (m, 4 H) 2.18 - 2.27 (m, 2 H) 3.31 (m, 1 H) 3.72 (s, 2 H) 4.76 (s, 2 H) 7.03 - 7.14 (m, 1 H) 7.23 - 7.30 (m, 1 H) 7.33 - 7.58 (m, 5 H)
(ESI pos.) m/z : 286 ([M+H]+)
【0086】
同様にして、以下の化合物を合成した。
{5’−[(シクロペンチルアミノ)メチル]−2’−フルオロビフェニル−3−イル}メタノール
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.31 - 1.43 (m, 2 H) 1.50 - 1.59 (m, 2 H) 1.65 - 1.74 (m, 2 H) 1.82 - 1.91 (m, 2 H) 3.09 - 3.17 (m, 1 H) 3.77 (s, 2 H) 4.75 (s, 2 H) 7.05 - 7.13 (m, 1 H) 7.22 - 7.29 (m, 1 H) 7.33 - 7.58 (m, 5 H)
(ESI pos.) m/z : 300 ([M+H]+)
【0087】
{2’−フルオロ−5’−[(ペンタン−3−イルアミノ)メチル]ビフェニル−3−イル}メタノール
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.83 - 0.93 (m, 6 H) 1.40 - 1.53 (m, 4 H) 2.41 - 2.47 (m, 1 H) 3.77 (s, 2 H) 4.75 (s, 2 H) 7.04 - 7.57 (m, 7 H)
(ESI pos.) m/z : 302 ([M+H]+)
【0088】
製造例3 N−(3−ブロモ−4−フルオロベンジル)−2−メトキシエタンアミン
【0089】
【化15】

【0090】
2−メトキシエチルアミン(337mg)、3−ブロモ−4−フルオロ−ベンズアルデヒド(1.00g)、クロロホルム(10mL)の混合物を室温で30分撹拌した。これに水素化トリアセトキシホウ素ナトリウム(1.33g)を加え、12時間反応した。反応液を1M水酸化ナトリウム水溶液で洗浄した後、無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下ろ液を留去した。得られた残渣をカラムクロマトグラフィー(シリカゲルカートリッジ、クロロホルム:メタノール=100:0〜97:3)で精製し、標題化合物(796mg)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 2.75 - 2.80 (m, 2 H) 3.36 (s, 3 H) 3.48 - 3.53 (m, 2 H) 3.76 (s, 2 H) 7.03 - 7.08 (m, 1 H) 7.21 - 7.25 (m, 1 H) 7.53 - 7.56 (m, 1 H)
(ESI pos.) m/z : 262、264 ([M+H]+)
【0091】
同様にして、以下の化合物を合成した。
N−(3−ブロモ−4−フルオロベンジル)シクロペンタンアミン
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.31 - 1.39 (m, 2 H) 1.51 - 1.59 (m, 2 H) 1.65 - 1.75 (m, 2 H) 1.81 - 1.89 (m, 2 H) 3.05 - 3.13 (m, 1 H) 3.72 (s, 2 H) 7.02 - 7.08 (m, 1 H) 7.20 - 7.25 (m, 1 H) 7.51 - 7.55 (m, 1 H)
(ESI pos.) m/z : 272、274 ([M+H]+)
【0092】
N−(3−ブロモ−4−フルオロベンジル)−2−メチルプロパン−1−アミン
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.92 (d, J=6.88 Hz, 6 H) 1.70 - 1.80 (m, 1 H) 2.41 (d, J=6.88 Hz, 2 H) 3.73 (s, 2 H) 7.06 (t, J=8.48 Hz, 1 H) 7.21 - 7.25 (m, 1 H) 7.52 - 7.56 (m, 1 H)
(ESI pos.) m/z : 260、262 ([M+H]+)
【0093】
N−(3−ブロモ−4−フルオロベンジル)プロパン−2−アミン
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.02 - 1.11 (m, 6 H) 2.77 - 2.90 (m, 1 H) 3.73 (s, 2 H) 7.00 - 7.08 (m, 1 H) 7.20 - 7.25 (m, 1 H) 7.47 - 7.55 (m, 1 H)
(ESI pos.) m/z : 246、248 ([M+H]+)
【0094】
N−(3−ブロモ−4−フルオロベンジル)シクロヘキサンアミン
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.01 - 1.32 (m, 5 H) 1.57 - 1.92 (m, 5 H) 2.36 - 2.48 (m, 1 H) 3.53 (s, 2 H) 6.98 - 7.03 (m, 1 H) 7.17 - 7.21 (m, 1 H) 7.47 (dd, J=6.65, 2.06 Hz, 1 H)
(ESI pos.) m/z : 286、288 ([M+H]+)
【0095】
2−[(3−ブロモ−4−フルオロベンジル)アミノ]プロパン−1−オール
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.12 (d, J=6.42 Hz, 3 H) 2.85 - 2.93 (m, 1 H) 3.33 - 3.41 (m, 1 H) 3.61 - 3.94 (m, 4 H) 7.06 - 7.11 (m, 1 H) 7.27 - 7.29 (m, 1 H) 7.55 - 7.58 (m, 1 H)
(ESI pos.) m/z : 262、264 ([M+H]+)
【0096】
製造例4 N−(3−ブロモ−4−フルオロベンジル)−N−シクロペンチル−1−メチル−1H−イミダゾール−4−カルボキサミド
【0097】
【化16】

【0098】
N−(3−ブロモ−4−フルオロベンジル)シクロペンタンアミン(1.50g)、1−メチル−1H−イミダゾール−4−カルボン酸(695mg)、ヘキサフルオロリン酸ウロニウム 2−(1H−7−アザベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルメタンアミニウム(HATU)(2.72g)、ジイソプロピルエチルアミン(2.55mL)とアセトニトリル(23mL)の混合物を室温で4時間撹拌した。反応液を酢酸エチルで希釈し、酢酸エチル溶液を水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=90:10〜20:80)で精製し、標題化合物(2.00g)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.48 - 1.95 (m, 8 H) 3.62 - 3.75 (m, 3 H) 4.42 - 5.85 (m, 3 H) 6.97 - 7.21 (m, 2 H) 7.27 - 7.47 (m, 2 H) 7.53 (s, 1 H)
(ESI pos.) m/z : 380、382 ([M+H]+)
【0099】
同様にして、以下の化合物を合成した。
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−(2−メチルプロピル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.77 - 1.00 (m, 6 H) 1.91 - 2.14 (m, 1 H) 3.17 - 3.28 (m, 1 H) 3.87 - 5.45 (m, 3 H) 7.00 - 7.26 (m, 2 H) 7.30 - 7.62 (m, 3 H)
(ESI pos.) m/z : 368、370 ([M+H]+)
【0100】
N−(3−ブロモ−4−フルオロベンジル)−N−(プロパン−2−イル)−1H−1,2,4−トリアゾール−3−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.17 - 1.29 (m, 6 H) 4.65 (s, 3 H) 7.01 - 7.25 (m, 2 H) 7.42 - 8.60 (m, 2 H)
(ESI pos.) m/z : 339、341 ([M-H]-)
【0101】
N−(3−ブロモ−4−フルオロベンジル)−N−シクロヘキシル−1H−1,2,4−トリアゾール−3−カルボキサミド
(ESI pos.) m/z : 379、381 ([M-H]-)
【0102】
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.11 - 1.26 (m, 6 H) 3.63 - 3.78 (m, 3 H) 4.48 - 5.79 (m, 3 H) 6.95 - 7.59 (m, 5 H)
(ESI pos.) m/z : 354、356 ([M+H]+)
【0103】
N−(3−ブロモ−4−フルオロベンジル)−N−シクロヘキシル−1−メチル−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.99 - 1.86 (m, 10 H) 3.70 (br. s., 3 H) 4.33 - 5.32 (m, 3 H) 6.95 - 7.58 (m, 5 H)
(ESI pos.) m/z : 394、396 ([M+H]+)
【0104】
N−(3−ブロモ−4−フルオロベンジル)−N−(2−メトキシエチル)−1−メチル−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 3.25 - 3.34 (m, 3 H) 3.48 - 3.75 (m, 6 H) 4.07 - 4.18 (m, 1 H) 4.70 - 4.83 (m, 1 H) 5.36 - 5.53 (m, 1 H) 7.00 - 7.24 (m, 2 H) 7.29 - 7.63 (m, 3 H)
(ESI pos.) m/z : 370、372 ([M+H]+)
【0105】
製造例5 N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−(プロパン−2−イル)−1H−1,2,4−トリアゾール−3−カルボキサミド
【0106】
【化17】

【0107】
N−(3−ブロモ−4−フルオロベンジル)−N−(プロパン−2−イル)−1H−1,2,4−トリアゾール−3−カルボキサミド(2.06g)とジメチルホルムアミド(20mL)との混合物に、水素化ナトリウム(約60%オイル、266mg)を加え30分撹拌した。ヨウ化メチル(1.1mL)を加えて、終夜、室温で撹拌した。反応液に水を加えて、クロロホルムで抽出した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、有機層を減圧下濃縮した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=50:50〜34:66〜0:100)で精製し、標題化合物(1.00g)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.13 - 1.23 (m, 6 H) 3.88 - 4.04 (m, 3 H) 4.60 - 4.83 (m, 3 H) 7.00 - 7.08 (m, 1 H) 7.20 - 8.13 (m, 3 H)
(ESI pos.) m/z : 395、397 ([M+H]+)
【0108】
同様にして以下の化合物を合成した。
N−(3−ブロモ−4−フルオロベンジル)−N−シクロヘキシル−1−メチル−1H−1,2,4−トリアゾール−3−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.95 - 1.89 (m, 10 H) 3.83 - 4.85 (m, 6 H) 6.95 - 8.17 (m, 4 H)
(ESI pos.) m/z : 355、357 ([M+H]+)
【0109】
製造例6 N−(3−ブロモ−4−フルオロベンジル)−1−メチル−1H−イミダゾール−4−カルボキサミド
【0110】
【化18】

【0111】
3−ブロモ−4−フルオロベンジルアミン(1.62g)、1−メチル−1H−イミダゾール−4−カルボン酸(1.0g)、HATU(4.52g)、ジイソプロピルエチルアミン(4.1mL)とアセトニトリル(26ml)を室温で1時間撹拌した。反応液に水とクロロホルムを加え撹拌後、クロロホルム層を分離し、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=50:50)と(シリカゲルカートリッジ、クロロホルム:メタノール=99:1〜90:10))で精製し、標題化合物(1.87g)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 3.74 (s, 3 H) 4.52 - 4.58 (m, 2 H) 7.03 - 7.09 (m, 1 H) 7.34 - 7.56 (m, 4 H)
(ESI pos.) m/z : 312、314 ([M+H]+)
【0112】
製造例7 N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−プロピル−1H−イミダゾール−4−カルボキサミド
【0113】
【化19】

【0114】
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−1H−イミダゾール−4−カルボキサミド(156mg)のテトラヒドロフラン(3mL)溶液に、水素化ナトリウム(約60%オイル、24mg)を加えて30分撹拌した。これに、1−ヨードプロパン(136mg)を加え室温で4時間撹拌した。さらに水素化ナトリウム(約60%オイル、12mg)を加えて、終夜撹拌した。水を加え酢酸エチルで抽出した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=90:10〜20:80)で精製し、標題化合物(56mg)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.81 - 0.94 (m, 3 H) 1.59 - 1.69 (m, 2 H) 3.72 (s, 5 H) 4.62 - 5.38 (m, 2 H) 7.16 - 7.62 (m, 5 H)
(ESI pos.) m/z : 354、356 ([M+H]+)
【0115】
製造例8 N−(4−ブロモ−3−フルオロベンジル)プロパン−2−アミン塩酸塩
【0116】
【化20】

イソプロピルアミン(13.3g)、3−ブロモ−4−フルオロベンズアルデヒド(13.3g)とクロロホルム(300mL)の混合物を室温で30分間撹拌した。これに水素化トリアセトキシホウ素ナトリウム(47.7g)を数回に分けて加え、室温で15時間撹拌した。2M 水酸化ナトリウム水溶液(150mL)を加え、室温で30分間撹拌した。クロロホルム層を分離し、水層をクロロホルムで抽出した。合わせたクロロホルム層を水で洗浄し、無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下クロロホルムを留去した。得られた残渣を酢酸エチル(150mL)に溶解し、4M 塩酸/酢酸エチル(150mL)を加えた。析出した固体をろ取し、標題化合物29.0gを得た。
1H NMR (600 MHz, DMSO-d6) d ppm 1.29 (d, J=6.42 Hz, 6 H) 3.22 - 3.34 (m, 1 H) 4.13 (s, 2 H) 7.42 - 7.51 (m, 1 H) 7.60 - 7.68 (m, 1 H) 7.95 - 8.04 (m, 1 H) 8.95 - 9.24 (m, 2 H)
【0117】
同様にして以下の化合物を合成した。
N−(3−ブロモ−4−メトキシベンジル)プロパン−2−アミン塩酸塩
1H NMR (200 MHz, DMSO-d6) d ppm 1.20 - 1.37 (m, 6 H) 3.14 - 3.37 (m, 1 H) 3.87 (s, 3 H) 3.98 - 4.17 (m, 2 H) 7.18 (d, J=8.35 Hz, 1 H) 7.55 (d, J=8.35 Hz, 1 H) 7.82 (s, 1 H) 8.98 (br. s., 2 H)
(ESI pos.) m/z : 258、260 ([M+H]+)
【0118】
N−(3−ブロモ−5−クロロベンジル)プロパン−2−アミン塩酸塩
1H NMR (200 MHz, DMSO-d6) d ppm 1.23 - 1.35 (m, 6 H) 3.17 - 3.40 (m, 1 H) 4.05 - 4.23 (m, 2 H) 7.71 - 7.97 (m, 3 H) 9.19 (br. s., 2 H)
(ESI pos.) m/z : 262、264 ([M+H]+)
【0119】
N−(3−ブロモ−4−メチルベンジル)プロパン−2−アミン塩酸塩
1H NMR (600 MHz, DMSO-d6) d ppm 1.24 - 1.31 (m, 6 H) 2.35 (s, 3 H) 3.22 - 3.30 (m, 1 H) 4.10 (s, 2 H) 7.40 - 7.43 (m, 1 H) 7.46 - 7.49 (m, 1 H) 7.83 (s, 1 H) 8.97 (br. s., 1 H)
(ESI pos.) m/z : 242、244 ([M+H]+)
【0120】
N−[3−ブロモ−5−(トリフルオロメチル)ベンジル]プロパン−2−アミン塩酸塩1H NMR (600 MHz, DMSO-d6) d ppm 1.30 (d, J=6.88 Hz, 6 H) 4.25 (s, 2 H) 8.01 - 8.20 (m, 3 H) 9.04 - 9.22 (m, 2 H)
(ESI pos.) m/z : 296、298 ([M+H]+)
【0121】
N−[3−ブロモ−5−(トリフルオロメトキシ)ベンジル]プロパン−2−アミン塩酸塩
1H NMR (200 MHz, DMSO-d6) d ppm 1.30 (d, J=6.59 Hz, 6 H) 3.20 - 3.40 (m, 1 H) 4.13 - 4.30 (m, 2 H) 7.72 (s, 1 H) 7.75 (s, 1 H) 7.94 (s, 1 H) 9.22 (br. s., 2 H)
(ESI pos.) m/z : 312、314 ([M+H]+)
【0122】
N−(3−ブロモ−4−クロロベンジル)プロパン−2−アミン塩酸塩
1H NMR (200 MHz, DMSO-d6) d ppm 1.29 (d, J=6.59 Hz, 6 H) 3.10 - 3.50 (m, 1 H) 4.14 (s, 1 H) 7.58 - 7.68 (m, 1 H) 7.68 - 7.77 (m, 1 H) 8.02 - 8.12 (m, 1 H) 9.23 (br. s., 2 H)
(ESI pos.) m/z : 262、264 ([M+H]+)
【0123】
製造例9 N−(3−ブロモ−4−フルオロベンジル)−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
【0124】
【化21】

N−(4−ブロモ−3−フルオロベンジル)プロパン−2−アミン塩酸塩(2.3g)、1H−イミダゾール−4−カルボン酸(1.18g)、HOBT(1.61g)、EDC塩酸塩(2.68g)、トリエチルアミン(2.4mL)とジメチルホルムアミド(40mL)の混合物を室温で、6日間撹拌した。減圧下、反応混合物を濃縮し、残渣に飽和炭酸水素ナトリウム水溶液を加え、30分間撹拌した。これを酢酸エチルで抽出し、酢酸エチル層を水で洗浄した。酢酸エチル層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン/酢酸エチル=90:10〜10:90)で精製し、標題化合物10.2gを得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.04 - 1.37 (m, 6 H) 4.49 - 5.78 (m, 3 H) 6.95 - 7.82 (m, 5 H)
(ESI pos.) m/z : 340、342 ([M+H]+)
【0125】
同様にして以下の化合物を合成した。
N−(3−ブロモ−4−メトキシベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.06 - 1.30 (m, 6 H) 3.70 (s, 3 H) 3.86 (s, 3 H) 4.41 - 5.81 (m, 3 H) 6.74 - 7.63 (m, 5 H)
(ESI pos.) m/z : 366、368 ([M+H]+)
【0126】
N−(3−ブロモ−5−クロロベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.05 - 1.30 (m, 6 H) 3.72 (s, 3 H) 4.46 - 5.83 (m, 3 H) 7.16 - 7.61 (m, 5 H)
(ESI pos.) m/z : 370、372 ([M+H]+)
【0127】
N−(3−ブロモ−4−メチルベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.10 - 1.25 (m, 6 H) 3.63 - 3.79 (m, 3 H) 4.52 - 5.82 (m, 3 H) 7.07 - 7.60 (m, 5 H)
(ESI pos.) m/z : 350、352 ([M+H]+)
【0128】
N−[3−ブロモ−5−(トリフルオロメチル)ベンジル]−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.04 - 1.30 (m, 6 H) 3.60 - 3.80 (m, 3 H) 4.56 - 5.91 (m, 3 H) 7.16 - 7.70 (m, 5 H)
(ESI pos.) m/z : 404、406 ([M+H]+)
【0129】
N−[3−ブロモ−5−(トリフルオロメトキシ)ベンジル]−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.10 - 1.31 (m, 6 H) 3.62 - 3.80 (m, 3 H) 4.50 - 5.87 (m, 3 H) 7.04 - 7.63 (m, 5 H)
(ESI pos.) m/z : 420、422 ([M+H]+)
【0130】
N−(3−ブロモ−4−クロロベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.03 - 1.32 (m, 6 H) 3.71 (s, 3 H) 4.41 - 5.86 (m, 3 H) 7.10 - 7.62 (m, 5 H)
(ESI pos.) m/z : 370、372 ([M+H]+)
【0131】
製造例10 N−[(3’,4’,5’,6−テトラフルオロビフェニル−3−イル)メチル]プロパン−2−アミン
【0132】
【化22】

N−(4−ブロモ−3−フルオロベンジル)プロパン−2−アミン(500mg)、(3,4,5−トリフルオロフェニル)ボロン酸(386mg)、炭酸セシウム(780mg)、テトラキス(トリフェニルホスフィン)パラジウム(230mg)、トルエン(2.2mL)、エタノール(2.2mL)と水(1.4mL)の混合物をマイクロウエーブ反応装置で、150℃で、30分間反応を行った。放冷後、飽和炭酸水素ナトリウムを加え、酢酸エチルで抽出した。酢酸エチル層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去し、得られた残渣をクロマトグラフィー(シリカゲルカートリッジ、クロロホルム/メタノール=100:0〜90:10)で精製し、標題化合物628mgを得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.11 (d, J=6.30 Hz, 6 H) 2.87 (spt, J=6.30 Hz, 1 H) 3.79 (s, 2 H) 7.08 - 7.14 (m, 1 H) 7.16 - 7.22 (m, 2 H) 7.30 - 7.36 (m, 2 H)
(ESI pos.) m/z : 298 ([M+H]+)
【0133】
同様にして以下の化合物を合成した。
2−({[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}アミノ)プロパン−1−オール
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.10 - 1.13 (m, 4 H) 2.85 - 2.91 (m, 1 H) 3.28 - 3.34 (m, 1 H) 3.60 - 3.65 (m, 1 H) 3.75 - 3.80 (m, 1 H) 3.89 - 3.94 (m, 1 H) 7.09 - 7.15 (m, 1 H) 7.27 - 7.41 (m, 4 H) 7.54 - 7.59 (m, 2 H)
(ESI pos.) m/z : 344 ([M+H]+)
【0134】
1−[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メタンアミン
1H NMR (200 MHz, CHLOROFORM-d) d ppm 3.91 (s, 2 H) 7.05 - 7.64 (m, 7 H)
【0135】
実施例1 N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
【0136】
【化23】

【0137】
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド(127mg)、4−トリフルオロメトキシフェニルボロン酸(154mg)、テトラキス(トリフェニルホスフィン)パラジウム(45mg)、炭酸カリウム(70mg)、ジメチルホルムアミド(3mL)とエタノール(1.5mL)の混合物をマイクロウエーブ反応装置(150℃、25分)で反応を行った。酢酸エチルを加え、セライト(Celite登録商標)ろ過後、酢酸エチル溶液を水で洗浄した。無水硫酸ナトリウムで酢酸エチル層を乾燥した。乾燥剤をろ別後、酢酸エチル層を減圧濃縮した。得られた残渣をカラムクロマトグラフィー((NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=90:10〜酢酸エチル)と(シリカゲルカートリッジ、クロロホルム:メタノール=100:0〜97:3))で精製し、標題化合物(77mg)を得た。
【0138】
実施例2 N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}−1−メチル−N−プロピル−1H−イミダゾール−4−カルボキサミド 塩酸塩
【0139】
【化24】

【0140】
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−プロピル−1H−イミダゾール−4−カルボキサミド(56mg)、4−トリフルオロメトキシフェニルボロン酸(65mg)、テトラキス(トリフェニルホスフィン)パラジウム(20mg)、炭酸カリウム(44mg)、ジメチルホルムアミド(1.3mL)とエタノール(0.6mL)の混合物をマイクロウエーブ反応装置(150℃、25分)で反応を行った。酢酸エチルを加え、酢酸エチル溶液を水で洗浄した。無水硫酸ナトリウムで酢酸エチル層を乾燥した。乾燥剤をろ別後、酢酸エチル層を減圧濃縮した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=80:20〜20:80)と(シリカゲルカートリッジ、クロロホルム:メタノール=100:0〜97:3)で精製し、得られた残渣を酢酸エチルに溶解し、4N塩酸/酢酸エチル(約1mL)を加え5分撹拌後、減圧下溶媒を留去した。残渣に、ジエチルエーテル加え固化し、固体をろ取し、標題化合物(24mg)を得た。
【0141】
実施例3 メチル 2’−フルオロ−5’−({[(1−メチル−1H−1,2,4−トリアゾール−3−イル)カルボニル](プロパン−2−イル)アミノ}メチル)ビフェニル−3−カルボキシラート
【0142】
【化25】

【0143】
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−(プロパン−2−イル)-1H−1,2,4−トリアゾール−3−カルボキサミド(492mg)、3−メトキシカルボニルフェニルボロン酸(274mg)、テトラキス(トリフェニルホスフィン)パラジウム(161mg)、炭酸セシウム(679mg)とトルエン/エタノール/水(3:3:2)(9mL)の混合物を100℃で1時間撹拌した。反応液に水を加え、酢酸エチルで抽出した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下濃縮した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=50:50〜0:100)で精製し、標題化合物(486mg)を得た。
【0144】
実施例4 N−{[6−フルオロ−3’−(ヒドロキシメチル)ビフェニル−3−イル]メチル}−1−メチル−N−(プロパン−2−イル)−1H−1,2,4−トリアゾール−3−カルボキサミド
【0145】
【化26】

【0146】
メチル 2’−フルオロ−5’−({[(1−メチル−1H−1,2,4−トリアゾール−3−イル)カルボニル](プロパン−2−イル)アミノ}メチル)ビフェニル−3−カルボキシラート(392mg)のエタノール(19mL)の混合物に、水素化ホウ素ナトリウム(723mg)を加え、終夜還流した。さらに、水素化ホウ素ナトリウム(362mg)を加え、5時間還流した。放冷後、アセトンを加えて撹拌した後、水を加えて、クロロホルムで抽出した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下濃縮した。得られた残渣をカラムクロマトグラフィー(シリカゲルカートリッジ、クロロホルム/メタノール=99:1〜97:3)で精製し、標題化合物(180mg)を得た。
【0147】
実施例5 N−シクロブチル−N−{[6−フルオロ−3’−(ヒドロキシメチル)ビフェニル−3−イル]メチル}−1−メチル−1H−イミダゾール−4−カルボキサミド
【0148】
【化27】

【0149】
{5’−[(シクロブチルアミノ)メチル]−2’−フルオロビフェニル−3−イル}メタノール(700mg)、1−メチル−1H−イミダゾール−4−カルボン酸(340mg)、HATU(1.21g)、ジイソプロピルエチルアミン(1.13mL)とアセトニトリル(10.5ml)の混合物を室温で2.5時間撹拌した。反応液を酢酸エチルで希釈し、有機層を水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(シリカゲルカートリッジ、クロロホルム:メタノール=98:2〜95:5)及び(NHシリカゲルカートリッジ、クロロホルム:メタノール=100:0〜98:2)で精製し、標題化合物(758mg)を得た。
【0150】
実施例6 1−エチル−N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
【化28】

【0151】
N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド(120mg)のジメチルホルムアミド(2mL)溶液に水素化ナトリウム(約60%オイル、12mg)を加え、室温で15分間撹拌した。これにヨードエタン(134mg)を加え、80℃で2時間撹拌した。飽和炭酸水素ナトリウム水溶液を加え、これを酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、有機層を減圧下濃縮し、得られた残渣を分取HPLCで精製し、標題化合物62mgを得た。
【0152】
実施例7 N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}−1−メチル−N−(プロパ−1−エン−2−イル)−1H−イミダゾール−4−カルボキサミド
【化29】

【0153】
1−[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メタンアミン(500mg)とアセトン(1mL)の混合物をマイクロウエーブ反応装置で、120℃、1時間反応した。反応溶液に無水硫酸ナトリウムを加え、乾燥剤をろ別後、減圧下溶媒を留去し、N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}プロパ−1−エン−2−アミンを得た。得られたN−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}プロパ−1−エン−2−アミンにクロロホルム(10mL)、トリエチルアミン(265mg)、及び1−メチル−1H−イミダゾール−4−カルボン酸クロリド(260mg)を加えて、室温で2日間撹拌した。反応液に水を加えて、クロロホルムで抽出した。フェーズセパレータでクロロホルム層を分離後、減圧下溶媒を留去し、得られた残渣をHPLCおよびTLCで精製し、標題化合物30mgを得た。
【0154】
実施例1から7で示した化合物と、同様の方法で合成した化合物の構造式とそれらの機器データを表1−1から1−6に示した。表中の実施例の欄に記載された数字は、その化合物が上記実施例1から7の内、どの実施例と同様な方法で合成されたかを示したものである。
【0155】
【表1−1】

【0156】
【表1−2】

【0157】
【表1−3】

【0158】
【表1−4】

【0159】
【表1−5】

【0160】
【表1−6】

【0161】
試験例1 [グリシン取り込み阻害実験]
グリシン取り込み実験はNeuron, 8, 927−935, 1992に掲載された方法に従って行った。ヒト1型グリシントランスポーター(GlyT1)が内在性に発現している神経膠腫であるT98G細胞を用いた。T98G細胞を96ウェルプレートに2.0×104個/ウェルにて播種し、炭酸ガスインキュベーター内にて一晩培養した。被検物質は100%DMSO溶液に溶解したのち、150mM塩化ナトリウム、1mM塩化カルシウム、5mM塩化カリウム、1mM塩化マグネシウム、10mMグルコースおよび0.2%ウシ血清アルブミンを含む10mMHEPES緩衝液(pH7.4)に溶解させた。細胞培養用培地を除去した後、細胞を被検物質で10分間前処置した。その後、被検物質および[3H]グリシン(最終濃度 250nM)を細胞に添加し、室温にて15分間インキュベートした。インキュベーション終了後、マニーホールドにて細胞外液を吸引し、細胞外に存在する余分な標識グリシンを除去したのち、0.5Mの水酸化ナトリウム水溶液にて細胞を溶解した。細胞内に取り込まれたグリシン量は、細胞溶解液中の放射活性を液体シンチレーションカウンターで測定することにより求めた。10μMのALX5407存在下におけるグリシン取り込み量を非特異的取り込みとし、10μMのALX5407非存在下の総取り込み量から非特異的取り込み量を差し引いたものを特異的取り込み量とした。また、被検物質の10-9〜10-5M濃度での抑制曲線からグリシン取り込み阻害活性(IC50値)を算出した。
【0162】
なおALX5407はN−[(3R)−3−([1,1’−ビフェニル]−4−イルオキシ)−3−(4−フルオロフェニル)プロピル]−N−メチルグリシンHCl塩である。
【0163】
本発明化合物のIC50値は、化合物41、43、46〜50、54については1μM以上であり、それ他の化合物については1μMより小さかった。さらに化合物3、4、5、30、32、33、37、51、53のIC50値は0.1μM以上であり、その他の化合物のIC50値は0.1μMより小さかった。例えば、化合物2、6、7、8、10、11、13、14、15、16、17、18、19、20、21、22、23、24、25、26、28、31、34、35、36、39、40、42、52のIC50値は、それぞれ12.6nM、14.6nM、25.9nM、11.0nM、14.8nM、35.1nM、4.33nM、2.78nM、21.3nM、42.5nM、18.8nM、8.89nM、18.6nM、7.19nM、13.6nM、11.6nM、21.4nM、14.2nM、25.4nM、40.0nM、22.6nM、21.0nM、49.4nM、48.9nM、38.2nM、48.5nM、35.9nM、48.3nM、30.7nMであった。
【0164】
試験例2 [膜透過性実験]
医薬品開発に当たって膜透過性は、経口投与する医薬の体内吸収率との観点から重要な要素の1つであり、膜透過性が高い化合物は医薬品として腸管からの良好な吸収が期待される(Pharmaceutical Research (2002) Vol.19, No.7, 921-925参照)。
膜透過性試験は、PAMPA EvolutionTM(pION社)を用いてpION社の推奨プロトコールに準じて行った。詳細には、評価化合物溶液(評価化合物のDMSO溶液を各pH(4.0, 5.0, 6.2, 7.4)に調整したsystem solutionに添加し、希釈したもの)を調製し、人工脂質(GIT-0)で脂質二重膜を形成させたsandwichプレートの下段(Donor)に添加した。上段(Acceptor)にはacceptor sink bufferを添加し、一定時間経過後、Donor及びAcceptor溶液のUV測定から得られた化合物の累積透過量より膜透過係数Pe(×10−6cm/sec)を算出し、化合物の膜透過性を評価した。その結果、本願化合物No.8、10、12、15、16、18〜21、23〜26、28、34〜36、39〜42、54は、高透過性マーカー化合物であるメトプロロールの膜透過係数より高く、良好な膜透過性を示した。
【0165】
試験例3 [P−gpの基質認識性試験]
中枢神経系に作用を及ぼす薬物は、一般に血中から脳内に移行することが、薬効の発現に重要である。血液脳関門には、薬物の移行性を制御している排出(efflux)transporterとして代表的なものにP-糖タンパク質(P-glycoprotein,P−gp)が存在しており、P−gpはその基質となる薬物の脳移行を阻害している。したがって、医薬品開発においてP−gpの基質として認識されないことが、脳移行性の指標となる。
P−gpの基質認識性試験は、J Pharmacol. Exp. Ther. (1992) Vol. 263, No. 2, 840-845及びJ Biol. Chem. (1992) Vol. 267, No. 34, 24248-24252に記載の方法に準じて行った。詳細には、トランスウェル上に4日間培養したLLC-GA5-COL300細胞(ブタ腎由来培養腎上皮細胞株LLC-PK1由来Human MDR1 発現系)を用い、試験直前にウェル内をHank's balanced salt solution(HBSS)にて置換して試験に供した。評価化合物溶液(評価化合物のDMSO溶液をHBSSにて希釈し,最終濃度10μMに調整したもの)を、LLC-GA5-COL300細胞のDonor側に添加後、Acceptor側から一定量のHBSSを経時的に採取し、LC-MS/MSにて採取サンプル中の評価化合物濃度を測定した。
Acceptor側への化合物の累積透過量より,Apical→Basal及びBasal→Apicalそれぞれの膜透過係数(×10-6cm/sec)を算出し、その比(Efflux Ratio)からP−gpの基質認識性を評価した。
その結果、本願化合物No.10、17、18、20、22、24、36、54は、Nature Reviews Drug Discovery (2010), Vol. 9, 215-236に記載された判定基準において、P−gpの基質として認識されないと判定され、良好な脳移行性が示唆された(Pharmaceutical Research (2001), Vol. 18, No. 12, 1660-1668参照)。この結果から、本願化合物は、中枢神経系に作用を及ぼす薬物として有効に用いられることが期待される。
試験例4:社会性認知試験
実験には雄性Sprague−Dawley系ラットを用い、すでに報告された方法に準じて行った(Shimazaki et al.,Psychopharmacology,209,263−270,2010)。
ラット(Adult)(9週齢)にMK−801(0.1mg/kg)を腹腔内投与した後、直ぐに試験ケージに入れ、30分間馴化させた。MK−801投与から30分後、若齢ラット(4週齢)をラット(adult)を入れた試験ケージに入れ、5分間放置した。5分間にラット(adult)が若齢ラットに対して行った社会性行動(臭い嗅ぎ行動(sniffing),毛づくろい行動(grooming),追尾行動(following))の時間を測定した(1回目探索時間)。その後、若齢ラットのみを試験ケージから取り出し、ホームケージに戻した。30分後、1回目探索と同じ若齢ラットを試験ケージに入れ、5分間にラット(adult)が若齢ラットに対して行った社会性行動(臭い嗅ぎ行動,毛づくろい行動,追尾行動)の時間を測定した(2回目探索時間)。社会性認知は2回目探索時間/1回目探索時間で示した。披験物質(化合物10)は1回目探索開始時間の1時間前に経口投与した。結果を下表に示す。溶媒投与群には、0.5%メチルセルロース水溶液を投与した。
【表2】

披験物質投与群は溶媒投与群と比較して、2回目の探索時間/1回目の探索時間を有意に減少させ、認知機能障害改善作用を有することが示された。
【産業上の利用可能性】
【0166】
本発明化合物は、1型グリシントランスポーター(GlyT1)阻害作用を有し、従って、グリシントランスポーターに関連する疾患、具体的には、統合失調症、アルツハイマー病、認知機能障害、認知症、不安障害(全般性不安障害、パニック障害、強迫性障害、社会不安障害、外傷後ストレス障害、特定の恐怖症、急性ストレス障害等)、うつ病、薬物依存、痙攣、振戦、疼痛、及び睡眠障害等の予防又は治療に有効である。
【技術分野】
【0001】
本発明は、グリシントランスポーター阻害作用を有する化合物に関する。
【背景技術】
【0002】
グルタミン酸受容体の一つであるNMDA受容体は脳内の神経細胞膜上に存在しており、神経の可塑性、認知、注意、記憶など様々な神経生理学的な現象に関わっている。NMDA受容体には複数のアロステリック結合部位が存在し、グリシン結合部位もその一つである(NMDA受容体複合体グリシン結合部位)。NMDA受容体複合体グリシン結合部位はNMDA受容体の活性化に関与していることが報告されている(非特許文献1)。
【0003】
グリシン作動性神経のシナプス前終末に活動電位が到達するとシナプス間隙へのグリシンの放出が開始される。放出されたグリシンはシナプス後部の受容体等と結合した後、トランスポーターによりシナプス間隙から取り除かれる。このことよりグリシンのトランスポーターは細胞外液にあるグリシン量を調節することでNMDA受容体の機能を調節していると考えられている。
【0004】
グリシントランスポーター(GlyT)は細胞外グリシンの細胞内への再取り込みに関わっているタンパクであり、現在までにGlyT1及びGlyT2の二つのサブタイプの存在が明らかとなっている。GlyT1は主に大脳皮質、海馬及び視床等に発現しており、統合失調症、アルツハイマー病、認知機能障害、認知症、不安障害(全般性不安障害、パニック障害、強迫性障害、社会不安障害、外傷後ストレス障害、特定の恐怖症、急性ストレス障害等)、うつ病、薬物依存、痙攣、振戦、疼痛、及び睡眠障害等の疾患との関連が報告されている(非特許文献2〜4)。
【0005】
GlyT1阻害作用を有し、5員環ヘテロアリールアミド構造をもつ化合物は以下の特許文献において報告がされている(特許文献1〜3)。これらの特許文献1〜3及び非特許文献5,6に記載された化合物は、該アミド構造の窒素原子に、窒素含有基が結合していることを特徴とする化合物である。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】WO2005/037216
【特許文献2】WO2006/106425
【特許文献3】WO2008/065500
【非特許文献】
【0007】
【非特許文献1】Molecular Psychiatry (2004) 9, 984-997
【非特許文献2】Current Medicinal Chemistry, 2006, 13, 1017-1044
【非特許文献3】Neuropsychopharmacology (2005), 1-23
【非特許文献4】Expert Opinion on Therapeutic Patents (2004) 14 (2) 201-214
【非特許文献5】Bioorganic & Medicinal Chemistry Letters (2009) 19 2974-2976
【非特許文献6】Bioorganic & Medicinal Chemistry Letters (2010) 20 907-911
【発明の概要】
【発明が解決しようとする課題】
【0008】
本発明は、グリシン取り込み阻害作用に基づいた統合失調症、アルツハイマー病、認知機能障害、認知症、不安障害(全般性不安障害、パニック障害、強迫性障害、社会不安障害、外傷後ストレス障害、特定の恐怖症、急性ストレス障害等)、うつ病、薬物依存、痙攣、振戦、疼痛、又は睡眠障害等の疾患の予防又は治療に有用な新規な化合物又はその医薬上許容される塩を提供することを目的とする。
【課題を解決するための手段】
【0009】
本発明者らはGlyT1に対し阻害作用を有する新規な骨格の化合物につき鋭意検討した結果、下記に示す式で表される化合物が優れたGlyT1阻害物質であることを見出し、本発明を完成するに至った。
【0010】
以下、本発明を詳細に説明する。本発明の態様(以下、「本発明化合物」という)は以下に示すものである。
(1)式[I]
【0011】
【化1】

(式中、
R1は、水素原子、又はC1-6アルキル基を示し、
R2は、C1-6アルキル基、C2-6アルケニル基、C3-6シクロアルキル基、C1-6ハロアルキル基、C1-6ヒドロキシアルキル基、又はC1-6アルコキシC1-6アルキル基を示し、
R3は、水素原子、C1-6アルキル基、C1-6アルコキシ基、C1-6ハロアルキル基、C1-6ハロアルコキシ基、又はハロゲン原子を示し、
R4は、フェニル基を示し、
該フェニル基は、C1-6アルキル基、C1-6アルコキシ基、C1-6ハロアルキル基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、C1-6アルコキシC1-6アルキル基、C2-7アルコキシカルボニル基、シアノ基、及びハロゲン原子から選択される1から3個の置換基で置換されてもよく、
Yは、式CH、又は
窒素原子を示す。)で表される化合物又はその医薬上許容される塩。
(2)R2が分岐C3-6アルキル基、又はC3-6シクロアルキル基である上記(1)に記載の化合物又はその医薬上許容される塩。
(3)Yが式CHである上記(1)又は(2)に記載の化合物又はその医薬上許容される塩。
(4)R3がハロゲン原子である上記(1)〜(3)のいずれか1つに記載の化合物又はその医薬上許容される塩。
(5)R3がフッ素原子である上記(1)〜(3)のいずれか1つに記載の化合物又はその医薬上許容される塩。
(6)R4が、フェニル基、又はC1-6アルコキシ基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、及びハロゲン原子から選択される1〜3個の置換基で置換されたフェニル基である上記(1)〜(5)のいずれか1つに記載の化合物又はその医薬上許容される塩。
(7)
式[I]の化合物が下式:
【化2】

(式中、
R1は、メチル基、又はエチル基を示し、
R4は、フェニル基、又は
C1-6アルコキシ基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、及びハロゲン原子から選択される1から3個の置換基で置換されたフェニル基を示す)で表される上記(1)に記載の化合物又はその医薬上許容される塩。
(8)
化合物が、
N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[6-フルオロ-3'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-[(4',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(3',6-ジフルオロ-4'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(3',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロ-3'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロ-4'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(4'-クロロ-6-フルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',5',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-{[3'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[4'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',5',6-テトラフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、又は
1-エチル-N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド
である上記(1)に記載の化合物又はその医薬上許容される塩。
(9)
化合物が、
N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[6-フルオロ-3'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-[(4',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[3'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[4'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',5',6-テトラフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、又は
1-エチル-N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド
である上記(1)に記載の化合物又はその医薬上許容される塩。
(10)上記(1)〜(9)のいずれか1つに記載の化合物又はその医薬上許容される塩を有効成分として含む医薬。
(11)上記(1)〜(9)のいずれか1つに記載の化合物又はその医薬上許容される塩を有効成分として含む、統合失調症、アルツハイマー病、認知機能障害、認知症、不安障害、うつ病、薬物依存、痙攣、振戦、又は睡眠障害の疾患の予防剤又は治療剤。
【発明の効果】
【0012】
本発明化合物はグリシントランスポーター(GlyT1)阻害活性を有する。また、本発明化合物は、以下の試験例で示すように高い膜透過性を示すため、経口投与する医薬にとって重要である腸管吸収に優れることが期待される。さらに、本発明化合物は、以下の試験例で示すように、薬物の脳移行性を制御している排出トランスポーターであるP−糖タンパク質の基質として認識されないため、良好な脳移行性が期待される。
【発明を実施するための形態】
【0013】
本明細書において用いる「C1-6アルキル基」とは直鎖状又は分岐鎖状の炭素数1〜6個のアルキル基を意味し、例えばメチル、エチル、プロピル、イソプロピル、ブチル、イソブチル、tert−ブチル、ペンチル、イソペンチル、ヘキシルを挙げることができる。
【0014】
本明細書において用いる「C2-6アルケニル基」とは直鎖状又は分岐鎖状の炭素数2〜6個のアルケニル基を意味し、例えばビニル、アリル、ブタ−2−エニル、プロパ−1−エン−2−イルを挙げることができる。
【0015】
本明細書において用いる「C3-6シクロアルキル基」とは炭素数3〜6個のシクロアルキル基を意味し、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基である。
【0016】
本明細書において用いる「C1-6アルコキシ基」とは直鎖状又は分岐鎖状の炭素数1〜6個のアルコキシ基を意味し、例えばメトキシ、エトキシ、プロポキシ、イソプロポキシ、ブトキシ、イソブトキシ、ペンチルオキシ、イソペンチルオキシ、ヘキシルオキシを挙げることができる。
【0017】
本明細書において用いる「C1-6アルコキシC1-6アルキル基」とはC1-6アルコキシ基で置換されたC1-6アルキル基を示し、例えば、メトキシメチル、メトキシエチル、メトキシプロピル、メトキシブチル、メトキシペンチル、メトキシヘキシル、エトキシメチル、エトキシエチル、エトキシプロピル、イソプロポキシメチル、イソプロポキシエチル、イソプロポキシプロピル、1-メトキシエチル、1-エトキシエチル、2-メトキシプロピル、2-エトキシプロピルを挙げることができる。
【0018】
本明細書において用いる「ハロゲン(ハロ)」とは、フッ素原子、塩素原子、臭素原子、ヨウ素原子である。
【0019】
本明細書において用いる「C1-6ハロアルキル基」とはハロゲン原子で置換された直鎖状又は分岐鎖状の炭素数1〜6個のアルキル基を意味し、ハロゲン原子の好ましい置換数は1〜3個であり、例えばフルオロメチル、ジフルオロメチル、トリフルオロメチル、トリクロロメチルを挙げることができる。
【0020】
本明細書において用いる「C1-6ハロアルコキシ基」とはハロゲン原子で置換された直鎖状又は分岐鎖状の炭素数1〜6個のアルコキシ基を意味し、ハロゲン原子の好ましい置換数は1〜3個であり、例えばフルオロメトキシ、ジフルオロメトキシ、トリフルオロメトキシを挙げることができる。
【0021】
本明細書において用いる「C1-6ヒドロキシアルキル基」とはヒドロキシ基で置換された直鎖状又は分岐鎖状の炭素数1〜6個のアルキル基を意味し、例えば、ヒドロキシメチル、2−ヒドロキシエチル、1−ヒドロキシエチル、3−ヒドロキシプロピル、2−ヒドロキシプロピル、1−ヒドロキシプロピルを挙げることができる。
【0022】
本明細書において用いる「C2-7アルコキシカルボニル基」とは、鎖状又は分岐鎖状の炭素数2〜7個のアルコキシカルボニル基を示し、例えば、メトキシカルボニル、エトキシカルボニル、プロポキシカルボニル、イソプロポキシカルボニル、ブトキシカルボニル、イソブトキシカルボニルを挙げることができる。
【0023】
本明細書中における「医薬上許容される塩」とは、薬剤的に許容することのできる酸付加塩を意味し、用いられる酸としては、硫酸、塩酸、臭化水素酸、硝酸及びリン酸等の無機酸、或いは、酢酸、シュウ酸、乳酸、クエン酸、リンゴ酸、グルコン酸、酒石酸、フマール酸、マレイン酸、メタンスルホン酸、エタンスルホン酸、ベンゼンスルホン酸及びp−トルエンスルホン酸等の有機酸を挙げることができる。遊離体から当該塩への変換は従来の方法で行うことができる。
【0024】
本発明化合物において、好ましい態様を以下にあげる。
R2は、好ましくは、分岐C3-6アルキル基、又はC3-6シクロアルキル基であり、より好ましくは、分岐C3-6アルキル基である。
R3は、好ましくはハロゲン原子であり、より好ましくはフッ素原子である。R3の
より好ましい例がフッ素原子である場合、式(I)化合物はより好ましくは下記式によって表される。
【化3】

R1は、好ましくはC1-6アルキル基であり、より好ましくはメチル基又はエチル基であり、さらにより好ましくはメチル基である。
R4は、好ましくは、フェニル基、又はC1-6アルコキシ基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、及びハロゲン原子から選択される1から3個の置換基で置換されたフェニル基である。
【0025】
本発明化合物は複数の不斉中心を含むことができる。従って前記化合物は光学活性体で存在するとともにそのラセミ体でも存在することができ、さらに複数のジアステレオマーも存在することができる。前記の全ての形態は本発明の範囲内に含まれる。個々の異性体は公知の方法、例えば光学活性な出発物質若しくは中間体の使用、中間体若しくは最終生成物の製造における光学選択的な反応又はジアステレオ選択的な反応、或いは中間体又は最終生成物の製造におけるクロマトグラフィーを用いた分離等により得ることが可能である。さらに、本発明化合物が水和物又は溶媒和物を形成する場合、それらも本発明の範囲内に含まれる。同様に、本発明化合物の水和物又は溶媒和物の医薬上許容される塩も本発明の範囲内に含まれる。
【0026】
本発明の他の態様は、以下に示す通りである。
(A)式[I]
【化4】

(式中、
R1は、水素原子、又はC1-6アルキル基を示し、
R2は、C1-6アルキル基、C3-6シクロアルキル基、C1-6ハロアルキル基、又はC1-6アルコキシC1-6アルキル基を示し、
R3は、水素原子、又はハロゲン原子を示し、
R4は、フェニル基を示し、
該フェニル基は、C1-6アルキル基、C1-6アルコキシ基、C1-6ハロアルキル基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、C1-6アルコキシC1-6アルキル基、C2-6アルコキシカルボニル基、シアノ基、及びハロゲン原子から選択される1から3個の置換基で置換されてもよく、
Yは、窒素原子、又は
式CHを示す。)で表される化合物又はその医薬上許容される塩。
(B)R1がC1-6アルキル基であり、
Yが式CHである上記(A)に記載の化合物又はその医薬上許容される塩。
(C)R1がC1-6アルキル基であり、
Yが窒素原子である上記(A)に記載の化合物又はその医薬上許容される塩。
(D)R3がハロゲン原子である上記(A)〜(C)のいずれかに記載の化合物又はその医薬上許容される塩。
(E)R3がフッ素原子である上記(A)〜(C)のいずれかに記載の化合物又はその医薬上許容される塩。
(F)R2が、C1-6アルキル基、又はC3-6シクロアルキル基である上記(A)〜(E)のいずれかに記載の化合物又はその医薬上許容される塩。
(G)R2が、C1-6アルコキシC1-6アルキル基である上記(A)〜(E)のいずれかに記載の化合物又はその医薬上許容される塩。
【0027】
本発明に係る化合物は、経口又は非経口的に投与することができる。その投与剤型は錠剤、カプセル剤、顆粒剤、散剤、粉剤、トローチ剤、軟膏剤、クリーム剤、乳剤、懸濁剤、坐剤、注射剤等であり、いずれも慣用の製剤技術(例えば、第15改正日本薬局方に規定する方法等)によって製造することができる。これらの投与剤型は、患者の症状、年齢及び治療の目的に応じて適宜選択することができる。
これらの製剤は、本発明の化合物を含有する組成物に薬理学的に許容されるキャリヤー、すなわち、賦形剤(例えば、結晶セルロース、デンプン、乳糖、マンニトール)、結合剤(例えば、ヒドロキシプロピルセルロース、ポリビニルピロリドン)、滑沢剤(例えば、ステアリン酸マグネシウム、タルク)、崩壊剤(例えば、カルボキシメチルセルロースカルシウム)、および/またはその他薬理学的に許容される各種添加剤を配合し、製造することができる。
【0028】
また、本発明の化合物を1以上の他の治療薬、種々の抗精神病薬(antipsychotics)、抗うつ薬、例えば、5HT3アンタゴニスト、5HT2アンタゴニスト、セロトニンアゴニスト、NK−1アンタゴニスト、選択的セロトニン再取込阻害薬(SSRI)、セロトニンノルアドレナリン再取込阻害薬(SNRI)、三環系抗うつ薬、ドーパミン作動性抗うつ薬、H3アンタゴニスト、5HT1Aアンタゴニスト、5HT1Bアンタゴニスト、5HT1Dアンタゴニスト、D1アゴニスト、M1アゴニスト、抗けいれん薬、認知機能増強薬、および、その他向精神薬(psychoactive drug)と共に使用してもよい。
【0029】
本発明の化合物と組み合わせて共に使用してもよい他の治療薬とは、例えばオンダンセトロン(ondansetron)、グラニセトロン(granisetron)、メトクロプラミド(metoclopramide)、スマトリプタン(sumatriptan)、ラウオルシン(rauwolscine)、ヨヒムビン(yohimbine)、メトクロプラミド(metoclopramide)、フルオキセチン(fluoxetine)、シタロプラム(citalopram)、エスシタロプラム(escitalopram)、フェモキセチン(femoxetine)、フルボキサミン(fluvoxamine)、パロキセチン(paroxetine)、インダルピン(indalpine)、サートラリン(sertraline)、ジメルジン(zimeldine)、ベンラファキシン(venlafaxine)、レボキセチン(reboxetine)、ミルナシプラン(Milnacipran)、デュロキセチン(duloxetine)、イミプラミン(imipramine)、アミトリプチリン(amitriptiline)、クロミプラミン(chlomipramine)、ノルトリプチリン(nortriptiline)、ブプロピオン(bupropion)、アミネプチン(amineptine)、ジバルプロエクス(divalproex)、カルバマゼピン(carbamazepine)、ジアゼパム(diazepam)、リスペリドン(risperidone)、オランザピン(olanzapine)、ジプラシドン(ziprasidone)、アリピプラゾール(aripiprazole)、クエチアピン(quetiapine)、ペロスピロン(perospirone)、クロザピン(clozapine)ハロペリドール(haloperidol)、ピモジド(pimozide)、ドロペリドール(droperidol)、クロルプロマジン(chlorpromazine)、チオリダジン(thioridazine)、メソリダジン(mesoridazine)、トリフルオペラジン(trifluoperazine)、ペルフェナジン(perphenazine)、フルフェナジン(fluphenazine)、チフルプロマジン(thiflupromazine)、プロクロルペラジン(prochlorperazine)、アセトフェナジン(acetophenazine)、チオチキセン(thiothixene)、クロルプロチキセン(chlorprothixene)、ラモトリジン(lamotrigine)、ロキサピン(loxapine)、モリンドン(molindone)等を挙げることができる。これら組み合わせは、同時に(同一の医薬処方において、または異なる医薬処方において)、別々に、または連続的に投与されればよい。
【0030】
本発明の化合物の組み合わせによる使用および治療方法に関連する特に有利な点には、個々の成分の通常使用される投与量よりも少ない投与量での同等または改善された効果を挙げることができる。また、精神障害の陽性症状および/または陰性症状および/または認知機能障害に対する治療効果のさらなる増強も期待される。本発明の組み合わせによる使用および治療方法は、ある種の神経弛緩薬での治療に十分に応答しない、または該治療に耐性のある患者の治療においても利益を提供しうる。
【0031】
本発明に係る化合物の投与量は、成人を治療する場合で1日1〜2000mgであり、これを1日1回又は数回に分けて投与する。この投与量は、患者の年齢、体重及び症状によって適宜増減することができる。
【0032】
式[I]の化合物は種々の合成方法によって製造することができる。以下の方法は、本発明化合物の製造法の例示であり、これに限定されるものではない。
【0033】
以下の一般的製造法中、「不活性溶媒」とは例えばメタノール、エタノール、イソプロパノール、n−ブタノール、エチレングリコール等のアルコール類、ジエチルエーテル、t−ブチルメチルエーテル、ジイソプロピルエーテル、テトラヒドロフラン、1,4−ジオキサン、1,2−ジメトキシエタン等のエーテル類、ペンタン、ヘキサン、ヘプタン、トルエン、ベンゼン、キシレン等の炭化水素類、酢酸エチル、ギ酸エチル等のエステル類、アセトン、メチルエチルケトン等のケトン類、クロロホルム、ジクロロメタン等のハロゲン化炭素系溶媒、ジメチルホルムアミド、N-メチルピロリドン等のアミド類、アセトニトリル、ジメチルスルホキシド、水又はこれらの混合溶媒等である。
【0034】
「塩基」とは例えば、水素化リチウム、水素化ナトリウム、水素化カリウム、水素化カルシウムなどのアルカリ金属又はアルカリ土類金属の水素化物;リチウムアミド、ナトリウムアミド、リチウムジイソプロピルアミド、リチウムジシクロヘキシルアミド、リチウムヘキサメチルジシラジド、ナトリウムヘキサメチルジシラジド、カリウムヘキサメチルジシラジドなどのアルカリ金属又はアルカリ土類金属のアミド;ナトリウムメトキシド、ナトリウムエトキシド、カリウム tert−ブトキシドなどのアルカリ金属又はアルカリ土類金属の低級アルコキシド;ブチルリチウム、sec−ブチルリチウム、tert−ブチルリチウム、メチルリチウムなどのアルキルリチウム;水酸化ナトリウム、水酸化カリウム、水酸化リチウム、水酸化バリウムなどのアルカリ金属又はアルカリ土類金属の水酸化物;炭酸ナトリウム、炭酸カリウム、炭酸セシウムなどのアルカリ金属又はアルカリ土類金属の炭酸塩;炭酸水素ナトリウム、炭酸水素カリウムなどのアルカリ金属又はアルカリ土類金属の炭酸水素塩;トリエチルアミン、N−メチルモルホリン、N,N−ジイソプロピルエチルアミン、1,8−ジアザビシクロ[5.4.0]ウンデカ−7−エン(DBU)、1,5−ジアザビシクロ[4.3.0]ノン−5−エン(DBN)、N,N−ジメチルアニリンなどのアミン;ピリジン、イミダゾール、2,6−ルチジンなどの塩基性ヘテロ環化合物などである。これらの塩基は当業者に公知である種々の反応条件に応じて適宜選択される。
【0035】
「酸」とは例えば、塩酸、臭化水素酸、硫酸、硝酸、リン酸などの無機酸及びp−トルエンスルホン酸、メタンスルホン酸、トリフルオロ酢酸、ギ酸、酢酸、クエン酸、シュウ酸などの有機酸である。これらの酸は当業者に公知である種々の反応条件に応じて適宜選択される。
「ルイス酸」とは例えば、三フッ化ホウ素、三塩化アルミニウム、四塩化チタン、三塩化鉄、塩化亜鉛、四塩化スズなどをあげることができる。
【0036】
一般的製造法1
【0037】
【化5】

【0038】
式中、X1は、臭素原子、ヨウ素原子、またはトリフルオロメタンスルホニルオキシ基を示し、その他の記号は前記と同義である。
【0039】
工程1:不活性溶媒中、塩基の存在下又は非存在下、パラジウム触媒及び必要に応じてパラジウム触媒の配位子を使用することにより化合物(1)に対して化合物(2)を反応させることにより、本発明化合物(I)を得ることができる。
【0040】
ここで、パラジウム触媒とは、例えば酢酸パラジウム、トリス(ジベンジリデンアセトン)ジパラジウム、テトラキス(トリフェニルホスフィン)パラジウム、ジクロロビス(トリフェニルホスフィン)パラジウム、(1,3−ジイソプロピルイミダゾール−2−イリデン)(3−クロロピリジル)パラジウム(II)二塩化物、[1,3−ビス(2,6−ジイソプロピルフェニル)イミダゾール−2−イリデン](3−クロロピリジル)パラジウム(II)二塩化物、塩化〔1,1’−ビス(ジフェニルホスフィノ)フェロセン〕パラジウム等を挙げることができ、配位子とは例えばトリフェニルホスフィン、2,2−ビス(ジフェニルホスフィノ)−1,1−ビナフチル(BINAP)、2−(ジ−tert−ブチルホスフィノ)ビフェニル、9,9−ジメチル−4,5−ビス(ジフェニルホスフィノ)キサンテン(Xantphos)等を挙げることができ、化合物(2)の例としては、R4MgClなどのGrignard反応剤、R4ZnClなどの亜鉛反応剤、R4とホウ酸又はホウ酸エステルが結合したものなどのホウ素反応剤やR4SnBu3などのスズ反応剤などが挙げられる。
【0041】
一般的製造法2
【0042】
【化6】

【0043】
式中、X2は、ハロゲン原子又はヒドロキシ基を示し、その他の記号は前記と同義である。
【0044】
工程2:不活性溶媒中、塩基存在下又は非存在下、化合物(3)とX2がハロゲン原子である化合物(4)を反応させ、本発明化合物(I)を得ることができる。或いは化合物(3)とX2が水酸基である化合物(4)を当業者に公知である種々のアミド化反応に供することにより、本発明化合物(I)を得ることができる。ここでアミド化反応とは、例えば不活性溶媒中、塩基存在下又は非存在下、O−(7−アザベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウム ヘキサフルオロリン酸(HATU)、O−(ベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウム ヘキサフルオロリン酸(HBTU)、N,N’−ジシクロヘキシルカルボジイミド(DCC)、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩(EDC・HCl)、ジフェニルホスホリルアジド(DPPA)又はカルボニルジイミダゾール(CDI)などの縮合剤を用いたアミド化反応、クロロ炭酸エチル、クロロ炭酸イソブチル又はトリメチルアセチルクロリドなどを用いた混合酸無水物経由のアミド化反応などである。ここで縮合剤を用いたアミド化反応の際、必要に応じて1−ヒドロキシベンゾトリアゾール(HOBt)、ヒドロキシスクシンイミド(HOSu)などの添加剤を使用することができる。
【0045】
一般的製造法3
【0046】
【化7】

【0047】
式中、Lは、ハロゲン原子、メタンスルホニルオキシ基、トリフルオロメタンスルホニルオキシ基又はp−トルエンスルホニルオキシ基などの脱離基を示し、Raは、C1-6アルキル基を示し、その他の記号は前記と同義である。
【0048】
工程3:不活性溶媒中、塩基存在下又は非存在下、化合物(5)と化合物(6)を反応させることにより、本発明化合物(I−1)を得ることができる。
【0049】
一般的製造法4
【0050】
【化8】

【0051】
式中の記号は前記と同義である。
【0052】
工程4:不活性溶媒中、塩基存在下又は非存在下、本発明の化合物(I-2)と化合物(7)を反応させることにより、本発明化合物(I−1)を得ることができる。
【0053】
一般的製造法5
【0054】
【化9】

【0055】
工程5:一般的製造法2の工程2と同様の方法で化合物(8)と化合物(4)から化合物(1)を合成することができる。
【0056】
一般的製造法6
【0057】
【化10】

【0058】
工程6:不活性溶媒中、酸存在下又は非存在下、還元剤を用いて、化合物(9)と化合物(10)を還元的アミノ化反応に供することにより化合物(8)を得ることができる。ここで還元剤とは例えば、水素化トリアセトキシホウ素ナトリウム、水素化シアノホウ素ナトリウム、水素化ホウ素ナトリウムなどである。
【0059】
工程7:一般的製造法1の工程1と同様の方法で化合物(8)と化合物(2)から化合物(3)を合成することができる。
【0060】
工程8:一般的製造法1の工程1と同様の方法で化合物(9)と化合物(2)から化合物(11)を合成することができる。
【0061】
工程9:一般的製造法6の工程6と同様の方法で化合物(11)と化合物(10)から化合物(3)を合成することができる。
【0062】
一般的製造法7
【0063】
【化11】

【0064】
式中、RbおよびRcは、独立して水素原子、C1-6アルキル基、C1-6ハロアルキル基、又はC1-6アルコキシC1-6アルキル基を示し、或いはRbとRcは結合する炭素原子と一緒になってC3-6シクロアルキル環を形成してもよい。
【0065】
工程10:一般的製造法6の工程6と同様の方法で化合物(12)と化合物(13)から化合物(8)を合成することができる。
【0066】
工程11:一般的製造法1の工程1と同様の方法で化合物(8)と化合物(2)から化合物(3)を合成することができる。
【0067】
工程12:一般的製造法1の工程1と同様の方法で化合物(12)と化合物(2)から化合物(14)を合成することができる。
【0068】
工程13:一般的製造法6の工程6と同様の方法で化合物(14)と化合物(13)から化合物(3)を合成することができる。
【0069】
一般的製造法8
【0070】
【化12】

【0071】
工程14:一般的製造法2の工程2と同様の方法で化合物(14)と化合物(4)から化合物(5)を合成することができる。
【0072】
工程15:一般的製造法2の工程2と同様の方法で化合物(12)と化合物(4)から化合物(15)を合成することができる。
【0073】
工程16:一般的製造法1の工程1と同様の方法で化合物(15)と化合物(2)から化合物(5)を合成することができる。
【実施例】
【0074】
次に、製造例、実施例及び試験例により本発明をさらに詳細に説明するが、本発明はこれらの実施例に限定されるものではない。
【0075】
カラムクロマトグラフィーを使用して精製した際の「NHシリカゲルカートリッジ」にはBiotage(登録商標)SNAPCartridge KP−NH、「シリカゲルカートリッジ」にはBiotage(登録商標)SNAPCartridge KP−Silを使用した。
【0076】
製造例及び実施例中記載の各機器データは以下の測定機器で測定した。
【0077】
MSスペクトル:島津LCMS−2010EV又はmicromass Platform LC
NMRスペクトル:[1H-NMR]600MHz:JNM−ECA600(日本電子)、500MHz:JNM−ECA500(日本電子)、300MHz:UNITYNOVA300(Varian Inc.)、200MHz:GEMINI2000/200(Varian Inc.)
【0078】
実施例中で使用したマイクロウエーブ反応装置はInitiator(Biotage AB)である。
【0079】
実施例中の化合物名はACD/Name (ACD/Labs 10.01, Advanced Chemistry Development Inc.)により命名した。
【0080】
製造例1 6−フルオロ−3’−(ヒドロキシメチル)ビフェニル−3−カルバルデヒド
【0081】
【化13】

【0082】
3−ブロモ−4−フルオロ−ベンズアルデヒド(1.00g)、3−(ヒドロキシメチル)フェニルボロン酸(787mg)、テトラキス(トリフェニルホスフィン)パラジウム(569mg)、炭酸カリウム(1.36g)、ジメチルホルムアミド(6mL)とエタノール(3mL)の混合物をマイクロウエーブ反応装置(150℃、20分)で反応を行った。酢酸エチルを加え、セライト(Celite登録商標)ろ過後、酢酸エチル溶液を水で洗浄した。無水硫酸ナトリウムで酢酸エチル層を乾燥した。乾燥剤をろ別後、酢酸エチル層を減圧濃縮した。得られた残渣をカラムクロマトグラフィー(シリカゲルカートリッジ、ヘキサン:酢酸エチル=80:20〜65:35)で精製し、標題化合物(1.10g)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.74 - 1.81 (m, 1 H) 4.74 - 4.82 (m, 2 H) 7.28 - 7.62 (m, 5 H) 7.85 - 7.91 (m, 1 H) 7.97 - 8.04 (m, 1 H) 10.0 (s, 1 H)
【0083】
製造例2 {5’−[(シクロブチルアミノ)メチル]−2’−フルオロビフェニル−3−イル}メタノール
【0084】
【化14】

【0085】
シクロブチルアミン(370mg)、6−フルオロ−3’−(ヒドロキシメチル)ビフェニル−3−カルバルデヒド(1.00g)とクロロホルム(10mL)の混合物を室温で30分撹拌した。これに水素化トリアセトキシホウ素ナトリウム(1.29g)を加え、1.5日撹拌した。反応液を1M水酸化ナトリウム水溶液で洗浄した後、無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(シリカゲルカートリッジ、ヘキサン:酢酸エチル=75:25〜15:85)で精製し、標題化合物(1.16g)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.59 - 1.79 (m, 4 H) 2.18 - 2.27 (m, 2 H) 3.31 (m, 1 H) 3.72 (s, 2 H) 4.76 (s, 2 H) 7.03 - 7.14 (m, 1 H) 7.23 - 7.30 (m, 1 H) 7.33 - 7.58 (m, 5 H)
(ESI pos.) m/z : 286 ([M+H]+)
【0086】
同様にして、以下の化合物を合成した。
{5’−[(シクロペンチルアミノ)メチル]−2’−フルオロビフェニル−3−イル}メタノール
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.31 - 1.43 (m, 2 H) 1.50 - 1.59 (m, 2 H) 1.65 - 1.74 (m, 2 H) 1.82 - 1.91 (m, 2 H) 3.09 - 3.17 (m, 1 H) 3.77 (s, 2 H) 4.75 (s, 2 H) 7.05 - 7.13 (m, 1 H) 7.22 - 7.29 (m, 1 H) 7.33 - 7.58 (m, 5 H)
(ESI pos.) m/z : 300 ([M+H]+)
【0087】
{2’−フルオロ−5’−[(ペンタン−3−イルアミノ)メチル]ビフェニル−3−イル}メタノール
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.83 - 0.93 (m, 6 H) 1.40 - 1.53 (m, 4 H) 2.41 - 2.47 (m, 1 H) 3.77 (s, 2 H) 4.75 (s, 2 H) 7.04 - 7.57 (m, 7 H)
(ESI pos.) m/z : 302 ([M+H]+)
【0088】
製造例3 N−(3−ブロモ−4−フルオロベンジル)−2−メトキシエタンアミン
【0089】
【化15】

【0090】
2−メトキシエチルアミン(337mg)、3−ブロモ−4−フルオロ−ベンズアルデヒド(1.00g)、クロロホルム(10mL)の混合物を室温で30分撹拌した。これに水素化トリアセトキシホウ素ナトリウム(1.33g)を加え、12時間反応した。反応液を1M水酸化ナトリウム水溶液で洗浄した後、無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下ろ液を留去した。得られた残渣をカラムクロマトグラフィー(シリカゲルカートリッジ、クロロホルム:メタノール=100:0〜97:3)で精製し、標題化合物(796mg)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 2.75 - 2.80 (m, 2 H) 3.36 (s, 3 H) 3.48 - 3.53 (m, 2 H) 3.76 (s, 2 H) 7.03 - 7.08 (m, 1 H) 7.21 - 7.25 (m, 1 H) 7.53 - 7.56 (m, 1 H)
(ESI pos.) m/z : 262、264 ([M+H]+)
【0091】
同様にして、以下の化合物を合成した。
N−(3−ブロモ−4−フルオロベンジル)シクロペンタンアミン
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.31 - 1.39 (m, 2 H) 1.51 - 1.59 (m, 2 H) 1.65 - 1.75 (m, 2 H) 1.81 - 1.89 (m, 2 H) 3.05 - 3.13 (m, 1 H) 3.72 (s, 2 H) 7.02 - 7.08 (m, 1 H) 7.20 - 7.25 (m, 1 H) 7.51 - 7.55 (m, 1 H)
(ESI pos.) m/z : 272、274 ([M+H]+)
【0092】
N−(3−ブロモ−4−フルオロベンジル)−2−メチルプロパン−1−アミン
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.92 (d, J=6.88 Hz, 6 H) 1.70 - 1.80 (m, 1 H) 2.41 (d, J=6.88 Hz, 2 H) 3.73 (s, 2 H) 7.06 (t, J=8.48 Hz, 1 H) 7.21 - 7.25 (m, 1 H) 7.52 - 7.56 (m, 1 H)
(ESI pos.) m/z : 260、262 ([M+H]+)
【0093】
N−(3−ブロモ−4−フルオロベンジル)プロパン−2−アミン
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.02 - 1.11 (m, 6 H) 2.77 - 2.90 (m, 1 H) 3.73 (s, 2 H) 7.00 - 7.08 (m, 1 H) 7.20 - 7.25 (m, 1 H) 7.47 - 7.55 (m, 1 H)
(ESI pos.) m/z : 246、248 ([M+H]+)
【0094】
N−(3−ブロモ−4−フルオロベンジル)シクロヘキサンアミン
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.01 - 1.32 (m, 5 H) 1.57 - 1.92 (m, 5 H) 2.36 - 2.48 (m, 1 H) 3.53 (s, 2 H) 6.98 - 7.03 (m, 1 H) 7.17 - 7.21 (m, 1 H) 7.47 (dd, J=6.65, 2.06 Hz, 1 H)
(ESI pos.) m/z : 286、288 ([M+H]+)
【0095】
2−[(3−ブロモ−4−フルオロベンジル)アミノ]プロパン−1−オール
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.12 (d, J=6.42 Hz, 3 H) 2.85 - 2.93 (m, 1 H) 3.33 - 3.41 (m, 1 H) 3.61 - 3.94 (m, 4 H) 7.06 - 7.11 (m, 1 H) 7.27 - 7.29 (m, 1 H) 7.55 - 7.58 (m, 1 H)
(ESI pos.) m/z : 262、264 ([M+H]+)
【0096】
製造例4 N−(3−ブロモ−4−フルオロベンジル)−N−シクロペンチル−1−メチル−1H−イミダゾール−4−カルボキサミド
【0097】
【化16】

【0098】
N−(3−ブロモ−4−フルオロベンジル)シクロペンタンアミン(1.50g)、1−メチル−1H−イミダゾール−4−カルボン酸(695mg)、ヘキサフルオロリン酸ウロニウム 2−(1H−7−アザベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルメタンアミニウム(HATU)(2.72g)、ジイソプロピルエチルアミン(2.55mL)とアセトニトリル(23mL)の混合物を室温で4時間撹拌した。反応液を酢酸エチルで希釈し、酢酸エチル溶液を水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=90:10〜20:80)で精製し、標題化合物(2.00g)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.48 - 1.95 (m, 8 H) 3.62 - 3.75 (m, 3 H) 4.42 - 5.85 (m, 3 H) 6.97 - 7.21 (m, 2 H) 7.27 - 7.47 (m, 2 H) 7.53 (s, 1 H)
(ESI pos.) m/z : 380、382 ([M+H]+)
【0099】
同様にして、以下の化合物を合成した。
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−(2−メチルプロピル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.77 - 1.00 (m, 6 H) 1.91 - 2.14 (m, 1 H) 3.17 - 3.28 (m, 1 H) 3.87 - 5.45 (m, 3 H) 7.00 - 7.26 (m, 2 H) 7.30 - 7.62 (m, 3 H)
(ESI pos.) m/z : 368、370 ([M+H]+)
【0100】
N−(3−ブロモ−4−フルオロベンジル)−N−(プロパン−2−イル)−1H−1,2,4−トリアゾール−3−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.17 - 1.29 (m, 6 H) 4.65 (s, 3 H) 7.01 - 7.25 (m, 2 H) 7.42 - 8.60 (m, 2 H)
(ESI pos.) m/z : 339、341 ([M-H]-)
【0101】
N−(3−ブロモ−4−フルオロベンジル)−N−シクロヘキシル−1H−1,2,4−トリアゾール−3−カルボキサミド
(ESI pos.) m/z : 379、381 ([M-H]-)
【0102】
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.11 - 1.26 (m, 6 H) 3.63 - 3.78 (m, 3 H) 4.48 - 5.79 (m, 3 H) 6.95 - 7.59 (m, 5 H)
(ESI pos.) m/z : 354、356 ([M+H]+)
【0103】
N−(3−ブロモ−4−フルオロベンジル)−N−シクロヘキシル−1−メチル−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.99 - 1.86 (m, 10 H) 3.70 (br. s., 3 H) 4.33 - 5.32 (m, 3 H) 6.95 - 7.58 (m, 5 H)
(ESI pos.) m/z : 394、396 ([M+H]+)
【0104】
N−(3−ブロモ−4−フルオロベンジル)−N−(2−メトキシエチル)−1−メチル−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 3.25 - 3.34 (m, 3 H) 3.48 - 3.75 (m, 6 H) 4.07 - 4.18 (m, 1 H) 4.70 - 4.83 (m, 1 H) 5.36 - 5.53 (m, 1 H) 7.00 - 7.24 (m, 2 H) 7.29 - 7.63 (m, 3 H)
(ESI pos.) m/z : 370、372 ([M+H]+)
【0105】
製造例5 N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−(プロパン−2−イル)−1H−1,2,4−トリアゾール−3−カルボキサミド
【0106】
【化17】

【0107】
N−(3−ブロモ−4−フルオロベンジル)−N−(プロパン−2−イル)−1H−1,2,4−トリアゾール−3−カルボキサミド(2.06g)とジメチルホルムアミド(20mL)との混合物に、水素化ナトリウム(約60%オイル、266mg)を加え30分撹拌した。ヨウ化メチル(1.1mL)を加えて、終夜、室温で撹拌した。反応液に水を加えて、クロロホルムで抽出した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、有機層を減圧下濃縮した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=50:50〜34:66〜0:100)で精製し、標題化合物(1.00g)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.13 - 1.23 (m, 6 H) 3.88 - 4.04 (m, 3 H) 4.60 - 4.83 (m, 3 H) 7.00 - 7.08 (m, 1 H) 7.20 - 8.13 (m, 3 H)
(ESI pos.) m/z : 395、397 ([M+H]+)
【0108】
同様にして以下の化合物を合成した。
N−(3−ブロモ−4−フルオロベンジル)−N−シクロヘキシル−1−メチル−1H−1,2,4−トリアゾール−3−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.95 - 1.89 (m, 10 H) 3.83 - 4.85 (m, 6 H) 6.95 - 8.17 (m, 4 H)
(ESI pos.) m/z : 355、357 ([M+H]+)
【0109】
製造例6 N−(3−ブロモ−4−フルオロベンジル)−1−メチル−1H−イミダゾール−4−カルボキサミド
【0110】
【化18】

【0111】
3−ブロモ−4−フルオロベンジルアミン(1.62g)、1−メチル−1H−イミダゾール−4−カルボン酸(1.0g)、HATU(4.52g)、ジイソプロピルエチルアミン(4.1mL)とアセトニトリル(26ml)を室温で1時間撹拌した。反応液に水とクロロホルムを加え撹拌後、クロロホルム層を分離し、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=50:50)と(シリカゲルカートリッジ、クロロホルム:メタノール=99:1〜90:10))で精製し、標題化合物(1.87g)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 3.74 (s, 3 H) 4.52 - 4.58 (m, 2 H) 7.03 - 7.09 (m, 1 H) 7.34 - 7.56 (m, 4 H)
(ESI pos.) m/z : 312、314 ([M+H]+)
【0112】
製造例7 N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−プロピル−1H−イミダゾール−4−カルボキサミド
【0113】
【化19】

【0114】
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−1H−イミダゾール−4−カルボキサミド(156mg)のテトラヒドロフラン(3mL)溶液に、水素化ナトリウム(約60%オイル、24mg)を加えて30分撹拌した。これに、1−ヨードプロパン(136mg)を加え室温で4時間撹拌した。さらに水素化ナトリウム(約60%オイル、12mg)を加えて、終夜撹拌した。水を加え酢酸エチルで抽出した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=90:10〜20:80)で精製し、標題化合物(56mg)を得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 0.81 - 0.94 (m, 3 H) 1.59 - 1.69 (m, 2 H) 3.72 (s, 5 H) 4.62 - 5.38 (m, 2 H) 7.16 - 7.62 (m, 5 H)
(ESI pos.) m/z : 354、356 ([M+H]+)
【0115】
製造例8 N−(4−ブロモ−3−フルオロベンジル)プロパン−2−アミン塩酸塩
【0116】
【化20】

イソプロピルアミン(13.3g)、3−ブロモ−4−フルオロベンズアルデヒド(13.3g)とクロロホルム(300mL)の混合物を室温で30分間撹拌した。これに水素化トリアセトキシホウ素ナトリウム(47.7g)を数回に分けて加え、室温で15時間撹拌した。2M 水酸化ナトリウム水溶液(150mL)を加え、室温で30分間撹拌した。クロロホルム層を分離し、水層をクロロホルムで抽出した。合わせたクロロホルム層を水で洗浄し、無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下クロロホルムを留去した。得られた残渣を酢酸エチル(150mL)に溶解し、4M 塩酸/酢酸エチル(150mL)を加えた。析出した固体をろ取し、標題化合物29.0gを得た。
1H NMR (600 MHz, DMSO-d6) d ppm 1.29 (d, J=6.42 Hz, 6 H) 3.22 - 3.34 (m, 1 H) 4.13 (s, 2 H) 7.42 - 7.51 (m, 1 H) 7.60 - 7.68 (m, 1 H) 7.95 - 8.04 (m, 1 H) 8.95 - 9.24 (m, 2 H)
【0117】
同様にして以下の化合物を合成した。
N−(3−ブロモ−4−メトキシベンジル)プロパン−2−アミン塩酸塩
1H NMR (200 MHz, DMSO-d6) d ppm 1.20 - 1.37 (m, 6 H) 3.14 - 3.37 (m, 1 H) 3.87 (s, 3 H) 3.98 - 4.17 (m, 2 H) 7.18 (d, J=8.35 Hz, 1 H) 7.55 (d, J=8.35 Hz, 1 H) 7.82 (s, 1 H) 8.98 (br. s., 2 H)
(ESI pos.) m/z : 258、260 ([M+H]+)
【0118】
N−(3−ブロモ−5−クロロベンジル)プロパン−2−アミン塩酸塩
1H NMR (200 MHz, DMSO-d6) d ppm 1.23 - 1.35 (m, 6 H) 3.17 - 3.40 (m, 1 H) 4.05 - 4.23 (m, 2 H) 7.71 - 7.97 (m, 3 H) 9.19 (br. s., 2 H)
(ESI pos.) m/z : 262、264 ([M+H]+)
【0119】
N−(3−ブロモ−4−メチルベンジル)プロパン−2−アミン塩酸塩
1H NMR (600 MHz, DMSO-d6) d ppm 1.24 - 1.31 (m, 6 H) 2.35 (s, 3 H) 3.22 - 3.30 (m, 1 H) 4.10 (s, 2 H) 7.40 - 7.43 (m, 1 H) 7.46 - 7.49 (m, 1 H) 7.83 (s, 1 H) 8.97 (br. s., 1 H)
(ESI pos.) m/z : 242、244 ([M+H]+)
【0120】
N−[3−ブロモ−5−(トリフルオロメチル)ベンジル]プロパン−2−アミン塩酸塩1H NMR (600 MHz, DMSO-d6) d ppm 1.30 (d, J=6.88 Hz, 6 H) 4.25 (s, 2 H) 8.01 - 8.20 (m, 3 H) 9.04 - 9.22 (m, 2 H)
(ESI pos.) m/z : 296、298 ([M+H]+)
【0121】
N−[3−ブロモ−5−(トリフルオロメトキシ)ベンジル]プロパン−2−アミン塩酸塩
1H NMR (200 MHz, DMSO-d6) d ppm 1.30 (d, J=6.59 Hz, 6 H) 3.20 - 3.40 (m, 1 H) 4.13 - 4.30 (m, 2 H) 7.72 (s, 1 H) 7.75 (s, 1 H) 7.94 (s, 1 H) 9.22 (br. s., 2 H)
(ESI pos.) m/z : 312、314 ([M+H]+)
【0122】
N−(3−ブロモ−4−クロロベンジル)プロパン−2−アミン塩酸塩
1H NMR (200 MHz, DMSO-d6) d ppm 1.29 (d, J=6.59 Hz, 6 H) 3.10 - 3.50 (m, 1 H) 4.14 (s, 1 H) 7.58 - 7.68 (m, 1 H) 7.68 - 7.77 (m, 1 H) 8.02 - 8.12 (m, 1 H) 9.23 (br. s., 2 H)
(ESI pos.) m/z : 262、264 ([M+H]+)
【0123】
製造例9 N−(3−ブロモ−4−フルオロベンジル)−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
【0124】
【化21】

N−(4−ブロモ−3−フルオロベンジル)プロパン−2−アミン塩酸塩(2.3g)、1H−イミダゾール−4−カルボン酸(1.18g)、HOBT(1.61g)、EDC塩酸塩(2.68g)、トリエチルアミン(2.4mL)とジメチルホルムアミド(40mL)の混合物を室温で、6日間撹拌した。減圧下、反応混合物を濃縮し、残渣に飽和炭酸水素ナトリウム水溶液を加え、30分間撹拌した。これを酢酸エチルで抽出し、酢酸エチル層を水で洗浄した。酢酸エチル層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン/酢酸エチル=90:10〜10:90)で精製し、標題化合物10.2gを得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.04 - 1.37 (m, 6 H) 4.49 - 5.78 (m, 3 H) 6.95 - 7.82 (m, 5 H)
(ESI pos.) m/z : 340、342 ([M+H]+)
【0125】
同様にして以下の化合物を合成した。
N−(3−ブロモ−4−メトキシベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.06 - 1.30 (m, 6 H) 3.70 (s, 3 H) 3.86 (s, 3 H) 4.41 - 5.81 (m, 3 H) 6.74 - 7.63 (m, 5 H)
(ESI pos.) m/z : 366、368 ([M+H]+)
【0126】
N−(3−ブロモ−5−クロロベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.05 - 1.30 (m, 6 H) 3.72 (s, 3 H) 4.46 - 5.83 (m, 3 H) 7.16 - 7.61 (m, 5 H)
(ESI pos.) m/z : 370、372 ([M+H]+)
【0127】
N−(3−ブロモ−4−メチルベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.10 - 1.25 (m, 6 H) 3.63 - 3.79 (m, 3 H) 4.52 - 5.82 (m, 3 H) 7.07 - 7.60 (m, 5 H)
(ESI pos.) m/z : 350、352 ([M+H]+)
【0128】
N−[3−ブロモ−5−(トリフルオロメチル)ベンジル]−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.04 - 1.30 (m, 6 H) 3.60 - 3.80 (m, 3 H) 4.56 - 5.91 (m, 3 H) 7.16 - 7.70 (m, 5 H)
(ESI pos.) m/z : 404、406 ([M+H]+)
【0129】
N−[3−ブロモ−5−(トリフルオロメトキシ)ベンジル]−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.10 - 1.31 (m, 6 H) 3.62 - 3.80 (m, 3 H) 4.50 - 5.87 (m, 3 H) 7.04 - 7.63 (m, 5 H)
(ESI pos.) m/z : 420、422 ([M+H]+)
【0130】
N−(3−ブロモ−4−クロロベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.03 - 1.32 (m, 6 H) 3.71 (s, 3 H) 4.41 - 5.86 (m, 3 H) 7.10 - 7.62 (m, 5 H)
(ESI pos.) m/z : 370、372 ([M+H]+)
【0131】
製造例10 N−[(3’,4’,5’,6−テトラフルオロビフェニル−3−イル)メチル]プロパン−2−アミン
【0132】
【化22】

N−(4−ブロモ−3−フルオロベンジル)プロパン−2−アミン(500mg)、(3,4,5−トリフルオロフェニル)ボロン酸(386mg)、炭酸セシウム(780mg)、テトラキス(トリフェニルホスフィン)パラジウム(230mg)、トルエン(2.2mL)、エタノール(2.2mL)と水(1.4mL)の混合物をマイクロウエーブ反応装置で、150℃で、30分間反応を行った。放冷後、飽和炭酸水素ナトリウムを加え、酢酸エチルで抽出した。酢酸エチル層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去し、得られた残渣をクロマトグラフィー(シリカゲルカートリッジ、クロロホルム/メタノール=100:0〜90:10)で精製し、標題化合物628mgを得た。
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.11 (d, J=6.30 Hz, 6 H) 2.87 (spt, J=6.30 Hz, 1 H) 3.79 (s, 2 H) 7.08 - 7.14 (m, 1 H) 7.16 - 7.22 (m, 2 H) 7.30 - 7.36 (m, 2 H)
(ESI pos.) m/z : 298 ([M+H]+)
【0133】
同様にして以下の化合物を合成した。
2−({[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}アミノ)プロパン−1−オール
1H NMR (600 MHz, CHLOROFORM-d) d ppm 1.10 - 1.13 (m, 4 H) 2.85 - 2.91 (m, 1 H) 3.28 - 3.34 (m, 1 H) 3.60 - 3.65 (m, 1 H) 3.75 - 3.80 (m, 1 H) 3.89 - 3.94 (m, 1 H) 7.09 - 7.15 (m, 1 H) 7.27 - 7.41 (m, 4 H) 7.54 - 7.59 (m, 2 H)
(ESI pos.) m/z : 344 ([M+H]+)
【0134】
1−[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メタンアミン
1H NMR (200 MHz, CHLOROFORM-d) d ppm 3.91 (s, 2 H) 7.05 - 7.64 (m, 7 H)
【0135】
実施例1 N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
【0136】
【化23】

【0137】
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド(127mg)、4−トリフルオロメトキシフェニルボロン酸(154mg)、テトラキス(トリフェニルホスフィン)パラジウム(45mg)、炭酸カリウム(70mg)、ジメチルホルムアミド(3mL)とエタノール(1.5mL)の混合物をマイクロウエーブ反応装置(150℃、25分)で反応を行った。酢酸エチルを加え、セライト(Celite登録商標)ろ過後、酢酸エチル溶液を水で洗浄した。無水硫酸ナトリウムで酢酸エチル層を乾燥した。乾燥剤をろ別後、酢酸エチル層を減圧濃縮した。得られた残渣をカラムクロマトグラフィー((NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=90:10〜酢酸エチル)と(シリカゲルカートリッジ、クロロホルム:メタノール=100:0〜97:3))で精製し、標題化合物(77mg)を得た。
【0138】
実施例2 N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}−1−メチル−N−プロピル−1H−イミダゾール−4−カルボキサミド 塩酸塩
【0139】
【化24】

【0140】
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−プロピル−1H−イミダゾール−4−カルボキサミド(56mg)、4−トリフルオロメトキシフェニルボロン酸(65mg)、テトラキス(トリフェニルホスフィン)パラジウム(20mg)、炭酸カリウム(44mg)、ジメチルホルムアミド(1.3mL)とエタノール(0.6mL)の混合物をマイクロウエーブ反応装置(150℃、25分)で反応を行った。酢酸エチルを加え、酢酸エチル溶液を水で洗浄した。無水硫酸ナトリウムで酢酸エチル層を乾燥した。乾燥剤をろ別後、酢酸エチル層を減圧濃縮した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=80:20〜20:80)と(シリカゲルカートリッジ、クロロホルム:メタノール=100:0〜97:3)で精製し、得られた残渣を酢酸エチルに溶解し、4N塩酸/酢酸エチル(約1mL)を加え5分撹拌後、減圧下溶媒を留去した。残渣に、ジエチルエーテル加え固化し、固体をろ取し、標題化合物(24mg)を得た。
【0141】
実施例3 メチル 2’−フルオロ−5’−({[(1−メチル−1H−1,2,4−トリアゾール−3−イル)カルボニル](プロパン−2−イル)アミノ}メチル)ビフェニル−3−カルボキシラート
【0142】
【化25】

【0143】
N−(3−ブロモ−4−フルオロベンジル)−1−メチル−N−(プロパン−2−イル)-1H−1,2,4−トリアゾール−3−カルボキサミド(492mg)、3−メトキシカルボニルフェニルボロン酸(274mg)、テトラキス(トリフェニルホスフィン)パラジウム(161mg)、炭酸セシウム(679mg)とトルエン/エタノール/水(3:3:2)(9mL)の混合物を100℃で1時間撹拌した。反応液に水を加え、酢酸エチルで抽出した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下濃縮した。得られた残渣をカラムクロマトグラフィー(NHシリカゲルカートリッジ、ヘキサン:酢酸エチル=50:50〜0:100)で精製し、標題化合物(486mg)を得た。
【0144】
実施例4 N−{[6−フルオロ−3’−(ヒドロキシメチル)ビフェニル−3−イル]メチル}−1−メチル−N−(プロパン−2−イル)−1H−1,2,4−トリアゾール−3−カルボキサミド
【0145】
【化26】

【0146】
メチル 2’−フルオロ−5’−({[(1−メチル−1H−1,2,4−トリアゾール−3−イル)カルボニル](プロパン−2−イル)アミノ}メチル)ビフェニル−3−カルボキシラート(392mg)のエタノール(19mL)の混合物に、水素化ホウ素ナトリウム(723mg)を加え、終夜還流した。さらに、水素化ホウ素ナトリウム(362mg)を加え、5時間還流した。放冷後、アセトンを加えて撹拌した後、水を加えて、クロロホルムで抽出した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下濃縮した。得られた残渣をカラムクロマトグラフィー(シリカゲルカートリッジ、クロロホルム/メタノール=99:1〜97:3)で精製し、標題化合物(180mg)を得た。
【0147】
実施例5 N−シクロブチル−N−{[6−フルオロ−3’−(ヒドロキシメチル)ビフェニル−3−イル]メチル}−1−メチル−1H−イミダゾール−4−カルボキサミド
【0148】
【化27】

【0149】
{5’−[(シクロブチルアミノ)メチル]−2’−フルオロビフェニル−3−イル}メタノール(700mg)、1−メチル−1H−イミダゾール−4−カルボン酸(340mg)、HATU(1.21g)、ジイソプロピルエチルアミン(1.13mL)とアセトニトリル(10.5ml)の混合物を室温で2.5時間撹拌した。反応液を酢酸エチルで希釈し、有機層を水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した。乾燥剤をろ別後、減圧下溶媒を留去した。得られた残渣をカラムクロマトグラフィー(シリカゲルカートリッジ、クロロホルム:メタノール=98:2〜95:5)及び(NHシリカゲルカートリッジ、クロロホルム:メタノール=100:0〜98:2)で精製し、標題化合物(758mg)を得た。
【0150】
実施例6 1−エチル−N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド
【化28】

【0151】
N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}−N−(プロパン−2−イル)−1H−イミダゾール−4−カルボキサミド(120mg)のジメチルホルムアミド(2mL)溶液に水素化ナトリウム(約60%オイル、12mg)を加え、室温で15分間撹拌した。これにヨードエタン(134mg)を加え、80℃で2時間撹拌した。飽和炭酸水素ナトリウム水溶液を加え、これを酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、有機層を減圧下濃縮し、得られた残渣を分取HPLCで精製し、標題化合物62mgを得た。
【0152】
実施例7 N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}−1−メチル−N−(プロパ−1−エン−2−イル)−1H−イミダゾール−4−カルボキサミド
【化29】

【0153】
1−[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メタンアミン(500mg)とアセトン(1mL)の混合物をマイクロウエーブ反応装置で、120℃、1時間反応した。反応溶液に無水硫酸ナトリウムを加え、乾燥剤をろ別後、減圧下溶媒を留去し、N−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}プロパ−1−エン−2−アミンを得た。得られたN−{[6−フルオロ−4’−(トリフルオロメトキシ)ビフェニル−3−イル]メチル}プロパ−1−エン−2−アミンにクロロホルム(10mL)、トリエチルアミン(265mg)、及び1−メチル−1H−イミダゾール−4−カルボン酸クロリド(260mg)を加えて、室温で2日間撹拌した。反応液に水を加えて、クロロホルムで抽出した。フェーズセパレータでクロロホルム層を分離後、減圧下溶媒を留去し、得られた残渣をHPLCおよびTLCで精製し、標題化合物30mgを得た。
【0154】
実施例1から7で示した化合物と、同様の方法で合成した化合物の構造式とそれらの機器データを表1−1から1−6に示した。表中の実施例の欄に記載された数字は、その化合物が上記実施例1から7の内、どの実施例と同様な方法で合成されたかを示したものである。
【0155】
【表1−1】

【0156】
【表1−2】

【0157】
【表1−3】

【0158】
【表1−4】

【0159】
【表1−5】

【0160】
【表1−6】

【0161】
試験例1 [グリシン取り込み阻害実験]
グリシン取り込み実験はNeuron, 8, 927−935, 1992に掲載された方法に従って行った。ヒト1型グリシントランスポーター(GlyT1)が内在性に発現している神経膠腫であるT98G細胞を用いた。T98G細胞を96ウェルプレートに2.0×104個/ウェルにて播種し、炭酸ガスインキュベーター内にて一晩培養した。被検物質は100%DMSO溶液に溶解したのち、150mM塩化ナトリウム、1mM塩化カルシウム、5mM塩化カリウム、1mM塩化マグネシウム、10mMグルコースおよび0.2%ウシ血清アルブミンを含む10mMHEPES緩衝液(pH7.4)に溶解させた。細胞培養用培地を除去した後、細胞を被検物質で10分間前処置した。その後、被検物質および[3H]グリシン(最終濃度 250nM)を細胞に添加し、室温にて15分間インキュベートした。インキュベーション終了後、マニーホールドにて細胞外液を吸引し、細胞外に存在する余分な標識グリシンを除去したのち、0.5Mの水酸化ナトリウム水溶液にて細胞を溶解した。細胞内に取り込まれたグリシン量は、細胞溶解液中の放射活性を液体シンチレーションカウンターで測定することにより求めた。10μMのALX5407存在下におけるグリシン取り込み量を非特異的取り込みとし、10μMのALX5407非存在下の総取り込み量から非特異的取り込み量を差し引いたものを特異的取り込み量とした。また、被検物質の10-9〜10-5M濃度での抑制曲線からグリシン取り込み阻害活性(IC50値)を算出した。
【0162】
なおALX5407はN−[(3R)−3−([1,1’−ビフェニル]−4−イルオキシ)−3−(4−フルオロフェニル)プロピル]−N−メチルグリシンHCl塩である。
【0163】
本発明化合物のIC50値は、化合物41、43、46〜50、54については1μM以上であり、それ他の化合物については1μMより小さかった。さらに化合物3、4、5、30、32、33、37、51、53のIC50値は0.1μM以上であり、その他の化合物のIC50値は0.1μMより小さかった。例えば、化合物2、6、7、8、10、11、13、14、15、16、17、18、19、20、21、22、23、24、25、26、28、31、34、35、36、39、40、42、52のIC50値は、それぞれ12.6nM、14.6nM、25.9nM、11.0nM、14.8nM、35.1nM、4.33nM、2.78nM、21.3nM、42.5nM、18.8nM、8.89nM、18.6nM、7.19nM、13.6nM、11.6nM、21.4nM、14.2nM、25.4nM、40.0nM、22.6nM、21.0nM、49.4nM、48.9nM、38.2nM、48.5nM、35.9nM、48.3nM、30.7nMであった。
【0164】
試験例2 [膜透過性実験]
医薬品開発に当たって膜透過性は、経口投与する医薬の体内吸収率との観点から重要な要素の1つであり、膜透過性が高い化合物は医薬品として腸管からの良好な吸収が期待される(Pharmaceutical Research (2002) Vol.19, No.7, 921-925参照)。
膜透過性試験は、PAMPA EvolutionTM(pION社)を用いてpION社の推奨プロトコールに準じて行った。詳細には、評価化合物溶液(評価化合物のDMSO溶液を各pH(4.0, 5.0, 6.2, 7.4)に調整したsystem solutionに添加し、希釈したもの)を調製し、人工脂質(GIT-0)で脂質二重膜を形成させたsandwichプレートの下段(Donor)に添加した。上段(Acceptor)にはacceptor sink bufferを添加し、一定時間経過後、Donor及びAcceptor溶液のUV測定から得られた化合物の累積透過量より膜透過係数Pe(×10−6cm/sec)を算出し、化合物の膜透過性を評価した。その結果、本願化合物No.8、10、12、15、16、18〜21、23〜26、28、34〜36、39〜42、54は、高透過性マーカー化合物であるメトプロロールの膜透過係数より高く、良好な膜透過性を示した。
【0165】
試験例3 [P−gpの基質認識性試験]
中枢神経系に作用を及ぼす薬物は、一般に血中から脳内に移行することが、薬効の発現に重要である。血液脳関門には、薬物の移行性を制御している排出(efflux)transporterとして代表的なものにP-糖タンパク質(P-glycoprotein,P−gp)が存在しており、P−gpはその基質となる薬物の脳移行を阻害している。したがって、医薬品開発においてP−gpの基質として認識されないことが、脳移行性の指標となる。
P−gpの基質認識性試験は、J Pharmacol. Exp. Ther. (1992) Vol. 263, No. 2, 840-845及びJ Biol. Chem. (1992) Vol. 267, No. 34, 24248-24252に記載の方法に準じて行った。詳細には、トランスウェル上に4日間培養したLLC-GA5-COL300細胞(ブタ腎由来培養腎上皮細胞株LLC-PK1由来Human MDR1 発現系)を用い、試験直前にウェル内をHank's balanced salt solution(HBSS)にて置換して試験に供した。評価化合物溶液(評価化合物のDMSO溶液をHBSSにて希釈し,最終濃度10μMに調整したもの)を、LLC-GA5-COL300細胞のDonor側に添加後、Acceptor側から一定量のHBSSを経時的に採取し、LC-MS/MSにて採取サンプル中の評価化合物濃度を測定した。
Acceptor側への化合物の累積透過量より,Apical→Basal及びBasal→Apicalそれぞれの膜透過係数(×10-6cm/sec)を算出し、その比(Efflux Ratio)からP−gpの基質認識性を評価した。
その結果、本願化合物No.10、17、18、20、22、24、36、54は、Nature Reviews Drug Discovery (2010), Vol. 9, 215-236に記載された判定基準において、P−gpの基質として認識されないと判定され、良好な脳移行性が示唆された(Pharmaceutical Research (2001), Vol. 18, No. 12, 1660-1668参照)。この結果から、本願化合物は、中枢神経系に作用を及ぼす薬物として有効に用いられることが期待される。
試験例4:社会性認知試験
実験には雄性Sprague−Dawley系ラットを用い、すでに報告された方法に準じて行った(Shimazaki et al.,Psychopharmacology,209,263−270,2010)。
ラット(Adult)(9週齢)にMK−801(0.1mg/kg)を腹腔内投与した後、直ぐに試験ケージに入れ、30分間馴化させた。MK−801投与から30分後、若齢ラット(4週齢)をラット(adult)を入れた試験ケージに入れ、5分間放置した。5分間にラット(adult)が若齢ラットに対して行った社会性行動(臭い嗅ぎ行動(sniffing),毛づくろい行動(grooming),追尾行動(following))の時間を測定した(1回目探索時間)。その後、若齢ラットのみを試験ケージから取り出し、ホームケージに戻した。30分後、1回目探索と同じ若齢ラットを試験ケージに入れ、5分間にラット(adult)が若齢ラットに対して行った社会性行動(臭い嗅ぎ行動,毛づくろい行動,追尾行動)の時間を測定した(2回目探索時間)。社会性認知は2回目探索時間/1回目探索時間で示した。披験物質(化合物10)は1回目探索開始時間の1時間前に経口投与した。結果を下表に示す。溶媒投与群には、0.5%メチルセルロース水溶液を投与した。
【表2】

披験物質投与群は溶媒投与群と比較して、2回目の探索時間/1回目の探索時間を有意に減少させ、認知機能障害改善作用を有することが示された。
【産業上の利用可能性】
【0166】
本発明化合物は、1型グリシントランスポーター(GlyT1)阻害作用を有し、従って、グリシントランスポーターに関連する疾患、具体的には、統合失調症、アルツハイマー病、認知機能障害、認知症、不安障害(全般性不安障害、パニック障害、強迫性障害、社会不安障害、外傷後ストレス障害、特定の恐怖症、急性ストレス障害等)、うつ病、薬物依存、痙攣、振戦、疼痛、及び睡眠障害等の予防又は治療に有効である。
【特許請求の範囲】
【請求項1】
式[I]
【化1】

(式中、
R1は、水素原子、又はC1-6アルキル基を示し、
R2は、C1-6アルキル基、C2-6アルケニル基、C3-6シクロアルキル基、C1-6ハロアルキル基、C1-6ヒドロキシアルキル基、又はC1-6アルコキシC1-6アルキル基を示し、
R3は、水素原子、C1-6アルキル基、C1-6アルコキシ基、C1-6ハロアルキル基、C1-6ハロアルコキシ基、又はハロゲン原子を示し、
R4は、フェニル基を示し、
該フェニル基は、C1-6アルキル基、C1-6アルコキシ基、C1-6ハロアルキル基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、C1-6アルコキシC1-6アルキル基、C2-7アルコキシカルボニル基、シアノ基、及びハロゲン原子から選択される1から3個の置換基で置換されてもよく、
Yは、式CH、又は
窒素原子を示す。)で表される化合物又はその医薬上許容される塩。
【請求項2】
R2が分岐C3-6アルキル基、又はC3-6シクロアルキル基である請求項1に記載の化合物又はその医薬上許容される塩。
【請求項3】
Yが式CHである請求項1又は2に記載の化合物又はその医薬上許容される塩。
【請求項4】
R3がハロゲン原子である請求項1〜3のいずれか1項に記載の化合物又はその医薬上許容される塩。
【請求項5】
R3がフッ素原子である請求項1〜3のいずれか1項に記載の化合物又はその医薬上許容される塩。
【請求項6】
R4が、フェニル基、又はC1-6アルコキシ基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、及びハロゲン原子から選択される1〜3個の置換基で置換されたフェニル基である請求項1〜5のいずれか1項に記載の化合物又はその医薬上許容される塩。
【請求項7】
式[I]の化合物が下記式
【化2】

(式中、
R1は、メチル基、又はエチル基を示し、
R4は、フェニル基、又は
C1-6アルコキシ基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、及びハロゲン原子から選択される1から3個の置換基で置換されたフェニル基を示す)で表される請求項1に記載の化合物又はその医薬上許容される塩。
【請求項8】
化合物が、
N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[6-フルオロ-3'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-[(4',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(3',6-ジフルオロ-4'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(3',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロ-3'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロ-4'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(4'-クロロ-6-フルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',5',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-{[3'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[4'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',5',6-テトラフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、又は
1-エチル-N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド
である請求項1に記載の化合物又はその医薬上許容される塩。
【請求項9】
化合物が、
N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[6-フルオロ-3'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-[(4',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[3'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[4'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',5',6-テトラフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、又は
1-エチル-N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド
である請求項1に記載の化合物又はその医薬上許容される塩。
【請求項10】
請求項1〜9のいずれか1項に記載の化合物又はその医薬上許容される塩を有効成分として含む医薬。
【請求項11】
請求項1〜9のいずれか1項に記載の化合物又はその医薬上許容される塩を有効成分として含む、統合失調症、アルツハイマー病、認知機能障害、認知症、不安障害、うつ病、薬物依存、痙攣、振戦、又は睡眠障害の疾患の予防剤又は治療剤。
【請求項1】
式[I]
【化1】

(式中、
R1は、水素原子、又はC1-6アルキル基を示し、
R2は、C1-6アルキル基、C2-6アルケニル基、C3-6シクロアルキル基、C1-6ハロアルキル基、C1-6ヒドロキシアルキル基、又はC1-6アルコキシC1-6アルキル基を示し、
R3は、水素原子、C1-6アルキル基、C1-6アルコキシ基、C1-6ハロアルキル基、C1-6ハロアルコキシ基、又はハロゲン原子を示し、
R4は、フェニル基を示し、
該フェニル基は、C1-6アルキル基、C1-6アルコキシ基、C1-6ハロアルキル基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、C1-6アルコキシC1-6アルキル基、C2-7アルコキシカルボニル基、シアノ基、及びハロゲン原子から選択される1から3個の置換基で置換されてもよく、
Yは、式CH、又は
窒素原子を示す。)で表される化合物又はその医薬上許容される塩。
【請求項2】
R2が分岐C3-6アルキル基、又はC3-6シクロアルキル基である請求項1に記載の化合物又はその医薬上許容される塩。
【請求項3】
Yが式CHである請求項1又は2に記載の化合物又はその医薬上許容される塩。
【請求項4】
R3がハロゲン原子である請求項1〜3のいずれか1項に記載の化合物又はその医薬上許容される塩。
【請求項5】
R3がフッ素原子である請求項1〜3のいずれか1項に記載の化合物又はその医薬上許容される塩。
【請求項6】
R4が、フェニル基、又はC1-6アルコキシ基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、及びハロゲン原子から選択される1〜3個の置換基で置換されたフェニル基である請求項1〜5のいずれか1項に記載の化合物又はその医薬上許容される塩。
【請求項7】
式[I]の化合物が下記式
【化2】

(式中、
R1は、メチル基、又はエチル基を示し、
R4は、フェニル基、又は
C1-6アルコキシ基、C1-6ハロアルコキシ基、C1-6ヒドロキシアルキル基、及びハロゲン原子から選択される1から3個の置換基で置換されたフェニル基を示す)で表される請求項1に記載の化合物又はその医薬上許容される塩。
【請求項8】
化合物が、
N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[6-フルオロ-3'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-[(4',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(3',6-ジフルオロ-4'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(3',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロ-3'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(6-フルオロ-4'-メトキシビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-[(4'-クロロ-6-フルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',5',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-{[3'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[4'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',5',6-テトラフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、又は
1-エチル-N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド
である請求項1に記載の化合物又はその医薬上許容される塩。
【請求項9】
化合物が、
N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[6-フルオロ-3'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',6-トリフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、
N-[(4',6-ジフルオロビフェニル-3-イル)メチル]-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[3'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
N-{[4'-(ジフルオロメトキシ)-6-フルオロビフェニル-3-イル]メチル}-1-メチル-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド、
1-メチル-N-(プロパン-2-イル)-N-[(3',4',5',6-テトラフルオロビフェニル-3-イル)メチル]-1H-イミダゾール-4-カルボキサミド、又は
1-エチル-N-{[6-フルオロ-4'-(トリフルオロメトキシ)ビフェニル-3-イル]メチル}-N-(プロパン-2-イル)-1H-イミダゾール-4-カルボキサミド
である請求項1に記載の化合物又はその医薬上許容される塩。
【請求項10】
請求項1〜9のいずれか1項に記載の化合物又はその医薬上許容される塩を有効成分として含む医薬。
【請求項11】
請求項1〜9のいずれか1項に記載の化合物又はその医薬上許容される塩を有効成分として含む、統合失調症、アルツハイマー病、認知機能障害、認知症、不安障害、うつ病、薬物依存、痙攣、振戦、又は睡眠障害の疾患の予防剤又は治療剤。
【公表番号】特表2012−533518(P2012−533518A)
【公表日】平成24年12月27日(2012.12.27)
【国際特許分類】
【出願番号】特願2012−502348(P2012−502348)
【出願日】平成22年7月15日(2010.7.15)
【国際出願番号】PCT/JP2010/062394
【国際公開番号】WO2011/007899
【国際公開日】平成23年1月20日(2011.1.20)
【出願人】(000002819)大正製薬株式会社 (437)
【Fターム(参考)】
【公表日】平成24年12月27日(2012.12.27)
【国際特許分類】
【出願日】平成22年7月15日(2010.7.15)
【国際出願番号】PCT/JP2010/062394
【国際公開番号】WO2011/007899
【国際公開日】平成23年1月20日(2011.1.20)
【出願人】(000002819)大正製薬株式会社 (437)
【Fターム(参考)】
[ Back to top ]

