分子性クラスターイオン系正極材料
【課題】低コストで、高エネルギー密度、さらには優れたサイクル特性を有するリチウムイオン二次電池等の二次電池用正極材を提供する。
【解決手段】化学式がA3(XMO24H6)(A:周期律表第1族の第2〜4周期の元素、X:周期律表第13族第2〜5周期の元素、M:周期律表第5〜6族の第4〜6周期の元素、)からなるポリオキソメタレートを含む正極材。
【解決手段】化学式がA3(XMO24H6)(A:周期律表第1族の第2〜4周期の元素、X:周期律表第13族第2〜5周期の元素、M:周期律表第5〜6族の第4〜6周期の元素、)からなるポリオキソメタレートを含む正極材。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、リチウムイオン二次電池等に利用され得る正極材料に関する。
【背景技術】
【0002】
近年、携帯電話、ノートパソコン、デジタルカメラ等のポータブル機器用電源として二次電池が広く使用されている。なかでも、コバルト酸リチウム、ニッケル酸リチウム、あるいはマンガン酸リチウム等のリチウム遷移金属酸化物を正極材、黒鉛等の炭素材料を負極材、そしてリチウム化合物を液体有機化合物に溶解した電解質を用いたリチウム二次電池が急速に普及している。
【0003】
前記リチウムイオン二次電池は、充電時には正極活物質であるリチウム遷移金属酸化物中のリチウムがリチウムイオンとなり負極の炭素層間に入り込み、放電時にはリチウムイオンが炭素層間から離脱して正極に移動して元のリチウム遷移金属酸化物になることにより充放電反応が進行する。このリチウムイオン二次電池は高出力電圧、高エネルギー密度、さらにはメモリー効果がない等、従来のニッケルカドミウム等の二次電池にはない優れた特徴を有している。
【0004】
しかし、リチウムイオン二次電池は、充放電を繰り返すことが可能な回数、すなわち、サイクル寿命については十分なものではなかった。特にエネルギー貯蔵用や電気自動車用の電源としてはサイクル寿命をさらに長くすることが必要であり、高温特性の改善、低コスト化も望まれていた。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2006−172753号公報
【特許文献2】特開2007−335331号公報
【特許文献3】特開2011−028999号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明の課題は、低コストで、高エネルギー密度、さらには優れたサイクル特性を有するリチウムイオン二次電池等の二次電池用正極材を提供することである。
【課題を解決するための手段】
【0007】
本発明者らは鋭意検討を重ねた結果、上記課題を解決する、分子性クラスタ−イオンを有する正極材を見出した。すなわち、本発明によれば以下の正極材が提供される。
【0008】
[1]二次電池用正極材であって、化学式がA3(XMO24H6)(A:周期律表第1族の第2〜4周期の元素、X:周期律表第13族第2〜5周期の元素、M:周期律表第5〜6族の第4〜6周期の元素)からなるポリオキソメタレートを含む正極材。
【0009】
[2]前記化学式において、AがLi、Na、Kのいずれか一であり、XがAlあるいはGaであり、MがV、Mo,Nbのいずれか一である、請求項1に記載の正極材。
【0010】
[3]前記二次電池がLiイオン二次電池である請求項1または2に記載の正極材。
【図面の簡単な説明】
【0011】
【図1】本発明のポリオキソメタレートのクラスタ−イオン構造を模式的に示す図である。
【図2】本発明の一実施例であるNa3AlMo6O24H6のリートベルト解析結果である。
【図3】本発明の一実施例である、正極にNa3AlMo6O24H6を用いた電池の充放電曲線を示す。
【図4】本発明の一実施例である、正極にNa3GaMo6O24H6を用いた電池の充放電曲線を示す。
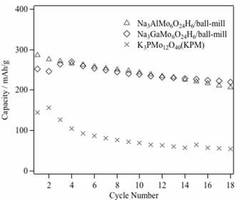
【図5】本発明の、正極にNa3AlMo6O24H6あるいはNa3GaMo6O24H6を用いた電池の充放電サイクル特性を示す。
【発明を実施するための形態】
【0012】
以下、図面を参照しつつ本発明の実施の形態について説明する。本発明は、以下の実施形態に限定されるものではなく、発明の範囲を逸脱しない限りにおいて、変更、修正、改良を加え得るものである。
【0013】
本発明のポリオキソメタレート(POM)は周期律表第5族あるいは第6族の遷移金属M(M=V、Mo、Nb等)が形成する分子性クラスターイオンである。ポリオキソメタレートは、第5族あるいは第6族の遷移金属の酸化力を利用した酸化触媒として従来から知られているが、一方では、溶液中で分子単体として安定に存在するため、分子単位でリチウムが脱挿入する機能を有すると考えられ、リチウムイオン二次電池電極材料として期待される。
【0014】
代表的なポリオキソメタレートとしては、Keggin型ポリオキソメタレートが知られているが、クラスタ−イオンユニットの構造安定性が低く、例えばKeggin型ポリオキソモリブデイトであるK3PMo12O40を正極材とするリチウム二次電池正極特性では急速に容量劣化を生じる。
【0015】
本発明では、クラスタ−イオンユニットが密な構造を有し、共有結合性が高く、分子ユニット中の非反応元素割合が高いAnderson型ポリオキソメタレートが好ましい。ポリオキソメタレートの化学式は、[XM6O24]y−(Xは周期律第15族〜第16族の第4〜第6周期の元素であり、より具体的には、Te5+、Sb5+等である)あるいは[X’M6O24H6]Z−(X’は周期律表第13族第2〜5周期の元素であり、より具体的にはAl、Gaである)。より好ましくは、[X’M6O24H6]Z−(X’は周期律表第13族第2〜5周期の元素であり、より具体的にはAl、Gaである)。なお、Mは周期律表第5〜6族の第4〜6周期の元素、より具体的にはV、Mo,Nbである。
【実施例】
【0016】
<粉末合成>
Anderson型ポリオキソメタレートの粉末合成、および比較としてKeggin型ポリオキソメタレートの粉末合成は以下の様に行った。
(実施例1:Na3[AlMo6O24H6]・7H2Oの合成)
モリブデン酸ナトリウム3.5 gと塩化アルミニウム0.8290 gを25 mlの水に溶解させ、pH=1.8になるまでHClを加えた。その後、しばらく加熱撹拌を行い、脱水させることで結晶を得た。その結晶をろ過、洗浄し、80℃で乾燥させた。
(実施例2:Li3[AlMo6O24H6]・7H2Oの合成)
モリブデン酸リチウム5 gと塩化アルミニウム0.4592 gを30 mlの水に溶解させ、pH=3.5になるまでHClを滴下した。しばらく加熱撹拌を行い、水を蒸発させることで結晶を得た。
(比較例:K3PMo12O40の合成)
ケギン型ポリオキソメタレートK3PMo12O40の合成には、市販のH3PMo12O40を蒸留水に溶解させ、塩化カリウムを過剰に加え、析出した沈殿をろ過した。得られた沈殿は、未反応の塩化カリウムを除去するために蒸留水で洗浄し、その後120℃で乾燥させた。
【0017】
これら実施例1、実施例2、および比較例の粉末結晶の同定は、X線回折(XRD)、フーリエ変換赤外線分光硬度計(FT−IR)、およびRaman分光法により行った。
【0018】
<電池作成・評価>
次にポリオキソメタレートの粉末試料を導電材であるアセチレングラックと重量比1:2の割合で混合して外径10 mm、厚み1 mmの正極合材を用い、負極に外径8 mm、厚み0.5 mmの金属リチウムから成る負極材、電解液として1M LiPF6を含むエチレンカーボネート(EC)とジエチルカーボネート(DEC)との混合溶媒(EC:DEC=3:7体積比)を用いてコイン型電池を作成し、電気化学測定を行った。50μAの定電流にて充電あるいは放電した場合の、正極試料の単位重量あたりの電気容量と電池電圧を測定した。
【0019】
(実施例1)
Anderson型ポリオキソメタレートとしてNa3AlMo6O24H6粉末を用い、アセチレンブラックとの混合を500rpmで1時間、外径55mmのボールミルで直径10mmと5mmの2種類のボールを使った混合と、比較として手混ぜ混合を行った。充放電結果を図3に示す。この結果から手混ぜ混合の場合はボールミル混合に比して、充電容量が小さく、また放電時の電圧降下が早いことがわかる。ボールミル混合では充電容量は280mAh/g以上の大きな値を示した。
【0020】
(実施例2)
Anderson型ポリオキソメタレートとしてNa3GaMo6O24H6粉末を用い、アセチレンブラックとの混合を500rpmで1時間、外径55mmのボールミルで直径10mmと5mmの2種類のボールを使った混合と、比較として手混ぜ混合を行った。充放電結果を図4に示す。実施例2は実施例1とほぼ同様の結果となった。
【0021】
次に、上記実施例1と2について、18回の充放電サイクルを行い、容量低下を調べた。比較のため、Keggin型ポリオキソメタレートであるK3PMo12O40を正極材に用いた電池も評価した。K3PMo12O40を正極材に用いると、数サイクルで30%という大きな容量低下が見られたが、実施例1および実施例2のAnderson型ポリオキソメタレートを正極に用いた電池では大きな容量低下は見られなかった。
【産業上の利用可能性】
【0022】
本発明のAnderson型ポリオキソメタレートは二次電池正極材に利用することができる。
【技術分野】
【0001】
本発明は、リチウムイオン二次電池等に利用され得る正極材料に関する。
【背景技術】
【0002】
近年、携帯電話、ノートパソコン、デジタルカメラ等のポータブル機器用電源として二次電池が広く使用されている。なかでも、コバルト酸リチウム、ニッケル酸リチウム、あるいはマンガン酸リチウム等のリチウム遷移金属酸化物を正極材、黒鉛等の炭素材料を負極材、そしてリチウム化合物を液体有機化合物に溶解した電解質を用いたリチウム二次電池が急速に普及している。
【0003】
前記リチウムイオン二次電池は、充電時には正極活物質であるリチウム遷移金属酸化物中のリチウムがリチウムイオンとなり負極の炭素層間に入り込み、放電時にはリチウムイオンが炭素層間から離脱して正極に移動して元のリチウム遷移金属酸化物になることにより充放電反応が進行する。このリチウムイオン二次電池は高出力電圧、高エネルギー密度、さらにはメモリー効果がない等、従来のニッケルカドミウム等の二次電池にはない優れた特徴を有している。
【0004】
しかし、リチウムイオン二次電池は、充放電を繰り返すことが可能な回数、すなわち、サイクル寿命については十分なものではなかった。特にエネルギー貯蔵用や電気自動車用の電源としてはサイクル寿命をさらに長くすることが必要であり、高温特性の改善、低コスト化も望まれていた。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2006−172753号公報
【特許文献2】特開2007−335331号公報
【特許文献3】特開2011−028999号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明の課題は、低コストで、高エネルギー密度、さらには優れたサイクル特性を有するリチウムイオン二次電池等の二次電池用正極材を提供することである。
【課題を解決するための手段】
【0007】
本発明者らは鋭意検討を重ねた結果、上記課題を解決する、分子性クラスタ−イオンを有する正極材を見出した。すなわち、本発明によれば以下の正極材が提供される。
【0008】
[1]二次電池用正極材であって、化学式がA3(XMO24H6)(A:周期律表第1族の第2〜4周期の元素、X:周期律表第13族第2〜5周期の元素、M:周期律表第5〜6族の第4〜6周期の元素)からなるポリオキソメタレートを含む正極材。
【0009】
[2]前記化学式において、AがLi、Na、Kのいずれか一であり、XがAlあるいはGaであり、MがV、Mo,Nbのいずれか一である、請求項1に記載の正極材。
【0010】
[3]前記二次電池がLiイオン二次電池である請求項1または2に記載の正極材。
【図面の簡単な説明】
【0011】
【図1】本発明のポリオキソメタレートのクラスタ−イオン構造を模式的に示す図である。
【図2】本発明の一実施例であるNa3AlMo6O24H6のリートベルト解析結果である。
【図3】本発明の一実施例である、正極にNa3AlMo6O24H6を用いた電池の充放電曲線を示す。
【図4】本発明の一実施例である、正極にNa3GaMo6O24H6を用いた電池の充放電曲線を示す。
【図5】本発明の、正極にNa3AlMo6O24H6あるいはNa3GaMo6O24H6を用いた電池の充放電サイクル特性を示す。
【発明を実施するための形態】
【0012】
以下、図面を参照しつつ本発明の実施の形態について説明する。本発明は、以下の実施形態に限定されるものではなく、発明の範囲を逸脱しない限りにおいて、変更、修正、改良を加え得るものである。
【0013】
本発明のポリオキソメタレート(POM)は周期律表第5族あるいは第6族の遷移金属M(M=V、Mo、Nb等)が形成する分子性クラスターイオンである。ポリオキソメタレートは、第5族あるいは第6族の遷移金属の酸化力を利用した酸化触媒として従来から知られているが、一方では、溶液中で分子単体として安定に存在するため、分子単位でリチウムが脱挿入する機能を有すると考えられ、リチウムイオン二次電池電極材料として期待される。
【0014】
代表的なポリオキソメタレートとしては、Keggin型ポリオキソメタレートが知られているが、クラスタ−イオンユニットの構造安定性が低く、例えばKeggin型ポリオキソモリブデイトであるK3PMo12O40を正極材とするリチウム二次電池正極特性では急速に容量劣化を生じる。
【0015】
本発明では、クラスタ−イオンユニットが密な構造を有し、共有結合性が高く、分子ユニット中の非反応元素割合が高いAnderson型ポリオキソメタレートが好ましい。ポリオキソメタレートの化学式は、[XM6O24]y−(Xは周期律第15族〜第16族の第4〜第6周期の元素であり、より具体的には、Te5+、Sb5+等である)あるいは[X’M6O24H6]Z−(X’は周期律表第13族第2〜5周期の元素であり、より具体的にはAl、Gaである)。より好ましくは、[X’M6O24H6]Z−(X’は周期律表第13族第2〜5周期の元素であり、より具体的にはAl、Gaである)。なお、Mは周期律表第5〜6族の第4〜6周期の元素、より具体的にはV、Mo,Nbである。
【実施例】
【0016】
<粉末合成>
Anderson型ポリオキソメタレートの粉末合成、および比較としてKeggin型ポリオキソメタレートの粉末合成は以下の様に行った。
(実施例1:Na3[AlMo6O24H6]・7H2Oの合成)
モリブデン酸ナトリウム3.5 gと塩化アルミニウム0.8290 gを25 mlの水に溶解させ、pH=1.8になるまでHClを加えた。その後、しばらく加熱撹拌を行い、脱水させることで結晶を得た。その結晶をろ過、洗浄し、80℃で乾燥させた。
(実施例2:Li3[AlMo6O24H6]・7H2Oの合成)
モリブデン酸リチウム5 gと塩化アルミニウム0.4592 gを30 mlの水に溶解させ、pH=3.5になるまでHClを滴下した。しばらく加熱撹拌を行い、水を蒸発させることで結晶を得た。
(比較例:K3PMo12O40の合成)
ケギン型ポリオキソメタレートK3PMo12O40の合成には、市販のH3PMo12O40を蒸留水に溶解させ、塩化カリウムを過剰に加え、析出した沈殿をろ過した。得られた沈殿は、未反応の塩化カリウムを除去するために蒸留水で洗浄し、その後120℃で乾燥させた。
【0017】
これら実施例1、実施例2、および比較例の粉末結晶の同定は、X線回折(XRD)、フーリエ変換赤外線分光硬度計(FT−IR)、およびRaman分光法により行った。
【0018】
<電池作成・評価>
次にポリオキソメタレートの粉末試料を導電材であるアセチレングラックと重量比1:2の割合で混合して外径10 mm、厚み1 mmの正極合材を用い、負極に外径8 mm、厚み0.5 mmの金属リチウムから成る負極材、電解液として1M LiPF6を含むエチレンカーボネート(EC)とジエチルカーボネート(DEC)との混合溶媒(EC:DEC=3:7体積比)を用いてコイン型電池を作成し、電気化学測定を行った。50μAの定電流にて充電あるいは放電した場合の、正極試料の単位重量あたりの電気容量と電池電圧を測定した。
【0019】
(実施例1)
Anderson型ポリオキソメタレートとしてNa3AlMo6O24H6粉末を用い、アセチレンブラックとの混合を500rpmで1時間、外径55mmのボールミルで直径10mmと5mmの2種類のボールを使った混合と、比較として手混ぜ混合を行った。充放電結果を図3に示す。この結果から手混ぜ混合の場合はボールミル混合に比して、充電容量が小さく、また放電時の電圧降下が早いことがわかる。ボールミル混合では充電容量は280mAh/g以上の大きな値を示した。
【0020】
(実施例2)
Anderson型ポリオキソメタレートとしてNa3GaMo6O24H6粉末を用い、アセチレンブラックとの混合を500rpmで1時間、外径55mmのボールミルで直径10mmと5mmの2種類のボールを使った混合と、比較として手混ぜ混合を行った。充放電結果を図4に示す。実施例2は実施例1とほぼ同様の結果となった。
【0021】
次に、上記実施例1と2について、18回の充放電サイクルを行い、容量低下を調べた。比較のため、Keggin型ポリオキソメタレートであるK3PMo12O40を正極材に用いた電池も評価した。K3PMo12O40を正極材に用いると、数サイクルで30%という大きな容量低下が見られたが、実施例1および実施例2のAnderson型ポリオキソメタレートを正極に用いた電池では大きな容量低下は見られなかった。
【産業上の利用可能性】
【0022】
本発明のAnderson型ポリオキソメタレートは二次電池正極材に利用することができる。
【特許請求の範囲】
【請求項1】
二次電池用正極材であって、化学式がA3(XMO24H6)(A:周期律表第1族の第2〜4周期の元素、X:周期律表第13族第2〜5周期の元素、M:周期律表第5〜6族の第4〜6周期の元素、)からなるポリオキソメタレートを含む正極材。
【請求項2】
前記化学式において、AがLi,Na、Kのいずれか一であり、XがAlあるいはGaであり、MがV、Mo,Nbのいずれか一である、請求項1に記載の正極材。
【請求項3】
前記二次電池がLiイオン二次電池である請求項1または2に記載の正極材。
【請求項1】
二次電池用正極材であって、化学式がA3(XMO24H6)(A:周期律表第1族の第2〜4周期の元素、X:周期律表第13族第2〜5周期の元素、M:周期律表第5〜6族の第4〜6周期の元素、)からなるポリオキソメタレートを含む正極材。
【請求項2】
前記化学式において、AがLi,Na、Kのいずれか一であり、XがAlあるいはGaであり、MがV、Mo,Nbのいずれか一である、請求項1に記載の正極材。
【請求項3】
前記二次電池がLiイオン二次電池である請求項1または2に記載の正極材。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2013−115028(P2013−115028A)
【公開日】平成25年6月10日(2013.6.10)
【国際特許分類】
【出願番号】特願2011−263333(P2011−263333)
【出願日】平成23年12月1日(2011.12.1)
【出願人】(304021277)国立大学法人 名古屋工業大学 (784)
【Fターム(参考)】
【公開日】平成25年6月10日(2013.6.10)
【国際特許分類】
【出願日】平成23年12月1日(2011.12.1)
【出願人】(304021277)国立大学法人 名古屋工業大学 (784)
【Fターム(参考)】
[ Back to top ]

