分析装置、分析方法、および分析用マイクロチップ
【課題】分析対象となる物質が他の物質との間で行う反応を適確かつ高精度に制御可能であるとともに、簡易で経済的な分析装置、分析方法、および分析用マイクロチップを提供する。
【解決手段】分析対象となる物質を含む検体およびこの検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、この複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップと、このマイクロチップ内の微粒子を所定のレーザ光によって光学的に捕捉する捕捉手段と、この捕捉手段で捕捉した微粒子を連結路を介して複数の溝部間を順次移送する移送手段と、特定物質と反応試薬との反応によって生成された物質を光学的に検出する検出手段とを備える。
【解決手段】分析対象となる物質を含む検体およびこの検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、この複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップと、このマイクロチップ内の微粒子を所定のレーザ光によって光学的に捕捉する捕捉手段と、この捕捉手段で捕捉した微粒子を連結路を介して複数の溝部間を順次移送する移送手段と、特定物質と反応試薬との反応によって生成された物質を光学的に検出する検出手段とを備える。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、検体に含まれる免疫等の成分を分析する分析装置、分析方法、および分析用マイクロチップに関するものである。
【背景技術】
【0002】
従来、血液や体液等の検体に含まれる免疫成分などを自動的に分析する技術として自動分析装置が知られている(例えば、特許文献1を参照)。この自動分析装置は、試薬が入った反応容器に検体を加え、反応容器内の試薬との間で生じた反応を光学的に検出するものである。この自動分析装置による検体の分析に必要な試薬量は、一つの検体に対して数ml(ミリリットル)〜数十ml程度と少量で済むが、コスト的な観点から見て、分析に用いる試薬量をさらに低減することのできる技術が待望されていた。また、従来の自動分析装置は、検体や試薬を分注する分注ノズルの洗浄に用いる洗浄水の廃液量も多く、この点においてもコスト面で改善の余地があった。
【0003】
このような状況を解決しうる技術として、検体の分析に必要な要素を微小なチップ上に集積化することによって分析を行うマイクロ分析システムがある(例えば、特許文献2を参照)。このマイクロ分析システムに関しては、システム外部から所定の磁場を印加することによって微細な流路内に存在する微粒子を操作し、この微粒子を表面修飾する物質と分析対象の物質との反応に基づいて分析を行う技術も開示されている(例えば、特許文献3を参照)。
【0004】
【特許文献1】特開平6−88828号公報
【特許文献2】特開2003−279471号公報
【特許文献3】特表2002−507750号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかしながら、上述した従来のマイクロ分析システムにおいて、免疫の分析に必要な抗原抗体反応等の反応を発生させるためには、システムの構造、特にチップの構造をある程度複雑化せざるを得ず、コストを十分に削減できるわけではなかった。
【0006】
また、システム外部から磁場を印加して微粒子を操作するマイクロ分析システムの場合、その微粒子の操作は2次元的な方向に限定されるので、チップ上の微細な3次元構造内において測定対象となる微粒子の位置やその移動速度の制御を適確かつ高精度に行うことは困難であり、免疫分析のように反応時間の制御が重要な測定系に適したものではなかった。
【0007】
本発明は、上記に鑑みてなされたものであって、分析対象となる物質が他の物質との間で行う反応を適確かつ高精度に制御可能であるとともに、簡易で経済的な分析装置、分析方法、および分析用マイクロチップを提供することを目的とする。
【課題を解決するための手段】
【0008】
上述した課題を解決し、目的を達成するために、請求項1記載の発明は、検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する分析装置であって、前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップと、前記マイクロチップが有する複数の溝部のいずれかに充填される液体に混合され、前記特定物質と特異的に反応する物質を表面修飾した微粒子に対して所定のレーザ光を照射することにより、前記微粒子を光学的に捕捉する捕捉手段と、前記捕捉手段で光学的に捕捉した微粒子を、前記複数の連結路を順次通過させることによって前記複数の溝部間で移送する移送手段と、前記移送手段が前記微粒子を移送した結果、前記特定物質と前記反応試薬との反応によって生成された物質を光学的に検出する検出手段と、を備えたことを特徴とする。
【0009】
請求項2記載の発明は、請求項1記載の発明において、前記検体の成分を分析するために必要な複数種類の液体は、所定の緩衝液に前記微粒子が混合されて成る微粒子混合液と、前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、を含むことを特徴とする。
【0010】
請求項3記載の発明は、検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する分析方法であって、前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップ内の前記複数の溝部のいずれかに充填される液体に混合され、前記特定物質と特異的に反応する物質を表面修飾した微粒子に対して所定のレーザ光を照射することにより、前記微粒子を光学的に捕捉する捕捉ステップと、前記捕捉ステップで光学的に捕捉した微粒子を、前記複数の連結路を順次通過させることによって前記複数の溝部間で移送する移送ステップと、前記移送ステップで前記微粒子を移送した結果、前記特定物質と前記反応試薬との反応によって生成された物質を光学的に検出する検出ステップと、を有することを特徴とする。
【0011】
請求項4記載の発明は、請求項3記載の発明において、前記移送ステップでは、前記微粒子を順次移送する各溝部において、各溝部に充填される物質に応じて溝部ごとに定められる時間だけ前記微粒子を保持することを特徴とする。
【0012】
請求項5記載の発明は、請求項3または4記載の発明において、前記検体の成分を分析するために必要な複数種類の液体は、所定の緩衝液に前記微粒子が混合されて成る微粒子混合液と、前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、を含むことを特徴とする。
【0013】
請求項6記載の発明は、検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する際に適用する分析用マイクロチップであって、前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部と、前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路と、を備えたことを特徴とする。
【0014】
請求項7記載の発明は、請求項6記載の発明において、前記検体の成分を分析するために必要な複数種類の液体は、前記特定物質と特異的に反応する物質を表面修飾し、前記複数の連結路を通過可能な微粒子が、所定の緩衝液に混合されて成る微粒子混合液と、前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、を含むことを特徴とする。
【発明の効果】
【0015】
本発明によれば、分析対象となる物質を含む検体およびこの検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、この複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップと、このマイクロチップ内の微粒子を所定のレーザ光によって光学的に捕捉する捕捉手段と、この捕捉手段で捕捉した微粒子を連結路を介して複数の溝部間を順次移送する移送手段と、特定物質と反応試薬との反応によって生成された物質を光学的に検出する検出手段とを備えることにより、分析対象となる物質が他の物質との間で行う反応を適確かつ高精度に制御可能であり、簡易で経済的な分析装置、分析方法、および分析用マイクロチップを提供することができる。
【発明を実施するための最良の形態】
【0016】
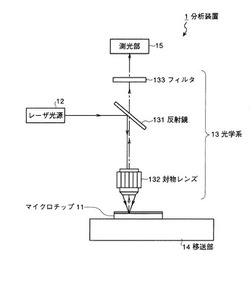
以下、添付図面を参照して本発明の実施の形態を説明する。図1は、本発明の一実施の形態に係る分析装置要部の構成を模式的に示す説明図である。同図に示す分析装置1は、複数の溝部および隣接する溝部間同士を連結する複数の連結路を有し、検体や分析に必要な液体等を充填するマイクロチップ11、所定のレーザ光を発生するレーザ光源12、レーザ光源12から発生するレーザ光を集光し、少なくともこの集光したレーザ光を所望の位置に照射する光学系13、マイクロチップ11の表面に平行な2次元方向にマイクロチップ11を移送する移送部14、マイクロチップ11内で生じる反応によって発生する光を測光する測光部15、ならびにレーザ光源12、光学系13、移送部14、および測光部15の動作制御を行う制御部16(図示せず)を備える。
【0017】
この実施の形態においては、マイクロチップ11内に存在する微粒子を光学系13から照射するレーザ光によって光学的に捕捉する「光ピンセット」と呼ばれる技術を適用する。この光ピンセットについて具体的に説明する。照射するレーザ光のビームを集光して絞り込むと、その照射レーザ光は集光レンズの焦点位置付近に存在する微粒子を通過するときに屈折する。この屈折による自身の運動量変化により、レーザ光は通過する微粒子を集光レンズ方向へ引き戻す力を及ぼす。その結果、微粒子はレーザ光によって光学的に捕捉される。この実施の形態に係る分析方法では、光ピンセットによって微粒子を光学的に捕捉した状態を保持しながら、検体の分析を行う。
【0018】
図2−1は、この実施の形態に係る分析用マイクロチップとして分析装置1に適用されるマイクロチップ11の詳細な構成を示す表面図である。また、図2−2は、図2−1に示すマイクロチップ11のX−X断面図(縦断面図)である。これらの図に示すマイクロチップ11は、正方形をなす表面がその表面の法線方向に微小な厚さを有する直方体形状をなしており、本体部111と、この本体部111の一方の表面に装着されるカバー部112とから成る。
【0019】
本体部111は、4つの溝部t1、t2、t3、およびt4を有するとともに、隣接する溝部同士を連結する3つの連結路c1、c2、およびc3を有する。溝部同士および連結路同士はそれぞれ同形状をなすとともに、それぞれ長手方向の中心軸が互いに平行である。カバー部112は、4つの溝部t1〜t4が設けられる側の表面に装着される。これらの本体部111およびカバー部112はガラスによって実現され、それらの表面をなす正方形の一辺の長さは、数cm程度である。また、本体部111の厚みは数mm程度であり、溝部t1〜t4の深さHは数百μm程度である。他方、カバー部112の厚みは数十μm程度である。
【0020】
本体部111に設けられる4つの溝部t1〜t4には、それぞれ異なる物質が充填される。より具体的には、一方の端部に位置する溝部t1には、生理食塩水等から成る所定の緩衝液に、検体に含まれる特定物質と特異的に結合する物質を表面修飾した微粒子Bを混合した微粒子混合液101が充填される。この溝部t1に隣接する溝部t2には、検体102が充填される。この溝部t2の溝部t1と反対側で隣接する溝部t3には、溝部t2を通過してきた後の微粒子Bを洗浄するための緩衝液103が充填される。この緩衝液103は、前述した微粒子混合液101で用いる緩衝液と同じものである。溝部t3と隣接し、この溝部t3に対して溝部t2と反対側に設けられる溝部t4には、検体に含まれる特定物質と反応して光学的に検出可能な物質を生成する一方、微粒子Bを表面実装する物質と特定物質との結合は阻害しない反応試薬を含む試薬溶液104が充填される。
【0021】
ここで、溝部t2に充填される検体102が血液の場合には、分析対象となる特定物質として、例えば血清中のγグロブリンなどの抗体を挙げることができる。この場合、微粒子Bを表面修飾して特定物質である抗体と特異的に結合する物質は抗原である。したがって、特定物質と微粒子Bを表面修飾する物質との特異的な反応とは、抗原抗体反応に他ならない。
【0022】
3つの連結路、すなわち、溝部t1と溝部t2を連絡する連結路c1、溝部t2と溝部t3を連結する連結路c2、および溝部t3と溝部t4を連結する連結路c3は、レーザ光を用いて捕捉した微粒子Bを溝部t1から溝部t2、t3、およびt4へと順次移送するために設けられる。このため、各連結路の深さhは微粒子Bの径よりも大きくなければならない。この実施の形態では、微粒子Bとして、その径が数μm〜数十μm程度のプラスチック製の球状粒子を用いるので、連結路の深さhは数十μm程度よりも大きい。この深さhの値は、一方で、隣接する溝部にそれぞれ充填される液体の混合がほとんど無視できる程度に小さくなければならない。換言すれば、連結路の深さhのとり得る値の上限は、隣接する溝部間の液体の混合が無視できる程度の値でなければならない。
【0023】
この実施の形態において、連結路c1〜c3は、本体部111の表面に平行な断面(横断面)が長方形状をなしている(図2−1および図2−2を参照)。それらの長方形は、長手方向に対して互いに平行であるが同一直線上は通過していない。これは、微粒子Bがある連結路を介して隣接する溝部に到達したとき、この到達した溝部に充填されている液体の一部がさらに隣接する溝部に流出したりするのを防止するためである。
【0024】
なお、図2−2に示す溝部t1〜t4の一つの縦断面の形状、および連結路c1〜c3のX−X線とは垂直な方向の縦断面の形状は、底辺の方が短い等脚台形をなしていれば、光ピンセットで捕捉した微粒子Bを移送する上で好ましいが、必ずしもこの形状に限定されるわけではない。また、溝部t1〜t4の本体部111に平行な方向の横断面は長方形状でなくてもよく、例えば円形や多角形などであっても構わない。
【0025】
マイクロチップ11のカバー部112は、溝部t1〜t4に充填される物質の蒸発を防止するために本体部111に装着される。このカバー部112には、溝部ごとに物質を充填するために、開閉自在な二つの孔部(入口と出口に相当)を設けてもよい。そして、ある溝部に物質を充填する際には、その溝部に対応する二つの孔部を開放する以外は、全ての孔部を閉鎖する。
【0026】
次に、光学系13について説明する。この実施の形態では、蛍光顕微鏡を用いて微粒子Bを表面実装する物質(抗原とする)と検体102に含まれる物質(抗体とする)との間で生じる抗原抗体反応を分析する。この場合、光学系13は、レーザ光源12から発生するレーザ光を反射する反射鏡131と、この反射鏡131で反射されたレーザ光を集光してマイクロチップ11内の微粒子Bを照射する対物レンズ132とを有する。反射鏡131は、入射光および励起光としてのレーザ光を反射する一方、抗体と蛍光性物質を含む反応試薬との反応によって生成される放射光は透過するダイクロックミラーである。光学系13は、この反射鏡131を透過した放射光から所望の周波数帯域の光を採光するフィルタ133をさらに有する。なお、反射鏡131は所定の回転軸に対して回動自在であり、制御部16の制御に基づいて、レーザ光の集光位置を調整する。また、対物レンズ132は光軸方向に移動自在であり、制御部16の制御に基づいてレーザ光の照射位置を調整する。
【0027】
このような光学系13において、対物レンズ132の開口数を大きく取り、この対物レンズ132で集光するレーザ光のビームを絞り込むと、その焦点位置付近に存在する微粒子Bを光ピンセットで捕捉することができる。この意味で、レーザ光源12と光学系13は、少なくとも捕捉手段の一部をなしている。なお、微粒子Bを捕捉するためには、微粒子Bの径がレーザ光の波長よりも大きく、なおかつ微粒子Bの屈折率が微粒子混合液101、検体102、緩衝液103、および試薬溶液104の屈折率よりも大きければより好ましい。
【0028】
移送部14は、マイクロチップ11の表面を水平方向に載置する載置面を有しており、マイクロチップ11の表面に平行な2次元方向、すなわち図1で水平方向を指向し、なおかつ紙面に垂直な2次元面方向に移動自在であり、光ピンセットによって捕捉した微粒子Bを、連結路ci(i=1,2,3)を介して溝部tiから隣接する溝部ti+1へと移送する機能を有する。この移送部14を用いることにより、マイクロチップ11の位置決めを容易にかつ高精度に行うことが可能となる。
【0029】
測光部15は、特定物質である抗体と反応試薬中に含まれる蛍光性物質との反応によって生成、放射され、反射鏡131を透過してくる蛍光のうち、フィルタ133を通過した周波数帯域の蛍光成分を受光してその強度を増幅する光電子増倍管を有する。測光部15は、レーザ光源12および光学系13とともに、放射される蛍光を検出する検出手段の一部をなす。
【0030】
制御部16は、上述したレーザ光源12、光学系13(反射鏡131、対物レンズ132、フィルタ133)、移送部14、および測光部15の動作制御を行うとともに、測光部15の測定結果に基づいて検体の成分の分析を行う機能を有しており、演算および制御機能を有するCPU(Central Processing Unit)等によって実現される。
【0031】
以上の構成を有する分析装置1が行う分析方法の詳細について、図3に示すフローチャート図を用いて説明する。まず、レーザ光源12から発生するレーザ光が、溝部t1に充填される微粒子混合液101内の微粒子Bのいずれかを照射するように、移送部14を移動してマイクロチップ11の位置決めを行い、少なくとも一つの微粒子Bを光ピンセットで捕捉する(ステップS1)。以後の過程において、光学系13によって実現される光ピンセットは、このステップS1で捕捉した微粒子Bを捕捉し続ける。図4−1は、このステップS1で捕捉する微粒子Bが抗原aによって表面実装された状態を模式的に示す説明図である。
【0032】
次に移送部14は、マイクロチップ11を移動することにより、ステップS1で捕捉した微粒子Bを連結路c1まで移動し、さらにこの連結路c1を通過させることによって溝部t2に移送し、所定時間この状態を保持する(ステップS2)。この状態を保持することによって、溝部t2内の検体102に含まれる特定物質としての抗体bが、微粒子Bを表面実装する抗原aと抗原抗体反応を行う。したがって、ここでいう所定時間とは、抗原aと抗体bが抗原抗体反応を起こすのに十分な時間である。図4−2は、このステップS2における抗原抗体反応の結果、微粒子Bの表面で、抗原aと抗体bが抗原抗体反応によって特異的に結合した状態を模式的に示す説明図である。
【0033】
その後、移送部14は、マイクロチップ11を移動することにより、光ピンセットで捕捉している微粒子Bを、連結路c2を介して溝部t3に移送し、所定時間この状態を保持する(ステップS3)。この状態を保持することによって、抗原抗体反応を起こした微粒子Bに付随して溝部t3内に到達した遊離抗体を、溝部t3に充填される緩衝液103によって分離洗浄(B/F分離)することができる。したがって、ここでいう所定時間は、ステップS2における所定時間とは異なるものであり、緩衝液103を用いて不要な抗体を微粒子Bから分離するのに必要な時間である。
【0034】
続いて、移送部14は、光ピンセットで捕捉している微粒子Bを、連結路c3を通過させることによって溝部t4に移送する(ステップS4)。この溝部t4内では、充填された試薬溶液104中の反応試薬に含まれる蛍光性物質cが微粒子Bに付着した抗体bと反応(化学結合)を生じる。そしてこの反応の結果、蛍光Lが発生する。この際には、微粒子Bを照射して捕捉している入射レーザ光が、励起光としての役割を果たす。図4−3は、蛍光性物質cが抗体bと化学結合し、レーザ光によって励起された結果、蛍光Lを放射する状態を模式的に示す説明図である。
【0035】
次に測光部15が、溝部t4内での反応によってから放射され、フィルタ133でフィルタリングされた蛍光Lの強度を測定する(ステップS5)。そして、測光部15で測定した結果を制御部16が分析する(ステップS6)。なお、分析装置1にデータを出力表示する出力部と、データを記憶する記憶部とをさらに設けることにより、このステップS6における分析結果を出力部で表示したり、記憶部に記憶したりしてもよい。
【0036】
以上説明した本発明の一実施の形態によれば、検体およびこの検体の成分を分析するのに必要な物質を含む液体を別個に充填する複数の溝部と、隣接する溝部同士を連結する連結路を有するマイクロチップと、このマイクロチップ内の微粒子を所定のレーザ光を用いた光ピンセット技術によって捕捉し、移送部でマイクロチップを移動させながら捕捉した微粒子を操作して反応を調整することにより、検体に含まれる特定物質が他の物質との間で行う抗原抗体反応を適確かつ高精度に制御することができる。
【0037】
この実施の形態では、分析に用いる検体や試薬はマイクロチップの溝部に充填する量で十分なため、数百nl(ナノリットル)程度の極めて微小な量で済む上、マイクロチップ自体の洗浄も分析終了まで不要なため、洗浄水も少量で済む。したがって、この実施の形態によれば、従来の分析システムに比べ、一段とコストを低く抑えることができ、経済的である。
【0038】
また、この実施の形態によれば、従来の分析装置のように試薬を別な容器などに置換する必要がなく、マイクロチップ本体の移送のみですべてのプロセスを実行するため、マイクロチップ自体のレイアウトの自由度が高く、その構成を単純にすることができる。したがって、この意味でもコストの低減という効果が得られる。
【0039】
さらに、この実施の形態によれば、例えば検体として血液を用いる場合、必要な血液の量が少なくて済むので、血液を採取される側の検体提供者の肉体的かつ心理的な負担を軽減させることができる。
【0040】
ここまで、本発明の好ましい一実施の形態を詳述してきたが、本発明はこの実施の形態によってのみ限定されるものではない。例えば、各溝部に充填する溶液の種類や分析に必要な溝部の数は、検体の成分の分析に必要な反応等に応じて適宜変更することが可能である。この意味で、本発明に係るマイクロチップのレイアウトは、各種免疫分析のために必要な抗原抗体反応等の反応を光学的に検出可能なものであれば如何なる構成であってもよく、溝部の個数が3個または5個以上であってもよい。これらの溝部のうち、互いに隣接する溝部同士に連結路が設けられる点は、上記一実施の形態と同様である。
【0041】
また、上述した一実施の形態においては蛍光分析を用いて検体の分析を行ったが、それ以外にも、ルミナール反応等に基づく化学発光分析や、検出光を物質に照射して透過してくる透過光から物質の吸光量を測定する吸光光度分析法等のよく知られた分析手法を用いることも可能である。これらの分析手法に応じて、分析装置、特に光学系の構成が適宜変更されることは勿論である。
【0042】
さらに、本発明に係る分析装置に、複数のマイクロチップを格納、保管する機能と、検体を保管して、この検体をマイクロチップの適当な溝部に分注する機能と、検体を分注したマイクロチップを移送する機能とをさらに具備させることにより、多数の検体の成分を自動かつ連続的に分析可能な自動分析装置を構成することも可能である。この場合には、マイクロチップにおいて、検体を充填する溝部だけは空にしておき、他の溝部には抗原抗体反応を起こすのに必要な所定の液体を予め充填したものを大量に製造しておけば、後から検体充填用の溝部に検体を充填するだけで検体の分析を行うことができる。
【0043】
このように、本発明は、ここでは記載していないさまざまな実施の形態等を含みうるものであり、特許請求の範囲により特定される技術的事項を逸脱しない範囲内において種々の設計変更等を施すことが可能である。
【図面の簡単な説明】
【0044】
【図1】本発明の一実施の形態に係る分析装置要部の構成を模式的に示す説明図である。
【図2−1】本発明の一実施の形態に係る分析用マイクロチップ表面の構成を示す平面図である。
【図2−2】図2−1のX−X断面図である。
【図3】本発明の一実施の形態に係る分析方法の処理の流れを示すフローチャート図である。
【図4−1】微粒子を抗原で表面実装した状態を模式的に示す説明図である。
【図4−2】微粒子の表面で、抗原と抗体が抗原抗体反応によって特異的に結合した状態を模式的に示す説明図である。
【図4−3】蛍光性物質が抗体と化学結合し、蛍光を放射する状態を模式的に示す説明図である。
【符号の説明】
【0045】
1 分析装置
11 マイクロチップ
12 レーザ光源
13 光学系
14 移送部
15 測光部
16 制御部
101 微粒子混合液
102 検体
103 緩衝液
104 試薬溶液
111 本体部
112 カバー部
131 反射鏡
132 対物レンズ
133 フィルタ
c1、c2、c3 連結路
t1、t2、t2、t4 溝部
B 微粒子
L 蛍光
a 抗原
b 抗体
c 蛍光性物質
【技術分野】
【0001】
本発明は、検体に含まれる免疫等の成分を分析する分析装置、分析方法、および分析用マイクロチップに関するものである。
【背景技術】
【0002】
従来、血液や体液等の検体に含まれる免疫成分などを自動的に分析する技術として自動分析装置が知られている(例えば、特許文献1を参照)。この自動分析装置は、試薬が入った反応容器に検体を加え、反応容器内の試薬との間で生じた反応を光学的に検出するものである。この自動分析装置による検体の分析に必要な試薬量は、一つの検体に対して数ml(ミリリットル)〜数十ml程度と少量で済むが、コスト的な観点から見て、分析に用いる試薬量をさらに低減することのできる技術が待望されていた。また、従来の自動分析装置は、検体や試薬を分注する分注ノズルの洗浄に用いる洗浄水の廃液量も多く、この点においてもコスト面で改善の余地があった。
【0003】
このような状況を解決しうる技術として、検体の分析に必要な要素を微小なチップ上に集積化することによって分析を行うマイクロ分析システムがある(例えば、特許文献2を参照)。このマイクロ分析システムに関しては、システム外部から所定の磁場を印加することによって微細な流路内に存在する微粒子を操作し、この微粒子を表面修飾する物質と分析対象の物質との反応に基づいて分析を行う技術も開示されている(例えば、特許文献3を参照)。
【0004】
【特許文献1】特開平6−88828号公報
【特許文献2】特開2003−279471号公報
【特許文献3】特表2002−507750号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかしながら、上述した従来のマイクロ分析システムにおいて、免疫の分析に必要な抗原抗体反応等の反応を発生させるためには、システムの構造、特にチップの構造をある程度複雑化せざるを得ず、コストを十分に削減できるわけではなかった。
【0006】
また、システム外部から磁場を印加して微粒子を操作するマイクロ分析システムの場合、その微粒子の操作は2次元的な方向に限定されるので、チップ上の微細な3次元構造内において測定対象となる微粒子の位置やその移動速度の制御を適確かつ高精度に行うことは困難であり、免疫分析のように反応時間の制御が重要な測定系に適したものではなかった。
【0007】
本発明は、上記に鑑みてなされたものであって、分析対象となる物質が他の物質との間で行う反応を適確かつ高精度に制御可能であるとともに、簡易で経済的な分析装置、分析方法、および分析用マイクロチップを提供することを目的とする。
【課題を解決するための手段】
【0008】
上述した課題を解決し、目的を達成するために、請求項1記載の発明は、検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する分析装置であって、前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップと、前記マイクロチップが有する複数の溝部のいずれかに充填される液体に混合され、前記特定物質と特異的に反応する物質を表面修飾した微粒子に対して所定のレーザ光を照射することにより、前記微粒子を光学的に捕捉する捕捉手段と、前記捕捉手段で光学的に捕捉した微粒子を、前記複数の連結路を順次通過させることによって前記複数の溝部間で移送する移送手段と、前記移送手段が前記微粒子を移送した結果、前記特定物質と前記反応試薬との反応によって生成された物質を光学的に検出する検出手段と、を備えたことを特徴とする。
【0009】
請求項2記載の発明は、請求項1記載の発明において、前記検体の成分を分析するために必要な複数種類の液体は、所定の緩衝液に前記微粒子が混合されて成る微粒子混合液と、前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、を含むことを特徴とする。
【0010】
請求項3記載の発明は、検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する分析方法であって、前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップ内の前記複数の溝部のいずれかに充填される液体に混合され、前記特定物質と特異的に反応する物質を表面修飾した微粒子に対して所定のレーザ光を照射することにより、前記微粒子を光学的に捕捉する捕捉ステップと、前記捕捉ステップで光学的に捕捉した微粒子を、前記複数の連結路を順次通過させることによって前記複数の溝部間で移送する移送ステップと、前記移送ステップで前記微粒子を移送した結果、前記特定物質と前記反応試薬との反応によって生成された物質を光学的に検出する検出ステップと、を有することを特徴とする。
【0011】
請求項4記載の発明は、請求項3記載の発明において、前記移送ステップでは、前記微粒子を順次移送する各溝部において、各溝部に充填される物質に応じて溝部ごとに定められる時間だけ前記微粒子を保持することを特徴とする。
【0012】
請求項5記載の発明は、請求項3または4記載の発明において、前記検体の成分を分析するために必要な複数種類の液体は、所定の緩衝液に前記微粒子が混合されて成る微粒子混合液と、前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、を含むことを特徴とする。
【0013】
請求項6記載の発明は、検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する際に適用する分析用マイクロチップであって、前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部と、前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路と、を備えたことを特徴とする。
【0014】
請求項7記載の発明は、請求項6記載の発明において、前記検体の成分を分析するために必要な複数種類の液体は、前記特定物質と特異的に反応する物質を表面修飾し、前記複数の連結路を通過可能な微粒子が、所定の緩衝液に混合されて成る微粒子混合液と、前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、を含むことを特徴とする。
【発明の効果】
【0015】
本発明によれば、分析対象となる物質を含む検体およびこの検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、この複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップと、このマイクロチップ内の微粒子を所定のレーザ光によって光学的に捕捉する捕捉手段と、この捕捉手段で捕捉した微粒子を連結路を介して複数の溝部間を順次移送する移送手段と、特定物質と反応試薬との反応によって生成された物質を光学的に検出する検出手段とを備えることにより、分析対象となる物質が他の物質との間で行う反応を適確かつ高精度に制御可能であり、簡易で経済的な分析装置、分析方法、および分析用マイクロチップを提供することができる。
【発明を実施するための最良の形態】
【0016】
以下、添付図面を参照して本発明の実施の形態を説明する。図1は、本発明の一実施の形態に係る分析装置要部の構成を模式的に示す説明図である。同図に示す分析装置1は、複数の溝部および隣接する溝部間同士を連結する複数の連結路を有し、検体や分析に必要な液体等を充填するマイクロチップ11、所定のレーザ光を発生するレーザ光源12、レーザ光源12から発生するレーザ光を集光し、少なくともこの集光したレーザ光を所望の位置に照射する光学系13、マイクロチップ11の表面に平行な2次元方向にマイクロチップ11を移送する移送部14、マイクロチップ11内で生じる反応によって発生する光を測光する測光部15、ならびにレーザ光源12、光学系13、移送部14、および測光部15の動作制御を行う制御部16(図示せず)を備える。
【0017】
この実施の形態においては、マイクロチップ11内に存在する微粒子を光学系13から照射するレーザ光によって光学的に捕捉する「光ピンセット」と呼ばれる技術を適用する。この光ピンセットについて具体的に説明する。照射するレーザ光のビームを集光して絞り込むと、その照射レーザ光は集光レンズの焦点位置付近に存在する微粒子を通過するときに屈折する。この屈折による自身の運動量変化により、レーザ光は通過する微粒子を集光レンズ方向へ引き戻す力を及ぼす。その結果、微粒子はレーザ光によって光学的に捕捉される。この実施の形態に係る分析方法では、光ピンセットによって微粒子を光学的に捕捉した状態を保持しながら、検体の分析を行う。
【0018】
図2−1は、この実施の形態に係る分析用マイクロチップとして分析装置1に適用されるマイクロチップ11の詳細な構成を示す表面図である。また、図2−2は、図2−1に示すマイクロチップ11のX−X断面図(縦断面図)である。これらの図に示すマイクロチップ11は、正方形をなす表面がその表面の法線方向に微小な厚さを有する直方体形状をなしており、本体部111と、この本体部111の一方の表面に装着されるカバー部112とから成る。
【0019】
本体部111は、4つの溝部t1、t2、t3、およびt4を有するとともに、隣接する溝部同士を連結する3つの連結路c1、c2、およびc3を有する。溝部同士および連結路同士はそれぞれ同形状をなすとともに、それぞれ長手方向の中心軸が互いに平行である。カバー部112は、4つの溝部t1〜t4が設けられる側の表面に装着される。これらの本体部111およびカバー部112はガラスによって実現され、それらの表面をなす正方形の一辺の長さは、数cm程度である。また、本体部111の厚みは数mm程度であり、溝部t1〜t4の深さHは数百μm程度である。他方、カバー部112の厚みは数十μm程度である。
【0020】
本体部111に設けられる4つの溝部t1〜t4には、それぞれ異なる物質が充填される。より具体的には、一方の端部に位置する溝部t1には、生理食塩水等から成る所定の緩衝液に、検体に含まれる特定物質と特異的に結合する物質を表面修飾した微粒子Bを混合した微粒子混合液101が充填される。この溝部t1に隣接する溝部t2には、検体102が充填される。この溝部t2の溝部t1と反対側で隣接する溝部t3には、溝部t2を通過してきた後の微粒子Bを洗浄するための緩衝液103が充填される。この緩衝液103は、前述した微粒子混合液101で用いる緩衝液と同じものである。溝部t3と隣接し、この溝部t3に対して溝部t2と反対側に設けられる溝部t4には、検体に含まれる特定物質と反応して光学的に検出可能な物質を生成する一方、微粒子Bを表面実装する物質と特定物質との結合は阻害しない反応試薬を含む試薬溶液104が充填される。
【0021】
ここで、溝部t2に充填される検体102が血液の場合には、分析対象となる特定物質として、例えば血清中のγグロブリンなどの抗体を挙げることができる。この場合、微粒子Bを表面修飾して特定物質である抗体と特異的に結合する物質は抗原である。したがって、特定物質と微粒子Bを表面修飾する物質との特異的な反応とは、抗原抗体反応に他ならない。
【0022】
3つの連結路、すなわち、溝部t1と溝部t2を連絡する連結路c1、溝部t2と溝部t3を連結する連結路c2、および溝部t3と溝部t4を連結する連結路c3は、レーザ光を用いて捕捉した微粒子Bを溝部t1から溝部t2、t3、およびt4へと順次移送するために設けられる。このため、各連結路の深さhは微粒子Bの径よりも大きくなければならない。この実施の形態では、微粒子Bとして、その径が数μm〜数十μm程度のプラスチック製の球状粒子を用いるので、連結路の深さhは数十μm程度よりも大きい。この深さhの値は、一方で、隣接する溝部にそれぞれ充填される液体の混合がほとんど無視できる程度に小さくなければならない。換言すれば、連結路の深さhのとり得る値の上限は、隣接する溝部間の液体の混合が無視できる程度の値でなければならない。
【0023】
この実施の形態において、連結路c1〜c3は、本体部111の表面に平行な断面(横断面)が長方形状をなしている(図2−1および図2−2を参照)。それらの長方形は、長手方向に対して互いに平行であるが同一直線上は通過していない。これは、微粒子Bがある連結路を介して隣接する溝部に到達したとき、この到達した溝部に充填されている液体の一部がさらに隣接する溝部に流出したりするのを防止するためである。
【0024】
なお、図2−2に示す溝部t1〜t4の一つの縦断面の形状、および連結路c1〜c3のX−X線とは垂直な方向の縦断面の形状は、底辺の方が短い等脚台形をなしていれば、光ピンセットで捕捉した微粒子Bを移送する上で好ましいが、必ずしもこの形状に限定されるわけではない。また、溝部t1〜t4の本体部111に平行な方向の横断面は長方形状でなくてもよく、例えば円形や多角形などであっても構わない。
【0025】
マイクロチップ11のカバー部112は、溝部t1〜t4に充填される物質の蒸発を防止するために本体部111に装着される。このカバー部112には、溝部ごとに物質を充填するために、開閉自在な二つの孔部(入口と出口に相当)を設けてもよい。そして、ある溝部に物質を充填する際には、その溝部に対応する二つの孔部を開放する以外は、全ての孔部を閉鎖する。
【0026】
次に、光学系13について説明する。この実施の形態では、蛍光顕微鏡を用いて微粒子Bを表面実装する物質(抗原とする)と検体102に含まれる物質(抗体とする)との間で生じる抗原抗体反応を分析する。この場合、光学系13は、レーザ光源12から発生するレーザ光を反射する反射鏡131と、この反射鏡131で反射されたレーザ光を集光してマイクロチップ11内の微粒子Bを照射する対物レンズ132とを有する。反射鏡131は、入射光および励起光としてのレーザ光を反射する一方、抗体と蛍光性物質を含む反応試薬との反応によって生成される放射光は透過するダイクロックミラーである。光学系13は、この反射鏡131を透過した放射光から所望の周波数帯域の光を採光するフィルタ133をさらに有する。なお、反射鏡131は所定の回転軸に対して回動自在であり、制御部16の制御に基づいて、レーザ光の集光位置を調整する。また、対物レンズ132は光軸方向に移動自在であり、制御部16の制御に基づいてレーザ光の照射位置を調整する。
【0027】
このような光学系13において、対物レンズ132の開口数を大きく取り、この対物レンズ132で集光するレーザ光のビームを絞り込むと、その焦点位置付近に存在する微粒子Bを光ピンセットで捕捉することができる。この意味で、レーザ光源12と光学系13は、少なくとも捕捉手段の一部をなしている。なお、微粒子Bを捕捉するためには、微粒子Bの径がレーザ光の波長よりも大きく、なおかつ微粒子Bの屈折率が微粒子混合液101、検体102、緩衝液103、および試薬溶液104の屈折率よりも大きければより好ましい。
【0028】
移送部14は、マイクロチップ11の表面を水平方向に載置する載置面を有しており、マイクロチップ11の表面に平行な2次元方向、すなわち図1で水平方向を指向し、なおかつ紙面に垂直な2次元面方向に移動自在であり、光ピンセットによって捕捉した微粒子Bを、連結路ci(i=1,2,3)を介して溝部tiから隣接する溝部ti+1へと移送する機能を有する。この移送部14を用いることにより、マイクロチップ11の位置決めを容易にかつ高精度に行うことが可能となる。
【0029】
測光部15は、特定物質である抗体と反応試薬中に含まれる蛍光性物質との反応によって生成、放射され、反射鏡131を透過してくる蛍光のうち、フィルタ133を通過した周波数帯域の蛍光成分を受光してその強度を増幅する光電子増倍管を有する。測光部15は、レーザ光源12および光学系13とともに、放射される蛍光を検出する検出手段の一部をなす。
【0030】
制御部16は、上述したレーザ光源12、光学系13(反射鏡131、対物レンズ132、フィルタ133)、移送部14、および測光部15の動作制御を行うとともに、測光部15の測定結果に基づいて検体の成分の分析を行う機能を有しており、演算および制御機能を有するCPU(Central Processing Unit)等によって実現される。
【0031】
以上の構成を有する分析装置1が行う分析方法の詳細について、図3に示すフローチャート図を用いて説明する。まず、レーザ光源12から発生するレーザ光が、溝部t1に充填される微粒子混合液101内の微粒子Bのいずれかを照射するように、移送部14を移動してマイクロチップ11の位置決めを行い、少なくとも一つの微粒子Bを光ピンセットで捕捉する(ステップS1)。以後の過程において、光学系13によって実現される光ピンセットは、このステップS1で捕捉した微粒子Bを捕捉し続ける。図4−1は、このステップS1で捕捉する微粒子Bが抗原aによって表面実装された状態を模式的に示す説明図である。
【0032】
次に移送部14は、マイクロチップ11を移動することにより、ステップS1で捕捉した微粒子Bを連結路c1まで移動し、さらにこの連結路c1を通過させることによって溝部t2に移送し、所定時間この状態を保持する(ステップS2)。この状態を保持することによって、溝部t2内の検体102に含まれる特定物質としての抗体bが、微粒子Bを表面実装する抗原aと抗原抗体反応を行う。したがって、ここでいう所定時間とは、抗原aと抗体bが抗原抗体反応を起こすのに十分な時間である。図4−2は、このステップS2における抗原抗体反応の結果、微粒子Bの表面で、抗原aと抗体bが抗原抗体反応によって特異的に結合した状態を模式的に示す説明図である。
【0033】
その後、移送部14は、マイクロチップ11を移動することにより、光ピンセットで捕捉している微粒子Bを、連結路c2を介して溝部t3に移送し、所定時間この状態を保持する(ステップS3)。この状態を保持することによって、抗原抗体反応を起こした微粒子Bに付随して溝部t3内に到達した遊離抗体を、溝部t3に充填される緩衝液103によって分離洗浄(B/F分離)することができる。したがって、ここでいう所定時間は、ステップS2における所定時間とは異なるものであり、緩衝液103を用いて不要な抗体を微粒子Bから分離するのに必要な時間である。
【0034】
続いて、移送部14は、光ピンセットで捕捉している微粒子Bを、連結路c3を通過させることによって溝部t4に移送する(ステップS4)。この溝部t4内では、充填された試薬溶液104中の反応試薬に含まれる蛍光性物質cが微粒子Bに付着した抗体bと反応(化学結合)を生じる。そしてこの反応の結果、蛍光Lが発生する。この際には、微粒子Bを照射して捕捉している入射レーザ光が、励起光としての役割を果たす。図4−3は、蛍光性物質cが抗体bと化学結合し、レーザ光によって励起された結果、蛍光Lを放射する状態を模式的に示す説明図である。
【0035】
次に測光部15が、溝部t4内での反応によってから放射され、フィルタ133でフィルタリングされた蛍光Lの強度を測定する(ステップS5)。そして、測光部15で測定した結果を制御部16が分析する(ステップS6)。なお、分析装置1にデータを出力表示する出力部と、データを記憶する記憶部とをさらに設けることにより、このステップS6における分析結果を出力部で表示したり、記憶部に記憶したりしてもよい。
【0036】
以上説明した本発明の一実施の形態によれば、検体およびこの検体の成分を分析するのに必要な物質を含む液体を別個に充填する複数の溝部と、隣接する溝部同士を連結する連結路を有するマイクロチップと、このマイクロチップ内の微粒子を所定のレーザ光を用いた光ピンセット技術によって捕捉し、移送部でマイクロチップを移動させながら捕捉した微粒子を操作して反応を調整することにより、検体に含まれる特定物質が他の物質との間で行う抗原抗体反応を適確かつ高精度に制御することができる。
【0037】
この実施の形態では、分析に用いる検体や試薬はマイクロチップの溝部に充填する量で十分なため、数百nl(ナノリットル)程度の極めて微小な量で済む上、マイクロチップ自体の洗浄も分析終了まで不要なため、洗浄水も少量で済む。したがって、この実施の形態によれば、従来の分析システムに比べ、一段とコストを低く抑えることができ、経済的である。
【0038】
また、この実施の形態によれば、従来の分析装置のように試薬を別な容器などに置換する必要がなく、マイクロチップ本体の移送のみですべてのプロセスを実行するため、マイクロチップ自体のレイアウトの自由度が高く、その構成を単純にすることができる。したがって、この意味でもコストの低減という効果が得られる。
【0039】
さらに、この実施の形態によれば、例えば検体として血液を用いる場合、必要な血液の量が少なくて済むので、血液を採取される側の検体提供者の肉体的かつ心理的な負担を軽減させることができる。
【0040】
ここまで、本発明の好ましい一実施の形態を詳述してきたが、本発明はこの実施の形態によってのみ限定されるものではない。例えば、各溝部に充填する溶液の種類や分析に必要な溝部の数は、検体の成分の分析に必要な反応等に応じて適宜変更することが可能である。この意味で、本発明に係るマイクロチップのレイアウトは、各種免疫分析のために必要な抗原抗体反応等の反応を光学的に検出可能なものであれば如何なる構成であってもよく、溝部の個数が3個または5個以上であってもよい。これらの溝部のうち、互いに隣接する溝部同士に連結路が設けられる点は、上記一実施の形態と同様である。
【0041】
また、上述した一実施の形態においては蛍光分析を用いて検体の分析を行ったが、それ以外にも、ルミナール反応等に基づく化学発光分析や、検出光を物質に照射して透過してくる透過光から物質の吸光量を測定する吸光光度分析法等のよく知られた分析手法を用いることも可能である。これらの分析手法に応じて、分析装置、特に光学系の構成が適宜変更されることは勿論である。
【0042】
さらに、本発明に係る分析装置に、複数のマイクロチップを格納、保管する機能と、検体を保管して、この検体をマイクロチップの適当な溝部に分注する機能と、検体を分注したマイクロチップを移送する機能とをさらに具備させることにより、多数の検体の成分を自動かつ連続的に分析可能な自動分析装置を構成することも可能である。この場合には、マイクロチップにおいて、検体を充填する溝部だけは空にしておき、他の溝部には抗原抗体反応を起こすのに必要な所定の液体を予め充填したものを大量に製造しておけば、後から検体充填用の溝部に検体を充填するだけで検体の分析を行うことができる。
【0043】
このように、本発明は、ここでは記載していないさまざまな実施の形態等を含みうるものであり、特許請求の範囲により特定される技術的事項を逸脱しない範囲内において種々の設計変更等を施すことが可能である。
【図面の簡単な説明】
【0044】
【図1】本発明の一実施の形態に係る分析装置要部の構成を模式的に示す説明図である。
【図2−1】本発明の一実施の形態に係る分析用マイクロチップ表面の構成を示す平面図である。
【図2−2】図2−1のX−X断面図である。
【図3】本発明の一実施の形態に係る分析方法の処理の流れを示すフローチャート図である。
【図4−1】微粒子を抗原で表面実装した状態を模式的に示す説明図である。
【図4−2】微粒子の表面で、抗原と抗体が抗原抗体反応によって特異的に結合した状態を模式的に示す説明図である。
【図4−3】蛍光性物質が抗体と化学結合し、蛍光を放射する状態を模式的に示す説明図である。
【符号の説明】
【0045】
1 分析装置
11 マイクロチップ
12 レーザ光源
13 光学系
14 移送部
15 測光部
16 制御部
101 微粒子混合液
102 検体
103 緩衝液
104 試薬溶液
111 本体部
112 カバー部
131 反射鏡
132 対物レンズ
133 フィルタ
c1、c2、c3 連結路
t1、t2、t2、t4 溝部
B 微粒子
L 蛍光
a 抗原
b 抗体
c 蛍光性物質
【特許請求の範囲】
【請求項1】
検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する分析装置であって、
前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップと、
前記マイクロチップが有する複数の溝部のいずれかに充填される液体に混合され、前記特定物質と特異的に反応する物質を表面修飾した微粒子に対して所定のレーザ光を照射することにより、前記微粒子を光学的に捕捉する捕捉手段と、
前記捕捉手段で光学的に捕捉した微粒子を、前記複数の連結路を順次通過させることによって前記複数の溝部間で移送する移送手段と、
前記移送手段が前記微粒子を移送した結果、前記特定物質と前記反応試薬との反応によって生成された物質を光学的に検出する検出手段と、
を備えたことを特徴とする分析装置。
【請求項2】
前記検体の成分を分析するために必要な複数種類の液体は、
所定の緩衝液に前記微粒子が混合されて成る微粒子混合液と、
前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、
を含むことを特徴とする請求項1記載の分析装置。
【請求項3】
検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する分析方法であって、
前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップ内の前記複数の溝部のいずれかに充填される液体に混合され、前記特定物質と特異的に反応する物質を表面修飾した微粒子に対して所定のレーザ光を照射することにより、前記微粒子を光学的に捕捉する捕捉ステップと、
前記捕捉ステップで光学的に捕捉した微粒子を、前記複数の連結路を順次通過させることによって前記複数の溝部間で移送する移送ステップと、
前記移送ステップで前記微粒子を移送した結果、前記特定物質と前記反応試薬との反応によって生成された物質を光学的に検出する検出ステップと、
を有することを特徴とする分析方法。
【請求項4】
前記移送ステップでは、
前記微粒子を順次移送する各溝部において、各溝部に充填される物質に応じて溝部ごとに定められる時間だけ前記微粒子を保持することを特徴とする請求項3記載の分析方法。
【請求項5】
前記検体の成分を分析するために必要な複数種類の液体は、
所定の緩衝液に前記微粒子が混合されて成る微粒子混合液と、
前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、
を含むことを特徴とする請求項3または4記載の分析方法。
【請求項6】
検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する際に適用する分析用マイクロチップであって、
前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部と、
前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路と、
を備えたことを特徴とする分析用マイクロチップ。
【請求項7】
前記検体の成分を分析するために必要な複数種類の液体は、
前記特定物質と特異的に反応する物質を表面修飾し、前記複数の連結路を通過可能な微粒子が、所定の緩衝液に混合されて成る微粒子混合液と、
前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、
を含むことを特徴とする請求項6記載の分析用マイクロチップ。
【請求項1】
検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する分析装置であって、
前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップと、
前記マイクロチップが有する複数の溝部のいずれかに充填される液体に混合され、前記特定物質と特異的に反応する物質を表面修飾した微粒子に対して所定のレーザ光を照射することにより、前記微粒子を光学的に捕捉する捕捉手段と、
前記捕捉手段で光学的に捕捉した微粒子を、前記複数の連結路を順次通過させることによって前記複数の溝部間で移送する移送手段と、
前記移送手段が前記微粒子を移送した結果、前記特定物質と前記反応試薬との反応によって生成された物質を光学的に検出する検出手段と、
を備えたことを特徴とする分析装置。
【請求項2】
前記検体の成分を分析するために必要な複数種類の液体は、
所定の緩衝液に前記微粒子が混合されて成る微粒子混合液と、
前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、
を含むことを特徴とする請求項1記載の分析装置。
【請求項3】
検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する分析方法であって、
前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部を有するとともに、前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路を有するマイクロチップ内の前記複数の溝部のいずれかに充填される液体に混合され、前記特定物質と特異的に反応する物質を表面修飾した微粒子に対して所定のレーザ光を照射することにより、前記微粒子を光学的に捕捉する捕捉ステップと、
前記捕捉ステップで光学的に捕捉した微粒子を、前記複数の連結路を順次通過させることによって前記複数の溝部間で移送する移送ステップと、
前記移送ステップで前記微粒子を移送した結果、前記特定物質と前記反応試薬との反応によって生成された物質を光学的に検出する検出ステップと、
を有することを特徴とする分析方法。
【請求項4】
前記移送ステップでは、
前記微粒子を順次移送する各溝部において、各溝部に充填される物質に応じて溝部ごとに定められる時間だけ前記微粒子を保持することを特徴とする請求項3記載の分析方法。
【請求項5】
前記検体の成分を分析するために必要な複数種類の液体は、
所定の緩衝液に前記微粒子が混合されて成る微粒子混合液と、
前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、
を含むことを特徴とする請求項3または4記載の分析方法。
【請求項6】
検体に含まれる特定物質と特異的に反応する物質を用いて前記検体の成分を分析する際に適用する分析用マイクロチップであって、
前記検体および当該検体の成分を分析するために必要な複数種類の液体を個別に充填する複数の溝部と、
前記複数の溝部のうち隣接する溝部同士をそれぞれ連結する複数の連結路と、
を備えたことを特徴とする分析用マイクロチップ。
【請求項7】
前記検体の成分を分析するために必要な複数種類の液体は、
前記特定物質と特異的に反応する物質を表面修飾し、前記複数の連結路を通過可能な微粒子が、所定の緩衝液に混合されて成る微粒子混合液と、
前記特定物質と反応して光学的に検出可能な物質を生成する反応試薬を含む試薬溶液と、
を含むことを特徴とする請求項6記載の分析用マイクロチップ。
【図1】


【図2−1】


【図2−2】


【図3】


【図4−1】


【図4−2】


【図4−3】




【図2−1】


【図2−2】


【図3】


【図4−1】


【図4−2】


【図4−3】


【公開番号】特開2007−315783(P2007−315783A)
【公開日】平成19年12月6日(2007.12.6)
【国際特許分類】
【出願番号】特願2006−142695(P2006−142695)
【出願日】平成18年5月23日(2006.5.23)
【出願人】(000000376)オリンパス株式会社 (11,466)
【Fターム(参考)】
【公開日】平成19年12月6日(2007.12.6)
【国際特許分類】
【出願日】平成18年5月23日(2006.5.23)
【出願人】(000000376)オリンパス株式会社 (11,466)
【Fターム(参考)】
[ Back to top ]

