異性体化合物の処理方法及び装置
【課題】所謂異性体化合物間の分離においては、吸着力、電荷、疎水性の差が小さく、化学的な相互作用の差を利用することは期待できない。一方、液体クロマトグラフィーに於いては保持及び分離が安定的に行われるシステム系全体の平衡化には時間がかかる。これを短時間で平衡化して簡単容易に異性体化合物間の分離を行えるようにする。
【解決手段】液体クロマトグラフィーに於いて使用するカラムの出口流路に抵抗を設け、その作動によりカラム入口圧力を10MPa〜100MPaに調整し異性体化合物を成分ごとに溶質挙動を変えることを特徴とする異性体化合物の処理方法。
【解決手段】液体クロマトグラフィーに於いて使用するカラムの出口流路に抵抗を設け、その作動によりカラム入口圧力を10MPa〜100MPaに調整し異性体化合物を成分ごとに溶質挙動を変えることを特徴とする異性体化合物の処理方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、液体クロマトグラフィーにおける異性体化合物の処理、特にその分離及び分取に関するものである。
【背景技術】
【0002】
クロマトグラフィーは、化合物の官能基の種類や大きさの違いによる吸着力・電荷・疎水性の差を利用して、成分分離に広く使われている手法である。しかし、分子量と官能基の種類が同一、つまり分子式が同一ではあるが、その分子構造が異なる化合物、所謂異性体化合物間の分離においては、吸着力・電荷・疎水性の差が小さいため、これらの化学的な相互作用の大きな差が期待できない。その目的ではカラムの基本的な分離性能が非常に高い、20万段以上の理論段数が得られるキャピラリーガスクロマトグラフィーが期待されるが、熱分解成分や高沸点化合物には適用できないので、分析の前に誘導体化するなどの手間のかかる手法が取られる。
【0003】
一方、前処理の手間が比較的かからない液体クロマトグラフィーではどうかというと、有機溶媒と水の割合を変える単純な溶離液の変更だけでは異性体化合物間の分離はできないことが多い。そのため、異性体化合物の認識能が高いシクロデキストリンなどの高分子化合物を溶離液に添加したり、これらの化合物を固定相としたLCカラムを用いたりするなどの種々の工夫を行う必要が出てくる。
特殊な溶離液への変更はベースラインの安定に時間を要し、場合によっては装置の接液部にダメージを与えることも考えられる。
【0004】
カラム温度を15℃以下に下げ、低温分析する手法も提案されているが、高価な冷却用オーブンが必要で、さらに、冷却するには多くのエネルギーも必要となる。時期によっては結露による装置へのダメージも考えられ、使いづらさやカラムを均一な温度にするための安定時間などを考慮すると実用に困難を伴う。
【0005】
液体クロマトグラフィーにおいて、保持及び分離が安定する、言い換えると、システム系すべての状態が平衡化するには、かなりの時間が必要となる。特に、異性体化合物分離においては特殊な溶離液を用いたり、分析温度を下げたりするのでより長い時間がかかってしまう。さらに、カラム変更においては、その付け替え時間、カラム内溶媒を溶離液に変化させるための中間溶媒の選択、その溶離液の平衡化ということで多大なる手間と時間がかかる。
【0006】
それに対して、流量及び圧力の変更は、平衡化が速く、液体クロマトグラフィーにおいては有効な手段となり得る。流量の変更は、保持が全体的に早くあるいは遅くなるだけで、個々の成分間の分離は大きく変化しないが、圧力の変更は、分離に様々影響するとの知見が得られてきている。
【0007】
Rogers らは、シリカ固定相、水移動相系で、メチルオレンジとエチルオレンジの保持について、20000psiまでは保持減少、20000psiより高圧になると、保持増加を認めた報告を行っており、後にion−pair RPLCにおいて2410barに昇圧するとメチルオレンジの保持増加が3.2倍になったこと、その原因としてイオンペア系は複雑な平衡系であり、高圧によるイオン対生成の増加が保持の増加をもたらした可能性の考えられることが示唆されている(非特許文献1)。
【0008】
Jorgensonらは、アセトニトリル (ACN)−水(40:60v/v)混合溶液の粘度(0.89cP)が、25℃、3500barで0.16cP/kbar増加することを報告している(非特許文献2)。
【0009】
McGuffinらはC10−C20脂肪酸のメトキシクマリン誘導体が、カラム入口圧力36−360barの増加により9%から24%保持増加したことを報告している(非特許文献3,4)。相互作用として分散力が、エントロピー的な効果と併せて考慮されていて、溶質、移動相、固定相すべてが圧縮されると考えられている。さらに、平面的芳香族(PAH)については保持増加7%、非平面的芳香族については効果は小さいかむしろ減少を報告している。
【0010】
Jorgensonらは2,3‐hydroxynaphthaleneについてオクタデシル(ODS)基結合シリカゲルカラムを用い1000barで12%の保持増加を報告している(非特許文献5)。
【0011】
田中らは、解離可能な溶質(酸、塩基)がそれらのpKa(酸解離定数)付近のpHにおいて溶出されるとき、圧力が溶質や緩衝溶液物質のpKaを変化させ、高圧がイオン化を促進するという報告を行っている。この結果、イオン化制御逆相クロマトグラフィーにおいて、移動相のpHや溶質のイオン化率が圧力によって変化し、弱酸、弱塩基の保持が変化し、分離パターンの変化をもたらす。この場合、圧力が、より大きな体積変化をもたらす種に対する圧力効果が、保持の変化の方向(増加あるいは減少)を支配すると考察している(非特許文献6)。
【0012】
Evansらはシクロデキストリン添加逆相クロマトグラフィー系、あるいはシクロデキストリン結合固定相系において、加圧によりシクロデキストリンへの取り込みが増加し、p‐nitrophenolの保持や、優先的に取り込まれる光学異性体化合物の保持が変化し、分離係数が変化(増加あるいは減少)する場合があることを報告している。このような環状構造ホスト物質による取り込み平衡系における圧力効果は、固定相における圧力効果より大きく、分離度はいずれの場合にも減少すると報告している(非特許文献7,8)。
【0013】
McCalleyらは、50MPa程度の加圧(カラムと検出器の間に30μm キャピラリーを接続)により、疎水性・中性物質について12%程度、極性、高分子物質についてさらに大きな増加、イオン(酸、塩基)性物質について50%以上の保持の増加が認められたと報告している。さらに、固定相による影響(C18がC1より大きな効果)を報告している。高圧による保持の増加は、高圧下で溶質が脱溶媒和し、保持を促進することによりもたらされると結論している。又、タンパク質のような高分子について、はるかに大きな圧力効果(保持の増加)が報告されている。(非特許文献9,10,11,12)
【0014】
以上のように注目されるべき見解を含む種々の発表がされている。しかし、これらの分離カラムの加圧による保持の変化に関する報告の多くは、親水性化合物に関するものである。50MPaの圧力増加に対して疎水性化合物でも、5−24%の保持の増加が認められているが、親水性化合物のように大きな保持の増加を報告しているものは見当たらない。
【0015】
加圧効果に関するこれまでの報告を分類すると、次の4つのタイプに表される。
タイプ1:非極性・疎水性化合物(長鎖アルキル化合物,PAH)の分散相互作用(McGuffin,McCalley):疎水性(平面的)溶質に対する保持の小さな増加(分散力の増加+立体排除)。
タイプ2:pKa付近のpHにおける弱酸,弱塩基のイオン化制御(Tanaka):弱酸、弱塩基について、pH,pKaの変化を通じた保持の変化(増加、減少)(溶媒和の増加(電縮)による高圧におけるイオン解離の促進)
タイプ3:pKaから離れたpHにおいて、イオンや親水性溶質の脱溶媒和(McCalley):親水性溶質やイオンについて、保持の大きな増加(溶質の脱溶媒和に基づいているとも考えられている)。
タイプ4: 環状構造ホストによるInclusion(取り込み)現象(錯体形成の増加)において、ホストの空間に取り込まれ得る親水性溶質について加圧による錯体生成の増加、光学異性体化合物間の分離係数のわずかな変化(増加あるいは減少)。
【先行技術文献】
【非特許文献】
【0016】
【非特許文献1】G.Prukop,L.B.Rogers,Sep.Sci.Technol.,13(1978)59.
【非特許文献2】J.W. Thompson, T.J. Kaiser, J.W. Jorgenson, J. Chromatogr. A 1134 (2006) 201.
【非特許文献3】V.L. McGuffin, S.-H. Chen, Anal. Chem. 69 (1997) 930.
【非特許文献4】V.L. McGuffin, C.E. Evans, J. Microcol. Sep. 3 (1993) 513.
【非特許文献5】J.S. Mellors, J.W. Jorgenson, Anal. Chem. 76 (2004) 5441.
【非特許文献6】N. Tanaka, T. Yoshimura, M. Araki, J. Chromatogr. 406 (1987) 247.
【非特許文献7】L.M. Ponton, S.M. Hoenigman, M. Cai, C.E. Evans, Anal. Chem. 72 (2000) 3581.
【非特許文献8】C.E. Evans, J.A. Davis, Anal. Chim. Acta 397 (1999) 163.
【非特許文献9】M. M. Fallas, U. D. Neue, M. R. Hadley, D. V. McCalley, Journal of Chromatography A, 1209 (2008) 195
【非特許文献10】S.-H. Chen, C.-T. Ho, K.-Y. Hsiao, J.-M. Chen, J. Chromatogr. A 891 (2000) 207.
【非特許文献11】M.A. Stadalius, H.S. Gold, L.R. Snyder, J. Chromatogr. 296 (1984) 31.
【非特許文献12】X. Liu, P. Szabelski, K. Kaczmarski, D. Zhou, G. Guiochon, J. Chromatogr. A 988 (2003) 205.
【発明の概要】
【発明が解決しようとする課題】
【0017】
このような背景があり、異性体化合物の分離においては、安定の早い簡単な溶離液で、分離を達成することが求められている。尚、ここでカラムは分離カラムの意で用いられ、分析カラム、分取カラムである。
【0018】
異性体化合物の分離を実現させるために、異性体各成分の分離を更に言えば異性体各成分ごとの溶質挙動(パターン)を変化させることが重要である。圧力による相互作用としては、タイプ1が普遍的に働き、加えて立体選択性が働くことにより、異性体化合物間の分離を変化させることが期待できる。
【0019】
液体クロマトグラフィーにおいては、流量を大きくするとカラム内の抵抗により、カラム入口圧力を上げることは可能であるが、出口側では大気圧になってしまい、カラム中央では、入口圧力の1/2の増加にとどまる。固定相に対する圧力効果は、入口の一部しか働かない上、カラムの分離性能が下がることが多い。圧力の増加のために温度を下げる方法は、実用的な温度では粘度の増加が大きくないので、圧力を上げる効果が小さい。
【0020】
一方、流速やカラム長さが変わると圧力が変化するが、カラム性能も同時に変化するので分離パターンの変化が、圧力の効果によるものか、他の要素によるものか不明確で安定した圧力の効果が得られない。一定の圧力効果を得るためには、カラム入口側の圧力効果と同じ効果をカラム出口でもたらす必要があり、出口側に入口と同じ背圧を加える必要がある。すなわち、カラム全体の平均的圧力が、通常の分析時の2倍以上になるように背圧を加えればその効果が最も明確に得られることになる。
【0021】
例えば、良く用いられる5μm粒子が充填されたカラムの場合、100%アセトニリルを溶離液として、線速度1mm/secで流した場合、分析圧力は、1MPa〜5MPaになる。出口側でも同じ圧力効果が働くように背圧を加えると、入口圧力は2倍の2MPa〜10MPaとなる。
【課題を解決するための手段】
【0022】
上記課題を達成するための手段としては下記の通りである。
その一として、液体クロマトグラフィーに於いて使用するカラムの出口流路に抵抗を設け、該抵抗の作動によりカラム入口圧力を10MPa〜100MPaに調整し異性体化合物を成分ごとに溶質挙動を変えることを特徴とする異性体化合物の処理方法である。
【0023】
その一として、溶質挙動の変化は溶質の分離であることを特徴とする異性体化合物の処理方法である。
【0024】
その一として、溶質挙動の変化は溶質出現順序の変化であることを特徴とする異性体化合物の処理方法である。
【0025】
その一として、溶質挙動の変化は溶質の合体であることを特徴とする異性体化合物の処理方法である。
【0026】
その一として、前記カラム入口圧力を100MPa〜10MPaの間で連続的又は段階的に下げながら異性体化合物の溶質挙動を変化させることを特徴とする異性体化合物処理方法である。
【0027】
その一として、溶離液の組成を変化させることで、前記カラム入口圧力を100MPa〜10MPaの間で連続的又は段階的に変化させ異性体化合物の溶質挙動を変化させることを特徴とする異性体化合物の処理方法である。
【0028】
その一として、カラム温度を変化させることで、前記カラム入口圧力を100MPa〜10MPaの間で変化させ、異性体化合物の溶質挙動を変化させることを特徴とする異性体化合物の処理方法である。
【0029】
その一として、前記カラムが分析カラムであることを特徴とする異性体化合物の分析方法である。
【0030】
その一として、前記カラムが分取カラムであることを特徴とする異性体化合物の分取方法である。
【0031】
その一として、異性体化合物を処理する装置であって、カラム出口流路に於いて、カラム出口から検出器までの間または検出器から排出の間またはその両方に抵抗を接続し、カラム入口圧力を所定の圧力に調整自在としたことを特徴とする異性体化合物の処理装置である。
【0032】
その一として、前記カラムに分析カラムを使用した異性体化合物分析装置である。
【0033】
その一として、前記カラムに分取カラムを使用した異性体化合物分取装置である。
【0034】
その一として、前記抵抗が抵抗管であることを特徴とする異性体化合物の処理装置である。
【0035】
その一として、前記抵抗管はチューブ、モノリスカラム、充填カラムのうちの一であることを特徴とする異性体化合物の処理装置である。
【0036】
その一として、前記抵抗が、液体が流通する空間容量を変化できるレギュレータであることを特徴とする異性体化合物の処理装置である。
【0037】
その一として、上記の何れかに記載の異性体化合物の処理装置であって、前記カラムとして分析カラムを使用したことを特徴とする異性体化合物の分析装置である。
【0038】
その一として、上記の何れかに記載の異性体化合物の処理装置であって、前記カラムとして分取カラムを使用したことを特徴とする異性体化合物の分取装置である。
【0039】
その一として、前記カラム出口流路側にバルブを設け、該バルブに複数の抵抗を接続し、接続する抵抗の選択により、所定のカラム入口圧力を得ることを特徴とする異性体化合物の処理装置である。
【0040】
その一として、10MPa以上の耐圧のある粒子状担体又はモノリス担体に固定相を2μmol/m2以上の密度に塗布又は化学結合させた充填剤を用いた異性体化合物分離カラムである。
【0041】
その一として、10MPa以上の耐圧のある粒子状担体又はモノリス担体に固定相を2μmol/m2以上の密度に塗布又は化学結合させた異性体化合物分離カラム用充填剤である。
【発明の効果】
【0042】
カラム出口から検出器までの間または検出器から排出の間またはその両方に、抵抗を接続し、分析圧力を10MPa以上にすることで、異性体化合物溶出の変化、例えば分離、分離順序の変更、合体等の変化をさせることが可能となった。分析圧力の変更では、平衡時間は短く、従来のような溶離液や温度を変えた場合の30分以上の平衡化待ち時間を無くすことができる。
【0043】
又、圧力調整は、従来から市販されている種々の方法が使用でき、簡単に実現可能である。
【0044】
又、単純な溶離液で、室温でも異性体化合物分離が可能となるので、従来多量の溶離液を用いて、温調が難しかった分取が簡単にできるようになった。
【図面の簡単な説明】
【0045】
【図1】本発明一実施例概略説明図
【図2】本発明−実施例対象異性体化合物トコフェロール図
【図3】本発明一実施例概略説明図
【図4】本発明一実施例概略説明図
【図5】本発明一実施例ロータリーバルブ図
【図6】本発明一実施例バルブ切換図
【図7】本発明一実施例レギュレータ図
【図8】本発明一実施例クロマトグラム
【図9】本発明一実施例クロマトグラム
【図10】本発明一実施例クロマトグラム
【図11】本発明一実施例クロマトグラム
【図12】本発明一実施例クロマトグラム
【図13】本発明一実施例クロマトグラム
【図14】本発明一実施例クロマトグラム
【図15】本発明一実施例クロマトグラム
【図16】本発明一実施例クロマトグラム
【図17】本発明一実施例クロマトグラム
【図18】本発明一実施例クロマトグラム
【図19】本発明一実施例クロマトグラム
【図20】本発明一実施例クロマトグラム
【図21】本発明一実施例クロマトグラム
【発明を実施するための形態】
【0046】
一般的に二酸化炭素の溶解において、その溶解度は、圧力に対して10MPa程度までは、大きく上昇し、10MPa以上では変化が少なく15MPaでほぼ一定となると言われている。
HPLCにおける試料成分の固定相への溶解度もほぼ同等の傾向を示すと考えられ、保持の早い安定を考えると、圧力における溶解度の変化が小さくなる10MPa以上が理想と考えられる。本願発明の実施例においても、10MPa以上で効果が得られることが実証されている。
【0047】
装置やカラムが許すならば、圧力が高い方が、カラム内の圧力勾配の影響が、システム全体に影響しないので、安定が早くなる。背圧を加えてシステム圧力を100MPaまで上げると、カラム部分の圧力影響は5%以下になり、カラムの種類やカラムサイズによる圧力変化影響もほとんど無くなる。従って、10MPa以上ならば異性体化合物の処理が可能であり、上限圧力は装置耐圧に依存される。
現在市販されている最も耐圧の高いHPLC装置は、耐圧150MPaであり、そのカラム部分の圧力影響は3%以下となるため、より安定なデータが得られることが期待される事になる。しかし、実際には溶離液を送り出す送液ポンプのプランジャーや試料導入を行うインジェクターなどの接液部には樹脂性のシール材が使用されており、150MPaでは磨耗が早く長時間の安定した送液ができない。従って、圧力調整の実用における上限は、100MPaと考えるのが適当である。
【0048】
異性体化合物の分離を再現良く変化させるすなわち、化合物間の分離をコントロールするには、カラム入口圧力を10MPa〜100MPa内になるように、カラム出口側即ちカラム出口流路に抵抗を接続し、調整することが非常に有用である。
【0049】
その場合、カラム出口側と検出器又は検出器セル間での抵抗増加でも異性体化合物分離は達成できるが、その部分でのデッドボリュームが生じるのでピーク形状が悪くなる懸念があり、検出器セルの後に抵抗を付けることが理想的である。
【0050】
また検出器セルそのものを抵抗として使用することも可能で本発明の効果が期待できる10MPa以上の耐圧セルならば何でも良いが、具体的には下記セルが使用できる。
検出器セルとしては一般的に石英やガラスが使用されることが多いが、そのままでは耐圧性が無いため、テフロン(登録商標)、ポリエチレン、ポリプロピレン、ポリエーテルエーテルケトン(以後PEEKと略す)などの検出に用いる光を透過する樹脂をコートした石英やガラス製セルなどが50MPa程度の耐圧が得られるので適している。また内径1mm未満の溶融シリカキャピラリーセルを用いると100MPa程度までの耐圧が得られ、そのままで本発明の異性体化合物分離を実現できる。
【0051】
しかしながら、キャピラリーの場合では内径が1mm未満であるため、用いることのできる流速が1mL/min程度に限定されてしまうという限界がある。より高流速を用いる分取を考えると、50MPa以上の背圧に耐えるためにはステンレスなどの金属製セルが好ましい。検出器セルに高圧が掛かると、数μmオーダーの表面の傷にも溶質が入り込み吸着原因になってしまう。物理的に研磨する方法は種々あるが、細かい検出器セルの機械的な内面加工には限界がある。そこで、テトラエトキシシラン、テトラメトキシシラン、シクロシロキサンなどのケイ酸化合物やポリシラザンなどの反応性試薬による化学処理によって、ガラス表面を形成させたセルを用いることが良い。
【0052】
カラム出口流路側に抵抗を接続し、圧力制御する方法としては、10MPa以上の圧力がカラム入口に掛かれば良く、特に規定するものではないが、具体的には下記のような方法が考えられる。
【0053】
内径0.15mm以下の中空抵抗管、好ましくは接液面がなめらかである溶融石英キャピラリーチューブを接続する方法が簡便で適している。
物理的な振動による破損を防ぐため、PEEKなどの樹脂チューブで、接続部または抵抗管全体を保護する事が有効である。
さらに、より短い長さでより強い抵抗を得るためには、100μm以下例えば50μmの貫通するスルーポアを持ち、かつ骨格が3次元的に繋がった一体型の所謂モノリス体をチューブ内に形成したモノリス抵抗管が好ましい。
【0054】
それらは、比較的デッドボリュームが小さいので、カラムと検出器又は検出器セルの間に設けても、十分使用できる。これら単独でも十分使用できるが、さらに、抵抗を接続しても良い。
【0055】
カラムと検出器又は検出器セル間で一定の抵抗を接続することで、すぐに圧力が10MPa以上で安定し、異性体化合物分離が安定して行える。さらに後に変化可能な異なる抵抗を設けることで、圧力を加えて調整できる。
【0056】
たとえば、カラムと検出器セル間にデッドボリュームの影響のないモノリス抵抗管を入れて、効果が得られる10MPa以上の20MPaになるようにする。
そのようなセルの後に40MPaとなる下記のような抵抗を設けると、カラム入口圧力は、20MPa〜60MPaまで調整できる。この場合には、セルには最大で40MPaしか掛らないので、市販されている耐圧40MPaセルを使用すればガラス化などの工夫は必要なく使用できる。
【0057】
検出器又は検出器セルの後での抵抗としては、HPLC充填カラムを抵抗管の代わりに用いることも可能である。さらに、複数の抵抗管をバルブに取り付け、順次流路を切り替えることで、順次圧力を変えることもできる。また、従来から市販されている高耐圧の液体用ニードルバルブも使用できる。ニードルの絞りを変えることで自由に流路抵抗を変化させられるので、自動で圧力を簡単に変えることができる。
【0058】
内径を順次細くした円錐状の抵抗管やモノリスフィルターを用いた抵抗調整など、背圧調整ができれば、従来技術が何でも使用できる。デッドボリュームの影響が考えられる場合には、低デッドボリュームの抵抗管とボリュームのある抵抗を組み合わせることが推奨される。
【0059】
用いるカラムとしては、特に限定される訳ではないが、高密度構造固定相を持ったLC充填タイプカラムやモノリスカラムが異性体化合物分離の変化が大きくなる。この溶出挙動変化としては、分離の拡大、促進、流出順序の変化、変更、合体が挙げられる。
【0060】
オリゴ糖や多糖誘導体やタンパク質などの剛直な構造を固定相とした粒子充填タイプカラムやモノリスカラムなどが、加圧による異性体化合物分離により効果を発揮する。
【0061】
具体的には、C16以上の長鎖アルキル鎖を持つ化合物固定相や平面的な構造を持つ芳香環を持つ固定相などは、高密度構造になり異性体化合物分離の変化が大きくなる。
【0062】
固定相や多孔質体によって異なるが、1〜2μmol/m2の固定相を導入すると1層に並んだ形での単分子層が形成される(モノメリック結合)。1μmol以下だと疎となり固定相としては低密度となる。高密度と言われる固定相では、結合基が多層に重なり(ポリメリック)導入された状態になり、2μmol/m2以上の固定相の場合が多い。
【0063】
担体として、シリカゲル、チタニア、ジルコニアなどの粒子状無機担体、それらに有機物を含む無機-有機のハイブリッド担体、スチレンジビルベンゼンポリマーなどの有機担体、無機モノリス体、無機−有機のハイブリッドモノリス、有機モノリスなどで、固定相を保持できる10MPa以上の担体ならば、どれでも適用できる。
【実施例1】
【0064】
カラム入口の圧力を10MPa以上にする方法として、具体的に下記の方法を実施した。
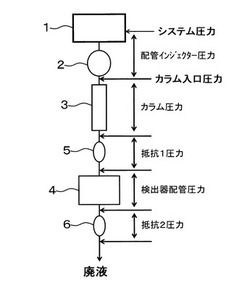
図1は一般的なLCシステムとしてのHPLCシステムであり、HPLCポンプ1、インジェクター2、カラム3、検出器4から構成される。移動相となる溶離液は、HPLCポンプ1により送り出され、インジェクター2,カラム3,検出器4の順に流れ、廃液される。
【0065】
図1の装置に於いては、カラム3の後に第1抵抗5、または検出器の後に第2抵抗6を設置した。HPLCシステム全体の圧力は、配管インジェクター圧力とカラム圧力と抵抗5圧力と検出器配管圧力と抵抗6圧力の合計値となって表わされる。カラム入口圧力は、システム全体の圧力から配管インジェクター圧力を引いた圧力となる。実際には、もっとも高性能が得られる線速度2mm/sec以下の場合では、配管インジェクター圧力は、0.5MPa以下であり、システム圧力とカラム入口圧力は同じと考えてよい。
【0066】
固定相となるHPLC充填カラムとして、内径4.6mm長さ25cmのInertsil(登録商標)C30(USPコード L62 トリアコンチル基結合シリカゲル 5μm ジーエルサイエンス社製)を用いて、トコフェロール異性体の分離をおこなった。トコフェロールは図2の構造を持ち、特にβとγの異性体はメチル基(図中Meと略す)の結合位置が異なるだけで、分離は難しい。溶離液としては、HPLCで広く使われもっとも単純な組成であるメタノール100%を使用し、流速500μL/min(線速度0.5mm/sec)、カラム温度40℃を分析条件とした。
【0067】
抵抗5と6を接続していない分析では、カラム入口圧力は、3.1MPaになり、異性体は分離していない(図8(1) 1:δ−トコフェロール、2:γ−トコフェロール、3:β−トコフェロール、4:α−トコフェロール 以下同じ)。
【0068】
抵抗5に、内径0.05mm溶融シリカキャピラリーチューブ40cmを設置し、抵抗6は接続無しとした結果、カラム入口圧力は、13MPaとなりピーク2,3に表される異性体の溶出が変化し分離が見られた(図8(2))。
【0069】
さらに抵抗5を内径0.03mm溶融シリカキャピラリーチューブ25cmに変える事で、カラム入口圧力は、49MPaとなり、異性体のγ−トコフェロールに対してβ−トコフェロールの溶出が、より遅くなり、結果として分離した(図8(3))。
【0070】
どちらのシステムもその容量は、1μL以下で、そのデッドボリュームによる遅れ時間は、0.1秒以下でありピーク形状への悪化影響もなかった。つまり、カラムとセル間にカラム入口圧力が10MPa以上になる抵抗を接続することで、単純な溶離液での異性体分離が行えることが確認された。
【0071】
さらに、抵抗の種類、接続場所を種々変えて、その効果を確かめた。
抵抗5に、モノリスキャピラリーチューブMonoCap(登録商標)内径0.2mm、長さ1.5cm(容量0.6μLスルーポア2μm)を接続した結果、圧力49MPaになり、図8(3)と同じく異性体が分離した。
【0072】
抵抗5に、内径0.05mm溶融シリカキャピラリーチューブ長さ40cmを接続し、セルの後に抵抗6としてInertSustainC18HPLCカラム(USPコード L1 オクタデシル基結合シリカゲル 2μm ジーエルサイエンス社製)内径2.1mm、長さ5cmを取り付けた。カラム入口圧は、49MPaとなり、図8(3)と同じく異性体が分離した。
【0073】
抵抗6に用いるカラムは、検出後であり分離に影響しないので、分離が悪くなった使い古したカラムでも良く経済的である。また、このシステムの場合、セルに掛かる圧力は、30MPaであり高耐圧の市販セルでも使用できるので、便利である。また、HPLCカラムは、キャピラリーチューブより詰まりにくく、抵抗変動が生じにくいためより有用である。
【0074】
抵抗5に内径0.03mm溶融シリカキャピラリーチューブ長さ5cmを接続し、抵抗6に、6方ロータリーバルブを5種類の抵抗を設けて接続した。ロータリーバルブを回すと段階的に抵抗を切換することができる。ロータリーバルブ7の出口ポート9には抵抗をつけず、出口ポート10に内径0.065mm PEEKチューブ30、長さ3mを取り付け、出口ポート11に内径0.05mm溶融シリカキャピラリーチューブ31長さ1.2mを取り付け、出口ポート12に内径0.03mm溶融シリカキャピラリーチューブ32長さ15cmを取り付け、出口ポート13に内径0.2mmモノリスキャピラリーチューブ33MonoCap、長さ2cm(スルーポア:1μm)を取り付け、出口ポート14に粒子径2μmHPLCカラム内径2.1mm、長さ15cmカラム34を取り付けた。
【0075】
ロータリーバルブ7を回してポート10に設定した場合には、カラム入口圧力は、13MPaとなり、図8(2)と同じ分離が得られた。回してポート11〜14に設定した場合には、カラム入口圧力は49MPaとなり、図8(3)と同じ分離が得られた。どのポートに回しても、異性体の分離に適用できる事が確認された。さらに、ポート10〜14に回して、圧力変動はほとんどなく、取り付ける抵抗を変える事で、自由に圧力を変更できることも確認できた。
【0076】
今回の検討で、抵抗管が詰まる事はなかったが、バルブシールによる汚れが出て来ることが考えられるので、詰まりにくいカラムやなるべく内径の太い抵抗が推奨される。
【0077】
抵抗5には図3に示すように抵抗を接続せず、抵抗6に6方切換バルブ7を接続し、図6に示すように抵抗管18、19を組み入れた。バルブを切り換えることにより、段階的に抵抗を変えることができる。抵抗として、内径0.05mm溶融シリカキャピラリーチューブ18長さ40cmと内径0.03mm溶融シリカキャピラリーチューブ長さ25cmを組み込み、切り換えたところ、それぞれ、カラム入口圧力が、13MPa、49MPaとなり、それぞれ、図8(2)、図8(3)と同様の分離が得られた。切換バルブの容量は、10μL以下と小さく、遅れ時間は、1秒程度であり、検出器セル前にも使用できる。
【0078】
抵抗5には、抵抗を接続せず、抵抗6にレギュレータを接続した。レギュレータは、図7に示すような構造で圧縮ばね23の荷重と出口側圧力による力の平衡を利用し、ピストンシール22の働きによりピストン21を移動させて液体が流通する空間容量を変化させるにより抵抗圧力を調整する事ができる。開放状態では、抵抗が掛からず、図8(1)と同じ分離状態であったが、圧力調整ねじ24を回して調整することにより13MPaにすると、図8(2)のように分離が見られ、さらに絞って調整すると、図8(3)のように異性体が分離した。
【0079】
圧力調整ねじ24を自動で機械的に調整すれば、圧力を連続的に可変できる事になる。その場合、10MPa以上の圧力にカラム入口圧がなれば、異性体分離効果が発揮されるので、実際には、10MPa以上になり、かつデッドボリュームの少ない抵抗管を前段に接続し、その後に、レギュレータを接続する事が推奨される。また、圧力変動も少なくシステム安定が早くなる。
【0080】
このように本発明においては、基本的には、10MPa以上の圧力をカラム入口に掛けられれば、手段は多種のものが利用でき、その抵抗の数や接続位置は限定されない。
【実施例2】
【0081】
実施例1と同じ試料であるトコフェロール異性体を用いて、Inertsil(登録商標)C30内径4.6mm、長さ250mmのHPLC充填カラムを用いて、単純な溶離液であるメタノール100%を用いて、従来から言われている温度効果と本発明である圧力効果の比較をおこなった。実施例1にあるように、図9(1)のように通常の条件では、βとγトコフェロール異性体は完全分離しない。しかし、カラム温度を下げる事により、図9(3)に示すように分離された。20℃で異性体の分離は達成されている。
【0082】
しかし、オーブン温度を20℃に設定し、モニター温度が設定値になったのは約30分後であった。そこで実際に分析を行ったが、ピーク保持時間は安定せず、3回目の分析から安定したデータが取れ始めた。オーブン温度が安定してから、約30分後にやっと保持時間が安定したことになり、オーブン温度設定からだと、1時間程度の平衡化時間が必要になることがわかった。当然、冷却には膨大なエネルギーが使われる事になる。
【0083】
同じカラム、同じ溶離液、同じ試料で本願発明の方法を実施した。
カラム温度は、30℃一定とし、カラムの後に、内径0.03mm、長さ28cmの溶融シリカキャピラリーチューブ(容量0.2μL)を抵抗として接続した。カラム入口圧力は57.9MPaとなり、20分程度で安定し、最初の分析から図10(1)のような安定したデータが得られた。さらに、その後に抵抗として、内径0.03mm、長さ10cmの溶融シリカキャピラリーチューブを接続した。カラム入口圧力は79MPaとなった。抵抗管を繋ぐジョイント部分の容量を入れても全容量は1μL以下であり、図10(2)のように完全分離したデータが得られた。
安定時間も、20分以内であり、圧力を掛けることによる異性体分離は従来方法よりも簡便で早く安定する事が確認された。
【実施例3】
【0084】
実施例1と同じ方法を、標準試料ではなく、実試料市販サプリメントのHPLC分析に適用した。
市販トコトリエノールサプリメント1粒をカッターで割り中身を10.5mg量り取り、ヘキサン/イソプロパノール=1:1 1mLで溶解しHPLC用試料とした。
Inertsil(登録商標)C30 内径4.6mm、長さ250mmのHPLC充填カラムを用いて、メタノール100%を流速0.5mL/min、カラム温度30度、検出295nmで分析して、従来法と本発明方法と比較してその効果を確かめた。
従来方法では 圧力3.1MPaで、異性体である 2)ガンマトコトリエノールと 3)ベータトコトリエノールは分離していない。(図11上)
本発明方法では破損防止のため、内径0.4mmのピークチューブを保護チューブとして被せた内径0.1mm 長さ25cmの溶融シリカキャピラリーを、抵抗管として、SUS 1/16 インチフェラルでカラムの後と検出器の間に接続し、その他は従来法と同条件で分析した。
カラム入口圧は、63.3MPaとなり図11下のように1)デルタトコトリエノール、2)ガンマトコトリエノール、 3)ベータトコトリエノール、4)アルファートコトリエノールという異性体4成分がすべて分離し、4成分がこのサプリメントに含まれていることがわかった。サプリメントからの抽出物という実試料分析にも、本発明による異性体分離が適用できることが確認された。
【実施例4】
【0085】
実施例1と同じ条件で脂肪酸メチルエステルである1.γ‐Methyl(z,z,z)‐6,9,12‐octadecatrienoateと2.α‐Methyl(z,z,z)‐9,12,15‐octadecatrienoateの異性体の分析を行った。
【0086】
使用し易く、置換が早い100%メタノール溶離液を用いて、流速0.5mL/minでInertsil(登録商標)C30内径4.6mm長さ250mmとInertsil(登録商標)ODS−P内径3.0mm、長さ200mmの2種類のカラムで本願発明方法を実施した。カラムの出口流路に高耐圧セルを接続し、その後に抵抗としてレギュレータを接続し、背圧を可変しながら実験を行った。
【0087】
Inertsil(登録商標)C30、内径4.6mm、長さ250mmにおいて、まず、背圧は掛けずに、分析を行ったところ、圧力7.4MPaでは、ほとんど分離できなかった(図12(1))。レギュレータのつまみを回して、カラム入口圧力を56.3MPaに調整すると、2成分の溶出時間が変化し、分離が見られた。(図12(2))完全分離ではないが、圧力が分離に効果的に作用していることが確認された(ピーク1:γ‐Methyl(z,z,z)‐6,9,12‐octadecatrienoate、ピーク2:α‐Methyl(z,z,z)‐9,12,15‐octadecatrienoate)。
【0088】
Inertsil(登録商標)ODS−P、内径3.0mm、長さ200mmにおいても、同様な事を行った。圧力を掛けない場合では、7.4MPaでほとんど分離せず(図12(1))、57.3MPaに調整すると、2成分の溶出時間が変化し、完全にベースライン分離となった(図12(2))。
【0089】
セルの前に内径0.03mm、長さ25cmの溶融シリカキャピラリーチューブを接続しても同じ効果が得られた。カラムの種類によっては大小はあるが、異性体の分離を変化させることにおいて圧力が効果的に働くことが確認された。
【実施例5】
【0090】
実施例1に示す本発明の方法及び装置を分取に適用した例を以下に示す。
Inertsil(登録商標)ODS−P(USPコード L1 オクタデシル基結合シリカゲル 5μm ジーエルサイエンス社製)内径20mm、長さ250mmの分取カラムを用いて、単純な溶離液である70%アセトニトリル水を流速10mL/minで送液し、キシレン異性体1.o−キシレン、2.m−キシレン、3.p−キシレンの分取を試みた。分離カラムの出口流路に内径0.13mm、長さ2mのコイル状に巻いたPEEKチューブを抵抗として接続し、分取を行った。分離カラム入口圧力は65MPaであった。抵抗管の容量は、0.03mLとなるが、流速が早いため、実際のピーク遅れ時間としては0.2秒以下でまったく影響しない。
【0091】
ODS‐Pにおいて、溶離液にβ‐シクロデキシトリンの添加をすることなく、単純な70%アセトニトリル水溶離液でキシレン異性体の分取が可能であった(図13)。
10分〜11.5分を第1分画(4)、11.6分〜12.8分を第2分画(5)12.8分〜13分を第3分画(6)として、各分画部をガスクロマトグラフィーを用いて純度チェックを行ったところ、第1分画(4)で、純度100%のo‐キシレンが99%の回収で得られ、第3分画(6)で純度98%p‐キシレンが70%回収率で得られ、第2分画(5)で、純度70%m‐キシレンが90%の回収率で得られ、目的成分が分取できる事が分かった。
従来の手法では、β‐シクロデキストリンが溶離液に含まれるため、分取後さらに取り除くことが必要となったが、本発明では添加成分のない単純な溶離液で行えるので、そのまま溶媒のみ蒸発させる事で濃縮または乾固が簡単に行えるので精製にも非常に適していることが判明した。
【0092】
自動でつまみ24を回すレギュレータ25を抵抗として用いて、50MPaから10MPaへ圧力を傾斜可変する圧力グラジエントを行い異性体を分取することも可能であった。流量が早いので、カラムと検出器セル間にレギュレータ25を設けても、デッドボリュームの影響はなく、異性体を分取することが可能となった。図7にレギュレータの一例を示す。概略、ボディー20にピストン21をピストンシール22を介して圧縮ばね23により流路を遮蔽する構造である。
【実施例6】
【0093】
実施例1に示す装置及び方法によりInertsil(登録商標)C30内径4.6mm、長さ250mm及びInertsil(登録商標)ODS‐P内径3mm、長さ200mmの分析カラムを用いて、単純な溶離液である50%アセトニトリル−水、20℃の一定温度で1.α‐エストラジオールと2.β‐エストラジオール異性体の分離を試みた。Inertsil(登録商標)C30、内径4.6mm、長さ250mmは、流速0.35mL/minとした。抵抗を接続していない従来の分析では圧力4.2MPaであり、異性体のピーク1,2は分離していた(図14(1))。
【0094】
抵抗として、内径0.03mm、長さ25cmの溶融シリカキャピラリーチューブをカラム出口に接続し、カラム圧力を71MPaとして分析した結果、分離せずに1本のピークとして溶出した(図14(2))。
【0095】
C30カラムでは、固定相となる官能基が高密度に存在するため、その固定相を加圧することで、より平面的なβ‐エストラジオールが、高密度な固定相の中に入り込みやすく、大きく溶出が遅れると考えられる。一方、α‐エストラジオールはβ一体に比べると分子の形が立体的であり、影響があまり顕著ではないため、結果的として71MPaでは分離しなくなっているが、異性体間の分離を変化させるために圧力が効果的であることは確認された。
【0096】
Inertsil(登録商標)ODS‐P内径3mm、長さ200mmの場合は、流速0.13mL/minとした。抵抗を接続しない従来の分析では圧力3.4MPaであり、2のβーエストラジオールが先に溶出している(図15(1))。抵抗として、内径0.03mm、長さ66cmの溶融シリカキャピラリーチューブをカラム出口に接続し、カラム圧力を71MPaとして分析した結果、逆にα―エストラジオールが先に溶出した(図15(2))。
【0097】
ODS‐Pでも、より平面的なβ‐エストラジオールはより強く保持され、溶出時間が遅くなり、3.4MPa時と比べてピークの溶出が逆転している。これらのことにより、圧力調整することで、分離を大きく変えることが可能であり、従来、溶離液変更で行なっていた分離の調製が、抵抗を接続し圧力を変えるだけで簡単にできることがわかった。
【実施例7】
【0098】
実施例1に示す装置及び方法により、Inertsil(登録商標)ODS‐P内径3mm、長さ200mmのカラムを用いて、イオン性の親水基を持った異性体化合物の分離に適用した。末端にカルボニル基を持った脂肪酸の異性体である、
1.Cis‐vaccenic acid(11Z‐Octadecenoic Acid)
2.Petroselinic acid(cis‐6‐Octadecenoic Acid)
3.Elaidic acid(trans‐9‐Octadecenoic Acid)
を試料とし、溶離液として、97.5%メタノール,2.5%10mMリン酸(H2O)混合移動相を用い、流速0.4mL/minで効果を検証した。
【0099】
抵抗を接続していない通常分析では、カラム入口圧は10MPa以下である3.2MPaとなり脂肪酸異性体分離していない(図16(1))。それに内径0.03mm、長さ15cmの溶融シリカキャピラリーチューブを抵抗としてカラム出口に接続すると、カラム入口圧は10MPa以上の40.2MPaとなり、異性体が分離した(図16(2))。
【0100】
イオン性の異性体の分離に於いても本発明の方法は効果がある事が確認された。なお、当然のことながら、溶離液としてバッファーを含んだ場合でも効果が得られることも確認された。
【0101】
以上から、従来の分析状態に、カラム入口圧が10MPa以上になるように、抵抗を加えるだけで、異性体の溶出挙動を変化させ、分離を変化させることができることがわかった。
【実施例8】
【0102】
実施例1に示す装置及び方法により、実施例2のトコフェロール異性体(1.σ‐tocopherol、2.γ‐tocopherol、3.β‐tocopherol、4.α‐tocopherol)を試料とし、異なるタイプの固定相を持つ充填カラムで分離を実施した。
【0103】
球状シリカゲルにオクタデシル基を結合させた、所謂ODSカラムの中で、Inertsil(登録商標)ODS‐3(USPコード L1 オクタデシル基結合シリカゲル 炭素量15% 5μm ジーエルサイエンス社製)内径3mm長さ100mm、Inertsil(登録商標)ODS‐EP(USPコード L1 オクタデシル基結合シリカゲル エンベット型 炭素量9% 5μm ジーエルサイエンス社製)内径3mm長さ100mm、Inertsil(登録商標)ODS‐P(USPコード L1 オクタデシル基結合シリカゲル 炭素量29% 5μm ジーエルサイエンス社製)内径3mm長さ200mmの3種類のカラムを用い、100%メタノール溶離液で流速0.2mL/minとし、抵抗として内径0.03mm長さ60cmの溶融シリカキャピラリーチューブをカラム出口に接続し、圧力効果を検証した。
【0104】
ODS‐3およびODS‐EPでは、圧力の増大により保持時間の増加はあるが、異性体間分離の変化は見られず、β体とγ体は分離しなかった(図17、図18)。
【0105】
それに対して、ODS‐Pでは、異性体化合物の溶出が変化し分離してきている(図19)。圧力効果の少ないODS‐3、ODS‐EPはそれぞれ、オクタデシル基の結合基密度が、1.3μmol/m2、1.7μmol/m2であり、圧力効果の高いODS‐Pでは、2.3μmol/m2である。ちなみに実施例2で使用したC30では、化学結合基の結合基密度は2.5mol/m2であり、異性体分離における圧力効果は、2mol/m2以上の高密度の固定相に有効であることがわかる。
【0106】
Inertsil(登録商標)ODS‐3 1.3μmol/m2、ODS‐EP 1.7μmol/m2、にもタイプ1と同様の圧力効果が働き、保持の増大だけが起こっているが、異性体化合物間の分離にめざましい変化はおきていない。異性体化合物は、結合基が同じでその配置が異なるだけであり、タイプ1〜4の効果による分離はあまり期待できない。
【0107】
C30、ODS‐Pにおいては、結合配置が異なり、分子の立体構造が異なる異性体化合物間の溶出が変化している事から、タイプ1の効果に加えて、充填剤として多層に重なり(ポリメリック結合)高密度の固定相の立体選択性効果が働いている事が解った。さらに、圧力を加えると、立体選択効果が大きく表れ分離が飛躍的に変化するものと思われる。
【0108】
なお、これらの充填カラムは一般に市販されているため簡単に入手でき、特殊な固定相を選択する必要が無く、異性体分離に適用できる。
【0109】
しかしながら、市販充填カラムを使用しなくても下記のような合成を行えば同様の固定相を作成できることは言うまでもない。具体的合成方法は以下のようである。表面積450m2/m2、細孔径10nm、粒子径5μmのシリカゲルに5%のオクタデシルトリクロロシランをトルエンに溶かした溶液中で、10時間以上還流反応を行い、市販のInertsil ODS‐EPと同様のオクタデシル基の結合基密度が、2μmol/m2以上の固定相が得られた(結合基密度2.1μmol/m2)。
【0110】
また、同じゲルに10%安息香酸トリアコンチル安息香酸トルエン溶液を塗布後、窒素中、120℃で減圧除去した結果、市販のInertsil C30と同様の結合基密度2.2μmol/m2の固定相が得られた。
【0111】
これらの固定相でも圧力増加による異性体間における分離の変化効果が得られており、合成方法や用いる担体はどのような物でも良いが、結合基密度が2μmol/m2以上になると、異性体間の分離変化効果が高くなることが確かめられた。
【実施例9】
【0112】
これまでの実施例から、10MPa以上の圧力がHPLCカラムに掛かる事が異性体分離に有効であり、具体的にはカラムの後に抵抗を取り付け、さらに変化させることで実現できることが確認された。
【0113】
一方、従来の溶離液割合を変化させるグラジエント分析においては、溶離液割合の変化とともにカラム圧力も変化する事が知られている。典型的な逆相分配カラムを用いたグラジエント分析では、有機溶媒量を増加させることにより早期の溶出を目的とするため、圧力は減少する変化が生じる。分析開始時の圧力が10MPa以上であってもグラジエント分析が進むと有機溶媒濃度が増え、溶離液の粘性が下がり最終的な分析圧力は5MPaに下がってしまう。これでは異性体間の分離には適用できない。
【0114】
そこで、カラムの後に抵抗管を付け10MPa以上の状態にし、異性体間の分離に適用できるか検証を行った。
試料には、1)シス11−オクタデシルメチルエステル、2)シス6−オクタデシルメチルエステル を用い、実験条件は以下のように設定してHPLC分析を行った。
HPLC分析カラム:Inertsil(登録商標)ODS‐P 3μm 内径3mm 長さ100mm
溶離液A:10mM リン酸水溶液
溶離液B:メタノール
流速:0.2mL/min
グラジエント:A/B 16/84 (初期) →15分リニアグラジエント→ 1/99 →30分までホールド→その後初期状態へ
検出波長:UV205nm
カラム温度19℃の場合、圧力は8.8MPa−5MPaに下がり、図21Aのクロマトグラムが得られた。内径0.4mmのピークチューブを保護チューブとして被せた内径0.1mm 長さ25cmの溶融シリカキャピラリーを、抵抗管として、SUS 1/16 インチフェラルでカラムの後と検出器の間に接続し、同じ条件で分析した結果が図21Bのクロマトグラムである。圧力は、62.4MPa−39.5MPaまで変化したが、それでも10MPa以上であり、ピークも高くなりより異性体は分離した。この結果より、グラジント時の溶媒変化による圧力変化も本発明の効果がある事が確認された。
【0115】
抵抗管を変えなくても、グラジエントの溶離液変化だけで、62.4MPa−39.5MPaまで変化でき、異性体分離状態も調整できた。本実施例では、水―メタノール系であるので、2倍弱の変化であるが、30%エタノール(10℃粘性4)−酢酸エチル(10℃粘性0.5)であれば、8倍程度の圧力変化が可能になるので、一番低い時に10MPa以上になるようにすれば、異性体分離には有効となる。
【0116】
また、HPLCにおいて、温度を上げると固定相内での溶質成分の移動速度は速くなるので、溶出が早くなりピーク形状が良くなる事は知られている。
そこで、本発明状態でカラム温度を変化させて分析した。
【0117】
20℃では、56.2‐35.8MPaまで、25℃では50.4‐32.0MPaまで圧力は変化し、図21C、Dのクロマトグラムが得られた。温度が上がるほど圧力は下がり、1と2の溶出は近づき異性体として分離能は悪くなる。しかし、それでもグラジエント終了時で10MPa以上を保持しており、これらの異性体は分離されている事が確認された。例えば、30%エタノールの場合、カラム温度で80℃粘度0.6℃粘度7であり、温度変化をさせると10倍近い圧力変化を起こす事ができる。
【0118】
この結果より、分析温度の調整は、10MPa以上の圧力を保持できれば、異性体の分離を保持しながら、ピーク形状を変化させる事も可能である事が明らかとなった。
従って、グラジエントに伴う溶媒割合変化と、カラム温度変化によって10倍弱の圧力変化が可能で、異性体分離を変化させる事ができ、さらに両方を組み合わせて変更する事で、10MPa〜100MPaまでの圧力変化も可能になることが確認された。
【実施例10】
【0119】
従来から圧力変化に応じて溶質の相比が変化し、保持時間が変化する現象は報告されているが、化合物の異性体間でその保持が変化し、異性体間の分離に効果があると言う報告はこれまで無かった。本発明に係るこの特性を確かめるために、実施例データをまとめて、どのような現象が起きているかを確認した。
【0120】
保持は、溶質(Solute)が固定相にどのくらい留まるかによって生じるので、圧力上昇に伴う保持比の変化から、固定相内に占める溶質容積変化量△Vが下記式より得られる。
△V=−気体定数×T(K)×ln(本発明を行った時の保持比/従来分析の場合の保持比)/本発明の実施圧力
△V1を溶質1の溶質容積変化量、△V2を溶質2の溶質容積変化量とすると、溶質1、溶質2の異性体化合物間の変化量の比である△△V値は、相比の影響を受けない数値となる。
【0121】
2種類のHPLC分析カラムについて分析した結果を下記の表にまとめた。溶質の構造の差に対応して、圧力を加える事で、固定相への取り込みが生じて、固定相内で体積変化が起き、異性体間の分離している事が判る。
【0122】
【表1】

【0123】
例えば、Inertsil(登録商標)ODS‐Pのカラムを用いる、異性体であるα-/γ-linolenic acid methyl esterの温度303K(20℃)の場合(表中の1行目)を例にとると、従来分析でのα-linolenic acid methyl esterの保持比は1.00、本発明の圧力50MPa掛けた場合の保持比は1.82、となり、上記の計算式により、△V1は、−30.2(−8.31x303xIn(1.82/1.00)/50)となる。
【0124】
その異性体である γ-linolenic acid methyl esterの保持比は1.12、本発明の圧力50MPa掛けた場合の保持比は2.45、となり、上記の計算式により△V2は、−39.4となる。両異性体間のその差△△Vは、端数処理をして−9.3となる。
【0125】
同様の方法で計算を行うと、異性体化合物毎に△△Vが得られる。この差の絶対値が大きいほど、より本発明の効果が期待できる異性体成分であると考えられる。
Inertsil(登録商標)C30カラムを使った場合でも、同様の方法で各化合物毎に△△Vが得られた。
【0126】
固定相の種類によって△△V値は異なり、今回の結果では、C30とODS‐Pについて同等の△△V値が得られる場合と、 △△V値(ODS‐P) > △△V値(C30)の場合があった。 表中2行目のm-/p-xylene や表中6行目β-/α-estradiolでは、ほぼ同じ値が、β-/γ-tocopherolではほぼ同じ絶対値が得られている。
【0127】
溶出順が固定相によって異なるため+―の違いがある場合もあるが、圧力変化に伴う固定相内での溶質の保持変化量はほぼ同じで、その異性体間での溶出変化効果はほぼ同じと考えられる。
【0128】
一方、表中1,3,4行目の化合物では、ODS‐Pの△△V値の絶対値がC30の △△V値の絶対値より大きくなる。
【0129】
表中2,6行目の化合物は、炭化水素鎖が主骨格となり剛的なサイトを持った溶質であり、表中1,3,4行目の化合物はエステル鎖を持っており柔軟なサイトの溶質と考えられる。
すなわち、C30の識別部位は剛的であり、ODS‐Pの認識部位は剛的なサイトと柔軟なサイトが存在するものと考えられる。
【0130】
以上のように、圧力効果の大きさを測る指標として△△V値の使用が示唆された。そして、この値を使用することで圧力効果により溶質の溶け込みに差が生じ、異性体間の分離が変化する事が明確になった。さらに、液相種によって異性体間の認識部位が異なり、化合物の構造も認識している事が推定できた。
【技術分野】
【0001】
本発明は、液体クロマトグラフィーにおける異性体化合物の処理、特にその分離及び分取に関するものである。
【背景技術】
【0002】
クロマトグラフィーは、化合物の官能基の種類や大きさの違いによる吸着力・電荷・疎水性の差を利用して、成分分離に広く使われている手法である。しかし、分子量と官能基の種類が同一、つまり分子式が同一ではあるが、その分子構造が異なる化合物、所謂異性体化合物間の分離においては、吸着力・電荷・疎水性の差が小さいため、これらの化学的な相互作用の大きな差が期待できない。その目的ではカラムの基本的な分離性能が非常に高い、20万段以上の理論段数が得られるキャピラリーガスクロマトグラフィーが期待されるが、熱分解成分や高沸点化合物には適用できないので、分析の前に誘導体化するなどの手間のかかる手法が取られる。
【0003】
一方、前処理の手間が比較的かからない液体クロマトグラフィーではどうかというと、有機溶媒と水の割合を変える単純な溶離液の変更だけでは異性体化合物間の分離はできないことが多い。そのため、異性体化合物の認識能が高いシクロデキストリンなどの高分子化合物を溶離液に添加したり、これらの化合物を固定相としたLCカラムを用いたりするなどの種々の工夫を行う必要が出てくる。
特殊な溶離液への変更はベースラインの安定に時間を要し、場合によっては装置の接液部にダメージを与えることも考えられる。
【0004】
カラム温度を15℃以下に下げ、低温分析する手法も提案されているが、高価な冷却用オーブンが必要で、さらに、冷却するには多くのエネルギーも必要となる。時期によっては結露による装置へのダメージも考えられ、使いづらさやカラムを均一な温度にするための安定時間などを考慮すると実用に困難を伴う。
【0005】
液体クロマトグラフィーにおいて、保持及び分離が安定する、言い換えると、システム系すべての状態が平衡化するには、かなりの時間が必要となる。特に、異性体化合物分離においては特殊な溶離液を用いたり、分析温度を下げたりするのでより長い時間がかかってしまう。さらに、カラム変更においては、その付け替え時間、カラム内溶媒を溶離液に変化させるための中間溶媒の選択、その溶離液の平衡化ということで多大なる手間と時間がかかる。
【0006】
それに対して、流量及び圧力の変更は、平衡化が速く、液体クロマトグラフィーにおいては有効な手段となり得る。流量の変更は、保持が全体的に早くあるいは遅くなるだけで、個々の成分間の分離は大きく変化しないが、圧力の変更は、分離に様々影響するとの知見が得られてきている。
【0007】
Rogers らは、シリカ固定相、水移動相系で、メチルオレンジとエチルオレンジの保持について、20000psiまでは保持減少、20000psiより高圧になると、保持増加を認めた報告を行っており、後にion−pair RPLCにおいて2410barに昇圧するとメチルオレンジの保持増加が3.2倍になったこと、その原因としてイオンペア系は複雑な平衡系であり、高圧によるイオン対生成の増加が保持の増加をもたらした可能性の考えられることが示唆されている(非特許文献1)。
【0008】
Jorgensonらは、アセトニトリル (ACN)−水(40:60v/v)混合溶液の粘度(0.89cP)が、25℃、3500barで0.16cP/kbar増加することを報告している(非特許文献2)。
【0009】
McGuffinらはC10−C20脂肪酸のメトキシクマリン誘導体が、カラム入口圧力36−360barの増加により9%から24%保持増加したことを報告している(非特許文献3,4)。相互作用として分散力が、エントロピー的な効果と併せて考慮されていて、溶質、移動相、固定相すべてが圧縮されると考えられている。さらに、平面的芳香族(PAH)については保持増加7%、非平面的芳香族については効果は小さいかむしろ減少を報告している。
【0010】
Jorgensonらは2,3‐hydroxynaphthaleneについてオクタデシル(ODS)基結合シリカゲルカラムを用い1000barで12%の保持増加を報告している(非特許文献5)。
【0011】
田中らは、解離可能な溶質(酸、塩基)がそれらのpKa(酸解離定数)付近のpHにおいて溶出されるとき、圧力が溶質や緩衝溶液物質のpKaを変化させ、高圧がイオン化を促進するという報告を行っている。この結果、イオン化制御逆相クロマトグラフィーにおいて、移動相のpHや溶質のイオン化率が圧力によって変化し、弱酸、弱塩基の保持が変化し、分離パターンの変化をもたらす。この場合、圧力が、より大きな体積変化をもたらす種に対する圧力効果が、保持の変化の方向(増加あるいは減少)を支配すると考察している(非特許文献6)。
【0012】
Evansらはシクロデキストリン添加逆相クロマトグラフィー系、あるいはシクロデキストリン結合固定相系において、加圧によりシクロデキストリンへの取り込みが増加し、p‐nitrophenolの保持や、優先的に取り込まれる光学異性体化合物の保持が変化し、分離係数が変化(増加あるいは減少)する場合があることを報告している。このような環状構造ホスト物質による取り込み平衡系における圧力効果は、固定相における圧力効果より大きく、分離度はいずれの場合にも減少すると報告している(非特許文献7,8)。
【0013】
McCalleyらは、50MPa程度の加圧(カラムと検出器の間に30μm キャピラリーを接続)により、疎水性・中性物質について12%程度、極性、高分子物質についてさらに大きな増加、イオン(酸、塩基)性物質について50%以上の保持の増加が認められたと報告している。さらに、固定相による影響(C18がC1より大きな効果)を報告している。高圧による保持の増加は、高圧下で溶質が脱溶媒和し、保持を促進することによりもたらされると結論している。又、タンパク質のような高分子について、はるかに大きな圧力効果(保持の増加)が報告されている。(非特許文献9,10,11,12)
【0014】
以上のように注目されるべき見解を含む種々の発表がされている。しかし、これらの分離カラムの加圧による保持の変化に関する報告の多くは、親水性化合物に関するものである。50MPaの圧力増加に対して疎水性化合物でも、5−24%の保持の増加が認められているが、親水性化合物のように大きな保持の増加を報告しているものは見当たらない。
【0015】
加圧効果に関するこれまでの報告を分類すると、次の4つのタイプに表される。
タイプ1:非極性・疎水性化合物(長鎖アルキル化合物,PAH)の分散相互作用(McGuffin,McCalley):疎水性(平面的)溶質に対する保持の小さな増加(分散力の増加+立体排除)。
タイプ2:pKa付近のpHにおける弱酸,弱塩基のイオン化制御(Tanaka):弱酸、弱塩基について、pH,pKaの変化を通じた保持の変化(増加、減少)(溶媒和の増加(電縮)による高圧におけるイオン解離の促進)
タイプ3:pKaから離れたpHにおいて、イオンや親水性溶質の脱溶媒和(McCalley):親水性溶質やイオンについて、保持の大きな増加(溶質の脱溶媒和に基づいているとも考えられている)。
タイプ4: 環状構造ホストによるInclusion(取り込み)現象(錯体形成の増加)において、ホストの空間に取り込まれ得る親水性溶質について加圧による錯体生成の増加、光学異性体化合物間の分離係数のわずかな変化(増加あるいは減少)。
【先行技術文献】
【非特許文献】
【0016】
【非特許文献1】G.Prukop,L.B.Rogers,Sep.Sci.Technol.,13(1978)59.
【非特許文献2】J.W. Thompson, T.J. Kaiser, J.W. Jorgenson, J. Chromatogr. A 1134 (2006) 201.
【非特許文献3】V.L. McGuffin, S.-H. Chen, Anal. Chem. 69 (1997) 930.
【非特許文献4】V.L. McGuffin, C.E. Evans, J. Microcol. Sep. 3 (1993) 513.
【非特許文献5】J.S. Mellors, J.W. Jorgenson, Anal. Chem. 76 (2004) 5441.
【非特許文献6】N. Tanaka, T. Yoshimura, M. Araki, J. Chromatogr. 406 (1987) 247.
【非特許文献7】L.M. Ponton, S.M. Hoenigman, M. Cai, C.E. Evans, Anal. Chem. 72 (2000) 3581.
【非特許文献8】C.E. Evans, J.A. Davis, Anal. Chim. Acta 397 (1999) 163.
【非特許文献9】M. M. Fallas, U. D. Neue, M. R. Hadley, D. V. McCalley, Journal of Chromatography A, 1209 (2008) 195
【非特許文献10】S.-H. Chen, C.-T. Ho, K.-Y. Hsiao, J.-M. Chen, J. Chromatogr. A 891 (2000) 207.
【非特許文献11】M.A. Stadalius, H.S. Gold, L.R. Snyder, J. Chromatogr. 296 (1984) 31.
【非特許文献12】X. Liu, P. Szabelski, K. Kaczmarski, D. Zhou, G. Guiochon, J. Chromatogr. A 988 (2003) 205.
【発明の概要】
【発明が解決しようとする課題】
【0017】
このような背景があり、異性体化合物の分離においては、安定の早い簡単な溶離液で、分離を達成することが求められている。尚、ここでカラムは分離カラムの意で用いられ、分析カラム、分取カラムである。
【0018】
異性体化合物の分離を実現させるために、異性体各成分の分離を更に言えば異性体各成分ごとの溶質挙動(パターン)を変化させることが重要である。圧力による相互作用としては、タイプ1が普遍的に働き、加えて立体選択性が働くことにより、異性体化合物間の分離を変化させることが期待できる。
【0019】
液体クロマトグラフィーにおいては、流量を大きくするとカラム内の抵抗により、カラム入口圧力を上げることは可能であるが、出口側では大気圧になってしまい、カラム中央では、入口圧力の1/2の増加にとどまる。固定相に対する圧力効果は、入口の一部しか働かない上、カラムの分離性能が下がることが多い。圧力の増加のために温度を下げる方法は、実用的な温度では粘度の増加が大きくないので、圧力を上げる効果が小さい。
【0020】
一方、流速やカラム長さが変わると圧力が変化するが、カラム性能も同時に変化するので分離パターンの変化が、圧力の効果によるものか、他の要素によるものか不明確で安定した圧力の効果が得られない。一定の圧力効果を得るためには、カラム入口側の圧力効果と同じ効果をカラム出口でもたらす必要があり、出口側に入口と同じ背圧を加える必要がある。すなわち、カラム全体の平均的圧力が、通常の分析時の2倍以上になるように背圧を加えればその効果が最も明確に得られることになる。
【0021】
例えば、良く用いられる5μm粒子が充填されたカラムの場合、100%アセトニリルを溶離液として、線速度1mm/secで流した場合、分析圧力は、1MPa〜5MPaになる。出口側でも同じ圧力効果が働くように背圧を加えると、入口圧力は2倍の2MPa〜10MPaとなる。
【課題を解決するための手段】
【0022】
上記課題を達成するための手段としては下記の通りである。
その一として、液体クロマトグラフィーに於いて使用するカラムの出口流路に抵抗を設け、該抵抗の作動によりカラム入口圧力を10MPa〜100MPaに調整し異性体化合物を成分ごとに溶質挙動を変えることを特徴とする異性体化合物の処理方法である。
【0023】
その一として、溶質挙動の変化は溶質の分離であることを特徴とする異性体化合物の処理方法である。
【0024】
その一として、溶質挙動の変化は溶質出現順序の変化であることを特徴とする異性体化合物の処理方法である。
【0025】
その一として、溶質挙動の変化は溶質の合体であることを特徴とする異性体化合物の処理方法である。
【0026】
その一として、前記カラム入口圧力を100MPa〜10MPaの間で連続的又は段階的に下げながら異性体化合物の溶質挙動を変化させることを特徴とする異性体化合物処理方法である。
【0027】
その一として、溶離液の組成を変化させることで、前記カラム入口圧力を100MPa〜10MPaの間で連続的又は段階的に変化させ異性体化合物の溶質挙動を変化させることを特徴とする異性体化合物の処理方法である。
【0028】
その一として、カラム温度を変化させることで、前記カラム入口圧力を100MPa〜10MPaの間で変化させ、異性体化合物の溶質挙動を変化させることを特徴とする異性体化合物の処理方法である。
【0029】
その一として、前記カラムが分析カラムであることを特徴とする異性体化合物の分析方法である。
【0030】
その一として、前記カラムが分取カラムであることを特徴とする異性体化合物の分取方法である。
【0031】
その一として、異性体化合物を処理する装置であって、カラム出口流路に於いて、カラム出口から検出器までの間または検出器から排出の間またはその両方に抵抗を接続し、カラム入口圧力を所定の圧力に調整自在としたことを特徴とする異性体化合物の処理装置である。
【0032】
その一として、前記カラムに分析カラムを使用した異性体化合物分析装置である。
【0033】
その一として、前記カラムに分取カラムを使用した異性体化合物分取装置である。
【0034】
その一として、前記抵抗が抵抗管であることを特徴とする異性体化合物の処理装置である。
【0035】
その一として、前記抵抗管はチューブ、モノリスカラム、充填カラムのうちの一であることを特徴とする異性体化合物の処理装置である。
【0036】
その一として、前記抵抗が、液体が流通する空間容量を変化できるレギュレータであることを特徴とする異性体化合物の処理装置である。
【0037】
その一として、上記の何れかに記載の異性体化合物の処理装置であって、前記カラムとして分析カラムを使用したことを特徴とする異性体化合物の分析装置である。
【0038】
その一として、上記の何れかに記載の異性体化合物の処理装置であって、前記カラムとして分取カラムを使用したことを特徴とする異性体化合物の分取装置である。
【0039】
その一として、前記カラム出口流路側にバルブを設け、該バルブに複数の抵抗を接続し、接続する抵抗の選択により、所定のカラム入口圧力を得ることを特徴とする異性体化合物の処理装置である。
【0040】
その一として、10MPa以上の耐圧のある粒子状担体又はモノリス担体に固定相を2μmol/m2以上の密度に塗布又は化学結合させた充填剤を用いた異性体化合物分離カラムである。
【0041】
その一として、10MPa以上の耐圧のある粒子状担体又はモノリス担体に固定相を2μmol/m2以上の密度に塗布又は化学結合させた異性体化合物分離カラム用充填剤である。
【発明の効果】
【0042】
カラム出口から検出器までの間または検出器から排出の間またはその両方に、抵抗を接続し、分析圧力を10MPa以上にすることで、異性体化合物溶出の変化、例えば分離、分離順序の変更、合体等の変化をさせることが可能となった。分析圧力の変更では、平衡時間は短く、従来のような溶離液や温度を変えた場合の30分以上の平衡化待ち時間を無くすことができる。
【0043】
又、圧力調整は、従来から市販されている種々の方法が使用でき、簡単に実現可能である。
【0044】
又、単純な溶離液で、室温でも異性体化合物分離が可能となるので、従来多量の溶離液を用いて、温調が難しかった分取が簡単にできるようになった。
【図面の簡単な説明】
【0045】
【図1】本発明一実施例概略説明図
【図2】本発明−実施例対象異性体化合物トコフェロール図
【図3】本発明一実施例概略説明図
【図4】本発明一実施例概略説明図
【図5】本発明一実施例ロータリーバルブ図
【図6】本発明一実施例バルブ切換図
【図7】本発明一実施例レギュレータ図
【図8】本発明一実施例クロマトグラム
【図9】本発明一実施例クロマトグラム
【図10】本発明一実施例クロマトグラム
【図11】本発明一実施例クロマトグラム
【図12】本発明一実施例クロマトグラム
【図13】本発明一実施例クロマトグラム
【図14】本発明一実施例クロマトグラム
【図15】本発明一実施例クロマトグラム
【図16】本発明一実施例クロマトグラム
【図17】本発明一実施例クロマトグラム
【図18】本発明一実施例クロマトグラム
【図19】本発明一実施例クロマトグラム
【図20】本発明一実施例クロマトグラム
【図21】本発明一実施例クロマトグラム
【発明を実施するための形態】
【0046】
一般的に二酸化炭素の溶解において、その溶解度は、圧力に対して10MPa程度までは、大きく上昇し、10MPa以上では変化が少なく15MPaでほぼ一定となると言われている。
HPLCにおける試料成分の固定相への溶解度もほぼ同等の傾向を示すと考えられ、保持の早い安定を考えると、圧力における溶解度の変化が小さくなる10MPa以上が理想と考えられる。本願発明の実施例においても、10MPa以上で効果が得られることが実証されている。
【0047】
装置やカラムが許すならば、圧力が高い方が、カラム内の圧力勾配の影響が、システム全体に影響しないので、安定が早くなる。背圧を加えてシステム圧力を100MPaまで上げると、カラム部分の圧力影響は5%以下になり、カラムの種類やカラムサイズによる圧力変化影響もほとんど無くなる。従って、10MPa以上ならば異性体化合物の処理が可能であり、上限圧力は装置耐圧に依存される。
現在市販されている最も耐圧の高いHPLC装置は、耐圧150MPaであり、そのカラム部分の圧力影響は3%以下となるため、より安定なデータが得られることが期待される事になる。しかし、実際には溶離液を送り出す送液ポンプのプランジャーや試料導入を行うインジェクターなどの接液部には樹脂性のシール材が使用されており、150MPaでは磨耗が早く長時間の安定した送液ができない。従って、圧力調整の実用における上限は、100MPaと考えるのが適当である。
【0048】
異性体化合物の分離を再現良く変化させるすなわち、化合物間の分離をコントロールするには、カラム入口圧力を10MPa〜100MPa内になるように、カラム出口側即ちカラム出口流路に抵抗を接続し、調整することが非常に有用である。
【0049】
その場合、カラム出口側と検出器又は検出器セル間での抵抗増加でも異性体化合物分離は達成できるが、その部分でのデッドボリュームが生じるのでピーク形状が悪くなる懸念があり、検出器セルの後に抵抗を付けることが理想的である。
【0050】
また検出器セルそのものを抵抗として使用することも可能で本発明の効果が期待できる10MPa以上の耐圧セルならば何でも良いが、具体的には下記セルが使用できる。
検出器セルとしては一般的に石英やガラスが使用されることが多いが、そのままでは耐圧性が無いため、テフロン(登録商標)、ポリエチレン、ポリプロピレン、ポリエーテルエーテルケトン(以後PEEKと略す)などの検出に用いる光を透過する樹脂をコートした石英やガラス製セルなどが50MPa程度の耐圧が得られるので適している。また内径1mm未満の溶融シリカキャピラリーセルを用いると100MPa程度までの耐圧が得られ、そのままで本発明の異性体化合物分離を実現できる。
【0051】
しかしながら、キャピラリーの場合では内径が1mm未満であるため、用いることのできる流速が1mL/min程度に限定されてしまうという限界がある。より高流速を用いる分取を考えると、50MPa以上の背圧に耐えるためにはステンレスなどの金属製セルが好ましい。検出器セルに高圧が掛かると、数μmオーダーの表面の傷にも溶質が入り込み吸着原因になってしまう。物理的に研磨する方法は種々あるが、細かい検出器セルの機械的な内面加工には限界がある。そこで、テトラエトキシシラン、テトラメトキシシラン、シクロシロキサンなどのケイ酸化合物やポリシラザンなどの反応性試薬による化学処理によって、ガラス表面を形成させたセルを用いることが良い。
【0052】
カラム出口流路側に抵抗を接続し、圧力制御する方法としては、10MPa以上の圧力がカラム入口に掛かれば良く、特に規定するものではないが、具体的には下記のような方法が考えられる。
【0053】
内径0.15mm以下の中空抵抗管、好ましくは接液面がなめらかである溶融石英キャピラリーチューブを接続する方法が簡便で適している。
物理的な振動による破損を防ぐため、PEEKなどの樹脂チューブで、接続部または抵抗管全体を保護する事が有効である。
さらに、より短い長さでより強い抵抗を得るためには、100μm以下例えば50μmの貫通するスルーポアを持ち、かつ骨格が3次元的に繋がった一体型の所謂モノリス体をチューブ内に形成したモノリス抵抗管が好ましい。
【0054】
それらは、比較的デッドボリュームが小さいので、カラムと検出器又は検出器セルの間に設けても、十分使用できる。これら単独でも十分使用できるが、さらに、抵抗を接続しても良い。
【0055】
カラムと検出器又は検出器セル間で一定の抵抗を接続することで、すぐに圧力が10MPa以上で安定し、異性体化合物分離が安定して行える。さらに後に変化可能な異なる抵抗を設けることで、圧力を加えて調整できる。
【0056】
たとえば、カラムと検出器セル間にデッドボリュームの影響のないモノリス抵抗管を入れて、効果が得られる10MPa以上の20MPaになるようにする。
そのようなセルの後に40MPaとなる下記のような抵抗を設けると、カラム入口圧力は、20MPa〜60MPaまで調整できる。この場合には、セルには最大で40MPaしか掛らないので、市販されている耐圧40MPaセルを使用すればガラス化などの工夫は必要なく使用できる。
【0057】
検出器又は検出器セルの後での抵抗としては、HPLC充填カラムを抵抗管の代わりに用いることも可能である。さらに、複数の抵抗管をバルブに取り付け、順次流路を切り替えることで、順次圧力を変えることもできる。また、従来から市販されている高耐圧の液体用ニードルバルブも使用できる。ニードルの絞りを変えることで自由に流路抵抗を変化させられるので、自動で圧力を簡単に変えることができる。
【0058】
内径を順次細くした円錐状の抵抗管やモノリスフィルターを用いた抵抗調整など、背圧調整ができれば、従来技術が何でも使用できる。デッドボリュームの影響が考えられる場合には、低デッドボリュームの抵抗管とボリュームのある抵抗を組み合わせることが推奨される。
【0059】
用いるカラムとしては、特に限定される訳ではないが、高密度構造固定相を持ったLC充填タイプカラムやモノリスカラムが異性体化合物分離の変化が大きくなる。この溶出挙動変化としては、分離の拡大、促進、流出順序の変化、変更、合体が挙げられる。
【0060】
オリゴ糖や多糖誘導体やタンパク質などの剛直な構造を固定相とした粒子充填タイプカラムやモノリスカラムなどが、加圧による異性体化合物分離により効果を発揮する。
【0061】
具体的には、C16以上の長鎖アルキル鎖を持つ化合物固定相や平面的な構造を持つ芳香環を持つ固定相などは、高密度構造になり異性体化合物分離の変化が大きくなる。
【0062】
固定相や多孔質体によって異なるが、1〜2μmol/m2の固定相を導入すると1層に並んだ形での単分子層が形成される(モノメリック結合)。1μmol以下だと疎となり固定相としては低密度となる。高密度と言われる固定相では、結合基が多層に重なり(ポリメリック)導入された状態になり、2μmol/m2以上の固定相の場合が多い。
【0063】
担体として、シリカゲル、チタニア、ジルコニアなどの粒子状無機担体、それらに有機物を含む無機-有機のハイブリッド担体、スチレンジビルベンゼンポリマーなどの有機担体、無機モノリス体、無機−有機のハイブリッドモノリス、有機モノリスなどで、固定相を保持できる10MPa以上の担体ならば、どれでも適用できる。
【実施例1】
【0064】
カラム入口の圧力を10MPa以上にする方法として、具体的に下記の方法を実施した。
図1は一般的なLCシステムとしてのHPLCシステムであり、HPLCポンプ1、インジェクター2、カラム3、検出器4から構成される。移動相となる溶離液は、HPLCポンプ1により送り出され、インジェクター2,カラム3,検出器4の順に流れ、廃液される。
【0065】
図1の装置に於いては、カラム3の後に第1抵抗5、または検出器の後に第2抵抗6を設置した。HPLCシステム全体の圧力は、配管インジェクター圧力とカラム圧力と抵抗5圧力と検出器配管圧力と抵抗6圧力の合計値となって表わされる。カラム入口圧力は、システム全体の圧力から配管インジェクター圧力を引いた圧力となる。実際には、もっとも高性能が得られる線速度2mm/sec以下の場合では、配管インジェクター圧力は、0.5MPa以下であり、システム圧力とカラム入口圧力は同じと考えてよい。
【0066】
固定相となるHPLC充填カラムとして、内径4.6mm長さ25cmのInertsil(登録商標)C30(USPコード L62 トリアコンチル基結合シリカゲル 5μm ジーエルサイエンス社製)を用いて、トコフェロール異性体の分離をおこなった。トコフェロールは図2の構造を持ち、特にβとγの異性体はメチル基(図中Meと略す)の結合位置が異なるだけで、分離は難しい。溶離液としては、HPLCで広く使われもっとも単純な組成であるメタノール100%を使用し、流速500μL/min(線速度0.5mm/sec)、カラム温度40℃を分析条件とした。
【0067】
抵抗5と6を接続していない分析では、カラム入口圧力は、3.1MPaになり、異性体は分離していない(図8(1) 1:δ−トコフェロール、2:γ−トコフェロール、3:β−トコフェロール、4:α−トコフェロール 以下同じ)。
【0068】
抵抗5に、内径0.05mm溶融シリカキャピラリーチューブ40cmを設置し、抵抗6は接続無しとした結果、カラム入口圧力は、13MPaとなりピーク2,3に表される異性体の溶出が変化し分離が見られた(図8(2))。
【0069】
さらに抵抗5を内径0.03mm溶融シリカキャピラリーチューブ25cmに変える事で、カラム入口圧力は、49MPaとなり、異性体のγ−トコフェロールに対してβ−トコフェロールの溶出が、より遅くなり、結果として分離した(図8(3))。
【0070】
どちらのシステムもその容量は、1μL以下で、そのデッドボリュームによる遅れ時間は、0.1秒以下でありピーク形状への悪化影響もなかった。つまり、カラムとセル間にカラム入口圧力が10MPa以上になる抵抗を接続することで、単純な溶離液での異性体分離が行えることが確認された。
【0071】
さらに、抵抗の種類、接続場所を種々変えて、その効果を確かめた。
抵抗5に、モノリスキャピラリーチューブMonoCap(登録商標)内径0.2mm、長さ1.5cm(容量0.6μLスルーポア2μm)を接続した結果、圧力49MPaになり、図8(3)と同じく異性体が分離した。
【0072】
抵抗5に、内径0.05mm溶融シリカキャピラリーチューブ長さ40cmを接続し、セルの後に抵抗6としてInertSustainC18HPLCカラム(USPコード L1 オクタデシル基結合シリカゲル 2μm ジーエルサイエンス社製)内径2.1mm、長さ5cmを取り付けた。カラム入口圧は、49MPaとなり、図8(3)と同じく異性体が分離した。
【0073】
抵抗6に用いるカラムは、検出後であり分離に影響しないので、分離が悪くなった使い古したカラムでも良く経済的である。また、このシステムの場合、セルに掛かる圧力は、30MPaであり高耐圧の市販セルでも使用できるので、便利である。また、HPLCカラムは、キャピラリーチューブより詰まりにくく、抵抗変動が生じにくいためより有用である。
【0074】
抵抗5に内径0.03mm溶融シリカキャピラリーチューブ長さ5cmを接続し、抵抗6に、6方ロータリーバルブを5種類の抵抗を設けて接続した。ロータリーバルブを回すと段階的に抵抗を切換することができる。ロータリーバルブ7の出口ポート9には抵抗をつけず、出口ポート10に内径0.065mm PEEKチューブ30、長さ3mを取り付け、出口ポート11に内径0.05mm溶融シリカキャピラリーチューブ31長さ1.2mを取り付け、出口ポート12に内径0.03mm溶融シリカキャピラリーチューブ32長さ15cmを取り付け、出口ポート13に内径0.2mmモノリスキャピラリーチューブ33MonoCap、長さ2cm(スルーポア:1μm)を取り付け、出口ポート14に粒子径2μmHPLCカラム内径2.1mm、長さ15cmカラム34を取り付けた。
【0075】
ロータリーバルブ7を回してポート10に設定した場合には、カラム入口圧力は、13MPaとなり、図8(2)と同じ分離が得られた。回してポート11〜14に設定した場合には、カラム入口圧力は49MPaとなり、図8(3)と同じ分離が得られた。どのポートに回しても、異性体の分離に適用できる事が確認された。さらに、ポート10〜14に回して、圧力変動はほとんどなく、取り付ける抵抗を変える事で、自由に圧力を変更できることも確認できた。
【0076】
今回の検討で、抵抗管が詰まる事はなかったが、バルブシールによる汚れが出て来ることが考えられるので、詰まりにくいカラムやなるべく内径の太い抵抗が推奨される。
【0077】
抵抗5には図3に示すように抵抗を接続せず、抵抗6に6方切換バルブ7を接続し、図6に示すように抵抗管18、19を組み入れた。バルブを切り換えることにより、段階的に抵抗を変えることができる。抵抗として、内径0.05mm溶融シリカキャピラリーチューブ18長さ40cmと内径0.03mm溶融シリカキャピラリーチューブ長さ25cmを組み込み、切り換えたところ、それぞれ、カラム入口圧力が、13MPa、49MPaとなり、それぞれ、図8(2)、図8(3)と同様の分離が得られた。切換バルブの容量は、10μL以下と小さく、遅れ時間は、1秒程度であり、検出器セル前にも使用できる。
【0078】
抵抗5には、抵抗を接続せず、抵抗6にレギュレータを接続した。レギュレータは、図7に示すような構造で圧縮ばね23の荷重と出口側圧力による力の平衡を利用し、ピストンシール22の働きによりピストン21を移動させて液体が流通する空間容量を変化させるにより抵抗圧力を調整する事ができる。開放状態では、抵抗が掛からず、図8(1)と同じ分離状態であったが、圧力調整ねじ24を回して調整することにより13MPaにすると、図8(2)のように分離が見られ、さらに絞って調整すると、図8(3)のように異性体が分離した。
【0079】
圧力調整ねじ24を自動で機械的に調整すれば、圧力を連続的に可変できる事になる。その場合、10MPa以上の圧力にカラム入口圧がなれば、異性体分離効果が発揮されるので、実際には、10MPa以上になり、かつデッドボリュームの少ない抵抗管を前段に接続し、その後に、レギュレータを接続する事が推奨される。また、圧力変動も少なくシステム安定が早くなる。
【0080】
このように本発明においては、基本的には、10MPa以上の圧力をカラム入口に掛けられれば、手段は多種のものが利用でき、その抵抗の数や接続位置は限定されない。
【実施例2】
【0081】
実施例1と同じ試料であるトコフェロール異性体を用いて、Inertsil(登録商標)C30内径4.6mm、長さ250mmのHPLC充填カラムを用いて、単純な溶離液であるメタノール100%を用いて、従来から言われている温度効果と本発明である圧力効果の比較をおこなった。実施例1にあるように、図9(1)のように通常の条件では、βとγトコフェロール異性体は完全分離しない。しかし、カラム温度を下げる事により、図9(3)に示すように分離された。20℃で異性体の分離は達成されている。
【0082】
しかし、オーブン温度を20℃に設定し、モニター温度が設定値になったのは約30分後であった。そこで実際に分析を行ったが、ピーク保持時間は安定せず、3回目の分析から安定したデータが取れ始めた。オーブン温度が安定してから、約30分後にやっと保持時間が安定したことになり、オーブン温度設定からだと、1時間程度の平衡化時間が必要になることがわかった。当然、冷却には膨大なエネルギーが使われる事になる。
【0083】
同じカラム、同じ溶離液、同じ試料で本願発明の方法を実施した。
カラム温度は、30℃一定とし、カラムの後に、内径0.03mm、長さ28cmの溶融シリカキャピラリーチューブ(容量0.2μL)を抵抗として接続した。カラム入口圧力は57.9MPaとなり、20分程度で安定し、最初の分析から図10(1)のような安定したデータが得られた。さらに、その後に抵抗として、内径0.03mm、長さ10cmの溶融シリカキャピラリーチューブを接続した。カラム入口圧力は79MPaとなった。抵抗管を繋ぐジョイント部分の容量を入れても全容量は1μL以下であり、図10(2)のように完全分離したデータが得られた。
安定時間も、20分以内であり、圧力を掛けることによる異性体分離は従来方法よりも簡便で早く安定する事が確認された。
【実施例3】
【0084】
実施例1と同じ方法を、標準試料ではなく、実試料市販サプリメントのHPLC分析に適用した。
市販トコトリエノールサプリメント1粒をカッターで割り中身を10.5mg量り取り、ヘキサン/イソプロパノール=1:1 1mLで溶解しHPLC用試料とした。
Inertsil(登録商標)C30 内径4.6mm、長さ250mmのHPLC充填カラムを用いて、メタノール100%を流速0.5mL/min、カラム温度30度、検出295nmで分析して、従来法と本発明方法と比較してその効果を確かめた。
従来方法では 圧力3.1MPaで、異性体である 2)ガンマトコトリエノールと 3)ベータトコトリエノールは分離していない。(図11上)
本発明方法では破損防止のため、内径0.4mmのピークチューブを保護チューブとして被せた内径0.1mm 長さ25cmの溶融シリカキャピラリーを、抵抗管として、SUS 1/16 インチフェラルでカラムの後と検出器の間に接続し、その他は従来法と同条件で分析した。
カラム入口圧は、63.3MPaとなり図11下のように1)デルタトコトリエノール、2)ガンマトコトリエノール、 3)ベータトコトリエノール、4)アルファートコトリエノールという異性体4成分がすべて分離し、4成分がこのサプリメントに含まれていることがわかった。サプリメントからの抽出物という実試料分析にも、本発明による異性体分離が適用できることが確認された。
【実施例4】
【0085】
実施例1と同じ条件で脂肪酸メチルエステルである1.γ‐Methyl(z,z,z)‐6,9,12‐octadecatrienoateと2.α‐Methyl(z,z,z)‐9,12,15‐octadecatrienoateの異性体の分析を行った。
【0086】
使用し易く、置換が早い100%メタノール溶離液を用いて、流速0.5mL/minでInertsil(登録商標)C30内径4.6mm長さ250mmとInertsil(登録商標)ODS−P内径3.0mm、長さ200mmの2種類のカラムで本願発明方法を実施した。カラムの出口流路に高耐圧セルを接続し、その後に抵抗としてレギュレータを接続し、背圧を可変しながら実験を行った。
【0087】
Inertsil(登録商標)C30、内径4.6mm、長さ250mmにおいて、まず、背圧は掛けずに、分析を行ったところ、圧力7.4MPaでは、ほとんど分離できなかった(図12(1))。レギュレータのつまみを回して、カラム入口圧力を56.3MPaに調整すると、2成分の溶出時間が変化し、分離が見られた。(図12(2))完全分離ではないが、圧力が分離に効果的に作用していることが確認された(ピーク1:γ‐Methyl(z,z,z)‐6,9,12‐octadecatrienoate、ピーク2:α‐Methyl(z,z,z)‐9,12,15‐octadecatrienoate)。
【0088】
Inertsil(登録商標)ODS−P、内径3.0mm、長さ200mmにおいても、同様な事を行った。圧力を掛けない場合では、7.4MPaでほとんど分離せず(図12(1))、57.3MPaに調整すると、2成分の溶出時間が変化し、完全にベースライン分離となった(図12(2))。
【0089】
セルの前に内径0.03mm、長さ25cmの溶融シリカキャピラリーチューブを接続しても同じ効果が得られた。カラムの種類によっては大小はあるが、異性体の分離を変化させることにおいて圧力が効果的に働くことが確認された。
【実施例5】
【0090】
実施例1に示す本発明の方法及び装置を分取に適用した例を以下に示す。
Inertsil(登録商標)ODS−P(USPコード L1 オクタデシル基結合シリカゲル 5μm ジーエルサイエンス社製)内径20mm、長さ250mmの分取カラムを用いて、単純な溶離液である70%アセトニトリル水を流速10mL/minで送液し、キシレン異性体1.o−キシレン、2.m−キシレン、3.p−キシレンの分取を試みた。分離カラムの出口流路に内径0.13mm、長さ2mのコイル状に巻いたPEEKチューブを抵抗として接続し、分取を行った。分離カラム入口圧力は65MPaであった。抵抗管の容量は、0.03mLとなるが、流速が早いため、実際のピーク遅れ時間としては0.2秒以下でまったく影響しない。
【0091】
ODS‐Pにおいて、溶離液にβ‐シクロデキシトリンの添加をすることなく、単純な70%アセトニトリル水溶離液でキシレン異性体の分取が可能であった(図13)。
10分〜11.5分を第1分画(4)、11.6分〜12.8分を第2分画(5)12.8分〜13分を第3分画(6)として、各分画部をガスクロマトグラフィーを用いて純度チェックを行ったところ、第1分画(4)で、純度100%のo‐キシレンが99%の回収で得られ、第3分画(6)で純度98%p‐キシレンが70%回収率で得られ、第2分画(5)で、純度70%m‐キシレンが90%の回収率で得られ、目的成分が分取できる事が分かった。
従来の手法では、β‐シクロデキストリンが溶離液に含まれるため、分取後さらに取り除くことが必要となったが、本発明では添加成分のない単純な溶離液で行えるので、そのまま溶媒のみ蒸発させる事で濃縮または乾固が簡単に行えるので精製にも非常に適していることが判明した。
【0092】
自動でつまみ24を回すレギュレータ25を抵抗として用いて、50MPaから10MPaへ圧力を傾斜可変する圧力グラジエントを行い異性体を分取することも可能であった。流量が早いので、カラムと検出器セル間にレギュレータ25を設けても、デッドボリュームの影響はなく、異性体を分取することが可能となった。図7にレギュレータの一例を示す。概略、ボディー20にピストン21をピストンシール22を介して圧縮ばね23により流路を遮蔽する構造である。
【実施例6】
【0093】
実施例1に示す装置及び方法によりInertsil(登録商標)C30内径4.6mm、長さ250mm及びInertsil(登録商標)ODS‐P内径3mm、長さ200mmの分析カラムを用いて、単純な溶離液である50%アセトニトリル−水、20℃の一定温度で1.α‐エストラジオールと2.β‐エストラジオール異性体の分離を試みた。Inertsil(登録商標)C30、内径4.6mm、長さ250mmは、流速0.35mL/minとした。抵抗を接続していない従来の分析では圧力4.2MPaであり、異性体のピーク1,2は分離していた(図14(1))。
【0094】
抵抗として、内径0.03mm、長さ25cmの溶融シリカキャピラリーチューブをカラム出口に接続し、カラム圧力を71MPaとして分析した結果、分離せずに1本のピークとして溶出した(図14(2))。
【0095】
C30カラムでは、固定相となる官能基が高密度に存在するため、その固定相を加圧することで、より平面的なβ‐エストラジオールが、高密度な固定相の中に入り込みやすく、大きく溶出が遅れると考えられる。一方、α‐エストラジオールはβ一体に比べると分子の形が立体的であり、影響があまり顕著ではないため、結果的として71MPaでは分離しなくなっているが、異性体間の分離を変化させるために圧力が効果的であることは確認された。
【0096】
Inertsil(登録商標)ODS‐P内径3mm、長さ200mmの場合は、流速0.13mL/minとした。抵抗を接続しない従来の分析では圧力3.4MPaであり、2のβーエストラジオールが先に溶出している(図15(1))。抵抗として、内径0.03mm、長さ66cmの溶融シリカキャピラリーチューブをカラム出口に接続し、カラム圧力を71MPaとして分析した結果、逆にα―エストラジオールが先に溶出した(図15(2))。
【0097】
ODS‐Pでも、より平面的なβ‐エストラジオールはより強く保持され、溶出時間が遅くなり、3.4MPa時と比べてピークの溶出が逆転している。これらのことにより、圧力調整することで、分離を大きく変えることが可能であり、従来、溶離液変更で行なっていた分離の調製が、抵抗を接続し圧力を変えるだけで簡単にできることがわかった。
【実施例7】
【0098】
実施例1に示す装置及び方法により、Inertsil(登録商標)ODS‐P内径3mm、長さ200mmのカラムを用いて、イオン性の親水基を持った異性体化合物の分離に適用した。末端にカルボニル基を持った脂肪酸の異性体である、
1.Cis‐vaccenic acid(11Z‐Octadecenoic Acid)
2.Petroselinic acid(cis‐6‐Octadecenoic Acid)
3.Elaidic acid(trans‐9‐Octadecenoic Acid)
を試料とし、溶離液として、97.5%メタノール,2.5%10mMリン酸(H2O)混合移動相を用い、流速0.4mL/minで効果を検証した。
【0099】
抵抗を接続していない通常分析では、カラム入口圧は10MPa以下である3.2MPaとなり脂肪酸異性体分離していない(図16(1))。それに内径0.03mm、長さ15cmの溶融シリカキャピラリーチューブを抵抗としてカラム出口に接続すると、カラム入口圧は10MPa以上の40.2MPaとなり、異性体が分離した(図16(2))。
【0100】
イオン性の異性体の分離に於いても本発明の方法は効果がある事が確認された。なお、当然のことながら、溶離液としてバッファーを含んだ場合でも効果が得られることも確認された。
【0101】
以上から、従来の分析状態に、カラム入口圧が10MPa以上になるように、抵抗を加えるだけで、異性体の溶出挙動を変化させ、分離を変化させることができることがわかった。
【実施例8】
【0102】
実施例1に示す装置及び方法により、実施例2のトコフェロール異性体(1.σ‐tocopherol、2.γ‐tocopherol、3.β‐tocopherol、4.α‐tocopherol)を試料とし、異なるタイプの固定相を持つ充填カラムで分離を実施した。
【0103】
球状シリカゲルにオクタデシル基を結合させた、所謂ODSカラムの中で、Inertsil(登録商標)ODS‐3(USPコード L1 オクタデシル基結合シリカゲル 炭素量15% 5μm ジーエルサイエンス社製)内径3mm長さ100mm、Inertsil(登録商標)ODS‐EP(USPコード L1 オクタデシル基結合シリカゲル エンベット型 炭素量9% 5μm ジーエルサイエンス社製)内径3mm長さ100mm、Inertsil(登録商標)ODS‐P(USPコード L1 オクタデシル基結合シリカゲル 炭素量29% 5μm ジーエルサイエンス社製)内径3mm長さ200mmの3種類のカラムを用い、100%メタノール溶離液で流速0.2mL/minとし、抵抗として内径0.03mm長さ60cmの溶融シリカキャピラリーチューブをカラム出口に接続し、圧力効果を検証した。
【0104】
ODS‐3およびODS‐EPでは、圧力の増大により保持時間の増加はあるが、異性体間分離の変化は見られず、β体とγ体は分離しなかった(図17、図18)。
【0105】
それに対して、ODS‐Pでは、異性体化合物の溶出が変化し分離してきている(図19)。圧力効果の少ないODS‐3、ODS‐EPはそれぞれ、オクタデシル基の結合基密度が、1.3μmol/m2、1.7μmol/m2であり、圧力効果の高いODS‐Pでは、2.3μmol/m2である。ちなみに実施例2で使用したC30では、化学結合基の結合基密度は2.5mol/m2であり、異性体分離における圧力効果は、2mol/m2以上の高密度の固定相に有効であることがわかる。
【0106】
Inertsil(登録商標)ODS‐3 1.3μmol/m2、ODS‐EP 1.7μmol/m2、にもタイプ1と同様の圧力効果が働き、保持の増大だけが起こっているが、異性体化合物間の分離にめざましい変化はおきていない。異性体化合物は、結合基が同じでその配置が異なるだけであり、タイプ1〜4の効果による分離はあまり期待できない。
【0107】
C30、ODS‐Pにおいては、結合配置が異なり、分子の立体構造が異なる異性体化合物間の溶出が変化している事から、タイプ1の効果に加えて、充填剤として多層に重なり(ポリメリック結合)高密度の固定相の立体選択性効果が働いている事が解った。さらに、圧力を加えると、立体選択効果が大きく表れ分離が飛躍的に変化するものと思われる。
【0108】
なお、これらの充填カラムは一般に市販されているため簡単に入手でき、特殊な固定相を選択する必要が無く、異性体分離に適用できる。
【0109】
しかしながら、市販充填カラムを使用しなくても下記のような合成を行えば同様の固定相を作成できることは言うまでもない。具体的合成方法は以下のようである。表面積450m2/m2、細孔径10nm、粒子径5μmのシリカゲルに5%のオクタデシルトリクロロシランをトルエンに溶かした溶液中で、10時間以上還流反応を行い、市販のInertsil ODS‐EPと同様のオクタデシル基の結合基密度が、2μmol/m2以上の固定相が得られた(結合基密度2.1μmol/m2)。
【0110】
また、同じゲルに10%安息香酸トリアコンチル安息香酸トルエン溶液を塗布後、窒素中、120℃で減圧除去した結果、市販のInertsil C30と同様の結合基密度2.2μmol/m2の固定相が得られた。
【0111】
これらの固定相でも圧力増加による異性体間における分離の変化効果が得られており、合成方法や用いる担体はどのような物でも良いが、結合基密度が2μmol/m2以上になると、異性体間の分離変化効果が高くなることが確かめられた。
【実施例9】
【0112】
これまでの実施例から、10MPa以上の圧力がHPLCカラムに掛かる事が異性体分離に有効であり、具体的にはカラムの後に抵抗を取り付け、さらに変化させることで実現できることが確認された。
【0113】
一方、従来の溶離液割合を変化させるグラジエント分析においては、溶離液割合の変化とともにカラム圧力も変化する事が知られている。典型的な逆相分配カラムを用いたグラジエント分析では、有機溶媒量を増加させることにより早期の溶出を目的とするため、圧力は減少する変化が生じる。分析開始時の圧力が10MPa以上であってもグラジエント分析が進むと有機溶媒濃度が増え、溶離液の粘性が下がり最終的な分析圧力は5MPaに下がってしまう。これでは異性体間の分離には適用できない。
【0114】
そこで、カラムの後に抵抗管を付け10MPa以上の状態にし、異性体間の分離に適用できるか検証を行った。
試料には、1)シス11−オクタデシルメチルエステル、2)シス6−オクタデシルメチルエステル を用い、実験条件は以下のように設定してHPLC分析を行った。
HPLC分析カラム:Inertsil(登録商標)ODS‐P 3μm 内径3mm 長さ100mm
溶離液A:10mM リン酸水溶液
溶離液B:メタノール
流速:0.2mL/min
グラジエント:A/B 16/84 (初期) →15分リニアグラジエント→ 1/99 →30分までホールド→その後初期状態へ
検出波長:UV205nm
カラム温度19℃の場合、圧力は8.8MPa−5MPaに下がり、図21Aのクロマトグラムが得られた。内径0.4mmのピークチューブを保護チューブとして被せた内径0.1mm 長さ25cmの溶融シリカキャピラリーを、抵抗管として、SUS 1/16 インチフェラルでカラムの後と検出器の間に接続し、同じ条件で分析した結果が図21Bのクロマトグラムである。圧力は、62.4MPa−39.5MPaまで変化したが、それでも10MPa以上であり、ピークも高くなりより異性体は分離した。この結果より、グラジント時の溶媒変化による圧力変化も本発明の効果がある事が確認された。
【0115】
抵抗管を変えなくても、グラジエントの溶離液変化だけで、62.4MPa−39.5MPaまで変化でき、異性体分離状態も調整できた。本実施例では、水―メタノール系であるので、2倍弱の変化であるが、30%エタノール(10℃粘性4)−酢酸エチル(10℃粘性0.5)であれば、8倍程度の圧力変化が可能になるので、一番低い時に10MPa以上になるようにすれば、異性体分離には有効となる。
【0116】
また、HPLCにおいて、温度を上げると固定相内での溶質成分の移動速度は速くなるので、溶出が早くなりピーク形状が良くなる事は知られている。
そこで、本発明状態でカラム温度を変化させて分析した。
【0117】
20℃では、56.2‐35.8MPaまで、25℃では50.4‐32.0MPaまで圧力は変化し、図21C、Dのクロマトグラムが得られた。温度が上がるほど圧力は下がり、1と2の溶出は近づき異性体として分離能は悪くなる。しかし、それでもグラジエント終了時で10MPa以上を保持しており、これらの異性体は分離されている事が確認された。例えば、30%エタノールの場合、カラム温度で80℃粘度0.6℃粘度7であり、温度変化をさせると10倍近い圧力変化を起こす事ができる。
【0118】
この結果より、分析温度の調整は、10MPa以上の圧力を保持できれば、異性体の分離を保持しながら、ピーク形状を変化させる事も可能である事が明らかとなった。
従って、グラジエントに伴う溶媒割合変化と、カラム温度変化によって10倍弱の圧力変化が可能で、異性体分離を変化させる事ができ、さらに両方を組み合わせて変更する事で、10MPa〜100MPaまでの圧力変化も可能になることが確認された。
【実施例10】
【0119】
従来から圧力変化に応じて溶質の相比が変化し、保持時間が変化する現象は報告されているが、化合物の異性体間でその保持が変化し、異性体間の分離に効果があると言う報告はこれまで無かった。本発明に係るこの特性を確かめるために、実施例データをまとめて、どのような現象が起きているかを確認した。
【0120】
保持は、溶質(Solute)が固定相にどのくらい留まるかによって生じるので、圧力上昇に伴う保持比の変化から、固定相内に占める溶質容積変化量△Vが下記式より得られる。
△V=−気体定数×T(K)×ln(本発明を行った時の保持比/従来分析の場合の保持比)/本発明の実施圧力
△V1を溶質1の溶質容積変化量、△V2を溶質2の溶質容積変化量とすると、溶質1、溶質2の異性体化合物間の変化量の比である△△V値は、相比の影響を受けない数値となる。
【0121】
2種類のHPLC分析カラムについて分析した結果を下記の表にまとめた。溶質の構造の差に対応して、圧力を加える事で、固定相への取り込みが生じて、固定相内で体積変化が起き、異性体間の分離している事が判る。
【0122】
【表1】

【0123】
例えば、Inertsil(登録商標)ODS‐Pのカラムを用いる、異性体であるα-/γ-linolenic acid methyl esterの温度303K(20℃)の場合(表中の1行目)を例にとると、従来分析でのα-linolenic acid methyl esterの保持比は1.00、本発明の圧力50MPa掛けた場合の保持比は1.82、となり、上記の計算式により、△V1は、−30.2(−8.31x303xIn(1.82/1.00)/50)となる。
【0124】
その異性体である γ-linolenic acid methyl esterの保持比は1.12、本発明の圧力50MPa掛けた場合の保持比は2.45、となり、上記の計算式により△V2は、−39.4となる。両異性体間のその差△△Vは、端数処理をして−9.3となる。
【0125】
同様の方法で計算を行うと、異性体化合物毎に△△Vが得られる。この差の絶対値が大きいほど、より本発明の効果が期待できる異性体成分であると考えられる。
Inertsil(登録商標)C30カラムを使った場合でも、同様の方法で各化合物毎に△△Vが得られた。
【0126】
固定相の種類によって△△V値は異なり、今回の結果では、C30とODS‐Pについて同等の△△V値が得られる場合と、 △△V値(ODS‐P) > △△V値(C30)の場合があった。 表中2行目のm-/p-xylene や表中6行目β-/α-estradiolでは、ほぼ同じ値が、β-/γ-tocopherolではほぼ同じ絶対値が得られている。
【0127】
溶出順が固定相によって異なるため+―の違いがある場合もあるが、圧力変化に伴う固定相内での溶質の保持変化量はほぼ同じで、その異性体間での溶出変化効果はほぼ同じと考えられる。
【0128】
一方、表中1,3,4行目の化合物では、ODS‐Pの△△V値の絶対値がC30の △△V値の絶対値より大きくなる。
【0129】
表中2,6行目の化合物は、炭化水素鎖が主骨格となり剛的なサイトを持った溶質であり、表中1,3,4行目の化合物はエステル鎖を持っており柔軟なサイトの溶質と考えられる。
すなわち、C30の識別部位は剛的であり、ODS‐Pの認識部位は剛的なサイトと柔軟なサイトが存在するものと考えられる。
【0130】
以上のように、圧力効果の大きさを測る指標として△△V値の使用が示唆された。そして、この値を使用することで圧力効果により溶質の溶け込みに差が生じ、異性体間の分離が変化する事が明確になった。さらに、液相種によって異性体間の認識部位が異なり、化合物の構造も認識している事が推定できた。
【特許請求の範囲】
【請求項1】
液体クロマトグラフィーに於いて使用するカラムの出口流路に抵抗を設け、前記抵抗の作動によりカラム入口圧力を10MPa〜100MPaに調整し、異性体化合物を成分ごとに溶質挙動を変化させることを特徴とする異性体化合物の処理方法。
【請求項2】
前記溶質挙動の変化は溶質の分離であることを特徴とする請求項1に記載の異性体化合物の処理方法。
【請求項3】
前記溶質挙動の変化は溶質出現順序の変化であることを特徴とする請求項1に記載の異性体化合物の処理方法。
【請求項4】
前記溶質挙動の変化は溶質の合体であることを特徴とする請求項1に記載の異性体化合物の処理方法。
【請求項5】
前記カラム入口圧力を100MPa〜10MPaの間で連続的又は段階的に下げながら異性体化合物の溶質挙動を変化させることを特徴とする請求項1から4のうち何れか一項に記載の異性体化合物処理方法。
【請求項6】
溶離液の組成を変化させることで、前記カラム入口圧力を100MPa〜10MPaの間で連続的又は段階的に変化させ異性体化合物の溶質挙動を変化させることを特徴とする請求項1から4のうち何れか一項に記載の異性体化合物の処理方法。
【請求項7】
カラム温度を変化させることで、前記カラム入口圧力を100MPa〜10MPaの間で変化させ、異性体化合物の溶質挙動を変化させることを特徴とする請求項1から4のうち何れか一項に記載の異性体化合物の処理方法。
【請求項8】
前記カラムが分析カラムであることを特徴とする請求項1から5のうち何れか一項に記載の異性体化合物の分析方法。
【請求項9】
前記カラムが分取カラムであることを特徴とする請求項1から5のうち何れか一項に記載の異性体化合物の分取方法。
【請求項10】
異性体化合物を処理する装置であって、カラム出口流路に於いて、カラム出口から検出器までの間、又は、検出器から排出の間、又はその両方に抵抗を接続し、カラム入口圧力を所定の圧力に調整自在としたことを特徴とする異性体化合物の処理装置。
【請求項11】
前記カラムに分析カラムを使用したことを特徴とする請求項8に記載の異性体化合物分析装置。
【請求項12】
前記カラムに分取カラムを使用したことを特徴とする請求項8に記載の異性体化合物分取装置。
【請求項13】
前記抵抗は、抵抗管であることを特徴とする請求項8に記載の異性体化合物の処理装置。
【請求項14】
前記抵抗管はチューブ、モノリスカラム又は充填カラムのうちの一であることを特徴とする請求項11記載の異性体化合物の処理装置。
【請求項15】
前記抵抗は、液体が流通する空間容量を変化できるレギュレータであることを特徴とする請求項8に記載の異性体化合物の処理装置。
【請求項16】
請求項8から13のうち何れか一項に記載の異性体化合物の処理装置であって、前記カラムとして分析カラムを使用したことを特徴とする異性体化合物の分析装置。
【請求項17】
請求項8乃至13のうち何れか一項に記載の異性体化合物の処理装置であって、前記カラムとして分取カラムを使用したことを特徴とする異性体化合物の分取装置。
【請求項18】
前記カラム出口流路側にバルブを設け、該バルブに複数の抵抗を接続し、接続する抵抗の選択により、所定のカラム入口圧力を得ることを特徴とする請求項8から13のうち何れか一項に記載の異性体化合物の処理装置。
【請求項19】
10MPa以上の耐圧のある粒子状担体又はモノリス担体に固定相を2μmol/m2以上の密度に塗布又は化学結合させた充填剤を用いたことを特徴とする異性体化合物分離カラム。
【請求項20】
10MPa以上の耐圧のある粒子状担体又はモノリス担体に固定相を2μmol/m2以上の密度に塗布又は化学結合させたことを特徴とする異性体化合物分離カラム用充填剤。
【請求項1】
液体クロマトグラフィーに於いて使用するカラムの出口流路に抵抗を設け、前記抵抗の作動によりカラム入口圧力を10MPa〜100MPaに調整し、異性体化合物を成分ごとに溶質挙動を変化させることを特徴とする異性体化合物の処理方法。
【請求項2】
前記溶質挙動の変化は溶質の分離であることを特徴とする請求項1に記載の異性体化合物の処理方法。
【請求項3】
前記溶質挙動の変化は溶質出現順序の変化であることを特徴とする請求項1に記載の異性体化合物の処理方法。
【請求項4】
前記溶質挙動の変化は溶質の合体であることを特徴とする請求項1に記載の異性体化合物の処理方法。
【請求項5】
前記カラム入口圧力を100MPa〜10MPaの間で連続的又は段階的に下げながら異性体化合物の溶質挙動を変化させることを特徴とする請求項1から4のうち何れか一項に記載の異性体化合物処理方法。
【請求項6】
溶離液の組成を変化させることで、前記カラム入口圧力を100MPa〜10MPaの間で連続的又は段階的に変化させ異性体化合物の溶質挙動を変化させることを特徴とする請求項1から4のうち何れか一項に記載の異性体化合物の処理方法。
【請求項7】
カラム温度を変化させることで、前記カラム入口圧力を100MPa〜10MPaの間で変化させ、異性体化合物の溶質挙動を変化させることを特徴とする請求項1から4のうち何れか一項に記載の異性体化合物の処理方法。
【請求項8】
前記カラムが分析カラムであることを特徴とする請求項1から5のうち何れか一項に記載の異性体化合物の分析方法。
【請求項9】
前記カラムが分取カラムであることを特徴とする請求項1から5のうち何れか一項に記載の異性体化合物の分取方法。
【請求項10】
異性体化合物を処理する装置であって、カラム出口流路に於いて、カラム出口から検出器までの間、又は、検出器から排出の間、又はその両方に抵抗を接続し、カラム入口圧力を所定の圧力に調整自在としたことを特徴とする異性体化合物の処理装置。
【請求項11】
前記カラムに分析カラムを使用したことを特徴とする請求項8に記載の異性体化合物分析装置。
【請求項12】
前記カラムに分取カラムを使用したことを特徴とする請求項8に記載の異性体化合物分取装置。
【請求項13】
前記抵抗は、抵抗管であることを特徴とする請求項8に記載の異性体化合物の処理装置。
【請求項14】
前記抵抗管はチューブ、モノリスカラム又は充填カラムのうちの一であることを特徴とする請求項11記載の異性体化合物の処理装置。
【請求項15】
前記抵抗は、液体が流通する空間容量を変化できるレギュレータであることを特徴とする請求項8に記載の異性体化合物の処理装置。
【請求項16】
請求項8から13のうち何れか一項に記載の異性体化合物の処理装置であって、前記カラムとして分析カラムを使用したことを特徴とする異性体化合物の分析装置。
【請求項17】
請求項8乃至13のうち何れか一項に記載の異性体化合物の処理装置であって、前記カラムとして分取カラムを使用したことを特徴とする異性体化合物の分取装置。
【請求項18】
前記カラム出口流路側にバルブを設け、該バルブに複数の抵抗を接続し、接続する抵抗の選択により、所定のカラム入口圧力を得ることを特徴とする請求項8から13のうち何れか一項に記載の異性体化合物の処理装置。
【請求項19】
10MPa以上の耐圧のある粒子状担体又はモノリス担体に固定相を2μmol/m2以上の密度に塗布又は化学結合させた充填剤を用いたことを特徴とする異性体化合物分離カラム。
【請求項20】
10MPa以上の耐圧のある粒子状担体又はモノリス担体に固定相を2μmol/m2以上の密度に塗布又は化学結合させたことを特徴とする異性体化合物分離カラム用充填剤。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【公開番号】特開2013−19892(P2013−19892A)
【公開日】平成25年1月31日(2013.1.31)
【国際特許分類】
【出願番号】特願2012−137336(P2012−137336)
【出願日】平成24年6月18日(2012.6.18)
【出願人】(390030188)ジーエルサイエンス株式会社 (37)
【公開日】平成25年1月31日(2013.1.31)
【国際特許分類】
【出願日】平成24年6月18日(2012.6.18)
【出願人】(390030188)ジーエルサイエンス株式会社 (37)
[ Back to top ]

