遺伝子操作非ヒト動物、および向精神薬開発法
【課題】自閉症の発生および異常な社会行動を防止する向精神薬の開発等に利用できるmotopsinノックアウト動物、及び向精神薬のスクリーニング方法などを提供すること。
【解決手段】本発明は、相同染色体上のmotopsin遺伝子を破壊することによって、motopsinの発現が抑制されたノックアウト動物等を提供する。作製したmotopsinノックアウトマウスは、行動検査において長時間の社会行動を示す点が認められるなど、ユニークな特徴を有するマウスであった。また、motopsinを阻害もしくは活性化する物質の探索は、向精神薬のスクリーニング方法として有用である。
【解決手段】本発明は、相同染色体上のmotopsin遺伝子を破壊することによって、motopsinの発現が抑制されたノックアウト動物等を提供する。作製したmotopsinノックアウトマウスは、行動検査において長時間の社会行動を示す点が認められるなど、ユニークな特徴を有するマウスであった。また、motopsinを阻害もしくは活性化する物質の探索は、向精神薬のスクリーニング方法として有用である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、motopsin遺伝子欠損動物と向精神薬開発に関し、より詳しくは、正常動物に比し社会行動が亢進しているmotopsin遺伝子欠損非ヒト動物、同遺伝子欠損動物又はmotopsinを用いた向精神薬のスクリーニング方法に関する。
【背景技術】
【0002】
Motopsinは、一次構造上セリンプロテアーゼの触媒領域において高い相同性を有しながら、プロリンリッチ領域、クリングル領域、スカベンジャーレセプターシステインリッチ領域を含む特徴的な制御領域をもつ蛋白質分解酵素(セリンプロテアーゼ)である。
【0003】
Motopsinは、脳や脊髄といった中枢神経系に豊富に含まれるが、肺や腎臓、皮膚にも存在している。MotopsinはSondereggerらが我々と同時期にneurotrypsinと報告した分子、HUGO nomenclatureによりprss12として認定された分子と同一のものである。特に胎児期後期から新生児期の神経系に高発現することが知られている。Motopsinは、in vitroにおいてゼラチンやtissue plasminogen activatorを分解することが報告されている。また、非症候群性精神遅滞の家系において第7エクソンの4塩基欠損によるナンセンス変異が報告されている。さらに、ショウジョウバエにおいてmotopsinオルソローグの欠損が長期記憶を障害することが報告されている。Motopsinの発現は神経機能の維持に重要であることが軸索傷害実験から示されている。また、motopsin蛋白質が主にニューロンの細胞体や樹状突起基部に存在しており、発現量が増加すると軸索にも輸送されることなども報告されている。しかしながら、ほ乳類を含む脊椎動物の脳内機能はほとんど知られておらず、motopsin欠損による発達障害発症機構は未だ十分に解明されていない。
【非特許文献1】Mitsui, S., Yamaguchi, N., Osako, Y., Yuri, K., Enzymatic properties and localization of motopsin (PRSS12), a protease whose absence causes mental retardation. Brain Research 1136, 1-12, 2007.
【非特許文献2】Numajiri, T., Mitsui, S., Hisa, Y., Ishida, T., Nishino, K., Yamaguchi, N., The expression of a motoneuron-specific serine protease, motopsin (PRSS12), after facial nerve axotomy in mice. Journal of Plastic, Reconstructive & Aesthetic Surgery 59, 393-397, 2006.
【非特許文献3】Iijima, N., Tanaka, M., Mitsui, S., Yamamura, Y., Yamaguchi, N., Ibata, Y., Expression of a novel serine protease (motopsin PRSS12) mRNA in the mouse brain. :in situ hybridization histochemical study. Mol. Brain Res. 66, 141-149, 1999.
【非特許文献4】Yamamura, Y., Yamashiro, Y., Tsuruoka, N., Nakazato, H., Tsujimura, A., Yamaguchi, N., Molecular cloning of a novel brain-specific serine protease with a kringle-like structure and three scavenger receptor cysteine-rich motifs. Biochemical and Biophyical Research Communications 239, 386-392, 1997.
【発明の開示】
【発明が解決しようとする課題】
【0004】
上記のように、motopsinは中枢神経系の発達や高次機能発現を調節することが示唆されているが、その機能については依然不明な点が多い。motopsinの機能を解明することは、神経系における細胞外プロテオリシスの仕組みや、情動行動や記憶・学習などの神経活動を総合的に理解し解明することにもつながり、その臨床応用が期待されるものである。
本発明は、上記の問題点に着目してなされたものであり、その目的は、対人関係に関する心的障害の発生を防止する向精神薬の開発等に使用できるmotopsinノックアウト動物を提供すること、また、motopsinの機能抑制或いは向上、阻害活性の測定による向精神薬のスクリーニング方法を提供することにある。
【課題を解決するための手段】
【0005】
我々は、motopsinが中枢神経系においてニューロン、特に錐体ニューロン、に特異的に発現していることを見出した。また、顔面神経ニューロンをはじめとする運動ニューロンでのmotopsinの発現は、軸索損傷などの細胞傷害で一過的に減少するが、神経機能の回復とともにmotopsinの発現も回復することを明らかにした。さらに、motopsinのノックアウトマウスを作製した。このmotopsinノックアウトマウスは、明瞭な形態異常を示さなかったものの、行動検査において社会行動の亢進が認められた。神経解剖学的解析においても野生型とは異なるユニークな特徴を有するマウスであることが見出され、これにより本発明を完成するに至った。
【0006】
即ち、本発明は第1に、motopsin遺伝子のDNA配列の全部または一部を改変或いは欠損させることにより得られ、相同染色体上の双方のmotopsin遺伝子が破壊され、motopsinの発現が抑制されたことを特徴とするノックアウト非ヒト動物を提供するものである。
本発明における「motopsin遺伝子が破壊され」とは、換言すれば、motopsin遺伝子領域の配列が人為的に改変されることによって、motopsin遺伝子の正常な発現が阻害されていること、そしてその結果、motopsin全長タンパク質の発現が抑制され、生体(特に脳)においてmotopsinが正常に機能していないことを意味する。
本発明の「ゲノム中のmotopsin遺伝子のDNA配列の全部または一部を改変或いは欠損させること」における「全部」とは、motopsinゲノムDNAのエクソン1の5’端から最後のエクソンの3’端までの領域をいう。また、「一部」とは、この領域の一部であって、motopsin遺伝子の正常な発現を阻害するのに必要な範囲・長さの領域、をいう。さらに、「改変」とは、単一または複数のヌクレオチドを置換、欠失、挿入、及び/又は転位させることにより、ゲノムDNA中の対象領域の塩基配列を他の塩基配列に改変することをいう。
【0007】
本発明のノックアウト動物は、公知の方法で製作することができる。例えば、後述のように遺伝子ターゲッティング法を用いて作製することができる。同方法において、motopsin遺伝子のエクソン1の少なくとも開始コドンを含む領域を相同組み換えにより他の塩基配列に置換することは、motopsinの正常な発現を阻害できるため、好ましいものである。また、本発明のノックアウト動物は、同方法によって作製されたノックアウト動物のみならず、さらにその子孫をも含むものであり、好ましくは以下の1又は2以上の特徴を有する。
(a)野生型動物と比較して社会行動が相対的に亢進している。
(b)野生型動物と比較して海馬および大脳皮質のニューロンにおいて樹状突起スパイン密度が減少している。
本発明のノックアウト動物としては、実験動物として多用されているマウス又はラットであることが好ましいが、これに限定されるものではなく、他の非ヒト哺乳動物であってもよい。
【0008】
本発明はまた、産業上有用な発明として、下記A)〜D)の発明を包含するものである。
A) ゲノム中のmotopsin遺伝子のDNA配列の全部または一部を改変することにより得られ、相同染色体上のmotopsin遺伝子が破壊され、motopsinの発現が抑制されたことを特徴とするノックアウト動物細胞。
B)Motopsinの機能を阻害或いは向上する物質をスクリーニングすることを特徴とする向精神薬のスクリーニング方法。
C) 向精神薬が、抗自閉症、抗共依存症、又は対人行動改善剤であることを特徴とする上記B)記載のスクリーニング方法。
D) 本発明のmotopsinノックアウト動物を用いることを特徴とする上記B)記載のスクリーニング方法。
【発明を実施するための最良の形態】
【0009】
以下、本発明の実施形態、具体的態様等について説明する。
本発明のmotopsinノックアウト動物は、遺伝子ターゲッティング法などの公知の方法を用いて作製することができる。以下では、遺伝子ターゲッティング法を用いたmotopsinノックアウト動物の作製方法について簡単に説明する(詳細は後述の実施例にて図面を参照しながら説明する。)。
【0010】
〔1〕ターゲッティングベクターの作製
まず、ターゲッティングベクター(ターゲッティングコンストラクト)の作製のため、対象となる動物のmotopsin遺伝子の一部を単離する。例えば、ノックアウトマウスを作製する場合は、マウスのゲノムDNAライブラリーからmotopsin遺伝子をスクリーニングすればよい。スクリーニングの条件、方法は特に限定されず、スクリーニングに用いるプローブについてもゲノムDNAやcDNAからPCR法などを用いて容易に調製することができる。
【0011】
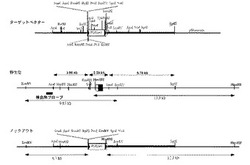
上記スクリーニングにより得られたゲノムDNAクローンを用いて、相同組み換えのためのターゲッティングベクターを構築する。ゲノムDNAクローンは勿論遺伝子全長である必要はなく、motopsin遺伝子を破壊しmotopsinの発現を抑制するために必要な領域のみクローニングすればよい。後述の実施例(マウス)においては、motopsinゲノムDNAのエクソン1(図1)を含む領域をサブクローニングし、開始コドンを含む領域を、相同組み換えにより他の塩基配列に置換することによってノックアウトマウスを作製した。
【0012】
ターゲッティングベクターは、公知の方法により作製することができ、大略、市販のプラスミドをバックボーンとして、上記ゲノムDNAクローン、ポジティブセレクション用のマーカー(PGKneoカセット等)、およびネガティブセレクション用のマーカー(DT−A遺伝子、HSV−tk遺伝子等)などの各フラグメントを適切に連結することにより作製することができる。このとき、目的とする制限酵素切断部位が適切な位置に配されるようターゲッティングベクターを設計するとよい。また、ターゲッティングの効率は相同領域の長さに依存するので、相同領域はできるだけ長いほうが好ましい。さらに、ターゲッティングベクターは環状より直鎖状のほうが好ましいので、直鎖状化のため相同領域以外の部分に一カ所適当な制限酵素切断部位を設けておくとよい。
【0013】
〔2〕Motopsinノックアウト動物の作製
上記方法により作製したターゲッティングベクターを、受精卵、初期胚、又は胚性幹細胞(ES細胞)などの個体形成能(分化全能性)をもつ細胞にエレクトロポレーション法等により導入し、その後、目的とする相同組み換えが起こった細胞を選別する。選別は、ポジティブ−ネガティブ選択法により薬剤を用いて効率よくスクリーニングできる。選別後、目的とする相同組み換えが起こった細胞を、サザンブロットやPCR法などによって確認する。最終的に所望の相同組み換えが確認された細胞を、妊娠中の輸卵管または子宮から採取された8細胞期胚または胚盤胞(ブラストシスト)に導入する。8細胞期胚または胚盤胞への細胞の導入は、マイクロインジェクション法等により行うことができるが、これに限定されるものではない。
【0014】
上記8細胞期胚または胚盤胞を常法に従い仮親に移植する。仮親から生まれた生殖系列キメラ動物(好ましくは雄)と、野生型motopsin遺伝子をホモで持つ野生型動物(好ましくは雌)とを交配させることにより、第1世代(F1)として、相同染色体上の一方のmotopsin遺伝子が相同組み換えにより破壊されたヘテロ接合体を得ることができる。さらに、これらヘテロ接合体同士を交配させることにより、第2世代(F2)として、相同染色体上の双方のPKN1motopsin遺伝子が破壊されたホモ接合体、即ち本発明のmotopsinノックアウト動物を得ることができる。ホモ接合体の同定は、体の一部(例えば尻尾)を切断し、DNAを抽出してサザンブロットやPCR法などによって遺伝子型を調べればよい。また、第2世代(F2)として、motopsinノックアウト動物と同腹の野生型動物(野生型遺伝子をホモで持つ)を得ることができるが、この野生型動物は対照実験に好適に用いることができる。
【0015】
Motopsinノックアウト動物の対象となる動物は、特に限定されるものではないが、ウシ、ブタ、ヒツジ、ヤギ、ウサギ、イヌ、ネコ、モルモット、ハムスター、マウス、ラットなどの哺乳動物が例示される。これらのうち、実験動物として用いるには、ウサギ、イヌ、ネコ、モルモット、ハムスター、マウス、ラットが好ましく、なかでも齧歯目がさらに好ましく、近交系が多数作出されており、受精卵の培養、体外受精等の技術が整っているマウス及びラットが、特に好ましい。
【0016】
以上説明した遺伝子ターゲッティング法は、あくまでその一例を示すものであって、公知の種々の変更が可能であることはいうまでもない。また、本発明以降に新たに開発された方法を使用するものであってもよい。
本発明のノックアウト動物細胞についても、上述した遺伝子ターゲッティング法によって作製可能である。
【0017】
〔3〕Motopsinノックアウト動物の利用法(有用性)
本発明のmotopsinノックアウト動物は、中枢神経系におけるmotopsin及びこれを阻害或いは活性化する物質の機能・役割について解析する研究ツールとして有用である。
【0018】
後述の実施例に示すように、実際にmotopsinノックアウトマウスを作製し種々の解析を行った結果、このmotopsinノックアウトマウスは明瞭な形態異常を示さず、また行動検査上、嗅覚依存探索行動、短期記憶学習、移動反応(locomotion)や立ち上がり反応(rearing)および不安行動も正常であった。しかしながら、motopsinノックアウトマウスは、ソーシャルレコグニションテストやレジデントイントルーダーテスト等でイントルーダーマウスに対してより長い間接触行動を示した。また、社会行動テストでは、既に提示されたファミリアなマウスに対する探索行動が延長していた。その一方、水迷路検査では野生型マウスと同等の学習能を示す実験結果が得られた。
【0019】
また、motopsinノックアウトマウスの脳スライス標本を用いた神経解剖的解析では、海馬や大脳皮質において樹状突起のスパイン密度の低下が観察された。
【0020】
これらの実験結果から、motopsinは、海馬や大脳皮質におけるシナプス形成あるいは発達・維持に関与し、motopsinの欠損は海馬や大脳皮質での機能低下が生じ、その結果、motopsinノックアウトマウスでは社会行動が亢進することが推測された。Motopsinノックアウトマウスは、神経細胞数の変化などの著しい形態異常は認められず、そのため、このような社会行動の変化はmotopsinの機能的抑制によって生じたものと考えられる。つまり、motopsinの阻害剤や活性化剤を投与し、社会行動の変化を測定することによって、抗自閉症薬、抗共依存症、対人行動改善剤などの向精神薬の候補物質の選択に用いることができる。
【0021】
このことは、motopsinの特異的阻害剤が向精神薬として医薬応用できることを示している。例えば、motopsin阻害剤によって自閉症を選択的に抑制する効果が得られ、臨床的には、motopsin阻害剤を自閉症改善薬として利用したり、motopsin亢進薬を対人依存症の予防薬とするなど、各種の精神神経疾患などに臨床応用することができる。
【0022】
〔4〕Motopsinの機能に着目した向精神薬のスクリーニング方法
上記のようにmotopsinの機能阻害物質は、自閉症治療薬、その他の心的作用、向精神作用を有する向精神薬として医薬応用し得ることが今回の解析の結果明らかになった。そこで本発明は、motopsinの機能阻害物質をスクリーニングすることを特徴とする向精神薬のスクリーニング方法を提供するものである。
【0023】
Motopsinの機能阻害物質としては、(a)motopsinの酵素活性を阻害する物質のほかに、(b)motopsinの発現を抑制することによってmotopsinの機能を阻害する物質、(c)motopsinの制御領域とアクチベーター(上流因子)との結合を阻害することによってmotopsinの機能を阻害する物質、が挙げられる。
【0024】
Motopsinはモザイク型セリンプロテアーゼファミリーであり、機能調節ドメインが各種の物質に結合して機能するので、motopsinの特異的・選択的阻害剤の探索のため、機能調節ドメインに着目したスクリーニングは好ましい方法である。具体的には、機能調節ドメインとの結合をin vitro又はin vivoにおいて阻害する物質を探索する方法である。
【0025】
この場合のスクリーニング方法としては、物質間の結合の有無や解離の有無を調べる従来公知の種々の方法を適用することができ、特に限定されるものではない。例えば、motopsinの機能調節ドメインを大腸菌等を用いて大量に発現させて精製し、試験管内での結合を蛍光基質などによって検出・測定する系を構築することができる。また、阻害剤のマススクリーニングに向けて98 wellまたは384 wellのマイクロタイタープレート等にmotopsinを固定し、それに結合したインヒビターを酵素、蛍光色素などで標識した抗体によって検出する系を確立することも可能である。
【0026】
motopsinとりわけその機能調節ドメインの高次構造の情報は、motopsinのニューロン上への局在を特異的に阻害する阻害剤の分子設計に有用であるので、このような情報を利用するものであってもよい。
【0027】
そのほか、(1)motopsinの機能調節ドメインをカラムに固定してこれと結合する物質を検索する方法や、(2)免疫沈降免疫ブロット法を用いてmotopsinの機能調節ドメインと相互作用蛋白質との結合を阻害する物質を検索する方法、(3)酵母two-hybrid法を用いて、motopsinの機能調節ドメインとの結合を検出する方法など、物質間の結合の有無や解離の有無を調べる従来公知の種々の方法を本発明のスクリーニング方法に適用可能である。また、本発明以降に新たに開発されたスクリーニング方法を使用するものであってもよい。
【0028】
Motopsinの機能調節ドメインとの結合活性をスクリーニングする方法の場合、使用するmotopsinは全長蛋白質であってもよいが、上述のように制御領域(又はその一部領域)に相当する部分蛋白質であっても勿論よい。
【0029】
また、このようなスクリーニング方法によって得られた活性阻害剤について、さらに海馬や大脳皮質のニューロンにおいて樹状突起スパイン密度を増加あるいは減少させる性質の有無を調べることによって、向精神薬を開発する方法は好ましい。
【0030】
勿論、本発明のスクリーニング方法として、motopsinの酵素活性を測定して被検物質のmotopsinに対する阻害効果、又は活性化効果を調べる方法を採用してもよい。例えば、精製したmotopsinとその基質(Z−Phe−Arg−MCA、ゼラチン、tissue plasminogen activator等)を用いて酵素活性の変化を測定する試験管内活性測定系(cell-free system)でのスクリーニング方法を挙げることができる。この方法の場合、多数の有機化合物のマススクリーニングのため、基質の加水分解の有無を蛍光等で検出する測定系を用いることが好ましい。
【0031】
精製酵素ではなく、細胞の粗精製画分を用いて、motopsinの活性測定を行ってもよい。この場合、motopsin以外の蛋白質分解酵素も存在するので、motopsin特異的な基質の加水分解の有無を検出する系を構築するなどの工夫が必要である。また、上記の方法は、試験管内反応系(cell-free system)でのスクリーニング方法であったが、培養細胞等を用いて細胞内で酵素活性を測定することによりスクリーニングを行ってもよい。
【0032】
その他、細胞内でのmotopsinの発現に影響を与え、その発現量を変化させる物質の探索には、常法に従ってmotopsinのmRNA量を定量する方法、あるいはmotopsin蛋白質の発現量を定量する方法などを採用することができる。
【実施例】
【0033】
以下、図面を参照しながら本発明の実施例について説明するが、本発明はこれら実施例によって何ら限定されるものではない。
〔方法〕
[1-1]Motopsinノックアウトマウスの作製
図1は、本実施例のmotopsinノックアウトマウスの作製に使用した遺伝子ターゲッティング法を説明する図である。図中、上から順に、正常のmotopsin遺伝子(Wild type allele)、motopsinノックアウトマウス作製のためのターゲッティングベクター(Targeting construct)、相同組み換えを起こしたmotopsin遺伝子破壊(変異)アレル(Disrupted allele)の構造をそれぞれ模式的に示す。
【0034】
まずターゲッティングベクター作製のため、マウスmotopsinのゲノムDNA約13kbをマウス129SvのゲノムDNAのPACライブラリーよりcDNAをプローブとしたハイブリダイゼーションによって調製した。得られたクローンをもとに、エクソン1の上流〜3.7kbpのApaI/SspI fragmentと、下流〜6.8kbpのSpeI/BglIIfragmentをアームとして、Neo耐性遺伝子の両側に挿入し、ターゲッティングベクターを作製した(図1)。なお、このターゲッティングベクターのバックボーンはpBluescriptである。
【0035】
上記ターゲッティングベクターを直鎖化後、129Sv ES細胞にエレクトロポレーションによって導入した。抗生物質G418耐性クローンをピックアップし、そのゲノムDNAを図1に示す5’プローブ(5’probe)および3’プローブ(3’probe)を用いたサザンブロッティングによって解析し、目的の相同組み換えが起こったアレル(Disrupted allele)を有するクローンを選択した。
【0036】
相同組み換えが起こった上記ES細胞のクローンを、公知の方法(Genes & Development 8,707−719, 1994)に従ってマウス初期胚にマイクロインジェクションすることにより、キメラマウスを得た。さらにこのキメラマウスを野生型C57BL/6Jマウスと交配し、得られたヘテロ接合体マウスの雌雄を交配することにより、ES細胞由来の変異アレルをホモで有するmotopsinノックアウトマウスを得ることができた。
【0037】
上記motopsinノックアウトマウスについて、C57BL/6Jとの戻し交配を6回以上繰り返して得られたmotopsinノックアウトマウスについて後述の行動実験を行った。
【0038】
[1-2]免疫化学的解析
抗motopsinポリクローナル抗体は、マウスmotopsinの組換え蛋白質をウサギに免疫して作製した(Brain Research 1136, 1−12, 2007)。マウスの脳は、9倍量の氷冷した1mM EDTA, 10μg/mL Leupeptin、10μg/mL Pepstatin,2mM phenylmethyl sulfonateを含むphosphate buffered saline(PBS,pH7.4)にて、ポリトロンを用いてホモジェナイズし、2倍濃度のSDS−polyacrilamide gel sample bufferと混和した。サンプルをSDS電気泳動後、polyvinylidene difluoride膜に転写し、1次抗体として抗motopsinポリクローナル抗体(2000倍希釈)、そして2次抗体として、AP−conjugated goat anti−rabbit IgG(CHEMICON,Temecula,CA)をTBS−T(50mM Tris−Cl, pH 7.4, 0.05% Tween−20)で希釈して使用した。免疫反応バンドの検出は、NBT/BCIP発色法によって行った。
【0039】
[1-3]免疫組織学的検査
組織切片の作製と免疫組織学的な解析は、既述の方法に従った(Brain Research 1136, 1−12, 2007)。以下に要点を記す。脳を4%パラホルムアルデヒド入りの0.1Mリン酸バッファー(PB,pH7,4)で灌流固定し、その後15時間同液で後固定を行った。そして20% sucrose in PBで2日間置いた後、クリオスタットで20μmの切片を調製した。切片は、0.3% H2O2/50% Methanol in PBで処理した後、1次抗体とインキュベートした。
【0040】
[1-4]ゴルジ染色
ゴルジ染色はGibbとKolbの方法(Journal of Neuroscience Methods 79, 1−4, 1998)に従って行った。深麻酔下でマウスをPBSで還流した後、脳を摘出してGolgi−Cox液(1%ニクロム酸カリウム、1%塩化水銀、1%クロム酸カリウム)につけて、暗所にて2週間以上放置する。30%sucrose in PBに2日以上つけた後ビブラトームにて180μmの厚さに薄切してスライドグラスに圧着させる。これをアンモニア水に浸して発色させた後、固定液(富士フイルムsuper Fuji fix)にて固定した。
【0041】
[1-5]行動学的検査
[1-5-1]オープンフィールドテスト
実験装置は天井部のない立方体の箱であった。側面および床面は厚さ3mmの透明アクリル版製で、内寸は、床部が40×40cm、高さが30cmであった。実験室は防音されており、実験装置内の被験動物の行動は天井部に設置した行動観察カメラによって撮影した。白熱灯点灯時の実験箱内の照度を床面で10Lux以下に設定した。
【0042】
各被験体に10分間のセッションを与えた。被験体を実験装置の中央部に置いてセッションを開始した。行動指標として、移動距離をビデオ撮影した画像を解析ソフト(エソビジョン)を用いて解析した。またセンタースクエアでの滞在時間を測定した。
【0043】
[1-5-2]高架式十字迷路テスト
10Lux以下の実験室に高架式十字(高さ50、アーム長30cm、通路幅5cm)を設置した。被験マウスを十字中央部に置き10分間自由に行動をさせて、その様子を天井部ビデオカメラにて撮影記録した。
【0044】
[1-5-3]ソーシャルレコグニションテスト
被験マウスと卵巣摘出術を施した雌マウスAを明所下で新しい飼育ケージにいれて1分間天井部のビデオカメラで撮影した後、雌マウスAを取り出した。5分後に再度雌マウスAを1分間、被験マウスに1分間提示・ビデオ撮影してとりだす。同様にして雌マウスAの提示を合計4回行った後、卵巣摘出術を施した別の雌マウスBを1分間被験マウスに提示して、その行動をビデオ撮影した。遺伝子型についての情報を持たない観察者が被験動物が提示動物に対して探索行動を示した時間を測定し、野生型マウスと比較した。
【0045】
Motopsinノックアウトマウスの雌マウスAに対する接触時間と雌マウスBに対する接触時間は、雌マウスA1回目34.7±2.6秒(平均値±標準誤差、以下同じ)、2回目39.3±2.4秒、3回目34.3±2.6秒、4回目33.0±3.3秒、雌マウスB;46.8±2.3秒であった。一方、野生型マウスにおいては、雌マウスA1回目30.5±4.0秒、2回目33.1±3.5秒、3回目26.0±3.8秒、4回目24.9±3.6秒、雌マウスB35.4±4.1秒であった。
【0046】
[1-5-4]レジデントイントルーダーテスト
被験マウスを1週間飼育したのち、イントルーダーマウスを被験マウスのケージに入れた。その後10分間の行動を天井に設置したビデオテープレコーダにて撮影記録した。
【0047】
Motopsinノックアウトマウスのイントルーダーマウスに対する接触時間および最初の接触までの潜時はそれぞれ、228.7±11.0秒、21.5±5.4秒であった。一方、野生型マウスでは169.4±28.4秒、37.9±8.8秒であった。
【0048】
[1-5-5]社会行動テスト
社会行動テストには、テストボックス(縦40cm×横60cm×高さ35cm)および2個の刺激動物用ワイヤーケージ(ステンレス製、直径11cm×高さ15cm)を用いた。まず、被験マウスを2個の空ワイヤーケージをいれたテストボックスに入れて10分間放置する。マウスのテストボックス内への解放はテストボックス中央においた円筒容器(直径11cm)にマウスを入れておき、検討容器を取り除くことで行った。一度マウスを円筒容器に戻し、一方のワイヤーケージに刺激用の雄マウス(刺激用マウスA)を入れた後、被験動物をテストボックス内を自由に10分間探索させる。再度、被験マウスを円筒容器に入れてから、空ワイヤーケージに新たに刺激用マウスBを入れる。円筒容器から試験動物を解放して10分間テストボックス内を自由に探索させる。以上の3セッションの間、天井よりビデオ撮影を行い、第2セッションでの被験マウスが空ワイヤーケージおよび刺激用マウスAのワイヤーケージに接触している時間、第3セッションでの刺激用マウスA,Bのワイヤーケージに接触している時間を計測し、motopsinノックアウトマウスと野生型マウスを比較した。
【0049】
社会性を検出するセッション2では、野生型マウス、motopsinノックアウトマウスが空ワイヤーケージvs刺激用マウスAワイヤーケージへ接触していた時間はそれぞれ4.5±1.0秒vs66.0±9.0秒、6.0±1.7秒vs77.0±8.1秒であった。新規社会に対する好気性を検出する第3セッションでの刺激用マウスAのワイヤーケージへの接触時間vs刺激用マウスBのそれに接触していた時間は、ノックアウトマウス;28.4±5.7秒vs49.0±7.3秒、野生型マウス;9.2±1.4秒vs37.5±7.0秒であった。
【0050】
[1-5-7]探索行動テスト
実験前日に10Lux以下の照度に設定した実験室にオープンフィールドテストで用いたフィールドを置き、その中に被験マウスを入れて30分間放置しフィールドに馴化させた。翌日、フィールド内の任意の位置にピンポン球を設置し、被験マウスを入れて10分間、行動をビデオ撮影する。被験マウスがピンポン球に接するまでの潜時と接している時間を計測した。
【0051】
Motopsinノックアウトマウスの潜時および接触時間は、35.0±14.0秒、8.8±1.4秒、であり、野生型マウスでは44.4±11.1秒、10.5±2.4秒であった。
【0052】
[1-5-6]嗅覚テスト
被験マウスは実験の12時間以上前より絶食しておいた。新しい飼育ケージの床敷きの下に飼育用飼料を隠しておいた。被験マウスをこのケージに投入してから、飼料を見つけるまでの潜時、および、飼料を見つけてから食するまでの時間を天井部より撮影したビデオ映像を元に測定した。
【0053】
Motopsinノックアウトマウスが飼料を見つけるまでの潜時、および見つけてから食するまでの時間は、それぞれ50.3±6.0秒、26.6±5.8秒であった。野生型マウスでは、72.3±12.9秒、60.6±12.4秒であった。
【0054】
[1-5-5]水迷路学習(WM)
実験装置は円筒形のプールと逃避台からなっていた。プールの内径は140cm、高さは60cmで、内壁は青色に塗装されていた。逃避台は直径10cm、厚さ3mmの円形アクリル版に台座を取り付けたものとした。プールの仮想の東西南北方向には、それぞれ、20cm四方の白いアクリル板に黒色の十字を貼り付けたもの(北)、同じく黒三角形を貼り付けたもの(南)、同じく黒正方形(東)、同じく黒丸(西)がプール内から見えるように掲げられていた。逃避台を仮想の北東方向に設置し、水位を逃避台の台面上約1cmに調節した。水はインクで白色に濁らせ、水温は21℃(±1℃)に維持した。
【0055】
1日1セッション5試行からなる獲得訓練を行った。逃避台のない北東以外の3象限いずれかの壁際から被験体をプールに投入して自由に遊泳させ、逃避台に達するまでの潜時を計測した。被験体が逃避台に載ると、10秒間そこに留めた。プールへ投入後60秒以内に被験体が逃避台に達しない場合は、実験者が逃避台の上へ誘導し、そこに10秒間留めた。投入する象限の順序は被験体毎にランダムとした。試行間間隔(逃避台から取り去ってから次にプールへ投入されるまでの時間)は30秒であった。
【0056】
最終日の試行セッションが終了して1時間後に避難台を取り除いて、被験マウスをプールに投入して、60秒間の遊泳させた(プローブテスト)。避難台のあった位置を通過する回数、潜時、および避難台があった象限での滞留割合を測定した。
【0057】
[1-5-8]Y迷路テスト
被験動物の短期記憶の程度はY迷路テストによって行った。照度30Luxの実験室に幅4cm、長さ40cmの通路を持つY字迷路を設置した。この迷路には高さ12cmの壁があるが、各壁の色は黄色(A)、グレー(B)、青色(C)といったように色彩が異なっている。迷路の中心に被験マウスを入れて8分間行動をビデオ撮影した。マウスは最も以前に進入した場所に進入する傾向があり、各通路への進入を記憶していればその進入順はABCABCABCのようになる。そこで異なる3つの通路に連続して進入した回数(上記の例では7)のその最大数(総進入数−2)に対する割合(%alternation)を短期記憶の程度として判定した。
【0058】
Motopsinノックアウトマウスは52.7±5.3%alternationを示し、野生型マウスは50.1±5.2%alternationを示した。
【0059】
〔結果〕
[2-1]
脳におけるmotopsinの機能を明らかにするため、図1に示すように、エクソン1aの開始コドンを含む領域をNeo耐性遺伝子で置き換えるターゲッティングベクターを構築し、motopsinノックアウトマウスを作製した。Motopsin遺伝子の欠落はサザンハイブリダイゼーションやPCR法によって確認できた。全体的な肉眼的および脳の光学顕微鏡検査において、motopsinノックアウトマウスは野生型マウスと明らかな差を認めなかった。特に中枢神経系に注意して観察を行ったが、皮質・海馬・線条体・小脳・視床・視床下部に明らかに異常な顕微鏡所見を認めなかった。また、仔マウスの遺伝子型は、正常のメンデル遺伝に従っていた。
【0060】
Motopsin mRNAの発現は野生型マウスやヘテロマウスではノーザンハイブリダイゼーションによって確認できたが、motopsinノックアウトマウスでは検出されなかった。Motopsinを認識する抗体を用いた免疫組織化学法の結果では、motopsinノックアウトマウス脳においては、motopsin陽性反応は検出されなかった。野生型マウス脳ではmotopsinは海馬、大脳皮質等で検出された(図2)。
【0061】
[2-2]Motopsinノックアウトマウスにおける情動行動
Motopsin欠損が、マウスの基礎的な神経機能に及ぼす影響を検討するため、motopsinノックアウトマウスの行動学的検査を行った。
Motopsinノックアウトマウスおよび野生型マウス用いてオープンフィールドテストを行った結果、それぞれの移動距離はmotopsinノックアウトマウスが2809.8±118.3cm、野生型マウスが2800.8±136.6cmであった。また、センタースクエアでの滞留時間はそれぞれ142.2±21.1秒、139.8±14.4秒であり、ゲノタイプによる差は認められなかった(図3)。また、高架式十字迷路の結果、motopsinノックアウトマウスのオープンアームでの滞留時間および進入比率は82.1±26.0秒、23.5±3.3%であり、野生型マウスでは54.9±15.6秒、19.6±2.4%であった(図4)。これらのことから、motopsinノックアウトマウスでは不安行動には異常が認められないといえる。
【0062】
[2-3]Motopsinノックアウトマウスにおける社会行動の異常
次に社会行動に障害があるかどうかを検討するため、ソーシャルレコグニションテスト、レジデントイントルーダーテスト、社会行動テストの3種類を行った(図5−7)。ソーシャルレコグニションテストでは、いずれのマウスも雌マウスAに対する接触時間がセッションを経るごとに有意に低下し、雌マウスBに対して有意に接触時間が遅延することから、刺激動物を認識していることが明らかである。しかし、意外なことにいずれの測定時点においてもmotopsinノックアウトマウスは野生型マウスに比べて有意に接触時間が長かった。この傾向は、レジデントイントルーダーテストにおいても確認された。
【0063】
社会行動テストにおいてもmotopsinノックアウトマウスは野生型マウスと異なる反応を示した。野生型マウスは第3セッションにおいて第2セッションで既に提示された刺激用マウスAに対しては接触時間が短くなるのに対して、motopsinノックアウトマウスは有意に長い接触時間を示した。以上の結果から、motopsinノックアウトマウスは社会行動が亢進しており、抗自閉症的な行動を示すことが明らかである。
【0064】
[2-4]Motopsinノックアウトマウスの探索および嗅覚行動
Motopsinノックアウトマウスにおいて観察された社会行動の亢進が社会的要素に特異的であること、および嗅覚異常に起因するもので無いことを確認するために、探索行動テストと嗅覚テストを行った(図8,9)。探索行動テストでは、無機物質に対する接触時間および最初に接触するまでの潜時にmotopsinノックアウトマウスと野生型マウスに差は認められなかった。嗅覚テストにおいても、餌を見つけるまでの時間にゲノタイプ間で有意差は認められなかったが、餌を見つけてから食べるまでの時間はmotopsinノックアウトマウスで有意に短かった。Motopsinノックアウトマウスによる無機物に対する野生型マウスと同様の反応性は社会性行動テストのセッション2において、空ケージに対する接触時間が両者において差が認められなかったことからも明らかである。従って、motopsinノックアウトマウスは社会性行動特有の異常を呈すると考えられた。
【0065】
[2-5]Motopsinノックアウトマウスの空間学習能
Motopsinノックアウトマウスの空間学習能を検討するために、モリス水迷路学習テストとY迷路テストを行った(図10,11)。モリス水迷路学習テストの獲得訓練では、motopsinノックアウトマウスは野生型マウスと同等の学習能を示した。プローブテストの結果、避難台領域を通過する回数、避難台があった象限での滞留時間も野生型マウスと同等であったが、避難台領域に到達する潜時がmotopsinノックアウトマウスでは有意に遅延していた。一方、Y迷路テストではmotopsinノックアウトマウスは野生型マウスと同等の%alternationを示したことから、短期記憶については異常が認められないといえる。
【0066】
[2-5]Motopsinノックアウトマウスのスパイン密度の低下
Motopsinノックアウトマウスが呈する行動学的異常の発症機構を明らかにするためにゴルジ染色によるニューロンの形態観察を行った。その結果、海馬の錐体ニューロンの20μm当たりのスパイン密度はmotopsinノックアウトマウスでは、頂上樹状突起では7.7±0.4個であり、基底樹状突起では8.4±0.2個であった。野生型マウスにおいてはそれぞれ、8.9±0.4個、8.3±0.2個であり、頂上樹状突起においてmotopsinノックアウトマウスは有意にスパイン密度が減少していた(図12)。
【0067】
[2-6]本実施例の結果と考察
今回motopsinノックアウトマウスにおいて、社会行動の亢進や空間記憶能の低下が認められ、また神経解剖学的検査において、海馬錐体ニューロンにおけるスパイン密度が低下するという現象が認められた。
【0068】
Motopsinノックアウトマウスがこれらの現象を引き起こした分子メカニズムについては今後更なる解析を要するが、近年、精神遅滞の原因遺伝子があいついで同定されてニューロンの細胞内情報伝達機構が乱れることでスパインの形態異常が引き起こされることが一因であると考えられつつある。しかし、従来知られている精神遅滞原因遺伝子が細胞内情報伝達に関わる分子であるのに対してmotopsinは細胞外に分泌されるプロテアーゼであることから、薬剤による制御がより容易であり、各種神経疾患に対する新たな治療・診断法を提供することができる。
【0069】
最近、tenascinCノックアウトマウスでは社会行動が向上していることが報告された。(European Journal of Neuroscience 23, 1255−1265, 2006)。しかし、このマウスでは不安反応の低下や探索行動の亢進が認められており、社会行動に特異的な変化とは言い難い。また、以前より精神遅滞原因遺伝子の欠損マウスに社会行動の異常が見られると報告されている。例えば、Mecp2に分断変異を持つマウスやSecretin受容体ノックアウトマウスでは刺激動物との接触時間が著しく減少することが報告されている(Journal of Neuroscience 26, 319−327, 2006、Human Molecular Genetics 15, 3241−3250, 2006)。しかし、これらのマウスでは社会行動以外にもロコモーター活性、空間学習能、不安行動等に異常が認められ、社会行動が特異的に亢進しているmotopsinノックアウトマウスとは表現型が異なっている。
【0070】
今回motopsinノックアウトマウスにおいては、社会行動の亢進が認められるものの、不安行動や空間学習能、社会性認識能力、探索行動などは正常であるという現象は非常ユニークである。このことは、motopsinの特異的阻害薬の探索が、抗自閉症薬など社会適応行動の亢進のための新薬開発につながることを示すものである。
【図面の簡単な説明】
【0071】
【図1】本発明の実施例に係るmotopsinノックアウトマウスの作出に用いた遺伝子ターゲッティング法を説明する図である。
【図2】Motopsinノックアウトマウスにおいてmotopsinの発現が認められないことをノーザンハイブリダイゼーションおよび免疫組織化学法によって確認したことを説明する図である。
【図3】オープンフィールドテストにおける移動反応とセンタースクエアでの滞在時間の測定結果を示すグラフである。
【図4】高架式十字迷路におけるオープンアームでの滞留時間および進入割合を示すグラフである。
【図5】ソーシャルレコグニションテストにおいて刺激動物との接触時間の測定結果を示すグラフである。
【図6】レジデントイントルーダーテストにおいて刺激動物との接触時間の測定結果を示すグラフである。
【図7】社会行動テストにおいて、空ワイヤーケージおよび刺激用マウスの入ったワイヤーケージへの接触時間結果を示すグラフである。
【図8】探索行動テストにおいて、無機物質へ接触するまでの潜時と接触時間の測定結果を示すグラフである。
【図9】嗅覚行動テストにおいて、餌を見つけるまでの潜時と見つけてから食するまでの時間の測定結果を示すグラフである。
【図10】モリス水迷路において、獲得訓練時の避難台への逃避時間の測定結果とプローブテスト時の各象限への滞在時間、仮想避難台への到達するまでの潜時を測定した結果を示すグラフである。
【図11】Y迷路テストにおける%alternationを示すグラフである。
【図12】海馬錐体ニューロンにおける樹状突起スパイン密度を計測した結果を示すグラフである。
【技術分野】
【0001】
本発明は、motopsin遺伝子欠損動物と向精神薬開発に関し、より詳しくは、正常動物に比し社会行動が亢進しているmotopsin遺伝子欠損非ヒト動物、同遺伝子欠損動物又はmotopsinを用いた向精神薬のスクリーニング方法に関する。
【背景技術】
【0002】
Motopsinは、一次構造上セリンプロテアーゼの触媒領域において高い相同性を有しながら、プロリンリッチ領域、クリングル領域、スカベンジャーレセプターシステインリッチ領域を含む特徴的な制御領域をもつ蛋白質分解酵素(セリンプロテアーゼ)である。
【0003】
Motopsinは、脳や脊髄といった中枢神経系に豊富に含まれるが、肺や腎臓、皮膚にも存在している。MotopsinはSondereggerらが我々と同時期にneurotrypsinと報告した分子、HUGO nomenclatureによりprss12として認定された分子と同一のものである。特に胎児期後期から新生児期の神経系に高発現することが知られている。Motopsinは、in vitroにおいてゼラチンやtissue plasminogen activatorを分解することが報告されている。また、非症候群性精神遅滞の家系において第7エクソンの4塩基欠損によるナンセンス変異が報告されている。さらに、ショウジョウバエにおいてmotopsinオルソローグの欠損が長期記憶を障害することが報告されている。Motopsinの発現は神経機能の維持に重要であることが軸索傷害実験から示されている。また、motopsin蛋白質が主にニューロンの細胞体や樹状突起基部に存在しており、発現量が増加すると軸索にも輸送されることなども報告されている。しかしながら、ほ乳類を含む脊椎動物の脳内機能はほとんど知られておらず、motopsin欠損による発達障害発症機構は未だ十分に解明されていない。
【非特許文献1】Mitsui, S., Yamaguchi, N., Osako, Y., Yuri, K., Enzymatic properties and localization of motopsin (PRSS12), a protease whose absence causes mental retardation. Brain Research 1136, 1-12, 2007.
【非特許文献2】Numajiri, T., Mitsui, S., Hisa, Y., Ishida, T., Nishino, K., Yamaguchi, N., The expression of a motoneuron-specific serine protease, motopsin (PRSS12), after facial nerve axotomy in mice. Journal of Plastic, Reconstructive & Aesthetic Surgery 59, 393-397, 2006.
【非特許文献3】Iijima, N., Tanaka, M., Mitsui, S., Yamamura, Y., Yamaguchi, N., Ibata, Y., Expression of a novel serine protease (motopsin PRSS12) mRNA in the mouse brain. :in situ hybridization histochemical study. Mol. Brain Res. 66, 141-149, 1999.
【非特許文献4】Yamamura, Y., Yamashiro, Y., Tsuruoka, N., Nakazato, H., Tsujimura, A., Yamaguchi, N., Molecular cloning of a novel brain-specific serine protease with a kringle-like structure and three scavenger receptor cysteine-rich motifs. Biochemical and Biophyical Research Communications 239, 386-392, 1997.
【発明の開示】
【発明が解決しようとする課題】
【0004】
上記のように、motopsinは中枢神経系の発達や高次機能発現を調節することが示唆されているが、その機能については依然不明な点が多い。motopsinの機能を解明することは、神経系における細胞外プロテオリシスの仕組みや、情動行動や記憶・学習などの神経活動を総合的に理解し解明することにもつながり、その臨床応用が期待されるものである。
本発明は、上記の問題点に着目してなされたものであり、その目的は、対人関係に関する心的障害の発生を防止する向精神薬の開発等に使用できるmotopsinノックアウト動物を提供すること、また、motopsinの機能抑制或いは向上、阻害活性の測定による向精神薬のスクリーニング方法を提供することにある。
【課題を解決するための手段】
【0005】
我々は、motopsinが中枢神経系においてニューロン、特に錐体ニューロン、に特異的に発現していることを見出した。また、顔面神経ニューロンをはじめとする運動ニューロンでのmotopsinの発現は、軸索損傷などの細胞傷害で一過的に減少するが、神経機能の回復とともにmotopsinの発現も回復することを明らかにした。さらに、motopsinのノックアウトマウスを作製した。このmotopsinノックアウトマウスは、明瞭な形態異常を示さなかったものの、行動検査において社会行動の亢進が認められた。神経解剖学的解析においても野生型とは異なるユニークな特徴を有するマウスであることが見出され、これにより本発明を完成するに至った。
【0006】
即ち、本発明は第1に、motopsin遺伝子のDNA配列の全部または一部を改変或いは欠損させることにより得られ、相同染色体上の双方のmotopsin遺伝子が破壊され、motopsinの発現が抑制されたことを特徴とするノックアウト非ヒト動物を提供するものである。
本発明における「motopsin遺伝子が破壊され」とは、換言すれば、motopsin遺伝子領域の配列が人為的に改変されることによって、motopsin遺伝子の正常な発現が阻害されていること、そしてその結果、motopsin全長タンパク質の発現が抑制され、生体(特に脳)においてmotopsinが正常に機能していないことを意味する。
本発明の「ゲノム中のmotopsin遺伝子のDNA配列の全部または一部を改変或いは欠損させること」における「全部」とは、motopsinゲノムDNAのエクソン1の5’端から最後のエクソンの3’端までの領域をいう。また、「一部」とは、この領域の一部であって、motopsin遺伝子の正常な発現を阻害するのに必要な範囲・長さの領域、をいう。さらに、「改変」とは、単一または複数のヌクレオチドを置換、欠失、挿入、及び/又は転位させることにより、ゲノムDNA中の対象領域の塩基配列を他の塩基配列に改変することをいう。
【0007】
本発明のノックアウト動物は、公知の方法で製作することができる。例えば、後述のように遺伝子ターゲッティング法を用いて作製することができる。同方法において、motopsin遺伝子のエクソン1の少なくとも開始コドンを含む領域を相同組み換えにより他の塩基配列に置換することは、motopsinの正常な発現を阻害できるため、好ましいものである。また、本発明のノックアウト動物は、同方法によって作製されたノックアウト動物のみならず、さらにその子孫をも含むものであり、好ましくは以下の1又は2以上の特徴を有する。
(a)野生型動物と比較して社会行動が相対的に亢進している。
(b)野生型動物と比較して海馬および大脳皮質のニューロンにおいて樹状突起スパイン密度が減少している。
本発明のノックアウト動物としては、実験動物として多用されているマウス又はラットであることが好ましいが、これに限定されるものではなく、他の非ヒト哺乳動物であってもよい。
【0008】
本発明はまた、産業上有用な発明として、下記A)〜D)の発明を包含するものである。
A) ゲノム中のmotopsin遺伝子のDNA配列の全部または一部を改変することにより得られ、相同染色体上のmotopsin遺伝子が破壊され、motopsinの発現が抑制されたことを特徴とするノックアウト動物細胞。
B)Motopsinの機能を阻害或いは向上する物質をスクリーニングすることを特徴とする向精神薬のスクリーニング方法。
C) 向精神薬が、抗自閉症、抗共依存症、又は対人行動改善剤であることを特徴とする上記B)記載のスクリーニング方法。
D) 本発明のmotopsinノックアウト動物を用いることを特徴とする上記B)記載のスクリーニング方法。
【発明を実施するための最良の形態】
【0009】
以下、本発明の実施形態、具体的態様等について説明する。
本発明のmotopsinノックアウト動物は、遺伝子ターゲッティング法などの公知の方法を用いて作製することができる。以下では、遺伝子ターゲッティング法を用いたmotopsinノックアウト動物の作製方法について簡単に説明する(詳細は後述の実施例にて図面を参照しながら説明する。)。
【0010】
〔1〕ターゲッティングベクターの作製
まず、ターゲッティングベクター(ターゲッティングコンストラクト)の作製のため、対象となる動物のmotopsin遺伝子の一部を単離する。例えば、ノックアウトマウスを作製する場合は、マウスのゲノムDNAライブラリーからmotopsin遺伝子をスクリーニングすればよい。スクリーニングの条件、方法は特に限定されず、スクリーニングに用いるプローブについてもゲノムDNAやcDNAからPCR法などを用いて容易に調製することができる。
【0011】
上記スクリーニングにより得られたゲノムDNAクローンを用いて、相同組み換えのためのターゲッティングベクターを構築する。ゲノムDNAクローンは勿論遺伝子全長である必要はなく、motopsin遺伝子を破壊しmotopsinの発現を抑制するために必要な領域のみクローニングすればよい。後述の実施例(マウス)においては、motopsinゲノムDNAのエクソン1(図1)を含む領域をサブクローニングし、開始コドンを含む領域を、相同組み換えにより他の塩基配列に置換することによってノックアウトマウスを作製した。
【0012】
ターゲッティングベクターは、公知の方法により作製することができ、大略、市販のプラスミドをバックボーンとして、上記ゲノムDNAクローン、ポジティブセレクション用のマーカー(PGKneoカセット等)、およびネガティブセレクション用のマーカー(DT−A遺伝子、HSV−tk遺伝子等)などの各フラグメントを適切に連結することにより作製することができる。このとき、目的とする制限酵素切断部位が適切な位置に配されるようターゲッティングベクターを設計するとよい。また、ターゲッティングの効率は相同領域の長さに依存するので、相同領域はできるだけ長いほうが好ましい。さらに、ターゲッティングベクターは環状より直鎖状のほうが好ましいので、直鎖状化のため相同領域以外の部分に一カ所適当な制限酵素切断部位を設けておくとよい。
【0013】
〔2〕Motopsinノックアウト動物の作製
上記方法により作製したターゲッティングベクターを、受精卵、初期胚、又は胚性幹細胞(ES細胞)などの個体形成能(分化全能性)をもつ細胞にエレクトロポレーション法等により導入し、その後、目的とする相同組み換えが起こった細胞を選別する。選別は、ポジティブ−ネガティブ選択法により薬剤を用いて効率よくスクリーニングできる。選別後、目的とする相同組み換えが起こった細胞を、サザンブロットやPCR法などによって確認する。最終的に所望の相同組み換えが確認された細胞を、妊娠中の輸卵管または子宮から採取された8細胞期胚または胚盤胞(ブラストシスト)に導入する。8細胞期胚または胚盤胞への細胞の導入は、マイクロインジェクション法等により行うことができるが、これに限定されるものではない。
【0014】
上記8細胞期胚または胚盤胞を常法に従い仮親に移植する。仮親から生まれた生殖系列キメラ動物(好ましくは雄)と、野生型motopsin遺伝子をホモで持つ野生型動物(好ましくは雌)とを交配させることにより、第1世代(F1)として、相同染色体上の一方のmotopsin遺伝子が相同組み換えにより破壊されたヘテロ接合体を得ることができる。さらに、これらヘテロ接合体同士を交配させることにより、第2世代(F2)として、相同染色体上の双方のPKN1motopsin遺伝子が破壊されたホモ接合体、即ち本発明のmotopsinノックアウト動物を得ることができる。ホモ接合体の同定は、体の一部(例えば尻尾)を切断し、DNAを抽出してサザンブロットやPCR法などによって遺伝子型を調べればよい。また、第2世代(F2)として、motopsinノックアウト動物と同腹の野生型動物(野生型遺伝子をホモで持つ)を得ることができるが、この野生型動物は対照実験に好適に用いることができる。
【0015】
Motopsinノックアウト動物の対象となる動物は、特に限定されるものではないが、ウシ、ブタ、ヒツジ、ヤギ、ウサギ、イヌ、ネコ、モルモット、ハムスター、マウス、ラットなどの哺乳動物が例示される。これらのうち、実験動物として用いるには、ウサギ、イヌ、ネコ、モルモット、ハムスター、マウス、ラットが好ましく、なかでも齧歯目がさらに好ましく、近交系が多数作出されており、受精卵の培養、体外受精等の技術が整っているマウス及びラットが、特に好ましい。
【0016】
以上説明した遺伝子ターゲッティング法は、あくまでその一例を示すものであって、公知の種々の変更が可能であることはいうまでもない。また、本発明以降に新たに開発された方法を使用するものであってもよい。
本発明のノックアウト動物細胞についても、上述した遺伝子ターゲッティング法によって作製可能である。
【0017】
〔3〕Motopsinノックアウト動物の利用法(有用性)
本発明のmotopsinノックアウト動物は、中枢神経系におけるmotopsin及びこれを阻害或いは活性化する物質の機能・役割について解析する研究ツールとして有用である。
【0018】
後述の実施例に示すように、実際にmotopsinノックアウトマウスを作製し種々の解析を行った結果、このmotopsinノックアウトマウスは明瞭な形態異常を示さず、また行動検査上、嗅覚依存探索行動、短期記憶学習、移動反応(locomotion)や立ち上がり反応(rearing)および不安行動も正常であった。しかしながら、motopsinノックアウトマウスは、ソーシャルレコグニションテストやレジデントイントルーダーテスト等でイントルーダーマウスに対してより長い間接触行動を示した。また、社会行動テストでは、既に提示されたファミリアなマウスに対する探索行動が延長していた。その一方、水迷路検査では野生型マウスと同等の学習能を示す実験結果が得られた。
【0019】
また、motopsinノックアウトマウスの脳スライス標本を用いた神経解剖的解析では、海馬や大脳皮質において樹状突起のスパイン密度の低下が観察された。
【0020】
これらの実験結果から、motopsinは、海馬や大脳皮質におけるシナプス形成あるいは発達・維持に関与し、motopsinの欠損は海馬や大脳皮質での機能低下が生じ、その結果、motopsinノックアウトマウスでは社会行動が亢進することが推測された。Motopsinノックアウトマウスは、神経細胞数の変化などの著しい形態異常は認められず、そのため、このような社会行動の変化はmotopsinの機能的抑制によって生じたものと考えられる。つまり、motopsinの阻害剤や活性化剤を投与し、社会行動の変化を測定することによって、抗自閉症薬、抗共依存症、対人行動改善剤などの向精神薬の候補物質の選択に用いることができる。
【0021】
このことは、motopsinの特異的阻害剤が向精神薬として医薬応用できることを示している。例えば、motopsin阻害剤によって自閉症を選択的に抑制する効果が得られ、臨床的には、motopsin阻害剤を自閉症改善薬として利用したり、motopsin亢進薬を対人依存症の予防薬とするなど、各種の精神神経疾患などに臨床応用することができる。
【0022】
〔4〕Motopsinの機能に着目した向精神薬のスクリーニング方法
上記のようにmotopsinの機能阻害物質は、自閉症治療薬、その他の心的作用、向精神作用を有する向精神薬として医薬応用し得ることが今回の解析の結果明らかになった。そこで本発明は、motopsinの機能阻害物質をスクリーニングすることを特徴とする向精神薬のスクリーニング方法を提供するものである。
【0023】
Motopsinの機能阻害物質としては、(a)motopsinの酵素活性を阻害する物質のほかに、(b)motopsinの発現を抑制することによってmotopsinの機能を阻害する物質、(c)motopsinの制御領域とアクチベーター(上流因子)との結合を阻害することによってmotopsinの機能を阻害する物質、が挙げられる。
【0024】
Motopsinはモザイク型セリンプロテアーゼファミリーであり、機能調節ドメインが各種の物質に結合して機能するので、motopsinの特異的・選択的阻害剤の探索のため、機能調節ドメインに着目したスクリーニングは好ましい方法である。具体的には、機能調節ドメインとの結合をin vitro又はin vivoにおいて阻害する物質を探索する方法である。
【0025】
この場合のスクリーニング方法としては、物質間の結合の有無や解離の有無を調べる従来公知の種々の方法を適用することができ、特に限定されるものではない。例えば、motopsinの機能調節ドメインを大腸菌等を用いて大量に発現させて精製し、試験管内での結合を蛍光基質などによって検出・測定する系を構築することができる。また、阻害剤のマススクリーニングに向けて98 wellまたは384 wellのマイクロタイタープレート等にmotopsinを固定し、それに結合したインヒビターを酵素、蛍光色素などで標識した抗体によって検出する系を確立することも可能である。
【0026】
motopsinとりわけその機能調節ドメインの高次構造の情報は、motopsinのニューロン上への局在を特異的に阻害する阻害剤の分子設計に有用であるので、このような情報を利用するものであってもよい。
【0027】
そのほか、(1)motopsinの機能調節ドメインをカラムに固定してこれと結合する物質を検索する方法や、(2)免疫沈降免疫ブロット法を用いてmotopsinの機能調節ドメインと相互作用蛋白質との結合を阻害する物質を検索する方法、(3)酵母two-hybrid法を用いて、motopsinの機能調節ドメインとの結合を検出する方法など、物質間の結合の有無や解離の有無を調べる従来公知の種々の方法を本発明のスクリーニング方法に適用可能である。また、本発明以降に新たに開発されたスクリーニング方法を使用するものであってもよい。
【0028】
Motopsinの機能調節ドメインとの結合活性をスクリーニングする方法の場合、使用するmotopsinは全長蛋白質であってもよいが、上述のように制御領域(又はその一部領域)に相当する部分蛋白質であっても勿論よい。
【0029】
また、このようなスクリーニング方法によって得られた活性阻害剤について、さらに海馬や大脳皮質のニューロンにおいて樹状突起スパイン密度を増加あるいは減少させる性質の有無を調べることによって、向精神薬を開発する方法は好ましい。
【0030】
勿論、本発明のスクリーニング方法として、motopsinの酵素活性を測定して被検物質のmotopsinに対する阻害効果、又は活性化効果を調べる方法を採用してもよい。例えば、精製したmotopsinとその基質(Z−Phe−Arg−MCA、ゼラチン、tissue plasminogen activator等)を用いて酵素活性の変化を測定する試験管内活性測定系(cell-free system)でのスクリーニング方法を挙げることができる。この方法の場合、多数の有機化合物のマススクリーニングのため、基質の加水分解の有無を蛍光等で検出する測定系を用いることが好ましい。
【0031】
精製酵素ではなく、細胞の粗精製画分を用いて、motopsinの活性測定を行ってもよい。この場合、motopsin以外の蛋白質分解酵素も存在するので、motopsin特異的な基質の加水分解の有無を検出する系を構築するなどの工夫が必要である。また、上記の方法は、試験管内反応系(cell-free system)でのスクリーニング方法であったが、培養細胞等を用いて細胞内で酵素活性を測定することによりスクリーニングを行ってもよい。
【0032】
その他、細胞内でのmotopsinの発現に影響を与え、その発現量を変化させる物質の探索には、常法に従ってmotopsinのmRNA量を定量する方法、あるいはmotopsin蛋白質の発現量を定量する方法などを採用することができる。
【実施例】
【0033】
以下、図面を参照しながら本発明の実施例について説明するが、本発明はこれら実施例によって何ら限定されるものではない。
〔方法〕
[1-1]Motopsinノックアウトマウスの作製
図1は、本実施例のmotopsinノックアウトマウスの作製に使用した遺伝子ターゲッティング法を説明する図である。図中、上から順に、正常のmotopsin遺伝子(Wild type allele)、motopsinノックアウトマウス作製のためのターゲッティングベクター(Targeting construct)、相同組み換えを起こしたmotopsin遺伝子破壊(変異)アレル(Disrupted allele)の構造をそれぞれ模式的に示す。
【0034】
まずターゲッティングベクター作製のため、マウスmotopsinのゲノムDNA約13kbをマウス129SvのゲノムDNAのPACライブラリーよりcDNAをプローブとしたハイブリダイゼーションによって調製した。得られたクローンをもとに、エクソン1の上流〜3.7kbpのApaI/SspI fragmentと、下流〜6.8kbpのSpeI/BglIIfragmentをアームとして、Neo耐性遺伝子の両側に挿入し、ターゲッティングベクターを作製した(図1)。なお、このターゲッティングベクターのバックボーンはpBluescriptである。
【0035】
上記ターゲッティングベクターを直鎖化後、129Sv ES細胞にエレクトロポレーションによって導入した。抗生物質G418耐性クローンをピックアップし、そのゲノムDNAを図1に示す5’プローブ(5’probe)および3’プローブ(3’probe)を用いたサザンブロッティングによって解析し、目的の相同組み換えが起こったアレル(Disrupted allele)を有するクローンを選択した。
【0036】
相同組み換えが起こった上記ES細胞のクローンを、公知の方法(Genes & Development 8,707−719, 1994)に従ってマウス初期胚にマイクロインジェクションすることにより、キメラマウスを得た。さらにこのキメラマウスを野生型C57BL/6Jマウスと交配し、得られたヘテロ接合体マウスの雌雄を交配することにより、ES細胞由来の変異アレルをホモで有するmotopsinノックアウトマウスを得ることができた。
【0037】
上記motopsinノックアウトマウスについて、C57BL/6Jとの戻し交配を6回以上繰り返して得られたmotopsinノックアウトマウスについて後述の行動実験を行った。
【0038】
[1-2]免疫化学的解析
抗motopsinポリクローナル抗体は、マウスmotopsinの組換え蛋白質をウサギに免疫して作製した(Brain Research 1136, 1−12, 2007)。マウスの脳は、9倍量の氷冷した1mM EDTA, 10μg/mL Leupeptin、10μg/mL Pepstatin,2mM phenylmethyl sulfonateを含むphosphate buffered saline(PBS,pH7.4)にて、ポリトロンを用いてホモジェナイズし、2倍濃度のSDS−polyacrilamide gel sample bufferと混和した。サンプルをSDS電気泳動後、polyvinylidene difluoride膜に転写し、1次抗体として抗motopsinポリクローナル抗体(2000倍希釈)、そして2次抗体として、AP−conjugated goat anti−rabbit IgG(CHEMICON,Temecula,CA)をTBS−T(50mM Tris−Cl, pH 7.4, 0.05% Tween−20)で希釈して使用した。免疫反応バンドの検出は、NBT/BCIP発色法によって行った。
【0039】
[1-3]免疫組織学的検査
組織切片の作製と免疫組織学的な解析は、既述の方法に従った(Brain Research 1136, 1−12, 2007)。以下に要点を記す。脳を4%パラホルムアルデヒド入りの0.1Mリン酸バッファー(PB,pH7,4)で灌流固定し、その後15時間同液で後固定を行った。そして20% sucrose in PBで2日間置いた後、クリオスタットで20μmの切片を調製した。切片は、0.3% H2O2/50% Methanol in PBで処理した後、1次抗体とインキュベートした。
【0040】
[1-4]ゴルジ染色
ゴルジ染色はGibbとKolbの方法(Journal of Neuroscience Methods 79, 1−4, 1998)に従って行った。深麻酔下でマウスをPBSで還流した後、脳を摘出してGolgi−Cox液(1%ニクロム酸カリウム、1%塩化水銀、1%クロム酸カリウム)につけて、暗所にて2週間以上放置する。30%sucrose in PBに2日以上つけた後ビブラトームにて180μmの厚さに薄切してスライドグラスに圧着させる。これをアンモニア水に浸して発色させた後、固定液(富士フイルムsuper Fuji fix)にて固定した。
【0041】
[1-5]行動学的検査
[1-5-1]オープンフィールドテスト
実験装置は天井部のない立方体の箱であった。側面および床面は厚さ3mmの透明アクリル版製で、内寸は、床部が40×40cm、高さが30cmであった。実験室は防音されており、実験装置内の被験動物の行動は天井部に設置した行動観察カメラによって撮影した。白熱灯点灯時の実験箱内の照度を床面で10Lux以下に設定した。
【0042】
各被験体に10分間のセッションを与えた。被験体を実験装置の中央部に置いてセッションを開始した。行動指標として、移動距離をビデオ撮影した画像を解析ソフト(エソビジョン)を用いて解析した。またセンタースクエアでの滞在時間を測定した。
【0043】
[1-5-2]高架式十字迷路テスト
10Lux以下の実験室に高架式十字(高さ50、アーム長30cm、通路幅5cm)を設置した。被験マウスを十字中央部に置き10分間自由に行動をさせて、その様子を天井部ビデオカメラにて撮影記録した。
【0044】
[1-5-3]ソーシャルレコグニションテスト
被験マウスと卵巣摘出術を施した雌マウスAを明所下で新しい飼育ケージにいれて1分間天井部のビデオカメラで撮影した後、雌マウスAを取り出した。5分後に再度雌マウスAを1分間、被験マウスに1分間提示・ビデオ撮影してとりだす。同様にして雌マウスAの提示を合計4回行った後、卵巣摘出術を施した別の雌マウスBを1分間被験マウスに提示して、その行動をビデオ撮影した。遺伝子型についての情報を持たない観察者が被験動物が提示動物に対して探索行動を示した時間を測定し、野生型マウスと比較した。
【0045】
Motopsinノックアウトマウスの雌マウスAに対する接触時間と雌マウスBに対する接触時間は、雌マウスA1回目34.7±2.6秒(平均値±標準誤差、以下同じ)、2回目39.3±2.4秒、3回目34.3±2.6秒、4回目33.0±3.3秒、雌マウスB;46.8±2.3秒であった。一方、野生型マウスにおいては、雌マウスA1回目30.5±4.0秒、2回目33.1±3.5秒、3回目26.0±3.8秒、4回目24.9±3.6秒、雌マウスB35.4±4.1秒であった。
【0046】
[1-5-4]レジデントイントルーダーテスト
被験マウスを1週間飼育したのち、イントルーダーマウスを被験マウスのケージに入れた。その後10分間の行動を天井に設置したビデオテープレコーダにて撮影記録した。
【0047】
Motopsinノックアウトマウスのイントルーダーマウスに対する接触時間および最初の接触までの潜時はそれぞれ、228.7±11.0秒、21.5±5.4秒であった。一方、野生型マウスでは169.4±28.4秒、37.9±8.8秒であった。
【0048】
[1-5-5]社会行動テスト
社会行動テストには、テストボックス(縦40cm×横60cm×高さ35cm)および2個の刺激動物用ワイヤーケージ(ステンレス製、直径11cm×高さ15cm)を用いた。まず、被験マウスを2個の空ワイヤーケージをいれたテストボックスに入れて10分間放置する。マウスのテストボックス内への解放はテストボックス中央においた円筒容器(直径11cm)にマウスを入れておき、検討容器を取り除くことで行った。一度マウスを円筒容器に戻し、一方のワイヤーケージに刺激用の雄マウス(刺激用マウスA)を入れた後、被験動物をテストボックス内を自由に10分間探索させる。再度、被験マウスを円筒容器に入れてから、空ワイヤーケージに新たに刺激用マウスBを入れる。円筒容器から試験動物を解放して10分間テストボックス内を自由に探索させる。以上の3セッションの間、天井よりビデオ撮影を行い、第2セッションでの被験マウスが空ワイヤーケージおよび刺激用マウスAのワイヤーケージに接触している時間、第3セッションでの刺激用マウスA,Bのワイヤーケージに接触している時間を計測し、motopsinノックアウトマウスと野生型マウスを比較した。
【0049】
社会性を検出するセッション2では、野生型マウス、motopsinノックアウトマウスが空ワイヤーケージvs刺激用マウスAワイヤーケージへ接触していた時間はそれぞれ4.5±1.0秒vs66.0±9.0秒、6.0±1.7秒vs77.0±8.1秒であった。新規社会に対する好気性を検出する第3セッションでの刺激用マウスAのワイヤーケージへの接触時間vs刺激用マウスBのそれに接触していた時間は、ノックアウトマウス;28.4±5.7秒vs49.0±7.3秒、野生型マウス;9.2±1.4秒vs37.5±7.0秒であった。
【0050】
[1-5-7]探索行動テスト
実験前日に10Lux以下の照度に設定した実験室にオープンフィールドテストで用いたフィールドを置き、その中に被験マウスを入れて30分間放置しフィールドに馴化させた。翌日、フィールド内の任意の位置にピンポン球を設置し、被験マウスを入れて10分間、行動をビデオ撮影する。被験マウスがピンポン球に接するまでの潜時と接している時間を計測した。
【0051】
Motopsinノックアウトマウスの潜時および接触時間は、35.0±14.0秒、8.8±1.4秒、であり、野生型マウスでは44.4±11.1秒、10.5±2.4秒であった。
【0052】
[1-5-6]嗅覚テスト
被験マウスは実験の12時間以上前より絶食しておいた。新しい飼育ケージの床敷きの下に飼育用飼料を隠しておいた。被験マウスをこのケージに投入してから、飼料を見つけるまでの潜時、および、飼料を見つけてから食するまでの時間を天井部より撮影したビデオ映像を元に測定した。
【0053】
Motopsinノックアウトマウスが飼料を見つけるまでの潜時、および見つけてから食するまでの時間は、それぞれ50.3±6.0秒、26.6±5.8秒であった。野生型マウスでは、72.3±12.9秒、60.6±12.4秒であった。
【0054】
[1-5-5]水迷路学習(WM)
実験装置は円筒形のプールと逃避台からなっていた。プールの内径は140cm、高さは60cmで、内壁は青色に塗装されていた。逃避台は直径10cm、厚さ3mmの円形アクリル版に台座を取り付けたものとした。プールの仮想の東西南北方向には、それぞれ、20cm四方の白いアクリル板に黒色の十字を貼り付けたもの(北)、同じく黒三角形を貼り付けたもの(南)、同じく黒正方形(東)、同じく黒丸(西)がプール内から見えるように掲げられていた。逃避台を仮想の北東方向に設置し、水位を逃避台の台面上約1cmに調節した。水はインクで白色に濁らせ、水温は21℃(±1℃)に維持した。
【0055】
1日1セッション5試行からなる獲得訓練を行った。逃避台のない北東以外の3象限いずれかの壁際から被験体をプールに投入して自由に遊泳させ、逃避台に達するまでの潜時を計測した。被験体が逃避台に載ると、10秒間そこに留めた。プールへ投入後60秒以内に被験体が逃避台に達しない場合は、実験者が逃避台の上へ誘導し、そこに10秒間留めた。投入する象限の順序は被験体毎にランダムとした。試行間間隔(逃避台から取り去ってから次にプールへ投入されるまでの時間)は30秒であった。
【0056】
最終日の試行セッションが終了して1時間後に避難台を取り除いて、被験マウスをプールに投入して、60秒間の遊泳させた(プローブテスト)。避難台のあった位置を通過する回数、潜時、および避難台があった象限での滞留割合を測定した。
【0057】
[1-5-8]Y迷路テスト
被験動物の短期記憶の程度はY迷路テストによって行った。照度30Luxの実験室に幅4cm、長さ40cmの通路を持つY字迷路を設置した。この迷路には高さ12cmの壁があるが、各壁の色は黄色(A)、グレー(B)、青色(C)といったように色彩が異なっている。迷路の中心に被験マウスを入れて8分間行動をビデオ撮影した。マウスは最も以前に進入した場所に進入する傾向があり、各通路への進入を記憶していればその進入順はABCABCABCのようになる。そこで異なる3つの通路に連続して進入した回数(上記の例では7)のその最大数(総進入数−2)に対する割合(%alternation)を短期記憶の程度として判定した。
【0058】
Motopsinノックアウトマウスは52.7±5.3%alternationを示し、野生型マウスは50.1±5.2%alternationを示した。
【0059】
〔結果〕
[2-1]
脳におけるmotopsinの機能を明らかにするため、図1に示すように、エクソン1aの開始コドンを含む領域をNeo耐性遺伝子で置き換えるターゲッティングベクターを構築し、motopsinノックアウトマウスを作製した。Motopsin遺伝子の欠落はサザンハイブリダイゼーションやPCR法によって確認できた。全体的な肉眼的および脳の光学顕微鏡検査において、motopsinノックアウトマウスは野生型マウスと明らかな差を認めなかった。特に中枢神経系に注意して観察を行ったが、皮質・海馬・線条体・小脳・視床・視床下部に明らかに異常な顕微鏡所見を認めなかった。また、仔マウスの遺伝子型は、正常のメンデル遺伝に従っていた。
【0060】
Motopsin mRNAの発現は野生型マウスやヘテロマウスではノーザンハイブリダイゼーションによって確認できたが、motopsinノックアウトマウスでは検出されなかった。Motopsinを認識する抗体を用いた免疫組織化学法の結果では、motopsinノックアウトマウス脳においては、motopsin陽性反応は検出されなかった。野生型マウス脳ではmotopsinは海馬、大脳皮質等で検出された(図2)。
【0061】
[2-2]Motopsinノックアウトマウスにおける情動行動
Motopsin欠損が、マウスの基礎的な神経機能に及ぼす影響を検討するため、motopsinノックアウトマウスの行動学的検査を行った。
Motopsinノックアウトマウスおよび野生型マウス用いてオープンフィールドテストを行った結果、それぞれの移動距離はmotopsinノックアウトマウスが2809.8±118.3cm、野生型マウスが2800.8±136.6cmであった。また、センタースクエアでの滞留時間はそれぞれ142.2±21.1秒、139.8±14.4秒であり、ゲノタイプによる差は認められなかった(図3)。また、高架式十字迷路の結果、motopsinノックアウトマウスのオープンアームでの滞留時間および進入比率は82.1±26.0秒、23.5±3.3%であり、野生型マウスでは54.9±15.6秒、19.6±2.4%であった(図4)。これらのことから、motopsinノックアウトマウスでは不安行動には異常が認められないといえる。
【0062】
[2-3]Motopsinノックアウトマウスにおける社会行動の異常
次に社会行動に障害があるかどうかを検討するため、ソーシャルレコグニションテスト、レジデントイントルーダーテスト、社会行動テストの3種類を行った(図5−7)。ソーシャルレコグニションテストでは、いずれのマウスも雌マウスAに対する接触時間がセッションを経るごとに有意に低下し、雌マウスBに対して有意に接触時間が遅延することから、刺激動物を認識していることが明らかである。しかし、意外なことにいずれの測定時点においてもmotopsinノックアウトマウスは野生型マウスに比べて有意に接触時間が長かった。この傾向は、レジデントイントルーダーテストにおいても確認された。
【0063】
社会行動テストにおいてもmotopsinノックアウトマウスは野生型マウスと異なる反応を示した。野生型マウスは第3セッションにおいて第2セッションで既に提示された刺激用マウスAに対しては接触時間が短くなるのに対して、motopsinノックアウトマウスは有意に長い接触時間を示した。以上の結果から、motopsinノックアウトマウスは社会行動が亢進しており、抗自閉症的な行動を示すことが明らかである。
【0064】
[2-4]Motopsinノックアウトマウスの探索および嗅覚行動
Motopsinノックアウトマウスにおいて観察された社会行動の亢進が社会的要素に特異的であること、および嗅覚異常に起因するもので無いことを確認するために、探索行動テストと嗅覚テストを行った(図8,9)。探索行動テストでは、無機物質に対する接触時間および最初に接触するまでの潜時にmotopsinノックアウトマウスと野生型マウスに差は認められなかった。嗅覚テストにおいても、餌を見つけるまでの時間にゲノタイプ間で有意差は認められなかったが、餌を見つけてから食べるまでの時間はmotopsinノックアウトマウスで有意に短かった。Motopsinノックアウトマウスによる無機物に対する野生型マウスと同様の反応性は社会性行動テストのセッション2において、空ケージに対する接触時間が両者において差が認められなかったことからも明らかである。従って、motopsinノックアウトマウスは社会性行動特有の異常を呈すると考えられた。
【0065】
[2-5]Motopsinノックアウトマウスの空間学習能
Motopsinノックアウトマウスの空間学習能を検討するために、モリス水迷路学習テストとY迷路テストを行った(図10,11)。モリス水迷路学習テストの獲得訓練では、motopsinノックアウトマウスは野生型マウスと同等の学習能を示した。プローブテストの結果、避難台領域を通過する回数、避難台があった象限での滞留時間も野生型マウスと同等であったが、避難台領域に到達する潜時がmotopsinノックアウトマウスでは有意に遅延していた。一方、Y迷路テストではmotopsinノックアウトマウスは野生型マウスと同等の%alternationを示したことから、短期記憶については異常が認められないといえる。
【0066】
[2-5]Motopsinノックアウトマウスのスパイン密度の低下
Motopsinノックアウトマウスが呈する行動学的異常の発症機構を明らかにするためにゴルジ染色によるニューロンの形態観察を行った。その結果、海馬の錐体ニューロンの20μm当たりのスパイン密度はmotopsinノックアウトマウスでは、頂上樹状突起では7.7±0.4個であり、基底樹状突起では8.4±0.2個であった。野生型マウスにおいてはそれぞれ、8.9±0.4個、8.3±0.2個であり、頂上樹状突起においてmotopsinノックアウトマウスは有意にスパイン密度が減少していた(図12)。
【0067】
[2-6]本実施例の結果と考察
今回motopsinノックアウトマウスにおいて、社会行動の亢進や空間記憶能の低下が認められ、また神経解剖学的検査において、海馬錐体ニューロンにおけるスパイン密度が低下するという現象が認められた。
【0068】
Motopsinノックアウトマウスがこれらの現象を引き起こした分子メカニズムについては今後更なる解析を要するが、近年、精神遅滞の原因遺伝子があいついで同定されてニューロンの細胞内情報伝達機構が乱れることでスパインの形態異常が引き起こされることが一因であると考えられつつある。しかし、従来知られている精神遅滞原因遺伝子が細胞内情報伝達に関わる分子であるのに対してmotopsinは細胞外に分泌されるプロテアーゼであることから、薬剤による制御がより容易であり、各種神経疾患に対する新たな治療・診断法を提供することができる。
【0069】
最近、tenascinCノックアウトマウスでは社会行動が向上していることが報告された。(European Journal of Neuroscience 23, 1255−1265, 2006)。しかし、このマウスでは不安反応の低下や探索行動の亢進が認められており、社会行動に特異的な変化とは言い難い。また、以前より精神遅滞原因遺伝子の欠損マウスに社会行動の異常が見られると報告されている。例えば、Mecp2に分断変異を持つマウスやSecretin受容体ノックアウトマウスでは刺激動物との接触時間が著しく減少することが報告されている(Journal of Neuroscience 26, 319−327, 2006、Human Molecular Genetics 15, 3241−3250, 2006)。しかし、これらのマウスでは社会行動以外にもロコモーター活性、空間学習能、不安行動等に異常が認められ、社会行動が特異的に亢進しているmotopsinノックアウトマウスとは表現型が異なっている。
【0070】
今回motopsinノックアウトマウスにおいては、社会行動の亢進が認められるものの、不安行動や空間学習能、社会性認識能力、探索行動などは正常であるという現象は非常ユニークである。このことは、motopsinの特異的阻害薬の探索が、抗自閉症薬など社会適応行動の亢進のための新薬開発につながることを示すものである。
【図面の簡単な説明】
【0071】
【図1】本発明の実施例に係るmotopsinノックアウトマウスの作出に用いた遺伝子ターゲッティング法を説明する図である。
【図2】Motopsinノックアウトマウスにおいてmotopsinの発現が認められないことをノーザンハイブリダイゼーションおよび免疫組織化学法によって確認したことを説明する図である。
【図3】オープンフィールドテストにおける移動反応とセンタースクエアでの滞在時間の測定結果を示すグラフである。
【図4】高架式十字迷路におけるオープンアームでの滞留時間および進入割合を示すグラフである。
【図5】ソーシャルレコグニションテストにおいて刺激動物との接触時間の測定結果を示すグラフである。
【図6】レジデントイントルーダーテストにおいて刺激動物との接触時間の測定結果を示すグラフである。
【図7】社会行動テストにおいて、空ワイヤーケージおよび刺激用マウスの入ったワイヤーケージへの接触時間結果を示すグラフである。
【図8】探索行動テストにおいて、無機物質へ接触するまでの潜時と接触時間の測定結果を示すグラフである。
【図9】嗅覚行動テストにおいて、餌を見つけるまでの潜時と見つけてから食するまでの時間の測定結果を示すグラフである。
【図10】モリス水迷路において、獲得訓練時の避難台への逃避時間の測定結果とプローブテスト時の各象限への滞在時間、仮想避難台への到達するまでの潜時を測定した結果を示すグラフである。
【図11】Y迷路テストにおける%alternationを示すグラフである。
【図12】海馬錐体ニューロンにおける樹状突起スパイン密度を計測した結果を示すグラフである。
【特許請求の範囲】
【請求項1】
相同染色体上のmotopsin遺伝子の一部又は全部の改変或いは欠損のため、motopsin遺伝子が正常に機能しないノックアウト非ヒト動物。
【請求項2】
Motopsin遺伝子のエクソン1の少なくとも開始コドンを含む領域を、相同組み換えにより他の塩基配列に置換することにより作製されたことを特徴とする請求項1記載のノックアウト動物。
【請求項3】
正常動物に比し、刺激動物への接触行動が亢進していることを特徴とする請求項1記載のノックアウト動物。
【請求項4】
正常動物に比し、接触を伴わなくとも刺激動物への探索行動が亢進していることを特徴とする請求項1記載のノックアウト動物。
【請求項5】
正常動物に比し、既に提示された刺激動物への接触行動または探索行動が減衰しないことを特徴とする請求項1記載のノックアウト動物。
【請求項6】
正常動物に比し、海馬または大脳皮質のニューロンの樹状突起スパイン密度が低下していることを特徴とする請求項1記載のノックアウト動物。
【請求項7】
マウス又はラットであることを特徴とする請求項1〜5のいずれか1項に記載のノックアウト動物。
【請求項8】
相同染色体上のmotopsin遺伝子の全部または一部が欠損又は改変され、motopsinの発現が抑制されていることを特徴とする動物細胞。
【請求項9】
Motopsinを活性化又は阻害する物質をスクリーニングすることを特徴とする向精神薬のスクリーニング方法。
【請求項10】
向精神薬が、抗自閉症、抗共依存症、又は対人行動改善剤であることを特徴とする請求項9記載のスクリーニング方法。
【請求項11】
請求項1記載のノックアウト動物を用いることを特徴とする請求項9記載のスクリーニング方法。
【請求項1】
相同染色体上のmotopsin遺伝子の一部又は全部の改変或いは欠損のため、motopsin遺伝子が正常に機能しないノックアウト非ヒト動物。
【請求項2】
Motopsin遺伝子のエクソン1の少なくとも開始コドンを含む領域を、相同組み換えにより他の塩基配列に置換することにより作製されたことを特徴とする請求項1記載のノックアウト動物。
【請求項3】
正常動物に比し、刺激動物への接触行動が亢進していることを特徴とする請求項1記載のノックアウト動物。
【請求項4】
正常動物に比し、接触を伴わなくとも刺激動物への探索行動が亢進していることを特徴とする請求項1記載のノックアウト動物。
【請求項5】
正常動物に比し、既に提示された刺激動物への接触行動または探索行動が減衰しないことを特徴とする請求項1記載のノックアウト動物。
【請求項6】
正常動物に比し、海馬または大脳皮質のニューロンの樹状突起スパイン密度が低下していることを特徴とする請求項1記載のノックアウト動物。
【請求項7】
マウス又はラットであることを特徴とする請求項1〜5のいずれか1項に記載のノックアウト動物。
【請求項8】
相同染色体上のmotopsin遺伝子の全部または一部が欠損又は改変され、motopsinの発現が抑制されていることを特徴とする動物細胞。
【請求項9】
Motopsinを活性化又は阻害する物質をスクリーニングすることを特徴とする向精神薬のスクリーニング方法。
【請求項10】
向精神薬が、抗自閉症、抗共依存症、又は対人行動改善剤であることを特徴とする請求項9記載のスクリーニング方法。
【請求項11】
請求項1記載のノックアウト動物を用いることを特徴とする請求項9記載のスクリーニング方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【公開番号】特開2008−237072(P2008−237072A)
【公開日】平成20年10月9日(2008.10.9)
【国際特許分類】
【出願番号】特願2007−80543(P2007−80543)
【出願日】平成19年3月27日(2007.3.27)
【出願人】(504174180)国立大学法人高知大学 (174)
【Fターム(参考)】
【公開日】平成20年10月9日(2008.10.9)
【国際特許分類】
【出願日】平成19年3月27日(2007.3.27)
【出願人】(504174180)国立大学法人高知大学 (174)
【Fターム(参考)】
[ Back to top ]

