α−グリコシルヘスペリジンを含有する経口投与・摂取用の、メラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、およびかゆみ抑制剤
【課題】α−グリコシルヘスペリジンを利用して、飲食品、経口剤として用いる、メラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、およびかゆみ抑制剤を提供する。
【解決手段】α−グリコシルヘスペリジンを有効成分として含有するメラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、および皮脂量低下抑制剤、並びに、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなるSCF産生抑制剤、かゆみ抑制剤。各剤は飲食品または経口剤(例えば、清涼飲料、錠菓、キャンディー、サプリメント等)として用いる。
【解決手段】α−グリコシルヘスペリジンを有効成分として含有するメラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、および皮脂量低下抑制剤、並びに、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなるSCF産生抑制剤、かゆみ抑制剤。各剤は飲食品または経口剤(例えば、清涼飲料、錠菓、キャンディー、サプリメント等)として用いる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、α−グリコシルヘスペリジンを有効成分として含有する経口投与・摂取用の、メラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、およびかゆみ抑制剤に関する。本発明は飲食品または経口剤に適用される。
【背景技術】
【0002】
柑橘類の皮に主成分として含まれるヘスペリジンにはビタミンP作用が知られているが、水に難溶性であることから、その使用用途は限定されていた。
【0003】
これに対し、糖転移酵素を用いてヘスペリジンにD−グルコース等の糖を等モル以上α結合させて水溶性としたα−グリコシルヘスペリジンを製造し、このα−グリコシルヘスペリジンを利用した飲食物、化粧品、医薬組成物等が種々提案されている(例えば、特許文献1〜3参照)。そして、特許文献1には、チアミン、リボフラビン、ビタミンCおよびビタミンEのいずれか1種以上と、α−グルコシルヘスペリジン(=ヘスペリジンに糖としてD−グルコース残基を等モル以上α結合)をビタミンP強化剤、黄色着色剤、酸化防止剤、安定剤、品質改良剤または紫外線吸収剤として含有する飲食物が記載され、特許文献2には、α−グルコシルヘスペリジンをビタミンP強化剤、黄色着色剤、酸化防止剤、安定剤、品質改良剤、紫外線吸収剤、美肌剤または色白剤として含有し、所望によりさらにビタミンEを含有する化粧品が記載され、特許文献3には、α−グルコシルヘスペリジンを有効成分とし、所望によりさらにチアミン、リボフラビン等を含有する、ウィルス性疾患、細菌性疾患、外傷性疾患、免疫疾患、リューマチ、糖尿病、循環器疾患または悪性腫瘍のための予防剤または治療剤が記載されている。
【0004】
しかしながら、α−グリコシルヘスペリジンにメラニン低下効果、皮膚明度低下抑制効果、皮膚粘弾性低下抑制効果、皮脂量低下抑制効果、SCF産生抑制効果、かゆみ抑制効果があることを見出し、α−グリコシルヘスペリジンをメラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、かゆみ抑制剤として飲食品または経口剤に利用することは、これまで具体的に提案されていなかった。
【0005】
なお「食品と科学」(非特許文献1)には、酵素処理ヘスペリジン(=α−グルコシルヘスペリジン)がチロシナーゼの阻害作用を有しており、メラニンの生成を抑制するとの記載があるが、効果の確認を示す実験データ等が具体的に示されていない。本発明者らは、ヘスペレチン(α−グルコシルヘスペリジンのアグリコン。血清中ではα−グルコシルヘスペリジンはヘスペレチンとして存在する)のメラニン低下作用がチロシナーゼ依存でないことを後掲の実施例において確認した。また該文献には、α−グルコシルヘスペリジンとケラチノサイトにおけるSCF産生抑制との関係については記載も示唆もない。
【0006】
【特許文献1】特許第3060227号公報
【特許文献2】特許第3549436号公報
【特許文献3】特開2004−123753号公報
【非特許文献1】湯本隆、「酵素処理ヘスペリジンの特性と利用」、食品と科学、食品と科学社、1999年2月号、p.90−94
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明はα−グリコシルヘスペリジンを利用して、飲食品または経口剤として用いる、メラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、およびかゆみ抑制剤を提供することを目的とする。
【課題を解決するための手段】
【0008】
上記課題を解決するために本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有するメラニン低下剤を提供する。
【0009】
また本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮膚明度低下抑制剤を提供する。
【0010】
また本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮膚粘弾性低下抑制剤を提供する。
【0011】
また本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮脂量低下抑制剤を提供する。
【0012】
また本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなるSCF産生抑制剤を提供する。
【0013】
また本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなるかゆみ抑制剤を提供する。
【0014】
また本発明は、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなる、メラニン抑制作用およびかゆみ抑制作用をともに有する経口剤を提供する。
【発明の効果】
【0015】
本発明によれば、α−グリコシルヘスペリジンを利用した経口投与・摂取用の、メラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、およびかゆみ抑制剤が提供される。本発明各剤は飲食品または経口剤として用いられる。本発明経口投与・摂取剤は、メラニン低下効果、皮膚明度低下抑制効果、皮膚粘弾性低下抑制効果、皮脂量低下抑制効果、SCF産生抑制効果、およびかゆみ抑制効果を併せもつことができる。
【発明を実施するための最良の形態】
【0016】
以下、本発明について詳述する。
【0017】
本発明に用いられるα−グリコシルヘスペリジンは、上記先行技術文献に記載のように公知の物質で、ヘスペリジンに糖(例えば、D−グルコース、D−フルクトース、D−ガラクトース等)が等モル以上α結合しているもので、水溶性化され、実質的に無味、無臭で、毒性の懸念がなく、生体内で容易にヘスペリジンと糖に加水分解され、ヘスペリジン本来の生理活性を有する。α−グリコシルヘスペリジンの代表例である、糖としてD−グルコースを用いたα−グルコシルヘスペリジン(以下、「α−Gヘスペリジン」と記す)は、下記(I)に示される化合物であり、該α−Gヘスペリジンのアグリコンであるヘスペリジンは下記式(II)に示される化合物である。また該ヘスペリジンのアグリコンが式(III)に示されるヘスペレチンである。
【0018】

【0019】

【0020】

【0021】
α−Gヘスペリジンは、例えば「酵素処理ヘスペリジン」((株)林原商事)等として市販され、ヘスペリジンは、例えば「Hesperidin」(和光純薬工業(株)。和光一級、型番:088-07341)等として市販され、ヘスペレチンは、例えば「4’-methoxy-3',5,7-trihydroxyflavuanone,97%」(名称:ヘスペレチン;Hesperetin)(Alfa Aesar社)等として市販され、これらを好適に用いることができる。ただしこれら例示に限定されるものでない。
【0022】
α−Gヘスペリジンは、体内において小腸α−グルコシダーゼによりルチン、ヘスペリジン等に分解され、これらはさらにβ−グルコシダーゼによりケルセチン、ヘスペレチン等に分解される。そしてケルセチン、ヘスペレチン等が消化管吸収され、抱合化されて、数種の活性異性体(一部メチル化)となる。すなわちα−Gヘスペリジンは、血中ではヘスペレチンとして血清タンパク質と結合した形で存在する。本発明者らは今回、後掲の実施例で示すように、この代謝されたヘスペレチンがケラチノサイトにおいてSCF産生抑制作用を示すことを初めて確認した。
【0023】
皮膚の表皮にはケラチノサイト以外に、メラニン色素を産生するメラノサイトが存在する。メラノサイトは基底層に沿って基底細胞間のところどころに点在する。
【0024】
メラノサイトでのメラニン色素産生は、出発物質であるチロシンが酸化されてドーパとなり、これがさらに酸化されてドーパキノンが生成され、この段階でチロシナーゼが関与し、次いでドーパクローム等を経て最終的にメラニン色素が産生されるが、チロシナーゼの存在でメラニン色素産生がより加速されることも知られている。したがって、メラノサイトにおけるチロシナーゼ作用を阻害することでメラニン低下を図ることができる。メラノサイトで産生されたメラニン色素は、メラノサイトの樹枝状突起を通して隣接する周囲のケラチノサイトに移行する。
【0025】
他方、ケラチノサイトでは、紫外線(UV)照射等によりメラノサイト刺激因子の生成が惹起されることが知られている。メラノサイト刺激因子はメラノサイトの増殖作用を示す。したがって、ケラチノサイトにおけるメラノサイト刺激因子の生成抑制を図ることでメラニン低下を図ることができる。メラノサイト刺激因子としては、α−メラノサイト刺激ホルモン(α−MSH:α-melanocyte stimulating hormone)、幹細胞増殖因子(SCF:stem cell factor)、ET−1(endothelin-1)等が挙げられる。
【0026】
上記因子の中でSCF(別名:kit ligand [KL]またはmast cell growth factor[MCF])は、皮膚のしみ部位等において発現が亢進していること、UV照射によりSCFの発現が亢進することが知られている(L. H. Kligman et al., Photochem. Photobiol. Vol.63, No.2 (1996) pp.123-127)。SCFはケラチノサイト、線維芽細胞、血管内皮細胞等において産生されるタンパク質である。SCFの作用としては、未分化造血幹細胞の増殖、生殖細胞の分化促進、肥満細胞の増殖促進、色素細胞の増殖促進作用等がある(Bio Science 用語ライブラリー サイトイカイン・増殖因子 羊土社(1995) 宮園浩平、菅村和夫編)。SCFには膜結合型(SCF−2)と、タンパク質分解酵素の作用により切断された膜から遊離する分泌型(SCF−1)があることが知られている。SCF−2はケラチノサイトなどに結合したまま色素細胞のSCFレセプターに結合して色素細胞の増殖を活性化し、またSCF−1はその切断部位において切断されて細胞膜から遊離し、色素細胞や肥満細胞のSCFレセプターに結合し、色素細胞の増殖を活性化し、また肥満細胞の増殖活性化および脱顆粒化をもたらす(T. Kunisada et al., J. Exp. Med., Vol.187, No.10, (1998) pp.1565-1573)。SCFの異常産生は色素細胞の異常増殖につながり、メラニン産生を亢進させ、しみ、そばかす、くすみ等の原因となる。また、肥満細胞の異常増殖、異常脱顆粒化にもつながり、ヒスタミン、セロトニン、LTB4等のケミカルメディエーターの遊離を亢進させ(J. Grabbe et el., Arch Dermatol Res (1984) 287:78-84)、掻痒、肌荒れ、敏感肌等の原因となる。したがって、SCFの抑制は、上記の現象や症状を抑制するということができる。
【0027】
本発明は、α−グリコシルヘスペリジンを有効成分として含有する経口投与・摂取用の、メラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、あるいはかゆみ抑制剤であり、これら各剤は、飲食品または経口剤である。本発明では、α−グリコシルへスペリジンとしてα−Gヘスペリジンが好適に用いられる。
【0028】
本発明の飲食品または経口剤は、例えば飲料、食品、健康食品、栄養機能食品、保健機能食品、特定保健用食品、美容食品等として用いることができる。
【0029】
α−グリコシルヘスペリジンは、ヘスペリジンと比較して水溶性が極めて大きい。また実質的に無味、無臭なので自由に調味、調香することができる。
【0030】
本発明の飲食品の形態としては、例えば、顆粒状、粒状、ペースト状、ゲル状、固形状、または、液体状に任意に成形することができる。これらには、食品中に含有することが認められている当業者に公知の各種物質、例えば、結合剤、崩壊剤、増粘剤、分散剤、吸収促進剤、矯味剤、緩衝剤、界面活性剤、溶解補助剤、保存剤、乳化剤、等張化剤、安定化剤やpH調製剤などの賦形剤を適宜含有させることができる。飲食品の具体例として、例えば、清涼飲料、グミ、キャンディー、錠菓等が挙げられる。ただしこれら例示に限定されるものでない。
【0031】
また経口剤としては、錠剤、硬カプセル剤、軟カプセル剤、粒剤若しくは丸剤等の固形製剤や、溶液、エマルジョン若しくはサスペンジョンなどの液剤の形態等で投与することができる。これらの製剤の調製にあたっては製剤化のために許容される添加剤、例えば賦形剤、安定剤、防腐剤、湿潤剤、乳化剤、滑沢剤、甘味料、着色料、香料、等張化剤、緩衝剤、酸化防止剤、pH調整剤等を併用して製剤化することができる。
【0032】
α−グリコシルヘスペリジンがメラニン低下効果、皮膚明度低下抑制効果、皮膚粘弾性低下抑制効果、皮脂量低下抑制効果、SCF産生抑制効果、かゆみ抑制効果を有することは、後掲の実施例で具体的に説明する。
【0033】
投与・摂取量は、含量、投与・摂取経路、投与・摂取頻度などによって、適宜調節することができる。通常、α−Gヘスペリジンとして、成人1日あたり、約0.001〜10.0gの範囲が好適である。
【実施例】
【0034】
以下、本発明を実施例に基づきさらに詳細に説明するが、本発明は以下の実施例に限定されるものではない。なお、以下の実施例において、α−Gヘスペリジンは「酵素処理ヘスペリジン」((株)林原商事)を、ヘスペリジンは「Hesperidin」(和光純薬工業(株)。和光一級、型番:088-07341)を、ヘスペレチンは「4’-methoxy-3',5,7-trihydroxyflavuanone,97%」(名称:ヘスペレチン;Hesperetin)(Alfa Aesar社)を、それぞれ用いた。配合量はすべて質量%で示す。
【0035】
実施例1
下記の方法でα−Gヘスペリジンの効果確認試験(小規模ヒト効果試験)を行った。
1.群構成(被験者群)
被験者(n=25名)を、アクティブ群(α−Gヘスペリジン投与群。n=13名)と、プラセボ群(対照群。n=12名)の2群に分けた。
2.試験試料
試験品: アクティブ群投与試料。錠菓(α−Gヘスペリジン100mg含有/1錠)。1日量5錠(=1日のα−Gヘスペリジン摂取量500mg)。
対照品: プラセボ群投与試料。上記試験品からα−Gヘスペリジンを抜去したもの。1日量5錠。
3.試験試料摂取方法
被験者は、摂取開始日より試験品または対照品を1日1回、朝食後に5錠を、12週間にわたり経口摂取した。
4.試験実施スケジュール
試験試料摂取開始時に測定を行い、開始から6週間後に中間測定、さらに6週間後(=摂取開始から12週間後)に最終測定を行った。
5.皮膚測定方法
測定時(摂取開始時、開始から6週間後、12週間後)のいずれにおいても、一定時間恒温恒湿条件下で皮膚を馴化させた後に測定を行った。
【0036】
[皮膚色〔L*(明度)、メラニン量〕]
頬部の一定部位の皮膚色を分光測色計CM−2600d(コニカミノルタホールディング(株)製)にて測定し、L*を計測した。
また同時に得られる皮膚反射スペクトルからLambert−Beerの式を用いて皮膚の吸光スペクトルを算出し、その吸光スペクトルが皮膚の主要な吸光成分であるメラニン、ヘモグロビンの吸光スペクトルの和で表せると仮定し、500〜700nmの範囲の10nmおきの21個の反射スペクトルを用いて重回帰分析することでメラニン量を算出した(特許第3727807号公報参照)。
【0037】
L*変化量(Δ)(0週、6週、12週)の結果を図1に示す。図1の結果から明らかなように、アクティブ群のほうが、プラセボ群よりもL*低下が抑制された。
またメラニン量変化量(Δ)(0週、6週、12週)の結果を図2に示す。図2の結果から明らかなように、メラニン量低下について、6週間、12週間とも、アクティブ群のほうが、プラセボ群よりもメラニン量が減少し、6週では統計学的な有意差が認められた。
【0038】
[皮脂量]
頬部の一定部位の皮脂量をセブメーター(Courage+Khazaka Electronic GmbH)を用いて測定した。皮脂量の変化量(Δ)(0週、6週、12週)の結果を図3に示す。図3の結果から明らかなように、アクティブ群のほうが、プラセボ群よりも皮脂量の低下が抑制された。
【0039】
[皮膚粘弾性]
頬部の一定部位の皮膚粘弾性を衝撃波測定装置・レビスコメーター(Courage+Khazaka Electronic GmbH)を用いて測定した。135度における粘弾性低下の変化量(Δ)(0週、6週、12週)結果を図4に示す。図4の結果から明らかなように、アクティブ群のほうが、プラセボ群に比べて、皮膚の粘弾性の低下が抑制された。
【0040】
上記実施例1の結果から、本発明品がメラニン低下効果、皮膚明度低下抑制効果、皮膚粘弾性低下抑制効果、皮脂量低下抑制効果を有することが確認された。本発明経口投与・摂取剤は、メラニン低下効果、皮膚明度低下抑制効果、皮膚粘弾性低下抑制効果、皮脂量低下抑制効果を併せもつことができる。
【0041】
実施例2
上記実施例1では、α−Gヘスペリジンを含む錠菓投与というヒト有効性試験により、メラニン低下効果等を有することが確認されたが、メラニン低下効果の作用機序についての確認はされていなかった。
そこで本実施例2では、α−Gヘスペリジンのメラニン低下効果の作用機序を解明するために、以下の実験を行った。
【0042】
1.B16メラノーマ細胞からのメラニン生成に対する作用の検討:
正常なメラノサイトおよびメラノーマ細胞に特異的に存在する酵素であるチロシナーゼは、L−チロシンをメラニン色素へと生成転換する。そこでα−Gヘスペリジンのメラニン低下効果の作用機序がチロシナーゼ依存性であるかどうかを調べた。
まず、B16メラノーマ細胞からのメラニン生成に対する作用を下記試験方法により検討した。
マウス由来B16メラノーマ細胞を5×104cells/wellの細胞密度で10%FBS−DMEM培地を用いて24穴プレートに播種し、1日間プレ培養した後、α−Gヘスペリジンのアグリコンであるヘスペリジン(質量分子量:610.56)および該ヘスペリジンのアグリコンであるヘスペレチン(質量分子量:302.30)をそれぞれ1μg/mL、3μg/mL、10μg/mL、30μg/mLの濃度となるよう添加した(終濃度0.5%DMSO含有培地に溶解して添加)。3日間培養した後、培地を除去し、PBS洗浄後、各wellに2N−NaOHを加えて細胞を溶解し、この細胞溶解液の吸光度測定(測定波長:405nm、参照波長:690nm)により、細胞内のメラニン量を測定した。
その結果、ヘスペリジンを添加したものでは、30μg/mLの濃度までメラニン生成抑制作用は認められなかった。また、ヘスペレチンを添加したものでは、濃度依存的にメラニンの生成が促進され、30μg/mLでは対照の約3倍のメラニン量であった。
【0043】
以上のように、ヘスペリジン、ヘスペレチンにB16メラノーマ細胞からのメラニン生成抑制作用が認められなかったことから、実施例1のヒト有効性試験によって認められたα−Gヘスペリジンのメラニン低下作用、明度低下作用は、チロシナーゼ依存性によるものではなく、別の機序によると考えられた。
【0044】
2.ケラチノサイト由来メラノサイト刺激因子の生成に対する作用の検討:
そこで、培養ヒトケラチノサイトにUV照射することで惹起されるメラノサイト刺激因子の生成に対するヘスペリジン、ヘスペレチンの作用を検討した。メラノサイト刺激因子はメラノサイトの増殖作用を示すことから、メラノサイト刺激因子の生成を抑制することによりメラニン生成を抑制することができる。本実施例では、メラノサイト刺激因子としてSCFを用いた。
(試験方法)
包皮由来正常ヒトケラチノサイト;NHEK(F)(Cascade Biologics,Inc.)を、細胞培養皿に播種してサブコンフルエントになるまで培養した(n=3)。
次いでUVB 20mJ/cm2を照射した直後、薬剤(ヘスペリジンおよびヘスペレチン。美白成分として公知のトラネキサム酸も参考薬剤として用いた)を添加し、2日間経過後の培養上清中のSCF量をSCF定量キット(Quantikine(R) Human SCF Kit、R&D Systems)を用いて定量した。
薬剤の細胞毒性によってSCF産生量が低下する可能性も考えられる。そこで薬剤を添加した場合の生細胞の数も併せて計測した。結果を図5に示す。図5中、最左側の棒グラフはUVB照射をせず、薬剤の添加がない場合の生細胞数を示し、最左側から2番目の棒グラフは薬剤添加がないが、UVB照射を行った場合の生細胞数を示す。図5に示す結果から明らかなように、ヘスペリジン、ヘスペレチン、トラネキサム酸のいずれにも、このような細胞毒性が認められなかったことから、SCF抑制作用が生体においてもある程度特異的に作用するといえる。
【0045】
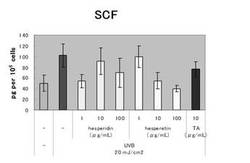
図6に細胞数106個あたりのSCF値を示す。図6中、最左側の棒グラフはUVB照射をせず、薬剤の添加がない場合の上清中のSCF値を示し、最左側から2番目の棒グラフは薬剤添加がないが、UVB照射を行った場合の上清中のSCF値を示す。
【0046】
図6の結果から明らかなように、ヘスペレチンを添加した場合、特に10μg/mL程度以上添加した場合、SCF値が低下しているのがわかる。また美白成分として公知のトラネキサム酸(TA)に比べ、SCF値は格段に低下し、用量依存的かつ100μg/mLで統計学的に有意である。
【0047】
すなわち、α−Gヘスペリジンの添加により、体内にて存在するヘスペレチンのSCF抑制効果が認められたことから、α−GヘスペリジンはSCF抑制作用によりメラニン低下作用を示すことが確認された。またSCF抑制効果が示されたことから、SCF産生亢進による掻痒、肌荒れ、敏感肌などの肌トラブルも抑制されるものと考えられる。
【0048】
以下に処方例を示す。
【0049】
処方例1:サプリメント(錠剤)
(配 合 成 分) (質量%)
ビタミンC 33.0
還元麦芽糖水飴粉末 25.7
α−Gヘスペリジン 17.0
結晶セルロース 10.0
澱粉分解物 10.0
ショ糖脂肪酸エステル 2.0
フラバンジェノール 1.3
アラビアゴム 0.5
二酸化チタン 0.5
(摂取例)
1錠500mgを1日6錠摂取する。
【0050】
処方例2:サプリメント(ハードカプセル)
(配 合 成 分) (質量%)
α−Gヘスペリジン 90.0
澱粉 10.0
(摂取例)
1カプセル280mgを1日4カプセル摂取する。
【0051】
処方例3 :サプリメント(顆粒剤)
(配 合 成 分) (質量%)
粉糖 35.0
澱粉 31.0
α−Gヘスペリジン 21.0
ビタミンC 10.0
ビタミンE 2.5
香料 0.5
(摂取例)
1日1パック(1.2g)を摂取する。
【0052】
処方例4:清涼飲料
(配 合 成 分) (質量%)
果糖ブドウ糖液糖 30.0
α−Gヘスペリジン 1.0
クエン酸 0.5
香料 適 量
精製水 残 余
【0053】
処方例5:グミ
(配 合 成 分) (質量%)
還元水飴 40.0
グラニュー糖 20.0
ブドウ糖 19.0
水 9.3
ゼラチン 5.0
α−Gヘスペリジン 5.0
クエン酸 1.0
香料 0.6
色素 0.1
【0054】
処方例6:錠菓
(配 合 成 分) (質量%)
ブドウ糖 40.0
乳糖 30.0
グラニュー糖 19.0
デンプン 5.0
ショ糖脂肪酸エステル 2.0
クエン酸 1.5
α−Gヘスペリジン 1.0
セルロース 1.0
香料 0.5
【0055】
処方例7:キャンディー
(配 合 成 分) (質量%)
砂糖 50.0
水飴 47.5
クエン酸 1.5
α−Gヘスペリジン 0.5
香料 0.5
【図面の簡単な説明】
【0056】
【図1】実施例1における、α−Gヘスペリジン投与群(アクティブ群)とプラセボ群の、頬のL*変化量(Δ)(0週、6週、12週)を示すグラフである。
【図2】実施例1における、α−Gヘスペリジン投与群(アクティブ群)とプラセボ群の、頬のメラニン量変化量(Δ)(0週、6週、12週)を示すグラフである。
【図3】実施例1における、α−Gヘスペリジン投与群(アクティブ群)とプラセボ群の、頬の皮脂量変化量(Δ)(0週、6週、12週)を示すグラフである。
【図4】実施例1における、α−Gヘスペリジン投与群(アクティブ群)とプラセボ群の、頬(135度)における皮膚粘弾性低下変化量(Δ)(0週、6週、12週)を示すグラフである。
【図5】実施例2における、UV照射されたケラチノサイトに対するヘスペリジン、ヘスペレチン添加の影響(生細胞数)を示すグラフである。
【図6】実施例2における、UV照射されたケラチノサイトに対するヘスペリジン、ヘスペレチン添加の影響(SCF抑制効果)を示すグラフである。
【技術分野】
【0001】
本発明は、α−グリコシルヘスペリジンを有効成分として含有する経口投与・摂取用の、メラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、およびかゆみ抑制剤に関する。本発明は飲食品または経口剤に適用される。
【背景技術】
【0002】
柑橘類の皮に主成分として含まれるヘスペリジンにはビタミンP作用が知られているが、水に難溶性であることから、その使用用途は限定されていた。
【0003】
これに対し、糖転移酵素を用いてヘスペリジンにD−グルコース等の糖を等モル以上α結合させて水溶性としたα−グリコシルヘスペリジンを製造し、このα−グリコシルヘスペリジンを利用した飲食物、化粧品、医薬組成物等が種々提案されている(例えば、特許文献1〜3参照)。そして、特許文献1には、チアミン、リボフラビン、ビタミンCおよびビタミンEのいずれか1種以上と、α−グルコシルヘスペリジン(=ヘスペリジンに糖としてD−グルコース残基を等モル以上α結合)をビタミンP強化剤、黄色着色剤、酸化防止剤、安定剤、品質改良剤または紫外線吸収剤として含有する飲食物が記載され、特許文献2には、α−グルコシルヘスペリジンをビタミンP強化剤、黄色着色剤、酸化防止剤、安定剤、品質改良剤、紫外線吸収剤、美肌剤または色白剤として含有し、所望によりさらにビタミンEを含有する化粧品が記載され、特許文献3には、α−グルコシルヘスペリジンを有効成分とし、所望によりさらにチアミン、リボフラビン等を含有する、ウィルス性疾患、細菌性疾患、外傷性疾患、免疫疾患、リューマチ、糖尿病、循環器疾患または悪性腫瘍のための予防剤または治療剤が記載されている。
【0004】
しかしながら、α−グリコシルヘスペリジンにメラニン低下効果、皮膚明度低下抑制効果、皮膚粘弾性低下抑制効果、皮脂量低下抑制効果、SCF産生抑制効果、かゆみ抑制効果があることを見出し、α−グリコシルヘスペリジンをメラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、かゆみ抑制剤として飲食品または経口剤に利用することは、これまで具体的に提案されていなかった。
【0005】
なお「食品と科学」(非特許文献1)には、酵素処理ヘスペリジン(=α−グルコシルヘスペリジン)がチロシナーゼの阻害作用を有しており、メラニンの生成を抑制するとの記載があるが、効果の確認を示す実験データ等が具体的に示されていない。本発明者らは、ヘスペレチン(α−グルコシルヘスペリジンのアグリコン。血清中ではα−グルコシルヘスペリジンはヘスペレチンとして存在する)のメラニン低下作用がチロシナーゼ依存でないことを後掲の実施例において確認した。また該文献には、α−グルコシルヘスペリジンとケラチノサイトにおけるSCF産生抑制との関係については記載も示唆もない。
【0006】
【特許文献1】特許第3060227号公報
【特許文献2】特許第3549436号公報
【特許文献3】特開2004−123753号公報
【非特許文献1】湯本隆、「酵素処理ヘスペリジンの特性と利用」、食品と科学、食品と科学社、1999年2月号、p.90−94
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明はα−グリコシルヘスペリジンを利用して、飲食品または経口剤として用いる、メラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、およびかゆみ抑制剤を提供することを目的とする。
【課題を解決するための手段】
【0008】
上記課題を解決するために本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有するメラニン低下剤を提供する。
【0009】
また本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮膚明度低下抑制剤を提供する。
【0010】
また本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮膚粘弾性低下抑制剤を提供する。
【0011】
また本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮脂量低下抑制剤を提供する。
【0012】
また本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなるSCF産生抑制剤を提供する。
【0013】
また本発明は、飲食品または経口剤として用いる、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなるかゆみ抑制剤を提供する。
【0014】
また本発明は、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなる、メラニン抑制作用およびかゆみ抑制作用をともに有する経口剤を提供する。
【発明の効果】
【0015】
本発明によれば、α−グリコシルヘスペリジンを利用した経口投与・摂取用の、メラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、およびかゆみ抑制剤が提供される。本発明各剤は飲食品または経口剤として用いられる。本発明経口投与・摂取剤は、メラニン低下効果、皮膚明度低下抑制効果、皮膚粘弾性低下抑制効果、皮脂量低下抑制効果、SCF産生抑制効果、およびかゆみ抑制効果を併せもつことができる。
【発明を実施するための最良の形態】
【0016】
以下、本発明について詳述する。
【0017】
本発明に用いられるα−グリコシルヘスペリジンは、上記先行技術文献に記載のように公知の物質で、ヘスペリジンに糖(例えば、D−グルコース、D−フルクトース、D−ガラクトース等)が等モル以上α結合しているもので、水溶性化され、実質的に無味、無臭で、毒性の懸念がなく、生体内で容易にヘスペリジンと糖に加水分解され、ヘスペリジン本来の生理活性を有する。α−グリコシルヘスペリジンの代表例である、糖としてD−グルコースを用いたα−グルコシルヘスペリジン(以下、「α−Gヘスペリジン」と記す)は、下記(I)に示される化合物であり、該α−Gヘスペリジンのアグリコンであるヘスペリジンは下記式(II)に示される化合物である。また該ヘスペリジンのアグリコンが式(III)に示されるヘスペレチンである。
【0018】

【0019】

【0020】

【0021】
α−Gヘスペリジンは、例えば「酵素処理ヘスペリジン」((株)林原商事)等として市販され、ヘスペリジンは、例えば「Hesperidin」(和光純薬工業(株)。和光一級、型番:088-07341)等として市販され、ヘスペレチンは、例えば「4’-methoxy-3',5,7-trihydroxyflavuanone,97%」(名称:ヘスペレチン;Hesperetin)(Alfa Aesar社)等として市販され、これらを好適に用いることができる。ただしこれら例示に限定されるものでない。
【0022】
α−Gヘスペリジンは、体内において小腸α−グルコシダーゼによりルチン、ヘスペリジン等に分解され、これらはさらにβ−グルコシダーゼによりケルセチン、ヘスペレチン等に分解される。そしてケルセチン、ヘスペレチン等が消化管吸収され、抱合化されて、数種の活性異性体(一部メチル化)となる。すなわちα−Gヘスペリジンは、血中ではヘスペレチンとして血清タンパク質と結合した形で存在する。本発明者らは今回、後掲の実施例で示すように、この代謝されたヘスペレチンがケラチノサイトにおいてSCF産生抑制作用を示すことを初めて確認した。
【0023】
皮膚の表皮にはケラチノサイト以外に、メラニン色素を産生するメラノサイトが存在する。メラノサイトは基底層に沿って基底細胞間のところどころに点在する。
【0024】
メラノサイトでのメラニン色素産生は、出発物質であるチロシンが酸化されてドーパとなり、これがさらに酸化されてドーパキノンが生成され、この段階でチロシナーゼが関与し、次いでドーパクローム等を経て最終的にメラニン色素が産生されるが、チロシナーゼの存在でメラニン色素産生がより加速されることも知られている。したがって、メラノサイトにおけるチロシナーゼ作用を阻害することでメラニン低下を図ることができる。メラノサイトで産生されたメラニン色素は、メラノサイトの樹枝状突起を通して隣接する周囲のケラチノサイトに移行する。
【0025】
他方、ケラチノサイトでは、紫外線(UV)照射等によりメラノサイト刺激因子の生成が惹起されることが知られている。メラノサイト刺激因子はメラノサイトの増殖作用を示す。したがって、ケラチノサイトにおけるメラノサイト刺激因子の生成抑制を図ることでメラニン低下を図ることができる。メラノサイト刺激因子としては、α−メラノサイト刺激ホルモン(α−MSH:α-melanocyte stimulating hormone)、幹細胞増殖因子(SCF:stem cell factor)、ET−1(endothelin-1)等が挙げられる。
【0026】
上記因子の中でSCF(別名:kit ligand [KL]またはmast cell growth factor[MCF])は、皮膚のしみ部位等において発現が亢進していること、UV照射によりSCFの発現が亢進することが知られている(L. H. Kligman et al., Photochem. Photobiol. Vol.63, No.2 (1996) pp.123-127)。SCFはケラチノサイト、線維芽細胞、血管内皮細胞等において産生されるタンパク質である。SCFの作用としては、未分化造血幹細胞の増殖、生殖細胞の分化促進、肥満細胞の増殖促進、色素細胞の増殖促進作用等がある(Bio Science 用語ライブラリー サイトイカイン・増殖因子 羊土社(1995) 宮園浩平、菅村和夫編)。SCFには膜結合型(SCF−2)と、タンパク質分解酵素の作用により切断された膜から遊離する分泌型(SCF−1)があることが知られている。SCF−2はケラチノサイトなどに結合したまま色素細胞のSCFレセプターに結合して色素細胞の増殖を活性化し、またSCF−1はその切断部位において切断されて細胞膜から遊離し、色素細胞や肥満細胞のSCFレセプターに結合し、色素細胞の増殖を活性化し、また肥満細胞の増殖活性化および脱顆粒化をもたらす(T. Kunisada et al., J. Exp. Med., Vol.187, No.10, (1998) pp.1565-1573)。SCFの異常産生は色素細胞の異常増殖につながり、メラニン産生を亢進させ、しみ、そばかす、くすみ等の原因となる。また、肥満細胞の異常増殖、異常脱顆粒化にもつながり、ヒスタミン、セロトニン、LTB4等のケミカルメディエーターの遊離を亢進させ(J. Grabbe et el., Arch Dermatol Res (1984) 287:78-84)、掻痒、肌荒れ、敏感肌等の原因となる。したがって、SCFの抑制は、上記の現象や症状を抑制するということができる。
【0027】
本発明は、α−グリコシルヘスペリジンを有効成分として含有する経口投与・摂取用の、メラニン低下剤、皮膚明度低下抑制剤、皮膚粘弾性低下抑制剤、皮脂量低下抑制剤、SCF産生抑制剤、あるいはかゆみ抑制剤であり、これら各剤は、飲食品または経口剤である。本発明では、α−グリコシルへスペリジンとしてα−Gヘスペリジンが好適に用いられる。
【0028】
本発明の飲食品または経口剤は、例えば飲料、食品、健康食品、栄養機能食品、保健機能食品、特定保健用食品、美容食品等として用いることができる。
【0029】
α−グリコシルヘスペリジンは、ヘスペリジンと比較して水溶性が極めて大きい。また実質的に無味、無臭なので自由に調味、調香することができる。
【0030】
本発明の飲食品の形態としては、例えば、顆粒状、粒状、ペースト状、ゲル状、固形状、または、液体状に任意に成形することができる。これらには、食品中に含有することが認められている当業者に公知の各種物質、例えば、結合剤、崩壊剤、増粘剤、分散剤、吸収促進剤、矯味剤、緩衝剤、界面活性剤、溶解補助剤、保存剤、乳化剤、等張化剤、安定化剤やpH調製剤などの賦形剤を適宜含有させることができる。飲食品の具体例として、例えば、清涼飲料、グミ、キャンディー、錠菓等が挙げられる。ただしこれら例示に限定されるものでない。
【0031】
また経口剤としては、錠剤、硬カプセル剤、軟カプセル剤、粒剤若しくは丸剤等の固形製剤や、溶液、エマルジョン若しくはサスペンジョンなどの液剤の形態等で投与することができる。これらの製剤の調製にあたっては製剤化のために許容される添加剤、例えば賦形剤、安定剤、防腐剤、湿潤剤、乳化剤、滑沢剤、甘味料、着色料、香料、等張化剤、緩衝剤、酸化防止剤、pH調整剤等を併用して製剤化することができる。
【0032】
α−グリコシルヘスペリジンがメラニン低下効果、皮膚明度低下抑制効果、皮膚粘弾性低下抑制効果、皮脂量低下抑制効果、SCF産生抑制効果、かゆみ抑制効果を有することは、後掲の実施例で具体的に説明する。
【0033】
投与・摂取量は、含量、投与・摂取経路、投与・摂取頻度などによって、適宜調節することができる。通常、α−Gヘスペリジンとして、成人1日あたり、約0.001〜10.0gの範囲が好適である。
【実施例】
【0034】
以下、本発明を実施例に基づきさらに詳細に説明するが、本発明は以下の実施例に限定されるものではない。なお、以下の実施例において、α−Gヘスペリジンは「酵素処理ヘスペリジン」((株)林原商事)を、ヘスペリジンは「Hesperidin」(和光純薬工業(株)。和光一級、型番:088-07341)を、ヘスペレチンは「4’-methoxy-3',5,7-trihydroxyflavuanone,97%」(名称:ヘスペレチン;Hesperetin)(Alfa Aesar社)を、それぞれ用いた。配合量はすべて質量%で示す。
【0035】
実施例1
下記の方法でα−Gヘスペリジンの効果確認試験(小規模ヒト効果試験)を行った。
1.群構成(被験者群)
被験者(n=25名)を、アクティブ群(α−Gヘスペリジン投与群。n=13名)と、プラセボ群(対照群。n=12名)の2群に分けた。
2.試験試料
試験品: アクティブ群投与試料。錠菓(α−Gヘスペリジン100mg含有/1錠)。1日量5錠(=1日のα−Gヘスペリジン摂取量500mg)。
対照品: プラセボ群投与試料。上記試験品からα−Gヘスペリジンを抜去したもの。1日量5錠。
3.試験試料摂取方法
被験者は、摂取開始日より試験品または対照品を1日1回、朝食後に5錠を、12週間にわたり経口摂取した。
4.試験実施スケジュール
試験試料摂取開始時に測定を行い、開始から6週間後に中間測定、さらに6週間後(=摂取開始から12週間後)に最終測定を行った。
5.皮膚測定方法
測定時(摂取開始時、開始から6週間後、12週間後)のいずれにおいても、一定時間恒温恒湿条件下で皮膚を馴化させた後に測定を行った。
【0036】
[皮膚色〔L*(明度)、メラニン量〕]
頬部の一定部位の皮膚色を分光測色計CM−2600d(コニカミノルタホールディング(株)製)にて測定し、L*を計測した。
また同時に得られる皮膚反射スペクトルからLambert−Beerの式を用いて皮膚の吸光スペクトルを算出し、その吸光スペクトルが皮膚の主要な吸光成分であるメラニン、ヘモグロビンの吸光スペクトルの和で表せると仮定し、500〜700nmの範囲の10nmおきの21個の反射スペクトルを用いて重回帰分析することでメラニン量を算出した(特許第3727807号公報参照)。
【0037】
L*変化量(Δ)(0週、6週、12週)の結果を図1に示す。図1の結果から明らかなように、アクティブ群のほうが、プラセボ群よりもL*低下が抑制された。
またメラニン量変化量(Δ)(0週、6週、12週)の結果を図2に示す。図2の結果から明らかなように、メラニン量低下について、6週間、12週間とも、アクティブ群のほうが、プラセボ群よりもメラニン量が減少し、6週では統計学的な有意差が認められた。
【0038】
[皮脂量]
頬部の一定部位の皮脂量をセブメーター(Courage+Khazaka Electronic GmbH)を用いて測定した。皮脂量の変化量(Δ)(0週、6週、12週)の結果を図3に示す。図3の結果から明らかなように、アクティブ群のほうが、プラセボ群よりも皮脂量の低下が抑制された。
【0039】
[皮膚粘弾性]
頬部の一定部位の皮膚粘弾性を衝撃波測定装置・レビスコメーター(Courage+Khazaka Electronic GmbH)を用いて測定した。135度における粘弾性低下の変化量(Δ)(0週、6週、12週)結果を図4に示す。図4の結果から明らかなように、アクティブ群のほうが、プラセボ群に比べて、皮膚の粘弾性の低下が抑制された。
【0040】
上記実施例1の結果から、本発明品がメラニン低下効果、皮膚明度低下抑制効果、皮膚粘弾性低下抑制効果、皮脂量低下抑制効果を有することが確認された。本発明経口投与・摂取剤は、メラニン低下効果、皮膚明度低下抑制効果、皮膚粘弾性低下抑制効果、皮脂量低下抑制効果を併せもつことができる。
【0041】
実施例2
上記実施例1では、α−Gヘスペリジンを含む錠菓投与というヒト有効性試験により、メラニン低下効果等を有することが確認されたが、メラニン低下効果の作用機序についての確認はされていなかった。
そこで本実施例2では、α−Gヘスペリジンのメラニン低下効果の作用機序を解明するために、以下の実験を行った。
【0042】
1.B16メラノーマ細胞からのメラニン生成に対する作用の検討:
正常なメラノサイトおよびメラノーマ細胞に特異的に存在する酵素であるチロシナーゼは、L−チロシンをメラニン色素へと生成転換する。そこでα−Gヘスペリジンのメラニン低下効果の作用機序がチロシナーゼ依存性であるかどうかを調べた。
まず、B16メラノーマ細胞からのメラニン生成に対する作用を下記試験方法により検討した。
マウス由来B16メラノーマ細胞を5×104cells/wellの細胞密度で10%FBS−DMEM培地を用いて24穴プレートに播種し、1日間プレ培養した後、α−Gヘスペリジンのアグリコンであるヘスペリジン(質量分子量:610.56)および該ヘスペリジンのアグリコンであるヘスペレチン(質量分子量:302.30)をそれぞれ1μg/mL、3μg/mL、10μg/mL、30μg/mLの濃度となるよう添加した(終濃度0.5%DMSO含有培地に溶解して添加)。3日間培養した後、培地を除去し、PBS洗浄後、各wellに2N−NaOHを加えて細胞を溶解し、この細胞溶解液の吸光度測定(測定波長:405nm、参照波長:690nm)により、細胞内のメラニン量を測定した。
その結果、ヘスペリジンを添加したものでは、30μg/mLの濃度までメラニン生成抑制作用は認められなかった。また、ヘスペレチンを添加したものでは、濃度依存的にメラニンの生成が促進され、30μg/mLでは対照の約3倍のメラニン量であった。
【0043】
以上のように、ヘスペリジン、ヘスペレチンにB16メラノーマ細胞からのメラニン生成抑制作用が認められなかったことから、実施例1のヒト有効性試験によって認められたα−Gヘスペリジンのメラニン低下作用、明度低下作用は、チロシナーゼ依存性によるものではなく、別の機序によると考えられた。
【0044】
2.ケラチノサイト由来メラノサイト刺激因子の生成に対する作用の検討:
そこで、培養ヒトケラチノサイトにUV照射することで惹起されるメラノサイト刺激因子の生成に対するヘスペリジン、ヘスペレチンの作用を検討した。メラノサイト刺激因子はメラノサイトの増殖作用を示すことから、メラノサイト刺激因子の生成を抑制することによりメラニン生成を抑制することができる。本実施例では、メラノサイト刺激因子としてSCFを用いた。
(試験方法)
包皮由来正常ヒトケラチノサイト;NHEK(F)(Cascade Biologics,Inc.)を、細胞培養皿に播種してサブコンフルエントになるまで培養した(n=3)。
次いでUVB 20mJ/cm2を照射した直後、薬剤(ヘスペリジンおよびヘスペレチン。美白成分として公知のトラネキサム酸も参考薬剤として用いた)を添加し、2日間経過後の培養上清中のSCF量をSCF定量キット(Quantikine(R) Human SCF Kit、R&D Systems)を用いて定量した。
薬剤の細胞毒性によってSCF産生量が低下する可能性も考えられる。そこで薬剤を添加した場合の生細胞の数も併せて計測した。結果を図5に示す。図5中、最左側の棒グラフはUVB照射をせず、薬剤の添加がない場合の生細胞数を示し、最左側から2番目の棒グラフは薬剤添加がないが、UVB照射を行った場合の生細胞数を示す。図5に示す結果から明らかなように、ヘスペリジン、ヘスペレチン、トラネキサム酸のいずれにも、このような細胞毒性が認められなかったことから、SCF抑制作用が生体においてもある程度特異的に作用するといえる。
【0045】
図6に細胞数106個あたりのSCF値を示す。図6中、最左側の棒グラフはUVB照射をせず、薬剤の添加がない場合の上清中のSCF値を示し、最左側から2番目の棒グラフは薬剤添加がないが、UVB照射を行った場合の上清中のSCF値を示す。
【0046】
図6の結果から明らかなように、ヘスペレチンを添加した場合、特に10μg/mL程度以上添加した場合、SCF値が低下しているのがわかる。また美白成分として公知のトラネキサム酸(TA)に比べ、SCF値は格段に低下し、用量依存的かつ100μg/mLで統計学的に有意である。
【0047】
すなわち、α−Gヘスペリジンの添加により、体内にて存在するヘスペレチンのSCF抑制効果が認められたことから、α−GヘスペリジンはSCF抑制作用によりメラニン低下作用を示すことが確認された。またSCF抑制効果が示されたことから、SCF産生亢進による掻痒、肌荒れ、敏感肌などの肌トラブルも抑制されるものと考えられる。
【0048】
以下に処方例を示す。
【0049】
処方例1:サプリメント(錠剤)
(配 合 成 分) (質量%)
ビタミンC 33.0
還元麦芽糖水飴粉末 25.7
α−Gヘスペリジン 17.0
結晶セルロース 10.0
澱粉分解物 10.0
ショ糖脂肪酸エステル 2.0
フラバンジェノール 1.3
アラビアゴム 0.5
二酸化チタン 0.5
(摂取例)
1錠500mgを1日6錠摂取する。
【0050】
処方例2:サプリメント(ハードカプセル)
(配 合 成 分) (質量%)
α−Gヘスペリジン 90.0
澱粉 10.0
(摂取例)
1カプセル280mgを1日4カプセル摂取する。
【0051】
処方例3 :サプリメント(顆粒剤)
(配 合 成 分) (質量%)
粉糖 35.0
澱粉 31.0
α−Gヘスペリジン 21.0
ビタミンC 10.0
ビタミンE 2.5
香料 0.5
(摂取例)
1日1パック(1.2g)を摂取する。
【0052】
処方例4:清涼飲料
(配 合 成 分) (質量%)
果糖ブドウ糖液糖 30.0
α−Gヘスペリジン 1.0
クエン酸 0.5
香料 適 量
精製水 残 余
【0053】
処方例5:グミ
(配 合 成 分) (質量%)
還元水飴 40.0
グラニュー糖 20.0
ブドウ糖 19.0
水 9.3
ゼラチン 5.0
α−Gヘスペリジン 5.0
クエン酸 1.0
香料 0.6
色素 0.1
【0054】
処方例6:錠菓
(配 合 成 分) (質量%)
ブドウ糖 40.0
乳糖 30.0
グラニュー糖 19.0
デンプン 5.0
ショ糖脂肪酸エステル 2.0
クエン酸 1.5
α−Gヘスペリジン 1.0
セルロース 1.0
香料 0.5
【0055】
処方例7:キャンディー
(配 合 成 分) (質量%)
砂糖 50.0
水飴 47.5
クエン酸 1.5
α−Gヘスペリジン 0.5
香料 0.5
【図面の簡単な説明】
【0056】
【図1】実施例1における、α−Gヘスペリジン投与群(アクティブ群)とプラセボ群の、頬のL*変化量(Δ)(0週、6週、12週)を示すグラフである。
【図2】実施例1における、α−Gヘスペリジン投与群(アクティブ群)とプラセボ群の、頬のメラニン量変化量(Δ)(0週、6週、12週)を示すグラフである。
【図3】実施例1における、α−Gヘスペリジン投与群(アクティブ群)とプラセボ群の、頬の皮脂量変化量(Δ)(0週、6週、12週)を示すグラフである。
【図4】実施例1における、α−Gヘスペリジン投与群(アクティブ群)とプラセボ群の、頬(135度)における皮膚粘弾性低下変化量(Δ)(0週、6週、12週)を示すグラフである。
【図5】実施例2における、UV照射されたケラチノサイトに対するヘスペリジン、ヘスペレチン添加の影響(生細胞数)を示すグラフである。
【図6】実施例2における、UV照射されたケラチノサイトに対するヘスペリジン、ヘスペレチン添加の影響(SCF抑制効果)を示すグラフである。
【特許請求の範囲】
【請求項1】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有するメラニン低下剤。
【請求項2】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮膚明度低下抑制剤。
【請求項3】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮膚粘弾性低下抑制剤。
【請求項4】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮脂量低下抑制剤。
【請求項5】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなるSCF産生抑制剤。
【請求項6】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなるかゆみ抑制剤。
【請求項7】
α−グリコシルヘスペリジンおよび/またはヘスペレチンからなる、メラニン抑制作用およびかゆみ抑制作用をともに有する経口剤。
【請求項1】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有するメラニン低下剤。
【請求項2】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮膚明度低下抑制剤。
【請求項3】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮膚粘弾性低下抑制剤。
【請求項4】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンを有効成分として含有する皮脂量低下抑制剤。
【請求項5】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなるSCF産生抑制剤。
【請求項6】
飲食品または経口剤として用いる、α−グリコシルヘスペリジンおよび/またはヘスペレチンからなるかゆみ抑制剤。
【請求項7】
α−グリコシルヘスペリジンおよび/またはヘスペレチンからなる、メラニン抑制作用およびかゆみ抑制作用をともに有する経口剤。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】




【図2】


【図3】


【図4】


【図5】


【図6】


【公開番号】特開2009−7336(P2009−7336A)
【公開日】平成21年1月15日(2009.1.15)
【国際特許分類】
【出願番号】特願2008−133778(P2008−133778)
【出願日】平成20年5月22日(2008.5.22)
【出願人】(000001959)株式会社資生堂 (1,748)
【出願人】(000155908)株式会社林原生物化学研究所 (168)
【Fターム(参考)】
【公開日】平成21年1月15日(2009.1.15)
【国際特許分類】
【出願日】平成20年5月22日(2008.5.22)
【出願人】(000001959)株式会社資生堂 (1,748)
【出願人】(000155908)株式会社林原生物化学研究所 (168)
【Fターム(参考)】
[ Back to top ]

