ε酸化鉄の製法
【課題】煩雑で粒径分布コントロールも困難な逆ミセル法を経ることなく、既存の粉末原料を用いてε−Fe2O3結晶を生成させる手法を提供する。
【解決手段】オキシ水酸化鉄(α−FeOOH)の粒子を水蒸気が混合された水素ガス雰囲気等の弱還元雰囲気下において300〜600℃の範囲の温度で熱処理することにより立方晶酸化鉄を生成させる熱処理工程Aと、熱処理工程Aで得られた粒子を大気等の酸化雰囲気下において700〜1300℃の範囲の温度で熱処理することにより立方晶酸化鉄からε−Fe2O3結晶を生成させる熱処理工程Bを有するε−Fe2O3結晶の製法が提供される。上記熱処理工程Aと熱処理工程Bでは、いずれもSi酸化物に覆われた状態の粒子に対して熱処理を施すことが望ましい。
【解決手段】オキシ水酸化鉄(α−FeOOH)の粒子を水蒸気が混合された水素ガス雰囲気等の弱還元雰囲気下において300〜600℃の範囲の温度で熱処理することにより立方晶酸化鉄を生成させる熱処理工程Aと、熱処理工程Aで得られた粒子を大気等の酸化雰囲気下において700〜1300℃の範囲の温度で熱処理することにより立方晶酸化鉄からε−Fe2O3結晶を生成させる熱処理工程Bを有するε−Fe2O3結晶の製法が提供される。上記熱処理工程Aと熱処理工程Bでは、いずれもSi酸化物に覆われた状態の粒子に対して熱処理を施すことが望ましい。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、ε−Fe2O3結晶の新たな製法に関する。
【背景技術】
【0002】
ε−Fe2O3は酸化鉄の中でも極めて稀な相であるが、最近、ナノオーダーの粒子サイズで室温において20kOe(1.59×106A/m)という巨大なHcを示すε−Fe2O3の存在が確認されている。Fe2O3の組成を有しながら結晶構造が異なる多形には最も普遍的なものとしてα−Fe2O3およびγ−Fe2O3があるが、ε−Fe2O3もその一つである。ε−Fe2O3の結晶構造と磁気的性質が明らかにされたのは、非特許文献1〜3に見られるように、ε−Fe2O3結晶をほぼ単相の状態で合成できるようになったごく最近のことである。
【0003】
このε−Fe2O3は巨大なHcを示すことから、高記録密度の磁気記録媒体その他の磁性用途、あるいは電波吸収用途への適用が期待されている。
【0004】
ε−Fe2O3結晶を再現性良く合成する手法としては、これまで非特許文献1〜3に示されるように、逆ミセル法とゾル−ゲル法を組み合わせた手法が知られている。これは、以下のようなものである。
【0005】
逆ミセル法は、界面活性剤を含んだ2種類のミセル溶液、すなわちミセル溶液I(原料ミセル)とミセル溶液II(中和剤ミセル)を混合することによって、ミセル内で水酸化鉄の沈殿反応を進行させることを要旨とする。例えばn−オクタンを油相とするミセル溶液Iの水相には、鉄源としての硝酸鉄(III)、および界面活性剤(例えば臭化セチルトリメチルアンモニウム)溶解させる。ε−Fe2O3結晶のFeサイトの一部を金属元素Mで置換させる場合はM源としてのM硝酸塩(例えばAlの場合、硝酸アルミニウム(III)9水和物、Gaの場合、硝酸ガリウム(III)n水和物、Inの場合、硝酸インジウム(III)3水和物)も溶解させる。同じくn−オクタンを油相とするミセル溶液IIの水相にはアンモニア水溶液を用いる。そして、ミセル溶液IとIIを混合し、両ミセル溶液から提供された種類の異なるミセル(原料ミセルと中和剤ミセル)を衝突・合体させる。このとき、中和反応によって、合体後のミセル内には結晶性に乏しい鉄水酸化物を主体とする「前駆体」が形成される。
【0006】
ゾル−ゲル法は、ミセル内で生成した前駆体の表面にSi酸化物(シリカを主体とするもの)をコーティングすることを要旨とする。例えばシラン(テトラエトキシシラン、テトラメトキシシランなど)を合体液に滴下しながら撹拌を続ける。これにより、微細な前駆体粒子表面にシランの加水分解によって生成したSi酸化物がコーティングされる。
【0007】
次いで、表面がSi酸化物で覆われた前駆体(鉄水酸化物)微粒子は、液から分離されたあと、所定の温度(700〜1300℃の範囲内)で大気雰囲気下での熱処理に供される。この熱処理によりε−Fe2O3結晶が生成する。粒子表面のSi酸化物は、アルカリ等を用いて大部分を溶解させることができ、少量のSi酸化物を粒子表面に残すことによって分散性を改善したε−Fe2O3結晶の粒子からなる粉末を得ることができる。
【0008】
なお、前駆体にアルカリ土類金属(Ba、Sr、Caなど)を含有させておくと、ε−Fe2O3結晶の成長段階でロッド状の粒子が成長しやすい。アルカリ土類金属を含有させない場合は球状の粒子が得られる。形状を制御するためのアルカリ土類金属を、以下において「形状制御剤」ということがある。形状制御剤は、ミセルI溶液に硝酸塩として添加される。
【0009】
【非特許文献1】Jian Jin,Shinichi Ohkoshi and Kazuhito Hashimoto,ADVANCED MATERIALS 2004,16,No.1,January 5,p.48-51
【非特許文献2】Jian Jin,Kazuhito Hashimoto and Shinichi Ohkoshi,JOURNAL OF MATERIALS CHIMISTRY 2005,15,p.1067-1071
【非特許文献3】Shunsuke Sakurai,Jian Jin,Kazuhito Hashimoto and Shinichi Ohkoshi,JOURNAL OF THE PHYSICAL SOCIETY OF JAPAN,Vol.74,No.7,July,2005,p.1946-1949
【非特許文献4】S.PONCE-CASTANEDA,J.R.MARTINEZ AND S.PALOMARES-SANCHEZ,Journal of Sol-Gel Science and Technology,27,2003,247-254
【発明の開示】
【発明が解決しようとする課題】
【0010】
従来は上記のようにしてε−Fe2O3結晶が合成され、研究用試料等として提供されていた。しかしながら、この合成法では、生成されるε−Fe2O3の粒度分布を制御することが極めて困難である。その理由として、まず前駆体の粒度分布を制御することが難しいことが挙げられる。前駆体サイズはミセル径によりほぼ決定される。ミセル径は溶媒の種類と使用する界面活性剤に応じて、水/界面活性剤比や水/オイル比によりある程度制御可能であるが、実際に安定なミセルが形成される条件範囲は狭く、ミセル径を広範囲で調整することは難しい。現実的には、前駆体サイズは数nm〜10nm程度となる。また、前駆体を熱処理する段階で生じる粒子同士の焼結現象もε−Fe2O3の粒度分布制御を難しくしている。前駆体サイズが上記のように小さいことから、そのままのサイズでε−Fe2O3粒子が生成すれば、超常磁性を呈する微小粒子が大部分を占める粉末が得られてしまう。そこで、超常磁性を示さない大きい粒子の存在割合ができるだけ多くなるように、熱処理時には焼結を積極的に利用して平均粒子径の増大を図ることが行われる。焼結を促進させるには、熱処理温度の上昇、熱処理時間の増大などの措置がとられるが、その場合には、粒度分布がブロードになることを回避できない。したがって、上記従来の方法では、生成されるε−Fe2O3の粒度分布を精度良くコントロールすることは事実上無理であった。磁気記録媒体や電波吸収体など、様々な磁性用途に応じた磁性粉末を提供するには、シャープな粒度分布をもつ磁性粉末が得られる製造プロセスの構築が望まれる。
【0011】
また、上記従来の合成法では、ミセルI(Fe等の硝酸塩を含む原料ミセル)とミセルII(アンモニア等の塩基性物質を含む中和剤ミセル)が衝突・合体するときに、ミセルI中の硝酸塩水溶液のpHが上昇することによる中和反応で水酸化物が生成する。ε−Fe2O3中のFeサイトの一部を3価の金属元素Mで置換したタイプのε−Fe2O3結晶(この置換により保磁力等の調整が可能である)を得たい場合には、ミセルI中にFeと金属元素Mを所定割合で配合しておく。しかし、FeとMは水酸化物を生成するpHが異なることから、FeとMとで中和反応速度に差が生じる(つまり、FeとMとの「共沈」という現象により水酸化物が生成されるわけではない)。このため、組成分布の均一な水酸化物が得られない可能性がある。この段階で組成分布にムラがあると、生成されるε−Fe2O3結晶も置換元素の濃度分布が不均一なものとなる可能性があり、その場合は所定の磁気特性が得られない恐れがある。
【0012】
さらに、上記従来の合成法は、ミセル溶液Iとミセル溶液IIを別々に作って混合させるという煩雑な過程を経るために、大量生産にはあまり適さない。
【0013】
本発明は、煩雑で粒径分布コントロールも困難な逆ミセル法を経ることなく、既存の粉末原料を用いてε−Fe2O3結晶を生成させることを目的とする。
【課題を解決するための手段】
【0014】
発明者らは詳細な検討の結果、立方晶酸化鉄のナノ粒子(粒子径は後述するTEM観察による粒子径で例えば200nm以下)をSi酸化物に覆われた状態で700〜1300℃の酸化雰囲気下で熱処理することにより、立方晶酸化鉄の結晶をε−Fe2O3の結晶に相変化させることができることを見出した。すなわち本発明で提供されるε−Fe2O3結晶の製法は、立方晶酸化鉄を前駆体としてε−Fe2O3結晶を得るものである。前駆体である立方晶酸化鉄のナノ粒子は、工業的に量産実績のあるオキシ水酸化鉄(α−FeOOH)の粒子を弱還元雰囲気下で熱処理することにより得ることができる。
【0015】
オキシ水酸化鉄(α−FeOOH)を出発物質とした場合には、以下の製法が提供される。すなわち、オキシ水酸化鉄の粒子を弱還元雰囲気下で熱処理することにより立方晶酸化鉄を生成させる熱処理工程Aと、熱処理工程Aで得られた粒子を酸化雰囲気下で熱処理することにより立方晶酸化鉄からε−Fe2O3結晶を生成させる熱処理工程Bを有するε−Fe2O3結晶の製法が提供される。上記熱処理工程Aと熱処理工程Bでは、いずれもSi酸化物(シリカを主体としたもの)に覆われた状態の粒子に対して熱処理を施すことが望ましい。
【0016】
熱処理工程Aでは、弱還元雰囲気として水蒸気が混合された水素ガス雰囲気を採用することができ、熱処理温度を300〜600℃の範囲内の温度とすることができる。
熱処理工程Bでは、酸化雰囲気として窒素と酸素の混合雰囲気(例えば大気)を採用することができ、熱処理温度を700〜1300℃の範囲内の温度とすることができる。
【0017】
ここでいう「立方晶酸化鉄」はγ−Fe2O3(マグヘマイト)にほぼ対応する立方晶のX線回折パターンが観測される酸化鉄であり、一般的なX線回折手法においてFe3O4(マグネタイト)のスピネル型立方晶の回折パターンと必ずしも厳密には区別できない。現時点でこの前駆体物質の詳しい構成はよくわかっていないが、γ−Fe2O3を主体とする結晶であると推察され、Fe3O4の存在も否定できない。いずれにしても、この前駆体である物質は、「オキシ水酸化鉄の粒子(粒子径が例えば200nm以下)を、例えばSi酸化物で覆われた状態において水蒸気を2〜30体積%好ましくは5〜20体積%混合した水素ガス雰囲気下で、300〜600℃好ましくは350〜500℃の範囲の温度で熱処理したときに、オキシ水酸化鉄から生じる立方晶の鉄酸化物」として特定されるものである。より具体的には後述の実施例の条件で得られる前駆体である。
【0018】
ここでいう「ε−Fe2O3結晶」には、特に断らない限り、Feサイトが他の元素で置換されていない純粋なε−Fe2O3結晶の他、Feサイトの一部が3価の金属元素Mで置換されており、前記純粋なε−Fe2O3結晶と空間群が同じである(すなわち空間群がPna21である)結晶が含まれる。Mは、例えばAl、Ga、Inの1種以上からなる。ただし、得られた粉末におけるMとFeのモル比をM:Fe=x:(2−x)と表すとき、0≦x<1であるものが好適な対象となる。この金属元素Mは前駆体である立方晶酸化鉄中に含有させておく。金属元素Mを含有する前駆体をオキシ水酸化鉄から生成させる場合は、熱処理工程Aに供する段階のオキシ水酸化鉄中にMを含有させておく。以下、Feサイトの一部が3価の金属元素Mで置換されたタイプのε−Fe2O3を「M置換ε−Fe2O3」ということがある。
【0019】
この製法で得られる粉末には、ε−Fe2O3結晶の他、不純物結晶としてα−Fe2O3と空間群が同じである結晶、γ−Fe2O3と空間群が同じである結晶、Fe3O4と空間群が同じである結晶、FeOと空間群が同じである結晶などが混在している場合がある。また、この製法で得られる粉末には、ε−Fe2O3結晶が成長する段階で形状制御剤として機能するアルカリ土類金属や、オキシ水酸化鉄粒子の形状制御等の目的で添加されるY等が含まれている場合がある。
【発明の効果】
【0020】
本発明によれば、煩雑な逆ミセル法によらず、オキシ水酸化鉄粉末(ゲーサイト;α−FeOOH)を原料として、2段階の熱処理による単純化されたプロセスによりε−Fe2O3結晶を生成させることができる。オキシ水酸化鉄は、現在、データストレージテープ等に使用するメタル粉の原料として使用されており、その製造技術は工業的に成熟されたものである。このため、本発明の製法はε−Fe2O3結晶の大量生産に適している。また、得られる磁性粉末の粒度分布は、使用するオキシ水酸化鉄の粒径によってコントロールすることができ、用途に応じて最適な粒度のε−Fe2O3結晶が提供可能になる。さらに、Feの一部を他の元素Mで置換したタイプのε−Fe2O3結晶を得る場合には、オキシ水酸化鉄を合成する湿式段階で元素Mを粒子中に比較的均一にドープすることができることから、組成分布が均一化された「M置換ε−Fe2O3」の結晶が得られ、組成変動による磁気特性への悪影響が低減されることが期待される。したがって本発明は、ε−Fe2O3結晶を用いた磁性体の実用化に寄与しうる。
【発明を実施するための最良の形態】
【0021】
本発明のε−Fe2O3結晶の製法では、立方晶酸化鉄を前駆体として、これを酸化雰囲気下の高温熱処理に供することによってε−Fe2O3結晶に相変化させる。その立方晶酸化鉄は工業的に量産可能なオキシ水酸化鉄ナノ粒子を原料として得られるものが好適に使用できる。オキシ水酸化鉄からの工程は以下のように表すことができる。
オキシ水酸化鉄→[熱処理工程A]→立方晶酸化鉄(前駆体)→[熱処理工程B]→ε−Fe2O3
【0022】
オキシ水酸化鉄のなかでもゲーサイト(α−FeOOH)は工業的に生産されており、粒子径制御等の技術も既に高い水準にある。したがって、本発明では所望の粒度分布に調整された原料粉(α−FeOOH)を使用することで、ε−Fe2O3の粒度分布を適正化できるメリットがある。これは、逆ミセル法の場合とは異なり、1つのミセル(すなわちα−FeOOHの1粒子)を1つのε−Fe2O3粒子にすることが原理的に可能だからである。例えば、原料粉として、ある程度大きい粒子からなり(例えば後述のTEM平均粒子径が30〜100nm)、シャープな粒度分布に調整されたオキシ水酸化鉄を使用し、かつε−Fe2O3を生成させる熱処理工程Bでの焼結をできるだけ防止するように制御すれば、超常磁性を示す微細粒子(粒子径が概ね15nm以下)の混合割合の少ないε−Fe2O3結晶の粒子を得ることが可能になる。非特許文献4にはβ−FeOOHを熱処理することによりε−Fe2O3が生成するとの記載があるが、β−FeOOHにおいて、現状のα−FeOOHのように幅広い粒子径の範囲で粒度分布を調整できるような技術をもって工業的に生産されている例は現時点で確認できていない。
以下、オキシ水酸化鉄合成工程から順に説明する。
【0023】
〔オキシ水酸化鉄合成工程〕
本発明で使用するオキシ水酸化鉄(α−FeOOH)は、例えば以下のような一般的な湿式工程により合成できる。まず2価のFeイオンを含む水溶液を用意する。例えば、第一鉄塩水溶液(FeSO4、FeCl2などの水溶液)を水酸化アルカリ(NaOHやKOH水溶液)や炭酸アルカリで中和した液が採用できる。「M置換ε−Fe2O3結晶」を得る場合には、この初期の液中にM含有塩を添加しておくことができる。Mは例えばAl、Ga、Inなどであり、これらを単独で含有させてもよいし、2種以上複合して含有させてもよい。また、やや球状化されたオキシ水酸化鉄を合成する場合は、この段階で液中にYを添加しておくことが有効である。Y源としては硫酸イットリウムが使用できる。また、前述の形状制御剤としてアルカリ土類金属を含有させる場合も、初期の液に形状制御剤元素を溶解させておく。
【0024】
この液に空気や純酸素などを吹き込んでFeを酸化させ、オキシ水酸化鉄の核晶を生成させる。その後、残りの2価のFeイオンを酸化させ、前記の核晶の上にオキシ水酸化鉄を析出させることによりオキシ水酸化鉄の粒子を成長させる。この成長過程での酸化反応は、通常、酸化剤として空気を使用することで十分進行させることができる。この成長過程において、前記M元素の溶解した液を同時に滴下することによりMを粒子中にドーピングさせることもできる。例えばMがAlである場合、硫酸Alやアルミン酸塩などを添加するとよい。さらには、酸化終了後に、M含有水溶液を添加することによってオキシ水酸化鉄粒子の周りにM元素水酸化物を被着させる方法などが採用できる。このようにして得られたオキシ水酸化鉄は、濾過、水洗工程を経た後、200℃以下の温度で乾燥して本発明の原料粉として使用することができる。あるいは、オキシ水酸化鉄の分散液を後工程に供することもできる。
【0025】
〔ゾル−ゲル工程〕
オキシ水酸化鉄粉末は、予めSi酸化物で覆われた状態としてから熱処理工程Aに供することが望ましい。Si酸化物で覆われたオキシ水酸化鉄粒子の状態を得るために、オキシ水酸化鉄粒子のミセル溶液を作り、ゾル−ゲル法を適用する。ミセル溶液は、後述の実施例に示すような方法で行うことができる。ゾル−ゲル法は前記した従来工程と同様の手法で実施すればよい。Si酸化物の被覆量は、原料中に含まれるSi含有量がSi/(Fe+M)×100で表されるモル比で50〜1000モル%の範囲とすることができる。
【0026】
〔熱処理工程A〕
オキシ水酸化鉄はメタル粉などの原料として既に広く使用されている。メタル粉の製造プロセスでは、通常、オキシ水酸化鉄を大気などの酸化性雰囲気下で加熱(例えば400℃程度)することにより、一旦、α−Fe2O3(ヘマタイト)を生成させている。ところが、発明者らの検討によれば、オキシ水酸化鉄の粒子を例えばSi酸化物に包まれた状態で300〜600℃の範囲内の弱還元雰囲気下に曝したとき、立方晶の酸化鉄が生成されることが確認された。この立方晶酸化鉄は前述のようにγ−Fe2O3(マグヘマイト)にほぼ対応する立方晶のX線回折パターンが観測される酸化鉄である。さらに発明者らは、この立方晶酸化鉄がε−Fe2O3結晶を得るための前駆体となり得ることを発見した。この熱処理工程Aは前駆体である立方晶酸化鉄を形成させるための熱処理である。
【0027】
弱還元雰囲気は、還元性ガス成分を主体としながら、若干量の酸化性ガス成分を混合させた雰囲気である。発明者らの検討によれば、弱還元雰囲気として、例えば水素ガスを主体とし、水蒸気を2〜30体積%程度好ましくは5〜20体積%程度混合した「水素−水蒸気混合ガス」が好適に使用できる。還元性が強くなるとオキシ水酸化鉄はα−Feに還元されやすくなる。α−Feは、後の熱処理工程Bで六方晶のα−Fe2O3に変化してしまうので、この熱処理工程Aではα−Feの生成をできるだけ抑えることが肝要である。つまり、単なる還元雰囲気(例えば水素ガス雰囲気)を採用することはできない。逆に、酸化性が勝る雰囲気では立方晶酸化鉄は得られず、六方晶のα−Fe2O3が生成されてしまうので注意を要する。
【0028】
温度は概ね300〜600℃の範囲とすることができ、350〜500℃の範囲がより好ましい。例えば400±50℃、あるいは400±25℃にコントロールして熱処理すればよい。熱処理時間は10〜120分程度の範囲とすることができる。
【0029】
ε−Fe2O3結晶のFeサイトの一部を置換する金属元素Mがオキシ水酸化鉄に含有されている場合には、元素Mを含有する立方晶酸化鉄が得られる。本明細書でいう「立方晶酸化鉄」には特に断らない限り、そのような元素Mを含有するタイプの立方晶酸化鉄も含まれる。
【0030】
〔熱処理工程B〕
次に、上記のようにして得られた立方晶酸化鉄(前駆体)の粒子を酸化雰囲気下で高温に保持する熱処理工程Bに供する。これにより立方晶酸化鉄をε−Fe2O3に相変化させる。ただし、熱処理工程Bに供する立方晶酸化鉄はオキシ水酸化鉄に由来するものに限定されるわけではない。同様の立方晶酸化鉄が得られる別の手法が見出された場合には、それを採用することができる。
【0031】
酸化雰囲気としては大気が利用できる。温度は概ね700〜1300℃の範囲でε−Fe2O3への相変化が起こりうるが、あまり温度が低いと立方晶酸化鉄相の残留が多くなりやすい。900〜1200℃とすることが好ましく、950〜1150℃がより好ましい。熱処理時間は0.5〜10時間程度の範囲で調整可能であるが、2〜5時間の範囲で良好な結果が得られやすい。
【0032】
この熱処理工程Bは、個々の立方晶酸化鉄の粒子がSi酸化物に覆われた状態で実施することが、立方晶酸化鉄からε−Fe2O3への相変化を実現するために極めて有効である。粒子を覆うSi酸化物の存在がα−Fe2O3への相変化ではなくε−Fe2O3への相変化を引き起こす上で有利に作用するものと考えられる。また、Si酸化物は粒子同士の焼結を防止する作用を有し、原料粉の段階で調整された所望の粒度分布を適切に反映させる役割を担う。さらに焼結現象の防止がε−Fe2O3結晶の生成にとって有利に働いている可能性もある。
【0033】
前駆体である立方晶酸化鉄に3価の金属元素M(Al、Ga、Inなど)が含まれている場合、この熱処理工程Bで生成されるε−Fe2O3結晶はFeサイトの一部がMで置換されたタイプの「M置換ε−Fe2O3」となる。また、熱処理工程Bを終えて得られた粉末には、ε−Fe2O3結晶の他に、γ−Fe2O3結晶、Fe3O4結晶(スピネル型立方晶)、α−Fe2O3結晶等の不純物結晶が存在する場合がある。
【0034】
〔Si酸化物除去工程〕
以上が本発明のε−Fe2O3の製法であるが、Si酸化物粒子で覆われた状態の前駆体粒子を熱処理工程Bに供すると、得られたε−Fe2O3結晶主体の粒子もSi酸化物に覆われたものとなり、このままでは磁性粉末としての取り扱い性に劣る。すなわち、多量のSi酸化物で覆われた粒子は液中や高分子基材中での分散性が良好ではなく、またε−Fe2O3結晶本来の磁気特性が十分に引き出せない。そこで、Si酸化物の大部分を除去することが望ましい。除去の手段としては、NaOHやKOHなどの強アルカリを溶解させた水溶液中に、熱処理工程Bを終えた粉末を入れて、撹拌することにより実施できる。溶解速度を上げる場合は、アルカリ溶液を加温するとよい。代表的には、NaOHなどのアルカリをシリカ分に対して、3モル倍以上添加し、水溶液温度が60〜70℃の状態で、磁性粉末を入れ撹拌すると、シリカを良好に溶解することができる。
【0035】
ただし、Si酸化物が完全に除去されてしまうと却って分散性が悪くなるので、最終的に粒子表面に存在するSi酸化物の量をSi/(Fe+M)×100で表されるSi含有量が0.1〜30モル%になるようにSi酸化物を残すことが望ましい。0.1〜5モル%とすることがより好ましい。置換元素Mを添加しない場合は、上記の式をM=0として適用する。Si酸化物の付着量を上記のようにコントロールするためには、後述実施例に示す〔手順6−2〕のようにして、再溶解処理を実施することが極めて有効である。
【0036】
なお、粒子の表面コーティング物質は、Si酸化物(シリカを主体とするもの)に限らず、化学的に安定で、融点の高い物質であり、かつ磁性粒子を溶解させずに除去可能な物質であれば、ゾル−ゲル工程を利用して種々のものが使用できると考えられる。例えば、低温で合成されるアルミナは、シリカと同様にアルカリにより容易に除去できるため、好ましい。また、カルシアやマグネシアも、弱酸で容易に溶解できるため、磁性粒子の溶解を最小限にとどめ溶解させることが可能であり、使用できると考えられる。
【実施例】
【0037】
以下に示す各例では粉末の粒子径をTEM(透過型電子顕微鏡:日本電子株式会社製 100CX−MarkII)により測定される粒子径で表示している。この粒子径は60万倍に拡大したTEM写真画像から各粒子の最も大きい径(長径)を測定することにより求めることができる。独立した粒子300個について求めた粒子径の平均値を、その粉末の平均粒子径とする。以下、これを「TEM平均粒子径」という。粒子径の標準偏差は、例えばマイクロソフト社の表計算ソフト「エクセル」に組み込まれているSTDEV関数を使って算出することができる。
【0038】
《実施例1》
本例は、Y(イットリウム)を添加することにより粒子形状を比較的球状化させたオキシ水酸化鉄(α−FeOOH)を原料粉に使用してε−Fe2O3結晶を得た例である。原料粉は、上で例示したオキシ水酸化鉄合成工程に準じた一般的な湿式工程により合成した。原料粉合成時の仕込み組成において、YとFeのモル比はY/Fe×100=1モル%である。実験は以下の手順に従った。
【0039】
〔手順1〕
原料粉であるオキシ水酸化鉄粉末を水相中に含むミセル溶液を以下のようにして調製する。テフロン(登録商標)製のフラスコ中に、水相として、NH3が0.8モル/L、CO2が0.4モル/L溶解した水溶液を準備し、これにオキシ水酸化鉄粉末を0.175モル/L分散させる。この分散スラリー6mLに、n−オクタン18.3mLおよび1−ブタノール3.7mLを入れ、室温で良く撹拌しながら溶解させる。さらに、界面活性剤としての臭化セチルトリメチルアンモニウムを、スラリー中の水分/界面活性剤のモル比が30となる量で添加し、撹拌により溶解させ、ミセル溶液を得る。
【0040】
このときのオキシ水酸化鉄粉末のTEM写真を図1に示す。TEM平均粒子径は39.8nm、粒子径の標準偏差は12.6nm、変動係数(標準偏差/TEM平均粒子径×100)は31.8%であった。
【0041】
〔手順2〕
手順1で得られた混合液を撹拌しながら、当該混合液にテトラエトキシシラン6mLを加える。約1日そのまま、撹拌し続ける。
【0042】
〔手順3〕
手順2で得られた溶液を遠心分離機にセットして遠心分離処理する。この処理で得られた沈殿物を回収する。回収された沈殿物をクロロホルムとメタノールの混合溶液を用いて複数回洗浄する。得られた沈殿物はSi酸化物で被覆されたオキシ水酸化物粒子からなるものである。
【0043】
〔手順4(熱処理工程A)〕
手順3で得られた沈殿物を乾燥した後、その乾燥粉に対し、水素ガス90体積%+水蒸気10体積%の混合ガス雰囲気下の炉内で400℃×1時間の熱処理を施す。
【0044】
手順4(熱処理工程A)を終えた段階の前駆体を粉末X線回折(XRD:リガク製RINT2000、線源Co−Kα線、電圧40kV、電流30mA)に供したところ、図4に示すX線回折パターンが得られた。結晶質物質の回折ピークとしては、γ−Fe2O3またはFe3O4のスピネル結晶構造に対応する「立方晶酸化鉄」のピークしか観測されなかった。
【0045】
〔手順5(熱処理工程B)〕
手順4で得られた熱処理粉に対し、大気雰囲気の炉内で1000℃×4時間の熱処理を施す。
【0046】
〔手順6−1〕
手順5で得られた熱処理粉を、メノウ製乳鉢で丁寧に解粒処理したのち、10モル/LのNaOH水溶液1L(リットル)中に入れ、液温70℃で24時間撹拌することにより、粒子表面に存在するSi酸化物の大部分を除去する。次いで、ろ過し、十分に水洗する。
【0047】
〔手順6−2〕
水洗された粉末を純水1L中に入れて分散させ、室温で撹拌しながらpHをモニターして希硝酸を少量ずつ添加していき、pH2.5〜3.0に調整する。撹拌を続けているとpHは変動するので、常にpH2.5〜3.0に調整する。pH調整しながら、撹拌を1時間実施する。アルカリで熱処理粉を処理するとシリカ分は溶解するが、同時にFeやM元素もわずかながら溶解し、アルカリ溶液中で溶解し難い無定形なFeケイ酸塩やM元素ケイ酸塩が液中で合成されることが確認されている。これらのケイ酸塩は、酸に対する溶解度が高いため、上記操作により除去を行う(再溶解処理)。
【0048】
以上の手順1から手順6−2を経ることによって、目的とする試料(磁性粉末)を得た。この粉末のTEM写真を図2に示す。TEM平均粒子径は32.5nm、粒子径の標準偏差は18.7nm、変動係数は57.6%であった。
【0049】
得られた試料を上記図4の場合と同様の条件で粉末X線回折に供したところ、図3に示す回折パターンが得られた。この回折パターンは、ε−Fe2O3の結晶構造(斜方晶、空間群Pna21)に対応するピークを有しており、ε−Fe2O3結晶の生成が確認された。その他には、不純物結晶としてα−Fe2O3の結晶構造(六方晶、空間群R−3c)に対応するピークも観測された。また、アモルファス状のSi酸化物に起因すると考えられるブロードなピークも観測された。
【0050】
得られた試料を蛍光X線分析(日本電子製JSX―3220)に供したところ、YとFeのモル比は、Y/Fe×100=1モル%であった。これは、オキシ水酸化鉄を合成する際の仕込み組成がそのまま反映された結果であった。また、得られた試料中に含まれるSi量は、Si/Fe×100によるモル比で2.1モル%であった。
【0051】
《実施例2》
本例は、Yを添加していないオキシ水酸化鉄(α−FeOOH)を原料粉に使用してε−Fe2O3結晶を得た例である。原料粉は、上で例示したオキシ水酸化鉄合成工程に準じた一般的な湿式工程により合成した。ただし、ε−Fe2O3結晶のFeサイトの一部を置換するための元素MとしてGaを含有するオキシ水酸化鉄を使用した。Gaはオキシ水酸化鉄合成の初期の液中に硝酸ガリウムを添加することにより含有させた。原料粉合成時の仕込み組成において、GaとFeのモル比はGa/Fe×100=1モル%である。
【0052】
実施例1と同様に上記手順1〜手順6−2を実施した。ただし、手順5における熱処理温度を1000℃から1100℃に変更した。それ以外は実施例1と同じ条件である。
【0053】
手順1を終えた段階のオキシ水酸化鉄粉末のTEM写真を図5に示す。TEM平均粒子径は66.5nm、粒子径の標準偏差は21.1nm、変動係数(標準偏差/TEM平均粒子径×100)は31.6%であった。
【0054】
手順4(熱処理工程A)を終えた段階の前駆体を上記と同様の条件で粉末X線回折に供したところ、結晶質物質の回折ピークとしては、実施例1の場合と同様に、γ−Fe2O3またはFe3O4のスピネル結晶構造に対応する「立方晶酸化鉄」ピークしか観測されなかった。
【0055】
手順6−2を終えて得られた試料(磁性粉体)のTEM写真を図6に示す。TEM平均粒子径は32.2nm、粒子径の標準偏差は31.6nm、変動係数は66.5%であった。
【0056】
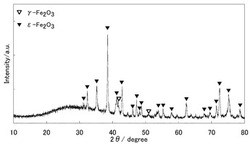
得られた試料を上記と同様の条件で粉末X線回折に供したところ、図7に示す回折パターンが得られた。この回折パターンは、ε−Fe2O3の結晶構造(斜方晶、空間群Pna21)に対応するピークを有しており、ε−Fe2O3結晶の生成が確認された。この結晶は実施例1で得られたε−Fe2O3結晶と比べ対応する各ピーク位置がわずかに高角側にシフトしていることから、格子定数が若干小さくなっている。これは、Feサイトの一部がFeよりも原子半径の小さいGaで置換された現象であると考えられる。不純物結晶としてα−Fe2O3の結晶構造(六方晶)に対応するピークと、γ−Fe2O3の結晶構造(立方晶)に対応するピークも観測された。
【0057】
得られた試料を上記と同様の蛍光X線分析に供したところ、GaとFeのモル比は、Ga/Fe×100=0.98モル%であった。これは、オキシ水酸化鉄を合成する際の仕込み組成がほぼそのまま反映された結果であった。また、得られた試料中に含まれるSi量は、Si/(Fe+Ga)×100によるモル比で1.0モル%であった。
【0058】
《実施例3》
本例は、実施例2において、オキシ水酸化鉄合成時の仕込み組成におけるGa含有量を、Ga/Fe×100によるモル比で1モル%から15モル%に増量させた例である。このとき、Gaの3モル%分はオキシ水酸化鉄合成の初期の液中に硝酸ガリウムを添加することによって含有させ、残りの12モル%分はオキシ水酸化鉄成長途中に硝酸ガリウム溶液を添加してドーピングすることにより含有させた。それ以外は上記手順1〜手順6−2における条件は熱処理温度を含め実施例2と共通である。
【0059】
手順1を終えた段階のオキシ水酸化鉄粉末のTEM写真を図8に示す。TEM平均粒子径は90.0nm、粒子径の標準偏差は21.2nm、変動係数(標準偏差/TEM平均粒子径×100)は30.2%であった。
【0060】
手順4(熱処理工程A)を終えた段階の前駆体を上記と同様の条件で粉末X線回折に供したところ、結晶質物質の回折ピークとしては、実施例1の場合と同様に、γ−Fe2O3またはFe3O4のスピネル結晶構造に対応する「立方晶酸化鉄」ピークしか観測されなかった。
【0061】
手順6−2を終えて得られた試料(磁性粉体)のTEM写真を図9に示す。TEM平均粒子径は47.2nm、粒子径の標準偏差は27.3nm、変動係数は57.8%であった。
【0062】
得られた試料を上記と同様の条件で粉末X線回折に供したところ、図10に示す回折パターンが得られた。この回折パターンは、ε−Fe2O3の結晶構造(斜方晶、空間群Pna21)に対応するピークを有しており、ε−Fe2O3結晶の生成が確認された。この結晶は実施例2の場合よりもさらに格子定数が若干小さくなっており、Feサイトの一部がFeよりも原子半径の小さいGaで置換されていることが肯定される。γ−Fe2O3結晶に対応するピークも観測されたが、α−Fe2O3結晶はほとんど検出されなかった。熱処理温度が同じである実施例2との対比から、Gaの置換量を増やしたことによって、不純物結晶であるα−Fe2O3結晶の生成が抑制される傾向が見られる。
【0063】
得られた試料を上記と同様の蛍光X線分析に供したところ、GaとFeのモル比は、Ga/Fe×100=13.6モル%であり、オキシ水酸化鉄を合成する際の仕込み組成に近い組成のものが得られた。また、得られた試料中に含まれるSi量は、Si/(Fe+Ga)×100によるモル比で1.0モル%であった。
【0064】
《比較例1》
本例は、実施例3で用いたオキシ水酸化鉄を原料粉に使用し、手順4の熱処理工程Aを省略したこと以外、実施例3と同様の条件で試料粉末を作成した例である。
【0065】
手順6−2を終えて得られた試料粉末のTEM写真を図11に示す。TEM平均粒子径は37.4nm、粒子径の標準偏差は18.1nm、変動係数は48.5%であった。
【0066】
得られた試料を上記と同様の条件で粉末X線回折に供したところ、図12に示す回折パターンが得られた。この回折パターンは、α−Fe2O3の結晶構造(六方晶、空間群R−3c)に対応するピークを示しており、ε−Fe2O3結晶の生成は認められなかった。
【0067】
得られた試料を上記と同様の蛍光X線分析に供したところ、GaとFeのモル比は、Ga/Fe×100=13.6モル%であり、オキシ水酸化鉄を合成する際の仕込み組成に近い組成のものが得られた。また、得られた試料中に含まれるSi量は、Si/(Fe+Ga)×100によるモル比で1.7モル%であった。
【0068】
《比較例2》
本例は、実施例3で用いたオキシ水酸化鉄を原料粉に使用し、手順4の熱処理工程Aにおいて、雰囲気を水素ガス100体積%の還元雰囲気に変更したこと以外、実施例3と同様の条件で試料粉末を作成した例である。
【0069】
手順4(熱処理工程A)を終えた段階の粉末を上記と同様の条件で粉末X線回折に供したところ、図14に示す回折パターンが得られた。原料粉であるオキシ水酸化鉄はα−Feにまで還元されてしまったことがわかる。
【0070】
手順6−2を終えて得られた試料粉末のTEM写真を図13に示す。TEM平均粒子径は34.6nm、粒子径の標準偏差は21.4nm、変動係数は61.7%であった。
【0071】
得られた試料を上記と同様の条件で粉末X線回折に供したところ、図15に示す回折パターンが得られた。この回折パターンは、α−Fe2O3の結晶構造(六方晶、空間群R−3c)に対応するピークを示しており、ε−Fe2O3結晶の生成は認められなかった。
【0072】
得られた試料を上記と同様の蛍光X線分析に供したところ、GaとFeのモル比は、Ga/Fe×100=13.6モル%であり、オキシ水酸化鉄を合成する際の仕込み組成に近い組成のものが得られた。また、得られた試料中に含まれるSi量は、Si/(Fe+Ga)×100によるモル比で1.2モル%であった。
【図面の簡単な説明】
【0073】
【図1】実施例1に使用したオキシ水酸化鉄のTEM写真。
【図2】実施例1で得られた試料粉末粒子のTEM写真。
【図3】実施例1で得られた試料粉末のX線回折パターン。
【図4】実施例1の熱処理工程Aで得られた前駆体のX線回折パターン。
【図5】実施例2に使用したオキシ水酸化鉄のTEM写真。
【図6】実施例2で得られた試料粉末粒子のTEM写真。
【図7】実施例2で得られた試料粉末のX線回折パターン。
【図8】実施例3に使用したオキシ水酸化鉄のTEM写真。
【図9】実施例3で得られた試料粉末粒子のTEM写真。
【図10】実施例3で得られた試料粉末のX線回折パターン。
【図11】比較例1で得られた試料粉末粒子のTEM写真。
【図12】比較例1で得られた試料粉末のX線回折パターン。
【図13】比較例2で得られた試料粉末粒子のTEM写真。
【図14】比較例2で得られた試料粉末のX線回折パターン。
【図15】比較例2の熱処理工程Aで得られた粉末のX線回折パターン。
【技術分野】
【0001】
本発明は、ε−Fe2O3結晶の新たな製法に関する。
【背景技術】
【0002】
ε−Fe2O3は酸化鉄の中でも極めて稀な相であるが、最近、ナノオーダーの粒子サイズで室温において20kOe(1.59×106A/m)という巨大なHcを示すε−Fe2O3の存在が確認されている。Fe2O3の組成を有しながら結晶構造が異なる多形には最も普遍的なものとしてα−Fe2O3およびγ−Fe2O3があるが、ε−Fe2O3もその一つである。ε−Fe2O3の結晶構造と磁気的性質が明らかにされたのは、非特許文献1〜3に見られるように、ε−Fe2O3結晶をほぼ単相の状態で合成できるようになったごく最近のことである。
【0003】
このε−Fe2O3は巨大なHcを示すことから、高記録密度の磁気記録媒体その他の磁性用途、あるいは電波吸収用途への適用が期待されている。
【0004】
ε−Fe2O3結晶を再現性良く合成する手法としては、これまで非特許文献1〜3に示されるように、逆ミセル法とゾル−ゲル法を組み合わせた手法が知られている。これは、以下のようなものである。
【0005】
逆ミセル法は、界面活性剤を含んだ2種類のミセル溶液、すなわちミセル溶液I(原料ミセル)とミセル溶液II(中和剤ミセル)を混合することによって、ミセル内で水酸化鉄の沈殿反応を進行させることを要旨とする。例えばn−オクタンを油相とするミセル溶液Iの水相には、鉄源としての硝酸鉄(III)、および界面活性剤(例えば臭化セチルトリメチルアンモニウム)溶解させる。ε−Fe2O3結晶のFeサイトの一部を金属元素Mで置換させる場合はM源としてのM硝酸塩(例えばAlの場合、硝酸アルミニウム(III)9水和物、Gaの場合、硝酸ガリウム(III)n水和物、Inの場合、硝酸インジウム(III)3水和物)も溶解させる。同じくn−オクタンを油相とするミセル溶液IIの水相にはアンモニア水溶液を用いる。そして、ミセル溶液IとIIを混合し、両ミセル溶液から提供された種類の異なるミセル(原料ミセルと中和剤ミセル)を衝突・合体させる。このとき、中和反応によって、合体後のミセル内には結晶性に乏しい鉄水酸化物を主体とする「前駆体」が形成される。
【0006】
ゾル−ゲル法は、ミセル内で生成した前駆体の表面にSi酸化物(シリカを主体とするもの)をコーティングすることを要旨とする。例えばシラン(テトラエトキシシラン、テトラメトキシシランなど)を合体液に滴下しながら撹拌を続ける。これにより、微細な前駆体粒子表面にシランの加水分解によって生成したSi酸化物がコーティングされる。
【0007】
次いで、表面がSi酸化物で覆われた前駆体(鉄水酸化物)微粒子は、液から分離されたあと、所定の温度(700〜1300℃の範囲内)で大気雰囲気下での熱処理に供される。この熱処理によりε−Fe2O3結晶が生成する。粒子表面のSi酸化物は、アルカリ等を用いて大部分を溶解させることができ、少量のSi酸化物を粒子表面に残すことによって分散性を改善したε−Fe2O3結晶の粒子からなる粉末を得ることができる。
【0008】
なお、前駆体にアルカリ土類金属(Ba、Sr、Caなど)を含有させておくと、ε−Fe2O3結晶の成長段階でロッド状の粒子が成長しやすい。アルカリ土類金属を含有させない場合は球状の粒子が得られる。形状を制御するためのアルカリ土類金属を、以下において「形状制御剤」ということがある。形状制御剤は、ミセルI溶液に硝酸塩として添加される。
【0009】
【非特許文献1】Jian Jin,Shinichi Ohkoshi and Kazuhito Hashimoto,ADVANCED MATERIALS 2004,16,No.1,January 5,p.48-51
【非特許文献2】Jian Jin,Kazuhito Hashimoto and Shinichi Ohkoshi,JOURNAL OF MATERIALS CHIMISTRY 2005,15,p.1067-1071
【非特許文献3】Shunsuke Sakurai,Jian Jin,Kazuhito Hashimoto and Shinichi Ohkoshi,JOURNAL OF THE PHYSICAL SOCIETY OF JAPAN,Vol.74,No.7,July,2005,p.1946-1949
【非特許文献4】S.PONCE-CASTANEDA,J.R.MARTINEZ AND S.PALOMARES-SANCHEZ,Journal of Sol-Gel Science and Technology,27,2003,247-254
【発明の開示】
【発明が解決しようとする課題】
【0010】
従来は上記のようにしてε−Fe2O3結晶が合成され、研究用試料等として提供されていた。しかしながら、この合成法では、生成されるε−Fe2O3の粒度分布を制御することが極めて困難である。その理由として、まず前駆体の粒度分布を制御することが難しいことが挙げられる。前駆体サイズはミセル径によりほぼ決定される。ミセル径は溶媒の種類と使用する界面活性剤に応じて、水/界面活性剤比や水/オイル比によりある程度制御可能であるが、実際に安定なミセルが形成される条件範囲は狭く、ミセル径を広範囲で調整することは難しい。現実的には、前駆体サイズは数nm〜10nm程度となる。また、前駆体を熱処理する段階で生じる粒子同士の焼結現象もε−Fe2O3の粒度分布制御を難しくしている。前駆体サイズが上記のように小さいことから、そのままのサイズでε−Fe2O3粒子が生成すれば、超常磁性を呈する微小粒子が大部分を占める粉末が得られてしまう。そこで、超常磁性を示さない大きい粒子の存在割合ができるだけ多くなるように、熱処理時には焼結を積極的に利用して平均粒子径の増大を図ることが行われる。焼結を促進させるには、熱処理温度の上昇、熱処理時間の増大などの措置がとられるが、その場合には、粒度分布がブロードになることを回避できない。したがって、上記従来の方法では、生成されるε−Fe2O3の粒度分布を精度良くコントロールすることは事実上無理であった。磁気記録媒体や電波吸収体など、様々な磁性用途に応じた磁性粉末を提供するには、シャープな粒度分布をもつ磁性粉末が得られる製造プロセスの構築が望まれる。
【0011】
また、上記従来の合成法では、ミセルI(Fe等の硝酸塩を含む原料ミセル)とミセルII(アンモニア等の塩基性物質を含む中和剤ミセル)が衝突・合体するときに、ミセルI中の硝酸塩水溶液のpHが上昇することによる中和反応で水酸化物が生成する。ε−Fe2O3中のFeサイトの一部を3価の金属元素Mで置換したタイプのε−Fe2O3結晶(この置換により保磁力等の調整が可能である)を得たい場合には、ミセルI中にFeと金属元素Mを所定割合で配合しておく。しかし、FeとMは水酸化物を生成するpHが異なることから、FeとMとで中和反応速度に差が生じる(つまり、FeとMとの「共沈」という現象により水酸化物が生成されるわけではない)。このため、組成分布の均一な水酸化物が得られない可能性がある。この段階で組成分布にムラがあると、生成されるε−Fe2O3結晶も置換元素の濃度分布が不均一なものとなる可能性があり、その場合は所定の磁気特性が得られない恐れがある。
【0012】
さらに、上記従来の合成法は、ミセル溶液Iとミセル溶液IIを別々に作って混合させるという煩雑な過程を経るために、大量生産にはあまり適さない。
【0013】
本発明は、煩雑で粒径分布コントロールも困難な逆ミセル法を経ることなく、既存の粉末原料を用いてε−Fe2O3結晶を生成させることを目的とする。
【課題を解決するための手段】
【0014】
発明者らは詳細な検討の結果、立方晶酸化鉄のナノ粒子(粒子径は後述するTEM観察による粒子径で例えば200nm以下)をSi酸化物に覆われた状態で700〜1300℃の酸化雰囲気下で熱処理することにより、立方晶酸化鉄の結晶をε−Fe2O3の結晶に相変化させることができることを見出した。すなわち本発明で提供されるε−Fe2O3結晶の製法は、立方晶酸化鉄を前駆体としてε−Fe2O3結晶を得るものである。前駆体である立方晶酸化鉄のナノ粒子は、工業的に量産実績のあるオキシ水酸化鉄(α−FeOOH)の粒子を弱還元雰囲気下で熱処理することにより得ることができる。
【0015】
オキシ水酸化鉄(α−FeOOH)を出発物質とした場合には、以下の製法が提供される。すなわち、オキシ水酸化鉄の粒子を弱還元雰囲気下で熱処理することにより立方晶酸化鉄を生成させる熱処理工程Aと、熱処理工程Aで得られた粒子を酸化雰囲気下で熱処理することにより立方晶酸化鉄からε−Fe2O3結晶を生成させる熱処理工程Bを有するε−Fe2O3結晶の製法が提供される。上記熱処理工程Aと熱処理工程Bでは、いずれもSi酸化物(シリカを主体としたもの)に覆われた状態の粒子に対して熱処理を施すことが望ましい。
【0016】
熱処理工程Aでは、弱還元雰囲気として水蒸気が混合された水素ガス雰囲気を採用することができ、熱処理温度を300〜600℃の範囲内の温度とすることができる。
熱処理工程Bでは、酸化雰囲気として窒素と酸素の混合雰囲気(例えば大気)を採用することができ、熱処理温度を700〜1300℃の範囲内の温度とすることができる。
【0017】
ここでいう「立方晶酸化鉄」はγ−Fe2O3(マグヘマイト)にほぼ対応する立方晶のX線回折パターンが観測される酸化鉄であり、一般的なX線回折手法においてFe3O4(マグネタイト)のスピネル型立方晶の回折パターンと必ずしも厳密には区別できない。現時点でこの前駆体物質の詳しい構成はよくわかっていないが、γ−Fe2O3を主体とする結晶であると推察され、Fe3O4の存在も否定できない。いずれにしても、この前駆体である物質は、「オキシ水酸化鉄の粒子(粒子径が例えば200nm以下)を、例えばSi酸化物で覆われた状態において水蒸気を2〜30体積%好ましくは5〜20体積%混合した水素ガス雰囲気下で、300〜600℃好ましくは350〜500℃の範囲の温度で熱処理したときに、オキシ水酸化鉄から生じる立方晶の鉄酸化物」として特定されるものである。より具体的には後述の実施例の条件で得られる前駆体である。
【0018】
ここでいう「ε−Fe2O3結晶」には、特に断らない限り、Feサイトが他の元素で置換されていない純粋なε−Fe2O3結晶の他、Feサイトの一部が3価の金属元素Mで置換されており、前記純粋なε−Fe2O3結晶と空間群が同じである(すなわち空間群がPna21である)結晶が含まれる。Mは、例えばAl、Ga、Inの1種以上からなる。ただし、得られた粉末におけるMとFeのモル比をM:Fe=x:(2−x)と表すとき、0≦x<1であるものが好適な対象となる。この金属元素Mは前駆体である立方晶酸化鉄中に含有させておく。金属元素Mを含有する前駆体をオキシ水酸化鉄から生成させる場合は、熱処理工程Aに供する段階のオキシ水酸化鉄中にMを含有させておく。以下、Feサイトの一部が3価の金属元素Mで置換されたタイプのε−Fe2O3を「M置換ε−Fe2O3」ということがある。
【0019】
この製法で得られる粉末には、ε−Fe2O3結晶の他、不純物結晶としてα−Fe2O3と空間群が同じである結晶、γ−Fe2O3と空間群が同じである結晶、Fe3O4と空間群が同じである結晶、FeOと空間群が同じである結晶などが混在している場合がある。また、この製法で得られる粉末には、ε−Fe2O3結晶が成長する段階で形状制御剤として機能するアルカリ土類金属や、オキシ水酸化鉄粒子の形状制御等の目的で添加されるY等が含まれている場合がある。
【発明の効果】
【0020】
本発明によれば、煩雑な逆ミセル法によらず、オキシ水酸化鉄粉末(ゲーサイト;α−FeOOH)を原料として、2段階の熱処理による単純化されたプロセスによりε−Fe2O3結晶を生成させることができる。オキシ水酸化鉄は、現在、データストレージテープ等に使用するメタル粉の原料として使用されており、その製造技術は工業的に成熟されたものである。このため、本発明の製法はε−Fe2O3結晶の大量生産に適している。また、得られる磁性粉末の粒度分布は、使用するオキシ水酸化鉄の粒径によってコントロールすることができ、用途に応じて最適な粒度のε−Fe2O3結晶が提供可能になる。さらに、Feの一部を他の元素Mで置換したタイプのε−Fe2O3結晶を得る場合には、オキシ水酸化鉄を合成する湿式段階で元素Mを粒子中に比較的均一にドープすることができることから、組成分布が均一化された「M置換ε−Fe2O3」の結晶が得られ、組成変動による磁気特性への悪影響が低減されることが期待される。したがって本発明は、ε−Fe2O3結晶を用いた磁性体の実用化に寄与しうる。
【発明を実施するための最良の形態】
【0021】
本発明のε−Fe2O3結晶の製法では、立方晶酸化鉄を前駆体として、これを酸化雰囲気下の高温熱処理に供することによってε−Fe2O3結晶に相変化させる。その立方晶酸化鉄は工業的に量産可能なオキシ水酸化鉄ナノ粒子を原料として得られるものが好適に使用できる。オキシ水酸化鉄からの工程は以下のように表すことができる。
オキシ水酸化鉄→[熱処理工程A]→立方晶酸化鉄(前駆体)→[熱処理工程B]→ε−Fe2O3
【0022】
オキシ水酸化鉄のなかでもゲーサイト(α−FeOOH)は工業的に生産されており、粒子径制御等の技術も既に高い水準にある。したがって、本発明では所望の粒度分布に調整された原料粉(α−FeOOH)を使用することで、ε−Fe2O3の粒度分布を適正化できるメリットがある。これは、逆ミセル法の場合とは異なり、1つのミセル(すなわちα−FeOOHの1粒子)を1つのε−Fe2O3粒子にすることが原理的に可能だからである。例えば、原料粉として、ある程度大きい粒子からなり(例えば後述のTEM平均粒子径が30〜100nm)、シャープな粒度分布に調整されたオキシ水酸化鉄を使用し、かつε−Fe2O3を生成させる熱処理工程Bでの焼結をできるだけ防止するように制御すれば、超常磁性を示す微細粒子(粒子径が概ね15nm以下)の混合割合の少ないε−Fe2O3結晶の粒子を得ることが可能になる。非特許文献4にはβ−FeOOHを熱処理することによりε−Fe2O3が生成するとの記載があるが、β−FeOOHにおいて、現状のα−FeOOHのように幅広い粒子径の範囲で粒度分布を調整できるような技術をもって工業的に生産されている例は現時点で確認できていない。
以下、オキシ水酸化鉄合成工程から順に説明する。
【0023】
〔オキシ水酸化鉄合成工程〕
本発明で使用するオキシ水酸化鉄(α−FeOOH)は、例えば以下のような一般的な湿式工程により合成できる。まず2価のFeイオンを含む水溶液を用意する。例えば、第一鉄塩水溶液(FeSO4、FeCl2などの水溶液)を水酸化アルカリ(NaOHやKOH水溶液)や炭酸アルカリで中和した液が採用できる。「M置換ε−Fe2O3結晶」を得る場合には、この初期の液中にM含有塩を添加しておくことができる。Mは例えばAl、Ga、Inなどであり、これらを単独で含有させてもよいし、2種以上複合して含有させてもよい。また、やや球状化されたオキシ水酸化鉄を合成する場合は、この段階で液中にYを添加しておくことが有効である。Y源としては硫酸イットリウムが使用できる。また、前述の形状制御剤としてアルカリ土類金属を含有させる場合も、初期の液に形状制御剤元素を溶解させておく。
【0024】
この液に空気や純酸素などを吹き込んでFeを酸化させ、オキシ水酸化鉄の核晶を生成させる。その後、残りの2価のFeイオンを酸化させ、前記の核晶の上にオキシ水酸化鉄を析出させることによりオキシ水酸化鉄の粒子を成長させる。この成長過程での酸化反応は、通常、酸化剤として空気を使用することで十分進行させることができる。この成長過程において、前記M元素の溶解した液を同時に滴下することによりMを粒子中にドーピングさせることもできる。例えばMがAlである場合、硫酸Alやアルミン酸塩などを添加するとよい。さらには、酸化終了後に、M含有水溶液を添加することによってオキシ水酸化鉄粒子の周りにM元素水酸化物を被着させる方法などが採用できる。このようにして得られたオキシ水酸化鉄は、濾過、水洗工程を経た後、200℃以下の温度で乾燥して本発明の原料粉として使用することができる。あるいは、オキシ水酸化鉄の分散液を後工程に供することもできる。
【0025】
〔ゾル−ゲル工程〕
オキシ水酸化鉄粉末は、予めSi酸化物で覆われた状態としてから熱処理工程Aに供することが望ましい。Si酸化物で覆われたオキシ水酸化鉄粒子の状態を得るために、オキシ水酸化鉄粒子のミセル溶液を作り、ゾル−ゲル法を適用する。ミセル溶液は、後述の実施例に示すような方法で行うことができる。ゾル−ゲル法は前記した従来工程と同様の手法で実施すればよい。Si酸化物の被覆量は、原料中に含まれるSi含有量がSi/(Fe+M)×100で表されるモル比で50〜1000モル%の範囲とすることができる。
【0026】
〔熱処理工程A〕
オキシ水酸化鉄はメタル粉などの原料として既に広く使用されている。メタル粉の製造プロセスでは、通常、オキシ水酸化鉄を大気などの酸化性雰囲気下で加熱(例えば400℃程度)することにより、一旦、α−Fe2O3(ヘマタイト)を生成させている。ところが、発明者らの検討によれば、オキシ水酸化鉄の粒子を例えばSi酸化物に包まれた状態で300〜600℃の範囲内の弱還元雰囲気下に曝したとき、立方晶の酸化鉄が生成されることが確認された。この立方晶酸化鉄は前述のようにγ−Fe2O3(マグヘマイト)にほぼ対応する立方晶のX線回折パターンが観測される酸化鉄である。さらに発明者らは、この立方晶酸化鉄がε−Fe2O3結晶を得るための前駆体となり得ることを発見した。この熱処理工程Aは前駆体である立方晶酸化鉄を形成させるための熱処理である。
【0027】
弱還元雰囲気は、還元性ガス成分を主体としながら、若干量の酸化性ガス成分を混合させた雰囲気である。発明者らの検討によれば、弱還元雰囲気として、例えば水素ガスを主体とし、水蒸気を2〜30体積%程度好ましくは5〜20体積%程度混合した「水素−水蒸気混合ガス」が好適に使用できる。還元性が強くなるとオキシ水酸化鉄はα−Feに還元されやすくなる。α−Feは、後の熱処理工程Bで六方晶のα−Fe2O3に変化してしまうので、この熱処理工程Aではα−Feの生成をできるだけ抑えることが肝要である。つまり、単なる還元雰囲気(例えば水素ガス雰囲気)を採用することはできない。逆に、酸化性が勝る雰囲気では立方晶酸化鉄は得られず、六方晶のα−Fe2O3が生成されてしまうので注意を要する。
【0028】
温度は概ね300〜600℃の範囲とすることができ、350〜500℃の範囲がより好ましい。例えば400±50℃、あるいは400±25℃にコントロールして熱処理すればよい。熱処理時間は10〜120分程度の範囲とすることができる。
【0029】
ε−Fe2O3結晶のFeサイトの一部を置換する金属元素Mがオキシ水酸化鉄に含有されている場合には、元素Mを含有する立方晶酸化鉄が得られる。本明細書でいう「立方晶酸化鉄」には特に断らない限り、そのような元素Mを含有するタイプの立方晶酸化鉄も含まれる。
【0030】
〔熱処理工程B〕
次に、上記のようにして得られた立方晶酸化鉄(前駆体)の粒子を酸化雰囲気下で高温に保持する熱処理工程Bに供する。これにより立方晶酸化鉄をε−Fe2O3に相変化させる。ただし、熱処理工程Bに供する立方晶酸化鉄はオキシ水酸化鉄に由来するものに限定されるわけではない。同様の立方晶酸化鉄が得られる別の手法が見出された場合には、それを採用することができる。
【0031】
酸化雰囲気としては大気が利用できる。温度は概ね700〜1300℃の範囲でε−Fe2O3への相変化が起こりうるが、あまり温度が低いと立方晶酸化鉄相の残留が多くなりやすい。900〜1200℃とすることが好ましく、950〜1150℃がより好ましい。熱処理時間は0.5〜10時間程度の範囲で調整可能であるが、2〜5時間の範囲で良好な結果が得られやすい。
【0032】
この熱処理工程Bは、個々の立方晶酸化鉄の粒子がSi酸化物に覆われた状態で実施することが、立方晶酸化鉄からε−Fe2O3への相変化を実現するために極めて有効である。粒子を覆うSi酸化物の存在がα−Fe2O3への相変化ではなくε−Fe2O3への相変化を引き起こす上で有利に作用するものと考えられる。また、Si酸化物は粒子同士の焼結を防止する作用を有し、原料粉の段階で調整された所望の粒度分布を適切に反映させる役割を担う。さらに焼結現象の防止がε−Fe2O3結晶の生成にとって有利に働いている可能性もある。
【0033】
前駆体である立方晶酸化鉄に3価の金属元素M(Al、Ga、Inなど)が含まれている場合、この熱処理工程Bで生成されるε−Fe2O3結晶はFeサイトの一部がMで置換されたタイプの「M置換ε−Fe2O3」となる。また、熱処理工程Bを終えて得られた粉末には、ε−Fe2O3結晶の他に、γ−Fe2O3結晶、Fe3O4結晶(スピネル型立方晶)、α−Fe2O3結晶等の不純物結晶が存在する場合がある。
【0034】
〔Si酸化物除去工程〕
以上が本発明のε−Fe2O3の製法であるが、Si酸化物粒子で覆われた状態の前駆体粒子を熱処理工程Bに供すると、得られたε−Fe2O3結晶主体の粒子もSi酸化物に覆われたものとなり、このままでは磁性粉末としての取り扱い性に劣る。すなわち、多量のSi酸化物で覆われた粒子は液中や高分子基材中での分散性が良好ではなく、またε−Fe2O3結晶本来の磁気特性が十分に引き出せない。そこで、Si酸化物の大部分を除去することが望ましい。除去の手段としては、NaOHやKOHなどの強アルカリを溶解させた水溶液中に、熱処理工程Bを終えた粉末を入れて、撹拌することにより実施できる。溶解速度を上げる場合は、アルカリ溶液を加温するとよい。代表的には、NaOHなどのアルカリをシリカ分に対して、3モル倍以上添加し、水溶液温度が60〜70℃の状態で、磁性粉末を入れ撹拌すると、シリカを良好に溶解することができる。
【0035】
ただし、Si酸化物が完全に除去されてしまうと却って分散性が悪くなるので、最終的に粒子表面に存在するSi酸化物の量をSi/(Fe+M)×100で表されるSi含有量が0.1〜30モル%になるようにSi酸化物を残すことが望ましい。0.1〜5モル%とすることがより好ましい。置換元素Mを添加しない場合は、上記の式をM=0として適用する。Si酸化物の付着量を上記のようにコントロールするためには、後述実施例に示す〔手順6−2〕のようにして、再溶解処理を実施することが極めて有効である。
【0036】
なお、粒子の表面コーティング物質は、Si酸化物(シリカを主体とするもの)に限らず、化学的に安定で、融点の高い物質であり、かつ磁性粒子を溶解させずに除去可能な物質であれば、ゾル−ゲル工程を利用して種々のものが使用できると考えられる。例えば、低温で合成されるアルミナは、シリカと同様にアルカリにより容易に除去できるため、好ましい。また、カルシアやマグネシアも、弱酸で容易に溶解できるため、磁性粒子の溶解を最小限にとどめ溶解させることが可能であり、使用できると考えられる。
【実施例】
【0037】
以下に示す各例では粉末の粒子径をTEM(透過型電子顕微鏡:日本電子株式会社製 100CX−MarkII)により測定される粒子径で表示している。この粒子径は60万倍に拡大したTEM写真画像から各粒子の最も大きい径(長径)を測定することにより求めることができる。独立した粒子300個について求めた粒子径の平均値を、その粉末の平均粒子径とする。以下、これを「TEM平均粒子径」という。粒子径の標準偏差は、例えばマイクロソフト社の表計算ソフト「エクセル」に組み込まれているSTDEV関数を使って算出することができる。
【0038】
《実施例1》
本例は、Y(イットリウム)を添加することにより粒子形状を比較的球状化させたオキシ水酸化鉄(α−FeOOH)を原料粉に使用してε−Fe2O3結晶を得た例である。原料粉は、上で例示したオキシ水酸化鉄合成工程に準じた一般的な湿式工程により合成した。原料粉合成時の仕込み組成において、YとFeのモル比はY/Fe×100=1モル%である。実験は以下の手順に従った。
【0039】
〔手順1〕
原料粉であるオキシ水酸化鉄粉末を水相中に含むミセル溶液を以下のようにして調製する。テフロン(登録商標)製のフラスコ中に、水相として、NH3が0.8モル/L、CO2が0.4モル/L溶解した水溶液を準備し、これにオキシ水酸化鉄粉末を0.175モル/L分散させる。この分散スラリー6mLに、n−オクタン18.3mLおよび1−ブタノール3.7mLを入れ、室温で良く撹拌しながら溶解させる。さらに、界面活性剤としての臭化セチルトリメチルアンモニウムを、スラリー中の水分/界面活性剤のモル比が30となる量で添加し、撹拌により溶解させ、ミセル溶液を得る。
【0040】
このときのオキシ水酸化鉄粉末のTEM写真を図1に示す。TEM平均粒子径は39.8nm、粒子径の標準偏差は12.6nm、変動係数(標準偏差/TEM平均粒子径×100)は31.8%であった。
【0041】
〔手順2〕
手順1で得られた混合液を撹拌しながら、当該混合液にテトラエトキシシラン6mLを加える。約1日そのまま、撹拌し続ける。
【0042】
〔手順3〕
手順2で得られた溶液を遠心分離機にセットして遠心分離処理する。この処理で得られた沈殿物を回収する。回収された沈殿物をクロロホルムとメタノールの混合溶液を用いて複数回洗浄する。得られた沈殿物はSi酸化物で被覆されたオキシ水酸化物粒子からなるものである。
【0043】
〔手順4(熱処理工程A)〕
手順3で得られた沈殿物を乾燥した後、その乾燥粉に対し、水素ガス90体積%+水蒸気10体積%の混合ガス雰囲気下の炉内で400℃×1時間の熱処理を施す。
【0044】
手順4(熱処理工程A)を終えた段階の前駆体を粉末X線回折(XRD:リガク製RINT2000、線源Co−Kα線、電圧40kV、電流30mA)に供したところ、図4に示すX線回折パターンが得られた。結晶質物質の回折ピークとしては、γ−Fe2O3またはFe3O4のスピネル結晶構造に対応する「立方晶酸化鉄」のピークしか観測されなかった。
【0045】
〔手順5(熱処理工程B)〕
手順4で得られた熱処理粉に対し、大気雰囲気の炉内で1000℃×4時間の熱処理を施す。
【0046】
〔手順6−1〕
手順5で得られた熱処理粉を、メノウ製乳鉢で丁寧に解粒処理したのち、10モル/LのNaOH水溶液1L(リットル)中に入れ、液温70℃で24時間撹拌することにより、粒子表面に存在するSi酸化物の大部分を除去する。次いで、ろ過し、十分に水洗する。
【0047】
〔手順6−2〕
水洗された粉末を純水1L中に入れて分散させ、室温で撹拌しながらpHをモニターして希硝酸を少量ずつ添加していき、pH2.5〜3.0に調整する。撹拌を続けているとpHは変動するので、常にpH2.5〜3.0に調整する。pH調整しながら、撹拌を1時間実施する。アルカリで熱処理粉を処理するとシリカ分は溶解するが、同時にFeやM元素もわずかながら溶解し、アルカリ溶液中で溶解し難い無定形なFeケイ酸塩やM元素ケイ酸塩が液中で合成されることが確認されている。これらのケイ酸塩は、酸に対する溶解度が高いため、上記操作により除去を行う(再溶解処理)。
【0048】
以上の手順1から手順6−2を経ることによって、目的とする試料(磁性粉末)を得た。この粉末のTEM写真を図2に示す。TEM平均粒子径は32.5nm、粒子径の標準偏差は18.7nm、変動係数は57.6%であった。
【0049】
得られた試料を上記図4の場合と同様の条件で粉末X線回折に供したところ、図3に示す回折パターンが得られた。この回折パターンは、ε−Fe2O3の結晶構造(斜方晶、空間群Pna21)に対応するピークを有しており、ε−Fe2O3結晶の生成が確認された。その他には、不純物結晶としてα−Fe2O3の結晶構造(六方晶、空間群R−3c)に対応するピークも観測された。また、アモルファス状のSi酸化物に起因すると考えられるブロードなピークも観測された。
【0050】
得られた試料を蛍光X線分析(日本電子製JSX―3220)に供したところ、YとFeのモル比は、Y/Fe×100=1モル%であった。これは、オキシ水酸化鉄を合成する際の仕込み組成がそのまま反映された結果であった。また、得られた試料中に含まれるSi量は、Si/Fe×100によるモル比で2.1モル%であった。
【0051】
《実施例2》
本例は、Yを添加していないオキシ水酸化鉄(α−FeOOH)を原料粉に使用してε−Fe2O3結晶を得た例である。原料粉は、上で例示したオキシ水酸化鉄合成工程に準じた一般的な湿式工程により合成した。ただし、ε−Fe2O3結晶のFeサイトの一部を置換するための元素MとしてGaを含有するオキシ水酸化鉄を使用した。Gaはオキシ水酸化鉄合成の初期の液中に硝酸ガリウムを添加することにより含有させた。原料粉合成時の仕込み組成において、GaとFeのモル比はGa/Fe×100=1モル%である。
【0052】
実施例1と同様に上記手順1〜手順6−2を実施した。ただし、手順5における熱処理温度を1000℃から1100℃に変更した。それ以外は実施例1と同じ条件である。
【0053】
手順1を終えた段階のオキシ水酸化鉄粉末のTEM写真を図5に示す。TEM平均粒子径は66.5nm、粒子径の標準偏差は21.1nm、変動係数(標準偏差/TEM平均粒子径×100)は31.6%であった。
【0054】
手順4(熱処理工程A)を終えた段階の前駆体を上記と同様の条件で粉末X線回折に供したところ、結晶質物質の回折ピークとしては、実施例1の場合と同様に、γ−Fe2O3またはFe3O4のスピネル結晶構造に対応する「立方晶酸化鉄」ピークしか観測されなかった。
【0055】
手順6−2を終えて得られた試料(磁性粉体)のTEM写真を図6に示す。TEM平均粒子径は32.2nm、粒子径の標準偏差は31.6nm、変動係数は66.5%であった。
【0056】
得られた試料を上記と同様の条件で粉末X線回折に供したところ、図7に示す回折パターンが得られた。この回折パターンは、ε−Fe2O3の結晶構造(斜方晶、空間群Pna21)に対応するピークを有しており、ε−Fe2O3結晶の生成が確認された。この結晶は実施例1で得られたε−Fe2O3結晶と比べ対応する各ピーク位置がわずかに高角側にシフトしていることから、格子定数が若干小さくなっている。これは、Feサイトの一部がFeよりも原子半径の小さいGaで置換された現象であると考えられる。不純物結晶としてα−Fe2O3の結晶構造(六方晶)に対応するピークと、γ−Fe2O3の結晶構造(立方晶)に対応するピークも観測された。
【0057】
得られた試料を上記と同様の蛍光X線分析に供したところ、GaとFeのモル比は、Ga/Fe×100=0.98モル%であった。これは、オキシ水酸化鉄を合成する際の仕込み組成がほぼそのまま反映された結果であった。また、得られた試料中に含まれるSi量は、Si/(Fe+Ga)×100によるモル比で1.0モル%であった。
【0058】
《実施例3》
本例は、実施例2において、オキシ水酸化鉄合成時の仕込み組成におけるGa含有量を、Ga/Fe×100によるモル比で1モル%から15モル%に増量させた例である。このとき、Gaの3モル%分はオキシ水酸化鉄合成の初期の液中に硝酸ガリウムを添加することによって含有させ、残りの12モル%分はオキシ水酸化鉄成長途中に硝酸ガリウム溶液を添加してドーピングすることにより含有させた。それ以外は上記手順1〜手順6−2における条件は熱処理温度を含め実施例2と共通である。
【0059】
手順1を終えた段階のオキシ水酸化鉄粉末のTEM写真を図8に示す。TEM平均粒子径は90.0nm、粒子径の標準偏差は21.2nm、変動係数(標準偏差/TEM平均粒子径×100)は30.2%であった。
【0060】
手順4(熱処理工程A)を終えた段階の前駆体を上記と同様の条件で粉末X線回折に供したところ、結晶質物質の回折ピークとしては、実施例1の場合と同様に、γ−Fe2O3またはFe3O4のスピネル結晶構造に対応する「立方晶酸化鉄」ピークしか観測されなかった。
【0061】
手順6−2を終えて得られた試料(磁性粉体)のTEM写真を図9に示す。TEM平均粒子径は47.2nm、粒子径の標準偏差は27.3nm、変動係数は57.8%であった。
【0062】
得られた試料を上記と同様の条件で粉末X線回折に供したところ、図10に示す回折パターンが得られた。この回折パターンは、ε−Fe2O3の結晶構造(斜方晶、空間群Pna21)に対応するピークを有しており、ε−Fe2O3結晶の生成が確認された。この結晶は実施例2の場合よりもさらに格子定数が若干小さくなっており、Feサイトの一部がFeよりも原子半径の小さいGaで置換されていることが肯定される。γ−Fe2O3結晶に対応するピークも観測されたが、α−Fe2O3結晶はほとんど検出されなかった。熱処理温度が同じである実施例2との対比から、Gaの置換量を増やしたことによって、不純物結晶であるα−Fe2O3結晶の生成が抑制される傾向が見られる。
【0063】
得られた試料を上記と同様の蛍光X線分析に供したところ、GaとFeのモル比は、Ga/Fe×100=13.6モル%であり、オキシ水酸化鉄を合成する際の仕込み組成に近い組成のものが得られた。また、得られた試料中に含まれるSi量は、Si/(Fe+Ga)×100によるモル比で1.0モル%であった。
【0064】
《比較例1》
本例は、実施例3で用いたオキシ水酸化鉄を原料粉に使用し、手順4の熱処理工程Aを省略したこと以外、実施例3と同様の条件で試料粉末を作成した例である。
【0065】
手順6−2を終えて得られた試料粉末のTEM写真を図11に示す。TEM平均粒子径は37.4nm、粒子径の標準偏差は18.1nm、変動係数は48.5%であった。
【0066】
得られた試料を上記と同様の条件で粉末X線回折に供したところ、図12に示す回折パターンが得られた。この回折パターンは、α−Fe2O3の結晶構造(六方晶、空間群R−3c)に対応するピークを示しており、ε−Fe2O3結晶の生成は認められなかった。
【0067】
得られた試料を上記と同様の蛍光X線分析に供したところ、GaとFeのモル比は、Ga/Fe×100=13.6モル%であり、オキシ水酸化鉄を合成する際の仕込み組成に近い組成のものが得られた。また、得られた試料中に含まれるSi量は、Si/(Fe+Ga)×100によるモル比で1.7モル%であった。
【0068】
《比較例2》
本例は、実施例3で用いたオキシ水酸化鉄を原料粉に使用し、手順4の熱処理工程Aにおいて、雰囲気を水素ガス100体積%の還元雰囲気に変更したこと以外、実施例3と同様の条件で試料粉末を作成した例である。
【0069】
手順4(熱処理工程A)を終えた段階の粉末を上記と同様の条件で粉末X線回折に供したところ、図14に示す回折パターンが得られた。原料粉であるオキシ水酸化鉄はα−Feにまで還元されてしまったことがわかる。
【0070】
手順6−2を終えて得られた試料粉末のTEM写真を図13に示す。TEM平均粒子径は34.6nm、粒子径の標準偏差は21.4nm、変動係数は61.7%であった。
【0071】
得られた試料を上記と同様の条件で粉末X線回折に供したところ、図15に示す回折パターンが得られた。この回折パターンは、α−Fe2O3の結晶構造(六方晶、空間群R−3c)に対応するピークを示しており、ε−Fe2O3結晶の生成は認められなかった。
【0072】
得られた試料を上記と同様の蛍光X線分析に供したところ、GaとFeのモル比は、Ga/Fe×100=13.6モル%であり、オキシ水酸化鉄を合成する際の仕込み組成に近い組成のものが得られた。また、得られた試料中に含まれるSi量は、Si/(Fe+Ga)×100によるモル比で1.2モル%であった。
【図面の簡単な説明】
【0073】
【図1】実施例1に使用したオキシ水酸化鉄のTEM写真。
【図2】実施例1で得られた試料粉末粒子のTEM写真。
【図3】実施例1で得られた試料粉末のX線回折パターン。
【図4】実施例1の熱処理工程Aで得られた前駆体のX線回折パターン。
【図5】実施例2に使用したオキシ水酸化鉄のTEM写真。
【図6】実施例2で得られた試料粉末粒子のTEM写真。
【図7】実施例2で得られた試料粉末のX線回折パターン。
【図8】実施例3に使用したオキシ水酸化鉄のTEM写真。
【図9】実施例3で得られた試料粉末粒子のTEM写真。
【図10】実施例3で得られた試料粉末のX線回折パターン。
【図11】比較例1で得られた試料粉末粒子のTEM写真。
【図12】比較例1で得られた試料粉末のX線回折パターン。
【図13】比較例2で得られた試料粉末粒子のTEM写真。
【図14】比較例2で得られた試料粉末のX線回折パターン。
【図15】比較例2の熱処理工程Aで得られた粉末のX線回折パターン。
【特許請求の範囲】
【請求項1】
立方晶酸化鉄の粒子をSi酸化物で覆われた状態において700〜1300℃の酸化雰囲気下で熱処理するε−Fe2O3結晶の製法。
【請求項2】
前記立方晶酸化鉄の粒子は、粒子径が200nm以下のものである請求項1に記載のε−Fe2O3結晶の製法。
【請求項3】
前記立方晶酸化鉄の粒子は、ε−Fe2O3のFeサイトの一部を置換するための金属元素Mを含有するものである請求項1または2に記載のε−Fe2O3結晶の製法。
【請求項4】
オキシ水酸化鉄の粒子を弱還元雰囲気下で熱処理することにより立方晶酸化鉄を生成させる熱処理工程Aと、熱処理工程Aで得られた粒子を酸化雰囲気下で熱処理することにより立方晶酸化鉄からε−Fe2O3結晶を生成させる熱処理工程Bを有するε−Fe2O3結晶の製法。
【請求項5】
オキシ水酸化鉄の粒子をSi酸化物に覆われた状態において弱還元雰囲気下で熱処理することにより立方晶酸化鉄を生成させる熱処理工程Aと、熱処理工程Aで得られた粒子をSi酸化物に覆われた状態において酸化雰囲気下で熱処理することにより立方晶酸化鉄からε−Fe2O3結晶を生成させる熱処理工程Bを有するε−Fe2O3結晶の製法。
【請求項6】
熱処理工程Aは、弱還元雰囲気が水蒸気を混合した水素ガス雰囲気であり、熱処理温度が300〜600℃の範囲の温度である請求項4または5に記載のε−Fe2O3結晶の製法。
【請求項7】
熱処理工程Bは、酸化雰囲気が窒素と酸素の混合雰囲気であり、熱処理温度が700〜1300℃の範囲の温度である請求項4または5に記載のε−Fe2O3結晶の製法。
【請求項8】
熱処理工程Aに供するオキシ水酸化鉄の粒子が、ε−Fe2O3のFeサイトの一部を置換するための金属元素Mを含有するものである請求項4または5に記載のε−Fe2O3結晶の製法。
【請求項1】
立方晶酸化鉄の粒子をSi酸化物で覆われた状態において700〜1300℃の酸化雰囲気下で熱処理するε−Fe2O3結晶の製法。
【請求項2】
前記立方晶酸化鉄の粒子は、粒子径が200nm以下のものである請求項1に記載のε−Fe2O3結晶の製法。
【請求項3】
前記立方晶酸化鉄の粒子は、ε−Fe2O3のFeサイトの一部を置換するための金属元素Mを含有するものである請求項1または2に記載のε−Fe2O3結晶の製法。
【請求項4】
オキシ水酸化鉄の粒子を弱還元雰囲気下で熱処理することにより立方晶酸化鉄を生成させる熱処理工程Aと、熱処理工程Aで得られた粒子を酸化雰囲気下で熱処理することにより立方晶酸化鉄からε−Fe2O3結晶を生成させる熱処理工程Bを有するε−Fe2O3結晶の製法。
【請求項5】
オキシ水酸化鉄の粒子をSi酸化物に覆われた状態において弱還元雰囲気下で熱処理することにより立方晶酸化鉄を生成させる熱処理工程Aと、熱処理工程Aで得られた粒子をSi酸化物に覆われた状態において酸化雰囲気下で熱処理することにより立方晶酸化鉄からε−Fe2O3結晶を生成させる熱処理工程Bを有するε−Fe2O3結晶の製法。
【請求項6】
熱処理工程Aは、弱還元雰囲気が水蒸気を混合した水素ガス雰囲気であり、熱処理温度が300〜600℃の範囲の温度である請求項4または5に記載のε−Fe2O3結晶の製法。
【請求項7】
熱処理工程Bは、酸化雰囲気が窒素と酸素の混合雰囲気であり、熱処理温度が700〜1300℃の範囲の温度である請求項4または5に記載のε−Fe2O3結晶の製法。
【請求項8】
熱処理工程Aに供するオキシ水酸化鉄の粒子が、ε−Fe2O3のFeサイトの一部を置換するための金属元素Mを含有するものである請求項4または5に記載のε−Fe2O3結晶の製法。
【図3】


【図4】


【図7】


【図10】


【図12】


【図14】


【図15】


【図1】


【図2】


【図5】


【図6】


【図8】


【図9】


【図11】


【図13】




【図4】


【図7】


【図10】


【図12】


【図14】


【図15】


【図1】


【図2】


【図5】


【図6】


【図8】


【図9】


【図11】


【図13】


【公開番号】特開2008−100871(P2008−100871A)
【公開日】平成20年5月1日(2008.5.1)
【国際特許分類】
【出願番号】特願2006−284464(P2006−284464)
【出願日】平成18年10月19日(2006.10.19)
【出願人】(504137912)国立大学法人 東京大学 (1,942)
【出願人】(506334182)DOWAエレクトロニクス株式会社 (336)
【Fターム(参考)】
【公開日】平成20年5月1日(2008.5.1)
【国際特許分類】
【出願日】平成18年10月19日(2006.10.19)
【出願人】(504137912)国立大学法人 東京大学 (1,942)
【出願人】(506334182)DOWAエレクトロニクス株式会社 (336)
【Fターム(参考)】
[ Back to top ]

