がん細胞またはがん発症性ウイルス感染細胞の増殖抑制剤
【課題】肝がん細胞及び白血病細胞の増殖を抑制しがんの改善に有効に使用できる細胞増殖抑制剤、ウイルス感染細胞の増殖を抑制しがん発症の阻止予防に有効に使用できる細胞増殖抑制剤を提供する。
【解決手段】
細胞増殖抑制剤の有効成分として、ブルーベリー葉の粉砕物、搾汁、あるいはその抽出成分を用いる。
【解決手段】
細胞増殖抑制剤の有効成分として、ブルーベリー葉の粉砕物、搾汁、あるいはその抽出成分を用いる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、がん細胞またはがん発症性ウイルス感染細胞の増殖を抑制するための材料(剤)、より詳細には天然の植物成分を有効成分とするがん細胞またはがん発症性ウイルス感染細胞の増殖抑制剤に関する。
【背景技術】
【0002】
日本人の死亡原因の第一位はがんであり、がん予防とがん治療は国民の健康上極めて重要な課題である。特に九州は、がんの中でも、成人T細胞白血病(Adult T-cell leukemia: ATL)を始めとする白血病、及び肝がんの発生率が高いとされている地域である。その理由の一つとして、九州にはヒトレトロウイルスHTLV-1(ヒトT細胞白血病ウイルス1型)に感染している人(HTLV-1キャリア)が多いことが挙げられる。ATLの発生にはHTLV-1が強く関係しており、HTLV-1感染者だけにATLが発生することが知られている。近年白血病の治療は非常に進歩しており、完治する白血病もある中で、ATLは最も治療に抵抗性の白血病である。加えて、他のウイルスと異なって、一旦HTLV-1に感染すると、一生涯身体の中にそのウイルスが存在し続ける。また、肝がんもC型肝炎ウイルス(Hepatitis C Virus:HCV)による持続感染が原因となって発症することが知られている。
【0003】
従って、がん細胞の増殖を抑制するというだけでなく、がんを発症する可能性のあるウイルス感染細胞の増殖を抑制することによってがんの発症を抑制することも必要である。
【0004】
非特許文献1には、疫学調査の結果として、緑黄色野菜や果物を多く摂取すると発がんのリスクが軽減されることが示されている。また、非特許文献2には、ブルーベリーを含むVaccinium属に属する植物の果実及び葉の酢酸エチル抽出物が、がんのプロモーター抑制の一つの指標であるキノンレダクターゼ誘導活性を有すること、また、非特許文献3では、Vaccinium属のビルベリー組織から誘導したカルスにより生産されたフラボノイド等を含む培養液が、乳がん細胞の増殖を抑制することが報告されている。
【0005】
しかしながら、上記したブルーベリー葉の酢酸エチル抽出物の抗がん機能(非特許文献2)は、キノンレダクターゼを誘導させることによって活性酸素の生成を妨害して発がんを抑制するというものであり、活性酸素の生成以外を要因として生じるがんに対しては有効とはいえない。また、がんの原因を除去することによって発がんを防止するものであるため、既にがん化した細胞に対しては有効とはいえない。
【0006】
また、がん全般に効く薬剤はなく、がんの種類によって治療薬物が異なることが当業界では周知となっている。例えば、非特許文献4によると、白血病は、化学療法(抗がん剤)で完治する可能性のあるがん、乳がんは病気の進行を遅らせることができるがん、そして肝がんは効果が期待できずがんも小さくなりもしないがんと、分類されている。従って、乳がん細胞の増殖抑制作用を有するものが(非特許文献3)、直ちに他のがん細胞に有効に使用できることにはならない。
【非特許文献1】M.M.Mathews-Roth,Pure Apll.Chem.,63, 147-156(2004)
【非特許文献2】J.Bomser, D.L.Madhavi, K.Singletary and M.A.L.Smith:Planta Medica.,62,212-216(1996)
【非特許文献3】浜松潮香「ブルーベリーの機能性研究;ブルーベリーの培養細胞による有用物質生産」,食品工業,43(2),44(2000)
【非特許文献4】国立がんセンターホームページ「がんに関する情報」の中の「治療−がんの薬物療法」http://www.ncc.go.jp/jp/ncc-cis/pub/treatment/010708.html
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明は、天然の植物成分に由来する、がん細胞(肝がん細胞、白血病細胞)またはがん発症性ウイルス感染細胞(HTLV-1感染細胞)の増殖を抑制するための材料(剤)を提供することを目的とする。さらに本発明は、かかる材料を有効成分とする医薬組成物および食品組成物を提供することを目的とする。特に、がん細胞またはがん発症性ウイルス感染細胞の増殖を特異的に抑制することのできる医薬組成物および食品組成物を提供することを目的とする。
【課題を解決するための手段】
【0008】
本発明者らは、上記目的を達成すべく鋭意研究を重ねていたところ、ブルーベリーの葉の溶媒抽出物に、特異的に肝がん細胞及び白血病細胞の増殖を抑制する作用があること、及び成人T細胞白血病(ATL)等の原因となるHTLV-1感染細胞の増殖を抑制する作用があることを見いだし、当該抽出物が上記作用に基づいて、肝がんや白血病に対する抗がん剤、また成人T細胞白血病(ATL)や肝がんの発症予防剤などの医薬組成物として有効であることを確信した。
【0009】
本発明はかかる知見に基づいて完成したものであり、下記の態様を有するものである:
項1.ブルーベリー葉の加工処理物を有効成分とする、肝がん細胞、白血病細胞、及びHTLV-1感染細胞よりなる群から選択される少なくとも1つの細胞に対する細胞増殖抑制剤。
項2.ブルーベリー葉の加工処理物が、葉の粉砕物、葉の搾汁、及び葉の抽出物よりなる群から選択される少なくとも1つである、項1記載の細胞増殖抑制剤。
項3.葉の抽出物が、ブルーベリー葉を水及びアルコールの少なくとも1つの溶媒で抽出して得られる抽出物である項2記載の細胞増殖抑制剤。
項4.白血病細胞が、ヒト急性前骨髄性白血病細胞、ヒトT細胞性白血病細胞、および成人T細胞白血病細胞よりなる群から選択される少なくとも1つである項1乃至3のいずれか1項に記載の細胞増殖抑制剤。
項5.項1乃至4のいずれかに1項に記載する細胞増殖抑制剤を含む医薬組成物。
項6.抗がん剤である、項5に記載する医薬組成物。
項7.肝がんまたは白血病に対する抗がん剤である、項6に記載する医薬組成物。
項8.成人T細胞白血病の発症予防剤である、項5に記載する医薬組成物。
項9.項1乃至4のいずれかに1項に記載する細胞増殖抑制剤を含む食品組成物。
項10.肝がん細胞、白血病細胞、及びHTLV-1感染細胞よりなる群から選択される少なくとも1つの細胞に対して細胞増殖抑制作用を有することを特徴とし、肝がんまたは白血病の予防または改善のために用いられる旨の表示を付した項9に記載する食品組成物。
【0010】
以下、本発明を詳説する。
【0011】
ブルーベリーは、ツツジ科(Ericaceae)スノキ属(Vaccinium)サイアノココス節(Cyanococcus)に分類される、アメリカ原産の落葉性あるいは常緑性の、低木性(または半高木性)の果樹である(Vander Kloet, 1988:玉田、1996)。ブルーベリーはおよそ6種類からなるが、果樹園芸上重要な種は、(1)ハイブッシュブルーベリー(Highbush blueberry, Vaccininum corymbosum.L)、(2)ラビットアイブルーベリー(Rabbiteye blueberry, V.ashei Reade)、(3)ローブッシュブルーベリー(Lowbush blueberry, V.angstifolium MichauxとV.myrtilloides Aition)の3つである。ブルーベリーは20世紀の初頭からアメリカ農務省あるいは州立大学によって野生種から改良された種類である。品種改良の方向は栽培が容易であり、果実が大きくて甘いなど良品種の生果生産を目標として進められ、今日では世界各国でつくられている。
【0012】
なお、本発明は、使用するブルーベリーについて、その種類やその由来・原産地を特に制限するものではなく、いずれも使用することができる。
【0013】
本発明はブルーベリーの葉を用いることを特徴とする。後述する実施例4の試験結果を示す図4、図5、図6から明らかなように、各種機能性が公知となっているブルーベリー果実に比較し、ブルーベリー葉は、9種類のがん細胞において、高いがん細胞増殖抑制作用をもっている。このことから、ブルーベリーの葉の癌細胞増殖抑制作用は、ブルーベリーの果実とは異なる成分あるいは機序によるものと推定でき、未利用資源としての域を脱しないブルーベリー葉の有効活用の可能性を大いに期待させるものである。
【0014】
ここで、ブルーベリー葉はそのままでも使用できるが、好ましくは加工処理を施したもの(加工処理物)が用いられる。加工処理物としては、ブルーベリーの葉の粉砕物(生、乾燥物)、ブルーベリー葉を搾って得られる搾汁またはブルーベリー葉を任意の溶媒で抽出して得られる抽出物を例示することができる。ブルーベリーの葉の加工処理物として、好ましくは抽出物である。
【0015】
乾燥粉砕物は、ブルーベリーの葉を例えばそのまま乾燥した後粉砕するか、又は生葉を細く切断した後乾燥することによって調製することができる。その乾燥には、本発明の薬効効果を損なわない方法であれば特に制限されず、真空凍結乾燥、熱風乾燥、遠赤外線乾燥、減圧乾燥、マイクロ波減圧乾燥及び過熱蒸気乾燥等を広く用いることができる。好ましくは成分変化の少ない真空凍結乾燥である。
【0016】
ブルーベリー葉の抽出物は、例えば葉をそのまま若しくは破砕物とした後抽出操作に供するか、また乾燥後、必要に応じて粉砕して抽出操作に供することによって調製することができる。また、葉を搾って得られる搾汁も抽出材料として使用することができ、これらは必要に応じて濃縮または乾燥して抽出操作に供することができる。
【0017】
ブルーベリー葉の抽出に用いる溶媒としては、特に制限されず、水、極性有機溶媒または非極性有機溶媒のいずれであってもよい。好ましくは水または水と相溶性のある極性溶媒を挙げることができる。水と相溶性のある極性溶媒としては、メタノール、エタノール、プロパノール及びブタノール等の炭素数1〜4の低級アルコール;エチレングリコール、ブチレングリコール、プロピレングリコール、グリセリンなどのグリコール類;エチルエーテル、アセトン、アセトニトリルを挙げることができる。かかる極性溶媒として、好ましくは低級アルコールであり、特に好ましくはエタノールである。
【0018】
これらの溶媒は、単独で用いてもよく、二種以上を組み合わせて使用することもできる。例えば、アセトンとエチルエーテルの混合溶媒(好ましくはアセトン:エチルエーテル=1:1(v/v)混合液)、上記極性有機溶媒と水との混合溶媒(含水溶媒)を挙げることができる。含水溶媒として好ましくは、低級アルコールと水との混合物(含水アルコール)、より好ましくはエタノールと水との混合物(含水エタノール)を例示することができる。含水アルコール中のアルコール濃度も特に制限されないが、例えば5〜90容量%、好ましくは30〜90容量%、より好ましくは50〜90容量%を挙げることができる。
【0019】
抽出方法としては、一般に用いられている方法をいずれも採用することができる。例えば、溶媒中にブルーベリー葉(そのまま若しくは粗末、細切物)、又はそれらの乾燥粉砕物(粉末など)を浸漬する方法;撹拌しながら抽出を行い、ろ過して抽出液を得る方法;またはパーコレーション法等を挙げることができる。なお、特に制限はされないが、例えば、抽出溶媒として80容量%の割合でエタノールを含む含水エタノールを用いる場合は、安定して抽出できる方法として室温下攪拌抽出を行うことが好ましい。
【0020】
得られた抽出物は、必要に応じて、ろ過または遠心分離などの操作により固形物を除去することも好ましい方法の一つである。次への工程で行われる操作に応じて、そのまま用いるか、または溶媒を留去して一部濃縮若しくは乾燥して用いてもよい。また濃縮あるいは乾燥後、さらに適正な洗浄溶媒、例えば、非溶解性溶媒で洗浄精製して用いても、またこれを更に適当な溶剤に溶解若しくは懸濁して用いることもできる。更に、本発明においては、例えば、上記のようにして得られた溶媒抽出液を、減圧乾燥、凍結乾燥等の通常の手段によりブルーベリー葉乾燥抽出エキスとして使用することもできる。
【0021】
斯くして得られるブルーベリー葉の粉砕物、搾汁液若しくは抽出物は、後述の実施例に記載するように、肝がん細胞、及び白血病細胞の増殖を抑制する作用を有している。ここで白血病細胞としては全てヒトの白血病細胞で、急性前骨髄性白血病細胞、急性リンパ性 (T細胞性) 白血病細胞、成人T細胞白血病細胞を挙げることができる。このため、本発明の細胞増殖抑制剤は、肝がんや白血病(例えば、急性前骨髄性白血病、T細胞性白血病、成人T細胞白血病)に対する抗がん剤(医薬組成物)の有効成分として、有効に用いることができる。また、本発明の細胞増殖抑制剤は、肝がん細胞、及び白血病細胞の増殖を抑制する作用を有する食品組成物(例えば、栄養補助食品、機能性食品、特定保健用食品など)の有効成分として有効に用いることができる。
【0022】
さらに、ブルーベリー葉の粉砕物、搾汁若しくは抽出物は、成人T細胞白血病発症性のウイルス感染細胞である、ヒトレトロウイルスHTLV-1感染細胞(HTLV-1感染細胞)の増殖を抑制する作用を有している。このため、本発明の細胞増殖抑制剤は、成人T細胞白血病の発症を阻止し予防するための組成物(医薬組成物や食品組成物)の有効成分として、有効に利用することができる。
【0023】
なお、HTLV-1感染細胞が関与する病気として、HAM(HTLV-1関連脊髄症)、HAU(HTLV-1関連ぶどう膜炎)、HAB (HTLV-1関連気管支・肺障害)が知られている。このため本発明の細胞増殖抑制剤は、HTLV-1感染細胞の増殖を抑制することによって、これらの病気(HTLV-1関連脊髄症、HTLV-1関連ぶどう膜炎、HTLV-1関連気管支・肺障害)の発症を阻止し予防するための組成物(医薬組成物や食品組成物)の有効成分として、有効に利用することができる。
【0024】
なお、本発明でいう細胞増殖抑制作用とは、細胞全体としての数(総細胞数)が減少する作用が認められればよく、細胞の発育・成長を阻止する作用や細胞を死滅させる作用などの作用機序の別を問わない。
【0025】
本発明の細胞増殖抑制剤は、上記ブルーベリー葉の粉砕物、搾汁若しくは抽出物そのものを単独で固体又は液体状で利用することもできるが、それに加えて薬学的若しくは食品上許容される担体または添加剤を配合して、固体又は液体状の医薬組成物または食品組成物として調製することができる。
【0026】
ゆえに本発明は、前述する細胞増殖抑制剤を有効成分とする医薬組成物または食品組成物を提供するものでもある。
【0027】
かかる本発明の医薬組成物または食品組成物は、上記本発明の細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)の作用(肝がん細胞増殖抑制作用、白血病細胞増殖抑制作用、HTLV-1感染細胞増殖抑制作用)に基づいて、肝がんに対する改善作用、白血病に対する予防若しくは改善作用、成人T細胞白血病(ATL)発症予防作用、またはHTLV-1感染細胞が関与する疾患(例えばHTLV-1関連脊髄症、HTLV-1関連ぶどう膜炎、HTLV-1関連気管支・肺障害)の発症予防作用を有している。
【0028】
本発明の医薬組成物は、その形態として特に制限されないが、経口に適した形態であることが好ましい。例えば、経口投与用固体組成物(固形医薬製剤)としては錠剤(糖衣錠を含む)、丸剤、カプセル剤、細粒剤、顆粒剤等の形態を、また経口投与用液状組成物(液状医薬製剤)としては乳濁剤、溶液剤、懸濁剤、シロップ剤などの形態を例示することができる。これらの製剤は、有効成分である細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)に加えて、各種製剤に応じて賦形剤、結合剤、崩壊剤、滑沢剤、着色料、矯味矯臭剤、pH調整剤等を適宜配合し、常法に従って調製することができる。
【0029】
なお、本発明の医薬組成物には、上記細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁液若しくは抽出物)に加えて、がん細胞増殖抑制作用(肝がん細胞増殖抑制作用、または白血病細胞増殖抑制作用)を有する他の成分が含まれていても良い。
【0030】
本発明の医薬組成物の投与量は、特に限定されず、所望の治療効果、投与法、治療期間、被験者の年齢、性別その他の条件などに応じて広範囲より適宜選択される。投与経路によっても異なるが、例えば体重60kgのヒトに対する投与量は、1回投与あたりの上記細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)の量(ブルーベリー葉の乾燥重量に換算して)として、約600〜6000 mg/(60kg体重)の範囲から適宜選択することができる。
【0031】
本発明が提供する医薬組成物に含まれる細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)の量は、その製剤形態や適用疾患の種類などによって種々異なり、一概に規定することはできないが、上記投与量(1投与あたり)に応じて適宜設定することができる。
【0032】
本発明の食品組成物も、その形態は特に制限されない。例えば、前述する細胞増殖抑制剤を、必要に応じて食品上配合が許容される担体や添加剤とともに、錠剤、丸剤、カプセル剤、顆粒剤、散剤、粉末剤、トローチ剤、または溶液(ドリンク)等の形態に調製してなるサプリメント(機能性食品)の形態を有するものであってもよい。
【0033】
本発明の食品組成物は、上記細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)を含有することによって、その肝がん細胞増殖抑制作用、白血病細胞増殖抑制作用、またはHTLV-1感染細胞増殖抑制作用を有している。このため、本発明が対象とする食品組成物には各種の効果を効能とする食品(例えば特定保健用食品、栄養補助食品、機能性食品等)も含まれる。
【0034】
特定保健用食品(条件付き特定保健用食品も含まれる)の中には、上記有効成分(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)を含有することにより、肝がんに対する改善作用、白血病に対する予防若しくは改善作用、成人T細胞白血病(ATL)発症予防作用、またはHTLV-1感染細胞が関与する疾患(HTLV-1関連脊髄症、HTLV-1関連ぶどう膜炎、HTLV-1関連気管支・肺障害等)の発症予防作用を有し、このため肝がん改善作用、白血病予防若しくは改善作用、成人T細胞白血病(ATL)発症予防、またはHTLV-1感染細胞が関与する疾患(HTLV-1関連脊髄症、HTLV-1関連ぶどう膜炎、HTLV-1関連気管支・肺障害等)の発症予防作用のために用いられる旨が包装パッケージに記載されてなる食品が含まれる。
【0035】
本発明が対象とする食品組成物としては、例えば乳飲料、乳酸菌飲料、果汁入り清涼飲料、清涼飲料、炭酸飲料、果汁飲料、野菜飲料、野菜・果実飲料、アルコール飲料、粉末飲料、コーヒー飲料、紅茶飲料、緑茶飲料、麦茶飲料などの飲料類;カスタードプリン、ミルクプリン、スフレプリン、果汁入りプリン等のプリン類、ゼリー、ババロア及びヨーグルト等のデザート類;アイスクリーム、アイスミルク、ラクトアイス、ミルクアイスクリーム、果汁入りアイスクリーム及びソフトクリーム、アイスキャンディー、シャーベット、氷菓等の冷菓類;チューインガムや風船ガム等のガム類(板ガム、糖衣状粒ガム);マーブルチョコレート等のコーティングチョコレートの他、イチゴチョコレート、ブルーベリーチョコレート及びメロンチョコレート等の風味を付加したチョコレート等のチョコレート類;ハードキャンディー(ボンボン、バターボール、マーブル等を含む)、ソフトキャンディー(キャラメル、ヌガー、グミキャンディー、マシュマロ等を含む)、ドロップ、タフィ等のキャラメル類;ハードビスケット、クッキー、おかき、煎餅等の焼き菓子類(以上、菓子類);コンソメスープ、ポタージュスープ等のスープ類;味噌、醤油、ドレッシング、ケチャップ、たれ、ソース、ふりかけなどの各種調味料;ストロベリージャム、ブルーベリージャム、マーマレード、リンゴジャム、杏ジャム、プレザーブ等のジャム類;赤ワイン等の果実酒;シロップ漬のチェリー、アンズ、リンゴ、イチゴ、桃等の加工用果実;ハム、ソーセージ、焼き豚等の畜肉加工品;魚肉ハム、魚肉ソーセージ、魚肉すり身、蒲鉾、竹輪、はんぺん、薩摩揚げ、伊達巻き、鯨ベーコン等の水産練り製品;うどん、冷麦、そうめん、ソバ、中華そば、スパゲッティ、マカロニ、ビーフン、はるさめ及びワンタン等の麺類;その他、各種総菜及び麩、田麩等の種々の加工食品を挙げることができる。好ましくは飲料、麺類、菓子類である。
【0036】
上記食品組成物に含まれる上記細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)の量、または摂取量は、特に限定されず、食品組成物の種類、目的とする機能・効能、並びにその他の諸条件などに応じて広範囲より適宜選択される。摂取量は、食品組成物の種類によっても異なるが、体重60kgのヒトに対して1回摂取あたりの細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)の量(ブルーベリー葉の乾燥重量に換算して)として、約600〜6000 mg/(60kg体重)の範囲から適宜選択するのが望ましい。
【発明の効果】
【0037】
本発明の細胞増殖抑制剤は、天然植物であるブルーベリー葉の加工処理物(例えば、ブルーベリー葉の粉砕物、搾汁又は抽出物)を有効成分とするものであって、肝がん細胞、及び白血病細胞に対して増殖抑制作用を有する。このため、本発明の細胞増殖抑制剤およびこれを有効成分とする組成物(医薬組成物、食品組成物)は、既にがん化した細胞に対しても作用しその増殖を抑制することによって、肝がんの改善または治療、及び白血病の改善または治療に有効に用いることができる。
【0038】
さらに本発明の細胞増殖抑制剤は、HTLV-1感染細胞に対しても増殖抑制作用を有する。このため、本発明の細胞増殖抑制剤及びこれを有効成分とする組成物(医薬組成物、食品組成物)は、HTLV-1感染によるがんの発症、とくに成人T細胞白血病の発症を阻止し予防するために有効に用いることができる。また、本発明の細胞増殖抑制剤及びこれを有効成分とする組成物(医薬組成物、食品組成物)は、HTLV-1感染細胞が関与する疾患(HTLV-1関連脊髄症、HTLV-1関連ぶどう膜炎、HTLV-1関連気管支・肺障害など)の発症を阻止し予防するために有効に用いることができる。
【0039】
また、本発明の細胞増殖抑制剤の有効成分(ブルーベリー葉の粉砕物、搾汁又は抽出物)は天然の食用植物に由来するものである。従って、本発明の細胞増殖抑制剤およびこれを含む組成物(医薬組成物、食品組成物)は、副作用が少なく長期にわたって服用または摂取することが可能である。
【発明を実施するための最良の形態】
【0040】
以下に、本発明を実施するための最良の形態として実施例を挙げて、本発明の内容をより詳細を説明する。但し、本発明は実施例だけに限定されるものではない。なお、特に言及しない限り、下記の実施例において「%」は「w/w%」を意味するものとする。
【0041】
実施例1 ブルーベリー葉の乾燥粉末物の調製
ブルーベリー〔ハイブッシュブルーベリー種(10品種):オニール、シャープブルー、ジョージア、フローダブルー、レベレイ、スパルタン、ダロウ、デューク、バークレイ、ハリソン、ラビットアイブルーベリー種(5品種):ウッダード、ガーデンブルー、ティフブルー、ホームベル、マイヤー〕の葉を品種ごとに、凍結温度-30℃、乾燥温度30℃、乾燥時間24時間で真空凍結乾燥(真空凍結乾燥機、FTS SYSTEM、Dura-Top MP&Dura-Dry MP)し、超遠心粉砕機(MRK&RETSCH、EM-1型)で0.5mmのスクリーンを通して粉砕して、ブルーベリー葉の乾燥粉末物を調製した。
【0042】
実施例2 ブルーベリー葉の抽出エキスの調製
実施例1で調製したブルーベリー〔ハイブッシュブルーベリー種(10品種):オニール、シャープブルー、ジョージア、フローダブルー、レベレイ、スパルタン、ダロウ、デューク、バークレイ、ハリソン、ラビットアイブルーベリー種(5品種):ウッダード、ガーデンブルー、ティフブルー、ホームベル、マイヤー〕の葉の乾燥粉末物に、それぞれ80容量%の割合でエタノールを含む含水エタノールを加え室温で30秒間激しく撹拌した後、ろ過した。ろ液を減圧濃縮して溶媒を留去し、さらに真空凍結乾燥処理し完全に溶媒を留去して、ブルーベリー葉の乾燥抽出エキスを調製した。
【0043】
実施例3 がん細胞増殖抑制試験
実施例2で調製したブルーベリー葉の乾燥抽出エキスのうち、ラビットアイブルーベリー種に属するホームベルの抽出エキスを用いて、各種のがん細胞の増殖抑制作用を調べた。
【0044】
(1)ヒト急性前骨髄性白血病細胞(HL60)に対する増殖抑制作用
ブルーベリー葉の抽出エキスのヒト急性前骨髄性白血病細胞(HL60)に対する増殖抑制作用を、WST-8アッセイを用いて評価した。なお、WST-8アッセイは生細胞の数を測定する方法である。すなわち、WST-8アッセイで用いるWST-8 〔2-(2-Methoxy-4-nitrophenyl)-3-(4-nitrophenyl)-5-(2,4-disulfophenyl)-2H-tetrazolium, monosodium salt〕は、細胞共存下、細胞内脱水素酵素により還元され、水溶性のホルマザンを生成するが、この生成されたホルマザン量が生細胞の数と比例することから、ホルマザンの吸光度(測定波長450nm/対照波長650nm)を直接測定することにより、生細胞数の測定ができるというものである。
【0045】
測定は、まず、抽出エキスの終濃度を62.5μg/ml、125μg/ml、250μg/ml、または500μg/mlになるようにリン酸緩衝液〔PBS(-)〕で希釈し(被験試料)、1μlずつ96穴プレートに分注した。ここにヒト急性前骨髄性白血病細胞(HL60)の懸濁液(1×105cells/ml)を100μlずつ加えて混合し、37℃、5%CO2存在下、相対湿度100%で48時間培養した。次いでWST-8混合試薬(商品名:Tetra Color ONE、SEIKAGAKU CORPORATION社製)を10μl加えてさらに4時間培養後、650nmを対照波長として450nmの吸光度を測定した。なお、上記被験試料に代えて、抽出エキスを添加しないリン酸緩衝液のみを用いて、上記と同様にして生存HL60細胞数を、吸光度(波長450nm)として測定した。これをコントロールとして、それに対する百分率で、抽出エキスで処理したHL60細胞の生存率を求めた。結果を表1及び図1に示す。
【0046】
【表1】

【0047】
表1及び図1からわかるように、ブルーベリー葉の抽出エキスには、ヒト急性前骨髄性白血病細胞(HL-60細胞)の増殖を抑制する非常に強い作用があることがわかる。
【0048】
(2)肝がん細胞(Huh-7、HLE、HLF)に対する増殖抑制作用
ブルーベリー葉の抽出エキスの各種ヒト肝がん細胞(Huh-7、HLE、HLF)に対する増殖抑制作用を、上記と同様に、WST-8アッセイを用いて評価した。具体的には、3種類の肝がん細胞(Huh-7、HLE、HLF)の懸濁液(1×104cells/ml)をそれぞれ100μlずつ96穴プレートに分注し、37℃、5%CO2存在下、相対湿度100%で24時間培養し細胞の接着を確認した。次いで、各ウェルに予め、終濃度が62.5μg/ml、125μg/ml、250μg/ml及び500μg/mlになるようにリン酸緩衝液(PBS(-))で濃度を調整しておいた抽出エキスを1μlずつ添加して(被験試料)、37℃、5%CO2存在下、相対湿度100%で72時間培養した。これにWST-8混合試薬(商品名:Tetra Color ONE、SEIKAGAKU CORPORATION社製)を10μl加えてさらに4時間培養後、650nmを対照波長として450nmの吸光度を測定した。
【0049】
なお、上記被験試料に代えて、抽出エキスを添加しないリン酸緩衝液のみを用いて、上記と同様にして生存細胞数を吸光度(波長450nm)として測定した。この場合のこれをコントロール(100%)として、それに対する百分率で、抽出エキスで処理した各種肝がん細胞(HuH-7, HLE, HLF)の生存率を求めた。結果を表2及び図2に示す。
【0050】
【表2】

【0051】
表2及び図2の結果から、ブルーベリー葉の抽出エキスには、肝がん細胞の増殖を抑制する非常に強い作用があることがわかる。
【0052】
(3)ヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)、及び成人T細胞白血病細胞(ATL細胞)(ED, Su9T01, S1T)に対する増殖抑制作用
ブルーベリー葉の抽出エキスの、ヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102,MT2)、及びATL細胞(ED,Su9T01,S1T)に対する増殖抑制作用を、MTTアッセイを用いて評価した。なお、HTLV-1(Human T cell leukemia virus type 1)は、ヒトで初めて発見されたレトロウイルスのことで、成人T細胞白血病(ATL:Adult T cell leukemia)などを引き起こすとされている。なお、MTTアッセイは、WST-8アッセイ同様、生細胞の数を測定する方法である。すなわち、MTTアッセイで用いるMTT〔3-(4,5-Dimethyl-2-thiazolyl)-2,5-diphenyl-2H tetrazolium bromide〕は黄色の化合物で、生細胞のミトコンドリアの呼吸鎖に作用し、存在する酵素によってテトラゾリウム環が開裂し、青色のホルマザンを生成する。この生成されたホルマザン量が生細胞の数と比例することから、ホルマザンの吸光度を直接測定することにより、生細胞数の測定ができるというものである。
【0053】
測定は、まず、ヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)、ATL細胞(ED, Su9T01, S1T)(合計7種類のがん細胞)の懸濁液(1×105cells/ml)をそれぞれ99μlずつ96穴プレートに分注した。これに、予め終濃度が3.91μg/ml、7.81μg/ml、15.6μg/ml、31.3μg/ml、62.5μg/ml、125μg/ml、250μg/ml及び500μg/mlになるようにリン酸緩衝液(PBS(-))で調整した抽出エキスを1μlずつ添加して(被験試料)、37℃、5%CO2存在下、相対湿度100%で48時間培養した。次いで、MTT試薬(商品名MTT lyophilized、同仁化学研究所製)を10μl加えてさらに4時間培養した後、100μlずつ溶解液(0.04M/HCl/イソプロピルアルコール)を加えよくピペッティングし、色素を溶解した。その後650nmを対照波長とし570nmの吸光度を測定した。
【0054】
なお、上記被験試料に代えて、抽出エキスを添加しないリン酸緩衝液のみを用いて、上記と同様にして生存細胞数を吸光度(波長570nm)として測定した。これをコントロール(100%)として、それに対する百分率で、抽出エキスで処理した各種がん細胞の生存率を求めた。
【0055】
7種類のがん細胞(Jurkat, MOLT4,HUT102, MT2,ED, Su9T01, S1T)に各種濃度のブルーベリー葉の抽出エキスを添加して48時間培養した後の生存率(%)を、表3及び図3に示す。
【0056】
【表3】

【0057】
これらの結果から、ブルーベリー葉の抽出エキスには、ヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)及び成人T細胞白血病細胞(ED, Su9T01, S1T)の増殖を抑制する強い作用があることがわかった。
【0058】
実施例4 ブルーベリーの葉または果実のがん細胞増殖抑制試験
(1)実施例3の方法に従って、ブルーベリー葉または果実から調製した抽出エキスのがん細胞増殖抑制作用を、ヒト急性前骨髄性白血病細胞(HL60)を用いて、実施例3(1)と同様にWST-8アッセイにて評価した。
【0059】
なお、ブルーベリー葉の抽出エキスは実施例2の方法で調製し、またブルーベリー果実の抽出エキスは、実施例1の方法と同様の方法で粉末化した試料を用いて実施例2の方法に従って調製した。
【0060】
測定は、まず、抽出エキスの終濃度を62.5μg/ml、125μg/ml、250μg/ml、または500μg/mlになるようにリン酸緩衝液〔PBS(-)〕で希釈し(被験試料)、1μlずつ96穴プレートに分注した。ここにヒト急性前骨髄性白血病細胞(HL60)の懸濁液(1×105cells/ml)を100μlずつ加えて混合し、37℃、5%CO2存在下、相対湿度100%で48時間培養した。次いでWST-8混合試薬(商品名:Tetra Color ONE、SEIKAGAKU CORPORATION社製)を10μl加えてさらに4時間培養後、650nmを対照波長として450nmの吸光度を測定した。なお、上記被験試料に代えて、抽出エキスを添加しないリン酸緩衝液のみを用いて、上記と同様にして生存HL60細胞数を、吸光度(波長450nm)として測定した。これをコントロールとして、それに対する百分率で、抽出エキスで処理したHL60細胞の生存率を求めた。
【0061】
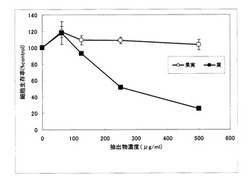
図4に示すように、ブルーベリー果実の抽出エキスに比べて、ブルーベリー葉の抽出エキスには、ヒト急性前骨髄性白血病細胞(HL60)に対して高い増殖抑制作用が認められた。
【0062】
(2)上記(1)と同様に、ブルーベリー葉または果実から調製した抽出エキスを終濃度4μg/ml、20μg/ml、100μg/ml、500μg/mlに調整し、がん細胞増殖抑制作用を、ヒト肝がん細胞(HLE)を用いて、WST-8アッセイにて評価した。結果を図5に示す。図5に示すように、ブルーベリー葉の抽出エキスには、ヒト肝がん細胞の増殖を抑制する非常に強い作用があるのに対し、ブルーベリーの果実の抽出エキスには、その作用はほとんど認められなかった。
【0063】
(3)上記(1)と同様に、ブルーベリー葉または果実から調製した抽出エキスのがん細胞増殖抑制作用をヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)、及びATL細胞(ED, Su9T01, S1T)を用いて、MTTアッセイにて評価した。結果を図6に示す。図6に示すように、ブルーベリーの果実の抽出エキスに比べて、ブルーベリー葉の抽出エキスには、上記7種類の細胞のいずれに対しても高い増殖抑制作用が認められた。
【0064】
実施例5 アポトーシス誘導効果
実施例2で製造したブルーベリー葉抽出エキス(ラビットアイブルーベリー種:ホームベル)によるATL細胞(Su9T01およびS1T細胞)増殖抑制および細胞致死効果を、トリパンブルー色素排除法により検討した。測定法は、2種類のATL細胞(Su9T01およびS1T細胞)懸濁液(1×105cells/ml)を1 mLずつ24穴プレートに分注し、37℃、5%CO2存在下、相対湿度100%で抽出エキスの終濃度を0μg/ml、12.5μg/ml、25μg/ml、50μg/ml、100μg/ml、または200μg/mlになるようにして、24および48時間培養した。サンプルの溶媒として用いたDMSOが終濃度0.1%となるよう培養した。
【0065】
表4及び図7に各種濃度のブルーベリー葉抽出エキスを用いてS1T細胞を培養した後(24または48時間)の生細胞の数(cells/ml)と生存率(%)を示す。
【0066】
【表4】

【0067】
また、表5及び図8に各種濃度のブルーベリー葉抽出エキスを用いてSu9T01細胞を培養した後(24または48時間)の生細胞の数(cells/ml)と生存率(%)を示す。
【0068】
【表5】

【0069】
アポトーシスの評価として、Annexin V染色法を用いた。細胞Su9T01細胞を用い、37℃、5%CO2存在下、相対湿度100%でブルーベリー葉抽出エキスの終濃度が0μg/ml(未処理)または50μg/mlになるように24時間培養した。培養終了後、細胞はPBSで洗浄後、Annexin V-FITC染色キット(Immunotech, PN IM 3546) を用いてアポトーシス細胞の染色を行い、フローサイトメーターにより測定を行った。結果を図9に示す。図9中、B4画分に示す細胞集団がアポトーシス陽性細胞(Annexin V陽性かつPropidium iodide陰性)の集団である。図9によると、0μg/ml(未処理)および50μg/mlブルーベリー葉抽出エキスを添加してSu9T01細胞を24時間培養した後のアポトーシス陽性細胞の割合はそれぞれ5.1%および34.33%であった。このことから、ブルーベリー葉は、ATL細胞にアポトーシスを介した細胞死を誘導していることがわかる。
【産業上の利用可能性】
【0070】
本発明のがん細胞またはがん発症性ウイルス感染細胞に対する増殖抑制用組成物は、工業的にはあまり利用されていないブルーベリー葉から得られる粉砕物、搾汁、または抽出物を有効成分とし、従来から治療が難しいとされている肝がんや白血病(中でも治療が難しい成人T細胞白血病)の改善及び予防に有効に利用することができるものである。とくに、本発明の組成物は、天然の食用植物に由来する成分を有効成分とするものであるため、医薬品や長期にわたって服用される飲食物としても安全に用いることができる。
【図面の簡単な説明】
【0071】
【図1】ブルーベリー葉抽出エキスのヒト急性前骨髄性白血病細胞(HL60)の増殖抑制効果を示すグラフである。
【図2】ブルーベリー葉抽出エキスのヒト肝がん細胞(Huh7、HLE、HLF)増殖抑制効果を示すグラフである。
【図3】ブルーベリー葉抽出エキスのヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)及びATL細胞(ED, Su9T01, S1T)増殖抑制効果を示すグラフである。
【図4】ブルーベリー葉抽出エキス及びブルーベリー果実抽出エキスの、ヒト急性前骨髄性白血病細胞(HL60)に対する細胞増殖抑制効果を対比したグラフである。
【図5】ブルーベリー葉抽出エキス及びブルーベリー果実抽出エキスの、ヒト肝がん細胞(HLE)増殖抑制効果を対比したグラフである。
【図6】ブルーベリー葉抽出エキス及びブルーベリー果実抽出エキスの、ヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)、及びATL細胞(ED, Su9T01, S1T)に対する細胞増殖抑制効果を対比したグラフである。
【図7】各種濃度のブルーベリー葉抽出エキスを用いてS1T細胞を培養した後(24または48時間)の生細胞の数(cells/ml)と生存率(%)を示す図である。
【図8】各種濃度のブルーベリー葉抽出エキスを用いてSu9T01細胞を培養した後(24または48時間)の生細胞の数(cells/ml)と生存率(%)を示す図である。
【図9】細胞Su9T01細胞を用いてフローサイトメーターにより、ブルーベリー葉抽出エキスのアポトーシス誘導作用を調べた結果を示す図である。
【技術分野】
【0001】
本発明は、がん細胞またはがん発症性ウイルス感染細胞の増殖を抑制するための材料(剤)、より詳細には天然の植物成分を有効成分とするがん細胞またはがん発症性ウイルス感染細胞の増殖抑制剤に関する。
【背景技術】
【0002】
日本人の死亡原因の第一位はがんであり、がん予防とがん治療は国民の健康上極めて重要な課題である。特に九州は、がんの中でも、成人T細胞白血病(Adult T-cell leukemia: ATL)を始めとする白血病、及び肝がんの発生率が高いとされている地域である。その理由の一つとして、九州にはヒトレトロウイルスHTLV-1(ヒトT細胞白血病ウイルス1型)に感染している人(HTLV-1キャリア)が多いことが挙げられる。ATLの発生にはHTLV-1が強く関係しており、HTLV-1感染者だけにATLが発生することが知られている。近年白血病の治療は非常に進歩しており、完治する白血病もある中で、ATLは最も治療に抵抗性の白血病である。加えて、他のウイルスと異なって、一旦HTLV-1に感染すると、一生涯身体の中にそのウイルスが存在し続ける。また、肝がんもC型肝炎ウイルス(Hepatitis C Virus:HCV)による持続感染が原因となって発症することが知られている。
【0003】
従って、がん細胞の増殖を抑制するというだけでなく、がんを発症する可能性のあるウイルス感染細胞の増殖を抑制することによってがんの発症を抑制することも必要である。
【0004】
非特許文献1には、疫学調査の結果として、緑黄色野菜や果物を多く摂取すると発がんのリスクが軽減されることが示されている。また、非特許文献2には、ブルーベリーを含むVaccinium属に属する植物の果実及び葉の酢酸エチル抽出物が、がんのプロモーター抑制の一つの指標であるキノンレダクターゼ誘導活性を有すること、また、非特許文献3では、Vaccinium属のビルベリー組織から誘導したカルスにより生産されたフラボノイド等を含む培養液が、乳がん細胞の増殖を抑制することが報告されている。
【0005】
しかしながら、上記したブルーベリー葉の酢酸エチル抽出物の抗がん機能(非特許文献2)は、キノンレダクターゼを誘導させることによって活性酸素の生成を妨害して発がんを抑制するというものであり、活性酸素の生成以外を要因として生じるがんに対しては有効とはいえない。また、がんの原因を除去することによって発がんを防止するものであるため、既にがん化した細胞に対しては有効とはいえない。
【0006】
また、がん全般に効く薬剤はなく、がんの種類によって治療薬物が異なることが当業界では周知となっている。例えば、非特許文献4によると、白血病は、化学療法(抗がん剤)で完治する可能性のあるがん、乳がんは病気の進行を遅らせることができるがん、そして肝がんは効果が期待できずがんも小さくなりもしないがんと、分類されている。従って、乳がん細胞の増殖抑制作用を有するものが(非特許文献3)、直ちに他のがん細胞に有効に使用できることにはならない。
【非特許文献1】M.M.Mathews-Roth,Pure Apll.Chem.,63, 147-156(2004)
【非特許文献2】J.Bomser, D.L.Madhavi, K.Singletary and M.A.L.Smith:Planta Medica.,62,212-216(1996)
【非特許文献3】浜松潮香「ブルーベリーの機能性研究;ブルーベリーの培養細胞による有用物質生産」,食品工業,43(2),44(2000)
【非特許文献4】国立がんセンターホームページ「がんに関する情報」の中の「治療−がんの薬物療法」http://www.ncc.go.jp/jp/ncc-cis/pub/treatment/010708.html
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明は、天然の植物成分に由来する、がん細胞(肝がん細胞、白血病細胞)またはがん発症性ウイルス感染細胞(HTLV-1感染細胞)の増殖を抑制するための材料(剤)を提供することを目的とする。さらに本発明は、かかる材料を有効成分とする医薬組成物および食品組成物を提供することを目的とする。特に、がん細胞またはがん発症性ウイルス感染細胞の増殖を特異的に抑制することのできる医薬組成物および食品組成物を提供することを目的とする。
【課題を解決するための手段】
【0008】
本発明者らは、上記目的を達成すべく鋭意研究を重ねていたところ、ブルーベリーの葉の溶媒抽出物に、特異的に肝がん細胞及び白血病細胞の増殖を抑制する作用があること、及び成人T細胞白血病(ATL)等の原因となるHTLV-1感染細胞の増殖を抑制する作用があることを見いだし、当該抽出物が上記作用に基づいて、肝がんや白血病に対する抗がん剤、また成人T細胞白血病(ATL)や肝がんの発症予防剤などの医薬組成物として有効であることを確信した。
【0009】
本発明はかかる知見に基づいて完成したものであり、下記の態様を有するものである:
項1.ブルーベリー葉の加工処理物を有効成分とする、肝がん細胞、白血病細胞、及びHTLV-1感染細胞よりなる群から選択される少なくとも1つの細胞に対する細胞増殖抑制剤。
項2.ブルーベリー葉の加工処理物が、葉の粉砕物、葉の搾汁、及び葉の抽出物よりなる群から選択される少なくとも1つである、項1記載の細胞増殖抑制剤。
項3.葉の抽出物が、ブルーベリー葉を水及びアルコールの少なくとも1つの溶媒で抽出して得られる抽出物である項2記載の細胞増殖抑制剤。
項4.白血病細胞が、ヒト急性前骨髄性白血病細胞、ヒトT細胞性白血病細胞、および成人T細胞白血病細胞よりなる群から選択される少なくとも1つである項1乃至3のいずれか1項に記載の細胞増殖抑制剤。
項5.項1乃至4のいずれかに1項に記載する細胞増殖抑制剤を含む医薬組成物。
項6.抗がん剤である、項5に記載する医薬組成物。
項7.肝がんまたは白血病に対する抗がん剤である、項6に記載する医薬組成物。
項8.成人T細胞白血病の発症予防剤である、項5に記載する医薬組成物。
項9.項1乃至4のいずれかに1項に記載する細胞増殖抑制剤を含む食品組成物。
項10.肝がん細胞、白血病細胞、及びHTLV-1感染細胞よりなる群から選択される少なくとも1つの細胞に対して細胞増殖抑制作用を有することを特徴とし、肝がんまたは白血病の予防または改善のために用いられる旨の表示を付した項9に記載する食品組成物。
【0010】
以下、本発明を詳説する。
【0011】
ブルーベリーは、ツツジ科(Ericaceae)スノキ属(Vaccinium)サイアノココス節(Cyanococcus)に分類される、アメリカ原産の落葉性あるいは常緑性の、低木性(または半高木性)の果樹である(Vander Kloet, 1988:玉田、1996)。ブルーベリーはおよそ6種類からなるが、果樹園芸上重要な種は、(1)ハイブッシュブルーベリー(Highbush blueberry, Vaccininum corymbosum.L)、(2)ラビットアイブルーベリー(Rabbiteye blueberry, V.ashei Reade)、(3)ローブッシュブルーベリー(Lowbush blueberry, V.angstifolium MichauxとV.myrtilloides Aition)の3つである。ブルーベリーは20世紀の初頭からアメリカ農務省あるいは州立大学によって野生種から改良された種類である。品種改良の方向は栽培が容易であり、果実が大きくて甘いなど良品種の生果生産を目標として進められ、今日では世界各国でつくられている。
【0012】
なお、本発明は、使用するブルーベリーについて、その種類やその由来・原産地を特に制限するものではなく、いずれも使用することができる。
【0013】
本発明はブルーベリーの葉を用いることを特徴とする。後述する実施例4の試験結果を示す図4、図5、図6から明らかなように、各種機能性が公知となっているブルーベリー果実に比較し、ブルーベリー葉は、9種類のがん細胞において、高いがん細胞増殖抑制作用をもっている。このことから、ブルーベリーの葉の癌細胞増殖抑制作用は、ブルーベリーの果実とは異なる成分あるいは機序によるものと推定でき、未利用資源としての域を脱しないブルーベリー葉の有効活用の可能性を大いに期待させるものである。
【0014】
ここで、ブルーベリー葉はそのままでも使用できるが、好ましくは加工処理を施したもの(加工処理物)が用いられる。加工処理物としては、ブルーベリーの葉の粉砕物(生、乾燥物)、ブルーベリー葉を搾って得られる搾汁またはブルーベリー葉を任意の溶媒で抽出して得られる抽出物を例示することができる。ブルーベリーの葉の加工処理物として、好ましくは抽出物である。
【0015】
乾燥粉砕物は、ブルーベリーの葉を例えばそのまま乾燥した後粉砕するか、又は生葉を細く切断した後乾燥することによって調製することができる。その乾燥には、本発明の薬効効果を損なわない方法であれば特に制限されず、真空凍結乾燥、熱風乾燥、遠赤外線乾燥、減圧乾燥、マイクロ波減圧乾燥及び過熱蒸気乾燥等を広く用いることができる。好ましくは成分変化の少ない真空凍結乾燥である。
【0016】
ブルーベリー葉の抽出物は、例えば葉をそのまま若しくは破砕物とした後抽出操作に供するか、また乾燥後、必要に応じて粉砕して抽出操作に供することによって調製することができる。また、葉を搾って得られる搾汁も抽出材料として使用することができ、これらは必要に応じて濃縮または乾燥して抽出操作に供することができる。
【0017】
ブルーベリー葉の抽出に用いる溶媒としては、特に制限されず、水、極性有機溶媒または非極性有機溶媒のいずれであってもよい。好ましくは水または水と相溶性のある極性溶媒を挙げることができる。水と相溶性のある極性溶媒としては、メタノール、エタノール、プロパノール及びブタノール等の炭素数1〜4の低級アルコール;エチレングリコール、ブチレングリコール、プロピレングリコール、グリセリンなどのグリコール類;エチルエーテル、アセトン、アセトニトリルを挙げることができる。かかる極性溶媒として、好ましくは低級アルコールであり、特に好ましくはエタノールである。
【0018】
これらの溶媒は、単独で用いてもよく、二種以上を組み合わせて使用することもできる。例えば、アセトンとエチルエーテルの混合溶媒(好ましくはアセトン:エチルエーテル=1:1(v/v)混合液)、上記極性有機溶媒と水との混合溶媒(含水溶媒)を挙げることができる。含水溶媒として好ましくは、低級アルコールと水との混合物(含水アルコール)、より好ましくはエタノールと水との混合物(含水エタノール)を例示することができる。含水アルコール中のアルコール濃度も特に制限されないが、例えば5〜90容量%、好ましくは30〜90容量%、より好ましくは50〜90容量%を挙げることができる。
【0019】
抽出方法としては、一般に用いられている方法をいずれも採用することができる。例えば、溶媒中にブルーベリー葉(そのまま若しくは粗末、細切物)、又はそれらの乾燥粉砕物(粉末など)を浸漬する方法;撹拌しながら抽出を行い、ろ過して抽出液を得る方法;またはパーコレーション法等を挙げることができる。なお、特に制限はされないが、例えば、抽出溶媒として80容量%の割合でエタノールを含む含水エタノールを用いる場合は、安定して抽出できる方法として室温下攪拌抽出を行うことが好ましい。
【0020】
得られた抽出物は、必要に応じて、ろ過または遠心分離などの操作により固形物を除去することも好ましい方法の一つである。次への工程で行われる操作に応じて、そのまま用いるか、または溶媒を留去して一部濃縮若しくは乾燥して用いてもよい。また濃縮あるいは乾燥後、さらに適正な洗浄溶媒、例えば、非溶解性溶媒で洗浄精製して用いても、またこれを更に適当な溶剤に溶解若しくは懸濁して用いることもできる。更に、本発明においては、例えば、上記のようにして得られた溶媒抽出液を、減圧乾燥、凍結乾燥等の通常の手段によりブルーベリー葉乾燥抽出エキスとして使用することもできる。
【0021】
斯くして得られるブルーベリー葉の粉砕物、搾汁液若しくは抽出物は、後述の実施例に記載するように、肝がん細胞、及び白血病細胞の増殖を抑制する作用を有している。ここで白血病細胞としては全てヒトの白血病細胞で、急性前骨髄性白血病細胞、急性リンパ性 (T細胞性) 白血病細胞、成人T細胞白血病細胞を挙げることができる。このため、本発明の細胞増殖抑制剤は、肝がんや白血病(例えば、急性前骨髄性白血病、T細胞性白血病、成人T細胞白血病)に対する抗がん剤(医薬組成物)の有効成分として、有効に用いることができる。また、本発明の細胞増殖抑制剤は、肝がん細胞、及び白血病細胞の増殖を抑制する作用を有する食品組成物(例えば、栄養補助食品、機能性食品、特定保健用食品など)の有効成分として有効に用いることができる。
【0022】
さらに、ブルーベリー葉の粉砕物、搾汁若しくは抽出物は、成人T細胞白血病発症性のウイルス感染細胞である、ヒトレトロウイルスHTLV-1感染細胞(HTLV-1感染細胞)の増殖を抑制する作用を有している。このため、本発明の細胞増殖抑制剤は、成人T細胞白血病の発症を阻止し予防するための組成物(医薬組成物や食品組成物)の有効成分として、有効に利用することができる。
【0023】
なお、HTLV-1感染細胞が関与する病気として、HAM(HTLV-1関連脊髄症)、HAU(HTLV-1関連ぶどう膜炎)、HAB (HTLV-1関連気管支・肺障害)が知られている。このため本発明の細胞増殖抑制剤は、HTLV-1感染細胞の増殖を抑制することによって、これらの病気(HTLV-1関連脊髄症、HTLV-1関連ぶどう膜炎、HTLV-1関連気管支・肺障害)の発症を阻止し予防するための組成物(医薬組成物や食品組成物)の有効成分として、有効に利用することができる。
【0024】
なお、本発明でいう細胞増殖抑制作用とは、細胞全体としての数(総細胞数)が減少する作用が認められればよく、細胞の発育・成長を阻止する作用や細胞を死滅させる作用などの作用機序の別を問わない。
【0025】
本発明の細胞増殖抑制剤は、上記ブルーベリー葉の粉砕物、搾汁若しくは抽出物そのものを単独で固体又は液体状で利用することもできるが、それに加えて薬学的若しくは食品上許容される担体または添加剤を配合して、固体又は液体状の医薬組成物または食品組成物として調製することができる。
【0026】
ゆえに本発明は、前述する細胞増殖抑制剤を有効成分とする医薬組成物または食品組成物を提供するものでもある。
【0027】
かかる本発明の医薬組成物または食品組成物は、上記本発明の細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)の作用(肝がん細胞増殖抑制作用、白血病細胞増殖抑制作用、HTLV-1感染細胞増殖抑制作用)に基づいて、肝がんに対する改善作用、白血病に対する予防若しくは改善作用、成人T細胞白血病(ATL)発症予防作用、またはHTLV-1感染細胞が関与する疾患(例えばHTLV-1関連脊髄症、HTLV-1関連ぶどう膜炎、HTLV-1関連気管支・肺障害)の発症予防作用を有している。
【0028】
本発明の医薬組成物は、その形態として特に制限されないが、経口に適した形態であることが好ましい。例えば、経口投与用固体組成物(固形医薬製剤)としては錠剤(糖衣錠を含む)、丸剤、カプセル剤、細粒剤、顆粒剤等の形態を、また経口投与用液状組成物(液状医薬製剤)としては乳濁剤、溶液剤、懸濁剤、シロップ剤などの形態を例示することができる。これらの製剤は、有効成分である細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)に加えて、各種製剤に応じて賦形剤、結合剤、崩壊剤、滑沢剤、着色料、矯味矯臭剤、pH調整剤等を適宜配合し、常法に従って調製することができる。
【0029】
なお、本発明の医薬組成物には、上記細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁液若しくは抽出物)に加えて、がん細胞増殖抑制作用(肝がん細胞増殖抑制作用、または白血病細胞増殖抑制作用)を有する他の成分が含まれていても良い。
【0030】
本発明の医薬組成物の投与量は、特に限定されず、所望の治療効果、投与法、治療期間、被験者の年齢、性別その他の条件などに応じて広範囲より適宜選択される。投与経路によっても異なるが、例えば体重60kgのヒトに対する投与量は、1回投与あたりの上記細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)の量(ブルーベリー葉の乾燥重量に換算して)として、約600〜6000 mg/(60kg体重)の範囲から適宜選択することができる。
【0031】
本発明が提供する医薬組成物に含まれる細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)の量は、その製剤形態や適用疾患の種類などによって種々異なり、一概に規定することはできないが、上記投与量(1投与あたり)に応じて適宜設定することができる。
【0032】
本発明の食品組成物も、その形態は特に制限されない。例えば、前述する細胞増殖抑制剤を、必要に応じて食品上配合が許容される担体や添加剤とともに、錠剤、丸剤、カプセル剤、顆粒剤、散剤、粉末剤、トローチ剤、または溶液(ドリンク)等の形態に調製してなるサプリメント(機能性食品)の形態を有するものであってもよい。
【0033】
本発明の食品組成物は、上記細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)を含有することによって、その肝がん細胞増殖抑制作用、白血病細胞増殖抑制作用、またはHTLV-1感染細胞増殖抑制作用を有している。このため、本発明が対象とする食品組成物には各種の効果を効能とする食品(例えば特定保健用食品、栄養補助食品、機能性食品等)も含まれる。
【0034】
特定保健用食品(条件付き特定保健用食品も含まれる)の中には、上記有効成分(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)を含有することにより、肝がんに対する改善作用、白血病に対する予防若しくは改善作用、成人T細胞白血病(ATL)発症予防作用、またはHTLV-1感染細胞が関与する疾患(HTLV-1関連脊髄症、HTLV-1関連ぶどう膜炎、HTLV-1関連気管支・肺障害等)の発症予防作用を有し、このため肝がん改善作用、白血病予防若しくは改善作用、成人T細胞白血病(ATL)発症予防、またはHTLV-1感染細胞が関与する疾患(HTLV-1関連脊髄症、HTLV-1関連ぶどう膜炎、HTLV-1関連気管支・肺障害等)の発症予防作用のために用いられる旨が包装パッケージに記載されてなる食品が含まれる。
【0035】
本発明が対象とする食品組成物としては、例えば乳飲料、乳酸菌飲料、果汁入り清涼飲料、清涼飲料、炭酸飲料、果汁飲料、野菜飲料、野菜・果実飲料、アルコール飲料、粉末飲料、コーヒー飲料、紅茶飲料、緑茶飲料、麦茶飲料などの飲料類;カスタードプリン、ミルクプリン、スフレプリン、果汁入りプリン等のプリン類、ゼリー、ババロア及びヨーグルト等のデザート類;アイスクリーム、アイスミルク、ラクトアイス、ミルクアイスクリーム、果汁入りアイスクリーム及びソフトクリーム、アイスキャンディー、シャーベット、氷菓等の冷菓類;チューインガムや風船ガム等のガム類(板ガム、糖衣状粒ガム);マーブルチョコレート等のコーティングチョコレートの他、イチゴチョコレート、ブルーベリーチョコレート及びメロンチョコレート等の風味を付加したチョコレート等のチョコレート類;ハードキャンディー(ボンボン、バターボール、マーブル等を含む)、ソフトキャンディー(キャラメル、ヌガー、グミキャンディー、マシュマロ等を含む)、ドロップ、タフィ等のキャラメル類;ハードビスケット、クッキー、おかき、煎餅等の焼き菓子類(以上、菓子類);コンソメスープ、ポタージュスープ等のスープ類;味噌、醤油、ドレッシング、ケチャップ、たれ、ソース、ふりかけなどの各種調味料;ストロベリージャム、ブルーベリージャム、マーマレード、リンゴジャム、杏ジャム、プレザーブ等のジャム類;赤ワイン等の果実酒;シロップ漬のチェリー、アンズ、リンゴ、イチゴ、桃等の加工用果実;ハム、ソーセージ、焼き豚等の畜肉加工品;魚肉ハム、魚肉ソーセージ、魚肉すり身、蒲鉾、竹輪、はんぺん、薩摩揚げ、伊達巻き、鯨ベーコン等の水産練り製品;うどん、冷麦、そうめん、ソバ、中華そば、スパゲッティ、マカロニ、ビーフン、はるさめ及びワンタン等の麺類;その他、各種総菜及び麩、田麩等の種々の加工食品を挙げることができる。好ましくは飲料、麺類、菓子類である。
【0036】
上記食品組成物に含まれる上記細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)の量、または摂取量は、特に限定されず、食品組成物の種類、目的とする機能・効能、並びにその他の諸条件などに応じて広範囲より適宜選択される。摂取量は、食品組成物の種類によっても異なるが、体重60kgのヒトに対して1回摂取あたりの細胞増殖抑制剤(ブルーベリー葉の粉砕物、搾汁若しくは抽出物)の量(ブルーベリー葉の乾燥重量に換算して)として、約600〜6000 mg/(60kg体重)の範囲から適宜選択するのが望ましい。
【発明の効果】
【0037】
本発明の細胞増殖抑制剤は、天然植物であるブルーベリー葉の加工処理物(例えば、ブルーベリー葉の粉砕物、搾汁又は抽出物)を有効成分とするものであって、肝がん細胞、及び白血病細胞に対して増殖抑制作用を有する。このため、本発明の細胞増殖抑制剤およびこれを有効成分とする組成物(医薬組成物、食品組成物)は、既にがん化した細胞に対しても作用しその増殖を抑制することによって、肝がんの改善または治療、及び白血病の改善または治療に有効に用いることができる。
【0038】
さらに本発明の細胞増殖抑制剤は、HTLV-1感染細胞に対しても増殖抑制作用を有する。このため、本発明の細胞増殖抑制剤及びこれを有効成分とする組成物(医薬組成物、食品組成物)は、HTLV-1感染によるがんの発症、とくに成人T細胞白血病の発症を阻止し予防するために有効に用いることができる。また、本発明の細胞増殖抑制剤及びこれを有効成分とする組成物(医薬組成物、食品組成物)は、HTLV-1感染細胞が関与する疾患(HTLV-1関連脊髄症、HTLV-1関連ぶどう膜炎、HTLV-1関連気管支・肺障害など)の発症を阻止し予防するために有効に用いることができる。
【0039】
また、本発明の細胞増殖抑制剤の有効成分(ブルーベリー葉の粉砕物、搾汁又は抽出物)は天然の食用植物に由来するものである。従って、本発明の細胞増殖抑制剤およびこれを含む組成物(医薬組成物、食品組成物)は、副作用が少なく長期にわたって服用または摂取することが可能である。
【発明を実施するための最良の形態】
【0040】
以下に、本発明を実施するための最良の形態として実施例を挙げて、本発明の内容をより詳細を説明する。但し、本発明は実施例だけに限定されるものではない。なお、特に言及しない限り、下記の実施例において「%」は「w/w%」を意味するものとする。
【0041】
実施例1 ブルーベリー葉の乾燥粉末物の調製
ブルーベリー〔ハイブッシュブルーベリー種(10品種):オニール、シャープブルー、ジョージア、フローダブルー、レベレイ、スパルタン、ダロウ、デューク、バークレイ、ハリソン、ラビットアイブルーベリー種(5品種):ウッダード、ガーデンブルー、ティフブルー、ホームベル、マイヤー〕の葉を品種ごとに、凍結温度-30℃、乾燥温度30℃、乾燥時間24時間で真空凍結乾燥(真空凍結乾燥機、FTS SYSTEM、Dura-Top MP&Dura-Dry MP)し、超遠心粉砕機(MRK&RETSCH、EM-1型)で0.5mmのスクリーンを通して粉砕して、ブルーベリー葉の乾燥粉末物を調製した。
【0042】
実施例2 ブルーベリー葉の抽出エキスの調製
実施例1で調製したブルーベリー〔ハイブッシュブルーベリー種(10品種):オニール、シャープブルー、ジョージア、フローダブルー、レベレイ、スパルタン、ダロウ、デューク、バークレイ、ハリソン、ラビットアイブルーベリー種(5品種):ウッダード、ガーデンブルー、ティフブルー、ホームベル、マイヤー〕の葉の乾燥粉末物に、それぞれ80容量%の割合でエタノールを含む含水エタノールを加え室温で30秒間激しく撹拌した後、ろ過した。ろ液を減圧濃縮して溶媒を留去し、さらに真空凍結乾燥処理し完全に溶媒を留去して、ブルーベリー葉の乾燥抽出エキスを調製した。
【0043】
実施例3 がん細胞増殖抑制試験
実施例2で調製したブルーベリー葉の乾燥抽出エキスのうち、ラビットアイブルーベリー種に属するホームベルの抽出エキスを用いて、各種のがん細胞の増殖抑制作用を調べた。
【0044】
(1)ヒト急性前骨髄性白血病細胞(HL60)に対する増殖抑制作用
ブルーベリー葉の抽出エキスのヒト急性前骨髄性白血病細胞(HL60)に対する増殖抑制作用を、WST-8アッセイを用いて評価した。なお、WST-8アッセイは生細胞の数を測定する方法である。すなわち、WST-8アッセイで用いるWST-8 〔2-(2-Methoxy-4-nitrophenyl)-3-(4-nitrophenyl)-5-(2,4-disulfophenyl)-2H-tetrazolium, monosodium salt〕は、細胞共存下、細胞内脱水素酵素により還元され、水溶性のホルマザンを生成するが、この生成されたホルマザン量が生細胞の数と比例することから、ホルマザンの吸光度(測定波長450nm/対照波長650nm)を直接測定することにより、生細胞数の測定ができるというものである。
【0045】
測定は、まず、抽出エキスの終濃度を62.5μg/ml、125μg/ml、250μg/ml、または500μg/mlになるようにリン酸緩衝液〔PBS(-)〕で希釈し(被験試料)、1μlずつ96穴プレートに分注した。ここにヒト急性前骨髄性白血病細胞(HL60)の懸濁液(1×105cells/ml)を100μlずつ加えて混合し、37℃、5%CO2存在下、相対湿度100%で48時間培養した。次いでWST-8混合試薬(商品名:Tetra Color ONE、SEIKAGAKU CORPORATION社製)を10μl加えてさらに4時間培養後、650nmを対照波長として450nmの吸光度を測定した。なお、上記被験試料に代えて、抽出エキスを添加しないリン酸緩衝液のみを用いて、上記と同様にして生存HL60細胞数を、吸光度(波長450nm)として測定した。これをコントロールとして、それに対する百分率で、抽出エキスで処理したHL60細胞の生存率を求めた。結果を表1及び図1に示す。
【0046】
【表1】

【0047】
表1及び図1からわかるように、ブルーベリー葉の抽出エキスには、ヒト急性前骨髄性白血病細胞(HL-60細胞)の増殖を抑制する非常に強い作用があることがわかる。
【0048】
(2)肝がん細胞(Huh-7、HLE、HLF)に対する増殖抑制作用
ブルーベリー葉の抽出エキスの各種ヒト肝がん細胞(Huh-7、HLE、HLF)に対する増殖抑制作用を、上記と同様に、WST-8アッセイを用いて評価した。具体的には、3種類の肝がん細胞(Huh-7、HLE、HLF)の懸濁液(1×104cells/ml)をそれぞれ100μlずつ96穴プレートに分注し、37℃、5%CO2存在下、相対湿度100%で24時間培養し細胞の接着を確認した。次いで、各ウェルに予め、終濃度が62.5μg/ml、125μg/ml、250μg/ml及び500μg/mlになるようにリン酸緩衝液(PBS(-))で濃度を調整しておいた抽出エキスを1μlずつ添加して(被験試料)、37℃、5%CO2存在下、相対湿度100%で72時間培養した。これにWST-8混合試薬(商品名:Tetra Color ONE、SEIKAGAKU CORPORATION社製)を10μl加えてさらに4時間培養後、650nmを対照波長として450nmの吸光度を測定した。
【0049】
なお、上記被験試料に代えて、抽出エキスを添加しないリン酸緩衝液のみを用いて、上記と同様にして生存細胞数を吸光度(波長450nm)として測定した。この場合のこれをコントロール(100%)として、それに対する百分率で、抽出エキスで処理した各種肝がん細胞(HuH-7, HLE, HLF)の生存率を求めた。結果を表2及び図2に示す。
【0050】
【表2】

【0051】
表2及び図2の結果から、ブルーベリー葉の抽出エキスには、肝がん細胞の増殖を抑制する非常に強い作用があることがわかる。
【0052】
(3)ヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)、及び成人T細胞白血病細胞(ATL細胞)(ED, Su9T01, S1T)に対する増殖抑制作用
ブルーベリー葉の抽出エキスの、ヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102,MT2)、及びATL細胞(ED,Su9T01,S1T)に対する増殖抑制作用を、MTTアッセイを用いて評価した。なお、HTLV-1(Human T cell leukemia virus type 1)は、ヒトで初めて発見されたレトロウイルスのことで、成人T細胞白血病(ATL:Adult T cell leukemia)などを引き起こすとされている。なお、MTTアッセイは、WST-8アッセイ同様、生細胞の数を測定する方法である。すなわち、MTTアッセイで用いるMTT〔3-(4,5-Dimethyl-2-thiazolyl)-2,5-diphenyl-2H tetrazolium bromide〕は黄色の化合物で、生細胞のミトコンドリアの呼吸鎖に作用し、存在する酵素によってテトラゾリウム環が開裂し、青色のホルマザンを生成する。この生成されたホルマザン量が生細胞の数と比例することから、ホルマザンの吸光度を直接測定することにより、生細胞数の測定ができるというものである。
【0053】
測定は、まず、ヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)、ATL細胞(ED, Su9T01, S1T)(合計7種類のがん細胞)の懸濁液(1×105cells/ml)をそれぞれ99μlずつ96穴プレートに分注した。これに、予め終濃度が3.91μg/ml、7.81μg/ml、15.6μg/ml、31.3μg/ml、62.5μg/ml、125μg/ml、250μg/ml及び500μg/mlになるようにリン酸緩衝液(PBS(-))で調整した抽出エキスを1μlずつ添加して(被験試料)、37℃、5%CO2存在下、相対湿度100%で48時間培養した。次いで、MTT試薬(商品名MTT lyophilized、同仁化学研究所製)を10μl加えてさらに4時間培養した後、100μlずつ溶解液(0.04M/HCl/イソプロピルアルコール)を加えよくピペッティングし、色素を溶解した。その後650nmを対照波長とし570nmの吸光度を測定した。
【0054】
なお、上記被験試料に代えて、抽出エキスを添加しないリン酸緩衝液のみを用いて、上記と同様にして生存細胞数を吸光度(波長570nm)として測定した。これをコントロール(100%)として、それに対する百分率で、抽出エキスで処理した各種がん細胞の生存率を求めた。
【0055】
7種類のがん細胞(Jurkat, MOLT4,HUT102, MT2,ED, Su9T01, S1T)に各種濃度のブルーベリー葉の抽出エキスを添加して48時間培養した後の生存率(%)を、表3及び図3に示す。
【0056】
【表3】

【0057】
これらの結果から、ブルーベリー葉の抽出エキスには、ヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)及び成人T細胞白血病細胞(ED, Su9T01, S1T)の増殖を抑制する強い作用があることがわかった。
【0058】
実施例4 ブルーベリーの葉または果実のがん細胞増殖抑制試験
(1)実施例3の方法に従って、ブルーベリー葉または果実から調製した抽出エキスのがん細胞増殖抑制作用を、ヒト急性前骨髄性白血病細胞(HL60)を用いて、実施例3(1)と同様にWST-8アッセイにて評価した。
【0059】
なお、ブルーベリー葉の抽出エキスは実施例2の方法で調製し、またブルーベリー果実の抽出エキスは、実施例1の方法と同様の方法で粉末化した試料を用いて実施例2の方法に従って調製した。
【0060】
測定は、まず、抽出エキスの終濃度を62.5μg/ml、125μg/ml、250μg/ml、または500μg/mlになるようにリン酸緩衝液〔PBS(-)〕で希釈し(被験試料)、1μlずつ96穴プレートに分注した。ここにヒト急性前骨髄性白血病細胞(HL60)の懸濁液(1×105cells/ml)を100μlずつ加えて混合し、37℃、5%CO2存在下、相対湿度100%で48時間培養した。次いでWST-8混合試薬(商品名:Tetra Color ONE、SEIKAGAKU CORPORATION社製)を10μl加えてさらに4時間培養後、650nmを対照波長として450nmの吸光度を測定した。なお、上記被験試料に代えて、抽出エキスを添加しないリン酸緩衝液のみを用いて、上記と同様にして生存HL60細胞数を、吸光度(波長450nm)として測定した。これをコントロールとして、それに対する百分率で、抽出エキスで処理したHL60細胞の生存率を求めた。
【0061】
図4に示すように、ブルーベリー果実の抽出エキスに比べて、ブルーベリー葉の抽出エキスには、ヒト急性前骨髄性白血病細胞(HL60)に対して高い増殖抑制作用が認められた。
【0062】
(2)上記(1)と同様に、ブルーベリー葉または果実から調製した抽出エキスを終濃度4μg/ml、20μg/ml、100μg/ml、500μg/mlに調整し、がん細胞増殖抑制作用を、ヒト肝がん細胞(HLE)を用いて、WST-8アッセイにて評価した。結果を図5に示す。図5に示すように、ブルーベリー葉の抽出エキスには、ヒト肝がん細胞の増殖を抑制する非常に強い作用があるのに対し、ブルーベリーの果実の抽出エキスには、その作用はほとんど認められなかった。
【0063】
(3)上記(1)と同様に、ブルーベリー葉または果実から調製した抽出エキスのがん細胞増殖抑制作用をヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)、及びATL細胞(ED, Su9T01, S1T)を用いて、MTTアッセイにて評価した。結果を図6に示す。図6に示すように、ブルーベリーの果実の抽出エキスに比べて、ブルーベリー葉の抽出エキスには、上記7種類の細胞のいずれに対しても高い増殖抑制作用が認められた。
【0064】
実施例5 アポトーシス誘導効果
実施例2で製造したブルーベリー葉抽出エキス(ラビットアイブルーベリー種:ホームベル)によるATL細胞(Su9T01およびS1T細胞)増殖抑制および細胞致死効果を、トリパンブルー色素排除法により検討した。測定法は、2種類のATL細胞(Su9T01およびS1T細胞)懸濁液(1×105cells/ml)を1 mLずつ24穴プレートに分注し、37℃、5%CO2存在下、相対湿度100%で抽出エキスの終濃度を0μg/ml、12.5μg/ml、25μg/ml、50μg/ml、100μg/ml、または200μg/mlになるようにして、24および48時間培養した。サンプルの溶媒として用いたDMSOが終濃度0.1%となるよう培養した。
【0065】
表4及び図7に各種濃度のブルーベリー葉抽出エキスを用いてS1T細胞を培養した後(24または48時間)の生細胞の数(cells/ml)と生存率(%)を示す。
【0066】
【表4】

【0067】
また、表5及び図8に各種濃度のブルーベリー葉抽出エキスを用いてSu9T01細胞を培養した後(24または48時間)の生細胞の数(cells/ml)と生存率(%)を示す。
【0068】
【表5】

【0069】
アポトーシスの評価として、Annexin V染色法を用いた。細胞Su9T01細胞を用い、37℃、5%CO2存在下、相対湿度100%でブルーベリー葉抽出エキスの終濃度が0μg/ml(未処理)または50μg/mlになるように24時間培養した。培養終了後、細胞はPBSで洗浄後、Annexin V-FITC染色キット(Immunotech, PN IM 3546) を用いてアポトーシス細胞の染色を行い、フローサイトメーターにより測定を行った。結果を図9に示す。図9中、B4画分に示す細胞集団がアポトーシス陽性細胞(Annexin V陽性かつPropidium iodide陰性)の集団である。図9によると、0μg/ml(未処理)および50μg/mlブルーベリー葉抽出エキスを添加してSu9T01細胞を24時間培養した後のアポトーシス陽性細胞の割合はそれぞれ5.1%および34.33%であった。このことから、ブルーベリー葉は、ATL細胞にアポトーシスを介した細胞死を誘導していることがわかる。
【産業上の利用可能性】
【0070】
本発明のがん細胞またはがん発症性ウイルス感染細胞に対する増殖抑制用組成物は、工業的にはあまり利用されていないブルーベリー葉から得られる粉砕物、搾汁、または抽出物を有効成分とし、従来から治療が難しいとされている肝がんや白血病(中でも治療が難しい成人T細胞白血病)の改善及び予防に有効に利用することができるものである。とくに、本発明の組成物は、天然の食用植物に由来する成分を有効成分とするものであるため、医薬品や長期にわたって服用される飲食物としても安全に用いることができる。
【図面の簡単な説明】
【0071】
【図1】ブルーベリー葉抽出エキスのヒト急性前骨髄性白血病細胞(HL60)の増殖抑制効果を示すグラフである。
【図2】ブルーベリー葉抽出エキスのヒト肝がん細胞(Huh7、HLE、HLF)増殖抑制効果を示すグラフである。
【図3】ブルーベリー葉抽出エキスのヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)及びATL細胞(ED, Su9T01, S1T)増殖抑制効果を示すグラフである。
【図4】ブルーベリー葉抽出エキス及びブルーベリー果実抽出エキスの、ヒト急性前骨髄性白血病細胞(HL60)に対する細胞増殖抑制効果を対比したグラフである。
【図5】ブルーベリー葉抽出エキス及びブルーベリー果実抽出エキスの、ヒト肝がん細胞(HLE)増殖抑制効果を対比したグラフである。
【図6】ブルーベリー葉抽出エキス及びブルーベリー果実抽出エキスの、ヒトT細胞性白血病細胞(Jurkat, MOLT4)、HTLV-1感染細胞(HUT102, MT2)、及びATL細胞(ED, Su9T01, S1T)に対する細胞増殖抑制効果を対比したグラフである。
【図7】各種濃度のブルーベリー葉抽出エキスを用いてS1T細胞を培養した後(24または48時間)の生細胞の数(cells/ml)と生存率(%)を示す図である。
【図8】各種濃度のブルーベリー葉抽出エキスを用いてSu9T01細胞を培養した後(24または48時間)の生細胞の数(cells/ml)と生存率(%)を示す図である。
【図9】細胞Su9T01細胞を用いてフローサイトメーターにより、ブルーベリー葉抽出エキスのアポトーシス誘導作用を調べた結果を示す図である。
【特許請求の範囲】
【請求項1】
ブルーベリー葉の加工処理物を有効成分とする、肝がん細胞、白血病細胞、及びHTLV-1感染細胞よりなる群から選択される少なくとも1つの細胞に対する細胞増殖抑制剤。
【請求項2】
ブルーベリー葉の加工処理物が、葉の粉砕物、葉の搾汁、及び葉の抽出物よりなる群から選択される少なくとも1つである、請求項1記載の細胞増殖抑制剤。
【請求項3】
請求項1または2に記載する細胞増殖抑制剤を含む医薬組成物。
【請求項4】
抗がん剤である、請求項3記載の医薬組成物。
【請求項5】
成人T細胞白血病の発症予防剤である、請求項3に記載する医薬組成物。
【請求項6】
請求項1または2に記載する細胞増殖抑制剤を含む食品組成物。
【請求項1】
ブルーベリー葉の加工処理物を有効成分とする、肝がん細胞、白血病細胞、及びHTLV-1感染細胞よりなる群から選択される少なくとも1つの細胞に対する細胞増殖抑制剤。
【請求項2】
ブルーベリー葉の加工処理物が、葉の粉砕物、葉の搾汁、及び葉の抽出物よりなる群から選択される少なくとも1つである、請求項1記載の細胞増殖抑制剤。
【請求項3】
請求項1または2に記載する細胞増殖抑制剤を含む医薬組成物。
【請求項4】
抗がん剤である、請求項3記載の医薬組成物。
【請求項5】
成人T細胞白血病の発症予防剤である、請求項3に記載する医薬組成物。
【請求項6】
請求項1または2に記載する細胞増殖抑制剤を含む食品組成物。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2007−22929(P2007−22929A)
【公開日】平成19年2月1日(2007.2.1)
【国際特許分類】
【出願番号】特願2005−203584(P2005−203584)
【出願日】平成17年7月12日(2005.7.12)
【出願人】(392001933)雲海酒造株式会社 (11)
【出願人】(504224153)国立大学法人 宮崎大学 (239)
【出願人】(391011700)宮崎県 (63)
【出願人】(503360115)独立行政法人科学技術振興機構 (1,734)
【Fターム(参考)】
【公開日】平成19年2月1日(2007.2.1)
【国際特許分類】
【出願日】平成17年7月12日(2005.7.12)
【出願人】(392001933)雲海酒造株式会社 (11)
【出願人】(504224153)国立大学法人 宮崎大学 (239)
【出願人】(391011700)宮崎県 (63)
【出願人】(503360115)独立行政法人科学技術振興機構 (1,734)
【Fターム(参考)】
[ Back to top ]

