アニオン検出用蛍光センサー
【課題】各種生物系の実験系においても使用することができるような水溶液中におけるアニオンを定量的に測定することができるセンサー化合物を提供する。
【解決手段】環状ポリアミンの金属錯体から成るアニオンホスト及び蛍光色素を有する化合物であって、該金属錯体の金属イオンとの配位結合において、該蛍光色素上の置換基とアニオンとの間の配位子交換機能によって蛍光色素のスペクトルに変化が生じることを特徴とする。
【解決手段】環状ポリアミンの金属錯体から成るアニオンホスト及び蛍光色素を有する化合物であって、該金属錯体の金属イオンとの配位結合において、該蛍光色素上の置換基とアニオンとの間の配位子交換機能によって蛍光色素のスペクトルに変化が生じることを特徴とする。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、特に水溶液中のアニオンを検出することの出来るセンサー化合物、及び該化合物を使用する各種測定方法に関する。
【背景技術】
【0002】
蛍光センサーは、生体系における生体分子の役割を分析し、解明するのに有用であり、例えば、蛍光CaII指示薬を用いて、細胞内CaIIのいくつかの機能が解明されてきた1。さらにその他に多数の金属センサー及びpHセンサーが開発されている2。
【0003】
多数の有機アニオン及び無機アニオンが生きている生物において重要な役割を担っているために、今やアニオン認識3及びアニオンセンサー検出4に関心が高まっている。アニオンセンサーの開発によって分子内にアニオン基を持つ生体有機分子を検出することができる新規のセンサーの開発にも繋がる。しかしながら、従来知られているほとんどのセンサーは有機媒質の中でしか機能せず、それらを生化学的又は生理学的な実験に使用するのは困難である。
一般にアニオンは、金属イオンのような陽イオンよりも大型なので、陽イオンよりも溶媒化の制約を受け易い。有機溶媒では、溶媒化エネルギーが比較的小さく、静電気の相互作用が効果的に働くので、アニオンを捕捉し、検出するのはさほど難しくはない。しかしながら、生体応用に適している水性溶媒では、強い水和のためにアニオンを認識するのは極めて困難である。今のところ、有機環境では多数が知られているけれども、水溶液中で作動する蛍光アニオンセンサーはほとんど開発されていない。
【0004】
水溶液中で使用するための蛍光アニオンセンサーは、2つの必要条件を満たさなければならない。1つは、水中でのアニオンに対する十分に強い親和性であり、もう11つは、アニオンの認識を蛍光シグナルに変換する能力である。既知のアニオンセンサーはほとんど、後者の必要条件は満たすけれども、水中でのアニオンに対して十分な親和性を持っていない。アニオンホストの中には、水性溶媒中でアニオンを捕捉することができるものもあるが、それらは単にホスト分子であって、センサー分子ではない。双方の必要条件を同時に満たすのは困難である。
【0005】
Crazuik et alは、水溶液中で作動する蛍光アニオンセンサーの開発に成功した5。このようなセンサーの検出メカニズムは、蛍光団に隣接したアミノ基のpKaをアニオンが結合することによって変化させることに基づいている。しかしながら、このセンサーではある特定のpH領域でしか測定できず、pH変化に敏感である。従って、このセンサー検出のメカニズムを生物実験に応用するのは困難である。
【発明の開示】
【発明が解決しようとする課題】
【0006】
従って、本発明の目的は、各種生物系の実験系においても使用することができるような水溶液中におけるアニオンを定量的に測定することができるセンサー化合物を提供することである。
【課題を解決するための手段】
【0007】
本発明者は上記課題を解決すべく鋭意研究した結果、アニオンを検出するための新規の手段を開発し、本発明を完成した。
即ち、本発明は、環状ポリアミンの金属錯体から成るアニオンホスト及び蛍光色素を有する化合物であって、該金属錯体の金属イオンとの配位結合において、該蛍光色素上の置換基とアニオンとの間の配位子交換機能によって蛍光色素のスペクトルに変化が生じることを特徴とする、前記化合物に係る。
より、具体的には、本発明は環状ポリアミンの金属錯体から成るアニオンホスト及び蛍光色素を有する化合物であって、該金属錯体の金属イオンとの配位結合に関与する該蛍光色素上の電子供与性置換基とアニオンとの間の配位子交換機能によって該蛍光色素上の電子供与性が増大し、その結果、蛍光色素のスペクトルに変化が生じることを特徴とするものである。
この蛍光色素上の電子供与性置換基とアニオンとの間の配位子交換機能とは、アニオンホスト(金属錯体)に対して配位力の強いアニオン種が存在しない水溶液系では、蛍光色素上の電子供与性置換基が金属イオンに配位しているが、配位力の強いアニオン種がその系に添加されることによって電子供与性置換基が金属イオンとの配位結合から外れ、その結果電子供与性置換基に生じる電子状態の変化が蛍光色素に伝わりその蛍光スペクトルに変化を及ぼす、より具体的には、蛍光色素の吸収(励起)スペクトルが長波長側にシフトするというものである。
従って、このような原理に基づき蛍光色素のスペクトルに変化が生じる化合物である限り、本発明化合物の各構成部分である環状ポリアミン、金属イオン、及び蛍光色素の構造及び種類は特に制限はない。
又、このような蛍光スペクトルの変化を効率よく起こさせる為には、アニオンホスト及び蛍光色素がリンカーを介して結合していることが好ましい。
【0008】
更に本発明は、このような化合物から成る蛍光センサー、特に、水溶液中のアニオンを検出することの出来る蛍光センサーに係る。
本発明のセンサーにより定量的に測定することが可能なアニオンの例としては、ピロリン酸イオン、リン酸イオン、及びハロゲンイオン等の無機アニオン、クエン酸イオン等の有機アニオン、並びに各種ヌクレオチドから成る群から選択される一種又は複数種のアニオンを挙げることが出来る。
【0009】
更に本発明は、本発明化合物をセンサーとして使用し、その蛍光色素の吸収(励起)スペクトルの長波長側へのシフトの度合いに基づき、例えば、水溶液中のアニオン濃度を測定する方法に係る。
更に本発明は、本発明化合物をセンサーとして使用し、その蛍光色素の吸収(励起)スペクトルの長波長側へのシフトの度合いに基づき、例えば、水溶液中のアニオン性残基の増減を測定する方法に係る。
更に本発明は、本発明化合物をセンサーとして使用し、蛍光強度の変化に基づき、アニオン性残基の増減を伴う反応に関与する酵素の活性を測定する方法に係る。このような酵素の例として、環状モノヌクレオチド特異的ホスホジエステラーゼ(ホスホジエステラーゼ3',5'-環状モノヌクレオチド)等のホスホジエステラーゼを挙げることが出来る。
【発明を実施するための最良の形態】
【0010】
本発明化合物において、環状ポリアミンを構成する窒素原子及び炭素原子の各個数及びそれらの総数に特に制限はないが、好ましくは)〜12、より好ましくは12であり、窒素原子数は好ましくは3又は4、より好ましくは4である。
具体的には好適な環状ポリアミンとして、1,4,7,10−テトラアザシクロデカン(サイクレン)を挙げることが出来る。
又、本発明化合物の蛍光色素上の電子供与性置換基にも特に制限はないが、蛍光色素、環状ポリアミン及び金属イオンの種類等に応じて当業者が適宜選択することができるが、好適例としてアミノ基を挙げ蛍光色素ることが出来る。
蛍光色素もその他の構成成分に応じて当業者が適宜選択することができるが、好適例としてが7位置換クマリン誘導体、例えば、7−アミノ−トリフルオロメチルクマリンを挙げることが出来る。
リンカーとしては、例えば、エチレン基及びメチレン基等のアルキレン基を使用することが出来る。
金属錯体を構成する金属の好適例として、CdII等の遷移金属を挙げることが出来る。
【0011】
本発明の化合物は、例えば、以下の実施例に具体的に示すような合成方法によって、当業者であれば容易に調製することが出来る。更に、各物質の入手方法、各化合物の合成方法、及び、合成された化合物(PDF)に関する性状分析データ等については、インターネットhttp://pubs.acs.orgを介して無償で入手可能である。
【実施例】
【0012】
以下、実施例により本発明をより具体的に説明するが、本発明はこれら実施例により何ら限定されるものではない。
【0013】
実施例1
化合物の調製
以下の化学反応式に示した4工程で、7-アミノ-4-トリフルオロメチルクマリンを出発物質として、サイクレン共役のクマリン(1)を合成し、NH−シリカゲル(フジ・シリシア・ケミカル株式会社)カラムクロマトグラフィによって精製した。こうして合成された本発明に属する化合物である、化合物(1)のCdII錯体、即ち、錯体1−CdIIは過塩素酸塩として得られ、2-プロパノール/H2Oから再結晶した。
【0014】
【化1】

【0015】
上に示したサイクレン共役のクマリン(1)及び錯体1−CdIIの合成経路において使用する反応試薬は次のとおりである。(a)TsCl ピリジン、
(b) BrCH2CH2Br、Cs2CO3、(c) 濃H2SO4、90℃(d) サイクレン、
(e) Cd(ClO4)2 60℃。
尚、本発明に属するその他の化合物も、当業者であれば、上記合成経路に準じて適宜合成することが出来る。
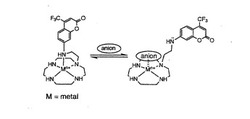
こうして合成された本発明化合物がアニオンを検出する蛍光センサーとして機能し、アニオンを検出する機構を図1に示した。ここで、Mn+はサイクレンによって安定的にキレートされうる金属イオンである。
【0016】
実施例2
本発明化合物の吸収スペクトルと励起スペクトル
どの金属が我々の設計概念に最も良く合致するかを見い出すために、我々は化合物(1)のZnII、CdII、及びCuIIとの錯体、及び金属なしでの化合物(1)の吸収スペクトル及び蛍光スペクトルを測定した。化合物(1)の濃度は5mM、 金属はすべて化合物(1)を基にして1.2当量加えた。溶液は100mMのHEPES(pH 7.4)で緩衝した。尚、測定は、UV-1600 UV可視分光計(日本、京都、島津)を用いて、25℃にて5mMの濃度で実施した。更に、蛍光分光計はF-4500(日本、東京、日立)を使用した。
得られた吸収スペクトル及び励起スペクトルを図2に示す。これらの金属はサイクレンによって強く配位されることが良く知られている。図1に示すようにアニオンのセンサー検出には7-アミノ基の金属への配位が求められ、金属の配位における窒素の単独電子対の関与がそのような波長のシフトを誘導するので、望ましいスペクトルの変化は、吸収スペクトル及び励起スペクトルの青色シフトであった。
ZnII、CdII、及びCuIIととの錯体の形成が極めて緩慢なために、十分な平衡化(3時間を超える)の後スペクトルを測定した。化合物(1)の吸収スペクトルのピークは382nmであり、錯体1−ZnII、錯体1−CdII及び錯体1−CuIIのそれは、それぞれ388nm、342nm及び342nmであった。即ち、CdII、及びCuIIを化合物(1)の溶液に加えた場合、それぞれの吸収スペクトルにおける青色シフトが認められた。このことは、7-アミノ基がCdII及びCuIIに配位するという考えを支持している。錯体1−ZnIIの吸収スペクトルはわずかに赤色シフトした。この赤色シフトは、ZnIIと7-アミノ-4-トリフルオロメチルクマリンとの間に何らかの相互作用があることを示しているが、上述の理由によって7-アミノ基は多分ZnIIには配位していないものと思われる。
化合物(1)、錯体1−ZnII、及び錯体1−CdIIの励起スペクトルは、錯体1−ZnIIの蛍光強度がやや増加したが、それらの吸収スペクトルに類似していた。一方、これらに対して、CuIIの性質(CuIIイオンは種々の蛍光化合物の蛍光を失活させることは一般に知られている)のために錯体1−CuIIの蛍光は顕著に低下した。
図1に示すアニオンのセンサー検出の原理から、中心金属イオンは、7-アミノ基を含む5つの窒素原子によって配位されることが必要である。従って、100mMのHEPESを含む中性水溶液中にて化合物(1)の7-アミノ基によってZnIIが配位されなければ、錯体1−ZnIIは、アニオンセンサーとして作用することはできない。さらに、錯体1−CuIIの蛍光は強く失活させられるので、これも蛍光センサーとしては適当ではない。
従って、吸収スペクトル及び励起スペクトルに基づいて、我々は、錯体1−CdIIが、図1に示すような我々の設計概念に基づく最も良好な蛍光アニオンセンサーであるという結論に達した。
【0017】
実施例3
電位差pH滴定
次に、参考文献12に詳細に記載されている手順に従って、1:1の金属-化合物(1)(0.17mMと0.5mM)錯体システム(化合物(1)・4HCO4、化合物(1)・4HClO4+Zn(ClO4)2及び化合物(1)・4HClO4+Cd(ClO4)2)について、イオン強度I=0.1M(Et4NClO4)、25℃にて電位差pH滴定実験を行った。配位子のプロトン化定数、金属錯体形成定数及び分布ダイヤグラムは、コンピュータ・プログラム、SUPERQUAD13及びMINIQUAD14を用いて算出した。
その結果を表1に示す。化合物(1)のプロトン化平衡定数は、9.67(logK1=logb011) 及び8.39(logK2 = logb012- logb011)であった。他のさらに低いpKaは算出できなかった。
【0018】
【表1】

【0019】
表1においてlogb110として示されるZnII及びCdIIに対する化合物(1)の安定定数を算出し、logK(錯体1−ZnII)及びlogK(錯体1−CdII)はそれぞれ10.80及び11.38であった。報告されているlogK(サイクレンZnII)及びlogK(サイクレンCdII)はそれぞれ16.2及び14.3である。化合物(1)-金属の配位形成が、サイクレンのそれと同じであるならば、logK(錯体1−ZnII)はlogK(1−CdII)よりも大きいことが期待されるが、そうはならず、すなわち、化合物(1)-金属錯体の相対的安定性の順序は、サイクレン金属錯体に比べて逆であった。この結果は、錯体1−CdIIの配位形成は、錯体1−ZnIIのそれとは異なることを示唆している。我々は、ZnIIに強く結合するアニオンが存在していなくても芳香族アミノ基がZnIIに配位するのを水分子が妨げる可能性があり、ZnIIは芳香族アミノ基によって配位されないとみなしている。一方、その結果は、CdIIが5つの窒素原子、すなわち、サイクレンの4つのアミノ基と芳香族アミノ基によってキレートされるという考えに一致している。従って、pH滴定の結果もまた、錯体1−CdIIが図1における設計原理を満たしていることを示唆している。
【0020】
実施例4
1-CdIIを用いたアニオンの蛍光検出
次に、種々のアニオンが励起スペクトルにどのような影響を持つのかを調べるために、合成した錯体1−CdII溶液(5mM)に種々のアニオンを加えた。スペクトルはすべて100mMのHEPES緩衝液(pH7.4)の存在下、25℃にて測定した。
錯体1−CdII溶液にピロリン酸ナトリウム(PPi)溶液を加えた場合、励起スペクトルは、 用量依存性に長い波長の方にシフトした。図3に示すように、10mMのPPiを加えた後、λmaxは、342nmから383nmにシフトした。錯体1−CdII溶液+10mMのPPiの励起スペクトルは、遊離の塩基(図2)のそれに類似していた(例えば、両者のピーク波長はおよそ380nmだった)。設計概念の項目で記載したように、7-アミノクマリンの場合、励起スペクトルの深色シフトは、7-アミノ基の電子密度が上昇したことを示す7。このような結果は、我々が期待したように、不安定な5番目の配位子(芳香族アミノ基)が用量依存性にPPiアニオンに置き換わったことを示している(図1)。要するに、中性の水溶液において、アミノ基が分子内にあったとしても、芳香族アミノ基よりもPPiの方がCdII-サイクレンに対して大きな親和性を持っていることが示された。
【0021】
更に、同様な方法を用いてその他のアニオンの効果を調べ、励起スペクトルのピークにおける蛍光測定値をアニオンの濃度に対してプロットし、以下の式に従って、各アニオンに対する錯体1−CdIIから成るセンサーの見かけの解離定数(Kd)を算出した。
式:F=(F0 + Fmax[A]/Kd) / (1 + [A]/Kd)
上式において、F0はアニオンなしの最初のFの値、FmaxはFの最大値、及び[A]は溶液に加えたアニオンの最終濃度を示す。尚、アニオンはすべてナトリウム塩又はカリウム塩として加えた。Kdはすべて、100mMのHEPES緩衝液(pH7.4)の条件下で算出した。
その結果を以下の表2に示す。*Kdは大きすぎて計算できなかった。
【0022】
【表2】

【0023】
表2の結果から明らかなように、クエン酸塩が強い親和性を示した。リン酸塩は、おそらくプロトン化形態のためにPPiよりも極めて低い親和性を持ち、HPO42−およびH2PO4−は、pH7.4の水溶液では優勢な種であり、それらはPPiよりも負の荷電数が少ない。過塩素酸塩は100mMでもいかなる変化も起こさなかった。オキソ酸に関しては、多価のアニオンは一価又は二価のアニオンよりも強く錯体1−CdIIに結合した。このようなデータは、アニオンが、複数点での認識を介して、おそらく金属とサイクレン環のNHプロトンの双方によって錯体1−CdIIと相互作用していることを示唆している。
ハロゲンイオンについては、スペクトル変化は、I−>Br−>Cl−>>F−の順で生じ、ソフト塩基度の程度を反映していた。このことは、CdIIがソフト酸であり、ソフト塩基に対して高い親和性を持つという事実に一致する。
【0024】
さて、一部のヌクレオチドが生物における重要な役割を持つ負に荷電した有機化合物であり、特に、cAMPやcGMPのような環状ヌクレオチドは細胞内セカンドメッセンジャーとして作用するので、種々のヌクレオチドのセンサー検出は極めて重要である。そこで、次にこれらのヌクレオチドについて検討した。
第1に、4種のヌクレオシド一リン酸、AMP、GMP、CMP及びUMPを5mMの錯体1−CdII溶液に加えた。興味深いことに、GMPだけが蛍光を失活させ、ほかの3種のヌクレオチドは無機アニオンのように励起スペクトルの赤色シフトを誘発した(図4[a])。又、見かけの解離定数を表2に示す。このような結果は、励起スペクトルの形状及び解離定数がヌクレオチドの塩基に依存することを示唆している。考えられる説明の1つは、クマリンが直接、ヌクレオチドの塩基と相互作用しているということである。
2つの環状ヌクレオチド、cAMPとcGMPは、それぞれその加水分解産物であるAMPとGMPよりも錯体1−CdIIに対して低い親和性を示した。cAMPとAMPのスペクトルデータを図4[b]に示す。10mMのcAMPを加えても錯体1−CdIIに1の励起スペクトルの変化は小さかった。このスペクトルは、100mMのAMPを加えた時のスペクトルに類似していた。1mM未満のcAMPの添加では錯体1−CdIIの励起スペクトルはほとんど変化しなかった。この結果を考慮すると、AMPとcAMPの結合強度の差異はおそらくアニオン部位の数に基づくものであった。
【0025】
実施例5
アニオンのセンサー検出の可逆性
次に、アニオンのセンサー検出の可逆性について調べた。センサー検出システムが可逆的であれば、CdIIに配位するアニオンの減少が励起スペクトルの青色シフトを生じ、それが元のスペクトルに回復するはずである。PPiを結合し、PPiがCdIIに配位するのを妨げるために、PPiを含む溶液に過剰量のMgIIを加えた。1mMのPPiを含む錯体1−CdII(5mM)の溶液に10mgのMg(ClO4)2を加えた場合、励起スペクトルは実際に青色にシフトしてλmax 345nmであった(図5[a])。このスペクトルはPPiを含んでいない錯体1−CdIIのスペクトルにほぼ正確に一致した。
更に、ピロリン酸の加水分解の影響を調べた。無機ピロホスファターゼは、1つのピロリン酸塩を2つのリン酸イオンに変換することが知られている9。リン酸塩はPPiよりも弱く錯体1−CdIIに配位するので、PPiの切断は、大量のMgIIイオンで見られたのと同じようなスペクトル変化を誘発するはずである。pH7.4にて1mMのピロリン酸塩を含む錯体1−CdII溶液に0.33U/mlの無機ピロホスファターゼと0.5mMのMg(ClO4)2を加えると、励起スペクトルのピークは短い波長の方に迅速にシフトした(図5[b])。これらの結果も、センサー検出メカニズムが可逆的であることを示している。
【0026】
実施例6
ホスホジエステラーゼの測定
生化学的応用へのこのシステムの可能性を調べるために、我々は、ホスホジエステラーゼ(PDE)の活性をモニターすることを試みた。我々は、環状ヌクレオチドのホスホジエステルの開裂によって環状ヌクレオチドのヌクレオシド一リン酸への変換、例えば、cAMPのAMPへの変換(化2)を触媒するホスホジエステラーゼ3',5'-環状モノヌクレオチド10を用いた。そのような酵素は細胞内シグナル伝達に関与するので、その活性11を感度良く検出するシステムを開発することは極めて重要である。
【0027】
【化2】

【0028】
実施例5で示されたように、錯体1−CdIIから成る本発明の蛍光センサーは、cAMPよりもはるかに強くAMPを認識した。従って次に、AMPの上昇をモニターすることによってPDE活性をリアルタイムで検出することを試みた。
即ち、pH7.4にて、100mMのHEPES、10mMのcAMP、10mMのCaCl2及び0.02U/mlのPDEアクチベータを含む5mMの錯体1−CdIIに2U/ml(最終濃度)のPDEを加えた後、数回、励起スペクトル(放射波長は500nm)を測定した。その結果、図6[a]及び[b]に示すように、蛍光強度(励起波長:380nm/ 放射波長:500nm)は徐々に増加した。このスペクトル変化は、cAMPからAMPへの変換を示している。このような結果から、ホスホジエステラーゼ3',5'-環状ヌクレオチド活性のリアルタイム蛍光測定に本発明化合物である錯体1−CdIIが有用であることが明らかにされた。又、このアプローチは、他の酵素活性の測定に応用可能であると期待される。
【0029】
本発明者は、スペクトル及びpH電位差のデータに基づいて、CdIIが7位置換クマリン誘導体の7-アミノ基によって弱く配位されるので、アニオンの一部がそれを置き換えることができ、その場所でCdIIイオンに配位することができ、下が手、このような化合物から成るアニオン検出用の蛍光センサーが可逆的であることを確認した。更に、本発明者は、本発明化合物である錯体1−CdIIを用いて、環状ヌクレオチドのホスホジエステル結合を加水分解するホスホジエステラーゼ活性を水溶液中でモニターできることを証明した。このような特徴を持ったセンサーはこれまでに知られておらず、本発明化合物である錯体1−CdIIは多数の生物学的及び分析的応用で好ましいアニオンセンサーになり得る。
【0030】
引用文献リスト
(1) (a) Grynkiewicz, G.; Poenie, M.; Tsien, R. Y. J. Bid. Chem. 1985,
260, 3440. (b) Minta, A.; Kao, J. P. Y.; Tsien, R. Y. J. Bid. Chem. 1989,264, 8171.
(2) de Silva, A. P.; Gunaratne, H. Q. N.; Gunnlaugsson, T.; Huxley, A. J. M.; McCoy, C. P.; Rademacher, J. T.; Rice, T. E. Chem. Rev. 1997, 97, 1515.
(3) (a) Schmidtchen, F. P.; Berger, M. Chem. Rev. 1997, 97, 1609.
(b) Kimura, E.; Koike, T. Chem. Commun. 1998, 1495. (c) Snowden, T. S.; Anslyn, E. V. Curr. Opin. Chem. Biol. 1999, 3, 740.
(4) (a) De Santis, G.; Fabbrizzi, L.; Licchelli, M.; Poggi, A.; Taglietti, A. Angew. Chem. Int. Ed. Engl.1996, 35, 202. (b) Fabbrizzi, L.; Faravelli, I.; Francese, G.; Licchelli, M.; Perotti, A.; Taglietti, A.Chem. Commun. 1998, 971. (c) Watanabe, S.; Onogawa, 0.; Komatsu, Y.; Yoshida, K. J. Am. Chem.Soc. 1998, 120, 229. (d) Niikura, K.; Metzger, A.; Anslyn, E. V. J. Am. Chem. Soc. 1998, 120,8533. (e)Nishizawa, S.;Kato, Y.; Teramae, N. J. Am. Chem. Soc. 1999, 121, 9463. (f) Miyaji, H.;Anzenbacher Jr, P.; Sessler, J. L.; Bleasdale, E.R.; Gale, P. A. Chem. Commun. 1999, 1723.
(5) Czarnik, A. W. Acc. Chem. Res. 1994, 27, 302.
(6) (a) Koike, T.; Kajitani, S.; Nakamura, I.; Kimura, E.; Shiro, M. J. Am. Chem. Soc. 1995, 117,1210. (b) Kimura, E.; Aoki, S.; Koike, T; Shiro, M. J. Am. Chem. Soc. 1997, 119, 3068.
(7) Wheelock, C. E. J. Am. Chem. Soc. 1959, 81, 1348.
(8) Kodama, M.; Kimura, E. J. Chem. Soc. Dalton Trans., 1977, 2269.
(9) (a) Moe, 0. A.; Butler, L. G. J. Biol. Chem. 1972, 247, 7308. (b) Cooperman, B. S.; Chiu, N.Y.; Bruckmann, R. H.; Bunick, G. J.; McKenna, G. P. Biochemistry, 1973, 12, 1665.
(10) Ho, H. C.; Teo, T. S.; Desai, R.; Wang, J. H. Biochim. Biophys. Acta, 1976, 429, 461.
(11) (a) Rutten, W. J.; Schoot, B. M.; De Pont, J. J. H. H. M. Biochim. Biophys. Acta, 1973, 315,378. (b) Thompson, W. J.; Appleman, M. M. Biochemistry, 1971, 10, 311. (c) Hiratsuka, T. J. Biol Chem., 1982, 257, 13354.
(12) Odani, A. Physical Methods in Supramolecular Chemistry (Comprehensive Supramolecular Chemistry, Vol.8), Davies J. E. D. and Ripmeester J. A., Eds., Pergamon, 1996, 8, 445.
(13) Gans, P.; Sabatini, A.; Vacca, A. J. Chem. Soc., Dalton Trans., 1985, 1195.
(14) Sabatini, A.; Vacca, A.; Gans P. Talanta 1974, 21, 53.
【図面の簡単な説明】
【0031】
【図1】図1は、本発明化合物がアニオンを検出する蛍光センサーとして機能し、アニオンを検出する機構を示す。
【図2】図2は、(a)種々の金属と化合物(1)の(a)吸収スペクトル及び(b)励起スペクトル(放射波長は500nm)を示す。ここで、縦軸:(a)蛍光強度、(b)吸収度、横軸:波長である。
【図3】図3は、100mMのHEPES緩衝液(pH7.4)中で25℃にてピロリン酸ナトリウム(0、0.003、0.01、0.03、0.1、0.3、3、10mM)を加えた場合の5mMの錯体1−CdIIの励起スペクトルを示す。放射波長は500nmであり、縦軸は「蛍光強度」、横軸は「波長」である。
【図4】図4は、(a)AMP、GMP、CMP及びUMP、並びに(b)AMP及びcAMPを加えた際の5mMの錯体1−CdIIにおける励起スペクトルの比較を示す。各ヌクレオチドの濃度は10mMである。
【図5】図5は、(a)1mMのNa4P2O7(記号なし)及び1mMのNa4P2O7+10mMのMg2(ClO4)2(白抜きのマル)を伴った錯体1−CdIIの励起スペクトル、及び、(b)無機ピロリン酸塩を添加する前(記号なし)及び添加後20分(白抜きのマル)の1mMのNa2P4O7を伴った錯体1−CdIIの励起スペクトルを示す。放射波長は500nmである。
【図6】図6は、ホスホジエステラーゼ活性の測定における、(a)錯体1−CdIIの励起スペクトルの変化(放射波長は500nm)、及び(b)蛍光強度-時間のプロット(励起/放射波長は380nm/500nm)を示す。
【技術分野】
【0001】
本発明は、特に水溶液中のアニオンを検出することの出来るセンサー化合物、及び該化合物を使用する各種測定方法に関する。
【背景技術】
【0002】
蛍光センサーは、生体系における生体分子の役割を分析し、解明するのに有用であり、例えば、蛍光CaII指示薬を用いて、細胞内CaIIのいくつかの機能が解明されてきた1。さらにその他に多数の金属センサー及びpHセンサーが開発されている2。
【0003】
多数の有機アニオン及び無機アニオンが生きている生物において重要な役割を担っているために、今やアニオン認識3及びアニオンセンサー検出4に関心が高まっている。アニオンセンサーの開発によって分子内にアニオン基を持つ生体有機分子を検出することができる新規のセンサーの開発にも繋がる。しかしながら、従来知られているほとんどのセンサーは有機媒質の中でしか機能せず、それらを生化学的又は生理学的な実験に使用するのは困難である。
一般にアニオンは、金属イオンのような陽イオンよりも大型なので、陽イオンよりも溶媒化の制約を受け易い。有機溶媒では、溶媒化エネルギーが比較的小さく、静電気の相互作用が効果的に働くので、アニオンを捕捉し、検出するのはさほど難しくはない。しかしながら、生体応用に適している水性溶媒では、強い水和のためにアニオンを認識するのは極めて困難である。今のところ、有機環境では多数が知られているけれども、水溶液中で作動する蛍光アニオンセンサーはほとんど開発されていない。
【0004】
水溶液中で使用するための蛍光アニオンセンサーは、2つの必要条件を満たさなければならない。1つは、水中でのアニオンに対する十分に強い親和性であり、もう11つは、アニオンの認識を蛍光シグナルに変換する能力である。既知のアニオンセンサーはほとんど、後者の必要条件は満たすけれども、水中でのアニオンに対して十分な親和性を持っていない。アニオンホストの中には、水性溶媒中でアニオンを捕捉することができるものもあるが、それらは単にホスト分子であって、センサー分子ではない。双方の必要条件を同時に満たすのは困難である。
【0005】
Crazuik et alは、水溶液中で作動する蛍光アニオンセンサーの開発に成功した5。このようなセンサーの検出メカニズムは、蛍光団に隣接したアミノ基のpKaをアニオンが結合することによって変化させることに基づいている。しかしながら、このセンサーではある特定のpH領域でしか測定できず、pH変化に敏感である。従って、このセンサー検出のメカニズムを生物実験に応用するのは困難である。
【発明の開示】
【発明が解決しようとする課題】
【0006】
従って、本発明の目的は、各種生物系の実験系においても使用することができるような水溶液中におけるアニオンを定量的に測定することができるセンサー化合物を提供することである。
【課題を解決するための手段】
【0007】
本発明者は上記課題を解決すべく鋭意研究した結果、アニオンを検出するための新規の手段を開発し、本発明を完成した。
即ち、本発明は、環状ポリアミンの金属錯体から成るアニオンホスト及び蛍光色素を有する化合物であって、該金属錯体の金属イオンとの配位結合において、該蛍光色素上の置換基とアニオンとの間の配位子交換機能によって蛍光色素のスペクトルに変化が生じることを特徴とする、前記化合物に係る。
より、具体的には、本発明は環状ポリアミンの金属錯体から成るアニオンホスト及び蛍光色素を有する化合物であって、該金属錯体の金属イオンとの配位結合に関与する該蛍光色素上の電子供与性置換基とアニオンとの間の配位子交換機能によって該蛍光色素上の電子供与性が増大し、その結果、蛍光色素のスペクトルに変化が生じることを特徴とするものである。
この蛍光色素上の電子供与性置換基とアニオンとの間の配位子交換機能とは、アニオンホスト(金属錯体)に対して配位力の強いアニオン種が存在しない水溶液系では、蛍光色素上の電子供与性置換基が金属イオンに配位しているが、配位力の強いアニオン種がその系に添加されることによって電子供与性置換基が金属イオンとの配位結合から外れ、その結果電子供与性置換基に生じる電子状態の変化が蛍光色素に伝わりその蛍光スペクトルに変化を及ぼす、より具体的には、蛍光色素の吸収(励起)スペクトルが長波長側にシフトするというものである。
従って、このような原理に基づき蛍光色素のスペクトルに変化が生じる化合物である限り、本発明化合物の各構成部分である環状ポリアミン、金属イオン、及び蛍光色素の構造及び種類は特に制限はない。
又、このような蛍光スペクトルの変化を効率よく起こさせる為には、アニオンホスト及び蛍光色素がリンカーを介して結合していることが好ましい。
【0008】
更に本発明は、このような化合物から成る蛍光センサー、特に、水溶液中のアニオンを検出することの出来る蛍光センサーに係る。
本発明のセンサーにより定量的に測定することが可能なアニオンの例としては、ピロリン酸イオン、リン酸イオン、及びハロゲンイオン等の無機アニオン、クエン酸イオン等の有機アニオン、並びに各種ヌクレオチドから成る群から選択される一種又は複数種のアニオンを挙げることが出来る。
【0009】
更に本発明は、本発明化合物をセンサーとして使用し、その蛍光色素の吸収(励起)スペクトルの長波長側へのシフトの度合いに基づき、例えば、水溶液中のアニオン濃度を測定する方法に係る。
更に本発明は、本発明化合物をセンサーとして使用し、その蛍光色素の吸収(励起)スペクトルの長波長側へのシフトの度合いに基づき、例えば、水溶液中のアニオン性残基の増減を測定する方法に係る。
更に本発明は、本発明化合物をセンサーとして使用し、蛍光強度の変化に基づき、アニオン性残基の増減を伴う反応に関与する酵素の活性を測定する方法に係る。このような酵素の例として、環状モノヌクレオチド特異的ホスホジエステラーゼ(ホスホジエステラーゼ3',5'-環状モノヌクレオチド)等のホスホジエステラーゼを挙げることが出来る。
【発明を実施するための最良の形態】
【0010】
本発明化合物において、環状ポリアミンを構成する窒素原子及び炭素原子の各個数及びそれらの総数に特に制限はないが、好ましくは)〜12、より好ましくは12であり、窒素原子数は好ましくは3又は4、より好ましくは4である。
具体的には好適な環状ポリアミンとして、1,4,7,10−テトラアザシクロデカン(サイクレン)を挙げることが出来る。
又、本発明化合物の蛍光色素上の電子供与性置換基にも特に制限はないが、蛍光色素、環状ポリアミン及び金属イオンの種類等に応じて当業者が適宜選択することができるが、好適例としてアミノ基を挙げ蛍光色素ることが出来る。
蛍光色素もその他の構成成分に応じて当業者が適宜選択することができるが、好適例としてが7位置換クマリン誘導体、例えば、7−アミノ−トリフルオロメチルクマリンを挙げることが出来る。
リンカーとしては、例えば、エチレン基及びメチレン基等のアルキレン基を使用することが出来る。
金属錯体を構成する金属の好適例として、CdII等の遷移金属を挙げることが出来る。
【0011】
本発明の化合物は、例えば、以下の実施例に具体的に示すような合成方法によって、当業者であれば容易に調製することが出来る。更に、各物質の入手方法、各化合物の合成方法、及び、合成された化合物(PDF)に関する性状分析データ等については、インターネットhttp://pubs.acs.orgを介して無償で入手可能である。
【実施例】
【0012】
以下、実施例により本発明をより具体的に説明するが、本発明はこれら実施例により何ら限定されるものではない。
【0013】
実施例1
化合物の調製
以下の化学反応式に示した4工程で、7-アミノ-4-トリフルオロメチルクマリンを出発物質として、サイクレン共役のクマリン(1)を合成し、NH−シリカゲル(フジ・シリシア・ケミカル株式会社)カラムクロマトグラフィによって精製した。こうして合成された本発明に属する化合物である、化合物(1)のCdII錯体、即ち、錯体1−CdIIは過塩素酸塩として得られ、2-プロパノール/H2Oから再結晶した。
【0014】
【化1】

【0015】
上に示したサイクレン共役のクマリン(1)及び錯体1−CdIIの合成経路において使用する反応試薬は次のとおりである。(a)TsCl ピリジン、
(b) BrCH2CH2Br、Cs2CO3、(c) 濃H2SO4、90℃(d) サイクレン、
(e) Cd(ClO4)2 60℃。
尚、本発明に属するその他の化合物も、当業者であれば、上記合成経路に準じて適宜合成することが出来る。
こうして合成された本発明化合物がアニオンを検出する蛍光センサーとして機能し、アニオンを検出する機構を図1に示した。ここで、Mn+はサイクレンによって安定的にキレートされうる金属イオンである。
【0016】
実施例2
本発明化合物の吸収スペクトルと励起スペクトル
どの金属が我々の設計概念に最も良く合致するかを見い出すために、我々は化合物(1)のZnII、CdII、及びCuIIとの錯体、及び金属なしでの化合物(1)の吸収スペクトル及び蛍光スペクトルを測定した。化合物(1)の濃度は5mM、 金属はすべて化合物(1)を基にして1.2当量加えた。溶液は100mMのHEPES(pH 7.4)で緩衝した。尚、測定は、UV-1600 UV可視分光計(日本、京都、島津)を用いて、25℃にて5mMの濃度で実施した。更に、蛍光分光計はF-4500(日本、東京、日立)を使用した。
得られた吸収スペクトル及び励起スペクトルを図2に示す。これらの金属はサイクレンによって強く配位されることが良く知られている。図1に示すようにアニオンのセンサー検出には7-アミノ基の金属への配位が求められ、金属の配位における窒素の単独電子対の関与がそのような波長のシフトを誘導するので、望ましいスペクトルの変化は、吸収スペクトル及び励起スペクトルの青色シフトであった。
ZnII、CdII、及びCuIIととの錯体の形成が極めて緩慢なために、十分な平衡化(3時間を超える)の後スペクトルを測定した。化合物(1)の吸収スペクトルのピークは382nmであり、錯体1−ZnII、錯体1−CdII及び錯体1−CuIIのそれは、それぞれ388nm、342nm及び342nmであった。即ち、CdII、及びCuIIを化合物(1)の溶液に加えた場合、それぞれの吸収スペクトルにおける青色シフトが認められた。このことは、7-アミノ基がCdII及びCuIIに配位するという考えを支持している。錯体1−ZnIIの吸収スペクトルはわずかに赤色シフトした。この赤色シフトは、ZnIIと7-アミノ-4-トリフルオロメチルクマリンとの間に何らかの相互作用があることを示しているが、上述の理由によって7-アミノ基は多分ZnIIには配位していないものと思われる。
化合物(1)、錯体1−ZnII、及び錯体1−CdIIの励起スペクトルは、錯体1−ZnIIの蛍光強度がやや増加したが、それらの吸収スペクトルに類似していた。一方、これらに対して、CuIIの性質(CuIIイオンは種々の蛍光化合物の蛍光を失活させることは一般に知られている)のために錯体1−CuIIの蛍光は顕著に低下した。
図1に示すアニオンのセンサー検出の原理から、中心金属イオンは、7-アミノ基を含む5つの窒素原子によって配位されることが必要である。従って、100mMのHEPESを含む中性水溶液中にて化合物(1)の7-アミノ基によってZnIIが配位されなければ、錯体1−ZnIIは、アニオンセンサーとして作用することはできない。さらに、錯体1−CuIIの蛍光は強く失活させられるので、これも蛍光センサーとしては適当ではない。
従って、吸収スペクトル及び励起スペクトルに基づいて、我々は、錯体1−CdIIが、図1に示すような我々の設計概念に基づく最も良好な蛍光アニオンセンサーであるという結論に達した。
【0017】
実施例3
電位差pH滴定
次に、参考文献12に詳細に記載されている手順に従って、1:1の金属-化合物(1)(0.17mMと0.5mM)錯体システム(化合物(1)・4HCO4、化合物(1)・4HClO4+Zn(ClO4)2及び化合物(1)・4HClO4+Cd(ClO4)2)について、イオン強度I=0.1M(Et4NClO4)、25℃にて電位差pH滴定実験を行った。配位子のプロトン化定数、金属錯体形成定数及び分布ダイヤグラムは、コンピュータ・プログラム、SUPERQUAD13及びMINIQUAD14を用いて算出した。
その結果を表1に示す。化合物(1)のプロトン化平衡定数は、9.67(logK1=logb011) 及び8.39(logK2 = logb012- logb011)であった。他のさらに低いpKaは算出できなかった。
【0018】
【表1】

【0019】
表1においてlogb110として示されるZnII及びCdIIに対する化合物(1)の安定定数を算出し、logK(錯体1−ZnII)及びlogK(錯体1−CdII)はそれぞれ10.80及び11.38であった。報告されているlogK(サイクレンZnII)及びlogK(サイクレンCdII)はそれぞれ16.2及び14.3である。化合物(1)-金属の配位形成が、サイクレンのそれと同じであるならば、logK(錯体1−ZnII)はlogK(1−CdII)よりも大きいことが期待されるが、そうはならず、すなわち、化合物(1)-金属錯体の相対的安定性の順序は、サイクレン金属錯体に比べて逆であった。この結果は、錯体1−CdIIの配位形成は、錯体1−ZnIIのそれとは異なることを示唆している。我々は、ZnIIに強く結合するアニオンが存在していなくても芳香族アミノ基がZnIIに配位するのを水分子が妨げる可能性があり、ZnIIは芳香族アミノ基によって配位されないとみなしている。一方、その結果は、CdIIが5つの窒素原子、すなわち、サイクレンの4つのアミノ基と芳香族アミノ基によってキレートされるという考えに一致している。従って、pH滴定の結果もまた、錯体1−CdIIが図1における設計原理を満たしていることを示唆している。
【0020】
実施例4
1-CdIIを用いたアニオンの蛍光検出
次に、種々のアニオンが励起スペクトルにどのような影響を持つのかを調べるために、合成した錯体1−CdII溶液(5mM)に種々のアニオンを加えた。スペクトルはすべて100mMのHEPES緩衝液(pH7.4)の存在下、25℃にて測定した。
錯体1−CdII溶液にピロリン酸ナトリウム(PPi)溶液を加えた場合、励起スペクトルは、 用量依存性に長い波長の方にシフトした。図3に示すように、10mMのPPiを加えた後、λmaxは、342nmから383nmにシフトした。錯体1−CdII溶液+10mMのPPiの励起スペクトルは、遊離の塩基(図2)のそれに類似していた(例えば、両者のピーク波長はおよそ380nmだった)。設計概念の項目で記載したように、7-アミノクマリンの場合、励起スペクトルの深色シフトは、7-アミノ基の電子密度が上昇したことを示す7。このような結果は、我々が期待したように、不安定な5番目の配位子(芳香族アミノ基)が用量依存性にPPiアニオンに置き換わったことを示している(図1)。要するに、中性の水溶液において、アミノ基が分子内にあったとしても、芳香族アミノ基よりもPPiの方がCdII-サイクレンに対して大きな親和性を持っていることが示された。
【0021】
更に、同様な方法を用いてその他のアニオンの効果を調べ、励起スペクトルのピークにおける蛍光測定値をアニオンの濃度に対してプロットし、以下の式に従って、各アニオンに対する錯体1−CdIIから成るセンサーの見かけの解離定数(Kd)を算出した。
式:F=(F0 + Fmax[A]/Kd) / (1 + [A]/Kd)
上式において、F0はアニオンなしの最初のFの値、FmaxはFの最大値、及び[A]は溶液に加えたアニオンの最終濃度を示す。尚、アニオンはすべてナトリウム塩又はカリウム塩として加えた。Kdはすべて、100mMのHEPES緩衝液(pH7.4)の条件下で算出した。
その結果を以下の表2に示す。*Kdは大きすぎて計算できなかった。
【0022】
【表2】

【0023】
表2の結果から明らかなように、クエン酸塩が強い親和性を示した。リン酸塩は、おそらくプロトン化形態のためにPPiよりも極めて低い親和性を持ち、HPO42−およびH2PO4−は、pH7.4の水溶液では優勢な種であり、それらはPPiよりも負の荷電数が少ない。過塩素酸塩は100mMでもいかなる変化も起こさなかった。オキソ酸に関しては、多価のアニオンは一価又は二価のアニオンよりも強く錯体1−CdIIに結合した。このようなデータは、アニオンが、複数点での認識を介して、おそらく金属とサイクレン環のNHプロトンの双方によって錯体1−CdIIと相互作用していることを示唆している。
ハロゲンイオンについては、スペクトル変化は、I−>Br−>Cl−>>F−の順で生じ、ソフト塩基度の程度を反映していた。このことは、CdIIがソフト酸であり、ソフト塩基に対して高い親和性を持つという事実に一致する。
【0024】
さて、一部のヌクレオチドが生物における重要な役割を持つ負に荷電した有機化合物であり、特に、cAMPやcGMPのような環状ヌクレオチドは細胞内セカンドメッセンジャーとして作用するので、種々のヌクレオチドのセンサー検出は極めて重要である。そこで、次にこれらのヌクレオチドについて検討した。
第1に、4種のヌクレオシド一リン酸、AMP、GMP、CMP及びUMPを5mMの錯体1−CdII溶液に加えた。興味深いことに、GMPだけが蛍光を失活させ、ほかの3種のヌクレオチドは無機アニオンのように励起スペクトルの赤色シフトを誘発した(図4[a])。又、見かけの解離定数を表2に示す。このような結果は、励起スペクトルの形状及び解離定数がヌクレオチドの塩基に依存することを示唆している。考えられる説明の1つは、クマリンが直接、ヌクレオチドの塩基と相互作用しているということである。
2つの環状ヌクレオチド、cAMPとcGMPは、それぞれその加水分解産物であるAMPとGMPよりも錯体1−CdIIに対して低い親和性を示した。cAMPとAMPのスペクトルデータを図4[b]に示す。10mMのcAMPを加えても錯体1−CdIIに1の励起スペクトルの変化は小さかった。このスペクトルは、100mMのAMPを加えた時のスペクトルに類似していた。1mM未満のcAMPの添加では錯体1−CdIIの励起スペクトルはほとんど変化しなかった。この結果を考慮すると、AMPとcAMPの結合強度の差異はおそらくアニオン部位の数に基づくものであった。
【0025】
実施例5
アニオンのセンサー検出の可逆性
次に、アニオンのセンサー検出の可逆性について調べた。センサー検出システムが可逆的であれば、CdIIに配位するアニオンの減少が励起スペクトルの青色シフトを生じ、それが元のスペクトルに回復するはずである。PPiを結合し、PPiがCdIIに配位するのを妨げるために、PPiを含む溶液に過剰量のMgIIを加えた。1mMのPPiを含む錯体1−CdII(5mM)の溶液に10mgのMg(ClO4)2を加えた場合、励起スペクトルは実際に青色にシフトしてλmax 345nmであった(図5[a])。このスペクトルはPPiを含んでいない錯体1−CdIIのスペクトルにほぼ正確に一致した。
更に、ピロリン酸の加水分解の影響を調べた。無機ピロホスファターゼは、1つのピロリン酸塩を2つのリン酸イオンに変換することが知られている9。リン酸塩はPPiよりも弱く錯体1−CdIIに配位するので、PPiの切断は、大量のMgIIイオンで見られたのと同じようなスペクトル変化を誘発するはずである。pH7.4にて1mMのピロリン酸塩を含む錯体1−CdII溶液に0.33U/mlの無機ピロホスファターゼと0.5mMのMg(ClO4)2を加えると、励起スペクトルのピークは短い波長の方に迅速にシフトした(図5[b])。これらの結果も、センサー検出メカニズムが可逆的であることを示している。
【0026】
実施例6
ホスホジエステラーゼの測定
生化学的応用へのこのシステムの可能性を調べるために、我々は、ホスホジエステラーゼ(PDE)の活性をモニターすることを試みた。我々は、環状ヌクレオチドのホスホジエステルの開裂によって環状ヌクレオチドのヌクレオシド一リン酸への変換、例えば、cAMPのAMPへの変換(化2)を触媒するホスホジエステラーゼ3',5'-環状モノヌクレオチド10を用いた。そのような酵素は細胞内シグナル伝達に関与するので、その活性11を感度良く検出するシステムを開発することは極めて重要である。
【0027】
【化2】

【0028】
実施例5で示されたように、錯体1−CdIIから成る本発明の蛍光センサーは、cAMPよりもはるかに強くAMPを認識した。従って次に、AMPの上昇をモニターすることによってPDE活性をリアルタイムで検出することを試みた。
即ち、pH7.4にて、100mMのHEPES、10mMのcAMP、10mMのCaCl2及び0.02U/mlのPDEアクチベータを含む5mMの錯体1−CdIIに2U/ml(最終濃度)のPDEを加えた後、数回、励起スペクトル(放射波長は500nm)を測定した。その結果、図6[a]及び[b]に示すように、蛍光強度(励起波長:380nm/ 放射波長:500nm)は徐々に増加した。このスペクトル変化は、cAMPからAMPへの変換を示している。このような結果から、ホスホジエステラーゼ3',5'-環状ヌクレオチド活性のリアルタイム蛍光測定に本発明化合物である錯体1−CdIIが有用であることが明らかにされた。又、このアプローチは、他の酵素活性の測定に応用可能であると期待される。
【0029】
本発明者は、スペクトル及びpH電位差のデータに基づいて、CdIIが7位置換クマリン誘導体の7-アミノ基によって弱く配位されるので、アニオンの一部がそれを置き換えることができ、その場所でCdIIイオンに配位することができ、下が手、このような化合物から成るアニオン検出用の蛍光センサーが可逆的であることを確認した。更に、本発明者は、本発明化合物である錯体1−CdIIを用いて、環状ヌクレオチドのホスホジエステル結合を加水分解するホスホジエステラーゼ活性を水溶液中でモニターできることを証明した。このような特徴を持ったセンサーはこれまでに知られておらず、本発明化合物である錯体1−CdIIは多数の生物学的及び分析的応用で好ましいアニオンセンサーになり得る。
【0030】
引用文献リスト
(1) (a) Grynkiewicz, G.; Poenie, M.; Tsien, R. Y. J. Bid. Chem. 1985,
260, 3440. (b) Minta, A.; Kao, J. P. Y.; Tsien, R. Y. J. Bid. Chem. 1989,264, 8171.
(2) de Silva, A. P.; Gunaratne, H. Q. N.; Gunnlaugsson, T.; Huxley, A. J. M.; McCoy, C. P.; Rademacher, J. T.; Rice, T. E. Chem. Rev. 1997, 97, 1515.
(3) (a) Schmidtchen, F. P.; Berger, M. Chem. Rev. 1997, 97, 1609.
(b) Kimura, E.; Koike, T. Chem. Commun. 1998, 1495. (c) Snowden, T. S.; Anslyn, E. V. Curr. Opin. Chem. Biol. 1999, 3, 740.
(4) (a) De Santis, G.; Fabbrizzi, L.; Licchelli, M.; Poggi, A.; Taglietti, A. Angew. Chem. Int. Ed. Engl.1996, 35, 202. (b) Fabbrizzi, L.; Faravelli, I.; Francese, G.; Licchelli, M.; Perotti, A.; Taglietti, A.Chem. Commun. 1998, 971. (c) Watanabe, S.; Onogawa, 0.; Komatsu, Y.; Yoshida, K. J. Am. Chem.Soc. 1998, 120, 229. (d) Niikura, K.; Metzger, A.; Anslyn, E. V. J. Am. Chem. Soc. 1998, 120,8533. (e)Nishizawa, S.;Kato, Y.; Teramae, N. J. Am. Chem. Soc. 1999, 121, 9463. (f) Miyaji, H.;Anzenbacher Jr, P.; Sessler, J. L.; Bleasdale, E.R.; Gale, P. A. Chem. Commun. 1999, 1723.
(5) Czarnik, A. W. Acc. Chem. Res. 1994, 27, 302.
(6) (a) Koike, T.; Kajitani, S.; Nakamura, I.; Kimura, E.; Shiro, M. J. Am. Chem. Soc. 1995, 117,1210. (b) Kimura, E.; Aoki, S.; Koike, T; Shiro, M. J. Am. Chem. Soc. 1997, 119, 3068.
(7) Wheelock, C. E. J. Am. Chem. Soc. 1959, 81, 1348.
(8) Kodama, M.; Kimura, E. J. Chem. Soc. Dalton Trans., 1977, 2269.
(9) (a) Moe, 0. A.; Butler, L. G. J. Biol. Chem. 1972, 247, 7308. (b) Cooperman, B. S.; Chiu, N.Y.; Bruckmann, R. H.; Bunick, G. J.; McKenna, G. P. Biochemistry, 1973, 12, 1665.
(10) Ho, H. C.; Teo, T. S.; Desai, R.; Wang, J. H. Biochim. Biophys. Acta, 1976, 429, 461.
(11) (a) Rutten, W. J.; Schoot, B. M.; De Pont, J. J. H. H. M. Biochim. Biophys. Acta, 1973, 315,378. (b) Thompson, W. J.; Appleman, M. M. Biochemistry, 1971, 10, 311. (c) Hiratsuka, T. J. Biol Chem., 1982, 257, 13354.
(12) Odani, A. Physical Methods in Supramolecular Chemistry (Comprehensive Supramolecular Chemistry, Vol.8), Davies J. E. D. and Ripmeester J. A., Eds., Pergamon, 1996, 8, 445.
(13) Gans, P.; Sabatini, A.; Vacca, A. J. Chem. Soc., Dalton Trans., 1985, 1195.
(14) Sabatini, A.; Vacca, A.; Gans P. Talanta 1974, 21, 53.
【図面の簡単な説明】
【0031】
【図1】図1は、本発明化合物がアニオンを検出する蛍光センサーとして機能し、アニオンを検出する機構を示す。
【図2】図2は、(a)種々の金属と化合物(1)の(a)吸収スペクトル及び(b)励起スペクトル(放射波長は500nm)を示す。ここで、縦軸:(a)蛍光強度、(b)吸収度、横軸:波長である。
【図3】図3は、100mMのHEPES緩衝液(pH7.4)中で25℃にてピロリン酸ナトリウム(0、0.003、0.01、0.03、0.1、0.3、3、10mM)を加えた場合の5mMの錯体1−CdIIの励起スペクトルを示す。放射波長は500nmであり、縦軸は「蛍光強度」、横軸は「波長」である。
【図4】図4は、(a)AMP、GMP、CMP及びUMP、並びに(b)AMP及びcAMPを加えた際の5mMの錯体1−CdIIにおける励起スペクトルの比較を示す。各ヌクレオチドの濃度は10mMである。
【図5】図5は、(a)1mMのNa4P2O7(記号なし)及び1mMのNa4P2O7+10mMのMg2(ClO4)2(白抜きのマル)を伴った錯体1−CdIIの励起スペクトル、及び、(b)無機ピロリン酸塩を添加する前(記号なし)及び添加後20分(白抜きのマル)の1mMのNa2P4O7を伴った錯体1−CdIIの励起スペクトルを示す。放射波長は500nmである。
【図6】図6は、ホスホジエステラーゼ活性の測定における、(a)錯体1−CdIIの励起スペクトルの変化(放射波長は500nm)、及び(b)蛍光強度-時間のプロット(励起/放射波長は380nm/500nm)を示す。
【特許請求の範囲】
【請求項1】
環状ポリアミンの金属錯体から成るアニオンホスト及び蛍光色素を有する化合物であって、該金属錯体の金属イオンとの配位結合において、該蛍光色素上の置換基とアニオンとの間の配位子交換機能によって蛍光色素のスペクトルに変化が生じることを特徴とする、前記化合物。
【請求項2】
環状ポリアミンの金属錯体から成るアニオンホスト及び蛍光色素を有する化合物であって、該金属錯体の金属イオンとの配位結合に関与する該蛍光色素上の電子供与性置換基とアニオンとの間の配位子交換機能によって該蛍光色素上の電子供与性が増大し、その結果、蛍光色素のスペクトルに変化が生じることを特徴とする、請求項1記載の化合物。
【請求項3】
金属錯体の金属イオンに対する配位力がより強いアニオンの存在によって、該金属錯体の金属イオンとの配位結合に関与する該蛍光色素上の電子供与性置換基が金属イオンとの配位結合からはずれることを特徴とする、請求項1又は2記載の化合物。
【請求項4】
蛍光色素の吸収(励起)スペクトルが長波長側にシフトすることを特徴とする、請求項1ないし3のいずれか一項に記載の化合物。
【請求項5】
アニオンホスト及び蛍光色素がリンカーを介して結合していることを特徴とする、請求項1ないし4のいずれか一項に記載の化合物。
【請求項6】
環状ポリアミンを構成する窒素原子及び炭素原子の総数が12であり、窒素原子数が4であることを特徴とする、請求項1ないし5のいずれか一項に記載の化合物。
【請求項7】
環状ポリアミンが1,4,7,10−テトラアザシクロデカンである、請求項6記載の化合物。
【請求項8】
蛍光色素上の電子供与性置換基がアミノ基である、請求項2ないし7のいずれか一項に記載の化合物。
【請求項9】
蛍光色素が7位置換クマリン誘導体である、請求項1ないし8のいずれか一項に記載の化合物。
【請求項10】
蛍光色素が7−アミノ−トリフルオロメチルクマリンである、請求項9に記載の化合物。
【請求項11】
リンカーがアルキレン基である、請求項5ないし10のいずれか一項に記載の化合物。
【請求項12】
リンカーがエチレン基である、請求項11に記載の化合物。
【請求項13】
金属錯体を構成する金属がCdである、請求項1ないし12のいずれか一項に記載の化合物。
【請求項14】
請求項1ないし13のいずれか一項に記載の化合物から成る蛍光センサー。
【請求項15】
水溶液中のアニオンを検出することの出来る、請求項14記載の蛍光センサー。
【請求項16】
アニオンが、ピロリン酸イオン、リン酸イオン、クエン酸イオン、ハロゲンイオン、及びヌクレオチドから成る群から選択される一種又は複数種のアニオンである、請求項15記載の蛍光センサー。
【請求項17】
請求項1ないし13のいずれか一項に記載の化合物をセンサーとして使用し、その蛍光色素の吸収(励起)スペクトルの長波長側へのシフトの度合いに基づき、アニオン濃度を測定する方法。
【請求項18】
水溶液中におけるアニオン濃度を測定することを特徴とする、請求項17に記載の測定方法。
【請求項19】
請求項1ないし13のいずれか一項に記載の化合物をセンサーとして使用し、その蛍光色素の吸収(励起)スペクトルの長波長側へのシフトの度合いに基づき、アニオン性残基の増減を測定する方法。
【請求項20】
水溶液中におけるアニオン性残基の増減を測定することを特徴とする、請求項19に記載の測定方法。
【請求項21】
請求項1ないし13のいずれか一項に記載の化合物をセンサーとして使用し、蛍光強度の変化に基づき、アニオン性残基の増減を伴う反応に関与する酵素の活性を測定する方法。
【請求項22】
酵素がホスホジエステラーゼである、請求項21に記載の方法。
【請求項23】
酵素が環状モノヌクレオチド特異的ホスホジエステラーゼである、請求項22に記載の方法。
【請求項1】
環状ポリアミンの金属錯体から成るアニオンホスト及び蛍光色素を有する化合物であって、該金属錯体の金属イオンとの配位結合において、該蛍光色素上の置換基とアニオンとの間の配位子交換機能によって蛍光色素のスペクトルに変化が生じることを特徴とする、前記化合物。
【請求項2】
環状ポリアミンの金属錯体から成るアニオンホスト及び蛍光色素を有する化合物であって、該金属錯体の金属イオンとの配位結合に関与する該蛍光色素上の電子供与性置換基とアニオンとの間の配位子交換機能によって該蛍光色素上の電子供与性が増大し、その結果、蛍光色素のスペクトルに変化が生じることを特徴とする、請求項1記載の化合物。
【請求項3】
金属錯体の金属イオンに対する配位力がより強いアニオンの存在によって、該金属錯体の金属イオンとの配位結合に関与する該蛍光色素上の電子供与性置換基が金属イオンとの配位結合からはずれることを特徴とする、請求項1又は2記載の化合物。
【請求項4】
蛍光色素の吸収(励起)スペクトルが長波長側にシフトすることを特徴とする、請求項1ないし3のいずれか一項に記載の化合物。
【請求項5】
アニオンホスト及び蛍光色素がリンカーを介して結合していることを特徴とする、請求項1ないし4のいずれか一項に記載の化合物。
【請求項6】
環状ポリアミンを構成する窒素原子及び炭素原子の総数が12であり、窒素原子数が4であることを特徴とする、請求項1ないし5のいずれか一項に記載の化合物。
【請求項7】
環状ポリアミンが1,4,7,10−テトラアザシクロデカンである、請求項6記載の化合物。
【請求項8】
蛍光色素上の電子供与性置換基がアミノ基である、請求項2ないし7のいずれか一項に記載の化合物。
【請求項9】
蛍光色素が7位置換クマリン誘導体である、請求項1ないし8のいずれか一項に記載の化合物。
【請求項10】
蛍光色素が7−アミノ−トリフルオロメチルクマリンである、請求項9に記載の化合物。
【請求項11】
リンカーがアルキレン基である、請求項5ないし10のいずれか一項に記載の化合物。
【請求項12】
リンカーがエチレン基である、請求項11に記載の化合物。
【請求項13】
金属錯体を構成する金属がCdである、請求項1ないし12のいずれか一項に記載の化合物。
【請求項14】
請求項1ないし13のいずれか一項に記載の化合物から成る蛍光センサー。
【請求項15】
水溶液中のアニオンを検出することの出来る、請求項14記載の蛍光センサー。
【請求項16】
アニオンが、ピロリン酸イオン、リン酸イオン、クエン酸イオン、ハロゲンイオン、及びヌクレオチドから成る群から選択される一種又は複数種のアニオンである、請求項15記載の蛍光センサー。
【請求項17】
請求項1ないし13のいずれか一項に記載の化合物をセンサーとして使用し、その蛍光色素の吸収(励起)スペクトルの長波長側へのシフトの度合いに基づき、アニオン濃度を測定する方法。
【請求項18】
水溶液中におけるアニオン濃度を測定することを特徴とする、請求項17に記載の測定方法。
【請求項19】
請求項1ないし13のいずれか一項に記載の化合物をセンサーとして使用し、その蛍光色素の吸収(励起)スペクトルの長波長側へのシフトの度合いに基づき、アニオン性残基の増減を測定する方法。
【請求項20】
水溶液中におけるアニオン性残基の増減を測定することを特徴とする、請求項19に記載の測定方法。
【請求項21】
請求項1ないし13のいずれか一項に記載の化合物をセンサーとして使用し、蛍光強度の変化に基づき、アニオン性残基の増減を伴う反応に関与する酵素の活性を測定する方法。
【請求項22】
酵素がホスホジエステラーゼである、請求項21に記載の方法。
【請求項23】
酵素が環状モノヌクレオチド特異的ホスホジエステラーゼである、請求項22に記載の方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】




【図2】


【図3】


【図4】


【図5】


【図6】


【公開番号】特開2008−58319(P2008−58319A)
【公開日】平成20年3月13日(2008.3.13)
【国際特許分類】
【出願番号】特願2007−225774(P2007−225774)
【出願日】平成19年8月31日(2007.8.31)
【分割の表示】特願2002−61098(P2002−61098)の分割
【原出願日】平成14年3月6日(2002.3.6)
【出願人】(503360115)独立行政法人科学技術振興機構 (1,734)
【Fターム(参考)】
【公開日】平成20年3月13日(2008.3.13)
【国際特許分類】
【出願日】平成19年8月31日(2007.8.31)
【分割の表示】特願2002−61098(P2002−61098)の分割
【原出願日】平成14年3月6日(2002.3.6)
【出願人】(503360115)独立行政法人科学技術振興機構 (1,734)
【Fターム(参考)】
[ Back to top ]

