アルカリ蓄電池用正極体およびその製造方法
【課題】正極活物質粒子の表面において導電材を均一にコートして強固な導電ネットワークを形成することにより、適用される電池の内部抵抗上昇が抑制されるアルカリ蓄電池用正極体およびその製造方法を提供する。
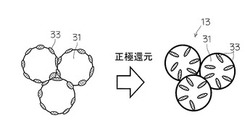
【解決手段】水酸化ニッケルを主成分とする活物質粒子31と、前記活物質粒子31の表面に付着する、コバルト化合物を主成分とする導電材33とを備えるアルカリ蓄電池に使用される正極体13に還元電流を流す。この還元電流を流す工程は、当該アルカリ蓄電池の活性化の前に行われることが好ましい。
【解決手段】水酸化ニッケルを主成分とする活物質粒子31と、前記活物質粒子31の表面に付着する、コバルト化合物を主成分とする導電材33とを備えるアルカリ蓄電池に使用される正極体13に還元電流を流す。この還元電流を流す工程は、当該アルカリ蓄電池の活性化の前に行われることが好ましい。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、主要な活物質として水酸化ニッケルを含み、導電材としてコバルト化合物を含むアルカリ蓄電池用の正極およびその製造方法に関する。
【背景技術】
【0002】
従来、主として携帯機器用の電源として使用する充放電可能な種々の二次電池が提案されてきた。さらに、近年、環境への配慮から、風力発電や太陽光発電のような自然エネルギーのロードレベリングや、自動車や電車などの車両の動力源に使用される大容量の二次電池が開発されている。自然エネルギー分野においては、主として、エネルギーの発生とその供給との平準化を図るために二次電池が用いられている。また、車両に二次電池を搭載した場合には、ブレーキ時に生じる回生電力をこの搭載電池に蓄えておき、車両の動力源として使用することができるので、車両の運行エネルギー効率を高めることができる。このような二次電池としては、エネルギー密度、負荷変動追従性、耐久性、製造コストなどの諸条件から、例えば、アルカリ蓄電池の一種であるニッケル水素二次電池が適しているとされる(例えば、特許文献1)。
【0003】
このような産業用に利用される二次電池には、きわめて高いレベルの耐久性が要求されるところ、ニッケル水素二次電池の充放電性能劣化の原因の一つとして、内部抵抗の増加が挙げられる。ニッケル水素二次電池の主たる正極活物質である水酸化ニッケル(Ni(OH)2)は、充電時に酸化されてオキシ水酸化ニッケル(NiOOH)になる。水酸化ニッケルが絶縁体であるのに対し、オキシ水酸化ニッケルは半導体であるため、電池の充電状態(SOC)が高いほど、電池の内部抵抗は低くなる。
【0004】
SOCが低い状態でも電極内の導電性を確保する必要があるため、導電材として水酸化コバルト(Co(OH)2)を添加したものが実用化されている(例えば、特許文献2)。この例では、図9に示すように、水酸化コバルトは、水酸化ニッケルの二次粒子表面をコーティングするように添加されており、電池の充電時に酸化されて導電性のあるオキシ水酸化コバルト(CoOOH)に変化する。なお、図9(a)の右下の像において、黒く写っている二次粒子の表面に存在する白く写っている部分がコバルト化合物である。また、図9(b)において、ほぼ球状の大径の粒子が二次粒子であり、その周囲に存在する粉砕された状態のものが一次粒子である。電池の通常の使用電圧範囲において、オキシ水酸化コバルトは還元されずに残るので、SOCが低い状態でも、ある程度の導電性を確保することができる。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2007−157479号公報
【特許文献2】特開2003−257425号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかし、上記の正極では、活物質である水酸化ニッケルの粒子表面に付着するコバルト化合物が粒子表面上で均一に分布していないので、活物質粒子間に形成される導電ネットワークの安定性が不十分であり、電池の充放電サイクルが進むにつれ、活物質粒子間の導電ネットワークが崩れてくる。その結果、SOCの低い領域において内部抵抗が増大し、これにより十分な繰り返し充放電サイクル寿命が得られない。
【0007】
本発明の目的は、上記の課題を解決するために、正極活物質粒子の表面において導電材を均一にコートして活物質粒子間に強固な導電ネットワークを形成することにより、適用される電池の内部抵抗上昇が抑制されるアルカリ蓄電池用正極体およびその製造方法を提供することにある。
【課題を解決するための手段】
【0008】
前記した目的を達成するために、本発明に係るアルカリ蓄電池用正極体の製造方法は、ニッケル化合物を主成分とする活物質粒子と、この活物質粒子の表面に付着する、コバルト化合物を主成分とする導電材とを含む正極体に還元電流を流す工程を含む。
【0009】
この構成によれば、導電材であるコバルト化合物の一部が還元電流によって溶解・分散し、還元析出される。その結果、前記導電材が粒径1〜3nmの微粒子として、活物質粒子表面に均一に分散し、正極活物質間に強固な導電ネットワークが形成されるので、当該正極体が使用されるアルカリ蓄電池の内部抵抗上昇が抑制され、電池の性能が向上する。
【0010】
本発明の一実施形態に係るアルカリ蓄電池用正極体の製造方法において、当該アルカリ蓄電池の活性化の前に前記還元電流を流すことが好ましい。この構成によれば、コバルトを高次に酸化して導電材として作用させる活性化工程の前に、正極活物質粒子の表面にコバルト化合物が均一にコートされるので、その後に行われる活性化工程においてきわめて強固な導電ネットワークが形成される。
【0011】
本発明の一実施形態に係るアルカリ蓄電池用正極体の製造方法において、前記導電材の少なくとも一部を、活物質一次粒子表面である活物質二次粒子内部に析出させることを含むことが好ましい。すなわち、前記活物質粒子は、より微細な一次粒子が複数凝集した二次粒子として形成されており、上記構成によれば、一次粒子表面に導電材が均一に析出することにより、導電材が活物質二次粒子内部にまで均一に分散する。これにより、正極活物質間に緻密でより強固な導電ネットワークが形成される。
【0012】
本発明の一実施形態に係るアルカリ蓄電池用正極体の製造方法において、前記導電材の30at%(アトミック%)以上を、Co3O4として形成することを含むことが好ましい。この構成によれば、導電材が、高い導電性を有するCo3O4を主要な化合物として含むことになり、電池の内部抵抗が一層効果的に抑制される。
【0013】
また、本発明に係るアルカリ蓄電池用正極体は、ニッケル化合物を主成分とする活物質粒子と、この活物質粒子の表面に付着する、コバルト化合物を主成分とする導電材とを含み、この導電材の少なくとも一部が、粒径1〜3nmの粒子として形成されている。この構成によれば、コバルト化合物を主成分とする導電材の一部が、粒径1〜3mmの微粒子として存在することにより、活物質二次粒子表面において均一に分散すると同時に、二次粒子内部である一次粒子表面にも析出する。その結果、正極活物質間に緻密な導電ネットワークが形成されるので、当該正極が使用されるアルカリ蓄電池の内部抵抗上昇が抑制され、電池の性能が向上する。
【0014】
本発明の一実施形態に係るアルカリ蓄電池用正極体は、前記導電材の30at%以上がCo3O4として形成されていることが好ましい。この構成によれば、導電材が、高い導電性を有するCo3O4を主要な化合物として含んでいるので、電池の内部抵抗が一層効果的に抑制される。
【0015】
本発明に係るアルカリ蓄電池は、本発明に係る上記製造方法によって製造された正極体、もしくは本発明に係る上記正極体を備える。この構成によれば、正極の活物質粒子間に強固な導電ネットワークが形成されていることにより、充放電を繰り返しても電池の内部抵抗上昇が抑制されるので、電池性能、特には繰り返し充放電サイクル寿命が大幅に向上する。
【発明の効果】
【0016】
以上のように、本発明に係るアルカリ蓄電池用正極体によれば、導電材であるコバルト化合物が活物質粒子表面で微粉化して均一にコートされることにより、正極体の活物質粒子間に強固な導電ネットワークが形成されるので、この正極体が適用されるアルカリ蓄電池は、充放電サイクルが経過した後も低い内部抵抗を維持できる。
【図面の簡単な説明】
【0017】
【図1】本発明の一実施形態に係る正極体が適用されるアルカリ蓄電池を示す斜視図である。
【図2】図1の電池内部の電極体の構造を模式的に示す断面図である。
【図3】本発明の一実施形態に係る正極体を模式的に示す拡大図である。
【図4】本発明の効果を確認する試験における正極のTEM観察像である。
【図5】本発明の効果を確認する試験における正極のXPS測定結果を示すグラフである。
【図6】本発明の効果を確認する試験における正極のXRD解析結果を示すグラフである。
【図7】本発明の効果を確認する試験における正極のTEM観察像である。
【図8】インピーダンス解析に用いた等価回路を示す回路図である。
【図9】従来例に係る正極体のSEM観察像である。
【発明を実施するための形態】
【0018】
以下、本発明に係る実施形態を図面に従って説明するが、本発明はこの実施形態に限定されるものではない。
【0019】
図1は、本発明の一実施形態に係るアルカリ蓄電池用正極体を備える角形のアルカリ蓄電池(以下単に「電池」という)1の構造を示す斜視図である。本実施形態に係る電池1は、水酸化ニッケルを主要な正極活物質とし、水素吸蔵合金を主要な負極活物質とし、アルカリ系水溶液を電解液とするニッケル水素二次電池として構成されており、正極および負極の集電板を兼ねる矩形の第1蓋部材3および第2蓋部材5と、これら第1および第2蓋部材3,5間に介在する絶縁素材からなる枠形部材7によって、電池1の角形のケーシング9が構成されている。
【0020】
図2の断面図に模式的に示すように、ケーシング9の内方には、プリーツ状に折り曲げられたセパレータ11と、電極すなわち正極体13と負極体15とからなる電極ユニット17が収容されている。正極体13は、多孔質の発泡ニッケルからなる正極基板に正極合材を充填して形成されている。同様に、負極体15は、多孔質のパンチングメタルからなる負極基板に負極合材を充填して形成されている。
【0021】
正極体13と負極体15とは、両電極体13,15が対向する方向Xに、セパレータ11を介して交互に積層されている。このように構成されている電極ユニット17は、その積層方向Xと、第1および第2蓋部材3,5の対向方向Yとが直交するように、ケーシング9内に配置されている。
【0022】
なお、電池1は、本発明に係る正極体が使用されるニッケル水素二次電池の一例であり、本発明に係る正極体は、円筒形、角形等電池の形状を問わず、また、巻取り式、積層式等、電極体の構造を問わず使用することができる。
【0023】
正極基板,負極基板としては、導電性材料、具体的には、例えば、上述の発泡ニッケル、パンチングメタルなどの多孔質部材のほか、ニッケルめっきを施した鋼板のような平板状の部材を使用することができる。正極基板,負極基板に平板状の部材を使用する場合には、正極・負極の合材を充填する代わりに各基板上に合材を塗布する。この場合、正極および負極基板を形成する素材としては、ニッケルめっき鋼板のほかにも、電気化学的な特性や機械的強度、耐食性などを考慮して、適宜選択することができ、例えば、ニッケル板、ステンレス鋼板、銅めっき鋼板、銀めっき鋼板、コバルトめっき鋼板、クロムめっき鋼板などが好ましく用いられる。
【0024】
正極基板に充填される正極合材は、正極活物質である水酸化ニッケル、導電材およびバインダーを主成分とし、これらを混合して作製される。また、負極基板に充填される負極合材は、負極活物質である水素吸蔵合金、導電材およびバインダーを主成分とし、これらを混合して作製される。
【0025】
セパレータ11は、耐アルカリ系水溶液性を有する材料で形成されていることが好ましく、例えば、ポリエチレン繊維やポリプロピレン繊維などのポリオレフィン系繊維、ポリフェニレンサルファイド繊維、ポリフルオロエチレン系繊維、ポリアミド系繊維など、またはこれらに親水化処理を施したものを使用することができる。また、電解液としては、アルカリ系水溶液、例えば、KOH水溶液、NaOH水溶液、LiOH水溶液などを用いることができる。
【0026】
次に、本実施形態に係る正極体13の構成について詳しく説明する。
【0027】
上述のように、本実施形態の正極体13は、水酸化ニッケル(Ni(OH)2)を活物質として含み、さらにコバルト化合物を導電材として含んでいる。より具体的には、図3に模式的に示すように、電池1(図2)の正極体13において、活物質粒子31は、より微細な一次粒子が複数凝集した二次粒子として形成されており、水酸化ニッケルの活物質二次粒子31の表面および二次粒子内部である一次粒子の表面に、粒径約1〜3nmの微粒子として、コバルト化合物からなる導電材33が付着している。導電材33であるコバルト化合物の一部は、電池1のコバルトを高次に酸化させる前の状態において、金属コバルトの状態で存在している。導電材33は、活物質粒子31の表面に均一な分布で付着しており、この導電材33を介して各活物質粒子31が互いに接触することにより、正極活物質粒子31間に導電ネットワーク35が形成されている。
【0028】
次に、本実施形態に係る正極体13の製造方法を説明する。
【0029】
まず、表面に水酸化コバルト(Co(OH)2)をコートした水酸化ニッケル(Ni(OH)2)の粒子からなる粉末を、バインダーと共に溶剤に溶いてペースト状にし、多孔質の正極基板に充填したものを乾燥、圧延して正極素材を作製する(正極素材作製工程)。このようにして作製された正極素材におけるコバルト化合物中のコバルトの酸化数は0〜+3であり、好ましくは+2である。
【0030】
次に、上記のようにして作製した正極体に、還元電流を流す(正極還元工程)。正極素材に還元電流を流す方法としては、例えば下記のa)、b)に示す方法が考えられるが、正極素材に所望の条件で還元電流を流すことができれば、これらに限られない。本実施形態ではa)の方法によって正極素材に還元電流を流している。
a)容器に注入した電解液に正極素材と、白金、ニッケル、ステンレス鋼等からなる対極を浸漬して所定量の還元電流を流す。
b)図1に示した態様の電池を組み立てて、電解液を注入し、電池に所定量の還元電流を流す。
なお、方法b)によって正極還元工程を施す場合には、その後電池を解体して負極体15を新しいものに交換した後に、完成品としての電池1を再組立てしてもよい。
【0031】
方法b)においては、負極が酸化されて劣化が生じる場合があるので、再組立てを行うことにより劣化した負極を劣化していない負極に交換する。しかし、還元電流を流す条件によっては、劣化の度合いが無視できる程度に小さい場合もあるので、このような場合には、再組立てを行わずにそのまま完成品の電池とすることもできる。
【0032】
正極還元工程の通電条件は、正極素材中のコバルト化合物におけるコバルトを、酸化数+2よりも小さい状態にまで還元することができれば特に限定されないが、好ましくは、コバルト化合物におけるコバルトを、酸化数0の状態、つまり金属コバルトの状態にまで還元することが好ましい。このような操作を経ることで、導電材33の一部が溶解・分散した後、粒径1〜3nm程度の微粒子として析出することにより、導電材33が活物質粒子31の表面および内部にきわめて均一な分布で付着する。
【0033】
通電方式は、定電流、定電圧、定電力のいずれでもよく、その他の方法でもよい。定電流方式で通電する場合、通電電流値の好ましい範囲は5〜300mA/g−Ni(OH)2であり、より好ましい範囲は5〜100mA/g−Ni(OH)2である。一方、定電圧方式で通電する場合、通電電圧値の好ましい範囲は、参照極であるAg/AgCl電極に対して−0.1〜−3.0Vであり、より好ましい範囲は−0.5〜−1.8Vである。また、正極還元工程は常温下で行うことが可能である。正極還元工程を行う環境温度の好ましい範囲は、20〜40℃であり、より好ましくは25〜35℃である。
【0034】
また、正極還元工程は、電池1の製造における活性化工程の前に行われることが好ましい。電池の活性化工程とは、電池の組立て後に電池を活性化させるために充放電を所定回数行うことをいう。コバルトを高次に酸化して導電材33として作用させる活性化工程の前に、正極活物質粒子31の表面にコバルト化合物が均一にコートされるので、その後に行われる活性化工程において、きわめて強固な導電ネットワーク35が形成される。
【0035】
なお、正極における、活物質に対する導電材の添加量としては、正極活物質100重量部に対して、導電材5〜30重量部添加するのが好ましく、導電材8〜15重量部添加するのがより好ましい。導電材の添加割合がこれよりも小さい場合には、十分な導電補助効果が得られず、活物質の利用率が低くなる。一方、導電材の添加割合がこれより大きい場合には、十分な電池のエネルギー密度が得られない。
【0036】
本実施形態に係る正極体およびその製造方法によれば、以下の効果が得られる。
【0037】
本実施形態に係る正極体13においては、図3に模式的に示すように、コバルト化合物を主成分とする導電材33が、正極還元工程を経ることにより、活物質粒子31の表面において微粉化して均一にコートされる。その結果、正極活物質粒子31間に強固な導電ネットワーク35が形成されるので、当該正極体13が使用される電池1の内部抵抗上昇が抑制され、電池1の性能が向上する。
【0038】
本実施形態における正極体13の製造方法、特には正極還元工程によって、コバルト化合物が微粉化し、かつ高い伝導性を有することは、以下の効果確認試験によって確認されている。なお、効果確認試験では、これに先立って行ったサイクリックボルタンメトリー測定により、正極還元工程が、正極体13の水酸化ニッケルではなく導電材中のコバルトに作用していることが確認されたため、コバルトの状態を重点的に見るために、水酸化ニッケルを用いず水酸化コバルトのみで正極を作製して試験を行った。
【0039】
水酸化コバルトを主成分とする正極体、水素吸蔵合金からなる負極体、スルホン化ポリプロピレン製のセパレータおよび6M KOH水溶液からなる電解液を用いて試験セルを作製し、正極還元工程および電池の初期活性化工程を施した。また、比較用セルとして、正極還元工程を施さない点以外は上記試験セルと同様に作製したものを用意した。これらのセルについて、水酸化コバルト正極に対して定電流充電を行い、異なるSOCにおいて正極のTEM観察、XRD解析およびXPS解析を行った。
【0040】
効果確認試験により、以下のことが確認された。
(1)図4のTEM像に示すように、正極還元工程を施した後の水酸化コバルトバルク粒子表面に、粒径約1〜3nmの金属コバルトが形成される。このような微粒子が分散することにより、本実施形態に係る正極体13を使用したアルカリ蓄電池においては、正極活物質二次粒子内部の空隙にコバルト化合物が侵入し、二次粒子内部である一次粒子表面に析出する。
(2)正極に対して充電方向に通電し、電位が高くなっていくにつれて、図5に示すように、正極還元工程を経ていない水酸化コバルト粒子の表面にはCoOOHの存在のみが確認されるのに対して、正極還元工程を経た水酸化コバルト粒子表面には、高電位においてもCoOOHと共にCo3O4の存在が認められる。Co3O4のXRD回折ピークは高い導電性を示すスピネル構造のものと一致しており、正極還元工程を経た水酸化コバルト粒子表面では、金属Coが導電性の高いCo3O4を経由してCoOOHまで酸化されることが示唆される。
(3)図6に、粒子表面に存在するコバルト化合物の組成をXPSにより解析した結果を示す。図6において、(a)は正極還元工程を施した正極のXPSプロファイルであり、(b)が正極還元工程を施さなかった正極のXPSプロファイルである。この結果をまとめた下表1に示すように、正極還元工程を経たコバルト化合物においては、正極還元工程を経ていないものと比較して、充電後にCo3O4の組成比が高くなる。このことから、還元工程を経て微粉化し、分散したコバルトの多くは、充電後に導電性の高いCo3O4として存在していると考えられ、特にはCo3O4の組成比が30at%以上であることが好ましく、50at%以上であることがより好ましいことが示唆される。
【0041】
【表1】

【0042】
なお、上記(1)の現象は、次のような反応機構によるものと考えられる。正極還元工程を施していないCo(OH)2電極のTEM像は、図7(a)に示すように、六方晶であることが確認されたのに対して、正極還元工程を施した直後のCo(OH)2電極のTEM像は、図7(b)に示すように、六方晶が歪んだ形状であった。これは、下記の反応により、Co(OH)2が溶解(ヒドロキシ錯体が形成)したためと考えられる。
Co(OH)2 + 2OH− → Co(OH)42−
さらに、この反応により形成されたヒドロキシ錯体が、Co(OH)2バルク表面でCo(OH)2として再析出し、それが次式の反応により還元されるか、
Co(OH)2 + 2e− → Co + 2OH−
または、次式の反応によってヒドロキシ錯体が直接還元されることにより、金属コバルトが形成されたと考えられる。
Co(OH)42− + 2e− → Co + 4OH−
【0043】
以下の実施例により本発明をさらに具体的に説明するが、本発明はこれらに限定されるものではない。
【実施例】
【0044】
(試験電池の作製)
本発明の実施例に係る電池として、下記の仕様の試験電池(ニッケル水素二次電池)を作製した。
・電池容量:3.6Ah
・正極体:コバルトコート水酸化ニッケル(正極還元工程あり)
・負極活物質:AB5型水素吸蔵合金
・セパレータ:ポリオレフィン不織布
・電解液:KOH 6M/LiOH 0.4M 水溶液
また、比較例に係る電池として、正極体に正極還元工程を施さないこと以外は上記実施例に係る電池と同じ使用の電池を作製した。
【0045】
(充放電サイクル試験)
充放電サイクル試験の充放電条件は、下記のとおりである。
・電流値:42.7mA/g−Ni(OH)2
・充放電量:80%
この条件で充放電を繰り返し、0サイクル目(充放電試験開始前)の初期容量に対する、600サイクル目、1000サイクル目の容量維持率を測定した。
【0046】
さらに、0サイクル目、600サイクル目および1000サイクル目の反応抵抗を交流インピーダンスとして下記の条件で測定した。
・電圧:OCV(開回路電圧)±5mV
・測定周波数:100kHz〜50mHz
このインピーダンス解析に用いた等価回路を図8に示す。図8のR1はオーミック抵抗(溶液抵抗、接触抵抗など)に、R2+R3は反応抵抗に、W1は拡散抵抗に、CPE2,3は電極の静電容量成分に、それぞれ相当する。
【0047】
また、SPring-8 BL16B2にて、0.2Cでカットオフ電圧1Vまで全量放電して取り出した各電極についてXAFSで測定した。標準物質である水酸化ニッケルおよびオキシ水酸化ニッケルの測定結果との比較から、放電後の各電極に残っているオキシ水酸化ニッケル量を算出し、これを不活性ニッケル量とした。これらの試験結果を下表2に示す。
【0048】
【表2】

【0049】
表2から分かるように、比較例では1000サイクル目の容量維持率が79%であったのに対し、実施例では100%であり、優れた充放電サイクル寿命性能を示した。また、SOC10%という低い充電状態での反応抵抗が、比較例では600サイクル後に6.7mΩ、1000サイクル後に36.1mΩであったのに対して、実施例では600サイクル後に1.9mΩ、1000サイクル後に3.6mΩであり、大幅に改善されていた。さらには、比較例では充放電サイクル試験後に不活性なオキシ水酸化ニッケルが生成しているのに対して、実施例では不活性ニッケルの生成が大幅に抑制できていることが確認された。これらの測定結果から、実施例では、充放電サイクルを繰り返した後においても不活性ニッケルの生成が抑制されることにより放電末期の内部抵抗上昇が抑えられており、その結果として優れた充放電サイクル寿命性能が得られることが確認された。
【0050】
なお、本実施形態では、電池1をニッケル水素二次電池として構成した例について説明したが、本発明は、他の種類のアルカリ蓄電池に使用される電極にも適用することが可能である。例えば、正極としては空気電極や酸化銀電極、負極としてはカドミウム、亜鉛、鉄などを主要な活物質とする電極に適用することができる。
【0051】
以上のとおり、図面を参照しながら本発明の好適な実施形態を説明したが、本発明の趣旨を逸脱しない範囲内で、種々の追加、変更または削除が可能である。したがって、そのようなものも本発明の範囲内に含まれる。
【符号の説明】
【0052】
1 電池
13 正極体
31 正極活物質粒子
33 正極導電材
【技術分野】
【0001】
本発明は、主要な活物質として水酸化ニッケルを含み、導電材としてコバルト化合物を含むアルカリ蓄電池用の正極およびその製造方法に関する。
【背景技術】
【0002】
従来、主として携帯機器用の電源として使用する充放電可能な種々の二次電池が提案されてきた。さらに、近年、環境への配慮から、風力発電や太陽光発電のような自然エネルギーのロードレベリングや、自動車や電車などの車両の動力源に使用される大容量の二次電池が開発されている。自然エネルギー分野においては、主として、エネルギーの発生とその供給との平準化を図るために二次電池が用いられている。また、車両に二次電池を搭載した場合には、ブレーキ時に生じる回生電力をこの搭載電池に蓄えておき、車両の動力源として使用することができるので、車両の運行エネルギー効率を高めることができる。このような二次電池としては、エネルギー密度、負荷変動追従性、耐久性、製造コストなどの諸条件から、例えば、アルカリ蓄電池の一種であるニッケル水素二次電池が適しているとされる(例えば、特許文献1)。
【0003】
このような産業用に利用される二次電池には、きわめて高いレベルの耐久性が要求されるところ、ニッケル水素二次電池の充放電性能劣化の原因の一つとして、内部抵抗の増加が挙げられる。ニッケル水素二次電池の主たる正極活物質である水酸化ニッケル(Ni(OH)2)は、充電時に酸化されてオキシ水酸化ニッケル(NiOOH)になる。水酸化ニッケルが絶縁体であるのに対し、オキシ水酸化ニッケルは半導体であるため、電池の充電状態(SOC)が高いほど、電池の内部抵抗は低くなる。
【0004】
SOCが低い状態でも電極内の導電性を確保する必要があるため、導電材として水酸化コバルト(Co(OH)2)を添加したものが実用化されている(例えば、特許文献2)。この例では、図9に示すように、水酸化コバルトは、水酸化ニッケルの二次粒子表面をコーティングするように添加されており、電池の充電時に酸化されて導電性のあるオキシ水酸化コバルト(CoOOH)に変化する。なお、図9(a)の右下の像において、黒く写っている二次粒子の表面に存在する白く写っている部分がコバルト化合物である。また、図9(b)において、ほぼ球状の大径の粒子が二次粒子であり、その周囲に存在する粉砕された状態のものが一次粒子である。電池の通常の使用電圧範囲において、オキシ水酸化コバルトは還元されずに残るので、SOCが低い状態でも、ある程度の導電性を確保することができる。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2007−157479号公報
【特許文献2】特開2003−257425号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかし、上記の正極では、活物質である水酸化ニッケルの粒子表面に付着するコバルト化合物が粒子表面上で均一に分布していないので、活物質粒子間に形成される導電ネットワークの安定性が不十分であり、電池の充放電サイクルが進むにつれ、活物質粒子間の導電ネットワークが崩れてくる。その結果、SOCの低い領域において内部抵抗が増大し、これにより十分な繰り返し充放電サイクル寿命が得られない。
【0007】
本発明の目的は、上記の課題を解決するために、正極活物質粒子の表面において導電材を均一にコートして活物質粒子間に強固な導電ネットワークを形成することにより、適用される電池の内部抵抗上昇が抑制されるアルカリ蓄電池用正極体およびその製造方法を提供することにある。
【課題を解決するための手段】
【0008】
前記した目的を達成するために、本発明に係るアルカリ蓄電池用正極体の製造方法は、ニッケル化合物を主成分とする活物質粒子と、この活物質粒子の表面に付着する、コバルト化合物を主成分とする導電材とを含む正極体に還元電流を流す工程を含む。
【0009】
この構成によれば、導電材であるコバルト化合物の一部が還元電流によって溶解・分散し、還元析出される。その結果、前記導電材が粒径1〜3nmの微粒子として、活物質粒子表面に均一に分散し、正極活物質間に強固な導電ネットワークが形成されるので、当該正極体が使用されるアルカリ蓄電池の内部抵抗上昇が抑制され、電池の性能が向上する。
【0010】
本発明の一実施形態に係るアルカリ蓄電池用正極体の製造方法において、当該アルカリ蓄電池の活性化の前に前記還元電流を流すことが好ましい。この構成によれば、コバルトを高次に酸化して導電材として作用させる活性化工程の前に、正極活物質粒子の表面にコバルト化合物が均一にコートされるので、その後に行われる活性化工程においてきわめて強固な導電ネットワークが形成される。
【0011】
本発明の一実施形態に係るアルカリ蓄電池用正極体の製造方法において、前記導電材の少なくとも一部を、活物質一次粒子表面である活物質二次粒子内部に析出させることを含むことが好ましい。すなわち、前記活物質粒子は、より微細な一次粒子が複数凝集した二次粒子として形成されており、上記構成によれば、一次粒子表面に導電材が均一に析出することにより、導電材が活物質二次粒子内部にまで均一に分散する。これにより、正極活物質間に緻密でより強固な導電ネットワークが形成される。
【0012】
本発明の一実施形態に係るアルカリ蓄電池用正極体の製造方法において、前記導電材の30at%(アトミック%)以上を、Co3O4として形成することを含むことが好ましい。この構成によれば、導電材が、高い導電性を有するCo3O4を主要な化合物として含むことになり、電池の内部抵抗が一層効果的に抑制される。
【0013】
また、本発明に係るアルカリ蓄電池用正極体は、ニッケル化合物を主成分とする活物質粒子と、この活物質粒子の表面に付着する、コバルト化合物を主成分とする導電材とを含み、この導電材の少なくとも一部が、粒径1〜3nmの粒子として形成されている。この構成によれば、コバルト化合物を主成分とする導電材の一部が、粒径1〜3mmの微粒子として存在することにより、活物質二次粒子表面において均一に分散すると同時に、二次粒子内部である一次粒子表面にも析出する。その結果、正極活物質間に緻密な導電ネットワークが形成されるので、当該正極が使用されるアルカリ蓄電池の内部抵抗上昇が抑制され、電池の性能が向上する。
【0014】
本発明の一実施形態に係るアルカリ蓄電池用正極体は、前記導電材の30at%以上がCo3O4として形成されていることが好ましい。この構成によれば、導電材が、高い導電性を有するCo3O4を主要な化合物として含んでいるので、電池の内部抵抗が一層効果的に抑制される。
【0015】
本発明に係るアルカリ蓄電池は、本発明に係る上記製造方法によって製造された正極体、もしくは本発明に係る上記正極体を備える。この構成によれば、正極の活物質粒子間に強固な導電ネットワークが形成されていることにより、充放電を繰り返しても電池の内部抵抗上昇が抑制されるので、電池性能、特には繰り返し充放電サイクル寿命が大幅に向上する。
【発明の効果】
【0016】
以上のように、本発明に係るアルカリ蓄電池用正極体によれば、導電材であるコバルト化合物が活物質粒子表面で微粉化して均一にコートされることにより、正極体の活物質粒子間に強固な導電ネットワークが形成されるので、この正極体が適用されるアルカリ蓄電池は、充放電サイクルが経過した後も低い内部抵抗を維持できる。
【図面の簡単な説明】
【0017】
【図1】本発明の一実施形態に係る正極体が適用されるアルカリ蓄電池を示す斜視図である。
【図2】図1の電池内部の電極体の構造を模式的に示す断面図である。
【図3】本発明の一実施形態に係る正極体を模式的に示す拡大図である。
【図4】本発明の効果を確認する試験における正極のTEM観察像である。
【図5】本発明の効果を確認する試験における正極のXPS測定結果を示すグラフである。
【図6】本発明の効果を確認する試験における正極のXRD解析結果を示すグラフである。
【図7】本発明の効果を確認する試験における正極のTEM観察像である。
【図8】インピーダンス解析に用いた等価回路を示す回路図である。
【図9】従来例に係る正極体のSEM観察像である。
【発明を実施するための形態】
【0018】
以下、本発明に係る実施形態を図面に従って説明するが、本発明はこの実施形態に限定されるものではない。
【0019】
図1は、本発明の一実施形態に係るアルカリ蓄電池用正極体を備える角形のアルカリ蓄電池(以下単に「電池」という)1の構造を示す斜視図である。本実施形態に係る電池1は、水酸化ニッケルを主要な正極活物質とし、水素吸蔵合金を主要な負極活物質とし、アルカリ系水溶液を電解液とするニッケル水素二次電池として構成されており、正極および負極の集電板を兼ねる矩形の第1蓋部材3および第2蓋部材5と、これら第1および第2蓋部材3,5間に介在する絶縁素材からなる枠形部材7によって、電池1の角形のケーシング9が構成されている。
【0020】
図2の断面図に模式的に示すように、ケーシング9の内方には、プリーツ状に折り曲げられたセパレータ11と、電極すなわち正極体13と負極体15とからなる電極ユニット17が収容されている。正極体13は、多孔質の発泡ニッケルからなる正極基板に正極合材を充填して形成されている。同様に、負極体15は、多孔質のパンチングメタルからなる負極基板に負極合材を充填して形成されている。
【0021】
正極体13と負極体15とは、両電極体13,15が対向する方向Xに、セパレータ11を介して交互に積層されている。このように構成されている電極ユニット17は、その積層方向Xと、第1および第2蓋部材3,5の対向方向Yとが直交するように、ケーシング9内に配置されている。
【0022】
なお、電池1は、本発明に係る正極体が使用されるニッケル水素二次電池の一例であり、本発明に係る正極体は、円筒形、角形等電池の形状を問わず、また、巻取り式、積層式等、電極体の構造を問わず使用することができる。
【0023】
正極基板,負極基板としては、導電性材料、具体的には、例えば、上述の発泡ニッケル、パンチングメタルなどの多孔質部材のほか、ニッケルめっきを施した鋼板のような平板状の部材を使用することができる。正極基板,負極基板に平板状の部材を使用する場合には、正極・負極の合材を充填する代わりに各基板上に合材を塗布する。この場合、正極および負極基板を形成する素材としては、ニッケルめっき鋼板のほかにも、電気化学的な特性や機械的強度、耐食性などを考慮して、適宜選択することができ、例えば、ニッケル板、ステンレス鋼板、銅めっき鋼板、銀めっき鋼板、コバルトめっき鋼板、クロムめっき鋼板などが好ましく用いられる。
【0024】
正極基板に充填される正極合材は、正極活物質である水酸化ニッケル、導電材およびバインダーを主成分とし、これらを混合して作製される。また、負極基板に充填される負極合材は、負極活物質である水素吸蔵合金、導電材およびバインダーを主成分とし、これらを混合して作製される。
【0025】
セパレータ11は、耐アルカリ系水溶液性を有する材料で形成されていることが好ましく、例えば、ポリエチレン繊維やポリプロピレン繊維などのポリオレフィン系繊維、ポリフェニレンサルファイド繊維、ポリフルオロエチレン系繊維、ポリアミド系繊維など、またはこれらに親水化処理を施したものを使用することができる。また、電解液としては、アルカリ系水溶液、例えば、KOH水溶液、NaOH水溶液、LiOH水溶液などを用いることができる。
【0026】
次に、本実施形態に係る正極体13の構成について詳しく説明する。
【0027】
上述のように、本実施形態の正極体13は、水酸化ニッケル(Ni(OH)2)を活物質として含み、さらにコバルト化合物を導電材として含んでいる。より具体的には、図3に模式的に示すように、電池1(図2)の正極体13において、活物質粒子31は、より微細な一次粒子が複数凝集した二次粒子として形成されており、水酸化ニッケルの活物質二次粒子31の表面および二次粒子内部である一次粒子の表面に、粒径約1〜3nmの微粒子として、コバルト化合物からなる導電材33が付着している。導電材33であるコバルト化合物の一部は、電池1のコバルトを高次に酸化させる前の状態において、金属コバルトの状態で存在している。導電材33は、活物質粒子31の表面に均一な分布で付着しており、この導電材33を介して各活物質粒子31が互いに接触することにより、正極活物質粒子31間に導電ネットワーク35が形成されている。
【0028】
次に、本実施形態に係る正極体13の製造方法を説明する。
【0029】
まず、表面に水酸化コバルト(Co(OH)2)をコートした水酸化ニッケル(Ni(OH)2)の粒子からなる粉末を、バインダーと共に溶剤に溶いてペースト状にし、多孔質の正極基板に充填したものを乾燥、圧延して正極素材を作製する(正極素材作製工程)。このようにして作製された正極素材におけるコバルト化合物中のコバルトの酸化数は0〜+3であり、好ましくは+2である。
【0030】
次に、上記のようにして作製した正極体に、還元電流を流す(正極還元工程)。正極素材に還元電流を流す方法としては、例えば下記のa)、b)に示す方法が考えられるが、正極素材に所望の条件で還元電流を流すことができれば、これらに限られない。本実施形態ではa)の方法によって正極素材に還元電流を流している。
a)容器に注入した電解液に正極素材と、白金、ニッケル、ステンレス鋼等からなる対極を浸漬して所定量の還元電流を流す。
b)図1に示した態様の電池を組み立てて、電解液を注入し、電池に所定量の還元電流を流す。
なお、方法b)によって正極還元工程を施す場合には、その後電池を解体して負極体15を新しいものに交換した後に、完成品としての電池1を再組立てしてもよい。
【0031】
方法b)においては、負極が酸化されて劣化が生じる場合があるので、再組立てを行うことにより劣化した負極を劣化していない負極に交換する。しかし、還元電流を流す条件によっては、劣化の度合いが無視できる程度に小さい場合もあるので、このような場合には、再組立てを行わずにそのまま完成品の電池とすることもできる。
【0032】
正極還元工程の通電条件は、正極素材中のコバルト化合物におけるコバルトを、酸化数+2よりも小さい状態にまで還元することができれば特に限定されないが、好ましくは、コバルト化合物におけるコバルトを、酸化数0の状態、つまり金属コバルトの状態にまで還元することが好ましい。このような操作を経ることで、導電材33の一部が溶解・分散した後、粒径1〜3nm程度の微粒子として析出することにより、導電材33が活物質粒子31の表面および内部にきわめて均一な分布で付着する。
【0033】
通電方式は、定電流、定電圧、定電力のいずれでもよく、その他の方法でもよい。定電流方式で通電する場合、通電電流値の好ましい範囲は5〜300mA/g−Ni(OH)2であり、より好ましい範囲は5〜100mA/g−Ni(OH)2である。一方、定電圧方式で通電する場合、通電電圧値の好ましい範囲は、参照極であるAg/AgCl電極に対して−0.1〜−3.0Vであり、より好ましい範囲は−0.5〜−1.8Vである。また、正極還元工程は常温下で行うことが可能である。正極還元工程を行う環境温度の好ましい範囲は、20〜40℃であり、より好ましくは25〜35℃である。
【0034】
また、正極還元工程は、電池1の製造における活性化工程の前に行われることが好ましい。電池の活性化工程とは、電池の組立て後に電池を活性化させるために充放電を所定回数行うことをいう。コバルトを高次に酸化して導電材33として作用させる活性化工程の前に、正極活物質粒子31の表面にコバルト化合物が均一にコートされるので、その後に行われる活性化工程において、きわめて強固な導電ネットワーク35が形成される。
【0035】
なお、正極における、活物質に対する導電材の添加量としては、正極活物質100重量部に対して、導電材5〜30重量部添加するのが好ましく、導電材8〜15重量部添加するのがより好ましい。導電材の添加割合がこれよりも小さい場合には、十分な導電補助効果が得られず、活物質の利用率が低くなる。一方、導電材の添加割合がこれより大きい場合には、十分な電池のエネルギー密度が得られない。
【0036】
本実施形態に係る正極体およびその製造方法によれば、以下の効果が得られる。
【0037】
本実施形態に係る正極体13においては、図3に模式的に示すように、コバルト化合物を主成分とする導電材33が、正極還元工程を経ることにより、活物質粒子31の表面において微粉化して均一にコートされる。その結果、正極活物質粒子31間に強固な導電ネットワーク35が形成されるので、当該正極体13が使用される電池1の内部抵抗上昇が抑制され、電池1の性能が向上する。
【0038】
本実施形態における正極体13の製造方法、特には正極還元工程によって、コバルト化合物が微粉化し、かつ高い伝導性を有することは、以下の効果確認試験によって確認されている。なお、効果確認試験では、これに先立って行ったサイクリックボルタンメトリー測定により、正極還元工程が、正極体13の水酸化ニッケルではなく導電材中のコバルトに作用していることが確認されたため、コバルトの状態を重点的に見るために、水酸化ニッケルを用いず水酸化コバルトのみで正極を作製して試験を行った。
【0039】
水酸化コバルトを主成分とする正極体、水素吸蔵合金からなる負極体、スルホン化ポリプロピレン製のセパレータおよび6M KOH水溶液からなる電解液を用いて試験セルを作製し、正極還元工程および電池の初期活性化工程を施した。また、比較用セルとして、正極還元工程を施さない点以外は上記試験セルと同様に作製したものを用意した。これらのセルについて、水酸化コバルト正極に対して定電流充電を行い、異なるSOCにおいて正極のTEM観察、XRD解析およびXPS解析を行った。
【0040】
効果確認試験により、以下のことが確認された。
(1)図4のTEM像に示すように、正極還元工程を施した後の水酸化コバルトバルク粒子表面に、粒径約1〜3nmの金属コバルトが形成される。このような微粒子が分散することにより、本実施形態に係る正極体13を使用したアルカリ蓄電池においては、正極活物質二次粒子内部の空隙にコバルト化合物が侵入し、二次粒子内部である一次粒子表面に析出する。
(2)正極に対して充電方向に通電し、電位が高くなっていくにつれて、図5に示すように、正極還元工程を経ていない水酸化コバルト粒子の表面にはCoOOHの存在のみが確認されるのに対して、正極還元工程を経た水酸化コバルト粒子表面には、高電位においてもCoOOHと共にCo3O4の存在が認められる。Co3O4のXRD回折ピークは高い導電性を示すスピネル構造のものと一致しており、正極還元工程を経た水酸化コバルト粒子表面では、金属Coが導電性の高いCo3O4を経由してCoOOHまで酸化されることが示唆される。
(3)図6に、粒子表面に存在するコバルト化合物の組成をXPSにより解析した結果を示す。図6において、(a)は正極還元工程を施した正極のXPSプロファイルであり、(b)が正極還元工程を施さなかった正極のXPSプロファイルである。この結果をまとめた下表1に示すように、正極還元工程を経たコバルト化合物においては、正極還元工程を経ていないものと比較して、充電後にCo3O4の組成比が高くなる。このことから、還元工程を経て微粉化し、分散したコバルトの多くは、充電後に導電性の高いCo3O4として存在していると考えられ、特にはCo3O4の組成比が30at%以上であることが好ましく、50at%以上であることがより好ましいことが示唆される。
【0041】
【表1】

【0042】
なお、上記(1)の現象は、次のような反応機構によるものと考えられる。正極還元工程を施していないCo(OH)2電極のTEM像は、図7(a)に示すように、六方晶であることが確認されたのに対して、正極還元工程を施した直後のCo(OH)2電極のTEM像は、図7(b)に示すように、六方晶が歪んだ形状であった。これは、下記の反応により、Co(OH)2が溶解(ヒドロキシ錯体が形成)したためと考えられる。
Co(OH)2 + 2OH− → Co(OH)42−
さらに、この反応により形成されたヒドロキシ錯体が、Co(OH)2バルク表面でCo(OH)2として再析出し、それが次式の反応により還元されるか、
Co(OH)2 + 2e− → Co + 2OH−
または、次式の反応によってヒドロキシ錯体が直接還元されることにより、金属コバルトが形成されたと考えられる。
Co(OH)42− + 2e− → Co + 4OH−
【0043】
以下の実施例により本発明をさらに具体的に説明するが、本発明はこれらに限定されるものではない。
【実施例】
【0044】
(試験電池の作製)
本発明の実施例に係る電池として、下記の仕様の試験電池(ニッケル水素二次電池)を作製した。
・電池容量:3.6Ah
・正極体:コバルトコート水酸化ニッケル(正極還元工程あり)
・負極活物質:AB5型水素吸蔵合金
・セパレータ:ポリオレフィン不織布
・電解液:KOH 6M/LiOH 0.4M 水溶液
また、比較例に係る電池として、正極体に正極還元工程を施さないこと以外は上記実施例に係る電池と同じ使用の電池を作製した。
【0045】
(充放電サイクル試験)
充放電サイクル試験の充放電条件は、下記のとおりである。
・電流値:42.7mA/g−Ni(OH)2
・充放電量:80%
この条件で充放電を繰り返し、0サイクル目(充放電試験開始前)の初期容量に対する、600サイクル目、1000サイクル目の容量維持率を測定した。
【0046】
さらに、0サイクル目、600サイクル目および1000サイクル目の反応抵抗を交流インピーダンスとして下記の条件で測定した。
・電圧:OCV(開回路電圧)±5mV
・測定周波数:100kHz〜50mHz
このインピーダンス解析に用いた等価回路を図8に示す。図8のR1はオーミック抵抗(溶液抵抗、接触抵抗など)に、R2+R3は反応抵抗に、W1は拡散抵抗に、CPE2,3は電極の静電容量成分に、それぞれ相当する。
【0047】
また、SPring-8 BL16B2にて、0.2Cでカットオフ電圧1Vまで全量放電して取り出した各電極についてXAFSで測定した。標準物質である水酸化ニッケルおよびオキシ水酸化ニッケルの測定結果との比較から、放電後の各電極に残っているオキシ水酸化ニッケル量を算出し、これを不活性ニッケル量とした。これらの試験結果を下表2に示す。
【0048】
【表2】

【0049】
表2から分かるように、比較例では1000サイクル目の容量維持率が79%であったのに対し、実施例では100%であり、優れた充放電サイクル寿命性能を示した。また、SOC10%という低い充電状態での反応抵抗が、比較例では600サイクル後に6.7mΩ、1000サイクル後に36.1mΩであったのに対して、実施例では600サイクル後に1.9mΩ、1000サイクル後に3.6mΩであり、大幅に改善されていた。さらには、比較例では充放電サイクル試験後に不活性なオキシ水酸化ニッケルが生成しているのに対して、実施例では不活性ニッケルの生成が大幅に抑制できていることが確認された。これらの測定結果から、実施例では、充放電サイクルを繰り返した後においても不活性ニッケルの生成が抑制されることにより放電末期の内部抵抗上昇が抑えられており、その結果として優れた充放電サイクル寿命性能が得られることが確認された。
【0050】
なお、本実施形態では、電池1をニッケル水素二次電池として構成した例について説明したが、本発明は、他の種類のアルカリ蓄電池に使用される電極にも適用することが可能である。例えば、正極としては空気電極や酸化銀電極、負極としてはカドミウム、亜鉛、鉄などを主要な活物質とする電極に適用することができる。
【0051】
以上のとおり、図面を参照しながら本発明の好適な実施形態を説明したが、本発明の趣旨を逸脱しない範囲内で、種々の追加、変更または削除が可能である。したがって、そのようなものも本発明の範囲内に含まれる。
【符号の説明】
【0052】
1 電池
13 正極体
31 正極活物質粒子
33 正極導電材
【特許請求の範囲】
【請求項1】
アルカリ蓄電池に使用される正極体を製造する方法であって、
ニッケル化合物を主成分とする活物質粒子と、この活物質粒子の表面に付着する、コバルト化合物を主成分とする導電材とを含む正極体に還元電流を流す工程を含む、
アルカリ蓄電池用正極体の製造方法。
【請求項2】
請求項1において、当該アルカリ蓄電池の活性化の前に前記還元電流を流すアルカリ蓄電池用正極体の製造方法。
【請求項3】
請求項1または2において、前記導電材の少なくとも一部を粒径1〜3nmの粒子として形成することを含む、アルカリ蓄電池用正極体の製造方法。
【請求項4】
請求項1〜3のいずれか一項において、前記導電材の少なくとも一部を、活物質一次粒子表面である活物質二次粒子内部に析出させることを含む、アルカリ蓄電池用正極体の製造方法。
【請求項5】
請求項1〜4のいずれか一項において、前記導電材の30at%以上をCo3O4として形成することを含むアルカリ蓄電池用正極体の製造方法。
【請求項6】
アルカリ蓄電池に使用される正極体であって、ニッケル化合物を主成分とする活物質粒子と、この活物質粒子の表面に付着する、コバルト化合物を主成分とする導電材とを含み、この導電材の少なくとも一部が、粒径1〜3nmの粒子として形成されているアルカリ蓄電池用正極体。
【請求項7】
請求項6において、前記導電材の少なくとも一部が、活物質一次粒子表面である活物質二次粒子内部に存在しているアルカリ蓄電池用正極体。
【請求項8】
請求項6または7において、前記導電材の30at%以上がCo3O4からなるアルカリ蓄電池用正極体。
【請求項9】
請求項1〜5のいずれか一項に記載の製造方法によって製造された正極体、もしくは請求項6〜8のいずれか一項に記載の正極体を備えるアルカリ蓄電池。
【請求項1】
アルカリ蓄電池に使用される正極体を製造する方法であって、
ニッケル化合物を主成分とする活物質粒子と、この活物質粒子の表面に付着する、コバルト化合物を主成分とする導電材とを含む正極体に還元電流を流す工程を含む、
アルカリ蓄電池用正極体の製造方法。
【請求項2】
請求項1において、当該アルカリ蓄電池の活性化の前に前記還元電流を流すアルカリ蓄電池用正極体の製造方法。
【請求項3】
請求項1または2において、前記導電材の少なくとも一部を粒径1〜3nmの粒子として形成することを含む、アルカリ蓄電池用正極体の製造方法。
【請求項4】
請求項1〜3のいずれか一項において、前記導電材の少なくとも一部を、活物質一次粒子表面である活物質二次粒子内部に析出させることを含む、アルカリ蓄電池用正極体の製造方法。
【請求項5】
請求項1〜4のいずれか一項において、前記導電材の30at%以上をCo3O4として形成することを含むアルカリ蓄電池用正極体の製造方法。
【請求項6】
アルカリ蓄電池に使用される正極体であって、ニッケル化合物を主成分とする活物質粒子と、この活物質粒子の表面に付着する、コバルト化合物を主成分とする導電材とを含み、この導電材の少なくとも一部が、粒径1〜3nmの粒子として形成されているアルカリ蓄電池用正極体。
【請求項7】
請求項6において、前記導電材の少なくとも一部が、活物質一次粒子表面である活物質二次粒子内部に存在しているアルカリ蓄電池用正極体。
【請求項8】
請求項6または7において、前記導電材の30at%以上がCo3O4からなるアルカリ蓄電池用正極体。
【請求項9】
請求項1〜5のいずれか一項に記載の製造方法によって製造された正極体、もしくは請求項6〜8のいずれか一項に記載の正極体を備えるアルカリ蓄電池。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図8】


【図9】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図8】


【図9】


【図7】


【公開番号】特開2012−99232(P2012−99232A)
【公開日】平成24年5月24日(2012.5.24)
【国際特許分類】
【出願番号】特願2010−243488(P2010−243488)
【出願日】平成22年10月29日(2010.10.29)
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成21年度独立行政法人新エネルギー・産業技術総合開発機構系統連系円滑化蓄電システム技術開発委託研究、産業技術力強化法第19条の適用を受ける特許出願
【出願人】(000000974)川崎重工業株式会社 (1,710)
【Fターム(参考)】
【公開日】平成24年5月24日(2012.5.24)
【国際特許分類】
【出願日】平成22年10月29日(2010.10.29)
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成21年度独立行政法人新エネルギー・産業技術総合開発機構系統連系円滑化蓄電システム技術開発委託研究、産業技術力強化法第19条の適用を受ける特許出願
【出願人】(000000974)川崎重工業株式会社 (1,710)
【Fターム(参考)】
[ Back to top ]

