アルカリ金属ケイ酸塩及び遷移金属を含むアルカリ金属ケイ酸塩の合成方法、並びにアルカリ金属ケイ酸塩及び遷移金属を含むアルカリ金属ケイ酸塩
【課題】微粒子化が容易なアルカリ金属ケイ酸塩の合成方法を提供すること、また、当該アルカリ金属ケイ酸塩を用いて遷移金属を含むアルカリ金属ケイ酸塩の合成方法を提供することである。
【解決手段】アルカリ金属塩を含む塩基性溶液を作製し、アルカリ金属塩を含む塩基性溶液とシリコン粒子を混合してアルカリ金属ケイ酸塩を含む塩基性溶液を作製し、アルカリ金属ケイ酸塩を含む塩基性溶液を当該アルカリ金属ケイ酸塩の貧溶媒に加えて、アルカリ金属ケイ酸塩を析出させてアルカリ金属ケイ酸塩を合成する。また、当該アルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合して混合物を作製し、混合物に加熱処理を行い、遷移金属を含むアルカリ金属ケイ酸塩を生成する。
【解決手段】アルカリ金属塩を含む塩基性溶液を作製し、アルカリ金属塩を含む塩基性溶液とシリコン粒子を混合してアルカリ金属ケイ酸塩を含む塩基性溶液を作製し、アルカリ金属ケイ酸塩を含む塩基性溶液を当該アルカリ金属ケイ酸塩の貧溶媒に加えて、アルカリ金属ケイ酸塩を析出させてアルカリ金属ケイ酸塩を合成する。また、当該アルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合して混合物を作製し、混合物に加熱処理を行い、遷移金属を含むアルカリ金属ケイ酸塩を生成する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、遷移金属を含むアルカリ金属ケイ酸塩の合成方法と、当該合成方法により作製された遷移金属を含むアルカリ金属ケイ酸塩に関する。
【0002】
また、遷移金属を含むアルカリ金属ケイ酸塩を正極活物質とした正極と、その作製方法に関する。また、当該正極を備えた蓄電装置と、その蓄電装置作製方法に関する。なお、本明細書において蓄電装置とは、蓄電機能を有する素子及び装置全般を指すものである。
【背景技術】
【0003】
近年、リチウム二次電池、リチウムイオンキャパシタなど蓄電装置の開発が行われている。
【0004】
特に、ケイ酸リチウムなどのアルカリ金属ケイ酸塩は、リチウム二次電池等の蓄電装置の正極活物質である、遷移金属を含むケイ酸リチウム塩を合成する際の前駆体となり得る(特許文献1参照)。
【0005】
例えば、遷移金属Mを含むアルカリ金属塩であるリチウムリン酸塩(LiMPO4)及びリチウムケイ酸塩(Li2MSiO4)は、次世代の正極活物質として提案されている。なお、当該遷移金属Mとしては、例えば、鉄(Fe)、マンガン(Mn)、ニッケル(Ni)、又はコバルト(Co)などである。
【0006】
上記LiMPO4及び上記Li2MSiO4は、汎用されている正極活物質であるLiCoO2のような酸化物に比べて、熱安定性が高く、リチウム二次電池の温度が異常上昇した場合でも酸素ガスの発生を抑制でき、引火性電解質の酸化発熱反応を抑制できる。
【0007】
上記LiMPO4は、リチウムイオンの挿入及び脱離が1電子反応によって行われ、LiMPO4の理論容量は約170mAh/gである。一方、Li2MSiO4は、リチウムイオンの挿入及び脱離が2電子反応によって行われることから、Li2MSiO4の理論容量は約330mAh/gと高容量である。それゆえ、Li2MSiO4を正極活物質に用いることで高容量な正極を作製できることが知られている。
【0008】
従来、Li2MSiO4は固相反応よる合成が一般的である。典型的な固相反応法は、各構成元素の供給源となる化合物をボールミルで長時間混合する工程と、650℃以上、さらには1000℃を超える温度で半日以上の加熱処理を複数回行う工程を有する(特許文献2参照)。
【0009】
そして、固相反応により合成した正極活物質を用いて正極を作製する場合、合成した正極活物質を粉砕し、その粉砕した正極活物質を用いて正極を作製する方法が採用されている(特許文献1参照)。
【先行技術文献】
【特許文献】
【0010】
【特許文献1】特開2009−104794号公報
【特許文献2】特開2007−335325号公報
【発明の概要】
【発明が解決しようとする課題】
【0011】
しかし、現状では、正極活物質にLi2MSiO4を用いた際、Li2MSiO4の理論容量に到達するような十分な容量を得ることは難しいとされている。これは、Li2MSiO4はリチウムイオンの拡散性が悪いためである。正極活物質を微粒子化することで、リチウムイオンの拡散距離を短くでき、リチウムイオンの拡散性を向上させることができるが、Li2MSiO4は上記のように固相反応よる合成が一般的であるため、微粒子化が難しい。
【0012】
さらに、従来の固相反応は長時間の加熱処理を伴うので、合成した正極活物質の粒子サイズが増大するという問題がある。このように粒子サイズが増大した正極活物質を用いて正極を作製すると、正極重量あたりの容量が低くなるため、高容量なリチウム二次電池の作製が難しくなる。
【0013】
それゆえ、従来から固相反応によって合成した正極活物質を機械的に粉砕することで粒子サイズを小さくする処理(微粒子化)を行い、その微粒子化した正極活物質を用いて正極を作製する手段が汎用されている。しかし、機械的な粉砕では、小さくできる粒子サイズに下限がある。さらに、機械的な粉砕でも長時間の処理を行えば、粒子サイズを均一にすることが可能であるといえるが、短時間で粒子サイズを均一することは難しい。
【0014】
そこで、本発明の一態様は、蓄電装置の正極活物質として機能し、微粒子化が容易な遷移金属を含むアルカリ金属ケイ酸塩の合成方法を提供することを課題とする。
【0015】
また、本発明の一態様は、上記合成方法を用いて作製した遷移金属を含むアルカリ金属ケイ酸塩を提供することを課題とする。
【0016】
さらに、本発明の一態様は、上記遷移金属を含むアルカリ金属ケイ酸塩の前駆体であるアルカリ金属ケイ酸塩の合成方法、及び当該合成方法を用いて作製したアルカリ金属ケイ酸塩を提供することも課題とする。
【課題を解決するための手段】
【0017】
本発明の一態様は、アルカリ金属塩を含む塩基性溶液を作製し、アルカリ金属塩を含む塩基性溶液とシリコン粒子を混合してアルカリ金属ケイ酸塩を含む塩基性溶液を作製し、アルカリ金属ケイ酸塩を含む塩基性溶液を当該アルカリ金属ケイ酸塩の貧溶媒に加えて、アルカリ金属ケイ酸塩を析出させることを特徴とする、アルカリ金属ケイ酸塩の合成方法である。
【0018】
また、上記したアルカリ金属ケイ酸塩の合成方法において、析出させたアルカリ金属ケイ酸塩を回収し、回収したアルカリ金属ケイ酸塩に加熱処理を行ってもよい。
【0019】
本発明の一態様は、アルカリ金属塩を含む塩基性溶液を作製し、アルカリ金属塩を含む塩基性溶液とシリコン粒子を混合してアルカリ金属ケイ酸塩を含む塩基性溶液を作製し、アルカリ金属ケイ酸塩を含む塩基性溶液を当該アルカリ金属ケイ酸塩の貧溶媒に加えて、アルカリ金属ケイ酸塩を析出させ、析出させたアルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合して混合物を作製し、混合物に加熱処理を行い、遷移金属を含むアルカリ金属ケイ酸塩を生成することを特徴とする、遷移金属を含むアルカリ金属ケイ酸塩の合成方法である。
【0020】
また、上記した遷移金属を含むアルカリ金属ケイ酸塩の合成方法において、析出させたアルカリ金属ケイ酸塩を回収し、回収したアルカリ金属ケイ酸塩に第1の加熱処理を行い、加熱処理したアルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合して混合物を作製し、混合物に第2の加熱処理を行って、遷移金属を含むアルカリ金属ケイ酸塩を生成してもよい。
【0021】
アルカリ金属塩を含む塩基性溶液は、pHが9以上であることが好ましい。また、貧溶媒に加えるアルカリ金属ケイ酸塩を含む塩基性溶液は、pHが9以上であることが好ましい。
【0022】
アルカリ金属塩を含む塩基性溶液の温度は、50℃以上70℃以下に保持することが好ましい。
【0023】
アルカリ金属ケイ酸塩の1つであるケイ酸リチウムの合成は、アルカリ金属塩を含む塩基性溶液を水酸化リチウム水溶液とし、貧溶媒は直鎖アルコール又はアセトンとすることで実施できる。
【0024】
上記したアルカリ金属ケイ酸塩の合成方法を用いることで、気体吸着法で測定される比表面積が50m2/g以上90m2/g以下であるアルカリ金属ケイ酸塩を合成することができる。
【0025】
また、上記したアルカリ金属ケイ酸塩の合成方法を用いることで、X線光電子分光法によって定量される炭素原子が10atom%以下であり、X線光電子分光法によって定量されるナトリウム原子が1atom%以下であるとするアルカリ金属ケイ酸塩を合成することができる。
【0026】
遷移金属を含むアルカリ金属ケイ酸塩の合成方法において、微粒子化した遷移金属を含む化合物の遷移金属は、鉄、マンガン、ニッケル又はコバルトのうちいずれか一以上である。特に、列挙した遷移金属の炭酸塩を用いることが好ましい。
【0027】
また、上記した遷移金属を含むアルカリ金属ケイ酸塩の合成方法において、析出させたアルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合した混合物に行う加熱処理(第2の加熱処理)は、700℃以上1000℃以下の不活性ガス雰囲気下で行うことが好ましい。
【0028】
上記した遷移金属を含むアルカリ金属ケイ酸塩の合成方法を用いることで、気体吸着法で測定される比表面積が50m2/g以上150m2/g以下である遷移金属を含むアルカリ金属ケイ酸塩を合成することができる。
【発明の効果】
【0029】
本発明の一態様により、微粒子化が容易である遷移金属を含むアルカリ金属ケイ酸塩の合成方法を提供することができ、特に、微粒子化が容易である遷移金属を含むリチウムケイ酸塩の合成方法を提供することができる。
【0030】
また、本発明の一態様により、粒子サイズが揃い、微粒子化された遷移金属を含むアルカリ金属ケイ酸塩を提供することができ、特に、粒子サイズが揃い、微粒子化された遷移金属を含むケイ酸リチウムを提供することができる。
【0031】
さらに、本発明の一態様により、遷移金属を含むアルカリ金属ケイ酸塩の前駆体であるアルカリ金属ケイ酸塩の合成方法、及び当該合成方法を用いて作製したアルカリ金属ケイ酸塩を提供することができる。
【0032】
本発明の一態様により、微粒子化された遷移金属を含むアルカリ金属ケイ酸塩を、蓄電装置の正極活物質として用いることで、正極重量あたりの容量が増大した正極を作製でき、高容量なリチウム二次電池を作製することできる。
【図面の簡単な説明】
【0033】
【図1】アルカリ金属ケイ酸塩の合成方法を説明する図。
【図2】遷移金属を含むアルカリ金属ケイ酸塩の合成方法を説明する図。
【図3】蓄電装置の一形態を説明するための断面図。
【図4】蓄電装置の負極の一態様を説明するための断面図。
【図5】蓄電装置の応用の形態を説明するための図。
【図6】蓄電装置の応用の形態を説明するための図。
【図7】化合物Aと比較化合物のX線回折パターン。
【図8】化合物Aと比較化合物の平面SEM像。
【図9】化合物B乃至化合物DのX線回折パターン。
【図10】化合物E及び化合物FのX線回折パターン。
【図11】化合物C及び化合物Dの平面SEM像。
【図12】化合物Eの平面SEM像。
【図13】ケイ酸リチウムの比表面積と作製した水酸化リチウム水溶液に対するシリコン濃度との関係を示す図。
【図14】化合物GのX線回折パターン。
【発明を実施するための形態】
【0034】
本明細書において、実施の形態及び実施例は図面を用いて以下に説明する。但し、本発明は以下の説明に限定されず、本発明の趣旨及びその範囲から逸脱することなくその形態及び詳細を様々に変更し得ることは当業者であれば容易に理解される。従って、本発明は以下に示す実施の形態の記載内容に限定して解釈されるものではないとする。なお、説明中に図面を参照するにあたり、同じものを指す符号は異なる図面間でも共通して用いる場合がある。また、同様のものを指す際には同じハッチパターンを使用し、特に符号を付さない場合がある。
【0035】
(実施の形態1)
本実施の形態では、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法ついて、以下、図面を参照して詳細に説明する。なお、具体的な合成例として、遷移金属をマンガンとし、アルカリ金属をリチウムとしたケイ酸マンガンリチウムの合成例を説明する。
【0036】
本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法は、前駆体であるアルカリ金属ケイ酸塩を合成し、その後、当該前駆体と微粒子化した遷移金属を含む化合物を反応させる合成方法である。例えば、ケイ酸マンガンリチウムの場合、始めに前駆体であるケイ酸リチウムを合成し、その後、ケイ酸リチウムと微粒子化したマンガン塩を反応させることで合成できる。
【0037】
〈前駆体の合成〉
そこで、始めに、前駆体であるアルカリ金属ケイ酸塩の合成方法について記載する。
【0038】
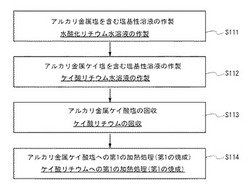
図1は、アルカリ金属ケイ酸塩の合成方法を説明する図である。なお、図1に示した各ステップにおいて、下線の記載は、ケイ酸マンガンリチウムの前駆体であるケイ酸リチウムを合成する場合の説明である。
【0039】
〈ステップS111〉
ステップS111として、アルカリ金属塩を含む塩基性溶液を作製する。当該アルカリ金属塩は、アルカリ金属ケイ酸塩におけるアルカリ金属源として機能する。
【0040】
具体的には、アルカリ金属塩を当該アルカリ金属塩の良溶媒に溶解させて、塩基性溶液を作製する。当該塩基性溶液は塩基性が強いほど、後述のステップS112において、シリコン粒子が当該塩基性溶液に溶解しやすくなり、ステップS112を効率的に行うことができる。そこで、当該塩基性溶液は水素イオン指数(pH)が9以上となるように調整することが好ましく、例えば当該塩基性溶液はpHが10程度となるように調整すればよい。
【0041】
また、アルカリ金属塩を含む塩基性溶液の作製は、アルカリ金属塩が溶解しやすいように良溶媒を加熱及び保温しながら行うことが好ましい。
【0042】
なお、ケイ酸リチウムを合成する場合、ステップS111として、アルカリ金属塩として水酸化リチウムを用いて、良溶媒を水とし、pHが10の水酸化リチウム水溶液を作製する。
【0043】
〈ステップS112〉
次に、ステップS112として、アルカリ金属ケイ酸塩を含む塩基性溶液を作製する。
【0044】
具体的には、アルカリ金属ケイ酸塩のシリコン源としてシリコン粒子を用意して、ステップS111で作製したアルカリ金属塩を含む塩基性溶液に当該シリコン粒子を加えて攪拌する。このように攪拌することで、アルカリ金属塩とシリコン粒子は水素ガスを放出しながら反応し、アルカリ金属ケイ酸塩が形成される。なお、当該アルカリ金属ケイ酸塩は、ステップS111で用いたアルカリ金属塩の良溶媒に溶解している。
【0045】
また、ステップS112で攪拌する方法としては、棒状、板状、プロペラ状の攪拌子を備えた装置(例えば、マグネチックスターラー及びメカニカルスターラー)などを用いて機械的に攪拌する方法を用いることができる。
【0046】
また、ステップS112において、機械的に攪拌する代わりに、シリコン粒子を加えたアルカリ金属塩を含む塩基性溶液に超音波を印加して、アルカリ金属塩とシリコンを反応させて、アルカリ金属ケイ酸塩を形成してもよい。
【0047】
なお、ステップS112において、加えたシリコン粒子がアルカリ金属塩を含む塩基性溶液中に局在しないように、常に攪拌しておくことが好ましい。
【0048】
また、ステップS112の反応によって、組成が異なる複数種のアルカリ金属ケイ酸塩が形成される場合がある。つまり、ステップS112を経て作製されたアルカリ金属ケイ酸塩を含む塩基性溶液には、組成が異なる複数種のアルカリ金属ケイ酸塩が含まれていてもよい。
【0049】
ステップS112は液相反応であることから、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法は液相反応を用いた合成方法である。
【0050】
ステップS112で用いるシリコン粒子は、できる限り高純度のシリコン粒子であること好ましいが、他の金属元素、シリコン酸化物及びシリコン窒化物の一以上が含まれているシリコン粒子であってもよい。例えば、公知のシリコン粉末を用いることができる。
【0051】
また、ステップS112において、シリコン粒子はアルカリ金属塩を含む塩基性溶液に溶解するまで攪拌すればよいので、シリコン粒子の粒子サイズ(例えば粒径)に特に限定はない。ただし、シリコン粒子の粒子サイズ(例えば粒径)は小さいほど、アルカリ金属塩を含む塩基性溶液にシリコン粒子を溶解させやすいことから、シリコン粒子はできる限り粒子サイズの小さいものを用いることが好ましい。
【0052】
また、ステップS112の液相反応は、ステップS111で作製したアルカリ金属塩を含む塩基性溶液の温度を室温より高くすることで、シリコン粒子を当該塩基性溶液に溶解させやすくなり、当該液相反応を効率的に進行させることができる。
【0053】
例えば、ステップS111で作製したアルカリ金属塩を含む塩基性溶液の温度を50℃以上70℃以下、好ましくは60℃程度にすることで、ステップS112の液相反応を効率的に進行させることができる。
【0054】
また、本発明の一態様に係る合成方法において、アルカリ金属ケイ酸塩の比表面積を大きく(別言すると粒子サイズを小さく)するには、シリコン粒子を加えたアルカリ金属塩を含む塩基性溶液中のシリコン濃度を高くすることが好ましいが、当該シリコン濃度とアルカリ金属ケイ酸塩の比表面積との関係には極大を有することがあるため、所望の比表面積が得られるように当該シリコン濃度を適宜選択することが好ましい。例えば、当該濃度は0.3mol/l程度とすればよい。
【0055】
また、ステップS112において、アルカリ金属塩がシリコン粒子より過剰となるようにシリコン粒子を混合することが好ましい。つまり、シリコン粒子を加えたアルカリ金属塩を含む塩基性溶液中において、シリコンのモル数よりもアルカリ金属のモル数が過剰となるようにシリコン粒子を加えることが好ましい。このようにすることで、未反応のシリコンを減少させることができ、目的物のアルカリ金属ケイ酸塩の収率を向上させることができる。また、ステップS112(特に、シリコン粒子を加えたアルカリ金属塩を含む塩基性溶液中)において、シリコンのモル数及びアルカリ金属のモル数の比率を変化させることで、当該比率に対応した組成を有するアルカリ金属ケイ酸塩を形成することができる。
【0056】
なお、ケイ酸リチウムを合成する場合、ステップS112として、ステップS111で作製した水酸化リチウム水溶液を60℃に加熱し、60℃に保った水酸化リチウム水溶液にシリコン粒子を加えて機械的に攪拌し、水酸化リチウムとシリコンを反応させてケイ酸リチウム水溶液を作製する。
【0057】
〈ステップS113〉
次に、ステップS113として、ステップS112で作製したアルカリ金属ケイ酸塩を含む塩基性溶液から、アルカリ金属ケイ酸塩を回収する。
【0058】
具体的には、アルカリ金属ケイ酸塩の貧溶媒を用意し、当該貧溶媒にステップS112で作製したアルカリ金属ケイ酸塩を含む塩基性溶液を加えて、貧溶媒中にアルカリ金属ケイ酸塩を析出させる。析出させた後、濾過、遠心分離又は透析など、いずれか一以上の操作を行い、アルカリ金属ケイ酸塩を回収する。その後、回収したアルカリ金属ケイ酸塩を乾燥させる。
【0059】
ステップS113において、アルカリ金属塩の良溶媒と目的物のアルカリ金属ケイ酸塩の貧溶媒は混和するが、貧溶媒の良溶媒に対する親和性によって、析出するアルカリ金属ケイ酸塩の組成が異なることがある。例えば、良溶媒に対する親和性が小さい場合、アルカリ金属のシリコンに対する組成が大きいアルカリ金属ケイ酸塩が析出する傾向にある。また、貧溶媒の良溶媒に対する親和性によって、析出するアルカリ金属ケイ酸塩の組成が同じでも、粒子サイズが異なることがある。そこで、所望の組成及び所望の粒子サイズを有するアルカリ金属ケイ酸塩が析出するように貧溶媒を適宜選択することが好ましい。
【0060】
例えば、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩を蓄電装置の正極活物質として用いる場合、遷移金属を含むアルカリ金属ケイ酸塩の気体吸着法で測定される比表面積は、50m2/g以上150m2/g以下(好ましくは、50m2/g以上70m2/g以下)であることが好ましい。そこで、前駆体であるアルカリ金属ケイ酸塩の気体吸着法で測定される比表面積は、50m2/g以上90m2/g以下となるように形成することが好ましい。なお、遷移金属を含むアルカリ金属ケイ酸塩及びアルカリ金属ケイ酸塩において、その粒子サイズと、気体吸着法での比表面積とには相関があり、この比表面積が大きいほど、粒子サイズ(例えば粒径)は小さい傾向にある。また、気体吸着法での比表面積は、自動比表面積細孔分布測定装置トライスターII3020(株式会社島津製作所製)で測定できる。さらに当該装置は、試料に窒素を一定期間吸着させた後、吸着した窒素量で当該試料の表面積を測定する装置である。
【0061】
貧溶媒中にアルカリ金属ケイ酸塩を析出させるには様々な方法を用いることができる。例えば、アルカリ金属ケイ酸塩を含む塩基性溶液を貧溶媒に滴下することでアルカリ金属ケイ酸塩を析出させることができる。また、攪拌している貧溶媒、又は超音波を印加している貧溶媒に、一定量の当該塩基性溶液を加えることでも目的物のアルカリ金属ケイ酸塩を析出させることができる。なお、貧溶媒の量は、加えるアルカリ金属ケイ酸塩を含む塩基性溶液より多いものとし、貧溶媒の攪拌は、ステップS112と同様の装置を用いて機械的に攪拌すればよい。
【0062】
貧溶媒にアルカリ金属ケイ酸塩を含む塩基性溶液を滴下する方法において、貧溶媒の量は、最終的に供給したアルカリ金属ケイ酸塩を含む塩基性溶液の量より多くする。この滴下する方法は、上記した他の方法に比べて、粒子サイズが小さく、その粒子サイズが揃ったアルカリ金属ケイ酸塩を析出させることができるため好ましい。アルカリ金属ケイ酸塩の粒子サイズを小さくするには、当該塩基性溶液を滴下する速度を遅く、その液滴のサイズは小さく制御することが好ましい。液滴のサイズを小さくするには、一度に滴下する液量を少なくすること、又は滴下する器具のノズル口径を小さくすればよい。なお、本明細書において、滴下する速度とは、1時間あたりに供給する液量をいう。例えば、貧溶媒に対して、滴下する速度は40ml/h以上80ml/h以下が好ましい。
【0063】
また、貧溶媒にアルカリ金属ケイ酸塩を含む塩基性溶液を滴下する際は、貧溶媒を攪拌しながら行うことが好ましい。攪拌する方法としては、ステップS112と同様の装置を用いて機械的に攪拌してもよく、超音波を印加してもよい。なお、攪拌する条件(回転数など)によっても析出するアルカリ金属ケイ酸塩の粒子サイズが変化するため、攪拌する条件は適宜選択することが好ましい。
【0064】
濾過、遠心分離及び透析などからいずれか一以上の操作を行って回収したアルカリ金属ケイ酸塩の乾燥は、真空雰囲気又は不活性ガス雰囲気で加熱すればよい。また、加熱する時間及び温度は、回収したアルカリ金属ケイ酸塩に含まれる溶媒(ステップS111の良溶媒及びステップS113の貧溶媒)を除去できる時間及び温度であればよく、当該良溶媒の沸点及び当該貧溶媒の沸点などを考慮して適宜選択すればよい。例えば、80℃以上200℃以下の温度で1時間以上3時間以下保持して真空乾燥すればよい。また、当該乾燥は昇温レートと降温レートに制限はなく、自然冷却を開始してから十分な時間、真空雰囲気下を保持してもよい。
【0065】
なお、ケイ酸リチウムを合成する場合、ステップS113として、ケイ酸リチウムの貧溶媒であるエタノールにケイ酸リチウム水溶液を40ml/h程度の速度で滴下し、エタノール中にケイ酸リチウムを析出させる。その後、濾過して析出したケイ酸リチウムを回収し、80℃真空雰囲気下で2時間加熱を保持し、その後、室温まで下がる時間を含めて2時間真空雰囲気下で保持、自然冷却する。
【0066】
また、ケイ酸リチウムを合成する場合、ステップS113として、ケイ酸リチウムの貧溶媒であるエタノールの代わりにメタノール、プロパノール、ブタノール、ペンタノール、又はアセトンなどを用いることができる。
【0067】
〈ステップS114〉
次に、乾燥させたアルカリ金属ケイ酸塩に第1の加熱処理(第1の焼成と言い換えてもよい。)を行う。なお、第1の加熱処理は昇温過程、加熱保持過程及び降温過程を備えるものとし、特に断りが無い限り、「加熱処理の時間」とは、加熱保持過程の時間のことをいう。
【0068】
ステップS114での第1の加熱処理の条件によって、アルカリ金属ケイ酸塩の粒子サイズは増大することがある。第1の加熱処理の温度が高いと当該粒子サイズは増大する傾向にあり、第1の加熱処理の時間が長いと当該粒子サイズは増大する傾向にある。そのため、第1の加熱処理の温度はできる限り低い方が好ましく、第1の加熱処理の時間もできる限り短い方が好ましい。
【0069】
第1の加熱処理の一例は以下の通りである。第1の加熱処理を行う雰囲気は、真空雰囲気下又は不活性ガス雰囲気下とし、第1の加熱処理の温度は500℃以上600℃以下とし、第1の加熱処理の時間は、1時間以上24時間以下、好ましくは10時間以上15時間以下として行う。
【0070】
ステップS114において、第1の加熱処理の回数は、アルカリ金属ケイ酸塩の合成にかかるタクトタイムを短くすることができるため、1回とすればよいが、複数回行ってもよい。さらに、1回の加熱処理(1回の焼成)は、仮焼成及び本焼成というように2段階に分けて行ってもよく、この場合、本焼成は仮焼成より高温で行うことが好ましい。
【0071】
また、ステップS113の乾燥と第1の加熱処理は同一の加熱装置を用いて連続して行ってもよく、このようにすることで、アルカリ金属ケイ酸塩の合成にかかるタクトタイムを短くすることができる。なお、ステップS113の乾燥は仮焼成であり、ステップS114の加熱処理は本焼成であるともいえる。
【0072】
なお、第1の加熱処理の条件によって、アルカリ金属ケイ酸塩の組成が変化することがある。従って、所望の組成となるように第1の加熱処理の条件を適宜選択することが好ましい。
【0073】
また、図1には示していないが、ステップS114の後のアルカリ金属ケイ酸塩を洗浄してもよい。このように洗浄することで、ステップS112で過剰に存在していたアルカリ金属塩を除去することができる。洗浄する溶媒に特に限定はないが、例えば水などを用いることができる。そして、洗浄した後は、ステップS113で記載した乾燥を行うことが望ましい。
【0074】
なお、第1の加熱処理を行わず、後述の第2の加熱処理に第1の加熱処理を兼ねさせてもよい。
【0075】
また、遷移金属を含むアルカリ金属ケイ酸塩の前駆体であるアルカリ金属ケイ酸塩の合成において、所望の組成とは異なる組成を有するアルカリ金属ケイ酸塩が生成された場合は、適宜精製し、所望の組成を有するアルカリ金属ケイ酸塩を回収すればよい。
【0076】
以上のステップにより、遷移金属を含むアルカリ金属ケイ酸塩の前駆体であるアルカリ金属ケイ酸塩を合成することができる。
【0077】
なお、ケイ酸リチウムを合成する場合、ステップS114として、乾燥したケイ酸リチウムに520℃窒素雰囲気下で10時間の加熱処理を行う。その後、水で1時間洗浄し、180℃真空雰囲気下で1時間加熱し、その後、室温まで下がる時間を含めて2時間真空雰囲気下を保持し、自然冷却する。以上のステップにより、ケイ酸マンガンリチウムの前駆体であるケイ酸リチウムを合成できる。
【0078】
蓄電装置用の正極活物質として機能する、遷移金属を含むアルカリ金属ケイ酸塩の粒子サイズは、前駆体であるアルカリ金属ケイ酸塩の粒子サイズを反映する。詳細には、前駆体であるアルカリ金属ケイ酸塩の粒子サイズが大きいと、最終的に得られる遷移金属を含むアルカリ金属ケイ酸塩の粒子サイズは大きくなる。それゆえ、微粒子化された前駆体と、微粒子化された遷移金属を含む化合物と、を反応させることによって、微粒子化された遷移金属を含むアルカリ金属ケイ酸塩を容易に合成することができる。つまり、前駆体であるアルカリ金属ケイ酸塩の粒子サイズを小さくして(微粒子化して)合成することは、遷移金属を含むアルカリ金属ケイ酸塩の粒子サイズを小さくする(微粒子化する)ために、極めて有用である。
【0079】
また、最終的に得られる遷移金属を含むアルカリ金属ケイ酸塩は、機械的強度が高く、機械的に粉砕して粒子サイズを小さくする(微粒子化する)ことが難しい場合がある。それゆえ、前駆体であるアルカリ金属ケイ酸塩の粒子サイズを小さくして(微粒子化して)合成することは、遷移金属を含むアルカリ金属ケイ酸塩の粒子サイズを小さくする(微粒子化する)ために、極めて有用である。
【0080】
〈目的物の合成〉
次に、合成した前駆体のアルカリ金属ケイ酸塩から、目的物である遷移金属を含むアルカリ金属ケイ酸塩を合成する方法について図2を参照して説明する。なお、図2に示した各ステップにおいて、下線の記載は、前駆体のケイ酸リチウムから目的物であるケイ酸マンガンリチウムを合成する場合の各ステップにおける説明である。
【0081】
〈ステップS115〉
まず、ステップS111乃至ステップS114を経て合成されたアルカリ金属ケイ酸塩と、微粒子化された遷移金属を含む化合物を混合して混合物を作製する。目的物である遷移金属を含むアルカリ金属ケイ酸塩の組成に応じて、当該アルカリ金属ケイ酸塩と、微粒子化された遷移金属を含む化合物の混合量を調整する。例えば、アルカリ金属の組成を遷移金属の組成に対して2倍とする場合、アルカリ金属ケイ酸塩と遷移金属を含む化合物のモル比が2となるように両化合物の混合量を調整する。
【0082】
遷移金属を含む化合物は、あらかじめ微粒子化しておくことが好ましい。微粒子化する方法としては、機械的に粉砕する、又は超音波を印加して粉砕しておけばよい。例えば、あらかじめ遷移金属を含む化合物だけを先に、後述するボールミル処理で機械的に粉砕し、微粒子化しておけばよい。
【0083】
また、機械的に粉砕し、微粒子化した遷移金属を含む化合物を、所望の孔径を有するフィルタ(例えば、メンブレンフィルタ)などを通過させる操作をしてもよい。この操作を行うことで、微粒子化した遷移金属を含む化合物において、粒子サイズの大きなものを除去すると共に粒子サイズを均一化することができる。
【0084】
また、遷移金属を含む化合物は、あらかじめ微粒子化しておくことで、アルカリ金属ケイ酸塩と遷移金属を含む化合物を均一に混合することができ、目的物である遷移金属を含むアルカリ金属ケイ酸塩を微粒子化することができる。さらに、目的物である遷移金属を含むアルカリ金属ケイ酸塩の結晶性を高めることもできる。
【0085】
遷移金属を含む化合物としては、鉄、マンガン、ニッケル又はコバルトのいずれか一以上を含む化合物であればよく、好ましくは、鉄、マンガン、ニッケル又はコバルトのいずれか一以上を含む炭酸塩を用いる。
【0086】
具体的に、アルカリ金属ケイ酸塩と、微粒子化された遷移金属を含む化合物の混合物はボールミル処理によって作製できる。ボールミル処理は、アルカリ金属ケイ酸塩及び遷移金属を含む化合物と、溶媒と、ボールと、を装置(ボールミル用ポット)に入れて混合を行う。溶媒としては、アセトン、又はエタノールなどのアルコールを用いることができ、混合した後、混合物を加熱して溶媒を除去することが好ましい。ボールは、金属製又はセラミック製等を用いることができる。ボールミル処理は、回転数50rpm以上500rpm以下、回転時間30分間以上5時間以下、ボール径φ0.5mm以上10mm以下で行う。
【0087】
また、アルカリ金属ケイ酸塩と、微粒子化された遷移金属を含む化合物の混合物を、所望の孔径を有するフィルタ(例えば、メンブレンフィルタ)などを通過させる操作をしてもよい。この操作を行うことで、粒子サイズの大きな混合物を除去すると共に粒子サイズを均一化することができる。
【0088】
なお、ケイ酸マンガンリチウムを合成する場合、ステップS115として、ケイ酸リチウムと、あらかじめ機械的に粉砕し、微粒子化した炭酸マンガンと、を所望の組成となるようにモル数比を調整し、溶媒をアセトンとしてボールミル処理を行い、混合物を作製する。なお、ボールミル処理後、当該混合物を加熱して溶媒のアセトンを蒸発させる。
【0089】
〈ステップS116〉
次に、ステップS115で作製された混合物に第2の加熱処理(第2の焼成ともいう。)を行う。
【0090】
第1の加熱処理と同様に、第2の加熱処理の条件(加熱温度及び加熱時間)によって、目的物である遷移金属を含むアルカリ金属ケイ酸塩の粒子サイズは増大することがある。
【0091】
第2の加熱処理の一例は以下の通りである。加熱処理(焼成)を行う雰囲気は、真空雰囲気下又は不活性ガス雰囲気下とし、加熱温度は700℃以上1100℃以下とし、加熱時間は、昇温過程及び降温過程を含めて1時間以上24時間以下、好ましくは加熱時間10時間以上15時間以下として行う。
【0092】
また、第2の加熱処理を行う際、前駆体であるアルカリ金属ケイ酸塩の粒子サイズが小さく、微粒子化されているほど、第2の加熱処理の加熱温度を下げることができる。上記第2の加熱処理の加熱温度は、遷移金属がマンガンである場合において、比較的低温といえる温度である。なお、焼成温度は1100℃以上としてもよい。
【0093】
ステップS116において、第2の加熱処理の回数は、1回とすればよいが、複数回行ってもよい。第2の加熱処理の回数を1回とすれば、目的物である遷移金属を含むアルカリ金属ケイ酸塩の合成にかかるタクトタイムを短くすることができるため、生産性を向上させることができる。
【0094】
さらに、1回の加熱処理(焼成)は、仮焼成及び本焼成というように2段階に分けて行ってもよく、この場合、本焼成は仮焼成より高温で行うことが好ましい。このように1回の加熱処理(焼成)を2段階に分けて行うことで、目的物である遷移金属を含むアルカリ金属ケイ酸塩の結晶性を向上させることができる。
【0095】
なお、第2の加熱処理を行う前に、混合物に加圧処理を行ってもよい。例えば、混合物をペレットに成型したものに第2の加熱処理を行うことができる。
【0096】
なお、ケイ酸マンガンリチウムを合成する場合、ステップS116としては、ステップS115で作製した混合物を粉体のまま窒素雰囲気下で、加熱温度700℃10時間の加熱処理を行う。
【0097】
以上のステップより、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩を合成することができる。
【0098】
本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法は、粒子サイズを小さくした(微粒子化した)アルカリ金属ケイ酸塩を前駆体とすることから、前駆体と遷移金属を含む化合物との混合物の加熱処理回数を1回に減らすことができ、加熱時間を短縮することができ、さらに加熱温度を低くすることができる。従って、加熱時間が長くなることで伴う粒子サイズの増大、及び加熱温度の高温化に伴う粒子サイズの増大を抑制することができるため、微粒子化された遷移金属を含むアルカリ金属ケイ酸塩を容易に合成することができる。
【0099】
本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法によって合成された遷移金属を含むアルカリ金属ケイ酸塩は、粒子サイズが小さく微粒子化されていることから、従来の固相反応により合成された遷移金属を含むアルカリ金属ケイ酸塩に比べて、粒子1つあたりの重量が軽い。さらに、粒子サイズが小さく微粒子化されていることから、リチウムイオンの拡散性が向上している。従って、本発明の一態様に係る微粒子化された遷移金属を含むアルカリ金属ケイ酸塩を蓄電装置の正極活物質に用いることで、正極重量あたりの容量が増大した正極を容易に作製することができる。さらには、高容量なリチウム二次電池を作製することできる。
【0100】
また、本実施の形態は、他の実施の形態及び実施例に記載した構成と適宜組み合わせて実施することが可能である。
【0101】
(実施の形態2)
本実施の形態では、本発明の一態様に係る蓄電装置について説明する。具体的には、実施の形態1で説明した遷移金属を含むアルカリ金属ケイ酸塩を正極活物質に適用した蓄電装置について説明する。
【0102】
本発明の一態様に係る蓄電装置は、少なくとも、正極、負極、セパレータ、及び電解質で構成される。
【0103】
また、本発明の一態様に係る蓄電装置は、アルカリ金属イオン、アルカリ土類金属イオン、ベリリウムイオン、又はマグネシウムイオンをキャリアイオンとする。なお、アルカリ金属イオンとしては、例えばリチウムイオン、ナトリウムイオン、又はカリウムイオンがある。アルカリ土類金属イオンとしては、例えばカルシウムイオン、ストロンチウムイオン、又はバリウムイオンがある。
【0104】
本実施の形態では、本発明の一態様に係る蓄電装置の一例として、キャリアイオンをリチウムイオンとしたリチウム二次電池を説明する。
【0105】
図3にリチウム二次電池100の断面図を示す。リチウム二次電池100は、正極集電体101及び正極活物質層102で構成される正極103と、負極集電体104及び負極活物質層105で構成される負極106と、正極103及び負極106で挟持されるセパレータ108とで構成される。なお、セパレータ108中には電解質107が含まれる。また、正極集電体101は外部端子111と接続し、負極集電体104は外部端子109と接続されている。外部端子111の端部はガスケット121に埋没されている。すなわち、外部端子109、111は、ガスケット121によって絶縁されている。
【0106】
正極集電体101には、例えば導電材料などを用いることができ、導電材料としては、例えばアルミニウム(Al)、銅(Cu)、ニッケル(Ni)、又はチタン(Ti)を用いることができる。また、正極集電体101としては、上記導電材料のうち複数からなる合金材料を用いることもでき、合金材料としては、例えばAl−Ni合金、又はAl−Cu合金などを用いることもできる。また、別途基板上に形成することにより設けられた導電層を剥離して正極集電体101として用いることもできる。
【0107】
正極活物質層102は、正極活物質、バインダ及び導電助剤を含む。正極活物質としては、実施の形態1で説明した遷移金属を含むアルカリ金属ケイ酸塩を用いることができる。本実施の形態ではリチウム二次電池を例に説明するため、正極活物質としてリチウムを含む材料を用いる。そこで、遷移金属を含むアルカリ金属ケイ酸塩は、遷移金属を含むリチウムケイ酸塩を用いることができ、例えば、ケイ酸マンガンリチウム(Li2MnSiO4)を用いることができる。
【0108】
実施の形態1で説明した遷移金属を含むアルカリ金属ケイ酸塩は、粒子サイズが小さく微粒子化されていることから、従来の固相反応により合成された遷移金属を含むアルカリ金属ケイ酸塩に比べて粒子1つあたりの重量が軽く、さらにリチウムイオンの拡散性が向上している。そのため、正極103の重量を低減させることができ、正極重量あたりの容量を増大させることができる。結果として、従来に比べてリチウム二次電池の容量を向上させることができる。
【0109】
バインダとしては、澱粉、カルボキシメチルセルロース、ヒドロキシプロピルセルロース、再生セルロース、ジアセチルセルロースなどの多糖類や、ポリビニルクロリド、ポリエチレン、ポリプロピレン、ポリビニルアルコール、ポリビニルピロリドン、ポリテトラフルオロエチレン、ポリフッ化ビニリデン、EPDM(Ethylene Propylene Diene Monomer)ゴム、スルホン化EPDMゴム、スチレンブタジエンゴム、ブタジエンゴム、フッ素ゴムなどのビニルポリマー、ポリエチレンオキシドなどのポリエーテルなどがある。
【0110】
また、導電助剤としては、蓄電装置中で化学変化を起こさない電子伝導性材料であればよい。例えば、黒鉛、炭素繊維などの炭素系材料、銅、ニッケル、アルミニウム若しくは銀などの金属材料又はこれらの混合物の粉末や繊維などを用いることができる。なお、導電助剤を膜状に形成して正極活物質をコーティングしてもよい。
【0111】
また、正極活物質層102形成する際、バインダ及び導電助剤の代わりにグラフェン又は多層グラフェンを混合させてもよい。なお、本明細書において、グラフェンとは、イオンを通過させる空隙を有し、sp2結合を有する1原子層の炭素分子で構成されたシート、又は当該シートが2枚乃至100枚積層された積層体をいう。また、当該グラフェンは、水素と炭素以外の元素の比率を15原子%以下、又は炭素以外の元素の比率を30原子%以下であることが好ましい。なお、グラフェンは、カリウムなどのアルカリ金属を添加したものでもよい。上記より、本明細書において、グラフェン類似体も当該グラフェンに含まれる。
【0112】
このように、導電助剤及びバインダの代わりにグラフェンを用いることで、正極103中の導電助剤及びバインダの含有量を低減させることできる。つまり、正極103の重量を低減させることができ、電極の重量あたりにおけるリチウム二次電池の容量を増大させることができる。結果として、従来に比べてリチウム二次電池の容量を向上させることができる。
【0113】
なお、「活物質」とは、厳密にはキャリアであるイオンの挿入及び脱離に関わる物質のみを指す。ただし本明細書では、塗布法を用いて正極活物質層102を形成する場合、便宜上、正極活物質層102の材料、すなわち、本来「正極活物質」である物質に、導電助剤やバインダなどを含めて正極活物質層102と呼ぶこととする。
【0114】
負極集電体104には、銅(Cu)、アルミニウム(Al)、ニッケル(Ni)、チタン(Ti)などの単体又はこれらの化合物を用いることができる。
【0115】
負極活物質層105には、リチウムの溶解・析出又はリチウムイオンのドープ・脱ドープが可能であれば特に限定されるものではなく、リチウム、アルミニウム、炭素系材料、スズ、シリコン、シリコン合金、及びゲルマニウムなどがある。又は、リチウム、アルミニウム、炭素系材料、スズ、シリコン、シリコン合金、及びゲルマニウムから選択される一以上を含む化合物でもよい。なお、リチウムイオンの挿入及び脱離が可能な炭素としては、粉末状若しくは繊維状の黒鉛、又はグラファイト等の黒鉛系炭素を用いることができる。また、シリコン、シリコン合金、ゲルマニウム、リチウム、アルミニウム、及びスズの方が、炭素系材料に比べてキャリアイオンを吸蔵できる容量が大きい。それゆえ、負極活物質層105に用いる材料の量を低減することができ、コストの節減、及びリチウム二次電池100の小型化が可能になる。
【0116】
また、負極活物質層105は、上記列挙した材料を印刷法、インクジェット法、CVD等により、凹凸状に形成したものでもよい。又は、上記列挙した材料を塗布法、スパッタリング法、蒸着法などで膜状に設けた後、当該膜状の材料を選択的に除去して、凹凸状に形成したものでもよい。
【0117】
なお、負極集電体104を用いず、上記列挙した負極活物質層105に適用できる材料単体を負極として用いてもよい。
【0118】
また、負極活物質層105の表面にグラフェンを形成してもよい。このようにすることで、リチウムの溶解又は析出、若しくはリチウムイオンの挿入又は脱離によって生じる負極活物質層105に与える影響を抑制することができる。当該影響とは、負極活物質層105が膨張又は収縮することで、負極活物質層105の微粉化又は剥離することである。
【0119】
電解質107は、上記列挙したキャリアイオンを有する塩である溶質と、溶媒と、を少なくとも含む。例えば、電解質107として、該塩が溶解した非水溶液、又は当該塩が溶解した水溶液を用いることができる。本実施の形態ではリチウム二次電池を例にしていることから、キャリアイオンであるリチウムイオンを有するリチウム塩を用いる。例えば、LiClO4、LiAsF6、LiBF4、LiPF6、Li(C2F5SO2)2Nなどのリチウム塩が挙げられる。なお、キャリアイオンをリチウム以外のアルカリ金属イオン又はアルカリ土類金属イオンとする場合には、電解質107の溶質として、アルカリ金属塩(例えば、ナトリウム塩又はカリウム塩など)、アルカリ土類金属塩(例えば、カルシウム塩、ストロンチウム塩又はバリウム塩など)、ベリリウム塩又はマグネシウム塩などを用いることができる。
【0120】
また、電解質107は、上記列挙したキャリアイオンを有する塩が溶解した非水溶液にすることが好ましい。つまり、電解質107の溶媒は、非プロトン性有機溶媒が好ましい。非プロトン性有機溶媒としては、例えば、エチレンカーボネート、プロピレンカーボネート、ジメチルカーボネート、ジエチルカーボネート、γーブチロラクトン、アセトニトリル、ジメトキシエタン及びテトラヒドロフランなどが挙げられ、これらの一又は複数を用いることができる。さらに、非プロトン性有機溶媒として、一のイオン液体又は複数のイオン液体を用いてもよい。イオン液体は、難燃性及び難揮発性であることから、リチウム二次電池100の内部温度が上昇した際にリチウム二次電池100の破裂又は発火などを抑制でき、安全性を高めることが可能となる。
【0121】
また、電解質107として、上記列挙したキャリアイオンを有する塩を含み、且つゲル化された高分子材料を用いることで、漏液性を含めた安全性が高まり、リチウム二次電池100の薄型化及び軽量化が可能となる。ゲル化される高分子材料の代表例としては、シリコンゲル、アクリルゲル、アクリロニトリルゲル、ポリエチレンオキサイド、ポリプロピレンオキサイド又はフッ素系ポリマーなどがある。
【0122】
さらに、電解質107としては、Li3PO4などの固体電解質を用いることができる。他の固体電解質としては、Li3PO4に窒素を混ぜたLixPOyNz(x、y、zは正の実数)、Li2S−SiS2、Li2S−P2S5、Li2S−B2S3等を用いることができ、上記列挙した固体電解質にLiIなどをドープしたものを用いることもできる。
【0123】
セパレータ108として、絶縁性の多孔体を用いる。例えば、紙、不織布、ガラス繊維、セラミックス、或いはナイロン(ポリアミド)、ビニロン(ポリビニルアルコール系繊維)、ポリエステル、アクリル、ポリオレフィン、ポリウレタンを用いた合成繊維等で形成されたものを用いればよい。ただし、電解質107に溶解しない材料を選ぶ必要がある。
【0124】
なお、本実施の形態では、リチウム二次電池100の外装形態として、密封されたボタン型を示しているが、これに限定されない。つまり、リチウム二次電池100を含め、本発明の一態様に係る蓄電装置の外装形態として、ラミネート型、円筒型、角型など様々な形状を採用することができる。また、本実施の形態のリチウム二次電池100では、正極103、負極106、及びセパレータ108が積層された構造を示したが、正極103、負極106、及びセパレータ108が捲回された構造であってもよい。
【0125】
次に、本発明の一態様に係る蓄電装置の作製方法について説明する。まず、正極103の作製方法について説明する。
【0126】
正極集電体101及び正極活物質層102の材料ついては上記列挙した材料から選択する。なお、正極活物質層102の正極活物質は、実施の形態1で説明した遷移金属を含むアルカリ金属ケイ酸塩、特にケイ酸マンガンリチウム(Li2MnSiO4)とする。
【0127】
正極集電体101上に、正極活物質層102を形成する。また正極活物質層102の形成方法は、塗布法又はスパッタリング法により形成すればよい。正極活物質層102を塗布法によって形成する場合は、正極活物質層102の材料に、導電助剤やバインダなどを混合させてペースト化したスラリーを作製する。そして、当該スラリーを正極集電体101上に塗布して乾燥させて形成する。正極活物質層102を塗布法により形成した場合、必要に応じて加圧成形するとよい。以上により、正極集電体101上に正極活物質層102が形成された正極103を作製できる。
【0128】
次に、負極106の作製方法について説明する。
【0129】
負極集電体104及び負極活物質層105の材料は上記列挙した材料から選択し、正極103と同様の方法を用いて、負極集電体104上に負極活物質層105を形成すればよい。なお、負極106に導電助剤及びバインダを用いる場合は、適宜、上記列挙した材料から選択し用いることができる。
【0130】
本実施の形態では、負極集電体104としてチタン箔を用い、負極活物質層105として、化学気相成長法又は物理気相成長法により形成したシリコンを用いる。
【0131】
負極活物質層105のシリコンは、非晶質シリコン、微結晶シリコン、多結晶シリコン又は単結晶シリコンなど結晶性を有するシリコンでもよい。
【0132】
例えば、負極活物質層105として、微結晶シリコンを負極集電体104上に形成し、微結晶シリコン中に存在する非結晶シリコンをエッチングにより除去したものを用いてもよい。微結晶シリコン中に存在する非結晶シリコンを除去すると、残った微結晶シリコンの表面積が大きくなる。微結晶シリコンの形成方法としては、例えば、プラズマCVD法又はスパッタリング法を用いることができる。
【0133】
また、負極活物質層105を、負極集電体104上にLP(Low Pressure)CVD装置を用いて形成したウィスカー状のシリコンとしてもよい(図4(A)参照)。なお、本明細書において、ウィスカー状のシリコンとは、共通部201aと、共通部201aから髭状(若しくは紐状又は繊維状)に突出した領域201bとを有するシリコンをいう。
【0134】
ウィスカー状のシリコンが、非晶質シリコンで形成されている場合、イオンの吸蔵及び放出に伴う体積変化に強い(例えば、体積膨張に伴う応力を緩和する)ため、繰り返しの充放電によって、負極活物質層が微粉化及び剥離することを防止でき、サイクル特性がさらに向上した蓄電装置を作製することができる(図4(A)参照)。
【0135】
ウィスカー状のシリコンが、微結晶シリコン、多結晶シリコン、単結晶シリコンのように結晶性を有するシリコンで形成されている場合、導電性及びイオン移動度に優れた結晶性を有する結晶構造が集電体と広範囲に接している。そのため、負極全体の導電性をさらに向上させることができ、さらに高速な充放電が可能となり、充放電容量がさらに向上した蓄電装置を作製することができる(図4(B)参照)。
【0136】
さらに、ウィスカー状のシリコンは、結晶性を有するシリコンで形成された芯202と、非晶質シリコンで形成されていて、芯を覆う外殻204と、で構成されていてもよい(図4(C)参照)。この場合、外殻204である非晶質シリコンは、イオンの吸蔵及び放出に伴う体積変化に強い(例えば、体積膨張に伴う応力を緩和する)という特色を有する。また、芯202である結晶性を有するシリコンは、導電性及びイオン移動度に優れており、イオンを吸蔵する速度及び放出する速度が単位質量あたりで速いという特徴と有する。従って、芯202及び外殻204を有するウィスカー状のシリコンを負極活物質層105として用いることで、高速に充放電が可能となり、充放電容量及びサイクル特性が向上したリチウム二次電池100を作製することができる。
【0137】
なお、共通部201aは、図4(C)のように、芯202を構成する結晶性を有するシリコンが負極集電体104の上面一部と接する形態の他に負極集電体104の上面全てが結晶性を有するシリコンと接する形態であってもよい。
【0138】
また、負極活物質層105の表面にグラフェン又は多層グラフェンを形成する場合は、酸化グラフェンが含まれる溶液に、負極活物質層105を設けた負極集電体104を参照電極と共に浸し、当該溶液を用いて電気泳動法により、負極活物質層105表面に酸化グラフェン層を形成し、これを加熱して還元処理をすることで実施できる。また、負極活物質層105の表面にグラフェン又は多層グラフェンを形成するには、当該溶液を用いたディップコート法でも実施でき、ディップコートした後は、加熱し還元処理すればよい。
【0139】
なお、負極活物質層105にリチウムをプレドープしてもよい。リチウムのプレドープ方法としては、スパッタリング法により負極活物質層105表面にリチウム層を形成すればよい。又は、負極活物質層105の表面にリチウム箔を設けることでも、負極活物質層105にリチウムをプレドープすることができる。
【0140】
電解質107の作製方法は、上記列挙した材料を適宜選択して用いればよい。本実施の形態では、溶質はリチウム塩であるLi(CF3SO2)2Nとし、溶媒はエチレンカーボネートとし、エチレンカーボネートとLi(CF3SO2)2Nを適宜混合してリチウムイオンを含む非水溶液とする。
【0141】
次に、正極103、セパレータ108、及び負極106を電解質107に含浸させる。次に、外部端子109上に、負極106、セパレータ108、ガスケット121、正極103、及び外部端子111の順に積層し、「コインかしめ機」で外部端子109及び外部端子111をかしめれば、コイン型のリチウム二次電池100を作製することができる。
【0142】
なお、外部端子111及び正極103の間、又は外部端子109及び負極106の間に、スペーサー、及びワッシャーを入れて、外部端子111及び正極103の接続、並びに外部端子109及び負極106の接続をより高めてもよい。
【0143】
また、本実施の形態は、他の実施の形態及び実施例に記載した構成と適宜組み合わせて実施することが可能である。
【0144】
(実施の形態3)
本発明の一態様に係る蓄電装置は、電力により駆動する様々な電気機器の電源として用いることができる。
【0145】
本発明の一態様に係る蓄電装置を用いた電気機器の具体例として、表示装置、照明装置、デスクトップ型或いはノート型のパーソナルコンピュータ、DVD(Digital Versatile Disc)などの記録媒体に記憶された静止画又は動画を再生する画像再生装置、携帯電話、携帯型ゲーム機、携帯情報端末、電子書籍、ビデオカメラ、デジタルスチルカメラ、電子レンジ等の高周波加熱装置、電気炊飯器、電気洗濯機、エアコンディショナーなどの空調設備、電気冷蔵庫、電気冷凍庫、電気冷凍冷蔵庫、DNA保存用冷凍庫や透析装置等の医療用電気機器などが挙げられる。また、蓄電装置からの電力を用いて電動機により推進する移動体なども、電気機器の範疇に含まれるものとする。上記移動体として、例えば、電気自動車、内燃機関と電動機を併せ持った複合型自動車(ハイブリッドカー)、電動アシスト自転車を含む原動機付自転車などが挙げられる。
【0146】
なお、上記電気機器は、消費電力の殆ど全てを賄うための蓄電装置(主電源と呼ぶ)として、本発明の一態様に係る蓄電装置を用いることができる。或いは、上記電気機器は、上記主電源や商用電源からの電力の供給が停止した場合に、電気機器への電力の供給を行うことができる蓄電装置(無停電電源と呼ぶ)として、本発明の一態様に係る蓄電装置を用いることができる。或いは、上記電気機器は、上記主電源や商用電源からの電気機器への電力の供給と並行して、電気機器への電力の供給を行うための蓄電装置(補助電源と呼ぶ)として、本発明の一態様に係る蓄電装置を用いることができる。
【0147】
図5に、上記電気機器の具体的な構成を示す。図5において、表示装置5000は、本発明の一態様に係る蓄電装置5004を用いた電気機器の一例である。具体的に、表示装置5000は、TV放送受信用の表示装置に相当し、筐体5001、表示部5002、スピーカー部5003、蓄電装置5004等を有する。本発明の一態様に係る蓄電装置5004は、筐体5001の内部に設けられている。表示装置5000は、商用電源から電力の供給を受けることもできるし、蓄電装置5004に蓄積された電力を用いることもできる。よって、停電などにより商用電源から電力の供給が受けられない時でも、本発明の一態様に係る蓄電装置5004を無停電電源として用いることで、表示装置5000の利用が可能となる。
【0148】
表示部5002には、液晶表示装置、有機EL素子などの発光素子を各画素に備えた発光装置、電気泳動表示装置、DMD(Digital Micromirror Device)、PDP(Plasma Display Panel)、FED(Field Emission Display)などの、半導体表示装置を用いることができる。
【0149】
なお、表示装置には、TV放送受信用の他、パーソナルコンピュータ用、広告表示用など、全ての情報表示用表示装置が含まれる。
【0150】
図5において、据え付け型の照明装置5100は、本発明の一態様に係る蓄電装置5103を用いた電気機器の一例である。具体的に、照明装置5100は、筐体5101、光源5102、蓄電装置5103等を有する。図5では、蓄電装置5103が、筐体5101及び光源5102が据え付けられた天井5104の内部に設けられている場合を例示しているが、蓄電装置5103は、筐体5101の内部に設けられていても良い。照明装置5100は、商用電源から電力の供給を受けることもできるし、蓄電装置5103に蓄積された電力を用いることもできる。よって、停電などにより商用電源から電力の供給が受けられない時でも、本発明の一態様に係る蓄電装置5103を無停電電源として用いることで、照明装置5100の利用が可能となる。
【0151】
なお、図5では天井5104に設けられた据え付け型の照明装置5100を例示しているが、本発明の一態様に係る蓄電装置は、天井5104以外、例えば側壁5105、床5106、窓5107等に設けられた据え付け型の照明装置に用いることもできるし、卓上型の照明装置などに用いることもできる。
【0152】
また、光源5102には、電力を利用して人工的に光を得る人工光源を用いることができる。具体的には、白熱電球、蛍光灯などの放電ランプ、LEDや有機EL素子などの発光素子が、上記人工光源の一例として挙げられる。
【0153】
図5において、室内機5200及び室外機5204を有するエアコンディショナーは、本発明の一態様に係る蓄電装置5203を用いた電気機器の一例である。具体的に、室内機5200は、筐体5201、送風口5202、蓄電装置5203等を有する。図5では、蓄電装置5203が、室内機5200に設けられている場合を例示しているが、蓄電装置5203は室外機5204に設けられていても良い。或いは、室内機5200と室外機5204の両方に、蓄電装置5203が設けられていても良い。エアコンディショナーは、商用電源から電力の供給を受けることもできるし、蓄電装置5203に蓄積された電力を用いることもできる。特に、室内機5200と室外機5204の両方に蓄電装置5203が設けられている場合、停電などにより商用電源から電力の供給が受けられない時でも、本発明の一態様に係る蓄電装置5203を無停電電源として用いることで、エアコンディショナーの利用が可能となる。
【0154】
なお、図5では、室内機と室外機で構成されるセパレート型のエアコンディショナーを例示しているが、室内機の機能と室外機の機能とを1つの筐体に有する一体型のエアコンディショナーに、本発明の一態様に係る蓄電装置を用いることもできる。
【0155】
図5において、電気冷凍冷蔵庫5300は、本発明の一態様に係る蓄電装置5304を用いた電気機器の一例である。具体的に、電気冷凍冷蔵庫5300は、筐体5301、冷蔵室用扉5302、冷凍室用扉5303、蓄電装置5304等を有する。図5では、蓄電装置5304が、筐体5301の内部に設けられている。電気冷凍冷蔵庫5300は、商用電源から電力の供給を受けることもできるし、蓄電装置5304に蓄積された電力を用いることもできる。よって、停電などにより商用電源から電力の供給が受けられない時でも、本発明の一態様に係る蓄電装置5304を無停電電源として用いることで、電気冷凍冷蔵庫5300の利用が可能となる。
【0156】
なお、上述した電気機器のうち、電子レンジ等の高周波加熱装置、電気炊飯器などの電気機器は、短時間で高い電力を必要とする。よって、商用電源では賄いきれない電力を補助するための補助電源として、本発明の一態様に係る蓄電装置を用いることで、電気機器の使用時に商用電源のブレーカーが落ちるのを防ぐことができる。
【0157】
また、電気機器が使用されない時間帯、特に、商用電源の供給元が供給可能な総電力量のうち、実際に使用される電力量の割合(電力使用率と呼ぶ)が低い時間帯において、蓄電装置に電力を蓄えておくことで、上記時間帯以外において電力使用率が高まるのを抑えることができる。例えば、電気冷凍冷蔵庫5300の場合、気温が低く、冷蔵室用扉5302、冷凍室用扉5303の開閉が行われない夜間において、蓄電装置5304に電力を蓄える。そして、気温が高くなり、冷蔵室用扉5302、冷凍室用扉5303の開閉が行われる昼間において、蓄電装置5304を補助電源として用いることで、昼間の電力使用率を低く抑えることができる。
【0158】
なお、本実施の形態は、他の実施の形態又は実施例に記載した構成と適宜組み合わせて実施することが可能である。
【0159】
(実施の形態4)
本実施の形態においては、上記実施の形態で説明した蓄電装置を用いた電気機器の例について図6(A)、図6(B)、及び図6(C)を用いて説明する。
【0160】
図6(A)及び図6(B)は2つ折り可能なタブレット型端末である。図6(A)は、開いた状態であり、タブレット型端末は、筐体9630、表示部9631a、表示部9631b、表示モード切り替えスイッチ9034、電源スイッチ9035、省電力モード切り替えスイッチ9036、留め具9033、操作スイッチ9038、を有する。
【0161】
表示部9631aは、一部をタッチパネルの領域9632aとすることができ、表示された操作キー9638にふれることでデータ入力をすることができる。なお、表示部9631aにおいては、一例として半分の領域が表示のみの機能を有する構成、もう半分の領域がタッチパネルの機能を有する構成を示しているが該構成に限定されない。表示部9631aの全ての領域がタッチパネルの機能を有する構成としても良い。例えば、表示部9631aの全面をキーボードボタン表示させてタッチパネルとし、表示部9631bを表示画面として用いることができる。
【0162】
また、表示部9631bにおいても表示部9631aと同様に、表示部9631bの一部をタッチパネルの領域9632bとすることができる。また、タッチパネルのキーボード表示切り替えボタン9639が表示されている位置に指やスタイラスなどでふれることで表示部9631bにキーボードボタン表示することができる。
【0163】
また、タッチパネルの領域9632aとタッチパネルの領域9632bに対して同時にタッチ入力することもできる。
【0164】
また、表示モード切り替えスイッチ9034は、縦表示又は横表示などの表示の向きを切り替え、白黒表示やカラー表示の切り替えなどを選択できる。省電力モード切り替えスイッチ9036は、タブレット型端末に内蔵している光センサで検出される使用時の外光の光量に応じて表示の輝度を最適なものとすることができる。タブレット型端末は光センサだけでなく、ジャイロ、加速度センサ等の傾きを検出するセンサなどの他の検出装置を内蔵させてもよい。
【0165】
また、図6(A)では表示部9631bと表示部9631aの表示面積が同じ例を示しているが特に限定されず、一方のサイズともう一方のサイズが異なっていてもよく、表示の品質も異なっていてもよい。例えば一方が他方よりも高精細な表示を行える表示パネルとしてもよい。
【0166】
図6(B)は、閉じた状態であり、タブレット型端末は、筐体9630、太陽電池9633、充放電制御回路9634、バッテリー9635、DCDCコンバータ9636を有する。なお、図6(B)では充放電制御回路9634の一例としてバッテリー9635、DCDCコンバータ9636を有する構成について示している。
【0167】
なお、タブレット型端末は2つ折り可能なため、未使用時に筐体9630を閉じた状態にすることができる。従って、表示部9631a、表示部9631bを保護できるため、耐久性に優れ、長期使用の観点からも信頼性の優れたタブレット型端末を提供できる。
【0168】
また、この他にも図6(A)及び図6(B)に示したタブレット型端末は、様々な情報(静止画、動画、テキスト画像など)を表示する機能、カレンダー、日付又は時刻などを表示部に表示する機能、表示部に表示した情報をタッチ入力操作又は編集するタッチ入力機能、様々なソフトウェア(プログラム)によって処理を制御する機能、等を有することができる。
【0169】
タブレット型端末の表面に装着された太陽電池9633によって、電力をタッチパネル、表示部、又は映像信号処理部等に供給することができる。なお、太陽電池9633は、筐体9630の一面又は二面に設けられ、効率的なバッテリー9635の充電を行う構成とすることができるため好適である。なおバッテリー9635としては、本発明の一態様に係る蓄電装置を用いると、小型化を図れる等の利点がある。
【0170】
また、図6(B)に示す充放電制御回路9634の構成、及び動作について図6(C)にブロック図を示し説明する。図6(C)には、太陽電池9633、バッテリー9635、DCDCコンバータ9636、コンバータ9637、スイッチ9650乃至スイッチ9654、表示部9631について示しており、バッテリー9635、DCDCコンバータ9636、コンバータ9637、スイッチ9650乃至スイッチ9654が、図6(B)に示す充放電制御回路9634に対応する箇所となる。
【0171】
外光により太陽電池9633により発電がされる場合の動作の例について説明する。太陽電池9633で発電した電力は、バッテリー9635を充電するための電圧となるようDCDCコンバータ9636で昇圧又は降圧がなされる。そして、表示部9631の動作に太陽電池9633からの電力が用いられる際にはスイッチ9650をオンにし、コンバータ9637で表示部9631に必要な電圧に昇圧又は降圧をすることとなる。また、表示部9631での表示を行わない際には、スイッチ9650をオフにし、スイッチ9652をオンにしてバッテリー9635の充電を行う構成とすればよい。
【0172】
なお太陽電池9633については、発電手段の一例として示したが、特に限定されず、圧電素子(ピエゾ素子)や熱電変換素子(ペルティエ素子)などの他の発電手段によるバッテリー9635の充電を行う構成であってもよい。例えば、無線(非接触)で電力を送受信して充電する無接点電力伝送モジュールや、また他の充電手段を組み合わせて行う構成としてもよい。
【0173】
また、上記実施の形態で説明した蓄電装置を具備していれば、図6に示した電気機器に特に限定されない。
【0174】
本実施の形態は、他の実施の形態に記載した構成と適宜組み合わせて実施することが可能である。
【実施例1】
【0175】
本実施例では、本発明の一態様に係るアルカリ金属ケイ酸塩の一例として、ケイ酸リチウムを合成し、その合成したケイ酸リチウムについて評価した結果を説明する。
【0176】
本実施例における合成方法は、図1及び図2、特に各ステップにおける下線の記載を参照して説明する。なお、本実施例においてアルカリ金属塩は水酸化リチウムであり、水酸化リチウムに対する良溶媒は水とし、水酸化リチウムに対する貧溶媒はエタノールとした。
【0177】
まず、反応容器に水(イオン交換水)400mlを入れ、水を60℃に加熱した。温度を60℃に保ったまま、攪拌装置でこの水を攪拌させながら水酸化リチウム二水和物20.14gを加えて、水酸化リチウム水溶液を作製した(ステップS111)。なお、水酸化リチウム二水和物は完全に溶解するまで攪拌し、作製した水酸化リチウム水溶液のpHは10に調整した。
【0178】
次に、作製した水酸化リチウム水溶液を60℃に保持したまま、シリコン粉末(株式会社高純度化学研究所製、純度99.999%、粒径75μm以下)を3.37g加えて、シリコン粉末が完全に溶解するまでさらに攪拌し、水酸化リチウムとシリコン粉末を液相反応で反応させ、ケイ酸リチウム水溶液を作製した(ステップS112)。なお、当該液相反応で作製されるケイ酸リチウムは、メタケイ酸リチウム(Li2SiO3)が主生成物であるが、副生成物としてオルトケイ酸リチウム(Li4SiO4)及びLi2Si2O5の一方又は双方を含むことがある。当該液相反応の化学反応式を以下に示す。
【0179】
【化1】

【0180】
また、ステップS112において、加えたシリコン粉末の質量は、ステップS111で用いた水酸化リチウムのモル数の1/4に相当する質量である。さらに、本実施例は、ステップS112において、作製したケイ酸リチウム水溶液に対するシリコン濃度が0.3mol/lとなるように、ステップS111で水酸化リチウム水溶液の水量を調整した。
【0181】
次に、回転数500rpm〜600rpmで攪拌されているエタノールにケイ酸リチウム水溶液を加えて、ケイ酸リチウムをエタノール中に析出させた。本実施例では、ケイ酸リチウム水溶液をシリンジに少量計り入れ、エタノール400mlに対して、当該シリンジから40ml/hの速度でエタノールに滴下した。
【0182】
次に、ケイ酸リチウムが析出しているエタノールを濾過してケイ酸リチウムを回収し、回収したケイ酸リチウムを乾燥させた(ステップS113)。本実施例では、加熱温度を80℃とし、真空雰囲気下で2時間加熱を保持した後、室温まで下がる時間を含めて2時間真空雰囲気下を保持し、自然冷却することでケイ酸リチウムを乾燥させた。
【0183】
次に、乾燥させたケイ酸リチウムに第1の加熱処理(第1の焼成)を行った(ステップS114)。本実施例では、加熱温度を520℃とし、窒素雰囲気下で10時間加熱した。
【0184】
次に、ステップS114を経たケイ酸リチウムと水(イオン交換水)50mlとを混合し、回転数300rpm〜400rpmで1時間攪拌して洗浄した。その後、加熱温度を180℃とし、真空雰囲気下で1時間加熱を保持した後、自然冷却で室温にまで下がる時間を含めて2時間真空雰囲気下を保持して、洗浄したケイ酸リチウムを乾燥させた。以上より、白色のケイ酸リチウム1.0gを得た。ステップS111乃至ステップS114を経て得られたケイ酸リチウムはメタケイ酸リチウム(Li2SiO3)であった。なお、本実施例で合成したケイ酸リチウムを化合物Aとする。
【0185】
次に、化合物Aの物性評価について説明する。比較化合物として、市販されているメタケイ酸リチウム(Li2SiO3)を用意した。比較化合物は、化合物Aとは異なる合成方法で合成され、機械的な粉砕により作製されたメタケイ酸リチウムである。
【0186】
〈X線回折法〉
化合物A及び比較化合物を同定するために、X線回折法(X‐ray diffraction:XRD)を用いて評価した。
【0187】
図7(A)には化合物Aの回折パターンを示し、図7(B)には比較化合物の回折パターンを示した。化合物Aの回折パターンはメタケイ酸リチウム(Li2SiO3)の標準回折パターンと同じであり、本実施例に示した合成方法で合成された化合物Aはメタケイ酸リチウムであることが確認された。また、同様に、比較化合物もメタケイ酸リチウムを主成分とすることが確認されたが、図7(B)に示すように、2θが20°〜25°の範囲に炭酸リチウム(Li2CO3)に由来するピークが確認された。これは、比較化合物を作製する際に用いた未反応の原料であると推測される。
【0188】
なお、ステップS112で作製されるケイ酸リチウムには、主生成物のメタケイ酸リチウム(Li2SiO3)の他に副生成物としてオルトケイ酸リチウム(Li4SiO4)及びLi2Si2O5の一方又は双方が含まれることがあるが、本実施例での合成条件によって、最終的に得られるケイ酸リチウムをメタケイ酸リチウム(Li2SiO3)にすることができた。
【0189】
〈SEM観察及び比表面積測定〉
化合物A及び比較化合物の表面形状を観察するために、SEM(Scanning Electron Microscope)観察を行った。図8(A)には化合物Aの平面SEM像を示し、図8(B)には比較化合物の平面SEM像を示した。図8(A)の倍率は10000倍であり、図8(B)の倍率は10000倍である。
【0190】
図8(A)及び(B)より、化合物Aの粒子は、比較化合物の粒子より粒子サイズが小さく、微粒子化されていることが確認できた。さらに、化合物Aの粒子は比較化合物の粒子よりも粒子サイズが均一であることが確認できた。
【0191】
また、気体吸着法を用いて化合物A及び比較化合物の比表面積を測定した。本実施例での比表面積は、自動比表面積細孔分布測定装置トライスターII3020(株式会社島津製作所製)で測定した。なお、当該装置は、試料に窒素を一定期間吸着させた後、吸着した窒素量で当該試料の表面積を測定する装置である。
【0192】
上記装置により測定した化合物Aの比表面積は、80.97m2/gであり、比較化合物の比表面積は、0.71m2/gであった。気体吸着法で測定される比表面積において、粒子サイズ(例えば粒径)が小さく、より微粒子化されている試料ほどその比表面積は大きい傾向にある。従って、本測定からも、化合物Aの粒子サイズは比較化合物の粒子サイズより小さく、より微粒子化されていることが確認できた。
【0193】
〈XPS法〉
化合物A及び比較化合物の組成を定量するために、X線光電子分光法(X−ray photoelectron spectroscopy:XPS)を用いて評価した。
【0194】
表1に、化合物A及び比較化合物の組成及びその定量値(単位atom%)を示した。
【0195】
【表1】

【0196】
表1からわかるように、化合物A及び比較化合物には、不純物元素である炭素(C)が含まれていることが確認されたが、化合物Aに含まれている量は、比較化合物に含まれている量に比べて非常に少ないことが確認された。XRD測定において、未反応の原料であると推測される炭酸リチウム(Li2CO3)が検出されたことは、化合物Aより比較化合物に多く炭素が含まれていることを肯定する結果である。さらに、化合物Aでは検出されなかったが、比較化合物では不純物元素であるナトリウム(Na)が含まれていることが確認された。従って、化合物Aは比較化合物に比べて高純度であることが確認された。
【0197】
以上より、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法は、アルカリ金属ケイ酸塩を機械的な粉砕では困難な粒子サイズにまで、その粒子サイズを揃えて微粒子化することができる。
【0198】
また、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法は、不純物が少なく高純度なアルカリ金属ケイ酸塩を容易に合成することができる。
【実施例2】
【0199】
本実施例では、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法において、析出させるアルカリ金属ケイ酸塩の貧溶媒を変化させた場合について説明する。なお、本実施例においてもアルカリ金属塩は、実施例1と同様に水酸化リチウムとし、水酸化リチウムに対する良溶媒は水とした。
【0200】
まず、実施例1と同様に、ステップS112までの工程を行った。
【0201】
次に、ケイ酸リチウム水溶液を貧溶媒に加えて、ケイ酸リチウムを当該貧溶媒中に析出させた。本実施例では、当該貧溶媒として、メタノール、エタノール、プロパノール、ブタノール及びペンタノール並びにアセトンを用意し、各々の貧溶媒にケイ酸リチウム水溶液を加えた。
【0202】
その後、析出したケイ酸リチウムを回収し、実施例1と同様の条件で回収したケイ酸リチウムを乾燥させた。そして、実施例1と同様に、ステップS114の工程を行った。貧溶媒をメタノールとして作製したケイ酸リチウムを化合物Bとし、貧溶媒をプロパノールとして作製したケイ酸リチウムを化合物Cとし、貧溶媒をブタノールとして作製したケイ酸リチウムを化合物Dとし、貧溶媒をペンタノールとして作製したケイ酸リチウムを化合物Eとし、貧溶媒をアセトンとして作製したケイ酸リチウムを化合物Fとする。
【0203】
次に、化合物B乃至化合物Fを同定するために、X線回折法(X‐ray diffraction:XRD)を用いて評価した。
【0204】
図9(A)に化合物B、図9(B)に化合物C、図9(C)に化合物D、図10(A)に化合物E、図10(B)に化合物Fの回折パターンを示した。図9(A)乃至(C)及び図10(A)並びに図10(B)より、貧溶媒の種類によって得られるケイ酸リチウムの組成に違いがあることが確認された。
【0205】
本実施例で用意した貧溶媒のうち、良溶媒として用いた水に対する親和性は、メタノール、エタノール、プロパノール、ブタノール、ペンタノール及びアセトンの順に低くなる。
【0206】
図9(A)より、良溶媒の水に対する親和性が一番高いメタノールを貧溶媒として用いた場合、得られたケイ酸リチウム(化合物B)は、Li2Si2O5であった。また、図10(B)より、良溶媒の水に対する親和性が一番低いアセトンを貧溶媒として用いた場合、得られたケイ酸リチウム(化合物F)は、オルトケイ酸リチウム(Li4SiO4)であった。
【0207】
また、エタノール、プロパノール、ブタノール及びペンタノールを貧溶媒として用いた場合、得られたケイ酸リチウム(化合物A、及び化合物C乃至化合物E)は、全てメタケイ酸リチウム(Li2SiO3)であった。図11(A)に化合物C、図11(B)に化合物D、図12に化合物Eの平面SEM像を示す。図8(A)、図11(A)、図11(B)、及び図12より、良溶媒として用いた水に対する親和性が変化するにつれて、得られたメタケイ酸リチウム(Li2SiO3)の粒子サイズは異なることが確認された。
【0208】
本実施例より、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法において、析出させるアルカリ金属ケイ酸塩の貧溶媒の良溶媒に対する親和性によって得られるアルカリ金属ケイ酸塩の組成及び粒子サイズが変わることが確認された。従って、所望の組成及び所望の粒子サイズを有するアルカリ金属ケイ酸塩が得られるように、良溶媒及び貧溶媒を選択することが好ましいことが確認された。
【実施例3】
【0209】
本実施例では、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法において、作製したアルカリ金属塩を含む塩基性溶液にシリコン粒子を加える際に、当該塩基性溶液に対するシリコン濃度を変化させた場合について説明する。なお、本実施例においてアルカリ金属塩は、実施例1と同様に水酸化リチウムとし、水酸化リチウムに対する良溶媒は水とした。
【0210】
具体的には、ステップS112の際、作製した水酸化リチウム水溶液に対するシリコン濃度を0.05mol/l、0.1mol/l、0.15mol/l、0.2mol/l、0.25mol/l、0.3mol/l、及び0.5mol/lに変化させた水溶液を用いてケイ酸リチウムを作製し、それぞれの濃度の水溶液を用いて作製されたケイ酸リチウムそれぞれの比表面積を評価した。なお、ケイ酸リチウムを作製する際の他の工程(ステップ)は、実施例1と同様であり、比表面積の測定も実施例1と同様の方法で行った。
【0211】
図13に、作製した水酸化リチウム水溶液に対するシリコン濃度と、得られたケイ酸リチウムの比表面積との関係を示した。なお、得られたケイ酸リチウムは全てメタケイ酸リチウム(Li2SiO3)であった。
【0212】
図13より、得られたケイ酸リチウムの比表面積は、シリコン濃度0.1mol/l以上で全て10m2/g以上60m2/g以下であり、得られるケイ酸リチウムの比表面積は、作製した水酸化リチウム水溶液に対するシリコン濃度に対して極大を有することが確認された。なお、本実施例において、水酸化リチウム水溶液に対するシリコン濃度が0.3mol/lの場合、化合物Aと同じケイ酸リチウムが得られることになるが、ケイ酸リチウムは粉体であるため、全てのケイ酸リチウムで同じ比表面積が常に測定されるわけではなく、ある程度の範囲を有して測定される。そのため、化合物Aが得られる条件でも、本実施例では異なる比表面積の値を示している。
【0213】
本実施例より、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法において、所望の粒子サイズを有するアルカリ金属ケイ酸塩が得られるように、作製したアルカリ金属塩を含む塩基性溶液に対するシリコン濃度を調製することが好ましいと確認できた。
【実施例4】
【0214】
本実施例では、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の一例として、ケイ酸マンガンリチウムを合成し、その合成したケイ酸マンガンリチウムについて評価した結果を説明する。
【0215】
ステップS111からステップS114までは実施例1と同様して行い、メタケイ酸リチウムを合成した。
【0216】
次に、炭酸マンガン(MnCO3)4.0gをボールミル処理にて粉砕した。当該ボールミル処理は、溶媒としてエタノールを添加し、回転数400rpm、回転時間2時間、ボール直径0.5mmの条件で行った。
【0217】
次に、得られたメタケイ酸リチウム2.20g及び炭酸マンガン2.80gをボールミル処理により混合し、メタケイ酸リチウム及び炭酸マンガンの混合物を作製した(ステップS115)。なお、ボールミル処理は、溶媒としてアセトンを添加し、回転数400rpm、回転時間2時間、ボール直径3mmの条件で行った。
【0218】
ボールミル処理後、混合物をポットから取り出し、50℃に加熱してアセトンを蒸発させた。
【0219】
次に、粉体の混合物に第2の加熱処理(第2の焼成)を行った(ステップS116)。本実施例では、加熱温度を700℃とし、窒素雰囲気下で10時間加熱して、ベージュ色の化合物を得た。なお、ステップS111乃至ステップS116を経て得られた化合物を化合物Gとする。
【0220】
以上のステップにより合成した化合物Gを同定するために、X線回折(XRD:X−ray diffraction)を用いて評価した。図14に化合物Gの回折パターンを示した。当該回折パターンより、化合物Gはケイ酸マンガンリチウム(Li2MnSO4)であることが確認された。また、図14の回折パターンには、2θ=40°付近に中間生成物の反応残りである酸化マンガンと推定されるピークは確認されなかった。
【0221】
本実施例より、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法を用いることで、従来、1000℃以上の高温で加熱処理する必要があったことに対して、700℃にまで加熱温度を下げても、中間生成物などの反応残りや未反応の原料を含まずに目的物である遷移金属を含むアルカリ金属ケイ酸塩を合成することができた。従って、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法は、従来の合成方法に比べて、作製コストを節減することができる。また、1回の加熱処理(焼成)で目的物を合成できることから、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法は、従来の合成方法に比べて、作製時間を短縮することができる。
【符号の説明】
【0222】
S111 ステップ
S112 ステップ
S113 ステップ
S114 ステップ
S115 ステップ
S116 ステップ
100 リチウム二次電池
101 正極集電体
102 正極活物質層
103 正極
104 負極集電体
105 負極活物質層
106 負極
107 電解質
108 セパレータ
109 外部端子
111 外部端子
121 ガスケット
201a 共通部
201b 領域
202 芯
204 外殻
5000 表示装置
5001 筐体
5002 表示部
5003 スピーカー部
5004 蓄電装置
5100 照明装置
5101 筐体
5102 光源
5103 蓄電装置
5104 天井
5105 側壁
5106 床
5107 窓
5200 室内機
5201 筐体
5202 送風口
5203 蓄電装置
5204 室外機
5300 電気冷凍冷蔵庫
5301 筐体
5302 冷蔵室用扉
5303 冷凍室用扉
5304 蓄電装置
9630 筐体
9631 表示部
9631a 表示部
9631b 表示部
9632a 領域
9632b 領域
9033 留め具
9034 表示モード切り替えスイッチ
9035 電源スイッチ
9036 省電力モード切り替えスイッチ
9038 操作スイッチ
9639 キーボード表示切り替えボタン
9633 太陽電池
9634 充放電制御回路
9635 バッテリー
9636 DCDCコンバータ
9637 コンバータ
9638 操作キー
【技術分野】
【0001】
本発明は、遷移金属を含むアルカリ金属ケイ酸塩の合成方法と、当該合成方法により作製された遷移金属を含むアルカリ金属ケイ酸塩に関する。
【0002】
また、遷移金属を含むアルカリ金属ケイ酸塩を正極活物質とした正極と、その作製方法に関する。また、当該正極を備えた蓄電装置と、その蓄電装置作製方法に関する。なお、本明細書において蓄電装置とは、蓄電機能を有する素子及び装置全般を指すものである。
【背景技術】
【0003】
近年、リチウム二次電池、リチウムイオンキャパシタなど蓄電装置の開発が行われている。
【0004】
特に、ケイ酸リチウムなどのアルカリ金属ケイ酸塩は、リチウム二次電池等の蓄電装置の正極活物質である、遷移金属を含むケイ酸リチウム塩を合成する際の前駆体となり得る(特許文献1参照)。
【0005】
例えば、遷移金属Mを含むアルカリ金属塩であるリチウムリン酸塩(LiMPO4)及びリチウムケイ酸塩(Li2MSiO4)は、次世代の正極活物質として提案されている。なお、当該遷移金属Mとしては、例えば、鉄(Fe)、マンガン(Mn)、ニッケル(Ni)、又はコバルト(Co)などである。
【0006】
上記LiMPO4及び上記Li2MSiO4は、汎用されている正極活物質であるLiCoO2のような酸化物に比べて、熱安定性が高く、リチウム二次電池の温度が異常上昇した場合でも酸素ガスの発生を抑制でき、引火性電解質の酸化発熱反応を抑制できる。
【0007】
上記LiMPO4は、リチウムイオンの挿入及び脱離が1電子反応によって行われ、LiMPO4の理論容量は約170mAh/gである。一方、Li2MSiO4は、リチウムイオンの挿入及び脱離が2電子反応によって行われることから、Li2MSiO4の理論容量は約330mAh/gと高容量である。それゆえ、Li2MSiO4を正極活物質に用いることで高容量な正極を作製できることが知られている。
【0008】
従来、Li2MSiO4は固相反応よる合成が一般的である。典型的な固相反応法は、各構成元素の供給源となる化合物をボールミルで長時間混合する工程と、650℃以上、さらには1000℃を超える温度で半日以上の加熱処理を複数回行う工程を有する(特許文献2参照)。
【0009】
そして、固相反応により合成した正極活物質を用いて正極を作製する場合、合成した正極活物質を粉砕し、その粉砕した正極活物質を用いて正極を作製する方法が採用されている(特許文献1参照)。
【先行技術文献】
【特許文献】
【0010】
【特許文献1】特開2009−104794号公報
【特許文献2】特開2007−335325号公報
【発明の概要】
【発明が解決しようとする課題】
【0011】
しかし、現状では、正極活物質にLi2MSiO4を用いた際、Li2MSiO4の理論容量に到達するような十分な容量を得ることは難しいとされている。これは、Li2MSiO4はリチウムイオンの拡散性が悪いためである。正極活物質を微粒子化することで、リチウムイオンの拡散距離を短くでき、リチウムイオンの拡散性を向上させることができるが、Li2MSiO4は上記のように固相反応よる合成が一般的であるため、微粒子化が難しい。
【0012】
さらに、従来の固相反応は長時間の加熱処理を伴うので、合成した正極活物質の粒子サイズが増大するという問題がある。このように粒子サイズが増大した正極活物質を用いて正極を作製すると、正極重量あたりの容量が低くなるため、高容量なリチウム二次電池の作製が難しくなる。
【0013】
それゆえ、従来から固相反応によって合成した正極活物質を機械的に粉砕することで粒子サイズを小さくする処理(微粒子化)を行い、その微粒子化した正極活物質を用いて正極を作製する手段が汎用されている。しかし、機械的な粉砕では、小さくできる粒子サイズに下限がある。さらに、機械的な粉砕でも長時間の処理を行えば、粒子サイズを均一にすることが可能であるといえるが、短時間で粒子サイズを均一することは難しい。
【0014】
そこで、本発明の一態様は、蓄電装置の正極活物質として機能し、微粒子化が容易な遷移金属を含むアルカリ金属ケイ酸塩の合成方法を提供することを課題とする。
【0015】
また、本発明の一態様は、上記合成方法を用いて作製した遷移金属を含むアルカリ金属ケイ酸塩を提供することを課題とする。
【0016】
さらに、本発明の一態様は、上記遷移金属を含むアルカリ金属ケイ酸塩の前駆体であるアルカリ金属ケイ酸塩の合成方法、及び当該合成方法を用いて作製したアルカリ金属ケイ酸塩を提供することも課題とする。
【課題を解決するための手段】
【0017】
本発明の一態様は、アルカリ金属塩を含む塩基性溶液を作製し、アルカリ金属塩を含む塩基性溶液とシリコン粒子を混合してアルカリ金属ケイ酸塩を含む塩基性溶液を作製し、アルカリ金属ケイ酸塩を含む塩基性溶液を当該アルカリ金属ケイ酸塩の貧溶媒に加えて、アルカリ金属ケイ酸塩を析出させることを特徴とする、アルカリ金属ケイ酸塩の合成方法である。
【0018】
また、上記したアルカリ金属ケイ酸塩の合成方法において、析出させたアルカリ金属ケイ酸塩を回収し、回収したアルカリ金属ケイ酸塩に加熱処理を行ってもよい。
【0019】
本発明の一態様は、アルカリ金属塩を含む塩基性溶液を作製し、アルカリ金属塩を含む塩基性溶液とシリコン粒子を混合してアルカリ金属ケイ酸塩を含む塩基性溶液を作製し、アルカリ金属ケイ酸塩を含む塩基性溶液を当該アルカリ金属ケイ酸塩の貧溶媒に加えて、アルカリ金属ケイ酸塩を析出させ、析出させたアルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合して混合物を作製し、混合物に加熱処理を行い、遷移金属を含むアルカリ金属ケイ酸塩を生成することを特徴とする、遷移金属を含むアルカリ金属ケイ酸塩の合成方法である。
【0020】
また、上記した遷移金属を含むアルカリ金属ケイ酸塩の合成方法において、析出させたアルカリ金属ケイ酸塩を回収し、回収したアルカリ金属ケイ酸塩に第1の加熱処理を行い、加熱処理したアルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合して混合物を作製し、混合物に第2の加熱処理を行って、遷移金属を含むアルカリ金属ケイ酸塩を生成してもよい。
【0021】
アルカリ金属塩を含む塩基性溶液は、pHが9以上であることが好ましい。また、貧溶媒に加えるアルカリ金属ケイ酸塩を含む塩基性溶液は、pHが9以上であることが好ましい。
【0022】
アルカリ金属塩を含む塩基性溶液の温度は、50℃以上70℃以下に保持することが好ましい。
【0023】
アルカリ金属ケイ酸塩の1つであるケイ酸リチウムの合成は、アルカリ金属塩を含む塩基性溶液を水酸化リチウム水溶液とし、貧溶媒は直鎖アルコール又はアセトンとすることで実施できる。
【0024】
上記したアルカリ金属ケイ酸塩の合成方法を用いることで、気体吸着法で測定される比表面積が50m2/g以上90m2/g以下であるアルカリ金属ケイ酸塩を合成することができる。
【0025】
また、上記したアルカリ金属ケイ酸塩の合成方法を用いることで、X線光電子分光法によって定量される炭素原子が10atom%以下であり、X線光電子分光法によって定量されるナトリウム原子が1atom%以下であるとするアルカリ金属ケイ酸塩を合成することができる。
【0026】
遷移金属を含むアルカリ金属ケイ酸塩の合成方法において、微粒子化した遷移金属を含む化合物の遷移金属は、鉄、マンガン、ニッケル又はコバルトのうちいずれか一以上である。特に、列挙した遷移金属の炭酸塩を用いることが好ましい。
【0027】
また、上記した遷移金属を含むアルカリ金属ケイ酸塩の合成方法において、析出させたアルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合した混合物に行う加熱処理(第2の加熱処理)は、700℃以上1000℃以下の不活性ガス雰囲気下で行うことが好ましい。
【0028】
上記した遷移金属を含むアルカリ金属ケイ酸塩の合成方法を用いることで、気体吸着法で測定される比表面積が50m2/g以上150m2/g以下である遷移金属を含むアルカリ金属ケイ酸塩を合成することができる。
【発明の効果】
【0029】
本発明の一態様により、微粒子化が容易である遷移金属を含むアルカリ金属ケイ酸塩の合成方法を提供することができ、特に、微粒子化が容易である遷移金属を含むリチウムケイ酸塩の合成方法を提供することができる。
【0030】
また、本発明の一態様により、粒子サイズが揃い、微粒子化された遷移金属を含むアルカリ金属ケイ酸塩を提供することができ、特に、粒子サイズが揃い、微粒子化された遷移金属を含むケイ酸リチウムを提供することができる。
【0031】
さらに、本発明の一態様により、遷移金属を含むアルカリ金属ケイ酸塩の前駆体であるアルカリ金属ケイ酸塩の合成方法、及び当該合成方法を用いて作製したアルカリ金属ケイ酸塩を提供することができる。
【0032】
本発明の一態様により、微粒子化された遷移金属を含むアルカリ金属ケイ酸塩を、蓄電装置の正極活物質として用いることで、正極重量あたりの容量が増大した正極を作製でき、高容量なリチウム二次電池を作製することできる。
【図面の簡単な説明】
【0033】
【図1】アルカリ金属ケイ酸塩の合成方法を説明する図。
【図2】遷移金属を含むアルカリ金属ケイ酸塩の合成方法を説明する図。
【図3】蓄電装置の一形態を説明するための断面図。
【図4】蓄電装置の負極の一態様を説明するための断面図。
【図5】蓄電装置の応用の形態を説明するための図。
【図6】蓄電装置の応用の形態を説明するための図。
【図7】化合物Aと比較化合物のX線回折パターン。
【図8】化合物Aと比較化合物の平面SEM像。
【図9】化合物B乃至化合物DのX線回折パターン。
【図10】化合物E及び化合物FのX線回折パターン。
【図11】化合物C及び化合物Dの平面SEM像。
【図12】化合物Eの平面SEM像。
【図13】ケイ酸リチウムの比表面積と作製した水酸化リチウム水溶液に対するシリコン濃度との関係を示す図。
【図14】化合物GのX線回折パターン。
【発明を実施するための形態】
【0034】
本明細書において、実施の形態及び実施例は図面を用いて以下に説明する。但し、本発明は以下の説明に限定されず、本発明の趣旨及びその範囲から逸脱することなくその形態及び詳細を様々に変更し得ることは当業者であれば容易に理解される。従って、本発明は以下に示す実施の形態の記載内容に限定して解釈されるものではないとする。なお、説明中に図面を参照するにあたり、同じものを指す符号は異なる図面間でも共通して用いる場合がある。また、同様のものを指す際には同じハッチパターンを使用し、特に符号を付さない場合がある。
【0035】
(実施の形態1)
本実施の形態では、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法ついて、以下、図面を参照して詳細に説明する。なお、具体的な合成例として、遷移金属をマンガンとし、アルカリ金属をリチウムとしたケイ酸マンガンリチウムの合成例を説明する。
【0036】
本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法は、前駆体であるアルカリ金属ケイ酸塩を合成し、その後、当該前駆体と微粒子化した遷移金属を含む化合物を反応させる合成方法である。例えば、ケイ酸マンガンリチウムの場合、始めに前駆体であるケイ酸リチウムを合成し、その後、ケイ酸リチウムと微粒子化したマンガン塩を反応させることで合成できる。
【0037】
〈前駆体の合成〉
そこで、始めに、前駆体であるアルカリ金属ケイ酸塩の合成方法について記載する。
【0038】
図1は、アルカリ金属ケイ酸塩の合成方法を説明する図である。なお、図1に示した各ステップにおいて、下線の記載は、ケイ酸マンガンリチウムの前駆体であるケイ酸リチウムを合成する場合の説明である。
【0039】
〈ステップS111〉
ステップS111として、アルカリ金属塩を含む塩基性溶液を作製する。当該アルカリ金属塩は、アルカリ金属ケイ酸塩におけるアルカリ金属源として機能する。
【0040】
具体的には、アルカリ金属塩を当該アルカリ金属塩の良溶媒に溶解させて、塩基性溶液を作製する。当該塩基性溶液は塩基性が強いほど、後述のステップS112において、シリコン粒子が当該塩基性溶液に溶解しやすくなり、ステップS112を効率的に行うことができる。そこで、当該塩基性溶液は水素イオン指数(pH)が9以上となるように調整することが好ましく、例えば当該塩基性溶液はpHが10程度となるように調整すればよい。
【0041】
また、アルカリ金属塩を含む塩基性溶液の作製は、アルカリ金属塩が溶解しやすいように良溶媒を加熱及び保温しながら行うことが好ましい。
【0042】
なお、ケイ酸リチウムを合成する場合、ステップS111として、アルカリ金属塩として水酸化リチウムを用いて、良溶媒を水とし、pHが10の水酸化リチウム水溶液を作製する。
【0043】
〈ステップS112〉
次に、ステップS112として、アルカリ金属ケイ酸塩を含む塩基性溶液を作製する。
【0044】
具体的には、アルカリ金属ケイ酸塩のシリコン源としてシリコン粒子を用意して、ステップS111で作製したアルカリ金属塩を含む塩基性溶液に当該シリコン粒子を加えて攪拌する。このように攪拌することで、アルカリ金属塩とシリコン粒子は水素ガスを放出しながら反応し、アルカリ金属ケイ酸塩が形成される。なお、当該アルカリ金属ケイ酸塩は、ステップS111で用いたアルカリ金属塩の良溶媒に溶解している。
【0045】
また、ステップS112で攪拌する方法としては、棒状、板状、プロペラ状の攪拌子を備えた装置(例えば、マグネチックスターラー及びメカニカルスターラー)などを用いて機械的に攪拌する方法を用いることができる。
【0046】
また、ステップS112において、機械的に攪拌する代わりに、シリコン粒子を加えたアルカリ金属塩を含む塩基性溶液に超音波を印加して、アルカリ金属塩とシリコンを反応させて、アルカリ金属ケイ酸塩を形成してもよい。
【0047】
なお、ステップS112において、加えたシリコン粒子がアルカリ金属塩を含む塩基性溶液中に局在しないように、常に攪拌しておくことが好ましい。
【0048】
また、ステップS112の反応によって、組成が異なる複数種のアルカリ金属ケイ酸塩が形成される場合がある。つまり、ステップS112を経て作製されたアルカリ金属ケイ酸塩を含む塩基性溶液には、組成が異なる複数種のアルカリ金属ケイ酸塩が含まれていてもよい。
【0049】
ステップS112は液相反応であることから、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法は液相反応を用いた合成方法である。
【0050】
ステップS112で用いるシリコン粒子は、できる限り高純度のシリコン粒子であること好ましいが、他の金属元素、シリコン酸化物及びシリコン窒化物の一以上が含まれているシリコン粒子であってもよい。例えば、公知のシリコン粉末を用いることができる。
【0051】
また、ステップS112において、シリコン粒子はアルカリ金属塩を含む塩基性溶液に溶解するまで攪拌すればよいので、シリコン粒子の粒子サイズ(例えば粒径)に特に限定はない。ただし、シリコン粒子の粒子サイズ(例えば粒径)は小さいほど、アルカリ金属塩を含む塩基性溶液にシリコン粒子を溶解させやすいことから、シリコン粒子はできる限り粒子サイズの小さいものを用いることが好ましい。
【0052】
また、ステップS112の液相反応は、ステップS111で作製したアルカリ金属塩を含む塩基性溶液の温度を室温より高くすることで、シリコン粒子を当該塩基性溶液に溶解させやすくなり、当該液相反応を効率的に進行させることができる。
【0053】
例えば、ステップS111で作製したアルカリ金属塩を含む塩基性溶液の温度を50℃以上70℃以下、好ましくは60℃程度にすることで、ステップS112の液相反応を効率的に進行させることができる。
【0054】
また、本発明の一態様に係る合成方法において、アルカリ金属ケイ酸塩の比表面積を大きく(別言すると粒子サイズを小さく)するには、シリコン粒子を加えたアルカリ金属塩を含む塩基性溶液中のシリコン濃度を高くすることが好ましいが、当該シリコン濃度とアルカリ金属ケイ酸塩の比表面積との関係には極大を有することがあるため、所望の比表面積が得られるように当該シリコン濃度を適宜選択することが好ましい。例えば、当該濃度は0.3mol/l程度とすればよい。
【0055】
また、ステップS112において、アルカリ金属塩がシリコン粒子より過剰となるようにシリコン粒子を混合することが好ましい。つまり、シリコン粒子を加えたアルカリ金属塩を含む塩基性溶液中において、シリコンのモル数よりもアルカリ金属のモル数が過剰となるようにシリコン粒子を加えることが好ましい。このようにすることで、未反応のシリコンを減少させることができ、目的物のアルカリ金属ケイ酸塩の収率を向上させることができる。また、ステップS112(特に、シリコン粒子を加えたアルカリ金属塩を含む塩基性溶液中)において、シリコンのモル数及びアルカリ金属のモル数の比率を変化させることで、当該比率に対応した組成を有するアルカリ金属ケイ酸塩を形成することができる。
【0056】
なお、ケイ酸リチウムを合成する場合、ステップS112として、ステップS111で作製した水酸化リチウム水溶液を60℃に加熱し、60℃に保った水酸化リチウム水溶液にシリコン粒子を加えて機械的に攪拌し、水酸化リチウムとシリコンを反応させてケイ酸リチウム水溶液を作製する。
【0057】
〈ステップS113〉
次に、ステップS113として、ステップS112で作製したアルカリ金属ケイ酸塩を含む塩基性溶液から、アルカリ金属ケイ酸塩を回収する。
【0058】
具体的には、アルカリ金属ケイ酸塩の貧溶媒を用意し、当該貧溶媒にステップS112で作製したアルカリ金属ケイ酸塩を含む塩基性溶液を加えて、貧溶媒中にアルカリ金属ケイ酸塩を析出させる。析出させた後、濾過、遠心分離又は透析など、いずれか一以上の操作を行い、アルカリ金属ケイ酸塩を回収する。その後、回収したアルカリ金属ケイ酸塩を乾燥させる。
【0059】
ステップS113において、アルカリ金属塩の良溶媒と目的物のアルカリ金属ケイ酸塩の貧溶媒は混和するが、貧溶媒の良溶媒に対する親和性によって、析出するアルカリ金属ケイ酸塩の組成が異なることがある。例えば、良溶媒に対する親和性が小さい場合、アルカリ金属のシリコンに対する組成が大きいアルカリ金属ケイ酸塩が析出する傾向にある。また、貧溶媒の良溶媒に対する親和性によって、析出するアルカリ金属ケイ酸塩の組成が同じでも、粒子サイズが異なることがある。そこで、所望の組成及び所望の粒子サイズを有するアルカリ金属ケイ酸塩が析出するように貧溶媒を適宜選択することが好ましい。
【0060】
例えば、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩を蓄電装置の正極活物質として用いる場合、遷移金属を含むアルカリ金属ケイ酸塩の気体吸着法で測定される比表面積は、50m2/g以上150m2/g以下(好ましくは、50m2/g以上70m2/g以下)であることが好ましい。そこで、前駆体であるアルカリ金属ケイ酸塩の気体吸着法で測定される比表面積は、50m2/g以上90m2/g以下となるように形成することが好ましい。なお、遷移金属を含むアルカリ金属ケイ酸塩及びアルカリ金属ケイ酸塩において、その粒子サイズと、気体吸着法での比表面積とには相関があり、この比表面積が大きいほど、粒子サイズ(例えば粒径)は小さい傾向にある。また、気体吸着法での比表面積は、自動比表面積細孔分布測定装置トライスターII3020(株式会社島津製作所製)で測定できる。さらに当該装置は、試料に窒素を一定期間吸着させた後、吸着した窒素量で当該試料の表面積を測定する装置である。
【0061】
貧溶媒中にアルカリ金属ケイ酸塩を析出させるには様々な方法を用いることができる。例えば、アルカリ金属ケイ酸塩を含む塩基性溶液を貧溶媒に滴下することでアルカリ金属ケイ酸塩を析出させることができる。また、攪拌している貧溶媒、又は超音波を印加している貧溶媒に、一定量の当該塩基性溶液を加えることでも目的物のアルカリ金属ケイ酸塩を析出させることができる。なお、貧溶媒の量は、加えるアルカリ金属ケイ酸塩を含む塩基性溶液より多いものとし、貧溶媒の攪拌は、ステップS112と同様の装置を用いて機械的に攪拌すればよい。
【0062】
貧溶媒にアルカリ金属ケイ酸塩を含む塩基性溶液を滴下する方法において、貧溶媒の量は、最終的に供給したアルカリ金属ケイ酸塩を含む塩基性溶液の量より多くする。この滴下する方法は、上記した他の方法に比べて、粒子サイズが小さく、その粒子サイズが揃ったアルカリ金属ケイ酸塩を析出させることができるため好ましい。アルカリ金属ケイ酸塩の粒子サイズを小さくするには、当該塩基性溶液を滴下する速度を遅く、その液滴のサイズは小さく制御することが好ましい。液滴のサイズを小さくするには、一度に滴下する液量を少なくすること、又は滴下する器具のノズル口径を小さくすればよい。なお、本明細書において、滴下する速度とは、1時間あたりに供給する液量をいう。例えば、貧溶媒に対して、滴下する速度は40ml/h以上80ml/h以下が好ましい。
【0063】
また、貧溶媒にアルカリ金属ケイ酸塩を含む塩基性溶液を滴下する際は、貧溶媒を攪拌しながら行うことが好ましい。攪拌する方法としては、ステップS112と同様の装置を用いて機械的に攪拌してもよく、超音波を印加してもよい。なお、攪拌する条件(回転数など)によっても析出するアルカリ金属ケイ酸塩の粒子サイズが変化するため、攪拌する条件は適宜選択することが好ましい。
【0064】
濾過、遠心分離及び透析などからいずれか一以上の操作を行って回収したアルカリ金属ケイ酸塩の乾燥は、真空雰囲気又は不活性ガス雰囲気で加熱すればよい。また、加熱する時間及び温度は、回収したアルカリ金属ケイ酸塩に含まれる溶媒(ステップS111の良溶媒及びステップS113の貧溶媒)を除去できる時間及び温度であればよく、当該良溶媒の沸点及び当該貧溶媒の沸点などを考慮して適宜選択すればよい。例えば、80℃以上200℃以下の温度で1時間以上3時間以下保持して真空乾燥すればよい。また、当該乾燥は昇温レートと降温レートに制限はなく、自然冷却を開始してから十分な時間、真空雰囲気下を保持してもよい。
【0065】
なお、ケイ酸リチウムを合成する場合、ステップS113として、ケイ酸リチウムの貧溶媒であるエタノールにケイ酸リチウム水溶液を40ml/h程度の速度で滴下し、エタノール中にケイ酸リチウムを析出させる。その後、濾過して析出したケイ酸リチウムを回収し、80℃真空雰囲気下で2時間加熱を保持し、その後、室温まで下がる時間を含めて2時間真空雰囲気下で保持、自然冷却する。
【0066】
また、ケイ酸リチウムを合成する場合、ステップS113として、ケイ酸リチウムの貧溶媒であるエタノールの代わりにメタノール、プロパノール、ブタノール、ペンタノール、又はアセトンなどを用いることができる。
【0067】
〈ステップS114〉
次に、乾燥させたアルカリ金属ケイ酸塩に第1の加熱処理(第1の焼成と言い換えてもよい。)を行う。なお、第1の加熱処理は昇温過程、加熱保持過程及び降温過程を備えるものとし、特に断りが無い限り、「加熱処理の時間」とは、加熱保持過程の時間のことをいう。
【0068】
ステップS114での第1の加熱処理の条件によって、アルカリ金属ケイ酸塩の粒子サイズは増大することがある。第1の加熱処理の温度が高いと当該粒子サイズは増大する傾向にあり、第1の加熱処理の時間が長いと当該粒子サイズは増大する傾向にある。そのため、第1の加熱処理の温度はできる限り低い方が好ましく、第1の加熱処理の時間もできる限り短い方が好ましい。
【0069】
第1の加熱処理の一例は以下の通りである。第1の加熱処理を行う雰囲気は、真空雰囲気下又は不活性ガス雰囲気下とし、第1の加熱処理の温度は500℃以上600℃以下とし、第1の加熱処理の時間は、1時間以上24時間以下、好ましくは10時間以上15時間以下として行う。
【0070】
ステップS114において、第1の加熱処理の回数は、アルカリ金属ケイ酸塩の合成にかかるタクトタイムを短くすることができるため、1回とすればよいが、複数回行ってもよい。さらに、1回の加熱処理(1回の焼成)は、仮焼成及び本焼成というように2段階に分けて行ってもよく、この場合、本焼成は仮焼成より高温で行うことが好ましい。
【0071】
また、ステップS113の乾燥と第1の加熱処理は同一の加熱装置を用いて連続して行ってもよく、このようにすることで、アルカリ金属ケイ酸塩の合成にかかるタクトタイムを短くすることができる。なお、ステップS113の乾燥は仮焼成であり、ステップS114の加熱処理は本焼成であるともいえる。
【0072】
なお、第1の加熱処理の条件によって、アルカリ金属ケイ酸塩の組成が変化することがある。従って、所望の組成となるように第1の加熱処理の条件を適宜選択することが好ましい。
【0073】
また、図1には示していないが、ステップS114の後のアルカリ金属ケイ酸塩を洗浄してもよい。このように洗浄することで、ステップS112で過剰に存在していたアルカリ金属塩を除去することができる。洗浄する溶媒に特に限定はないが、例えば水などを用いることができる。そして、洗浄した後は、ステップS113で記載した乾燥を行うことが望ましい。
【0074】
なお、第1の加熱処理を行わず、後述の第2の加熱処理に第1の加熱処理を兼ねさせてもよい。
【0075】
また、遷移金属を含むアルカリ金属ケイ酸塩の前駆体であるアルカリ金属ケイ酸塩の合成において、所望の組成とは異なる組成を有するアルカリ金属ケイ酸塩が生成された場合は、適宜精製し、所望の組成を有するアルカリ金属ケイ酸塩を回収すればよい。
【0076】
以上のステップにより、遷移金属を含むアルカリ金属ケイ酸塩の前駆体であるアルカリ金属ケイ酸塩を合成することができる。
【0077】
なお、ケイ酸リチウムを合成する場合、ステップS114として、乾燥したケイ酸リチウムに520℃窒素雰囲気下で10時間の加熱処理を行う。その後、水で1時間洗浄し、180℃真空雰囲気下で1時間加熱し、その後、室温まで下がる時間を含めて2時間真空雰囲気下を保持し、自然冷却する。以上のステップにより、ケイ酸マンガンリチウムの前駆体であるケイ酸リチウムを合成できる。
【0078】
蓄電装置用の正極活物質として機能する、遷移金属を含むアルカリ金属ケイ酸塩の粒子サイズは、前駆体であるアルカリ金属ケイ酸塩の粒子サイズを反映する。詳細には、前駆体であるアルカリ金属ケイ酸塩の粒子サイズが大きいと、最終的に得られる遷移金属を含むアルカリ金属ケイ酸塩の粒子サイズは大きくなる。それゆえ、微粒子化された前駆体と、微粒子化された遷移金属を含む化合物と、を反応させることによって、微粒子化された遷移金属を含むアルカリ金属ケイ酸塩を容易に合成することができる。つまり、前駆体であるアルカリ金属ケイ酸塩の粒子サイズを小さくして(微粒子化して)合成することは、遷移金属を含むアルカリ金属ケイ酸塩の粒子サイズを小さくする(微粒子化する)ために、極めて有用である。
【0079】
また、最終的に得られる遷移金属を含むアルカリ金属ケイ酸塩は、機械的強度が高く、機械的に粉砕して粒子サイズを小さくする(微粒子化する)ことが難しい場合がある。それゆえ、前駆体であるアルカリ金属ケイ酸塩の粒子サイズを小さくして(微粒子化して)合成することは、遷移金属を含むアルカリ金属ケイ酸塩の粒子サイズを小さくする(微粒子化する)ために、極めて有用である。
【0080】
〈目的物の合成〉
次に、合成した前駆体のアルカリ金属ケイ酸塩から、目的物である遷移金属を含むアルカリ金属ケイ酸塩を合成する方法について図2を参照して説明する。なお、図2に示した各ステップにおいて、下線の記載は、前駆体のケイ酸リチウムから目的物であるケイ酸マンガンリチウムを合成する場合の各ステップにおける説明である。
【0081】
〈ステップS115〉
まず、ステップS111乃至ステップS114を経て合成されたアルカリ金属ケイ酸塩と、微粒子化された遷移金属を含む化合物を混合して混合物を作製する。目的物である遷移金属を含むアルカリ金属ケイ酸塩の組成に応じて、当該アルカリ金属ケイ酸塩と、微粒子化された遷移金属を含む化合物の混合量を調整する。例えば、アルカリ金属の組成を遷移金属の組成に対して2倍とする場合、アルカリ金属ケイ酸塩と遷移金属を含む化合物のモル比が2となるように両化合物の混合量を調整する。
【0082】
遷移金属を含む化合物は、あらかじめ微粒子化しておくことが好ましい。微粒子化する方法としては、機械的に粉砕する、又は超音波を印加して粉砕しておけばよい。例えば、あらかじめ遷移金属を含む化合物だけを先に、後述するボールミル処理で機械的に粉砕し、微粒子化しておけばよい。
【0083】
また、機械的に粉砕し、微粒子化した遷移金属を含む化合物を、所望の孔径を有するフィルタ(例えば、メンブレンフィルタ)などを通過させる操作をしてもよい。この操作を行うことで、微粒子化した遷移金属を含む化合物において、粒子サイズの大きなものを除去すると共に粒子サイズを均一化することができる。
【0084】
また、遷移金属を含む化合物は、あらかじめ微粒子化しておくことで、アルカリ金属ケイ酸塩と遷移金属を含む化合物を均一に混合することができ、目的物である遷移金属を含むアルカリ金属ケイ酸塩を微粒子化することができる。さらに、目的物である遷移金属を含むアルカリ金属ケイ酸塩の結晶性を高めることもできる。
【0085】
遷移金属を含む化合物としては、鉄、マンガン、ニッケル又はコバルトのいずれか一以上を含む化合物であればよく、好ましくは、鉄、マンガン、ニッケル又はコバルトのいずれか一以上を含む炭酸塩を用いる。
【0086】
具体的に、アルカリ金属ケイ酸塩と、微粒子化された遷移金属を含む化合物の混合物はボールミル処理によって作製できる。ボールミル処理は、アルカリ金属ケイ酸塩及び遷移金属を含む化合物と、溶媒と、ボールと、を装置(ボールミル用ポット)に入れて混合を行う。溶媒としては、アセトン、又はエタノールなどのアルコールを用いることができ、混合した後、混合物を加熱して溶媒を除去することが好ましい。ボールは、金属製又はセラミック製等を用いることができる。ボールミル処理は、回転数50rpm以上500rpm以下、回転時間30分間以上5時間以下、ボール径φ0.5mm以上10mm以下で行う。
【0087】
また、アルカリ金属ケイ酸塩と、微粒子化された遷移金属を含む化合物の混合物を、所望の孔径を有するフィルタ(例えば、メンブレンフィルタ)などを通過させる操作をしてもよい。この操作を行うことで、粒子サイズの大きな混合物を除去すると共に粒子サイズを均一化することができる。
【0088】
なお、ケイ酸マンガンリチウムを合成する場合、ステップS115として、ケイ酸リチウムと、あらかじめ機械的に粉砕し、微粒子化した炭酸マンガンと、を所望の組成となるようにモル数比を調整し、溶媒をアセトンとしてボールミル処理を行い、混合物を作製する。なお、ボールミル処理後、当該混合物を加熱して溶媒のアセトンを蒸発させる。
【0089】
〈ステップS116〉
次に、ステップS115で作製された混合物に第2の加熱処理(第2の焼成ともいう。)を行う。
【0090】
第1の加熱処理と同様に、第2の加熱処理の条件(加熱温度及び加熱時間)によって、目的物である遷移金属を含むアルカリ金属ケイ酸塩の粒子サイズは増大することがある。
【0091】
第2の加熱処理の一例は以下の通りである。加熱処理(焼成)を行う雰囲気は、真空雰囲気下又は不活性ガス雰囲気下とし、加熱温度は700℃以上1100℃以下とし、加熱時間は、昇温過程及び降温過程を含めて1時間以上24時間以下、好ましくは加熱時間10時間以上15時間以下として行う。
【0092】
また、第2の加熱処理を行う際、前駆体であるアルカリ金属ケイ酸塩の粒子サイズが小さく、微粒子化されているほど、第2の加熱処理の加熱温度を下げることができる。上記第2の加熱処理の加熱温度は、遷移金属がマンガンである場合において、比較的低温といえる温度である。なお、焼成温度は1100℃以上としてもよい。
【0093】
ステップS116において、第2の加熱処理の回数は、1回とすればよいが、複数回行ってもよい。第2の加熱処理の回数を1回とすれば、目的物である遷移金属を含むアルカリ金属ケイ酸塩の合成にかかるタクトタイムを短くすることができるため、生産性を向上させることができる。
【0094】
さらに、1回の加熱処理(焼成)は、仮焼成及び本焼成というように2段階に分けて行ってもよく、この場合、本焼成は仮焼成より高温で行うことが好ましい。このように1回の加熱処理(焼成)を2段階に分けて行うことで、目的物である遷移金属を含むアルカリ金属ケイ酸塩の結晶性を向上させることができる。
【0095】
なお、第2の加熱処理を行う前に、混合物に加圧処理を行ってもよい。例えば、混合物をペレットに成型したものに第2の加熱処理を行うことができる。
【0096】
なお、ケイ酸マンガンリチウムを合成する場合、ステップS116としては、ステップS115で作製した混合物を粉体のまま窒素雰囲気下で、加熱温度700℃10時間の加熱処理を行う。
【0097】
以上のステップより、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩を合成することができる。
【0098】
本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法は、粒子サイズを小さくした(微粒子化した)アルカリ金属ケイ酸塩を前駆体とすることから、前駆体と遷移金属を含む化合物との混合物の加熱処理回数を1回に減らすことができ、加熱時間を短縮することができ、さらに加熱温度を低くすることができる。従って、加熱時間が長くなることで伴う粒子サイズの増大、及び加熱温度の高温化に伴う粒子サイズの増大を抑制することができるため、微粒子化された遷移金属を含むアルカリ金属ケイ酸塩を容易に合成することができる。
【0099】
本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法によって合成された遷移金属を含むアルカリ金属ケイ酸塩は、粒子サイズが小さく微粒子化されていることから、従来の固相反応により合成された遷移金属を含むアルカリ金属ケイ酸塩に比べて、粒子1つあたりの重量が軽い。さらに、粒子サイズが小さく微粒子化されていることから、リチウムイオンの拡散性が向上している。従って、本発明の一態様に係る微粒子化された遷移金属を含むアルカリ金属ケイ酸塩を蓄電装置の正極活物質に用いることで、正極重量あたりの容量が増大した正極を容易に作製することができる。さらには、高容量なリチウム二次電池を作製することできる。
【0100】
また、本実施の形態は、他の実施の形態及び実施例に記載した構成と適宜組み合わせて実施することが可能である。
【0101】
(実施の形態2)
本実施の形態では、本発明の一態様に係る蓄電装置について説明する。具体的には、実施の形態1で説明した遷移金属を含むアルカリ金属ケイ酸塩を正極活物質に適用した蓄電装置について説明する。
【0102】
本発明の一態様に係る蓄電装置は、少なくとも、正極、負極、セパレータ、及び電解質で構成される。
【0103】
また、本発明の一態様に係る蓄電装置は、アルカリ金属イオン、アルカリ土類金属イオン、ベリリウムイオン、又はマグネシウムイオンをキャリアイオンとする。なお、アルカリ金属イオンとしては、例えばリチウムイオン、ナトリウムイオン、又はカリウムイオンがある。アルカリ土類金属イオンとしては、例えばカルシウムイオン、ストロンチウムイオン、又はバリウムイオンがある。
【0104】
本実施の形態では、本発明の一態様に係る蓄電装置の一例として、キャリアイオンをリチウムイオンとしたリチウム二次電池を説明する。
【0105】
図3にリチウム二次電池100の断面図を示す。リチウム二次電池100は、正極集電体101及び正極活物質層102で構成される正極103と、負極集電体104及び負極活物質層105で構成される負極106と、正極103及び負極106で挟持されるセパレータ108とで構成される。なお、セパレータ108中には電解質107が含まれる。また、正極集電体101は外部端子111と接続し、負極集電体104は外部端子109と接続されている。外部端子111の端部はガスケット121に埋没されている。すなわち、外部端子109、111は、ガスケット121によって絶縁されている。
【0106】
正極集電体101には、例えば導電材料などを用いることができ、導電材料としては、例えばアルミニウム(Al)、銅(Cu)、ニッケル(Ni)、又はチタン(Ti)を用いることができる。また、正極集電体101としては、上記導電材料のうち複数からなる合金材料を用いることもでき、合金材料としては、例えばAl−Ni合金、又はAl−Cu合金などを用いることもできる。また、別途基板上に形成することにより設けられた導電層を剥離して正極集電体101として用いることもできる。
【0107】
正極活物質層102は、正極活物質、バインダ及び導電助剤を含む。正極活物質としては、実施の形態1で説明した遷移金属を含むアルカリ金属ケイ酸塩を用いることができる。本実施の形態ではリチウム二次電池を例に説明するため、正極活物質としてリチウムを含む材料を用いる。そこで、遷移金属を含むアルカリ金属ケイ酸塩は、遷移金属を含むリチウムケイ酸塩を用いることができ、例えば、ケイ酸マンガンリチウム(Li2MnSiO4)を用いることができる。
【0108】
実施の形態1で説明した遷移金属を含むアルカリ金属ケイ酸塩は、粒子サイズが小さく微粒子化されていることから、従来の固相反応により合成された遷移金属を含むアルカリ金属ケイ酸塩に比べて粒子1つあたりの重量が軽く、さらにリチウムイオンの拡散性が向上している。そのため、正極103の重量を低減させることができ、正極重量あたりの容量を増大させることができる。結果として、従来に比べてリチウム二次電池の容量を向上させることができる。
【0109】
バインダとしては、澱粉、カルボキシメチルセルロース、ヒドロキシプロピルセルロース、再生セルロース、ジアセチルセルロースなどの多糖類や、ポリビニルクロリド、ポリエチレン、ポリプロピレン、ポリビニルアルコール、ポリビニルピロリドン、ポリテトラフルオロエチレン、ポリフッ化ビニリデン、EPDM(Ethylene Propylene Diene Monomer)ゴム、スルホン化EPDMゴム、スチレンブタジエンゴム、ブタジエンゴム、フッ素ゴムなどのビニルポリマー、ポリエチレンオキシドなどのポリエーテルなどがある。
【0110】
また、導電助剤としては、蓄電装置中で化学変化を起こさない電子伝導性材料であればよい。例えば、黒鉛、炭素繊維などの炭素系材料、銅、ニッケル、アルミニウム若しくは銀などの金属材料又はこれらの混合物の粉末や繊維などを用いることができる。なお、導電助剤を膜状に形成して正極活物質をコーティングしてもよい。
【0111】
また、正極活物質層102形成する際、バインダ及び導電助剤の代わりにグラフェン又は多層グラフェンを混合させてもよい。なお、本明細書において、グラフェンとは、イオンを通過させる空隙を有し、sp2結合を有する1原子層の炭素分子で構成されたシート、又は当該シートが2枚乃至100枚積層された積層体をいう。また、当該グラフェンは、水素と炭素以外の元素の比率を15原子%以下、又は炭素以外の元素の比率を30原子%以下であることが好ましい。なお、グラフェンは、カリウムなどのアルカリ金属を添加したものでもよい。上記より、本明細書において、グラフェン類似体も当該グラフェンに含まれる。
【0112】
このように、導電助剤及びバインダの代わりにグラフェンを用いることで、正極103中の導電助剤及びバインダの含有量を低減させることできる。つまり、正極103の重量を低減させることができ、電極の重量あたりにおけるリチウム二次電池の容量を増大させることができる。結果として、従来に比べてリチウム二次電池の容量を向上させることができる。
【0113】
なお、「活物質」とは、厳密にはキャリアであるイオンの挿入及び脱離に関わる物質のみを指す。ただし本明細書では、塗布法を用いて正極活物質層102を形成する場合、便宜上、正極活物質層102の材料、すなわち、本来「正極活物質」である物質に、導電助剤やバインダなどを含めて正極活物質層102と呼ぶこととする。
【0114】
負極集電体104には、銅(Cu)、アルミニウム(Al)、ニッケル(Ni)、チタン(Ti)などの単体又はこれらの化合物を用いることができる。
【0115】
負極活物質層105には、リチウムの溶解・析出又はリチウムイオンのドープ・脱ドープが可能であれば特に限定されるものではなく、リチウム、アルミニウム、炭素系材料、スズ、シリコン、シリコン合金、及びゲルマニウムなどがある。又は、リチウム、アルミニウム、炭素系材料、スズ、シリコン、シリコン合金、及びゲルマニウムから選択される一以上を含む化合物でもよい。なお、リチウムイオンの挿入及び脱離が可能な炭素としては、粉末状若しくは繊維状の黒鉛、又はグラファイト等の黒鉛系炭素を用いることができる。また、シリコン、シリコン合金、ゲルマニウム、リチウム、アルミニウム、及びスズの方が、炭素系材料に比べてキャリアイオンを吸蔵できる容量が大きい。それゆえ、負極活物質層105に用いる材料の量を低減することができ、コストの節減、及びリチウム二次電池100の小型化が可能になる。
【0116】
また、負極活物質層105は、上記列挙した材料を印刷法、インクジェット法、CVD等により、凹凸状に形成したものでもよい。又は、上記列挙した材料を塗布法、スパッタリング法、蒸着法などで膜状に設けた後、当該膜状の材料を選択的に除去して、凹凸状に形成したものでもよい。
【0117】
なお、負極集電体104を用いず、上記列挙した負極活物質層105に適用できる材料単体を負極として用いてもよい。
【0118】
また、負極活物質層105の表面にグラフェンを形成してもよい。このようにすることで、リチウムの溶解又は析出、若しくはリチウムイオンの挿入又は脱離によって生じる負極活物質層105に与える影響を抑制することができる。当該影響とは、負極活物質層105が膨張又は収縮することで、負極活物質層105の微粉化又は剥離することである。
【0119】
電解質107は、上記列挙したキャリアイオンを有する塩である溶質と、溶媒と、を少なくとも含む。例えば、電解質107として、該塩が溶解した非水溶液、又は当該塩が溶解した水溶液を用いることができる。本実施の形態ではリチウム二次電池を例にしていることから、キャリアイオンであるリチウムイオンを有するリチウム塩を用いる。例えば、LiClO4、LiAsF6、LiBF4、LiPF6、Li(C2F5SO2)2Nなどのリチウム塩が挙げられる。なお、キャリアイオンをリチウム以外のアルカリ金属イオン又はアルカリ土類金属イオンとする場合には、電解質107の溶質として、アルカリ金属塩(例えば、ナトリウム塩又はカリウム塩など)、アルカリ土類金属塩(例えば、カルシウム塩、ストロンチウム塩又はバリウム塩など)、ベリリウム塩又はマグネシウム塩などを用いることができる。
【0120】
また、電解質107は、上記列挙したキャリアイオンを有する塩が溶解した非水溶液にすることが好ましい。つまり、電解質107の溶媒は、非プロトン性有機溶媒が好ましい。非プロトン性有機溶媒としては、例えば、エチレンカーボネート、プロピレンカーボネート、ジメチルカーボネート、ジエチルカーボネート、γーブチロラクトン、アセトニトリル、ジメトキシエタン及びテトラヒドロフランなどが挙げられ、これらの一又は複数を用いることができる。さらに、非プロトン性有機溶媒として、一のイオン液体又は複数のイオン液体を用いてもよい。イオン液体は、難燃性及び難揮発性であることから、リチウム二次電池100の内部温度が上昇した際にリチウム二次電池100の破裂又は発火などを抑制でき、安全性を高めることが可能となる。
【0121】
また、電解質107として、上記列挙したキャリアイオンを有する塩を含み、且つゲル化された高分子材料を用いることで、漏液性を含めた安全性が高まり、リチウム二次電池100の薄型化及び軽量化が可能となる。ゲル化される高分子材料の代表例としては、シリコンゲル、アクリルゲル、アクリロニトリルゲル、ポリエチレンオキサイド、ポリプロピレンオキサイド又はフッ素系ポリマーなどがある。
【0122】
さらに、電解質107としては、Li3PO4などの固体電解質を用いることができる。他の固体電解質としては、Li3PO4に窒素を混ぜたLixPOyNz(x、y、zは正の実数)、Li2S−SiS2、Li2S−P2S5、Li2S−B2S3等を用いることができ、上記列挙した固体電解質にLiIなどをドープしたものを用いることもできる。
【0123】
セパレータ108として、絶縁性の多孔体を用いる。例えば、紙、不織布、ガラス繊維、セラミックス、或いはナイロン(ポリアミド)、ビニロン(ポリビニルアルコール系繊維)、ポリエステル、アクリル、ポリオレフィン、ポリウレタンを用いた合成繊維等で形成されたものを用いればよい。ただし、電解質107に溶解しない材料を選ぶ必要がある。
【0124】
なお、本実施の形態では、リチウム二次電池100の外装形態として、密封されたボタン型を示しているが、これに限定されない。つまり、リチウム二次電池100を含め、本発明の一態様に係る蓄電装置の外装形態として、ラミネート型、円筒型、角型など様々な形状を採用することができる。また、本実施の形態のリチウム二次電池100では、正極103、負極106、及びセパレータ108が積層された構造を示したが、正極103、負極106、及びセパレータ108が捲回された構造であってもよい。
【0125】
次に、本発明の一態様に係る蓄電装置の作製方法について説明する。まず、正極103の作製方法について説明する。
【0126】
正極集電体101及び正極活物質層102の材料ついては上記列挙した材料から選択する。なお、正極活物質層102の正極活物質は、実施の形態1で説明した遷移金属を含むアルカリ金属ケイ酸塩、特にケイ酸マンガンリチウム(Li2MnSiO4)とする。
【0127】
正極集電体101上に、正極活物質層102を形成する。また正極活物質層102の形成方法は、塗布法又はスパッタリング法により形成すればよい。正極活物質層102を塗布法によって形成する場合は、正極活物質層102の材料に、導電助剤やバインダなどを混合させてペースト化したスラリーを作製する。そして、当該スラリーを正極集電体101上に塗布して乾燥させて形成する。正極活物質層102を塗布法により形成した場合、必要に応じて加圧成形するとよい。以上により、正極集電体101上に正極活物質層102が形成された正極103を作製できる。
【0128】
次に、負極106の作製方法について説明する。
【0129】
負極集電体104及び負極活物質層105の材料は上記列挙した材料から選択し、正極103と同様の方法を用いて、負極集電体104上に負極活物質層105を形成すればよい。なお、負極106に導電助剤及びバインダを用いる場合は、適宜、上記列挙した材料から選択し用いることができる。
【0130】
本実施の形態では、負極集電体104としてチタン箔を用い、負極活物質層105として、化学気相成長法又は物理気相成長法により形成したシリコンを用いる。
【0131】
負極活物質層105のシリコンは、非晶質シリコン、微結晶シリコン、多結晶シリコン又は単結晶シリコンなど結晶性を有するシリコンでもよい。
【0132】
例えば、負極活物質層105として、微結晶シリコンを負極集電体104上に形成し、微結晶シリコン中に存在する非結晶シリコンをエッチングにより除去したものを用いてもよい。微結晶シリコン中に存在する非結晶シリコンを除去すると、残った微結晶シリコンの表面積が大きくなる。微結晶シリコンの形成方法としては、例えば、プラズマCVD法又はスパッタリング法を用いることができる。
【0133】
また、負極活物質層105を、負極集電体104上にLP(Low Pressure)CVD装置を用いて形成したウィスカー状のシリコンとしてもよい(図4(A)参照)。なお、本明細書において、ウィスカー状のシリコンとは、共通部201aと、共通部201aから髭状(若しくは紐状又は繊維状)に突出した領域201bとを有するシリコンをいう。
【0134】
ウィスカー状のシリコンが、非晶質シリコンで形成されている場合、イオンの吸蔵及び放出に伴う体積変化に強い(例えば、体積膨張に伴う応力を緩和する)ため、繰り返しの充放電によって、負極活物質層が微粉化及び剥離することを防止でき、サイクル特性がさらに向上した蓄電装置を作製することができる(図4(A)参照)。
【0135】
ウィスカー状のシリコンが、微結晶シリコン、多結晶シリコン、単結晶シリコンのように結晶性を有するシリコンで形成されている場合、導電性及びイオン移動度に優れた結晶性を有する結晶構造が集電体と広範囲に接している。そのため、負極全体の導電性をさらに向上させることができ、さらに高速な充放電が可能となり、充放電容量がさらに向上した蓄電装置を作製することができる(図4(B)参照)。
【0136】
さらに、ウィスカー状のシリコンは、結晶性を有するシリコンで形成された芯202と、非晶質シリコンで形成されていて、芯を覆う外殻204と、で構成されていてもよい(図4(C)参照)。この場合、外殻204である非晶質シリコンは、イオンの吸蔵及び放出に伴う体積変化に強い(例えば、体積膨張に伴う応力を緩和する)という特色を有する。また、芯202である結晶性を有するシリコンは、導電性及びイオン移動度に優れており、イオンを吸蔵する速度及び放出する速度が単位質量あたりで速いという特徴と有する。従って、芯202及び外殻204を有するウィスカー状のシリコンを負極活物質層105として用いることで、高速に充放電が可能となり、充放電容量及びサイクル特性が向上したリチウム二次電池100を作製することができる。
【0137】
なお、共通部201aは、図4(C)のように、芯202を構成する結晶性を有するシリコンが負極集電体104の上面一部と接する形態の他に負極集電体104の上面全てが結晶性を有するシリコンと接する形態であってもよい。
【0138】
また、負極活物質層105の表面にグラフェン又は多層グラフェンを形成する場合は、酸化グラフェンが含まれる溶液に、負極活物質層105を設けた負極集電体104を参照電極と共に浸し、当該溶液を用いて電気泳動法により、負極活物質層105表面に酸化グラフェン層を形成し、これを加熱して還元処理をすることで実施できる。また、負極活物質層105の表面にグラフェン又は多層グラフェンを形成するには、当該溶液を用いたディップコート法でも実施でき、ディップコートした後は、加熱し還元処理すればよい。
【0139】
なお、負極活物質層105にリチウムをプレドープしてもよい。リチウムのプレドープ方法としては、スパッタリング法により負極活物質層105表面にリチウム層を形成すればよい。又は、負極活物質層105の表面にリチウム箔を設けることでも、負極活物質層105にリチウムをプレドープすることができる。
【0140】
電解質107の作製方法は、上記列挙した材料を適宜選択して用いればよい。本実施の形態では、溶質はリチウム塩であるLi(CF3SO2)2Nとし、溶媒はエチレンカーボネートとし、エチレンカーボネートとLi(CF3SO2)2Nを適宜混合してリチウムイオンを含む非水溶液とする。
【0141】
次に、正極103、セパレータ108、及び負極106を電解質107に含浸させる。次に、外部端子109上に、負極106、セパレータ108、ガスケット121、正極103、及び外部端子111の順に積層し、「コインかしめ機」で外部端子109及び外部端子111をかしめれば、コイン型のリチウム二次電池100を作製することができる。
【0142】
なお、外部端子111及び正極103の間、又は外部端子109及び負極106の間に、スペーサー、及びワッシャーを入れて、外部端子111及び正極103の接続、並びに外部端子109及び負極106の接続をより高めてもよい。
【0143】
また、本実施の形態は、他の実施の形態及び実施例に記載した構成と適宜組み合わせて実施することが可能である。
【0144】
(実施の形態3)
本発明の一態様に係る蓄電装置は、電力により駆動する様々な電気機器の電源として用いることができる。
【0145】
本発明の一態様に係る蓄電装置を用いた電気機器の具体例として、表示装置、照明装置、デスクトップ型或いはノート型のパーソナルコンピュータ、DVD(Digital Versatile Disc)などの記録媒体に記憶された静止画又は動画を再生する画像再生装置、携帯電話、携帯型ゲーム機、携帯情報端末、電子書籍、ビデオカメラ、デジタルスチルカメラ、電子レンジ等の高周波加熱装置、電気炊飯器、電気洗濯機、エアコンディショナーなどの空調設備、電気冷蔵庫、電気冷凍庫、電気冷凍冷蔵庫、DNA保存用冷凍庫や透析装置等の医療用電気機器などが挙げられる。また、蓄電装置からの電力を用いて電動機により推進する移動体なども、電気機器の範疇に含まれるものとする。上記移動体として、例えば、電気自動車、内燃機関と電動機を併せ持った複合型自動車(ハイブリッドカー)、電動アシスト自転車を含む原動機付自転車などが挙げられる。
【0146】
なお、上記電気機器は、消費電力の殆ど全てを賄うための蓄電装置(主電源と呼ぶ)として、本発明の一態様に係る蓄電装置を用いることができる。或いは、上記電気機器は、上記主電源や商用電源からの電力の供給が停止した場合に、電気機器への電力の供給を行うことができる蓄電装置(無停電電源と呼ぶ)として、本発明の一態様に係る蓄電装置を用いることができる。或いは、上記電気機器は、上記主電源や商用電源からの電気機器への電力の供給と並行して、電気機器への電力の供給を行うための蓄電装置(補助電源と呼ぶ)として、本発明の一態様に係る蓄電装置を用いることができる。
【0147】
図5に、上記電気機器の具体的な構成を示す。図5において、表示装置5000は、本発明の一態様に係る蓄電装置5004を用いた電気機器の一例である。具体的に、表示装置5000は、TV放送受信用の表示装置に相当し、筐体5001、表示部5002、スピーカー部5003、蓄電装置5004等を有する。本発明の一態様に係る蓄電装置5004は、筐体5001の内部に設けられている。表示装置5000は、商用電源から電力の供給を受けることもできるし、蓄電装置5004に蓄積された電力を用いることもできる。よって、停電などにより商用電源から電力の供給が受けられない時でも、本発明の一態様に係る蓄電装置5004を無停電電源として用いることで、表示装置5000の利用が可能となる。
【0148】
表示部5002には、液晶表示装置、有機EL素子などの発光素子を各画素に備えた発光装置、電気泳動表示装置、DMD(Digital Micromirror Device)、PDP(Plasma Display Panel)、FED(Field Emission Display)などの、半導体表示装置を用いることができる。
【0149】
なお、表示装置には、TV放送受信用の他、パーソナルコンピュータ用、広告表示用など、全ての情報表示用表示装置が含まれる。
【0150】
図5において、据え付け型の照明装置5100は、本発明の一態様に係る蓄電装置5103を用いた電気機器の一例である。具体的に、照明装置5100は、筐体5101、光源5102、蓄電装置5103等を有する。図5では、蓄電装置5103が、筐体5101及び光源5102が据え付けられた天井5104の内部に設けられている場合を例示しているが、蓄電装置5103は、筐体5101の内部に設けられていても良い。照明装置5100は、商用電源から電力の供給を受けることもできるし、蓄電装置5103に蓄積された電力を用いることもできる。よって、停電などにより商用電源から電力の供給が受けられない時でも、本発明の一態様に係る蓄電装置5103を無停電電源として用いることで、照明装置5100の利用が可能となる。
【0151】
なお、図5では天井5104に設けられた据え付け型の照明装置5100を例示しているが、本発明の一態様に係る蓄電装置は、天井5104以外、例えば側壁5105、床5106、窓5107等に設けられた据え付け型の照明装置に用いることもできるし、卓上型の照明装置などに用いることもできる。
【0152】
また、光源5102には、電力を利用して人工的に光を得る人工光源を用いることができる。具体的には、白熱電球、蛍光灯などの放電ランプ、LEDや有機EL素子などの発光素子が、上記人工光源の一例として挙げられる。
【0153】
図5において、室内機5200及び室外機5204を有するエアコンディショナーは、本発明の一態様に係る蓄電装置5203を用いた電気機器の一例である。具体的に、室内機5200は、筐体5201、送風口5202、蓄電装置5203等を有する。図5では、蓄電装置5203が、室内機5200に設けられている場合を例示しているが、蓄電装置5203は室外機5204に設けられていても良い。或いは、室内機5200と室外機5204の両方に、蓄電装置5203が設けられていても良い。エアコンディショナーは、商用電源から電力の供給を受けることもできるし、蓄電装置5203に蓄積された電力を用いることもできる。特に、室内機5200と室外機5204の両方に蓄電装置5203が設けられている場合、停電などにより商用電源から電力の供給が受けられない時でも、本発明の一態様に係る蓄電装置5203を無停電電源として用いることで、エアコンディショナーの利用が可能となる。
【0154】
なお、図5では、室内機と室外機で構成されるセパレート型のエアコンディショナーを例示しているが、室内機の機能と室外機の機能とを1つの筐体に有する一体型のエアコンディショナーに、本発明の一態様に係る蓄電装置を用いることもできる。
【0155】
図5において、電気冷凍冷蔵庫5300は、本発明の一態様に係る蓄電装置5304を用いた電気機器の一例である。具体的に、電気冷凍冷蔵庫5300は、筐体5301、冷蔵室用扉5302、冷凍室用扉5303、蓄電装置5304等を有する。図5では、蓄電装置5304が、筐体5301の内部に設けられている。電気冷凍冷蔵庫5300は、商用電源から電力の供給を受けることもできるし、蓄電装置5304に蓄積された電力を用いることもできる。よって、停電などにより商用電源から電力の供給が受けられない時でも、本発明の一態様に係る蓄電装置5304を無停電電源として用いることで、電気冷凍冷蔵庫5300の利用が可能となる。
【0156】
なお、上述した電気機器のうち、電子レンジ等の高周波加熱装置、電気炊飯器などの電気機器は、短時間で高い電力を必要とする。よって、商用電源では賄いきれない電力を補助するための補助電源として、本発明の一態様に係る蓄電装置を用いることで、電気機器の使用時に商用電源のブレーカーが落ちるのを防ぐことができる。
【0157】
また、電気機器が使用されない時間帯、特に、商用電源の供給元が供給可能な総電力量のうち、実際に使用される電力量の割合(電力使用率と呼ぶ)が低い時間帯において、蓄電装置に電力を蓄えておくことで、上記時間帯以外において電力使用率が高まるのを抑えることができる。例えば、電気冷凍冷蔵庫5300の場合、気温が低く、冷蔵室用扉5302、冷凍室用扉5303の開閉が行われない夜間において、蓄電装置5304に電力を蓄える。そして、気温が高くなり、冷蔵室用扉5302、冷凍室用扉5303の開閉が行われる昼間において、蓄電装置5304を補助電源として用いることで、昼間の電力使用率を低く抑えることができる。
【0158】
なお、本実施の形態は、他の実施の形態又は実施例に記載した構成と適宜組み合わせて実施することが可能である。
【0159】
(実施の形態4)
本実施の形態においては、上記実施の形態で説明した蓄電装置を用いた電気機器の例について図6(A)、図6(B)、及び図6(C)を用いて説明する。
【0160】
図6(A)及び図6(B)は2つ折り可能なタブレット型端末である。図6(A)は、開いた状態であり、タブレット型端末は、筐体9630、表示部9631a、表示部9631b、表示モード切り替えスイッチ9034、電源スイッチ9035、省電力モード切り替えスイッチ9036、留め具9033、操作スイッチ9038、を有する。
【0161】
表示部9631aは、一部をタッチパネルの領域9632aとすることができ、表示された操作キー9638にふれることでデータ入力をすることができる。なお、表示部9631aにおいては、一例として半分の領域が表示のみの機能を有する構成、もう半分の領域がタッチパネルの機能を有する構成を示しているが該構成に限定されない。表示部9631aの全ての領域がタッチパネルの機能を有する構成としても良い。例えば、表示部9631aの全面をキーボードボタン表示させてタッチパネルとし、表示部9631bを表示画面として用いることができる。
【0162】
また、表示部9631bにおいても表示部9631aと同様に、表示部9631bの一部をタッチパネルの領域9632bとすることができる。また、タッチパネルのキーボード表示切り替えボタン9639が表示されている位置に指やスタイラスなどでふれることで表示部9631bにキーボードボタン表示することができる。
【0163】
また、タッチパネルの領域9632aとタッチパネルの領域9632bに対して同時にタッチ入力することもできる。
【0164】
また、表示モード切り替えスイッチ9034は、縦表示又は横表示などの表示の向きを切り替え、白黒表示やカラー表示の切り替えなどを選択できる。省電力モード切り替えスイッチ9036は、タブレット型端末に内蔵している光センサで検出される使用時の外光の光量に応じて表示の輝度を最適なものとすることができる。タブレット型端末は光センサだけでなく、ジャイロ、加速度センサ等の傾きを検出するセンサなどの他の検出装置を内蔵させてもよい。
【0165】
また、図6(A)では表示部9631bと表示部9631aの表示面積が同じ例を示しているが特に限定されず、一方のサイズともう一方のサイズが異なっていてもよく、表示の品質も異なっていてもよい。例えば一方が他方よりも高精細な表示を行える表示パネルとしてもよい。
【0166】
図6(B)は、閉じた状態であり、タブレット型端末は、筐体9630、太陽電池9633、充放電制御回路9634、バッテリー9635、DCDCコンバータ9636を有する。なお、図6(B)では充放電制御回路9634の一例としてバッテリー9635、DCDCコンバータ9636を有する構成について示している。
【0167】
なお、タブレット型端末は2つ折り可能なため、未使用時に筐体9630を閉じた状態にすることができる。従って、表示部9631a、表示部9631bを保護できるため、耐久性に優れ、長期使用の観点からも信頼性の優れたタブレット型端末を提供できる。
【0168】
また、この他にも図6(A)及び図6(B)に示したタブレット型端末は、様々な情報(静止画、動画、テキスト画像など)を表示する機能、カレンダー、日付又は時刻などを表示部に表示する機能、表示部に表示した情報をタッチ入力操作又は編集するタッチ入力機能、様々なソフトウェア(プログラム)によって処理を制御する機能、等を有することができる。
【0169】
タブレット型端末の表面に装着された太陽電池9633によって、電力をタッチパネル、表示部、又は映像信号処理部等に供給することができる。なお、太陽電池9633は、筐体9630の一面又は二面に設けられ、効率的なバッテリー9635の充電を行う構成とすることができるため好適である。なおバッテリー9635としては、本発明の一態様に係る蓄電装置を用いると、小型化を図れる等の利点がある。
【0170】
また、図6(B)に示す充放電制御回路9634の構成、及び動作について図6(C)にブロック図を示し説明する。図6(C)には、太陽電池9633、バッテリー9635、DCDCコンバータ9636、コンバータ9637、スイッチ9650乃至スイッチ9654、表示部9631について示しており、バッテリー9635、DCDCコンバータ9636、コンバータ9637、スイッチ9650乃至スイッチ9654が、図6(B)に示す充放電制御回路9634に対応する箇所となる。
【0171】
外光により太陽電池9633により発電がされる場合の動作の例について説明する。太陽電池9633で発電した電力は、バッテリー9635を充電するための電圧となるようDCDCコンバータ9636で昇圧又は降圧がなされる。そして、表示部9631の動作に太陽電池9633からの電力が用いられる際にはスイッチ9650をオンにし、コンバータ9637で表示部9631に必要な電圧に昇圧又は降圧をすることとなる。また、表示部9631での表示を行わない際には、スイッチ9650をオフにし、スイッチ9652をオンにしてバッテリー9635の充電を行う構成とすればよい。
【0172】
なお太陽電池9633については、発電手段の一例として示したが、特に限定されず、圧電素子(ピエゾ素子)や熱電変換素子(ペルティエ素子)などの他の発電手段によるバッテリー9635の充電を行う構成であってもよい。例えば、無線(非接触)で電力を送受信して充電する無接点電力伝送モジュールや、また他の充電手段を組み合わせて行う構成としてもよい。
【0173】
また、上記実施の形態で説明した蓄電装置を具備していれば、図6に示した電気機器に特に限定されない。
【0174】
本実施の形態は、他の実施の形態に記載した構成と適宜組み合わせて実施することが可能である。
【実施例1】
【0175】
本実施例では、本発明の一態様に係るアルカリ金属ケイ酸塩の一例として、ケイ酸リチウムを合成し、その合成したケイ酸リチウムについて評価した結果を説明する。
【0176】
本実施例における合成方法は、図1及び図2、特に各ステップにおける下線の記載を参照して説明する。なお、本実施例においてアルカリ金属塩は水酸化リチウムであり、水酸化リチウムに対する良溶媒は水とし、水酸化リチウムに対する貧溶媒はエタノールとした。
【0177】
まず、反応容器に水(イオン交換水)400mlを入れ、水を60℃に加熱した。温度を60℃に保ったまま、攪拌装置でこの水を攪拌させながら水酸化リチウム二水和物20.14gを加えて、水酸化リチウム水溶液を作製した(ステップS111)。なお、水酸化リチウム二水和物は完全に溶解するまで攪拌し、作製した水酸化リチウム水溶液のpHは10に調整した。
【0178】
次に、作製した水酸化リチウム水溶液を60℃に保持したまま、シリコン粉末(株式会社高純度化学研究所製、純度99.999%、粒径75μm以下)を3.37g加えて、シリコン粉末が完全に溶解するまでさらに攪拌し、水酸化リチウムとシリコン粉末を液相反応で反応させ、ケイ酸リチウム水溶液を作製した(ステップS112)。なお、当該液相反応で作製されるケイ酸リチウムは、メタケイ酸リチウム(Li2SiO3)が主生成物であるが、副生成物としてオルトケイ酸リチウム(Li4SiO4)及びLi2Si2O5の一方又は双方を含むことがある。当該液相反応の化学反応式を以下に示す。
【0179】
【化1】

【0180】
また、ステップS112において、加えたシリコン粉末の質量は、ステップS111で用いた水酸化リチウムのモル数の1/4に相当する質量である。さらに、本実施例は、ステップS112において、作製したケイ酸リチウム水溶液に対するシリコン濃度が0.3mol/lとなるように、ステップS111で水酸化リチウム水溶液の水量を調整した。
【0181】
次に、回転数500rpm〜600rpmで攪拌されているエタノールにケイ酸リチウム水溶液を加えて、ケイ酸リチウムをエタノール中に析出させた。本実施例では、ケイ酸リチウム水溶液をシリンジに少量計り入れ、エタノール400mlに対して、当該シリンジから40ml/hの速度でエタノールに滴下した。
【0182】
次に、ケイ酸リチウムが析出しているエタノールを濾過してケイ酸リチウムを回収し、回収したケイ酸リチウムを乾燥させた(ステップS113)。本実施例では、加熱温度を80℃とし、真空雰囲気下で2時間加熱を保持した後、室温まで下がる時間を含めて2時間真空雰囲気下を保持し、自然冷却することでケイ酸リチウムを乾燥させた。
【0183】
次に、乾燥させたケイ酸リチウムに第1の加熱処理(第1の焼成)を行った(ステップS114)。本実施例では、加熱温度を520℃とし、窒素雰囲気下で10時間加熱した。
【0184】
次に、ステップS114を経たケイ酸リチウムと水(イオン交換水)50mlとを混合し、回転数300rpm〜400rpmで1時間攪拌して洗浄した。その後、加熱温度を180℃とし、真空雰囲気下で1時間加熱を保持した後、自然冷却で室温にまで下がる時間を含めて2時間真空雰囲気下を保持して、洗浄したケイ酸リチウムを乾燥させた。以上より、白色のケイ酸リチウム1.0gを得た。ステップS111乃至ステップS114を経て得られたケイ酸リチウムはメタケイ酸リチウム(Li2SiO3)であった。なお、本実施例で合成したケイ酸リチウムを化合物Aとする。
【0185】
次に、化合物Aの物性評価について説明する。比較化合物として、市販されているメタケイ酸リチウム(Li2SiO3)を用意した。比較化合物は、化合物Aとは異なる合成方法で合成され、機械的な粉砕により作製されたメタケイ酸リチウムである。
【0186】
〈X線回折法〉
化合物A及び比較化合物を同定するために、X線回折法(X‐ray diffraction:XRD)を用いて評価した。
【0187】
図7(A)には化合物Aの回折パターンを示し、図7(B)には比較化合物の回折パターンを示した。化合物Aの回折パターンはメタケイ酸リチウム(Li2SiO3)の標準回折パターンと同じであり、本実施例に示した合成方法で合成された化合物Aはメタケイ酸リチウムであることが確認された。また、同様に、比較化合物もメタケイ酸リチウムを主成分とすることが確認されたが、図7(B)に示すように、2θが20°〜25°の範囲に炭酸リチウム(Li2CO3)に由来するピークが確認された。これは、比較化合物を作製する際に用いた未反応の原料であると推測される。
【0188】
なお、ステップS112で作製されるケイ酸リチウムには、主生成物のメタケイ酸リチウム(Li2SiO3)の他に副生成物としてオルトケイ酸リチウム(Li4SiO4)及びLi2Si2O5の一方又は双方が含まれることがあるが、本実施例での合成条件によって、最終的に得られるケイ酸リチウムをメタケイ酸リチウム(Li2SiO3)にすることができた。
【0189】
〈SEM観察及び比表面積測定〉
化合物A及び比較化合物の表面形状を観察するために、SEM(Scanning Electron Microscope)観察を行った。図8(A)には化合物Aの平面SEM像を示し、図8(B)には比較化合物の平面SEM像を示した。図8(A)の倍率は10000倍であり、図8(B)の倍率は10000倍である。
【0190】
図8(A)及び(B)より、化合物Aの粒子は、比較化合物の粒子より粒子サイズが小さく、微粒子化されていることが確認できた。さらに、化合物Aの粒子は比較化合物の粒子よりも粒子サイズが均一であることが確認できた。
【0191】
また、気体吸着法を用いて化合物A及び比較化合物の比表面積を測定した。本実施例での比表面積は、自動比表面積細孔分布測定装置トライスターII3020(株式会社島津製作所製)で測定した。なお、当該装置は、試料に窒素を一定期間吸着させた後、吸着した窒素量で当該試料の表面積を測定する装置である。
【0192】
上記装置により測定した化合物Aの比表面積は、80.97m2/gであり、比較化合物の比表面積は、0.71m2/gであった。気体吸着法で測定される比表面積において、粒子サイズ(例えば粒径)が小さく、より微粒子化されている試料ほどその比表面積は大きい傾向にある。従って、本測定からも、化合物Aの粒子サイズは比較化合物の粒子サイズより小さく、より微粒子化されていることが確認できた。
【0193】
〈XPS法〉
化合物A及び比較化合物の組成を定量するために、X線光電子分光法(X−ray photoelectron spectroscopy:XPS)を用いて評価した。
【0194】
表1に、化合物A及び比較化合物の組成及びその定量値(単位atom%)を示した。
【0195】
【表1】

【0196】
表1からわかるように、化合物A及び比較化合物には、不純物元素である炭素(C)が含まれていることが確認されたが、化合物Aに含まれている量は、比較化合物に含まれている量に比べて非常に少ないことが確認された。XRD測定において、未反応の原料であると推測される炭酸リチウム(Li2CO3)が検出されたことは、化合物Aより比較化合物に多く炭素が含まれていることを肯定する結果である。さらに、化合物Aでは検出されなかったが、比較化合物では不純物元素であるナトリウム(Na)が含まれていることが確認された。従って、化合物Aは比較化合物に比べて高純度であることが確認された。
【0197】
以上より、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法は、アルカリ金属ケイ酸塩を機械的な粉砕では困難な粒子サイズにまで、その粒子サイズを揃えて微粒子化することができる。
【0198】
また、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法は、不純物が少なく高純度なアルカリ金属ケイ酸塩を容易に合成することができる。
【実施例2】
【0199】
本実施例では、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法において、析出させるアルカリ金属ケイ酸塩の貧溶媒を変化させた場合について説明する。なお、本実施例においてもアルカリ金属塩は、実施例1と同様に水酸化リチウムとし、水酸化リチウムに対する良溶媒は水とした。
【0200】
まず、実施例1と同様に、ステップS112までの工程を行った。
【0201】
次に、ケイ酸リチウム水溶液を貧溶媒に加えて、ケイ酸リチウムを当該貧溶媒中に析出させた。本実施例では、当該貧溶媒として、メタノール、エタノール、プロパノール、ブタノール及びペンタノール並びにアセトンを用意し、各々の貧溶媒にケイ酸リチウム水溶液を加えた。
【0202】
その後、析出したケイ酸リチウムを回収し、実施例1と同様の条件で回収したケイ酸リチウムを乾燥させた。そして、実施例1と同様に、ステップS114の工程を行った。貧溶媒をメタノールとして作製したケイ酸リチウムを化合物Bとし、貧溶媒をプロパノールとして作製したケイ酸リチウムを化合物Cとし、貧溶媒をブタノールとして作製したケイ酸リチウムを化合物Dとし、貧溶媒をペンタノールとして作製したケイ酸リチウムを化合物Eとし、貧溶媒をアセトンとして作製したケイ酸リチウムを化合物Fとする。
【0203】
次に、化合物B乃至化合物Fを同定するために、X線回折法(X‐ray diffraction:XRD)を用いて評価した。
【0204】
図9(A)に化合物B、図9(B)に化合物C、図9(C)に化合物D、図10(A)に化合物E、図10(B)に化合物Fの回折パターンを示した。図9(A)乃至(C)及び図10(A)並びに図10(B)より、貧溶媒の種類によって得られるケイ酸リチウムの組成に違いがあることが確認された。
【0205】
本実施例で用意した貧溶媒のうち、良溶媒として用いた水に対する親和性は、メタノール、エタノール、プロパノール、ブタノール、ペンタノール及びアセトンの順に低くなる。
【0206】
図9(A)より、良溶媒の水に対する親和性が一番高いメタノールを貧溶媒として用いた場合、得られたケイ酸リチウム(化合物B)は、Li2Si2O5であった。また、図10(B)より、良溶媒の水に対する親和性が一番低いアセトンを貧溶媒として用いた場合、得られたケイ酸リチウム(化合物F)は、オルトケイ酸リチウム(Li4SiO4)であった。
【0207】
また、エタノール、プロパノール、ブタノール及びペンタノールを貧溶媒として用いた場合、得られたケイ酸リチウム(化合物A、及び化合物C乃至化合物E)は、全てメタケイ酸リチウム(Li2SiO3)であった。図11(A)に化合物C、図11(B)に化合物D、図12に化合物Eの平面SEM像を示す。図8(A)、図11(A)、図11(B)、及び図12より、良溶媒として用いた水に対する親和性が変化するにつれて、得られたメタケイ酸リチウム(Li2SiO3)の粒子サイズは異なることが確認された。
【0208】
本実施例より、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法において、析出させるアルカリ金属ケイ酸塩の貧溶媒の良溶媒に対する親和性によって得られるアルカリ金属ケイ酸塩の組成及び粒子サイズが変わることが確認された。従って、所望の組成及び所望の粒子サイズを有するアルカリ金属ケイ酸塩が得られるように、良溶媒及び貧溶媒を選択することが好ましいことが確認された。
【実施例3】
【0209】
本実施例では、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法において、作製したアルカリ金属塩を含む塩基性溶液にシリコン粒子を加える際に、当該塩基性溶液に対するシリコン濃度を変化させた場合について説明する。なお、本実施例においてアルカリ金属塩は、実施例1と同様に水酸化リチウムとし、水酸化リチウムに対する良溶媒は水とした。
【0210】
具体的には、ステップS112の際、作製した水酸化リチウム水溶液に対するシリコン濃度を0.05mol/l、0.1mol/l、0.15mol/l、0.2mol/l、0.25mol/l、0.3mol/l、及び0.5mol/lに変化させた水溶液を用いてケイ酸リチウムを作製し、それぞれの濃度の水溶液を用いて作製されたケイ酸リチウムそれぞれの比表面積を評価した。なお、ケイ酸リチウムを作製する際の他の工程(ステップ)は、実施例1と同様であり、比表面積の測定も実施例1と同様の方法で行った。
【0211】
図13に、作製した水酸化リチウム水溶液に対するシリコン濃度と、得られたケイ酸リチウムの比表面積との関係を示した。なお、得られたケイ酸リチウムは全てメタケイ酸リチウム(Li2SiO3)であった。
【0212】
図13より、得られたケイ酸リチウムの比表面積は、シリコン濃度0.1mol/l以上で全て10m2/g以上60m2/g以下であり、得られるケイ酸リチウムの比表面積は、作製した水酸化リチウム水溶液に対するシリコン濃度に対して極大を有することが確認された。なお、本実施例において、水酸化リチウム水溶液に対するシリコン濃度が0.3mol/lの場合、化合物Aと同じケイ酸リチウムが得られることになるが、ケイ酸リチウムは粉体であるため、全てのケイ酸リチウムで同じ比表面積が常に測定されるわけではなく、ある程度の範囲を有して測定される。そのため、化合物Aが得られる条件でも、本実施例では異なる比表面積の値を示している。
【0213】
本実施例より、本発明の一態様に係るアルカリ金属ケイ酸塩の合成方法において、所望の粒子サイズを有するアルカリ金属ケイ酸塩が得られるように、作製したアルカリ金属塩を含む塩基性溶液に対するシリコン濃度を調製することが好ましいと確認できた。
【実施例4】
【0214】
本実施例では、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の一例として、ケイ酸マンガンリチウムを合成し、その合成したケイ酸マンガンリチウムについて評価した結果を説明する。
【0215】
ステップS111からステップS114までは実施例1と同様して行い、メタケイ酸リチウムを合成した。
【0216】
次に、炭酸マンガン(MnCO3)4.0gをボールミル処理にて粉砕した。当該ボールミル処理は、溶媒としてエタノールを添加し、回転数400rpm、回転時間2時間、ボール直径0.5mmの条件で行った。
【0217】
次に、得られたメタケイ酸リチウム2.20g及び炭酸マンガン2.80gをボールミル処理により混合し、メタケイ酸リチウム及び炭酸マンガンの混合物を作製した(ステップS115)。なお、ボールミル処理は、溶媒としてアセトンを添加し、回転数400rpm、回転時間2時間、ボール直径3mmの条件で行った。
【0218】
ボールミル処理後、混合物をポットから取り出し、50℃に加熱してアセトンを蒸発させた。
【0219】
次に、粉体の混合物に第2の加熱処理(第2の焼成)を行った(ステップS116)。本実施例では、加熱温度を700℃とし、窒素雰囲気下で10時間加熱して、ベージュ色の化合物を得た。なお、ステップS111乃至ステップS116を経て得られた化合物を化合物Gとする。
【0220】
以上のステップにより合成した化合物Gを同定するために、X線回折(XRD:X−ray diffraction)を用いて評価した。図14に化合物Gの回折パターンを示した。当該回折パターンより、化合物Gはケイ酸マンガンリチウム(Li2MnSO4)であることが確認された。また、図14の回折パターンには、2θ=40°付近に中間生成物の反応残りである酸化マンガンと推定されるピークは確認されなかった。
【0221】
本実施例より、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法を用いることで、従来、1000℃以上の高温で加熱処理する必要があったことに対して、700℃にまで加熱温度を下げても、中間生成物などの反応残りや未反応の原料を含まずに目的物である遷移金属を含むアルカリ金属ケイ酸塩を合成することができた。従って、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法は、従来の合成方法に比べて、作製コストを節減することができる。また、1回の加熱処理(焼成)で目的物を合成できることから、本発明の一態様に係る遷移金属を含むアルカリ金属ケイ酸塩の合成方法は、従来の合成方法に比べて、作製時間を短縮することができる。
【符号の説明】
【0222】
S111 ステップ
S112 ステップ
S113 ステップ
S114 ステップ
S115 ステップ
S116 ステップ
100 リチウム二次電池
101 正極集電体
102 正極活物質層
103 正極
104 負極集電体
105 負極活物質層
106 負極
107 電解質
108 セパレータ
109 外部端子
111 外部端子
121 ガスケット
201a 共通部
201b 領域
202 芯
204 外殻
5000 表示装置
5001 筐体
5002 表示部
5003 スピーカー部
5004 蓄電装置
5100 照明装置
5101 筐体
5102 光源
5103 蓄電装置
5104 天井
5105 側壁
5106 床
5107 窓
5200 室内機
5201 筐体
5202 送風口
5203 蓄電装置
5204 室外機
5300 電気冷凍冷蔵庫
5301 筐体
5302 冷蔵室用扉
5303 冷凍室用扉
5304 蓄電装置
9630 筐体
9631 表示部
9631a 表示部
9631b 表示部
9632a 領域
9632b 領域
9033 留め具
9034 表示モード切り替えスイッチ
9035 電源スイッチ
9036 省電力モード切り替えスイッチ
9038 操作スイッチ
9639 キーボード表示切り替えボタン
9633 太陽電池
9634 充放電制御回路
9635 バッテリー
9636 DCDCコンバータ
9637 コンバータ
9638 操作キー
【特許請求の範囲】
【請求項1】
アルカリ金属塩を含む塩基性溶液を作製し、
前記アルカリ金属塩を含む塩基性溶液とシリコン粒子を混合してアルカリ金属ケイ酸塩を含む塩基性溶液を作製し、
前記アルカリ金属ケイ酸塩を含む塩基性溶液を前記アルカリ金属ケイ酸塩の貧溶媒に加えて、前記アルカリ金属ケイ酸塩を析出させることを特徴とするアルカリ金属ケイ酸塩の合成方法。
【請求項2】
アルカリ金属塩を含む塩基性溶液を作製し、
前記塩基性溶液にシリコン粒子を加えて、前記シリコン粒子を加えた塩基性溶液を攪拌して、前記アルカリ金属塩と前記シリコン粒子を反応させて、アルカリ金属ケイ酸塩を含む塩基性溶液を作製し、
前記アルカリ金属ケイ酸塩を含む塩基性溶液を前記アルカリ金属ケイ酸塩の貧溶媒に加えて、前記貧溶媒中に前記アルカリ金属ケイ酸塩を析出させた後、前記析出したアルカリ金属ケイ酸塩を回収し、
前記回収したアルカリ金属ケイ酸塩に加熱処理を行うことを特徴とするアルカリ金属ケイ酸塩の合成方法。
【請求項3】
請求項1又は請求項2において、
前記アルカリ金属塩を含む塩基性溶液は、pHが9以上であることを特徴とするアルカリ金属ケイ酸塩の合成方法。
【請求項4】
請求項1乃至請求項3のいずれか一において、
前記アルカリ金属塩を含む塩基性溶液は、50℃以上70℃以下に保持することを特徴とするアルカリ金属ケイ酸塩の合成方法。
【請求項5】
請求項1乃至請求項4のいずれか一において、
前記アルカリ金属塩を含む塩基性溶液は水酸化リチウム水溶液であり、
前記貧溶媒は直鎖アルコール又はアセトンであることを特徴とするアルカリ金属ケイ酸塩の合成方法。
【請求項6】
気体吸着法で測定される比表面積が50m2/g以上90m2/g以下であることを特徴とするアルカリ金属ケイ酸塩。
【請求項7】
X線光電子分光法によって定量される炭素原子が10atom%以下であり、X線光電子分光法によって定量されるナトリウム原子が1atom%以下であることを特徴とするアルカリ金属ケイ酸塩。
【請求項8】
アルカリ金属塩を含む塩基性溶液を作製し、
前記アルカリ金属塩を含む塩基性溶液とシリコン粒子を混合してアルカリ金属ケイ酸塩を含む塩基性溶液を作製し、
前記アルカリ金属ケイ酸塩を含む塩基性溶液を前記アルカリ金属ケイ酸塩の貧溶媒に加えて、前記アルカリ金属ケイ酸塩を析出させ、
前記析出させたアルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合して混合物を作製し、
前記混合物に加熱処理を行い、前記遷移金属を含むアルカリ金属ケイ酸塩を生成することを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項9】
アルカリ金属塩を含む塩基性溶液を作製し、
前記塩基性溶液にシリコン粉末を加えて、前記シリコン粉末を加えた塩基性溶液を攪拌して、前記アルカリ金属塩と前記シリコン粉末を反応させて、アルカリ金属ケイ酸塩を含む塩基性溶液を作製し、
前記アルカリ金属ケイ酸塩を含む塩基性溶液を前記アルカリ金属ケイ酸塩の貧溶媒に加えて、前記貧溶媒中に前記アルカリ金属ケイ酸塩を析出させた後、前記析出したアルカリ金属ケイ酸塩を回収し、
前記回収したアルカリ金属ケイ酸塩に第1の加熱処理を行い、
前記加熱処理したアルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合して混合物を作製し、
前記混合物に第2の加熱処理を行い、前記遷移金属を含むアルカリ金属ケイ酸塩を生成することを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項10】
請求項8又は請求項9において、
前記アルカリ金属塩を含む塩基性溶液は、pHが9以上であることを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項11】
請求項8乃至請求項10のいずれか一において、
前記アルカリ金属塩を含む塩基性溶液は、50℃以上70℃以下に保持することを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項12】
請求項8乃至請求項11のいずれか一において、
前記アルカリ金属塩を含む塩基性溶液は水酸化リチウム水溶液であり、
前記貧溶媒は直鎖アルコール又はアセトンであることを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項13】
請求項8乃至請求項12のいずれか一において、
前記遷移金属は、鉄、マンガン、ニッケル又はコバルトのうちいずれか一以上であることを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項14】
請求項8乃至請求項13のいずれか一において、
前記遷移金属を含む化合物は、鉄、マンガン、ニッケル又はコバルトのうちいずれか一以上を含む炭酸塩であることを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項15】
請求項8乃至請求項14のいずれか一において、
前記混合物に行う加熱処理は、700℃以上1000℃以下の不活性ガス雰囲気下で行うことを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項16】
請求項8乃至請求項15のいずれか一において、
前記生成した遷移金属を含むアルカリ金属ケイ酸塩は、気体吸着法で測定される比表面積が50m2/g以上150m2/g以下であることを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項17】
気体吸着法で測定される比表面積が50m2/g以上150m2/g以下である遷移金属を含むアルカリ金属ケイ酸塩。
【請求項1】
アルカリ金属塩を含む塩基性溶液を作製し、
前記アルカリ金属塩を含む塩基性溶液とシリコン粒子を混合してアルカリ金属ケイ酸塩を含む塩基性溶液を作製し、
前記アルカリ金属ケイ酸塩を含む塩基性溶液を前記アルカリ金属ケイ酸塩の貧溶媒に加えて、前記アルカリ金属ケイ酸塩を析出させることを特徴とするアルカリ金属ケイ酸塩の合成方法。
【請求項2】
アルカリ金属塩を含む塩基性溶液を作製し、
前記塩基性溶液にシリコン粒子を加えて、前記シリコン粒子を加えた塩基性溶液を攪拌して、前記アルカリ金属塩と前記シリコン粒子を反応させて、アルカリ金属ケイ酸塩を含む塩基性溶液を作製し、
前記アルカリ金属ケイ酸塩を含む塩基性溶液を前記アルカリ金属ケイ酸塩の貧溶媒に加えて、前記貧溶媒中に前記アルカリ金属ケイ酸塩を析出させた後、前記析出したアルカリ金属ケイ酸塩を回収し、
前記回収したアルカリ金属ケイ酸塩に加熱処理を行うことを特徴とするアルカリ金属ケイ酸塩の合成方法。
【請求項3】
請求項1又は請求項2において、
前記アルカリ金属塩を含む塩基性溶液は、pHが9以上であることを特徴とするアルカリ金属ケイ酸塩の合成方法。
【請求項4】
請求項1乃至請求項3のいずれか一において、
前記アルカリ金属塩を含む塩基性溶液は、50℃以上70℃以下に保持することを特徴とするアルカリ金属ケイ酸塩の合成方法。
【請求項5】
請求項1乃至請求項4のいずれか一において、
前記アルカリ金属塩を含む塩基性溶液は水酸化リチウム水溶液であり、
前記貧溶媒は直鎖アルコール又はアセトンであることを特徴とするアルカリ金属ケイ酸塩の合成方法。
【請求項6】
気体吸着法で測定される比表面積が50m2/g以上90m2/g以下であることを特徴とするアルカリ金属ケイ酸塩。
【請求項7】
X線光電子分光法によって定量される炭素原子が10atom%以下であり、X線光電子分光法によって定量されるナトリウム原子が1atom%以下であることを特徴とするアルカリ金属ケイ酸塩。
【請求項8】
アルカリ金属塩を含む塩基性溶液を作製し、
前記アルカリ金属塩を含む塩基性溶液とシリコン粒子を混合してアルカリ金属ケイ酸塩を含む塩基性溶液を作製し、
前記アルカリ金属ケイ酸塩を含む塩基性溶液を前記アルカリ金属ケイ酸塩の貧溶媒に加えて、前記アルカリ金属ケイ酸塩を析出させ、
前記析出させたアルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合して混合物を作製し、
前記混合物に加熱処理を行い、前記遷移金属を含むアルカリ金属ケイ酸塩を生成することを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項9】
アルカリ金属塩を含む塩基性溶液を作製し、
前記塩基性溶液にシリコン粉末を加えて、前記シリコン粉末を加えた塩基性溶液を攪拌して、前記アルカリ金属塩と前記シリコン粉末を反応させて、アルカリ金属ケイ酸塩を含む塩基性溶液を作製し、
前記アルカリ金属ケイ酸塩を含む塩基性溶液を前記アルカリ金属ケイ酸塩の貧溶媒に加えて、前記貧溶媒中に前記アルカリ金属ケイ酸塩を析出させた後、前記析出したアルカリ金属ケイ酸塩を回収し、
前記回収したアルカリ金属ケイ酸塩に第1の加熱処理を行い、
前記加熱処理したアルカリ金属ケイ酸塩と、微粒子化した遷移金属を含む化合物を混合して混合物を作製し、
前記混合物に第2の加熱処理を行い、前記遷移金属を含むアルカリ金属ケイ酸塩を生成することを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項10】
請求項8又は請求項9において、
前記アルカリ金属塩を含む塩基性溶液は、pHが9以上であることを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項11】
請求項8乃至請求項10のいずれか一において、
前記アルカリ金属塩を含む塩基性溶液は、50℃以上70℃以下に保持することを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項12】
請求項8乃至請求項11のいずれか一において、
前記アルカリ金属塩を含む塩基性溶液は水酸化リチウム水溶液であり、
前記貧溶媒は直鎖アルコール又はアセトンであることを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項13】
請求項8乃至請求項12のいずれか一において、
前記遷移金属は、鉄、マンガン、ニッケル又はコバルトのうちいずれか一以上であることを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項14】
請求項8乃至請求項13のいずれか一において、
前記遷移金属を含む化合物は、鉄、マンガン、ニッケル又はコバルトのうちいずれか一以上を含む炭酸塩であることを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項15】
請求項8乃至請求項14のいずれか一において、
前記混合物に行う加熱処理は、700℃以上1000℃以下の不活性ガス雰囲気下で行うことを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項16】
請求項8乃至請求項15のいずれか一において、
前記生成した遷移金属を含むアルカリ金属ケイ酸塩は、気体吸着法で測定される比表面積が50m2/g以上150m2/g以下であることを特徴とする遷移金属を含むアルカリ金属ケイ酸塩の合成方法。
【請求項17】
気体吸着法で測定される比表面積が50m2/g以上150m2/g以下である遷移金属を含むアルカリ金属ケイ酸塩。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図9】


【図10】


【図13】


【図14】


【図8】


【図11】


【図12】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図9】


【図10】


【図13】


【図14】


【図8】


【図11】


【図12】


【公開番号】特開2013−63896(P2013−63896A)
【公開日】平成25年4月11日(2013.4.11)
【国際特許分類】
【出願番号】特願2012−187286(P2012−187286)
【出願日】平成24年8月28日(2012.8.28)
【出願人】(000153878)株式会社半導体エネルギー研究所 (5,264)
【Fターム(参考)】
【公開日】平成25年4月11日(2013.4.11)
【国際特許分類】
【出願日】平成24年8月28日(2012.8.28)
【出願人】(000153878)株式会社半導体エネルギー研究所 (5,264)
【Fターム(参考)】
[ Back to top ]

