アルキル芳香族化合物の酸化
アルキル芳香族化合物を対応するヒドロペルオキシドに酸化するための方法において、アルキル芳香族化合物を含む供給原料が環状イミドを含む触媒の存在下で酸素含有ガスと接触させられる。その接触は約90℃〜約150℃の温度で行なわれ、環状イミドが供給原料中のアルキル芳香族化合物の約0.05質量%〜約5質量%の量で存在し、触媒がアルカリ金属化合物を実質的に含まない。その接触が前記供給原料中のアルキル芳香族化合物の少なくとも一部を対応するヒドロペルオキシドに酸化する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明はアルキル芳香族化合物の酸化方法及びその酸化生成物をフェノール及び対応するケトンに変換するための方法に関する。
【背景技術】
【0002】
フェノールは化学工業における重要な製品であり、例えば、フェノール樹脂、ビスフェノールA、ε-カプロラクタム、アジピン酸、及び可塑剤の製造に有益である。
現在、フェノールの製造に最も普通の経路はホック方法である。これは最初の工程がクメンを製造するためのプロピレンによるベンゼンのアルキル化を伴ない、続いて対応するヒドロペルオキシドへのクメンの酸化次いで等モル量のフェノールとアセトンを製造するためのヒドロペルオキシドの開裂を伴なう3工程方法である。しかしながら、フェノールについての世界の需要がアセトンについての需要よりも迅速に増大しつつある。加えて、ブテンのコストに対するプロピレンのコストが、プロピレンの発展する不足のためにおそらく増大する。
こうして、供給原料としてプロピレンに代えてブテン又は高級アルケンを使用し、アセトンではなく、メチルエチルケトン(ME)又は高級ケトン、例えば、シクロヘキサノンを同時製造する方法がフェノールの製造に魅力的な別の経路であるかもしれない。例えば、MEK(これはラッカー、溶媒として、また潤滑油の脱蝋に有益である)についての増大する市場がある。加えて、シクロヘキサノンは工業用溶媒、酸化反応の活性剤として、またアジピン酸、シクロヘキサノン樹脂、シクロヘキサノンオキシム、カプロラクタム及びナイロン6の製造に使用される。
フェノール及びMEKはsec-ブチルベンゼンを酸化してsec-ブチルベンゼンヒドロペルオキシドを得、そのペルオキシドを所望のフェノール及びメチルエチルケトンに分解する方法でsec-ブチルベンゼンから製造し得ることが知られている。このような方法の総説が“フェノール”と題するProcess Economics Report No. 22B (1977年12月にStanford Research Institute により公表)の113-121頁及び261-263頁に記載されている。
例えば、本件出願人の国際特許公開WO06/015826に、本発明者らはフェノール及びメチルエチルケトンの製造方法を記載しており、その方法ではベンゼンがアルキル化条件下でゼオライトベータ又は12.4±0.25Å、6.9±0.15Å、3.57±0.07Å及び3.42±0.07Åにd-間隔最大を含むX線回折パターンを有するモレキュラーシーブを含む触媒とC4アルキル化剤と接触させられてsec-ブチルベンゼンを含むアルキル化流出物を生成する。次いでsec-ブチルベンゼンが酸化されてヒドロペルオキシドを生成し、そのヒドロペルオキシドが分解されてフェノール及びメチルエチルケトンを生成する。その酸化工程は約70℃〜約200℃、例えば、約90℃〜約130℃の温度、及び約0.5気圧〜約10気圧(50〜1000kPa)の圧力を含む条件下で触媒を用いて、又は用いずに行ない得る。好適な触媒は公開された米国特許出願第2003/0083527号に記載されたN-ヒドロキシ置換環状イミドを含むと言われている。
【0003】
sec-ブチルベンゼン又はシクロヘキシルベンゼンヒドロペルオキシドに高度に選択的であり、既存の酸化方法よりも不純物の存在に敏感ではなく、しかもフェノールとMEK又はフェノールとシクロヘキサノンの有効な商業規模の製造を可能にするsec-ブチルベンゼン及びシクロヘキシルベンゼンの酸化方法を見い出すようにとの要望がある。
遊離基開始剤、例えば、ペルオキシ化合物又はアゾ化合物と組み合わせての、N-ヒドロキシフタルイミドの如き、或る種の環状イミドが、アルキル芳香族炭化水素、例えば、クメン、シクロヘキシルベンゼン、シクロドデシルベンゼン及びsec-ブチルベンゼンを含む、多種の脂肪族又は芳香族炭化水素から対応するヒドロペルオキシドへの接触酸化に有効な触媒であることが、例えば、米国特許第6,852,893号及び同第6,720,462号から知られている。これらの特許はその酸化が0〜500℃の温度及び10-6モル%〜10モル%の触媒対酸化すべき炭化水素のモル比を含む広範囲のプロセス条件にわたって行ない得ることを教示している。しかしながら、示唆がsec-ブチルベンゼンヒドロペルオキシドへのsec-ブチルベンゼン又はシクロヘキシルベンゼンヒドロペルオキシドへのシクロヘキシルベンゼンの選択的酸化方法の効力、又は好ましい条件につきいずれの特許にも提示されていない。
米国特許第7,038,089号は炭化水素、特にエチルベンゼンを130〜160℃の範囲の温度で環状イミド化合物及びアルカリ金属化合物を含む触媒の存在下で酸素含有ガスで酸化することを含むヒドロペルオキシドをそれらの対応する炭化水素から調製するための方法を開示している。特に、その’089特許はエチルベンゼンの酸化が環状イミド及びアルカリ金属化合物を含む触媒の存在下で行なわれる場合に、高い反応速度及び対応するヒドロペルオキシドへの高い選択性が、その触媒系からの両成分が独立に使用される場合に得られるものよりも優れて、同時に得られることを教示している。対照的に、その’089特許によれば、環状イミド単独が触媒として使用される場合に、高いイミド濃度がコスト及び生成物不純物の理由のために避けられる必要があるが、イミド濃度を許容レベルに低下することが、反応速度を増すために温度の上昇を必要とし、許容できないレベルへのヒドロペルオキシドへの選択性の減少をもたらす。
【発明の概要】
【課題を解決するための手段】
【0004】
本発明によれば、sec-ブチルベンゼン及びシクロヘキシルベンゼンを用いて、酸化がアルカリ金属化合物を添加しないで、環状イミド触媒の存在下で商業上実行し得る転化率かつsec-ブチルベンゼン及びシクロヘキシルベンゼンヒドロペルオキシド選択率で行うことができ、但し、その転化が温度及び環状イミド濃度の比較的狭い範囲にわたって行なわれることを条件とすることが今わかった。sec-ブチルベンゼン酸化及びシクロヘキシルベンゼンを用いる、米国特許第7,038,089号の教示とは逆に、アルカリ金属化合物の存在が酸化触媒の活性及びヒドロペルオキシド選択性を重大に低下することがわかった。
一局面において、本発明はアルキル芳香族化合物を対応するアルキル芳香族ヒドロペルオキシドに酸化するための方法にあり、その方法は一般式(I):
【0005】
【化1】

(式中、R1 及びR2 は夫々独立に水素又は1個から4個までの炭素原子を有するアルキル基を表し、但し、R1 及びR2 が結合されて4個から10個までの炭素原子を有する環式基を形成してもよいことを条件とし、前記環式基が必要により置換されていてもよく、かつR3 は水素、1個から4個までの炭素原子を有する1個以上のアルキル基又はシクロヘキシル基を表す)のアルキル芳香族化合物を一般式(II):
【0006】
【化2】

【0007】
(式中、R1 及びR2 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、但し、R1 及びR2 が共有結合を介して互いに結合し得ることを条件とし、
Q1 及びQ2 の夫々は独立にC、CH、CR3から選ばれ、
X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、
YはO又はOHであり、
kは0、1、又は2であり、
lは0、1、又は2であり、
mは1〜3であり、かつ
R3 はR1についてリストされたもののいずれであってもよい)
の環状イミドを含む触媒の存在下で酸素と接触させることを含み、かつ
前記接触が約90℃〜約150℃の温度で行なわれ、前記環状イミドが前記供給原料中のアルキル芳香族化合物の約0.05質量%〜約5質量%の量で存在し、かつ前記触媒がアルカリ金属化合物を実質的に含まず、前記接触が前記供給原料中のアルキル芳香族化合物の少なくとも一部を対応するアルキル芳香族ヒドロペルオキシドに酸化する。
都合良くは、前記環状イミドが一般式(III)に従う。
【0008】
【化3】

【0009】
式中、R7、R8、R9、及びR10 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、
X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、
YはO又はOHであり、
kは0、1、又は2であり、かつ
lは0、1、又は2である。
都合良くは、前記一般式(I)のアルキル芳香族化合物がエチルベンゼン、クメン、sec-ブチルベンゼン、p-メチル-sec-ブチルベンゼン、1,4-ジフェニルシクロヘキサン、sec-ペンチルベンゼン、sec-ヘキシルベンゼン、シクロペンチルベンゼン、シクロヘキシルベンゼン及びシクロオクチルベンゼンから選ばれ、sec-ブチルベンゼン及びシクロヘキシルベンゼンが好ましい。
都合良くは、前記接触が約120℃〜約150℃、例えば、約125℃〜約140℃の温度、及び約15kPa〜約500kPa、例えば、15kPa〜約150kPaの圧力で行なわれる。
都合良くは、前記環状イミドが前記接触中に前記供給原料中のアルキル芳香族化合物の約0.05質量%〜約5質量%の量で存在する。
都合良くは、前記接触が前記アルキル芳香族化合物の時間当たり少なくとも4質量%を少なくとも90質量%の選択率で対応するアルキル芳香族ヒドロペルオキシドに変換する。
一実施態様において、本発明の方法は更にヒドロペルオキシドをフェノール及び一般式R1COCH2R2 (IV) (式中、R1 及びR2 は式(I)中と同じ意味を有する)のアルデヒド又はケトンに変換することを含む。
【図面の簡単な説明】
【0010】
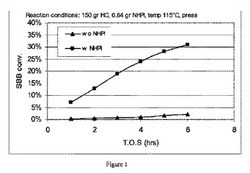
【図1】例1の方法のN-ヒドロキシフタルイミド(NHPI)の不在下及び例2の方法の0.43質量%のNHPIの存在下の115℃におけるsec-ブチルベンゼンの酸化における流れの時間 (T.O.S) に対しsec-ブチルベンゼン転化率をプロットするグラフである。
【図1(a)】例1の方法のNHPIの不在下及び例2の方法の0.43質量%のNHPIの存在下の115℃におけるsec-ブチルベンゼンの酸化におけるsec-ブチルベンゼン転化率に対しsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図2】例3の方法の種々の量のNHPIによる115℃におけるsec-ブチルベンゼンの酸化におけるNHPI濃度に対し反応速度及びsec-ブチルベンゼンヒドロペルオキシド収率をプロットするグラフである。
【図3】例3の方法の種々の量のNHPIによる115℃におけるsec-ブチルベンゼンの酸化におけるNHPI濃度に対しsec-ブチルベンゼン転化率及びsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図4】例4の方法の種々の量のNHPIによる125℃におけるsec-ブチルベンゼンの酸化におけるsec-ブチルベンゼン転化率に対しsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図5(a)】例5の方法の0.05質量%のNHPIの存在下の115℃〜150℃の種々の温度におけるsec-ブチルベンゼンの酸化におけるsec-ブチルベンゼン転化率に対しsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図5(b)】例5の方法の0.10質量%のNHPIの存在下の115℃〜150℃の種々の温度におけるsec-ブチルベンゼンの酸化におけるsec-ブチルベンゼン転化率に対しsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図6(a)】例5の方法の0.05質量%のNHPIの存在下のsec-ブチルベンゼンの酸化における温度に対し反応速度及びsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図6(b)】例5の方法の0.10質量%のNHPIの存在下のsec-ブチルベンゼンの酸化における温度に対し反応速度及びsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【発明を実施するための形態】
【0011】
“基”、及び“置換基”という用語はこの書類中で互換可能に使用される。この開示の目的のために、“ヒドロカルビル基”は水素原子と20個までの炭素原子を含み、線状、分岐、又は環状、そして環状の場合に、芳香族又は非芳香族であってもよい基であると定義される。“置換ヒドロカルビル基”はヒドロカルビル基中の少なくとも1個の水素原子が少なくとも1個の官能基で置換されている基又は少なくとも1個の非炭化水素原子もしくは基がヒドロカルビル基内に挿入されている基である。
本明細書に使用されている、周期律表の族についての新しいナンバリングスキームがChemical and Engineering News, 63(5), 27 (1985)に開示されているように使用される。
アルキル芳香族化合物を対応するヒドロペルオキシドに酸化するため、そして必要により(a)で生成された得られるヒドロペルオキシドを開裂してフェノール及び対応するケトンを生成するための方法が本明細書に記載される。その酸化方法はアルキル芳香族化合物を含む供給原料を対応するアルキル芳香族ヒドロペルオキシドへと接触させることを含み、その方法は一般式(I):
【0012】
【化4】

(式中、R1 及びR2 は夫々独立に水素又は1個から4個までの炭素原子を有するアルキル基を表し、但し、R1 及びR2 が結合されて4個から10個までの炭素原子を有する環式基を形成してもよいことを条件とし、前記環式基が必要により置換されていてもよく、かつR3 は水素、1個から4個までの炭素原子を有する1個以上のアルキル基又はシクロヘキシル基を表す)のアルキル芳香族化合物を一般式(II):
【0013】
【化5】

【0014】
(式中、R1 及びR2 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、但し、R1 及びR2 が共有結合を介して互いに結合し得ることを条件とし、Q1 及びQ2 の夫々は独立にC、CH、CR3から選ばれ、X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、YはO又はOHであり、kは0、1、又は2であり、lは0、1、又は2であり、mは1〜3であり、かつR3 はR1についてリストされたもの(基又は原子)のいずれであってもよい)
の環状イミドを含む触媒の存在下で酸素と接触させることを含む。その酸化は約90℃〜約150℃の温度で行なわれ、環状イミドが供給原料中のアルキル芳香族化合物の約0.05質量%〜約5質量%の量で存在し、かつ触媒がアルカリ金属化合物を実質的に含まない。
“R1 及びR2 が結合されてもよいことを条件として”等という表現は、R1 及びR2の夫々が(“1価の”)アルキル基であることの別型として、“R1” 及び “R2” と称される二つの“アルキル”実体が(“2価の”)ヒドロカルビル鎖(その鎖中に2〜8個の炭素を有する)に結合され、その“2価の”鎖の夫々の末端が式(I)中に明示されたC原子に結合され始めて環を形成することを意味するのに本明細書に使用される。こうして、実施態様において、R1 及びR2 が式(I)の炭素原子に連結するヒドロカルビル部分を一緒に構成して4個から10個までの炭素原子を有する環式基、都合良くはシクロヘキシル基を形成し、これは1個から4個までの炭素原子を有する1個以上のアルキル基又は1個以上のフェニル基で置換されていてもよい。好適なアルキル芳香族化合物の例はエチルベンゼン、クメン、sec-ブチルベンゼン、p-メチル-sec-ブチルベンゼン、1,4-ジフェニルシクロヘキサン、sec-ペンチルベンゼン、sec-ヘキシルベンゼン、シクロペンチルベンゼン、シクロヘキシルベンゼン及びシクロオクチルベンゼンであり、sec-ブチルベンゼン及びシクロヘキシルベンゼンが好ましい。また、R1 及びR2 が結合されて環式基を形成する場合、その環式環を形成する炭素の数が4から10までであることが理解されるであろう。しかしながら、その環それ自体が1個以上の置換基、例えば、1個から4個までの炭素原子を有する1個以上のアルキル基又は、1,4-ジフェニルシクロヘキサンの場合のように、1個以上のフェニル基を有してもよい。
【0015】
sec-ブチルベンゼン製造
一実施態様において、アルキル芳香族化合物がsec-ブチルベンゼン(これはベンゼンをアルキル化条件下で不均一触媒の存在下で少なくとも一種のC4 アルキル化剤でアルキル化することにより製造されてもよい)であってもよい。そのアルキル化条件は都合良くは約60℃から約260℃まで、例えば、約100℃〜約200℃の温度を含む。そのアルキル化の圧力は都合良くは7000kPa以下、例えば、約1000kPaから約3500kPaまでである。そのアルキル化は都合良くはC4 アルキル化剤を基準として約0.1hr-1〜約50hr-1、例えば、約1hr-1〜約10hr-1の毎時の質量空間速度(WHSV)で行なわれる。
C4 アルキル化剤は都合良くは少なくとも一種の線状ブテン、即ち、ブテン-1、ブテン-2又はこれらの混合物を含む。アルキル化剤はまたエタン、プロパン、ブタン、LPG及び軽質ナフサのスチームクラッキング、ナフサ及びその他の製油所供給原料の接触クラッキング及び低級オレフィンへのメタノールの如き酸素化物の変換により得られるような線状ブテンを含むオレフィン性C4 炭化水素混合物であってもよい。例えば、下記のC4 炭化水素混合物が一般にスチームクラッキングを使用するあらゆる製油所でオレフィンを製造するのに利用でき、C4 アルキル化剤としての使用に適している:スチームクラッキングされた粗ブテン流、ラフィネート-1(スチームクラッキングされた粗ブテン流からブタジエンを除去するための溶剤抽出又は水素化後に残っている生成物)及びラフィネート-2(スチームクラッキングされた粗ブテン流からのブタジエン及びイソブテンの除去後に残っている生成物)。
【0016】
シクロヘキシルベンゼン製造
更なる実用的な実施態様において、一般式(I)のアルキル芳香族化合物がシクロヘキシルベンゼンであり、ベンゼンを不均一二機能性触媒(これは典型的にはパラジウム、ルテニウム、ニッケル及びコバルトからなる群から選ばれた、水素化活性を有する少なくとも一種の金属、及びアルキル化活性を有する結晶性無機酸化物物質、典型的にはMCM-22ファミリー(以下に特定される)の少なくとも一種のモレキュラーシーブを含む)の存在下で水素と接触させることにより製造されることが好ましい。その接触工程は都合良くは約50℃〜約350℃の温度及び/又は約100kPa〜約7000kPaの圧力及び/又は約0.01〜約100のベンゼン対水素モル比及び/又は約0.01〜約100のWHSVで行なわれる。
本発明に従って酸化されるアルキル芳香族化合物がシクロヘキシルベンゼンである場合には、その酸化生成物がシクロヘキシルベンゼンヒドロペルオキシドであり、開裂生成物がフェノール及びシクロヘキサノンを含む。その開裂工程からの粗シクロヘキサノン及び粗フェノールが更なる精製にかけられて精製されたシクロヘキサノン及びフェノールを生成してもよい。好適な精製方法として、シクロヘキサノン及びフェノールをその他の種から分離するための一連の蒸留塔が挙げられるが、これに限定されない。粗又は精製シクロヘキサノンそれ自体はそれをフェノールに変換するために脱水素化にかけられてもよい。このような脱水素化は、例えば、白金、ニッケル又はパラジウムの如き触媒により行なわれてもよい。
【0017】
そのアルキル化触媒は都合良くはゼオライトベータであり、これが米国特許第3,308,069号に詳しく記載されており、又は更に好ましくはMCM-22ファミリーの少なくとも一種のモレキュラーシーブである。本明細書に使用される“MCM-22 ファミリー物質”(又は“MCM-22 ファミリーの物質”もしくは“MCM-22 ファミリーのモレキュラーシーブ”或いは“MCM-22ファミリーゼオライト”)という用語は、
・普通の第一級(first degree)結晶性ビルディングブロック単位セル(その単位セルはMWWフレームワークトポロジーを有する)からつくられたモレキュラーシーブ(単位セルは原子の空間配置であり、これは三次元空間中でタイルにされた場合に結晶構造を記載する。このような結晶構造が“ゼオライトフレームワーク型のアトラス”, 第五編, 2001(その全内容が参考として含まれる)に説明されている);
・一つの単位セル厚さ、好ましくは一つのc-単位セル厚さの単層を形成する、このようなMWWフレームワークトポロジー単位セルの2次元のタイリング(tiling)である、普通の第二級(second degree)ビルディングブロックからつくられたモレキュラーシーブ;
・一つ以上の単位セル厚さの層である、普通の第二級ビルディングブロックからつくられたモレキュラーシーブ(一つより多い単位セル厚さの層が一単位セル厚さの少なくとも二つの単層を積み重ね、充填し、又は結合することからつくられる。このような第二級ビルディングブロックの積み重ねは規則的な様式、不規則な様式、ランダム様式、又はこれらのあらゆる組み合わせであってもよい);及び
・MWWフレームワークトポロジーを有する単位セルのあらゆる規則的又はランダムな2次元又は3次元の組み合わせによりつくられたモレキュラーシーブ
の一つ以上を含む。
【0018】
MCM-22ファミリーのモレキュラーシーブは12.4±0.25、6.9±0.15、3.57±0.07及び3.42±0.07 Åにd-間隔最大を含むX線回折パターンを有するモレキュラーシーブを含む。その物質を特性決定するのに使用されるX線回折データは通常の技術により、例えば、入射放射線としての銅のK-α二重線及び収集システムとしてのシンチレーションカウンター及び関連コンピュータを備えたディフラクトメーターを使用して得られる。
MCM-22ファミリーの物質として、MCM-22 (米国特許第4,954,325号に記載されている)、PSH-3 (米国特許第4,439,409号に記載されている)、SSZ-25 (米国特許第4,826,667号に記載されている)、ERB-1 (欧州特許第0293032号に記載されている)、ITQ-1 (米国特許第6,077,498号に記載されている), ITQ-2 (国際特許公開WO97/17290に記載されている)、MCM-36 (米国特許第5,250,277号に記載されている)、MCM-49 (米国特許第5,236,575号に記載されている)、MCM-56 (米国特許第5,362,697号に記載されている)、UZM-8 (米国特許第6,756,030号に記載されている)、及びこれらの混合物が挙げられる。MCM-22ファミリーのモレキュラーシーブはアルキル化触媒として好ましい。何とならば、それらがその他のブチルベンゼン異性体と較べて、sec-ブチルベンゼンの生成に高度に選択的であるとわかったからである。モレキュラーシーブは(a) MCM-49、(b) MCM-56 並びに(c) MCM-49 及びMCM-56のイソタイプ、例えば、ITQ-2から選ばれることが好ましい。
酸化方法
本方法における酸化工程はアルキル芳香族化合物、例えば、sec-ブチルベンゼン及びシクロヘキシルベンゼンを含む供給原料を下記の一般式(II)の環状イミドを含む触媒の存在下で酸素含有ガスと接触させることにより達成される。
【0019】
【化6】

【0020】
式中、R1 及びR2 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、但し、R1 及びR2 が共有結合を介して互いに結合し得ることを条件とし、Q1 及びQ2 の夫々は独立にC、CH、CR3から選ばれ、X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、YはO又はOHであり、kは0、1、又は2であり、lは0、1、又は2であり、mは1〜3、例えば、1、2又は3であり、かつR3 はR1についてリストされたもの(基、又は原子)のいずれであってもよい。都合良くは、R1 及びR2 の夫々が独立に脂肪族アルコキシ基又は芳香族アルコキシ基、カルボキシル基、アルコキシ-カルボニル基及び炭化水素基から選ばれ、これらの基の夫々が1〜20個の炭素原子を有する。
一般に、酸化触媒として使用される環状イミドは一般式(III)に従う。
【0021】
【化7】

【0022】
式中、R7、R8、R9、及びR10 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、YはO又はOHであり、kは0、1、又は2であり、かつlは0、1、又は2である。都合良くは、R7、R8、R9、及びR10 の夫々が独立に脂肪族アルコキシ基又は芳香族アルコキシ基、カルボキシル基、アルコキシ-カルボニル基及び炭化水素基から選ばれ、これらの基の夫々が1〜20個の炭素原子を有する。
一つの実用的な実施態様において、環状イミド触媒がN-ヒドロキシフタルイミドを含む。
環状イミド触媒は前記供給原料中のアルキル芳香族化合物の約0.05質量%〜約5質量%、一般に約0.1質量%〜約1質量%の量で酸化供給原料に添加される。更に、環状イミド触媒は前記供給原料中のアルキル芳香族化合物の(i)約0.05質量%〜約0.10質量%、(ii)約0.1質量%〜約0.2質量%、(iii)約0.2質量%〜約0.3質量%、(iv)約0.3質量%〜約0.4質量%、(v)約0.4質量%〜約0.5質量%、(vi)約0.1質量%〜約0.5質量%、及び(vii)約0.1質量%〜約0.3質量%の量で酸化供給原料に添加されてもよい。更に、その酸化はアルカリ金属化合物の実質的な不在下(その酸化反応混合物の0.00001質量%未満)で行なわれる。
その酸化工程は約90℃〜約150℃、例えば、約120℃〜約150℃、例えば、約125℃〜約140℃の比較的高い温度で行なわれる。何とならば、N-ヒドロキシフタルイミドの存在下のアルキル芳香族化合物酸化では、変換反応プロフィールに対するヒドロペルオキシド選択率が温度を上昇することにより影響されないことがわかったからである。酸化工程は都合良くは約15kPa〜約500kPa、例えば、15kPa〜約150kPaの圧力で行なわれる。環状イミド触媒の濃度及び酸化温度を本明細書に記載されたように調節することにより、時間当たり少なくとも4質量%の前記アルキル芳香族化合物転化率が少なくとも90質量%の対応するヒドロペルオキシドへの選択率とともに得られることがわかる。
【0023】
フェノールの製造
本酸化方法により生成されたヒドロペルオキシドは酸開裂によりフェノール及び対応するケトンに変換し得る。勿論、フェノールはその後にアセトンと反応させられてポリカーボネート及びエポキシ樹脂の製造における前駆体である、ビスフェノールAを生成し得る。
ヒドロペルオキシド開裂反応は都合良くはヒドロペルオキシドを液相中で約20℃〜約150℃、例えば、約40℃〜約120℃の温度、及び/又は約50kPa〜約2500kPa、例えば、約100kPa〜約1000kPaの圧力及び/又はヒドロペルオキシドを基準として約0.1hr-1〜約100hr-1、好ましくは約1hr-1〜約50hr-1の毎時の液空間速度(LHSV)で触媒と接触させることにより行なわれる。ヒドロペルオキシドは開裂反応に不活性の有機溶媒、例えば、メチルエチルケトン、シクロヘキサノン、フェノール、sec-ブチルベンゼン又はシクロヘキシルベンゼン中で希釈されて、熱除去を助けることが好ましい。その開裂反応は都合良くは接触蒸留ユニット中で行なわれる。
その開裂工程で使用される触媒は均一触媒又は不均一触媒であってもよい。
好適な均一開裂触媒として、硫酸、過塩素酸、リン酸、塩酸及びp-トルエンスルホン酸が挙げられる。塩化第二鉄、三フッ化ホウ素、二酸化硫黄及び三酸化硫黄がまた有効な均一開裂触媒である。好ましい均一開裂触媒は硫酸である。
ヒドロペルオキシドの開裂における使用に適した不均一触媒として、スメクタイトクレー、例えば、米国特許第4,870,217号(テキサコ)(その全開示が参考として本明細書に含まれる)に記載された、酸性モンモリロナイトシリカ-アルミナクレーが挙げられる。
今、本発明が下記の非限定実施例を参照して更に特別に記載される。
【実施例】
【0024】
例1.NHPIを用いないSBB酸化
TCIアメリカにより供給されたsec-ブチルベンゼン(SBB) 150gを撹拌機、熱伝対、ガス入り口、サンプリングポート及び水除去のためのディーン・スタークトラップを含む冷却器を取り付けた300mlのパール反応器に計量して入れた。その反応器及び内容物を700rpmで撹拌し、5分間にわたって250cc/分の流量で窒素でスパージした。次いでその反応器を窒素で690kPag(100psig)に加圧し、その間窒素スパージ下に維持し、次いで115℃に加熱した。反応温度に達した時、ガスを窒素から空気に切り替え、反応器を6時間にわたって250cc/分で空気でスパージした。サンプルを1時間毎に採取し、ガスクロマトグラフィーにより分析した。6時間後、ガスを逆に窒素に切り替え、加熱を停止した。反応器が冷却した時、それを圧力解除し、内容物を除去した。転化率結果を図1に示し、転化率結果に対してプロットされた選択率結果を図1(a)に示す。
例2.NHPIの存在下のSBB酸化
N-ヒドロキシフタルイミド(NHPI)0.64g(0.43質量%)をsec-ブチルベンゼン(SBB)150gを含むパール反応器に計量して入れた以外は、例1の方法を繰り返した。再度、転化率結果を図1に示し、選択率結果を図1(a)に示し、これらからNHPIの添加がSBB転化率レベルを著しく改良したことがわかるであろう。NHPIの添加はまた均等転化率レベルを基準とするsec-ブチルベンゼンヒドロペルオキシド(SBBHP)への選択率を改良した。
例3:NHPIの異なるレベルにおけるSBB酸化
【0025】
例2の操作をNHPIの異なる量、即ち、0.05質量%、0.125質量%、0.215質量%及び0.43質量%の添加で繰り返した。結果を図2及び図3にプロットし、反応速度及びsec-ブチルベンゼンヒドロペルオキシド収率(SBB転化率とSBBHP選択率の積)についてのNHPI濃度の影響を示す。データはSBBヒドロペルオキシドへの選択率が異なる収率及びNHPI含量でフラットであることを示す。
例4:異なるNHPI濃度及び125℃の温度におけるSBB酸化
例3の操作を0.05質量%、0.215質量%及び0.43質量%の量のNHPIの添加並びに125℃に上昇された反応温度で繰り返した。結果を図4にプロットし、125℃でヒドロペルオキシド選択率及びSBB転化率がNHPI濃度を増大することにより有意に影響されることを示す。一層高いNHPI濃度で、一層高い選択率が同じ転化率レベルで得られる。
例5:異なる温度並びに0.05質量%及び0.10質量%のNHPI濃度におけるSBB酸化
例3の操作を0.05質量%及び0.10質量%の量のNHPIの添加並びに115℃〜150℃の間で変化された反応温度で繰り返した。結果を図5及び図6にプロットし、これらのNHPI濃度で115℃〜125℃の間で温度を変化させることは転化率プロフィールに対する選択率に影響しないことを示す。
本発明が特別な実施態様を参照して記載され、説明されたが、当業者は本発明が本明細書に必ずしも説明されていない変化に適合することを認めるであろう。この理由のために、本発明の真の範囲を決める目的のために特許請求の範囲のみが参考にされるべきである。
【技術分野】
【0001】
本発明はアルキル芳香族化合物の酸化方法及びその酸化生成物をフェノール及び対応するケトンに変換するための方法に関する。
【背景技術】
【0002】
フェノールは化学工業における重要な製品であり、例えば、フェノール樹脂、ビスフェノールA、ε-カプロラクタム、アジピン酸、及び可塑剤の製造に有益である。
現在、フェノールの製造に最も普通の経路はホック方法である。これは最初の工程がクメンを製造するためのプロピレンによるベンゼンのアルキル化を伴ない、続いて対応するヒドロペルオキシドへのクメンの酸化次いで等モル量のフェノールとアセトンを製造するためのヒドロペルオキシドの開裂を伴なう3工程方法である。しかしながら、フェノールについての世界の需要がアセトンについての需要よりも迅速に増大しつつある。加えて、ブテンのコストに対するプロピレンのコストが、プロピレンの発展する不足のためにおそらく増大する。
こうして、供給原料としてプロピレンに代えてブテン又は高級アルケンを使用し、アセトンではなく、メチルエチルケトン(ME)又は高級ケトン、例えば、シクロヘキサノンを同時製造する方法がフェノールの製造に魅力的な別の経路であるかもしれない。例えば、MEK(これはラッカー、溶媒として、また潤滑油の脱蝋に有益である)についての増大する市場がある。加えて、シクロヘキサノンは工業用溶媒、酸化反応の活性剤として、またアジピン酸、シクロヘキサノン樹脂、シクロヘキサノンオキシム、カプロラクタム及びナイロン6の製造に使用される。
フェノール及びMEKはsec-ブチルベンゼンを酸化してsec-ブチルベンゼンヒドロペルオキシドを得、そのペルオキシドを所望のフェノール及びメチルエチルケトンに分解する方法でsec-ブチルベンゼンから製造し得ることが知られている。このような方法の総説が“フェノール”と題するProcess Economics Report No. 22B (1977年12月にStanford Research Institute により公表)の113-121頁及び261-263頁に記載されている。
例えば、本件出願人の国際特許公開WO06/015826に、本発明者らはフェノール及びメチルエチルケトンの製造方法を記載しており、その方法ではベンゼンがアルキル化条件下でゼオライトベータ又は12.4±0.25Å、6.9±0.15Å、3.57±0.07Å及び3.42±0.07Åにd-間隔最大を含むX線回折パターンを有するモレキュラーシーブを含む触媒とC4アルキル化剤と接触させられてsec-ブチルベンゼンを含むアルキル化流出物を生成する。次いでsec-ブチルベンゼンが酸化されてヒドロペルオキシドを生成し、そのヒドロペルオキシドが分解されてフェノール及びメチルエチルケトンを生成する。その酸化工程は約70℃〜約200℃、例えば、約90℃〜約130℃の温度、及び約0.5気圧〜約10気圧(50〜1000kPa)の圧力を含む条件下で触媒を用いて、又は用いずに行ない得る。好適な触媒は公開された米国特許出願第2003/0083527号に記載されたN-ヒドロキシ置換環状イミドを含むと言われている。
【0003】
sec-ブチルベンゼン又はシクロヘキシルベンゼンヒドロペルオキシドに高度に選択的であり、既存の酸化方法よりも不純物の存在に敏感ではなく、しかもフェノールとMEK又はフェノールとシクロヘキサノンの有効な商業規模の製造を可能にするsec-ブチルベンゼン及びシクロヘキシルベンゼンの酸化方法を見い出すようにとの要望がある。
遊離基開始剤、例えば、ペルオキシ化合物又はアゾ化合物と組み合わせての、N-ヒドロキシフタルイミドの如き、或る種の環状イミドが、アルキル芳香族炭化水素、例えば、クメン、シクロヘキシルベンゼン、シクロドデシルベンゼン及びsec-ブチルベンゼンを含む、多種の脂肪族又は芳香族炭化水素から対応するヒドロペルオキシドへの接触酸化に有効な触媒であることが、例えば、米国特許第6,852,893号及び同第6,720,462号から知られている。これらの特許はその酸化が0〜500℃の温度及び10-6モル%〜10モル%の触媒対酸化すべき炭化水素のモル比を含む広範囲のプロセス条件にわたって行ない得ることを教示している。しかしながら、示唆がsec-ブチルベンゼンヒドロペルオキシドへのsec-ブチルベンゼン又はシクロヘキシルベンゼンヒドロペルオキシドへのシクロヘキシルベンゼンの選択的酸化方法の効力、又は好ましい条件につきいずれの特許にも提示されていない。
米国特許第7,038,089号は炭化水素、特にエチルベンゼンを130〜160℃の範囲の温度で環状イミド化合物及びアルカリ金属化合物を含む触媒の存在下で酸素含有ガスで酸化することを含むヒドロペルオキシドをそれらの対応する炭化水素から調製するための方法を開示している。特に、その’089特許はエチルベンゼンの酸化が環状イミド及びアルカリ金属化合物を含む触媒の存在下で行なわれる場合に、高い反応速度及び対応するヒドロペルオキシドへの高い選択性が、その触媒系からの両成分が独立に使用される場合に得られるものよりも優れて、同時に得られることを教示している。対照的に、その’089特許によれば、環状イミド単独が触媒として使用される場合に、高いイミド濃度がコスト及び生成物不純物の理由のために避けられる必要があるが、イミド濃度を許容レベルに低下することが、反応速度を増すために温度の上昇を必要とし、許容できないレベルへのヒドロペルオキシドへの選択性の減少をもたらす。
【発明の概要】
【課題を解決するための手段】
【0004】
本発明によれば、sec-ブチルベンゼン及びシクロヘキシルベンゼンを用いて、酸化がアルカリ金属化合物を添加しないで、環状イミド触媒の存在下で商業上実行し得る転化率かつsec-ブチルベンゼン及びシクロヘキシルベンゼンヒドロペルオキシド選択率で行うことができ、但し、その転化が温度及び環状イミド濃度の比較的狭い範囲にわたって行なわれることを条件とすることが今わかった。sec-ブチルベンゼン酸化及びシクロヘキシルベンゼンを用いる、米国特許第7,038,089号の教示とは逆に、アルカリ金属化合物の存在が酸化触媒の活性及びヒドロペルオキシド選択性を重大に低下することがわかった。
一局面において、本発明はアルキル芳香族化合物を対応するアルキル芳香族ヒドロペルオキシドに酸化するための方法にあり、その方法は一般式(I):
【0005】
【化1】

(式中、R1 及びR2 は夫々独立に水素又は1個から4個までの炭素原子を有するアルキル基を表し、但し、R1 及びR2 が結合されて4個から10個までの炭素原子を有する環式基を形成してもよいことを条件とし、前記環式基が必要により置換されていてもよく、かつR3 は水素、1個から4個までの炭素原子を有する1個以上のアルキル基又はシクロヘキシル基を表す)のアルキル芳香族化合物を一般式(II):
【0006】
【化2】

【0007】
(式中、R1 及びR2 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、但し、R1 及びR2 が共有結合を介して互いに結合し得ることを条件とし、
Q1 及びQ2 の夫々は独立にC、CH、CR3から選ばれ、
X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、
YはO又はOHであり、
kは0、1、又は2であり、
lは0、1、又は2であり、
mは1〜3であり、かつ
R3 はR1についてリストされたもののいずれであってもよい)
の環状イミドを含む触媒の存在下で酸素と接触させることを含み、かつ
前記接触が約90℃〜約150℃の温度で行なわれ、前記環状イミドが前記供給原料中のアルキル芳香族化合物の約0.05質量%〜約5質量%の量で存在し、かつ前記触媒がアルカリ金属化合物を実質的に含まず、前記接触が前記供給原料中のアルキル芳香族化合物の少なくとも一部を対応するアルキル芳香族ヒドロペルオキシドに酸化する。
都合良くは、前記環状イミドが一般式(III)に従う。
【0008】
【化3】

【0009】
式中、R7、R8、R9、及びR10 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、
X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、
YはO又はOHであり、
kは0、1、又は2であり、かつ
lは0、1、又は2である。
都合良くは、前記一般式(I)のアルキル芳香族化合物がエチルベンゼン、クメン、sec-ブチルベンゼン、p-メチル-sec-ブチルベンゼン、1,4-ジフェニルシクロヘキサン、sec-ペンチルベンゼン、sec-ヘキシルベンゼン、シクロペンチルベンゼン、シクロヘキシルベンゼン及びシクロオクチルベンゼンから選ばれ、sec-ブチルベンゼン及びシクロヘキシルベンゼンが好ましい。
都合良くは、前記接触が約120℃〜約150℃、例えば、約125℃〜約140℃の温度、及び約15kPa〜約500kPa、例えば、15kPa〜約150kPaの圧力で行なわれる。
都合良くは、前記環状イミドが前記接触中に前記供給原料中のアルキル芳香族化合物の約0.05質量%〜約5質量%の量で存在する。
都合良くは、前記接触が前記アルキル芳香族化合物の時間当たり少なくとも4質量%を少なくとも90質量%の選択率で対応するアルキル芳香族ヒドロペルオキシドに変換する。
一実施態様において、本発明の方法は更にヒドロペルオキシドをフェノール及び一般式R1COCH2R2 (IV) (式中、R1 及びR2 は式(I)中と同じ意味を有する)のアルデヒド又はケトンに変換することを含む。
【図面の簡単な説明】
【0010】
【図1】例1の方法のN-ヒドロキシフタルイミド(NHPI)の不在下及び例2の方法の0.43質量%のNHPIの存在下の115℃におけるsec-ブチルベンゼンの酸化における流れの時間 (T.O.S) に対しsec-ブチルベンゼン転化率をプロットするグラフである。
【図1(a)】例1の方法のNHPIの不在下及び例2の方法の0.43質量%のNHPIの存在下の115℃におけるsec-ブチルベンゼンの酸化におけるsec-ブチルベンゼン転化率に対しsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図2】例3の方法の種々の量のNHPIによる115℃におけるsec-ブチルベンゼンの酸化におけるNHPI濃度に対し反応速度及びsec-ブチルベンゼンヒドロペルオキシド収率をプロットするグラフである。
【図3】例3の方法の種々の量のNHPIによる115℃におけるsec-ブチルベンゼンの酸化におけるNHPI濃度に対しsec-ブチルベンゼン転化率及びsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図4】例4の方法の種々の量のNHPIによる125℃におけるsec-ブチルベンゼンの酸化におけるsec-ブチルベンゼン転化率に対しsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図5(a)】例5の方法の0.05質量%のNHPIの存在下の115℃〜150℃の種々の温度におけるsec-ブチルベンゼンの酸化におけるsec-ブチルベンゼン転化率に対しsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図5(b)】例5の方法の0.10質量%のNHPIの存在下の115℃〜150℃の種々の温度におけるsec-ブチルベンゼンの酸化におけるsec-ブチルベンゼン転化率に対しsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図6(a)】例5の方法の0.05質量%のNHPIの存在下のsec-ブチルベンゼンの酸化における温度に対し反応速度及びsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【図6(b)】例5の方法の0.10質量%のNHPIの存在下のsec-ブチルベンゼンの酸化における温度に対し反応速度及びsec-ブチルベンゼンヒドロペルオキシド選択率をプロットするグラフである。
【発明を実施するための形態】
【0011】
“基”、及び“置換基”という用語はこの書類中で互換可能に使用される。この開示の目的のために、“ヒドロカルビル基”は水素原子と20個までの炭素原子を含み、線状、分岐、又は環状、そして環状の場合に、芳香族又は非芳香族であってもよい基であると定義される。“置換ヒドロカルビル基”はヒドロカルビル基中の少なくとも1個の水素原子が少なくとも1個の官能基で置換されている基又は少なくとも1個の非炭化水素原子もしくは基がヒドロカルビル基内に挿入されている基である。
本明細書に使用されている、周期律表の族についての新しいナンバリングスキームがChemical and Engineering News, 63(5), 27 (1985)に開示されているように使用される。
アルキル芳香族化合物を対応するヒドロペルオキシドに酸化するため、そして必要により(a)で生成された得られるヒドロペルオキシドを開裂してフェノール及び対応するケトンを生成するための方法が本明細書に記載される。その酸化方法はアルキル芳香族化合物を含む供給原料を対応するアルキル芳香族ヒドロペルオキシドへと接触させることを含み、その方法は一般式(I):
【0012】
【化4】

(式中、R1 及びR2 は夫々独立に水素又は1個から4個までの炭素原子を有するアルキル基を表し、但し、R1 及びR2 が結合されて4個から10個までの炭素原子を有する環式基を形成してもよいことを条件とし、前記環式基が必要により置換されていてもよく、かつR3 は水素、1個から4個までの炭素原子を有する1個以上のアルキル基又はシクロヘキシル基を表す)のアルキル芳香族化合物を一般式(II):
【0013】
【化5】

【0014】
(式中、R1 及びR2 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、但し、R1 及びR2 が共有結合を介して互いに結合し得ることを条件とし、Q1 及びQ2 の夫々は独立にC、CH、CR3から選ばれ、X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、YはO又はOHであり、kは0、1、又は2であり、lは0、1、又は2であり、mは1〜3であり、かつR3 はR1についてリストされたもの(基又は原子)のいずれであってもよい)
の環状イミドを含む触媒の存在下で酸素と接触させることを含む。その酸化は約90℃〜約150℃の温度で行なわれ、環状イミドが供給原料中のアルキル芳香族化合物の約0.05質量%〜約5質量%の量で存在し、かつ触媒がアルカリ金属化合物を実質的に含まない。
“R1 及びR2 が結合されてもよいことを条件として”等という表現は、R1 及びR2の夫々が(“1価の”)アルキル基であることの別型として、“R1” 及び “R2” と称される二つの“アルキル”実体が(“2価の”)ヒドロカルビル鎖(その鎖中に2〜8個の炭素を有する)に結合され、その“2価の”鎖の夫々の末端が式(I)中に明示されたC原子に結合され始めて環を形成することを意味するのに本明細書に使用される。こうして、実施態様において、R1 及びR2 が式(I)の炭素原子に連結するヒドロカルビル部分を一緒に構成して4個から10個までの炭素原子を有する環式基、都合良くはシクロヘキシル基を形成し、これは1個から4個までの炭素原子を有する1個以上のアルキル基又は1個以上のフェニル基で置換されていてもよい。好適なアルキル芳香族化合物の例はエチルベンゼン、クメン、sec-ブチルベンゼン、p-メチル-sec-ブチルベンゼン、1,4-ジフェニルシクロヘキサン、sec-ペンチルベンゼン、sec-ヘキシルベンゼン、シクロペンチルベンゼン、シクロヘキシルベンゼン及びシクロオクチルベンゼンであり、sec-ブチルベンゼン及びシクロヘキシルベンゼンが好ましい。また、R1 及びR2 が結合されて環式基を形成する場合、その環式環を形成する炭素の数が4から10までであることが理解されるであろう。しかしながら、その環それ自体が1個以上の置換基、例えば、1個から4個までの炭素原子を有する1個以上のアルキル基又は、1,4-ジフェニルシクロヘキサンの場合のように、1個以上のフェニル基を有してもよい。
【0015】
sec-ブチルベンゼン製造
一実施態様において、アルキル芳香族化合物がsec-ブチルベンゼン(これはベンゼンをアルキル化条件下で不均一触媒の存在下で少なくとも一種のC4 アルキル化剤でアルキル化することにより製造されてもよい)であってもよい。そのアルキル化条件は都合良くは約60℃から約260℃まで、例えば、約100℃〜約200℃の温度を含む。そのアルキル化の圧力は都合良くは7000kPa以下、例えば、約1000kPaから約3500kPaまでである。そのアルキル化は都合良くはC4 アルキル化剤を基準として約0.1hr-1〜約50hr-1、例えば、約1hr-1〜約10hr-1の毎時の質量空間速度(WHSV)で行なわれる。
C4 アルキル化剤は都合良くは少なくとも一種の線状ブテン、即ち、ブテン-1、ブテン-2又はこれらの混合物を含む。アルキル化剤はまたエタン、プロパン、ブタン、LPG及び軽質ナフサのスチームクラッキング、ナフサ及びその他の製油所供給原料の接触クラッキング及び低級オレフィンへのメタノールの如き酸素化物の変換により得られるような線状ブテンを含むオレフィン性C4 炭化水素混合物であってもよい。例えば、下記のC4 炭化水素混合物が一般にスチームクラッキングを使用するあらゆる製油所でオレフィンを製造するのに利用でき、C4 アルキル化剤としての使用に適している:スチームクラッキングされた粗ブテン流、ラフィネート-1(スチームクラッキングされた粗ブテン流からブタジエンを除去するための溶剤抽出又は水素化後に残っている生成物)及びラフィネート-2(スチームクラッキングされた粗ブテン流からのブタジエン及びイソブテンの除去後に残っている生成物)。
【0016】
シクロヘキシルベンゼン製造
更なる実用的な実施態様において、一般式(I)のアルキル芳香族化合物がシクロヘキシルベンゼンであり、ベンゼンを不均一二機能性触媒(これは典型的にはパラジウム、ルテニウム、ニッケル及びコバルトからなる群から選ばれた、水素化活性を有する少なくとも一種の金属、及びアルキル化活性を有する結晶性無機酸化物物質、典型的にはMCM-22ファミリー(以下に特定される)の少なくとも一種のモレキュラーシーブを含む)の存在下で水素と接触させることにより製造されることが好ましい。その接触工程は都合良くは約50℃〜約350℃の温度及び/又は約100kPa〜約7000kPaの圧力及び/又は約0.01〜約100のベンゼン対水素モル比及び/又は約0.01〜約100のWHSVで行なわれる。
本発明に従って酸化されるアルキル芳香族化合物がシクロヘキシルベンゼンである場合には、その酸化生成物がシクロヘキシルベンゼンヒドロペルオキシドであり、開裂生成物がフェノール及びシクロヘキサノンを含む。その開裂工程からの粗シクロヘキサノン及び粗フェノールが更なる精製にかけられて精製されたシクロヘキサノン及びフェノールを生成してもよい。好適な精製方法として、シクロヘキサノン及びフェノールをその他の種から分離するための一連の蒸留塔が挙げられるが、これに限定されない。粗又は精製シクロヘキサノンそれ自体はそれをフェノールに変換するために脱水素化にかけられてもよい。このような脱水素化は、例えば、白金、ニッケル又はパラジウムの如き触媒により行なわれてもよい。
【0017】
そのアルキル化触媒は都合良くはゼオライトベータであり、これが米国特許第3,308,069号に詳しく記載されており、又は更に好ましくはMCM-22ファミリーの少なくとも一種のモレキュラーシーブである。本明細書に使用される“MCM-22 ファミリー物質”(又は“MCM-22 ファミリーの物質”もしくは“MCM-22 ファミリーのモレキュラーシーブ”或いは“MCM-22ファミリーゼオライト”)という用語は、
・普通の第一級(first degree)結晶性ビルディングブロック単位セル(その単位セルはMWWフレームワークトポロジーを有する)からつくられたモレキュラーシーブ(単位セルは原子の空間配置であり、これは三次元空間中でタイルにされた場合に結晶構造を記載する。このような結晶構造が“ゼオライトフレームワーク型のアトラス”, 第五編, 2001(その全内容が参考として含まれる)に説明されている);
・一つの単位セル厚さ、好ましくは一つのc-単位セル厚さの単層を形成する、このようなMWWフレームワークトポロジー単位セルの2次元のタイリング(tiling)である、普通の第二級(second degree)ビルディングブロックからつくられたモレキュラーシーブ;
・一つ以上の単位セル厚さの層である、普通の第二級ビルディングブロックからつくられたモレキュラーシーブ(一つより多い単位セル厚さの層が一単位セル厚さの少なくとも二つの単層を積み重ね、充填し、又は結合することからつくられる。このような第二級ビルディングブロックの積み重ねは規則的な様式、不規則な様式、ランダム様式、又はこれらのあらゆる組み合わせであってもよい);及び
・MWWフレームワークトポロジーを有する単位セルのあらゆる規則的又はランダムな2次元又は3次元の組み合わせによりつくられたモレキュラーシーブ
の一つ以上を含む。
【0018】
MCM-22ファミリーのモレキュラーシーブは12.4±0.25、6.9±0.15、3.57±0.07及び3.42±0.07 Åにd-間隔最大を含むX線回折パターンを有するモレキュラーシーブを含む。その物質を特性決定するのに使用されるX線回折データは通常の技術により、例えば、入射放射線としての銅のK-α二重線及び収集システムとしてのシンチレーションカウンター及び関連コンピュータを備えたディフラクトメーターを使用して得られる。
MCM-22ファミリーの物質として、MCM-22 (米国特許第4,954,325号に記載されている)、PSH-3 (米国特許第4,439,409号に記載されている)、SSZ-25 (米国特許第4,826,667号に記載されている)、ERB-1 (欧州特許第0293032号に記載されている)、ITQ-1 (米国特許第6,077,498号に記載されている), ITQ-2 (国際特許公開WO97/17290に記載されている)、MCM-36 (米国特許第5,250,277号に記載されている)、MCM-49 (米国特許第5,236,575号に記載されている)、MCM-56 (米国特許第5,362,697号に記載されている)、UZM-8 (米国特許第6,756,030号に記載されている)、及びこれらの混合物が挙げられる。MCM-22ファミリーのモレキュラーシーブはアルキル化触媒として好ましい。何とならば、それらがその他のブチルベンゼン異性体と較べて、sec-ブチルベンゼンの生成に高度に選択的であるとわかったからである。モレキュラーシーブは(a) MCM-49、(b) MCM-56 並びに(c) MCM-49 及びMCM-56のイソタイプ、例えば、ITQ-2から選ばれることが好ましい。
酸化方法
本方法における酸化工程はアルキル芳香族化合物、例えば、sec-ブチルベンゼン及びシクロヘキシルベンゼンを含む供給原料を下記の一般式(II)の環状イミドを含む触媒の存在下で酸素含有ガスと接触させることにより達成される。
【0019】
【化6】

【0020】
式中、R1 及びR2 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、但し、R1 及びR2 が共有結合を介して互いに結合し得ることを条件とし、Q1 及びQ2 の夫々は独立にC、CH、CR3から選ばれ、X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、YはO又はOHであり、kは0、1、又は2であり、lは0、1、又は2であり、mは1〜3、例えば、1、2又は3であり、かつR3 はR1についてリストされたもの(基、又は原子)のいずれであってもよい。都合良くは、R1 及びR2 の夫々が独立に脂肪族アルコキシ基又は芳香族アルコキシ基、カルボキシル基、アルコキシ-カルボニル基及び炭化水素基から選ばれ、これらの基の夫々が1〜20個の炭素原子を有する。
一般に、酸化触媒として使用される環状イミドは一般式(III)に従う。
【0021】
【化7】

【0022】
式中、R7、R8、R9、及びR10 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、YはO又はOHであり、kは0、1、又は2であり、かつlは0、1、又は2である。都合良くは、R7、R8、R9、及びR10 の夫々が独立に脂肪族アルコキシ基又は芳香族アルコキシ基、カルボキシル基、アルコキシ-カルボニル基及び炭化水素基から選ばれ、これらの基の夫々が1〜20個の炭素原子を有する。
一つの実用的な実施態様において、環状イミド触媒がN-ヒドロキシフタルイミドを含む。
環状イミド触媒は前記供給原料中のアルキル芳香族化合物の約0.05質量%〜約5質量%、一般に約0.1質量%〜約1質量%の量で酸化供給原料に添加される。更に、環状イミド触媒は前記供給原料中のアルキル芳香族化合物の(i)約0.05質量%〜約0.10質量%、(ii)約0.1質量%〜約0.2質量%、(iii)約0.2質量%〜約0.3質量%、(iv)約0.3質量%〜約0.4質量%、(v)約0.4質量%〜約0.5質量%、(vi)約0.1質量%〜約0.5質量%、及び(vii)約0.1質量%〜約0.3質量%の量で酸化供給原料に添加されてもよい。更に、その酸化はアルカリ金属化合物の実質的な不在下(その酸化反応混合物の0.00001質量%未満)で行なわれる。
その酸化工程は約90℃〜約150℃、例えば、約120℃〜約150℃、例えば、約125℃〜約140℃の比較的高い温度で行なわれる。何とならば、N-ヒドロキシフタルイミドの存在下のアルキル芳香族化合物酸化では、変換反応プロフィールに対するヒドロペルオキシド選択率が温度を上昇することにより影響されないことがわかったからである。酸化工程は都合良くは約15kPa〜約500kPa、例えば、15kPa〜約150kPaの圧力で行なわれる。環状イミド触媒の濃度及び酸化温度を本明細書に記載されたように調節することにより、時間当たり少なくとも4質量%の前記アルキル芳香族化合物転化率が少なくとも90質量%の対応するヒドロペルオキシドへの選択率とともに得られることがわかる。
【0023】
フェノールの製造
本酸化方法により生成されたヒドロペルオキシドは酸開裂によりフェノール及び対応するケトンに変換し得る。勿論、フェノールはその後にアセトンと反応させられてポリカーボネート及びエポキシ樹脂の製造における前駆体である、ビスフェノールAを生成し得る。
ヒドロペルオキシド開裂反応は都合良くはヒドロペルオキシドを液相中で約20℃〜約150℃、例えば、約40℃〜約120℃の温度、及び/又は約50kPa〜約2500kPa、例えば、約100kPa〜約1000kPaの圧力及び/又はヒドロペルオキシドを基準として約0.1hr-1〜約100hr-1、好ましくは約1hr-1〜約50hr-1の毎時の液空間速度(LHSV)で触媒と接触させることにより行なわれる。ヒドロペルオキシドは開裂反応に不活性の有機溶媒、例えば、メチルエチルケトン、シクロヘキサノン、フェノール、sec-ブチルベンゼン又はシクロヘキシルベンゼン中で希釈されて、熱除去を助けることが好ましい。その開裂反応は都合良くは接触蒸留ユニット中で行なわれる。
その開裂工程で使用される触媒は均一触媒又は不均一触媒であってもよい。
好適な均一開裂触媒として、硫酸、過塩素酸、リン酸、塩酸及びp-トルエンスルホン酸が挙げられる。塩化第二鉄、三フッ化ホウ素、二酸化硫黄及び三酸化硫黄がまた有効な均一開裂触媒である。好ましい均一開裂触媒は硫酸である。
ヒドロペルオキシドの開裂における使用に適した不均一触媒として、スメクタイトクレー、例えば、米国特許第4,870,217号(テキサコ)(その全開示が参考として本明細書に含まれる)に記載された、酸性モンモリロナイトシリカ-アルミナクレーが挙げられる。
今、本発明が下記の非限定実施例を参照して更に特別に記載される。
【実施例】
【0024】
例1.NHPIを用いないSBB酸化
TCIアメリカにより供給されたsec-ブチルベンゼン(SBB) 150gを撹拌機、熱伝対、ガス入り口、サンプリングポート及び水除去のためのディーン・スタークトラップを含む冷却器を取り付けた300mlのパール反応器に計量して入れた。その反応器及び内容物を700rpmで撹拌し、5分間にわたって250cc/分の流量で窒素でスパージした。次いでその反応器を窒素で690kPag(100psig)に加圧し、その間窒素スパージ下に維持し、次いで115℃に加熱した。反応温度に達した時、ガスを窒素から空気に切り替え、反応器を6時間にわたって250cc/分で空気でスパージした。サンプルを1時間毎に採取し、ガスクロマトグラフィーにより分析した。6時間後、ガスを逆に窒素に切り替え、加熱を停止した。反応器が冷却した時、それを圧力解除し、内容物を除去した。転化率結果を図1に示し、転化率結果に対してプロットされた選択率結果を図1(a)に示す。
例2.NHPIの存在下のSBB酸化
N-ヒドロキシフタルイミド(NHPI)0.64g(0.43質量%)をsec-ブチルベンゼン(SBB)150gを含むパール反応器に計量して入れた以外は、例1の方法を繰り返した。再度、転化率結果を図1に示し、選択率結果を図1(a)に示し、これらからNHPIの添加がSBB転化率レベルを著しく改良したことがわかるであろう。NHPIの添加はまた均等転化率レベルを基準とするsec-ブチルベンゼンヒドロペルオキシド(SBBHP)への選択率を改良した。
例3:NHPIの異なるレベルにおけるSBB酸化
【0025】
例2の操作をNHPIの異なる量、即ち、0.05質量%、0.125質量%、0.215質量%及び0.43質量%の添加で繰り返した。結果を図2及び図3にプロットし、反応速度及びsec-ブチルベンゼンヒドロペルオキシド収率(SBB転化率とSBBHP選択率の積)についてのNHPI濃度の影響を示す。データはSBBヒドロペルオキシドへの選択率が異なる収率及びNHPI含量でフラットであることを示す。
例4:異なるNHPI濃度及び125℃の温度におけるSBB酸化
例3の操作を0.05質量%、0.215質量%及び0.43質量%の量のNHPIの添加並びに125℃に上昇された反応温度で繰り返した。結果を図4にプロットし、125℃でヒドロペルオキシド選択率及びSBB転化率がNHPI濃度を増大することにより有意に影響されることを示す。一層高いNHPI濃度で、一層高い選択率が同じ転化率レベルで得られる。
例5:異なる温度並びに0.05質量%及び0.10質量%のNHPI濃度におけるSBB酸化
例3の操作を0.05質量%及び0.10質量%の量のNHPIの添加並びに115℃〜150℃の間で変化された反応温度で繰り返した。結果を図5及び図6にプロットし、これらのNHPI濃度で115℃〜125℃の間で温度を変化させることは転化率プロフィールに対する選択率に影響しないことを示す。
本発明が特別な実施態様を参照して記載され、説明されたが、当業者は本発明が本明細書に必ずしも説明されていない変化に適合することを認めるであろう。この理由のために、本発明の真の範囲を決める目的のために特許請求の範囲のみが参考にされるべきである。
【特許請求の範囲】
【請求項1】
アルキル芳香族化合物を対応するアルキル芳香族ヒドロペルオキシドに酸化するための方法であって、一般式(I):
【化1】

(式中、R1 及びR2 は夫々独立に水素又は1個から4個までの炭素原子を有するアルキル基を表し、但し、R1 及びR2 が結合されて4個から10個までの炭素原子を有する環式基を形成してもよいことを条件とし、前記環式基が必要により置換されていてもよく、かつR3 は水素、1個から4個までの炭素原子を有する1個以上のアルキル基又はシクロヘキシル基を表す)のアルキル芳香族化合物を一般式(II):
【化2】

(式中、R1 及びR2 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、但し、R1 及びR2 が共有結合を介して互いに結合し得ることを条件とし、
Q1 及びQ2 の夫々は独立にC、CH、CR3から選ばれ、
X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、
YはO又はOHであり、
kは0、1、又は2であり、
lは0、1、又は2であり、
mは1〜3であり、かつ
R3 はR1 についてリストされたもののいずれであってもよい)
の環状イミドを含む触媒の存在下で酸素と接触させることを含み、かつ
前記接触が約90℃〜約150℃の温度で行なわれ、前記環状イミドが前記供給原料中のアルキル芳香族化合物の約0.05質量%〜約5質量%の量で存在し、かつ前記触媒がアルカリ金属化合物を実質的に含まず、前記接触が前記供給原料中のアルキル芳香族化合物の少なくとも一部を対応するアルキル芳香族ヒドロペルオキシドに酸化することを特徴とする上記方法。
【請求項2】
前記環状イミドが一般式(II):
【化3】

(式中、R7、R8、R9、及びR10 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、
X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、
YはO又はOHであり、
kは0、1、又は2であり、かつ
lは0、1、又は2である)
に従う、請求項1記載の方法。
【請求項3】
前記環状イミドがN-ヒドロキシフタルイミドを含む、請求項1から2のいずれかに記載の方法。
【請求項4】
前記接触を約120℃〜約150℃の温度及び約15kPa〜約500kPaの圧力で行なう、請求項1から3のいずれかに記載の方法。
【請求項5】
前記接触を約125℃〜約140℃の温度及び約15kPa〜約150kPaの圧力で行なう、請求項1から3のいずれか1項記載の方法。
【請求項6】
前記環状イミドが前記接触中に前記供給原料中のアルキル芳香族化合物の約0.1質量%〜約1質量%の量で存在する、請求項1から5のいずれかに記載の方法。
【請求項7】
前記環状イミドが前記接触中に前記供給原料中のアルキル芳香族化合物の約0.05質量%〜約0.5質量%の量で存在する、請求項1から5のいずれか1項記載の方法。
【請求項8】
前記接触が少なくとも90質量%の対応するアルキル芳香族ヒドロペルオキシドへの選択率で前記アルキル芳香族化合物の時間当たり少なくとも4質量%を変換する、請求項1から7のいずれかに記載の方法。
【請求項9】
前記アルキル芳香族化合物がクメン、sec-ブチルベンゼン、及びシクロヘキシルベンゼンから選ばれる、請求項1から8のいずれかに記載の方法。
【請求項10】
前記アルキル芳香族化合物がsec-ブチルベンゼンから選ばれる、請求項1から9のいずれかに記載の方法。
【請求項11】
前記アルキル芳香族化合物がシクロヘキシルベンゼンから選ばれる、請求項1から10のいずれかに記載の方法。
【請求項12】
アルキル芳香族ヒドロペルオキシドを開裂してフェノール及び対応するケトンを製造する工程を更に含む、請求項1から11のいずれかに記載の方法。
【請求項13】
開裂を触媒の存在下で行なう、請求項12記載の方法。
【請求項14】
開裂を均一触媒の存在下で行なう、請求項12記載の方法。
【請求項15】
前記均一触媒が硫酸、過塩素酸、リン酸、塩酸、p-トルエンスルホン酸、塩化第二鉄、三フッ化ホウ素、二酸化硫黄及び三酸化硫黄の少なくとも一種を含む、請求項14記載の方法。
【請求項16】
開裂を不均一触媒の存在下で行なう、請求項12記載の方法。
【請求項17】
前記不均一触媒がスメクタイトクレーを含む、請求項16記載の方法。
【請求項18】
開裂を約40℃〜約120℃の温度、約100kPa〜約1000kPaの圧力、及びヒドロペルオキシドを基準として約1hr-1〜約50hr-1の毎時の液空間速度(LHSV)で行なう、請求項12記載の方法。
【請求項1】
アルキル芳香族化合物を対応するアルキル芳香族ヒドロペルオキシドに酸化するための方法であって、一般式(I):
【化1】

(式中、R1 及びR2 は夫々独立に水素又は1個から4個までの炭素原子を有するアルキル基を表し、但し、R1 及びR2 が結合されて4個から10個までの炭素原子を有する環式基を形成してもよいことを条件とし、前記環式基が必要により置換されていてもよく、かつR3 は水素、1個から4個までの炭素原子を有する1個以上のアルキル基又はシクロヘキシル基を表す)のアルキル芳香族化合物を一般式(II):
【化2】

(式中、R1 及びR2 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、但し、R1 及びR2 が共有結合を介して互いに結合し得ることを条件とし、
Q1 及びQ2 の夫々は独立にC、CH、CR3から選ばれ、
X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、
YはO又はOHであり、
kは0、1、又は2であり、
lは0、1、又は2であり、
mは1〜3であり、かつ
R3 はR1 についてリストされたもののいずれであってもよい)
の環状イミドを含む触媒の存在下で酸素と接触させることを含み、かつ
前記接触が約90℃〜約150℃の温度で行なわれ、前記環状イミドが前記供給原料中のアルキル芳香族化合物の約0.05質量%〜約5質量%の量で存在し、かつ前記触媒がアルカリ金属化合物を実質的に含まず、前記接触が前記供給原料中のアルキル芳香族化合物の少なくとも一部を対応するアルキル芳香族ヒドロペルオキシドに酸化することを特徴とする上記方法。
【請求項2】
前記環状イミドが一般式(II):
【化3】

(式中、R7、R8、R9、及びR10 の夫々は独立に1〜20個の炭素原子を有するヒドロカルビル基及び置換ヒドロカルビル基、又は基SO3H、NH2、OH、及びNO2 もしくは原子H、F、Cl、Br、及びIから選ばれ、
X及びZの夫々は独立にC、S、CH2 、N、P及び周期律表の4族の元素から選ばれ、
YはO又はOHであり、
kは0、1、又は2であり、かつ
lは0、1、又は2である)
に従う、請求項1記載の方法。
【請求項3】
前記環状イミドがN-ヒドロキシフタルイミドを含む、請求項1から2のいずれかに記載の方法。
【請求項4】
前記接触を約120℃〜約150℃の温度及び約15kPa〜約500kPaの圧力で行なう、請求項1から3のいずれかに記載の方法。
【請求項5】
前記接触を約125℃〜約140℃の温度及び約15kPa〜約150kPaの圧力で行なう、請求項1から3のいずれか1項記載の方法。
【請求項6】
前記環状イミドが前記接触中に前記供給原料中のアルキル芳香族化合物の約0.1質量%〜約1質量%の量で存在する、請求項1から5のいずれかに記載の方法。
【請求項7】
前記環状イミドが前記接触中に前記供給原料中のアルキル芳香族化合物の約0.05質量%〜約0.5質量%の量で存在する、請求項1から5のいずれか1項記載の方法。
【請求項8】
前記接触が少なくとも90質量%の対応するアルキル芳香族ヒドロペルオキシドへの選択率で前記アルキル芳香族化合物の時間当たり少なくとも4質量%を変換する、請求項1から7のいずれかに記載の方法。
【請求項9】
前記アルキル芳香族化合物がクメン、sec-ブチルベンゼン、及びシクロヘキシルベンゼンから選ばれる、請求項1から8のいずれかに記載の方法。
【請求項10】
前記アルキル芳香族化合物がsec-ブチルベンゼンから選ばれる、請求項1から9のいずれかに記載の方法。
【請求項11】
前記アルキル芳香族化合物がシクロヘキシルベンゼンから選ばれる、請求項1から10のいずれかに記載の方法。
【請求項12】
アルキル芳香族ヒドロペルオキシドを開裂してフェノール及び対応するケトンを製造する工程を更に含む、請求項1から11のいずれかに記載の方法。
【請求項13】
開裂を触媒の存在下で行なう、請求項12記載の方法。
【請求項14】
開裂を均一触媒の存在下で行なう、請求項12記載の方法。
【請求項15】
前記均一触媒が硫酸、過塩素酸、リン酸、塩酸、p-トルエンスルホン酸、塩化第二鉄、三フッ化ホウ素、二酸化硫黄及び三酸化硫黄の少なくとも一種を含む、請求項14記載の方法。
【請求項16】
開裂を不均一触媒の存在下で行なう、請求項12記載の方法。
【請求項17】
前記不均一触媒がスメクタイトクレーを含む、請求項16記載の方法。
【請求項18】
開裂を約40℃〜約120℃の温度、約100kPa〜約1000kPaの圧力、及びヒドロペルオキシドを基準として約1hr-1〜約50hr-1の毎時の液空間速度(LHSV)で行なう、請求項12記載の方法。
【図1】


【図1(a)】


【図2】


【図3】


【図4】


【図5(a)】


【図5(b)】


【図6(a)】


【図6(b)】




【図1(a)】


【図2】


【図3】


【図4】


【図5(a)】


【図5(b)】


【図6(a)】


【図6(b)】


【公表番号】特表2012−512155(P2012−512155A)
【公表日】平成24年5月31日(2012.5.31)
【国際特許分類】
【出願番号】特願2011−540720(P2011−540720)
【出願日】平成21年9月17日(2009.9.17)
【国際出願番号】PCT/US2009/057239
【国際公開番号】WO2010/074779
【国際公開日】平成22年7月1日(2010.7.1)
【出願人】(501357658)エクソンモービル ケミカル パテンツ インコーポレイテッド (2)
【Fターム(参考)】
【公表日】平成24年5月31日(2012.5.31)
【国際特許分類】
【出願日】平成21年9月17日(2009.9.17)
【国際出願番号】PCT/US2009/057239
【国際公開番号】WO2010/074779
【国際公開日】平成22年7月1日(2010.7.1)
【出願人】(501357658)エクソンモービル ケミカル パテンツ インコーポレイテッド (2)
【Fターム(参考)】
[ Back to top ]

