アンスラサイクリン系抗がん剤治療の有効性を判定する方法、及びアンスラサイクリン系抗がん剤治療の有効性の診断支援方法
【課題】より高精度に癌の再発リスクを判定しうる、新規なアンスラサイクリン系抗がん剤治療の有効性判定方法、及びより高精度にアンスラサイクリン系抗がん剤治療の有効性診断を支援しうる、新規なアンスラサイクリン系抗がん剤治療の有効性の診断支援方法を提供する
【解決手段】
本発明による癌の再発リスクの判定方法は、被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、下記式(1)に基づいて判定スコアを求め、得られた判定スコアに基づいてアンスラサイクリン系抗がん剤治療の有効性を判定することを特徴とする。
判定スコア=F(x)×G(y) ・・・(1)
(式中、xは第1CDK比活性を表し、yは比活性比を表す)
【解決手段】
本発明による癌の再発リスクの判定方法は、被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、下記式(1)に基づいて判定スコアを求め、得られた判定スコアに基づいてアンスラサイクリン系抗がん剤治療の有効性を判定することを特徴とする。
判定スコア=F(x)×G(y) ・・・(1)
(式中、xは第1CDK比活性を表し、yは比活性比を表す)
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、サイクリン依存性キナーゼの発現量と活性値とに基づいて、アンスラサイクリン系抗がん剤治療の有効性を判定する、アンスラサイクリン系抗がん剤治療の有効性判定方法に関する。また、本発明は、サイクリン依存性キナーゼの発現量と活性値とに基づいて、アンスラサイクリン系抗がん剤治療の有効性の診断支援情報を提供する、アンスラサイクリン系抗がん剤治療の有効性の診断支援方法に関する。
【背景技術】
【0002】
従来、サイクリン依存性キナーゼ(以下、単に「CDK」とも称する)を利用した抗がん剤治療の有効性を予測する方法が提案されている。
【0003】
例えば、特許文献1には、患者から採取した腫瘍細胞のサイクリン依存性キナーゼの活性値、発現量、及び活性値と発現量の比からなる群より選択される少なくとも1つのパラメータと、選択されたパラメータに対応する閾値とを比較し、その結果に基づいて患者の抗がん剤治療の有効性を予測する方法が記載されている。この方法によれば、抗がん剤に対する感受性を高率に予測判定することができる。
【0004】
【特許文献1】特開2007−6882号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
本発明は、より高精度に抗がん剤治療の有効性を判定しうる、新規なアンスラサイクリン系抗がん剤治療の有効性判定方法を提供することを目的とするものである。また、本発明は、より高精度に抗がん剤治療の有効性診断を支援しうる、新規な抗がん剤治療の有効性の診断支援方法を提供することを目的とするものである。
【課題を解決するための手段】
【0006】
上記の課題を解決するため、本発明の第1の観点によるアンスラサイクリン系抗がん剤治療の有効性判定方法は、被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、下記式(1)に基づいて判定スコアを求め、得られた判定スコアに基づいてアンスラサイクリン系抗がん剤治療の有効性を判定することを特徴とする。
判定スコア=F(x)×G(y) ・・・(1)
(式中、xは第1CDK比活性を表し、この第1CDK比活性は、第1CDK活性値/第1CDK発現量で示される:
式中、yは比活性比を表し、この比活性比は、第2CDK比活性/第1CDK比活性で示され、第2CDK比活性は、第2CDK活性値/第2CDK発現量で示される)
【0007】
本発明において算出される判定スコアとは、後述するように、その癌患者における癌の再発リスクを反映するパラメータである。癌の再発リスクは細胞の増殖能に関係しており、異常な増殖能を有する細胞は癌化する可能性が高いと考えられている。抗がん剤は通常、癌患者に投与されることで細胞の増殖能を低減し、癌の増殖を防ぐものであるため、抗がん剤治療の有効性は細胞の増殖能と密接に関係している。
そこで、癌の再発リスクを反映する判定スコアと、抗がん剤、特にアンスラサイクリン系抗がん剤治療の有効性(抗がん剤治療の結果)との関係について研究を行った結果、本発明者らは、癌の判定スコアと抗がん剤治療の有効性とに相関があることを見出した。
ゆえに、癌の再発リスクを反映する判定スコアを指標としてアンスラサイクリン系抗がん剤治療の有効性を判定することにより、高精度に抗がん剤治療の有効性を判定することができる。
【0008】
また、本発明の別の観点によるアンスラサイクリン系抗がん剤治療の有効性の診断支援方法は、被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、第1CDKの比活性と、第2CDKの比活性の二つのパラメータからなり、下記式(2)に基づいて算出される判定スコアの異なる領域毎に分割された判定図に、得られた第1CDK比活性及び第2CDK比活性をプロットして表示することを特徴とする。
判定スコア=F(x)×G(y) ・・・(2)
(式中、xは第1CDK比活性を表し、この第1CDK比活性は、第1CDK活性値/第1CDK発現量で示される:
式中、yは比活性比を表し、この比活性比は、第2CDK比活性/第1CDK比活性で示され、第2CDK比活性は、第2CDK活性値/第2CDK発現量で示される)
【発明の効果】
【0009】
本発明によれば、高精度にアンスラサイクリン系抗がん剤治療の有効性を判定しうる、アンスラサイクリン系抗がん剤治療の有効性判定方法を提供することができる。また、本発明によれば、高精度にアンスラサイクリン系抗がん剤治療の有効性の診断支援方法を提供することができる。
【発明を実施するための最良の形態】
【0010】
[1]アンスラサイクリン系抗がん剤治療の有効性判定方法
本発明の第1の観点による判定方法は、被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、得られた第1CDK及び第2CDKの発現量と活性値とに基づいて判定スコアを求め、得られた判定スコアに基づいてアンスラサイクリン系抗がん剤治療の有効性を判定することを特徴とする。
【0011】
ここで、本明細書における「がん」は、上皮細胞がん、造血器由来のがん、肉腫などを含む。がんの種類としては、例えば、乳がん、胃がん、大腸がん、食道がん、前立腺がん、白血病、骨肉腫等が挙げられる。
【0012】
また、本明細書における「抗がん剤」とは、上述のがんに対して抗腫瘍効果のある化学物質のことをいうものとする。
【0013】
また、本明細書におけるアンスラサイクリン系抗がん剤とは、アグリコンであるアンスラサイクリノンに1〜3種のアミノ酸または中性糖が結合した一群の抗生物質である。アンスラサイクリン系抗がん剤としては、例えばダウノルビシン、ドキソルビシン、アクラルビシン、エピルビシン、ブレオマイシンなどが挙げられる。
【0014】
また、本明細書における「再発」とは、悪性腫瘍を摘出するために臓器を部分切除した後、残存臓器に同じ悪性腫瘍が再現する場合、及び原発巣から腫瘍細胞が分離して遠隔組織(遠隔臓器)へ運ばれ、そこで自立的に増殖する場合(転移再発)をいうものとする。
【0015】
また、本明細書における「再発リスク」とは、悪性腫瘍が摘出された癌患者の身体に癌が再発する危険、または癌が再発することによって癌患者が死亡する危険を意味する。本明細書中で特に断らない限り、「再発リスク」はそのいずれも含むものとする。
【0016】
(1)被検癌患者から採取した悪性腫瘍から、第1のCDK及び第2のCDKの発現量と活性値を取得する工程
被検癌患者から採取される悪性腫瘍は、例えば被検癌患者の生体組織のうち、繊維性結合組織、軟骨組織、骨組織、血液、リンパ等の支持組織、上皮組織、筋組織、神経組織を構成する細胞であればよい。特に、本実施形態による判定方法に用いられる細胞としては、個体としての調和を破り、増殖の制御機構に異常を来たしている組織の腫瘍細胞のように、病理的情報を得たい細胞が好適である。例えば、乳、肺、肝臓、胃、大腸、膵臓、皮膚、子宮、精巣、卵巣、甲状腺、副甲状腺、リンパ系統、骨髄などの位置にできる腫瘍の細胞が好適な対象となる。
【0017】
サイクリン依存性キナーゼ(CDK)とは、サイクリンと結合して活性化される酵素群の総称で、単独では活性をもたないが、サイクリンと結合して活性型となる。CDKは、その種類に応じて、細胞周期の特定時期で機能している。CDKとしては、CDK1、CDK2、CDK4、CDK6、サイクリンA依存性キナーゼ、サイクリンB依存性キナーゼ、及びサイクリンD依存性キナーゼなどが挙げられる。
ここに挙げた複数種のCDKから第1のCDKと第2のCDKとを決定し、被検癌患者から採取された悪性腫瘍の第1のCDKと、第2のCDKの発現量及び活性値を測定する。
【0018】
CDK活性値とは、特定のサイクリンと結合して、そのサイクリンをリン酸化する基質の量から算出されるキナーゼ活性のレベル(単位をU(ユニット)で表す)をいう。なお、前記CDKがリン酸化する基質としては、例えば、活性型CDK1及び活性型CDK2については、ヒストンH1が挙げられ、活性型CDK4及び活性型CDK6については、Rb(網膜芽細胞腫タンパク質)が挙げられる。CDK活性値は、慣用のCDK活性測定方法によって測定することができる。具体的には、測定試料の細胞溶解液から活性型CDKを含む試料を調製し、試料と、32P標識したATP(γ−〔32P〕−ATP)とを用いて、基質タンパク質に32Pを取り込ませ、32P標識されたリン酸化基質の標識量を測定し、標準品で作成された検量線をもとに定量する方法がある。また放射性物質の標識を用いない方法としては、特開2002−335997号に開示の方法が挙げられる。この方法は、検体の細胞可溶化液から、目的の活性型CDKを含む試料を調製し、アデノシン5'−O−(3−チオトリホスフェート)(ATP−γS)と基質を反応させて、該基質タンパク質のセリン又はスレオニン残基にモノチオリン酸基を導入し、導入されたモノチオリン酸基の硫黄原子に標識蛍光物質又は標識酵素を結合させることによって基質タンパク質を標識し、標識されたチオリン酸基質の標識量(標識蛍光物質を用いた場合には蛍光量)を測定し、標準品で作成された検量線に基づいて定量する方法である。
【0019】
活性測定に供する試料は、測定対象となる悪性腫瘍を含む組織の可溶化液から目的のCDKを特異的に採集することにより調製する。この場合、試料は目的のCDKに特異的な抗CDK抗体を用いて調製してもよいし、特定のサイクリン依存性キナーゼ(例えばサイクリンA依存性キナーゼ、サイクリンB依存性キナーゼ、サイクリンE依存性キナーゼ)活性測定の場合には、抗サイクリン抗体を用いて調製する。いずれの場合も活性型CDK以外のCDKが試料に含まれることになる。例えばサイクリン・CDK複合体にCDKインヒビターが結合した複合体も含まれる。また、抗CDK抗体を用いた場合には、CDK単体、CDKとサイクリン及び/又はCDKインヒビターの複合体、CDKとその他の化合物との複合体などが含まれる。従って、活性値は、活性型、不活性型、各種競合反応が混在する状態下で、リン酸化された基質の単位(U)として測定される。
【0020】
CDK発現量とは、測定対象となる悪性腫瘍を含む組織の細胞可溶化液に含まれる目的のCDK量(分子個数に対応する単位)であって、タンパク質混合物から目的のタンパク質量を測定する従来公知の方法で測定できる。例えば、ELISA法、ウェスタンブロット法などを使用してもよいし、特開2003−130871号に開示の方法で測定することもできる。目的のタンパク質(CDK)は、特異的抗体を用いて捕捉すればよい。例えば、抗CDK1抗体を用いることにより、細胞内に存在するCDK1のすべて(CDK単体、CDKとサイクリン及び/又はCDKインヒビターの複合体、CDKとその他の化合物との複合体を含む)を捕捉できる。
【0021】
(2)判定スコアを算出する工程
上記の工程によって得られた2種類のCDKの発現量と活性値に基づいて判定スコアSを求める。判定スコアSは、下記式(3)乃至(5)によって求められる。
S=F(x)×G(y) ・・・(3)
F(x)=a/(1+Exp(−(x−b)×c)) ・・・(4)
G(y)=d/(1+Exp(−(y−e)×f)) ・・・(5)
(式中、a〜fは定数)
上記式において、xは第1のCDKの比活性を表し、yは比活性比を表す。ここで、CDK比活性は、CDK活性値/CDK発現量で示され、比活性比は、第2CDK比活性/第1CDK比活性で示される。上記式(3)乃至(5)、比活性及び比活性比については、後に詳しく説明する。
【0022】
(3)判定スコアに基づいて抗がん剤治療の有効性を判定する工程
上記において得られた判定スコアSと、予め設定された閾値とを比較して、アンスラサイクリン系抗がん剤治療の有効性を判定する。例えば、被検癌患者の判定スコアSと閾値とを比較し、被検癌患者の判定スコアSが閾値より高い場合には、被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性が高く、被検癌患者の判定スコアSが閾値より低い場合には、被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性が低いというようにして、アンスラサイクリン系抗がん剤治療の有効性を判定することができる。
【0023】
閾値は、抗がん剤の種類、癌の種類により適宜設定される値である。具体的には、所定の癌患者に対してアンスラサイクリン系抗がん剤を投与した治療結果と判定スコアSとの関係を、多くの抗がん剤治療結果について調べ、アンスラサイクリン系抗がん剤による治療が有効であった症例と、有効でなかった症例とに区別しうるような判定スコアSを閾値とすることができる。
このように、実際の臨床治療結果に基づいて閾値を設定することにより、信頼性の高い抗がん剤治療の有効性の予測が可能となる。
【0024】
ここで、上記式(3)乃至(5)について説明する。
【0025】
まず、CDK比活性と、比活性比の意義について説明する。
CDK比活性は、CDK活性値/CDK発現量によって示されることからも明らかなように、CDKの発現量に対する活性値の比である。CDK比活性は、試料に含まれる単位CDKタンパク質量あたりのCDK酵素活性を反映するパラメータであって、細胞に存在しているCDKのうちの活性を示すCDKの割合に相当し、判定対象である悪性腫瘍細胞の増殖状態に基づくCDK活性レベルを示す。
【0026】
また、比活性比は、第2CDK比活性/第1CDK比活性によって示されることからも明らかなように、第1CDKの比活性に対する第2CDKの比活性の比である。CDK比活性比は、特定の細胞周期において活性を示す二種類のCDKの活性レベルの比であり、癌患者の細胞においていずれのCDK活性が優位であるか(細胞周期のいずれの時期にある細胞割合がどの程度であるか)を反映するパラメータである。
一般に、癌細胞は正常な増殖制御を逸脱して増殖が活発に行われていることから、DNAの複製期であるS期と、DNA合成の終了から有糸分裂の開始の間であるG2期にある細胞の割合が多い場合に、その細胞が癌化しているものと考えることができる。また、癌細胞に見られる異数倍体性は、細胞分裂期であるM期を異常な状態で経過した場合や、又はM期を経ずにG1期に進み、そのままS期に移行したときに発生するものと考えられるため、M期に存在する細胞割合が少ない場合にも、その細胞が癌化していると考えることができる。
そこで、例えば、第1のCDKとして細胞周期のG2期からM期に移行する際に活性を示すCDK1を、第2のCDKとして細胞周期のG1期からS期に移行する際に活性を示すCDK2を使用し、これらに基づいてCDK比活性比を求めた場合には、得られるCDK比活性比は、S期またはG2期にある細胞が、M期にある細胞に比べてどれだけ多く存在するかを反映する数値であり、細胞の増殖能を正確に反映するパラメータとして用いることができる。
【0027】
次に、判定スコアSを算出するための式(3)乃至(5)について説明する。
上記において説明したように、第1CDK比活性と、第2CDK比活性とに基づくCDK比活性比を得ることにより、細胞の増殖能(癌の再発リスク)に相関するパラメータを得ることができる。
しかしながら、CDK比活性比が細胞の増殖能(癌の再発リスク)に相関しない場合がありうる。例えば、上記において例示したように、第1のCDKとしてCDK1を、第2のCDKとしてCDK2を用いてCDK比活性比を求めたとき、CDK1比活性が異常に大きい場合には、CDK比活性比の値は小さくなるが、これは別の観点からみれば、CDK1と複合体を形成するサイクリンが高発現し、CDK1が異常に活性化されていることともいえる。
細胞は、ある細胞周期に活性化するCDKが少なくても、他の特定のCDKが代償的に働くことによって増殖することが可能であるとも考えられており、特定のCDKが異常に活性化されている場合にも、細胞動態に異常を来たしていると考えることができる。
【0028】
そこで、癌の再発リスクが、(1)第1CDKの比活性、(2)第1CDKと第2CDKの比活性比、の二つのリスク要素によって規定されるものと考え、これらのリスク要素に基づいて癌の再発リスクを評価することとした。上記(1)、(2)の各リスク要素に基づいて癌が再発する確率を、数値的に評価する尺度を用いて、それぞれリスクスコアRS(1)、リスクスコアRS(2)とする。さらに、上記(1)、(2)のリスク要素によって結果的に癌が再発する確率を、数値的に評価する尺度を用いて、再発リスクスコアRRSとする。結果的に癌が再発する確率(再発リスク)は、上記(1)、(2)の二つのリスク要素によって癌が再発する確率の積によって与えられるので、再発リスクスコアRRSは、リスクスコアRS(1)とリスクスコアRS(2)の積に比例する値で与えられる。したがって、
RRS=RS(1)×RS(2) ・・・(6)
が成り立つ。
【0029】
リスクスコアRS(1)及びリスクスコアRS(2)は、以下のようにして求められる。
図1(a)は、複数の被検癌患者から得られたCDK1比活性と癌の再発率との関係を示したヒストグラムであり、図1(b)は、複数の被検癌患者から得られたCDK1とCDK2の比活性比と癌の再発率との関係を示したヒストグラムである。同図においては、複数の被検癌患者を、当該被検癌患者から得られたCDK1比活性、又はCDK1とCDK2の比活性比に基づいて階級分けし、各階級に含まれる症例の総数を白抜きの棒グラフで、各階級に含まれる再発症例を網掛けの棒グラフで示した。さらに、各階級における癌の再発確率(再発症例数/症例総数)を求め、折れ線で示した。
【0030】
同図からも明らかなように、癌の再発確率は、CDK1比活性、又はCDK1とCDK2の比活性比に伴って単調に増加することがわかる。したがって、各階級ごとの癌の再発確率を近似することにより、CDK1比活性をリスク要素とするリスクスコアRS(1)、及びCDK1とCDK2の比活性比をリスク要素とするリスクスコアRS(2)を得ることができる。そこで、CDK1比活性の値をx、CDK1とCDK2の比活性比をyとして、各階級ごとの癌の再発確率をロジスティック関数によって近似することにより、リスクスコアRS(1)及びリスクスコアRS(2)を得ることができる。すなわち、リスクスコアRS(1)及びリスクスコアRS(2)はそれぞれ、
RS(1);F(x)=a/(1+Exp(−(x−b)×c)) ・・・(7)
RS(2);G(y)=d/(1+Exp(−(y−e)×f)) ・・・(8)
(式中、a〜fは定数)
によって表される。
【0031】
上記式(6)によって求められる再発リスクスコアRRSは、第1CDKと第2CDKの発現量と活性値とに基づく被検癌患者の癌の再発リスクを数値化したものである。この再発リスクスコアRRSと、被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性との関係について調べた結果、両者の間に密接な相関関係が認められた。よって、上記式(6)によって算出される再発リスクスコアRRSを、アンスラサイクリン系抗がん剤治療の有効性を判定するための指標(判定スコアS)として用いることにより、高精度にアンスラサイクリン系抗がん剤治療の有効性を判定することが可能となる。
したがって、アンスラサイクリン系抗がん剤治療の有効性を判定するための判定スコアSは、
S=F(x)×G(y) ・・・(9)
として求められる。
【0032】
上記実施形態においては、判定スコアSを算出して、これを閾値と比較することによりアンスラサイクリン系抗がん剤治療の有効性を判定する方法について説明したが、これに限らず、他の判定基準とともにアンスラサイクリン系抗がん剤治療の有効性を判定するようにしてもよい。
【0033】
例えば、被検癌患者の悪性腫瘍から、判定スコアSとは別に、第1のCDKの比活性を算出して、判定スコアSを第1の判定基準とし、第1CDK比活性を第2の判定基準として、二つの判定基準に基づいてアンスラサイクリン系抗がん剤治療の有効性を判定するように構成することができる。
【0034】
具体的には、まず、上記において説明したように、被検癌患者から第1のCDK及び第2のCDKの発現量と活性値を取得し、判定スコアSと、第1CDK比活性を算出する。
次に、得られた判定スコアSと第1CDK比活性を、それぞれに対する閾値とを比較してアンスラサイクリン系抗がん剤治療の有効性を判定する。
より具体的には、判定スコアSに対する閾値として第1の閾値を、第1CDK比活性に対する閾値として第2の閾値を設定し、被検癌患者から得られる判定スコアS及び第1CDK比活性のいずれか一方が閾値以上である場合にはアンスラサイクリン系抗がん剤治療の有効性が高いと判定し、判定スコアS及び第1CDK比活性のいずれもが閾値未満である場合にはアンスラサイクリン系抗がん剤治療の有効性が低いと判定する。
【0035】
第1の閾値と第2の閾値は、それぞれ2つ以上の閾値を含んでもよい。例えば、第1の閾値として第1閾値aと第1閾値bを設定し、第2の閾値として第2閾値aと、第2閾値bを予め設定しておく。そして、判定スコアSが第1閾値a以上であるか、または、第1CDK比活性が第2閾値a以上であるとき、アンスラサイクリン系抗がん剤治療の有効性が高いと判定し、判定スコアSが第1閾値b未満であり、かつ、第1CDK比活性が第2閾値b未満であるとき、アンスラサイクリン系抗がん剤治療の有効性が低いと判定し、判定スコアSが第1閾値a未満、第1閾値b以上であり、かつ、第1CDK比活性が第2閾値a未満、第2閾値b以上であるとき、アンスラサイクリン系抗がん剤治療の有効性が中程度であると判定する。
このように、判定スコアSと、他の判定基準とによってアンスラサイクリン系抗がん剤治療の有効性を判定することにより、より精度の高い判定を行うことが可能となる。
【0036】
また本実施形態においては、アンスラサイクリン系抗がん剤治療の有効性を判定するための判定図を表示することにより、アンスラサイクリン系抗がん剤治療の有効性診断を支援する方法を提供する。
図2は、上記において説明した判定スコアSを模式的に説明するための図である。図2(a)は、CDK1比活性の対数(x軸)、CDK2比活性の対数(y軸)、及び判定スコアS(z軸)をパラメータとする三次元グラフであり、図2(b)は、図2(a)の判定スコアS(z軸)を二次元平面に投影したグラフである。
【0037】
図2(b)に示したように、判定スコアSを二次元グラフに投影すると、判定スコアSが等しくなる点を結んだ、複数の等高線状の曲線が描かれる。
例えば、曲線CL1上の点はすべて、等しい判定スコアSとなるCDK1比活性及びCDK2比活性の点であり、曲線CL2上の点はすべて、等しい判定スコアSとなるCDK1比活性及びCDK2比活性の点である。そして、曲線によって囲まれた領域は常に曲線上の点より判定スコアSが高くなる領域であるから(図2(a)参照)、例えば、曲線CL1が判定スコアS=Mとなる点を結んで描かれたものである場合、この曲線CL1によって囲まれた領域はすべて、判定スコアS≧Mとなる領域である。また、曲線CL1が判定スコアSが所定値Mとなる点を、曲線CL2が判定スコアSが所定値Nとなる点を結んで描かれたものである場合、曲線CL1と曲線CL2とによって囲まれた領域Sは、M≦判定スコアS<Nとなる領域である。
【0038】
このように、第1CDK比活性(x軸)及び第2CDK比活性(y軸)からなる二次元グラフは、等しい判定スコアSとなる点を結んだ曲線(カットオフライン)によって、判定スコアSの異なる領域毎に分割することができる。
【0039】
アンスラサイクリン系抗がん剤治療の有効性を判定するための判定図は、次のようにして作成することができる。
まず、判定スコアSに対する閾値を設定する。判定スコアSに対する閾値は、アンスラサイクリン系抗がん剤治療の有効性の判定に有効な値であればよく、例えば、その閾値を超えるか否かによってアンスラサイクリン系抗がん剤治療の有効性が高い癌患者とアンスラサイクリン系抗がん剤治療の有効性が低い癌患者とに分類しうるような閾値が用いられる。
次に、第1CDK比活性と第2CDK比活性の二つのパラメータからなる二次元グラフ上に、判定スコアSが閾値となる点を結んでカットオフラインを作成し、二次元グラフを判定スコアSが閾値以上となる領域と、閾値以下となる領域とに分割する。このカットオフラインは、アンスラサイクリン系抗がん剤治療の有効性判定の基準となる値に基づいて作成されているから、二次元グラフは、アンスラサイクリン系抗がん剤治療の有効性が高い領域と低い領域とに分割される。このようにして、アンスラサイクリン系抗がん剤治療の有効性を判定するための判定図が作成される。
【0040】
このような判定図に、被検癌患者の悪性腫瘍から得られた第1CDK及び第2CDKの発現量と活性値とに基づいて算出された第1CDK比活性及び第2CDK比活性をプロットする。判定図は、閾値となるカットオフラインによってアンスラサイクリン系抗がん剤治療の有効性の高い領域と低い領域とに分割されているから、被検癌患者の第1CDK比活性及び第2CDK比活性が判定図にプロットされることにより、その患者におけるアンスラサイクリン系抗がん剤治療の有効性が高いか低いかを一目で理解することができる。このような判定図を表示すれば、医師は判定図を見るだけで癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を判断することができ、患者の診断に役立つ情報を提供することができる。
【0041】
図3は、本実施形態によるアンスラサイクリン系抗がん剤治療の有効性の診断支援方法に使用される判定図の一例を示した図である。この判定図は、x座標に第1CDK比活性、y座標に第2CDK比活性をとり、その分布領域を、カットオフラインBL1によって、アンスラサイクリン系抗がん剤治療の有効性の高い領域(Highゾーン)と、アンスラサイクリン系抗がん剤治療の有効性の低い領域(Lowゾーン)とに分割したものである。
【0042】
いま、ある癌患者Aから得られた第1CDK比活性と第2CDK比活性とに基づいて、判定図上に点Aがプロットされたとする。図3に示したように、点Aは、Highゾーンに属していることから、この癌患者Aは、アンスラサイクリン系抗がん剤治療の有効性が高いと判定することができる。
同様に、ある癌患者Bから得られた第1CDK比活性と第2CDK比活性とに基づいて、判定図上に点Bがプロットされたとする。図3に示したように、点Bは、Lowゾーンに属していることから、この癌患者Bは、アンスラサイクリン系抗がん剤治療の有効性が低いと判定することができる。
【0043】
アンスラサイクリン系抗がん剤治療の有効性を判定するための判定図は、その用途に応じて異なる形態の判定図を用いることができる。
図4は、本実施形態によるアンスラサイクリン系抗がん剤治療の有効性の診断支援方法に使用される判定図の他の例を示した図である。この判定図は、x座標に第1CDK比活性、y座標に第2CDK比活性をとり、その分布領域を、カットオフラインBL2及びカットオフラインBL3とによって、アンスラサイクリン系抗がん剤治療の有効性の高い領域(Highゾーン)、アンスラサイクリン系抗がん剤治療の有効性の低い領域(Lowゾーン)、中間領域(Int.ゾーン)の3つの領域に分割したものである。
このように3つ以上の領域に分割された判定図を用いることにより、被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を段階的に判定することができる。
【0044】
図5は、本実施形態によるアンスラサイクリン系抗がん剤治療の有効性の診断支援方法に使用される判定図の他の例を示した図である。この判定図は、判定スコアSが閾値となる点を結んで描かれる曲線と、第1CDK比活性の閾値を示す直線とを結合して作成されるカットオフラインBL4とカットオフラインBL5とによって、その分布領域を、アンスラサイクリン系抗がん剤治療の有効性の高い領域(Highゾーン)、アンスラサイクリン系抗がん剤治療の有効性の低い領域(Lowゾーン)、中間領域(Int.ゾーン)の3つの領域に分割したものである。
このように、判定スコアSと第1CDK比活性とに基づいて分割された判定図を用いることにより、被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性をより高精度に判定することができる。
【0045】
[2]判定装置
次に、本実施形態のアンスラサイクリン系抗がん剤治療の有効性判定装置について説明する。
【0046】
図6は、本実施形態における判定装置の概略構成を示すブロック図である。本実施形態における判定装置1は、被検癌患者から得られたデータに基づいてその癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を判定する装置であって、図6に示すように、制御装置10と、測定装置20とを備えて構成されている。制御装置10は、測定装置20から出力された測定データを解析して癌の再発リスクを判定し、判定結果を出力するための装置であり、測定装置20は、被検癌患者から採取された悪性腫瘍を測定して測定データを制御装置10へ出力するための装置である。
【0047】
制御装置10は、パーソナルコンピュータ(PC)からなり、制御部101と、キーボード103と、表示部105とを備えている。制御部101は、CPU101aと、ROM101bと、RAM101cと、ハードディスク101dと、画像出力インターフェース101eと、通信インターフェース101fと、画像出力インターフェース101gと、バス101hとを備え、各部はバス101hを介して接続されており、相互にデータの送受信が可能である。
【0048】
CPU101aは、ROM101bに記憶されているコンピュータプログラムおよびRAM101cにロードされたコンピュータプログラムを実行することが可能である。ROM101bには、CPU101aによって実行されるコンピュータプログラムおよびCPU101aがコンピュータプログラムを実行するためのデータなどが記録されている。RAM101cは、ROM101bおよびハードディスク101dに記録されているコンピュータプログラムの読み出しに用いられる。また、これらのコンピュータプログラムを実行するときに、CPU101aの作業領域として利用される。
【0049】
ハードディスク101dには、オペレーティングシステム(OS)やアプリケーションプログラムなど、CPU101aに実行させるための種々のコンピュータプログラムおよびそのコンピュータプログラムの実行に用いるデータがインストールされている。
ハードディスク101dにインストールされているアプリケーションプログラム101iには、本発明によるアンスラサイクリン系抗がん剤治療の有効性の判定方法を実現するためのアプリケーションプログラムが含まれている。
【0050】
入出力インタフェース101eには、キーボード103やマウス(図示せず)が接続されている。通信インタフェース101fには測定装置20が接続されており、制御部101は、通信インタフェース101fを介して測定装置2とデータの送受信が可能である。
【0051】
画像出力インタフェース101gは、表示部105に接続されており、CPU101aから与えられた画像データに応じた映像信号を表示部105に出力する。表示部105は、入力された映像信号にしたがって、画像(画面)を表示する。
【0052】
判定装置10と通信インタフェース101fを介して接続される測定装置20は、生体組織からCDKの発現量と活性値を測定するための装置である。このような、生体組織からCDK発現量及びCDK活性値を測定するための測定装置として、特開2007−74975号公報に記載されているような装置を用いることができる。
【0053】
なお、本実施形態において、判定装置1は、測定装置20によって得られた測定データを受け付け、測定データに基づいて被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を判定するように構成されているが、このような構成に限られず、例えば、予めCDK発現量及びCDK活性値を測定しておき、キーボード103から測定データを入力する構成であってもよい。
【0054】
図7は、本実施形態に係る判定装置1によるアンスラサイクリン系抗がん剤治療の有効性判定処理を示すフローチャートである。
このフローチャートによる処理は、ハードディスク101dにインストールされたアプリケーションプログラム101iがRAM101cに読み出され、CPU101aがRAM101cに読み出されたアプリケーションプログラム101iを実行することによって実現される。
【0055】
まず、ステップS101において、CPU101aは、測定装置20から測定データを受信したか否かを判定する処理を実行する。CPU101aが、測定装置20から測定データを受信していないと判定した場合(ステップS101においてNO)には、処理がリターンされる。
なお、ここでいう測定データとは、測定装置20が生体組織を測定することによって得られた少なくとも2種類のCDKの発現量と活性値である。
【0056】
CPU101aが測定装置20から測定データを受信したと判定した場合(ステップS101においてYES)には、ステップS102の処理に進み、CPU101aは、判定スコアSを算出する処理を実行する。
アプリケーションプログラム101iには、アンスラサイクリン系抗がん剤治療の有効性判定方法において記載したような、第1CDK及び第2CDKの発現量及び活性値に基づいて判定スコアSを算出するための式が組み込まれており、CPU101aがアプリケーションプログラム101iを実行することによって判定スコアSが算出される。
【0057】
ついでステップS103の処理に進み、CPU101aは、アンスラサイクリン系抗がん剤治療の有効性を判定する処理を実行する。この処理は、ステップS102において算出された判定スコアSを、アプリケーションプログラム101i内に設定された所定の閾値と比較することにより行われる。
CPU101aは、判定スコアSが所定の閾値以上であるとき、アンスラサイクリン系抗がん剤治療の有効性「高」と判定し、判定スコアSが所定の閾値未満であるとき、アンスラサイクリン系抗がん剤治療の有効性「低」と判定する。
【0058】
ついで、ステップS104の処理に進み、CPU101aは、判定図を作成する処理を実行する。
判定図は、上記のアンスラサイクリン系抗がん剤治療の有効性判定方法において説明したような、第1CDK比活性と第2CDK比活性の二つのパラメータからなる二次元グラフであって、その分布領域が、アンスラサイクリン系抗がん剤治療の有効性の異なる領域毎に分割された二次元グラフである。この二次元グラフは、判定スコアSが所定の閾値となる点を結んで描かれるカットオフライン、アンスラサイクリン系抗がん剤治療の有効性が高い領域と、低い領域とに分割されている。この判定図には、アンスラサイクリン系抗がん剤治療の有効性の判定が行われた検体がプロットされて表示される。
【0059】
ついでステップS105の処理に進み、CPU101aは、ステップS103において得られた有効性の判定結果と、ステップS105において作成された判定図を、表示部105に表示させる処理を実行する。
【0060】
図8は、判定結果の表示画面の一例を示す図である。図に示すように、表示部105に表示される判定結果の表示画面105aには、判定が行われた検体の検体番号、有効性の判定結果、及び判定図105bが表示される。
判定図105bは、ステップS105において作成された二次元グラフであって、アンスラサイクリン系抗がん剤治療の有効性の判定が行われた検体のCDK1比活性及びCDK2比活性がプロットされて表示される(図中、★印で表示している)。このように、判定スコアSに基づく有効性の判定結果とともに判定図を表示することにより、被検癌患者の有効性の程度を視覚的に知ることができる。
【0061】
なお、表示画面には、有効性の判定が行われた検体のみをプロットした判定図105bを表示した例について説明したが、このような構成に限られず、例えば、アンスラサイクリン系の抗がん剤による治療が有効であった癌患者の検体と、アンスラサイクリン系の抗がん剤による治療が有効でなかった癌患者の検体とを含む複数の検体を同時にプロットした判定図を表示する構成であってもよい。このような構成とすることにより、アンスラサイクリン系抗がん剤治療の有効性に関する統計的な情報をも提供することができる。
【実施例】
【0062】
本実施形態による判定方法を用いて癌患者のアンスラサイクリン系抗がん剤治療の有効性を判定した。
悪性腫瘍摘出後にアンスラサイクリン系抗がん剤が投与された癌患者のアンスラサイクリン系抗がん剤の投与前に摘出された悪性腫瘍からCDK1、CDK2の発現量と活性値を測定した。
【0063】
得られたCDK1、CDK2の発現量及び活性値を用いて、下記式(10)乃至(12)に基づいて判定スコアSを算出した。
RS1;F(x)=0.18/(1+Exp(−(x−1.6)×7) ・・・(10)
RS2;G(y)=0.25/(1+Exp(−(y−1.0)×6) ・・・(11)
S=2500×F(x)×G(y) ・・・(12)
x=CDK1活性値/CDK1発現量
y=(CDK2活性値×CDK1発現量)/(CDK2発現量×CDK1活性値)
【0064】
次に、各症例から得られた判定スコアSを下記の条件と比較して、癌患者を、アンスラサイクリン系抗がん剤治療の有効性の高い群(Highグループ)、有効性の低い群(Lowグループ)に分類した。
Highグループ: S≧2.3
Lowグループ: S<2.3
【0065】
各患者群において、5年以内に再発した患者数と、各患者群における5年以内累積再発率を算出した。その結果を表1に示す。
【0066】
【表1】

【0067】
表1に示したように、本実施形態による判定方法によって癌患者を分類した結果、Highグループに該当した患者数は11人、Lowグループに該当した患者数は38人であり、各患者群において5年以内に再発した患者数はそれぞれ1人、15人であった。各患者群における5年以内の累積再発率は、Highグループが10.0%、Lowグループが40.3%であり、Highグループの患者群は、Lowグループの患者群に比べて5年間の無再発生存率が有意に高いことがわかる。さらに、母集団における5年以内累積再発率は33.6%であり、これと比較しても、Highグループの患者群の無再発生存率が高いことがわかる。
この結果から、本判定方法によってアンスラサイクリン系抗がん剤治療の有効性が高いと判定された癌患者は、アンスラサイクリン系抗がん剤の投与によって癌の再発が効果的に抑制されており、本実施形態による判定方法によって、癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を精度良く判定可能であることが実証された。
【0068】
この判定結果は、本実施形態による判定図を用いた判定方法によっても得ることができる。その判定方法は以下のとおりである。
【0069】
まず、本実施例における癌患者のCDK1及びCDK2の発現量と活性値とを用いて、下記式(14)及び(15)に基づいて、各癌患者のCDK1比活性及びCDK2比活性を算出した。
CDK1比活性=CDK1活性値/CDK1発現量 ・・・(13)
CDK2比活性=CDK2活性値/CDK2発現量 ・・・(14)
【0070】
次に、得られたCDK1比活性とCDK2比活性とに基づいて、癌患者を、図9に示すようなCDK1比活性及びCDK2比活性の二つのパラメータからなる二次元グラフにプロットした。
【0071】
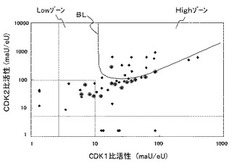
図9は、CDK1比活性(x軸)及びCDK2比活性(y軸)に基づいて本実施例における癌患者をプロットした二次元グラフであって、カットオフラインCLによって、癌患者を、アンスラサイクリン系抗がん剤治療の有効性の高い群(Highグループ)と、低い群(Lowグループ)とに分類したものである。
図9において、カットオフラインCLは、CDK1比活性とCDK2比活性とに基づいて求められる判定スコアSの値が2.3となる点を結んで描かれる曲線である。
同図において、悪性腫瘍摘出後5年以内に癌が再発した患者については、円で囲って表示してある。
【0072】
このような判定図を用いて癌患者を分類した結果、表2と全く同様の分類結果を得ることができ、本実施形態による再発リスク判定図を用いることによっても、癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を適切に判定可能であることが実証された。
したがって、本実施形態による判定図を表示することにより、信頼性の高いアンスラサイクリン系抗がん剤治療の有効性の診断支援情報を提供できることが示唆された。
【図面の簡単な説明】
【0073】
【図1】図1(a)は、複数の被検癌患者から得られたCDK1比活性と癌の再発率との関係を示したヒストグラムであり、図1(b)は、複数の被検癌患者から得られたCDK1とCDK2の比活性比と癌の再発率との関係を示したヒストグラムである。
【図2】判定スコアSを模式的に説明するための図であり、図2(a)は、CDK1比活性の対数(x軸)、CDK2比活性の対数(y軸)、及び判定スコアS(z軸)をパラメータとする三次元グラフであり、図2(b)は、図2(a)の判定スコアS(z軸)を二次元平面に投影したグラフである。
【図3】本実施形態による支援方法に使用される再発リスク判定図の一例を示した図である。
【図4】本実施形態による支援方法に使用される再発リスク判定図の他の例を示した図である。
【図5】本実施形態による支援方法に使用される再発リスク判定図の他の例を示した図である。
【図6】本実施形態の判定装置の概略構成を示すブロック図である。
【図7】本実施形態の判定装置によるアンスラサイクリン系抗がん剤治療の有効性の判定処理を示すフローチャートである。
【図8】本実施形態の判定装置における判定結果の表示画面の一例を示す図である。
【図9】CDK1比活性(x軸)及びCDK2比活性(y軸)に基づいて本実施例における癌患者をプロットした二次元グラフであって、カットオフラインCLによって、癌患者をアンスラサイクリン系抗がん剤治療の有効性の高い群(Highグループ)と、低い群(Lowグループ)とに分類したものである。
【符号の説明】
【0074】
1 判定装置
10 制御装置
20 測定装置
101 制御部
101a CPU
101b ROM
101c RAM
101d ハードディスク
101e 入出力インターフェース
101f 通信インターフェース
101g 画像出力インターフェース
101h バス
101i アプリケーションプログラム
103 キーボード
105 表示部
105a 表示画面
105b 判定図
【技術分野】
【0001】
本発明は、サイクリン依存性キナーゼの発現量と活性値とに基づいて、アンスラサイクリン系抗がん剤治療の有効性を判定する、アンスラサイクリン系抗がん剤治療の有効性判定方法に関する。また、本発明は、サイクリン依存性キナーゼの発現量と活性値とに基づいて、アンスラサイクリン系抗がん剤治療の有効性の診断支援情報を提供する、アンスラサイクリン系抗がん剤治療の有効性の診断支援方法に関する。
【背景技術】
【0002】
従来、サイクリン依存性キナーゼ(以下、単に「CDK」とも称する)を利用した抗がん剤治療の有効性を予測する方法が提案されている。
【0003】
例えば、特許文献1には、患者から採取した腫瘍細胞のサイクリン依存性キナーゼの活性値、発現量、及び活性値と発現量の比からなる群より選択される少なくとも1つのパラメータと、選択されたパラメータに対応する閾値とを比較し、その結果に基づいて患者の抗がん剤治療の有効性を予測する方法が記載されている。この方法によれば、抗がん剤に対する感受性を高率に予測判定することができる。
【0004】
【特許文献1】特開2007−6882号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
本発明は、より高精度に抗がん剤治療の有効性を判定しうる、新規なアンスラサイクリン系抗がん剤治療の有効性判定方法を提供することを目的とするものである。また、本発明は、より高精度に抗がん剤治療の有効性診断を支援しうる、新規な抗がん剤治療の有効性の診断支援方法を提供することを目的とするものである。
【課題を解決するための手段】
【0006】
上記の課題を解決するため、本発明の第1の観点によるアンスラサイクリン系抗がん剤治療の有効性判定方法は、被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、下記式(1)に基づいて判定スコアを求め、得られた判定スコアに基づいてアンスラサイクリン系抗がん剤治療の有効性を判定することを特徴とする。
判定スコア=F(x)×G(y) ・・・(1)
(式中、xは第1CDK比活性を表し、この第1CDK比活性は、第1CDK活性値/第1CDK発現量で示される:
式中、yは比活性比を表し、この比活性比は、第2CDK比活性/第1CDK比活性で示され、第2CDK比活性は、第2CDK活性値/第2CDK発現量で示される)
【0007】
本発明において算出される判定スコアとは、後述するように、その癌患者における癌の再発リスクを反映するパラメータである。癌の再発リスクは細胞の増殖能に関係しており、異常な増殖能を有する細胞は癌化する可能性が高いと考えられている。抗がん剤は通常、癌患者に投与されることで細胞の増殖能を低減し、癌の増殖を防ぐものであるため、抗がん剤治療の有効性は細胞の増殖能と密接に関係している。
そこで、癌の再発リスクを反映する判定スコアと、抗がん剤、特にアンスラサイクリン系抗がん剤治療の有効性(抗がん剤治療の結果)との関係について研究を行った結果、本発明者らは、癌の判定スコアと抗がん剤治療の有効性とに相関があることを見出した。
ゆえに、癌の再発リスクを反映する判定スコアを指標としてアンスラサイクリン系抗がん剤治療の有効性を判定することにより、高精度に抗がん剤治療の有効性を判定することができる。
【0008】
また、本発明の別の観点によるアンスラサイクリン系抗がん剤治療の有効性の診断支援方法は、被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、第1CDKの比活性と、第2CDKの比活性の二つのパラメータからなり、下記式(2)に基づいて算出される判定スコアの異なる領域毎に分割された判定図に、得られた第1CDK比活性及び第2CDK比活性をプロットして表示することを特徴とする。
判定スコア=F(x)×G(y) ・・・(2)
(式中、xは第1CDK比活性を表し、この第1CDK比活性は、第1CDK活性値/第1CDK発現量で示される:
式中、yは比活性比を表し、この比活性比は、第2CDK比活性/第1CDK比活性で示され、第2CDK比活性は、第2CDK活性値/第2CDK発現量で示される)
【発明の効果】
【0009】
本発明によれば、高精度にアンスラサイクリン系抗がん剤治療の有効性を判定しうる、アンスラサイクリン系抗がん剤治療の有効性判定方法を提供することができる。また、本発明によれば、高精度にアンスラサイクリン系抗がん剤治療の有効性の診断支援方法を提供することができる。
【発明を実施するための最良の形態】
【0010】
[1]アンスラサイクリン系抗がん剤治療の有効性判定方法
本発明の第1の観点による判定方法は、被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、得られた第1CDK及び第2CDKの発現量と活性値とに基づいて判定スコアを求め、得られた判定スコアに基づいてアンスラサイクリン系抗がん剤治療の有効性を判定することを特徴とする。
【0011】
ここで、本明細書における「がん」は、上皮細胞がん、造血器由来のがん、肉腫などを含む。がんの種類としては、例えば、乳がん、胃がん、大腸がん、食道がん、前立腺がん、白血病、骨肉腫等が挙げられる。
【0012】
また、本明細書における「抗がん剤」とは、上述のがんに対して抗腫瘍効果のある化学物質のことをいうものとする。
【0013】
また、本明細書におけるアンスラサイクリン系抗がん剤とは、アグリコンであるアンスラサイクリノンに1〜3種のアミノ酸または中性糖が結合した一群の抗生物質である。アンスラサイクリン系抗がん剤としては、例えばダウノルビシン、ドキソルビシン、アクラルビシン、エピルビシン、ブレオマイシンなどが挙げられる。
【0014】
また、本明細書における「再発」とは、悪性腫瘍を摘出するために臓器を部分切除した後、残存臓器に同じ悪性腫瘍が再現する場合、及び原発巣から腫瘍細胞が分離して遠隔組織(遠隔臓器)へ運ばれ、そこで自立的に増殖する場合(転移再発)をいうものとする。
【0015】
また、本明細書における「再発リスク」とは、悪性腫瘍が摘出された癌患者の身体に癌が再発する危険、または癌が再発することによって癌患者が死亡する危険を意味する。本明細書中で特に断らない限り、「再発リスク」はそのいずれも含むものとする。
【0016】
(1)被検癌患者から採取した悪性腫瘍から、第1のCDK及び第2のCDKの発現量と活性値を取得する工程
被検癌患者から採取される悪性腫瘍は、例えば被検癌患者の生体組織のうち、繊維性結合組織、軟骨組織、骨組織、血液、リンパ等の支持組織、上皮組織、筋組織、神経組織を構成する細胞であればよい。特に、本実施形態による判定方法に用いられる細胞としては、個体としての調和を破り、増殖の制御機構に異常を来たしている組織の腫瘍細胞のように、病理的情報を得たい細胞が好適である。例えば、乳、肺、肝臓、胃、大腸、膵臓、皮膚、子宮、精巣、卵巣、甲状腺、副甲状腺、リンパ系統、骨髄などの位置にできる腫瘍の細胞が好適な対象となる。
【0017】
サイクリン依存性キナーゼ(CDK)とは、サイクリンと結合して活性化される酵素群の総称で、単独では活性をもたないが、サイクリンと結合して活性型となる。CDKは、その種類に応じて、細胞周期の特定時期で機能している。CDKとしては、CDK1、CDK2、CDK4、CDK6、サイクリンA依存性キナーゼ、サイクリンB依存性キナーゼ、及びサイクリンD依存性キナーゼなどが挙げられる。
ここに挙げた複数種のCDKから第1のCDKと第2のCDKとを決定し、被検癌患者から採取された悪性腫瘍の第1のCDKと、第2のCDKの発現量及び活性値を測定する。
【0018】
CDK活性値とは、特定のサイクリンと結合して、そのサイクリンをリン酸化する基質の量から算出されるキナーゼ活性のレベル(単位をU(ユニット)で表す)をいう。なお、前記CDKがリン酸化する基質としては、例えば、活性型CDK1及び活性型CDK2については、ヒストンH1が挙げられ、活性型CDK4及び活性型CDK6については、Rb(網膜芽細胞腫タンパク質)が挙げられる。CDK活性値は、慣用のCDK活性測定方法によって測定することができる。具体的には、測定試料の細胞溶解液から活性型CDKを含む試料を調製し、試料と、32P標識したATP(γ−〔32P〕−ATP)とを用いて、基質タンパク質に32Pを取り込ませ、32P標識されたリン酸化基質の標識量を測定し、標準品で作成された検量線をもとに定量する方法がある。また放射性物質の標識を用いない方法としては、特開2002−335997号に開示の方法が挙げられる。この方法は、検体の細胞可溶化液から、目的の活性型CDKを含む試料を調製し、アデノシン5'−O−(3−チオトリホスフェート)(ATP−γS)と基質を反応させて、該基質タンパク質のセリン又はスレオニン残基にモノチオリン酸基を導入し、導入されたモノチオリン酸基の硫黄原子に標識蛍光物質又は標識酵素を結合させることによって基質タンパク質を標識し、標識されたチオリン酸基質の標識量(標識蛍光物質を用いた場合には蛍光量)を測定し、標準品で作成された検量線に基づいて定量する方法である。
【0019】
活性測定に供する試料は、測定対象となる悪性腫瘍を含む組織の可溶化液から目的のCDKを特異的に採集することにより調製する。この場合、試料は目的のCDKに特異的な抗CDK抗体を用いて調製してもよいし、特定のサイクリン依存性キナーゼ(例えばサイクリンA依存性キナーゼ、サイクリンB依存性キナーゼ、サイクリンE依存性キナーゼ)活性測定の場合には、抗サイクリン抗体を用いて調製する。いずれの場合も活性型CDK以外のCDKが試料に含まれることになる。例えばサイクリン・CDK複合体にCDKインヒビターが結合した複合体も含まれる。また、抗CDK抗体を用いた場合には、CDK単体、CDKとサイクリン及び/又はCDKインヒビターの複合体、CDKとその他の化合物との複合体などが含まれる。従って、活性値は、活性型、不活性型、各種競合反応が混在する状態下で、リン酸化された基質の単位(U)として測定される。
【0020】
CDK発現量とは、測定対象となる悪性腫瘍を含む組織の細胞可溶化液に含まれる目的のCDK量(分子個数に対応する単位)であって、タンパク質混合物から目的のタンパク質量を測定する従来公知の方法で測定できる。例えば、ELISA法、ウェスタンブロット法などを使用してもよいし、特開2003−130871号に開示の方法で測定することもできる。目的のタンパク質(CDK)は、特異的抗体を用いて捕捉すればよい。例えば、抗CDK1抗体を用いることにより、細胞内に存在するCDK1のすべて(CDK単体、CDKとサイクリン及び/又はCDKインヒビターの複合体、CDKとその他の化合物との複合体を含む)を捕捉できる。
【0021】
(2)判定スコアを算出する工程
上記の工程によって得られた2種類のCDKの発現量と活性値に基づいて判定スコアSを求める。判定スコアSは、下記式(3)乃至(5)によって求められる。
S=F(x)×G(y) ・・・(3)
F(x)=a/(1+Exp(−(x−b)×c)) ・・・(4)
G(y)=d/(1+Exp(−(y−e)×f)) ・・・(5)
(式中、a〜fは定数)
上記式において、xは第1のCDKの比活性を表し、yは比活性比を表す。ここで、CDK比活性は、CDK活性値/CDK発現量で示され、比活性比は、第2CDK比活性/第1CDK比活性で示される。上記式(3)乃至(5)、比活性及び比活性比については、後に詳しく説明する。
【0022】
(3)判定スコアに基づいて抗がん剤治療の有効性を判定する工程
上記において得られた判定スコアSと、予め設定された閾値とを比較して、アンスラサイクリン系抗がん剤治療の有効性を判定する。例えば、被検癌患者の判定スコアSと閾値とを比較し、被検癌患者の判定スコアSが閾値より高い場合には、被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性が高く、被検癌患者の判定スコアSが閾値より低い場合には、被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性が低いというようにして、アンスラサイクリン系抗がん剤治療の有効性を判定することができる。
【0023】
閾値は、抗がん剤の種類、癌の種類により適宜設定される値である。具体的には、所定の癌患者に対してアンスラサイクリン系抗がん剤を投与した治療結果と判定スコアSとの関係を、多くの抗がん剤治療結果について調べ、アンスラサイクリン系抗がん剤による治療が有効であった症例と、有効でなかった症例とに区別しうるような判定スコアSを閾値とすることができる。
このように、実際の臨床治療結果に基づいて閾値を設定することにより、信頼性の高い抗がん剤治療の有効性の予測が可能となる。
【0024】
ここで、上記式(3)乃至(5)について説明する。
【0025】
まず、CDK比活性と、比活性比の意義について説明する。
CDK比活性は、CDK活性値/CDK発現量によって示されることからも明らかなように、CDKの発現量に対する活性値の比である。CDK比活性は、試料に含まれる単位CDKタンパク質量あたりのCDK酵素活性を反映するパラメータであって、細胞に存在しているCDKのうちの活性を示すCDKの割合に相当し、判定対象である悪性腫瘍細胞の増殖状態に基づくCDK活性レベルを示す。
【0026】
また、比活性比は、第2CDK比活性/第1CDK比活性によって示されることからも明らかなように、第1CDKの比活性に対する第2CDKの比活性の比である。CDK比活性比は、特定の細胞周期において活性を示す二種類のCDKの活性レベルの比であり、癌患者の細胞においていずれのCDK活性が優位であるか(細胞周期のいずれの時期にある細胞割合がどの程度であるか)を反映するパラメータである。
一般に、癌細胞は正常な増殖制御を逸脱して増殖が活発に行われていることから、DNAの複製期であるS期と、DNA合成の終了から有糸分裂の開始の間であるG2期にある細胞の割合が多い場合に、その細胞が癌化しているものと考えることができる。また、癌細胞に見られる異数倍体性は、細胞分裂期であるM期を異常な状態で経過した場合や、又はM期を経ずにG1期に進み、そのままS期に移行したときに発生するものと考えられるため、M期に存在する細胞割合が少ない場合にも、その細胞が癌化していると考えることができる。
そこで、例えば、第1のCDKとして細胞周期のG2期からM期に移行する際に活性を示すCDK1を、第2のCDKとして細胞周期のG1期からS期に移行する際に活性を示すCDK2を使用し、これらに基づいてCDK比活性比を求めた場合には、得られるCDK比活性比は、S期またはG2期にある細胞が、M期にある細胞に比べてどれだけ多く存在するかを反映する数値であり、細胞の増殖能を正確に反映するパラメータとして用いることができる。
【0027】
次に、判定スコアSを算出するための式(3)乃至(5)について説明する。
上記において説明したように、第1CDK比活性と、第2CDK比活性とに基づくCDK比活性比を得ることにより、細胞の増殖能(癌の再発リスク)に相関するパラメータを得ることができる。
しかしながら、CDK比活性比が細胞の増殖能(癌の再発リスク)に相関しない場合がありうる。例えば、上記において例示したように、第1のCDKとしてCDK1を、第2のCDKとしてCDK2を用いてCDK比活性比を求めたとき、CDK1比活性が異常に大きい場合には、CDK比活性比の値は小さくなるが、これは別の観点からみれば、CDK1と複合体を形成するサイクリンが高発現し、CDK1が異常に活性化されていることともいえる。
細胞は、ある細胞周期に活性化するCDKが少なくても、他の特定のCDKが代償的に働くことによって増殖することが可能であるとも考えられており、特定のCDKが異常に活性化されている場合にも、細胞動態に異常を来たしていると考えることができる。
【0028】
そこで、癌の再発リスクが、(1)第1CDKの比活性、(2)第1CDKと第2CDKの比活性比、の二つのリスク要素によって規定されるものと考え、これらのリスク要素に基づいて癌の再発リスクを評価することとした。上記(1)、(2)の各リスク要素に基づいて癌が再発する確率を、数値的に評価する尺度を用いて、それぞれリスクスコアRS(1)、リスクスコアRS(2)とする。さらに、上記(1)、(2)のリスク要素によって結果的に癌が再発する確率を、数値的に評価する尺度を用いて、再発リスクスコアRRSとする。結果的に癌が再発する確率(再発リスク)は、上記(1)、(2)の二つのリスク要素によって癌が再発する確率の積によって与えられるので、再発リスクスコアRRSは、リスクスコアRS(1)とリスクスコアRS(2)の積に比例する値で与えられる。したがって、
RRS=RS(1)×RS(2) ・・・(6)
が成り立つ。
【0029】
リスクスコアRS(1)及びリスクスコアRS(2)は、以下のようにして求められる。
図1(a)は、複数の被検癌患者から得られたCDK1比活性と癌の再発率との関係を示したヒストグラムであり、図1(b)は、複数の被検癌患者から得られたCDK1とCDK2の比活性比と癌の再発率との関係を示したヒストグラムである。同図においては、複数の被検癌患者を、当該被検癌患者から得られたCDK1比活性、又はCDK1とCDK2の比活性比に基づいて階級分けし、各階級に含まれる症例の総数を白抜きの棒グラフで、各階級に含まれる再発症例を網掛けの棒グラフで示した。さらに、各階級における癌の再発確率(再発症例数/症例総数)を求め、折れ線で示した。
【0030】
同図からも明らかなように、癌の再発確率は、CDK1比活性、又はCDK1とCDK2の比活性比に伴って単調に増加することがわかる。したがって、各階級ごとの癌の再発確率を近似することにより、CDK1比活性をリスク要素とするリスクスコアRS(1)、及びCDK1とCDK2の比活性比をリスク要素とするリスクスコアRS(2)を得ることができる。そこで、CDK1比活性の値をx、CDK1とCDK2の比活性比をyとして、各階級ごとの癌の再発確率をロジスティック関数によって近似することにより、リスクスコアRS(1)及びリスクスコアRS(2)を得ることができる。すなわち、リスクスコアRS(1)及びリスクスコアRS(2)はそれぞれ、
RS(1);F(x)=a/(1+Exp(−(x−b)×c)) ・・・(7)
RS(2);G(y)=d/(1+Exp(−(y−e)×f)) ・・・(8)
(式中、a〜fは定数)
によって表される。
【0031】
上記式(6)によって求められる再発リスクスコアRRSは、第1CDKと第2CDKの発現量と活性値とに基づく被検癌患者の癌の再発リスクを数値化したものである。この再発リスクスコアRRSと、被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性との関係について調べた結果、両者の間に密接な相関関係が認められた。よって、上記式(6)によって算出される再発リスクスコアRRSを、アンスラサイクリン系抗がん剤治療の有効性を判定するための指標(判定スコアS)として用いることにより、高精度にアンスラサイクリン系抗がん剤治療の有効性を判定することが可能となる。
したがって、アンスラサイクリン系抗がん剤治療の有効性を判定するための判定スコアSは、
S=F(x)×G(y) ・・・(9)
として求められる。
【0032】
上記実施形態においては、判定スコアSを算出して、これを閾値と比較することによりアンスラサイクリン系抗がん剤治療の有効性を判定する方法について説明したが、これに限らず、他の判定基準とともにアンスラサイクリン系抗がん剤治療の有効性を判定するようにしてもよい。
【0033】
例えば、被検癌患者の悪性腫瘍から、判定スコアSとは別に、第1のCDKの比活性を算出して、判定スコアSを第1の判定基準とし、第1CDK比活性を第2の判定基準として、二つの判定基準に基づいてアンスラサイクリン系抗がん剤治療の有効性を判定するように構成することができる。
【0034】
具体的には、まず、上記において説明したように、被検癌患者から第1のCDK及び第2のCDKの発現量と活性値を取得し、判定スコアSと、第1CDK比活性を算出する。
次に、得られた判定スコアSと第1CDK比活性を、それぞれに対する閾値とを比較してアンスラサイクリン系抗がん剤治療の有効性を判定する。
より具体的には、判定スコアSに対する閾値として第1の閾値を、第1CDK比活性に対する閾値として第2の閾値を設定し、被検癌患者から得られる判定スコアS及び第1CDK比活性のいずれか一方が閾値以上である場合にはアンスラサイクリン系抗がん剤治療の有効性が高いと判定し、判定スコアS及び第1CDK比活性のいずれもが閾値未満である場合にはアンスラサイクリン系抗がん剤治療の有効性が低いと判定する。
【0035】
第1の閾値と第2の閾値は、それぞれ2つ以上の閾値を含んでもよい。例えば、第1の閾値として第1閾値aと第1閾値bを設定し、第2の閾値として第2閾値aと、第2閾値bを予め設定しておく。そして、判定スコアSが第1閾値a以上であるか、または、第1CDK比活性が第2閾値a以上であるとき、アンスラサイクリン系抗がん剤治療の有効性が高いと判定し、判定スコアSが第1閾値b未満であり、かつ、第1CDK比活性が第2閾値b未満であるとき、アンスラサイクリン系抗がん剤治療の有効性が低いと判定し、判定スコアSが第1閾値a未満、第1閾値b以上であり、かつ、第1CDK比活性が第2閾値a未満、第2閾値b以上であるとき、アンスラサイクリン系抗がん剤治療の有効性が中程度であると判定する。
このように、判定スコアSと、他の判定基準とによってアンスラサイクリン系抗がん剤治療の有効性を判定することにより、より精度の高い判定を行うことが可能となる。
【0036】
また本実施形態においては、アンスラサイクリン系抗がん剤治療の有効性を判定するための判定図を表示することにより、アンスラサイクリン系抗がん剤治療の有効性診断を支援する方法を提供する。
図2は、上記において説明した判定スコアSを模式的に説明するための図である。図2(a)は、CDK1比活性の対数(x軸)、CDK2比活性の対数(y軸)、及び判定スコアS(z軸)をパラメータとする三次元グラフであり、図2(b)は、図2(a)の判定スコアS(z軸)を二次元平面に投影したグラフである。
【0037】
図2(b)に示したように、判定スコアSを二次元グラフに投影すると、判定スコアSが等しくなる点を結んだ、複数の等高線状の曲線が描かれる。
例えば、曲線CL1上の点はすべて、等しい判定スコアSとなるCDK1比活性及びCDK2比活性の点であり、曲線CL2上の点はすべて、等しい判定スコアSとなるCDK1比活性及びCDK2比活性の点である。そして、曲線によって囲まれた領域は常に曲線上の点より判定スコアSが高くなる領域であるから(図2(a)参照)、例えば、曲線CL1が判定スコアS=Mとなる点を結んで描かれたものである場合、この曲線CL1によって囲まれた領域はすべて、判定スコアS≧Mとなる領域である。また、曲線CL1が判定スコアSが所定値Mとなる点を、曲線CL2が判定スコアSが所定値Nとなる点を結んで描かれたものである場合、曲線CL1と曲線CL2とによって囲まれた領域Sは、M≦判定スコアS<Nとなる領域である。
【0038】
このように、第1CDK比活性(x軸)及び第2CDK比活性(y軸)からなる二次元グラフは、等しい判定スコアSとなる点を結んだ曲線(カットオフライン)によって、判定スコアSの異なる領域毎に分割することができる。
【0039】
アンスラサイクリン系抗がん剤治療の有効性を判定するための判定図は、次のようにして作成することができる。
まず、判定スコアSに対する閾値を設定する。判定スコアSに対する閾値は、アンスラサイクリン系抗がん剤治療の有効性の判定に有効な値であればよく、例えば、その閾値を超えるか否かによってアンスラサイクリン系抗がん剤治療の有効性が高い癌患者とアンスラサイクリン系抗がん剤治療の有効性が低い癌患者とに分類しうるような閾値が用いられる。
次に、第1CDK比活性と第2CDK比活性の二つのパラメータからなる二次元グラフ上に、判定スコアSが閾値となる点を結んでカットオフラインを作成し、二次元グラフを判定スコアSが閾値以上となる領域と、閾値以下となる領域とに分割する。このカットオフラインは、アンスラサイクリン系抗がん剤治療の有効性判定の基準となる値に基づいて作成されているから、二次元グラフは、アンスラサイクリン系抗がん剤治療の有効性が高い領域と低い領域とに分割される。このようにして、アンスラサイクリン系抗がん剤治療の有効性を判定するための判定図が作成される。
【0040】
このような判定図に、被検癌患者の悪性腫瘍から得られた第1CDK及び第2CDKの発現量と活性値とに基づいて算出された第1CDK比活性及び第2CDK比活性をプロットする。判定図は、閾値となるカットオフラインによってアンスラサイクリン系抗がん剤治療の有効性の高い領域と低い領域とに分割されているから、被検癌患者の第1CDK比活性及び第2CDK比活性が判定図にプロットされることにより、その患者におけるアンスラサイクリン系抗がん剤治療の有効性が高いか低いかを一目で理解することができる。このような判定図を表示すれば、医師は判定図を見るだけで癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を判断することができ、患者の診断に役立つ情報を提供することができる。
【0041】
図3は、本実施形態によるアンスラサイクリン系抗がん剤治療の有効性の診断支援方法に使用される判定図の一例を示した図である。この判定図は、x座標に第1CDK比活性、y座標に第2CDK比活性をとり、その分布領域を、カットオフラインBL1によって、アンスラサイクリン系抗がん剤治療の有効性の高い領域(Highゾーン)と、アンスラサイクリン系抗がん剤治療の有効性の低い領域(Lowゾーン)とに分割したものである。
【0042】
いま、ある癌患者Aから得られた第1CDK比活性と第2CDK比活性とに基づいて、判定図上に点Aがプロットされたとする。図3に示したように、点Aは、Highゾーンに属していることから、この癌患者Aは、アンスラサイクリン系抗がん剤治療の有効性が高いと判定することができる。
同様に、ある癌患者Bから得られた第1CDK比活性と第2CDK比活性とに基づいて、判定図上に点Bがプロットされたとする。図3に示したように、点Bは、Lowゾーンに属していることから、この癌患者Bは、アンスラサイクリン系抗がん剤治療の有効性が低いと判定することができる。
【0043】
アンスラサイクリン系抗がん剤治療の有効性を判定するための判定図は、その用途に応じて異なる形態の判定図を用いることができる。
図4は、本実施形態によるアンスラサイクリン系抗がん剤治療の有効性の診断支援方法に使用される判定図の他の例を示した図である。この判定図は、x座標に第1CDK比活性、y座標に第2CDK比活性をとり、その分布領域を、カットオフラインBL2及びカットオフラインBL3とによって、アンスラサイクリン系抗がん剤治療の有効性の高い領域(Highゾーン)、アンスラサイクリン系抗がん剤治療の有効性の低い領域(Lowゾーン)、中間領域(Int.ゾーン)の3つの領域に分割したものである。
このように3つ以上の領域に分割された判定図を用いることにより、被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を段階的に判定することができる。
【0044】
図5は、本実施形態によるアンスラサイクリン系抗がん剤治療の有効性の診断支援方法に使用される判定図の他の例を示した図である。この判定図は、判定スコアSが閾値となる点を結んで描かれる曲線と、第1CDK比活性の閾値を示す直線とを結合して作成されるカットオフラインBL4とカットオフラインBL5とによって、その分布領域を、アンスラサイクリン系抗がん剤治療の有効性の高い領域(Highゾーン)、アンスラサイクリン系抗がん剤治療の有効性の低い領域(Lowゾーン)、中間領域(Int.ゾーン)の3つの領域に分割したものである。
このように、判定スコアSと第1CDK比活性とに基づいて分割された判定図を用いることにより、被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性をより高精度に判定することができる。
【0045】
[2]判定装置
次に、本実施形態のアンスラサイクリン系抗がん剤治療の有効性判定装置について説明する。
【0046】
図6は、本実施形態における判定装置の概略構成を示すブロック図である。本実施形態における判定装置1は、被検癌患者から得られたデータに基づいてその癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を判定する装置であって、図6に示すように、制御装置10と、測定装置20とを備えて構成されている。制御装置10は、測定装置20から出力された測定データを解析して癌の再発リスクを判定し、判定結果を出力するための装置であり、測定装置20は、被検癌患者から採取された悪性腫瘍を測定して測定データを制御装置10へ出力するための装置である。
【0047】
制御装置10は、パーソナルコンピュータ(PC)からなり、制御部101と、キーボード103と、表示部105とを備えている。制御部101は、CPU101aと、ROM101bと、RAM101cと、ハードディスク101dと、画像出力インターフェース101eと、通信インターフェース101fと、画像出力インターフェース101gと、バス101hとを備え、各部はバス101hを介して接続されており、相互にデータの送受信が可能である。
【0048】
CPU101aは、ROM101bに記憶されているコンピュータプログラムおよびRAM101cにロードされたコンピュータプログラムを実行することが可能である。ROM101bには、CPU101aによって実行されるコンピュータプログラムおよびCPU101aがコンピュータプログラムを実行するためのデータなどが記録されている。RAM101cは、ROM101bおよびハードディスク101dに記録されているコンピュータプログラムの読み出しに用いられる。また、これらのコンピュータプログラムを実行するときに、CPU101aの作業領域として利用される。
【0049】
ハードディスク101dには、オペレーティングシステム(OS)やアプリケーションプログラムなど、CPU101aに実行させるための種々のコンピュータプログラムおよびそのコンピュータプログラムの実行に用いるデータがインストールされている。
ハードディスク101dにインストールされているアプリケーションプログラム101iには、本発明によるアンスラサイクリン系抗がん剤治療の有効性の判定方法を実現するためのアプリケーションプログラムが含まれている。
【0050】
入出力インタフェース101eには、キーボード103やマウス(図示せず)が接続されている。通信インタフェース101fには測定装置20が接続されており、制御部101は、通信インタフェース101fを介して測定装置2とデータの送受信が可能である。
【0051】
画像出力インタフェース101gは、表示部105に接続されており、CPU101aから与えられた画像データに応じた映像信号を表示部105に出力する。表示部105は、入力された映像信号にしたがって、画像(画面)を表示する。
【0052】
判定装置10と通信インタフェース101fを介して接続される測定装置20は、生体組織からCDKの発現量と活性値を測定するための装置である。このような、生体組織からCDK発現量及びCDK活性値を測定するための測定装置として、特開2007−74975号公報に記載されているような装置を用いることができる。
【0053】
なお、本実施形態において、判定装置1は、測定装置20によって得られた測定データを受け付け、測定データに基づいて被検癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を判定するように構成されているが、このような構成に限られず、例えば、予めCDK発現量及びCDK活性値を測定しておき、キーボード103から測定データを入力する構成であってもよい。
【0054】
図7は、本実施形態に係る判定装置1によるアンスラサイクリン系抗がん剤治療の有効性判定処理を示すフローチャートである。
このフローチャートによる処理は、ハードディスク101dにインストールされたアプリケーションプログラム101iがRAM101cに読み出され、CPU101aがRAM101cに読み出されたアプリケーションプログラム101iを実行することによって実現される。
【0055】
まず、ステップS101において、CPU101aは、測定装置20から測定データを受信したか否かを判定する処理を実行する。CPU101aが、測定装置20から測定データを受信していないと判定した場合(ステップS101においてNO)には、処理がリターンされる。
なお、ここでいう測定データとは、測定装置20が生体組織を測定することによって得られた少なくとも2種類のCDKの発現量と活性値である。
【0056】
CPU101aが測定装置20から測定データを受信したと判定した場合(ステップS101においてYES)には、ステップS102の処理に進み、CPU101aは、判定スコアSを算出する処理を実行する。
アプリケーションプログラム101iには、アンスラサイクリン系抗がん剤治療の有効性判定方法において記載したような、第1CDK及び第2CDKの発現量及び活性値に基づいて判定スコアSを算出するための式が組み込まれており、CPU101aがアプリケーションプログラム101iを実行することによって判定スコアSが算出される。
【0057】
ついでステップS103の処理に進み、CPU101aは、アンスラサイクリン系抗がん剤治療の有効性を判定する処理を実行する。この処理は、ステップS102において算出された判定スコアSを、アプリケーションプログラム101i内に設定された所定の閾値と比較することにより行われる。
CPU101aは、判定スコアSが所定の閾値以上であるとき、アンスラサイクリン系抗がん剤治療の有効性「高」と判定し、判定スコアSが所定の閾値未満であるとき、アンスラサイクリン系抗がん剤治療の有効性「低」と判定する。
【0058】
ついで、ステップS104の処理に進み、CPU101aは、判定図を作成する処理を実行する。
判定図は、上記のアンスラサイクリン系抗がん剤治療の有効性判定方法において説明したような、第1CDK比活性と第2CDK比活性の二つのパラメータからなる二次元グラフであって、その分布領域が、アンスラサイクリン系抗がん剤治療の有効性の異なる領域毎に分割された二次元グラフである。この二次元グラフは、判定スコアSが所定の閾値となる点を結んで描かれるカットオフライン、アンスラサイクリン系抗がん剤治療の有効性が高い領域と、低い領域とに分割されている。この判定図には、アンスラサイクリン系抗がん剤治療の有効性の判定が行われた検体がプロットされて表示される。
【0059】
ついでステップS105の処理に進み、CPU101aは、ステップS103において得られた有効性の判定結果と、ステップS105において作成された判定図を、表示部105に表示させる処理を実行する。
【0060】
図8は、判定結果の表示画面の一例を示す図である。図に示すように、表示部105に表示される判定結果の表示画面105aには、判定が行われた検体の検体番号、有効性の判定結果、及び判定図105bが表示される。
判定図105bは、ステップS105において作成された二次元グラフであって、アンスラサイクリン系抗がん剤治療の有効性の判定が行われた検体のCDK1比活性及びCDK2比活性がプロットされて表示される(図中、★印で表示している)。このように、判定スコアSに基づく有効性の判定結果とともに判定図を表示することにより、被検癌患者の有効性の程度を視覚的に知ることができる。
【0061】
なお、表示画面には、有効性の判定が行われた検体のみをプロットした判定図105bを表示した例について説明したが、このような構成に限られず、例えば、アンスラサイクリン系の抗がん剤による治療が有効であった癌患者の検体と、アンスラサイクリン系の抗がん剤による治療が有効でなかった癌患者の検体とを含む複数の検体を同時にプロットした判定図を表示する構成であってもよい。このような構成とすることにより、アンスラサイクリン系抗がん剤治療の有効性に関する統計的な情報をも提供することができる。
【実施例】
【0062】
本実施形態による判定方法を用いて癌患者のアンスラサイクリン系抗がん剤治療の有効性を判定した。
悪性腫瘍摘出後にアンスラサイクリン系抗がん剤が投与された癌患者のアンスラサイクリン系抗がん剤の投与前に摘出された悪性腫瘍からCDK1、CDK2の発現量と活性値を測定した。
【0063】
得られたCDK1、CDK2の発現量及び活性値を用いて、下記式(10)乃至(12)に基づいて判定スコアSを算出した。
RS1;F(x)=0.18/(1+Exp(−(x−1.6)×7) ・・・(10)
RS2;G(y)=0.25/(1+Exp(−(y−1.0)×6) ・・・(11)
S=2500×F(x)×G(y) ・・・(12)
x=CDK1活性値/CDK1発現量
y=(CDK2活性値×CDK1発現量)/(CDK2発現量×CDK1活性値)
【0064】
次に、各症例から得られた判定スコアSを下記の条件と比較して、癌患者を、アンスラサイクリン系抗がん剤治療の有効性の高い群(Highグループ)、有効性の低い群(Lowグループ)に分類した。
Highグループ: S≧2.3
Lowグループ: S<2.3
【0065】
各患者群において、5年以内に再発した患者数と、各患者群における5年以内累積再発率を算出した。その結果を表1に示す。
【0066】
【表1】

【0067】
表1に示したように、本実施形態による判定方法によって癌患者を分類した結果、Highグループに該当した患者数は11人、Lowグループに該当した患者数は38人であり、各患者群において5年以内に再発した患者数はそれぞれ1人、15人であった。各患者群における5年以内の累積再発率は、Highグループが10.0%、Lowグループが40.3%であり、Highグループの患者群は、Lowグループの患者群に比べて5年間の無再発生存率が有意に高いことがわかる。さらに、母集団における5年以内累積再発率は33.6%であり、これと比較しても、Highグループの患者群の無再発生存率が高いことがわかる。
この結果から、本判定方法によってアンスラサイクリン系抗がん剤治療の有効性が高いと判定された癌患者は、アンスラサイクリン系抗がん剤の投与によって癌の再発が効果的に抑制されており、本実施形態による判定方法によって、癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を精度良く判定可能であることが実証された。
【0068】
この判定結果は、本実施形態による判定図を用いた判定方法によっても得ることができる。その判定方法は以下のとおりである。
【0069】
まず、本実施例における癌患者のCDK1及びCDK2の発現量と活性値とを用いて、下記式(14)及び(15)に基づいて、各癌患者のCDK1比活性及びCDK2比活性を算出した。
CDK1比活性=CDK1活性値/CDK1発現量 ・・・(13)
CDK2比活性=CDK2活性値/CDK2発現量 ・・・(14)
【0070】
次に、得られたCDK1比活性とCDK2比活性とに基づいて、癌患者を、図9に示すようなCDK1比活性及びCDK2比活性の二つのパラメータからなる二次元グラフにプロットした。
【0071】
図9は、CDK1比活性(x軸)及びCDK2比活性(y軸)に基づいて本実施例における癌患者をプロットした二次元グラフであって、カットオフラインCLによって、癌患者を、アンスラサイクリン系抗がん剤治療の有効性の高い群(Highグループ)と、低い群(Lowグループ)とに分類したものである。
図9において、カットオフラインCLは、CDK1比活性とCDK2比活性とに基づいて求められる判定スコアSの値が2.3となる点を結んで描かれる曲線である。
同図において、悪性腫瘍摘出後5年以内に癌が再発した患者については、円で囲って表示してある。
【0072】
このような判定図を用いて癌患者を分類した結果、表2と全く同様の分類結果を得ることができ、本実施形態による再発リスク判定図を用いることによっても、癌患者におけるアンスラサイクリン系抗がん剤治療の有効性を適切に判定可能であることが実証された。
したがって、本実施形態による判定図を表示することにより、信頼性の高いアンスラサイクリン系抗がん剤治療の有効性の診断支援情報を提供できることが示唆された。
【図面の簡単な説明】
【0073】
【図1】図1(a)は、複数の被検癌患者から得られたCDK1比活性と癌の再発率との関係を示したヒストグラムであり、図1(b)は、複数の被検癌患者から得られたCDK1とCDK2の比活性比と癌の再発率との関係を示したヒストグラムである。
【図2】判定スコアSを模式的に説明するための図であり、図2(a)は、CDK1比活性の対数(x軸)、CDK2比活性の対数(y軸)、及び判定スコアS(z軸)をパラメータとする三次元グラフであり、図2(b)は、図2(a)の判定スコアS(z軸)を二次元平面に投影したグラフである。
【図3】本実施形態による支援方法に使用される再発リスク判定図の一例を示した図である。
【図4】本実施形態による支援方法に使用される再発リスク判定図の他の例を示した図である。
【図5】本実施形態による支援方法に使用される再発リスク判定図の他の例を示した図である。
【図6】本実施形態の判定装置の概略構成を示すブロック図である。
【図7】本実施形態の判定装置によるアンスラサイクリン系抗がん剤治療の有効性の判定処理を示すフローチャートである。
【図8】本実施形態の判定装置における判定結果の表示画面の一例を示す図である。
【図9】CDK1比活性(x軸)及びCDK2比活性(y軸)に基づいて本実施例における癌患者をプロットした二次元グラフであって、カットオフラインCLによって、癌患者をアンスラサイクリン系抗がん剤治療の有効性の高い群(Highグループ)と、低い群(Lowグループ)とに分類したものである。
【符号の説明】
【0074】
1 判定装置
10 制御装置
20 測定装置
101 制御部
101a CPU
101b ROM
101c RAM
101d ハードディスク
101e 入出力インターフェース
101f 通信インターフェース
101g 画像出力インターフェース
101h バス
101i アプリケーションプログラム
103 キーボード
105 表示部
105a 表示画面
105b 判定図
【特許請求の範囲】
【請求項1】
被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、
下記式(1)に基づいて判定スコアを求め、
得られた判定スコアに基づいてアンスラサイクリン系抗がん剤治療の有効性を判定する、アンスラサイクリン系抗がん剤治療の有効性判定方法。
判定スコア=F(x)×G(y) ・・・(1)
(式中、xは第1CDK比活性を表し、この第1CDK比活性は、第1CDK活性値/第1CDK発現量で示される:
式中、yは比活性比を表し、この比活性比は、第2CDK比活性/第1CDK比活性で示され、第2CDK比活性は、第2CDK活性値/第2CDK発現量で示される)
【請求項2】
判定スコアを、所定の閾値と比較することによりアンスラサイクリン系抗がん剤治療の有効性を判定する請求項1に記載の判定方法。
【請求項3】
前記F(x)は、xと癌の再発率との相関関係に基づく関数であり、
前記G(y)は、yと癌の再発率との相関関係に基づく関数である請求項1又は2に記載の判定方法。
【請求項4】
被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、
第1CDKの比活性と、第2CDKの比活性の二つのパラメータからなり、下記式(2)に基づいて算出される判定スコアの異なる領域毎に分割された判定図に、得られた第1CDK比活性及び第2CDK比活性をプロットして表示するアンスラサイクリン系抗がん剤治療の有効性の診断支援方法。
判定スコア=F(x)×G(y) ・・・(2)
(式中、xは第1CDK比活性を表し、この第1CDK比活性は、第1CDK活性値/第1CDK発現量で示される:
式中、yは比活性比を表し、この比活性比は、第2CDK比活性/第1CDK比活性で示され、第2CDK比活性は、第2CDK活性値/第2CDK発現量で示される)
【請求項5】
さらに、判定図に基づくアンスラサイクリン系抗がん剤治療の有効性の判定結果を表示する請求項4に記載のアンスラサイクリン系抗がん剤治療の有効性の診断支援方法。
【請求項1】
被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、
下記式(1)に基づいて判定スコアを求め、
得られた判定スコアに基づいてアンスラサイクリン系抗がん剤治療の有効性を判定する、アンスラサイクリン系抗がん剤治療の有効性判定方法。
判定スコア=F(x)×G(y) ・・・(1)
(式中、xは第1CDK比活性を表し、この第1CDK比活性は、第1CDK活性値/第1CDK発現量で示される:
式中、yは比活性比を表し、この比活性比は、第2CDK比活性/第1CDK比活性で示され、第2CDK比活性は、第2CDK活性値/第2CDK発現量で示される)
【請求項2】
判定スコアを、所定の閾値と比較することによりアンスラサイクリン系抗がん剤治療の有効性を判定する請求項1に記載の判定方法。
【請求項3】
前記F(x)は、xと癌の再発率との相関関係に基づく関数であり、
前記G(y)は、yと癌の再発率との相関関係に基づく関数である請求項1又は2に記載の判定方法。
【請求項4】
被検癌患者から採取した悪性腫瘍から、第1のサイクリン依存性キナーゼ(CDK)及び第2のCDKの発現量と活性値を取得し、
第1CDKの比活性と、第2CDKの比活性の二つのパラメータからなり、下記式(2)に基づいて算出される判定スコアの異なる領域毎に分割された判定図に、得られた第1CDK比活性及び第2CDK比活性をプロットして表示するアンスラサイクリン系抗がん剤治療の有効性の診断支援方法。
判定スコア=F(x)×G(y) ・・・(2)
(式中、xは第1CDK比活性を表し、この第1CDK比活性は、第1CDK活性値/第1CDK発現量で示される:
式中、yは比活性比を表し、この比活性比は、第2CDK比活性/第1CDK比活性で示され、第2CDK比活性は、第2CDK活性値/第2CDK発現量で示される)
【請求項5】
さらに、判定図に基づくアンスラサイクリン系抗がん剤治療の有効性の判定結果を表示する請求項4に記載のアンスラサイクリン系抗がん剤治療の有効性の診断支援方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2009−232816(P2009−232816A)
【公開日】平成21年10月15日(2009.10.15)
【国際特許分類】
【出願番号】特願2008−86213(P2008−86213)
【出願日】平成20年3月28日(2008.3.28)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 研究集会名 第66回 日本癌学会学術総会 主催者名 日本癌学会会長 鶴尾 隆 開催日 平成19年10月5日
【出願人】(390014960)シスメックス株式会社 (810)
【Fターム(参考)】
【公開日】平成21年10月15日(2009.10.15)
【国際特許分類】
【出願日】平成20年3月28日(2008.3.28)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 研究集会名 第66回 日本癌学会学術総会 主催者名 日本癌学会会長 鶴尾 隆 開催日 平成19年10月5日
【出願人】(390014960)シスメックス株式会社 (810)
【Fターム(参考)】
[ Back to top ]

