イオン定量分析方法およびフッ素イオン定量分析方法
【課題】PEFCの生成水である排出水中の高分子電解質膜材料由来の成分を見出すと共に、簡便にフッ素イオン濃度とフッ素イオン排出量を算出することができるPEFCのフッ素イオン定量方法を提供する。
【解決手段】PEFC運転時に発生する反応水である排出水は、PEFCアノード21側の排出水ドレンタンク22とPEFCカソード13側の排出水ドレンタンク14とに回収される。排出水中のイオン成分分析は計測器1(15)のイオンクロマトグラフで行ない、主に高分子電解質膜の分解成分と電池内構成部材由来の成分とを検出する。排出水は電気伝導率の計測に用いられる計測器2(16)の電気伝導率計と、pHの測定に用いられる計測器3(17)の水素イオン濃度計(pHメーター)とにより計測され、電導率とフッ素イオン濃度およびフッ素イオン排出量との関係を求める。
【解決手段】PEFC運転時に発生する反応水である排出水は、PEFCアノード21側の排出水ドレンタンク22とPEFCカソード13側の排出水ドレンタンク14とに回収される。排出水中のイオン成分分析は計測器1(15)のイオンクロマトグラフで行ない、主に高分子電解質膜の分解成分と電池内構成部材由来の成分とを検出する。排出水は電気伝導率の計測に用いられる計測器2(16)の電気伝導率計と、pHの測定に用いられる計測器3(17)の水素イオン濃度計(pHメーター)とにより計測され、電導率とフッ素イオン濃度およびフッ素イオン排出量との関係を求める。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のイオン成分を分析するイオン定量分析方法等に関する。
【背景技術】
【0002】
固体高分子電解質膜型燃料電池(Polymer Electrolyte Fuel Cell : PEFC)には、陽イオン(カチオン:cation)交換膜からなる電解質膜が用いられている。PEFCの単セルは、上記電解質膜の両側にカーボンを主体とする基材に貴金属系の触媒電極層を接合した負極(アノード)側電極および正極(カソード)側電極を接合した電極と上記電解質膜との接合体をセパレーターで挟むことにより構成される。通常は、この単セルを所定数だけ積層して所望の電圧を得ることができるような電池が構成される。
【0003】
高分子電解質膜には、フッ素系のカチオン交換膜、特にパーフルオロスルホン酸ポリマー(Perfluorocarbon Sulphonic Acid Polymer : PFS。構成元素:C、F、O、S、H)が用いられている。パーフルオロスルホン酸ポリマーは、フッ素樹脂の主鎖が集まった撥水性(疎水性)の骨格領域(テフロン(登録商標)骨格)に、スルホン酸基(-SO3H)を末端につけた側鎖が付いてクラスター領域を構成する構造を有している。現在、高分子電解質膜については高含水率を保つための運転条件のコントロールおよび膜質の改良等の研究開発が盛んに行なわれている。上記セパレーターの役目は、各電極への反応ガスの供給、隣り合う単セル間の反応ガスの隔離、および電極からの集電である。アノード側電極には主に水素を含有する燃料ガスが供給されており、触媒電極上で当該水素がイオン化され電解質を介してカソード側電極へと移動する。その間に生じた電子が外部回路に取り出されて直流の電気エネルギーとして利用される。カソード側電極には主に酸素を含有するガスあるいは空気が供給されているために、このカソード側電極では水素イオンと電子および酸素が反応して水が生成される。
【0004】
上述のパーフルオロスルホン酸ポリマーを用いたPEFCでは、運転条件等によりパーフルオロスルホン酸ポリマーの電解質膜が分解劣化し、燃料電池の性能が低下してくることがある。特許文献1には、アノード側電極の反応界面付近の高分子電解質膜を十分に湿潤させることにより、カソード側電極からアノード側電極への水の逆拡散を抑制してカソード側電極の反応界面付近に豊富に水を存在させ、カソード側電極の触媒層中に滞留した過酸化水素水等を速やかに燃料電池の外部へ排出させて、燃料電池の耐久性を向上させる技術が記載されている。
【0005】
特許文献2には、高分子電解質の分解を抑制するために、負荷が停止してから所定の時間が経過するまで、カソード側電極に対して酸化剤ガスの供給を行い、アノード側電極に対して燃料ガスの供給を行なって、所定のタイミングで酸化剤ガスおよび燃料ガスの供給を停止する技術が記載されている。これにより、高分子電解質膜を透過した水素イオンによってカソード側電極の電位を低下させることができるため、カソード側電極において触媒層の触媒活性が回復する。上記所定の時間を短くすることにより、高分子電解質膜の分解を抑制することができると記載されている。
【0006】
一方、PEFCの運転において、長時間連続試験後に高分子電解質膜の薄膜化が観察されており、薄膜化の主要因として電解質膜を構成するポリマーの化学的分解による消失が推定されている。この消失により、高分子電解質膜の材質に由来するフッ素イオンおよび硫酸イオンが分解成分として燃料電池から排出水中に溶出する問題がある。これらの成分の溶出量が多く且つ持続的な溶出であると、高分子電解質膜が部分的に消失して当該膜に孔が開く結果、発電ができなくなると言われている。このため、上記成分の溶出を防ぐことが重要であり、最適な燃料電池の運転条件の決定にも関連する。
【0007】
ここで、PEFCの運転試験条件について簡単に説明する。PEFCの運転試験条件には、例えば燃料電池(単セル)の大きさの違い、電極触媒、燃料ガスと空気流量、ガス差圧、アノード側電極およびカソード側電極の加湿露点、セル温度等、種々のパラメータがあり、これらのパラメータを用いて出力試験等が行なわれている。燃料電池の運転によって生成された水の排出水の回収は、排出水総量(リットルL)、採取時間(h)、試験用電池電極面積(cm2)等の違いを明らかにして行い、排出水中のフッ素イオン濃度(mg/L)を求めて電池特性と運転条件の検討が行なわれる。
【0008】
特許文献3には、PEFCの運転方法を、生成水等における不純物イオンの溶出の程度を測定する不純物イオン測定ステップと、不純物イオン測定ステップで測定された測定値に基づきPEFCが所定の電池性能低下領域にあるかどうかを判断する判断ステップと、所定の電池性能低下領域にあると判断された場合に、PEFCを当該領域から回避させる回避ステップとを含むように構成する技術が記載されている。溶出の程度が測定される不純物イオンは、電池性能を低下させる原因となるイオンであれば特に種類が限定されるものではないと記載されている。
【0009】
特許文献4には、燃料電池システムを通過する流体(改質ガス)のパラメータ(改質ガス中の水分量)を、PEFC内の生成水の影響を考慮して制御する技術が開示されている。すなわち、燃料電池制御の応答遅れに対して燃料電池内の生成水の影響を考慮する点が記載されている。
【0010】
【特許文献1】特開2003−178780号公報
【特許文献2】特開2004−172106号公報
【特許文献3】特開2004−127548号公報
【特許文献4】特開2000−40519号公報
【発明の開示】
【発明が解決しようとする課題】
【0011】
上述の特許文献1には、アノード側電極の反応界面付近の高分子電解質膜を十分に湿潤させることにより、結果的にカソード側電極の触媒層中に滞留した過酸化水素水等を速やかに燃料電池の外部へ排出させる点が記載されている。しかし、燃料電池の生成水である排出水中の電解質膜材料由来の成分を見出すという観点に関してはまったく開示されていない。
【0012】
上述の特許文献2には、高分子電解質の分解を抑制するために、所定のタイミングで酸化剤ガスおよび燃料ガスの供給を停止することにより、高分子電解質膜の分解を抑制する点について記載されている。しかし、特許文献1と同様に、燃料電池の生成水である排出水中の電解質膜材料由来の成分を見出すという観点に関してはまったく開示されていない。
【0013】
上述の特許文献3には、PEFCの運転方法を構成する際に、生成水等における不純物イオンの溶出の程度を測定する不純物イオン測定ステップを含ませる点について記載されている。しかし、特許文献3では、溶出の程度が測定される不純物イオンは電池性能を低下させる原因となるイオンであれば特に種類が限定されるものではないとされている。このため、不純物イオンとしてフッ化物イオンについて記載されているものの、燃料電池の生成水である排出水中の電解質膜材料由来の成分を見出すという観点は開示されてはいない。
【0014】
上述の特許文献4には、燃料電池制御の応答遅れに対して燃料電池内の生成水の影響を考慮する点について記載されている。しかし、排出水の成分を評価するものではない。特許文献4には燃料電池に供給される酸素の圧力を制御すること等が記載されており、電解質膜の分解の観点では言及していないため、燃料電池の良好な運転を期待できるものではない。すなわち、特許文献4に記載されている燃料電池システムの運転方法は、電池運転制御の応答遅れに対する燃料電池内の生成水の影響対策であり、燃料ガス中の水蒸気量等を制御することなどが示されているものであって、排出水の成分の評価とは異なっている。
【0015】
上述のように、従来技術には、燃料電池の生成水である排出水中の電解質膜材料由来の成分を見出すと共に、当該成分の濃度および量を算出する方法が示されていないという問題があった。しかし、主に高分子電解質膜の分解の観点から言えば、フッ素イオン濃度を迅速に且つ微量定量分析ができる方法(フッ素イオン濃度の算出方法)と、フッ素イオン濃度(mg/L)測定後に運転方法に反映できる指標値を求める方法(フッ素イオン量の算出方法)とが重要である。
【0016】
そこで、本発明の目的は、上記問題を解決するためになされたものであり、PEFCの生成水である排出水中の高分子電解質膜材料由来の成分を見出すと共に、簡便にフッ素イオン濃度とフッ素イオン排出量を算出することができるPEFCのフッ素イオン定量方法を提供することにある。
【課題を解決するための手段】
【0017】
この発明のイオン定量分析方法は、フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のイオン成分を分析するイオン定量分析方法であって、前記高分子電解質膜型燃料電池のアノード側及びカソード側排出水中からイオンクロマトグラフ法により検出されたフッ素イオン濃度を高分子電解質膜の分解成分の指標とすることを特徴とする。
【0018】
この発明のフッ素イオン定量分析方法は、フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のフッ素イオン成分を分析するフッ素イオン定量分析方法であって、前記高分子電解質膜型燃料電池のアノード側の排出水中から測定された電導率とカソード側の排出水中から測定された電導率とに基づき、高分子電解質膜から分解したフッ素イオン濃度を定量分析することを特徴とする。
【0019】
この発明のフッ素イオン定量分析方法は、フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のフッ素イオン成分を分析するフッ素イオン定量分析方法であって、前記高分子電解質膜型燃料電池のアノード側及びカソード側の全排出水中から測定された電導率と、アノード側の排出水中から測定された電導率と、カソード側の排出水中から測定された電導率とに基づき、高分子電解質膜から分解したフッ素イオン排出量を定量分析することを特徴とする。
【0020】
ここで、この発明のフッ素イオン定量分析方法において、前記フッ素イオン排出量は、排出水総量、排出水中のフッ素イオン濃度、所定の採取時間及び前記高分子電解質膜型燃料電池の電極面積に基づいて求めることができる。
【発明の効果】
【0021】
本発明のフッ素イオン定量方法によれば、フッ素系の陽イオン交換膜を高分子電解質に用いるPEFCにおいて、反応生成水の排出水をイオンクロマトグラフ法で分析した結果、排出水の電導率とフッ素イオン濃度との相関係数は0.98以上であり、相関性が良好であることが分かった。このため、排出水中では微量レベルであるが、イオン成分はフッ素イオンが支配的であることが示された。さらに、簡便な計測器を用いて排出水の電気伝導率を測定することにより、簡便にフッ素イオン濃度およびフッ素イオン排出量を算出することができるPEFCのフッ素イオン定量方法を提供することができるという効果がある。
【発明を実施するための最良の形態】
【0022】
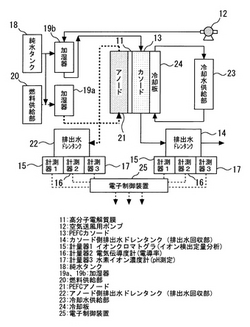
以下、まず本発明のPEFCのフッ素イオン定量方法に用いられるPEFCシステムの構成について説明し、次に各実施例について図面を参照して詳細に説明する。図1は、本発明のPEFCのフッ素イオン定量方法に用いられるPEFCシステムの構成図である。図1では省略しているが、本PEFCシステムも通常の燃料電池システムと同様に、改質系機器、電池スタック、熱交換器、回転機等の補機類から構成される。図1に示されるように、高分子電解質膜11にはフッ素系の陽イオン交換膜が用いられ、PEFCアノード21とPEFCカソード13との接合体をセパレーター(不図示)により挟んで単セルが構成される。本明細書に示される実験では、実験目的によって電池電極面積が50〜6000cm2と異なり、例えば単セルからセルを積層したスタックを用いている。この燃料電池では、燃料供給部20から供給される主に水素を含有するガスが純水タンク18から供給される水と共に加湿器19aに送られ、湿度が調整された後にPEFCアノード21に供給される。空気送風用ポンプ12からの空気も同様に加湿器19bを介して湿度が調整された後、PEFCカソード13に供給される。PEFCアノード21では水素がイオン化され、高分子電解質膜11を介してPEFCカソード13側へと移動する。PEFCカソード13側では主に上記水素イオンと電子および酸素とが反応して発電され、同時に水が生成される。燃料電池の運転時には、電池スタック(不図示)の冷却板24で冷却され循環する冷却水供給部23から供給される冷却水により熱交換される。上述のように生成された生成水は、各々PEFCアノード21側の排出水ドレンタンク(排出水回収部)22とPEFCカソード13側の排出水ドレンタンク(排出水回収部)14とに回収される。このようにして、PEFCの運転時に発生する反応水である排出水は、各々ドレンタンク22および14に回収される。
【0023】
排出水中のイオン成分分析は、排出水を分取してイオン種の分離機能を有し、イオン検出定量分析に用いられる計測器1(15)のイオンクロマトグラフで行なわれ、主に高分子電解質膜の分解成分と電池内構成部材由来の成分とを検出することができる。排出水中のイオン成分は、高分子電解質膜の分解成分であるフッ素イオン(F−)および硫酸イオン(SO42−)、または燃料電池内有機材料由来の酢酸イオン(CH3COO−)であり、さらに燃料電池への供給ガス等に由来した塩化物イオン(Cl−)である。これらのイオン成分が排出水分析評価の指標となるが、いずれも微量である。これらのイオン成分の中でも特にイオン成分量を求める高分子電解質膜の分解成分の指標とする主たる成分は、フッ素イオンである。
【0024】
排出水は上記計測器1(15)と同様に設置し、電気伝導率(電導率または電気伝導度とも言う。)の計測に用いられる計測器2(16)の電気伝導率計と、pHの測定に用いられる計測器3(17)の水素イオン濃度計(pHメーター)とにより計測される。その後は後述する指標値により、電子制御装置(電子制御部)25から燃料電池の運転制御(点線で示す。)を行なうことができる。
【0025】
本明細書における実験では、PEFCアノード21側およびPEFCカソード13側の排出水のイオン分析を行ない、高分子電解質膜の分解成分を把握した。以下では、実施例1において、排出水のイオン成分(特にフッ素イオン濃度)の分析方法、電気伝導率測定方法および水素イオン濃度(pH)測定方法について述べた後、排出水の電導率とフッ素イオン濃度との関係について述べる。次いで実施例2において、PEFCアノード21側およびPEFCカソード13側の排出水の電導率とフッ素イオン排出量との関係について述べる。
【実施例1】
【0026】
(排出水のイオン成分の分析方法、電気伝導率測定方法および水素イオン濃度(pH)測定方法)
【0027】
1.排出水のイオン成分の分析法
図2は、イオン成分の分析方法の一例として陰イオンの分析を行なうイオンクロマトグラフ分析装置(測定装置)32の構成略図を示す。このイオンクロマトグラフ分析装置32は排出試料液中のイオン成分の分離定量分析を行う装置の一例である。図2に示されるように、イオンクロマトグラフ分析装置32は試料導入バルブ37、ガードカラム38、分離カラム39、除去システム40および検出セル41から構成されている。イオンクロマトグラフィーは、強電解質の溶離液35と共に排出水試料31を試料導入バルブ37から注入し、イオン交換樹脂製の分離カラム39を通す。ガードカラム38は分離カラム39を保護するために設けられている。分離カラム39内では水和半径の大小、Van der Waals力の相互作用によってイオン種の相互分離を行なう。この後、除去システム(サプレッサー)40を通すことによりバックグラウンドの伝導度を下げ、目的とするイオン種を高感度でクロマトグラムとして得るものである。溶離液35は電解質溶液調整部34で調整された陰イオンクロマトグラフ溶離液(KOH:水酸化カリウム)であり、脱気装置(デガッサー)36により溶離液35中に溶存する気体が除去されている。排出水試料31は、イオン成分を含む液であり、懸濁物質は孔径0.2μmのフィルタにより濾過済みである。
【0028】
イオンクロマトグラフ法は、数mLの試料液を用いて、1回の測定で数種の陰イオン成分を同時に測定することができ、分別定量分析を行なうことができる方法である。検出器(検出セル)41にはフローセル型の電導度検出器を用いており、データ処理装置33において、各イオン成分の電導度に基づくイオンクロマトグラムのピーク面積および高さから、目的とする分析試料溶液中のイオン成分濃度が求められる。分析試料溶液中のイオン濃度を求めることにより、イオン成分量(単位:ppm、mg/Lあるいはμg)として算出することができる。陽イオンを分析する際は、分離カラム39と溶離液35とを陽イオン分析用に別途組み替えることによって行なうことができる。
【0029】
次に検量線の検討を行ない、定量分析ができるようにした。イオンクロマトグラフ法によるイオン成分分離分析条件を次に示す。
【0030】
(イオン成分測定条件)
イオンクロマトグラフ分析装置32(分離カラム39を含む。)、溶離液35はすべてDIONEX社製の物を用いた。
【0031】
(1)方法:イオンクロマトグラフ法
(2)分離カラム39:陰イオン用 IonPac AS17/IonPac AG17、 陽イオン用 IonPac CS14/IonPac CG14
(3)溶離液35:陰イオン用 EGC-KOH(水酸化カリウム 10Mmスタート・ステップグラジェント)、
陽イオン用IonPac EGC-MSA(メタルスルホン酸、ステップグラジェント)
(4)除去システム40:オートサプレッサー(ASRS)、(CSRS)
(5)試料液量:25μLループ法
(6)定量法:イオンクロマトグラムピーク面積とイオン成分濃度の検量線法
【0032】
図3は、他の陰イオンから分離定量分析する際のフッ素イオン(F−)、硫酸イオン(SO42−)、酢酸イオン(CH3COO−)、塩化物イオン(Cl−)等の存在を示す陰イオン標準液のクロマトグラムの例を示す。図3において横軸は溶離時間(min)、縦軸は面積である。図4は、フッ素イオンのピーク面積(縦軸)とフッ素イオン濃度(ppb)との関係からなる検量線の例を示す。実施例1に係る試料液中フッ素イオン濃度の実験式1を次に示す。式1中のXは面積である(以下の式においても同様)。
【0033】
フッ素イオン(F− ppb) = 2500X 相関係数 1 (1)
【0034】
図4に示されるように、フッ素イオン濃度とピーク面積との相関係数は0.9999以上であり良好であった。イオンクロマトグラフ法による排出水中のイオン分析は、測定により得られたイオンのピーク面積からフッ素イオンの液中濃度を算出することにより、定量分析することができる。
【0035】
2.電導率測定方法
水溶液の電気抵抗は、溶存イオン量が増大すると低下する。電導率(σ)は抵抗(ρ)の逆数であるから(σ=1/ρ)、抵抗の減少は電導率の増大を意味する。水中の溶存物質が比較的少量の場合には、電導率はその量にほぼ比例して変化すると考えられるので、電導率を測定すれば全溶解物質のおおよその値を短時間で推定できる。
【0036】
電導率の測定には同一形状の2個の平板白金電極を備えたセルを用い、これに試料水を満たして電気抵抗が測定され、比電導率(ohm-1・cm-1)が求められる。流路に適用できるフロー型セルを用いてもよい。さらに現在では電導率の単位は25℃における、ミリジーメンス毎メートルと呼称され、(mS/m)で表されるのが一般的になっている。排出水の電導率の測定はイオン成分の存在に関係するので、水質評価項目として有効である。
【0037】
3.水素イオン濃度測定方法
水溶液中の水素イオン濃度[H+]の逆数の対数をその溶液のpHという(pH=−log10[H+])。現在ではガラス電極pHメータによる測定が行なわれている。排出水のpHの測定はイオン成分の存在と水素イオン濃度に関係するので、水質評価項目として計測する。
【0038】
4.排出水の電導率、pHとフッ素イオン濃度との関係
次に、上記の測定条件で実試料である排出水のフッ素イオンの分析と排出水の電導率、pHの分析測定を行なった。実試料はPEFCの運転時の排出水である。PEFCの運転試験条件には、例えば電池(単セル)の大きさの違い、電極触媒、燃料ガスと空気流量、ガス差圧、PEFCアノード21およびPEFCカソード13の加湿露点、セル温度等、種々のパラメータがあり、出力試験等が行なわれている。上述のように、本明細書に示す実験では実験目的によって電池電極面積が50〜6000cm2と異なる単セルからセルを積層したスタックを用いている。さらにPEFCアノード21加湿露点を54〜80(℃)、PEFCカソード13加湿露点を63〜85(℃)と変えて実験を行ない、排出水採水のための燃料電池運転時間を1〜373時間とした。
【0039】
図5は、排出水の電導率(mS/m。縦軸)とフッ素イオン濃度(mg/L。横軸)との関係を示す線図である。図5に示されるように、電導率とフッ素イオン濃度との相関係数が0.98以上であり、相関性が良好であることが分かる。これは、排出水中では微量レベルであるが、イオン成分はフッ素イオンが支配的であることを示している。試料液中フッ素イオン濃度F−
(mg/L)の実験式2を次に示す。
【0040】
F− (mg/L)=0.6744X−0.1707 (2)
【0041】
以上より、本発明の実施例1によれば、フッ素系の陽イオン交換膜を高分子電解質に用いるPEFCにおいて、反応生成水の排出水をイオンクロマトグラフ法で分析した。PEFC運転時に発生する反応水である排出水は、PEFCアノード21側の排出水ドレンタンク22とPEFCカソード13側の排出水ドレンタンク14とに回収される。排出水中のイオン成分分析は計測器1(15)のイオンクロマトグラフで行なわれ、主に高分子電解質膜の分解成分と電池内構成部材由来の成分とを検出することができる。排出水は上記計測器1(15)と同様に設置し、電気伝導率の計測に用いられる計測器2(16)の電気伝導率計と、pHの測定に用いられる計測器3(17)の水素イオン濃度計(pHメーター)とにより計測される。計測の結果、排出水の電導率とフッ素イオン濃度との相関係数は0.98以上であって相関性が良好であることが分かり、排出水中では微量レベルであるが、イオン成分はフッ素イオンが支配的であることが示された。さらに、簡便な計測器2(16)を用いて排出水の電気伝導率を測定することにより、簡便にフッ素イオン濃度を算出することができるPEFCのフッ素イオン定量方法を提供することができた。
【実施例2】
【0042】
実施例1では、高分子電解質膜の分解調査の観点から、排出水中のフッ素イオン濃度(mg/L) と電導率に相関性があることを見出し、フッ素イオン濃度を迅速にかつ微量定量分析ができる方法を見出した。実施例2では、PEFCの高分子電解質膜の分解成分は排出液中のフッ素イオン量とし、排出水総量(リットル)、排出水中のフッ素イオン濃度(mg/L)、24時間当りの採取時間(日。所定の採取時間)、電池電極面積(cm2)の関係から排出量(フッ素イオンμg/day/cm2)をPEFCアノード21からの排出水およびPEFCカソード13からの排出水から求めた値とその合計量の値を求めた。つまり、排出水中のフッ素イオン濃度は予めイオンクロマトグラフ法で求めた値と排出水の電気伝導度との関係からフッ素イオン量が求められる検量線を得る。次いで、排出量(フッ素イオンμg/day/cm2)は排出水の電気伝導度から得られるようにした。
【0043】
図6は、PEFCアノード21側とPEFCカソード13側の全排出水試料液の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。図6に示されるように、全排出水試料液の電導率とフッ素イオン排出量との相関係数は0.95以上であり、相関性が良好であることが分かる。試料液中フッ素イオン排出量F− (μg/day/cm2)の実験式3を次に示す。
【0044】
F− (μg/day/cm2)=1.191X−0.1022 (3)
【0045】
図7は、PEFCアノード21側の排出水試料液の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。PEFCアノード21側の排出水試料液の電導率とフッ素イオン排出量との相関係数は0.96以上であり、相関性が良好であることが分かる。試料液中フッ素イオン排出量F− (μg/day/cm2)の実験式4を次に示す。
【0046】
F− (μg/day/cm2)=0.8095X−0.1063 (4)
【0047】
図8は、PEFCカソード13側の排出水試料液の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。PEFCカソード13側の排出水試料液の電導率とフッ素イオン排出量との相関係数は0.97以上であり、相関性が良好であることが分かる。試料液中フッ素イオン排出量F− (μg/day/cm2)の実験式5を次に示す。
【0048】
F− (μg/day/cm2)=1.186X+0.112 (5)
【0049】
以上のことから、排出量(フッ素イオンμg/day/cm2)は、排出水の電気伝導度を直接計測することによっても得られることが分かった。つまり、高分子電解質膜の分解成分である排出水のイオンは主にフッ素イオンであり、電導率に関係していることを見出した。排出水中の硫酸イオン等の他のイオンとの関係は極めて小さいことを示唆している。
【0050】
以上より、本発明の実施例2によれば、PEFCの高分子電解質膜の分解成分は排出液中のフッ素イオン量とし、排出水総量(リットル)、排出水中のフッ素イオン濃度(mg/L)、24時間当りの採取時間(日)、電池電極面積(cm2)の関係から排出量(フッ素イオンμg/day/cm2)をPEFCアノード21からの排出水およびPEFCカソード13からの排出水から求めた値とその合計量の値を求めた。全排出水試料液の電導率とフッ素イオン排出量との相関係数は0.95以上であり、相関性が良好であることが分かった。PEFCアノード21側の排出水試料液の電導率とフッ素イオン排出量との相関係数は0.96以上であり、相関性が良好であることが分かった。PEFCカソード13側の排出水試料液の電導率とフッ素イオン排出量との相関係数は0.97以上であり、相関性が良好であることが分かった。この結果、排出水中のイオン成分はフッ素イオンが支配的であることが示された。さらに、簡便な計測器2(16)を用いて排出水の電気伝導率を測定することにより、簡便にフッ素イオン排出量を算出することができるPEFCのフッ素イオン定量方法を提供することができた。
【産業上の利用可能性】
【0051】
本発明の活用例として、PEFCの運転条件に反映することが挙げられる。すなわち、PEFC運転時間の経過毎に、反応水である排出水のフッ素イオン排出量の変動を把握できる。排出水の電導率測定値とフッ素イオン排出量との関係は図6、図7、図8で確認しているので、PEFCの運転条件に反映させてフッ素イオン排出量を制御できる。この結果、簡便で安定した燃料電池の運転ができるようになり、排出水の電導率測定値とフッ素イオン排出量とを運転の指標として利用することができる。
【図面の簡単な説明】
【0052】
【図1】本発明のPEFCのフッ素イオン定量方法に用いられるPEFCシステムの構成図である。
【図2】イオン成分の分析方法の一例としてイオンクロマトグラフ分析装置(測定装置)32の構成を示す略図である。
【図3】他の陰イオンから分離定量分析する際のフッ素イオン(F−)、硫酸イオン(SO42−)、酢酸イオン(CH3COO−)、塩化物イオン(Cl−)等の存在を示す陰イオン標準液のクロマトグラムの例を示す図である。
【図4】フッ素イオンのピーク面積(縦軸)とフッ素イオン濃度(ppb)との関係からなる検量線の例を示す図である。
【図5】排出水の電導率(mS/m。縦軸)とフッ素イオン濃度(mg/L。横軸)との関係を示す線図である。
【図6】PEFCアノード21側とPEFCカソード13側の排出水の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。
【図7】PEFCアノード21側の排出水試料液の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。
【図8】EFCカソード13側の排出水試料液の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。
【符号の説明】
【0053】
11 高分子電解質膜、 12 空気送風用ポンプ、 13 PEFCカソード、 14 PEFCカソード13側の排出水ドレンタンク(排出水回収部)、15 計測器1(イオンクロマトグラフ)、 16 計測器2(電気伝導率計)、 17 計測器2(水素イオン濃度計)、 18 純水タンク、 19a、19b 加湿器、 20 燃料供給部、 21 PEFCアノード、 22 PEFCアノード21側の排出水ドレンタンク(排出水回収部)、 23 冷却水供給部、 24 冷却板、 25 電子制御装置、 31 排出水試料、 32 イオンクロマトグラフ測定装置、 33 データ処理装置、 34 電解質溶液調整部、 35 陰イオンクロマトグラフ溶離液、 36 脱気装置(デガッサー)、 37 試料導入バルブ、 38 ガードカラム、 39 分離カラム、 40 除去システム(サプレッサー)、 41 検出セル。
【技術分野】
【0001】
本発明は、フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のイオン成分を分析するイオン定量分析方法等に関する。
【背景技術】
【0002】
固体高分子電解質膜型燃料電池(Polymer Electrolyte Fuel Cell : PEFC)には、陽イオン(カチオン:cation)交換膜からなる電解質膜が用いられている。PEFCの単セルは、上記電解質膜の両側にカーボンを主体とする基材に貴金属系の触媒電極層を接合した負極(アノード)側電極および正極(カソード)側電極を接合した電極と上記電解質膜との接合体をセパレーターで挟むことにより構成される。通常は、この単セルを所定数だけ積層して所望の電圧を得ることができるような電池が構成される。
【0003】
高分子電解質膜には、フッ素系のカチオン交換膜、特にパーフルオロスルホン酸ポリマー(Perfluorocarbon Sulphonic Acid Polymer : PFS。構成元素:C、F、O、S、H)が用いられている。パーフルオロスルホン酸ポリマーは、フッ素樹脂の主鎖が集まった撥水性(疎水性)の骨格領域(テフロン(登録商標)骨格)に、スルホン酸基(-SO3H)を末端につけた側鎖が付いてクラスター領域を構成する構造を有している。現在、高分子電解質膜については高含水率を保つための運転条件のコントロールおよび膜質の改良等の研究開発が盛んに行なわれている。上記セパレーターの役目は、各電極への反応ガスの供給、隣り合う単セル間の反応ガスの隔離、および電極からの集電である。アノード側電極には主に水素を含有する燃料ガスが供給されており、触媒電極上で当該水素がイオン化され電解質を介してカソード側電極へと移動する。その間に生じた電子が外部回路に取り出されて直流の電気エネルギーとして利用される。カソード側電極には主に酸素を含有するガスあるいは空気が供給されているために、このカソード側電極では水素イオンと電子および酸素が反応して水が生成される。
【0004】
上述のパーフルオロスルホン酸ポリマーを用いたPEFCでは、運転条件等によりパーフルオロスルホン酸ポリマーの電解質膜が分解劣化し、燃料電池の性能が低下してくることがある。特許文献1には、アノード側電極の反応界面付近の高分子電解質膜を十分に湿潤させることにより、カソード側電極からアノード側電極への水の逆拡散を抑制してカソード側電極の反応界面付近に豊富に水を存在させ、カソード側電極の触媒層中に滞留した過酸化水素水等を速やかに燃料電池の外部へ排出させて、燃料電池の耐久性を向上させる技術が記載されている。
【0005】
特許文献2には、高分子電解質の分解を抑制するために、負荷が停止してから所定の時間が経過するまで、カソード側電極に対して酸化剤ガスの供給を行い、アノード側電極に対して燃料ガスの供給を行なって、所定のタイミングで酸化剤ガスおよび燃料ガスの供給を停止する技術が記載されている。これにより、高分子電解質膜を透過した水素イオンによってカソード側電極の電位を低下させることができるため、カソード側電極において触媒層の触媒活性が回復する。上記所定の時間を短くすることにより、高分子電解質膜の分解を抑制することができると記載されている。
【0006】
一方、PEFCの運転において、長時間連続試験後に高分子電解質膜の薄膜化が観察されており、薄膜化の主要因として電解質膜を構成するポリマーの化学的分解による消失が推定されている。この消失により、高分子電解質膜の材質に由来するフッ素イオンおよび硫酸イオンが分解成分として燃料電池から排出水中に溶出する問題がある。これらの成分の溶出量が多く且つ持続的な溶出であると、高分子電解質膜が部分的に消失して当該膜に孔が開く結果、発電ができなくなると言われている。このため、上記成分の溶出を防ぐことが重要であり、最適な燃料電池の運転条件の決定にも関連する。
【0007】
ここで、PEFCの運転試験条件について簡単に説明する。PEFCの運転試験条件には、例えば燃料電池(単セル)の大きさの違い、電極触媒、燃料ガスと空気流量、ガス差圧、アノード側電極およびカソード側電極の加湿露点、セル温度等、種々のパラメータがあり、これらのパラメータを用いて出力試験等が行なわれている。燃料電池の運転によって生成された水の排出水の回収は、排出水総量(リットルL)、採取時間(h)、試験用電池電極面積(cm2)等の違いを明らかにして行い、排出水中のフッ素イオン濃度(mg/L)を求めて電池特性と運転条件の検討が行なわれる。
【0008】
特許文献3には、PEFCの運転方法を、生成水等における不純物イオンの溶出の程度を測定する不純物イオン測定ステップと、不純物イオン測定ステップで測定された測定値に基づきPEFCが所定の電池性能低下領域にあるかどうかを判断する判断ステップと、所定の電池性能低下領域にあると判断された場合に、PEFCを当該領域から回避させる回避ステップとを含むように構成する技術が記載されている。溶出の程度が測定される不純物イオンは、電池性能を低下させる原因となるイオンであれば特に種類が限定されるものではないと記載されている。
【0009】
特許文献4には、燃料電池システムを通過する流体(改質ガス)のパラメータ(改質ガス中の水分量)を、PEFC内の生成水の影響を考慮して制御する技術が開示されている。すなわち、燃料電池制御の応答遅れに対して燃料電池内の生成水の影響を考慮する点が記載されている。
【0010】
【特許文献1】特開2003−178780号公報
【特許文献2】特開2004−172106号公報
【特許文献3】特開2004−127548号公報
【特許文献4】特開2000−40519号公報
【発明の開示】
【発明が解決しようとする課題】
【0011】
上述の特許文献1には、アノード側電極の反応界面付近の高分子電解質膜を十分に湿潤させることにより、結果的にカソード側電極の触媒層中に滞留した過酸化水素水等を速やかに燃料電池の外部へ排出させる点が記載されている。しかし、燃料電池の生成水である排出水中の電解質膜材料由来の成分を見出すという観点に関してはまったく開示されていない。
【0012】
上述の特許文献2には、高分子電解質の分解を抑制するために、所定のタイミングで酸化剤ガスおよび燃料ガスの供給を停止することにより、高分子電解質膜の分解を抑制する点について記載されている。しかし、特許文献1と同様に、燃料電池の生成水である排出水中の電解質膜材料由来の成分を見出すという観点に関してはまったく開示されていない。
【0013】
上述の特許文献3には、PEFCの運転方法を構成する際に、生成水等における不純物イオンの溶出の程度を測定する不純物イオン測定ステップを含ませる点について記載されている。しかし、特許文献3では、溶出の程度が測定される不純物イオンは電池性能を低下させる原因となるイオンであれば特に種類が限定されるものではないとされている。このため、不純物イオンとしてフッ化物イオンについて記載されているものの、燃料電池の生成水である排出水中の電解質膜材料由来の成分を見出すという観点は開示されてはいない。
【0014】
上述の特許文献4には、燃料電池制御の応答遅れに対して燃料電池内の生成水の影響を考慮する点について記載されている。しかし、排出水の成分を評価するものではない。特許文献4には燃料電池に供給される酸素の圧力を制御すること等が記載されており、電解質膜の分解の観点では言及していないため、燃料電池の良好な運転を期待できるものではない。すなわち、特許文献4に記載されている燃料電池システムの運転方法は、電池運転制御の応答遅れに対する燃料電池内の生成水の影響対策であり、燃料ガス中の水蒸気量等を制御することなどが示されているものであって、排出水の成分の評価とは異なっている。
【0015】
上述のように、従来技術には、燃料電池の生成水である排出水中の電解質膜材料由来の成分を見出すと共に、当該成分の濃度および量を算出する方法が示されていないという問題があった。しかし、主に高分子電解質膜の分解の観点から言えば、フッ素イオン濃度を迅速に且つ微量定量分析ができる方法(フッ素イオン濃度の算出方法)と、フッ素イオン濃度(mg/L)測定後に運転方法に反映できる指標値を求める方法(フッ素イオン量の算出方法)とが重要である。
【0016】
そこで、本発明の目的は、上記問題を解決するためになされたものであり、PEFCの生成水である排出水中の高分子電解質膜材料由来の成分を見出すと共に、簡便にフッ素イオン濃度とフッ素イオン排出量を算出することができるPEFCのフッ素イオン定量方法を提供することにある。
【課題を解決するための手段】
【0017】
この発明のイオン定量分析方法は、フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のイオン成分を分析するイオン定量分析方法であって、前記高分子電解質膜型燃料電池のアノード側及びカソード側排出水中からイオンクロマトグラフ法により検出されたフッ素イオン濃度を高分子電解質膜の分解成分の指標とすることを特徴とする。
【0018】
この発明のフッ素イオン定量分析方法は、フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のフッ素イオン成分を分析するフッ素イオン定量分析方法であって、前記高分子電解質膜型燃料電池のアノード側の排出水中から測定された電導率とカソード側の排出水中から測定された電導率とに基づき、高分子電解質膜から分解したフッ素イオン濃度を定量分析することを特徴とする。
【0019】
この発明のフッ素イオン定量分析方法は、フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のフッ素イオン成分を分析するフッ素イオン定量分析方法であって、前記高分子電解質膜型燃料電池のアノード側及びカソード側の全排出水中から測定された電導率と、アノード側の排出水中から測定された電導率と、カソード側の排出水中から測定された電導率とに基づき、高分子電解質膜から分解したフッ素イオン排出量を定量分析することを特徴とする。
【0020】
ここで、この発明のフッ素イオン定量分析方法において、前記フッ素イオン排出量は、排出水総量、排出水中のフッ素イオン濃度、所定の採取時間及び前記高分子電解質膜型燃料電池の電極面積に基づいて求めることができる。
【発明の効果】
【0021】
本発明のフッ素イオン定量方法によれば、フッ素系の陽イオン交換膜を高分子電解質に用いるPEFCにおいて、反応生成水の排出水をイオンクロマトグラフ法で分析した結果、排出水の電導率とフッ素イオン濃度との相関係数は0.98以上であり、相関性が良好であることが分かった。このため、排出水中では微量レベルであるが、イオン成分はフッ素イオンが支配的であることが示された。さらに、簡便な計測器を用いて排出水の電気伝導率を測定することにより、簡便にフッ素イオン濃度およびフッ素イオン排出量を算出することができるPEFCのフッ素イオン定量方法を提供することができるという効果がある。
【発明を実施するための最良の形態】
【0022】
以下、まず本発明のPEFCのフッ素イオン定量方法に用いられるPEFCシステムの構成について説明し、次に各実施例について図面を参照して詳細に説明する。図1は、本発明のPEFCのフッ素イオン定量方法に用いられるPEFCシステムの構成図である。図1では省略しているが、本PEFCシステムも通常の燃料電池システムと同様に、改質系機器、電池スタック、熱交換器、回転機等の補機類から構成される。図1に示されるように、高分子電解質膜11にはフッ素系の陽イオン交換膜が用いられ、PEFCアノード21とPEFCカソード13との接合体をセパレーター(不図示)により挟んで単セルが構成される。本明細書に示される実験では、実験目的によって電池電極面積が50〜6000cm2と異なり、例えば単セルからセルを積層したスタックを用いている。この燃料電池では、燃料供給部20から供給される主に水素を含有するガスが純水タンク18から供給される水と共に加湿器19aに送られ、湿度が調整された後にPEFCアノード21に供給される。空気送風用ポンプ12からの空気も同様に加湿器19bを介して湿度が調整された後、PEFCカソード13に供給される。PEFCアノード21では水素がイオン化され、高分子電解質膜11を介してPEFCカソード13側へと移動する。PEFCカソード13側では主に上記水素イオンと電子および酸素とが反応して発電され、同時に水が生成される。燃料電池の運転時には、電池スタック(不図示)の冷却板24で冷却され循環する冷却水供給部23から供給される冷却水により熱交換される。上述のように生成された生成水は、各々PEFCアノード21側の排出水ドレンタンク(排出水回収部)22とPEFCカソード13側の排出水ドレンタンク(排出水回収部)14とに回収される。このようにして、PEFCの運転時に発生する反応水である排出水は、各々ドレンタンク22および14に回収される。
【0023】
排出水中のイオン成分分析は、排出水を分取してイオン種の分離機能を有し、イオン検出定量分析に用いられる計測器1(15)のイオンクロマトグラフで行なわれ、主に高分子電解質膜の分解成分と電池内構成部材由来の成分とを検出することができる。排出水中のイオン成分は、高分子電解質膜の分解成分であるフッ素イオン(F−)および硫酸イオン(SO42−)、または燃料電池内有機材料由来の酢酸イオン(CH3COO−)であり、さらに燃料電池への供給ガス等に由来した塩化物イオン(Cl−)である。これらのイオン成分が排出水分析評価の指標となるが、いずれも微量である。これらのイオン成分の中でも特にイオン成分量を求める高分子電解質膜の分解成分の指標とする主たる成分は、フッ素イオンである。
【0024】
排出水は上記計測器1(15)と同様に設置し、電気伝導率(電導率または電気伝導度とも言う。)の計測に用いられる計測器2(16)の電気伝導率計と、pHの測定に用いられる計測器3(17)の水素イオン濃度計(pHメーター)とにより計測される。その後は後述する指標値により、電子制御装置(電子制御部)25から燃料電池の運転制御(点線で示す。)を行なうことができる。
【0025】
本明細書における実験では、PEFCアノード21側およびPEFCカソード13側の排出水のイオン分析を行ない、高分子電解質膜の分解成分を把握した。以下では、実施例1において、排出水のイオン成分(特にフッ素イオン濃度)の分析方法、電気伝導率測定方法および水素イオン濃度(pH)測定方法について述べた後、排出水の電導率とフッ素イオン濃度との関係について述べる。次いで実施例2において、PEFCアノード21側およびPEFCカソード13側の排出水の電導率とフッ素イオン排出量との関係について述べる。
【実施例1】
【0026】
(排出水のイオン成分の分析方法、電気伝導率測定方法および水素イオン濃度(pH)測定方法)
【0027】
1.排出水のイオン成分の分析法
図2は、イオン成分の分析方法の一例として陰イオンの分析を行なうイオンクロマトグラフ分析装置(測定装置)32の構成略図を示す。このイオンクロマトグラフ分析装置32は排出試料液中のイオン成分の分離定量分析を行う装置の一例である。図2に示されるように、イオンクロマトグラフ分析装置32は試料導入バルブ37、ガードカラム38、分離カラム39、除去システム40および検出セル41から構成されている。イオンクロマトグラフィーは、強電解質の溶離液35と共に排出水試料31を試料導入バルブ37から注入し、イオン交換樹脂製の分離カラム39を通す。ガードカラム38は分離カラム39を保護するために設けられている。分離カラム39内では水和半径の大小、Van der Waals力の相互作用によってイオン種の相互分離を行なう。この後、除去システム(サプレッサー)40を通すことによりバックグラウンドの伝導度を下げ、目的とするイオン種を高感度でクロマトグラムとして得るものである。溶離液35は電解質溶液調整部34で調整された陰イオンクロマトグラフ溶離液(KOH:水酸化カリウム)であり、脱気装置(デガッサー)36により溶離液35中に溶存する気体が除去されている。排出水試料31は、イオン成分を含む液であり、懸濁物質は孔径0.2μmのフィルタにより濾過済みである。
【0028】
イオンクロマトグラフ法は、数mLの試料液を用いて、1回の測定で数種の陰イオン成分を同時に測定することができ、分別定量分析を行なうことができる方法である。検出器(検出セル)41にはフローセル型の電導度検出器を用いており、データ処理装置33において、各イオン成分の電導度に基づくイオンクロマトグラムのピーク面積および高さから、目的とする分析試料溶液中のイオン成分濃度が求められる。分析試料溶液中のイオン濃度を求めることにより、イオン成分量(単位:ppm、mg/Lあるいはμg)として算出することができる。陽イオンを分析する際は、分離カラム39と溶離液35とを陽イオン分析用に別途組み替えることによって行なうことができる。
【0029】
次に検量線の検討を行ない、定量分析ができるようにした。イオンクロマトグラフ法によるイオン成分分離分析条件を次に示す。
【0030】
(イオン成分測定条件)
イオンクロマトグラフ分析装置32(分離カラム39を含む。)、溶離液35はすべてDIONEX社製の物を用いた。
【0031】
(1)方法:イオンクロマトグラフ法
(2)分離カラム39:陰イオン用 IonPac AS17/IonPac AG17、 陽イオン用 IonPac CS14/IonPac CG14
(3)溶離液35:陰イオン用 EGC-KOH(水酸化カリウム 10Mmスタート・ステップグラジェント)、
陽イオン用IonPac EGC-MSA(メタルスルホン酸、ステップグラジェント)
(4)除去システム40:オートサプレッサー(ASRS)、(CSRS)
(5)試料液量:25μLループ法
(6)定量法:イオンクロマトグラムピーク面積とイオン成分濃度の検量線法
【0032】
図3は、他の陰イオンから分離定量分析する際のフッ素イオン(F−)、硫酸イオン(SO42−)、酢酸イオン(CH3COO−)、塩化物イオン(Cl−)等の存在を示す陰イオン標準液のクロマトグラムの例を示す。図3において横軸は溶離時間(min)、縦軸は面積である。図4は、フッ素イオンのピーク面積(縦軸)とフッ素イオン濃度(ppb)との関係からなる検量線の例を示す。実施例1に係る試料液中フッ素イオン濃度の実験式1を次に示す。式1中のXは面積である(以下の式においても同様)。
【0033】
フッ素イオン(F− ppb) = 2500X 相関係数 1 (1)
【0034】
図4に示されるように、フッ素イオン濃度とピーク面積との相関係数は0.9999以上であり良好であった。イオンクロマトグラフ法による排出水中のイオン分析は、測定により得られたイオンのピーク面積からフッ素イオンの液中濃度を算出することにより、定量分析することができる。
【0035】
2.電導率測定方法
水溶液の電気抵抗は、溶存イオン量が増大すると低下する。電導率(σ)は抵抗(ρ)の逆数であるから(σ=1/ρ)、抵抗の減少は電導率の増大を意味する。水中の溶存物質が比較的少量の場合には、電導率はその量にほぼ比例して変化すると考えられるので、電導率を測定すれば全溶解物質のおおよその値を短時間で推定できる。
【0036】
電導率の測定には同一形状の2個の平板白金電極を備えたセルを用い、これに試料水を満たして電気抵抗が測定され、比電導率(ohm-1・cm-1)が求められる。流路に適用できるフロー型セルを用いてもよい。さらに現在では電導率の単位は25℃における、ミリジーメンス毎メートルと呼称され、(mS/m)で表されるのが一般的になっている。排出水の電導率の測定はイオン成分の存在に関係するので、水質評価項目として有効である。
【0037】
3.水素イオン濃度測定方法
水溶液中の水素イオン濃度[H+]の逆数の対数をその溶液のpHという(pH=−log10[H+])。現在ではガラス電極pHメータによる測定が行なわれている。排出水のpHの測定はイオン成分の存在と水素イオン濃度に関係するので、水質評価項目として計測する。
【0038】
4.排出水の電導率、pHとフッ素イオン濃度との関係
次に、上記の測定条件で実試料である排出水のフッ素イオンの分析と排出水の電導率、pHの分析測定を行なった。実試料はPEFCの運転時の排出水である。PEFCの運転試験条件には、例えば電池(単セル)の大きさの違い、電極触媒、燃料ガスと空気流量、ガス差圧、PEFCアノード21およびPEFCカソード13の加湿露点、セル温度等、種々のパラメータがあり、出力試験等が行なわれている。上述のように、本明細書に示す実験では実験目的によって電池電極面積が50〜6000cm2と異なる単セルからセルを積層したスタックを用いている。さらにPEFCアノード21加湿露点を54〜80(℃)、PEFCカソード13加湿露点を63〜85(℃)と変えて実験を行ない、排出水採水のための燃料電池運転時間を1〜373時間とした。
【0039】
図5は、排出水の電導率(mS/m。縦軸)とフッ素イオン濃度(mg/L。横軸)との関係を示す線図である。図5に示されるように、電導率とフッ素イオン濃度との相関係数が0.98以上であり、相関性が良好であることが分かる。これは、排出水中では微量レベルであるが、イオン成分はフッ素イオンが支配的であることを示している。試料液中フッ素イオン濃度F−
(mg/L)の実験式2を次に示す。
【0040】
F− (mg/L)=0.6744X−0.1707 (2)
【0041】
以上より、本発明の実施例1によれば、フッ素系の陽イオン交換膜を高分子電解質に用いるPEFCにおいて、反応生成水の排出水をイオンクロマトグラフ法で分析した。PEFC運転時に発生する反応水である排出水は、PEFCアノード21側の排出水ドレンタンク22とPEFCカソード13側の排出水ドレンタンク14とに回収される。排出水中のイオン成分分析は計測器1(15)のイオンクロマトグラフで行なわれ、主に高分子電解質膜の分解成分と電池内構成部材由来の成分とを検出することができる。排出水は上記計測器1(15)と同様に設置し、電気伝導率の計測に用いられる計測器2(16)の電気伝導率計と、pHの測定に用いられる計測器3(17)の水素イオン濃度計(pHメーター)とにより計測される。計測の結果、排出水の電導率とフッ素イオン濃度との相関係数は0.98以上であって相関性が良好であることが分かり、排出水中では微量レベルであるが、イオン成分はフッ素イオンが支配的であることが示された。さらに、簡便な計測器2(16)を用いて排出水の電気伝導率を測定することにより、簡便にフッ素イオン濃度を算出することができるPEFCのフッ素イオン定量方法を提供することができた。
【実施例2】
【0042】
実施例1では、高分子電解質膜の分解調査の観点から、排出水中のフッ素イオン濃度(mg/L) と電導率に相関性があることを見出し、フッ素イオン濃度を迅速にかつ微量定量分析ができる方法を見出した。実施例2では、PEFCの高分子電解質膜の分解成分は排出液中のフッ素イオン量とし、排出水総量(リットル)、排出水中のフッ素イオン濃度(mg/L)、24時間当りの採取時間(日。所定の採取時間)、電池電極面積(cm2)の関係から排出量(フッ素イオンμg/day/cm2)をPEFCアノード21からの排出水およびPEFCカソード13からの排出水から求めた値とその合計量の値を求めた。つまり、排出水中のフッ素イオン濃度は予めイオンクロマトグラフ法で求めた値と排出水の電気伝導度との関係からフッ素イオン量が求められる検量線を得る。次いで、排出量(フッ素イオンμg/day/cm2)は排出水の電気伝導度から得られるようにした。
【0043】
図6は、PEFCアノード21側とPEFCカソード13側の全排出水試料液の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。図6に示されるように、全排出水試料液の電導率とフッ素イオン排出量との相関係数は0.95以上であり、相関性が良好であることが分かる。試料液中フッ素イオン排出量F− (μg/day/cm2)の実験式3を次に示す。
【0044】
F− (μg/day/cm2)=1.191X−0.1022 (3)
【0045】
図7は、PEFCアノード21側の排出水試料液の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。PEFCアノード21側の排出水試料液の電導率とフッ素イオン排出量との相関係数は0.96以上であり、相関性が良好であることが分かる。試料液中フッ素イオン排出量F− (μg/day/cm2)の実験式4を次に示す。
【0046】
F− (μg/day/cm2)=0.8095X−0.1063 (4)
【0047】
図8は、PEFCカソード13側の排出水試料液の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。PEFCカソード13側の排出水試料液の電導率とフッ素イオン排出量との相関係数は0.97以上であり、相関性が良好であることが分かる。試料液中フッ素イオン排出量F− (μg/day/cm2)の実験式5を次に示す。
【0048】
F− (μg/day/cm2)=1.186X+0.112 (5)
【0049】
以上のことから、排出量(フッ素イオンμg/day/cm2)は、排出水の電気伝導度を直接計測することによっても得られることが分かった。つまり、高分子電解質膜の分解成分である排出水のイオンは主にフッ素イオンであり、電導率に関係していることを見出した。排出水中の硫酸イオン等の他のイオンとの関係は極めて小さいことを示唆している。
【0050】
以上より、本発明の実施例2によれば、PEFCの高分子電解質膜の分解成分は排出液中のフッ素イオン量とし、排出水総量(リットル)、排出水中のフッ素イオン濃度(mg/L)、24時間当りの採取時間(日)、電池電極面積(cm2)の関係から排出量(フッ素イオンμg/day/cm2)をPEFCアノード21からの排出水およびPEFCカソード13からの排出水から求めた値とその合計量の値を求めた。全排出水試料液の電導率とフッ素イオン排出量との相関係数は0.95以上であり、相関性が良好であることが分かった。PEFCアノード21側の排出水試料液の電導率とフッ素イオン排出量との相関係数は0.96以上であり、相関性が良好であることが分かった。PEFCカソード13側の排出水試料液の電導率とフッ素イオン排出量との相関係数は0.97以上であり、相関性が良好であることが分かった。この結果、排出水中のイオン成分はフッ素イオンが支配的であることが示された。さらに、簡便な計測器2(16)を用いて排出水の電気伝導率を測定することにより、簡便にフッ素イオン排出量を算出することができるPEFCのフッ素イオン定量方法を提供することができた。
【産業上の利用可能性】
【0051】
本発明の活用例として、PEFCの運転条件に反映することが挙げられる。すなわち、PEFC運転時間の経過毎に、反応水である排出水のフッ素イオン排出量の変動を把握できる。排出水の電導率測定値とフッ素イオン排出量との関係は図6、図7、図8で確認しているので、PEFCの運転条件に反映させてフッ素イオン排出量を制御できる。この結果、簡便で安定した燃料電池の運転ができるようになり、排出水の電導率測定値とフッ素イオン排出量とを運転の指標として利用することができる。
【図面の簡単な説明】
【0052】
【図1】本発明のPEFCのフッ素イオン定量方法に用いられるPEFCシステムの構成図である。
【図2】イオン成分の分析方法の一例としてイオンクロマトグラフ分析装置(測定装置)32の構成を示す略図である。
【図3】他の陰イオンから分離定量分析する際のフッ素イオン(F−)、硫酸イオン(SO42−)、酢酸イオン(CH3COO−)、塩化物イオン(Cl−)等の存在を示す陰イオン標準液のクロマトグラムの例を示す図である。
【図4】フッ素イオンのピーク面積(縦軸)とフッ素イオン濃度(ppb)との関係からなる検量線の例を示す図である。
【図5】排出水の電導率(mS/m。縦軸)とフッ素イオン濃度(mg/L。横軸)との関係を示す線図である。
【図6】PEFCアノード21側とPEFCカソード13側の排出水の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。
【図7】PEFCアノード21側の排出水試料液の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。
【図8】EFCカソード13側の排出水試料液の電導率(mS/m。縦軸)とフッ素イオン排出量(μg/day/cm2。横軸)との関係を示す線図である。
【符号の説明】
【0053】
11 高分子電解質膜、 12 空気送風用ポンプ、 13 PEFCカソード、 14 PEFCカソード13側の排出水ドレンタンク(排出水回収部)、15 計測器1(イオンクロマトグラフ)、 16 計測器2(電気伝導率計)、 17 計測器2(水素イオン濃度計)、 18 純水タンク、 19a、19b 加湿器、 20 燃料供給部、 21 PEFCアノード、 22 PEFCアノード21側の排出水ドレンタンク(排出水回収部)、 23 冷却水供給部、 24 冷却板、 25 電子制御装置、 31 排出水試料、 32 イオンクロマトグラフ測定装置、 33 データ処理装置、 34 電解質溶液調整部、 35 陰イオンクロマトグラフ溶離液、 36 脱気装置(デガッサー)、 37 試料導入バルブ、 38 ガードカラム、 39 分離カラム、 40 除去システム(サプレッサー)、 41 検出セル。
【特許請求の範囲】
【請求項1】
フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のイオン成分を分析するイオン定量分析方法であって、
前記高分子電解質膜型燃料電池のアノード側及びカソード側排出水中からイオンクロマトグラフ法により検出されたフッ素イオン濃度を高分子電解質膜の分解成分の指標とすることを特徴とするイオン定量分析方法。
【請求項2】
フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のフッ素イオン成分を分析するフッ素イオン定量分析方法であって、
前記高分子電解質膜型燃料電池のアノード側の排出水中から測定された電導率とカソード側の排出水中から測定された電導率とに基づき、高分子電解質膜から分解したフッ素イオン濃度を定量分析することを特徴とするフッ素イオン定量分析方法。
【請求項3】
フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のフッ素イオン成分を分析するフッ素イオン定量分析方法であって、
前記高分子電解質膜型燃料電池のアノード側及びカソード側の全排出水中から測定された電導率と、アノード側の排出水中から測定された電導率と、カソード側の排出水中から測定された電導率とに基づき、高分子電解質膜から分解したフッ素イオン排出量を定量分析することを特徴とするフッ素イオン定量分析方法。
【請求項4】
請求項3記載のフッ素イオン定量分析方法において、前記フッ素イオン排出量は、排出水総量、排出水中のフッ素イオン濃度、所定の採取時間及び前記高分子電解質膜型燃料電池の電極面積に基づいて求めることを特徴とするフッ素イオン定量分析方法。
【請求項1】
フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のイオン成分を分析するイオン定量分析方法であって、
前記高分子電解質膜型燃料電池のアノード側及びカソード側排出水中からイオンクロマトグラフ法により検出されたフッ素イオン濃度を高分子電解質膜の分解成分の指標とすることを特徴とするイオン定量分析方法。
【請求項2】
フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のフッ素イオン成分を分析するフッ素イオン定量分析方法であって、
前記高分子電解質膜型燃料電池のアノード側の排出水中から測定された電導率とカソード側の排出水中から測定された電導率とに基づき、高分子電解質膜から分解したフッ素イオン濃度を定量分析することを特徴とするフッ素イオン定量分析方法。
【請求項3】
フッ素系の陽イオン交換膜を高分子電解質に用いる高分子電解質膜型燃料電池の排出水中のフッ素イオン成分を分析するフッ素イオン定量分析方法であって、
前記高分子電解質膜型燃料電池のアノード側及びカソード側の全排出水中から測定された電導率と、アノード側の排出水中から測定された電導率と、カソード側の排出水中から測定された電導率とに基づき、高分子電解質膜から分解したフッ素イオン排出量を定量分析することを特徴とするフッ素イオン定量分析方法。
【請求項4】
請求項3記載のフッ素イオン定量分析方法において、前記フッ素イオン排出量は、排出水総量、排出水中のフッ素イオン濃度、所定の採取時間及び前記高分子電解質膜型燃料電池の電極面積に基づいて求めることを特徴とするフッ素イオン定量分析方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【公開番号】特開2006−78226(P2006−78226A)
【公開日】平成18年3月23日(2006.3.23)
【国際特許分類】
【出願番号】特願2004−259988(P2004−259988)
【出願日】平成16年9月7日(2004.9.7)
【出願人】(000005234)富士電機ホールディングス株式会社 (3,146)
【Fターム(参考)】
【公開日】平成18年3月23日(2006.3.23)
【国際特許分類】
【出願日】平成16年9月7日(2004.9.7)
【出願人】(000005234)富士電機ホールディングス株式会社 (3,146)
【Fターム(参考)】
[ Back to top ]

