インピーダンス測定値を用いて生物学的な状態を決定する医療装置
【課題】被験者の皮膚の病状を診断するための医療装置。
【解決手段】複数の電極を有した導電性のプローブを備えており、かつ各電極は複数のマイクロニードルを具備している。このとき、各電極はベース基板を有している。マイクロニードルは、この基板と一体に形成され、互いに横方向に間隔を空けた関係に配置され、角質層を貫通するのに十分な長さを有している。マイクロニードルは、少なくとも部分的に傾斜した形状に構成されている。この装置ための電極、マイクロニードルの配列、インピーダンス測定を用いた生物学的な状態の診断方法に関連している。この診断方法は癌、好ましくは基底細胞癌、悪性黒色腫、扁平上皮癌である皮膚癌、あるいはそのような病変の前駆体に特に関連している。
【解決手段】複数の電極を有した導電性のプローブを備えており、かつ各電極は複数のマイクロニードルを具備している。このとき、各電極はベース基板を有している。マイクロニードルは、この基板と一体に形成され、互いに横方向に間隔を空けた関係に配置され、角質層を貫通するのに十分な長さを有している。マイクロニードルは、少なくとも部分的に傾斜した形状に構成されている。この装置ための電極、マイクロニードルの配列、インピーダンス測定を用いた生物学的な状態の診断方法に関連している。この診断方法は癌、好ましくは基底細胞癌、悪性黒色腫、扁平上皮癌である皮膚癌、あるいはそのような病変の前駆体に特に関連している。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、全般的に生物学的な状態を診断する分野に関し、より詳しくは、医療装置、そのような装置に用いる電極、そのような電極に用いるミクロ構造、および被検者の皮膚の病状、特に皮膚癌、例えば基底細胞癌、悪性黒色腫、扁平上皮癌あるいはその前駆体の存在を皮膚インピーダンス測定値を用いて非侵襲的に診断する方法に関する。
【背景技術】
【0002】
基底細胞癌(BCC)は、最も一般的な皮膚癌である。その発生率は、世界中の多くの国、例えばスウェーデンにおいて増加している。例えば同種異系の臓器を移植した後における長期の免疫抑制は、BCCおよび他の皮膚腫瘍の発症リスクを増大させる。このことは、紫外線光あるいは電離性放射線を浴びた後にも当てはまる。遺伝との明白な関連性はないと思われ、多くの患者においては他のいかなる素因も見い出されない。しかしながら、特に色素が沈着した病変の場合には、経験を積んだ皮膚科医でさえも皮膚の腫瘍の臨床的診断は困難である。診療所においては、経験を積んだ肉眼と組織学的検査のための皮膚生検法との組み合わせに加えて、さらに診断を補助するものが必要である。
【0003】
皮膚腫瘍の臨床的診断のような生物学的な判定は、検体採取を伴う侵襲性の技術よりも優れている非侵襲性の方法で行うことが一般的には望ましい。非侵襲性の技術はより便利であり、例えば痛みがより少なく、感染のリスクもより低い。したがって、生物学的な判定を行うための多くの非侵襲性の技術が提案されてきた。
【0004】
米国特許第5,036,861号、1991年8月6日、Sembrowich他。
米国特許第5,115,133号、1992年5月19日、Knudson。
米国特許第5,146,091号、1992年9月8日、Knudson。
米国特許第5,197,951号、1993年1月19日、Knudson。
米国特許第5,222,496号、1993年6月29日、Clarke他。
PCT/US94/08816、国際特許公開WO95/04496号公報、1995年2月16日、 Solid State Farms。
米国特許第5,433,197号、1995年7月18日、Stark。
PCT/US97/13267、国際特許公開WO98/04190号公報、1998年2月5日、 Dermal Therapy (Barbados) Inc.。
PCT/US98/02037、国際特許公開WO99/39627号公報、1999年8月12日、Dermal Therapy (Barbados) Inc.。
PCT/IB00/01464、国際特許公開WO01/26338号公報、2000年10月13日、Sesstrunk他。
【0005】
しかしながら、上述した文献の全てが、血液のブドウ糖レベルを評価する技術を開示している。したがって、被検者の皮膚の病状、特に皮膚癌、例えば基底細胞癌の存在の診断には適していない。
【0006】
電気インピーダンスは、生体および生物学的な物質、特に粘膜、皮膚および臓器の皮膜のような組織における微細な変化のきわめて高感度な表示手段を構成し、したがって組織の構造的な特性の変化を非侵襲的に測定するための効果的な手段を提供することが判明してきている。PCT/SE91/00703には、同軸なリングシステムに配列された多くの電極を具備する測定用電極を備えた、生体および生物学的な物質の電気インピーダンスを非侵襲的に測定するための装置が開示されている。これらの電極は、検査を受ける実際の組織を決める電流の経路が制御信号によって定まるように、制御ユニットによって駆動される。この制御信号を変化させることにより、検査する領域を選択することができる。2つのリングが電圧を供給し、2つのリングの間の関係が2つのリングの間に配置される仮想的な注入点を生じさせる。2つの注入点の間の電圧関係を調整することによって仮想注入点を前後に移動させることができ、したがって組織の貫通深さを選択することができる。しかしながら、人間の皮膚は複雑で不均質かつ異方性の多層構造であり、電子的に非線形な特性を有している。最も非線形な特性は角質層(表皮の最外側層)に位置している。したがって、その深さが高度に関連しているにもかかわらず、2つの深さからの補間あるいは外挿によって計算することができない情報が全ての深さに存在している。しかしながら、PCT/SE91/00703に開示されている装置には、例えば皮膚癌およびアレルギー反応が現れる角質層の下側の皮膚層における組織の変化について、信頼性の高い結果を供給することができないという大きな弱点がある。このことは、皮膚の非侵襲的な電気インピーダンスのスペクトルが、特に低い周波数において角質層の誘電特性によって支配されるという事実に起因している。角質層は、その下に横たわっている生体皮膚層からの反応が角質層からの反応と混乱して生体皮膚からの臨床関連情報を弱める、(広くα分散と呼ばれている)特性を有している。このことは、PCT/SE91/00703に開示されている測定用電極を用いた角質層の下に現れる電気インピーダンス現象の評価を、困難かつ予測不能なものとしている。
【0007】
国際特許公開WO01/52731号公報は、電気的な生体電位が生きている被検者の身体内部で作り出されていることを検出するための医用電極を開示している。この電極は、皮膚を貫通するように構成された多くのマイクロニードルを有している。これらのマイクロニードルは、胚芽層に到達するために充分に長く、それらの表面上において導電性であり、かつ互いに接続されて配列を形成している。国際特許公開WO01/52731号公報によると、このマイクロニードルは「釘」に似ている。すなわち、それらは一定のあるいは徐々に減少する直径を有した実質的に円形の断面を有したステムと、実質的に球形あるいは針状の先端を有した先端部とを有している。欧州特許公開1437091号公報には、生体および生物学的な物質のインピーダンス測定を用いる、生物学的な状態を診断するための装置が開示されている。この装置は、複数の電極を有したプローブを備えているが、角質層を貫通するのに十分な長さをそれぞれ有した多数のマイクロニードルが各電極に設けられている。欧州特許公開1437091号公報のマイクロニードルもまた「釘」に似ている。すなわち、それらは、一定のあるいは徐々に減少する直径を具備した実質的に円形の断面を有するステムと、実質的に球形あるいは針状の先端を有した先端部とを有している。
【0008】
しかしながら、実際的な試験は、従来技術のマイクロニードルを有した電極が、そのマイクロニードルを胚芽層内に適切に貫通させるために相当の力、あるいは電極を前後に傾けるといったかなりの操作を必要とすることを示した。このことは、テストを実行するオペレータ、例えば医師あるいは看護婦ばかりでなく、患者にとっても不快でありかつ煩わしい。さらに、このことはまた、使用の間にニードルが破損する可能性を回避するために、例えばその寸法を増すことによってニードルが充分な強度を有するように設計されることを必要とする。
【0009】
したがって、非侵襲的に被検者の皮膚の病状、特に皮膚癌、例えば基底細胞癌、悪性黒色腫、扁平上皮癌あるいはその前駆体の存在を診断するための、改善された医療電極、装置の必要性が存在する。
【発明の開示】
【発明が解決しようとする課題】
【0010】
したがって、本発明の目的は、改良された装置、そのような装置に用いる電極装置、そのような電極に用いるミクロ構造、および被検者の皮膚の病状、特に皮膚癌、例えば基底細胞癌、悪性黒色腫、扁平上皮癌あるいはその前駆体の存在を正確にかつ高い信頼性で診断する方法を提供することにある。
【0011】
本発明の他の目的は、良好な貫通能力を具備したマイクロニードルを有する、被験者の皮膚の病状を診断するための改良された装置、およびそのような装置のためのプローブを提供することにある。
【0012】
本発明のさらなる目的は、高い構造強度のマイクロニードルを有する、被験者の皮膚の病状を診断するための改良された装置、およびそのような装置のためのプローブを提供することにある。
【0013】
本発明のさらに他の目的は、電気的な特性が良好なマイクロニードルを有する、被験者の皮膚の病状を診断するための改良された装置、およびそのような装置のためのプローブを提供することにある。
【0014】
本発明のさらに別の目的は、被験者の皮膚の病状を診断する装置およびそのような装置に用いるプローブのための、効率が高くかつ信頼できる方法で製造することができるマイクロニードルを提供することにある。
【0015】
これらのおよび他の目的は、独立請求項に定められている機能を有した医療装置および方法を提供する本発明によって達成される。本発明の好ましい実施形態は、従属請求項にその特徴が表されている。
【課題を解決するための手段】
【0016】
本発明の一態様によると、被験者の皮膚の病状を診断するための医療装置であって、複数の電極を有している導電性のプローブを備え、各電極は複数のマイクロニードルを具備しており、前記プローブは、前記マイクロニードルが角質層を貫通するように被験者の表面に対して配置されるようになっており、前記医療装置は、皮膚インピーダンス値を得るために電極に電流を通すことを含むインピーダンス測定セッションを開始するように構成されるとともに、得られたインピーダンス値が病気にかかった状態を示すかどうかを決定するために参照データを用いる、医療装置が提供される。各電極はベース基板を有しており、前記マイクロニードルは、前記基板と一体的に形成されるとともに、互いに横方向に間隔を空けた関係に配置され、かつ角質層を貫通するのに十分な長さを有しており、前記マイクロニードルには少なくとも部分的に傾斜した形状が設けられる。
【0017】
本発明の第2の態様によると、被験者の皮膚の病状を診断するべく被験者の皮膚表面に配置されるように構成される、複数のマイクロニードルを具備した電極が提供される。前記電極はベース基板を有しており、前記マイクロニードルは、前記基板と一体的に形成されるとともに、互いに横方向に間隔を空けた関係に配置され、かつ被験者の皮膚表面に配置されたときに角質層を貫通するのに十分な長さを有しており、前記マイクロニードルには少なくとも部分的に傾斜した形状が設けられる。
【0018】
本発明の第3の態様によると、ミクロ構造の配列であって、ベース基板と、同時に形成されてこの基板の表面から突出するマイクロニードルの配列とを備え、前記マイクロニードルは、互いに横方向に間隔を空けた関係に配置され、かつ被験者の皮膚表面に配置されたときに角質層を貫通するのに十分な長さを有しており、前記マイクロニードルに少なくとも部分的に傾斜した形状が設けられているミクロ構造の配列が提供される。
【0019】
本発明のさらに別の態様によると、被験者の皮膚の病状を診断する方法であって、基板と一体的に形成されるとともに、互いに横方向に間隔を空けた関係に配置され、かつ角質層を貫通するのに十分な長さを有しており、さらに少なくとも部分的に傾斜した形状が設けられているマイクロニードルが角質層を貫通するように、被験者の皮膚表面に導電性のプローブを配置する段階と、皮膚のインピーダンス値を得るために電極を介して電流を通過させる段階と、得られたインピーダンス値が病気にかかった状態を示すかどうかを決定するために参照データを用いる段階と、を備える方法が提供される。
【0020】
このように、本発明は、皮膚の非侵襲性の電気インピーダンススペクトルが、特に低い周波数において角質層の誘電特性によって支配されるという知見に基づいている。角質層は、その下に横たわっている生体皮膚層からの反応が角質層からの反応と混乱して生体皮膚からの臨床関連情報を弱める(広くα分散と呼ばれている)特性を有している。より詳しくは、本発明は、高い構造強度、良好な電気的特性(例えば導電性)、および貫通能力を有したマイクロニードルの設計に基礎を置いている。
【0021】
本発明は、いくつかの利点をもたらす。一つの利点は、角質層の下方に現れる電気インピーダンス現象を、本発明を用いることによって信頼できる方法で評価することができることにある。これにより、本発明を用いることによって、被験者の皮膚の病状、特に皮膚癌、例えば基底細胞癌、悪性黒色腫、扁平上皮癌、あるいはその前駆体の存在を、正確かつ信頼できる方法で診断することができる。
【0022】
他の利点は、本発明の電極が角質層を貫通するために必要とする圧力が、従来の電極のそれより少ないことにある。これにより、本発明の電極は、負荷される圧力、したがってオペレータによって左右される度合いが低い。これはまた、従来の電極で実行されるテストに比べると、テストを受ける患者あるいは被験者の不都合をより少ないものとする。
【0023】
さらなる利点は、本発明による電極のマイクロニードルが高い構造強度を有しており、したがってこれらの針には耐久性があることである。
【0024】
さらに他の利点は、本発明によるマイクロニードルが被験者の皮膚と接触する表面を大きくすることができ、針と角質層との間の良好な導電性に結びつき、翻って高い精度および信頼性のインピーダンス測定をもたらすことにある。
【0025】
本発明の一実施形態によると、各マイクロニードルには、少なくとも部分的に傾斜した形状を具備した先端部が設けられる。この特別な設計は、良好な貫通力を有することが見出された。これにより、この電極は負荷される圧力、したがってオペレータによって左右される度合いが低いから、従来の電極で実行されるテストに比べると、テストを受ける被験者の不都合がより少なくなる。
【0026】
さらに他の実施形態においては、マイクロニードルには、少なくとも部分的に傾斜する端面を具備した先端部が設けられる。
【0027】
さらに別の実施形態においては、マイクロニードルはそれぞれ実質的に三角形の断面に構成される。この設計は、高い構造強度および高い貫通能力を有することが見出された。さらに、それは被験者の皮膚に対する大きな接触表面を有する。このことは、針と角質層との間の良好な導電性に結びつき、翻って高い精度および信頼性のインピーダンス測定をもたらす。
【0028】
あるいは、マイクロニードルはそれぞれ、実質的に菱形、正方形に似た形、楕円形、多角形、矩形あるいは円形の断面に構成される。
【0029】
本発明の一実施形態によると、電極の配列は、使い捨て使用のために、プローブ上に着脱自在に取り付けることができるキャップ上に設けられる。これにより、一人の被験者における測定を実行した後に、電極を具備しているキャップを取り外して廃棄し、新しいキャップをプローブに取り付けることができる。したがって、衛生的な状態で測定することができる。
【0030】
一実施形態においては、ベース基板がウエハ要素から形成され、かつマイクロニードルは異方性エッチングプロセス、マスキングプロセス、および基板上の深堀反応性イオンエッチング(DRIE)プロセスの連続的なシーケンスを含むプロセスによって、このウエハ要素から製作される。この製造プロセスは高い構造強度を有したマイクロニードルの配列をもたらすとともに、このプロセスは高い歩留まり率を有する。
【0031】
本発明の他の実施形態によると、第1の電極および第2の電極のマイクロニードルが第1の距離で互いに横方向に間隔を空けて配置され、第1の電極および第3の電極のマイクロニードルが第2の距離で互いに間隔を空けて配置され、第1および第2の電極を用いて得られた値と第1および第3の電極を用いて得られた値との間における、皮膚インピーダンスの第1および第2の値あるいは皮膚インピーダンスの値の混合値を得るために、第1および第2の電極間の電位と第1および第3の電極間の電位との比率は段階的にあるいは徐々に変更される。これにより、測定が実行される深さを、正確かつ信頼できる方法で選択することができる。
【0032】
加えて本発明は、生物学的な状態、例えば被験者の皮膚の特性の変化あるいは被験者の組織の特性の変化を測定し、監視し、検出するために用いることができる。さらに本発明は、腎臓のような臓器の組織の生物学的な状態を測定し、監視し、かつ検出するために用いることができる。
【0033】
本発明の一実施形態によると、電極は矩形の棒として製作される。他の実施形態によると、基本的な機能と両立する他の構造もまた考えることができる。例えばC字形、あるいは同軸に電極を設計することができる。ガード、信号アース、ドリブンガード(driven guard)他を支持する追加の電極を設けることもできる。電磁干渉を最小化するために、確立されたエンジニアリング方式に基づいてケーブルおよびシースを構成することができる。さらに、現地の安全規則に適合するように設計することができる。
【0034】
本発明を特徴づける特色、構成および操作の方法、さらなる目的および利点は、添付の図面と共になされる以下の説明からより良好に理解されるであろう。図面は例証を目的としたものであり、かつ説明が本発明の限界を定めることを意図していないことは、明白に理解されるべきである。本発明によって達成されるこれらの目的および他の目的、もたらされる利点は、以下の説明を添付の図面と共に読むことによって明らかとなる。
【発明を実施するための最良の形態】
【0035】
本発明のプローブは多数の、少なくとも3つの電極を有し、かつ本発明においては各電極に少なくとも一つのマイクロニードルが設けられ、それによってマイクロニードル化された表面が形成されて様々な皮膚深さでの測定を可能にしている。プローブは、3つの矩形の領域あるいは棒を有しており、各棒は57本(19×3)のマイクロニードルの配列を具備している。各棒は、幅が1mmで長さは5mmである。最も近い棒の間の距離は0.2mmであり、かつ第2および第3の棒の間の距離は1.8ミリメートルであるしたがって、プローブの作動部分は約5×5mmである。各マイクロニードルは、そのベース部から測定すると約100マイクロメートルの長さを有しており、かつ約30マイクロメートルの厚みを有している。マイクロニードルは、好ましくはシリコンから製造されるとともに、約2マイクロメートルの厚みの金で覆われている。同程度の寸法を有した導電性表面を構成する任意の材料も機能するが、生体適合性のものが選択されなければならない。このプローブについては、図7a、図7b、図8aおよび図8bを参照して以下に詳述する。
【0036】
ここで、図1a、図1b、図2aおよび図2bを参照し、本発明による、被検者の皮膚の病状を診断するための上述した電極に用いるミクロ構造あるいはマイクロニードルの実施形態について説明する。各電極には配列として構成された複数のそのようなマイクロニードルが設けられているが、明快さのために1本のマイクロニードルについて以下に説明する。実施形態の側面図、すなわちベース基板に対し垂直な平面に沿った実施形態の断面図、および実施形態の平面図、すなわち基板に対し平行な平面に沿った断面図が、それぞれ図1aおよび図1bに示されている。他の実施形態の側面図、すなわち基板に対して垂直な平面に沿った実施形態の断面図、および実施形態の平面図、すなわち基板に対し平行な平面に沿った断面図が、図2aおよび図2bに示されている。
【0037】
上述したように、各プローブには、基板と一体に形成されるとともに、互いに横方向に間隔を空ける関係で配置され、かつ角質層を貫通するのに十分な長さを有している複数のマイクロニードルが設けられている。まず最初に図1aを参照すると、本発明によるそのようなマイクロニードルの一実施形態が、基板に対して垂直な平面に沿って示されている。マイクロニードル10は、例えばSOIタイプのシリコンウエハであるベース基板12上に設けられている。このマイクロニードル10には、傾斜した先端部14あるいは少なくとも部分的に斜め形状の先端部が設けられている。この先端部14、すなわち斜めの表面は、マイクロニードル10の一部を構成している。図1bには、矢印B方向の平面図が、、図1a中のA−A破断線で示されている、すなわちマイクロニードル10の基部における、基板12に対して実質的に平行な平面に沿った断面で示されている。この図から判るように、マイクロニードル10はこの平面においては三角形の断面を有している。マイクロニードルの寸法b1およびs1は高さh1に沿って実質的に一定であり、かつベース基板12の表面から高さh2−h1に沿った方向において連続的にテーパ状である。ここで留意されるべきことは、基板12の一部だけが図1bに示されていることである。図1aおよび図1bの実施形態の寸法は、以下の表1に示されている。図2aおよび図2bを参照すると、本発明のマイクロニードルの他の実施形態が、基板に対して垂直な平面に沿って示されている。マイクロニードル20は、例えばSOIタイプのシリコンウエハであるベース基板12上に配置されている。このマイクロニードル20には、傾斜した先端部24あるいは斜め形状の先端部が設けられている。この実施形態においては、先端部24がベース基板12に向けて延びている。図2bには、矢印B方向の平面図が、図2a中のA−A破断線で示されている、すなわちマイクロニードル10の基部における、基板12に対して実質的に平行な平面に沿った断面で示されている。この図から判るように、マイクロニードル20はこの平面においては三角形の断面を有している。この場合、基板12に対し平行な断面は、ベース基板12の表面から離れる方向において連続的にテーパ状である。ここで留意されるべきことは、基板12の一部だけが図2bに示されていることである。図2aおよび図2bの実施形態の寸法もまた、以下の表1に示されている。例えば、図2aおよび図2bに示されている実施形態においては、h1は実質的にゼロである。
【表1】

【0038】
シリコンウエハの平面から延びるマイクロニードルの製造は周知である。例えば、米国特許公開2004/0243063号公報、"Microneedle array module and method for fabricating the same", Shuvo R., and Aaron J. F.、および米国特許第6,334,865号、"Microneedle devices and methods for manufacture and use thereof, Allen M. G., et al.を参照されたい。
【0039】
本発明のマイクロニードルの配列は、ウエハ(基板)から形成することができる。このとき、傾斜した表面がエッチングプロセスによって基板上に設けられ、かつ(フォトレジストを用いたリソグラフィのような)適切なパターニングプロセスを用いてこの傾斜した表面上にマスクが設けられる。次いで、ニードルの構造は、第2のエッチングプロセスによって所望の構造に形成される。この傾斜した表面は、針の先端に斜めの端面を有したニードルの製造を可能にする。
【0040】
このウエハに似た基板は、<100>、<110>等の結晶方向/配向を呈する表面を有した単一結晶シリコンとすることができる。しかしながら、同一あるいは同程度の処理技術を受けることができる他の結晶性物質もまた適している。より詳しくは、有用な出発基板はいわゆるSOIウエハ(Silicon On Insulator)である。SOIウエハが明瞭なエッチングストップ層を提供するからである。そのようなストップ層は、製作する構造の寸法(すなわち高さ、幅、凹所の深さ等)を定めるために、かつエッチングの望ましくない副作用を取り除くために実用的である。
【0041】
ここで図3aおよび図3bを参照すると、図3aはエッチングされたウエハの側面図を示し、図3bは同じウエハの平面図を示している。上述したように、傾斜した表面30を得るエッチングプロセスが最初に実行される。好ましくは、異方性エッチングプロセスが、通常は含水水酸化カリウムを用いて実行される。このエッチングプロセスは<100>平面が水平であるシリコンウエハ12に作用し、エッチング媒体に耐性のある細長い帯の形態のマスク34が、マスクの下方から出発して54.7度の角度で<111>平面に追従しつつ水平な<100>平面まで下がる下り坂/傾斜の側面を有した「隆起」に似た構造をもたらす。このことは、図3aおよび図3bに模式的に示されている。ピラミッド状の構造の高さは、エッチング、例えばエッチング時間によって定まる。明確に定義されたSi厚みを有するSOIウエハを用いる場合、その高さはきわめて正確に制御することができる。酸化物層がエッチングストップ層として作用するからである。
【0042】
ここで図4a,図4b、および図5a〜図5fを参照すると、図4aはマスク層が設けられたエッチングされるウエハの側面図を示しており、かつ図4bは結果として得られた針の側面図を示している。図5a〜図5fは、異なる構造の針を形成するための異なるマスク構造、および結果として得られる針の構造を示している。図4aから判るように、最終的な構造、すなわち傾斜した先端表面を有した針を画成するために傾斜表面40がパターニングされる。傾斜表面40上に一様な厚みのマスク層42を設けるために、リソグラフィプロセスが用いられる。例えば、最適には、従来の方法(したがって、それ自体は公知)のスプレー技術によるフォトレジストを用いて表面全体がカバーされるようにし、次いで、製造する構造を画成する所望のマスク部だけが硬化44するように光線に露光させる。その後、レジストのうち硬化させなかった残留部分を溶解/洗浄によって除去する。このレジストは、硬化していない部分を取り除く前の状態が図4aに模式的に示されている。
【0043】
次いで、等方性エッチング処理を実行する。好ましい処理は、深堀反応性イオンエッチング(DRIE)である。これにより、結晶面の配向によって結果が左右されることはなく、マスクは突出構造の直立壁を画成する。反対側の傾斜面、すなわち突出構造を生じさせるためにマスキングされる表面は、等方性のDRIEによって傾斜面として残存する。結果として得られる針46は図4bに示されている。図4bにおいては、マスク44は未だ取り除かれていない。
【0044】
図5a〜図5fから判るように、この方法を用いることによって三角形、円形、正方形、楕円形、多角形、その他といった複数の異なる形状の針を形成することができる。図5a〜図5cは、硬化したマスク51、52、53が設けられている隆起を示す平面図である。図5d〜図5eには、結果として得られたニードルの側面図が示されているが、傾斜した先端部を有する三角形の針54が図5dに、傾斜した先端部を有する菱形の針55が図5eに、かつ傾斜した先端部を有する円形の針が図5fに示されている。
【0045】
上述した方法の他の実施形態においては、斜めに形付けられた先端部を有する突出構造を作るための出発基板は、上述した突出する「隆起」の代わりにウエハにV字形の凹部60を有している。図6aを参照されたい。
【0046】
これらの凹部は、レジストに細長いスリットを残すべく、第1実施形態のマスクとは「反対に」出発ウエハをマスキングすることによって製作される。その後、このマスキングされたウエハは、非等方性のエッチング、例えばスリットを介して感光したウエハの材料に選択的に作用する水酸化カリウムエッチングを受け、その傾斜面が結晶性のウエハの<111>平面に対応するV溝60を生じさせる。今や複数のV溝を有しているウエハは、上述した実施形態と同様に、適切には一様な層のレジストを達成するためにその上に噴霧されるレジストを用いることによって適切にマスクされ、第1実施形態に類似した所望の構造の形状が画成される。図6aには、所望の針を画成する硬化したマスク部分62が示されている。次にDRIEエッチングを行うと、それによってウエハ材料がエッチングされ、垂直に突出する構造、例えば針64が形成される。
【0047】
上述したSOIウエハアプローチを用いる代わりの製造プロセスは、Silex ABの名で本出願と同日に出願されて係属中のスウェーデン国特許出願(発明の名称:「マイクロニードルおよび用途」)の主題である。また、上述した製造方法のさらなる詳細は、Silex ABの名で本出願と同日に出願されて係属中のスウェーデン国特許出願(発明の名称:「マイクロニードルおよび用途」)の主題である。
【0048】
ここで図7a〜図7dを参照すると、本発明の電極が設けられている着脱自在なキャップを有したプローブの実施形態が示されている。このプローブは多数の、少なくとも3つの電極を有しており、かつ各電極は突出表面、すなわち図1および図2を参照して上述したマイクロニードルの配列が設けられた表面を有していて、様々な皮膚深さでの測定が可能となっている。図7aに示した実施形態において、このプローブは3つの矩形の領域あるいは棒を有しているが、各棒は57本(19×3)の針の配列を具備している。しかしながら、当業者が理解するように、このプローブは、他の配列構造、例えば51本(17×3)、24本(2×12)、60本(12×5)、あるいは39本(13×3)の針を具備する他の構造の棒あるいは領域を有することができる。図7b〜図7dには、着脱自在な電極キャップが如何にしてプローブに取り付けられるかが示されている。これより、被験者に対する測定が実行された後には、電極を具備しているキャップを取り除いて廃棄するとともに、新しいキャップをプローブに取り付けることができるから、衛生的な状態でテストを行うことができる。
【0049】
図8aには図7a〜図7dに示したプローブの断面図が示されており、かつ図8bは図8a中のうち円で囲まれている部分Cの拡大図である。プローブ80は、好ましくは鋼あるいは他の耐久性のある材料のような金属から製造されたハウジング81を備えるが、それはまた、使用の間、例えばオペレータが被験者の皮膚に電極を押圧する測定の間に、ハンドルあるいはシャフトとして機能する。図7b〜図7dに示されている着脱自在なキャップ82は、プローブ80の端部に着脱自在に取り付けることができる。好ましくは、キャップ82は合成樹脂のような材料から製造されて、プローブのユーザがこのキャップ82をハウジング81の先端に螺合させることができるようにしている。着脱自在なキャップ82には、ベース基板86上に構成された電極83a〜83cが設けられている。この実施形態においては、57本(19×3)のマイクロニードルの配列をそれぞれ具備している3つ電極83a〜83cがキャップ82上に設けられている。キャップ82は、衛生上の理由から使い捨てとなっている。さらにまた、図8bから判るように、このキャップ82が有している接続手段84の電極、この場合は6つの電極は、このキャップ82をプローブ80に完全に取り付けたときに、プローブ80のハウジング81内に配置されている対応する接続手段85が有している電極、この場合は6つの電極と接触するように構成されている。それによって、キャップ82の電極83a〜83cに電流を供給することができる。
【0050】
図8aおよび図8bにおいて、電極83a〜83cは矩形の棒として製作されているが、この分野の当業者が理解するように、基本的な機能と両立する他の位相幾何学的な形状もまた考えられる。例えば電極はC字形あるいは同軸に設計することができる。ガード、信号アース、ドリブンガード(driven guard)他を支持する追加の電極も設けることができる。電磁干渉を最小化するために、確立されたエンジニアリング方式に基づいてケーブルおよびシースを構成することができる。さらに、現地の安全規則に適合するように設計することができる。
【0051】
上述したように、マイクロニードルは、互いに横方向に間隔を空けて配置されるとともに、角質層を貫通するのに十分な長さを有している。プローブは被験者の皮膚表面への配置に適するように構成され、マイクロニードルが角質層を貫通する。好ましくは、インピーダンスを測定する前に、例えば0.9%の食塩液を用いて皮膚表面部位を濡らす。この部位は、測定の前に、例えば60秒にわたって濡らすことができる。
【0052】
本発明の装置は、皮膚インピーダンスの値のスペクトル/範囲を得るために電極を介して電流を通過させるとともに、得られたインピーダンス値が病気にかかった状態を示すかどうかを決定するために参照データを用いるのに適している。電流の周波数は、約10Hz〜約10MHzである。
【0053】
マイクロニードル化されたプローブのない装置は、ストックホルム(スウェーデン)のSciBase ABから入手することができる、SciBase II深さ選択スペクトロメータとして公知である。接続されるプローブのためのピン割当ては、以下の通りとすることができる。
1. スタートボタン
2. 検出(同軸(従来のプローブ)なスクリーン3を用いる、図8bに参照符号83aで示されている第1電極用)
3. アース(検出用)
4. 近位側エキサイタ(同軸(従来のプローブ)なスクリーン5を用いる、図8bに参照符号83cで示されている第2(中間)電極用)
5. アース(近位側の注入点用)
6. アース
7. 遠位側エキサイタ(同軸(従来のプローブ)なスクリーン8を用いる、図8bに参照符号83bで示されている第3(最も右側の)電極用)。
8. 接地(遠位側の注入点用)。
9. シャシー
10. 予備
11. 予備
12. アース
13. アース
14. 充電器
【0054】
好ましくは、インピーダンスは、SciBase II深さ選択測定スペクトロメータを用いて1kHzから2.5 MHzまで対数的に35分配された周波数で、5つの深さ設定において測定される。この実施形態においては、1デカードにつき10の周波数を用いる。
【0055】
この信号は、電圧駆動信号であり、かつ人間の生きている細胞の静止電位である約70mVを下回る0〜50mV平方2乗平均の信号強度を有する。
【0056】
各マイクロニードルの長さは、少なくとも20、あるいは少なくとも30、あるいは少なくとも40、あるいは少なくとも50、あるいは少なくとも60、あるいは少なくとも70、あるいは少なくとも80、あるいは少なくとも90マイクロメートルとすることができる。加えて、各マイクロニードルの長さは、最長250、あるいは最長240、あるいは最長230、あるいは最長220、あるいは最長210、あるいは最長200、あるいは最長190、あるいは最長180、あるいは最長170、あるいは最長160、あるいは最長150、あるいは最長140、あるいは最長130、あるいは最長100マイクロメートルとすることができる。
【0057】
他の実施形態においては、各マイクロニードルは約30マイクロメートルの厚みを有する。
【0058】
本発明のプローブは3つの電極を備えており、第1および第2の電極は互いに第1の距離を空けて配置され、第1および第3の電極は互いに第2の距離を空けて配置されている。これは図8bに示されているが、検出電極83aは、近位側エキサイタ電極83cおよび遠位側エキサイタ電極83bに対し間隔を空けて配置されている。第1の距離および第2距離は互いに異なっている。第1の距離は約0.1mm〜約40mmの間であり、第2の距離は約1mm〜約50mmの間である。この装置は、第1および第2の皮膚インピーダンスの値を得るために、第1および第2の電極の間と第1および第3の電極の間の電位との比率を徐々にあるいは段階的に変化させるように構成されている。具体的には、第1の距離は、約0.1mm〜約40mm、あるいは約0.1mm〜約30mm、あるいは約0.1mm〜約25mm、あるいは約0.1mm〜約20mm、あるいは約0.1mm〜約15mm、あるいは約0.2mm〜約10mm、あるいは約0.2mm〜約5mm、あるいは約0.2mm〜約3mm、あるいは約0.2mm〜約2mm、あるいは約0.2mm〜約1.5mm、あるいは約0.2mm〜約1mm、あるいは約0.2mm〜約0.5mmである。加えて、第2の距離は約1mm〜約50mm、あるいは約1mm〜約40mm、あるいは約1mm〜約30mm、あるいは約1mm〜約15mm、あるいは約1mm〜約10mm、あるいは約1mm〜約9mm、あるいは約1mm〜約8mm、あるいは約1mm〜約7mm、あるいは約2mm〜約8mm、あるいは約3mm〜約7mm、あるいは約4mm〜約7mm、あるいは約4mm〜約6mm、あるいは約5mmである。
【0059】
さらにまた、各電極は、少なくとも2つのマイクロニードル、あるいは少なくとも3本のマイクロニードル、あるいは少なくとも4本のマイクロニードル、あるいは少なくとも5本のマイクロニードル、あるいは少なくとも6本のマイクロニードル、あるいは少なくとも7本のマイクロニードル、あるいは少なくとも8本のマイクロニードル、あるいは少なくとも9本のマイクロニードル、あるいは少なくとも10本のマイクロニードル、あるいは少なくとも12本のマイクロニードル、あるいは少なくとも15本のマイクロニードル、あるいは少なくとも18本のマイクロニードル、あるいは少なくとも20本のマイクロニードル、あるいは少なくとも25本のマイクロニードル、あるいは少なくとも30本のマイクロニードル、あるいは少なくとも35本のマイクロニードル、あるいは少なくとも50本のマイクロニードルを具備することができる。上述したように、図7および図8に示したプローブは3つの矩形の領域あるいは棒を有しており、かつ各棒は57本(19×3)のマイクロニードルの配列を具備しているが、当業者が理解するように、多数の他の配列構造、例えば39本(13×3)、45本(15×3)、24本(12×2)、48本(4×12)、65本(13×5)あるいは、51本(17×3)のマイクロニードルの配列もまた考え得る。他の実施形態においては、マイクロニードルは非直線状に配列される。また、1列のマイクロニードルだけを具備している電極もまた考え得る。本発明によるプローブを用いた基底細胞癌あるいは悪性黒色腫を病んでいる被験者のインピーダンス測定は、通常の(正常な)皮膚の第1部位、および病気にかかっている皮膚の第2の部位において、Emtestam I, Nicander I, Stenstr[delta]m M, Ollmar S. "Electrical impedance of nodular basal cell carcinoma: a pilot study", Dermatology 1998; 197: 313-316、およびKapoor S. "Bioelectric impedance techniques for clinical detection of skin cancer using simple electrical impedance indices", Skin Res Technol 2003; 9: 257-261、およびBeetner DG, Kapoor S, Manjunath S, Zhou X, Stoecker WV "Differentation among basal cell carcinoma, benign lesions, and normal skin using electric impedance", IEEE Trans Biomed Eng 2003; 50: 1020-1025に記載されているアプローチに基づいて実行することができる。しかしながら、これらの参考文献に記載されている測定は、従来のプローブおよびインピーダンススペクトロメータの早期のバージョンを用いて得られたものである。
【0060】
図9aおよび図9bには、図1aおよび図1bを参照して説明した実施形態に基づいて設計された、すなわち三角形断面のマイクロニードルを具備するプローブを用いて実行された、基礎細胞癌を病んでいる被験者の測定の結果が示されている。図9aには通常の(正常な)皮膚の第1部位、すなわち参照部位における測定が、また図9bには病気にかかっている皮膚の第2部位の測定結果が、それぞれ示されている。これらの図から判るように、正常な皮膚の部位で実行した測定結果と病気にかかった皮膚の部位で実行した測定結果との間には、位相および大きさの両方において、インピーダンスにかなりのずれがある。
【0061】
皮膚癌は、できるだけ早く発見して取り除くことが望ましい。このように、外科手術および検体の組織学的な評価がなされない限り様々な癌と混同され得る他の病変ばかりでなく、例えば光化学作用性角質繊維(扁平上皮癌の前駆体)および形成異常性母斑(悪性黒色腫の前駆体)といった皮膚癌の前駆体も、本発明のインピーダンス測定を用いて本願明細書に説明した方法で検出することができる。
【0062】
加えて、本発明は、例えば被験者の皮膚の性質の変化、あるいは被験者の組織の性質の変化といった、生物学的な状態の測定、監視、検出のために用いられることができる。さらに、本発明はまた、腎臓のような臓器の組織の生物学的な状態の測定、監視、検出のために用いることができる。
【0063】
本発明の例示的な実施形態を示しかつ説明してきたが、本願明細書に記載したように本発明に対し多くの変更、修正あるいは改造をなし得ることは当業者には明らかである。したがって、本発明の上記の説明および添付した図面が非限定的な実例であり、かつ保護の範囲は添付された請求の範囲によって定められることは理解されるべきである。
【図面の簡単な説明】
【0064】
【図1a】本発明の電極に用いるマイクロニードルの一実施形態を模式的に示す側面図。
【図1b】本発明の電極に用いる図1aに示したマイクロニードルを模式的に示す平面図。
【図2a】本発明の電極に用いるマイクロニードルの他の実施形態を模式的に示す側面図。
【図2b】本発明の電極に用いる図2aに示したマイクロニードルを模式的に示す平面図。
【図3a】本発明のマイクロニードルの一実施形態を製造する間におけるエッチングされたウエハを模式的に示す側面図。
【図3b】本発明のマイクロニードルを製造する間における図3aのエッチングされたウエハを模式的に示す平面図。
【図4a】マスク層が設けられているエッチングされたウエハを模式的に示す側面図。
【図4b】図4aのマスク層から生じたニードルを模式的に示す側面図。
【図5a】第1のマスク構造によってもたらされる、異方性エッチングプロセスによって製造された隆起を模式的に示す平面図。
【図5b】第2のマスク構造によってもたらされる、異方性エッチングプロセスによって製造された隆起を模式的に示す平面図。
【図5c】第3のマスク構造によって提供される、異方性エッチングプロセスによって製造された隆起を模式的に示す平面図。
【図5d】第1のマスク構造によって得られたニードルを模式的に示す側面図。
【図5e】第2のマスク構造によって得られたニードルを模式的に示す側面図。
【図5f】第3のマスク構造によって得られたニードルを模式的に示す側面図。
【図6a】マスク層によってもたらされるエッチングされたウエハを模式的に示す側面図。
【図6b】図6aのマスク層から生じたニードルを模式的に示す側面図。
【図7a】着脱自在のキャップ上に配列された、本発明のマイクロニードルを具備する電極を有したプローブの一実施形態を示す図。
【図7b】本発明のマイクロニードルを具備した電極を有する着脱自在なキャップを、図7aに示したプローブ上に取り付ける手順を示す図。
【図7c】本発明のマイクロニードルを具備した電極を有する着脱自在のキャップを、図7aに示したプローブ上に示す取り付ける手順を示す図。
【図7d】本発明のマイクロニードルを具備した電極を有する着脱自在なキャップを、図7aに示したプローブ上に取り付けるための手順を示す図。
【図8a】本発明のマイクロニードルを具備した、着脱自在なキャップ上に設けられている電極を備えるプローブの断面図。
【図8b】図8aに示されているキャップを拡大して示す断面図。
【図9a】通常の皮膚(健康な皮膚)の第1の部位、すなわち参照部位において本発明のプローブを用いた測定によって得られた結果を示す図。
【図9b】病気にかかった皮膚の第2の部位において、本発明のプローブを用いた測定によって得られた結果を示す図。
【技術分野】
【0001】
本発明は、全般的に生物学的な状態を診断する分野に関し、より詳しくは、医療装置、そのような装置に用いる電極、そのような電極に用いるミクロ構造、および被検者の皮膚の病状、特に皮膚癌、例えば基底細胞癌、悪性黒色腫、扁平上皮癌あるいはその前駆体の存在を皮膚インピーダンス測定値を用いて非侵襲的に診断する方法に関する。
【背景技術】
【0002】
基底細胞癌(BCC)は、最も一般的な皮膚癌である。その発生率は、世界中の多くの国、例えばスウェーデンにおいて増加している。例えば同種異系の臓器を移植した後における長期の免疫抑制は、BCCおよび他の皮膚腫瘍の発症リスクを増大させる。このことは、紫外線光あるいは電離性放射線を浴びた後にも当てはまる。遺伝との明白な関連性はないと思われ、多くの患者においては他のいかなる素因も見い出されない。しかしながら、特に色素が沈着した病変の場合には、経験を積んだ皮膚科医でさえも皮膚の腫瘍の臨床的診断は困難である。診療所においては、経験を積んだ肉眼と組織学的検査のための皮膚生検法との組み合わせに加えて、さらに診断を補助するものが必要である。
【0003】
皮膚腫瘍の臨床的診断のような生物学的な判定は、検体採取を伴う侵襲性の技術よりも優れている非侵襲性の方法で行うことが一般的には望ましい。非侵襲性の技術はより便利であり、例えば痛みがより少なく、感染のリスクもより低い。したがって、生物学的な判定を行うための多くの非侵襲性の技術が提案されてきた。
【0004】
米国特許第5,036,861号、1991年8月6日、Sembrowich他。
米国特許第5,115,133号、1992年5月19日、Knudson。
米国特許第5,146,091号、1992年9月8日、Knudson。
米国特許第5,197,951号、1993年1月19日、Knudson。
米国特許第5,222,496号、1993年6月29日、Clarke他。
PCT/US94/08816、国際特許公開WO95/04496号公報、1995年2月16日、 Solid State Farms。
米国特許第5,433,197号、1995年7月18日、Stark。
PCT/US97/13267、国際特許公開WO98/04190号公報、1998年2月5日、 Dermal Therapy (Barbados) Inc.。
PCT/US98/02037、国際特許公開WO99/39627号公報、1999年8月12日、Dermal Therapy (Barbados) Inc.。
PCT/IB00/01464、国際特許公開WO01/26338号公報、2000年10月13日、Sesstrunk他。
【0005】
しかしながら、上述した文献の全てが、血液のブドウ糖レベルを評価する技術を開示している。したがって、被検者の皮膚の病状、特に皮膚癌、例えば基底細胞癌の存在の診断には適していない。
【0006】
電気インピーダンスは、生体および生物学的な物質、特に粘膜、皮膚および臓器の皮膜のような組織における微細な変化のきわめて高感度な表示手段を構成し、したがって組織の構造的な特性の変化を非侵襲的に測定するための効果的な手段を提供することが判明してきている。PCT/SE91/00703には、同軸なリングシステムに配列された多くの電極を具備する測定用電極を備えた、生体および生物学的な物質の電気インピーダンスを非侵襲的に測定するための装置が開示されている。これらの電極は、検査を受ける実際の組織を決める電流の経路が制御信号によって定まるように、制御ユニットによって駆動される。この制御信号を変化させることにより、検査する領域を選択することができる。2つのリングが電圧を供給し、2つのリングの間の関係が2つのリングの間に配置される仮想的な注入点を生じさせる。2つの注入点の間の電圧関係を調整することによって仮想注入点を前後に移動させることができ、したがって組織の貫通深さを選択することができる。しかしながら、人間の皮膚は複雑で不均質かつ異方性の多層構造であり、電子的に非線形な特性を有している。最も非線形な特性は角質層(表皮の最外側層)に位置している。したがって、その深さが高度に関連しているにもかかわらず、2つの深さからの補間あるいは外挿によって計算することができない情報が全ての深さに存在している。しかしながら、PCT/SE91/00703に開示されている装置には、例えば皮膚癌およびアレルギー反応が現れる角質層の下側の皮膚層における組織の変化について、信頼性の高い結果を供給することができないという大きな弱点がある。このことは、皮膚の非侵襲的な電気インピーダンスのスペクトルが、特に低い周波数において角質層の誘電特性によって支配されるという事実に起因している。角質層は、その下に横たわっている生体皮膚層からの反応が角質層からの反応と混乱して生体皮膚からの臨床関連情報を弱める、(広くα分散と呼ばれている)特性を有している。このことは、PCT/SE91/00703に開示されている測定用電極を用いた角質層の下に現れる電気インピーダンス現象の評価を、困難かつ予測不能なものとしている。
【0007】
国際特許公開WO01/52731号公報は、電気的な生体電位が生きている被検者の身体内部で作り出されていることを検出するための医用電極を開示している。この電極は、皮膚を貫通するように構成された多くのマイクロニードルを有している。これらのマイクロニードルは、胚芽層に到達するために充分に長く、それらの表面上において導電性であり、かつ互いに接続されて配列を形成している。国際特許公開WO01/52731号公報によると、このマイクロニードルは「釘」に似ている。すなわち、それらは一定のあるいは徐々に減少する直径を有した実質的に円形の断面を有したステムと、実質的に球形あるいは針状の先端を有した先端部とを有している。欧州特許公開1437091号公報には、生体および生物学的な物質のインピーダンス測定を用いる、生物学的な状態を診断するための装置が開示されている。この装置は、複数の電極を有したプローブを備えているが、角質層を貫通するのに十分な長さをそれぞれ有した多数のマイクロニードルが各電極に設けられている。欧州特許公開1437091号公報のマイクロニードルもまた「釘」に似ている。すなわち、それらは、一定のあるいは徐々に減少する直径を具備した実質的に円形の断面を有するステムと、実質的に球形あるいは針状の先端を有した先端部とを有している。
【0008】
しかしながら、実際的な試験は、従来技術のマイクロニードルを有した電極が、そのマイクロニードルを胚芽層内に適切に貫通させるために相当の力、あるいは電極を前後に傾けるといったかなりの操作を必要とすることを示した。このことは、テストを実行するオペレータ、例えば医師あるいは看護婦ばかりでなく、患者にとっても不快でありかつ煩わしい。さらに、このことはまた、使用の間にニードルが破損する可能性を回避するために、例えばその寸法を増すことによってニードルが充分な強度を有するように設計されることを必要とする。
【0009】
したがって、非侵襲的に被検者の皮膚の病状、特に皮膚癌、例えば基底細胞癌、悪性黒色腫、扁平上皮癌あるいはその前駆体の存在を診断するための、改善された医療電極、装置の必要性が存在する。
【発明の開示】
【発明が解決しようとする課題】
【0010】
したがって、本発明の目的は、改良された装置、そのような装置に用いる電極装置、そのような電極に用いるミクロ構造、および被検者の皮膚の病状、特に皮膚癌、例えば基底細胞癌、悪性黒色腫、扁平上皮癌あるいはその前駆体の存在を正確にかつ高い信頼性で診断する方法を提供することにある。
【0011】
本発明の他の目的は、良好な貫通能力を具備したマイクロニードルを有する、被験者の皮膚の病状を診断するための改良された装置、およびそのような装置のためのプローブを提供することにある。
【0012】
本発明のさらなる目的は、高い構造強度のマイクロニードルを有する、被験者の皮膚の病状を診断するための改良された装置、およびそのような装置のためのプローブを提供することにある。
【0013】
本発明のさらに他の目的は、電気的な特性が良好なマイクロニードルを有する、被験者の皮膚の病状を診断するための改良された装置、およびそのような装置のためのプローブを提供することにある。
【0014】
本発明のさらに別の目的は、被験者の皮膚の病状を診断する装置およびそのような装置に用いるプローブのための、効率が高くかつ信頼できる方法で製造することができるマイクロニードルを提供することにある。
【0015】
これらのおよび他の目的は、独立請求項に定められている機能を有した医療装置および方法を提供する本発明によって達成される。本発明の好ましい実施形態は、従属請求項にその特徴が表されている。
【課題を解決するための手段】
【0016】
本発明の一態様によると、被験者の皮膚の病状を診断するための医療装置であって、複数の電極を有している導電性のプローブを備え、各電極は複数のマイクロニードルを具備しており、前記プローブは、前記マイクロニードルが角質層を貫通するように被験者の表面に対して配置されるようになっており、前記医療装置は、皮膚インピーダンス値を得るために電極に電流を通すことを含むインピーダンス測定セッションを開始するように構成されるとともに、得られたインピーダンス値が病気にかかった状態を示すかどうかを決定するために参照データを用いる、医療装置が提供される。各電極はベース基板を有しており、前記マイクロニードルは、前記基板と一体的に形成されるとともに、互いに横方向に間隔を空けた関係に配置され、かつ角質層を貫通するのに十分な長さを有しており、前記マイクロニードルには少なくとも部分的に傾斜した形状が設けられる。
【0017】
本発明の第2の態様によると、被験者の皮膚の病状を診断するべく被験者の皮膚表面に配置されるように構成される、複数のマイクロニードルを具備した電極が提供される。前記電極はベース基板を有しており、前記マイクロニードルは、前記基板と一体的に形成されるとともに、互いに横方向に間隔を空けた関係に配置され、かつ被験者の皮膚表面に配置されたときに角質層を貫通するのに十分な長さを有しており、前記マイクロニードルには少なくとも部分的に傾斜した形状が設けられる。
【0018】
本発明の第3の態様によると、ミクロ構造の配列であって、ベース基板と、同時に形成されてこの基板の表面から突出するマイクロニードルの配列とを備え、前記マイクロニードルは、互いに横方向に間隔を空けた関係に配置され、かつ被験者の皮膚表面に配置されたときに角質層を貫通するのに十分な長さを有しており、前記マイクロニードルに少なくとも部分的に傾斜した形状が設けられているミクロ構造の配列が提供される。
【0019】
本発明のさらに別の態様によると、被験者の皮膚の病状を診断する方法であって、基板と一体的に形成されるとともに、互いに横方向に間隔を空けた関係に配置され、かつ角質層を貫通するのに十分な長さを有しており、さらに少なくとも部分的に傾斜した形状が設けられているマイクロニードルが角質層を貫通するように、被験者の皮膚表面に導電性のプローブを配置する段階と、皮膚のインピーダンス値を得るために電極を介して電流を通過させる段階と、得られたインピーダンス値が病気にかかった状態を示すかどうかを決定するために参照データを用いる段階と、を備える方法が提供される。
【0020】
このように、本発明は、皮膚の非侵襲性の電気インピーダンススペクトルが、特に低い周波数において角質層の誘電特性によって支配されるという知見に基づいている。角質層は、その下に横たわっている生体皮膚層からの反応が角質層からの反応と混乱して生体皮膚からの臨床関連情報を弱める(広くα分散と呼ばれている)特性を有している。より詳しくは、本発明は、高い構造強度、良好な電気的特性(例えば導電性)、および貫通能力を有したマイクロニードルの設計に基礎を置いている。
【0021】
本発明は、いくつかの利点をもたらす。一つの利点は、角質層の下方に現れる電気インピーダンス現象を、本発明を用いることによって信頼できる方法で評価することができることにある。これにより、本発明を用いることによって、被験者の皮膚の病状、特に皮膚癌、例えば基底細胞癌、悪性黒色腫、扁平上皮癌、あるいはその前駆体の存在を、正確かつ信頼できる方法で診断することができる。
【0022】
他の利点は、本発明の電極が角質層を貫通するために必要とする圧力が、従来の電極のそれより少ないことにある。これにより、本発明の電極は、負荷される圧力、したがってオペレータによって左右される度合いが低い。これはまた、従来の電極で実行されるテストに比べると、テストを受ける患者あるいは被験者の不都合をより少ないものとする。
【0023】
さらなる利点は、本発明による電極のマイクロニードルが高い構造強度を有しており、したがってこれらの針には耐久性があることである。
【0024】
さらに他の利点は、本発明によるマイクロニードルが被験者の皮膚と接触する表面を大きくすることができ、針と角質層との間の良好な導電性に結びつき、翻って高い精度および信頼性のインピーダンス測定をもたらすことにある。
【0025】
本発明の一実施形態によると、各マイクロニードルには、少なくとも部分的に傾斜した形状を具備した先端部が設けられる。この特別な設計は、良好な貫通力を有することが見出された。これにより、この電極は負荷される圧力、したがってオペレータによって左右される度合いが低いから、従来の電極で実行されるテストに比べると、テストを受ける被験者の不都合がより少なくなる。
【0026】
さらに他の実施形態においては、マイクロニードルには、少なくとも部分的に傾斜する端面を具備した先端部が設けられる。
【0027】
さらに別の実施形態においては、マイクロニードルはそれぞれ実質的に三角形の断面に構成される。この設計は、高い構造強度および高い貫通能力を有することが見出された。さらに、それは被験者の皮膚に対する大きな接触表面を有する。このことは、針と角質層との間の良好な導電性に結びつき、翻って高い精度および信頼性のインピーダンス測定をもたらす。
【0028】
あるいは、マイクロニードルはそれぞれ、実質的に菱形、正方形に似た形、楕円形、多角形、矩形あるいは円形の断面に構成される。
【0029】
本発明の一実施形態によると、電極の配列は、使い捨て使用のために、プローブ上に着脱自在に取り付けることができるキャップ上に設けられる。これにより、一人の被験者における測定を実行した後に、電極を具備しているキャップを取り外して廃棄し、新しいキャップをプローブに取り付けることができる。したがって、衛生的な状態で測定することができる。
【0030】
一実施形態においては、ベース基板がウエハ要素から形成され、かつマイクロニードルは異方性エッチングプロセス、マスキングプロセス、および基板上の深堀反応性イオンエッチング(DRIE)プロセスの連続的なシーケンスを含むプロセスによって、このウエハ要素から製作される。この製造プロセスは高い構造強度を有したマイクロニードルの配列をもたらすとともに、このプロセスは高い歩留まり率を有する。
【0031】
本発明の他の実施形態によると、第1の電極および第2の電極のマイクロニードルが第1の距離で互いに横方向に間隔を空けて配置され、第1の電極および第3の電極のマイクロニードルが第2の距離で互いに間隔を空けて配置され、第1および第2の電極を用いて得られた値と第1および第3の電極を用いて得られた値との間における、皮膚インピーダンスの第1および第2の値あるいは皮膚インピーダンスの値の混合値を得るために、第1および第2の電極間の電位と第1および第3の電極間の電位との比率は段階的にあるいは徐々に変更される。これにより、測定が実行される深さを、正確かつ信頼できる方法で選択することができる。
【0032】
加えて本発明は、生物学的な状態、例えば被験者の皮膚の特性の変化あるいは被験者の組織の特性の変化を測定し、監視し、検出するために用いることができる。さらに本発明は、腎臓のような臓器の組織の生物学的な状態を測定し、監視し、かつ検出するために用いることができる。
【0033】
本発明の一実施形態によると、電極は矩形の棒として製作される。他の実施形態によると、基本的な機能と両立する他の構造もまた考えることができる。例えばC字形、あるいは同軸に電極を設計することができる。ガード、信号アース、ドリブンガード(driven guard)他を支持する追加の電極を設けることもできる。電磁干渉を最小化するために、確立されたエンジニアリング方式に基づいてケーブルおよびシースを構成することができる。さらに、現地の安全規則に適合するように設計することができる。
【0034】
本発明を特徴づける特色、構成および操作の方法、さらなる目的および利点は、添付の図面と共になされる以下の説明からより良好に理解されるであろう。図面は例証を目的としたものであり、かつ説明が本発明の限界を定めることを意図していないことは、明白に理解されるべきである。本発明によって達成されるこれらの目的および他の目的、もたらされる利点は、以下の説明を添付の図面と共に読むことによって明らかとなる。
【発明を実施するための最良の形態】
【0035】
本発明のプローブは多数の、少なくとも3つの電極を有し、かつ本発明においては各電極に少なくとも一つのマイクロニードルが設けられ、それによってマイクロニードル化された表面が形成されて様々な皮膚深さでの測定を可能にしている。プローブは、3つの矩形の領域あるいは棒を有しており、各棒は57本(19×3)のマイクロニードルの配列を具備している。各棒は、幅が1mmで長さは5mmである。最も近い棒の間の距離は0.2mmであり、かつ第2および第3の棒の間の距離は1.8ミリメートルであるしたがって、プローブの作動部分は約5×5mmである。各マイクロニードルは、そのベース部から測定すると約100マイクロメートルの長さを有しており、かつ約30マイクロメートルの厚みを有している。マイクロニードルは、好ましくはシリコンから製造されるとともに、約2マイクロメートルの厚みの金で覆われている。同程度の寸法を有した導電性表面を構成する任意の材料も機能するが、生体適合性のものが選択されなければならない。このプローブについては、図7a、図7b、図8aおよび図8bを参照して以下に詳述する。
【0036】
ここで、図1a、図1b、図2aおよび図2bを参照し、本発明による、被検者の皮膚の病状を診断するための上述した電極に用いるミクロ構造あるいはマイクロニードルの実施形態について説明する。各電極には配列として構成された複数のそのようなマイクロニードルが設けられているが、明快さのために1本のマイクロニードルについて以下に説明する。実施形態の側面図、すなわちベース基板に対し垂直な平面に沿った実施形態の断面図、および実施形態の平面図、すなわち基板に対し平行な平面に沿った断面図が、それぞれ図1aおよび図1bに示されている。他の実施形態の側面図、すなわち基板に対して垂直な平面に沿った実施形態の断面図、および実施形態の平面図、すなわち基板に対し平行な平面に沿った断面図が、図2aおよび図2bに示されている。
【0037】
上述したように、各プローブには、基板と一体に形成されるとともに、互いに横方向に間隔を空ける関係で配置され、かつ角質層を貫通するのに十分な長さを有している複数のマイクロニードルが設けられている。まず最初に図1aを参照すると、本発明によるそのようなマイクロニードルの一実施形態が、基板に対して垂直な平面に沿って示されている。マイクロニードル10は、例えばSOIタイプのシリコンウエハであるベース基板12上に設けられている。このマイクロニードル10には、傾斜した先端部14あるいは少なくとも部分的に斜め形状の先端部が設けられている。この先端部14、すなわち斜めの表面は、マイクロニードル10の一部を構成している。図1bには、矢印B方向の平面図が、、図1a中のA−A破断線で示されている、すなわちマイクロニードル10の基部における、基板12に対して実質的に平行な平面に沿った断面で示されている。この図から判るように、マイクロニードル10はこの平面においては三角形の断面を有している。マイクロニードルの寸法b1およびs1は高さh1に沿って実質的に一定であり、かつベース基板12の表面から高さh2−h1に沿った方向において連続的にテーパ状である。ここで留意されるべきことは、基板12の一部だけが図1bに示されていることである。図1aおよび図1bの実施形態の寸法は、以下の表1に示されている。図2aおよび図2bを参照すると、本発明のマイクロニードルの他の実施形態が、基板に対して垂直な平面に沿って示されている。マイクロニードル20は、例えばSOIタイプのシリコンウエハであるベース基板12上に配置されている。このマイクロニードル20には、傾斜した先端部24あるいは斜め形状の先端部が設けられている。この実施形態においては、先端部24がベース基板12に向けて延びている。図2bには、矢印B方向の平面図が、図2a中のA−A破断線で示されている、すなわちマイクロニードル10の基部における、基板12に対して実質的に平行な平面に沿った断面で示されている。この図から判るように、マイクロニードル20はこの平面においては三角形の断面を有している。この場合、基板12に対し平行な断面は、ベース基板12の表面から離れる方向において連続的にテーパ状である。ここで留意されるべきことは、基板12の一部だけが図2bに示されていることである。図2aおよび図2bの実施形態の寸法もまた、以下の表1に示されている。例えば、図2aおよび図2bに示されている実施形態においては、h1は実質的にゼロである。
【表1】

【0038】
シリコンウエハの平面から延びるマイクロニードルの製造は周知である。例えば、米国特許公開2004/0243063号公報、"Microneedle array module and method for fabricating the same", Shuvo R., and Aaron J. F.、および米国特許第6,334,865号、"Microneedle devices and methods for manufacture and use thereof, Allen M. G., et al.を参照されたい。
【0039】
本発明のマイクロニードルの配列は、ウエハ(基板)から形成することができる。このとき、傾斜した表面がエッチングプロセスによって基板上に設けられ、かつ(フォトレジストを用いたリソグラフィのような)適切なパターニングプロセスを用いてこの傾斜した表面上にマスクが設けられる。次いで、ニードルの構造は、第2のエッチングプロセスによって所望の構造に形成される。この傾斜した表面は、針の先端に斜めの端面を有したニードルの製造を可能にする。
【0040】
このウエハに似た基板は、<100>、<110>等の結晶方向/配向を呈する表面を有した単一結晶シリコンとすることができる。しかしながら、同一あるいは同程度の処理技術を受けることができる他の結晶性物質もまた適している。より詳しくは、有用な出発基板はいわゆるSOIウエハ(Silicon On Insulator)である。SOIウエハが明瞭なエッチングストップ層を提供するからである。そのようなストップ層は、製作する構造の寸法(すなわち高さ、幅、凹所の深さ等)を定めるために、かつエッチングの望ましくない副作用を取り除くために実用的である。
【0041】
ここで図3aおよび図3bを参照すると、図3aはエッチングされたウエハの側面図を示し、図3bは同じウエハの平面図を示している。上述したように、傾斜した表面30を得るエッチングプロセスが最初に実行される。好ましくは、異方性エッチングプロセスが、通常は含水水酸化カリウムを用いて実行される。このエッチングプロセスは<100>平面が水平であるシリコンウエハ12に作用し、エッチング媒体に耐性のある細長い帯の形態のマスク34が、マスクの下方から出発して54.7度の角度で<111>平面に追従しつつ水平な<100>平面まで下がる下り坂/傾斜の側面を有した「隆起」に似た構造をもたらす。このことは、図3aおよび図3bに模式的に示されている。ピラミッド状の構造の高さは、エッチング、例えばエッチング時間によって定まる。明確に定義されたSi厚みを有するSOIウエハを用いる場合、その高さはきわめて正確に制御することができる。酸化物層がエッチングストップ層として作用するからである。
【0042】
ここで図4a,図4b、および図5a〜図5fを参照すると、図4aはマスク層が設けられたエッチングされるウエハの側面図を示しており、かつ図4bは結果として得られた針の側面図を示している。図5a〜図5fは、異なる構造の針を形成するための異なるマスク構造、および結果として得られる針の構造を示している。図4aから判るように、最終的な構造、すなわち傾斜した先端表面を有した針を画成するために傾斜表面40がパターニングされる。傾斜表面40上に一様な厚みのマスク層42を設けるために、リソグラフィプロセスが用いられる。例えば、最適には、従来の方法(したがって、それ自体は公知)のスプレー技術によるフォトレジストを用いて表面全体がカバーされるようにし、次いで、製造する構造を画成する所望のマスク部だけが硬化44するように光線に露光させる。その後、レジストのうち硬化させなかった残留部分を溶解/洗浄によって除去する。このレジストは、硬化していない部分を取り除く前の状態が図4aに模式的に示されている。
【0043】
次いで、等方性エッチング処理を実行する。好ましい処理は、深堀反応性イオンエッチング(DRIE)である。これにより、結晶面の配向によって結果が左右されることはなく、マスクは突出構造の直立壁を画成する。反対側の傾斜面、すなわち突出構造を生じさせるためにマスキングされる表面は、等方性のDRIEによって傾斜面として残存する。結果として得られる針46は図4bに示されている。図4bにおいては、マスク44は未だ取り除かれていない。
【0044】
図5a〜図5fから判るように、この方法を用いることによって三角形、円形、正方形、楕円形、多角形、その他といった複数の異なる形状の針を形成することができる。図5a〜図5cは、硬化したマスク51、52、53が設けられている隆起を示す平面図である。図5d〜図5eには、結果として得られたニードルの側面図が示されているが、傾斜した先端部を有する三角形の針54が図5dに、傾斜した先端部を有する菱形の針55が図5eに、かつ傾斜した先端部を有する円形の針が図5fに示されている。
【0045】
上述した方法の他の実施形態においては、斜めに形付けられた先端部を有する突出構造を作るための出発基板は、上述した突出する「隆起」の代わりにウエハにV字形の凹部60を有している。図6aを参照されたい。
【0046】
これらの凹部は、レジストに細長いスリットを残すべく、第1実施形態のマスクとは「反対に」出発ウエハをマスキングすることによって製作される。その後、このマスキングされたウエハは、非等方性のエッチング、例えばスリットを介して感光したウエハの材料に選択的に作用する水酸化カリウムエッチングを受け、その傾斜面が結晶性のウエハの<111>平面に対応するV溝60を生じさせる。今や複数のV溝を有しているウエハは、上述した実施形態と同様に、適切には一様な層のレジストを達成するためにその上に噴霧されるレジストを用いることによって適切にマスクされ、第1実施形態に類似した所望の構造の形状が画成される。図6aには、所望の針を画成する硬化したマスク部分62が示されている。次にDRIEエッチングを行うと、それによってウエハ材料がエッチングされ、垂直に突出する構造、例えば針64が形成される。
【0047】
上述したSOIウエハアプローチを用いる代わりの製造プロセスは、Silex ABの名で本出願と同日に出願されて係属中のスウェーデン国特許出願(発明の名称:「マイクロニードルおよび用途」)の主題である。また、上述した製造方法のさらなる詳細は、Silex ABの名で本出願と同日に出願されて係属中のスウェーデン国特許出願(発明の名称:「マイクロニードルおよび用途」)の主題である。
【0048】
ここで図7a〜図7dを参照すると、本発明の電極が設けられている着脱自在なキャップを有したプローブの実施形態が示されている。このプローブは多数の、少なくとも3つの電極を有しており、かつ各電極は突出表面、すなわち図1および図2を参照して上述したマイクロニードルの配列が設けられた表面を有していて、様々な皮膚深さでの測定が可能となっている。図7aに示した実施形態において、このプローブは3つの矩形の領域あるいは棒を有しているが、各棒は57本(19×3)の針の配列を具備している。しかしながら、当業者が理解するように、このプローブは、他の配列構造、例えば51本(17×3)、24本(2×12)、60本(12×5)、あるいは39本(13×3)の針を具備する他の構造の棒あるいは領域を有することができる。図7b〜図7dには、着脱自在な電極キャップが如何にしてプローブに取り付けられるかが示されている。これより、被験者に対する測定が実行された後には、電極を具備しているキャップを取り除いて廃棄するとともに、新しいキャップをプローブに取り付けることができるから、衛生的な状態でテストを行うことができる。
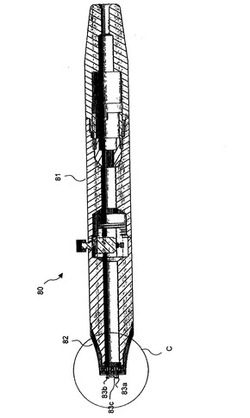
【0049】
図8aには図7a〜図7dに示したプローブの断面図が示されており、かつ図8bは図8a中のうち円で囲まれている部分Cの拡大図である。プローブ80は、好ましくは鋼あるいは他の耐久性のある材料のような金属から製造されたハウジング81を備えるが、それはまた、使用の間、例えばオペレータが被験者の皮膚に電極を押圧する測定の間に、ハンドルあるいはシャフトとして機能する。図7b〜図7dに示されている着脱自在なキャップ82は、プローブ80の端部に着脱自在に取り付けることができる。好ましくは、キャップ82は合成樹脂のような材料から製造されて、プローブのユーザがこのキャップ82をハウジング81の先端に螺合させることができるようにしている。着脱自在なキャップ82には、ベース基板86上に構成された電極83a〜83cが設けられている。この実施形態においては、57本(19×3)のマイクロニードルの配列をそれぞれ具備している3つ電極83a〜83cがキャップ82上に設けられている。キャップ82は、衛生上の理由から使い捨てとなっている。さらにまた、図8bから判るように、このキャップ82が有している接続手段84の電極、この場合は6つの電極は、このキャップ82をプローブ80に完全に取り付けたときに、プローブ80のハウジング81内に配置されている対応する接続手段85が有している電極、この場合は6つの電極と接触するように構成されている。それによって、キャップ82の電極83a〜83cに電流を供給することができる。
【0050】
図8aおよび図8bにおいて、電極83a〜83cは矩形の棒として製作されているが、この分野の当業者が理解するように、基本的な機能と両立する他の位相幾何学的な形状もまた考えられる。例えば電極はC字形あるいは同軸に設計することができる。ガード、信号アース、ドリブンガード(driven guard)他を支持する追加の電極も設けることができる。電磁干渉を最小化するために、確立されたエンジニアリング方式に基づいてケーブルおよびシースを構成することができる。さらに、現地の安全規則に適合するように設計することができる。
【0051】
上述したように、マイクロニードルは、互いに横方向に間隔を空けて配置されるとともに、角質層を貫通するのに十分な長さを有している。プローブは被験者の皮膚表面への配置に適するように構成され、マイクロニードルが角質層を貫通する。好ましくは、インピーダンスを測定する前に、例えば0.9%の食塩液を用いて皮膚表面部位を濡らす。この部位は、測定の前に、例えば60秒にわたって濡らすことができる。
【0052】
本発明の装置は、皮膚インピーダンスの値のスペクトル/範囲を得るために電極を介して電流を通過させるとともに、得られたインピーダンス値が病気にかかった状態を示すかどうかを決定するために参照データを用いるのに適している。電流の周波数は、約10Hz〜約10MHzである。
【0053】
マイクロニードル化されたプローブのない装置は、ストックホルム(スウェーデン)のSciBase ABから入手することができる、SciBase II深さ選択スペクトロメータとして公知である。接続されるプローブのためのピン割当ては、以下の通りとすることができる。
1. スタートボタン
2. 検出(同軸(従来のプローブ)なスクリーン3を用いる、図8bに参照符号83aで示されている第1電極用)
3. アース(検出用)
4. 近位側エキサイタ(同軸(従来のプローブ)なスクリーン5を用いる、図8bに参照符号83cで示されている第2(中間)電極用)
5. アース(近位側の注入点用)
6. アース
7. 遠位側エキサイタ(同軸(従来のプローブ)なスクリーン8を用いる、図8bに参照符号83bで示されている第3(最も右側の)電極用)。
8. 接地(遠位側の注入点用)。
9. シャシー
10. 予備
11. 予備
12. アース
13. アース
14. 充電器
【0054】
好ましくは、インピーダンスは、SciBase II深さ選択測定スペクトロメータを用いて1kHzから2.5 MHzまで対数的に35分配された周波数で、5つの深さ設定において測定される。この実施形態においては、1デカードにつき10の周波数を用いる。
【0055】
この信号は、電圧駆動信号であり、かつ人間の生きている細胞の静止電位である約70mVを下回る0〜50mV平方2乗平均の信号強度を有する。
【0056】
各マイクロニードルの長さは、少なくとも20、あるいは少なくとも30、あるいは少なくとも40、あるいは少なくとも50、あるいは少なくとも60、あるいは少なくとも70、あるいは少なくとも80、あるいは少なくとも90マイクロメートルとすることができる。加えて、各マイクロニードルの長さは、最長250、あるいは最長240、あるいは最長230、あるいは最長220、あるいは最長210、あるいは最長200、あるいは最長190、あるいは最長180、あるいは最長170、あるいは最長160、あるいは最長150、あるいは最長140、あるいは最長130、あるいは最長100マイクロメートルとすることができる。
【0057】
他の実施形態においては、各マイクロニードルは約30マイクロメートルの厚みを有する。
【0058】
本発明のプローブは3つの電極を備えており、第1および第2の電極は互いに第1の距離を空けて配置され、第1および第3の電極は互いに第2の距離を空けて配置されている。これは図8bに示されているが、検出電極83aは、近位側エキサイタ電極83cおよび遠位側エキサイタ電極83bに対し間隔を空けて配置されている。第1の距離および第2距離は互いに異なっている。第1の距離は約0.1mm〜約40mmの間であり、第2の距離は約1mm〜約50mmの間である。この装置は、第1および第2の皮膚インピーダンスの値を得るために、第1および第2の電極の間と第1および第3の電極の間の電位との比率を徐々にあるいは段階的に変化させるように構成されている。具体的には、第1の距離は、約0.1mm〜約40mm、あるいは約0.1mm〜約30mm、あるいは約0.1mm〜約25mm、あるいは約0.1mm〜約20mm、あるいは約0.1mm〜約15mm、あるいは約0.2mm〜約10mm、あるいは約0.2mm〜約5mm、あるいは約0.2mm〜約3mm、あるいは約0.2mm〜約2mm、あるいは約0.2mm〜約1.5mm、あるいは約0.2mm〜約1mm、あるいは約0.2mm〜約0.5mmである。加えて、第2の距離は約1mm〜約50mm、あるいは約1mm〜約40mm、あるいは約1mm〜約30mm、あるいは約1mm〜約15mm、あるいは約1mm〜約10mm、あるいは約1mm〜約9mm、あるいは約1mm〜約8mm、あるいは約1mm〜約7mm、あるいは約2mm〜約8mm、あるいは約3mm〜約7mm、あるいは約4mm〜約7mm、あるいは約4mm〜約6mm、あるいは約5mmである。
【0059】
さらにまた、各電極は、少なくとも2つのマイクロニードル、あるいは少なくとも3本のマイクロニードル、あるいは少なくとも4本のマイクロニードル、あるいは少なくとも5本のマイクロニードル、あるいは少なくとも6本のマイクロニードル、あるいは少なくとも7本のマイクロニードル、あるいは少なくとも8本のマイクロニードル、あるいは少なくとも9本のマイクロニードル、あるいは少なくとも10本のマイクロニードル、あるいは少なくとも12本のマイクロニードル、あるいは少なくとも15本のマイクロニードル、あるいは少なくとも18本のマイクロニードル、あるいは少なくとも20本のマイクロニードル、あるいは少なくとも25本のマイクロニードル、あるいは少なくとも30本のマイクロニードル、あるいは少なくとも35本のマイクロニードル、あるいは少なくとも50本のマイクロニードルを具備することができる。上述したように、図7および図8に示したプローブは3つの矩形の領域あるいは棒を有しており、かつ各棒は57本(19×3)のマイクロニードルの配列を具備しているが、当業者が理解するように、多数の他の配列構造、例えば39本(13×3)、45本(15×3)、24本(12×2)、48本(4×12)、65本(13×5)あるいは、51本(17×3)のマイクロニードルの配列もまた考え得る。他の実施形態においては、マイクロニードルは非直線状に配列される。また、1列のマイクロニードルだけを具備している電極もまた考え得る。本発明によるプローブを用いた基底細胞癌あるいは悪性黒色腫を病んでいる被験者のインピーダンス測定は、通常の(正常な)皮膚の第1部位、および病気にかかっている皮膚の第2の部位において、Emtestam I, Nicander I, Stenstr[delta]m M, Ollmar S. "Electrical impedance of nodular basal cell carcinoma: a pilot study", Dermatology 1998; 197: 313-316、およびKapoor S. "Bioelectric impedance techniques for clinical detection of skin cancer using simple electrical impedance indices", Skin Res Technol 2003; 9: 257-261、およびBeetner DG, Kapoor S, Manjunath S, Zhou X, Stoecker WV "Differentation among basal cell carcinoma, benign lesions, and normal skin using electric impedance", IEEE Trans Biomed Eng 2003; 50: 1020-1025に記載されているアプローチに基づいて実行することができる。しかしながら、これらの参考文献に記載されている測定は、従来のプローブおよびインピーダンススペクトロメータの早期のバージョンを用いて得られたものである。
【0060】
図9aおよび図9bには、図1aおよび図1bを参照して説明した実施形態に基づいて設計された、すなわち三角形断面のマイクロニードルを具備するプローブを用いて実行された、基礎細胞癌を病んでいる被験者の測定の結果が示されている。図9aには通常の(正常な)皮膚の第1部位、すなわち参照部位における測定が、また図9bには病気にかかっている皮膚の第2部位の測定結果が、それぞれ示されている。これらの図から判るように、正常な皮膚の部位で実行した測定結果と病気にかかった皮膚の部位で実行した測定結果との間には、位相および大きさの両方において、インピーダンスにかなりのずれがある。
【0061】
皮膚癌は、できるだけ早く発見して取り除くことが望ましい。このように、外科手術および検体の組織学的な評価がなされない限り様々な癌と混同され得る他の病変ばかりでなく、例えば光化学作用性角質繊維(扁平上皮癌の前駆体)および形成異常性母斑(悪性黒色腫の前駆体)といった皮膚癌の前駆体も、本発明のインピーダンス測定を用いて本願明細書に説明した方法で検出することができる。
【0062】
加えて、本発明は、例えば被験者の皮膚の性質の変化、あるいは被験者の組織の性質の変化といった、生物学的な状態の測定、監視、検出のために用いられることができる。さらに、本発明はまた、腎臓のような臓器の組織の生物学的な状態の測定、監視、検出のために用いることができる。
【0063】
本発明の例示的な実施形態を示しかつ説明してきたが、本願明細書に記載したように本発明に対し多くの変更、修正あるいは改造をなし得ることは当業者には明らかである。したがって、本発明の上記の説明および添付した図面が非限定的な実例であり、かつ保護の範囲は添付された請求の範囲によって定められることは理解されるべきである。
【図面の簡単な説明】
【0064】
【図1a】本発明の電極に用いるマイクロニードルの一実施形態を模式的に示す側面図。
【図1b】本発明の電極に用いる図1aに示したマイクロニードルを模式的に示す平面図。
【図2a】本発明の電極に用いるマイクロニードルの他の実施形態を模式的に示す側面図。
【図2b】本発明の電極に用いる図2aに示したマイクロニードルを模式的に示す平面図。
【図3a】本発明のマイクロニードルの一実施形態を製造する間におけるエッチングされたウエハを模式的に示す側面図。
【図3b】本発明のマイクロニードルを製造する間における図3aのエッチングされたウエハを模式的に示す平面図。
【図4a】マスク層が設けられているエッチングされたウエハを模式的に示す側面図。
【図4b】図4aのマスク層から生じたニードルを模式的に示す側面図。
【図5a】第1のマスク構造によってもたらされる、異方性エッチングプロセスによって製造された隆起を模式的に示す平面図。
【図5b】第2のマスク構造によってもたらされる、異方性エッチングプロセスによって製造された隆起を模式的に示す平面図。
【図5c】第3のマスク構造によって提供される、異方性エッチングプロセスによって製造された隆起を模式的に示す平面図。
【図5d】第1のマスク構造によって得られたニードルを模式的に示す側面図。
【図5e】第2のマスク構造によって得られたニードルを模式的に示す側面図。
【図5f】第3のマスク構造によって得られたニードルを模式的に示す側面図。
【図6a】マスク層によってもたらされるエッチングされたウエハを模式的に示す側面図。
【図6b】図6aのマスク層から生じたニードルを模式的に示す側面図。
【図7a】着脱自在のキャップ上に配列された、本発明のマイクロニードルを具備する電極を有したプローブの一実施形態を示す図。
【図7b】本発明のマイクロニードルを具備した電極を有する着脱自在なキャップを、図7aに示したプローブ上に取り付ける手順を示す図。
【図7c】本発明のマイクロニードルを具備した電極を有する着脱自在のキャップを、図7aに示したプローブ上に示す取り付ける手順を示す図。
【図7d】本発明のマイクロニードルを具備した電極を有する着脱自在なキャップを、図7aに示したプローブ上に取り付けるための手順を示す図。
【図8a】本発明のマイクロニードルを具備した、着脱自在なキャップ上に設けられている電極を備えるプローブの断面図。
【図8b】図8aに示されているキャップを拡大して示す断面図。
【図9a】通常の皮膚(健康な皮膚)の第1の部位、すなわち参照部位において本発明のプローブを用いた測定によって得られた結果を示す図。
【図9b】病気にかかった皮膚の第2の部位において、本発明のプローブを用いた測定によって得られた結果を示す図。
【特許請求の範囲】
【請求項1】
被験者の皮膚の病状を診断するための医療装置であって、
複数の電極を有している導電性のプローブを備え、
各電極は複数のマイクロニードルを具備しており、
前記プローブは、前記マイクロニードルが角質層を貫通するように被験者の表面に配置されるようになっており、
前記医療装置は、皮膚インピーダンス値を得るために電極に電流を通すことを含むインピーダンス測定セッションを開始するように構成されるとともに、得られたインピーダンス値が病気にかかった状態を示すかどうかを決定するために参照データを用いる、医療装置において、
各電極はベース基板を有し、
前記マイクロニードルは、前記基板と一体的に形成されるとともに、互いに横方向に間隔を空けた関係に配置され、かつ角質層を貫通するのに十分な長さを有しており、
前記マイクロニードルには、少なくとも部分的に傾斜した形状が設けられていることを特徴とする医療装置。
【請求項2】
各マイクロニードルには、少なくとも部分的に傾斜した形状を具備する先端部が設けられていることを特徴とする請求項1に記載した医療装置。
【請求項3】
前記マイクロニードルには、少なくとも部分的に傾斜した端面を具備する先端部が設けられていることを特徴とする請求項1または2に記載した医療装置。
【請求項4】
前記マイクロニードルは、それぞれ実質的に三角形の断面に構成されていることを特徴とする請求項1乃至3のいずれか一項に記載した医療装置。
【請求項5】
前記マイクロニードルは、それぞれ実質的に菱形、正方形に似た形、楕円形、多角形、矩形、あるいは円形の断面に構成されていることを特徴とする請求項1乃至3のいずれか一項に記載した医療装置。
【請求項6】
前記マイクロニードルは、それぞれ皮膚表面の下方から胚芽層にあるいは角質層を通って、真皮内にではなく生きている表皮内に貫通する長さを有していることを特徴とする請求項1乃至5のいずれか一項に記載した医療装置。
【請求項7】
前記医療装置は、対象の表面に配置されたときに、前記マイクロニードルが皮膚表面の下方から胚芽層にあるいは角質層を通って、真皮内にではなく生きている表皮内に貫通したことの指標を与えるように構成されていることを特徴とする請求項1乃至6のいずれか一項に記載した医療装置。
【請求項8】
前記医療装置は、対象の表面に配置されたときに、皮膚インピーダンス値を得るために予め定められた周波数スペクトルの下端の周波数の電流を電極を介して通過させるとともに、
前記得られたインピーダンス値を前記周波数のために予め定められている参照インピーダンス値と比較し、前記得られたインピーダンス値が前記参照値以下である場合に前記マイクロニードルが角質層を貫通したと決定するように構成されていることを特徴とする請求項7に記載した医療装置。
【請求項9】
前記病状が癌、好ましくは皮膚癌であることを特徴とする請求項1乃至8のいずれか一項に記載した医療装置。
【請求項10】
前記皮膚癌が、基底細胞癌、悪性黒色腫、扁平上皮癌、あるいはそのような病変の前駆体であることを特徴とする請求項9に記載した医療装置。
【請求項11】
各マイクロニードルは、それぞれ少なくとも約10μm、最高で約250μmの長さを有していることを特徴とする請求項1乃至10のいずれか一項に記載した医療装置。
【請求項12】
各マイクロニードルは、それぞれ約100μmの長さを有していることを特徴とする請求項1乃至11のいずれか一項に記載した医療装置。
【請求項13】
前記プローブは、前記マイクロニードルを具備した3つの電極を備え、
第1の電極および第2の電極のマイクロニードルは、第1の距離で互いに横方向に間隔を空けて配置され、
前記第1の電極および第3の電極のマイクロニードルは、第2の距離で互いに間隔を空けて配置され、
前記装置は、前記第1および第2の電極を用いて得られた値と前記第1および第3の電極を用いて得られた値との間における、皮膚インピーダンスの第1および第2の値あるいは皮膚インピーダンスの値の混合値を得るために、前記第1および第2の電極間の電位と前記第1および第3の電極間の電位との比率を徐々に変更するように構成されていることを特徴とする請求項1乃至12のいずれか一項に記載した医療装置。
【請求項14】
前記第1の距離および前記第2距離が互いに異なっていることを特徴とする請求項13に記載した医療装置。
【請求項15】
前記第1の距離が約0.1mm〜約40mmであることを特徴とする請求項13または14に記載した医療装置。
【請求項16】
前記第2の距離が約1mm〜約50mmであることを特徴とする請求項13乃至15のいずれか一項に記載した医療装置。
【請求項17】
前記電流は、約10Hz〜約10MHzの予め定められた周波数スペクトルの周波数を有していることを特徴とする請求項1乃至16のいずれか一項に記載した医療装置。
【請求項18】
前記装置は、複数の対数的に分配された周波数において前記電極を介して前記電流を通過させるように構成されており、
前記周波数は1kHz〜2.5MHzの範囲にあることを特徴とする請求項17に記載した医療装置。
【請求項19】
前記電極は、前記プローブに取り付けられるように構成された着脱自在なキャップ上に配置され、
前記キャップは、前記キャップを前記プローブに取り付けたときに前記電極に電流を供給するように構成された接続手段を有していることを特徴とする請求項1乃至18のいずれか一項に記載した医療装置。
【請求項20】
被験者の皮膚の病状を診断するべく被験者の皮膚表面に配置されるように構成されるとともに、複数のマイクロニードルを有する電極において、
前記電極はベース基板を有しており、
前記マイクロニードルは、前記基板と一体的に形成されるとともに、互いに横方向に間隔を空けた関係に配置され、かつ被験者の皮膚表面に配置されたときに角質層を貫通するのに十分な長さを有しており、
前記マイクロニードルには、少なくとも部分的に傾斜した形状が設けられていることを特徴とする電極。
【請求項21】
前記マイクロニードルには、それぞれ少なくとも部分的に傾斜した形状を具備する先端部が設けられていることを特徴とする請求項20に記載した電極。
【請求項22】
前記マイクロニードルには、少なくとも部分的に傾斜した端面を具備する先端部が設けられていることを特徴とする請求項20または21に記載した電極。
【請求項23】
前記マイクロニードルは、それぞれ実質的に三角形断面に構成されていることを特徴とする請求項20乃至22のいずれか一項に記載した電極。
【請求項24】
前記マイクロニードルは、それそれ実質的に菱形、正方形に似た形、楕円形、多角形、矩形、あるいは円形の断面に構成されていることを特徴とする請求項20乃至22のいずれか一項に記載した電極。
【請求項25】
前記マイクロニードルは、それぞれ皮膚表面の下方から胚芽層にあるいは角質層を通って、真皮内にではなく生きている表皮内に貫通する長さを有していることを特徴とする請求項20乃至24のいずれか一項に記載した電極。
【請求項26】
各マイクロニードルは、それぞれ少なくとも約10μm、最高で約250μmの長さを有していることを特徴とする請求項20乃至25のいずれか一項に記載した電極。
【請求項27】
各マイクロニードルは、それぞれ約100μmの長さを有していることを特徴とする請求項20乃至26のいずれか一項に記載した電極。
【請求項28】
ベース基板と、
同時に形成されて前記基板の表面から突出するマイクロニードルの配列とによって特徴付けられるミクロ構造の配列であって、
前記マイクロニードルは、互いに横方向に間隔を空けた関係に配置され、かつ被験者の皮膚表面に配置されたときに角質層を貫通するのに十分な長さを有しており、
前記マイクロニードルには、少なくとも部分的に傾斜した形状が設けられていることを特徴とする配列。
【請求項29】
前記マイクロニードルには、それぞれ少なくとも部分的に傾斜した形状を具備する先端部が設けられていることを特徴とする請求項28に記載した配列。
【請求項30】
前記マイクロニードルには、少なくとも部分的に傾斜した端面を具備する先端部が設けられていることを特徴とする請求項28または29に記載した配列。
【請求項31】
前記マイクロニードルは、それぞれ実質的に三角形の断面に構成されていることを特徴とする請求項28乃至30のいずれか一項に記載した配列。
【請求項32】
前記マイクロニードルは、それそれ実質的に菱形、正方形に似た形、楕円形、多角形、矩形、あるいは円形の断面に構成されていることを特徴とする請求項28乃至30のいずれか一項に記載した配列。
【請求項33】
被験者の皮膚の病状を診断する方法であって、
請求項1乃至19のいずれか一項に基づいて構成された導電性のプローブを被験者の皮膚表面に配置する段階と、
皮膚のインピーダンス値を得るために予め定められた周波数スペクトルの下端の周波数の電流を電極を介して通過させる段階と、
得られたインピーダンス値が病気にかかった状態を示しているかどうかを決定するために参照データを用いる段階と、
によって特徴付けられる方法。
【請求項34】
前記病状が癌、好ましくは皮膚癌であることを特徴とする請求項33に記載した方法。
【請求項35】
前記皮膚癌が、基底細胞癌、悪性黒色腫、扁平上皮癌、あるいはそのような病変の前駆体であることを特徴とする請求項34に記載した方法。
【請求項36】
識別力を改善するべく皮膚の性質のより多くの状況を把握するために、前記マイクロニードルを具備した電極と非侵襲性表面の電極(従来プローブ)の両方を用いることを特徴とする請求項33乃至35のいずれか一項に記載した方法。
【請求項37】
前記プローブは、前記マイクロニードルを具備した電極を備えており、
第1の電極および第2の電極のマイクロニードルは、第1の距離で互いに横方向に間隔を空けて配置され、
前記第1の電極および第3の電極のマイクロニードルは、第2の距離で互いに間隔を空けて配置され、
前記電流を通過させる段階は、前記第1および第2の電極を用いて得られた値と前記第1および第3の電極を用いて得られた値との間における、皮膚インピーダンスの第1および第2の値あるいは皮膚インピーンスの値の混合値を得るために、前記第1および第2の電極間の電位と前記第1および第3の電極間の電位との比率を徐々に変更する段階をさらに備えることを特徴とする請求項33乃至36のいずれか一項に記載した方法。
【請求項38】
前記電流は、約10Hz〜約10MHzの予め定められた周波数スペクトルの周波数を有していることを特徴とする請求項33乃至37のいずれか一項に記載した方法。
【請求項39】
前記電流を通過させる段階は、複数の対数的に分配された周波数において前記電極を介して前記電流を通過させる段階を含み、
前記周波数が1kHz〜2.5MHzの範囲にあることを特徴とする請求項38に記載した方法。
【請求項40】
導電性のプローブに取り付けられるように構成された着脱自在なキャップであって、
前記キャップは、
請求項20乃至27のいずれか一項に記載されている少なくとも3つの電極と、
前記キャップを前記プローブに取り付けたときに前記電極に電流を供給するように構成された接続手段とを有していることを特徴とするキャップ。
【請求項41】
コンピュータ上で実行されるときに、請求項33乃至39のいずれか一項に記載されている方法の各段階を実行することを特徴とするコンピュータプログラム製品。
【請求項42】
請求項33乃至39のいずれか一項に記載されている方法の各段階をコンピュータに実行させるための指令を含んでいることを特徴とするコンピュータ読み取り可能な記録媒体。
【請求項1】
被験者の皮膚の病状を診断するための医療装置であって、
複数の電極を有している導電性のプローブを備え、
各電極は複数のマイクロニードルを具備しており、
前記プローブは、前記マイクロニードルが角質層を貫通するように被験者の表面に配置されるようになっており、
前記医療装置は、皮膚インピーダンス値を得るために電極に電流を通すことを含むインピーダンス測定セッションを開始するように構成されるとともに、得られたインピーダンス値が病気にかかった状態を示すかどうかを決定するために参照データを用いる、医療装置において、
各電極はベース基板を有し、
前記マイクロニードルは、前記基板と一体的に形成されるとともに、互いに横方向に間隔を空けた関係に配置され、かつ角質層を貫通するのに十分な長さを有しており、
前記マイクロニードルには、少なくとも部分的に傾斜した形状が設けられていることを特徴とする医療装置。
【請求項2】
各マイクロニードルには、少なくとも部分的に傾斜した形状を具備する先端部が設けられていることを特徴とする請求項1に記載した医療装置。
【請求項3】
前記マイクロニードルには、少なくとも部分的に傾斜した端面を具備する先端部が設けられていることを特徴とする請求項1または2に記載した医療装置。
【請求項4】
前記マイクロニードルは、それぞれ実質的に三角形の断面に構成されていることを特徴とする請求項1乃至3のいずれか一項に記載した医療装置。
【請求項5】
前記マイクロニードルは、それぞれ実質的に菱形、正方形に似た形、楕円形、多角形、矩形、あるいは円形の断面に構成されていることを特徴とする請求項1乃至3のいずれか一項に記載した医療装置。
【請求項6】
前記マイクロニードルは、それぞれ皮膚表面の下方から胚芽層にあるいは角質層を通って、真皮内にではなく生きている表皮内に貫通する長さを有していることを特徴とする請求項1乃至5のいずれか一項に記載した医療装置。
【請求項7】
前記医療装置は、対象の表面に配置されたときに、前記マイクロニードルが皮膚表面の下方から胚芽層にあるいは角質層を通って、真皮内にではなく生きている表皮内に貫通したことの指標を与えるように構成されていることを特徴とする請求項1乃至6のいずれか一項に記載した医療装置。
【請求項8】
前記医療装置は、対象の表面に配置されたときに、皮膚インピーダンス値を得るために予め定められた周波数スペクトルの下端の周波数の電流を電極を介して通過させるとともに、
前記得られたインピーダンス値を前記周波数のために予め定められている参照インピーダンス値と比較し、前記得られたインピーダンス値が前記参照値以下である場合に前記マイクロニードルが角質層を貫通したと決定するように構成されていることを特徴とする請求項7に記載した医療装置。
【請求項9】
前記病状が癌、好ましくは皮膚癌であることを特徴とする請求項1乃至8のいずれか一項に記載した医療装置。
【請求項10】
前記皮膚癌が、基底細胞癌、悪性黒色腫、扁平上皮癌、あるいはそのような病変の前駆体であることを特徴とする請求項9に記載した医療装置。
【請求項11】
各マイクロニードルは、それぞれ少なくとも約10μm、最高で約250μmの長さを有していることを特徴とする請求項1乃至10のいずれか一項に記載した医療装置。
【請求項12】
各マイクロニードルは、それぞれ約100μmの長さを有していることを特徴とする請求項1乃至11のいずれか一項に記載した医療装置。
【請求項13】
前記プローブは、前記マイクロニードルを具備した3つの電極を備え、
第1の電極および第2の電極のマイクロニードルは、第1の距離で互いに横方向に間隔を空けて配置され、
前記第1の電極および第3の電極のマイクロニードルは、第2の距離で互いに間隔を空けて配置され、
前記装置は、前記第1および第2の電極を用いて得られた値と前記第1および第3の電極を用いて得られた値との間における、皮膚インピーダンスの第1および第2の値あるいは皮膚インピーダンスの値の混合値を得るために、前記第1および第2の電極間の電位と前記第1および第3の電極間の電位との比率を徐々に変更するように構成されていることを特徴とする請求項1乃至12のいずれか一項に記載した医療装置。
【請求項14】
前記第1の距離および前記第2距離が互いに異なっていることを特徴とする請求項13に記載した医療装置。
【請求項15】
前記第1の距離が約0.1mm〜約40mmであることを特徴とする請求項13または14に記載した医療装置。
【請求項16】
前記第2の距離が約1mm〜約50mmであることを特徴とする請求項13乃至15のいずれか一項に記載した医療装置。
【請求項17】
前記電流は、約10Hz〜約10MHzの予め定められた周波数スペクトルの周波数を有していることを特徴とする請求項1乃至16のいずれか一項に記載した医療装置。
【請求項18】
前記装置は、複数の対数的に分配された周波数において前記電極を介して前記電流を通過させるように構成されており、
前記周波数は1kHz〜2.5MHzの範囲にあることを特徴とする請求項17に記載した医療装置。
【請求項19】
前記電極は、前記プローブに取り付けられるように構成された着脱自在なキャップ上に配置され、
前記キャップは、前記キャップを前記プローブに取り付けたときに前記電極に電流を供給するように構成された接続手段を有していることを特徴とする請求項1乃至18のいずれか一項に記載した医療装置。
【請求項20】
被験者の皮膚の病状を診断するべく被験者の皮膚表面に配置されるように構成されるとともに、複数のマイクロニードルを有する電極において、
前記電極はベース基板を有しており、
前記マイクロニードルは、前記基板と一体的に形成されるとともに、互いに横方向に間隔を空けた関係に配置され、かつ被験者の皮膚表面に配置されたときに角質層を貫通するのに十分な長さを有しており、
前記マイクロニードルには、少なくとも部分的に傾斜した形状が設けられていることを特徴とする電極。
【請求項21】
前記マイクロニードルには、それぞれ少なくとも部分的に傾斜した形状を具備する先端部が設けられていることを特徴とする請求項20に記載した電極。
【請求項22】
前記マイクロニードルには、少なくとも部分的に傾斜した端面を具備する先端部が設けられていることを特徴とする請求項20または21に記載した電極。
【請求項23】
前記マイクロニードルは、それぞれ実質的に三角形断面に構成されていることを特徴とする請求項20乃至22のいずれか一項に記載した電極。
【請求項24】
前記マイクロニードルは、それそれ実質的に菱形、正方形に似た形、楕円形、多角形、矩形、あるいは円形の断面に構成されていることを特徴とする請求項20乃至22のいずれか一項に記載した電極。
【請求項25】
前記マイクロニードルは、それぞれ皮膚表面の下方から胚芽層にあるいは角質層を通って、真皮内にではなく生きている表皮内に貫通する長さを有していることを特徴とする請求項20乃至24のいずれか一項に記載した電極。
【請求項26】
各マイクロニードルは、それぞれ少なくとも約10μm、最高で約250μmの長さを有していることを特徴とする請求項20乃至25のいずれか一項に記載した電極。
【請求項27】
各マイクロニードルは、それぞれ約100μmの長さを有していることを特徴とする請求項20乃至26のいずれか一項に記載した電極。
【請求項28】
ベース基板と、
同時に形成されて前記基板の表面から突出するマイクロニードルの配列とによって特徴付けられるミクロ構造の配列であって、
前記マイクロニードルは、互いに横方向に間隔を空けた関係に配置され、かつ被験者の皮膚表面に配置されたときに角質層を貫通するのに十分な長さを有しており、
前記マイクロニードルには、少なくとも部分的に傾斜した形状が設けられていることを特徴とする配列。
【請求項29】
前記マイクロニードルには、それぞれ少なくとも部分的に傾斜した形状を具備する先端部が設けられていることを特徴とする請求項28に記載した配列。
【請求項30】
前記マイクロニードルには、少なくとも部分的に傾斜した端面を具備する先端部が設けられていることを特徴とする請求項28または29に記載した配列。
【請求項31】
前記マイクロニードルは、それぞれ実質的に三角形の断面に構成されていることを特徴とする請求項28乃至30のいずれか一項に記載した配列。
【請求項32】
前記マイクロニードルは、それそれ実質的に菱形、正方形に似た形、楕円形、多角形、矩形、あるいは円形の断面に構成されていることを特徴とする請求項28乃至30のいずれか一項に記載した配列。
【請求項33】
被験者の皮膚の病状を診断する方法であって、
請求項1乃至19のいずれか一項に基づいて構成された導電性のプローブを被験者の皮膚表面に配置する段階と、
皮膚のインピーダンス値を得るために予め定められた周波数スペクトルの下端の周波数の電流を電極を介して通過させる段階と、
得られたインピーダンス値が病気にかかった状態を示しているかどうかを決定するために参照データを用いる段階と、
によって特徴付けられる方法。
【請求項34】
前記病状が癌、好ましくは皮膚癌であることを特徴とする請求項33に記載した方法。
【請求項35】
前記皮膚癌が、基底細胞癌、悪性黒色腫、扁平上皮癌、あるいはそのような病変の前駆体であることを特徴とする請求項34に記載した方法。
【請求項36】
識別力を改善するべく皮膚の性質のより多くの状況を把握するために、前記マイクロニードルを具備した電極と非侵襲性表面の電極(従来プローブ)の両方を用いることを特徴とする請求項33乃至35のいずれか一項に記載した方法。
【請求項37】
前記プローブは、前記マイクロニードルを具備した電極を備えており、
第1の電極および第2の電極のマイクロニードルは、第1の距離で互いに横方向に間隔を空けて配置され、
前記第1の電極および第3の電極のマイクロニードルは、第2の距離で互いに間隔を空けて配置され、
前記電流を通過させる段階は、前記第1および第2の電極を用いて得られた値と前記第1および第3の電極を用いて得られた値との間における、皮膚インピーダンスの第1および第2の値あるいは皮膚インピーンスの値の混合値を得るために、前記第1および第2の電極間の電位と前記第1および第3の電極間の電位との比率を徐々に変更する段階をさらに備えることを特徴とする請求項33乃至36のいずれか一項に記載した方法。
【請求項38】
前記電流は、約10Hz〜約10MHzの予め定められた周波数スペクトルの周波数を有していることを特徴とする請求項33乃至37のいずれか一項に記載した方法。
【請求項39】
前記電流を通過させる段階は、複数の対数的に分配された周波数において前記電極を介して前記電流を通過させる段階を含み、
前記周波数が1kHz〜2.5MHzの範囲にあることを特徴とする請求項38に記載した方法。
【請求項40】
導電性のプローブに取り付けられるように構成された着脱自在なキャップであって、
前記キャップは、
請求項20乃至27のいずれか一項に記載されている少なくとも3つの電極と、
前記キャップを前記プローブに取り付けたときに前記電極に電流を供給するように構成された接続手段とを有していることを特徴とするキャップ。
【請求項41】
コンピュータ上で実行されるときに、請求項33乃至39のいずれか一項に記載されている方法の各段階を実行することを特徴とするコンピュータプログラム製品。
【請求項42】
請求項33乃至39のいずれか一項に記載されている方法の各段階をコンピュータに実行させるための指令を含んでいることを特徴とするコンピュータ読み取り可能な記録媒体。
【図1a】


【図1b】


【図2a】


【図2b】


【図3a】


【図3b】


【図4a】


【図4b】


【図5a】


【図5b】


【図5c】


【図5d】


【図5e】


【図5f】


【図6a】


【図6b】


【図7a】


【図7b】


【図7c】


【図7d】


【図8a】


【図8b】


【図9a】


【図9b】




【図1b】


【図2a】


【図2b】


【図3a】


【図3b】


【図4a】


【図4b】


【図5a】


【図5b】


【図5c】


【図5d】


【図5e】


【図5f】


【図6a】


【図6b】


【図7a】


【図7b】


【図7c】


【図7d】


【図8a】


【図8b】


【図9a】


【図9b】


【公開番号】特開2012−143571(P2012−143571A)
【公開日】平成24年8月2日(2012.8.2)
【国際特許分類】
【出願番号】特願2012−43843(P2012−43843)
【出願日】平成24年2月29日(2012.2.29)
【分割の表示】特願2008−544850(P2008−544850)の分割
【原出願日】平成18年12月12日(2006.12.12)
【出願人】(310014425)サイベース、アクチボラグ (1)
【氏名又は名称原語表記】SCIBASE AB
【Fターム(参考)】
【公開日】平成24年8月2日(2012.8.2)
【国際特許分類】
【出願日】平成24年2月29日(2012.2.29)
【分割の表示】特願2008−544850(P2008−544850)の分割
【原出願日】平成18年12月12日(2006.12.12)
【出願人】(310014425)サイベース、アクチボラグ (1)
【氏名又は名称原語表記】SCIBASE AB
【Fターム(参考)】
[ Back to top ]

