インフルエンザウイルス感染予防用組成物
【課題】インフルエンザウイルスに対し、優れた感染予防効果を有し、かつ経口摂取に適し、さらに経口安全性に優れ、連続摂取が可能なインフルエンザウイルス感染予防用組成物を提供する。
【解決手段】ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を含有させる。
【解決手段】ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を含有させる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、インフルエンザウイルスに対して感染予防効果を有する、インフルエンザウイルス感染予防用組成物に関する。
【背景技術】
【0002】
インフルエンザ(流行性感冒)は、インフルエンザウイルスに感染することにより発症する流行性の疾患であり、悪寒、発熱、頭痛、全身倦怠感、筋肉痛を特徴とし、咽喉痛、咳、鼻水、鼻閉等の気道症状を伴う。さらに、重篤な合併症として、急性脳症や肺炎等が知られている。
【0003】
インフルエンザの予防は、主としてインフルエンザワクチンにより行われる。ところが、ヒトのインフルエンザの原因となるインフルエンザウイルスにはA型とB型があり、A型には、ウイルス表面の糖タンパク質の変異による亜型が多数存在することから、インフルエンザワクチンが効果的でない場合がある。また、ショック、アナフィラキシー様症状、ギラン・バレー症候群等の重篤な副作用も報告されており、発熱者、急性疾患を有する者、アナフィラキシーを起こしたことのある者など、ワクチンを接種できない者も存在する。
【0004】
一方、抗インフルエンザウイルス薬として、オセルタミビルやザナミビルが用いられる。これらはA型およびB型インフルエンザウイルスに特異的な抗ウイルス薬であるが、症状発現後48時間を経過した後に投与した場合の有効性は確認されておらず、ショック、アナフィラキシー様症状の他、精神・神経症状も副作用として報告されている。また、予防的に使用できる対象者の条件が定められているため、通常は感染予防に用いることはできない。
【0005】
そこで、インフルエンザウイルスに対する感染を予防するべく、日常的に摂取することができて免疫力を向上させ得る安全な組成物が求められる。その一環として、プロバイオティクスの利用が検討されている。
【0006】
「プロバイオティクス」とは、生体内、特に腸管内の正常細菌叢に作用し、そのバランスを改善することにより生体に利益をもたらす生きた微生物、および前記微生物を含む製品をいうが、病原性細菌、ウイルス等に対し、殺菌性物質の産生、栄養成分の競合的摂取、付着部位の競合、代謝酵素活性の促進または抑制等を介した殺菌効果、抗体産生能の活性化、マクロファージ貪食能の亢進等による免疫能賦活効果などが報告されている。
【0007】
「プロバイオティクス」に用いられる微生物としては、ラクトバシラス(Lactobacillus)属、ビフィドバクテリウム(Biffidobacterium)属、エンテロコッカス(Enterococcus)属、リューコノストック(Leuconostoc)属、ペディオコッカス(Pediococcus)属等の乳酸菌が代表的である。これら乳酸菌の免疫系に対する作用については、乳酸菌菌体の細胞質画分および/または細胞質画分含有物を含有する免疫賦活組成物(特許文献1)等が開示されている。さらに、ラブレ菌(Lactobacillus brevis subsp. coagulans)の凍結乾燥粉末について、インターフェロンαおよびγ産生、ならびにナチュラルキラー(NK)細胞活性化作用が報告されている(特許文献2)。ウイルス感染の治療および予防に関しては、ストレプトコッカス フェカリス(Streptococcus faecalis;フェカリス菌の旧学名)の抗ウイルス活性(特許文献3)、バシラス コアグランス(Bacillus coagulans)等の有胞子性乳酸菌を含有する感冒ウイルスまたはインフルエンザウイルス感染性疾患の予防または治療用組成物(特許文献4)、ラクトバシラス プランタラム(Lactobacillus plantarum)、ラクトバシラス ラムノーザス(Lactobacillus rhamnosus)、ラクトバシラス ファーメンタム(Lactobacillus fermentum)、ラクトバシラス パラカゼイ(Lactobacillus paracasei)、ラクトバシラス ガセリ(Lactobacillus gasseri)等の乳酸菌の使用(特許文献5)が開示されている。
【0008】
しかしながら、上記特許文献1に記載された免疫賦活作用や、特許文献2に記載されたインターフェロン産生・NK細胞活性化作用は、宿主の免疫力の個体差や体調等により、十分に発揮されない場合がある。また、上記特許文献3には、フェカリス等菌がin vitroで抗インフルエンザウイルス活性を示すことは記載されているが、インフルエンザウイルスに対するin vivoの感染予防効果を具体的に示す記載はない。また、特許文献4に記載された抗インフルエンザウイルス活性は、十分に高いとはいえず(図1参照)、特許文献5においても、インフルエンザイウイルスに対する感染予防効果は示されていない。かかる状況の下、インフルエンザウイルスに対して優れた感染予防効果を有し、かつ連続摂取可能な安全性の高い組成物が求められているが、上記のプロバイオティクスに用いられる細菌類のうち特定の細菌を組み合わせて用いた場合に、インフルエンザウイルスに対して優れた感染予防効果が得られたという報告は、これまでなされていない。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開平5−252900号公報
【特許文献2】特開平6−206826号公報
【特許文献3】特開昭50−76295号公報
【特許文献4】特開2008−13543号公報
【特許文献5】特表2009−511470号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
そこで、本発明においては、プロバイオティクスに用いられる微生物を用い、インフルエンザウイルスに対して優れた感染予防効果を有するとともに、経口安全性に優れ、連続して経口摂取することが可能な組成物を提供することを目的とする。
【課題を解決するための手段】
【0011】
本発明者らは、上記の課題を解決するべく鋭意検討した結果、ラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を含有させることにより、インフルエンザウイルスに対して、優れた感染予防効果が得られることを見いだし、本発明を完成するに至った。
【0012】
すなわち、本発明は次の[1]〜[5]に関する。
[1]ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を含有する、インフルエンザウイルス感染予防用組成物。
[2]ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物とを、1:5〜1:50の乾燥重量比で含有する、上記[1]に記載のインフルエンザウイルス感染予防用組成物。
[3]ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体を菌数にて1×108個以上と、フェカリス菌(Enterococcus faecalis)の菌体を菌数にて1×109個以上含有する、上記[1]または[2]に記載のインフルエンザウイルス感染予防用組成物。
[4]上記[1]〜[3]のいずれかに記載のインフルエンザウイルス感染予防用組成物を含有する、医薬品。
[5]上記[1]〜[3]のいずれかに記載のインフルエンザウイルス感染予防用組成物を含有する、飲食品。
【発明の効果】
【0013】
本発明のインフルエンザウイルス感染予防用組成物を摂取することにより、インフルエンザウイルスに対する感染を有効に予防することができる。さらに、本発明のインフルエンザウイルス感染予防用組成物は経口摂取に適し、経口安全性に優れるため、インフルエンザの流行期間中の長期間にわたり、連続して経口摂取させることができる。
【図面の簡単な説明】
【0014】
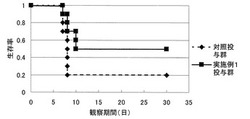
【図1】図1は、実施例1のインフルエンザウイルス感染予防用組成物について、マウスを用いた感染予防実験の結果を示す図である。
【発明を実施するための形態】
【0015】
本発明のインフルエンザウイルス感染予防用組成物は、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を含有してなる。
【0016】
本発明において用いるラブレ菌(Lactobacillus brevis subsp. coagulans)は、すぐきの漬物から単離された乳酸菌(グラム陽性桿菌)であり、便通を整え、腸内環境を良好な状態にする効果を有するといわれている。また、フェカリス菌(Enterococcus faecalis)も、腸内に常在する乳酸菌(グラム陽性球菌)である。本発明の目的には、ラブレ菌(Lactobacillus brevis subsp. coagulans)としては、Lactobacillus brevis subsp. coagulans NT株等が好ましく、フェカリス菌(Enterococcus faecalis)としては、Enterococcus faecalis NT株等が好ましく用いられる。これらは、通常の乳酸菌培養用培地、たとえばMRS培地等を用いて培養することができる。
【0017】
本発明においては、ラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)は、上記乳酸菌用培地による培養液をそのまま、もしくは濃縮して用いてもよく、また前記培養液より、遠心分離もしくはフィルターろ過等の手法によって菌体を分離し、それら菌体をそのままもしくは滅菌精製水等に懸濁し、または凍結乾燥して用いることができる。あるいは、分離、集菌した前記菌体について、加熱滅菌、高圧蒸気滅菌等の処理を行った後に用いることもできる。
【0018】
さらにまた、分離、集菌した前記菌体より、溶媒により抽出した抽出物を用いることもできる。抽出に用い得る溶媒としては、水;メタノール、エタノール、イソプロパノール等の低級アルコール類;エチレングリコール、ジエチレングリコール、プロピレングリコール、ジプロピレングリコール、1,3−ブチレングリコール、グリセリン等の多価アルコール類;アセトン等のケトン類;酢酸エチル等のエステル類;リン酸緩衝液、トリス塩酸緩衝液等の緩衝液;生理食塩水;リン酸緩衝生理食塩水などが挙げられる。抽出温度としては、0℃程度から抽出に用いる溶媒の沸点以下の温度とするのが好ましく、4℃程度から25℃程度とするのがより好ましい。抽出は、前記溶媒中に菌体を浸漬あるいは懸濁し、または前記溶媒中でホモジナイズすること等により行うことができる。抽出時間としては、抽出に用いる溶媒の種類や抽出温度にもよるが、通常10分程度から72時間程度である。前記菌体の溶媒による抽出物は、そのまま用いてもよく、濃縮、乾固し、または透析、分画等の精製処理を行った後に用いてもよい。
【0019】
本発明のインフルエンザウイルス感染予防用組成物には、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物は、乾燥重量比にして、1:5〜1:50の範囲で混合して用いることが好ましく、1:10〜1:20の範囲で用いることがより好ましい。ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を、乾燥重量比にして1:5〜1:50の範囲で用いた場合、インフルエンザウイルスに対し良好な感染予防効果を発揮し得る。
【0020】
また、本発明のインフルエンザウイルス感染予防用組成物には、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体を菌数にて1×108個以上、フェカリス菌(Enterococcus faecalis)の菌体を菌数にて1×109個以上含有させることが好ましい。
【0021】
また、本発明のインフルエンザウイルス感染予防用組成物には、本発明の特徴を損なわない範囲で、生菌製剤や発酵食品に汎用される他の細菌類の菌体またはそれらの抽出物を含有させることもできる。かかる細菌類としては、ガッセリ菌(Lactobacillus gasseri)、アシドフィルス菌(Lactobacillus acidophilus)、カゼイ菌(Lactobacillus casei)等のラブレ菌(Lactobacillus brevis subsp. coagulans)以外のラクトバシラス属(Lactobacillus sp.)の細菌;ビフィドバクテリウム ビフィダム(Bifidobacterium bifidum)、ビフィドバクテリウム ロンガム(Bifidobacterium longum)、ビフィドバクテリウム ブレーベ(Bifidobacterium breve)、ビフィドバクテリウム インファンティス(Bifidobacterium infantis)、ビフィドバクテリウム アドレスセンティス(Bifidobacterium adolescentis)等のビフィドバクテリウム属(Bifidobacterium sp.)の細菌;フェシウム菌(Enterococcus faecium)等、フェカリス菌(Enterococcus faecalis)以外のエンテロコッカス属(Enterococcus sp.)の細菌;ラクトコッカス ラクティス(Lactococcus lactis)、ラクトコッカス クレモリス(Lactococcus cremoris)等のラクトコッカス属(Lactococcus sp.)の細菌;ペディオコッカス ダムノスス(Pediococcus damnosus)等のペディオコッカス属(Pediococcus sp.)の細菌;リューコノストック マセンテロイデス(Leuconostoc masenteroides)等のリューコノストック属(Leuconostoc sp.)の細菌;酪酸菌(Clostridium butyricum)、納豆菌(Bacillus subtilis var. natto)などが挙げられる。
【0022】
上記の他の細菌類についても、ラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)と同様に、それぞれの培養液やその濃縮物、分離した菌体、菌体の凍結乾燥物や滅菌処理物を用いることができる。また、上記他の細菌類の抽出物としては、ラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)について上記したのと同様の溶媒による抽出物を用いることができる。
【0023】
本発明のインフルエンザウイルス感染予防用組成物は、上記のラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物の混合物をそのまま医薬品または飲食品として提供してもよく、水の他、エタノール等のアルコール類、グリセリン、プロピレングリコール等の多価アルコール類、油脂類、ゲル、ミセル、エマルション、粉体、カプセル、リポソームなど、医薬品または飲食品用の担体に含有させて提供してもよい。
【0024】
医薬品としては、液剤、懸濁剤、乳剤、シロップ剤等の液状製剤;ゼリー剤、スラリー剤等の半固形状製剤;散剤、錠剤、丸剤、顆粒剤、ゲル剤、カプセル剤、チュアブル剤等の固形状製剤などの形態で提供することができる。これらのなかでも、家庭において容易に摂取できることから、経口投与に適する形態で提供されることが好ましい。本発明のインフルエンザウイルス感染予防用組成物を含有する医薬品においては、その製剤化に際し必要に応じて、賦形剤、結合剤、滑沢剤、崩壊剤、界面活性剤、増粘剤、コーティング剤、pH調整剤、抗酸化剤、嬌味剤、防腐剤、着色剤、香味剤等の一般的な医薬品添加物を添加することができる。
【0025】
上記賦形剤としては、結晶セルロース、ヒドロキシプロピルセルロース等のセルロースおよびその誘導体;コムギデンプン、トウモロコシデンプン、カルボキシメチルスターチナトリウム、デキストリン等のデンプンおよびその誘導体;アラビアゴム、アルギン酸ナトリウム等の天然高分子化合物;ブドウ糖、マルトース、ソルビトール、マルチトール、マンニトール等の糖および糖アルコール;塩化ナトリウム、炭酸カルシウム、ケイ酸マグネシウム等の無機塩類などが挙げられる。
【0026】
上記結合剤としては、グアーガム、合成ケイ酸アルミニウム、ステアリン酸、高分子ポリビニルピロリドン、乳糖などが、上記滑沢剤としては、タルク、ステアリン酸マグネシウム、ポリエチレングリコール6000などが、上記崩壊剤としては、アジピン酸、ステアリン酸カルシウム、白糖などが挙げられる。
【0027】
上記界面活性剤としては、ショ糖脂肪酸エステル、大豆レシチン、ポリオキシエチレン硬化ヒマシ油、ポリオキシエチレンソルビタン脂肪酸エステルなどが、増粘剤としては、カルボキシメチルセルロースナトリウム、カルボキシビニルポリマー、キサンタンガム、ゼラチンなどが、コーティング剤としては、アクリル酸エチル・メタクリル酸メチルコポリマー分散液、カラメル、カルナウバロウ、セラック、白糖、プルランなどが挙げられる。
【0028】
pH調整剤としては、クエン酸、クエン酸ナトリウム、酢酸、酢酸ナトリウム、水酸化ナトリウムなどが、抗酸化剤としては、アスコルビン酸、酢酸トコフェロール、天然ビタミンE、没食子酸プロピルなどが、嬌味剤としては、アスパルテーム、カンゾウエキス、サッカリンなどが挙げられ、防腐剤としては、安息香酸ナトリウム、エデト酸ナトリウム、ソルビン酸、ソルビン酸ナトリウム、パラオキシ安息香酸メチル、パラオキシ安息香酸ブチルなどが、着色剤としては、ベンガラ、黄酸化鉄、黒酸化鉄、カルミン、食用青色1号、食用黄色4号、食用黄色4号アルミニウムレーキ、食用赤色2号、銅クロロフィリンナトリウムなどが、香味剤としては、オイゲノール、バニリン、メントールなどが挙げられる。
【0029】
飲食品としては、液状、懸濁状、乳状等の液状飲食品;スラリー状、ゼリー状、クリーム状等の半固形状飲食品;粉末状、顆粒状、タブレット状、シート状、ゲル状、カプセル状等の固形状飲食品などの形態で提供することができる。また、一般の加工食品のほか、特定保健用食品、栄養機能食品等の保健機能食品や、栄養補助食品などとすることができる。これら飲食品には、本発明のインフルエンザウイルス感染予防用組成物のほかに、一般的な飲食品用添加物を添加することができる。
【0030】
上記添加物としては、たとえば甘味料、着色料、保存料、増粘安定剤、酸化防止剤、発色剤、漂白剤、防かび剤、ガムベース、苦味料、酵素、光沢剤、酸味料、調味料、乳化剤、強化剤、製造用剤、香料、香辛料抽出物等が挙げられる。
【0031】
本発明のインフルエンザウイルス感染予防用組成物は、摂取させる対象者の性別、年齢、体重、体調等により異なるが、成人(体重60kg)につき1日あたり、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物の総乾燥重量にして通常は1mg〜20mg、好ましくは1mg〜5mgを摂取させる。なお、前記の量を1回で摂取させてもよく、数回に分けて摂取させてもよい。
【0032】
特に、飲食品が特定保健用食品、栄養機能食品等の保健機能食品や、栄養補助食品である場合には、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を、上記により設定された1回あたりの摂取単位量を含有するように、1食分ずつ包装した形態や、1回あたりの摂取単位量を懸濁あるいは溶解した飲料を、1食あたりの飲み切りの形態で瓶等に充填した形態で提供することが好ましい。
【0033】
なお、本発明のインフルエンザウイルス感染予防用組成物は、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を主な成分として含有するものであり、経口安全性が高く、腸内細菌叢に対し悪影響を与えることもないので、長期間連続して経口摂取させることができる。特に、インフルエンザは、毎年季節的な流行を示すため、インフルエンザウイルスに対する感染の予防は長期間にわたり必要となることが多い。従って、インフルエンザウイルスに対する感染を有効に予防するためには、本発明のインフルエンザウイルス感染予防用組成物を、インフルエンザの流行が始まる前から終息するまでの期間中、連続して摂取させることが好ましい。
【0034】
本発明のインフルエンザウイルス感染予防用組成物は、医薬品製剤または飲食品の一般的な製造方法、たとえば日本薬局方製剤総則や医薬品製造指針に記載された方法により、製造することができる。すなわち、上記したラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を、必要により懸濁化剤または分散剤を加えて水等の溶剤に懸濁または分散して懸濁剤または分散剤とし、あるいは乳化剤と油性成分を加えて乳化して乳剤とする。また、前記を粉末化し、必要に応じて賦形剤、結合剤、崩壊剤等の添加剤とともに混合して粉末状または微粒状として散剤とする。また、粉末化したラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物に、必要に応じて賦形剤等の添加剤を加えて混合し、均質化したものを粒状とし、整粒して顆粒剤とする。さらに、前記のように、粒状もしくは成形物としたものを硬カプセルに充填して、硬カプセル剤とし、ラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を粉末化し、必要により賦形剤等の添加剤を加えて混合し、均質化したものを、ゼラチン等のカプセル基剤にグリセリンまたはソルビトール等を加えて可塑性を増したもので被包成形して、軟カプセル剤とすることができる。さらにまた、顆粒状とした本発明のインフルエンザウイルス感染予防用組成物を圧縮成形したり、溶媒で湿潤させた後、型に流し込んで成形することにより、錠剤とすることができる。
【0035】
上記の顆粒剤やカプセル剤は、徐放性または腸溶性被膜により処理したり、徐放性または腸溶性の剤皮で処理したりして、徐放性または腸溶性製剤とすることができる。また、錠剤の場合も、糖衣錠やフィルムコーティング錠、徐放錠もしくは腸溶錠とすることができる。
【実施例】
【0036】
さらに、本発明について、実施例により詳細に説明する。
【0037】
[実施例1]インフルエンザウイルス感染予防用組成物
ラブレ菌(Lactobacillus brevis subsp. coagulans NT)はラブレ菌生産用培地にて約30℃で約48時間培養し、培養液を遠心分離(15,000r.p.m.、10分)して集菌し、蒸留水で1回洗浄した後、121℃で15分間加熱滅菌処理した。一方、フェカリス菌(Enterococcus faecalis NT)は乳酸菌フェカリス生産用培地にて37℃で約18時間培養し、培養液を遠心分離(15,000r.p.m.、10分)して集菌し、滅菌水で1回洗浄した後、121℃で15分間加熱滅菌処理した。前記の加熱滅菌処理菌体を、それぞれ乾燥重量にして0.16mgおよび3.0mg混合して、実施例1のインフルエンザウイルス感染予防用組成物とした。本組成物3.16mgは、成人(体重60kg)に対し、1日にラブレ菌(Lactobacillus brevis subsp. coagulans NT)およびフェカリス菌(Enterococcus faecalis NT)の各菌体を、それぞれ菌数にて7.5×108個および1.0×1010個摂取させる量を含有する。
【0038】
[感染予防実験]
実施例1のインフルエンザウイルス感染予防用組成物について、次に示す実験方法により評価した。
【0039】
BALB/cマウス(雌、8週齢)を4群(各群n=10)に分け、表1に示すように実施例1のインフルエンザウイルス感染予防用組成物を投与した。実施例1の組成物は、成人(体重60kg)の1日当たりの摂取量を、体重20gに対する量に換算し、当該換算量の約10倍を、リン酸緩衝生理食塩水0.2mLに懸濁して、経口ゾンデにて投与した。
【0040】
【表1】

【0041】
表1の各群に対し、ペントバルビタール麻酔下にてインフルエンザウイルスA型(H1N1)PR8株1×104pfu(plaque forming unit)を含むリン酸緩衝生理食塩水20μLを経鼻投与して、インフルエンザウイルスを感染させた。インフルエンザウイルス感染後、実施例1の組成物投与群には、さらに1週間、実施例1の感染予防用組成物を投与し、マウスの生死を30日間観察した。
【0042】
実施例1の感染予防用組成物を、インフルエンザウイルス感染の1週間前から投与した群において生存率が向上する傾向が見られたが、実施例1の感染予防用組成物の投与期間を2週間および4週間と延長しても、感染予防効果の増強は認められなかった。同様の感染予防実験を2回繰り返した結果、実施例1の感染予防用組成物をインフルエンザウイルス感染の1週間前から投与した場合に、図1に示すように、対照群との間に、統計学的に有意な感染予防効果が認められた(p<0.05)。
【産業上の利用可能性】
【0043】
以上詳述したように、本発明により、経口摂取に適し、インフルエンザウイルスに対する感染を良好に予防することのできるインフルエンザウイルス感染予防用組成物を提供することができる。本発明のインフルエンザウイルス感染予防用組成物は経口安全性が高く、インフルエンザの流行期間にわたり、長期間連続して経口摂取させることができる。また、重篤な副作用を生じることが少ないため、インフルエンザワクチンや抗ウイルス薬に対し過敏性反応を示す者や、発熱者等の病者に対しても、摂取させることができる。
【技術分野】
【0001】
本発明は、インフルエンザウイルスに対して感染予防効果を有する、インフルエンザウイルス感染予防用組成物に関する。
【背景技術】
【0002】
インフルエンザ(流行性感冒)は、インフルエンザウイルスに感染することにより発症する流行性の疾患であり、悪寒、発熱、頭痛、全身倦怠感、筋肉痛を特徴とし、咽喉痛、咳、鼻水、鼻閉等の気道症状を伴う。さらに、重篤な合併症として、急性脳症や肺炎等が知られている。
【0003】
インフルエンザの予防は、主としてインフルエンザワクチンにより行われる。ところが、ヒトのインフルエンザの原因となるインフルエンザウイルスにはA型とB型があり、A型には、ウイルス表面の糖タンパク質の変異による亜型が多数存在することから、インフルエンザワクチンが効果的でない場合がある。また、ショック、アナフィラキシー様症状、ギラン・バレー症候群等の重篤な副作用も報告されており、発熱者、急性疾患を有する者、アナフィラキシーを起こしたことのある者など、ワクチンを接種できない者も存在する。
【0004】
一方、抗インフルエンザウイルス薬として、オセルタミビルやザナミビルが用いられる。これらはA型およびB型インフルエンザウイルスに特異的な抗ウイルス薬であるが、症状発現後48時間を経過した後に投与した場合の有効性は確認されておらず、ショック、アナフィラキシー様症状の他、精神・神経症状も副作用として報告されている。また、予防的に使用できる対象者の条件が定められているため、通常は感染予防に用いることはできない。
【0005】
そこで、インフルエンザウイルスに対する感染を予防するべく、日常的に摂取することができて免疫力を向上させ得る安全な組成物が求められる。その一環として、プロバイオティクスの利用が検討されている。
【0006】
「プロバイオティクス」とは、生体内、特に腸管内の正常細菌叢に作用し、そのバランスを改善することにより生体に利益をもたらす生きた微生物、および前記微生物を含む製品をいうが、病原性細菌、ウイルス等に対し、殺菌性物質の産生、栄養成分の競合的摂取、付着部位の競合、代謝酵素活性の促進または抑制等を介した殺菌効果、抗体産生能の活性化、マクロファージ貪食能の亢進等による免疫能賦活効果などが報告されている。
【0007】
「プロバイオティクス」に用いられる微生物としては、ラクトバシラス(Lactobacillus)属、ビフィドバクテリウム(Biffidobacterium)属、エンテロコッカス(Enterococcus)属、リューコノストック(Leuconostoc)属、ペディオコッカス(Pediococcus)属等の乳酸菌が代表的である。これら乳酸菌の免疫系に対する作用については、乳酸菌菌体の細胞質画分および/または細胞質画分含有物を含有する免疫賦活組成物(特許文献1)等が開示されている。さらに、ラブレ菌(Lactobacillus brevis subsp. coagulans)の凍結乾燥粉末について、インターフェロンαおよびγ産生、ならびにナチュラルキラー(NK)細胞活性化作用が報告されている(特許文献2)。ウイルス感染の治療および予防に関しては、ストレプトコッカス フェカリス(Streptococcus faecalis;フェカリス菌の旧学名)の抗ウイルス活性(特許文献3)、バシラス コアグランス(Bacillus coagulans)等の有胞子性乳酸菌を含有する感冒ウイルスまたはインフルエンザウイルス感染性疾患の予防または治療用組成物(特許文献4)、ラクトバシラス プランタラム(Lactobacillus plantarum)、ラクトバシラス ラムノーザス(Lactobacillus rhamnosus)、ラクトバシラス ファーメンタム(Lactobacillus fermentum)、ラクトバシラス パラカゼイ(Lactobacillus paracasei)、ラクトバシラス ガセリ(Lactobacillus gasseri)等の乳酸菌の使用(特許文献5)が開示されている。
【0008】
しかしながら、上記特許文献1に記載された免疫賦活作用や、特許文献2に記載されたインターフェロン産生・NK細胞活性化作用は、宿主の免疫力の個体差や体調等により、十分に発揮されない場合がある。また、上記特許文献3には、フェカリス等菌がin vitroで抗インフルエンザウイルス活性を示すことは記載されているが、インフルエンザウイルスに対するin vivoの感染予防効果を具体的に示す記載はない。また、特許文献4に記載された抗インフルエンザウイルス活性は、十分に高いとはいえず(図1参照)、特許文献5においても、インフルエンザイウイルスに対する感染予防効果は示されていない。かかる状況の下、インフルエンザウイルスに対して優れた感染予防効果を有し、かつ連続摂取可能な安全性の高い組成物が求められているが、上記のプロバイオティクスに用いられる細菌類のうち特定の細菌を組み合わせて用いた場合に、インフルエンザウイルスに対して優れた感染予防効果が得られたという報告は、これまでなされていない。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開平5−252900号公報
【特許文献2】特開平6−206826号公報
【特許文献3】特開昭50−76295号公報
【特許文献4】特開2008−13543号公報
【特許文献5】特表2009−511470号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
そこで、本発明においては、プロバイオティクスに用いられる微生物を用い、インフルエンザウイルスに対して優れた感染予防効果を有するとともに、経口安全性に優れ、連続して経口摂取することが可能な組成物を提供することを目的とする。
【課題を解決するための手段】
【0011】
本発明者らは、上記の課題を解決するべく鋭意検討した結果、ラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を含有させることにより、インフルエンザウイルスに対して、優れた感染予防効果が得られることを見いだし、本発明を完成するに至った。
【0012】
すなわち、本発明は次の[1]〜[5]に関する。
[1]ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を含有する、インフルエンザウイルス感染予防用組成物。
[2]ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物とを、1:5〜1:50の乾燥重量比で含有する、上記[1]に記載のインフルエンザウイルス感染予防用組成物。
[3]ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体を菌数にて1×108個以上と、フェカリス菌(Enterococcus faecalis)の菌体を菌数にて1×109個以上含有する、上記[1]または[2]に記載のインフルエンザウイルス感染予防用組成物。
[4]上記[1]〜[3]のいずれかに記載のインフルエンザウイルス感染予防用組成物を含有する、医薬品。
[5]上記[1]〜[3]のいずれかに記載のインフルエンザウイルス感染予防用組成物を含有する、飲食品。
【発明の効果】
【0013】
本発明のインフルエンザウイルス感染予防用組成物を摂取することにより、インフルエンザウイルスに対する感染を有効に予防することができる。さらに、本発明のインフルエンザウイルス感染予防用組成物は経口摂取に適し、経口安全性に優れるため、インフルエンザの流行期間中の長期間にわたり、連続して経口摂取させることができる。
【図面の簡単な説明】
【0014】
【図1】図1は、実施例1のインフルエンザウイルス感染予防用組成物について、マウスを用いた感染予防実験の結果を示す図である。
【発明を実施するための形態】
【0015】
本発明のインフルエンザウイルス感染予防用組成物は、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を含有してなる。
【0016】
本発明において用いるラブレ菌(Lactobacillus brevis subsp. coagulans)は、すぐきの漬物から単離された乳酸菌(グラム陽性桿菌)であり、便通を整え、腸内環境を良好な状態にする効果を有するといわれている。また、フェカリス菌(Enterococcus faecalis)も、腸内に常在する乳酸菌(グラム陽性球菌)である。本発明の目的には、ラブレ菌(Lactobacillus brevis subsp. coagulans)としては、Lactobacillus brevis subsp. coagulans NT株等が好ましく、フェカリス菌(Enterococcus faecalis)としては、Enterococcus faecalis NT株等が好ましく用いられる。これらは、通常の乳酸菌培養用培地、たとえばMRS培地等を用いて培養することができる。
【0017】
本発明においては、ラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)は、上記乳酸菌用培地による培養液をそのまま、もしくは濃縮して用いてもよく、また前記培養液より、遠心分離もしくはフィルターろ過等の手法によって菌体を分離し、それら菌体をそのままもしくは滅菌精製水等に懸濁し、または凍結乾燥して用いることができる。あるいは、分離、集菌した前記菌体について、加熱滅菌、高圧蒸気滅菌等の処理を行った後に用いることもできる。
【0018】
さらにまた、分離、集菌した前記菌体より、溶媒により抽出した抽出物を用いることもできる。抽出に用い得る溶媒としては、水;メタノール、エタノール、イソプロパノール等の低級アルコール類;エチレングリコール、ジエチレングリコール、プロピレングリコール、ジプロピレングリコール、1,3−ブチレングリコール、グリセリン等の多価アルコール類;アセトン等のケトン類;酢酸エチル等のエステル類;リン酸緩衝液、トリス塩酸緩衝液等の緩衝液;生理食塩水;リン酸緩衝生理食塩水などが挙げられる。抽出温度としては、0℃程度から抽出に用いる溶媒の沸点以下の温度とするのが好ましく、4℃程度から25℃程度とするのがより好ましい。抽出は、前記溶媒中に菌体を浸漬あるいは懸濁し、または前記溶媒中でホモジナイズすること等により行うことができる。抽出時間としては、抽出に用いる溶媒の種類や抽出温度にもよるが、通常10分程度から72時間程度である。前記菌体の溶媒による抽出物は、そのまま用いてもよく、濃縮、乾固し、または透析、分画等の精製処理を行った後に用いてもよい。
【0019】
本発明のインフルエンザウイルス感染予防用組成物には、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物は、乾燥重量比にして、1:5〜1:50の範囲で混合して用いることが好ましく、1:10〜1:20の範囲で用いることがより好ましい。ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を、乾燥重量比にして1:5〜1:50の範囲で用いた場合、インフルエンザウイルスに対し良好な感染予防効果を発揮し得る。
【0020】
また、本発明のインフルエンザウイルス感染予防用組成物には、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体を菌数にて1×108個以上、フェカリス菌(Enterococcus faecalis)の菌体を菌数にて1×109個以上含有させることが好ましい。
【0021】
また、本発明のインフルエンザウイルス感染予防用組成物には、本発明の特徴を損なわない範囲で、生菌製剤や発酵食品に汎用される他の細菌類の菌体またはそれらの抽出物を含有させることもできる。かかる細菌類としては、ガッセリ菌(Lactobacillus gasseri)、アシドフィルス菌(Lactobacillus acidophilus)、カゼイ菌(Lactobacillus casei)等のラブレ菌(Lactobacillus brevis subsp. coagulans)以外のラクトバシラス属(Lactobacillus sp.)の細菌;ビフィドバクテリウム ビフィダム(Bifidobacterium bifidum)、ビフィドバクテリウム ロンガム(Bifidobacterium longum)、ビフィドバクテリウム ブレーベ(Bifidobacterium breve)、ビフィドバクテリウム インファンティス(Bifidobacterium infantis)、ビフィドバクテリウム アドレスセンティス(Bifidobacterium adolescentis)等のビフィドバクテリウム属(Bifidobacterium sp.)の細菌;フェシウム菌(Enterococcus faecium)等、フェカリス菌(Enterococcus faecalis)以外のエンテロコッカス属(Enterococcus sp.)の細菌;ラクトコッカス ラクティス(Lactococcus lactis)、ラクトコッカス クレモリス(Lactococcus cremoris)等のラクトコッカス属(Lactococcus sp.)の細菌;ペディオコッカス ダムノスス(Pediococcus damnosus)等のペディオコッカス属(Pediococcus sp.)の細菌;リューコノストック マセンテロイデス(Leuconostoc masenteroides)等のリューコノストック属(Leuconostoc sp.)の細菌;酪酸菌(Clostridium butyricum)、納豆菌(Bacillus subtilis var. natto)などが挙げられる。
【0022】
上記の他の細菌類についても、ラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)と同様に、それぞれの培養液やその濃縮物、分離した菌体、菌体の凍結乾燥物や滅菌処理物を用いることができる。また、上記他の細菌類の抽出物としては、ラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)について上記したのと同様の溶媒による抽出物を用いることができる。
【0023】
本発明のインフルエンザウイルス感染予防用組成物は、上記のラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物の混合物をそのまま医薬品または飲食品として提供してもよく、水の他、エタノール等のアルコール類、グリセリン、プロピレングリコール等の多価アルコール類、油脂類、ゲル、ミセル、エマルション、粉体、カプセル、リポソームなど、医薬品または飲食品用の担体に含有させて提供してもよい。
【0024】
医薬品としては、液剤、懸濁剤、乳剤、シロップ剤等の液状製剤;ゼリー剤、スラリー剤等の半固形状製剤;散剤、錠剤、丸剤、顆粒剤、ゲル剤、カプセル剤、チュアブル剤等の固形状製剤などの形態で提供することができる。これらのなかでも、家庭において容易に摂取できることから、経口投与に適する形態で提供されることが好ましい。本発明のインフルエンザウイルス感染予防用組成物を含有する医薬品においては、その製剤化に際し必要に応じて、賦形剤、結合剤、滑沢剤、崩壊剤、界面活性剤、増粘剤、コーティング剤、pH調整剤、抗酸化剤、嬌味剤、防腐剤、着色剤、香味剤等の一般的な医薬品添加物を添加することができる。
【0025】
上記賦形剤としては、結晶セルロース、ヒドロキシプロピルセルロース等のセルロースおよびその誘導体;コムギデンプン、トウモロコシデンプン、カルボキシメチルスターチナトリウム、デキストリン等のデンプンおよびその誘導体;アラビアゴム、アルギン酸ナトリウム等の天然高分子化合物;ブドウ糖、マルトース、ソルビトール、マルチトール、マンニトール等の糖および糖アルコール;塩化ナトリウム、炭酸カルシウム、ケイ酸マグネシウム等の無機塩類などが挙げられる。
【0026】
上記結合剤としては、グアーガム、合成ケイ酸アルミニウム、ステアリン酸、高分子ポリビニルピロリドン、乳糖などが、上記滑沢剤としては、タルク、ステアリン酸マグネシウム、ポリエチレングリコール6000などが、上記崩壊剤としては、アジピン酸、ステアリン酸カルシウム、白糖などが挙げられる。
【0027】
上記界面活性剤としては、ショ糖脂肪酸エステル、大豆レシチン、ポリオキシエチレン硬化ヒマシ油、ポリオキシエチレンソルビタン脂肪酸エステルなどが、増粘剤としては、カルボキシメチルセルロースナトリウム、カルボキシビニルポリマー、キサンタンガム、ゼラチンなどが、コーティング剤としては、アクリル酸エチル・メタクリル酸メチルコポリマー分散液、カラメル、カルナウバロウ、セラック、白糖、プルランなどが挙げられる。
【0028】
pH調整剤としては、クエン酸、クエン酸ナトリウム、酢酸、酢酸ナトリウム、水酸化ナトリウムなどが、抗酸化剤としては、アスコルビン酸、酢酸トコフェロール、天然ビタミンE、没食子酸プロピルなどが、嬌味剤としては、アスパルテーム、カンゾウエキス、サッカリンなどが挙げられ、防腐剤としては、安息香酸ナトリウム、エデト酸ナトリウム、ソルビン酸、ソルビン酸ナトリウム、パラオキシ安息香酸メチル、パラオキシ安息香酸ブチルなどが、着色剤としては、ベンガラ、黄酸化鉄、黒酸化鉄、カルミン、食用青色1号、食用黄色4号、食用黄色4号アルミニウムレーキ、食用赤色2号、銅クロロフィリンナトリウムなどが、香味剤としては、オイゲノール、バニリン、メントールなどが挙げられる。
【0029】
飲食品としては、液状、懸濁状、乳状等の液状飲食品;スラリー状、ゼリー状、クリーム状等の半固形状飲食品;粉末状、顆粒状、タブレット状、シート状、ゲル状、カプセル状等の固形状飲食品などの形態で提供することができる。また、一般の加工食品のほか、特定保健用食品、栄養機能食品等の保健機能食品や、栄養補助食品などとすることができる。これら飲食品には、本発明のインフルエンザウイルス感染予防用組成物のほかに、一般的な飲食品用添加物を添加することができる。
【0030】
上記添加物としては、たとえば甘味料、着色料、保存料、増粘安定剤、酸化防止剤、発色剤、漂白剤、防かび剤、ガムベース、苦味料、酵素、光沢剤、酸味料、調味料、乳化剤、強化剤、製造用剤、香料、香辛料抽出物等が挙げられる。
【0031】
本発明のインフルエンザウイルス感染予防用組成物は、摂取させる対象者の性別、年齢、体重、体調等により異なるが、成人(体重60kg)につき1日あたり、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物の総乾燥重量にして通常は1mg〜20mg、好ましくは1mg〜5mgを摂取させる。なお、前記の量を1回で摂取させてもよく、数回に分けて摂取させてもよい。
【0032】
特に、飲食品が特定保健用食品、栄養機能食品等の保健機能食品や、栄養補助食品である場合には、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を、上記により設定された1回あたりの摂取単位量を含有するように、1食分ずつ包装した形態や、1回あたりの摂取単位量を懸濁あるいは溶解した飲料を、1食あたりの飲み切りの形態で瓶等に充填した形態で提供することが好ましい。
【0033】
なお、本発明のインフルエンザウイルス感染予防用組成物は、ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を主な成分として含有するものであり、経口安全性が高く、腸内細菌叢に対し悪影響を与えることもないので、長期間連続して経口摂取させることができる。特に、インフルエンザは、毎年季節的な流行を示すため、インフルエンザウイルスに対する感染の予防は長期間にわたり必要となることが多い。従って、インフルエンザウイルスに対する感染を有効に予防するためには、本発明のインフルエンザウイルス感染予防用組成物を、インフルエンザの流行が始まる前から終息するまでの期間中、連続して摂取させることが好ましい。
【0034】
本発明のインフルエンザウイルス感染予防用組成物は、医薬品製剤または飲食品の一般的な製造方法、たとえば日本薬局方製剤総則や医薬品製造指針に記載された方法により、製造することができる。すなわち、上記したラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物、およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を、必要により懸濁化剤または分散剤を加えて水等の溶剤に懸濁または分散して懸濁剤または分散剤とし、あるいは乳化剤と油性成分を加えて乳化して乳剤とする。また、前記を粉末化し、必要に応じて賦形剤、結合剤、崩壊剤等の添加剤とともに混合して粉末状または微粒状として散剤とする。また、粉末化したラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物に、必要に応じて賦形剤等の添加剤を加えて混合し、均質化したものを粒状とし、整粒して顆粒剤とする。さらに、前記のように、粒状もしくは成形物としたものを硬カプセルに充填して、硬カプセル剤とし、ラブレ菌(Lactobacillus brevis subsp. coagulans)およびフェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を粉末化し、必要により賦形剤等の添加剤を加えて混合し、均質化したものを、ゼラチン等のカプセル基剤にグリセリンまたはソルビトール等を加えて可塑性を増したもので被包成形して、軟カプセル剤とすることができる。さらにまた、顆粒状とした本発明のインフルエンザウイルス感染予防用組成物を圧縮成形したり、溶媒で湿潤させた後、型に流し込んで成形することにより、錠剤とすることができる。
【0035】
上記の顆粒剤やカプセル剤は、徐放性または腸溶性被膜により処理したり、徐放性または腸溶性の剤皮で処理したりして、徐放性または腸溶性製剤とすることができる。また、錠剤の場合も、糖衣錠やフィルムコーティング錠、徐放錠もしくは腸溶錠とすることができる。
【実施例】
【0036】
さらに、本発明について、実施例により詳細に説明する。
【0037】
[実施例1]インフルエンザウイルス感染予防用組成物
ラブレ菌(Lactobacillus brevis subsp. coagulans NT)はラブレ菌生産用培地にて約30℃で約48時間培養し、培養液を遠心分離(15,000r.p.m.、10分)して集菌し、蒸留水で1回洗浄した後、121℃で15分間加熱滅菌処理した。一方、フェカリス菌(Enterococcus faecalis NT)は乳酸菌フェカリス生産用培地にて37℃で約18時間培養し、培養液を遠心分離(15,000r.p.m.、10分)して集菌し、滅菌水で1回洗浄した後、121℃で15分間加熱滅菌処理した。前記の加熱滅菌処理菌体を、それぞれ乾燥重量にして0.16mgおよび3.0mg混合して、実施例1のインフルエンザウイルス感染予防用組成物とした。本組成物3.16mgは、成人(体重60kg)に対し、1日にラブレ菌(Lactobacillus brevis subsp. coagulans NT)およびフェカリス菌(Enterococcus faecalis NT)の各菌体を、それぞれ菌数にて7.5×108個および1.0×1010個摂取させる量を含有する。
【0038】
[感染予防実験]
実施例1のインフルエンザウイルス感染予防用組成物について、次に示す実験方法により評価した。
【0039】
BALB/cマウス(雌、8週齢)を4群(各群n=10)に分け、表1に示すように実施例1のインフルエンザウイルス感染予防用組成物を投与した。実施例1の組成物は、成人(体重60kg)の1日当たりの摂取量を、体重20gに対する量に換算し、当該換算量の約10倍を、リン酸緩衝生理食塩水0.2mLに懸濁して、経口ゾンデにて投与した。
【0040】
【表1】

【0041】
表1の各群に対し、ペントバルビタール麻酔下にてインフルエンザウイルスA型(H1N1)PR8株1×104pfu(plaque forming unit)を含むリン酸緩衝生理食塩水20μLを経鼻投与して、インフルエンザウイルスを感染させた。インフルエンザウイルス感染後、実施例1の組成物投与群には、さらに1週間、実施例1の感染予防用組成物を投与し、マウスの生死を30日間観察した。
【0042】
実施例1の感染予防用組成物を、インフルエンザウイルス感染の1週間前から投与した群において生存率が向上する傾向が見られたが、実施例1の感染予防用組成物の投与期間を2週間および4週間と延長しても、感染予防効果の増強は認められなかった。同様の感染予防実験を2回繰り返した結果、実施例1の感染予防用組成物をインフルエンザウイルス感染の1週間前から投与した場合に、図1に示すように、対照群との間に、統計学的に有意な感染予防効果が認められた(p<0.05)。
【産業上の利用可能性】
【0043】
以上詳述したように、本発明により、経口摂取に適し、インフルエンザウイルスに対する感染を良好に予防することのできるインフルエンザウイルス感染予防用組成物を提供することができる。本発明のインフルエンザウイルス感染予防用組成物は経口安全性が高く、インフルエンザの流行期間にわたり、長期間連続して経口摂取させることができる。また、重篤な副作用を生じることが少ないため、インフルエンザワクチンや抗ウイルス薬に対し過敏性反応を示す者や、発熱者等の病者に対しても、摂取させることができる。
【特許請求の範囲】
【請求項1】
ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を含有する、インフルエンザウイルス感染予防用組成物。
【請求項2】
ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物とを、1:5〜1:50の乾燥重量比で含有する、請求項1に記載のインフルエンザウイルス感染予防用組成物。
【請求項3】
ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体を菌数にて1×108個以上、フェカリス菌(Enterococcus faecalis)の菌体を菌数にて1×109個以上含有する請求項1または2に記載のインフルエンザウイルス感染予防用組成物。
【請求項4】
請求項1〜3のいずれか1項に記載のインフルエンザウイルス感染予防用組成物を含有する、医薬品。
【請求項5】
請求項1〜3のいずれか1項に記載のインフルエンザウイルス感染予防用組成物を含有する、飲食品。
【請求項1】
ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物を含有する、インフルエンザウイルス感染予防用組成物。
【請求項2】
ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体またはその抽出物と、フェカリス菌(Enterococcus faecalis)の菌体またはその抽出物とを、1:5〜1:50の乾燥重量比で含有する、請求項1に記載のインフルエンザウイルス感染予防用組成物。
【請求項3】
ラブレ菌(Lactobacillus brevis subsp. coagulans)の菌体を菌数にて1×108個以上、フェカリス菌(Enterococcus faecalis)の菌体を菌数にて1×109個以上含有する請求項1または2に記載のインフルエンザウイルス感染予防用組成物。
【請求項4】
請求項1〜3のいずれか1項に記載のインフルエンザウイルス感染予防用組成物を含有する、医薬品。
【請求項5】
請求項1〜3のいずれか1項に記載のインフルエンザウイルス感染予防用組成物を含有する、飲食品。
【図1】




【公開番号】特開2012−136450(P2012−136450A)
【公開日】平成24年7月19日(2012.7.19)
【国際特許分類】
【出願番号】特願2010−288857(P2010−288857)
【出願日】平成22年12月24日(2010.12.24)
【出願人】(392008541)日東薬品工業株式会社 (7)
【Fターム(参考)】
【公開日】平成24年7月19日(2012.7.19)
【国際特許分類】
【出願日】平成22年12月24日(2010.12.24)
【出願人】(392008541)日東薬品工業株式会社 (7)
【Fターム(参考)】
[ Back to top ]

