ウイルス関連悪性腫瘍治療剤
【課題】 成人T細胞白血病、バーキットリンパ腫等のウイルス関連悪性腫瘍の治療や予防に有効な物質を見出し、これを利用する臨床上有用性の高いウイルス関連悪性腫瘍治療剤を開発すること。
【解決手段】 フコキサンチンまたはフコキサンチノールを有効成分とするウイルス関連悪性腫瘍治療剤。
【解決手段】 フコキサンチンまたはフコキサンチノールを有効成分とするウイルス関連悪性腫瘍治療剤。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、ウイルス関連悪性腫瘍治療剤に関し、更に詳細には、成人T細胞白血病、バーキットリンパ腫等、ウイルス感染を起源として発生する悪性腫瘍の治療や予防に有効なウイルス関連悪性腫瘍治療剤に関する。
【背景技術】
【0002】
本明細書において、ウイルス関連悪性腫瘍とは、成人T細胞白血病(adult T-cell leukemia;以下、「ATL」と略す)やバーキットリンパ腫(Burkitt's lymphoma;以下、「BL」と略す)等のウイルス感染を起源として発生する悪性腫瘍を指す。
【0003】
このうち、ATLはヒトレトロウイルス(human retrovirus)であるヒトT細胞白血病ウイルスI型(human T-cell leukemia virus type I;以下、「HTLV−I」と略す)感染を原因とし、CD4+T細胞を起源とする予後不良の白血病・リンパ腫である。日本全国でそのHTLV−I感染者(HTLV−Iキャリア)は約120万人(人口の約1%)と推定されており、日本の中でも南西日本(九州、沖縄、四国地方)に多いことが知られ、また、海外に於いては、カリブ海地域、南アメリカなどの熱帯地方に多いという地域特異性がある。
【0004】
ATLに由来する白血病細胞の多くは、CD4陽性CD8陰性のヘルパーT細胞の表現型を持ち、特異な核変形を伴う。そして、ATLは、C型レトロウイルスであるHTLV−I(当初は、ATLVと呼ばれていた。)が、原因ウイルスであることが明らかにされているが、HTLV−Iキャリアは、ATLだけでなく、悪性腫瘍の発生頻度が高いこと、更には、HAM(HTLV-I-associated myelopathy)と呼ばれる神経疾患及び免疫疾患を引き起こすことが疫学的な調査によって明らかにされ、HTLV−IはATLのみならず、他の疾患にも関与していることが明らかにされつつある。
【0005】
この他、リウマチ様の慢性関節炎やシェーグレン症候群、目の葡萄膜炎などへの関与も指摘されている。HTLV−I感染によるATLは、一旦発症すると、病状は急激に悪化し、その治療は困難を極めているのが現状である。従来の治療法としては、悪性リンパ腫に準じた化学療法或いは放射線療法などがあるが、それらは一時的な対症療法に過ぎず、残念ながら本質的な治療法とはなっていない。
【0006】
一方、バーキットリンパ腫(BL)はヘルペスウイルスの1種であるエプスタイン・バーウイルス(Epstein-Barr virus:以下、「EBV」という)感染が1つの原因としてあげられる血液腫瘍である。免疫不全患者に発症する日和見リンパ腫では、EBV関連のBLが多く、やはり予後不良である。EBVは若年成人の伝染性単核症の原因ウイルスでもあり、その他、上咽頭癌、一部の胃癌やホジキン病との関連も知られている。
【0007】
しかしながら、これらウイルス感染を起源とするウイルス関連悪性腫瘍には、臨床上有効性が高く、かつ安全性にも優れた薬剤がないのが現状であり、新規な医薬品の開発が強く望まれていた。
【発明の開示】
【発明が解決しようとする課題】
【0008】
従って本発明は、ウイルス関連悪性腫瘍の治療や予防に有効な物質を見出し、これを利用する臨床上有用性の高いウイルス関連悪性腫瘍治療剤を開発することをその課題とするものである。
【課題を解決するための手段】
【0009】
本発明者は、永年HTLV−IやEBVの研究に取り組み、臨床上有用なATLやBLの治療薬についても探索してきた。そしてその結果、海藻中に含まれるフコキサンチンおよびフコキサンチノールが、これらのウイルス関連悪性腫瘍に対し特異的に作用し、治療薬としての目的を達成できることを見い出し本発明を完成した。
【0010】
すなわち本発明は、フコキサンチンまたはフコキサンチノールを有効成分とするウイルス関連悪性腫瘍治療剤である。
【0011】
また本発明は、ウイルス関連悪性腫瘍患者にフコキサンチンまたはフコキサンチノールを投与することを特徴とするウイルス関連悪性腫瘍治療方法である。
【0012】
更に本発明は、ウイルス関連悪性腫瘍治療剤製造のための、フコキサンチンまたはフコキサンチノールの使用である。
【発明の効果】
【0013】
本発明のウイルス関連悪性腫瘍治療剤(以下、「悪性腫瘍治療剤」という)の有効成分であるフコキサンチンやフコキサンチノールは、HTLV−1感染細胞や、ATL細胞に対して選択的に作用し、正常細胞には実質的に作用しないものである。すなわち、フコキサンチンやフコキサンチノールが上記細胞等に対してアポトーシスを引き起こす濃度は、β−カロチンやアスタキサンチンのアポトーシス惹起濃度を遙かに下回るものであり、特に、フコキサンチノールは1マイクロモル以下の濃度でアポトーシスを引き起こし、しかも上記細胞の生存率は、ほぼ0である。
【0014】
このように、フコキサンチンやフコキサンチノールは、ウイルス関連悪性腫瘍について特異的に、極めて高い割合でアポトーシスを引き起こすものであるため、これを有効成分とする悪性腫瘍治療剤は、ATLやBL等のウイルス感染を起源として発生する悪性腫瘍の治療、予防に極めて有用なものである。
【発明を実施するための最良の形態】
【0015】
本発明の悪性腫瘍治療剤の有効成分は、フコキサンチンまたはフコキサンチノールである。このうち、フコキサンチンは、我々が日常摂取している海藻、例えば、ワカメ、コンブ、ヒジキ等の褐藻類に含まれる化合物であり、下記式(I)で示される低毒性のカロテノイドである。また、フコキサンチノールは、このフコキサンチンの加水分解により得られる脱アセチル化物であり下記式(II)で示されるものである。
【0016】
【化1】

【0017】
ところで、上記のフコキサンチンには、インビトロ(in vitro)での神経芽細胞腫、前立腺癌、悪性黒色腫、大腸癌、急性前骨髄球性白血病細胞への増殖抑制活性や大腸癌や十二指腸腫瘍の発癌抑制活性があることは知られていたが、これらの癌とは異なるウイルス関連白血病・リンパ腫等のウイルス関連悪性腫瘍に対する優れた抗腫瘍活性を有することは全く知られていない。更に、フコキサンチンの脱アセチル化物であるフコキサンチノールが、フコキサンチンに比べ、更に優れたウイルス関連悪性腫瘍に対する優れた抗腫瘍活性を有することは、全く知られていないことであった。
【0018】
このように、フコキサンチンや、フコキサンチノールが、ウイルス関連悪性腫瘍に対する治療剤等として、ATLやBLの予防及び治療に効果的に使用されるということは、本発明者の新知見によるものである。
【0019】
上記のように、フコキサンチンは、ワカメ、コンブ、ヒジキ等の褐藻類に含まれる化合物であるが、本発明で使用するフコキサンチンとして好ましいものの一例としては、ホンダワラ科の海藻や乾燥ワカメ等の褐藻をメタノールやアセトンなどの有機溶媒に浸し、18時間程度、室温、遮光条件で抽出し、得られた抽出液を濃縮後、ダイヤイオンHP20(三菱化学)、Toyopear1 HW40F(東ソー)、ODS(和光純薬、Wakogel50C18)などを用いた液体クロマトグラフィーによる分離を行い、さらに再結晶操作を繰り返すことにより得られるフコキサンチン精製品が挙げられる。
【0020】
また、フコキサンチノールは、上記フコキサンチンを加水分解することにより得られた脱アセチル化物であり、例えば、フコキサンチンに、種々の加水分解酵素を作用させることにより得られる。
【0021】
より具体的に、本発明で用いられるフコキサンチノールの一例としては、公知文献(T.Matsuno,M.Ookubo,T.NishizawaandI.Shimizu,Chem.Pharm.Bull.:32,4309−4315,1984)に記載の方法を一部改変したリパーゼ分解法によって得られるフコキサンチノールを挙げることができる。
【0022】
上記したフコキサンチンあるいはフコキサンチノールは、必要により、公知の精製手段により精製した後、本発明の悪性腫瘍治療剤の有効成分として使用することができる。
【0023】
すなわち、本発明の悪性腫瘍治療剤を製造するに当たっては、フコキサンチンあるいはフコキサンチノール(以下、「フコキサンチン類」ということがある)を公知の医薬担体と組み合わせることにより、悪性腫瘍治療剤とすることができる。
【0024】
この悪性腫瘍治療剤は、錠剤、カプセル剤、粉剤、顆粒剤等や、液剤、シロップ剤等の経口剤や、注射剤、点滴用剤、外用剤、坐剤、貼付剤等の非経口剤とすることができる。
【0025】
上記の各製剤の製造において使用しうる医薬担体の例としては、デンプン、乳糖、ショ糖、マンニトール、コーンスターチ、結晶セルロース、カルボキシメチルセルロース、ケイ酸糖の賦形剤、ポリビニルアルコール、ポリビニルピロリドン、ポリビニルエーテル、エチルセルロース、アラビアゴム、トラガント、ゼラチン、ヒドロキシプロピルセルロース、デキストリン、ペクチン等結合剤、ステアリン酸マグネシウム、タルク、ポリエチレングリコール等の滑沢剤、崩壊剤、崩壊助剤、安定剤の公知の固形剤用担体や、水、エチルアルコール、エチレングリコール、グリセリン等の液剤成分、ポリオキシエチレンソルビタン脂肪酸エステル等の界面活性剤、ブドウ糖、アミノ酸等の呈味成分、溶解補助剤、着色料、保存料等の液剤用担体を挙げることができる。また、外用剤、坐剤、貼付剤については、これらの剤型に応じた公知の担体を使用することができる。
【0026】
本発明の悪性腫瘍治療剤に配合されるフコキサンチン類の量は、対象疾患、疾患程度、患者年齢等によっても相違するが、例えば、フコキサンチンを有効成分とする経口製剤の場合は、大人一人当たり一日量として、0.1mgないし300mg程度とすることが好ましく、血管内投与の場合は、その10/1程度とすることが好ましい。
【0027】
また、フコキサンチノールを有効成分とする経口製剤の場合は、大人一人当たり一日量として、0.05mgないし100mg程度とすることが好ましく、血管内投与の場合は、その10/1程度とすることが好ましい。
【実施例】
【0028】
以下、参考例および実施例を挙げ、本発明を更に詳しく説明するが、本発明はこれら実施例等に何ら制約されるものではない。
【0029】
参 考 例 1
フコキサンチンの調製:
細切した乾燥ホンダワラ3.15Kgを、メタノール20Lを用い、室温、18時間の条件で2回抽出した、抽出液を1Lまで濃縮し、ヘキサン800mLで2回分配した。メタノール層を濃縮し、HP20カラム(φ55×150mm)に添加し、メタノール1.5Lおよびアセトン600mLで溶出した。メタノール溶出液を濃縮し、HW40Fカラム(φ30×500mm)に添加し、メタノールで溶出した。フコキサンチン画分を濃縮し、90%メタノールからの再結晶操作を2回行い、精製フコキサンチンを200mg得た。HPLCおよび1H−NMRスペクトルにより95%以上の純度であること確認し、NMRおよびMSスペクトルによりその化学構造を確認した。以下の実施例では、この精製フコキサンチンをフコキサンチンとして用いた。
【0030】
参 考 例 2
フコキサンチノールの調製:
参考例1で得たフコキサンチン精製品100mgをアセトン2mLに溶解した。一方、リパーゼとして、Candidarugosa由来のリパーゼ(Sigma社)2gを用い、これを0.1Mリン酸緩衝液(pH7.0)22.5mLに溶解した。両溶液を混ぜ合わせ、37℃で18時間加温した。反応液をろ過し、溶媒除去した後、残渣をアセトン50mLで抽出し、フコキサンチン反応物を回収した。反応物について再度、上記のリパーゼ反応を行った。フコキサンチン反応物をHPLC(ナカライテスク製CosmosilODS5C18−AR−II20×250mm、80%MeOH、5mL/min)により分離・精製を行い、フコキサンチノール精製物を得た。HPLCおよび1H−NMRスペクトルにより95%以上の純度であること確認し、NMRおよびMSスペクトルにより化学構造を確認した。以下の実施例では、この精製フコキサンチノールをフコキサンチノールとして用いた。
【0031】
実 施 例 1
ウイルス感染細胞株増殖能の測定:
( 方 法 )
それぞれ、10%牛胎児血清加RPMI1640培地により2×105個/mLに調整したHTLV−I感染T細胞株(MT−2、MT−4、HUT−102、ED−40515(−))、EBV感染B細胞株(Raji、Daudi、B95−8/BJAB、B95−8/Ramos、LCL−Ka、LCL−Ku)、子宮頚癌細胞株(HeLa)、慢性骨髄性白血病細胞株(K−562)を、細胞数が1×104個/穴となるように、96穴プレートに蒔いた。
【0032】
次いで、最終濃度が10、5、2.5、1.25、0.625μM(フコキサンチン、フコキサンチノール)あるいは10、5、2.5μM(β−カロテン、アスタキサンチン)になるように、フコキサンチン、フコキサンチノール、β−カロテン、アスタキサンチンを50μL/穴添加し、37℃で、24時間培養した。その後、発色基質としてWST−8(和光純薬工業社製)を5μL/穴添加し、37℃で4時間培養した。培養後、マイクロプレートリーダーを用いて、450nmの吸光度を測定し、下式により細胞の生存率を求めた。
【0033】
[数1]
細胞生存率(%)= [ 1 − (A − B)/A ] × 100
A:薬剤無処理時の吸光度
B:薬剤処理時の吸光度
【0034】
( 結 果 )
フコキサンチンおよびフコキサンチノールが、HTLV−I感染T細胞株やEBV感染B細胞株の増殖能に与える影響を図1および図2に示した。この結果から明らかなように、フコキサンチンおよびフコキサンチノールは、濃度依存性にすべてのHTLV−I感染T細胞株とEBV感染BL細胞株の増殖を抑制した。また、これら細胞株の増殖抑制能は、フコキサンチンに比べ、フコキサンチノールのほうが有意に高かった。
【0035】
一方、β−カロテンおよびアスタキサンチンが、HTLV−I感染T細胞株の増殖能に対する影響を同様な試験で調べた結果を図3に示す。この結果から明らかなように、他のキサンチン類は、HTLV−I感染T細胞株の増殖に軽微な影響を及ぼすのみであり、フコキサンチン類が優れた増殖抑制能を有することが示された。
【0036】
実 施 例 2
健常人および成人T細胞白血病(ATL)患者末梢血単核球の増殖能の測定
【0037】
( 方 法 )
まず、末梢血単核球(PBMC)をフィコール(Ficol)遠心比重法により分離し、これを10%牛胎児血清加RPMI1640培地を用いて2×106/mLに調整した後、細胞数が1×105個/穴となるように、96穴プレートに蒔いた。
【0038】
次いで、最終濃度が10、5、2.5、1.25、0.625μM(フコキサンチン)あるいは2.5、1.25、0.625μM(フコキサンチノール)になるように、フコキサンチンおよびフコキサンチノールを50μL/穴添加し、37℃で24時間培養した。その後、WST−8を5μL/穴添加し、37℃で4時間培養した。培養後、マイクロプレートリーダーを用い、450nmの吸光度を測定し、前記の式により、細胞の生存率を求めた。
【0039】
( 結 果 )
フコキサンチンおよびフコキサンチノールが、健常人(1名)のPBMCおよび成人T細胞白血病(ATL、5名)患者のPBMCの増殖能に与える影響を図4に示した。この結果から明らかなように、フコキサンチンおよびフコキサンチノールはATL患者白血病細胞に対しても濃度依存性に増殖抑制効果を認めたが、健常人のPBMCに対する毒性は認められなかった。また、フコキサンチンに比べ、フコキサンチノールのほうが増殖能に及ぼす影響は強かった。
【0040】
実 施 例 3
HTLV−I感染細胞株の細胞周期測定
( 方 法 )
HTLV−I感染細胞株(MT−2、MT−4、HUT−102、ED−40515(−))を、1×106細胞でセルカルチャープレートに蒔き、これにフコキサンチンを5μMで添加し、37℃で24時間培養した。24時間後に細胞を回収し、これをヨウ化プロピジウムで染色後、フローサイトメーターにてDNA含量を測定した。このDNA含量の結果から、各細胞周期の細胞群の分布を算出することにより、各細胞の細胞周期を判定した。
【0041】
( 結 果 )
フコキサンチンが、HTLV−I感染細胞株の細胞周期に与える影響を図5に示した。
この結果、GI期の細胞群が増加していたことから、フコキサンチンはすべてのHTLV−I感染細胞株の細胞周期をG1期で停止させたことが示された。
【0042】
実 施 例 4
HTLV−I感染細胞株のアポトーシス測定
( 方 法 )
HTLV−I感染細胞株(MT−2、MT−4、HUT−102、ED−40515(−))を、1×106細胞でセルカルチャープレートに蒔き、これに、種々の濃度のフコキサンチン(10、5、2.5μM)あるいはフコキサンチノール(10、5、2.5、1.25、0.625μM)を添加し、37℃で24時間培養した。24時間後に細胞を回収し、アネキシンVで染色後、フローサイトメーターを用い、アポトーシス陽性細胞率(%)を測定した。
【0043】
( 結 果 )
フコキサンチノールが、HTLV−I感染細胞株のアポトーシスに与える影響を図6に、フコキサンチンおよびフコキサンチノールの濃度と、MT−2のアポトーシスの関係を図7および図8に示した。この結果からフコキサンチンはすべてのHTLV−I感染細胞株にアポトーシスを誘導し(図6)、その作用は濃度依存性であることが示された(図7)。また、フコキサンチノールもHTLV−I感染細胞株であるMT−2にアポトーシスを誘導し、その効果はフコキサンチンに比べ強いことが示された(図8)。
【産業上の利用可能性】
【0044】
以上の、実施例で示すように、フコキサンチンおよびフコキサンチノールはHTLV−I感染T細胞株、EBV感染BL細胞株、EBV感染B細胞株、ATL細胞等のウイルス関連悪性腫瘍の生存率を濃度依存性に低下させるものであり、しかも、健常人末梢血単核球に対しては、何の影響も与えるものでなかった。
【0045】
従って、本発明のウイルス関連悪性腫瘍治療剤は、ウイルス感染リンパ球に選択的な抗腫瘍効果を有するものであり、実用性のある新しいATLあるいはバーキットリンパ腫等の治療ないし予防剤として、有利に使用することができるものである。
【図面の簡単な説明】
【0046】
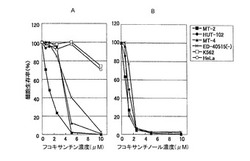
【図1】フコキサンチンおよびフコキサンチノールが、HTLV−I感染T細胞株の増殖能に与える影響を示した図である。Aはフコキサンチン、Bはフコキサンチノールについてのものである。
【図2】フコキサンチンおよびフコキサンチノールが、EBV感染B細胞株の増殖能に与える影響を示した図である。Aはフコキサンチン、Bはフコキサンチノールについてのものである。
【図3】β−カロテンおよびアスタキサンチンが、HTLV−I感染T細胞株の増殖能に与える影響を示した図である。Aはβ−カロテン、Bはアスタキサンチンについてのものである。
【図4】フコキサンチンおよびフコキサンチノールが、健常人およびATL患者末梢血単核球の生存に与える影響を示した図である。Aはフコキサンチン、Bはフコキサンチノールについてのものである。
【図5】フコキサンチンが、HTLV−I感染細胞株の細胞周期に与える影響を示した図である。
【図6】フコキサンチンが、HTLV−I感染細胞株のアポトーシスに与える影響を示した図である。
【図7】フコキサンチンが、濃度依存性にHTLV−I感染細胞株であるMT−2のアポトーシスに与える影響を示した図である。
【図8】フコキサンチノールが、濃度依存性にHTLV−I感染細胞株であるMT−2のアポトーシスに与える影響を示した図である。 以 上
【技術分野】
【0001】
本発明は、ウイルス関連悪性腫瘍治療剤に関し、更に詳細には、成人T細胞白血病、バーキットリンパ腫等、ウイルス感染を起源として発生する悪性腫瘍の治療や予防に有効なウイルス関連悪性腫瘍治療剤に関する。
【背景技術】
【0002】
本明細書において、ウイルス関連悪性腫瘍とは、成人T細胞白血病(adult T-cell leukemia;以下、「ATL」と略す)やバーキットリンパ腫(Burkitt's lymphoma;以下、「BL」と略す)等のウイルス感染を起源として発生する悪性腫瘍を指す。
【0003】
このうち、ATLはヒトレトロウイルス(human retrovirus)であるヒトT細胞白血病ウイルスI型(human T-cell leukemia virus type I;以下、「HTLV−I」と略す)感染を原因とし、CD4+T細胞を起源とする予後不良の白血病・リンパ腫である。日本全国でそのHTLV−I感染者(HTLV−Iキャリア)は約120万人(人口の約1%)と推定されており、日本の中でも南西日本(九州、沖縄、四国地方)に多いことが知られ、また、海外に於いては、カリブ海地域、南アメリカなどの熱帯地方に多いという地域特異性がある。
【0004】
ATLに由来する白血病細胞の多くは、CD4陽性CD8陰性のヘルパーT細胞の表現型を持ち、特異な核変形を伴う。そして、ATLは、C型レトロウイルスであるHTLV−I(当初は、ATLVと呼ばれていた。)が、原因ウイルスであることが明らかにされているが、HTLV−Iキャリアは、ATLだけでなく、悪性腫瘍の発生頻度が高いこと、更には、HAM(HTLV-I-associated myelopathy)と呼ばれる神経疾患及び免疫疾患を引き起こすことが疫学的な調査によって明らかにされ、HTLV−IはATLのみならず、他の疾患にも関与していることが明らかにされつつある。
【0005】
この他、リウマチ様の慢性関節炎やシェーグレン症候群、目の葡萄膜炎などへの関与も指摘されている。HTLV−I感染によるATLは、一旦発症すると、病状は急激に悪化し、その治療は困難を極めているのが現状である。従来の治療法としては、悪性リンパ腫に準じた化学療法或いは放射線療法などがあるが、それらは一時的な対症療法に過ぎず、残念ながら本質的な治療法とはなっていない。
【0006】
一方、バーキットリンパ腫(BL)はヘルペスウイルスの1種であるエプスタイン・バーウイルス(Epstein-Barr virus:以下、「EBV」という)感染が1つの原因としてあげられる血液腫瘍である。免疫不全患者に発症する日和見リンパ腫では、EBV関連のBLが多く、やはり予後不良である。EBVは若年成人の伝染性単核症の原因ウイルスでもあり、その他、上咽頭癌、一部の胃癌やホジキン病との関連も知られている。
【0007】
しかしながら、これらウイルス感染を起源とするウイルス関連悪性腫瘍には、臨床上有効性が高く、かつ安全性にも優れた薬剤がないのが現状であり、新規な医薬品の開発が強く望まれていた。
【発明の開示】
【発明が解決しようとする課題】
【0008】
従って本発明は、ウイルス関連悪性腫瘍の治療や予防に有効な物質を見出し、これを利用する臨床上有用性の高いウイルス関連悪性腫瘍治療剤を開発することをその課題とするものである。
【課題を解決するための手段】
【0009】
本発明者は、永年HTLV−IやEBVの研究に取り組み、臨床上有用なATLやBLの治療薬についても探索してきた。そしてその結果、海藻中に含まれるフコキサンチンおよびフコキサンチノールが、これらのウイルス関連悪性腫瘍に対し特異的に作用し、治療薬としての目的を達成できることを見い出し本発明を完成した。
【0010】
すなわち本発明は、フコキサンチンまたはフコキサンチノールを有効成分とするウイルス関連悪性腫瘍治療剤である。
【0011】
また本発明は、ウイルス関連悪性腫瘍患者にフコキサンチンまたはフコキサンチノールを投与することを特徴とするウイルス関連悪性腫瘍治療方法である。
【0012】
更に本発明は、ウイルス関連悪性腫瘍治療剤製造のための、フコキサンチンまたはフコキサンチノールの使用である。
【発明の効果】
【0013】
本発明のウイルス関連悪性腫瘍治療剤(以下、「悪性腫瘍治療剤」という)の有効成分であるフコキサンチンやフコキサンチノールは、HTLV−1感染細胞や、ATL細胞に対して選択的に作用し、正常細胞には実質的に作用しないものである。すなわち、フコキサンチンやフコキサンチノールが上記細胞等に対してアポトーシスを引き起こす濃度は、β−カロチンやアスタキサンチンのアポトーシス惹起濃度を遙かに下回るものであり、特に、フコキサンチノールは1マイクロモル以下の濃度でアポトーシスを引き起こし、しかも上記細胞の生存率は、ほぼ0である。
【0014】
このように、フコキサンチンやフコキサンチノールは、ウイルス関連悪性腫瘍について特異的に、極めて高い割合でアポトーシスを引き起こすものであるため、これを有効成分とする悪性腫瘍治療剤は、ATLやBL等のウイルス感染を起源として発生する悪性腫瘍の治療、予防に極めて有用なものである。
【発明を実施するための最良の形態】
【0015】
本発明の悪性腫瘍治療剤の有効成分は、フコキサンチンまたはフコキサンチノールである。このうち、フコキサンチンは、我々が日常摂取している海藻、例えば、ワカメ、コンブ、ヒジキ等の褐藻類に含まれる化合物であり、下記式(I)で示される低毒性のカロテノイドである。また、フコキサンチノールは、このフコキサンチンの加水分解により得られる脱アセチル化物であり下記式(II)で示されるものである。
【0016】
【化1】

【0017】
ところで、上記のフコキサンチンには、インビトロ(in vitro)での神経芽細胞腫、前立腺癌、悪性黒色腫、大腸癌、急性前骨髄球性白血病細胞への増殖抑制活性や大腸癌や十二指腸腫瘍の発癌抑制活性があることは知られていたが、これらの癌とは異なるウイルス関連白血病・リンパ腫等のウイルス関連悪性腫瘍に対する優れた抗腫瘍活性を有することは全く知られていない。更に、フコキサンチンの脱アセチル化物であるフコキサンチノールが、フコキサンチンに比べ、更に優れたウイルス関連悪性腫瘍に対する優れた抗腫瘍活性を有することは、全く知られていないことであった。
【0018】
このように、フコキサンチンや、フコキサンチノールが、ウイルス関連悪性腫瘍に対する治療剤等として、ATLやBLの予防及び治療に効果的に使用されるということは、本発明者の新知見によるものである。
【0019】
上記のように、フコキサンチンは、ワカメ、コンブ、ヒジキ等の褐藻類に含まれる化合物であるが、本発明で使用するフコキサンチンとして好ましいものの一例としては、ホンダワラ科の海藻や乾燥ワカメ等の褐藻をメタノールやアセトンなどの有機溶媒に浸し、18時間程度、室温、遮光条件で抽出し、得られた抽出液を濃縮後、ダイヤイオンHP20(三菱化学)、Toyopear1 HW40F(東ソー)、ODS(和光純薬、Wakogel50C18)などを用いた液体クロマトグラフィーによる分離を行い、さらに再結晶操作を繰り返すことにより得られるフコキサンチン精製品が挙げられる。
【0020】
また、フコキサンチノールは、上記フコキサンチンを加水分解することにより得られた脱アセチル化物であり、例えば、フコキサンチンに、種々の加水分解酵素を作用させることにより得られる。
【0021】
より具体的に、本発明で用いられるフコキサンチノールの一例としては、公知文献(T.Matsuno,M.Ookubo,T.NishizawaandI.Shimizu,Chem.Pharm.Bull.:32,4309−4315,1984)に記載の方法を一部改変したリパーゼ分解法によって得られるフコキサンチノールを挙げることができる。
【0022】
上記したフコキサンチンあるいはフコキサンチノールは、必要により、公知の精製手段により精製した後、本発明の悪性腫瘍治療剤の有効成分として使用することができる。
【0023】
すなわち、本発明の悪性腫瘍治療剤を製造するに当たっては、フコキサンチンあるいはフコキサンチノール(以下、「フコキサンチン類」ということがある)を公知の医薬担体と組み合わせることにより、悪性腫瘍治療剤とすることができる。
【0024】
この悪性腫瘍治療剤は、錠剤、カプセル剤、粉剤、顆粒剤等や、液剤、シロップ剤等の経口剤や、注射剤、点滴用剤、外用剤、坐剤、貼付剤等の非経口剤とすることができる。
【0025】
上記の各製剤の製造において使用しうる医薬担体の例としては、デンプン、乳糖、ショ糖、マンニトール、コーンスターチ、結晶セルロース、カルボキシメチルセルロース、ケイ酸糖の賦形剤、ポリビニルアルコール、ポリビニルピロリドン、ポリビニルエーテル、エチルセルロース、アラビアゴム、トラガント、ゼラチン、ヒドロキシプロピルセルロース、デキストリン、ペクチン等結合剤、ステアリン酸マグネシウム、タルク、ポリエチレングリコール等の滑沢剤、崩壊剤、崩壊助剤、安定剤の公知の固形剤用担体や、水、エチルアルコール、エチレングリコール、グリセリン等の液剤成分、ポリオキシエチレンソルビタン脂肪酸エステル等の界面活性剤、ブドウ糖、アミノ酸等の呈味成分、溶解補助剤、着色料、保存料等の液剤用担体を挙げることができる。また、外用剤、坐剤、貼付剤については、これらの剤型に応じた公知の担体を使用することができる。
【0026】
本発明の悪性腫瘍治療剤に配合されるフコキサンチン類の量は、対象疾患、疾患程度、患者年齢等によっても相違するが、例えば、フコキサンチンを有効成分とする経口製剤の場合は、大人一人当たり一日量として、0.1mgないし300mg程度とすることが好ましく、血管内投与の場合は、その10/1程度とすることが好ましい。
【0027】
また、フコキサンチノールを有効成分とする経口製剤の場合は、大人一人当たり一日量として、0.05mgないし100mg程度とすることが好ましく、血管内投与の場合は、その10/1程度とすることが好ましい。
【実施例】
【0028】
以下、参考例および実施例を挙げ、本発明を更に詳しく説明するが、本発明はこれら実施例等に何ら制約されるものではない。
【0029】
参 考 例 1
フコキサンチンの調製:
細切した乾燥ホンダワラ3.15Kgを、メタノール20Lを用い、室温、18時間の条件で2回抽出した、抽出液を1Lまで濃縮し、ヘキサン800mLで2回分配した。メタノール層を濃縮し、HP20カラム(φ55×150mm)に添加し、メタノール1.5Lおよびアセトン600mLで溶出した。メタノール溶出液を濃縮し、HW40Fカラム(φ30×500mm)に添加し、メタノールで溶出した。フコキサンチン画分を濃縮し、90%メタノールからの再結晶操作を2回行い、精製フコキサンチンを200mg得た。HPLCおよび1H−NMRスペクトルにより95%以上の純度であること確認し、NMRおよびMSスペクトルによりその化学構造を確認した。以下の実施例では、この精製フコキサンチンをフコキサンチンとして用いた。
【0030】
参 考 例 2
フコキサンチノールの調製:
参考例1で得たフコキサンチン精製品100mgをアセトン2mLに溶解した。一方、リパーゼとして、Candidarugosa由来のリパーゼ(Sigma社)2gを用い、これを0.1Mリン酸緩衝液(pH7.0)22.5mLに溶解した。両溶液を混ぜ合わせ、37℃で18時間加温した。反応液をろ過し、溶媒除去した後、残渣をアセトン50mLで抽出し、フコキサンチン反応物を回収した。反応物について再度、上記のリパーゼ反応を行った。フコキサンチン反応物をHPLC(ナカライテスク製CosmosilODS5C18−AR−II20×250mm、80%MeOH、5mL/min)により分離・精製を行い、フコキサンチノール精製物を得た。HPLCおよび1H−NMRスペクトルにより95%以上の純度であること確認し、NMRおよびMSスペクトルにより化学構造を確認した。以下の実施例では、この精製フコキサンチノールをフコキサンチノールとして用いた。
【0031】
実 施 例 1
ウイルス感染細胞株増殖能の測定:
( 方 法 )
それぞれ、10%牛胎児血清加RPMI1640培地により2×105個/mLに調整したHTLV−I感染T細胞株(MT−2、MT−4、HUT−102、ED−40515(−))、EBV感染B細胞株(Raji、Daudi、B95−8/BJAB、B95−8/Ramos、LCL−Ka、LCL−Ku)、子宮頚癌細胞株(HeLa)、慢性骨髄性白血病細胞株(K−562)を、細胞数が1×104個/穴となるように、96穴プレートに蒔いた。
【0032】
次いで、最終濃度が10、5、2.5、1.25、0.625μM(フコキサンチン、フコキサンチノール)あるいは10、5、2.5μM(β−カロテン、アスタキサンチン)になるように、フコキサンチン、フコキサンチノール、β−カロテン、アスタキサンチンを50μL/穴添加し、37℃で、24時間培養した。その後、発色基質としてWST−8(和光純薬工業社製)を5μL/穴添加し、37℃で4時間培養した。培養後、マイクロプレートリーダーを用いて、450nmの吸光度を測定し、下式により細胞の生存率を求めた。
【0033】
[数1]
細胞生存率(%)= [ 1 − (A − B)/A ] × 100
A:薬剤無処理時の吸光度
B:薬剤処理時の吸光度
【0034】
( 結 果 )
フコキサンチンおよびフコキサンチノールが、HTLV−I感染T細胞株やEBV感染B細胞株の増殖能に与える影響を図1および図2に示した。この結果から明らかなように、フコキサンチンおよびフコキサンチノールは、濃度依存性にすべてのHTLV−I感染T細胞株とEBV感染BL細胞株の増殖を抑制した。また、これら細胞株の増殖抑制能は、フコキサンチンに比べ、フコキサンチノールのほうが有意に高かった。
【0035】
一方、β−カロテンおよびアスタキサンチンが、HTLV−I感染T細胞株の増殖能に対する影響を同様な試験で調べた結果を図3に示す。この結果から明らかなように、他のキサンチン類は、HTLV−I感染T細胞株の増殖に軽微な影響を及ぼすのみであり、フコキサンチン類が優れた増殖抑制能を有することが示された。
【0036】
実 施 例 2
健常人および成人T細胞白血病(ATL)患者末梢血単核球の増殖能の測定
【0037】
( 方 法 )
まず、末梢血単核球(PBMC)をフィコール(Ficol)遠心比重法により分離し、これを10%牛胎児血清加RPMI1640培地を用いて2×106/mLに調整した後、細胞数が1×105個/穴となるように、96穴プレートに蒔いた。
【0038】
次いで、最終濃度が10、5、2.5、1.25、0.625μM(フコキサンチン)あるいは2.5、1.25、0.625μM(フコキサンチノール)になるように、フコキサンチンおよびフコキサンチノールを50μL/穴添加し、37℃で24時間培養した。その後、WST−8を5μL/穴添加し、37℃で4時間培養した。培養後、マイクロプレートリーダーを用い、450nmの吸光度を測定し、前記の式により、細胞の生存率を求めた。
【0039】
( 結 果 )
フコキサンチンおよびフコキサンチノールが、健常人(1名)のPBMCおよび成人T細胞白血病(ATL、5名)患者のPBMCの増殖能に与える影響を図4に示した。この結果から明らかなように、フコキサンチンおよびフコキサンチノールはATL患者白血病細胞に対しても濃度依存性に増殖抑制効果を認めたが、健常人のPBMCに対する毒性は認められなかった。また、フコキサンチンに比べ、フコキサンチノールのほうが増殖能に及ぼす影響は強かった。
【0040】
実 施 例 3
HTLV−I感染細胞株の細胞周期測定
( 方 法 )
HTLV−I感染細胞株(MT−2、MT−4、HUT−102、ED−40515(−))を、1×106細胞でセルカルチャープレートに蒔き、これにフコキサンチンを5μMで添加し、37℃で24時間培養した。24時間後に細胞を回収し、これをヨウ化プロピジウムで染色後、フローサイトメーターにてDNA含量を測定した。このDNA含量の結果から、各細胞周期の細胞群の分布を算出することにより、各細胞の細胞周期を判定した。
【0041】
( 結 果 )
フコキサンチンが、HTLV−I感染細胞株の細胞周期に与える影響を図5に示した。
この結果、GI期の細胞群が増加していたことから、フコキサンチンはすべてのHTLV−I感染細胞株の細胞周期をG1期で停止させたことが示された。
【0042】
実 施 例 4
HTLV−I感染細胞株のアポトーシス測定
( 方 法 )
HTLV−I感染細胞株(MT−2、MT−4、HUT−102、ED−40515(−))を、1×106細胞でセルカルチャープレートに蒔き、これに、種々の濃度のフコキサンチン(10、5、2.5μM)あるいはフコキサンチノール(10、5、2.5、1.25、0.625μM)を添加し、37℃で24時間培養した。24時間後に細胞を回収し、アネキシンVで染色後、フローサイトメーターを用い、アポトーシス陽性細胞率(%)を測定した。
【0043】
( 結 果 )
フコキサンチノールが、HTLV−I感染細胞株のアポトーシスに与える影響を図6に、フコキサンチンおよびフコキサンチノールの濃度と、MT−2のアポトーシスの関係を図7および図8に示した。この結果からフコキサンチンはすべてのHTLV−I感染細胞株にアポトーシスを誘導し(図6)、その作用は濃度依存性であることが示された(図7)。また、フコキサンチノールもHTLV−I感染細胞株であるMT−2にアポトーシスを誘導し、その効果はフコキサンチンに比べ強いことが示された(図8)。
【産業上の利用可能性】
【0044】
以上の、実施例で示すように、フコキサンチンおよびフコキサンチノールはHTLV−I感染T細胞株、EBV感染BL細胞株、EBV感染B細胞株、ATL細胞等のウイルス関連悪性腫瘍の生存率を濃度依存性に低下させるものであり、しかも、健常人末梢血単核球に対しては、何の影響も与えるものでなかった。
【0045】
従って、本発明のウイルス関連悪性腫瘍治療剤は、ウイルス感染リンパ球に選択的な抗腫瘍効果を有するものであり、実用性のある新しいATLあるいはバーキットリンパ腫等の治療ないし予防剤として、有利に使用することができるものである。
【図面の簡単な説明】
【0046】
【図1】フコキサンチンおよびフコキサンチノールが、HTLV−I感染T細胞株の増殖能に与える影響を示した図である。Aはフコキサンチン、Bはフコキサンチノールについてのものである。
【図2】フコキサンチンおよびフコキサンチノールが、EBV感染B細胞株の増殖能に与える影響を示した図である。Aはフコキサンチン、Bはフコキサンチノールについてのものである。
【図3】β−カロテンおよびアスタキサンチンが、HTLV−I感染T細胞株の増殖能に与える影響を示した図である。Aはβ−カロテン、Bはアスタキサンチンについてのものである。
【図4】フコキサンチンおよびフコキサンチノールが、健常人およびATL患者末梢血単核球の生存に与える影響を示した図である。Aはフコキサンチン、Bはフコキサンチノールについてのものである。
【図5】フコキサンチンが、HTLV−I感染細胞株の細胞周期に与える影響を示した図である。
【図6】フコキサンチンが、HTLV−I感染細胞株のアポトーシスに与える影響を示した図である。
【図7】フコキサンチンが、濃度依存性にHTLV−I感染細胞株であるMT−2のアポトーシスに与える影響を示した図である。
【図8】フコキサンチノールが、濃度依存性にHTLV−I感染細胞株であるMT−2のアポトーシスに与える影響を示した図である。 以 上
【特許請求の範囲】
【請求項1】
フコキサンチンまたはフコキサンチノールを有効成分とするウイルス関連悪性腫瘍治療剤。
【請求項2】
成人T細胞白血病またはバーキットリンパ腫を治療、予防するものである請求項第1項記載のウイルス関連悪性腫瘍治療剤。
【請求項3】
経口投与形態である請求項第1項または第2項記載のウイルス関連悪性腫瘍治療剤。
【請求項4】
非経口投与形態である請求項第1項または第2項記載のウイルス関連悪性腫瘍治療剤。
【請求項1】
フコキサンチンまたはフコキサンチノールを有効成分とするウイルス関連悪性腫瘍治療剤。
【請求項2】
成人T細胞白血病またはバーキットリンパ腫を治療、予防するものである請求項第1項記載のウイルス関連悪性腫瘍治療剤。
【請求項3】
経口投与形態である請求項第1項または第2項記載のウイルス関連悪性腫瘍治療剤。
【請求項4】
非経口投与形態である請求項第1項または第2項記載のウイルス関連悪性腫瘍治療剤。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【公開番号】特開2008−19174(P2008−19174A)
【公開日】平成20年1月31日(2008.1.31)
【国際特許分類】
【出願番号】特願2006−190076(P2006−190076)
【出願日】平成18年7月11日(2006.7.11)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成18年3月8日 沖縄産学官連携推進協議会主催の「第1回沖縄産学官連携推進フォーラム」において文書をもって発表
【出願人】(592234908)株式会社トロピカルテクノセンター (14)
【出願人】(504145308)国立大学法人 琉球大学 (100)
【Fターム(参考)】
【公開日】平成20年1月31日(2008.1.31)
【国際特許分類】
【出願日】平成18年7月11日(2006.7.11)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成18年3月8日 沖縄産学官連携推進協議会主催の「第1回沖縄産学官連携推進フォーラム」において文書をもって発表
【出願人】(592234908)株式会社トロピカルテクノセンター (14)
【出願人】(504145308)国立大学法人 琉球大学 (100)
【Fターム(参考)】
[ Back to top ]

