エピメタボリックシフター、多次元細胞内分子、または環境影響因子を使用する腫瘍性障害の診断のための方法
エピメタボリックシフター、多次元細胞内分子、または環境影響因子を使用して、ヒトにおいて腫瘍性障害を診断するための方法および製剤が記載される。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
被験体が腫瘍性障害に罹患しているかどうかを評価する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記被験体が腫瘍性障害に罹患していることの指標となり、それにより、前記被験体が腫瘍性障害に罹患しているかどうかを評価する、前記方法。
【請求項2】
被験体が腫瘍性障害に罹患しているかどうかを評価する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節される;ならびに、
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記被験体が腫瘍性障害に罹患していることの指標となり、それにより、前記被験体が腫瘍性障害に罹患しているかどうかを評価する、前記方法。
【請求項3】
被験体に腫瘍性障害を発症する素因があるかどうかを予後診断する方法であって:
(1)前記被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および5〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記被験体に腫瘍性障害を発症する素因があることの指標となり、それにより、前記被験体に腫瘍性障害を発症する素因があるかどうかを予後診断する、前記方法。
【請求項4】
被験体に腫瘍性障害を発症する素因があるかどうかを予後診断する方法であって:
(1)前記被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記被験体に腫瘍性障害を発症する素因があることの指標となり、それにより、前記被験体に腫瘍性障害を発症する素因があるかどうかを予後診断する、前記方法。
【請求項5】
被験体において腫瘍性障害の再発を予後診断する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、腫瘍性障害の再発の指標となり、それにより、前記被験体における腫瘍性障害の再発を予後診断する、前記方法。
【請求項6】
被験体において腫瘍性障害の再発を予後診断する方法であって:
(1)前記被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、腫瘍性障害の再発の指標となり、それにより、前記被験体における腫瘍性障害の再発を予後診断する、前記方法。
【請求項7】
腫瘍性障害を持つ被験体の生存を予後診断する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、被験体の生存の指標となり、それにより、腫瘍性障害を持つ被験体の生存を予後診断する、前記方法。
【請求項8】
腫瘍性障害を持つ被験体の生存を予後診断する方法であって:
(1)前記被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、被験体の生存の指標となり、それにより、腫瘍性障害を持つ被験体の生存を予後診断する、前記方法。
【請求項9】
被験体において腫瘍性障害の侵襲性を予後診断する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記腫瘍性障害が侵襲性であることの指標となり、それにより、前記被験体の腫瘍性障害の侵襲性を予後診断する、前記方法。
【請求項10】
被験体において腫瘍性障害の侵襲性を予後診断する方法であって:
(1)前記被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記腫瘍性障害が侵襲性であることの指標となり、それにより、前記被験体の腫瘍性障害の侵襲性を予後診断する、前記方法。
【請求項11】
被験体において腫瘍性障害の進行を監視する方法であって、被験体に処置レジメンの少なくとも一部を投与する前に前記被験体から得られた第1の試料中に存在するマーカーの発現レベルと、処置レジメンの少なくとも一部の投与後に前記被験体から得られた第2の試料中に存在するマーカーの発現レベルを比較することを含み、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択され、それにより、前記被験体における腫瘍性障害の進行を監視する、前記方法。
【請求項12】
被験体において腫瘍性障害の進行を監視する方法であって:被験体に処置レジメンの少なくとも一部を投与する前に前記被験体から得られた第1の試料中に存在するマーカーの発現レベルと、処置レジメンの少なくとも一部の投与後に前記被験体から得られた第2の試料中に存在するマーカーの発現レベルを比較することを含み、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節され、それにより、前記被験体における腫瘍性障害の進行を監視する、前記方法。
【請求項13】
被験体において腫瘍性障害の処置について治療の有効性を評価するための方法であって:被験体に処置レジメンの少なくとも一部を投与する前に前記被験体から得られた第1の試料中に存在するマーカーの発現レベルと、処置レジメンの少なくとも一部の投与後に前記被験体から得られた第2の試料中に存在するマーカーの発現レベルを比較することを含み、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択され、前記第1の試料と比較した前記第2の試料中のマーカーの発現レベルにおける調節が、前記治療が前記被験体の腫瘍性障害の処置に有効であることの指標となる、前記方法。
【請求項14】
被験体の腫瘍性障害の処置について治療の有効性を評価するための方法であって:被験体に処置レジメンの少なくとも一部を投与する前に前記被験体から得られた第1の試料中に存在するマーカーの発現レベルと、処置レジメンの少なくとも一部の投与後に前記被験体から得られた第2の試料中に存在するマーカーの発現レベルを比較することを含み、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節され、前記第1の試料と比較した前記第2の試料中のマーカーの発現レベルにおける調節が、前記治療が前記被験体の腫瘍性障害の処置に有効であることの指標となる、前記方法。
【請求項15】
それが必要な被験体の腫瘍性障害の処置について環境影響因子化合物の有効性を評価する方法であって:
(1)正の倍率変化および/または負の倍率変化を有している、被験体から得られた生物試料中に存在する1つまたは複数のマーカーの発現レベルを決定すること、ここで、前記生物試料は、環境影響因子化合物に曝されており、そして前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;
(2)被験体から得られた第2の生物試料中に存在する1つまたは複数のマーカーの発現レベルを決定すること、ここで、前記試料は、環境影響因子化合物に曝されていない;ならびに、
(3)環境影響因子化合物に曝された生物試料中での1つまたは複数のマーカーの発現レベルと、環境影響因子化合物に曝されていない生物試料中での1つまたは複数のマーカーの発現レベルを比較すること
を含み、
ここで、第2の試料中に存在する1つまたは複数のマーカーの発現レベルと比較した、環境影響因子化合物に曝された生物試料中に存在する負の倍率変化を有する1つまたは複数のマーカーの発現レベルの低下が、前記環境影響因子化合物が腫瘍性障害を有している被験体の腫瘍性障害の処置に有効であることの指標となり、第2の試料中に存在する1つまたは複数のマーカーの発現レベルと比較した、環境影響因子化合物に曝された生物試料中に存在する正の倍率変化を有する1つまたは複数のマーカーの発現レベルの増大が、前記環境影響因子化合物が腫瘍性障害を有している被験体において腫瘍性障害の処置に有効であることの指標となり、
それにより、腫瘍性障害を有している被験体の腫瘍性障害の処置についての前記環境影響因子化合物の有効性を評価する、前記方法。
【請求項16】
それが必要な被験体の腫瘍性障害の処置について環境影響因子化合物の有効性を評価する方法であって:
(1)被験体から得られた生物試料中に存在する1つまたは複数のマーカーの発現レベルを決定すること、ここで、前記生物試料は環境影響因子化合物に曝されており、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現は、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように上方調節または下方調節される;
(2)被験体から得られた第2の生物試料中に存在する1つまたは複数のマーカーの発現レベルを決定すること、ここで、前記試料は、環境影響因子化合物に曝されていない;ならびに、
(3)環境影響因子化合物に曝された生物試料中での1つまたは複数のマーカーの発現レベルと、環境影響因子化合物に曝されていない生物試料中での1つまたは複数のマーカーの発現レベルを比較すること
を含み、
ここで、前記環境影響因子化合物に曝された生物試料中での、第2の試料中に存在する1つまたは複数のマーカーの発現レベルと比較した1つまたは複数の下方調節されたマーカーの発現レベルの低下が、前記環境影響因子化合物が腫瘍性障害を有している被験体の腫瘍性障害の処置に有効であることの指標となり、そして
ここでは、前記環境影響因子化合物に曝された生物試料中での、第2の試料中に存在する1つまたは複数のマーカーの発現レベルと比較した1つまたは複数の上方調節されたマーカーの発現レベルにおける増大が、前記環境影響因子化合物が腫瘍性障害を有している被験体の腫瘍性障害の処置に有効であることの指標となり、
それにより、腫瘍性障害を有している被験体の腫瘍性障害の処置についての前記環境影響因子化合物の有効性を評価する、前記方法。
【請求項17】
被験体の腫瘍性障害を処置するための化合物を同定する方法であって:
(1)被験体から生物試料を得ること;
(2)前記生物試料を試験化合物と接触させること;
(3)前記被験体から得られた生物試料中に存在する、正の倍率変化および/または負の倍率変化を有している1つまたは複数のマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;
(4)生物試料中の1つまたは複数のマーカーの発現レベルを試験化合物と接触させなかった対照試料と比較すること;ならびに、
(5)生物試料中に存在する1つ以上のマーカーの発現のレベルをネガティブ倍数変化を伴って減少させる試験化合物、および/または生物試料中に存在する1つ以上のマーカーの発現のレベルをポジティブ倍数変化を伴って増加させる試験化合物を選択すること
を含み、
それにより、被験体の腫瘍性障害を処置するための化合物を同定する、前記方法。
【請求項18】
被験体の腫瘍性障害を処置するための化合物を同定する方法であって:
(1)被験体から生物試料を得ること;
(2)前記生物試料を試験化合物と接触させること;
(3)前記被験体から得られた生物試料中に存在する1つまたは複数のマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中で、前記マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように上方調節されているかまたは下方調節されている;
(4)生物試料中の1つまたは複数のマーカーの発現レベルを試験化合物と接触させなかった対照試料と比較すること;ならびに、
(5)前記生物試料中で1つまたは複数の下方調節されたマーカーの発現レベルを低下させる、および/あるいは前記生物試料中で1つまたは複数の上方調節されたマーカーの発現レベルを増大させる試験化合物を選択すること
を含み、
それにより、被験体の腫瘍性障害を処置するための化合物を同定する、前記方法。
【請求項19】
腫瘍性障害が、白血病、リンパ腫、黒色腫、癌腫、および肉腫からなる群より選択される腫瘍性障害である、請求項1〜18のいずれか1項に記載の方法。
【請求項20】
哺乳動物の癌性細胞中では、前記マーカーが、細胞代謝エネルギーの解糖からミトコンドリアの酸化的リン酸化へのシフトを、正常な生理学的条件下にある哺乳動物の正常な細胞中で観察されるレベルに向かうように選択的に誘発する、請求項1〜19のいずれか1項に記載の方法。
【請求項21】
試料は被験体から得られる流体を含む、請求項1〜20のいずれか1項に記載の方法。
【請求項22】
前記流体が、血液、嘔吐物、唾液、リンパ液、嚢胞液、尿、気管支洗浄により収集された流体、腹腔洗浄により収集された流体、および婦人科学的流体からなる群より選択される、請求項21に記載の方法。
【請求項23】
試料が血液試料またはその成分である、請求項22に記載の方法。
【請求項24】
試料が被験体から得られた組織またはその成分を含む、請求項1〜20のいずれか1項に記載の方法。
【請求項25】
組織が、骨、結合組織、軟骨、肺、肝臓、腎臓、筋肉組織、心臓、膵臓、および皮膚からなる群より選択される、請求項24に記載の方法。
【請求項26】
前記被験体がヒトである、請求項1〜25のいずれか1項に記載の方法。
【請求項27】
生物試料中のマーカーの発現レベルは、試料中の転写されたポリヌクレオチドまたはその一部をアッセイすることによって決定される、請求項1〜26のいずれか1項に記載の方法。
【請求項28】
転写されたポリヌクレオチドをアッセイすることは、転写されたポリヌクレオチドを増幅することを含む、請求項27に記載の方法。
【請求項29】
被験体試料におけるマーカーの発現レベルは、試料中でタンパク質またはその一部をアッセイすることによって決定される、請求項1〜26のいずれか1項に記載の方法。
【請求項30】
タンパク質が、前記タンパク質に特異的に結合する試薬を使用してアッセイされる、請求項1〜29のいずれか1項に記載の方法。
【請求項31】
前記試薬が標識されている、請求項30に記載の方法。
【請求項32】
前記試薬が、抗体および抗原結合性抗体フラグメントからなる群より選択される、請求項30に記載の方法。
【請求項33】
試料中のマーカーの発現レベルは、前記試料の、ポリメラーゼ連鎖反応(PCR)増幅反応、逆転写酵素PCR分析、一本鎖コンホメーション多型分析(SSCP)、ミスマッチ切断検出、ヘテロ二重鎖分析、サザンブロット分析、ノーザンブロット分析、ウェスタンブロット分析、インサイチュハイブリダイゼーション、アレイ分析、デオキシリボ核酸配列決定、制限フラグメント長多型分析、およびこれらの組み合わせまたは下位組み合わせからなる群より選択される技術を使用して決定される、請求項1〜32のいずれか1項に記載の方法。
【請求項34】
試料中のマーカーの発現レベルが、免疫組織化学、免疫細胞化学、フローサイトメトリー、ELISA、および質量分析からなる群より選択される技術を使用して決定される、請求項1〜32のいずれか1項に記載の方法。
【請求項35】
マーカーが、HNF4アルファ、Bcl−xl、Bcl−xS、BNIP−2、Bcl−2、Birc6、Bcl−2−L11(Bim)、XIAP、BRAF、Bax、c−Jun、Bmf、PUMA、cMyc、トランスアルドラーゼ1、COQ1、COQ3、COQ6、プレニルトランスフェラーゼ、4−ヒドロベンゾエート、好中球サイトゾル因子2、1酸化窒素シンターゼ2A、スーパーオキシドディスムターゼ2、VDAC、Baxチャネル、ANT、シトクロムc、複合体1、複合体II、複合体III、複合体IV、Foxo3a、DJ−1、IDH−1、Cpt1C、およびカムキナーゼIIからなる群より選択されるマーカーである、請求項1〜34のいずれか1項に記載の方法。
【請求項36】
マーカーが、アポトーシスと関連するマーカーである、請求項1〜34のいずれか1項に記載の方法。
【請求項37】
マーカーが、酸化ストレスと関連するマーカーである、請求項1〜34のいずれか1項に記載の方法。
【請求項38】
マーカーが、熱ショックと関連するマーカーである、請求項1〜34のいずれか1項に記載の方法。
【請求項39】
マーカーが、血管形成と関連するマーカーである、請求項1〜34のいずれか1項に記載の方法。
【請求項40】
複数のマーカーの発現レベルが決定される、請求項1〜34のいずれか1項に記載の方法。
【請求項41】
前記被験体が、環境影響因子化合物、外科手術、放射線治療、ホルモン療法、抗体療法、成長因子を用いた治療、サイトカイン、および化学療法からなる群より選択される治療で処置されている、請求項5〜8、11、および12のいずれか1項に記載の方法。
【請求項42】
前記治療に環境影響因子化合物が含まれる、請求項13〜14または41のいずれか1項に記載の方法。
【請求項43】
前記治療に、外科手術、放射線治療、ホルモン療法、抗体療法、成長因子を用いた治療、サイトカイン、および化学療法からなる群より選択される処置レジメンがさらに含まれる、請求項42に記載の方法。
【請求項44】
環境影響因子化合物が、多次元細胞内分子(MIM)またはエピメタボリックシフター(エピシフター)である、請求項41または42に記載の方法。
【請求項45】
環境影響因子化合物がCoQ10である、請求項41または42に記載の方法。
【請求項46】
環境影響因子化合物がビタミンD3である、請求項41または42に記載の方法。
【請求項47】
環境影響因子化合物が、アセチルCoA、パルミチル、L−カルニチン、チロシン、フェニルアラニン、システイン、および小分子からなる群より選択される化合物である、請求項41または42に記載の方法。
【請求項48】
環境影響因子化合物が、フィブロネクチン、TNFアルファ、IL−5、IL−12、IL−23、血管形成因子、およびアポトーシス因子からなる群より選択される化合物である、請求項41または42に記載の方法。
【請求項49】
被験体が腫瘍性障害に罹患しているかどうかを評価するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに前記被験体が腫瘍性障害に罹患しているかどうかを評価するためのキットの使用についての説明書を含む、前記キット。
【請求項50】
被験体に腫瘍性障害を発症する素因があるかどうかを予後診断するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに前記被験体に腫瘍性障害を発症する素因があるかどうかを予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項51】
被験体において腫瘍性障害の再発を予後診断するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを評価するための試薬、ならびに腫瘍性障害の再発を予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項52】
腫瘍性障害の再発を予後診断するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを評価するための試薬、ならびに腫瘍性障害の再発を予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項53】
腫瘍性障害を持つ被験体の生存を予後診断するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに前記腫瘍性障害を持つ被験体の生存を予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項54】
被験体の腫瘍性障害について侵襲性を予後診断するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに前記被験体の腫瘍性障害について侵襲性を予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項55】
被験体において腫瘍性障害の進行を監視するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに被験体において腫瘍性障害の進行を予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項56】
腫瘍性障害の処置についての治療の有効性を評価するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに腫瘍性障害の処置についての前記治療の有効性を評価するためのキットの使用についての説明書を含む、前記キット。
【請求項57】
腫瘍性障害を有している被験体において、腫瘍性障害の処置についての環境影響因子化合物の有効性を評価するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに前記腫瘍性障害を有している被験体において、腫瘍性障害の処置についての環境影響因子化合物の有効性を評価するためのキットの使用についての説明書を含む、前記キット。
【請求項58】
被験体から生物試料を入手するための手段をさらに含む、請求項49〜57のいずれか1項に記載のキット。
【請求項59】
対照試料をさらに含む、請求項49〜58のいずれか1項に記載のキット。
【請求項60】
少なくとも1つのマーカーの発現レベルを決定するための手段が、試料中の転写されたポリヌクレオチドまたはその一部をアッセイするための手段を含む、請求項49〜59のいずれか1項に記載のキット。
【請求項61】
少なくとも1つのマーカーの発現レベルを決定するための手段が、試料中のタンパク質またはその一部をアッセイするための手段を含む、請求項49〜59のいずれか1項に記載のキット。
【請求項62】
環境影響因子化合物をさらに含む、請求項49〜61のいずれか1項に記載のキット。
【請求項63】
複数のマーカーの発現レベルを決定するための試薬を含む、請求項49〜62のいずれか1項に記載のキット。
【請求項64】
被験体がCoQ10反応性状態に罹患しているか否かを評価する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、対照試料中のマーカーの発現レベルと比較された、被験体から入手された生物試料中のマーカーの発現レベルの調節は、被験体がCoQ10反応性状態に罹患していることの指標となり、それにより、前記被験体がCoQ10反応性状態に罹患しているか否かを評価する、前記方法。
【請求項65】
CoQ10反応性状態が腫瘍性障害である、請求項64に記載の方法。
【請求項1】
被験体が腫瘍性障害に罹患しているかどうかを評価する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記被験体が腫瘍性障害に罹患していることの指標となり、それにより、前記被験体が腫瘍性障害に罹患しているかどうかを評価する、前記方法。
【請求項2】
被験体が腫瘍性障害に罹患しているかどうかを評価する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節される;ならびに、
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記被験体が腫瘍性障害に罹患していることの指標となり、それにより、前記被験体が腫瘍性障害に罹患しているかどうかを評価する、前記方法。
【請求項3】
被験体に腫瘍性障害を発症する素因があるかどうかを予後診断する方法であって:
(1)前記被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および5〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記被験体に腫瘍性障害を発症する素因があることの指標となり、それにより、前記被験体に腫瘍性障害を発症する素因があるかどうかを予後診断する、前記方法。
【請求項4】
被験体に腫瘍性障害を発症する素因があるかどうかを予後診断する方法であって:
(1)前記被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記被験体に腫瘍性障害を発症する素因があることの指標となり、それにより、前記被験体に腫瘍性障害を発症する素因があるかどうかを予後診断する、前記方法。
【請求項5】
被験体において腫瘍性障害の再発を予後診断する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、腫瘍性障害の再発の指標となり、それにより、前記被験体における腫瘍性障害の再発を予後診断する、前記方法。
【請求項6】
被験体において腫瘍性障害の再発を予後診断する方法であって:
(1)前記被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、腫瘍性障害の再発の指標となり、それにより、前記被験体における腫瘍性障害の再発を予後診断する、前記方法。
【請求項7】
腫瘍性障害を持つ被験体の生存を予後診断する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、被験体の生存の指標となり、それにより、腫瘍性障害を持つ被験体の生存を予後診断する、前記方法。
【請求項8】
腫瘍性障害を持つ被験体の生存を予後診断する方法であって:
(1)前記被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、被験体の生存の指標となり、それにより、腫瘍性障害を持つ被験体の生存を予後診断する、前記方法。
【請求項9】
被験体において腫瘍性障害の侵襲性を予後診断する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記腫瘍性障害が侵襲性であることの指標となり、それにより、前記被験体の腫瘍性障害の侵襲性を予後診断する、前記方法。
【請求項10】
被験体において腫瘍性障害の侵襲性を予後診断する方法であって:
(1)前記被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、前記対照試料中のマーカーの発現レベルと比較した前記被験体から得られた生物試料中のマーカーの発現レベルにおける調節が、前記腫瘍性障害が侵襲性であることの指標となり、それにより、前記被験体の腫瘍性障害の侵襲性を予後診断する、前記方法。
【請求項11】
被験体において腫瘍性障害の進行を監視する方法であって、被験体に処置レジメンの少なくとも一部を投与する前に前記被験体から得られた第1の試料中に存在するマーカーの発現レベルと、処置レジメンの少なくとも一部の投与後に前記被験体から得られた第2の試料中に存在するマーカーの発現レベルを比較することを含み、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択され、それにより、前記被験体における腫瘍性障害の進行を監視する、前記方法。
【請求項12】
被験体において腫瘍性障害の進行を監視する方法であって:被験体に処置レジメンの少なくとも一部を投与する前に前記被験体から得られた第1の試料中に存在するマーカーの発現レベルと、処置レジメンの少なくとも一部の投与後に前記被験体から得られた第2の試料中に存在するマーカーの発現レベルを比較することを含み、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節され、それにより、前記被験体における腫瘍性障害の進行を監視する、前記方法。
【請求項13】
被験体において腫瘍性障害の処置について治療の有効性を評価するための方法であって:被験体に処置レジメンの少なくとも一部を投与する前に前記被験体から得られた第1の試料中に存在するマーカーの発現レベルと、処置レジメンの少なくとも一部の投与後に前記被験体から得られた第2の試料中に存在するマーカーの発現レベルを比較することを含み、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択され、前記第1の試料と比較した前記第2の試料中のマーカーの発現レベルにおける調節が、前記治療が前記被験体の腫瘍性障害の処置に有効であることの指標となる、前記方法。
【請求項14】
被験体の腫瘍性障害の処置について治療の有効性を評価するための方法であって:被験体に処置レジメンの少なくとも一部を投与する前に前記被験体から得られた第1の試料中に存在するマーカーの発現レベルと、処置レジメンの少なくとも一部の投与後に前記被験体から得られた第2の試料中に存在するマーカーの発現レベルを比較することを含み、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように調節され、前記第1の試料と比較した前記第2の試料中のマーカーの発現レベルにおける調節が、前記治療が前記被験体の腫瘍性障害の処置に有効であることの指標となる、前記方法。
【請求項15】
それが必要な被験体の腫瘍性障害の処置について環境影響因子化合物の有効性を評価する方法であって:
(1)正の倍率変化および/または負の倍率変化を有している、被験体から得られた生物試料中に存在する1つまたは複数のマーカーの発現レベルを決定すること、ここで、前記生物試料は、環境影響因子化合物に曝されており、そして前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;
(2)被験体から得られた第2の生物試料中に存在する1つまたは複数のマーカーの発現レベルを決定すること、ここで、前記試料は、環境影響因子化合物に曝されていない;ならびに、
(3)環境影響因子化合物に曝された生物試料中での1つまたは複数のマーカーの発現レベルと、環境影響因子化合物に曝されていない生物試料中での1つまたは複数のマーカーの発現レベルを比較すること
を含み、
ここで、第2の試料中に存在する1つまたは複数のマーカーの発現レベルと比較した、環境影響因子化合物に曝された生物試料中に存在する負の倍率変化を有する1つまたは複数のマーカーの発現レベルの低下が、前記環境影響因子化合物が腫瘍性障害を有している被験体の腫瘍性障害の処置に有効であることの指標となり、第2の試料中に存在する1つまたは複数のマーカーの発現レベルと比較した、環境影響因子化合物に曝された生物試料中に存在する正の倍率変化を有する1つまたは複数のマーカーの発現レベルの増大が、前記環境影響因子化合物が腫瘍性障害を有している被験体において腫瘍性障害の処置に有効であることの指標となり、
それにより、腫瘍性障害を有している被験体の腫瘍性障害の処置についての前記環境影響因子化合物の有効性を評価する、前記方法。
【請求項16】
それが必要な被験体の腫瘍性障害の処置について環境影響因子化合物の有効性を評価する方法であって:
(1)被験体から得られた生物試料中に存在する1つまたは複数のマーカーの発現レベルを決定すること、ここで、前記生物試料は環境影響因子化合物に曝されており、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中では、マーカーの発現は、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように上方調節または下方調節される;
(2)被験体から得られた第2の生物試料中に存在する1つまたは複数のマーカーの発現レベルを決定すること、ここで、前記試料は、環境影響因子化合物に曝されていない;ならびに、
(3)環境影響因子化合物に曝された生物試料中での1つまたは複数のマーカーの発現レベルと、環境影響因子化合物に曝されていない生物試料中での1つまたは複数のマーカーの発現レベルを比較すること
を含み、
ここで、前記環境影響因子化合物に曝された生物試料中での、第2の試料中に存在する1つまたは複数のマーカーの発現レベルと比較した1つまたは複数の下方調節されたマーカーの発現レベルの低下が、前記環境影響因子化合物が腫瘍性障害を有している被験体の腫瘍性障害の処置に有効であることの指標となり、そして
ここでは、前記環境影響因子化合物に曝された生物試料中での、第2の試料中に存在する1つまたは複数のマーカーの発現レベルと比較した1つまたは複数の上方調節されたマーカーの発現レベルにおける増大が、前記環境影響因子化合物が腫瘍性障害を有している被験体の腫瘍性障害の処置に有効であることの指標となり、
それにより、腫瘍性障害を有している被験体の腫瘍性障害の処置についての前記環境影響因子化合物の有効性を評価する、前記方法。
【請求項17】
被験体の腫瘍性障害を処置するための化合物を同定する方法であって:
(1)被験体から生物試料を得ること;
(2)前記生物試料を試験化合物と接触させること;
(3)前記被験体から得られた生物試料中に存在する、正の倍率変化および/または負の倍率変化を有している1つまたは複数のマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;
(4)生物試料中の1つまたは複数のマーカーの発現レベルを試験化合物と接触させなかった対照試料と比較すること;ならびに、
(5)生物試料中に存在する1つ以上のマーカーの発現のレベルをネガティブ倍数変化を伴って減少させる試験化合物、および/または生物試料中に存在する1つ以上のマーカーの発現のレベルをポジティブ倍数変化を伴って増加させる試験化合物を選択すること
を含み、
それにより、被験体の腫瘍性障害を処置するための化合物を同定する、前記方法。
【請求項18】
被験体の腫瘍性障害を処置するための化合物を同定する方法であって:
(1)被験体から生物試料を得ること;
(2)前記生物試料を試験化合物と接触させること;
(3)前記被験体から得られた生物試料中に存在する1つまたは複数のマーカーの発現レベルを決定すること、ここで、細胞代謝エネルギーが解糖からミトコンドリアの酸化的リン酸化にシフトするように誘導された腫瘍性障害の癌性細胞中で、前記マーカーの発現が、正常な生理学的条件下にある被験体の正常な細胞中で観察されるレベルに向かうように上方調節されているかまたは下方調節されている;
(4)生物試料中の1つまたは複数のマーカーの発現レベルを試験化合物と接触させなかった対照試料と比較すること;ならびに、
(5)前記生物試料中で1つまたは複数の下方調節されたマーカーの発現レベルを低下させる、および/あるいは前記生物試料中で1つまたは複数の上方調節されたマーカーの発現レベルを増大させる試験化合物を選択すること
を含み、
それにより、被験体の腫瘍性障害を処置するための化合物を同定する、前記方法。
【請求項19】
腫瘍性障害が、白血病、リンパ腫、黒色腫、癌腫、および肉腫からなる群より選択される腫瘍性障害である、請求項1〜18のいずれか1項に記載の方法。
【請求項20】
哺乳動物の癌性細胞中では、前記マーカーが、細胞代謝エネルギーの解糖からミトコンドリアの酸化的リン酸化へのシフトを、正常な生理学的条件下にある哺乳動物の正常な細胞中で観察されるレベルに向かうように選択的に誘発する、請求項1〜19のいずれか1項に記載の方法。
【請求項21】
試料は被験体から得られる流体を含む、請求項1〜20のいずれか1項に記載の方法。
【請求項22】
前記流体が、血液、嘔吐物、唾液、リンパ液、嚢胞液、尿、気管支洗浄により収集された流体、腹腔洗浄により収集された流体、および婦人科学的流体からなる群より選択される、請求項21に記載の方法。
【請求項23】
試料が血液試料またはその成分である、請求項22に記載の方法。
【請求項24】
試料が被験体から得られた組織またはその成分を含む、請求項1〜20のいずれか1項に記載の方法。
【請求項25】
組織が、骨、結合組織、軟骨、肺、肝臓、腎臓、筋肉組織、心臓、膵臓、および皮膚からなる群より選択される、請求項24に記載の方法。
【請求項26】
前記被験体がヒトである、請求項1〜25のいずれか1項に記載の方法。
【請求項27】
生物試料中のマーカーの発現レベルは、試料中の転写されたポリヌクレオチドまたはその一部をアッセイすることによって決定される、請求項1〜26のいずれか1項に記載の方法。
【請求項28】
転写されたポリヌクレオチドをアッセイすることは、転写されたポリヌクレオチドを増幅することを含む、請求項27に記載の方法。
【請求項29】
被験体試料におけるマーカーの発現レベルは、試料中でタンパク質またはその一部をアッセイすることによって決定される、請求項1〜26のいずれか1項に記載の方法。
【請求項30】
タンパク質が、前記タンパク質に特異的に結合する試薬を使用してアッセイされる、請求項1〜29のいずれか1項に記載の方法。
【請求項31】
前記試薬が標識されている、請求項30に記載の方法。
【請求項32】
前記試薬が、抗体および抗原結合性抗体フラグメントからなる群より選択される、請求項30に記載の方法。
【請求項33】
試料中のマーカーの発現レベルは、前記試料の、ポリメラーゼ連鎖反応(PCR)増幅反応、逆転写酵素PCR分析、一本鎖コンホメーション多型分析(SSCP)、ミスマッチ切断検出、ヘテロ二重鎖分析、サザンブロット分析、ノーザンブロット分析、ウェスタンブロット分析、インサイチュハイブリダイゼーション、アレイ分析、デオキシリボ核酸配列決定、制限フラグメント長多型分析、およびこれらの組み合わせまたは下位組み合わせからなる群より選択される技術を使用して決定される、請求項1〜32のいずれか1項に記載の方法。
【請求項34】
試料中のマーカーの発現レベルが、免疫組織化学、免疫細胞化学、フローサイトメトリー、ELISA、および質量分析からなる群より選択される技術を使用して決定される、請求項1〜32のいずれか1項に記載の方法。
【請求項35】
マーカーが、HNF4アルファ、Bcl−xl、Bcl−xS、BNIP−2、Bcl−2、Birc6、Bcl−2−L11(Bim)、XIAP、BRAF、Bax、c−Jun、Bmf、PUMA、cMyc、トランスアルドラーゼ1、COQ1、COQ3、COQ6、プレニルトランスフェラーゼ、4−ヒドロベンゾエート、好中球サイトゾル因子2、1酸化窒素シンターゼ2A、スーパーオキシドディスムターゼ2、VDAC、Baxチャネル、ANT、シトクロムc、複合体1、複合体II、複合体III、複合体IV、Foxo3a、DJ−1、IDH−1、Cpt1C、およびカムキナーゼIIからなる群より選択されるマーカーである、請求項1〜34のいずれか1項に記載の方法。
【請求項36】
マーカーが、アポトーシスと関連するマーカーである、請求項1〜34のいずれか1項に記載の方法。
【請求項37】
マーカーが、酸化ストレスと関連するマーカーである、請求項1〜34のいずれか1項に記載の方法。
【請求項38】
マーカーが、熱ショックと関連するマーカーである、請求項1〜34のいずれか1項に記載の方法。
【請求項39】
マーカーが、血管形成と関連するマーカーである、請求項1〜34のいずれか1項に記載の方法。
【請求項40】
複数のマーカーの発現レベルが決定される、請求項1〜34のいずれか1項に記載の方法。
【請求項41】
前記被験体が、環境影響因子化合物、外科手術、放射線治療、ホルモン療法、抗体療法、成長因子を用いた治療、サイトカイン、および化学療法からなる群より選択される治療で処置されている、請求項5〜8、11、および12のいずれか1項に記載の方法。
【請求項42】
前記治療に環境影響因子化合物が含まれる、請求項13〜14または41のいずれか1項に記載の方法。
【請求項43】
前記治療に、外科手術、放射線治療、ホルモン療法、抗体療法、成長因子を用いた治療、サイトカイン、および化学療法からなる群より選択される処置レジメンがさらに含まれる、請求項42に記載の方法。
【請求項44】
環境影響因子化合物が、多次元細胞内分子(MIM)またはエピメタボリックシフター(エピシフター)である、請求項41または42に記載の方法。
【請求項45】
環境影響因子化合物がCoQ10である、請求項41または42に記載の方法。
【請求項46】
環境影響因子化合物がビタミンD3である、請求項41または42に記載の方法。
【請求項47】
環境影響因子化合物が、アセチルCoA、パルミチル、L−カルニチン、チロシン、フェニルアラニン、システイン、および小分子からなる群より選択される化合物である、請求項41または42に記載の方法。
【請求項48】
環境影響因子化合物が、フィブロネクチン、TNFアルファ、IL−5、IL−12、IL−23、血管形成因子、およびアポトーシス因子からなる群より選択される化合物である、請求項41または42に記載の方法。
【請求項49】
被験体が腫瘍性障害に罹患しているかどうかを評価するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに前記被験体が腫瘍性障害に罹患しているかどうかを評価するためのキットの使用についての説明書を含む、前記キット。
【請求項50】
被験体に腫瘍性障害を発症する素因があるかどうかを予後診断するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに前記被験体に腫瘍性障害を発症する素因があるかどうかを予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項51】
被験体において腫瘍性障害の再発を予後診断するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを評価するための試薬、ならびに腫瘍性障害の再発を予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項52】
腫瘍性障害の再発を予後診断するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを評価するための試薬、ならびに腫瘍性障害の再発を予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項53】
腫瘍性障害を持つ被験体の生存を予後診断するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに前記腫瘍性障害を持つ被験体の生存を予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項54】
被験体の腫瘍性障害について侵襲性を予後診断するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに前記被験体の腫瘍性障害について侵襲性を予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項55】
被験体において腫瘍性障害の進行を監視するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに被験体において腫瘍性障害の進行を予後診断するためのキットの使用についての説明書を含む、前記キット。
【請求項56】
腫瘍性障害の処置についての治療の有効性を評価するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに腫瘍性障害の処置についての前記治療の有効性を評価するためのキットの使用についての説明書を含む、前記キット。
【請求項57】
腫瘍性障害を有している被験体において、腫瘍性障害の処置についての環境影響因子化合物の有効性を評価するためのキットであって、表2〜4および6〜29に列挙するマーカーからなる群より選択される少なくとも1つのマーカーの発現レベルを決定するための試薬、ならびに前記腫瘍性障害を有している被験体において、腫瘍性障害の処置についての環境影響因子化合物の有効性を評価するためのキットの使用についての説明書を含む、前記キット。
【請求項58】
被験体から生物試料を入手するための手段をさらに含む、請求項49〜57のいずれか1項に記載のキット。
【請求項59】
対照試料をさらに含む、請求項49〜58のいずれか1項に記載のキット。
【請求項60】
少なくとも1つのマーカーの発現レベルを決定するための手段が、試料中の転写されたポリヌクレオチドまたはその一部をアッセイするための手段を含む、請求項49〜59のいずれか1項に記載のキット。
【請求項61】
少なくとも1つのマーカーの発現レベルを決定するための手段が、試料中のタンパク質またはその一部をアッセイするための手段を含む、請求項49〜59のいずれか1項に記載のキット。
【請求項62】
環境影響因子化合物をさらに含む、請求項49〜61のいずれか1項に記載のキット。
【請求項63】
複数のマーカーの発現レベルを決定するための試薬を含む、請求項49〜62のいずれか1項に記載のキット。
【請求項64】
被験体がCoQ10反応性状態に罹患しているか否かを評価する方法であって:
(1)被験体から得られた生物試料中に存在するマーカーの発現レベルを決定すること、ここで、前記マーカーは、表2〜4および6〜29に列挙するマーカーからなる群より選択される;ならびに
(2)被験体から得られた生物試料中に存在するマーカーの発現レベルを対照試料中に存在するマーカーの発現レベルと比較すること
を含み、
ここで、対照試料中のマーカーの発現レベルと比較された、被験体から入手された生物試料中のマーカーの発現レベルの調節は、被験体がCoQ10反応性状態に罹患していることの指標となり、それにより、前記被験体がCoQ10反応性状態に罹患しているか否かを評価する、前記方法。
【請求項65】
CoQ10反応性状態が腫瘍性障害である、請求項64に記載の方法。
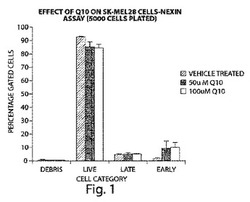
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13A】


【図13B】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13A】


【図13B】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【公表番号】特表2012−526555(P2012−526555A)
【公表日】平成24年11月1日(2012.11.1)
【国際特許分類】
【出願番号】特願2012−510951(P2012−510951)
【出願日】平成22年5月11日(2010.5.11)
【国際出願番号】PCT/US2010/034427
【国際公開番号】WO2010/132486
【国際公開日】平成22年11月18日(2010.11.18)
【出願人】(511181278)バーグ バイオシステムズ,エルエルシー (7)
【Fターム(参考)】
【公表日】平成24年11月1日(2012.11.1)
【国際特許分類】
【出願日】平成22年5月11日(2010.5.11)
【国際出願番号】PCT/US2010/034427
【国際公開番号】WO2010/132486
【国際公開日】平成22年11月18日(2010.11.18)
【出願人】(511181278)バーグ バイオシステムズ,エルエルシー (7)
【Fターム(参考)】
[ Back to top ]

