オレフィン重合体の製造方法
【課題】触媒由来の金属成分が重合体へ混入することを簡便かつ効率的に低減できるオレフィン重合体の製造方法を提供する。
【解決手段】メタロセン触媒存在下、1種以上の炭素数6〜20のα−オレフィンを重合してオレフィン重合体を製造し、前記触媒の失活前又は失活と同時に、溶媒で重合反応液を希釈することにより、失活時の重合反応液の液粘度を10mPa・s以下に低下させ、触媒の失活脱灰を促進するオレフィン重合体の製造方法。
【解決手段】メタロセン触媒存在下、1種以上の炭素数6〜20のα−オレフィンを重合してオレフィン重合体を製造し、前記触媒の失活前又は失活と同時に、溶媒で重合反応液を希釈することにより、失活時の重合反応液の液粘度を10mPa・s以下に低下させ、触媒の失活脱灰を促進するオレフィン重合体の製造方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、オレフィン重合体の製造方法及びそれによって得られたオレフィン重合体に関する。
【背景技術】
【0002】
通常、メタロセン触媒を用いたポリα−オレフィンの重合反応の多くが連続系で行われており、モノマー転化率は30〜70%程度であるがさらに高い生産性が求められている。
【0003】
例えば、特許文献1では、従来のオレフィン系重合体の製造技術では、反応終了時におけるオレフィン系重合体の濃度は、重合反応溶液中2〜40質量%であり、過度の重合反応を防止するため、活性プロトン含有含酸素化合物を添加していた。
また、ポリα−オレフィンの製造工程においては、過度の重合を防止したり、製品品質の悪化を防ぐため、重合反応終了後に触媒を失活させ、金属成分を除去(脱灰)する必要がある。
【0004】
例えば、ポリα−オレフィンの製造方法において、重合後の粗生成物と固体吸収剤(アルミナ、酸性白土、セライト等)とを接触させることで、触媒残渣を吸収したのち、濾過する方法や、水酸基を有する化合物を添加して、金属錯体触媒成分を不溶化させて除去する方法が示されている(特許文献2)。しかしながら、この方法では、数千〜数百wtppmの固体を遠心分離やろ過によって除去するための大型の遠心分離機やろ過機が必要になり、生産性が低下する。
また、未処理で製品を製造すると、製品中に金属成分が数十〜数百wtppm含まれてしまった。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2008−231261号公報
【特許文献2】特開2003−96128号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明の目的は、触媒由来の金属成分が重合体へ混入することを簡便かつ効率的に低減できるオレフィン重合体の製造方法を提供することである。
【課題を解決するための手段】
【0007】
オレフィン重合の重合反応液の粘度を高めることにより、高いモノマー転化率(例えば90%以上)が得られるが、高い粘度が失活・脱灰を妨げる、そこで、重合反応液の粘度を低くして失活・脱灰を促進することを見出し、本発明を完成させた。
本発明によれば、以下のオレフィン重合体の製造方法等が提供される。
1.メタロセン触媒存在下、1種以上の炭素数6〜20のα−オレフィンを重合してオレフィン重合体を製造し、前記触媒の失活前又は失活と同時に、溶媒で重合反応液を希釈することにより、失活時の重合反応液の液粘度を10mPa・s以下に低下させ、触媒の失活脱灰を促進するオレフィン重合体の製造方法。
2.前記溶媒として、後工程で除去可能である沸点を有する溶媒を用いる1に記載のオレフィン重合体の製造方法。
3.前記溶媒として、後工程で除去した未反応モノマー又は重合反応溶媒を用いる1又は2に記載のオレフィン重合体の製造方法。
4.1〜3のいずれかに記載のオレフィン重合体の製造方法により得られるオレフィン重合体。
【発明の効果】
【0008】
本発明によれば、触媒由来の金属成分が重合体へ混入することを簡便かつ効率的に低減できるオレフィン重合体の製造方法が提供できる。
【図面の簡単な説明】
【0009】
【図1】本発明の一実施形態を示す図である。
【図2】希釈率と重合反応液の液粘度の関係を示す図である。
【図3】実施例1及び比較例1〜3の重合反応液の液粘度と金属除去効率の関係を示す図である。
【発明を実施するための形態】
【0010】
本発明のオレフィン重合体の製造方法は、メタロセン触媒存在下、1種以上の炭素数6〜20のα−オレフィンを重合してオレフィン重合体を製造し、その後触媒を失活させる。その失活の前又は失活と同時に、溶媒で重合反応液を希釈することにより、重合反応液の失活時の液粘度を10mPa・s以下に低下させる。粘度を低下させることにより、触媒の失活脱灰を促進できる。
【0011】
一般に、重合触媒の失活のため、重合反応液に失活剤(例えばNaOH水溶液)を撹拌混合する。これにより、重合反応液(通常油相)中に含まれる触媒のほとんどが、失活剤(通常水相)に抽出される。その後、重合反応液を油相、失活剤を水相として、油水分離を行い、重合反応液から触媒を分離する。
【0012】
重合反応の転化率は、生産性の観点から、好ましくは85%以上であり、より好ましくは90%以上である。この場合、重合反応液は20mPa・s〜500mPa・s程度の高粘度状態になる場合もある。
【0013】
高粘度状態の重合反応液(通常油相)と、失活剤(通常水相)を撹拌混合すると、通常の混合割合では、油相が連続相となるため、油相の粘度の影響を受け、撹拌混合・油水分離が困難な操作となる。さらに、油相の粘度が高いために、物質移動が制限され、触媒の失活が進み難い。
触媒が失活されずに反応液中に残存したままの場合、後工程の蒸留操作で熱分解を促進させたり、製品に残存したりして、潤滑油としての性能を著しく損なう恐れがある。
【0014】
油相の液粘度を下げる方法としては、プロセスの運転条件(温度、圧力)を変えること、特に温度を上げることにより、一般的に液粘度は顕著に低下させることができる。しかしながら、触媒の失活前に温度を上げると、過度の重合を促進させたり、触媒残渣の金属成分によって製品品質が悪化したりするので好ましくない。
【0015】
本発明によれば、失活剤との混合時又は混合前に、重合反応液を溶媒で希釈し、油相粘度を低下させることにより、撹拌混合と物質移動を促進し、触媒の失活を完了させる。即ち、本発明では、モノマー転化率を上げ粘度が高くなっても容易に失活・脱灰ができる。
【0016】
重合に用いる炭素数6〜20のα−オレフィンは、好ましくは炭素数6〜14のα−オレフィンであり、より好ましくは炭素数8〜12のα−オレフィンであり、さらに好ましくは1−デセン、1−オクテン及び1−ドデセンである。本発明の重合体は通常2〜200量体であり、4〜200量体が好ましい。
【0017】
本発明の重合工程においては、重合触媒として(A)メタロセン化合物を用い、メタロセン化合物の他に(B)(b−1)有機アルミニウムオキシ化合物、(b−2)上記メタロセン化合物と反応してカチオンに変換しうるイオン性化合物、又は(C)有機アルミニウム化合物等を用いることができる。メタロセン化合物その他重合触媒を「重合触媒」とする。
【0018】
上記(A)メタロセン化合物としては、下記一般式(I)〜(IV)で表されるものが用いられる。
(C1)(C2)M1X1X2Y1aY2b (I)
(式中M1はチタン、ジルコニウム又はハフニウムを表し、C1及びC2は、それぞれ独立に、シクロペンタジエニル基又はインデニル基あるいはそれらのアルキル置換体を表し、C1及びC2は互いに同じでも異なっていてもよい。また、X1、X2は、それぞれ独立に、σ結合性配位子又はキレート性配位子を表し、X1及びX2は互いに同じでも異なっていてもよい。Y1、Y2は、それぞれ独立に、ルイス塩基を表し、Y1及びY2は互いに同じでも異なっていてもよい。a及びbは、それぞれ独立に、0又は1を表す。)
【0019】
【化1】

【0020】
(式中、M2はチタン、ジルコニウム又はハフニウムであり、C3及びC4は、それぞれ独立に、シクロペンタジエニル基又はインデニル基あるいはそれらのアルキル置換体を表し、C3及びC4は互いに同じでも異なっていてもよい。また、X3、X4は、それぞれ独立に、σ結合性配位子又はキレート性配位子を表し、X3及びX4は互いに同じでも異なっていてもよい。Y3、Y4はルイス塩基、c及びdは、それぞれ独立に、0又は1を表し、Y1及びY2は互いに同じでも異なっていてもよい。Aは架橋基であり、−R2C−又は−R2Si−を表し、Rは、それぞれ独立に、水素原子又は炭化水素基を表す。)
【0021】
【化2】

【0022】
(式中、R1〜R6は、それぞれ独立に、水素原子、ハロゲン原子、炭素数1〜20、好ましくは炭素数1〜10、より好ましくは炭素数1〜4の炭化水素基(例えばアルキル基)、又はハロゲン原子、ケイ素原子、酸素原子、イオウ原子、窒素原子及びリン原子から選ばれる一種以上の原子を含有する炭素数1〜20の有機基を示す。R1〜R3から選ばれる少なくとも1つが水素原子であり、R4〜R6から選ばれる少なくとも1つが水素原子である。Ra、Rbは、それぞれ独立に、下記一般式(a)で表わされる連結基である。X1及びX2は、それぞれ独立に、水素原子、ハロゲン原子、炭素数1〜20の炭化水素基、又はハロゲン原子、ケイ素原子、酸素原子、イオウ原子、窒素原子及びリン原子から選ばれる一種以上の原子を含有する炭素数1〜20の有機基を示す。Mは周期表第4〜6族の遷移金属を示す。)
【0023】
【化3】

【0024】
(式中、nは1〜3の整数である。R7及びR8は、それぞれ独立に、水素原子、ハロゲン原子、炭素数1〜20の炭化水素基、又は炭素数1〜20のハロゲン含有炭化水素基を示し、好ましくは水素原子又は炭素数1〜4の炭化水素基、より好ましくは水素原子又は炭素数1〜4のアルキル基である。Bは周期表第14族の原子を示す。
Ra及びRbの好ましい例としては、−CR7R8−、−SiR7R8−、−CR7R8−CR7R8−、及び−SiR7R8−SiR7R8−が挙げられる。
【0025】
【化4】

【0026】
(式中、R9〜R18及びX1、X2は、それぞれ独立に、水素原子、ハロゲン原子、炭素数1〜20の炭化水素基、好ましくは炭素数1〜10、より好ましくは炭素数1〜4の炭化水素基(例えばアルキル基)、炭素数1〜20のハロゲン含有炭化水素基、ケイ素含有基、酸素含有基、イオウ含有基、窒素含有基又はリン含有基を示し、隣接する基と互いに結合して環を形成してもよい。Rc、Rdは、それぞれ独立に、二つの配位子を結合する二価の基であって、炭素数1〜20、好ましくは炭素数1〜10、より好ましくは炭素数1〜4の2価の炭化水素基、炭素数1〜20の2価のハロゲン含有炭化水素基、2価のケイ素含有基、2価のゲルマニウム含有基、2価の錫含有基、−O−、−CO−、−S−、−SO2−、−NR19−、−PR19−、−P(O)R19−、−BR19−又は−AlR19−を示し、R19は水素原子、ハロゲン原子、炭素数1〜20の炭化水素基、又は炭素数1〜20のハロゲン含有炭化水素基を示す。Mは周期律表第4〜6族の遷移金属を示す。)
【0027】
前記一般式(I)で表わされるメタロセン化合物の具体例としては、ビス(シクロペンタジエニル)ジルコニウムジクロリド、ビス(メチルシクロペンタジエニル)ジルコニウムジクロリド、ビス(エチルシクロペンタジエニル)ジルコニウムジクロリド、ビス(イソプロピルシクロペンタジエニル)ジルコニウムジクロリド、ビス(n−プロピルシクロペンタジエニル)ジルコニウムジクロリド、ビス(n−ブチルシクロペンタジエニル)ジルコニウムジクロリド、ビス(t−ブチルシクロペンタジエニル)ジルコニウムジクロリド、ビス(ヘキシルシクロペンタジエニル)ジルコニウムジクロリド、ビス(トリメチルシリルシクロペンタジエニル)ジルコニウムジクロリド、ビス(トリメチルシリルメチルシクロペンタジエニル)ジルコニウムジクロリド、ビス(シクロペンタジエニル)ジルコニウムクロロヒドリド、ビス(シクロペンタジエニル)メチルジルコニウムクロリド、ビス(シクロペンタジエニル)エチルジルコニウムクロリド、ビス(シクロペンタジエニル)メトキシジルコニウムクロリド、ビス(シクロペンタジエニル)フェニルジルコニウムクロリド、ビス(シクロペンタジエニル)ジメチルジルコニウム、ビス(シクロペンタジエニル)ジフェニルジルコニウム、ビス(シクロペンタジエニル)ジネオペンチルジルコニウム、ビス(シクロペンタジエニル)ジヒドロジルコニウム、ビス(シクロペンタジエニル)ジメトキシジルコニウム、更には、上記に記載の化合物において、これらの化合物の塩素原子を臭素原子、ヨウ素原子、水素原子、メチル基、フェニル基等に置き換えたもの、又、上記化合物の中心金属のジルコニウムをチタニウム、ハフニウムに置き換えたものを挙げることができる。
【0028】
前記一般式(II)で表されるメタロセン化合物の具体例としては、エチレン−ビス(シクロペンタジエニル)ハフニウムジクロリド、エチレン−ビス(シクロペンタジエニル)ジルコニウムジクロリド、メチレン−ビス(シクロペンタジエニル)ハフニウムジクロリド、メチレン−ビス(シクロペンタジエニル)ジルコニウムジクロリド、イソプロピリデン−ビス(シクロペンタジエニル)ハフニウムジクロリド、イソプロピリデン−ビス(シクロペンタジエニル)ジルコニウムジクロリド、ジメチルシリレン−ビス(シクロペンタジエニル)ハフニウムジクロリド、ジメチルシリレン−ビス(シクロペンタジエニル)ジルコニウムジクロリド等が挙げられる。
【0029】
前記一般式(III)で表されるメタロセン化合物の具体例としては、(1,1’−エチレン)(2,2’−エチレン)ビスシクロペンタジエニルジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(3−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(4−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(3,4−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(3,5−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビスシクロペンタジエニルジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(3−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(4−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(3,4−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(3,5−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビスシクロペンタジエニルジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(3−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(4−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(3,4−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(3,5−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−ジメチルシリレン)ビスシクロペンタジエニルジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−ジメチルシリレン)ビス(3−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−ジメチルシリレン)ビス(4−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−ジメチルシリレン)ビス(3,4−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−ジメチルシリレン)ビス(3,5−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−イソプロピリデン)ビス(3−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−イソプロピリデン)ビス(4−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−イソプロピリデン)ビス(3,4−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−イソプロピリデン)ビス(3,5−ジメチルシクロペンタジエニル)ジルコニウムジクロリド等のジクロル体及び上記化合物のジメチル体、ジエチル体、ジヒドロ体、ジフェニル体、ジベンジル体等ならびにそれらのチタン、ハフニウム錯体を例示することができる。
【0030】
前記一般式(IV)で表される化合物としては、例えば、(1,1’−エチレン)(2,2’−エチレン)ビスインデニルジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(3−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(4−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(5−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(5,6−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(4,5−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(5,6−ジメチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビスインデニルジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(3−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(4−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(5−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(5,6−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(4,5−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(5,6−ジメチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビスインデニルジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(3−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(4−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(5−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(5,6−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(4,5−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(5,6−ジメチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビスインデニルジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(3−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(4−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(5−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(5,6−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(4,5−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(5,6−ジメチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビスインデニルジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(3−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(4−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(5−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(5,6−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(4,5−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(5,6−ジメチルインデニル)ジルコニウムジクロリド等のジクロル体及び上記化合物のジメチル体、ジエチル体、ジヒドロ体、ジフェニル体、ジベンジル体等ならびにそれらのチタン、ハフニウム錯体を例示することができる。
【0031】
(A)成分として用いられるメタロセン化合物としては、一種用いてもよく、二種以上を組み合わせて用いてもよい。
【0032】
(b−1)有機アルミニウムオキシ化合物としては、下記一般式(V)で示される鎖状アルミノキサン、及び、下記一般式(VI)で示される環状アルミノキサンを挙げることができる。
【0033】
【化5】

【0034】
(一般式(V)及び(VI)において、R20〜R25は、それぞれ独立に、炭素数1〜20、好ましくは1〜12の炭化水素基又はハロゲン原子を示す。当該炭化水素基としては、アルキル基,アルケニル基,アリール基,アリールアルキル基等が挙げられる。nは重合度を示し、通常2〜50、好ましくは2〜40の整数である。尚、各R20〜R25は互いに同じでも異なっていてもよい。)
【0035】
前記アルミノキサンの具体例としては、メチルアルミノキサン、エチルアルミノキサン、イソブチルアルミノキサン等が挙げられる。
【0036】
前記アルミノキサンの製造方法としては、アルキルアルミニウムと水等の縮合剤とを接触させる方法を挙げることができるが、その手段については特に限定はなく、公知の方法に準じて反応させればよい。例えば、有機アルミニウム化合物を有機溶剤に溶解しておき、これを水と接触させる方法、重合時に当初有機アルミニウム化合物を加えておき、後に水を添加する方法、金属塩等に含有されている結晶水、無機物や有機物への吸着水を有機アルミニウム化合物と反応させる方法、テトラアルキルジアルミノキサンにトリアルキルアルミニウムを反応させ、さらに水を反応させる方法等がある。尚、アルミノキサンとしては、トルエン不溶性のものであってもよい。これらのアルミノキサンは一種用いてもよく、二種以上を組み合わせて用いてもよい。
【0037】
一方、(b−2)成分としては、前記(A)成分のメタロセン化合物と反応してカチオンに変換しうるイオン性化合物であれば、いずれのものでも使用できるが、次の一般式(VII)、(VIII)で表されるものを好適に使用することができる。
([L1−R26]k+)a([Z]−)b ・・・(VII)
([L2]k+)a([Z]−)b ・・・(VIII)
【0038】
一般式(VII)において、L1はルイス塩基を示し、R26は水素原子、炭素数1〜20のアルキル基、又は、アリール基、アルキルアリール基及びアリールアルキル基から選ばれる炭素数6〜20の炭化水素基を示す。
【0039】
ここで、L1の具体例としては、アンモニア,メチルアミン,アニリン,ジメチルアミン,ジエチルアミン,N−メチルアニリン,ジフェニルアミン,N,N−ジメチルアニリン,トリメチルアミン,トリエチルアミン,トリ−n−ブチルアミン,メチルジフェニルアミン,ピリジン,p−ブロモ−N,N−ジメチルアニリン,p−ニトロ−N,N−ジメチルアニリン等のアミン類、トリエチルホスフィン,トリフェニルホスフィン,ジフェニルホスフィン等のホスフィン類、テトラヒドロチオフェン等のチオエーテル類、安息香酸エチル等のエステル類、アセトニトリル,ベンゾニトリル等のニトリル類等を挙げることができる。R26の具体例としては、水素原子,メチル基,エチル基,ベンジル基,トリチル基等を挙げることができる。
【0040】
一般式(VIII)において、L2はM1、R27R28M2、R29C又はR30M2を表す。R27及びR28は、それぞれ独立に、シクロペンタジエニル基、置換シクロペンタジエニル基、インデニル基又はフルオレニル基を示し、R29は炭素数1〜20のアルキル基、又は、アリール基、アルキルアリール基及びアリールアルキル基から選ばれる炭素数6〜20の炭化水素基を示す。R30はテトラフェニルポルフィリン、フタロシアニン等の大環状配位子を示す。
M1は、周期律表第1〜3、11〜13、17族元素を含むものであり、M2は、周期律表第7〜12族元素を示す。
【0041】
ここで、R27、R28の具体例としては、シクロペンタジエニル基、メチルシクロペンタジエニル基、エチルシクロペンタジエニル基、ペンタメチルシクロペンタジエニル基等を挙げることができる。R29の具体例としては、フェニル基,p−トリル基,p−メトキシフェニル基等を挙げることができ、R30の具体例としては、テトラフェニルポルフィリン,フタロシアニン等を挙げることができる。また、M1の具体例としては、Li,Na,K,Ag,Cu,Br,I,I3等を挙げることができ、M2の具体例としては、Mn,Fe,Co,Ni,Zn等を挙げることができる。
【0042】
一般式(VII)及び(VIII)において、kは[L1−R26]、[L2]のイオン価数で1〜3の整数、aは1以上の整数、b=(k×a)である。
[Z]−は、非配位性アニオン[Z1]−又は[Z2]−を表す。
[Z1]−は複数の基が元素に結合したアニオン、即ち[M3G1G2・・・Gf]−を表す。ここで、M3は周期律表第5〜15族元素、好ましくは周期律表第13〜15族元素を示す。G1〜Gfはそれぞれ水素原子、ハロゲン原子、炭素数1〜20のアルキル基、炭素数2〜40のジアルキルアミノ基、炭素数1〜20のアルコキシ基、炭素数6〜20のアリール基、炭素数6〜20のアリールオキシ基、炭素数7〜40のアルキルアリール基、炭素数7〜40のアリールアルキル基、炭素数1〜20のハロゲン置換炭化水素基、炭素数1〜20のアシルオキシ基又は有機メタロイド基又は炭素数2〜20のヘテロ原子含有炭化水素基を示す。G1〜Gfのうち二つ以上が環を形成してもよい。fは[(中心金属M3の原子価)+1]の整数を示す。
[Z2]−は酸解離定数の逆数の対数(pKa)が−10以下のブレンステッド酸単独又はブレンステッド酸及びルイス酸の組合わせの共役塩基、又は一般的に超強酸と定義される酸の共役塩基を示す。また、ルイス塩基が配位していてもよい。
【0043】
ここで、[Z1]−、即ち[M3G1G2・・・Gf]−において、M3の具体例としては、B,Al,Si,P,As,Sb等、好ましくはB及びAlを挙げることができる。また、G1,G2〜Gfの具体例としては、ジアルキルアミノ基としてジメチルアミノ基,ジエチルアミノ基等、アルコキシ基又はアリールオキシ基として、メトキシ基,エトキシ基,n−プロポキシ基,フェノキシ基等、炭化水素基として、メチル基,エチル基,n−プロピル基,イソプロピル基,n−ブチル基,イソブチル基,n−オクチル基,n−エイコシル基,フェニル基,p−トリル基,ベンジル基,4−t−ブチルフェニル基,3,5−ジメチルフェニル基等、ハロゲン原子として、フッ素,塩素,臭素,ヨウ素、ヘテロ原子含有炭化水素基として、p−フルオロフェニル基,3,5−ジフルオロフェニル基,ペンタクロロフェニル基,3,4,5−トリフルオロフェニル基,ペンタフルオロフェニル基,3,5−ビス(トリフルオロメチル)フェニル基,ビス(トリメチルシリル)メチル基等、有機メタロイド基として、ペンタメチルアンチモン基、トリメチルシリル基,トリメチルゲルミル基,ジフェニルアルシン基,ジシクロヘキシルアンチモン基,ジフェニルホウ素基等を挙げることができる。
【0044】
また、非配位性のアニオン、即ちpKaが−10以下のブレンステッド酸単独又はブレンステッド酸及びルイス酸の組合わせの共役塩基[Z2]−の具体例としては、トリフルオロメタンスルホン酸アニオン(CF3SO3)−,ビス(トリフルオロメタンスルホニル)メチルアニオン,ビス(トリフルオロメタンスルホニル)ベンジルアニオン,ビス(トリフルオロメタンスルホニル)アミド,過塩素酸アニオン(ClO4)−,トリフルオロ酢酸アニオン(CF3COO)−,ヘキサフルオロアンチモンアニオン(SbF6)−,フルオロスルホン酸アニオン(FSO3)−,クロロスルホン酸アニオン(ClSO3)−,フルオロスルホン酸アニオン/5−フッ化アンチモン(FSO3/SbF5)−,フルオロスルホン酸アニオン/5−フッ化ヒ素(FSO3/AsF5)−,トリフルオロメタンスルホン酸/5−フッ化アンチモン(CF3SO3/SbF5)−等を挙げることができる。
【0045】
このような(b−2)成分化合物の具体例としては、テトラフェニルホウ酸トリエチルアンモニウム,テトラフェニルホウ酸トリ−n−ブチルアンモニウム,テトラフェニルホウ酸トリメチルアンモニウム,テトラフェニルホウ酸テトラエチルアンモニウム,テトラフェニルホウ酸メチル(トリ−n−ブチル)アンモニウム,テトラフェニルホウ酸ベンジル(トリ−n−ブチル)アンモニウム,テトラフェニルホウ酸ジメチルジフェニルアンモニウム,テトラフェニルホウ酸トリフェニル(メチル)アンモニウム,テトラフェニルホウ酸トリメチルアニリニウム,テトラフェニルホウ酸メチルピリジニウム,テトラフェニルホウ酸ベンジルピリジニウム,テトラフェニルホウ酸メチル(2−シアノピリジニウム),テトラキス(ペンタフルオロフェニル)ホウ酸トリエチルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸トリ−n−ブチルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸トリフェニルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸テトラ−n−ブチルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸テトラエチルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸ベンジル(トリ−n−ブチル)アンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸メチルジフェニルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸トリフェニル(メチル)アンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸メチルアニリニウム,テトラキス(ペンタフルオロフェニル)ホウ酸ジメチルアニリニウム,テトラキス(ペンタフルオロフェニル)ホウ酸トリメチルアニリニウム,テトラキス(ペンタフルオロフェニル)ホウ酸メチルピリジニウム,テトラキス(ペンタフルオロフェニル)ホウ酸ベンジルピリジニウム,テトラキス(ペンタフルオロフェニル)ホウ酸メチル(2−シアノピリジニウム),テトラキス(ペンタフルオロフェニル)ホウ酸ベンジル(2−シアノピリジニウム),テトラキス(ペンタフルオロフェニル)ホウ酸メチル(4−シアノピリジニウム),テトラキス(ペンタフルオロフェニル)ホウ酸トリフェニルホスホニウム,テトラキス[ビス(3,5−ジトリフルオロメチル)フェニル]ホウ酸ジメチルアニリニウム,テトラフェニルホウ酸フェロセニウム,テトラフェニルホウ酸銀,テトラフェニルホウ酸トリチル,テトラフェニルホウ酸テトラフェニルポルフィリンマンガン,テトラキス(ペンタフルオロフェニル)ホウ酸フェロセニウム,テトラキス(ペンタフルオロフェニル)ホウ酸(1,1’−ジメチルフェロセニウム),テトラキス(ペンタフルオロフェニル)ホウ酸デカメチルフェロセニウム,テトラキス(ペンタフルオロフェニル)ホウ酸銀,テトラキス(ペンタフルオロフェニル)ホウ酸トリチル,テトラキス(ペンタフルオロフェニル)ホウ酸リチウム,テトラキス(ペンタフルオロフェニル)ホウ酸ナトリウム,テトラキス(ペンタフルオロフェニル)ホウ酸テトラフェニルポルフィリンマンガン,テトラフルオロホウ酸銀,ヘキサフルオロリン酸銀,ヘキサフルオロヒ素酸銀,過塩素酸銀,トリフルオロ酢酸銀,トリフルオロメタンスルホン酸銀等を挙げることができる。
【0046】
この(b−2)成分は一種用いてもよく、また二種以上を組み合わせて用いてもよい。本発明において、(B)成分を用いる場合、(A)成分と(B)成分との使用割合は、(B)成分として(b−1)成分を用いた場合には、モル比で、好ましくは1:1〜1:1,000,000、より好ましくは1:10〜1:10,000、(b−2)成分を用いた場合には、モル比で、好ましくは10:1〜1:100、より好ましくは2:1〜1:10である。また、(B)成分としては、(b−1)及び(b−2)等を単独又は二種以上組み合わせて用いることもできる。
【0047】
本発明における触媒としては、前記の(A)成分及び(B)成分を主成分として含有するものであってもよいし、また、(A)成分、(B)成分及び(C)有機アルミニウム化合物を主成分として含有するものであってもよい。ここで、(C)成分の有機アルミニウム化合物としては、一般式(IX)
(R31)vAlQ3−v ・・・(IX)
(式中、R31は炭素数1〜10のアルキル基、Qは水素原子、炭素数1〜20のアルコキシ基,炭素数6〜20のアリール基又はハロゲン原子を示し、vは1〜3の整数である。)で示される化合物が用いられる。
【0048】
前記一般式(IX)で示される化合物の具体例としては、トリメチルアルミニウム,トリエチルアルミニウム,トリイソプロピルアルミニウム,トリイソブチルアルミニウム,ジメチルアルミニウムクロリド,ジエチルアルミニウムクロリド,メチルアルミニウムジクロリド,エチルアルミニウムジクロリド,ジメチルアルミニウムフルオリド,ジイソブチルアルミニウムヒドリド,ジエチルアルミニウムヒドリド,エチルアルミニウムセスキクロリド等を挙げることができる。これらの有機アルミニウム化合物は、一種用いてもよく、二種以上を組合せて用いてもよい。前記(A)成分と(C)成分との使用割合は、モル比で、好ましくは1:1〜1:10,000、より好ましくは1:5〜1:2,000、さらに好ましくは1:10〜1:1,000である。この(C)成分を用いることにより、遷移金属当たりの活性を向上させることができるが、あまり多いと有機アルミニウム化合物が無駄になるとともに、α−オレフィン重合体中に多量に残存し、好ましくない。
【0049】
本発明において、重合方法は特に制限されず、塊状重合法、溶液重合法、懸濁重合法、スラリー重合法、気相重合法等のいずれの方法を用いてもよい。
重合条件については、重合温度は通常0〜200℃、好ましくは30〜150℃、より好ましくは40〜120℃である。また、原料モノマーに対する触媒の使用割合は、原料モノマー/上記(A)成分(モル比)が好ましくは1〜108,特に100〜105となることが好ましい。さらに、重合時間は通常5分〜20時間、反応圧力は好ましくは常圧〜0.2MPaG、特に好ましくは常圧〜0.1MPaGである。
【0050】
重合工程はコスト面から無溶媒で行うことが好ましいが、溶媒を用いることもできる。その場合、例えば、ベンゼン,トルエン,キシレン,エチルベンゼン等の芳香族炭化水素、シクロペンタン,シクロヘキサン,メチルシクロヘキサン等の脂環式炭化水素、ペンタン,ヘキサン,ヘプタン,オクタン等の脂肪族炭化水素、クロロホルム,ジクロロメタン等のハロゲン化炭化水素等を用いることができる。これらの溶媒は一種を単独で用いてもよく、二種以上のものを組み合わせてもよい。また、1−デセン等のモノマーを溶媒として用いてもよい。
【0051】
重合後、過度の重合を防止するために、重合反応液に失活剤(触媒非活性化剤)を加えて重合触媒を失活させる。
希釈溶媒の添加は、失活剤の添加の前に添加してもよいし、失活剤の添加と共に添加してもよい。
重合触媒を失活させる前に希釈を行う場合、希釈後、できるだけ速やかに触媒失活を行うことが望ましい。希釈から失活までの時間が長いと、重合生成物が影響を受ける恐れがあるためである。
一方、重合反応の開始前又は重合反応中に希釈溶媒を添加すると、反応器内のモノマー濃度が低下して重合反応速度が低下するため、生産性が低下する恐れがある。
本発明では、重合反応液を溶媒で希釈し、油相粘度を低下させるため、油水混合のための撹拌槽、油水分離のための静置分離槽、微粒子除去のためのフィルター設備をサイズダウンすることができ、コストダウンにも繋がる。
【0052】
上記希釈は、失活時の重合反応液の液粘度が10mPa・s以下、好ましくは5mPa・s以下となるように行う。液粘度は実施例に記載の方法で測定できる。
尚、失活時の重合反応液の液粘度は、希釈後の重合反応溶液と同じである。
失活剤と混合したとき、液液分離する場合は、重合反応液の液粘度として、通常、油相側の液粘度を測定する。
希釈後の重合反応液の液粘度が高いと、触媒の失活が遅くなり、ろ過を行っても触媒由来のアルミニウムが重合反応液中に溶解した状態で残存する恐れがある。
【0053】
図2に、重合反応液(80℃における液粘度:78mPa・s)に1−デセンを加えて希釈した場合の、希釈溶媒の添加量(希釈率)と重合反応液の液粘度の関係を示す。図2においてドットは実測値である。
希釈率[%]=[R/(R+F)]×100[wt./wt.]
F:重合反応液量
R:希釈溶媒量
【0054】
希釈に用いる溶媒(希釈液)は、通常、重合生成物に影響しないような不活性炭化水素系溶媒を用いることができる。例えば、トルエン、キシレン等の環状炭化水素、1−デセン、1−オクテン、1−ドデセン等の炭素数6〜20の不飽和炭化水素、又はこれらの2量体を用いることもできる。
また、前述した重合工程溶媒を用いることができる。
ただし、重合反応液に対して十分粘度が低いことが求められるので、希釈溶媒の液粘度は、例えば、40℃において1mPa・s以下であり、望ましくは0.5mPa・s以下である。
【0055】
また、後工程(失活後)、即ち、失活に続く工程で、蒸留分離が可能であるように、希釈溶媒の沸点は好ましくは250℃以下、より好ましくは200℃以下、さらに好ましくは100℃以下である。希釈溶媒の沸点がこの範囲であると、後述する蒸留工程で希釈溶媒を蒸留分離し、希釈・失活工程で再度重合反応液の希釈に用いることができる。
【0056】
失活剤としては、例えばアルコール、水、及び酸、アルカリ、含酸素化合物等の水溶液が挙げられ、具体的には、水酸化ナトリウム水溶液、エタノール、イソプロピルアルコール、塩酸及びアセトン等が挙げられる。
【0057】
失活剤の添加後、通常、図1に示すような脱灰、蒸留を経てオレフィン重合体を得ることができる。
図1に示すように、蒸留除去された軽質分(未反応モノマーや重合溶媒、オレフィン重合体2量体等)をリサイクルし、失活の際の希釈溶媒として用いるとコストの面から望ましい。
【0058】
脱灰で除かれる金属として触媒、助触媒に含まれるアルミニウム、ジルコニウム等が挙げられる。
金属除去率が高いほど潤滑油として好ましい性状となる。通常の触媒使用量であれば95%以上の金属除去率が求められ、そのためには失活時の重合反応液の液粘度を10mPa・s以下とすることが好ましい。さらに97%以上の金属除去率が求められる場合には、5mPa・s以下まで低下させることがより好ましい。
【0059】
触媒の金属成分を除去後、上記の重合反応液を蒸留して軽質分を留去し、オレフィンオレゴマーを得る。
【実施例】
【0060】
実施例1
[触媒の調製]
500mLのガラス製シュレンク瓶に窒素雰囲気下で、以下の化合物を以下の割合で混合して触媒溶液A,B,Nを調製した。
触媒溶液A:トルエン1Lに対してトリイソブチルアルミニウム50mmol
触媒溶液B:トルエン1Lに対して粉末状のN,N−ジメチルアニリニウム−テトラキス(ペンタフルオロフェニル)ボレート4mmol
触媒溶液N:トルエン1Lに対して(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)−ビス(シクロペンタジエニル)ジルコニウムジクロリド1mmol
【0061】
[重合反応]
内容積100Lのステンレス製オートクレーブを十分乾燥し、窒素乾燥の後に、1−オクテン11.94kgと1−ドデセン17.99kgを仕込み、水素0.02MPaGを導入し、触媒溶液Aを400mL入れて、95℃に昇温し、1時間保持した。
次に触媒溶液B200mL、及び触媒溶液N200mLをオートクレーブに投入し、105℃に昇温して保持した。
【0062】
30分後、触媒溶液A200mL、触媒溶液B200mL、触媒溶液N200mLをオートクレーブに投入した。
30分後(反応開始から1時間後)、触媒溶液A300mL、触媒溶液B300mL、及び触媒溶液N300mLをオートクレーブに投入した。
1時間後(反応開始から2時間後)、触媒溶液A400mL、触媒溶液B400mL、及び触媒溶液N400mLをオートクレーブに投入した。
1時間後(反応開始から3時間後)、触媒溶液A400mL、触媒溶液B400mL、及び触媒溶液N400mLをオートクレーブに投入した。
1時間後(反応開始から4時間後)、触媒溶液A500mL、触媒溶液B500mL、及び触媒溶液N500mLをオートクレーブに投入した。
1時間後(反応開始から5時間後)、触媒溶液A500mL、触媒溶液B500mL、及び触媒溶液N500mLをオートクレーブに投入した。
2時間後(反応開始から7時間後)、内容物を重合反応液として取り出した。
重合反応中の平均温度は105℃であり、この重合反応液の原料転化率は90%、40℃における液粘度は91mPa・sであった。
【0063】
転化率と液粘度は以下の方法で測定した。
(1)転化率
試料0.05gをジクロロメタン5mlに溶解してガスクロマトグラフィー(GC)を用いて算出した。
(GC測定条件)
カラム:HT−SIMDISTCB(5m×0.53mmφ,膜厚:0.17μm)
カラム温度:40℃(0.1min)、20℃/minで420℃まで上昇、420℃(15min)
注入口(COC)温度:オーブントラック
検出器(FID)温度:440℃
キャリアガス:He
線速度:40cm/sec
モード:コンスタントフロー
注入量:0.5μl
(2)液粘度
エー・アンド・デイ株式会社製の音叉型振動式粘度計で測定した。
【0064】
[希釈・失活・脱灰]
重合反応液400gと、1−デセン600g(40℃における液粘度:0.4mPa・s)を2Lフラスコで混合し、希釈した重合反応液を得た。希釈した重合反応液の40℃における粘度は8.4mPa・sであった。
この希釈した重合反応液と1%水酸化ナトリウム水溶液を油水比(W/O)0.1[vol/vol]で、加温したスタティックミキサーを用いて、80℃において混合した。このときの油相粘度は80℃で4.2mPa・sであり、撹拌強度は約20kW/m3(通過線速約0.2m/s)であり、滞留時間は約1秒であった。
【0065】
油水混合液を窒素雰囲気でメスシリンダーに採取し、油水分離後、油相をサンプリングして、公称孔径0.2μm(ADVANTEC社製 T020A−)のフィルターを用いて、固体微粒子を濾過して除去した。
その結果、濾液中の金属分濃度は20wtppmから1wtppm未満まで低下した。金属分濃度は灰化処理の後、ICP発光法で分析した。
尚、灰化処理とは、金属分の定量のために、サンプルを燃焼して含まれる金属分を灰にすることである。
【0066】
比較例1
[触媒の調製]
触媒溶液として、以下の触媒溶液A’、B’及びN’をそれぞれ100mLのガラス製シュレンク瓶に窒素雰囲気下で調製した。
触媒溶液A’:トリイソブチルアルミニウムの1mmol/mLトルエン溶液;45mL
触媒溶液B’:N,N−ジメチルアニリニウム−テトラキス(ペンタフルオロフェニル)ボレートの40mmol/Lトルエン溶液;90mL
触媒溶液N’:(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)−ビス(シクロペンタジエニル)ジルコニウムジクロリドの10mmol/Lトルエン溶液;90mL
【0067】
[重合反応]
内容積100Lのステンレス製オートクレーブを十分乾燥し、窒素乾燥の後に、1−オクテン18.1kgと1−ドデセン26.7kgを仕込み、トリイソブチルアルミニウム9mmol(トルエン溶液9L)を入れて、水素0.01MPaGを導入し、90℃に昇温した。
上記の触媒溶液A’,B’,N’を以下の所定量で、以下のように順次投入しながら、5時間反応させた。触媒投入は計4回行い、4回目の触媒投入後2時間反応させた。内容物を重合反応液として取り出した。この重合反応液は原料転化率90%であり、40℃における液粘度は175mPa・sであった。
【0068】
反応開始(スタート)=触媒投入1回目
反応開始1時間経過後=触媒投入2回目
反応開始2時間経過後=触媒投入3回目
反応開始3時間経過後=触媒投入4回目
反応開始5時間経過後=反応終了
1回の触媒投入量は、触媒溶液A’11.25mL、触媒溶液N’22.5mL、及び触媒溶液B’22.5mLとした。
【0069】
[失活・脱灰]
上記の重合反応液と1%水酸化ナトリウム水溶液を油水比(W/O)0.5[vol/vol]で、バッチ式の撹拌槽を用いて80℃において混合した。80℃における油相粘度は78mPa・sであった。
このときの撹拌強度は約0.2kW/m3(撹拌回転数200rpm)で、撹拌時間は10分間とした。その後、撹拌を停止し、30分間静置して、油水分離後、油相をサンプリングして、公称孔径0.8μm(ADVANTEC社製 T080A−)のフィルターを用いて、固体微粒子を濾過して除去した。
その結果、濾液中の金属分濃度は、28wtppmから10wtppmまで低下した。金属分濃度は灰化処理を行った後、ICP発光法で分析した。
【0070】
比較例2
[重合反応]
比較例1の[重合反応]と同様にして重合反応液を得た。
【0071】
[希釈・失活・脱灰]
上記の重合反応液300mLと触媒溶液A’2mL、トルエン200mLを十分に混合し、80℃における液粘度を17mPa・s(40℃における液粘度:40mPa・s)に調整した。この粘度調整した重合反応液と1%水酸化ナトリウム水溶液を油水比(W/O)[0.2vol/vol]で、スタティックミキサーを用いて80℃において混合した。80℃における油相粘度は17mPa・sであった。
尚、重合反応液に触媒溶液A’を加えたのは、金属分を増加することで、液粘度による効果の有無を明確にするためである。
【0072】
このときの撹拌強度は約250kW/m3(通過線速約0.85m/s)であり、滞留時間は約0.1秒であった。油水混合液を窒素雰囲気でメスシリンダーに採取し、油水分離後、油相をサンプリングして、公称孔径0.2μm(ADVANTEC社製 T020A−)のフィルターを用いて、固体微粒子を濾過して除去した。
その結果、濾液中の金属分濃度は、130wtppmから17wtppmまで低下した。金属分濃度はICP発光法で分析した。
【0073】
比較例3
[重合反応]
比較例1の[重合反応]と同様にして重合反応液を得た。
【0074】
[希釈・失活・脱灰]
上記の重合反応液475mLと触媒溶液A’2mL、トルエン25mLを十分に混合し、80℃における液粘度を60mPa・s(40℃における液粘度:128mPa・s)に調整した。この粘度調整した重合反応液と1%水酸化ナトリウム水溶液を油水比(W/O)0.2[vol/vol]で、スタティックミキサーを用いて80℃において混合した。80℃における油相粘度は60mPa・sであった。
【0075】
このときの撹拌強度は約20kW/m3(通過線速約0.2m/s)であり、滞留時間は約1秒であった。油水混合液を窒素雰囲気でメスシリンダーに採取し、油水分離後、油相をサンプリングして、公称孔径0.8μm(ADVANTEC社製 T080A−)のフィルターを用いて、固体微粒子を濾過して除去した。
その結果、濾液中の金属分濃度は、155wtppmから43wtppmまで低下した。金属分濃度はICP発光法で分析した。
【0076】
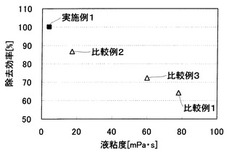
実施例及び比較例の結果(重合反応液の液粘度と金属除去率の関係)を図3に示す。図3より、重合反応液の液粘度の上昇に伴って、触媒由来の金属除去率は顕著に低下する。
【産業上の利用可能性】
【0077】
本発明の製造方法によって得られたオレフィン重合体は潤滑油基材として使用できる。
【技術分野】
【0001】
本発明は、オレフィン重合体の製造方法及びそれによって得られたオレフィン重合体に関する。
【背景技術】
【0002】
通常、メタロセン触媒を用いたポリα−オレフィンの重合反応の多くが連続系で行われており、モノマー転化率は30〜70%程度であるがさらに高い生産性が求められている。
【0003】
例えば、特許文献1では、従来のオレフィン系重合体の製造技術では、反応終了時におけるオレフィン系重合体の濃度は、重合反応溶液中2〜40質量%であり、過度の重合反応を防止するため、活性プロトン含有含酸素化合物を添加していた。
また、ポリα−オレフィンの製造工程においては、過度の重合を防止したり、製品品質の悪化を防ぐため、重合反応終了後に触媒を失活させ、金属成分を除去(脱灰)する必要がある。
【0004】
例えば、ポリα−オレフィンの製造方法において、重合後の粗生成物と固体吸収剤(アルミナ、酸性白土、セライト等)とを接触させることで、触媒残渣を吸収したのち、濾過する方法や、水酸基を有する化合物を添加して、金属錯体触媒成分を不溶化させて除去する方法が示されている(特許文献2)。しかしながら、この方法では、数千〜数百wtppmの固体を遠心分離やろ過によって除去するための大型の遠心分離機やろ過機が必要になり、生産性が低下する。
また、未処理で製品を製造すると、製品中に金属成分が数十〜数百wtppm含まれてしまった。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2008−231261号公報
【特許文献2】特開2003−96128号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明の目的は、触媒由来の金属成分が重合体へ混入することを簡便かつ効率的に低減できるオレフィン重合体の製造方法を提供することである。
【課題を解決するための手段】
【0007】
オレフィン重合の重合反応液の粘度を高めることにより、高いモノマー転化率(例えば90%以上)が得られるが、高い粘度が失活・脱灰を妨げる、そこで、重合反応液の粘度を低くして失活・脱灰を促進することを見出し、本発明を完成させた。
本発明によれば、以下のオレフィン重合体の製造方法等が提供される。
1.メタロセン触媒存在下、1種以上の炭素数6〜20のα−オレフィンを重合してオレフィン重合体を製造し、前記触媒の失活前又は失活と同時に、溶媒で重合反応液を希釈することにより、失活時の重合反応液の液粘度を10mPa・s以下に低下させ、触媒の失活脱灰を促進するオレフィン重合体の製造方法。
2.前記溶媒として、後工程で除去可能である沸点を有する溶媒を用いる1に記載のオレフィン重合体の製造方法。
3.前記溶媒として、後工程で除去した未反応モノマー又は重合反応溶媒を用いる1又は2に記載のオレフィン重合体の製造方法。
4.1〜3のいずれかに記載のオレフィン重合体の製造方法により得られるオレフィン重合体。
【発明の効果】
【0008】
本発明によれば、触媒由来の金属成分が重合体へ混入することを簡便かつ効率的に低減できるオレフィン重合体の製造方法が提供できる。
【図面の簡単な説明】
【0009】
【図1】本発明の一実施形態を示す図である。
【図2】希釈率と重合反応液の液粘度の関係を示す図である。
【図3】実施例1及び比較例1〜3の重合反応液の液粘度と金属除去効率の関係を示す図である。
【発明を実施するための形態】
【0010】
本発明のオレフィン重合体の製造方法は、メタロセン触媒存在下、1種以上の炭素数6〜20のα−オレフィンを重合してオレフィン重合体を製造し、その後触媒を失活させる。その失活の前又は失活と同時に、溶媒で重合反応液を希釈することにより、重合反応液の失活時の液粘度を10mPa・s以下に低下させる。粘度を低下させることにより、触媒の失活脱灰を促進できる。
【0011】
一般に、重合触媒の失活のため、重合反応液に失活剤(例えばNaOH水溶液)を撹拌混合する。これにより、重合反応液(通常油相)中に含まれる触媒のほとんどが、失活剤(通常水相)に抽出される。その後、重合反応液を油相、失活剤を水相として、油水分離を行い、重合反応液から触媒を分離する。
【0012】
重合反応の転化率は、生産性の観点から、好ましくは85%以上であり、より好ましくは90%以上である。この場合、重合反応液は20mPa・s〜500mPa・s程度の高粘度状態になる場合もある。
【0013】
高粘度状態の重合反応液(通常油相)と、失活剤(通常水相)を撹拌混合すると、通常の混合割合では、油相が連続相となるため、油相の粘度の影響を受け、撹拌混合・油水分離が困難な操作となる。さらに、油相の粘度が高いために、物質移動が制限され、触媒の失活が進み難い。
触媒が失活されずに反応液中に残存したままの場合、後工程の蒸留操作で熱分解を促進させたり、製品に残存したりして、潤滑油としての性能を著しく損なう恐れがある。
【0014】
油相の液粘度を下げる方法としては、プロセスの運転条件(温度、圧力)を変えること、特に温度を上げることにより、一般的に液粘度は顕著に低下させることができる。しかしながら、触媒の失活前に温度を上げると、過度の重合を促進させたり、触媒残渣の金属成分によって製品品質が悪化したりするので好ましくない。
【0015】
本発明によれば、失活剤との混合時又は混合前に、重合反応液を溶媒で希釈し、油相粘度を低下させることにより、撹拌混合と物質移動を促進し、触媒の失活を完了させる。即ち、本発明では、モノマー転化率を上げ粘度が高くなっても容易に失活・脱灰ができる。
【0016】
重合に用いる炭素数6〜20のα−オレフィンは、好ましくは炭素数6〜14のα−オレフィンであり、より好ましくは炭素数8〜12のα−オレフィンであり、さらに好ましくは1−デセン、1−オクテン及び1−ドデセンである。本発明の重合体は通常2〜200量体であり、4〜200量体が好ましい。
【0017】
本発明の重合工程においては、重合触媒として(A)メタロセン化合物を用い、メタロセン化合物の他に(B)(b−1)有機アルミニウムオキシ化合物、(b−2)上記メタロセン化合物と反応してカチオンに変換しうるイオン性化合物、又は(C)有機アルミニウム化合物等を用いることができる。メタロセン化合物その他重合触媒を「重合触媒」とする。
【0018】
上記(A)メタロセン化合物としては、下記一般式(I)〜(IV)で表されるものが用いられる。
(C1)(C2)M1X1X2Y1aY2b (I)
(式中M1はチタン、ジルコニウム又はハフニウムを表し、C1及びC2は、それぞれ独立に、シクロペンタジエニル基又はインデニル基あるいはそれらのアルキル置換体を表し、C1及びC2は互いに同じでも異なっていてもよい。また、X1、X2は、それぞれ独立に、σ結合性配位子又はキレート性配位子を表し、X1及びX2は互いに同じでも異なっていてもよい。Y1、Y2は、それぞれ独立に、ルイス塩基を表し、Y1及びY2は互いに同じでも異なっていてもよい。a及びbは、それぞれ独立に、0又は1を表す。)
【0019】
【化1】

【0020】
(式中、M2はチタン、ジルコニウム又はハフニウムであり、C3及びC4は、それぞれ独立に、シクロペンタジエニル基又はインデニル基あるいはそれらのアルキル置換体を表し、C3及びC4は互いに同じでも異なっていてもよい。また、X3、X4は、それぞれ独立に、σ結合性配位子又はキレート性配位子を表し、X3及びX4は互いに同じでも異なっていてもよい。Y3、Y4はルイス塩基、c及びdは、それぞれ独立に、0又は1を表し、Y1及びY2は互いに同じでも異なっていてもよい。Aは架橋基であり、−R2C−又は−R2Si−を表し、Rは、それぞれ独立に、水素原子又は炭化水素基を表す。)
【0021】
【化2】

【0022】
(式中、R1〜R6は、それぞれ独立に、水素原子、ハロゲン原子、炭素数1〜20、好ましくは炭素数1〜10、より好ましくは炭素数1〜4の炭化水素基(例えばアルキル基)、又はハロゲン原子、ケイ素原子、酸素原子、イオウ原子、窒素原子及びリン原子から選ばれる一種以上の原子を含有する炭素数1〜20の有機基を示す。R1〜R3から選ばれる少なくとも1つが水素原子であり、R4〜R6から選ばれる少なくとも1つが水素原子である。Ra、Rbは、それぞれ独立に、下記一般式(a)で表わされる連結基である。X1及びX2は、それぞれ独立に、水素原子、ハロゲン原子、炭素数1〜20の炭化水素基、又はハロゲン原子、ケイ素原子、酸素原子、イオウ原子、窒素原子及びリン原子から選ばれる一種以上の原子を含有する炭素数1〜20の有機基を示す。Mは周期表第4〜6族の遷移金属を示す。)
【0023】
【化3】

【0024】
(式中、nは1〜3の整数である。R7及びR8は、それぞれ独立に、水素原子、ハロゲン原子、炭素数1〜20の炭化水素基、又は炭素数1〜20のハロゲン含有炭化水素基を示し、好ましくは水素原子又は炭素数1〜4の炭化水素基、より好ましくは水素原子又は炭素数1〜4のアルキル基である。Bは周期表第14族の原子を示す。
Ra及びRbの好ましい例としては、−CR7R8−、−SiR7R8−、−CR7R8−CR7R8−、及び−SiR7R8−SiR7R8−が挙げられる。
【0025】
【化4】

【0026】
(式中、R9〜R18及びX1、X2は、それぞれ独立に、水素原子、ハロゲン原子、炭素数1〜20の炭化水素基、好ましくは炭素数1〜10、より好ましくは炭素数1〜4の炭化水素基(例えばアルキル基)、炭素数1〜20のハロゲン含有炭化水素基、ケイ素含有基、酸素含有基、イオウ含有基、窒素含有基又はリン含有基を示し、隣接する基と互いに結合して環を形成してもよい。Rc、Rdは、それぞれ独立に、二つの配位子を結合する二価の基であって、炭素数1〜20、好ましくは炭素数1〜10、より好ましくは炭素数1〜4の2価の炭化水素基、炭素数1〜20の2価のハロゲン含有炭化水素基、2価のケイ素含有基、2価のゲルマニウム含有基、2価の錫含有基、−O−、−CO−、−S−、−SO2−、−NR19−、−PR19−、−P(O)R19−、−BR19−又は−AlR19−を示し、R19は水素原子、ハロゲン原子、炭素数1〜20の炭化水素基、又は炭素数1〜20のハロゲン含有炭化水素基を示す。Mは周期律表第4〜6族の遷移金属を示す。)
【0027】
前記一般式(I)で表わされるメタロセン化合物の具体例としては、ビス(シクロペンタジエニル)ジルコニウムジクロリド、ビス(メチルシクロペンタジエニル)ジルコニウムジクロリド、ビス(エチルシクロペンタジエニル)ジルコニウムジクロリド、ビス(イソプロピルシクロペンタジエニル)ジルコニウムジクロリド、ビス(n−プロピルシクロペンタジエニル)ジルコニウムジクロリド、ビス(n−ブチルシクロペンタジエニル)ジルコニウムジクロリド、ビス(t−ブチルシクロペンタジエニル)ジルコニウムジクロリド、ビス(ヘキシルシクロペンタジエニル)ジルコニウムジクロリド、ビス(トリメチルシリルシクロペンタジエニル)ジルコニウムジクロリド、ビス(トリメチルシリルメチルシクロペンタジエニル)ジルコニウムジクロリド、ビス(シクロペンタジエニル)ジルコニウムクロロヒドリド、ビス(シクロペンタジエニル)メチルジルコニウムクロリド、ビス(シクロペンタジエニル)エチルジルコニウムクロリド、ビス(シクロペンタジエニル)メトキシジルコニウムクロリド、ビス(シクロペンタジエニル)フェニルジルコニウムクロリド、ビス(シクロペンタジエニル)ジメチルジルコニウム、ビス(シクロペンタジエニル)ジフェニルジルコニウム、ビス(シクロペンタジエニル)ジネオペンチルジルコニウム、ビス(シクロペンタジエニル)ジヒドロジルコニウム、ビス(シクロペンタジエニル)ジメトキシジルコニウム、更には、上記に記載の化合物において、これらの化合物の塩素原子を臭素原子、ヨウ素原子、水素原子、メチル基、フェニル基等に置き換えたもの、又、上記化合物の中心金属のジルコニウムをチタニウム、ハフニウムに置き換えたものを挙げることができる。
【0028】
前記一般式(II)で表されるメタロセン化合物の具体例としては、エチレン−ビス(シクロペンタジエニル)ハフニウムジクロリド、エチレン−ビス(シクロペンタジエニル)ジルコニウムジクロリド、メチレン−ビス(シクロペンタジエニル)ハフニウムジクロリド、メチレン−ビス(シクロペンタジエニル)ジルコニウムジクロリド、イソプロピリデン−ビス(シクロペンタジエニル)ハフニウムジクロリド、イソプロピリデン−ビス(シクロペンタジエニル)ジルコニウムジクロリド、ジメチルシリレン−ビス(シクロペンタジエニル)ハフニウムジクロリド、ジメチルシリレン−ビス(シクロペンタジエニル)ジルコニウムジクロリド等が挙げられる。
【0029】
前記一般式(III)で表されるメタロセン化合物の具体例としては、(1,1’−エチレン)(2,2’−エチレン)ビスシクロペンタジエニルジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(3−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(4−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(3,4−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(3,5−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビスシクロペンタジエニルジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(3−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(4−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(3,4−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(3,5−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビスシクロペンタジエニルジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(3−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(4−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(3,4−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(3,5−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−ジメチルシリレン)ビスシクロペンタジエニルジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−ジメチルシリレン)ビス(3−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−ジメチルシリレン)ビス(4−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−ジメチルシリレン)ビス(3,4−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−ジメチルシリレン)ビス(3,5−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−イソプロピリデン)ビス(3−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−イソプロピリデン)ビス(4−メチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−イソプロピリデン)ビス(3,4−ジメチルシクロペンタジエニル)ジルコニウムジクロリド、(1,1’−イソプロピリデン)(2,2’−イソプロピリデン)ビス(3,5−ジメチルシクロペンタジエニル)ジルコニウムジクロリド等のジクロル体及び上記化合物のジメチル体、ジエチル体、ジヒドロ体、ジフェニル体、ジベンジル体等ならびにそれらのチタン、ハフニウム錯体を例示することができる。
【0030】
前記一般式(IV)で表される化合物としては、例えば、(1,1’−エチレン)(2,2’−エチレン)ビスインデニルジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(3−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(4−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(5−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(5,6−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(4,5−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−エチレン)ビス(5,6−ジメチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビスインデニルジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(3−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(4−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(5−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(5,6−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(4,5−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)ビス(5,6−ジメチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビスインデニルジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(3−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(4−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(5−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(5,6−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(4,5−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−エチレン)ビス(5,6−ジメチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビスインデニルジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(3−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(4−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(5−メチルインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(5,6−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(4,5−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−エチレン)(2,2’−ジメチルシリレン)ビス(5,6−ジメチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビスインデニルジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(3−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(4−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(5−メチルインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(5,6−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(4,5−ベンゾインデニル)ジルコニウムジクロリド、(1,1’−ジメチルシリレン)(2,2’−イソプロピリデン)ビス(5,6−ジメチルインデニル)ジルコニウムジクロリド等のジクロル体及び上記化合物のジメチル体、ジエチル体、ジヒドロ体、ジフェニル体、ジベンジル体等ならびにそれらのチタン、ハフニウム錯体を例示することができる。
【0031】
(A)成分として用いられるメタロセン化合物としては、一種用いてもよく、二種以上を組み合わせて用いてもよい。
【0032】
(b−1)有機アルミニウムオキシ化合物としては、下記一般式(V)で示される鎖状アルミノキサン、及び、下記一般式(VI)で示される環状アルミノキサンを挙げることができる。
【0033】
【化5】

【0034】
(一般式(V)及び(VI)において、R20〜R25は、それぞれ独立に、炭素数1〜20、好ましくは1〜12の炭化水素基又はハロゲン原子を示す。当該炭化水素基としては、アルキル基,アルケニル基,アリール基,アリールアルキル基等が挙げられる。nは重合度を示し、通常2〜50、好ましくは2〜40の整数である。尚、各R20〜R25は互いに同じでも異なっていてもよい。)
【0035】
前記アルミノキサンの具体例としては、メチルアルミノキサン、エチルアルミノキサン、イソブチルアルミノキサン等が挙げられる。
【0036】
前記アルミノキサンの製造方法としては、アルキルアルミニウムと水等の縮合剤とを接触させる方法を挙げることができるが、その手段については特に限定はなく、公知の方法に準じて反応させればよい。例えば、有機アルミニウム化合物を有機溶剤に溶解しておき、これを水と接触させる方法、重合時に当初有機アルミニウム化合物を加えておき、後に水を添加する方法、金属塩等に含有されている結晶水、無機物や有機物への吸着水を有機アルミニウム化合物と反応させる方法、テトラアルキルジアルミノキサンにトリアルキルアルミニウムを反応させ、さらに水を反応させる方法等がある。尚、アルミノキサンとしては、トルエン不溶性のものであってもよい。これらのアルミノキサンは一種用いてもよく、二種以上を組み合わせて用いてもよい。
【0037】
一方、(b−2)成分としては、前記(A)成分のメタロセン化合物と反応してカチオンに変換しうるイオン性化合物であれば、いずれのものでも使用できるが、次の一般式(VII)、(VIII)で表されるものを好適に使用することができる。
([L1−R26]k+)a([Z]−)b ・・・(VII)
([L2]k+)a([Z]−)b ・・・(VIII)
【0038】
一般式(VII)において、L1はルイス塩基を示し、R26は水素原子、炭素数1〜20のアルキル基、又は、アリール基、アルキルアリール基及びアリールアルキル基から選ばれる炭素数6〜20の炭化水素基を示す。
【0039】
ここで、L1の具体例としては、アンモニア,メチルアミン,アニリン,ジメチルアミン,ジエチルアミン,N−メチルアニリン,ジフェニルアミン,N,N−ジメチルアニリン,トリメチルアミン,トリエチルアミン,トリ−n−ブチルアミン,メチルジフェニルアミン,ピリジン,p−ブロモ−N,N−ジメチルアニリン,p−ニトロ−N,N−ジメチルアニリン等のアミン類、トリエチルホスフィン,トリフェニルホスフィン,ジフェニルホスフィン等のホスフィン類、テトラヒドロチオフェン等のチオエーテル類、安息香酸エチル等のエステル類、アセトニトリル,ベンゾニトリル等のニトリル類等を挙げることができる。R26の具体例としては、水素原子,メチル基,エチル基,ベンジル基,トリチル基等を挙げることができる。
【0040】
一般式(VIII)において、L2はM1、R27R28M2、R29C又はR30M2を表す。R27及びR28は、それぞれ独立に、シクロペンタジエニル基、置換シクロペンタジエニル基、インデニル基又はフルオレニル基を示し、R29は炭素数1〜20のアルキル基、又は、アリール基、アルキルアリール基及びアリールアルキル基から選ばれる炭素数6〜20の炭化水素基を示す。R30はテトラフェニルポルフィリン、フタロシアニン等の大環状配位子を示す。
M1は、周期律表第1〜3、11〜13、17族元素を含むものであり、M2は、周期律表第7〜12族元素を示す。
【0041】
ここで、R27、R28の具体例としては、シクロペンタジエニル基、メチルシクロペンタジエニル基、エチルシクロペンタジエニル基、ペンタメチルシクロペンタジエニル基等を挙げることができる。R29の具体例としては、フェニル基,p−トリル基,p−メトキシフェニル基等を挙げることができ、R30の具体例としては、テトラフェニルポルフィリン,フタロシアニン等を挙げることができる。また、M1の具体例としては、Li,Na,K,Ag,Cu,Br,I,I3等を挙げることができ、M2の具体例としては、Mn,Fe,Co,Ni,Zn等を挙げることができる。
【0042】
一般式(VII)及び(VIII)において、kは[L1−R26]、[L2]のイオン価数で1〜3の整数、aは1以上の整数、b=(k×a)である。
[Z]−は、非配位性アニオン[Z1]−又は[Z2]−を表す。
[Z1]−は複数の基が元素に結合したアニオン、即ち[M3G1G2・・・Gf]−を表す。ここで、M3は周期律表第5〜15族元素、好ましくは周期律表第13〜15族元素を示す。G1〜Gfはそれぞれ水素原子、ハロゲン原子、炭素数1〜20のアルキル基、炭素数2〜40のジアルキルアミノ基、炭素数1〜20のアルコキシ基、炭素数6〜20のアリール基、炭素数6〜20のアリールオキシ基、炭素数7〜40のアルキルアリール基、炭素数7〜40のアリールアルキル基、炭素数1〜20のハロゲン置換炭化水素基、炭素数1〜20のアシルオキシ基又は有機メタロイド基又は炭素数2〜20のヘテロ原子含有炭化水素基を示す。G1〜Gfのうち二つ以上が環を形成してもよい。fは[(中心金属M3の原子価)+1]の整数を示す。
[Z2]−は酸解離定数の逆数の対数(pKa)が−10以下のブレンステッド酸単独又はブレンステッド酸及びルイス酸の組合わせの共役塩基、又は一般的に超強酸と定義される酸の共役塩基を示す。また、ルイス塩基が配位していてもよい。
【0043】
ここで、[Z1]−、即ち[M3G1G2・・・Gf]−において、M3の具体例としては、B,Al,Si,P,As,Sb等、好ましくはB及びAlを挙げることができる。また、G1,G2〜Gfの具体例としては、ジアルキルアミノ基としてジメチルアミノ基,ジエチルアミノ基等、アルコキシ基又はアリールオキシ基として、メトキシ基,エトキシ基,n−プロポキシ基,フェノキシ基等、炭化水素基として、メチル基,エチル基,n−プロピル基,イソプロピル基,n−ブチル基,イソブチル基,n−オクチル基,n−エイコシル基,フェニル基,p−トリル基,ベンジル基,4−t−ブチルフェニル基,3,5−ジメチルフェニル基等、ハロゲン原子として、フッ素,塩素,臭素,ヨウ素、ヘテロ原子含有炭化水素基として、p−フルオロフェニル基,3,5−ジフルオロフェニル基,ペンタクロロフェニル基,3,4,5−トリフルオロフェニル基,ペンタフルオロフェニル基,3,5−ビス(トリフルオロメチル)フェニル基,ビス(トリメチルシリル)メチル基等、有機メタロイド基として、ペンタメチルアンチモン基、トリメチルシリル基,トリメチルゲルミル基,ジフェニルアルシン基,ジシクロヘキシルアンチモン基,ジフェニルホウ素基等を挙げることができる。
【0044】
また、非配位性のアニオン、即ちpKaが−10以下のブレンステッド酸単独又はブレンステッド酸及びルイス酸の組合わせの共役塩基[Z2]−の具体例としては、トリフルオロメタンスルホン酸アニオン(CF3SO3)−,ビス(トリフルオロメタンスルホニル)メチルアニオン,ビス(トリフルオロメタンスルホニル)ベンジルアニオン,ビス(トリフルオロメタンスルホニル)アミド,過塩素酸アニオン(ClO4)−,トリフルオロ酢酸アニオン(CF3COO)−,ヘキサフルオロアンチモンアニオン(SbF6)−,フルオロスルホン酸アニオン(FSO3)−,クロロスルホン酸アニオン(ClSO3)−,フルオロスルホン酸アニオン/5−フッ化アンチモン(FSO3/SbF5)−,フルオロスルホン酸アニオン/5−フッ化ヒ素(FSO3/AsF5)−,トリフルオロメタンスルホン酸/5−フッ化アンチモン(CF3SO3/SbF5)−等を挙げることができる。
【0045】
このような(b−2)成分化合物の具体例としては、テトラフェニルホウ酸トリエチルアンモニウム,テトラフェニルホウ酸トリ−n−ブチルアンモニウム,テトラフェニルホウ酸トリメチルアンモニウム,テトラフェニルホウ酸テトラエチルアンモニウム,テトラフェニルホウ酸メチル(トリ−n−ブチル)アンモニウム,テトラフェニルホウ酸ベンジル(トリ−n−ブチル)アンモニウム,テトラフェニルホウ酸ジメチルジフェニルアンモニウム,テトラフェニルホウ酸トリフェニル(メチル)アンモニウム,テトラフェニルホウ酸トリメチルアニリニウム,テトラフェニルホウ酸メチルピリジニウム,テトラフェニルホウ酸ベンジルピリジニウム,テトラフェニルホウ酸メチル(2−シアノピリジニウム),テトラキス(ペンタフルオロフェニル)ホウ酸トリエチルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸トリ−n−ブチルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸トリフェニルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸テトラ−n−ブチルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸テトラエチルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸ベンジル(トリ−n−ブチル)アンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸メチルジフェニルアンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸トリフェニル(メチル)アンモニウム,テトラキス(ペンタフルオロフェニル)ホウ酸メチルアニリニウム,テトラキス(ペンタフルオロフェニル)ホウ酸ジメチルアニリニウム,テトラキス(ペンタフルオロフェニル)ホウ酸トリメチルアニリニウム,テトラキス(ペンタフルオロフェニル)ホウ酸メチルピリジニウム,テトラキス(ペンタフルオロフェニル)ホウ酸ベンジルピリジニウム,テトラキス(ペンタフルオロフェニル)ホウ酸メチル(2−シアノピリジニウム),テトラキス(ペンタフルオロフェニル)ホウ酸ベンジル(2−シアノピリジニウム),テトラキス(ペンタフルオロフェニル)ホウ酸メチル(4−シアノピリジニウム),テトラキス(ペンタフルオロフェニル)ホウ酸トリフェニルホスホニウム,テトラキス[ビス(3,5−ジトリフルオロメチル)フェニル]ホウ酸ジメチルアニリニウム,テトラフェニルホウ酸フェロセニウム,テトラフェニルホウ酸銀,テトラフェニルホウ酸トリチル,テトラフェニルホウ酸テトラフェニルポルフィリンマンガン,テトラキス(ペンタフルオロフェニル)ホウ酸フェロセニウム,テトラキス(ペンタフルオロフェニル)ホウ酸(1,1’−ジメチルフェロセニウム),テトラキス(ペンタフルオロフェニル)ホウ酸デカメチルフェロセニウム,テトラキス(ペンタフルオロフェニル)ホウ酸銀,テトラキス(ペンタフルオロフェニル)ホウ酸トリチル,テトラキス(ペンタフルオロフェニル)ホウ酸リチウム,テトラキス(ペンタフルオロフェニル)ホウ酸ナトリウム,テトラキス(ペンタフルオロフェニル)ホウ酸テトラフェニルポルフィリンマンガン,テトラフルオロホウ酸銀,ヘキサフルオロリン酸銀,ヘキサフルオロヒ素酸銀,過塩素酸銀,トリフルオロ酢酸銀,トリフルオロメタンスルホン酸銀等を挙げることができる。
【0046】
この(b−2)成分は一種用いてもよく、また二種以上を組み合わせて用いてもよい。本発明において、(B)成分を用いる場合、(A)成分と(B)成分との使用割合は、(B)成分として(b−1)成分を用いた場合には、モル比で、好ましくは1:1〜1:1,000,000、より好ましくは1:10〜1:10,000、(b−2)成分を用いた場合には、モル比で、好ましくは10:1〜1:100、より好ましくは2:1〜1:10である。また、(B)成分としては、(b−1)及び(b−2)等を単独又は二種以上組み合わせて用いることもできる。
【0047】
本発明における触媒としては、前記の(A)成分及び(B)成分を主成分として含有するものであってもよいし、また、(A)成分、(B)成分及び(C)有機アルミニウム化合物を主成分として含有するものであってもよい。ここで、(C)成分の有機アルミニウム化合物としては、一般式(IX)
(R31)vAlQ3−v ・・・(IX)
(式中、R31は炭素数1〜10のアルキル基、Qは水素原子、炭素数1〜20のアルコキシ基,炭素数6〜20のアリール基又はハロゲン原子を示し、vは1〜3の整数である。)で示される化合物が用いられる。
【0048】
前記一般式(IX)で示される化合物の具体例としては、トリメチルアルミニウム,トリエチルアルミニウム,トリイソプロピルアルミニウム,トリイソブチルアルミニウム,ジメチルアルミニウムクロリド,ジエチルアルミニウムクロリド,メチルアルミニウムジクロリド,エチルアルミニウムジクロリド,ジメチルアルミニウムフルオリド,ジイソブチルアルミニウムヒドリド,ジエチルアルミニウムヒドリド,エチルアルミニウムセスキクロリド等を挙げることができる。これらの有機アルミニウム化合物は、一種用いてもよく、二種以上を組合せて用いてもよい。前記(A)成分と(C)成分との使用割合は、モル比で、好ましくは1:1〜1:10,000、より好ましくは1:5〜1:2,000、さらに好ましくは1:10〜1:1,000である。この(C)成分を用いることにより、遷移金属当たりの活性を向上させることができるが、あまり多いと有機アルミニウム化合物が無駄になるとともに、α−オレフィン重合体中に多量に残存し、好ましくない。
【0049】
本発明において、重合方法は特に制限されず、塊状重合法、溶液重合法、懸濁重合法、スラリー重合法、気相重合法等のいずれの方法を用いてもよい。
重合条件については、重合温度は通常0〜200℃、好ましくは30〜150℃、より好ましくは40〜120℃である。また、原料モノマーに対する触媒の使用割合は、原料モノマー/上記(A)成分(モル比)が好ましくは1〜108,特に100〜105となることが好ましい。さらに、重合時間は通常5分〜20時間、反応圧力は好ましくは常圧〜0.2MPaG、特に好ましくは常圧〜0.1MPaGである。
【0050】
重合工程はコスト面から無溶媒で行うことが好ましいが、溶媒を用いることもできる。その場合、例えば、ベンゼン,トルエン,キシレン,エチルベンゼン等の芳香族炭化水素、シクロペンタン,シクロヘキサン,メチルシクロヘキサン等の脂環式炭化水素、ペンタン,ヘキサン,ヘプタン,オクタン等の脂肪族炭化水素、クロロホルム,ジクロロメタン等のハロゲン化炭化水素等を用いることができる。これらの溶媒は一種を単独で用いてもよく、二種以上のものを組み合わせてもよい。また、1−デセン等のモノマーを溶媒として用いてもよい。
【0051】
重合後、過度の重合を防止するために、重合反応液に失活剤(触媒非活性化剤)を加えて重合触媒を失活させる。
希釈溶媒の添加は、失活剤の添加の前に添加してもよいし、失活剤の添加と共に添加してもよい。
重合触媒を失活させる前に希釈を行う場合、希釈後、できるだけ速やかに触媒失活を行うことが望ましい。希釈から失活までの時間が長いと、重合生成物が影響を受ける恐れがあるためである。
一方、重合反応の開始前又は重合反応中に希釈溶媒を添加すると、反応器内のモノマー濃度が低下して重合反応速度が低下するため、生産性が低下する恐れがある。
本発明では、重合反応液を溶媒で希釈し、油相粘度を低下させるため、油水混合のための撹拌槽、油水分離のための静置分離槽、微粒子除去のためのフィルター設備をサイズダウンすることができ、コストダウンにも繋がる。
【0052】
上記希釈は、失活時の重合反応液の液粘度が10mPa・s以下、好ましくは5mPa・s以下となるように行う。液粘度は実施例に記載の方法で測定できる。
尚、失活時の重合反応液の液粘度は、希釈後の重合反応溶液と同じである。
失活剤と混合したとき、液液分離する場合は、重合反応液の液粘度として、通常、油相側の液粘度を測定する。
希釈後の重合反応液の液粘度が高いと、触媒の失活が遅くなり、ろ過を行っても触媒由来のアルミニウムが重合反応液中に溶解した状態で残存する恐れがある。
【0053】
図2に、重合反応液(80℃における液粘度:78mPa・s)に1−デセンを加えて希釈した場合の、希釈溶媒の添加量(希釈率)と重合反応液の液粘度の関係を示す。図2においてドットは実測値である。
希釈率[%]=[R/(R+F)]×100[wt./wt.]
F:重合反応液量
R:希釈溶媒量
【0054】
希釈に用いる溶媒(希釈液)は、通常、重合生成物に影響しないような不活性炭化水素系溶媒を用いることができる。例えば、トルエン、キシレン等の環状炭化水素、1−デセン、1−オクテン、1−ドデセン等の炭素数6〜20の不飽和炭化水素、又はこれらの2量体を用いることもできる。
また、前述した重合工程溶媒を用いることができる。
ただし、重合反応液に対して十分粘度が低いことが求められるので、希釈溶媒の液粘度は、例えば、40℃において1mPa・s以下であり、望ましくは0.5mPa・s以下である。
【0055】
また、後工程(失活後)、即ち、失活に続く工程で、蒸留分離が可能であるように、希釈溶媒の沸点は好ましくは250℃以下、より好ましくは200℃以下、さらに好ましくは100℃以下である。希釈溶媒の沸点がこの範囲であると、後述する蒸留工程で希釈溶媒を蒸留分離し、希釈・失活工程で再度重合反応液の希釈に用いることができる。
【0056】
失活剤としては、例えばアルコール、水、及び酸、アルカリ、含酸素化合物等の水溶液が挙げられ、具体的には、水酸化ナトリウム水溶液、エタノール、イソプロピルアルコール、塩酸及びアセトン等が挙げられる。
【0057】
失活剤の添加後、通常、図1に示すような脱灰、蒸留を経てオレフィン重合体を得ることができる。
図1に示すように、蒸留除去された軽質分(未反応モノマーや重合溶媒、オレフィン重合体2量体等)をリサイクルし、失活の際の希釈溶媒として用いるとコストの面から望ましい。
【0058】
脱灰で除かれる金属として触媒、助触媒に含まれるアルミニウム、ジルコニウム等が挙げられる。
金属除去率が高いほど潤滑油として好ましい性状となる。通常の触媒使用量であれば95%以上の金属除去率が求められ、そのためには失活時の重合反応液の液粘度を10mPa・s以下とすることが好ましい。さらに97%以上の金属除去率が求められる場合には、5mPa・s以下まで低下させることがより好ましい。
【0059】
触媒の金属成分を除去後、上記の重合反応液を蒸留して軽質分を留去し、オレフィンオレゴマーを得る。
【実施例】
【0060】
実施例1
[触媒の調製]
500mLのガラス製シュレンク瓶に窒素雰囲気下で、以下の化合物を以下の割合で混合して触媒溶液A,B,Nを調製した。
触媒溶液A:トルエン1Lに対してトリイソブチルアルミニウム50mmol
触媒溶液B:トルエン1Lに対して粉末状のN,N−ジメチルアニリニウム−テトラキス(ペンタフルオロフェニル)ボレート4mmol
触媒溶液N:トルエン1Lに対して(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)−ビス(シクロペンタジエニル)ジルコニウムジクロリド1mmol
【0061】
[重合反応]
内容積100Lのステンレス製オートクレーブを十分乾燥し、窒素乾燥の後に、1−オクテン11.94kgと1−ドデセン17.99kgを仕込み、水素0.02MPaGを導入し、触媒溶液Aを400mL入れて、95℃に昇温し、1時間保持した。
次に触媒溶液B200mL、及び触媒溶液N200mLをオートクレーブに投入し、105℃に昇温して保持した。
【0062】
30分後、触媒溶液A200mL、触媒溶液B200mL、触媒溶液N200mLをオートクレーブに投入した。
30分後(反応開始から1時間後)、触媒溶液A300mL、触媒溶液B300mL、及び触媒溶液N300mLをオートクレーブに投入した。
1時間後(反応開始から2時間後)、触媒溶液A400mL、触媒溶液B400mL、及び触媒溶液N400mLをオートクレーブに投入した。
1時間後(反応開始から3時間後)、触媒溶液A400mL、触媒溶液B400mL、及び触媒溶液N400mLをオートクレーブに投入した。
1時間後(反応開始から4時間後)、触媒溶液A500mL、触媒溶液B500mL、及び触媒溶液N500mLをオートクレーブに投入した。
1時間後(反応開始から5時間後)、触媒溶液A500mL、触媒溶液B500mL、及び触媒溶液N500mLをオートクレーブに投入した。
2時間後(反応開始から7時間後)、内容物を重合反応液として取り出した。
重合反応中の平均温度は105℃であり、この重合反応液の原料転化率は90%、40℃における液粘度は91mPa・sであった。
【0063】
転化率と液粘度は以下の方法で測定した。
(1)転化率
試料0.05gをジクロロメタン5mlに溶解してガスクロマトグラフィー(GC)を用いて算出した。
(GC測定条件)
カラム:HT−SIMDISTCB(5m×0.53mmφ,膜厚:0.17μm)
カラム温度:40℃(0.1min)、20℃/minで420℃まで上昇、420℃(15min)
注入口(COC)温度:オーブントラック
検出器(FID)温度:440℃
キャリアガス:He
線速度:40cm/sec
モード:コンスタントフロー
注入量:0.5μl
(2)液粘度
エー・アンド・デイ株式会社製の音叉型振動式粘度計で測定した。
【0064】
[希釈・失活・脱灰]
重合反応液400gと、1−デセン600g(40℃における液粘度:0.4mPa・s)を2Lフラスコで混合し、希釈した重合反応液を得た。希釈した重合反応液の40℃における粘度は8.4mPa・sであった。
この希釈した重合反応液と1%水酸化ナトリウム水溶液を油水比(W/O)0.1[vol/vol]で、加温したスタティックミキサーを用いて、80℃において混合した。このときの油相粘度は80℃で4.2mPa・sであり、撹拌強度は約20kW/m3(通過線速約0.2m/s)であり、滞留時間は約1秒であった。
【0065】
油水混合液を窒素雰囲気でメスシリンダーに採取し、油水分離後、油相をサンプリングして、公称孔径0.2μm(ADVANTEC社製 T020A−)のフィルターを用いて、固体微粒子を濾過して除去した。
その結果、濾液中の金属分濃度は20wtppmから1wtppm未満まで低下した。金属分濃度は灰化処理の後、ICP発光法で分析した。
尚、灰化処理とは、金属分の定量のために、サンプルを燃焼して含まれる金属分を灰にすることである。
【0066】
比較例1
[触媒の調製]
触媒溶液として、以下の触媒溶液A’、B’及びN’をそれぞれ100mLのガラス製シュレンク瓶に窒素雰囲気下で調製した。
触媒溶液A’:トリイソブチルアルミニウムの1mmol/mLトルエン溶液;45mL
触媒溶液B’:N,N−ジメチルアニリニウム−テトラキス(ペンタフルオロフェニル)ボレートの40mmol/Lトルエン溶液;90mL
触媒溶液N’:(1,1’−ジメチルシリレン)(2,2’−ジメチルシリレン)−ビス(シクロペンタジエニル)ジルコニウムジクロリドの10mmol/Lトルエン溶液;90mL
【0067】
[重合反応]
内容積100Lのステンレス製オートクレーブを十分乾燥し、窒素乾燥の後に、1−オクテン18.1kgと1−ドデセン26.7kgを仕込み、トリイソブチルアルミニウム9mmol(トルエン溶液9L)を入れて、水素0.01MPaGを導入し、90℃に昇温した。
上記の触媒溶液A’,B’,N’を以下の所定量で、以下のように順次投入しながら、5時間反応させた。触媒投入は計4回行い、4回目の触媒投入後2時間反応させた。内容物を重合反応液として取り出した。この重合反応液は原料転化率90%であり、40℃における液粘度は175mPa・sであった。
【0068】
反応開始(スタート)=触媒投入1回目
反応開始1時間経過後=触媒投入2回目
反応開始2時間経過後=触媒投入3回目
反応開始3時間経過後=触媒投入4回目
反応開始5時間経過後=反応終了
1回の触媒投入量は、触媒溶液A’11.25mL、触媒溶液N’22.5mL、及び触媒溶液B’22.5mLとした。
【0069】
[失活・脱灰]
上記の重合反応液と1%水酸化ナトリウム水溶液を油水比(W/O)0.5[vol/vol]で、バッチ式の撹拌槽を用いて80℃において混合した。80℃における油相粘度は78mPa・sであった。
このときの撹拌強度は約0.2kW/m3(撹拌回転数200rpm)で、撹拌時間は10分間とした。その後、撹拌を停止し、30分間静置して、油水分離後、油相をサンプリングして、公称孔径0.8μm(ADVANTEC社製 T080A−)のフィルターを用いて、固体微粒子を濾過して除去した。
その結果、濾液中の金属分濃度は、28wtppmから10wtppmまで低下した。金属分濃度は灰化処理を行った後、ICP発光法で分析した。
【0070】
比較例2
[重合反応]
比較例1の[重合反応]と同様にして重合反応液を得た。
【0071】
[希釈・失活・脱灰]
上記の重合反応液300mLと触媒溶液A’2mL、トルエン200mLを十分に混合し、80℃における液粘度を17mPa・s(40℃における液粘度:40mPa・s)に調整した。この粘度調整した重合反応液と1%水酸化ナトリウム水溶液を油水比(W/O)[0.2vol/vol]で、スタティックミキサーを用いて80℃において混合した。80℃における油相粘度は17mPa・sであった。
尚、重合反応液に触媒溶液A’を加えたのは、金属分を増加することで、液粘度による効果の有無を明確にするためである。
【0072】
このときの撹拌強度は約250kW/m3(通過線速約0.85m/s)であり、滞留時間は約0.1秒であった。油水混合液を窒素雰囲気でメスシリンダーに採取し、油水分離後、油相をサンプリングして、公称孔径0.2μm(ADVANTEC社製 T020A−)のフィルターを用いて、固体微粒子を濾過して除去した。
その結果、濾液中の金属分濃度は、130wtppmから17wtppmまで低下した。金属分濃度はICP発光法で分析した。
【0073】
比較例3
[重合反応]
比較例1の[重合反応]と同様にして重合反応液を得た。
【0074】
[希釈・失活・脱灰]
上記の重合反応液475mLと触媒溶液A’2mL、トルエン25mLを十分に混合し、80℃における液粘度を60mPa・s(40℃における液粘度:128mPa・s)に調整した。この粘度調整した重合反応液と1%水酸化ナトリウム水溶液を油水比(W/O)0.2[vol/vol]で、スタティックミキサーを用いて80℃において混合した。80℃における油相粘度は60mPa・sであった。
【0075】
このときの撹拌強度は約20kW/m3(通過線速約0.2m/s)であり、滞留時間は約1秒であった。油水混合液を窒素雰囲気でメスシリンダーに採取し、油水分離後、油相をサンプリングして、公称孔径0.8μm(ADVANTEC社製 T080A−)のフィルターを用いて、固体微粒子を濾過して除去した。
その結果、濾液中の金属分濃度は、155wtppmから43wtppmまで低下した。金属分濃度はICP発光法で分析した。
【0076】
実施例及び比較例の結果(重合反応液の液粘度と金属除去率の関係)を図3に示す。図3より、重合反応液の液粘度の上昇に伴って、触媒由来の金属除去率は顕著に低下する。
【産業上の利用可能性】
【0077】
本発明の製造方法によって得られたオレフィン重合体は潤滑油基材として使用できる。
【特許請求の範囲】
【請求項1】
メタロセン触媒存在下、1種以上の炭素数6〜20のα−オレフィンを重合してオレフィン重合体を製造し、前記触媒の失活前又は失活と同時に、溶媒で重合反応液を希釈することにより、失活時の重合反応液の液粘度を10mPa・s以下に低下させ、触媒の失活脱灰を促進するオレフィン重合体の製造方法。
【請求項2】
前記溶媒として、後工程で除去可能である沸点を有する溶媒を用いる請求項1に記載のオレフィン重合体の製造方法。
【請求項3】
前記溶媒として、後工程で除去した未反応モノマー又は重合反応溶媒を用いる請求項1又は2に記載のオレフィン重合体の製造方法。
【請求項4】
請求項1〜3のいずれかに記載のオレフィン重合体の製造方法により得られるオレフィン重合体。
【請求項1】
メタロセン触媒存在下、1種以上の炭素数6〜20のα−オレフィンを重合してオレフィン重合体を製造し、前記触媒の失活前又は失活と同時に、溶媒で重合反応液を希釈することにより、失活時の重合反応液の液粘度を10mPa・s以下に低下させ、触媒の失活脱灰を促進するオレフィン重合体の製造方法。
【請求項2】
前記溶媒として、後工程で除去可能である沸点を有する溶媒を用いる請求項1に記載のオレフィン重合体の製造方法。
【請求項3】
前記溶媒として、後工程で除去した未反応モノマー又は重合反応溶媒を用いる請求項1又は2に記載のオレフィン重合体の製造方法。
【請求項4】
請求項1〜3のいずれかに記載のオレフィン重合体の製造方法により得られるオレフィン重合体。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2013−18906(P2013−18906A)
【公開日】平成25年1月31日(2013.1.31)
【国際特許分類】
【出願番号】特願2011−154777(P2011−154777)
【出願日】平成23年7月13日(2011.7.13)
【出願人】(000183646)出光興産株式会社 (2,069)
【Fターム(参考)】
【公開日】平成25年1月31日(2013.1.31)
【国際特許分類】
【出願日】平成23年7月13日(2011.7.13)
【出願人】(000183646)出光興産株式会社 (2,069)
【Fターム(参考)】
[ Back to top ]

