オートタキシン測定によるステロイド服用効果の検査方法
【課題】ステロイドの服用または服用効果を簡便にモニター可能な方法およびそれを利用した試薬を提供すること。
【解決手段】ステロイドの服用によりヒト血液中のオートタキシン濃度が低値化することを利用したステロイド服用効果の検査方法、および前記方法を利用した検査試薬により、前記課題を解決する。
【解決手段】ステロイドの服用によりヒト血液中のオートタキシン濃度が低値化することを利用したステロイド服用効果の検査方法、および前記方法を利用した検査試薬により、前記課題を解決する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明はヒト検体中のオートタキシン濃度を測定することでステロイドの服用または服用効果をモニターする方法、前記方法を利用した試薬、およびステロイド服用によるヒトオートタキシンの低減方法に関する。
【背景技術】
【0002】
ステロイド薬は、その抗炎症作用、抗アレルギー作用、免疫抑制作用から非常に広い疾患で用いられる薬である。具体的には、
(1)内科・小児科領域においては、
(1−1)甲状腺疾患における慢性副腎皮質機能不全、急性副腎皮質機能不全、副腎性器症候群、亜急性甲状腺炎、甲状腺中毒症、甲状腺疾患に伴う悪性眼球突出症、ACTH(副腎皮質刺激ホルモン)単独欠損症、
(1−2)リウマチ疾患における関節リウマチ、若年性関節リウマチ、リウマチ熱、リウマチ性多発筋痛、膠原病におけるエリテマトーデス、全身性血管炎、多発性筋炎、皮膚筋炎、強皮症、
(1−3)腎疾患におけるネフローゼ及びネフローゼ症候群、
(1−4)心疾患におけるうっ血性心不全、
(1−5)アレルギー性疾患における気管支喘息、喘息性気管支炎、薬剤その他の化学物質によるアレルギー・中毒、血清病、重症感染症における重症感染症、
(1−6)血液疾患における溶血性貧血、白血病、顆粒球減少症、紫斑病、再生不良性貧血、凝固因子の障害による出血性素因、
(1−7)消化器疾患における限局性腸炎、潰瘍性大腸炎、
(1−8)重症消耗性疾患における全身状態の改善、
(1−9)肝疾患における劇症肝炎、胆汁うっ滞型急性肝炎、慢性肝炎、肝硬変、
(1−10)肺疾患におけるサルコイドーシス、びまん性間質性肺炎、
(1−11)結核性疾患における肺結核、結核性髄膜炎、結核性胸膜炎、結核性腹膜炎、結核性心のう炎、
(1−12)神経疾患における脳脊髄炎、末梢神経炎、筋強直症、重症筋無力症、多発性硬化症、小舞踏病、顔面神経麻痺、脊髄蜘網膜炎、
(1−13)悪性腫瘍における悪性リンパ腫及び類似疾患(近縁疾患)、乳癌の再発転移、
(1−14)その他の内科的疾患として特発性低血糖症、原因不明の発熱、
(2)外科領域における副腎摘除、臓器・組織移植、侵襲後肺水腫、副腎皮質機能不全患者に対する外科的侵襲、蛇毒・昆虫毒、
(3)整形外科領域における強直性脊椎炎、
(4)産婦人科領域における卵管整形術後の癒着防止、副腎皮質機能障害による排卵障害、
(5)泌尿器科領域における前立腺癌、陰茎硬結、
(6)皮膚科領域における外用薬が功を奏さないまたは重傷の湿疹・皮膚炎群、痒疹群、乾癬、掌蹠膿疱症、毛孔性紅色粃糠疹、扁平苔癬、成年性浮腫性硬化症、紅斑症、アナフィラクトイド紫斑、ウェーバークリスチャン病、皮膚粘膜眼症候群、レイノー病、円形脱毛症、天疱瘡群、デューリング疱疹状皮膚炎、先天性表皮水疱症、帯状疱疹、紅皮症、顔面播種状粟粒性狼瘡、アレルギー性血管炎、潰瘍性慢性膿皮症、新生児スクレレーマ、好酸球性筋膜炎、
(7)眼科領域における内眼・視神経・眼窩・眼筋の炎症性疾患、外眼部及び前眼部の炎症性疾患、術後炎症、
(8)耳鼻咽喉科領域における急性・慢性中耳炎、滲出性中耳炎・耳管狭窄症、メニエル病及びメニエル症候群、急性感音性難聴、血管運動性鼻炎、アレルギー性鼻炎、花粉症、副鼻腔炎・鼻茸、進行性壊疽性鼻炎、喉頭炎・喉頭浮腫、食道の炎症及び食道拡張術後、耳鼻咽喉科領域の手術後の後療法、難治性口内炎及び舌炎、嗅覚障害、急性・慢性唾液腺炎、
などの治療に用いられる。
【0003】
このように非常に多岐に渡り利用されているステロイド薬であるが、副作用、特に長期服用または大量服用による副作用が問題となっている。副作用としては血圧上昇、浮腫、耐糖能障害、脂質代謝異常、骨粗鬆症、骨頭無菌性壊死、消化性潰瘍、筋力低下、ムーンフェイス、精神症状、不眠、ざ瘡、皮膚線条、白内障、緑内障、白血球増多、低カリウム血症、副腎皮質機能不全などが知られている。
【0004】
したがって、ステロイド薬を投与するに際しては、治療効果が確認され次第、速やかに投与を停止または投与量を低減させるのが好ましい。しかし、ステロイド薬の生体内濃度測定は容易ではなく、血液検体からの抽出、大型装置での分析などが必要なため汎用できるものではない。また、ステロイド薬は前述したように非常に多くの疾患で利用されており、ステロイド薬を処方された患者によっては服用コンプライアンスが遵守されない場合も少なくないが、それを確認するのは困難である。ステロイド薬の処方は、服用による外見的治療効果の確認や副作用の発生などにより調整される場合がほとんどであり、生体内濃度など定量的制御がされていないため、過剰服用による副作用が懸念されている。そのため、生体内におけるステロイド薬の濃度を簡便にモニターでき、かつ必要以上のステロイド薬の服用が避けられるステロイド薬モニター方法が切望されている。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】WO2008/016186号
【非特許文献】
【0006】
【非特許文献1】J.Biol.Chem.、256、2524−2529、1992
【非特許文献2】Nat.Rev.Cancer、3、582−591、2003
【非特許文献3】Int.J.Cancer、10、109、833−838、2004
【非特許文献4】Blood、106、2138−2146、2005
【非特許文献5】Clin.Chim.Acta、388、51−58、2008
【発明の概要】
【発明が解決しようとする課題】
【0007】
ステロイドを服用する治療は非常に多岐にわたる疾患で実施されているが、副作用が大きいことから過剰服用は回避するのが好ましい。ステロイドを服用する治療では、疾病の治癒の確認により服用量の低減または停止をコントロールしたり、副作用の発症確認のもと服用量をコントロールするのが現状である。また、ステロイド薬は汎用されていることから服用コンプライアンスの遵守が行われないケースも多く、服用量を定量的にモニター可能な方法が切望されている。しかしながら、従来のステロイド薬のモニター方法は高度な分析技術、装置が必要であるため簡便には実施できなかった。
【0008】
そこで、本願発明の課題は簡便にステロイド薬のモニターが可能な方法およびそれを利用した試薬を提供することにある。
【課題を解決するための手段】
【0009】
前記課題を鑑み発明者が鋭意検討した結果、皮膚疾患治療においてステロイド服用を実施することにより血清中のオートタキシン濃度が低下することを見出し、かつ前記現象は皮膚疾患の種類によらずステロイド服用による一般的な現象であることを見出すことで、本発明を完成するに至った。
【0010】
詳しくは、本願は下記の発明を包含する:
(1)ヒト検体中のオートタキシン濃度を測定することによるステロイド服用効果の検査方法。
(2)ステロイド服用前のヒト検体中のオートタキシン濃度を指標とする(1)に記載の検査方法。
(3)ステロイドがプレドニゾロン、コルチゾン、ヒドロコルチゾン、メチルプレドニゾロン、デキサメタゾン、ベタメタゾンのいずれかである(1)または(2)に記載の検査方法。
(4)免疫化学的手法でヒト検体中のオートタキシン濃度を測定する(1)から(3)のいずれかに記載の検査方法。
(5)ヒト検体中のオートタキシン濃度を測定する方法がリゾホスホリパーゼD活性を測定する方法である(1)から(3)のいずれかに記載の検査方法。
(6)(1)から(5)のいずれかに記載の検査方法を利用したステロイド服用効果の検査試薬。
(7)ステロイドを服用することによるヒトオートタキシンの低減方法。
(8)ステロイドおよびオートタキシン拮抗剤を併用服用することによるヒトオートタキシンの低減方法。
(9)ステロイドがプレドニゾロン、コルチゾン、ヒドロコルチゾン、メチルプレドニゾロン、デキサメタゾン、ベタメタゾンのいずれかである(7)または(8)に記載の低減方法。
(10)悪性腫瘍の増殖または転移の阻害を目的とする(7)から(9)のいずれかに記載の低減方法。
(11) ヒトオートタキシンの低減を必要とする疾患を患うヒトのための、ステロイドを投与することによるヒトオートタキシンの低減方法。
(12) ヒトオートタキシンの低減を必要とする疾患が、悪性腫瘍、妊娠高血圧症候群及び慢性肝疾患から選ばれる疾患である、(11)の低減方法。
(13) ステロイドを含むヒトオートタキシン低減用の医薬組成物。
(14) さらに、オートタキシン拮抗剤を含む(13)に記載の医薬組成物。
(15) ヒト検体中のオートタキシン濃度を測定し、基準と比較することによるステロイド服用効果の検査方法。
(16) ステロイドの用量とオートタキシン濃度についての検量線に基づき、ステロイド服用前に測定したヒト検体中のオートタキシン濃度から算出したオートタキシン濃度予測値を基準とする、(15)に記載のステロイド服用効果の検査方法。
【発明の効果】
【0011】
本発明によれば、ヒト検体中のオートタキシン濃度を測定することによりステロイド服用モニターが定量的に可能となる。オートタキシンの測定はオートタキシンが有する酵素活性であるリゾホスホリパーゼD活性を測定することでも可能であるが、特許文献1に記載の免疫学的定量試薬を用いて測定すると検体中に含まれる内在性の測定妨害因子や競合酵素の影響を受けることなく、かつ短時間でヒトオートタキシンを定量可能である。さらに、ステロイド服用によりヒトオートタキシンが低減するため、ヒトオートタキシン低減を目的とした治療、例えば癌の増殖や転移に対してステロイドを服用することにより、ヒトオートタキシンを効率よく低減させることが期待できる。
【図面の簡単な説明】
【0012】
【図1】好酸球性筋膜炎患者(A)および皮膚筋炎患者(B)におけるプレドニゾロン服用時の血清オートタキシン濃度の変動を示す。図中数値は前日のプレドニゾロン服用量(mg/日)を示す。
【図2】2例の全身性強皮症患者(A)(B)におけるプレドニゾロン服用時の血清オートタキシン濃度の変動を示す。図中数値は前日のプレドニゾロン服用量(mg/日)を示す。
【図3】全身性強皮症におけるプレドニゾロン服用時のオートタキシン濃度およびリゾホスホリパーゼD活性の変動を示す。図中黒丸はオートタキシン濃度を、白四角はリゾホスホリパーゼD活性を、それぞれ示す。図中数値は前日のプレドニゾロン服用量(mg/日)を示す。
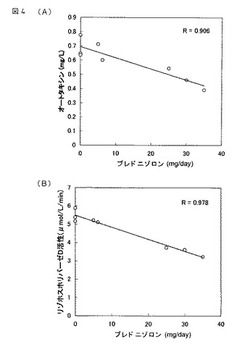
【図4】プレドニゾロン服用量とオートタキシン濃度(A)またはリゾホスホリパーゼD活性(B)との相関性を示す。
【発明を実施するための形態】
【0013】
以下、本発明を詳細に説明する。
ヒトオートタキシンは、1992年にM.L.StrackeらによってA2058ヒト黒色腫細胞培養培地から細胞運動性を惹起する物質として単離された分子量約125KDaの糖蛋白質である(非特許文献1)。オートタキシンはそのリゾホスホリパーゼD活性によりリゾホスファチジルコリンを基質としリゾホスファチジン酸(LPA)を産生する。生体内ではLPAが癌の増殖や転移に関与していることが多くの研究者により示され(非特許文献2から4)、その産生酵素であるオートタキシンと様々な疾病との因果関係が研究されている。最近になり、ヒトオートタキシンを定量する手法が確立され(特許文献1、非特許文献5)、様々な疾患の診断マーカーとして期待されている。
【0014】
そこで、発明者がステロイド服用とオートタキシン濃度との関係を鋭意検討した結果、
ステロイド服用によりヒト血液中のオートタキシン濃度が低値化することを見出し、さらにステロイド服用量に比例してヒト血液中のオートタキシン濃度が低値化することを見出した。ヒト検体中のオートタキシン濃度は、例えば特許文献1に記載の免疫化学的手法を用いた方法により検体の前処理を必要とすることなく精度よく定量できる。そのため、例えば特許文献1に記載の方法を利用した試薬でヒト検体中のオートタキシン濃度を測定することにより、これまで困難であったステロイド服用効果の定量的モニターが容易となり、ステロイド薬の過剰投与を定量的にコントロールすることが可能となる。また本発明の方法により、服用コンプライアンスが遵守されているか確認可能となる。
【0015】
ステロイドを服用した場合、ステロイド服用量やステロイドの種類に応じて、オートタキシン濃度が用量依存的に減少する(図4A)。したがって、ステロイドを服用後の患者のオートタキシン濃度は、図4Aのようにステロイド服用量とオートタキシン濃度(又は低減割合)をプロットして直線回帰することにより得た検量線を用いて、予測することができる。検量線は、ステロイド毎に定める必要がある。
【0016】
医師は、ステロイドの用量とオートタキシン濃度(又は低減割合)についての検量線に基づき、処方したステロイド用量から患者のオートタキシン濃度を予測することができ、この予測値に対して患者におけるオートタキシン濃度の実測値が有意に高いか又は低い場合、服薬コンプライアンスが遵守されていないと判断することができる。例えば、医師が1日30mgのプレドニゾロンを処方している場合、図4Aの検量線に従うと、服用前のオートタキシン濃度に対して約30%程度低下することが予測され、この予測濃度より有意に高い又は低い場合は服薬コンプライアンスが遵守されていないこととなる。具体的に、検量線から得られた予測値に対して、少なくとも10%以上、好ましくは20%、30%、40%、50%、70%、80%、又は90%の乖離がある場合、服薬コンプライアンスが遵守されていないと判断することができる。
【0017】
ステロイドの服用効果をモニターする場合、服用前のオートタキシン濃度からの低下割合を、治療段階に応じて決められた一定の範囲に保つことが望まれる。ステロイドは一般に副作用が強く、かつ退薬症状が出ることが知られているため、副作用を抑えつつ治療を行い、かつ退薬症状を抑えるため、治療の初期段階では比較的高いオートタキシン濃度の低下割合、例えば40〜70%、好ましくは50〜60%の低下割合を維持し、治療の進行と供に、徐々にオートタキシン濃度の低下割合を低減するように、ステロイド量をコントロールすることが望ましい。例えば、治療中期では20〜50%、好ましくは30〜40%の低下割合、治療後期では10〜30%、好ましくは10〜20%の低下割合を維持するようにステロイド量をコントロールすることが望ましい。
【0018】
今回見出したステロイド服用によるヒト検体中のオートタキシン濃度の低値化現象から、ステロイド服用がヒトオートタキシンを低減する手法となり得ることが期待される。そのため、患者へステロイドを服用する手法が、ヒトオートタキシンが関与する疾患、特にヒトオートタキシンが有するリゾホスホリパーゼD活性により産生されるLPAが関与する癌の増殖や転移を制御する手法となり得ることが期待できる。特にステロイド薬を、ヒトオートタキシンの低減を目的とした分子標的薬などの拮抗薬を用いた治療の際の補助薬として利用することにより、分子標的薬によるオートタキシン拮抗効果を向上させることが期待できる。ステロイド薬自体は既に安全性が確認されており、分子標的薬などの新規薬物と作用機序が異なることから、組み合わせた服用も容易であることが想到され、治療薬、治療補助薬としての利用は容易と想到される。
【0019】
なお、本発明で使用するステロイドは、疾患の治療に通常用いられるステロイド系抗炎症薬であれば特に制限はなく、アムシノニド、アメロメタゾン、アルクロメタゾン、ウロベタゾール、オキシブチニン、クロチカゾン、クロベタゾール、コルチゾン、シクレゾニド、シクロメタゾン、ジフラゾン、ジフルプレドナート、チキソコルトール、デキサメタゾン、デキシブデソニド、デソキシコルチコステロン、デフラザコルト、デプロドン、トリアムシノロン、トルテロジン、ハイドロコルチゾン、パラメタゾン、ハルシノニド、ハロプレドン、ハロメタゾン、ヒドロキシコルチゾン、ヒドロコルチゾン、ブデソニド、フルオシノニド、フルオシノロン、フルオシノロンアセトニド、フルオロメトロン、フルチカゾン、フルドロコルチゾン、フルニソリド、フルプレドニゾロン、フルメタゾン、フルランドレノリド、プレドニカルベート、プレドニゾロン、プロゲステロン、ベクロメタゾン、ベタメタゾン、メチルプレドニゾロン、メドリゾン、メプレドニゾン、モメタゾン、リメキソロン、ロフレポニド、およびその医薬上許容される塩、溶媒和物などが例示される。好ましいステロイドとしてプレドニゾロン、コルチゾン、ヒドロコルチゾン、メチルプレドニゾロン、デキサメタゾン、ベタメタゾン、ベクロメタゾン、フルチカゾンが挙げられる。
【実施例】
【0020】
以下に本発明をさらに詳細に説明するために実施例を示すが、これら実施例は本発明の一例を示すものであり、本発明は実施例に限定されるものではない。なお、実施例で使用した血清検体の採取および測定は東京大学医学部附属病院で実施し、研究倫理について東京大学大学院医学系研究科倫理委員会での承認のもと実施した。また、オートタキシン濃度の測定は特許文献1の方法に基づき自動免疫測定装置AIAシリーズ(東ソー社製)を用い実施し、リゾホスホリパーゼD活性測定は用手法により実施した。
【0021】
血清中ヒトオートタキシンの濃度測定
ヒトオートタキシンモノクローナル抗体R10.23を固相用抗体として用い、ヒトオートタキシンモノクローナル抗体R10.21を二次抗体として用いた2ステップ2抗体サンドイッチELISAにより、血清中のヒトオートタキシンを測定した。固相用抗体R10.23はペプシン消化によりF(ab)2化し使用した。R10.23を96穴イムノプレート(NUNC社製)に2μg/mL濃度で50μL/ウェルにて添加し、一昼夜、4℃にてプレートに結合させた。TBSにより3回洗浄後、3% BSAを含むTBSを250μL/ウェルで添加し2時間ブロッキング処理を行った。TBSにより3回洗浄後、ヒトオートタキシン標準品(0、0.34、0.675、1.35、2.70、5.40μg/mL)ならびに濃度未知のヒト血清をELISAアッセイ緩衝液で1/5に希釈し50μL/ウェルにて添加した。室温で2時間反応後、TBSTにより4回洗浄し、0.8μg/mLのビオチン標識R10.21を含むELISAアッセイ緩衝液を50μL/ウェル添加した。室温で2時間放置後、TBSTにより4回洗浄し、1000倍希釈したHRP標識ストレプトアビジン(Zymed社製)を含むELISA緩衝液を50μL/ウェル添加した。1時間室温放置後、TBSTにより6回洗浄し、TMB基質を50μL/ウェルで添加した。室温30分後、1N−リン酸により反応を停止し450nmの吸光度を測定した。ヒトオートタキシンの標準品による検量線の回帰を、3次回帰により行った。ヒトオートタキシン濃度依存的に450nmの吸光度上昇が確認された。本検量線を用い未知濃度のヒト血清で得られた450nmの吸光度より検体中のヒトオートタキシンの濃度を算出した。
【0022】
血清中のリゾホスホリパーゼD活性の濃度測定
リゾホスフォリパーゼD活性測定はFEBS letters 571,197−204,2004を若干変更し行った。具体的には、サンプル20μLと2mMのリゾホスファチジルコリン(14:0−リゾホスファチジルコリン)、100mM Tris−HCl、500mM NaCl、5mM MgCl2、0.05% Triton X−100(pH9.0)を含む基質溶液20μLを混合し、37℃にて6時間から一昼夜反応させた。続いて本酵素反応により生成したコリンを定量するため、0.5mM TOOS(N−エチル−N−(2−ヒドロキシ−3−スルフォプロピル)−3−メチルアニリン)、10Unit/mL 西洋ワサビペルオキシダーゼ、0.01% Triton X−100、100mM Tris−HCl(pH8.0)からなるR1溶液150μLを加え5分間放置した後、1mM 4−アミノアンチピリン、10Unit/mL コリンオキシダーゼ、0.01% Triton X−100、100mM Tris−HCl(pH8.0)からなるR2溶液50μLを加えた。30分後、生成したコリンを550nmの吸光度で測定し、既知濃度の塩化コリンを基準にしてリゾホスホリパーゼD活性値とした。
【0023】
実施例1:好酸球性筋膜炎患者および皮膚筋炎患者におけるオートタキシン濃度モニター
女性好酸球性筋膜炎患者および男性皮膚筋炎患者に対しステロイドの一つであるプレドニゾロンを服用した際の、経過時間に伴う血清中のオートタキシン濃度を測定した。好酸球性筋膜炎患者ではプレドニゾロン未服用時のオートタキシン濃度は1.187mg/Lであったが、プレドニゾロン服用によりオートタキシン濃度は低値化し、プレドニゾロン服用量が13.5mg/日まではその低値が維持されていることが示された(図1A)。皮膚筋炎患者では8mg/日の低用量服用から75mg/日の高用量服用によりオートタキシン濃度が低値化することが示され、20mg/日のプレドニゾロンを継続服用する過程でオートタキシン濃度は低値を維持することが示された(図1B)。また、好酸球性筋膜炎患者および皮膚筋炎患者それぞれにおいて、プレドニゾロン服用量を減らすとオートタキシン濃度の上昇が認められた(図1AおよびB)。
【0024】
実施例2:全身性強皮症患者におけるオートタキシン濃度モニター
2例の全身性強皮症患者に対しプレドニゾロンを服用した際の、経過時間に伴う血清中のオートタキシン濃度を測定した。いずれの患者においてもプレドニゾロン服用前のオートタキシン濃度と比較し、プレドニゾロン服用後のオートタキシン濃度は低値化した(図2AおよびB)。また、プレドニゾロン服用量を減らすとオートタキシン濃度の上昇が認められた(図2B)。
【0025】
実施例3:全身性強皮症患者におけるオートタキシン濃度とリゾホスホリパーゼD活性のモニター
全身性強皮症患者に対しプレドニゾロンを服用した際の、経過時間に伴う血清中のオートタキシン濃度およびリゾホスホリパーゼD活性を測定した。血清オートタキシン濃度、リゾホスホリパーゼD活性いずれもプレドニゾロン服用量を同等にモニターできることが確認された(図3)。また、プレドニゾロン投与量とオートタキシン濃度またはリゾホスホリパーゼD活性との関係をプロットしたところ、プレドニゾロン服用量に対するオートタキシン濃度(相関係数0.906)(図4A)およびリゾホスホリパーゼD活性は非常に良好な相関性(相関係数0.978)(図4B)を示していた。よって、オートタキシンまたはリゾホスホリパーゼD活性を測定することによりプレドニゾロン服用量をモニターすることが可能であることがわかる。
【技術分野】
【0001】
本発明はヒト検体中のオートタキシン濃度を測定することでステロイドの服用または服用効果をモニターする方法、前記方法を利用した試薬、およびステロイド服用によるヒトオートタキシンの低減方法に関する。
【背景技術】
【0002】
ステロイド薬は、その抗炎症作用、抗アレルギー作用、免疫抑制作用から非常に広い疾患で用いられる薬である。具体的には、
(1)内科・小児科領域においては、
(1−1)甲状腺疾患における慢性副腎皮質機能不全、急性副腎皮質機能不全、副腎性器症候群、亜急性甲状腺炎、甲状腺中毒症、甲状腺疾患に伴う悪性眼球突出症、ACTH(副腎皮質刺激ホルモン)単独欠損症、
(1−2)リウマチ疾患における関節リウマチ、若年性関節リウマチ、リウマチ熱、リウマチ性多発筋痛、膠原病におけるエリテマトーデス、全身性血管炎、多発性筋炎、皮膚筋炎、強皮症、
(1−3)腎疾患におけるネフローゼ及びネフローゼ症候群、
(1−4)心疾患におけるうっ血性心不全、
(1−5)アレルギー性疾患における気管支喘息、喘息性気管支炎、薬剤その他の化学物質によるアレルギー・中毒、血清病、重症感染症における重症感染症、
(1−6)血液疾患における溶血性貧血、白血病、顆粒球減少症、紫斑病、再生不良性貧血、凝固因子の障害による出血性素因、
(1−7)消化器疾患における限局性腸炎、潰瘍性大腸炎、
(1−8)重症消耗性疾患における全身状態の改善、
(1−9)肝疾患における劇症肝炎、胆汁うっ滞型急性肝炎、慢性肝炎、肝硬変、
(1−10)肺疾患におけるサルコイドーシス、びまん性間質性肺炎、
(1−11)結核性疾患における肺結核、結核性髄膜炎、結核性胸膜炎、結核性腹膜炎、結核性心のう炎、
(1−12)神経疾患における脳脊髄炎、末梢神経炎、筋強直症、重症筋無力症、多発性硬化症、小舞踏病、顔面神経麻痺、脊髄蜘網膜炎、
(1−13)悪性腫瘍における悪性リンパ腫及び類似疾患(近縁疾患)、乳癌の再発転移、
(1−14)その他の内科的疾患として特発性低血糖症、原因不明の発熱、
(2)外科領域における副腎摘除、臓器・組織移植、侵襲後肺水腫、副腎皮質機能不全患者に対する外科的侵襲、蛇毒・昆虫毒、
(3)整形外科領域における強直性脊椎炎、
(4)産婦人科領域における卵管整形術後の癒着防止、副腎皮質機能障害による排卵障害、
(5)泌尿器科領域における前立腺癌、陰茎硬結、
(6)皮膚科領域における外用薬が功を奏さないまたは重傷の湿疹・皮膚炎群、痒疹群、乾癬、掌蹠膿疱症、毛孔性紅色粃糠疹、扁平苔癬、成年性浮腫性硬化症、紅斑症、アナフィラクトイド紫斑、ウェーバークリスチャン病、皮膚粘膜眼症候群、レイノー病、円形脱毛症、天疱瘡群、デューリング疱疹状皮膚炎、先天性表皮水疱症、帯状疱疹、紅皮症、顔面播種状粟粒性狼瘡、アレルギー性血管炎、潰瘍性慢性膿皮症、新生児スクレレーマ、好酸球性筋膜炎、
(7)眼科領域における内眼・視神経・眼窩・眼筋の炎症性疾患、外眼部及び前眼部の炎症性疾患、術後炎症、
(8)耳鼻咽喉科領域における急性・慢性中耳炎、滲出性中耳炎・耳管狭窄症、メニエル病及びメニエル症候群、急性感音性難聴、血管運動性鼻炎、アレルギー性鼻炎、花粉症、副鼻腔炎・鼻茸、進行性壊疽性鼻炎、喉頭炎・喉頭浮腫、食道の炎症及び食道拡張術後、耳鼻咽喉科領域の手術後の後療法、難治性口内炎及び舌炎、嗅覚障害、急性・慢性唾液腺炎、
などの治療に用いられる。
【0003】
このように非常に多岐に渡り利用されているステロイド薬であるが、副作用、特に長期服用または大量服用による副作用が問題となっている。副作用としては血圧上昇、浮腫、耐糖能障害、脂質代謝異常、骨粗鬆症、骨頭無菌性壊死、消化性潰瘍、筋力低下、ムーンフェイス、精神症状、不眠、ざ瘡、皮膚線条、白内障、緑内障、白血球増多、低カリウム血症、副腎皮質機能不全などが知られている。
【0004】
したがって、ステロイド薬を投与するに際しては、治療効果が確認され次第、速やかに投与を停止または投与量を低減させるのが好ましい。しかし、ステロイド薬の生体内濃度測定は容易ではなく、血液検体からの抽出、大型装置での分析などが必要なため汎用できるものではない。また、ステロイド薬は前述したように非常に多くの疾患で利用されており、ステロイド薬を処方された患者によっては服用コンプライアンスが遵守されない場合も少なくないが、それを確認するのは困難である。ステロイド薬の処方は、服用による外見的治療効果の確認や副作用の発生などにより調整される場合がほとんどであり、生体内濃度など定量的制御がされていないため、過剰服用による副作用が懸念されている。そのため、生体内におけるステロイド薬の濃度を簡便にモニターでき、かつ必要以上のステロイド薬の服用が避けられるステロイド薬モニター方法が切望されている。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】WO2008/016186号
【非特許文献】
【0006】
【非特許文献1】J.Biol.Chem.、256、2524−2529、1992
【非特許文献2】Nat.Rev.Cancer、3、582−591、2003
【非特許文献3】Int.J.Cancer、10、109、833−838、2004
【非特許文献4】Blood、106、2138−2146、2005
【非特許文献5】Clin.Chim.Acta、388、51−58、2008
【発明の概要】
【発明が解決しようとする課題】
【0007】
ステロイドを服用する治療は非常に多岐にわたる疾患で実施されているが、副作用が大きいことから過剰服用は回避するのが好ましい。ステロイドを服用する治療では、疾病の治癒の確認により服用量の低減または停止をコントロールしたり、副作用の発症確認のもと服用量をコントロールするのが現状である。また、ステロイド薬は汎用されていることから服用コンプライアンスの遵守が行われないケースも多く、服用量を定量的にモニター可能な方法が切望されている。しかしながら、従来のステロイド薬のモニター方法は高度な分析技術、装置が必要であるため簡便には実施できなかった。
【0008】
そこで、本願発明の課題は簡便にステロイド薬のモニターが可能な方法およびそれを利用した試薬を提供することにある。
【課題を解決するための手段】
【0009】
前記課題を鑑み発明者が鋭意検討した結果、皮膚疾患治療においてステロイド服用を実施することにより血清中のオートタキシン濃度が低下することを見出し、かつ前記現象は皮膚疾患の種類によらずステロイド服用による一般的な現象であることを見出すことで、本発明を完成するに至った。
【0010】
詳しくは、本願は下記の発明を包含する:
(1)ヒト検体中のオートタキシン濃度を測定することによるステロイド服用効果の検査方法。
(2)ステロイド服用前のヒト検体中のオートタキシン濃度を指標とする(1)に記載の検査方法。
(3)ステロイドがプレドニゾロン、コルチゾン、ヒドロコルチゾン、メチルプレドニゾロン、デキサメタゾン、ベタメタゾンのいずれかである(1)または(2)に記載の検査方法。
(4)免疫化学的手法でヒト検体中のオートタキシン濃度を測定する(1)から(3)のいずれかに記載の検査方法。
(5)ヒト検体中のオートタキシン濃度を測定する方法がリゾホスホリパーゼD活性を測定する方法である(1)から(3)のいずれかに記載の検査方法。
(6)(1)から(5)のいずれかに記載の検査方法を利用したステロイド服用効果の検査試薬。
(7)ステロイドを服用することによるヒトオートタキシンの低減方法。
(8)ステロイドおよびオートタキシン拮抗剤を併用服用することによるヒトオートタキシンの低減方法。
(9)ステロイドがプレドニゾロン、コルチゾン、ヒドロコルチゾン、メチルプレドニゾロン、デキサメタゾン、ベタメタゾンのいずれかである(7)または(8)に記載の低減方法。
(10)悪性腫瘍の増殖または転移の阻害を目的とする(7)から(9)のいずれかに記載の低減方法。
(11) ヒトオートタキシンの低減を必要とする疾患を患うヒトのための、ステロイドを投与することによるヒトオートタキシンの低減方法。
(12) ヒトオートタキシンの低減を必要とする疾患が、悪性腫瘍、妊娠高血圧症候群及び慢性肝疾患から選ばれる疾患である、(11)の低減方法。
(13) ステロイドを含むヒトオートタキシン低減用の医薬組成物。
(14) さらに、オートタキシン拮抗剤を含む(13)に記載の医薬組成物。
(15) ヒト検体中のオートタキシン濃度を測定し、基準と比較することによるステロイド服用効果の検査方法。
(16) ステロイドの用量とオートタキシン濃度についての検量線に基づき、ステロイド服用前に測定したヒト検体中のオートタキシン濃度から算出したオートタキシン濃度予測値を基準とする、(15)に記載のステロイド服用効果の検査方法。
【発明の効果】
【0011】
本発明によれば、ヒト検体中のオートタキシン濃度を測定することによりステロイド服用モニターが定量的に可能となる。オートタキシンの測定はオートタキシンが有する酵素活性であるリゾホスホリパーゼD活性を測定することでも可能であるが、特許文献1に記載の免疫学的定量試薬を用いて測定すると検体中に含まれる内在性の測定妨害因子や競合酵素の影響を受けることなく、かつ短時間でヒトオートタキシンを定量可能である。さらに、ステロイド服用によりヒトオートタキシンが低減するため、ヒトオートタキシン低減を目的とした治療、例えば癌の増殖や転移に対してステロイドを服用することにより、ヒトオートタキシンを効率よく低減させることが期待できる。
【図面の簡単な説明】
【0012】
【図1】好酸球性筋膜炎患者(A)および皮膚筋炎患者(B)におけるプレドニゾロン服用時の血清オートタキシン濃度の変動を示す。図中数値は前日のプレドニゾロン服用量(mg/日)を示す。
【図2】2例の全身性強皮症患者(A)(B)におけるプレドニゾロン服用時の血清オートタキシン濃度の変動を示す。図中数値は前日のプレドニゾロン服用量(mg/日)を示す。
【図3】全身性強皮症におけるプレドニゾロン服用時のオートタキシン濃度およびリゾホスホリパーゼD活性の変動を示す。図中黒丸はオートタキシン濃度を、白四角はリゾホスホリパーゼD活性を、それぞれ示す。図中数値は前日のプレドニゾロン服用量(mg/日)を示す。
【図4】プレドニゾロン服用量とオートタキシン濃度(A)またはリゾホスホリパーゼD活性(B)との相関性を示す。
【発明を実施するための形態】
【0013】
以下、本発明を詳細に説明する。
ヒトオートタキシンは、1992年にM.L.StrackeらによってA2058ヒト黒色腫細胞培養培地から細胞運動性を惹起する物質として単離された分子量約125KDaの糖蛋白質である(非特許文献1)。オートタキシンはそのリゾホスホリパーゼD活性によりリゾホスファチジルコリンを基質としリゾホスファチジン酸(LPA)を産生する。生体内ではLPAが癌の増殖や転移に関与していることが多くの研究者により示され(非特許文献2から4)、その産生酵素であるオートタキシンと様々な疾病との因果関係が研究されている。最近になり、ヒトオートタキシンを定量する手法が確立され(特許文献1、非特許文献5)、様々な疾患の診断マーカーとして期待されている。
【0014】
そこで、発明者がステロイド服用とオートタキシン濃度との関係を鋭意検討した結果、
ステロイド服用によりヒト血液中のオートタキシン濃度が低値化することを見出し、さらにステロイド服用量に比例してヒト血液中のオートタキシン濃度が低値化することを見出した。ヒト検体中のオートタキシン濃度は、例えば特許文献1に記載の免疫化学的手法を用いた方法により検体の前処理を必要とすることなく精度よく定量できる。そのため、例えば特許文献1に記載の方法を利用した試薬でヒト検体中のオートタキシン濃度を測定することにより、これまで困難であったステロイド服用効果の定量的モニターが容易となり、ステロイド薬の過剰投与を定量的にコントロールすることが可能となる。また本発明の方法により、服用コンプライアンスが遵守されているか確認可能となる。
【0015】
ステロイドを服用した場合、ステロイド服用量やステロイドの種類に応じて、オートタキシン濃度が用量依存的に減少する(図4A)。したがって、ステロイドを服用後の患者のオートタキシン濃度は、図4Aのようにステロイド服用量とオートタキシン濃度(又は低減割合)をプロットして直線回帰することにより得た検量線を用いて、予測することができる。検量線は、ステロイド毎に定める必要がある。
【0016】
医師は、ステロイドの用量とオートタキシン濃度(又は低減割合)についての検量線に基づき、処方したステロイド用量から患者のオートタキシン濃度を予測することができ、この予測値に対して患者におけるオートタキシン濃度の実測値が有意に高いか又は低い場合、服薬コンプライアンスが遵守されていないと判断することができる。例えば、医師が1日30mgのプレドニゾロンを処方している場合、図4Aの検量線に従うと、服用前のオートタキシン濃度に対して約30%程度低下することが予測され、この予測濃度より有意に高い又は低い場合は服薬コンプライアンスが遵守されていないこととなる。具体的に、検量線から得られた予測値に対して、少なくとも10%以上、好ましくは20%、30%、40%、50%、70%、80%、又は90%の乖離がある場合、服薬コンプライアンスが遵守されていないと判断することができる。
【0017】
ステロイドの服用効果をモニターする場合、服用前のオートタキシン濃度からの低下割合を、治療段階に応じて決められた一定の範囲に保つことが望まれる。ステロイドは一般に副作用が強く、かつ退薬症状が出ることが知られているため、副作用を抑えつつ治療を行い、かつ退薬症状を抑えるため、治療の初期段階では比較的高いオートタキシン濃度の低下割合、例えば40〜70%、好ましくは50〜60%の低下割合を維持し、治療の進行と供に、徐々にオートタキシン濃度の低下割合を低減するように、ステロイド量をコントロールすることが望ましい。例えば、治療中期では20〜50%、好ましくは30〜40%の低下割合、治療後期では10〜30%、好ましくは10〜20%の低下割合を維持するようにステロイド量をコントロールすることが望ましい。
【0018】
今回見出したステロイド服用によるヒト検体中のオートタキシン濃度の低値化現象から、ステロイド服用がヒトオートタキシンを低減する手法となり得ることが期待される。そのため、患者へステロイドを服用する手法が、ヒトオートタキシンが関与する疾患、特にヒトオートタキシンが有するリゾホスホリパーゼD活性により産生されるLPAが関与する癌の増殖や転移を制御する手法となり得ることが期待できる。特にステロイド薬を、ヒトオートタキシンの低減を目的とした分子標的薬などの拮抗薬を用いた治療の際の補助薬として利用することにより、分子標的薬によるオートタキシン拮抗効果を向上させることが期待できる。ステロイド薬自体は既に安全性が確認されており、分子標的薬などの新規薬物と作用機序が異なることから、組み合わせた服用も容易であることが想到され、治療薬、治療補助薬としての利用は容易と想到される。
【0019】
なお、本発明で使用するステロイドは、疾患の治療に通常用いられるステロイド系抗炎症薬であれば特に制限はなく、アムシノニド、アメロメタゾン、アルクロメタゾン、ウロベタゾール、オキシブチニン、クロチカゾン、クロベタゾール、コルチゾン、シクレゾニド、シクロメタゾン、ジフラゾン、ジフルプレドナート、チキソコルトール、デキサメタゾン、デキシブデソニド、デソキシコルチコステロン、デフラザコルト、デプロドン、トリアムシノロン、トルテロジン、ハイドロコルチゾン、パラメタゾン、ハルシノニド、ハロプレドン、ハロメタゾン、ヒドロキシコルチゾン、ヒドロコルチゾン、ブデソニド、フルオシノニド、フルオシノロン、フルオシノロンアセトニド、フルオロメトロン、フルチカゾン、フルドロコルチゾン、フルニソリド、フルプレドニゾロン、フルメタゾン、フルランドレノリド、プレドニカルベート、プレドニゾロン、プロゲステロン、ベクロメタゾン、ベタメタゾン、メチルプレドニゾロン、メドリゾン、メプレドニゾン、モメタゾン、リメキソロン、ロフレポニド、およびその医薬上許容される塩、溶媒和物などが例示される。好ましいステロイドとしてプレドニゾロン、コルチゾン、ヒドロコルチゾン、メチルプレドニゾロン、デキサメタゾン、ベタメタゾン、ベクロメタゾン、フルチカゾンが挙げられる。
【実施例】
【0020】
以下に本発明をさらに詳細に説明するために実施例を示すが、これら実施例は本発明の一例を示すものであり、本発明は実施例に限定されるものではない。なお、実施例で使用した血清検体の採取および測定は東京大学医学部附属病院で実施し、研究倫理について東京大学大学院医学系研究科倫理委員会での承認のもと実施した。また、オートタキシン濃度の測定は特許文献1の方法に基づき自動免疫測定装置AIAシリーズ(東ソー社製)を用い実施し、リゾホスホリパーゼD活性測定は用手法により実施した。
【0021】
血清中ヒトオートタキシンの濃度測定
ヒトオートタキシンモノクローナル抗体R10.23を固相用抗体として用い、ヒトオートタキシンモノクローナル抗体R10.21を二次抗体として用いた2ステップ2抗体サンドイッチELISAにより、血清中のヒトオートタキシンを測定した。固相用抗体R10.23はペプシン消化によりF(ab)2化し使用した。R10.23を96穴イムノプレート(NUNC社製)に2μg/mL濃度で50μL/ウェルにて添加し、一昼夜、4℃にてプレートに結合させた。TBSにより3回洗浄後、3% BSAを含むTBSを250μL/ウェルで添加し2時間ブロッキング処理を行った。TBSにより3回洗浄後、ヒトオートタキシン標準品(0、0.34、0.675、1.35、2.70、5.40μg/mL)ならびに濃度未知のヒト血清をELISAアッセイ緩衝液で1/5に希釈し50μL/ウェルにて添加した。室温で2時間反応後、TBSTにより4回洗浄し、0.8μg/mLのビオチン標識R10.21を含むELISAアッセイ緩衝液を50μL/ウェル添加した。室温で2時間放置後、TBSTにより4回洗浄し、1000倍希釈したHRP標識ストレプトアビジン(Zymed社製)を含むELISA緩衝液を50μL/ウェル添加した。1時間室温放置後、TBSTにより6回洗浄し、TMB基質を50μL/ウェルで添加した。室温30分後、1N−リン酸により反応を停止し450nmの吸光度を測定した。ヒトオートタキシンの標準品による検量線の回帰を、3次回帰により行った。ヒトオートタキシン濃度依存的に450nmの吸光度上昇が確認された。本検量線を用い未知濃度のヒト血清で得られた450nmの吸光度より検体中のヒトオートタキシンの濃度を算出した。
【0022】
血清中のリゾホスホリパーゼD活性の濃度測定
リゾホスフォリパーゼD活性測定はFEBS letters 571,197−204,2004を若干変更し行った。具体的には、サンプル20μLと2mMのリゾホスファチジルコリン(14:0−リゾホスファチジルコリン)、100mM Tris−HCl、500mM NaCl、5mM MgCl2、0.05% Triton X−100(pH9.0)を含む基質溶液20μLを混合し、37℃にて6時間から一昼夜反応させた。続いて本酵素反応により生成したコリンを定量するため、0.5mM TOOS(N−エチル−N−(2−ヒドロキシ−3−スルフォプロピル)−3−メチルアニリン)、10Unit/mL 西洋ワサビペルオキシダーゼ、0.01% Triton X−100、100mM Tris−HCl(pH8.0)からなるR1溶液150μLを加え5分間放置した後、1mM 4−アミノアンチピリン、10Unit/mL コリンオキシダーゼ、0.01% Triton X−100、100mM Tris−HCl(pH8.0)からなるR2溶液50μLを加えた。30分後、生成したコリンを550nmの吸光度で測定し、既知濃度の塩化コリンを基準にしてリゾホスホリパーゼD活性値とした。
【0023】
実施例1:好酸球性筋膜炎患者および皮膚筋炎患者におけるオートタキシン濃度モニター
女性好酸球性筋膜炎患者および男性皮膚筋炎患者に対しステロイドの一つであるプレドニゾロンを服用した際の、経過時間に伴う血清中のオートタキシン濃度を測定した。好酸球性筋膜炎患者ではプレドニゾロン未服用時のオートタキシン濃度は1.187mg/Lであったが、プレドニゾロン服用によりオートタキシン濃度は低値化し、プレドニゾロン服用量が13.5mg/日まではその低値が維持されていることが示された(図1A)。皮膚筋炎患者では8mg/日の低用量服用から75mg/日の高用量服用によりオートタキシン濃度が低値化することが示され、20mg/日のプレドニゾロンを継続服用する過程でオートタキシン濃度は低値を維持することが示された(図1B)。また、好酸球性筋膜炎患者および皮膚筋炎患者それぞれにおいて、プレドニゾロン服用量を減らすとオートタキシン濃度の上昇が認められた(図1AおよびB)。
【0024】
実施例2:全身性強皮症患者におけるオートタキシン濃度モニター
2例の全身性強皮症患者に対しプレドニゾロンを服用した際の、経過時間に伴う血清中のオートタキシン濃度を測定した。いずれの患者においてもプレドニゾロン服用前のオートタキシン濃度と比較し、プレドニゾロン服用後のオートタキシン濃度は低値化した(図2AおよびB)。また、プレドニゾロン服用量を減らすとオートタキシン濃度の上昇が認められた(図2B)。
【0025】
実施例3:全身性強皮症患者におけるオートタキシン濃度とリゾホスホリパーゼD活性のモニター
全身性強皮症患者に対しプレドニゾロンを服用した際の、経過時間に伴う血清中のオートタキシン濃度およびリゾホスホリパーゼD活性を測定した。血清オートタキシン濃度、リゾホスホリパーゼD活性いずれもプレドニゾロン服用量を同等にモニターできることが確認された(図3)。また、プレドニゾロン投与量とオートタキシン濃度またはリゾホスホリパーゼD活性との関係をプロットしたところ、プレドニゾロン服用量に対するオートタキシン濃度(相関係数0.906)(図4A)およびリゾホスホリパーゼD活性は非常に良好な相関性(相関係数0.978)(図4B)を示していた。よって、オートタキシンまたはリゾホスホリパーゼD活性を測定することによりプレドニゾロン服用量をモニターすることが可能であることがわかる。
【特許請求の範囲】
【請求項1】
ヒト検体中のオートタキシン濃度を測定することによるステロイド服用効果の検査方法。
【請求項2】
ステロイド服用前のヒト検体中のオートタキシン濃度を指標とする請求項1記載の検査方法。
【請求項3】
ステロイドがプレドニゾロン、コルチゾン、ヒドロコルチゾン、メチルプレドニゾロン、デキサメタゾン、ベタメタゾンのいずれかである請求項1または2記載の検査方法。
【請求項4】
免疫化学的手法でヒト検体中のオートタキシン濃度を測定する請求項1から3のいずれかに記載の検査方法。
【請求項5】
ヒト検体中のオートタキシン濃度を測定する方法がリゾホスホリパーゼD活性を測定する方法である請求項1から3のいずれかに記載の検査方法。
【請求項6】
請求項1から5のいずれかに記載の検査方法を利用したステロイド服用効果の検査試薬。
【請求項7】
ステロイドを服用することによるヒトオートタキシンの低減方法。
【請求項8】
ステロイドおよびオートタキシン拮抗剤を併用服用することによるヒトオートタキシンの低減方法。
【請求項9】
ステロイドがプレドニゾロン、コルチゾン、ヒドロコルチゾン、メチルプレドニゾロン、デキサメタゾン、ベタメタゾンのいずれかである請求項7または8に記載の低減方法。
【請求項10】
悪性腫瘍の増殖または転移の阻害を目的とする請求項7から9のいずれかに記載の低減方法。
【請求項1】
ヒト検体中のオートタキシン濃度を測定することによるステロイド服用効果の検査方法。
【請求項2】
ステロイド服用前のヒト検体中のオートタキシン濃度を指標とする請求項1記載の検査方法。
【請求項3】
ステロイドがプレドニゾロン、コルチゾン、ヒドロコルチゾン、メチルプレドニゾロン、デキサメタゾン、ベタメタゾンのいずれかである請求項1または2記載の検査方法。
【請求項4】
免疫化学的手法でヒト検体中のオートタキシン濃度を測定する請求項1から3のいずれかに記載の検査方法。
【請求項5】
ヒト検体中のオートタキシン濃度を測定する方法がリゾホスホリパーゼD活性を測定する方法である請求項1から3のいずれかに記載の検査方法。
【請求項6】
請求項1から5のいずれかに記載の検査方法を利用したステロイド服用効果の検査試薬。
【請求項7】
ステロイドを服用することによるヒトオートタキシンの低減方法。
【請求項8】
ステロイドおよびオートタキシン拮抗剤を併用服用することによるヒトオートタキシンの低減方法。
【請求項9】
ステロイドがプレドニゾロン、コルチゾン、ヒドロコルチゾン、メチルプレドニゾロン、デキサメタゾン、ベタメタゾンのいずれかである請求項7または8に記載の低減方法。
【請求項10】
悪性腫瘍の増殖または転移の阻害を目的とする請求項7から9のいずれかに記載の低減方法。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2012−2588(P2012−2588A)
【公開日】平成24年1月5日(2012.1.5)
【国際特許分類】
【出願番号】特願2010−136250(P2010−136250)
【出願日】平成22年6月15日(2010.6.15)
【出願人】(504137912)国立大学法人 東京大学 (1,942)
【出願人】(000003300)東ソー株式会社 (1,901)
【Fターム(参考)】
【公開日】平成24年1月5日(2012.1.5)
【国際特許分類】
【出願日】平成22年6月15日(2010.6.15)
【出願人】(504137912)国立大学法人 東京大学 (1,942)
【出願人】(000003300)東ソー株式会社 (1,901)
【Fターム(参考)】
[ Back to top ]

