キシロオリゴ糖および酸性キシロオリゴ糖の製造方法
【課題】着色が低減された高純度のキシロオリゴ糖および酸性キシロオリゴ糖の安価な製造方法を提供する。
【解決手段】
リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する方法において、リグノセルロース材料をヘミセルラーゼで処理した後のろ液を逆浸透膜で濃縮し、濃縮液を限外ろ過膜で処理後、限外濾過膜で処理したろ液を酸処理する。また、限外濾過膜で処理したろ液をループにより連続的に逆浸透膜に戻す。
【解決手段】
リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する方法において、リグノセルロース材料をヘミセルラーゼで処理した後のろ液を逆浸透膜で濃縮し、濃縮液を限外ろ過膜で処理後、限外濾過膜で処理したろ液を酸処理する。また、限外濾過膜で処理したろ液をループにより連続的に逆浸透膜に戻す。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する工程で、オリゴ糖に含まれる着色物質を効率的に除去するキシロオリゴ糖および酸性キシロオリゴ糖を製造する方法に関する。また、糖濃度の高いキシロオリゴ糖および酸性キシロオリゴ糖を含む糖液を製造する方法に関する。
【背景技術】
【0002】
オリゴ糖類は腸内有用細菌の選択的な増殖促進効果によりおなかの調子を良好に保つ機能を有し、特定保健用食品として認定された乳酸菌飲料や菓子類にも利用されている有用な糖類である。食品としての用途だけではなく、畜産飼料に配合されたり、化粧品に乳化剤、保湿成分として配合されて用いられている。
多くのオリゴ糖類の中で、例えば、小麦フスマやコーンコブに由来するキシロオリゴ糖は、他のオリゴ糖と比較し少量で整腸作用を発揮することが知られている。キシロオリゴ糖は、他のオリゴ糖と同様に腸内善玉菌であるビフィズス菌の増殖を選択的に促進し、腸内悪玉菌である大腸菌の増殖を相対的に抑制する作用があることが知られている。大腸菌や腸内腐敗発酵菌は、腸内で増殖しながら発ガン性物質を生産することが報告されており、腸内に存在する大腸菌や腸内腐敗発酵菌の数を減らすことは健康を維持する上で重要である(非特許文献1参照)。
【0003】
オリゴ糖類を経口摂取した場合、胃酸や消化酵素の酸加水分解によりオリゴ糖の重合度が低下し、最終的には大腸菌やクロストリジウム属等の腐敗性嫌気性菌に資化されることが知られている。しかし、2量体や3量体を主成分とするキシロオリゴ糖組成物は、オリゴ糖の中でも胃酸に対する抵抗性が他のオリゴ糖に比べて比較的高く(特許文献1参照)、経口摂取したオリゴ糖のほとんどが分解されずに腸内に到達する可能性が高い。
現在、平均重合度が5量体程度のキシロオリゴ糖(特許文献2参照)や、平均重合度が12量体前後の長鎖キシロオリゴ糖が製造可能であることが報告されている(特許文献3参照)。鎖長が長いキシロオリゴ糖は腸内でもキシロース(単糖)まで分解されにくく、鎖長の短いキシロオリゴ糖と比較し強い整腸作用が期待される為、重合度の大きなキシロオリゴ糖の開発が望まれている。
【0004】
一方、酸性キシロオリゴ糖はキシロオリゴ糖1分子中に少なくとも1つ以上のウロン酸残基を側鎖として有するキシロオリゴ糖である(特許文献4参照)。酸性キシロオリゴ糖には、抗炎症作用(特許文献5参照)、メラニン生成抑制作用(特許文献6参照)、アトピー性皮膚炎改善作用(特許文献7及び8参照)等の機能が認められており、機能性食品だけではなく化粧品等へも利用可能な素材として期待されている。
【0005】
キシロオリゴ糖及び酸性キシロオリゴ糖を製造する場合、原料、酵素由来の着色物質、酸処理工程で加熱により生成される着色物質を製造工程において除去することが大きな課題である。酸性キシロオリゴ糖はキシロオリゴ糖の側鎖にウロン酸が付加しており、負電荷を有している。現在、酸性キシロオリゴ糖とキシロオリゴ糖(ウロン酸の付加していないキシロオリゴ糖)を含む糖液をイオン交換樹脂に通液し、酸性キシロオリゴ糖のみを樹脂に吸着させてキシロオリゴ糖と分離させた後、樹脂に吸着している酸性キシロオリゴ糖を塩で溶出させて製造している。特に酸性キシロオリゴ糖については塩による溶出の際に樹脂に吸着している着色物資も酸性キシロオリゴ糖に混合されて溶出されるため、イオン交換樹脂のみでは効率的に着色物質を除去することが困難であった。従って、イオン交換以外に、活性炭処理等の方法を用いて着色物質を除去する必要があった。しかし、活性炭処理では、製造コストの増加、オリゴ糖の収率の低減、処理時間の増大等の問題があった。また、着色物質は、キシロオリゴ糖及び酸性キシロオリゴ糖の生理活性を低減させ、さらに、オリゴ糖の味、溶解性、保存性等の物理的特性にに影響を及ぼす可能性がある。従って、より着色物質や不純物の含量の少ないキシロオリゴ糖及び酸性キシロオリゴ糖を製造する技術の開発が望まれている。
【0006】
また、キシロオリゴ糖及び酸性キシロオリゴ糖を製造する場合、製造工程を効率化し、コストの低減を図ることも重要な課題である。製造工程において、精製前のオリゴ糖溶液の糖濃度を現状より高めることができれば、精製に供するオリゴ糖溶液の処理量が低減できる。これにより、精製工程での負荷が低減でき、製造コストの低下、製造に要する時間の短縮が可能となる。従って、より精製前のオリゴ糖溶液の糖濃度を高める方法の開発が望まれている。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特許第2549638号
【特許文献2】特許第1078778号
【特許文献3】特開2003−48901
【特許文献4】特許第4073661号
【特許文献5】特開2003−221339
【特許文献6】特許第3772749号
【特許文献7】特開2004−210664
【特許文献8】特許第4232461号
【0008】
【非特許文献1】金沢ら:大腸細菌叢-とくに胆汁酸代謝と大腸発癌について-.総合臨床、26、 1042〜1050 (1977)
【発明の開示】
【発明が解決しようとする課題】
【0009】
本発明は、リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する工程で、オリゴ糖を含む糖液に含まれる着色を効率的に低減し、また、糖濃度の高い糖液を製造することを課題とする。
【課題を解決するための手段】
【0010】
本発明者らは、リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する方法において、リグノセルロース材料をヘミセルラーゼで処理した後のろ液を逆浸透膜で濃縮し、濃縮液を限外ろ過膜で処理後、限外濾過膜で処理したろ液を酸処理することにより糖液の着色を効率的に低減できることを見出した。また、限外濾過膜で処理したろ液をループにより連続的に逆浸透膜に戻すことにより高濃度の糖液の製造ができることを見出した。
【0011】
具体的には、本発明は以下の(1)〜(7)の構成を採用する。
(1)リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する方法において、リグノセルロース材料をヘミセルラーゼで処理した後のろ液を逆浸透膜で濃縮する濃縮工程、得られた濃縮液を限外ろ過膜で処理する脱色工程、限外濾過膜で脱色された糖液を酸で加水分解する酸処理工程、からなる工程を有することを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(2)前記(1)項の限外濾過膜で脱色された糖液をループにより連続的に逆浸透膜に戻すことを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(3)前記(1)項又は(2)項に記載の限外濾過膜の分画分子量が5000〜30000であることを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(4)前記(1)項に記載のリグノセルロース材料が、木材の微細化物であることを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(5)前記(4)項に記載の木材の微細化物が化学的処理により得られたパルプであることを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(6)前記(5)項に記載の化学的処理により得られたパルプが広葉樹由来のクラフトパルプであることを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(7)前記(1)項に記載のヘミセルラーゼが、キシラナーゼであることを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【発明の効果】
【0012】
本発明により、キシロオリゴ糖及び酸性キシロオリゴ糖を含む糖液の着色を効率的に低減させることができ、その結果として着色が低減されたキシロオリゴ糖及び酸性キシロオリゴ糖が提供される。さらに、本発明により、精製に供する糖液の糖濃度を効率的に高めることができるため、精製工程での負荷(コスト)を低減でき、また、精製工程に要する時間が短縮できるため生産効率の高いキシロオリゴ糖および酸性キシロオリゴ糖の製造方法が提供される。
【図面の簡単な説明】
【0013】
【図1】実施例1、実施例2、実施例3の製造工程フローを示す図
【図2】比較例1、比較例2、比較例3の製造工程フローを示す図
【図3】実施例4の製造工程フローを示す図
【図4】実施例4の糖濃度を示す図
【発明を実施するための最良の形態】
【0014】
以下、本発明の構成について詳述するが、本発明はこれにより限定されるものではない。本発明のキシロオリゴ及び酸性キシロオリゴ糖を得るための原料として木本性植物、あるいは草本性植物由来のリグノセルロースを用いることができる。木本性植物由来のリグノセルロース原料としては広葉樹、針葉樹の木部や樹皮を用いるのが好ましいが、枝、葉等の他の部位も用いることができる。草本性植物由来のリグノセルロース原料としては、ケナフ、麻、バガス、イネ等の茎、葉等の部位を特に限定なく用いることができる。本発明では、木本性植物の木部や樹皮の部位、あるいは草本性植物の茎、枝葉等の部位を微細化処理した微細化物を用いることができる。微細化処理後、パルプの形状にして用いることが好ましい。用いるパルプとしては、化学パルプ、機械パルプ、脱墨パルプ等、特に限定されないが、広葉樹由来の化学パルプが好ましい。化学パルプを得るための蒸解法としては、クラフト蒸解、ポリサルファイド蒸解、ソーダ蒸解、アルカリサルファイト蒸解等の公知の蒸解法が挙げられ、パルプの品質、パルプを得るためのエネルギー効率等を考慮した場合、クラフト蒸解法を用いることが好ましい。また、クラフト蒸解後、酸素漂白したパルプを用いることがより好ましい。クラフト蒸解後、酸素漂白した広葉樹由来のパルプでは、グルコース、アラビノース等の構成糖がほとんど含まれず、キシロースがほぼ100%近く含まれるという特徴があるため、用いる原料としてより好ましい。
【0015】
原料としてパルプを用いる場合、使用するパルプをパルプ製造工程よりキシロオリゴ及び酸性キシロオリゴ糖の糖製造工程へ移送する。移送の手段としては、低濃度のパルプであればポンプによるライン移送、高濃度のパルプであればベルトコンベア等の方法が挙げられ、移送方法は特に限定されない。
【0016】
原料として用いるパルプは、例えば、タンク内で水に懸濁後、ドラムフィルターに移送しドラムフィルターで水で洗浄後、脱水する。この工程でパルプに含まれる微細な懸濁物、リグニンおよび有機酸等の不純物が除かれるため洗浄することが好ましい。パルプの洗浄方法としては、パルプを水で洗浄後、脱水できる装置であれば特に限定されない。また、この洗浄工程で水にpH調整剤や温度調節した洗浄水を添加することにより、洗浄後のパルプのpHや温度を調節し、後段でのヘミセルラーゼの至適反応条件を調節することもできる。
【0017】
原料として用いるパルプは、前記の工程の後、ヘミセルラーゼ処理を行う反応装置へポンプで移送する。原料とヘミセルラーゼを混合する方法は、反応槽へ移送する前に混合しても良いし、反応槽内で混合しても良い。高濃度のパルプをヘミセルラーゼで処理する場合、反応槽の形状としては、円筒型が連続的に移送できるため好ましいが、酵素反応が行えるものであれば特に限定されない。高濃度のパルプをヘミセルラーゼで処理する場合、スクリューミキサー等(例えば、トランポスクリュー等)の混合機を用いて反応槽へ移送される前にパルプとキシラナーゼを均一に混和させておくことが好ましい。用いる混合機としては、パルプとヘミセルラーゼを均一に混合できる装置であれば特に限定なく用いることができる。一方、低濃度のパルプをヘミセルラーゼで処理する場合、反応槽の形状は特に限定されないが、例えば、攪拌機を備えた反応槽内でパルプ懸濁液を攪拌しながらオリゴ糖の溶出に最適な滞留時間でヘミセルラーゼ処理を行い、パルプ懸濁液(オリゴ糖を含む)を連続的に回収する方法が挙げられる。これらの反応槽は、ヘミセルラーゼの至適反応温度を維持する為に温度調節用のジャケットや断熱材ケーシングを具備することが好ましい。
【0018】
本発明で用いるヘミセルラーゼとしては、キシラナーゼ活性を含むものであれば特に限定されない。ヘミセルラーゼとしては、例えば、商品名カルタザイム(クラリアント社製)、パルプザイム(ノボノルディスク社製)、エコパルプ(ローム・エンザイム社製)、スミチーム(新日本化学工業社製)、マルチフェクトキシラナーゼ(ジェネンコア社製)、キシラナーゼコンク(アドバンスド・バイオケミカルス社製)等の市販の酵素製剤や、トリコデルマ(Trichoderma)属、テルモミセス(Thermomyces)属、オウレオバシヂウム(Aureobasidium)属、ストレプトミセス(Streptomyces)属、アスペルギルス(Aspergillus)属、クロストリジウム(Clostridium)属、バチルス(Bacillus)属、テルモトガ(Thermotoga)属、テルモアスクス(Thermoascus)属、カルドセラム(Caldocellum)属、テルモモノスポラ(Thermomonospora)属等の微生物により生産されるキシラナーゼが挙げられる。
【0019】
パルプのヘミセルラーゼ処理工程では、パルプに対するヘミセルラーゼの添加量、反応時間を調節することにより、パルプから溶出されるオリゴ糖の濃度やオリゴ糖の重合度を調節することができる。一般に、ヘミセルラーゼの添加量が多いほど、また反応時間が長いほど反応液中のオリゴ糖濃度は高くなり、且つオリゴ糖の重合度は小さくなる。従って、高重合度のオリゴ糖を含む高濃度の糖液を安定して得るためには、パルプに対して適量のヘミセルラーゼ(低分子まで分解されない程度のヘミセルラーゼ)を添加し、反応後の糖液(パルプを除いたオリゴ糖を含むろ液)の一部を酵素反応槽に戻し再度、酵素反応させることが好ましい。これによりオリゴ糖の重合度を高い状態に維持しながら、時間経過と共に高重合度のオリゴ糖の糖濃度を高めることができる。パルプに対して過剰のヘミセルラーゼを添加したり、反応時間を長くすると、溶出したオリゴ糖が更にヘミセルラーゼで分解され、キシロース、キシロビオースのような鎖長の短いオリゴ糖にまで分解されるため好ましくない。
【0020】
反応槽内でのパルプ濃度、反応時間、キシラナーゼ添加量は任意に設定可能であるが、パルプ濃度は2〜20質量%が好ましく、7〜15質量%がさらに好ましい。パルプ濃度が低すぎるとオリゴ糖の濃度を高めることが困難となり、また、処理液の容量が増大するため、反応設備の大型化が必要となるという問題が生じる。一方、パルプ濃度が高すぎるとヘミセルラーゼとパルプの均一な混合やパルプの移送が困難となり、また、糖液の回収量が減少するため好ましくない。パルプに対する適したヘミセルラーゼ添加量及び反応時間は、用いる酵素の種類によって異なる。例えば、マルチフェクトキシラナーゼの場合、反応時間は10〜240分が好ましく、30〜90分がより好ましい。また、パルプに対するヘミセルラーゼの添加量は2〜200(unit/g−乾燥パルプ)が好ましく、10〜100(unit/g−乾燥パルプ)がより好ましい。
【0021】
本発明により、パルプをヘミセルラーゼ処理した反応液中に溶出されるオリゴ糖の重合度は、用いる酵素の種類や反応条件によって変動するが、例えば、マルチフェクトキシラナーゼを用いる場合、パルプ濃度10質量%、反応時間45分、反応温度50℃、pH6.0、パルプに対する酵素添加量50(unit/g−乾燥パルプ)の条件では、1〜15量体の分布を持つ平均重合度が5量体程度のキシロオリゴ糖、および1〜20量体の分布を持つ平均重合度10量体程度の酸性キシロオリゴが糖液中に溶出される。
【0022】
ヘミセルラーゼで処理したパルプに含まれるオリゴ糖を回収するための手段は特に限定されないが、例えば、スクリュープレス等の装置を使用してパルプを圧搾してろ液(オリゴ糖含有)を回収しても良いし、ドラムフィルター等の装置を使用してパルプを水で置換洗浄し、オリゴ糖を含有するろ液を回収しても良い。このようにして得られたオリゴ糖を含有するろ液は次の濃縮工程へ移送される。また、前述したようにろ液の一部を酵素反応槽に戻し、再度、ヘミセルラーゼで反応させても良い。
【0023】
パルプをヘミセルラーゼで反応させた後のろ液は、次の濃縮工程へ移送する前に前処理により原料由来の残渣を除くことが好ましい。前処理としては、バッグフィルター、フィルタープレス、プレコートフィルター、セラミックフィルター等の精密ろ過処理や凝集沈殿処理が挙げられ、これらの処理を併用しても良い。精密ろ過処理を行う場合は、サブミクロンオーダーの濾過精度を持つフィルターが好ましい。凝集沈殿処理を行う場合は、硫酸バンド、ポリ塩化アルミニウム等の無機系凝集剤や、ポリアクリルアミド系、ポリアミジン系等の高分子凝集剤あるいはキトサン等の天然高分子凝集剤を用いることができる。前処理の方法は、パルプ、懸濁物質等の微細な不溶成分を除去することができる方法であれば、前記の方法に限定されない。
【0024】
本発明では、パルプをヘミセルラーゼで反応させた後のろ液中に含まれるオリゴ糖溶液は、後段での精製負荷を低減するために、濃縮により糖液中の濃度を高濃度にすることが望ましい。糖液を濃縮するために逆浸透膜を用いる。逆浸透膜を用いる方法では、キシロース、キシロビオース等の低分子(重合度の小さい糖)や反応後の糖液に含まれる低分子物質(例えば、炭酸ナトリウム、チオ硫酸ナトリウム等の無機物、有機酸、等)が透過液として除去され、高分子(重合度の大きいキシロオリゴ糖)のみが選択的に濃縮されるという利点がある。また、膜濃縮では運転コストが溶媒抽出による方法と比較し安価であり、また、危険性のある溶媒を使用する必要がないため好ましい。
しかし、逆浸透膜の膜エレメントを連続的に運転する場合、オリゴ糖の製造工程で使用する原水中に存在するコロイド性物質や微細な懸濁物質、特に酵素反応後の糖液に不純物として含まれるリグニン等が膜の表面上に付着し、蓄積されて運転時間の経過と共に膜のろ過比抵抗が増大して透過流束が低下するという問題が生じる。特にリグニン等の高分子は透過液として膜外に排出されないためオリゴ糖と共に濃縮されて、結果として時間経過と共に膜の表面に付着し膜の操作圧力を上昇させる。操作圧力が限界値まで上昇すると、連続運転が困難となり、オリゴ糖の生産効率が低下(運転コスト増加、製造時間延長)するため好ましくない。また、精製に供する糖液の糖濃度は、できるだけ高濃度にした方が後段の製造コストが低減できるというメリットがある。しかし、運転開始後、短時間でリグニン等の不純物が膜に付着すると糖濃度が充分に高濃度になる前に膜の操作圧力が限界値に達し糖液の濃度をそれ以上に高濃度にすることができなくなる。従って、膜エレメントの性能劣化を最小限にし、長時間にわたり安定して逆浸透膜装置を運転することが課題であった。この問題を解決するために検討した結果、後述する限外濾過膜で処理した後のろ液をループにより連続的に逆浸透膜に戻すことにより糖濃縮液の糖濃度を高めることが可能となった。
【0025】
本発明では、逆浸透膜で濃縮した糖液を、次に、限外濾過膜により着色物質や不純物を除去する。逆浸透膜で濃縮中の糖液は、糖液の一部を連続的に限外濾過膜に移送しても良いし、糖濃度が一定の値に達してから限外濾過装置を停止し、濃縮した糖液の全量を限外濾過膜に移送しても良い。
従来は、後述する酸処理の後に限外濾過膜による処理を実施していた。しかし、酸処理前の糖濃縮液には原料や酵素由来の不純物(リグニン、酵素由来のタンパク質等)が混合しており、加熱(酸処理)により、糖液の着色が増大するという問題が生じた。糖液を加熱すると、例えば、アミノ酸や蛋白質の共存下で糖を加熱することによるメイラード反応による糖の褐変化、カラメル物質の増加等、加熱により糖液中に新たな着色物質が増加する。この問題を解決するために検討した結果、後述の酸処理の前に糖濃縮液を限外ろ過膜で処理することにより、糖濃縮液に含まれる不純物をあらかじめ除去することができ、結果として酸処理工程で発生する着色物質の生成を低減することが可能となった。
また、限外濾過膜による処理では、糖濃縮液に元々含まれる原料由来のリグニンや着色物質等の高分子の不純物を除去することもできる。
用いる限外濾過膜の分画分子量は、5000〜30000が好ましい。分画分子量が5000より小さいとオリゴ糖の回収率が低下し、膜への抵抗が増加しオリゴ糖の生産効率が低下するため好ましくない。また、分画分子量が30000より大きいと着色物質や不純物の除去率が低下するため好ましくない。
【0026】
本発明では、前記の限外濾過膜で処理した後のろ液をループにより連続的に逆浸透膜に戻す(図3参照)。逆浸透膜へ戻す限外濾過膜処理後のろ液の液量はろ液の全量でも良いし、一部でもよい。ろ液の全量を戻す場合は、逆浸透膜内の糖濃度が一定の値に達してから限外濾過装置を停止し、次の酸処理工程へ移送する。一方、ろ液の一部を戻す場合は、逆浸透膜へ戻さない残りのろ液を逆浸透膜から連続的に酸処理工程へ移送する。
前述の逆浸透膜で糖液が濃縮される時にオリゴ糖と共に不純物として含まれるリグニン等の高分子物質も濃度が上昇するが、限外濾過膜で処理した後のろ液をループにより連続的に逆浸透膜に戻すことにより、リグニン等の不純物のみを濃縮中の糖液から除去できる。その結果として、逆浸透膜の操作圧力の上昇を抑制することができ、オリゴ糖の濃度をより高めることができる。
【0027】
前記の限外濾過膜で処理した糖液(図1参照)、あるいは、逆浸透膜で濃縮した糖液(図3参照)は、次に酸処理を行う。糖液中に含まれるキシロオリゴ糖及び酸性キシロオリゴ糖の一部はリグニンと結合して複合体(リグニン−キシロオリゴ糖複合体、リグニン−酸性キシロオリゴ糖複合体)として存在する。酸処理により、複合体からキシロオリゴ糖および酸性キシロオリゴ糖を遊離させることができる。酸処理の方法としては、例えば、糖液に酸を添加してpHを5以下に調整し、高温で加熱する方法が挙げられる。pH調整に用いる酸は、特に限定されないが、例えば、硫酸、塩酸等の鉱酸の他、シュウ酸、酢酸等の有機酸が挙げられる。酸処理のpHは2〜5が好ましく、さらにpH3.5〜4.0の範囲がより好ましい。pHが2より低いと糖液に含まれるキシロオリゴ糖及び酸性キシロオリゴ糖からキシロースへの加水分解が促進され、オリゴ糖の回収率が低下するため好ましくない。またpHが5より高いと150℃以下の温度では複合体からオリゴ糖の遊離が抑制されるため好ましくない。酸処理の温度は、特に限定されないが、100〜200℃が好ましく、105〜170℃がより好ましく、110〜125℃がさらに好ましい。100℃より低い温度では、複合体からのオリゴ糖の遊離が抑制されるため好ましくない。また、170℃を越えると、キシロオリゴ糖および酸性キシロオリゴ糖からキシロースへの分解が促進されオリゴ糖の収率が低下するため好ましくない。また、酸処理中の圧力は大気圧〜5kg/cm2の範囲であることが好ましい。
【0028】
酸処理後の糖液には、酸処理で生成した着色物質、前記の限外濾過膜で除去されなかった原料由来のリグニン、着色物質等が含まれており、その一部は不溶性残渣として存在している。これらの不溶性残渣を遠心分離、セラミックフィルター等によるフィルターろ過、ろ布等によるろ過で除去することが好ましい。
【0029】
酸処理後の糖液中に含まれる着色物質等の不純物の含量をさらに低減するために、活性炭処理を行うことが好ましい。用いる活性炭の種類としては、糖液中の着色物質等の不純物の含量を低減する能力を有するものであれば特に限定されない。
【0030】
前記の操作で着色物質等の不純物を低減した糖液に含まれるキシロオリゴ糖と酸性キシロオリゴ糖をイオン交換樹脂を用いて分離・精製する。分離・精製の方法として、例えば、オリゴ糖を含む糖濃縮液を強カチオン樹脂→弱アニオン樹脂→強カチオン樹脂→弱アニオン樹脂の順に通液する方法を用いることができる。この方法では、酸性キシロオリゴ糖がアニオン樹脂に吸着されるため、キシロオリゴ糖のみをろ液として回収することができる。次に、アニオン樹脂に、例えば、塩化ナトリウム等の塩を通液することにより酸性キシロオリゴ糖を樹脂から溶出させて回収することができる。回収したキシロオリゴ糖及び酸性キシロオリゴ糖を含む溶液を、例えば、エバポレーション等の濃縮装置で濃縮することができる。オリゴ糖を含む溶液をスプレードライで乾燥することにより、キシロオリゴ糖及び酸性キシロオリゴ糖の粉末が得られる。
【実施例】
【0031】
以下に、本発明を実施例により詳細に説明するが、本発明は以下の実施例に限定されるものではない。以下に示す%は、特に断らない限りすべて質量%を示し、対パルプの添加率はパルプの絶乾質量に対する質量の比率を示す。なお、各測定法は以下のとおりである。
〈測定法の概要〉
全糖量の定量
全糖量は検量線をD−キシロース(和光純薬工業製)を用いて作製し、フェノール硫酸法(還元糖の定量法;学会出版センター)で定量した。
(2)還元糖量の定量
還元糖量は検量線をD−キシロース(和光純薬工業製)を用いて作製し、ソモジ−ネルソン法(還元糖の定量法;学会出版センター)で定量した。
(3)平均重合度の決定法
サンプル糖液を50℃に保ち15000rpmで15分間遠心分離し不溶物を除去後、上清液の全糖量を還元糖量(共にキシロース換算)を測定した。全糖量を還元糖量で割って平均重合度を求めた。
(4)酵素力価の定義
酵素として用いたキシラナーゼの活性測定にはバーチウッドキシラン(シグマ社製)を基質として用いた。酵素力価の定義はキシラナーゼがキシランを分解することで得られる還元糖の還元力をDNS法(還元糖の定量法;学会出版センター)を用いて測定し、1分間に1マイクロモルのキシロースに相当する還元力を生成させる酵素量を1unitとした。
【0032】
<実施例1>
[オリゴ糖濃縮液の製造]
混合広葉樹チップ(国内産広葉樹チップ20%、ユーカリ材80%)をクラフト蒸解後、酸素脱リグニンしパルプ(原料)を得た。以降の操作は、連続的に行った。タンクにパルプ及び高温水(60℃)を添加し、パルプ濃度(最終濃度)を1.6質量%に調製した(容量10m3)。次に、タンクに濃硫酸を添加、攪拌してpH5.5に調整後、ドラムフィルター(新菱製作所製:φ2000×600 SUF)でパルプを脱水洗浄した。脱水後のパルプ(パルプ濃度20質量%)に温水(50℃)を添加し、パルプ濃度を10質量%に調製後、マルチフェクトキシラナーゼ(ジェネンコア社製)を対パルプ50unit(乾燥パルプ1g当たり)となるように添加して、トランポスクリュー(新菱製作所:220x850 HC-C)で均一に混合した。混合後のパルプを中濃度ポンプ(新菱製作所:200×RPK)で容積2m3の円筒型反応槽(φ800mm×4000mmH)の入口から押し込み、円筒型反応槽内で連続的に酵素反応を行った(反応時間40分間、温度50℃)。円筒型反応槽内の出口から排出されたパルプ(酵素反応後のパルプ)をスクリュープレス(新菱製作所:250×1000 SPH−EN)でパルプ濃度が40質量%になるまで脱水して、キシラナーゼ反応後のろ液を得た。酵素反応開始から60分以降は、キシラナーゼ反応後のろ液の一部をトランポスクリューに戻し、ドラムフィルターで脱水した20質量%濃度のパルプを温水(50℃)の替わりに戻したキシラナーゼ反応後のろ液でパルプ濃度を10質量%に調整した。酵素反応開始から150分後、反応後のろ液中の全糖濃度は0.92%に上昇し、この時点での糖液に含まれるキシロオリゴ糖の平均重合度は4.7であった。以上のパルプのキシラナーゼ処理を24時間連続して実施した。酵素反応開始から150分以降は、糖濃度約0.90%の反応ろ液を安定して回収すことができた。最終的に糖濃度0.90%のキシラナーゼ反応後のろ液を15m3得た。得られた反応ろ液を、ミクロンレート1μmのバックフィルター(ISPフィルターズ製)、次にミクロンレート0.2μmのセラミックフィルター(日本ポール製)でろ過して、清澄なろ液(糖液)を得た。このろ液を逆浸透膜(日東電工製:NTR−7450、膜質:スルホン化ポリエーテルスルホン系、膜面積:6.5m2−2本)で液温50℃、流量1400〜1800L/hの運転条件で15倍に濃縮し、全糖濃度11%の濃縮液を1m3得た。
[オリゴ糖の精製]
図1に示す製造工程で、前記([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを分画分子量10000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いて、透過流速350L/hで処理した。限外濾過膜を通過したろ液(糖を含む画分)を濃硫酸でpH3.5に調整後、121℃で45分間処理(酸処理)した。ろ液を50℃まで冷却後、酸処理後で生成した不溶性残渣をミクロンレート0.2μmのセラミックフィルター(日本ポール製)で除去した。この糖液を一部採取して全糖濃度を0.2%に調製(蒸留水で希釈)し、350nmの波長における吸光度(着色度)を測定した(表1)。次に、ろ液480Lに対して活性炭(三倉化成製:PM−SX)10kgを添加し、50℃で2時間処理後、糖液を回収した。この糖液を、SV1.5で強カチオン樹脂(三菱化学製:PK−218、300L)→弱アニオン樹脂(三菱化学製:WA30、300L)→強カチオン樹脂(三菱化学製:PK−218、300L)→弱アニオン樹脂(三菱化学製:WA30、300L)からなる4床4塔式イオン交換樹脂に通液し、キシロオリゴ糖糖液(糖濃度4.3質量%、550L)を得た。得られたキシロオリゴ糖溶液を強カチオン樹脂でpH7に調整後、スプレードライヤー(大川原化工機製:ODA−25型)で処理して、キシロオリゴ糖粉末23.0kg(平均重合度5.0)を得た。次に、2塔目及び4塔目の弱アニオン樹脂に50mM塩化ナトリウム水溶液をSV1.5で通液し、イオン交換樹脂に吸着している酸性キシロオリゴ糖を溶出させ、酸性キシロオリゴ糖溶液(糖濃度2.8質量%、400L)を得た。得られた酸性キシロオリゴ糖溶液を、強カチオン樹脂でpH5に調整後、糖濃度20質量%までエバポール(大川原化工機:CEP-1)で濃縮した。次に、スプレードライヤー(大川原化工機製:ODA-25型)で処理して、酸性キシロオリゴ糖粉末11.3kg(平均重合度11.0)を得た。得られたキシロオリゴ糖及び酸性キシロオリゴ糖を蒸留水で全糖濃度5質量%に調整し、350nmの波長における吸光度(着色度)を測定した(表2)。
【0033】
<比較例1>
図2に示す製造工程で、実施例1([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを、濃硫酸でpH3.5に調整後、121℃で45分間処理(酸処理)した。糖濃縮液を50℃まで冷却後、酸処理後で生成した不溶性残渣をミクロンレート0.2μmのセラミックフィルター(日本ポール製)で除去した。次に、糖濃縮液を分画分子量10000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いて、透過流速350L/hで処理した。この糖液を一部採取して全糖濃度を0.2質量%に調製(蒸留水で希釈)し、350nmの波長における吸光度(着色度)を測定した(表1)。次に、限外濾過膜を通過したろ液480Lに対して活性炭(三倉化成製:PM−SX)10kgを添加し、50℃で2時間処理し糖液を回収した。この糖液を、SV1.5で強カチオン樹脂(三菱化学製:PK−218、300L)→弱アニオン樹脂(三菱化学製:WA30、300L)→強カチオン樹脂(三菱化学製:PK−218、300L)→弱アニオン樹脂(三菱化学製:WA30、300L)からなる4床4塔式イオン交換樹脂に通液し、キシロオリゴ糖溶液(糖濃度3.9質量%、550L)を得た。得られたキシロオリゴ糖溶液を強カチオン樹脂でpH7に調整後、スプレードライヤー(大川原化工機製:ODA−25型)で処理して、キシロオリゴ糖粉末20.6kg(平均重合度5.1)を得た。次に、2塔目及び4塔目の弱アニオン樹脂に50mM塩化ナトリウム水溶液をSV1.5で通液しイオン交換樹脂に吸着している酸性キシロオリゴ糖を溶出させ、酸性キシロオリゴ糖溶液(糖濃度2.4質量%、400L)を得た。得られた酸性キシロオリゴ糖溶液を、強カチオン樹脂でpH5に調整後、糖濃度20質量%までエバポール(大河原化工機:CEP-1)で濃縮した。次に、スプレードライヤー(大川原化工機製:ODA−25型)で処理して、酸性キシロオリゴ糖粉末9.5kg(平均重合度11.0)を得た。得られたキシロオリゴ糖及び酸性キシロオリゴ糖を蒸留水で全糖濃度5質量%に調整し、350nmの波長における吸光度(着色度)を測定した(表2)。
【0034】
分画分子量10000の限外濾過膜を用いて試験した結果を表1および表2に示す。糖濃縮液を限外濾過した後に酸処理した場合(実施例1)では、糖濃縮液を酸処理後に限外濾過した場合(比較例1)と比較し糖液の着色度(吸光度350nm)が減少した(表1)。また、糖濃縮液を限外濾過した後に酸処理した場合(実施例1)では、糖濃縮液を酸処理後に限外濾過した場合(比較例1)と比較し精製後のキシロオリゴ糖液及び酸性キシロオリゴ糖の着色度(吸光度350nm)が減少した(表2)。以上の結果から、糖濃縮液を限外濾過した後に酸処理を行うことで、酸処理で生成される着色物質の含量を低減できることが判明した。この結果により、後段の精製工程で脱色を目的として使用する活性炭の量を低減でき、コスト低減が可能となる。
【0035】
【表1】

【0036】
【表2】

【0037】
<実施例2>
[オリゴ糖の精製]
図1に示す製造工程で実施例1([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを精製した。分画分子量5000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いた以外は実施例1と同様の方法で実施した。糖液の採取についても実施例1と同様の工程の箇所で実施し、糖液の350nmの波長における吸光度(着色度)を測定した(表3)。尚、イオン交換樹脂処理後のキシロオリゴ糖溶液の糖濃度は3.7質量%(550L)、酸性キシロオリゴ糖溶液の糖濃度は2.3質量%(400L)であった。また、精製後、得られたキシロオリゴ糖粉末は19.1kg(平均重合度4.9)、酸性キシロオリゴ糖粉末は9.5kg(平均重合度10.8)であった。
【0038】
<比較例2>
図2に示す製造工程で実施例1([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを精製した。分画分子量5000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いた以外は比較例1と同様の方法で実施した。糖液の採取についても比較例1と同様の工程の箇所で実施し、糖液の350nmの波長における吸光度(着色度)を測定した(表3)。尚、イオン交換樹脂処理後のキシロオリゴ糖溶液の糖濃度は3.3質量%(550L)、酸性キシロオリゴ糖溶液の糖濃度は2.0質量%(400L)であった。また、精製後、得られたキシロオリゴ糖粉末は16.8kg(平均重合度4.9)、酸性キシロオリゴ糖粉末は8.4kg(平均重合度10.9)であった。
【0039】
分画分子量5000の限外濾過膜を用いて試験した結果を表3および表4に示す。糖濃縮液を限外濾過した後に酸処理した場合(実施例2)では、糖濃縮液を酸処理後に限外濾過した場合(比較例2)と比較し糖液の着色度(吸光度350nm)が減少した(表3)。また、糖濃縮液を限外濾過した後に酸処理した場合(実施例2)では、糖濃縮液を酸処理後に限外濾過した場合(比較例2)と比較し精製後のキシロオリゴ糖液及び酸性キシロオリゴ糖の着色度(吸光度350nm)が減少した(表4)。
【0040】
【表3】

【0041】
【表4】

【0042】
<実施例3>
[オリゴ糖の精製]
図1に示す製造工程で実施例1([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを精製した。分画分子量30000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いた以外は実施例1と同様の方法で実施した。糖液の採取についても実施例1と同様の工程の箇所で実施し、糖液の350nmの波長における吸光度(着色度)を測定した(表5)。尚、イオン交換樹脂処理後のキシロオリゴ糖溶液の糖濃度は4.0質量%(550L)、酸性キシロオリゴ糖溶液の糖濃度は2.7質量%(400L)であった。また、精製後、得られたキシロオリゴ糖粉末は22.0kg(平均重合度5.1)、酸性キシロオリゴ糖粉末は11.0kg(平均重合度11.2)であった。
【0043】
<比較例3>
図2に示す製造工程で実施例1([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを精製した。分画分子量30000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いた以外は比較例1と同様の方法で実施した。糖液の採取についても比較例1と同様の工程の箇所で実施し、糖液の350nmの波長における吸光度(着色度)を測定した(表5)。尚、イオン交換樹脂処理後のキシロオリゴ糖溶液の糖濃度は3.9質量%(550L)、酸性キシロオリゴ糖溶液の糖濃度は2.5質量%(400L)であった。また、精製後、得られたキシロオリゴ糖粉末は21.2kg(平均重合度5.1)、酸性キシロオリゴ糖粉末は10.7kg(平均重合度11.1)であった。
【0044】
分画分子量30000の限外濾過膜を用いて試験した結果を表5および表6に示す。糖濃縮液を限外濾過した後に酸処理した場合(実施例3)では、糖濃縮液を酸処理後に限外濾過した場合(比較例3)と比較し糖液の着色度(吸光度350nm)が減少した(表5)。また、糖濃縮液を限外濾過した後に酸処理した場合(実施例3)では、糖濃縮液を酸処理後に限外濾過した場合(比較例3)と比較し精製後のキシロオリゴ糖液及び酸性キシロオリゴ糖の着色度(吸光度350nm)が減少した(表6)。
【0045】
【表5】

【0046】
【表6】

【0047】
<実施例4>
[逆浸透膜と限外濾過膜の間へのループ導入による連続循環の検討]
実施例1([オリゴ糖濃縮液の製造])と同様の方法で、パルプを原料として糖濃縮液を製造した。糖濃縮液製造の逆浸透膜(日東電工製:NTR−7450)で濃縮された糖液を連続的に限外濾過装置(オスモニクス製UF膜モジュール、分画分子量10000)を用いて、透過流速350L/hで限外ろ過膜による処理を行った。図3に示すように限外濾過膜を通過したろ液(糖を含む画分)を前記の逆浸透膜(日東電工製:NTR−7450)へ戻し、逆浸透膜→限外濾過膜の工程を連続的に循環させ、糖濃度が一定以上に濃縮されるまで限外濾過を継続した。ループによる連続循環開始後、逆浸透膜入口の操作圧力を経時的に測定した。また、逆浸透膜内の糖液を採取し、糖液の全糖濃度を測定した。
【0048】
<比較例4>
実施例4記載の方法で、ループによる連続循環を行わない方法を比較例4とした(製造工程フローは図1と同様)。実施例4と同様に、逆浸透膜入口の操作圧力を測定した。また、逆浸透膜内の糖液を採取し、糖液の全糖濃度を測定した(逆浸透膜の運転開始後、同一の時間経過におけるデータを実施例4と比較した)。
【0049】
逆浸透膜入口の操作圧力と逆浸透膜内の糖濃度の関係を図4に示す。逆浸透膜と限外濾過膜の間にループをつくり、糖液を連続循環させた場合(実施例4)では、連続循環させない場合(比較例4)と比較し、同じ操作圧力(逆浸透膜)において高濃度の糖液を得ることができた。操作圧力1.9MPaの場合、実施例4では糖濃度15.2質量%、比較例4では、糖濃度11.0質量%であった。また、実施例で4は、比較例4と比較し酸処理以降の精製工程に要する時間を約4時間短縮することができた。
【産業上の利用可能性】
【0050】
本発明により、着色が低減された高純度のキシロオリゴ糖および酸性キシロオリゴ糖が効率良く製造できるため、キシロオリゴ糖及び酸性キシロオリゴ糖を安価に製造することができる。
【技術分野】
【0001】
本発明は、リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する工程で、オリゴ糖に含まれる着色物質を効率的に除去するキシロオリゴ糖および酸性キシロオリゴ糖を製造する方法に関する。また、糖濃度の高いキシロオリゴ糖および酸性キシロオリゴ糖を含む糖液を製造する方法に関する。
【背景技術】
【0002】
オリゴ糖類は腸内有用細菌の選択的な増殖促進効果によりおなかの調子を良好に保つ機能を有し、特定保健用食品として認定された乳酸菌飲料や菓子類にも利用されている有用な糖類である。食品としての用途だけではなく、畜産飼料に配合されたり、化粧品に乳化剤、保湿成分として配合されて用いられている。
多くのオリゴ糖類の中で、例えば、小麦フスマやコーンコブに由来するキシロオリゴ糖は、他のオリゴ糖と比較し少量で整腸作用を発揮することが知られている。キシロオリゴ糖は、他のオリゴ糖と同様に腸内善玉菌であるビフィズス菌の増殖を選択的に促進し、腸内悪玉菌である大腸菌の増殖を相対的に抑制する作用があることが知られている。大腸菌や腸内腐敗発酵菌は、腸内で増殖しながら発ガン性物質を生産することが報告されており、腸内に存在する大腸菌や腸内腐敗発酵菌の数を減らすことは健康を維持する上で重要である(非特許文献1参照)。
【0003】
オリゴ糖類を経口摂取した場合、胃酸や消化酵素の酸加水分解によりオリゴ糖の重合度が低下し、最終的には大腸菌やクロストリジウム属等の腐敗性嫌気性菌に資化されることが知られている。しかし、2量体や3量体を主成分とするキシロオリゴ糖組成物は、オリゴ糖の中でも胃酸に対する抵抗性が他のオリゴ糖に比べて比較的高く(特許文献1参照)、経口摂取したオリゴ糖のほとんどが分解されずに腸内に到達する可能性が高い。
現在、平均重合度が5量体程度のキシロオリゴ糖(特許文献2参照)や、平均重合度が12量体前後の長鎖キシロオリゴ糖が製造可能であることが報告されている(特許文献3参照)。鎖長が長いキシロオリゴ糖は腸内でもキシロース(単糖)まで分解されにくく、鎖長の短いキシロオリゴ糖と比較し強い整腸作用が期待される為、重合度の大きなキシロオリゴ糖の開発が望まれている。
【0004】
一方、酸性キシロオリゴ糖はキシロオリゴ糖1分子中に少なくとも1つ以上のウロン酸残基を側鎖として有するキシロオリゴ糖である(特許文献4参照)。酸性キシロオリゴ糖には、抗炎症作用(特許文献5参照)、メラニン生成抑制作用(特許文献6参照)、アトピー性皮膚炎改善作用(特許文献7及び8参照)等の機能が認められており、機能性食品だけではなく化粧品等へも利用可能な素材として期待されている。
【0005】
キシロオリゴ糖及び酸性キシロオリゴ糖を製造する場合、原料、酵素由来の着色物質、酸処理工程で加熱により生成される着色物質を製造工程において除去することが大きな課題である。酸性キシロオリゴ糖はキシロオリゴ糖の側鎖にウロン酸が付加しており、負電荷を有している。現在、酸性キシロオリゴ糖とキシロオリゴ糖(ウロン酸の付加していないキシロオリゴ糖)を含む糖液をイオン交換樹脂に通液し、酸性キシロオリゴ糖のみを樹脂に吸着させてキシロオリゴ糖と分離させた後、樹脂に吸着している酸性キシロオリゴ糖を塩で溶出させて製造している。特に酸性キシロオリゴ糖については塩による溶出の際に樹脂に吸着している着色物資も酸性キシロオリゴ糖に混合されて溶出されるため、イオン交換樹脂のみでは効率的に着色物質を除去することが困難であった。従って、イオン交換以外に、活性炭処理等の方法を用いて着色物質を除去する必要があった。しかし、活性炭処理では、製造コストの増加、オリゴ糖の収率の低減、処理時間の増大等の問題があった。また、着色物質は、キシロオリゴ糖及び酸性キシロオリゴ糖の生理活性を低減させ、さらに、オリゴ糖の味、溶解性、保存性等の物理的特性にに影響を及ぼす可能性がある。従って、より着色物質や不純物の含量の少ないキシロオリゴ糖及び酸性キシロオリゴ糖を製造する技術の開発が望まれている。
【0006】
また、キシロオリゴ糖及び酸性キシロオリゴ糖を製造する場合、製造工程を効率化し、コストの低減を図ることも重要な課題である。製造工程において、精製前のオリゴ糖溶液の糖濃度を現状より高めることができれば、精製に供するオリゴ糖溶液の処理量が低減できる。これにより、精製工程での負荷が低減でき、製造コストの低下、製造に要する時間の短縮が可能となる。従って、より精製前のオリゴ糖溶液の糖濃度を高める方法の開発が望まれている。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特許第2549638号
【特許文献2】特許第1078778号
【特許文献3】特開2003−48901
【特許文献4】特許第4073661号
【特許文献5】特開2003−221339
【特許文献6】特許第3772749号
【特許文献7】特開2004−210664
【特許文献8】特許第4232461号
【0008】
【非特許文献1】金沢ら:大腸細菌叢-とくに胆汁酸代謝と大腸発癌について-.総合臨床、26、 1042〜1050 (1977)
【発明の開示】
【発明が解決しようとする課題】
【0009】
本発明は、リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する工程で、オリゴ糖を含む糖液に含まれる着色を効率的に低減し、また、糖濃度の高い糖液を製造することを課題とする。
【課題を解決するための手段】
【0010】
本発明者らは、リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する方法において、リグノセルロース材料をヘミセルラーゼで処理した後のろ液を逆浸透膜で濃縮し、濃縮液を限外ろ過膜で処理後、限外濾過膜で処理したろ液を酸処理することにより糖液の着色を効率的に低減できることを見出した。また、限外濾過膜で処理したろ液をループにより連続的に逆浸透膜に戻すことにより高濃度の糖液の製造ができることを見出した。
【0011】
具体的には、本発明は以下の(1)〜(7)の構成を採用する。
(1)リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する方法において、リグノセルロース材料をヘミセルラーゼで処理した後のろ液を逆浸透膜で濃縮する濃縮工程、得られた濃縮液を限外ろ過膜で処理する脱色工程、限外濾過膜で脱色された糖液を酸で加水分解する酸処理工程、からなる工程を有することを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(2)前記(1)項の限外濾過膜で脱色された糖液をループにより連続的に逆浸透膜に戻すことを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(3)前記(1)項又は(2)項に記載の限外濾過膜の分画分子量が5000〜30000であることを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(4)前記(1)項に記載のリグノセルロース材料が、木材の微細化物であることを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(5)前記(4)項に記載の木材の微細化物が化学的処理により得られたパルプであることを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(6)前記(5)項に記載の化学的処理により得られたパルプが広葉樹由来のクラフトパルプであることを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
(7)前記(1)項に記載のヘミセルラーゼが、キシラナーゼであることを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【発明の効果】
【0012】
本発明により、キシロオリゴ糖及び酸性キシロオリゴ糖を含む糖液の着色を効率的に低減させることができ、その結果として着色が低減されたキシロオリゴ糖及び酸性キシロオリゴ糖が提供される。さらに、本発明により、精製に供する糖液の糖濃度を効率的に高めることができるため、精製工程での負荷(コスト)を低減でき、また、精製工程に要する時間が短縮できるため生産効率の高いキシロオリゴ糖および酸性キシロオリゴ糖の製造方法が提供される。
【図面の簡単な説明】
【0013】
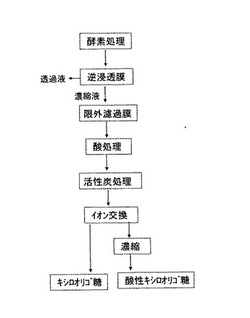
【図1】実施例1、実施例2、実施例3の製造工程フローを示す図
【図2】比較例1、比較例2、比較例3の製造工程フローを示す図
【図3】実施例4の製造工程フローを示す図
【図4】実施例4の糖濃度を示す図
【発明を実施するための最良の形態】
【0014】
以下、本発明の構成について詳述するが、本発明はこれにより限定されるものではない。本発明のキシロオリゴ及び酸性キシロオリゴ糖を得るための原料として木本性植物、あるいは草本性植物由来のリグノセルロースを用いることができる。木本性植物由来のリグノセルロース原料としては広葉樹、針葉樹の木部や樹皮を用いるのが好ましいが、枝、葉等の他の部位も用いることができる。草本性植物由来のリグノセルロース原料としては、ケナフ、麻、バガス、イネ等の茎、葉等の部位を特に限定なく用いることができる。本発明では、木本性植物の木部や樹皮の部位、あるいは草本性植物の茎、枝葉等の部位を微細化処理した微細化物を用いることができる。微細化処理後、パルプの形状にして用いることが好ましい。用いるパルプとしては、化学パルプ、機械パルプ、脱墨パルプ等、特に限定されないが、広葉樹由来の化学パルプが好ましい。化学パルプを得るための蒸解法としては、クラフト蒸解、ポリサルファイド蒸解、ソーダ蒸解、アルカリサルファイト蒸解等の公知の蒸解法が挙げられ、パルプの品質、パルプを得るためのエネルギー効率等を考慮した場合、クラフト蒸解法を用いることが好ましい。また、クラフト蒸解後、酸素漂白したパルプを用いることがより好ましい。クラフト蒸解後、酸素漂白した広葉樹由来のパルプでは、グルコース、アラビノース等の構成糖がほとんど含まれず、キシロースがほぼ100%近く含まれるという特徴があるため、用いる原料としてより好ましい。
【0015】
原料としてパルプを用いる場合、使用するパルプをパルプ製造工程よりキシロオリゴ及び酸性キシロオリゴ糖の糖製造工程へ移送する。移送の手段としては、低濃度のパルプであればポンプによるライン移送、高濃度のパルプであればベルトコンベア等の方法が挙げられ、移送方法は特に限定されない。
【0016】
原料として用いるパルプは、例えば、タンク内で水に懸濁後、ドラムフィルターに移送しドラムフィルターで水で洗浄後、脱水する。この工程でパルプに含まれる微細な懸濁物、リグニンおよび有機酸等の不純物が除かれるため洗浄することが好ましい。パルプの洗浄方法としては、パルプを水で洗浄後、脱水できる装置であれば特に限定されない。また、この洗浄工程で水にpH調整剤や温度調節した洗浄水を添加することにより、洗浄後のパルプのpHや温度を調節し、後段でのヘミセルラーゼの至適反応条件を調節することもできる。
【0017】
原料として用いるパルプは、前記の工程の後、ヘミセルラーゼ処理を行う反応装置へポンプで移送する。原料とヘミセルラーゼを混合する方法は、反応槽へ移送する前に混合しても良いし、反応槽内で混合しても良い。高濃度のパルプをヘミセルラーゼで処理する場合、反応槽の形状としては、円筒型が連続的に移送できるため好ましいが、酵素反応が行えるものであれば特に限定されない。高濃度のパルプをヘミセルラーゼで処理する場合、スクリューミキサー等(例えば、トランポスクリュー等)の混合機を用いて反応槽へ移送される前にパルプとキシラナーゼを均一に混和させておくことが好ましい。用いる混合機としては、パルプとヘミセルラーゼを均一に混合できる装置であれば特に限定なく用いることができる。一方、低濃度のパルプをヘミセルラーゼで処理する場合、反応槽の形状は特に限定されないが、例えば、攪拌機を備えた反応槽内でパルプ懸濁液を攪拌しながらオリゴ糖の溶出に最適な滞留時間でヘミセルラーゼ処理を行い、パルプ懸濁液(オリゴ糖を含む)を連続的に回収する方法が挙げられる。これらの反応槽は、ヘミセルラーゼの至適反応温度を維持する為に温度調節用のジャケットや断熱材ケーシングを具備することが好ましい。
【0018】
本発明で用いるヘミセルラーゼとしては、キシラナーゼ活性を含むものであれば特に限定されない。ヘミセルラーゼとしては、例えば、商品名カルタザイム(クラリアント社製)、パルプザイム(ノボノルディスク社製)、エコパルプ(ローム・エンザイム社製)、スミチーム(新日本化学工業社製)、マルチフェクトキシラナーゼ(ジェネンコア社製)、キシラナーゼコンク(アドバンスド・バイオケミカルス社製)等の市販の酵素製剤や、トリコデルマ(Trichoderma)属、テルモミセス(Thermomyces)属、オウレオバシヂウム(Aureobasidium)属、ストレプトミセス(Streptomyces)属、アスペルギルス(Aspergillus)属、クロストリジウム(Clostridium)属、バチルス(Bacillus)属、テルモトガ(Thermotoga)属、テルモアスクス(Thermoascus)属、カルドセラム(Caldocellum)属、テルモモノスポラ(Thermomonospora)属等の微生物により生産されるキシラナーゼが挙げられる。
【0019】
パルプのヘミセルラーゼ処理工程では、パルプに対するヘミセルラーゼの添加量、反応時間を調節することにより、パルプから溶出されるオリゴ糖の濃度やオリゴ糖の重合度を調節することができる。一般に、ヘミセルラーゼの添加量が多いほど、また反応時間が長いほど反応液中のオリゴ糖濃度は高くなり、且つオリゴ糖の重合度は小さくなる。従って、高重合度のオリゴ糖を含む高濃度の糖液を安定して得るためには、パルプに対して適量のヘミセルラーゼ(低分子まで分解されない程度のヘミセルラーゼ)を添加し、反応後の糖液(パルプを除いたオリゴ糖を含むろ液)の一部を酵素反応槽に戻し再度、酵素反応させることが好ましい。これによりオリゴ糖の重合度を高い状態に維持しながら、時間経過と共に高重合度のオリゴ糖の糖濃度を高めることができる。パルプに対して過剰のヘミセルラーゼを添加したり、反応時間を長くすると、溶出したオリゴ糖が更にヘミセルラーゼで分解され、キシロース、キシロビオースのような鎖長の短いオリゴ糖にまで分解されるため好ましくない。
【0020】
反応槽内でのパルプ濃度、反応時間、キシラナーゼ添加量は任意に設定可能であるが、パルプ濃度は2〜20質量%が好ましく、7〜15質量%がさらに好ましい。パルプ濃度が低すぎるとオリゴ糖の濃度を高めることが困難となり、また、処理液の容量が増大するため、反応設備の大型化が必要となるという問題が生じる。一方、パルプ濃度が高すぎるとヘミセルラーゼとパルプの均一な混合やパルプの移送が困難となり、また、糖液の回収量が減少するため好ましくない。パルプに対する適したヘミセルラーゼ添加量及び反応時間は、用いる酵素の種類によって異なる。例えば、マルチフェクトキシラナーゼの場合、反応時間は10〜240分が好ましく、30〜90分がより好ましい。また、パルプに対するヘミセルラーゼの添加量は2〜200(unit/g−乾燥パルプ)が好ましく、10〜100(unit/g−乾燥パルプ)がより好ましい。
【0021】
本発明により、パルプをヘミセルラーゼ処理した反応液中に溶出されるオリゴ糖の重合度は、用いる酵素の種類や反応条件によって変動するが、例えば、マルチフェクトキシラナーゼを用いる場合、パルプ濃度10質量%、反応時間45分、反応温度50℃、pH6.0、パルプに対する酵素添加量50(unit/g−乾燥パルプ)の条件では、1〜15量体の分布を持つ平均重合度が5量体程度のキシロオリゴ糖、および1〜20量体の分布を持つ平均重合度10量体程度の酸性キシロオリゴが糖液中に溶出される。
【0022】
ヘミセルラーゼで処理したパルプに含まれるオリゴ糖を回収するための手段は特に限定されないが、例えば、スクリュープレス等の装置を使用してパルプを圧搾してろ液(オリゴ糖含有)を回収しても良いし、ドラムフィルター等の装置を使用してパルプを水で置換洗浄し、オリゴ糖を含有するろ液を回収しても良い。このようにして得られたオリゴ糖を含有するろ液は次の濃縮工程へ移送される。また、前述したようにろ液の一部を酵素反応槽に戻し、再度、ヘミセルラーゼで反応させても良い。
【0023】
パルプをヘミセルラーゼで反応させた後のろ液は、次の濃縮工程へ移送する前に前処理により原料由来の残渣を除くことが好ましい。前処理としては、バッグフィルター、フィルタープレス、プレコートフィルター、セラミックフィルター等の精密ろ過処理や凝集沈殿処理が挙げられ、これらの処理を併用しても良い。精密ろ過処理を行う場合は、サブミクロンオーダーの濾過精度を持つフィルターが好ましい。凝集沈殿処理を行う場合は、硫酸バンド、ポリ塩化アルミニウム等の無機系凝集剤や、ポリアクリルアミド系、ポリアミジン系等の高分子凝集剤あるいはキトサン等の天然高分子凝集剤を用いることができる。前処理の方法は、パルプ、懸濁物質等の微細な不溶成分を除去することができる方法であれば、前記の方法に限定されない。
【0024】
本発明では、パルプをヘミセルラーゼで反応させた後のろ液中に含まれるオリゴ糖溶液は、後段での精製負荷を低減するために、濃縮により糖液中の濃度を高濃度にすることが望ましい。糖液を濃縮するために逆浸透膜を用いる。逆浸透膜を用いる方法では、キシロース、キシロビオース等の低分子(重合度の小さい糖)や反応後の糖液に含まれる低分子物質(例えば、炭酸ナトリウム、チオ硫酸ナトリウム等の無機物、有機酸、等)が透過液として除去され、高分子(重合度の大きいキシロオリゴ糖)のみが選択的に濃縮されるという利点がある。また、膜濃縮では運転コストが溶媒抽出による方法と比較し安価であり、また、危険性のある溶媒を使用する必要がないため好ましい。
しかし、逆浸透膜の膜エレメントを連続的に運転する場合、オリゴ糖の製造工程で使用する原水中に存在するコロイド性物質や微細な懸濁物質、特に酵素反応後の糖液に不純物として含まれるリグニン等が膜の表面上に付着し、蓄積されて運転時間の経過と共に膜のろ過比抵抗が増大して透過流束が低下するという問題が生じる。特にリグニン等の高分子は透過液として膜外に排出されないためオリゴ糖と共に濃縮されて、結果として時間経過と共に膜の表面に付着し膜の操作圧力を上昇させる。操作圧力が限界値まで上昇すると、連続運転が困難となり、オリゴ糖の生産効率が低下(運転コスト増加、製造時間延長)するため好ましくない。また、精製に供する糖液の糖濃度は、できるだけ高濃度にした方が後段の製造コストが低減できるというメリットがある。しかし、運転開始後、短時間でリグニン等の不純物が膜に付着すると糖濃度が充分に高濃度になる前に膜の操作圧力が限界値に達し糖液の濃度をそれ以上に高濃度にすることができなくなる。従って、膜エレメントの性能劣化を最小限にし、長時間にわたり安定して逆浸透膜装置を運転することが課題であった。この問題を解決するために検討した結果、後述する限外濾過膜で処理した後のろ液をループにより連続的に逆浸透膜に戻すことにより糖濃縮液の糖濃度を高めることが可能となった。
【0025】
本発明では、逆浸透膜で濃縮した糖液を、次に、限外濾過膜により着色物質や不純物を除去する。逆浸透膜で濃縮中の糖液は、糖液の一部を連続的に限外濾過膜に移送しても良いし、糖濃度が一定の値に達してから限外濾過装置を停止し、濃縮した糖液の全量を限外濾過膜に移送しても良い。
従来は、後述する酸処理の後に限外濾過膜による処理を実施していた。しかし、酸処理前の糖濃縮液には原料や酵素由来の不純物(リグニン、酵素由来のタンパク質等)が混合しており、加熱(酸処理)により、糖液の着色が増大するという問題が生じた。糖液を加熱すると、例えば、アミノ酸や蛋白質の共存下で糖を加熱することによるメイラード反応による糖の褐変化、カラメル物質の増加等、加熱により糖液中に新たな着色物質が増加する。この問題を解決するために検討した結果、後述の酸処理の前に糖濃縮液を限外ろ過膜で処理することにより、糖濃縮液に含まれる不純物をあらかじめ除去することができ、結果として酸処理工程で発生する着色物質の生成を低減することが可能となった。
また、限外濾過膜による処理では、糖濃縮液に元々含まれる原料由来のリグニンや着色物質等の高分子の不純物を除去することもできる。
用いる限外濾過膜の分画分子量は、5000〜30000が好ましい。分画分子量が5000より小さいとオリゴ糖の回収率が低下し、膜への抵抗が増加しオリゴ糖の生産効率が低下するため好ましくない。また、分画分子量が30000より大きいと着色物質や不純物の除去率が低下するため好ましくない。
【0026】
本発明では、前記の限外濾過膜で処理した後のろ液をループにより連続的に逆浸透膜に戻す(図3参照)。逆浸透膜へ戻す限外濾過膜処理後のろ液の液量はろ液の全量でも良いし、一部でもよい。ろ液の全量を戻す場合は、逆浸透膜内の糖濃度が一定の値に達してから限外濾過装置を停止し、次の酸処理工程へ移送する。一方、ろ液の一部を戻す場合は、逆浸透膜へ戻さない残りのろ液を逆浸透膜から連続的に酸処理工程へ移送する。
前述の逆浸透膜で糖液が濃縮される時にオリゴ糖と共に不純物として含まれるリグニン等の高分子物質も濃度が上昇するが、限外濾過膜で処理した後のろ液をループにより連続的に逆浸透膜に戻すことにより、リグニン等の不純物のみを濃縮中の糖液から除去できる。その結果として、逆浸透膜の操作圧力の上昇を抑制することができ、オリゴ糖の濃度をより高めることができる。
【0027】
前記の限外濾過膜で処理した糖液(図1参照)、あるいは、逆浸透膜で濃縮した糖液(図3参照)は、次に酸処理を行う。糖液中に含まれるキシロオリゴ糖及び酸性キシロオリゴ糖の一部はリグニンと結合して複合体(リグニン−キシロオリゴ糖複合体、リグニン−酸性キシロオリゴ糖複合体)として存在する。酸処理により、複合体からキシロオリゴ糖および酸性キシロオリゴ糖を遊離させることができる。酸処理の方法としては、例えば、糖液に酸を添加してpHを5以下に調整し、高温で加熱する方法が挙げられる。pH調整に用いる酸は、特に限定されないが、例えば、硫酸、塩酸等の鉱酸の他、シュウ酸、酢酸等の有機酸が挙げられる。酸処理のpHは2〜5が好ましく、さらにpH3.5〜4.0の範囲がより好ましい。pHが2より低いと糖液に含まれるキシロオリゴ糖及び酸性キシロオリゴ糖からキシロースへの加水分解が促進され、オリゴ糖の回収率が低下するため好ましくない。またpHが5より高いと150℃以下の温度では複合体からオリゴ糖の遊離が抑制されるため好ましくない。酸処理の温度は、特に限定されないが、100〜200℃が好ましく、105〜170℃がより好ましく、110〜125℃がさらに好ましい。100℃より低い温度では、複合体からのオリゴ糖の遊離が抑制されるため好ましくない。また、170℃を越えると、キシロオリゴ糖および酸性キシロオリゴ糖からキシロースへの分解が促進されオリゴ糖の収率が低下するため好ましくない。また、酸処理中の圧力は大気圧〜5kg/cm2の範囲であることが好ましい。
【0028】
酸処理後の糖液には、酸処理で生成した着色物質、前記の限外濾過膜で除去されなかった原料由来のリグニン、着色物質等が含まれており、その一部は不溶性残渣として存在している。これらの不溶性残渣を遠心分離、セラミックフィルター等によるフィルターろ過、ろ布等によるろ過で除去することが好ましい。
【0029】
酸処理後の糖液中に含まれる着色物質等の不純物の含量をさらに低減するために、活性炭処理を行うことが好ましい。用いる活性炭の種類としては、糖液中の着色物質等の不純物の含量を低減する能力を有するものであれば特に限定されない。
【0030】
前記の操作で着色物質等の不純物を低減した糖液に含まれるキシロオリゴ糖と酸性キシロオリゴ糖をイオン交換樹脂を用いて分離・精製する。分離・精製の方法として、例えば、オリゴ糖を含む糖濃縮液を強カチオン樹脂→弱アニオン樹脂→強カチオン樹脂→弱アニオン樹脂の順に通液する方法を用いることができる。この方法では、酸性キシロオリゴ糖がアニオン樹脂に吸着されるため、キシロオリゴ糖のみをろ液として回収することができる。次に、アニオン樹脂に、例えば、塩化ナトリウム等の塩を通液することにより酸性キシロオリゴ糖を樹脂から溶出させて回収することができる。回収したキシロオリゴ糖及び酸性キシロオリゴ糖を含む溶液を、例えば、エバポレーション等の濃縮装置で濃縮することができる。オリゴ糖を含む溶液をスプレードライで乾燥することにより、キシロオリゴ糖及び酸性キシロオリゴ糖の粉末が得られる。
【実施例】
【0031】
以下に、本発明を実施例により詳細に説明するが、本発明は以下の実施例に限定されるものではない。以下に示す%は、特に断らない限りすべて質量%を示し、対パルプの添加率はパルプの絶乾質量に対する質量の比率を示す。なお、各測定法は以下のとおりである。
〈測定法の概要〉
全糖量の定量
全糖量は検量線をD−キシロース(和光純薬工業製)を用いて作製し、フェノール硫酸法(還元糖の定量法;学会出版センター)で定量した。
(2)還元糖量の定量
還元糖量は検量線をD−キシロース(和光純薬工業製)を用いて作製し、ソモジ−ネルソン法(還元糖の定量法;学会出版センター)で定量した。
(3)平均重合度の決定法
サンプル糖液を50℃に保ち15000rpmで15分間遠心分離し不溶物を除去後、上清液の全糖量を還元糖量(共にキシロース換算)を測定した。全糖量を還元糖量で割って平均重合度を求めた。
(4)酵素力価の定義
酵素として用いたキシラナーゼの活性測定にはバーチウッドキシラン(シグマ社製)を基質として用いた。酵素力価の定義はキシラナーゼがキシランを分解することで得られる還元糖の還元力をDNS法(還元糖の定量法;学会出版センター)を用いて測定し、1分間に1マイクロモルのキシロースに相当する還元力を生成させる酵素量を1unitとした。
【0032】
<実施例1>
[オリゴ糖濃縮液の製造]
混合広葉樹チップ(国内産広葉樹チップ20%、ユーカリ材80%)をクラフト蒸解後、酸素脱リグニンしパルプ(原料)を得た。以降の操作は、連続的に行った。タンクにパルプ及び高温水(60℃)を添加し、パルプ濃度(最終濃度)を1.6質量%に調製した(容量10m3)。次に、タンクに濃硫酸を添加、攪拌してpH5.5に調整後、ドラムフィルター(新菱製作所製:φ2000×600 SUF)でパルプを脱水洗浄した。脱水後のパルプ(パルプ濃度20質量%)に温水(50℃)を添加し、パルプ濃度を10質量%に調製後、マルチフェクトキシラナーゼ(ジェネンコア社製)を対パルプ50unit(乾燥パルプ1g当たり)となるように添加して、トランポスクリュー(新菱製作所:220x850 HC-C)で均一に混合した。混合後のパルプを中濃度ポンプ(新菱製作所:200×RPK)で容積2m3の円筒型反応槽(φ800mm×4000mmH)の入口から押し込み、円筒型反応槽内で連続的に酵素反応を行った(反応時間40分間、温度50℃)。円筒型反応槽内の出口から排出されたパルプ(酵素反応後のパルプ)をスクリュープレス(新菱製作所:250×1000 SPH−EN)でパルプ濃度が40質量%になるまで脱水して、キシラナーゼ反応後のろ液を得た。酵素反応開始から60分以降は、キシラナーゼ反応後のろ液の一部をトランポスクリューに戻し、ドラムフィルターで脱水した20質量%濃度のパルプを温水(50℃)の替わりに戻したキシラナーゼ反応後のろ液でパルプ濃度を10質量%に調整した。酵素反応開始から150分後、反応後のろ液中の全糖濃度は0.92%に上昇し、この時点での糖液に含まれるキシロオリゴ糖の平均重合度は4.7であった。以上のパルプのキシラナーゼ処理を24時間連続して実施した。酵素反応開始から150分以降は、糖濃度約0.90%の反応ろ液を安定して回収すことができた。最終的に糖濃度0.90%のキシラナーゼ反応後のろ液を15m3得た。得られた反応ろ液を、ミクロンレート1μmのバックフィルター(ISPフィルターズ製)、次にミクロンレート0.2μmのセラミックフィルター(日本ポール製)でろ過して、清澄なろ液(糖液)を得た。このろ液を逆浸透膜(日東電工製:NTR−7450、膜質:スルホン化ポリエーテルスルホン系、膜面積:6.5m2−2本)で液温50℃、流量1400〜1800L/hの運転条件で15倍に濃縮し、全糖濃度11%の濃縮液を1m3得た。
[オリゴ糖の精製]
図1に示す製造工程で、前記([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを分画分子量10000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いて、透過流速350L/hで処理した。限外濾過膜を通過したろ液(糖を含む画分)を濃硫酸でpH3.5に調整後、121℃で45分間処理(酸処理)した。ろ液を50℃まで冷却後、酸処理後で生成した不溶性残渣をミクロンレート0.2μmのセラミックフィルター(日本ポール製)で除去した。この糖液を一部採取して全糖濃度を0.2%に調製(蒸留水で希釈)し、350nmの波長における吸光度(着色度)を測定した(表1)。次に、ろ液480Lに対して活性炭(三倉化成製:PM−SX)10kgを添加し、50℃で2時間処理後、糖液を回収した。この糖液を、SV1.5で強カチオン樹脂(三菱化学製:PK−218、300L)→弱アニオン樹脂(三菱化学製:WA30、300L)→強カチオン樹脂(三菱化学製:PK−218、300L)→弱アニオン樹脂(三菱化学製:WA30、300L)からなる4床4塔式イオン交換樹脂に通液し、キシロオリゴ糖糖液(糖濃度4.3質量%、550L)を得た。得られたキシロオリゴ糖溶液を強カチオン樹脂でpH7に調整後、スプレードライヤー(大川原化工機製:ODA−25型)で処理して、キシロオリゴ糖粉末23.0kg(平均重合度5.0)を得た。次に、2塔目及び4塔目の弱アニオン樹脂に50mM塩化ナトリウム水溶液をSV1.5で通液し、イオン交換樹脂に吸着している酸性キシロオリゴ糖を溶出させ、酸性キシロオリゴ糖溶液(糖濃度2.8質量%、400L)を得た。得られた酸性キシロオリゴ糖溶液を、強カチオン樹脂でpH5に調整後、糖濃度20質量%までエバポール(大川原化工機:CEP-1)で濃縮した。次に、スプレードライヤー(大川原化工機製:ODA-25型)で処理して、酸性キシロオリゴ糖粉末11.3kg(平均重合度11.0)を得た。得られたキシロオリゴ糖及び酸性キシロオリゴ糖を蒸留水で全糖濃度5質量%に調整し、350nmの波長における吸光度(着色度)を測定した(表2)。
【0033】
<比較例1>
図2に示す製造工程で、実施例1([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを、濃硫酸でpH3.5に調整後、121℃で45分間処理(酸処理)した。糖濃縮液を50℃まで冷却後、酸処理後で生成した不溶性残渣をミクロンレート0.2μmのセラミックフィルター(日本ポール製)で除去した。次に、糖濃縮液を分画分子量10000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いて、透過流速350L/hで処理した。この糖液を一部採取して全糖濃度を0.2質量%に調製(蒸留水で希釈)し、350nmの波長における吸光度(着色度)を測定した(表1)。次に、限外濾過膜を通過したろ液480Lに対して活性炭(三倉化成製:PM−SX)10kgを添加し、50℃で2時間処理し糖液を回収した。この糖液を、SV1.5で強カチオン樹脂(三菱化学製:PK−218、300L)→弱アニオン樹脂(三菱化学製:WA30、300L)→強カチオン樹脂(三菱化学製:PK−218、300L)→弱アニオン樹脂(三菱化学製:WA30、300L)からなる4床4塔式イオン交換樹脂に通液し、キシロオリゴ糖溶液(糖濃度3.9質量%、550L)を得た。得られたキシロオリゴ糖溶液を強カチオン樹脂でpH7に調整後、スプレードライヤー(大川原化工機製:ODA−25型)で処理して、キシロオリゴ糖粉末20.6kg(平均重合度5.1)を得た。次に、2塔目及び4塔目の弱アニオン樹脂に50mM塩化ナトリウム水溶液をSV1.5で通液しイオン交換樹脂に吸着している酸性キシロオリゴ糖を溶出させ、酸性キシロオリゴ糖溶液(糖濃度2.4質量%、400L)を得た。得られた酸性キシロオリゴ糖溶液を、強カチオン樹脂でpH5に調整後、糖濃度20質量%までエバポール(大河原化工機:CEP-1)で濃縮した。次に、スプレードライヤー(大川原化工機製:ODA−25型)で処理して、酸性キシロオリゴ糖粉末9.5kg(平均重合度11.0)を得た。得られたキシロオリゴ糖及び酸性キシロオリゴ糖を蒸留水で全糖濃度5質量%に調整し、350nmの波長における吸光度(着色度)を測定した(表2)。
【0034】
分画分子量10000の限外濾過膜を用いて試験した結果を表1および表2に示す。糖濃縮液を限外濾過した後に酸処理した場合(実施例1)では、糖濃縮液を酸処理後に限外濾過した場合(比較例1)と比較し糖液の着色度(吸光度350nm)が減少した(表1)。また、糖濃縮液を限外濾過した後に酸処理した場合(実施例1)では、糖濃縮液を酸処理後に限外濾過した場合(比較例1)と比較し精製後のキシロオリゴ糖液及び酸性キシロオリゴ糖の着色度(吸光度350nm)が減少した(表2)。以上の結果から、糖濃縮液を限外濾過した後に酸処理を行うことで、酸処理で生成される着色物質の含量を低減できることが判明した。この結果により、後段の精製工程で脱色を目的として使用する活性炭の量を低減でき、コスト低減が可能となる。
【0035】
【表1】

【0036】
【表2】

【0037】
<実施例2>
[オリゴ糖の精製]
図1に示す製造工程で実施例1([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを精製した。分画分子量5000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いた以外は実施例1と同様の方法で実施した。糖液の採取についても実施例1と同様の工程の箇所で実施し、糖液の350nmの波長における吸光度(着色度)を測定した(表3)。尚、イオン交換樹脂処理後のキシロオリゴ糖溶液の糖濃度は3.7質量%(550L)、酸性キシロオリゴ糖溶液の糖濃度は2.3質量%(400L)であった。また、精製後、得られたキシロオリゴ糖粉末は19.1kg(平均重合度4.9)、酸性キシロオリゴ糖粉末は9.5kg(平均重合度10.8)であった。
【0038】
<比較例2>
図2に示す製造工程で実施例1([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを精製した。分画分子量5000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いた以外は比較例1と同様の方法で実施した。糖液の採取についても比較例1と同様の工程の箇所で実施し、糖液の350nmの波長における吸光度(着色度)を測定した(表3)。尚、イオン交換樹脂処理後のキシロオリゴ糖溶液の糖濃度は3.3質量%(550L)、酸性キシロオリゴ糖溶液の糖濃度は2.0質量%(400L)であった。また、精製後、得られたキシロオリゴ糖粉末は16.8kg(平均重合度4.9)、酸性キシロオリゴ糖粉末は8.4kg(平均重合度10.9)であった。
【0039】
分画分子量5000の限外濾過膜を用いて試験した結果を表3および表4に示す。糖濃縮液を限外濾過した後に酸処理した場合(実施例2)では、糖濃縮液を酸処理後に限外濾過した場合(比較例2)と比較し糖液の着色度(吸光度350nm)が減少した(表3)。また、糖濃縮液を限外濾過した後に酸処理した場合(実施例2)では、糖濃縮液を酸処理後に限外濾過した場合(比較例2)と比較し精製後のキシロオリゴ糖液及び酸性キシロオリゴ糖の着色度(吸光度350nm)が減少した(表4)。
【0040】
【表3】

【0041】
【表4】

【0042】
<実施例3>
[オリゴ糖の精製]
図1に示す製造工程で実施例1([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを精製した。分画分子量30000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いた以外は実施例1と同様の方法で実施した。糖液の採取についても実施例1と同様の工程の箇所で実施し、糖液の350nmの波長における吸光度(着色度)を測定した(表5)。尚、イオン交換樹脂処理後のキシロオリゴ糖溶液の糖濃度は4.0質量%(550L)、酸性キシロオリゴ糖溶液の糖濃度は2.7質量%(400L)であった。また、精製後、得られたキシロオリゴ糖粉末は22.0kg(平均重合度5.1)、酸性キシロオリゴ糖粉末は11.0kg(平均重合度11.2)であった。
【0043】
<比較例3>
図2に示す製造工程で実施例1([オリゴ糖濃縮液の製造])で得られた濃縮糖液500Lを精製した。分画分子量30000の限外濾過膜(限外濾過装置:オスモニクス製UF膜モジュール)を用いた以外は比較例1と同様の方法で実施した。糖液の採取についても比較例1と同様の工程の箇所で実施し、糖液の350nmの波長における吸光度(着色度)を測定した(表5)。尚、イオン交換樹脂処理後のキシロオリゴ糖溶液の糖濃度は3.9質量%(550L)、酸性キシロオリゴ糖溶液の糖濃度は2.5質量%(400L)であった。また、精製後、得られたキシロオリゴ糖粉末は21.2kg(平均重合度5.1)、酸性キシロオリゴ糖粉末は10.7kg(平均重合度11.1)であった。
【0044】
分画分子量30000の限外濾過膜を用いて試験した結果を表5および表6に示す。糖濃縮液を限外濾過した後に酸処理した場合(実施例3)では、糖濃縮液を酸処理後に限外濾過した場合(比較例3)と比較し糖液の着色度(吸光度350nm)が減少した(表5)。また、糖濃縮液を限外濾過した後に酸処理した場合(実施例3)では、糖濃縮液を酸処理後に限外濾過した場合(比較例3)と比較し精製後のキシロオリゴ糖液及び酸性キシロオリゴ糖の着色度(吸光度350nm)が減少した(表6)。
【0045】
【表5】

【0046】
【表6】

【0047】
<実施例4>
[逆浸透膜と限外濾過膜の間へのループ導入による連続循環の検討]
実施例1([オリゴ糖濃縮液の製造])と同様の方法で、パルプを原料として糖濃縮液を製造した。糖濃縮液製造の逆浸透膜(日東電工製:NTR−7450)で濃縮された糖液を連続的に限外濾過装置(オスモニクス製UF膜モジュール、分画分子量10000)を用いて、透過流速350L/hで限外ろ過膜による処理を行った。図3に示すように限外濾過膜を通過したろ液(糖を含む画分)を前記の逆浸透膜(日東電工製:NTR−7450)へ戻し、逆浸透膜→限外濾過膜の工程を連続的に循環させ、糖濃度が一定以上に濃縮されるまで限外濾過を継続した。ループによる連続循環開始後、逆浸透膜入口の操作圧力を経時的に測定した。また、逆浸透膜内の糖液を採取し、糖液の全糖濃度を測定した。
【0048】
<比較例4>
実施例4記載の方法で、ループによる連続循環を行わない方法を比較例4とした(製造工程フローは図1と同様)。実施例4と同様に、逆浸透膜入口の操作圧力を測定した。また、逆浸透膜内の糖液を採取し、糖液の全糖濃度を測定した(逆浸透膜の運転開始後、同一の時間経過におけるデータを実施例4と比較した)。
【0049】
逆浸透膜入口の操作圧力と逆浸透膜内の糖濃度の関係を図4に示す。逆浸透膜と限外濾過膜の間にループをつくり、糖液を連続循環させた場合(実施例4)では、連続循環させない場合(比較例4)と比較し、同じ操作圧力(逆浸透膜)において高濃度の糖液を得ることができた。操作圧力1.9MPaの場合、実施例4では糖濃度15.2質量%、比較例4では、糖濃度11.0質量%であった。また、実施例で4は、比較例4と比較し酸処理以降の精製工程に要する時間を約4時間短縮することができた。
【産業上の利用可能性】
【0050】
本発明により、着色が低減された高純度のキシロオリゴ糖および酸性キシロオリゴ糖が効率良く製造できるため、キシロオリゴ糖及び酸性キシロオリゴ糖を安価に製造することができる。
【特許請求の範囲】
【請求項1】
リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する方法において、リグノセルロース材料をヘミセルラーゼで処理した後のろ液を逆浸透膜で濃縮する濃縮工程、得られた濃縮液を限外ろ過膜で処理する脱色工程、限外濾過膜で脱色された糖液を酸で加水分解する酸処理工程、からなる工程を有することを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項2】
限外濾過膜で脱色された糖液の全部または一部をループにより連続的に逆浸透膜に戻すことを特徴とする請求項1に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項3】
限外濾過膜の分画分子量が5000〜30000であることを特徴とする請求項1または2に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項4】
リグノセルロース材料が、木材の微細化物であることを特徴とする請求項1に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項5】
木材の微細化物が化学的処理により得られたパルプであることを特徴とする請求項4に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項6】
化学的処理により得られたパルプが広葉樹由来のクラフトパルプであることを特徴とする請求項5に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項7】
ヘミセルラーゼが、キシラナーゼであることを特徴とする請求項1に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項1】
リグノセルロース材料を原料としてキシロオリゴ糖および酸性キシロオリゴ糖を製造する方法において、リグノセルロース材料をヘミセルラーゼで処理した後のろ液を逆浸透膜で濃縮する濃縮工程、得られた濃縮液を限外ろ過膜で処理する脱色工程、限外濾過膜で脱色された糖液を酸で加水分解する酸処理工程、からなる工程を有することを特徴とするキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項2】
限外濾過膜で脱色された糖液の全部または一部をループにより連続的に逆浸透膜に戻すことを特徴とする請求項1に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項3】
限外濾過膜の分画分子量が5000〜30000であることを特徴とする請求項1または2に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項4】
リグノセルロース材料が、木材の微細化物であることを特徴とする請求項1に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項5】
木材の微細化物が化学的処理により得られたパルプであることを特徴とする請求項4に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項6】
化学的処理により得られたパルプが広葉樹由来のクラフトパルプであることを特徴とする請求項5に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【請求項7】
ヘミセルラーゼが、キシラナーゼであることを特徴とする請求項1に記載のキシロオリゴ糖および酸性キシロオリゴ糖の製造方法。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2012−100546(P2012−100546A)
【公開日】平成24年5月31日(2012.5.31)
【国際特許分類】
【出願番号】特願2010−249276(P2010−249276)
【出願日】平成22年11月8日(2010.11.8)
【出願人】(000122298)王子製紙株式会社 (2,055)
【Fターム(参考)】
【公開日】平成24年5月31日(2012.5.31)
【国際特許分類】
【出願日】平成22年11月8日(2010.11.8)
【出願人】(000122298)王子製紙株式会社 (2,055)
【Fターム(参考)】
[ Back to top ]

