クロピドグレル抵抗性のリスクを決定するための方法
【課題】栓球阻害剤による治療が計画されている患者について、クロピドグレルによる処置に対する非応答性のリスクを評価することを可能にする方法を提供する。
【解決手段】a)患者がクロピドグレルを未だ服用していない時点において患者から得た試料中の栓球活性を測定するステップ、及びb)測定された栓球活性を、統計的に決定された判定限界と、比較するステップを備えてなる、患者のクロピドグレル抵抗性のリスクを決定するための方法であって、判定限界を超えて増加している栓球機能によって、その患者に関して、クロピドグレル抵抗性のリスクの増加が示される方法。
【解決手段】a)患者がクロピドグレルを未だ服用していない時点において患者から得た試料中の栓球活性を測定するステップ、及びb)測定された栓球活性を、統計的に決定された判定限界と、比較するステップを備えてなる、患者のクロピドグレル抵抗性のリスクを決定するための方法であって、判定限界を超えて増加している栓球機能によって、その患者に関して、クロピドグレル抵抗性のリスクの増加が示される方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、個別化治療を目標とする心血管状態及び血栓状態の診断の分野の発明である。特に、本発明は、クロピドグレルによる治療の恩恵が得られない可能性が高い患者を同定するための方法に関する。
【背景技術】
【0002】
クロピドグレル(商標名:Plavix(登録商標)、Iscover(登録商標))は、血液凝固を阻害する薬物であり、心筋梗塞や脳卒中等の急性心血管状態又は血栓状態を患っている患者又はそのようなイベントを患ったことがあり、再発性血栓イベントのリスクを低下させるために予防的に処置を継続しなければならない患者のルーチン処置に、ますます、多用されている。クロピドグレルは、例えば、冠血管にステントが埋め込まれている患者に対して、ステント血栓症と呼ばれているものを避けるための処置をする場合にも投与される。
【0003】
クロピドグレルは、P2Y12アンタゴニストであり、栓球上でADP受容体P2Y12を不可逆的に阻害し、それ故に、栓球の活性化及び凝集を阻害するので、血小板阻害剤又は栓球阻害剤として作用する。クロピドグレルは、多くの場合、もう一つの栓球阻害剤であるアセチルサリチル酸(ASA)と組み合わせて投与される。何故ならば、この処置により、脳卒中又は心筋梗塞のリスクが有意に低下するからである。
【0004】
しかし、多くのクロピドグレル処置患者では、栓球活性の阻害という所望の効果が達成されないことが、知られている。クロピドグレル治療に対するこの非応答性は、クロピドグレル抵抗性又は治療時血小板高反応性(high on−treatment platelet reactivity:HPR)と呼ばれている(非特許文献1)。この効果欠如の原因は不明である。
【0005】
クロピドグレル抵抗性患者のクロピドグレルによる処置は、これらの患者については、治療にも拘らず血栓イベントが再発するリスクが低下していないこと、そして、例えば栓球機能検査により、クロピドグレル抵抗性が診断され、治療が別の製剤に切り換えられるまでは、このリスクが持続することを、意味する。血栓イベントの再発からの最適な防御をクロピドグレル抵抗性患者に提供するには、該患者を最初から他の栓球阻害剤で処置する必要があるであろう。しかしながら、今までのところ、患者を実際にクロピドグレルで処置することなく、そして、効果の欠如を立証することなく、患者をクロピドグレル抵抗性であると診断することができる方法は知られていない。
【0006】
従って、恐らくクロピドグレル抵抗性であろうと考えられる患者を同定することを可能にする方法があることが望ましい。その方法は、クロピドグレルによる処置を実施する必要が全くなく、むしろ、最初から代替的栓球阻害剤を投与することが可能になるという利点を有するものであろう。それによって、その方法は、クロピドグレル抵抗性患者が、他の栓球阻害剤を用いて的を絞った方法で、最初から効果的な治療を受けることができるという利点を有するものであろう。そして、その結果、患者の血栓イベントの再発が起きるリスクが最初から低下するであろう。
【先行技術文献】
【非特許文献】
【0007】
【非特許文献1】Bonello,L.ら「Consensus and future directions on the definition of high on−treatment platelet reactivity to adenosine diphosphate」J Am Coll Cardiol.2010 Sep 14;56(12):919−33
【発明の概要】
【発明が解決しようとする課題】
【0008】
従って、本発明の目的は、栓球阻害剤による治療が計画されている患者について、クロピドグレルによる処置に対する非応答性のリスクを評価することを可能にする方法を提供することである。
【課題を解決するための手段】
【0009】
この目的は、患者がクロピドグレルを未だ服用していない時点において患者から得た試料中の栓球活性を決定することによって、達成される。増加した栓球活性を有する患者については、クロピドグレル抵抗性のリスクが増加していることが分かった。
【0010】
従って、本発明は、
a)患者がクロピドグレルを未だ服用していない時点において患者から得た試料中の栓球活性を測定するステップ、及び
b)測定された栓球活性を統計的に決定された判定限界と比較するステップ
を備えてなる、患者のクロピドグレル抵抗性のリスクを決定するための方法であって、
判定限界を超えて増加している栓球機能によって、その患者に関して、クロピドグレル抵抗性のリスクの増加が示される方法、を提供する。
【発明を実施するための形態】
【0011】
本発明の文脈において、用語「クロピドグレル」は、活性成分(S)−α−(2−クロロフェニル)−6,7−ジヒドロチエノ[3,2−c]ピリジン−5(4H)−酢酸メチル及びその薬学的に活性な塩、例えば、硫酸水素塩、ベシル酸塩(ベンゼンスルホン酸塩)又は塩酸塩を含む。
【0012】
用語「クロピドグレル抵抗性」は、クロピドグレル治療に対する患者の非応答性、又は、患者におけるクロピドグレル治療の効果の欠如を意味すると理解すべきである。クロピドグレルの投与に、所望の効果(即ち、測定可能な栓球活性阻害)が伴わない場合に、クロピドグレル抵抗性が存在する。
【0013】
クロピドグレルによる治療の適応症は、心血管状態又は血栓状態のような、血栓形成のリスクの増加に伴う状態、例えば心筋梗塞、不安定狭心症、虚血性脳卒中及び末梢動脈閉塞性疾患並びに冠動脈への血管支持体(ステント)の埋め込みである。
【0014】
従って、本発明の方法は、好ましくは、上述の状態の一つを患っている患者及び/又はステントの埋め込みが計画されている患者であって、それ故にクロピドグレルによる抗血栓治療を考慮すべき患者におけるクロピドグレル抵抗性のリスクを決定するのに、適している。
【0015】
栓球活性は、栓球機能検査により測定される。栓球機能の決定については、一連の異なる検査フォーマット、例えば様々な栓球凝集検査、が知られている。検査フォーマットに応じて、患者から得た全血試料中又は多血小板血漿試料(PRP試料)中の栓球機能を決定することができる。
【0016】
本発明の方法の一実施形態においては、栓球活性の測定は、患者の試料、好ましくは全血試料又はPRP試料、を少なくとも一つの栓球活性化因子、好ましくはADP(アデノシン5’−二リン酸)、コラーゲン、エピネフリン、アラキドン酸、リストセチン及びトロンビンからなる群から選択される少なくとも一つの栓球活性化因子、と接触させるステップを含む。用語「栓球活性化因子」は、栓球の凝集を誘起することができる物質を意味すると理解すべきである。好ましくは、試料を、栓球活性化因子の組合せ、好ましくはコラーゲンとADPとの組合せ(Col/ADP)又はコラーゲンとエピネフリンとの組合せ(Col/EPI)と、接触させる。
【0017】
本発明の方法の更なる一実施形態では、栓球活性の測定は、患者の試料を少なくとも一つの栓球活性化因子と接触させるだけではなく、患者の試料を、細胞内アデニル酸シクラーゼの活性化因子、好ましくはプロスタグランジンE1(PGE1)、フォルスコリン、プロスタグランジンI2、イロプロスト及びシカプロストからなる群から選択される細胞内アデニル酸シクラーゼの活性化因子、と接触させるステップをも、含む。
【0018】
次に、例えば、多血小板血漿における栓球凝集体形成の速度を測定するか、栓球の最大凝集塊を、例えば光透過凝集測定法(Born血小板凝集)によって、測定することにより、栓球活性の測定値を決定することができる。
【0019】
本発明の方法の特に好ましい一実施形態では、アスピリンの栓球阻害効果に対して非感受性である方法が、栓球活性を測定するために使用される。クロピドグレルによる治療が計画されている患者には、血栓形成のリスクを最小限に抑えるために、ほとんどの場合、栓球阻害剤アスピリンによる処置も行なわれる。栓球活性を測定するためにアスピリン非感受性の方法を使用することによってアスピリンの栓球阻害効果を排除すると、クロピドグレル抵抗性のリスクの決定がより正確になることが分かった。更に、P2Y(12)アンタゴニスト、例えばクロピドグレル、の栓球阻害効果の決定に対して感受性である方法を使用すると、クロピドグレル抵抗性のリスクの決定がより一層正確になることが分かった。そのような方法は、例えば欧州特許出願公開第1850134号のパラグラフ21に記載されている。
【0020】
本発明の方法の好ましい一実施形態では、栓球活性の測定が、全血において、流動条件下で、従って、高い剪断力の存在下で、行なわれる。そのような検査原理は、例えば、血小板機能アナライザーシステム(PFA−100(登録商標)、INNOVANCE(登録商標)PFA−200、シーメンス ヘルスケア ダイアグノスティクス プロダクツ ゲゼルシヤフト ミツト ベシユレンクテル ハフツング、マールブルク、ドイツ国)等において、実施される。
【0021】
比較的小さい動脈血管において優勢な流動条件及び剪断力をシミュレートするために、マイナス約40mbarの陰圧を専用カートリッジ内で生じさせ、試料リザーバー中に位置するクエン酸加全血が、約100〜200μmの直径を有する毛細管を貫流する。毛細管は、仕切り要素、例えば膜、によって閉じられた測定チャンバーに開口しており、この仕切り要素は、中央に毛細管開口部を有していて、陰圧ゆえに、血液がその中を流れる。ほとんどの場合、膜は、少なくとも開口部周囲の領域において、栓球凝集を誘起する1つ以上の活性化因子を含有するので、通過する血液は、開口部の領域において、凝集誘起物質と接触することになる。誘起された栓球の接着及び凝集の結果、開口部の領域において、血小板血栓(血栓)が形成され、それが膜開口部を閉じ、血流を停止させる。このシステムでは、典型的には、膜開口部の閉鎖までの時間が測定される。この「閉鎖時間」(CT)は、栓球の機能的効率と相関する。閉鎖時間により栓球機能を決定する方法において使用するためのカートリッジは、例えば、特許文献国際公開第97/34698号に記載されている。好ましいカートリッジは、コラーゲン(Col)と更にADP又はエピネフリン(EPI)のいずれか一方とで被覆された膜又はADPとプロスタグランジンE1(PGE1)とで被覆された膜を有する。様々な仕切り要素とその製造及び使用が、例えば特許文献欧州特許第716744号又は欧州特許出願公開第1850134号等に、記載されている。
【0022】
従って、本発明の方法の好ましい一実施形態において、栓球活性の測定は、試料、好ましくは全血試料、を毛細管に通し、続いて仕切り要素中の開口部に通すステップ、及び、仕切り要素中の開口部における血小板血栓の形成によって開口部が閉鎖されるまでの時間を測定するステップを含む。
【0023】
仕切り要素が、少なくとも一つの栓球活性化因子、例えば、ADP(アデノシン5’−二リン酸)、コラーゲン、エピネフリン、アラキドン酸、リストセチン及びトロンビンからなる群から選択されるものを含有するのが好ましい。仕切り要素が、栓球活性化因子の組合せ、特にコラーゲンとADPとの組合せ(Col/ADP)又はコラーゲンとエピネフリンとの組合せ(Col/EPI)を含有するのが、特に好ましい。場合により、仕切り要素は、更に、細胞内アデニル酸シクラーゼの活性化因子、好ましくはプロスタグランジンE1(PGE1)、フォルスコリン、プロスタグランジンI2、イロプロスト及びシカプロストからなる群から選択される細胞内アデニル酸シクラーゼの活性化因子、を含有してもよい。
【0024】
特に好ましくは、仕切り要素が、栓球活性化因子としてのADPと、プロスタグランジンE1(PGE1)、フォルスコリン、プロスタグランジンI2、イロプロスト及びシカプロストからなる群から選択される細胞内アデニル酸シクラーゼの活性化因子と、カルシウムイオンとを、含有する。そのような仕切り要素により、方法は、アスピリン非感受性になり、同時に、P2Y(12)アンタゴニスト、例えばクロピドグレル、の栓球阻害効果の決定に対しては感受性になる。
【0025】
本発明の方法の好ましい一実施形態では、栓球活性の測定が、以下の要素:
試料を保持するための保持チャンバー、
保持チャンバーから測定チャンバーへと試料が通される毛細管、
仕切り要素によって2つの区画に分割されている測定チャンバーであって、そのうちの第1区画が毛細管から試料を取り込む、測定チャンバー、及び
測定チャンバーを2つの区画に分割する仕切り要素であって、試料が第1区画から第2区画へと流れることができる開口部を有する仕切り要素、
を含有する装置を使用することを含む。
【0026】
このような装置の仕切り要素は、少なくとも一つの栓球活性化因子、好ましくは上述した栓球活性化因子の組合せの一つ、を含有する。仕切り要素は、更に、上述した細胞内アデニル酸シクラーゼ活性化因子の一つを、含有してもよい。
【0027】
どの検査原理を使って栓球活性を測定するかには関係なく、本発明では、患者から得た試料において測定された栓球活性を、統計的に決定された判定限界(カットオフ値とも呼ばれている)と、比較する。
【0028】
判定限界の決定には、例えば、受信者動作特性曲線(ROC曲線)分析の統計手法を使用することが可能である。この手法を使えば、同じ患者についてクロピドグレルの摂取前と摂取後の両方で栓球機能を決定したデータに基づいて、クロピドグレル抵抗性のリスクが増加している患者をクロピドグレル抵抗性のリスクが明確に低い患者から区別することを可能にする、2クラス分類のための最適の判定限界を算出することが可能である。この目的のためには、少なくとも60人の患者、更に望ましくは120人以上の患者、から得た結果を、計算に含めるべきである。
【0029】
「クロピドグレル抵抗性のリスクの増加」とは、ある患者においてクロピドグレルが効果を有さない蓋然性が約2倍〜4倍増加していることを意味し、リスクが増加している場合は、患者の半数超がクロピドグレルに対して非応答性であると、理解すべきである。低リスクの場合、この数は、患者のおよそ4分の1〜5分の1でしかない。
【図面の簡単な説明】
【0030】
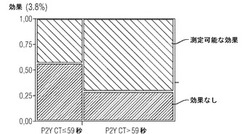
【図1】クロピドグレル摂取前の3.8%濃度クエン酸加全血を使用した場合において、INNOVANCE PFA P2Y閉鎖時間(「P2Y CT」)が59秒以下及び59秒を超えるときの、クロピドグレルの投与に対する患者の応答(「効果」)の分布に関するモザイクプロットである。タイルの幅と高さは、総個体数に対する2つのクラスの相対的比率を示す。
【図2】クロピドグレル摂取前の3.2%濃度クエン酸加全血を使用した場合において、INNOVANCE PFA P2Y閉鎖時間(「P2Y CT」)が60秒以下及び60秒を超えるときの、クロピドグレルの投与に対するASA治療を受けている患者の応答(「効果」)の分布に関するモザイクプロットである。タイルの幅と高さは、総個体数に対する2つのクラスの相対的比率を示す。
【実施例】
【0031】
試験計画
ステントの外科的挿入のために選ばれた心血管状態を患っている143人の患者から血液を採取した。ここで、血液は、この術式の通例どおり、300mg又は600mgのクロピドグレル(初回負荷量)を服用する前及び服用の6〜24時間後に採取した。
【0032】
患者は、固有の栓球欠陥によって、VWF欠陥(VWD)によって、又はアセチルサリチル酸以外の栓球凝集阻害剤の摂取によって、引き起こされる栓球機能障害を示す医学的記録及び検査結果のいずれも持っていなかった。大半の患者は、血液採取の時点で既に、毎日81mg又は100mgのアセチルサリチル酸(ASA)を服用中であった。
【0033】
患者試料中の栓球活性は、血小板機能アナライザーシステム(PFA−100(登録商標)、シーメンス ヘルスケア ダイアグノスティクス プロダクツ ゲゼルシヤフト ミツト ベシユレンクテル ハフツング、マールブルク、ドイツ国)を使って決定した。
【0034】
PFAシステムを使って、流動条件下で、従って高い剪断力の存在下で、全血試料における一次止血を測定する。このシステムでは、栓球機能の尺度として、専用カートリッジにおける膜開口部の閉鎖までの時間(閉鎖時間)が測定される。閉鎖時間は、栓球機能に逆比例する。即ち、閉鎖時間が長いほど、栓球活性は低い。
【0035】
異なるタイプの膜を有するカートリッジにより、栓球の異なる機能を決定することが可能になる。コラーゲン(Col)及びADPの被覆を有する膜(Col/ADP;アスピリン非感受性)又はコラーゲン(Col)及びエピネフリン(EPI)の被覆を有する膜(Col/EPI;アスピリン感受性)、又はADP、プロスタグランジンE1及びカルシウムイオンの被覆を有する膜(INNOVANCE(登録商標)PFA P2Y;アスピリン非感受性でP2Y(12)アンタゴニストの栓球阻害効果に対して感受性)が設けられたカートリッジを使用した。
【0036】
3つの異なるタイプのカートリッジについて、正常な栓球機能と低下した栓球機能との弁別を可能にする閉鎖時間(CT)(単位:秒)の閾値(カットオフ値)を、前もって決定しておいた。栓球機能が低下した試料は、カットオフ値を上回る、延長された閉鎖時間を有する。クロピドグレルの投与後にカートリッジに特異的なカットオフ値を上回る閉鎖時間を有する試料は、クロピドグレル治療の所望の効果、即ち、栓球活性の測定可能な阻害を示した。対照的に、クロピドグレルの投与後にカートリッジに特異的なカットオフ値を下回る閉鎖時間を有する試料は、クロピドグレル治療の効果の欠如、即ち、クロピドグレル抵抗性(又は治療時血小板高反応性)を示した。
【0037】
正常な栓球機能を低下した栓球機能から弁別するための、異なるタイプのカートリッジについての閉鎖時間のカットオフ値(単位:秒)を、表1に示す。
【表1】

【0038】
INNOVANCE PFA P2Yカートリッジを用いた閉鎖時間測定は、3.2%及び3.8%クエン酸加全血の両方を使って行なったが、Col/EPI及びCol/ADP閉鎖時間は、3.2%クエン酸加全血についてのみ測定した。
【0039】
全体的にみて、クロピドグレル摂取後に行なわれるINNOVANCE PFA P2Yカートリッジを使った閉鎖時間測定により、調査した患者の45.8%(3.2%クエン酸加全血について)又は37.5%(3.8%クエン酸加全血について)が、クロピドグレル抵抗性であることが分かった。
【0040】
クロピドグレル治療によって何らかの測定可能な栓球活性阻害を達成することが可能でなく、従ってクロピドグレル抵抗性に悩まされている患者群は、クロピドグレル摂取前に既に、クロピドグレル治療に応答する他方の患者群と比較して、有意に増加している栓球機能を(短い閉鎖時間の形で)示していることが、観察された。
【0041】
このように、クロピドグレル摂取前に異常に増加している栓球機能を決定することにより、クロピドグレル抵抗性のリスクの増加を予測することが可能になる。
【0042】
判定限界の決定
クロピドグレル摂取前に、異常に増加している栓球機能を正常な栓球機能から、弁別することができ、従ってクロピドグレル抵抗性のリスクの増加を決定することができるように、143人の患者から得た結果を、最適判定限界の計算に使用した。各タイプのカートリッジについて、そして、また、INNOVANCE PFA P2Yカートリッジの場合は、更に、使用した各クエン酸濃度について、個別の判定限界を算出した。ROC曲線分析に使用する分類変数は、対応するクエン酸加全血におけるクロピドグレルに対する応答とした。
【0043】
【表2】

【0044】
短い閉鎖時間の予測値
クロピドグレル摂取前の3.8%クエン酸加全血の場合の或る患者のINNOVANCE PFA P2Y閉鎖時間が59秒以下であるとすると、この患者がクロピドグレルに応答しない相対リスクは、59秒を上回る閉鎖時間を有する患者のそれより98%高い(相対リスク:1.98;p<0.002;フィッシャーの正確確率検定)。結果の分布を図1に示す。
【0045】
クロピドグレル摂取前の3.2%クエン酸加全血の場合の或る患者のINNOVANCE PFA P2Y閉鎖時間が60秒以下であるとすると、この患者がクロピドグレルに応答しない相対リスクは、60秒を上回る閉鎖時間を有する患者のそれより61%高い(相対リスク:1.61;p<0.02;フィッシャーの正確確率検定)。ASA治療を受けている患者からの結果の分布を図2に示す。
【0046】
クロピドグレル摂取前の3.2%クエン酸加全血の場合の或る患者のCol/EPI閉鎖時間が140秒以下であるとすると、この患者がクロピドグレルに応答しない相対リスクは、140秒を上回る閉鎖時間を有する患者のそれより78%高い(相対リスク:1.78;p<0.004;フィッシャーの正確確率検定)。
【0047】
興味深いことに、クロピドグレル摂取後の3.8%クエン酸加全血の場合のINNOVANCE PFA P2Y測定を行なった場合、3.2%クエン酸加全血についてクロピドグレル摂取前に測定されたCol/EPI閉鎖時間が140秒以下である場合には、患者がクロピドグレルに応答しない相対リスクは164%も高い(相対リスク:2.64;p<0.0001;フィッシャーの正確確率検定)。
【0048】
ASA治療を受けている或る患者のCol/ADP閉鎖時間が、クロピドグレル摂取前の3.2%クエン酸加全血において、91秒以下であるとすると、この患者がクロピドグレルに応答しない相対リスクは、91秒を上回る閉鎖時間を有する患者のそれより47%高い(相対リスク:1.47;p=0.06;フィッシャーの正確確率検定)。
【技術分野】
【0001】
本発明は、個別化治療を目標とする心血管状態及び血栓状態の診断の分野の発明である。特に、本発明は、クロピドグレルによる治療の恩恵が得られない可能性が高い患者を同定するための方法に関する。
【背景技術】
【0002】
クロピドグレル(商標名:Plavix(登録商標)、Iscover(登録商標))は、血液凝固を阻害する薬物であり、心筋梗塞や脳卒中等の急性心血管状態又は血栓状態を患っている患者又はそのようなイベントを患ったことがあり、再発性血栓イベントのリスクを低下させるために予防的に処置を継続しなければならない患者のルーチン処置に、ますます、多用されている。クロピドグレルは、例えば、冠血管にステントが埋め込まれている患者に対して、ステント血栓症と呼ばれているものを避けるための処置をする場合にも投与される。
【0003】
クロピドグレルは、P2Y12アンタゴニストであり、栓球上でADP受容体P2Y12を不可逆的に阻害し、それ故に、栓球の活性化及び凝集を阻害するので、血小板阻害剤又は栓球阻害剤として作用する。クロピドグレルは、多くの場合、もう一つの栓球阻害剤であるアセチルサリチル酸(ASA)と組み合わせて投与される。何故ならば、この処置により、脳卒中又は心筋梗塞のリスクが有意に低下するからである。
【0004】
しかし、多くのクロピドグレル処置患者では、栓球活性の阻害という所望の効果が達成されないことが、知られている。クロピドグレル治療に対するこの非応答性は、クロピドグレル抵抗性又は治療時血小板高反応性(high on−treatment platelet reactivity:HPR)と呼ばれている(非特許文献1)。この効果欠如の原因は不明である。
【0005】
クロピドグレル抵抗性患者のクロピドグレルによる処置は、これらの患者については、治療にも拘らず血栓イベントが再発するリスクが低下していないこと、そして、例えば栓球機能検査により、クロピドグレル抵抗性が診断され、治療が別の製剤に切り換えられるまでは、このリスクが持続することを、意味する。血栓イベントの再発からの最適な防御をクロピドグレル抵抗性患者に提供するには、該患者を最初から他の栓球阻害剤で処置する必要があるであろう。しかしながら、今までのところ、患者を実際にクロピドグレルで処置することなく、そして、効果の欠如を立証することなく、患者をクロピドグレル抵抗性であると診断することができる方法は知られていない。
【0006】
従って、恐らくクロピドグレル抵抗性であろうと考えられる患者を同定することを可能にする方法があることが望ましい。その方法は、クロピドグレルによる処置を実施する必要が全くなく、むしろ、最初から代替的栓球阻害剤を投与することが可能になるという利点を有するものであろう。それによって、その方法は、クロピドグレル抵抗性患者が、他の栓球阻害剤を用いて的を絞った方法で、最初から効果的な治療を受けることができるという利点を有するものであろう。そして、その結果、患者の血栓イベントの再発が起きるリスクが最初から低下するであろう。
【先行技術文献】
【非特許文献】
【0007】
【非特許文献1】Bonello,L.ら「Consensus and future directions on the definition of high on−treatment platelet reactivity to adenosine diphosphate」J Am Coll Cardiol.2010 Sep 14;56(12):919−33
【発明の概要】
【発明が解決しようとする課題】
【0008】
従って、本発明の目的は、栓球阻害剤による治療が計画されている患者について、クロピドグレルによる処置に対する非応答性のリスクを評価することを可能にする方法を提供することである。
【課題を解決するための手段】
【0009】
この目的は、患者がクロピドグレルを未だ服用していない時点において患者から得た試料中の栓球活性を決定することによって、達成される。増加した栓球活性を有する患者については、クロピドグレル抵抗性のリスクが増加していることが分かった。
【0010】
従って、本発明は、
a)患者がクロピドグレルを未だ服用していない時点において患者から得た試料中の栓球活性を測定するステップ、及び
b)測定された栓球活性を統計的に決定された判定限界と比較するステップ
を備えてなる、患者のクロピドグレル抵抗性のリスクを決定するための方法であって、
判定限界を超えて増加している栓球機能によって、その患者に関して、クロピドグレル抵抗性のリスクの増加が示される方法、を提供する。
【発明を実施するための形態】
【0011】
本発明の文脈において、用語「クロピドグレル」は、活性成分(S)−α−(2−クロロフェニル)−6,7−ジヒドロチエノ[3,2−c]ピリジン−5(4H)−酢酸メチル及びその薬学的に活性な塩、例えば、硫酸水素塩、ベシル酸塩(ベンゼンスルホン酸塩)又は塩酸塩を含む。
【0012】
用語「クロピドグレル抵抗性」は、クロピドグレル治療に対する患者の非応答性、又は、患者におけるクロピドグレル治療の効果の欠如を意味すると理解すべきである。クロピドグレルの投与に、所望の効果(即ち、測定可能な栓球活性阻害)が伴わない場合に、クロピドグレル抵抗性が存在する。
【0013】
クロピドグレルによる治療の適応症は、心血管状態又は血栓状態のような、血栓形成のリスクの増加に伴う状態、例えば心筋梗塞、不安定狭心症、虚血性脳卒中及び末梢動脈閉塞性疾患並びに冠動脈への血管支持体(ステント)の埋め込みである。
【0014】
従って、本発明の方法は、好ましくは、上述の状態の一つを患っている患者及び/又はステントの埋め込みが計画されている患者であって、それ故にクロピドグレルによる抗血栓治療を考慮すべき患者におけるクロピドグレル抵抗性のリスクを決定するのに、適している。
【0015】
栓球活性は、栓球機能検査により測定される。栓球機能の決定については、一連の異なる検査フォーマット、例えば様々な栓球凝集検査、が知られている。検査フォーマットに応じて、患者から得た全血試料中又は多血小板血漿試料(PRP試料)中の栓球機能を決定することができる。
【0016】
本発明の方法の一実施形態においては、栓球活性の測定は、患者の試料、好ましくは全血試料又はPRP試料、を少なくとも一つの栓球活性化因子、好ましくはADP(アデノシン5’−二リン酸)、コラーゲン、エピネフリン、アラキドン酸、リストセチン及びトロンビンからなる群から選択される少なくとも一つの栓球活性化因子、と接触させるステップを含む。用語「栓球活性化因子」は、栓球の凝集を誘起することができる物質を意味すると理解すべきである。好ましくは、試料を、栓球活性化因子の組合せ、好ましくはコラーゲンとADPとの組合せ(Col/ADP)又はコラーゲンとエピネフリンとの組合せ(Col/EPI)と、接触させる。
【0017】
本発明の方法の更なる一実施形態では、栓球活性の測定は、患者の試料を少なくとも一つの栓球活性化因子と接触させるだけではなく、患者の試料を、細胞内アデニル酸シクラーゼの活性化因子、好ましくはプロスタグランジンE1(PGE1)、フォルスコリン、プロスタグランジンI2、イロプロスト及びシカプロストからなる群から選択される細胞内アデニル酸シクラーゼの活性化因子、と接触させるステップをも、含む。
【0018】
次に、例えば、多血小板血漿における栓球凝集体形成の速度を測定するか、栓球の最大凝集塊を、例えば光透過凝集測定法(Born血小板凝集)によって、測定することにより、栓球活性の測定値を決定することができる。
【0019】
本発明の方法の特に好ましい一実施形態では、アスピリンの栓球阻害効果に対して非感受性である方法が、栓球活性を測定するために使用される。クロピドグレルによる治療が計画されている患者には、血栓形成のリスクを最小限に抑えるために、ほとんどの場合、栓球阻害剤アスピリンによる処置も行なわれる。栓球活性を測定するためにアスピリン非感受性の方法を使用することによってアスピリンの栓球阻害効果を排除すると、クロピドグレル抵抗性のリスクの決定がより正確になることが分かった。更に、P2Y(12)アンタゴニスト、例えばクロピドグレル、の栓球阻害効果の決定に対して感受性である方法を使用すると、クロピドグレル抵抗性のリスクの決定がより一層正確になることが分かった。そのような方法は、例えば欧州特許出願公開第1850134号のパラグラフ21に記載されている。
【0020】
本発明の方法の好ましい一実施形態では、栓球活性の測定が、全血において、流動条件下で、従って、高い剪断力の存在下で、行なわれる。そのような検査原理は、例えば、血小板機能アナライザーシステム(PFA−100(登録商標)、INNOVANCE(登録商標)PFA−200、シーメンス ヘルスケア ダイアグノスティクス プロダクツ ゲゼルシヤフト ミツト ベシユレンクテル ハフツング、マールブルク、ドイツ国)等において、実施される。
【0021】
比較的小さい動脈血管において優勢な流動条件及び剪断力をシミュレートするために、マイナス約40mbarの陰圧を専用カートリッジ内で生じさせ、試料リザーバー中に位置するクエン酸加全血が、約100〜200μmの直径を有する毛細管を貫流する。毛細管は、仕切り要素、例えば膜、によって閉じられた測定チャンバーに開口しており、この仕切り要素は、中央に毛細管開口部を有していて、陰圧ゆえに、血液がその中を流れる。ほとんどの場合、膜は、少なくとも開口部周囲の領域において、栓球凝集を誘起する1つ以上の活性化因子を含有するので、通過する血液は、開口部の領域において、凝集誘起物質と接触することになる。誘起された栓球の接着及び凝集の結果、開口部の領域において、血小板血栓(血栓)が形成され、それが膜開口部を閉じ、血流を停止させる。このシステムでは、典型的には、膜開口部の閉鎖までの時間が測定される。この「閉鎖時間」(CT)は、栓球の機能的効率と相関する。閉鎖時間により栓球機能を決定する方法において使用するためのカートリッジは、例えば、特許文献国際公開第97/34698号に記載されている。好ましいカートリッジは、コラーゲン(Col)と更にADP又はエピネフリン(EPI)のいずれか一方とで被覆された膜又はADPとプロスタグランジンE1(PGE1)とで被覆された膜を有する。様々な仕切り要素とその製造及び使用が、例えば特許文献欧州特許第716744号又は欧州特許出願公開第1850134号等に、記載されている。
【0022】
従って、本発明の方法の好ましい一実施形態において、栓球活性の測定は、試料、好ましくは全血試料、を毛細管に通し、続いて仕切り要素中の開口部に通すステップ、及び、仕切り要素中の開口部における血小板血栓の形成によって開口部が閉鎖されるまでの時間を測定するステップを含む。
【0023】
仕切り要素が、少なくとも一つの栓球活性化因子、例えば、ADP(アデノシン5’−二リン酸)、コラーゲン、エピネフリン、アラキドン酸、リストセチン及びトロンビンからなる群から選択されるものを含有するのが好ましい。仕切り要素が、栓球活性化因子の組合せ、特にコラーゲンとADPとの組合せ(Col/ADP)又はコラーゲンとエピネフリンとの組合せ(Col/EPI)を含有するのが、特に好ましい。場合により、仕切り要素は、更に、細胞内アデニル酸シクラーゼの活性化因子、好ましくはプロスタグランジンE1(PGE1)、フォルスコリン、プロスタグランジンI2、イロプロスト及びシカプロストからなる群から選択される細胞内アデニル酸シクラーゼの活性化因子、を含有してもよい。
【0024】
特に好ましくは、仕切り要素が、栓球活性化因子としてのADPと、プロスタグランジンE1(PGE1)、フォルスコリン、プロスタグランジンI2、イロプロスト及びシカプロストからなる群から選択される細胞内アデニル酸シクラーゼの活性化因子と、カルシウムイオンとを、含有する。そのような仕切り要素により、方法は、アスピリン非感受性になり、同時に、P2Y(12)アンタゴニスト、例えばクロピドグレル、の栓球阻害効果の決定に対しては感受性になる。
【0025】
本発明の方法の好ましい一実施形態では、栓球活性の測定が、以下の要素:
試料を保持するための保持チャンバー、
保持チャンバーから測定チャンバーへと試料が通される毛細管、
仕切り要素によって2つの区画に分割されている測定チャンバーであって、そのうちの第1区画が毛細管から試料を取り込む、測定チャンバー、及び
測定チャンバーを2つの区画に分割する仕切り要素であって、試料が第1区画から第2区画へと流れることができる開口部を有する仕切り要素、
を含有する装置を使用することを含む。
【0026】
このような装置の仕切り要素は、少なくとも一つの栓球活性化因子、好ましくは上述した栓球活性化因子の組合せの一つ、を含有する。仕切り要素は、更に、上述した細胞内アデニル酸シクラーゼ活性化因子の一つを、含有してもよい。
【0027】
どの検査原理を使って栓球活性を測定するかには関係なく、本発明では、患者から得た試料において測定された栓球活性を、統計的に決定された判定限界(カットオフ値とも呼ばれている)と、比較する。
【0028】
判定限界の決定には、例えば、受信者動作特性曲線(ROC曲線)分析の統計手法を使用することが可能である。この手法を使えば、同じ患者についてクロピドグレルの摂取前と摂取後の両方で栓球機能を決定したデータに基づいて、クロピドグレル抵抗性のリスクが増加している患者をクロピドグレル抵抗性のリスクが明確に低い患者から区別することを可能にする、2クラス分類のための最適の判定限界を算出することが可能である。この目的のためには、少なくとも60人の患者、更に望ましくは120人以上の患者、から得た結果を、計算に含めるべきである。
【0029】
「クロピドグレル抵抗性のリスクの増加」とは、ある患者においてクロピドグレルが効果を有さない蓋然性が約2倍〜4倍増加していることを意味し、リスクが増加している場合は、患者の半数超がクロピドグレルに対して非応答性であると、理解すべきである。低リスクの場合、この数は、患者のおよそ4分の1〜5分の1でしかない。
【図面の簡単な説明】
【0030】
【図1】クロピドグレル摂取前の3.8%濃度クエン酸加全血を使用した場合において、INNOVANCE PFA P2Y閉鎖時間(「P2Y CT」)が59秒以下及び59秒を超えるときの、クロピドグレルの投与に対する患者の応答(「効果」)の分布に関するモザイクプロットである。タイルの幅と高さは、総個体数に対する2つのクラスの相対的比率を示す。
【図2】クロピドグレル摂取前の3.2%濃度クエン酸加全血を使用した場合において、INNOVANCE PFA P2Y閉鎖時間(「P2Y CT」)が60秒以下及び60秒を超えるときの、クロピドグレルの投与に対するASA治療を受けている患者の応答(「効果」)の分布に関するモザイクプロットである。タイルの幅と高さは、総個体数に対する2つのクラスの相対的比率を示す。
【実施例】
【0031】
試験計画
ステントの外科的挿入のために選ばれた心血管状態を患っている143人の患者から血液を採取した。ここで、血液は、この術式の通例どおり、300mg又は600mgのクロピドグレル(初回負荷量)を服用する前及び服用の6〜24時間後に採取した。
【0032】
患者は、固有の栓球欠陥によって、VWF欠陥(VWD)によって、又はアセチルサリチル酸以外の栓球凝集阻害剤の摂取によって、引き起こされる栓球機能障害を示す医学的記録及び検査結果のいずれも持っていなかった。大半の患者は、血液採取の時点で既に、毎日81mg又は100mgのアセチルサリチル酸(ASA)を服用中であった。
【0033】
患者試料中の栓球活性は、血小板機能アナライザーシステム(PFA−100(登録商標)、シーメンス ヘルスケア ダイアグノスティクス プロダクツ ゲゼルシヤフト ミツト ベシユレンクテル ハフツング、マールブルク、ドイツ国)を使って決定した。
【0034】
PFAシステムを使って、流動条件下で、従って高い剪断力の存在下で、全血試料における一次止血を測定する。このシステムでは、栓球機能の尺度として、専用カートリッジにおける膜開口部の閉鎖までの時間(閉鎖時間)が測定される。閉鎖時間は、栓球機能に逆比例する。即ち、閉鎖時間が長いほど、栓球活性は低い。
【0035】
異なるタイプの膜を有するカートリッジにより、栓球の異なる機能を決定することが可能になる。コラーゲン(Col)及びADPの被覆を有する膜(Col/ADP;アスピリン非感受性)又はコラーゲン(Col)及びエピネフリン(EPI)の被覆を有する膜(Col/EPI;アスピリン感受性)、又はADP、プロスタグランジンE1及びカルシウムイオンの被覆を有する膜(INNOVANCE(登録商標)PFA P2Y;アスピリン非感受性でP2Y(12)アンタゴニストの栓球阻害効果に対して感受性)が設けられたカートリッジを使用した。
【0036】
3つの異なるタイプのカートリッジについて、正常な栓球機能と低下した栓球機能との弁別を可能にする閉鎖時間(CT)(単位:秒)の閾値(カットオフ値)を、前もって決定しておいた。栓球機能が低下した試料は、カットオフ値を上回る、延長された閉鎖時間を有する。クロピドグレルの投与後にカートリッジに特異的なカットオフ値を上回る閉鎖時間を有する試料は、クロピドグレル治療の所望の効果、即ち、栓球活性の測定可能な阻害を示した。対照的に、クロピドグレルの投与後にカートリッジに特異的なカットオフ値を下回る閉鎖時間を有する試料は、クロピドグレル治療の効果の欠如、即ち、クロピドグレル抵抗性(又は治療時血小板高反応性)を示した。
【0037】
正常な栓球機能を低下した栓球機能から弁別するための、異なるタイプのカートリッジについての閉鎖時間のカットオフ値(単位:秒)を、表1に示す。
【表1】

【0038】
INNOVANCE PFA P2Yカートリッジを用いた閉鎖時間測定は、3.2%及び3.8%クエン酸加全血の両方を使って行なったが、Col/EPI及びCol/ADP閉鎖時間は、3.2%クエン酸加全血についてのみ測定した。
【0039】
全体的にみて、クロピドグレル摂取後に行なわれるINNOVANCE PFA P2Yカートリッジを使った閉鎖時間測定により、調査した患者の45.8%(3.2%クエン酸加全血について)又は37.5%(3.8%クエン酸加全血について)が、クロピドグレル抵抗性であることが分かった。
【0040】
クロピドグレル治療によって何らかの測定可能な栓球活性阻害を達成することが可能でなく、従ってクロピドグレル抵抗性に悩まされている患者群は、クロピドグレル摂取前に既に、クロピドグレル治療に応答する他方の患者群と比較して、有意に増加している栓球機能を(短い閉鎖時間の形で)示していることが、観察された。
【0041】
このように、クロピドグレル摂取前に異常に増加している栓球機能を決定することにより、クロピドグレル抵抗性のリスクの増加を予測することが可能になる。
【0042】
判定限界の決定
クロピドグレル摂取前に、異常に増加している栓球機能を正常な栓球機能から、弁別することができ、従ってクロピドグレル抵抗性のリスクの増加を決定することができるように、143人の患者から得た結果を、最適判定限界の計算に使用した。各タイプのカートリッジについて、そして、また、INNOVANCE PFA P2Yカートリッジの場合は、更に、使用した各クエン酸濃度について、個別の判定限界を算出した。ROC曲線分析に使用する分類変数は、対応するクエン酸加全血におけるクロピドグレルに対する応答とした。
【0043】
【表2】

【0044】
短い閉鎖時間の予測値
クロピドグレル摂取前の3.8%クエン酸加全血の場合の或る患者のINNOVANCE PFA P2Y閉鎖時間が59秒以下であるとすると、この患者がクロピドグレルに応答しない相対リスクは、59秒を上回る閉鎖時間を有する患者のそれより98%高い(相対リスク:1.98;p<0.002;フィッシャーの正確確率検定)。結果の分布を図1に示す。
【0045】
クロピドグレル摂取前の3.2%クエン酸加全血の場合の或る患者のINNOVANCE PFA P2Y閉鎖時間が60秒以下であるとすると、この患者がクロピドグレルに応答しない相対リスクは、60秒を上回る閉鎖時間を有する患者のそれより61%高い(相対リスク:1.61;p<0.02;フィッシャーの正確確率検定)。ASA治療を受けている患者からの結果の分布を図2に示す。
【0046】
クロピドグレル摂取前の3.2%クエン酸加全血の場合の或る患者のCol/EPI閉鎖時間が140秒以下であるとすると、この患者がクロピドグレルに応答しない相対リスクは、140秒を上回る閉鎖時間を有する患者のそれより78%高い(相対リスク:1.78;p<0.004;フィッシャーの正確確率検定)。
【0047】
興味深いことに、クロピドグレル摂取後の3.8%クエン酸加全血の場合のINNOVANCE PFA P2Y測定を行なった場合、3.2%クエン酸加全血についてクロピドグレル摂取前に測定されたCol/EPI閉鎖時間が140秒以下である場合には、患者がクロピドグレルに応答しない相対リスクは164%も高い(相対リスク:2.64;p<0.0001;フィッシャーの正確確率検定)。
【0048】
ASA治療を受けている或る患者のCol/ADP閉鎖時間が、クロピドグレル摂取前の3.2%クエン酸加全血において、91秒以下であるとすると、この患者がクロピドグレルに応答しない相対リスクは、91秒を上回る閉鎖時間を有する患者のそれより47%高い(相対リスク:1.47;p=0.06;フィッシャーの正確確率検定)。
【特許請求の範囲】
【請求項1】
a)患者がクロピドグレルを未だ服用していない時点において患者から得た試料中の栓球活性を測定するステップ、及び
b)測定された栓球活性を、統計的に決定された判定限界と、比較するステップ
を備えてなる、患者のクロピドグレル抵抗性のリスクを決定するための方法であって、
判定限界を超えて増加している栓球機能によって、その患者に関して、クロピドグレル抵抗性のリスクの増加が示される方法。
【請求項2】
患者が心血管状態若しくは血栓状態を患っているか、ステント埋め込みのために選択されているかの、いずれか一方又は両方である、請求項1に記載の方法。
【請求項3】
ステップa)における栓球活性の測定が、
試料を少なくとも一つの栓球活性化因子と接触させるステップ
を含む、請求項1又は2に記載の方法。
【請求項4】
試料を栓球活性化因子の組合せと接触させる、請求項3に記載の方法。
【請求項5】
試料を更に細胞内アデニル酸シクラーゼの活性化因子と接触させる、請求項3又は4に記載の方法。
【請求項6】
ステップa)における栓球活性の測定が、
試料を毛細管に通し、続いて仕切り要素中の開口部に通すステップ、及び
仕切り要素中の開口部における血小板血栓の形成によって開口部が閉鎖されるまでの時間を測定するステップ
を含む、請求項1〜5のいずれか1項に記載の方法。
【請求項7】
仕切り要素が少なくとも一つの栓球活性化因子を含有する、請求項6に記載の方法。
【請求項8】
ステップa)における栓球活性の測定が、アスピリンの栓球阻害効果に対して非感受性である方法を使用する、請求項1に記載の方法。
【請求項9】
前記方法が更にP2Y(12)アンタゴニストの栓球阻害効果に対して感受性である、請求項8に記載の方法。
【請求項10】
試料が全血又は多血小板血漿である、請求項1〜9のいずれか1項に記載の方法。
【請求項11】
ステップa)における栓球活性の測定が、以下の要素:
試料を保持するための保持チャンバー、
保持チャンバーから測定チャンバーへと試料が通される毛細管、
仕切り要素によって2つの区画に分割されている測定チャンバーであって、そのうちの第1区画が毛細管から試料を取り込む、測定チャンバー、及び
測定チャンバーを2つの区画に分割する仕切り要素であって、試料が第1区画から第2区画へと流れることができる開口部を有する仕切り要素、
を含有する装置を使用することを含み、
仕切り要素が少なくとも一つの栓球活性化因子を含有する、請求項1〜10のいずれか1項に記載の方法。
【請求項12】
仕切り要素が、栓球活性化因子としてのADPと、プロスタグランジンE1(PGE1)、フォルスコリン、プロスタグランジンI2、イロプロスト及びシカプロストからなる群から選択される細胞内アデニル酸シクラーゼの活性化因子と、カルシウムイオンとを含有する、請求項11に記載の方法。
【請求項1】
a)患者がクロピドグレルを未だ服用していない時点において患者から得た試料中の栓球活性を測定するステップ、及び
b)測定された栓球活性を、統計的に決定された判定限界と、比較するステップ
を備えてなる、患者のクロピドグレル抵抗性のリスクを決定するための方法であって、
判定限界を超えて増加している栓球機能によって、その患者に関して、クロピドグレル抵抗性のリスクの増加が示される方法。
【請求項2】
患者が心血管状態若しくは血栓状態を患っているか、ステント埋め込みのために選択されているかの、いずれか一方又は両方である、請求項1に記載の方法。
【請求項3】
ステップa)における栓球活性の測定が、
試料を少なくとも一つの栓球活性化因子と接触させるステップ
を含む、請求項1又は2に記載の方法。
【請求項4】
試料を栓球活性化因子の組合せと接触させる、請求項3に記載の方法。
【請求項5】
試料を更に細胞内アデニル酸シクラーゼの活性化因子と接触させる、請求項3又は4に記載の方法。
【請求項6】
ステップa)における栓球活性の測定が、
試料を毛細管に通し、続いて仕切り要素中の開口部に通すステップ、及び
仕切り要素中の開口部における血小板血栓の形成によって開口部が閉鎖されるまでの時間を測定するステップ
を含む、請求項1〜5のいずれか1項に記載の方法。
【請求項7】
仕切り要素が少なくとも一つの栓球活性化因子を含有する、請求項6に記載の方法。
【請求項8】
ステップa)における栓球活性の測定が、アスピリンの栓球阻害効果に対して非感受性である方法を使用する、請求項1に記載の方法。
【請求項9】
前記方法が更にP2Y(12)アンタゴニストの栓球阻害効果に対して感受性である、請求項8に記載の方法。
【請求項10】
試料が全血又は多血小板血漿である、請求項1〜9のいずれか1項に記載の方法。
【請求項11】
ステップa)における栓球活性の測定が、以下の要素:
試料を保持するための保持チャンバー、
保持チャンバーから測定チャンバーへと試料が通される毛細管、
仕切り要素によって2つの区画に分割されている測定チャンバーであって、そのうちの第1区画が毛細管から試料を取り込む、測定チャンバー、及び
測定チャンバーを2つの区画に分割する仕切り要素であって、試料が第1区画から第2区画へと流れることができる開口部を有する仕切り要素、
を含有する装置を使用することを含み、
仕切り要素が少なくとも一つの栓球活性化因子を含有する、請求項1〜10のいずれか1項に記載の方法。
【請求項12】
仕切り要素が、栓球活性化因子としてのADPと、プロスタグランジンE1(PGE1)、フォルスコリン、プロスタグランジンI2、イロプロスト及びシカプロストからなる群から選択される細胞内アデニル酸シクラーゼの活性化因子と、カルシウムイオンとを含有する、請求項11に記載の方法。
【図1】


【図2】




【図2】


【公開番号】特開2012−242380(P2012−242380A)
【公開日】平成24年12月10日(2012.12.10)
【国際特許分類】
【出願番号】特願2012−107777(P2012−107777)
【出願日】平成24年5月9日(2012.5.9)
【出願人】(510259921)シーメンス ヘルスケア ダイアグノスティクス プロダクツ ゲゼルシヤフト ミツト ベシユレンクテル ハフツング (11)
【Fターム(参考)】
【公開日】平成24年12月10日(2012.12.10)
【国際特許分類】
【出願日】平成24年5月9日(2012.5.9)
【出願人】(510259921)シーメンス ヘルスケア ダイアグノスティクス プロダクツ ゲゼルシヤフト ミツト ベシユレンクテル ハフツング (11)
【Fターム(参考)】
[ Back to top ]

