グラム陽性細菌用抗菌剤及び抗菌活性増強剤
【課題】抗生物質耐性菌の出現に対抗し得る、新規な抗菌手段を提供すること。
【解決手段】クマザサ葉抽出物を有効成分として含むグラム陽性細菌用抗菌剤、該抗菌剤と特定の抗生物質との組み合わせを含むグラム陽性細菌用抗菌剤、並びにクマザサ葉抽出物を有効成分として含む抗菌活性増強剤を提供した。
【効果】本発明の抗菌剤は、従来院内感染等で問題となっているMRSAやバンコマイシン耐性菌に対しても抗菌活性を示す。また、特定の抗生物質の抗菌活性を増強する作用も有する。
【解決手段】クマザサ葉抽出物を有効成分として含むグラム陽性細菌用抗菌剤、該抗菌剤と特定の抗生物質との組み合わせを含むグラム陽性細菌用抗菌剤、並びにクマザサ葉抽出物を有効成分として含む抗菌活性増強剤を提供した。
【効果】本発明の抗菌剤は、従来院内感染等で問題となっているMRSAやバンコマイシン耐性菌に対しても抗菌活性を示す。また、特定の抗生物質の抗菌活性を増強する作用も有する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明はグラム陽性細菌用抗菌剤及び抗菌活性増強剤に関する。
【背景技術】
【0002】
近年、抗生物質の使用が普遍化すると共に、耐性菌が出現し、感染症治療が次第に難しくなっている。このような問題に答えるべく、新しい抗生物質の探索や抗生剤の適正使用が進められている。
【0003】
例えば、植物から新しい抗菌性物質を探索する試みがなされており、緑茶カテキンがメチシリン耐性黄色ブドウ球菌に抗菌作用を示すこと(非特許文献1)、緑茶成分がβ−ラクタム系抗菌薬の効果を増強すること(非特許文献2)が報告されている。
【0004】
クマザサは、古くから食品の鮮度保持や民間療法に用いられてきた。例えば、クマザサの単剤軟膏として長期療養者の褥瘡等の治療に利用されてきており、クマザサには抗菌活性があると考えられている。特許文献1〜3には、クマザサ抽出物を利用した抗菌性材料や皮膚外用剤が記載されている。しかしながら、これまでに、クマザサの抗菌活性や抗菌スペクトルについて十分に詳細な検討はなされていない。
【0005】
耐性菌の問題についての対応策としては、従来の抗菌システムとは異なる、新規な抗菌システムを数多く構築することが重要である。現状においても、耐性菌に対しても有効な抗菌手段は不足しており、新規な抗菌手段の確立が望まれている。
【0006】
【特許文献1】国際公開第99/62444号パンフレット
【特許文献2】特開2004−323430号公報
【特許文献3】特開2000−44419号公報
【非特許文献1】感染症学雑誌、69(10): 1126-34 (1995)
【非特許文献2】J Antimicrob Chemother. 42(2):211-6.(1998)
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明は、抗生物質耐性菌の出現に対抗し得る、新規な抗菌手段を提供することにある。
【課題を解決するための手段】
【0008】
本願発明者は、鋭意研究の結果、クマザサ葉抽出物がグラム陽性細菌に対して抗菌活性を示すことを見出した。そして、クマザサ葉抽出物はメチシリン耐性黄色ブドウ球菌やバンコマイシン耐性腸球菌等の抗生物質耐性菌に対して定まった抗菌活性を示すこと、さらには、クマザサ葉抽出物が抗生物質耐性菌に対する抗生物質の効果を相乗的ないしは相加的に増強し、耐性菌の抗菌が可能になることを見出し、本願発明を完成した。
【0009】
すなわち、本発明は、クマザサ葉抽出物を有効成分として含むグラム陽性細菌用抗菌剤を提供する。また、本発明は、上記本発明の抗菌剤と、β−ラクタム系抗生物質、グリコペプチド系抗生物質及びテトラサイクリン系抗生物質からなる群より選択される少なくとも1種の抗生物質との組み合わせを含むグラム陽性細菌用抗菌剤を提供する。さらに、本発明は、クマザサ葉抽出物を有効成分として含む抗菌活性増強剤を提供する。
【発明の効果】
【0010】
本発明により、新しい抗菌機作を持った低毒性且つ低コストの抗菌剤が提供された。本発明の抗菌剤は、従来院内感染等で問題となっているMRSAやバンコマイシン耐性菌に対しても抗菌活性を示す。また、特定の抗生物質の抗菌活性を増強する作用も有する。クマザサが持つ抗菌システムの研究は、新規な抗菌作用を持った新薬の開発に貢献する。また、抗生物質の抗菌活性を増強する作用を利用し、従来の抗生物質と配合した新しい医薬への応用が期待できる。本発明は、抗生物質耐性菌の治療分野に大いに貢献するものである。
【発明を実施するための最良の形態】
【0011】
本発明の抗菌剤は、クマザサ葉抽出物、好ましくはクマザサ葉の細胞の原形質成分を有効成分とする。クマザサは、イネ科 (Poaceae) ササ属(Sasa)の植物であり、学名はSasa veitchii (Carr.)である。クマザサの葉は淡竹葉(タンチクヨウ)という生薬名で呼ばれることもある。クマザサ葉抽出物は、クマザサの葉から公知の常法により抽出して得ることができる。抽出方法は特に限定されないが、水性溶媒中で抽出する方法が好ましい。すなわち、クマザサ葉抽出物としては、水可溶性の原形質成分が好ましい。クマザサの葉は乾燥葉でも生葉でもよいが、生葉から抽出することが好ましい。例えば、クマザサの生葉をアルカリ処理又は高温(60℃〜130℃程度)の水中で処理して細胞壁を破壊した後、水中で常圧又は加圧抽出することで細胞内容物(原形質成分)を得ることができる。また、クマザサ葉抽出物は種々のものが市販されており、そのような市販品を用いることもできる。なお、クマザサ細胞原形質成分のうち、抗菌活性を発揮する成分の本体は明らかではないが、可溶性の耐熱性成分であると考えられる(下記実施例表1参照)。
【0012】
本発明の抗菌剤が抗菌活性を示す菌は、グラム陽性細菌である。下記実施例に示される通り、クマザサ葉抽出物は、グラム陰性細菌である大腸菌や緑膿菌に対しては抗菌活性を示さず、グラム陽性細菌に対して抗菌活性を示す。グラム陽性細菌としては特に限定されず、MSSA(メチシリン感受性黄色ブドウ球菌)やVSE(バンコマイシン感受性腸球菌)等のように抗生物質に感受性の細菌であっても、また、MRSA(メチシリン耐性黄色ブドウ球菌)やVRE(バンコマイシン耐性腸球菌)等の多剤耐性菌であっても、本発明の抗菌剤により抗菌することができる。このような多剤耐性菌は、通常、メチシリンやバンコマイシンのみならず、一般的に用いられているアンピシリンやペニシリン等の多くの抗生物質に対し耐性を有している。クマザサ葉抽出物がMRSAやVREのような抗生物質耐性菌に対しても抗菌作用を示すということは従来知られておらず、本願発明者による新たな知見である。
【0013】
細菌類の抗生物質の耐性については、米国のCLSI(Clinical and Laboratory Standards Institute, 旧NCCLS)によって、各菌種毎に種々の抗生物質について、MIC(最小発育阻止濃度)に基づく基準値が定められており、この分野においては一般にこれを基準として耐性菌であるか否かの分類が行われる。この基準値は当業者であれば容易に入手可能である。本発明においても、抗生物質耐性菌であるか否かはこの基準値により判断することができ、「抗生物質耐性菌」とは、CLSIが推奨する微量液体希釈法で測定した場合のある抗生物質のその菌に対するMICが、CLSIの基準値よりも高いことを意味する。例えば、上記基準では、VREの抗生物質耐性に関し、バンコマイシンについてはMICが32μg/mL以上をバンコマイシン耐性、アンピシリンについてはMICが16μg/mL以上をアンピシリン耐性と定められているので、「バンコマイシン耐性腸球菌」は、微量液体希釈法で測定したバンコマイシンのMICが32μg/mL以上の腸球菌株を意味する。なお、微量液体希釈法は周知の常法であり、具体的には下記実施例に記載されている。
【0014】
上記本発明の抗菌剤は、クマザサ葉抽出物のみから成るものであってもよいし、また、感染症治療に用いる場合には、公知の賦形剤、担体等と混合し、投与方法に適した形態に調製したものであってもよい。クマザサ葉抽出物は、抽出後の原液のままでもよいし、所望により適宜水又は生理食塩水等で希釈して用いてもよい。本発明の抗菌剤の投与方法としては、経口投与の他、経皮、皮下、筋肉内、腹腔内、動脈内、静脈内、直腸内等への非経口投与が挙げられる。具体的には、例えば抽出原液をそのままあるいは適宜希釈して経口投与又は注射若しくは点滴により非経口投与することができ、また、軟膏剤やパッチ剤として経皮投与することができるが、これらに限定されない。
【0015】
本発明の抗菌剤の使用量は、有効成分として用いるクマザサ葉抽出物の対象細菌に対するMICやMBC(最小殺菌濃度)に応じて適宜選択することができる。通常、標的組織における濃度や血中濃度がMIC又はMBC以上となるような濃度で用いられる。具体的には、感染症の治療に用いる場合、例えば抽出原液若しくは濃度0.1%程度以上の抽出原液希釈液を経口投与、又は抽出原液若しくは濃度0.05%程度以上の抽出原液希釈液を注射若しくは点滴により非経口投与することができ、外用剤の場合には抽出原液を濃度0.1%程度以上で含有する軟膏剤等として適用することができるが、これらに限定されない。また、器具の殺菌等に用いる場合には、抽出原液又は濃度0.1%程度以上の希釈液を用いることができるが、これに限定されない。なお、MIC及びMBCの測定方法は周知の常法であり、例えば、クマザサ葉抽出物の希釈系列を調製して細菌を播種し、24時間程度培養後に細菌の増殖を観察(目視等)することによりMICを測定することができる。また、肉眼で細菌の増殖が認められない希釈系列の培養液を抗菌剤フリーのプレート上に播種して培養し、菌の増殖の有無を調べることで、MBCを測定することができる。
【0016】
また、上記本発明の抗菌剤は、細菌が耐性を獲得することで単剤では効果が失われてしまった抗生物質と組み合わせて用いると、該抗生物質の抗菌活性を相乗的ないしは相加的に増強し、耐性菌を抗菌できるようになる。例えば、メチシリンやアンピシリンに対し耐性を獲得したMRSA菌株に対し、アンピシリンと本発明の抗菌剤とを組み合わせて投与すると、アンピシリンのMIC値も本発明の抗菌剤のMIC値もいずれも低下し、より低濃度で抗菌活性を発揮することができるようになる(下記実施例参照)。本発明は、このように、上記したクマザサ葉抽出物を有効成分とする抗菌剤と、抗生物質との組み合わせを含むグラム陽性細菌用の抗菌剤も提供する(以下、この抗菌剤を便宜上「組み合わせ剤」と呼ぶことがある)。該組み合わせ剤の形態は、単体の剤として、クマザサ葉抽出物を有効成分とする抗菌剤にさらに抗生物質を含有させたものであってもよいし、また、別個の剤として調製したものをセットにした形態であってもよい。
【0017】
クマザサ葉抽出物と組み合わせる抗生物質としては、β−ラクタム系抗生物質、グリコペプチド系抗生物質及びテトラサイクリン系抗生物質からなる群より選択される少なくとも1種の抗生物質が好ましい。β−ラクタム系抗生物質としては、例えばアンピシリン等のペニシリン系抗生物質等が挙げられる。グリコペプチド系抗生物質としてはバンコマイシン等が挙げられる。テトラサイクリン系抗生物質としては、テトラサイクリン、ミノサイクリン等が挙げられる。これらの抗生物質の1種又は2種以上をクマザサ葉抽出物と組み合わせて用いることができる。特に、組み合わせる抗生物質としては、アンピシリン、バンコマイシン及びテトラサイクリンからなる群より選択される少なくとも1種が好ましい。
【0018】
クマザサ葉抽出物による抗生物質の抗菌活性の増強効果は、組み合わせて用いる抗生物質に対して耐性を獲得していない感受性菌に対しては認められない。増強効果が認められるのは、抗生物質耐性菌に対してである。例えば、バンコマイシン感受性の腸球菌に対して、バンコマイシンとクマザサ葉抽出物との組み合わせ剤を用いても、バンコマイシンのMICの低下は認められない(図3A)。バンコマイシン耐性腸球菌に対してバンコマイシンとの組み合わせ剤を用いた場合に、バンコマイシンのMICが低下する(図3B、C)。従って、組み合わせ剤は、該組み合わせ剤中に含有される抗生物質が単独では抗菌活性を発揮できない耐性菌に対して用いることが効果的で望ましい。ただし、感受性菌に用いても、増強効果がないだけで抗生物質の抗菌活性が低下するわけではないので、組み合わせ剤を感受性菌に用いることは差し支えない。
【0019】
クマザサ葉抽出物と抗生物質とを併用する場合、それぞれの使用量は、増強効果(相乗効果又は相加効果)の程度に応じて適宜選択することができる。増強効果の程度は、菌種と抗生物質の種類に応じて異なり得るが、増強効果の評価は常法により容易に行うことができる。例えば、下記実施例に記載されるように、チェッカーボード法により算出されるFIC(Fractional Inhibitory Concentration)indexを指標として併用による抗菌活性の増強効果を評価することができる。チェッカーボード法は、例えば以下のようにして行うことができる。すなわち、各希釈段階のクマザサ葉抽出物と抗生物質とを種々に組み合わせてプレートのウェルに分注し、これに適当量の標的細菌を添加後、24時間程度培養し、菌の増殖を目視等により判定する。クマザサ葉抽出物(A)とβ−ラクタム系抗生物質(B)のMIC(併用時及び単独使用時)をそれぞれ特定後、以下の式によりFIC indexを算出するという方法で行なうことができる。FIC indexは1より小さいほど相乗効果が高く、通常、FIC indexが0.8程度以上の場合を増強効果なし、0.6〜0.8程度を相加効果あり、0.6程度未満を相乗効果ありと評価するが、これに限定されない。
FIC index={AのMIC(併用時)/AのMIC(単独)}+{BのMIC(併用時)/BのMIC(単独)}
【0020】
上記したように、クマザサ葉抽出物には、抗生物質の抗菌活性を増強する作用があるので、本発明により、クマザサ葉抽出物を有効成分として含む抗菌活性増強剤も提供される。クマザサ葉抽出物は、上記したように、感受性菌に対しては抗生物質の抗菌活性を増強する作用を発揮しないため、本発明の抗菌活性増強剤は、抗生物質耐性菌に対して用いられる。より詳細には、耐性菌の出現により単独では抗菌効果を発揮できなくなった抗生物質の、該耐性菌に対する抗菌活性を増強するために用いられる。抗菌活性増強剤の使用量や使用方法は、組み合わせ剤について上記したのと同様である。
【0021】
クマザサ葉抽出物が抗生物質の効果を増強する作用機序は明らかではないが、下記実施例に示される通り、クマザサ葉抽出物による抗生物質の抗菌活性増強作用は明らかに存在する。抗菌活性増強作用が好ましく認められる抗生物質と耐性菌の組み合わせの具体例を以下に例示するが、これらに限定されない。
メチシリン耐性菌:アンピシリン、バンコマイシン
バンコマイシン耐性菌:アンピシリン、バンコマイシン、テトラサイクリン
【実施例】
【0022】
以下、実施例に基づき本発明をより具体的に説明する。
【0023】
実施例1 クマザサ葉抽出物の抗菌活性
医薬品サンクロン(サンクロン株式会社製、クマザサの細胞原形質液)をクマザサ葉抽出物として実験に用いた。サンクロンは、クマザサの生葉をアルカリ処理後、水で抽出して細胞の原形質を取り出すことにより調製された、クマザサ細胞原形質液であり、液体状の抽出物からなるものである。サンクロンを高圧蒸気滅菌処理に付したもの(高温処理)と高温処理に付さないもの(未処理)の2通りで検討した。
【0024】
クマザサ原形質液の抗菌活性の測定は、微量液体希釈法により行なった。96穴マイクロプレートに希釈濃度系列を作り、各種細菌を接種して(75×103細胞/ウェル)37℃にて24時間培養した。希釈系列は、サンクロン原液を1倍希釈とし、2〜2048倍までの12段階の希釈系列を調製した。MIC(最小発育阻止濃度)については、培養後のプレートを目視にて観察し、濁りが観察された場合を発育ありとして、発育が認められなかった最低濃度をMICとした。MBC(最小殺菌濃度)については、発育が認められなかったウェルから溶液を採取して、抗生物質を含まない培地に添加し、37℃にて24時間インキュベートした後、目視にて濁りの有無を観察し、濁りが観察されなかった最低濃度をMBCとした。その結果を表1に示す。
【0025】
【表1】

MRSA: メチシリン耐性黄色ブドウ球菌
MSSA: メチシリン感受性黄色ブドウ球菌
VRE: バンコマイシン耐性腸球菌
VSE: バンコマイシン感受性腸球菌
【0026】
クマザサ原形質液は、単独で、グラム陽性球菌である黄色ブドウ球菌、腸球菌に抗菌活性を示した。メチシリン耐性黄色ブドウ球菌やバンコマイシン耐性腸球菌に対しても、感受性菌に対する抗菌活性と同等の抗菌活性を示していた。一方、グラム陰性細菌である緑膿菌と大腸菌に対しては、MIC及びMBCが50v/v%と非常に高濃度であり、抗菌活性を示さなかった。
【0027】
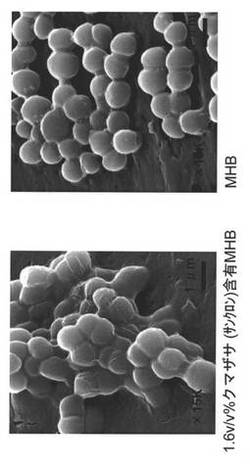
クマザサ原形質液を1.6v/v%含有するミューラーヒントン培地(MHB)中でMRSA N315株を培養し、走査型電子顕微鏡(SEM)を用いて菌体の形態変化を観察した。その結果、図1に示す通り、培養24時間後にはMRSAの溶菌が観察された。
【0028】
高温処理の有無により、クマザサ原形質液の抗菌活性に差異は認められなかった。このことから、クマザサ原形質液中の抗菌活性成分の本体は耐熱性成分であると推察される。
【0029】
実施例2 クマザサ葉抽出物による抗生物質の抗菌活性増強作用
1. MRSAに対する各種抗生物質の抗菌活性の増強作用
(1) MRSAに対するアンピシリンの抗菌活性の増強作用
クマザサ原形質液とアンピシリン(ABPC)とを併用した際の、MRSAに対する抗菌活性の増強効果を調べた。増強効果の測定はチェッカーボード法により行なった。プレートの横方向に向かってクマザサ原形質液の12.5、6.3、3.2、1.6、0.8、0.4、0.2、0.1、0.05、0.03、0.0までの11段階の希釈系列を調製した。また、プレートの縦方向に向かってアンピシリンの16段階の希釈系列(原液512μg/mlを1倍とし、2〜214倍希釈及び0.0μg/ml)を調製した。各ウェルに75×103細胞/ウェルとなるように菌液(MRSA N315菌株)を接種して37℃にて24時間培養後、増殖の判定を行なった。FIC indexは次式により算出した。結果を表2に示す。
FIC index={クマザサのMIC(併用時)/クマザサのMIC(単独)}+{ABPCのMIC(併用時)/ABPCのMIC(単独)}
【0030】
【表2】

【0031】
FIC indexは数値が1より小さいほど相乗効果が高い。MRSA N315株に対しては、アンピシリン0.5〜1μg/ml、クマザサ原形質液0.4v/v%で相乗効果が高かった。
【0032】
(2) MRSAに対するテトラサイクリン及びバンコマイシンの抗菌活性の増強作用
クマザサ原形質液がテトラサイクリン(TC)及びバンコマイシン(VCM)の抗菌活性を増強するか否か検討した。菌株としてMRSA N315株を用いて、上記チェッカーボード法により行なった。クマザサ原形質液は12.5v/v%〜0v/v%の11段階の希釈系列とした。TCは1, 0.5, 0.25, 0.125, 0.063, 0.031, 0.016, 0.0μg/mlの8段階、VCMは8, 4, 2, 1, 0.5, 0.25, 0.125, 0.0μg/mlの8段階とした。TC単独でのMICは0.5μg/ml、VCM単独でのMICは1μg/mlだった。結果を下記表3に示す。表中には上記したABPCについての結果も併せて示す。
【0033】
【表3】

【0034】
VCMとの併用ではMRSAに対して相加効果が認められた。TCとの併用では、TCの抗菌活性の増強作用は認められなかった。
【0035】
ABPCはβ−ラクタム系抗生物質のうちのペニシリン系抗生物質である。β−ラクタム系抗生物質は、細菌の細胞壁合成の最終段階に関与する酵素であるペニシリン結合タンパク質に結合して活性を阻害し、これにより抗菌活性を発揮する。TCはテトラサイクリン系抗生物質であり、リボソームに作用してタンパク質合成を阻害することで抗菌活性を発揮する。VCMはグリコペプチド系抗生物質であり、細胞壁合成酵素の基質に結合して細胞壁合成を阻害することにより抗菌活性を発揮する。クマザサ原形質液による抗生物質の抗菌活性の増強作用の機序として、クマザサ原形質液中の成分が細菌の細胞壁合成になんらかの影響を及ぼしている可能性が考えられる。
【0036】
(3) クマザサ抽出物の高温処理の影響について
高温処理したクマザサ原形質液を用いて、上記と同様にMRSAに対する各種抗生物質の抗菌活性の増強効果を評価した。結果を下記表4に示す。
【0037】
【表4】

【0038】
ABPCへの相乗効果は高温処理により失われなかったが、VCMへの相加効果は高温処理により失われ、増強効果が認められなかった。抗生物質の抗菌活性を増強する作用に重要なクマザサ成分は、抗生物質の種類により異なると推察される。
【0039】
(4) MSSAに対するABPC併用の効果について
MSSA ATCC6538株とMRSA N315株について、上記チェッカーボード法によりアンピシリン及びクマザサ併用時のそれぞれのMICを測定した。クマザサ原形質液としては、高温処理と非処理(サンクロン)の2通りを検討した。その結果、図2に示す通り、高温処理及び非処理いずれもMRSAに対してABPCの抗菌活性を増強する作用が認められた。相乗効果に重要な成分も耐熱性の成分であると推察される。MSSAに対しては、ABPCの抗菌活性の増強は認められなかった。
【0040】
2.VREに対する各種抗生物質の抗菌活性の増強作用
上記チェッカーボード法により、腸球菌に対して各種抗生物質とクマザサ原形質液とを併用した際のMICを測定し、抗菌活性の増強効果を評価した。腸球菌として、VRE NTCT12201株とVSE JCM5804株を用いた。結果を表5及び6に示す。また、VRE NTCT12201株に対する併用効果の結果をまとめて表7に示す。なお、表5及び表6中、各種抗生物質のMICの単位はμg/ml、クマザサ原形質液のMICの単位はv/v%である。
【0041】
【表5】

【0042】
【表6】

【0043】
【表7】

【0044】
図3は、VSE JCM5804株(図3A)、VRE NTCT02000株(図3B)、VRE NTCT12201株(図3C)に対してクマザサ原形質液と各種抗生物質とを併用した際のMIC値の変化を示すグラフである。感受性菌のVSEに対しては、いずれの抗生物質でも、クマザサ原形質液を併用してもMICの低下は認められなかった。耐性菌のVREに対しては、検討した全ての抗生物質でクマザサ併用によるMICの低下が観察された。
【図面の簡単な説明】
【0045】
【図1】1.6v/v%クマザサ原形質液含有培地中で24時間培養したMRSA N315株の形態を走査型電子顕微鏡(SEM)で観察した写真である。
【図2】MRSAとMSSAに対してクマザサ原形質液とアンピシリンとを併用した際のMIC値の変化を示すグラフである。
【図3】VSEとVREに対してクマザサ原形質液と各種抗生物質とを併用した際のMIC値の変化を示すグラフである。A)VSE JCM5804株、B)VRE NTCT02000株、C)VRE NTCT12201株。
【技術分野】
【0001】
本発明はグラム陽性細菌用抗菌剤及び抗菌活性増強剤に関する。
【背景技術】
【0002】
近年、抗生物質の使用が普遍化すると共に、耐性菌が出現し、感染症治療が次第に難しくなっている。このような問題に答えるべく、新しい抗生物質の探索や抗生剤の適正使用が進められている。
【0003】
例えば、植物から新しい抗菌性物質を探索する試みがなされており、緑茶カテキンがメチシリン耐性黄色ブドウ球菌に抗菌作用を示すこと(非特許文献1)、緑茶成分がβ−ラクタム系抗菌薬の効果を増強すること(非特許文献2)が報告されている。
【0004】
クマザサは、古くから食品の鮮度保持や民間療法に用いられてきた。例えば、クマザサの単剤軟膏として長期療養者の褥瘡等の治療に利用されてきており、クマザサには抗菌活性があると考えられている。特許文献1〜3には、クマザサ抽出物を利用した抗菌性材料や皮膚外用剤が記載されている。しかしながら、これまでに、クマザサの抗菌活性や抗菌スペクトルについて十分に詳細な検討はなされていない。
【0005】
耐性菌の問題についての対応策としては、従来の抗菌システムとは異なる、新規な抗菌システムを数多く構築することが重要である。現状においても、耐性菌に対しても有効な抗菌手段は不足しており、新規な抗菌手段の確立が望まれている。
【0006】
【特許文献1】国際公開第99/62444号パンフレット
【特許文献2】特開2004−323430号公報
【特許文献3】特開2000−44419号公報
【非特許文献1】感染症学雑誌、69(10): 1126-34 (1995)
【非特許文献2】J Antimicrob Chemother. 42(2):211-6.(1998)
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明は、抗生物質耐性菌の出現に対抗し得る、新規な抗菌手段を提供することにある。
【課題を解決するための手段】
【0008】
本願発明者は、鋭意研究の結果、クマザサ葉抽出物がグラム陽性細菌に対して抗菌活性を示すことを見出した。そして、クマザサ葉抽出物はメチシリン耐性黄色ブドウ球菌やバンコマイシン耐性腸球菌等の抗生物質耐性菌に対して定まった抗菌活性を示すこと、さらには、クマザサ葉抽出物が抗生物質耐性菌に対する抗生物質の効果を相乗的ないしは相加的に増強し、耐性菌の抗菌が可能になることを見出し、本願発明を完成した。
【0009】
すなわち、本発明は、クマザサ葉抽出物を有効成分として含むグラム陽性細菌用抗菌剤を提供する。また、本発明は、上記本発明の抗菌剤と、β−ラクタム系抗生物質、グリコペプチド系抗生物質及びテトラサイクリン系抗生物質からなる群より選択される少なくとも1種の抗生物質との組み合わせを含むグラム陽性細菌用抗菌剤を提供する。さらに、本発明は、クマザサ葉抽出物を有効成分として含む抗菌活性増強剤を提供する。
【発明の効果】
【0010】
本発明により、新しい抗菌機作を持った低毒性且つ低コストの抗菌剤が提供された。本発明の抗菌剤は、従来院内感染等で問題となっているMRSAやバンコマイシン耐性菌に対しても抗菌活性を示す。また、特定の抗生物質の抗菌活性を増強する作用も有する。クマザサが持つ抗菌システムの研究は、新規な抗菌作用を持った新薬の開発に貢献する。また、抗生物質の抗菌活性を増強する作用を利用し、従来の抗生物質と配合した新しい医薬への応用が期待できる。本発明は、抗生物質耐性菌の治療分野に大いに貢献するものである。
【発明を実施するための最良の形態】
【0011】
本発明の抗菌剤は、クマザサ葉抽出物、好ましくはクマザサ葉の細胞の原形質成分を有効成分とする。クマザサは、イネ科 (Poaceae) ササ属(Sasa)の植物であり、学名はSasa veitchii (Carr.)である。クマザサの葉は淡竹葉(タンチクヨウ)という生薬名で呼ばれることもある。クマザサ葉抽出物は、クマザサの葉から公知の常法により抽出して得ることができる。抽出方法は特に限定されないが、水性溶媒中で抽出する方法が好ましい。すなわち、クマザサ葉抽出物としては、水可溶性の原形質成分が好ましい。クマザサの葉は乾燥葉でも生葉でもよいが、生葉から抽出することが好ましい。例えば、クマザサの生葉をアルカリ処理又は高温(60℃〜130℃程度)の水中で処理して細胞壁を破壊した後、水中で常圧又は加圧抽出することで細胞内容物(原形質成分)を得ることができる。また、クマザサ葉抽出物は種々のものが市販されており、そのような市販品を用いることもできる。なお、クマザサ細胞原形質成分のうち、抗菌活性を発揮する成分の本体は明らかではないが、可溶性の耐熱性成分であると考えられる(下記実施例表1参照)。
【0012】
本発明の抗菌剤が抗菌活性を示す菌は、グラム陽性細菌である。下記実施例に示される通り、クマザサ葉抽出物は、グラム陰性細菌である大腸菌や緑膿菌に対しては抗菌活性を示さず、グラム陽性細菌に対して抗菌活性を示す。グラム陽性細菌としては特に限定されず、MSSA(メチシリン感受性黄色ブドウ球菌)やVSE(バンコマイシン感受性腸球菌)等のように抗生物質に感受性の細菌であっても、また、MRSA(メチシリン耐性黄色ブドウ球菌)やVRE(バンコマイシン耐性腸球菌)等の多剤耐性菌であっても、本発明の抗菌剤により抗菌することができる。このような多剤耐性菌は、通常、メチシリンやバンコマイシンのみならず、一般的に用いられているアンピシリンやペニシリン等の多くの抗生物質に対し耐性を有している。クマザサ葉抽出物がMRSAやVREのような抗生物質耐性菌に対しても抗菌作用を示すということは従来知られておらず、本願発明者による新たな知見である。
【0013】
細菌類の抗生物質の耐性については、米国のCLSI(Clinical and Laboratory Standards Institute, 旧NCCLS)によって、各菌種毎に種々の抗生物質について、MIC(最小発育阻止濃度)に基づく基準値が定められており、この分野においては一般にこれを基準として耐性菌であるか否かの分類が行われる。この基準値は当業者であれば容易に入手可能である。本発明においても、抗生物質耐性菌であるか否かはこの基準値により判断することができ、「抗生物質耐性菌」とは、CLSIが推奨する微量液体希釈法で測定した場合のある抗生物質のその菌に対するMICが、CLSIの基準値よりも高いことを意味する。例えば、上記基準では、VREの抗生物質耐性に関し、バンコマイシンについてはMICが32μg/mL以上をバンコマイシン耐性、アンピシリンについてはMICが16μg/mL以上をアンピシリン耐性と定められているので、「バンコマイシン耐性腸球菌」は、微量液体希釈法で測定したバンコマイシンのMICが32μg/mL以上の腸球菌株を意味する。なお、微量液体希釈法は周知の常法であり、具体的には下記実施例に記載されている。
【0014】
上記本発明の抗菌剤は、クマザサ葉抽出物のみから成るものであってもよいし、また、感染症治療に用いる場合には、公知の賦形剤、担体等と混合し、投与方法に適した形態に調製したものであってもよい。クマザサ葉抽出物は、抽出後の原液のままでもよいし、所望により適宜水又は生理食塩水等で希釈して用いてもよい。本発明の抗菌剤の投与方法としては、経口投与の他、経皮、皮下、筋肉内、腹腔内、動脈内、静脈内、直腸内等への非経口投与が挙げられる。具体的には、例えば抽出原液をそのままあるいは適宜希釈して経口投与又は注射若しくは点滴により非経口投与することができ、また、軟膏剤やパッチ剤として経皮投与することができるが、これらに限定されない。
【0015】
本発明の抗菌剤の使用量は、有効成分として用いるクマザサ葉抽出物の対象細菌に対するMICやMBC(最小殺菌濃度)に応じて適宜選択することができる。通常、標的組織における濃度や血中濃度がMIC又はMBC以上となるような濃度で用いられる。具体的には、感染症の治療に用いる場合、例えば抽出原液若しくは濃度0.1%程度以上の抽出原液希釈液を経口投与、又は抽出原液若しくは濃度0.05%程度以上の抽出原液希釈液を注射若しくは点滴により非経口投与することができ、外用剤の場合には抽出原液を濃度0.1%程度以上で含有する軟膏剤等として適用することができるが、これらに限定されない。また、器具の殺菌等に用いる場合には、抽出原液又は濃度0.1%程度以上の希釈液を用いることができるが、これに限定されない。なお、MIC及びMBCの測定方法は周知の常法であり、例えば、クマザサ葉抽出物の希釈系列を調製して細菌を播種し、24時間程度培養後に細菌の増殖を観察(目視等)することによりMICを測定することができる。また、肉眼で細菌の増殖が認められない希釈系列の培養液を抗菌剤フリーのプレート上に播種して培養し、菌の増殖の有無を調べることで、MBCを測定することができる。
【0016】
また、上記本発明の抗菌剤は、細菌が耐性を獲得することで単剤では効果が失われてしまった抗生物質と組み合わせて用いると、該抗生物質の抗菌活性を相乗的ないしは相加的に増強し、耐性菌を抗菌できるようになる。例えば、メチシリンやアンピシリンに対し耐性を獲得したMRSA菌株に対し、アンピシリンと本発明の抗菌剤とを組み合わせて投与すると、アンピシリンのMIC値も本発明の抗菌剤のMIC値もいずれも低下し、より低濃度で抗菌活性を発揮することができるようになる(下記実施例参照)。本発明は、このように、上記したクマザサ葉抽出物を有効成分とする抗菌剤と、抗生物質との組み合わせを含むグラム陽性細菌用の抗菌剤も提供する(以下、この抗菌剤を便宜上「組み合わせ剤」と呼ぶことがある)。該組み合わせ剤の形態は、単体の剤として、クマザサ葉抽出物を有効成分とする抗菌剤にさらに抗生物質を含有させたものであってもよいし、また、別個の剤として調製したものをセットにした形態であってもよい。
【0017】
クマザサ葉抽出物と組み合わせる抗生物質としては、β−ラクタム系抗生物質、グリコペプチド系抗生物質及びテトラサイクリン系抗生物質からなる群より選択される少なくとも1種の抗生物質が好ましい。β−ラクタム系抗生物質としては、例えばアンピシリン等のペニシリン系抗生物質等が挙げられる。グリコペプチド系抗生物質としてはバンコマイシン等が挙げられる。テトラサイクリン系抗生物質としては、テトラサイクリン、ミノサイクリン等が挙げられる。これらの抗生物質の1種又は2種以上をクマザサ葉抽出物と組み合わせて用いることができる。特に、組み合わせる抗生物質としては、アンピシリン、バンコマイシン及びテトラサイクリンからなる群より選択される少なくとも1種が好ましい。
【0018】
クマザサ葉抽出物による抗生物質の抗菌活性の増強効果は、組み合わせて用いる抗生物質に対して耐性を獲得していない感受性菌に対しては認められない。増強効果が認められるのは、抗生物質耐性菌に対してである。例えば、バンコマイシン感受性の腸球菌に対して、バンコマイシンとクマザサ葉抽出物との組み合わせ剤を用いても、バンコマイシンのMICの低下は認められない(図3A)。バンコマイシン耐性腸球菌に対してバンコマイシンとの組み合わせ剤を用いた場合に、バンコマイシンのMICが低下する(図3B、C)。従って、組み合わせ剤は、該組み合わせ剤中に含有される抗生物質が単独では抗菌活性を発揮できない耐性菌に対して用いることが効果的で望ましい。ただし、感受性菌に用いても、増強効果がないだけで抗生物質の抗菌活性が低下するわけではないので、組み合わせ剤を感受性菌に用いることは差し支えない。
【0019】
クマザサ葉抽出物と抗生物質とを併用する場合、それぞれの使用量は、増強効果(相乗効果又は相加効果)の程度に応じて適宜選択することができる。増強効果の程度は、菌種と抗生物質の種類に応じて異なり得るが、増強効果の評価は常法により容易に行うことができる。例えば、下記実施例に記載されるように、チェッカーボード法により算出されるFIC(Fractional Inhibitory Concentration)indexを指標として併用による抗菌活性の増強効果を評価することができる。チェッカーボード法は、例えば以下のようにして行うことができる。すなわち、各希釈段階のクマザサ葉抽出物と抗生物質とを種々に組み合わせてプレートのウェルに分注し、これに適当量の標的細菌を添加後、24時間程度培養し、菌の増殖を目視等により判定する。クマザサ葉抽出物(A)とβ−ラクタム系抗生物質(B)のMIC(併用時及び単独使用時)をそれぞれ特定後、以下の式によりFIC indexを算出するという方法で行なうことができる。FIC indexは1より小さいほど相乗効果が高く、通常、FIC indexが0.8程度以上の場合を増強効果なし、0.6〜0.8程度を相加効果あり、0.6程度未満を相乗効果ありと評価するが、これに限定されない。
FIC index={AのMIC(併用時)/AのMIC(単独)}+{BのMIC(併用時)/BのMIC(単独)}
【0020】
上記したように、クマザサ葉抽出物には、抗生物質の抗菌活性を増強する作用があるので、本発明により、クマザサ葉抽出物を有効成分として含む抗菌活性増強剤も提供される。クマザサ葉抽出物は、上記したように、感受性菌に対しては抗生物質の抗菌活性を増強する作用を発揮しないため、本発明の抗菌活性増強剤は、抗生物質耐性菌に対して用いられる。より詳細には、耐性菌の出現により単独では抗菌効果を発揮できなくなった抗生物質の、該耐性菌に対する抗菌活性を増強するために用いられる。抗菌活性増強剤の使用量や使用方法は、組み合わせ剤について上記したのと同様である。
【0021】
クマザサ葉抽出物が抗生物質の効果を増強する作用機序は明らかではないが、下記実施例に示される通り、クマザサ葉抽出物による抗生物質の抗菌活性増強作用は明らかに存在する。抗菌活性増強作用が好ましく認められる抗生物質と耐性菌の組み合わせの具体例を以下に例示するが、これらに限定されない。
メチシリン耐性菌:アンピシリン、バンコマイシン
バンコマイシン耐性菌:アンピシリン、バンコマイシン、テトラサイクリン
【実施例】
【0022】
以下、実施例に基づき本発明をより具体的に説明する。
【0023】
実施例1 クマザサ葉抽出物の抗菌活性
医薬品サンクロン(サンクロン株式会社製、クマザサの細胞原形質液)をクマザサ葉抽出物として実験に用いた。サンクロンは、クマザサの生葉をアルカリ処理後、水で抽出して細胞の原形質を取り出すことにより調製された、クマザサ細胞原形質液であり、液体状の抽出物からなるものである。サンクロンを高圧蒸気滅菌処理に付したもの(高温処理)と高温処理に付さないもの(未処理)の2通りで検討した。
【0024】
クマザサ原形質液の抗菌活性の測定は、微量液体希釈法により行なった。96穴マイクロプレートに希釈濃度系列を作り、各種細菌を接種して(75×103細胞/ウェル)37℃にて24時間培養した。希釈系列は、サンクロン原液を1倍希釈とし、2〜2048倍までの12段階の希釈系列を調製した。MIC(最小発育阻止濃度)については、培養後のプレートを目視にて観察し、濁りが観察された場合を発育ありとして、発育が認められなかった最低濃度をMICとした。MBC(最小殺菌濃度)については、発育が認められなかったウェルから溶液を採取して、抗生物質を含まない培地に添加し、37℃にて24時間インキュベートした後、目視にて濁りの有無を観察し、濁りが観察されなかった最低濃度をMBCとした。その結果を表1に示す。
【0025】
【表1】

MRSA: メチシリン耐性黄色ブドウ球菌
MSSA: メチシリン感受性黄色ブドウ球菌
VRE: バンコマイシン耐性腸球菌
VSE: バンコマイシン感受性腸球菌
【0026】
クマザサ原形質液は、単独で、グラム陽性球菌である黄色ブドウ球菌、腸球菌に抗菌活性を示した。メチシリン耐性黄色ブドウ球菌やバンコマイシン耐性腸球菌に対しても、感受性菌に対する抗菌活性と同等の抗菌活性を示していた。一方、グラム陰性細菌である緑膿菌と大腸菌に対しては、MIC及びMBCが50v/v%と非常に高濃度であり、抗菌活性を示さなかった。
【0027】
クマザサ原形質液を1.6v/v%含有するミューラーヒントン培地(MHB)中でMRSA N315株を培養し、走査型電子顕微鏡(SEM)を用いて菌体の形態変化を観察した。その結果、図1に示す通り、培養24時間後にはMRSAの溶菌が観察された。
【0028】
高温処理の有無により、クマザサ原形質液の抗菌活性に差異は認められなかった。このことから、クマザサ原形質液中の抗菌活性成分の本体は耐熱性成分であると推察される。
【0029】
実施例2 クマザサ葉抽出物による抗生物質の抗菌活性増強作用
1. MRSAに対する各種抗生物質の抗菌活性の増強作用
(1) MRSAに対するアンピシリンの抗菌活性の増強作用
クマザサ原形質液とアンピシリン(ABPC)とを併用した際の、MRSAに対する抗菌活性の増強効果を調べた。増強効果の測定はチェッカーボード法により行なった。プレートの横方向に向かってクマザサ原形質液の12.5、6.3、3.2、1.6、0.8、0.4、0.2、0.1、0.05、0.03、0.0までの11段階の希釈系列を調製した。また、プレートの縦方向に向かってアンピシリンの16段階の希釈系列(原液512μg/mlを1倍とし、2〜214倍希釈及び0.0μg/ml)を調製した。各ウェルに75×103細胞/ウェルとなるように菌液(MRSA N315菌株)を接種して37℃にて24時間培養後、増殖の判定を行なった。FIC indexは次式により算出した。結果を表2に示す。
FIC index={クマザサのMIC(併用時)/クマザサのMIC(単独)}+{ABPCのMIC(併用時)/ABPCのMIC(単独)}
【0030】
【表2】

【0031】
FIC indexは数値が1より小さいほど相乗効果が高い。MRSA N315株に対しては、アンピシリン0.5〜1μg/ml、クマザサ原形質液0.4v/v%で相乗効果が高かった。
【0032】
(2) MRSAに対するテトラサイクリン及びバンコマイシンの抗菌活性の増強作用
クマザサ原形質液がテトラサイクリン(TC)及びバンコマイシン(VCM)の抗菌活性を増強するか否か検討した。菌株としてMRSA N315株を用いて、上記チェッカーボード法により行なった。クマザサ原形質液は12.5v/v%〜0v/v%の11段階の希釈系列とした。TCは1, 0.5, 0.25, 0.125, 0.063, 0.031, 0.016, 0.0μg/mlの8段階、VCMは8, 4, 2, 1, 0.5, 0.25, 0.125, 0.0μg/mlの8段階とした。TC単独でのMICは0.5μg/ml、VCM単独でのMICは1μg/mlだった。結果を下記表3に示す。表中には上記したABPCについての結果も併せて示す。
【0033】
【表3】

【0034】
VCMとの併用ではMRSAに対して相加効果が認められた。TCとの併用では、TCの抗菌活性の増強作用は認められなかった。
【0035】
ABPCはβ−ラクタム系抗生物質のうちのペニシリン系抗生物質である。β−ラクタム系抗生物質は、細菌の細胞壁合成の最終段階に関与する酵素であるペニシリン結合タンパク質に結合して活性を阻害し、これにより抗菌活性を発揮する。TCはテトラサイクリン系抗生物質であり、リボソームに作用してタンパク質合成を阻害することで抗菌活性を発揮する。VCMはグリコペプチド系抗生物質であり、細胞壁合成酵素の基質に結合して細胞壁合成を阻害することにより抗菌活性を発揮する。クマザサ原形質液による抗生物質の抗菌活性の増強作用の機序として、クマザサ原形質液中の成分が細菌の細胞壁合成になんらかの影響を及ぼしている可能性が考えられる。
【0036】
(3) クマザサ抽出物の高温処理の影響について
高温処理したクマザサ原形質液を用いて、上記と同様にMRSAに対する各種抗生物質の抗菌活性の増強効果を評価した。結果を下記表4に示す。
【0037】
【表4】

【0038】
ABPCへの相乗効果は高温処理により失われなかったが、VCMへの相加効果は高温処理により失われ、増強効果が認められなかった。抗生物質の抗菌活性を増強する作用に重要なクマザサ成分は、抗生物質の種類により異なると推察される。
【0039】
(4) MSSAに対するABPC併用の効果について
MSSA ATCC6538株とMRSA N315株について、上記チェッカーボード法によりアンピシリン及びクマザサ併用時のそれぞれのMICを測定した。クマザサ原形質液としては、高温処理と非処理(サンクロン)の2通りを検討した。その結果、図2に示す通り、高温処理及び非処理いずれもMRSAに対してABPCの抗菌活性を増強する作用が認められた。相乗効果に重要な成分も耐熱性の成分であると推察される。MSSAに対しては、ABPCの抗菌活性の増強は認められなかった。
【0040】
2.VREに対する各種抗生物質の抗菌活性の増強作用
上記チェッカーボード法により、腸球菌に対して各種抗生物質とクマザサ原形質液とを併用した際のMICを測定し、抗菌活性の増強効果を評価した。腸球菌として、VRE NTCT12201株とVSE JCM5804株を用いた。結果を表5及び6に示す。また、VRE NTCT12201株に対する併用効果の結果をまとめて表7に示す。なお、表5及び表6中、各種抗生物質のMICの単位はμg/ml、クマザサ原形質液のMICの単位はv/v%である。
【0041】
【表5】

【0042】
【表6】

【0043】
【表7】

【0044】
図3は、VSE JCM5804株(図3A)、VRE NTCT02000株(図3B)、VRE NTCT12201株(図3C)に対してクマザサ原形質液と各種抗生物質とを併用した際のMIC値の変化を示すグラフである。感受性菌のVSEに対しては、いずれの抗生物質でも、クマザサ原形質液を併用してもMICの低下は認められなかった。耐性菌のVREに対しては、検討した全ての抗生物質でクマザサ併用によるMICの低下が観察された。
【図面の簡単な説明】
【0045】
【図1】1.6v/v%クマザサ原形質液含有培地中で24時間培養したMRSA N315株の形態を走査型電子顕微鏡(SEM)で観察した写真である。
【図2】MRSAとMSSAに対してクマザサ原形質液とアンピシリンとを併用した際のMIC値の変化を示すグラフである。
【図3】VSEとVREに対してクマザサ原形質液と各種抗生物質とを併用した際のMIC値の変化を示すグラフである。A)VSE JCM5804株、B)VRE NTCT02000株、C)VRE NTCT12201株。
【特許請求の範囲】
【請求項1】
クマザサ葉抽出物を有効成分として含むグラム陽性細菌用抗菌剤。
【請求項2】
前記グラム陽性細菌は抗生物質耐性菌である請求項1記載の抗菌剤。
【請求項3】
前記抗生物質耐性菌は、バンコマイシン耐性菌、アンピシリン耐性菌又はメチシリン耐性菌である請求項2記載の抗菌剤。
【請求項4】
前記抗生物質耐性菌は、バンコマイシン耐性腸球菌又はメチシリン耐性黄色ブドウ球菌である請求項3記載の抗菌剤。
【請求項5】
クマザサ細胞の原形質成分を有効成分とする請求項1ないし4のいずれか1項に記載の抗菌剤。
【請求項6】
請求項1ないし5のいずれか1項に記載の抗菌剤と、β−ラクタム系抗生物質、グリコペプチド系抗生物質及びテトラサイクリン系抗生物質からなる群より選択される少なくとも1種の抗生物質との組み合わせを含むグラム陽性細菌用抗菌剤。
【請求項7】
前記β−ラクタム系抗生物質はペニシリン系抗生物質である請求項6記載の抗菌剤。
【請求項8】
前記ペニシリン系抗生物質はアンピシリンである請求項7記載の抗菌剤。
【請求項9】
前記グリコペプチド系抗生物質はバンコマイシンである請求項6ないし8のいずれか1項に記載の抗菌剤。
【請求項10】
前記テトラサイクリン系抗生物質はテトラサイクリンである請求項6ないし9のいずれか1項に記載の抗菌剤。
【請求項11】
クマザサ葉抽出物を有効成分として含む抗菌活性増強剤。
【請求項12】
抗生物質耐性菌に対する抗生物質の抗菌活性を増強する請求項11記載の抗菌活性増強剤。
【請求項13】
メチシリン耐性菌に対するβ−ラクタム系抗生物質又はグリコペプチド系抗生物質の抗菌活性を増強する請求項12記載の抗菌活性増強剤。
【請求項14】
アンピシリン又はバンコマイシンの抗菌活性を増強する請求項13記載の抗菌活性増強剤。
【請求項15】
前記メチシリン耐性菌はメチシリン耐性黄色ブドウ球菌である請求項13又は14記載の抗菌活性増強剤。
【請求項16】
バンコマイシン耐性菌に対するβ−ラクタム系抗生物質、グリコペプチド系抗生物質又はテトラサイクリン系抗生物質の抗菌活性を増強する請求項12記載の抗菌活性増強剤。
【請求項17】
アンピシリン、バンコマイシン又はテトラサイクリンの抗菌活性を増強する請求項16記載の抗菌活性増強剤。
【請求項18】
前記バンコマイシン耐性菌はバンコマイシン耐性腸球菌である請求項16又は17記載の抗菌活性増強剤。
【請求項19】
クマザサ細胞の原形質成分を有効成分とする請求項11ないし18のいずれか1項に記載の抗菌活性増強剤。
【請求項1】
クマザサ葉抽出物を有効成分として含むグラム陽性細菌用抗菌剤。
【請求項2】
前記グラム陽性細菌は抗生物質耐性菌である請求項1記載の抗菌剤。
【請求項3】
前記抗生物質耐性菌は、バンコマイシン耐性菌、アンピシリン耐性菌又はメチシリン耐性菌である請求項2記載の抗菌剤。
【請求項4】
前記抗生物質耐性菌は、バンコマイシン耐性腸球菌又はメチシリン耐性黄色ブドウ球菌である請求項3記載の抗菌剤。
【請求項5】
クマザサ細胞の原形質成分を有効成分とする請求項1ないし4のいずれか1項に記載の抗菌剤。
【請求項6】
請求項1ないし5のいずれか1項に記載の抗菌剤と、β−ラクタム系抗生物質、グリコペプチド系抗生物質及びテトラサイクリン系抗生物質からなる群より選択される少なくとも1種の抗生物質との組み合わせを含むグラム陽性細菌用抗菌剤。
【請求項7】
前記β−ラクタム系抗生物質はペニシリン系抗生物質である請求項6記載の抗菌剤。
【請求項8】
前記ペニシリン系抗生物質はアンピシリンである請求項7記載の抗菌剤。
【請求項9】
前記グリコペプチド系抗生物質はバンコマイシンである請求項6ないし8のいずれか1項に記載の抗菌剤。
【請求項10】
前記テトラサイクリン系抗生物質はテトラサイクリンである請求項6ないし9のいずれか1項に記載の抗菌剤。
【請求項11】
クマザサ葉抽出物を有効成分として含む抗菌活性増強剤。
【請求項12】
抗生物質耐性菌に対する抗生物質の抗菌活性を増強する請求項11記載の抗菌活性増強剤。
【請求項13】
メチシリン耐性菌に対するβ−ラクタム系抗生物質又はグリコペプチド系抗生物質の抗菌活性を増強する請求項12記載の抗菌活性増強剤。
【請求項14】
アンピシリン又はバンコマイシンの抗菌活性を増強する請求項13記載の抗菌活性増強剤。
【請求項15】
前記メチシリン耐性菌はメチシリン耐性黄色ブドウ球菌である請求項13又は14記載の抗菌活性増強剤。
【請求項16】
バンコマイシン耐性菌に対するβ−ラクタム系抗生物質、グリコペプチド系抗生物質又はテトラサイクリン系抗生物質の抗菌活性を増強する請求項12記載の抗菌活性増強剤。
【請求項17】
アンピシリン、バンコマイシン又はテトラサイクリンの抗菌活性を増強する請求項16記載の抗菌活性増強剤。
【請求項18】
前記バンコマイシン耐性菌はバンコマイシン耐性腸球菌である請求項16又は17記載の抗菌活性増強剤。
【請求項19】
クマザサ細胞の原形質成分を有効成分とする請求項11ないし18のいずれか1項に記載の抗菌活性増強剤。
【図2】


【図3】


【図1】




【図3】


【図1】


【公開番号】特開2010−59100(P2010−59100A)
【公開日】平成22年3月18日(2010.3.18)
【国際特許分類】
【出願番号】特願2008−226702(P2008−226702)
【出願日】平成20年9月4日(2008.9.4)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成20年3月5日 日本薬学会第128年会組織委員会発行の「日本薬学会第128年会要旨集」に発表
【出願人】(505155528)公立大学法人横浜市立大学 (101)
【Fターム(参考)】
【公開日】平成22年3月18日(2010.3.18)
【国際特許分類】
【出願日】平成20年9月4日(2008.9.4)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成20年3月5日 日本薬学会第128年会組織委員会発行の「日本薬学会第128年会要旨集」に発表
【出願人】(505155528)公立大学法人横浜市立大学 (101)
【Fターム(参考)】
[ Back to top ]

