ゲル中の被分析物に試薬を加える方法及び装置
本発明は、ゲル中の被分析物に試薬を加える方法及び装置に関するものであり、本発明は、さらに、液状の分先対称物質と試薬の混合物を、ゲルから、第二の容器、例えばマイクロタイタープレートに移す方法及び装置を提供する。本発明は、生体分子、例えば、核酸、炭水化物、タンパク質、ペプチドの操作に有用である。特に、本発明は、等電点電気泳動のゲル中でタンパク質及びペプチドを操作する用途に用いることができる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、ゲル中の被分析物に試薬を加える方法及び装置に関するものであり、特に、生体分子、例えばペプチド、タンパク質、炭水化物、又は核酸の分離に使用したゲルに試薬を加える方法及び装置に関するものである。
【背景技術】
【0002】
生体分子、例えばタンパク質、ペプチド、核酸の識別及び定量を行う前に、或いは、そうした識別及び定量と並行して、それらの生体分子を分離するには、各種の方法を用いることができる。こうした生体分子をサイズ及び/又は帯電の有無によって分離する場合には、一般に、ゲル電気泳動が利用される。
【0003】
今日では、タンパク質やペプチドの種類や組成の判別は、質量分析を用いて行うことが多い。この場合、必要な情報を集めることができるように、まず第一の工程で、タンパク質を、酵素的手段又は化学的手段によってペプチドに切断する。最も一般的なアプローチは、タンパク質を特定のアミノ酸残基で切断する酵素を用いて消化を行う酵素消化法で、典型的な酵素としては、タンパク質をリジン又はアルギニン残基の後ろで加水分解するトリプシンを挙げることができる。極めて限られた数のタンパク質を含むサンプルでトリプシンによる消化を行う場合には、存在するタンパク質の種類を、消化によって得られたペプチドの質量から判定することが可能である。識別の目的で使用される第二のアプローチは、一次質量スペクトルで分離されたイオンから、衝突誘発二次質量スペクトルイオンを生成するアプローチである。二次質量スペクトルは、ペプチドを構成するアミノ酸残基の質量についての情報を含んでいるので、こうした質量を、一次スペクトルから選んだイオンの質量と組み合わせたものを、トリプシンペプチド並びにこのペプチドに対応するタンパク質の識別に使用することができる。MS/MSスペクトルは、酵素によって消化したペプチドの識別や特性解析ばかりでなく、生体サンプル中にもともと存在するペプチドにも利用できることはいうまでもない。プロテオームの研究では、MS又はMS/MSを、タンパク質の識別ばかりでなく、相対的定量化にも使用することが通例となっている(Aebersoldら; Nature, 2003, 422, 198−207)。
【0004】
MALDI−MSのターゲットに適用するサンプルは、限られた数のペプチドしか含有できず、同様に、ESI−MSの場合も時間単位あたり、限られた数のペプチドしか許容されない。サンプルは、通常、何千ものタンパク質を含む極めて複雑な混合物で、こうした数のタンパク質は、消化後は、10万以上〜百万以上のペプチドと対応することになる。したがって、質量分析による特性解析や定量化を行う前に、ペプチドをしっかりと分離しておく必要があり、その際には、電気泳動やクロマトグラフィーに基づいた方法をはじめとする様々な分離方法を使用することができ、通常、複数の分離工程が必要とされる。
【0005】
こうした分離は、トリプシンによる消化を行う前に、タンパク質のレベルでのみ行うこともできる。こうしたアプローチの典型例は、二次元(2−D)電気泳動である。或いは、第一工程で、タンパク質のレベルで分離しておいてから、消化を行い、最後に得られたペプチドを質量分析の前に分離することもできる。このアプローチの一例では、タンパク質のレベルで逆相クロマトグラフィー(RPC)を使用し、その後、消化を行ってから、得られたペプチドを、ESI MS/MSを行う前に逆相クロマトグラフィーで分離する。また、別のアプローチとしては、タンパク質のレベルでSDS−電気泳動を行っておいてから、消化を行い、さらにRPCを行う方法が記載されている(Breciら; Proteomics, 2005, 5, 2018−2028)。最後に、トリプシンによる消化を行ってから、ペプチドのレベルで多次元分離を行うことができる。こうしたタイプのアプローチとしては、MudPit(Washburnら、Nat Biotechnol., 2001, 19, 242−247)、より従来法的なイオン交換クロマトグラフィーを行っておいてからRPCを行う方法(Pengら、Journal of Proteome Research, 2003, 2, 43−50)、ペプチドの等電点電気泳動(IEF)を行ってからRPCを行う方法(Cargileら; Electrophoresis, 2004, 25, 936−945)を挙げることができる。
【0006】
トリプシンによる消化を第一工程として行う場合には、別のアプローチとして、ペプチドの小分画を選択しうるような方法を使用することによって、サンプルの複雑さを下げるようなアプローチを挙げることができる(例えば、iCAT [Aebersoldら、Proteomics, 2005, 5, 380−387] 又はCOFRADIC [Vandekerckhoveら、Nat Biotechnol., 2003, 21, 566−569])。
【0007】
一般に、IEFやSDS電気泳動のような電気泳動技術は、ゲル中でタンパク質のレベルで使用した場合には、クロマトグラフィーを利用した方法より、解像度及びタンパク質収量がはるかに高い。これらの2種の方法、すなわちIEFとSDSを組み合わせた二次元電気泳動も、極めて複雑なサンプルの分離を、タンパク質レベルで行う場合には、普通に使用されるアプローチである。しかし、電気泳動技術には、労働集約的で、熟練を要することが多く、自動化が困難だという欠点がある。
【0008】
また、被分析物をゲルから抽出する際にも、様々な問題がある。
【0009】
電気泳動のゲルを処理して、ペプチド、タンパク質、炭水化物、又は核酸を含むゲル分画を回収し、さらなる分離に備えたり、被分析物を分析できるようにしたりする過程では、操作者は様々な困難に遭遇する。ゲルがガラス又はプラスチックの板上に存在する場合には、個々のバンド又は分画をプレートからブロッティングしたり、スパチュラ又は鋭利なナイフなどを用いて掻き取ったりして、第二ゲル又は反応容器に注意深く移して、さらなる分析に備える必要がある。IPGストリップの場合のように、ゲルがプラスチックシートに担持されている場合には、ストリップを、はさみ又は鋭利な刃物で細かい断片に注意深く切断してから、この断片を別のゲル又は反応容器に移して、さらなる処理/分析に備えることになる。
【0010】
ゲルからバンド又はスポットを回収する自動サンプリングシステムは公知であり、例えば、国際公開第02/071072号に記載されている。実際、二次元電気泳動では、自動ピッカーが頻繁に用いられて、そうした場合には、ゲルは、タンパク質又はペプチドサンプルを検出する目的で染色されるのが通常である。しかし、こうしたシステムでは、大抵の場合、ゲルをピペットに吸引するので、ピペットの内外に吸着したゲルが失われる。さらに、こうしたシステムでは、タンパク質/ペプチドの染色が必要で、サンプルが失われたり汚染したりすることのないよう、装置を注意深く操作せねばならないので、作業が労働集約的で、多大な時間を要することになる。
【0011】
当業者であれば、ゲルのバンド又は分画を手動でプレート又はストリップから回収するプロセスというのは、ゲルを適切な数の分画に均等に分割して、ゲルから確実に被分析物を定量的に回収できるようにせねばならず、また、この移動の過程で使用する「汚染した」器具類によるクロスコンタミネーションを防止する必要があり、しかも入念に作業を進めねばならず、きわめて時間のかかる作業となることがあることがわかるはずである。このクロスコンタミネーションの問題は、IPGストリップを用いて被分析物を分離し、さらなる処理/分析に備えて、ストリップをはさみやメスを用いてバンドに切り離す場合には、特に重要である。というのも、こうした器具の刃は、ストリップからゲルの次のバンドを切り出す前に十分に清浄化しておく必要があるからである。また、こうしたプロセスは、一般に、ペプチド又はタンパク質を検出する目的でゲルを予め染色しておく工程をさらに含むので、システムが極度に労働集約的となる。
【0012】
当業者であれば、さらなる処理に備えて、ゲルのバンドをプレート又はIPGストリップから回収し、第二のゲル又は反応容器に移動する際に生じる上述のような問題が、バンド又は分画の数が増えるにつれて深刻になることもわかるはずである。したがって、例えば、IPGストリップを50個程度に分割し、その50個ほどの分割片のそれぞれを、別のゲル又は反応容器に移すような場合には、クロスコンタミネーションの可能性が増し、回収量が減る可能性が高まることになる。
【0013】
ゲルからのサンプル抽出に伴う問題を回避するために、等電点電気泳動による分離を、液相で実施することもできる(Zuoら; Methods Mol Biol., 2004, 244, 361−75)。Zuoらが使用した装置は、膜によって隔てられ、滴定によって特定のpHの値に保持された一連のチャンバーを備えている。しかし、このアプローチの不利な点として、ペプチドやタンパク質は、等電点付近では溶解度が低く、その結果、沈殿や凝集が生じて、等電点電気泳動の間のペプチドやタンパク質の解像度が低くなってしまうことを挙げることができる。
【0014】
Michelら(Electrophoresis, 2003, 24, 3−11)には、生体サンプルを等電点(pI)によって分画し、化合物を直接回収してさらなる分析に使用する方法が記載されている。この「オフ−ゲル(off−gel)IEF」と名づけられた方法では、IPGストリップを、両端が開放したマルチウェル器具を使用して、一連のウェルに分割し、タンパク質サンプルをIPGバッファーに加え、その後、電気泳動を実施して、タンパク質混合物を分離する。その後、各ウェルの内容物を取り出して、質量分析によるタンパク質の分析を行うのだが、この方法では解像度は0.1pH単位であった。しかし、上述のZuoらのアプローチと同じく、電気泳動の間にタンパク質は液相中に存在しており、その結果、沈殿や凝集の危険性が増大する。このMichelらのアプローチでは、タンパク質は、マルチウェル器具に溶液を加えることなく、ゲルのみで電気泳動を行った場合と比較して、電界のずっと低い領域に存在する形状となっている。そのため、従来のゲルでの電気泳動に比べて、この電気泳動では解像度が低く、電気泳動に要する時間も長くなる。
【0015】
同じグループ(Hellerら.; Electrophoresis, 2005, 26, 1174−1188)が、最近、タンパク質とそのアイソフォームの分離と識別に、「オフ−ゲルIEF」を利用することについて報告している。この方法は、二段階法で、第一段階で、タンパク質とそのアイソフォームをpIを利用して分離し、第二段階で、トリプシン処理したペプチド断片の分離と識別を行う。
【0016】
IEFは、分離したタンパク質を、膜で隔てられたチャンバーに入った溶液中に回収する形状でも実施できる(Righettiら; J. Biochem. Biophys. Meth., 1987, 15, 199−206)。このアプローチも、等電点に近いタンパク質は、凝集や沈殿を生じやすいという事実によって制限される。
【0017】
タンパク質を含むゲル断片をゲルから単離し、タンパク質分解性の消化を行い、その後、生成した切断ペプチドを識別するゲル中でのタンパク質処理方法を記載した他のシステムも開示されている。国際公開第02/071072号には、自動化されたシステムが記載されており、このシステムでは、単離したタンパク質−ゲル断片を、底部に疎水性フィルター膜が設けられた第一マイクロタイタープレートの対応する数の反応容器に、ロボットアーム装置で直接移動し、プロテアーゼとともにインキュベートする。加水分解の後、ペプチド生成物は、疎水性フィルター膜を通して第二マイクロタイタープレートへと濾過され、さらなる分析に備えて濃縮される。
【0018】
このように、ゲル中で電気泳動で分離を行うことによって卓越した解像度が得られるものの、上述したように、ゲルから液相にサンプルを移動する際には問題が生じることも多く、そのため、自動化が困難となっている。
【特許文献1】国際公開第02/071072号パンフレット
【非特許文献1】Aebersold et al; Nature, 2003, 422, 198-207
【非特許文献2】Breci et al; Proteomics, 2005, 5, 2018-2028
【非特許文献3】Washburn et al; Nat Biotechnol., 2001, 19, 242-247
【非特許文献4】Peng et al; Journal of Proteome Research, 2003, 2, 43-50
【非特許文献5】Cargile et al; Electrophoresis, 2004, 25, 936-945
【非特許文献6】Aebersold et al; Proteomics, 2005, 5, 380-387
【非特許文献7】Vandekerckhove et al; Nat Biotechnol., 2003, 21, 566-569
【非特許文献8】Zuo et al; Methods Mol Biol., 2004, 244, 361-75
【非特許文献9】Michel et al; Electrophoresis, 2003, 24, 3-11
【非特許文献10】Heller et al; Electrophoresis, 2005, 26, 1174-1188
【非特許文献11】Righetti et al; J. Biochem. Biophys. Meth., 1987, 15, 199-206
【発明の開示】
【発明が解決しようとする課題】
【0019】
したがって、本発明の目的は、先行技術の諸問題を軽減しつつ、ゲル分画を調製して、さらなる処理や操作を可能とする方法及びシステムを提供することにある。本発明の別の目的は、被分析物を検出するために、ゲルを予め染色しておく必要がない方法及びシステムを提供することにある。本発明のさらに別の目的は、化学的又は酵素的修飾の前又は後に、試薬をゲル分画に加えて、被分析物をゲルから溶出させる方法及びシステムを提供することにある。
【課題を解決するための手段】
【0020】
本発明の第一の態様では、ゲル中の被分析物に試薬を加える方法を提供する。この方法は、
i)端部が開放しており、それぞれ1以上の壁部で画成されたチャンバーが複数設けられた本体を備えるマルチウェルテンプレートを、ゲルに向かって移動させて、ゲルと1以上の壁部との間に複数のウェルを形成する工程と、
ii)必要に応じて、被分析物を、クロマトグラフィー又は電気泳動によってゲル中で分離する工程と、
iii)上記のウェルの1以上に試薬を加えて、液上の被分析物と試薬の混合物を生成する工程を含む方法であって、
試薬は、被分析物を溶解するか、被分析物又はその環境を修飾・変化しうるものである。
【0021】
試薬は、バッファーとするのが適当で、バッファーのpHは、との特定の被分析物に応じて変化させることができる。
【0022】
試薬を、酸又はアルカリとするのも適当で、この酸又はアルカリは、被分析物、又は、被分析物が存在している環境を変化させることができる。
【0023】
試薬を、酵素とするのも適当で、この酵素は、加水分解酵素であるのが好ましく、核酸分解酵素又はタンパク質分解酵素であるのがさらに好ましく、タンパク質分解酵素であるのが特に好ましい。
【0024】
試薬は、検出可能な成分とするのが適当であり、こうした検出可能なマーカーは、例えば、アイソトープ又は蛍光標識を含むものとすることができる。
【0025】
ゲルは、シート上に担持されているのが適当である。
【0026】
この方法は、ゲル又はシートをベースプレートに載置する工程をさらに含むものとするのが適当である。ベースプレートは、例えば、水平電気泳動装置の冷却プレートに対応するものとすることもできる。
【0027】
この方法は、ゲル又はシートをリテーナに載置する工程をさらに含むものとするのが適当である。
【0028】
この方法は、ゲル又はシート、或いはリテーナを、ベースプレートの所定の位置に位置決めする工程をさらに含むものとするのが適当であり、ベースプレートの一方の表面上には、この表面上で、ゲル又はシート、或いはゲル又はシートのリテーナを位置決めするための1以上の凹部及び/又は凸部がさらに設けられていることが好ましい。
【0029】
リテーナの一方の表面上には、ゲル又はシートを受け止めるための1以上の凹部又は凸部が設けられているのが適当である。このリテーナの1以上の凹部又は凸部には、シートを位置決めするための位置決め手段がさらに設けられていることが好ましい。
【0030】
この方法は、マルチウェルテンプレートを、トッププレートの開口部に挿入する工程をさらに含むのが適当である。
【0031】
この方法は、マルチウェルテンプレートに設けられた開放端チャンバーの位置に対応する複数の開口部が設けられた固定用ストリップを、トッププレート内に載置されたマルチウェルテンプレートの端部を覆うように装着する工程をさらに含むのが適当である。
【0032】
ベースプレート及び/又はトッププレート及び/又は固定用ストリップは、ゲルの所定位置に形成された複数のウェルを、ベースプレート及びトッププレートに対して位置決めするための固定手段をさらに備えていることが好ましいまた、この固定手段は、ベースプレートに設けられたネジ穴と、トッププレートに設けられたネジ用の開口部と、固定用ストリップとを含むものとするのが、さらに好ましい。
【0033】
ゲルは、好ましくは、ポリアクリルアミドゲルであり、より好ましくは、SDSゲル又は等電点電気泳動ゲルである。
【0034】
マルチウェルテンプレートの本体は、第一部分と第二部分とに分かれたものとし、第一部分は、トッププレートの開口部への挿入に適した形状、第二部分は、ゲルに向かって移動するのに適した基部に向かって傾斜のついた形状とすることが適当である。第一部分と第二部分とは、トッププレートの開口部内にマルチウェルテンプレートを担持するためのフランジによって隔てられていることが好ましい。
【0035】
被分析物は、ペプチド、タンパク質、核酸、又は炭水化物とするのが適当であり、ペプチド又はタンパク質とするのが好適である。
【0036】
マルチウェルテンプレートをゲルに向かって移動させるのは、クロマトグラフィー又は電気泳動によってゲル中で被分析物を分離した後とするのが好適である。しかし、状況によっては、クロマトグラフィー又は電気泳動によってゲル中で被分析物を分離する前に、マルチウェルテンプレートをゲルに向かって移動させることが好ましい場合もある。こうした場合には、マルチウェルテンプレートとゲルによって形成された1以上のウェルに、液状の試薬を加える前に、クロマトグラフィー又は電気泳動による分離を完了させておくものと理解されたい。
【0037】
液状の試薬は、手動で、例えばピペットを使用することによって加えるのが適当である。
【0038】
この方法は、液状の被分析物と試薬の混合物を、手動又は自動化された手段で第二容器に移す工程をさらに含むものとするのが適当である。手動の手段の例としては、手動で操作するピペットを挙げることができ、自動化手段の例としては、自動化又はプログラマブルな液体取扱い装置を挙げることができる。
【0039】
この第二容器は、マイクロタイタープレートのウェルとするのが好ましい。
【0040】
試薬を、自動液体取扱い装置で加えるか、及び/又は、液状の被分析物と試薬の混合物を、自動液体取扱い装置で移すのが適当である。自動液体取扱い装置は、コンピュータで制御するものとするのが好ましい。
【0041】
本発明の第二の態様では、上述の方法を実施するためのシステム提供する。このシステムは、
i)端部が開放しており、それぞれ1以上の壁部で画成されたチャンバーが複数設けられた本体を備えたマルチウェルテンプレートと、
ii)自動液体取扱い装置と
を備えている。
【0042】
このシステムは、コンピュータで制御するものとすることが好ましい。
【0043】
次に、本発明の方法及び装置を、図面を参照しつつ説明する。
【発明を実施するための最良の形態】
【0044】
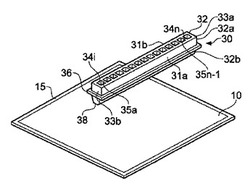
試薬は、図1に示すマルチウェルテンプレート(30)を使用することによって、請求の範囲に記載した方法にしたがって、ゲル(10)中に存在する被分析物に加えることができる。図には、プラスチック又は金属など、適当な材料から形成されたマルチウェルテンプレート(30)を、プラスチック又はガラスなどで形成されたシート(15)で担持されたポリアクリルアミドゲル(10)に載置したところを示してある。ゲル(10)は、被分析物を含んでおり、この被分析物は、通常、電気泳動で分離ずみである。つまり、ゲルは、例えば、タンパク質又はペプチドを含むことができる。マルチウェルテンプレート(30)は、2枚の細長い側壁部(31a、31b)と、その末端に接合された2枚の末端壁部(33a、33b)を備えた細長い本体(32)から構成されている。本体(32)の長軸に沿って、端部が開放したチャンバー(34i〜n)が複数配置され、隣接チャンバー同士は、間に介在する壁部(35a〜35n−1)によって隔てられており、各壁部(35a〜35n−1)は、側壁部31aからもう一方の側壁部31bまで延在している。各チャンバー(34)の形状は、円、楕円、多角形、正方形、長方形(図示)など、各種のものとすることができる。
【0045】
マルチウェルテンプレート(30)をゲル(10)に向かって移動させ、マルチウェルテンプレートの本体のテーパー部分(32b)でゲル(10)を押して、マルチウェルテンプレートの基部(38)が、ゲル(10)を担持しているシートと近接するようにする。マルチウェルテンプレート(30)がこの位置に来ると、ウェルが画成され、ゲル又はプラスチックシートがウェルの底部を、テンプレートの壁部がウェルの壁部を画成することになる。
【0046】
液状の試薬、例えばバッファー又はタンパク質分解酵素の溶液を、1以上のウェル(34)に加え、液状の被分析物と試薬の混合物を形成する。試薬がバッファーなどの場合には、試薬によって被分析物が溶解され、(試薬がタンパク質分解酵素やタンパク質などの場合には、)試薬によって被分析物が修飾され、(試薬が酸などの場合には、)試薬によって被分析物が存在している環境が変化する。
【0047】
図2に、ゲル中の被分析物に試薬を加える際に使用することのできる別の装置の図を図2に示す。ゲル(110)、例えばSDSゲルが、シート(115)の表面に載置されている。シート(115)は、プラスチック又は金属材料製のベースプレート(120)に載置され、このベースプレート(120)には、シートをベースプレート(120)に対して所定位置に位置させるための凹部(122)が設けられている。ベースプレート(120)の四隅には、固定手段であるネジ穴(124a−c、124dは図示せず)が設けてあるので、ベースプレート(120)のネジ(図示せず)を、トッププレート(140)の所定位置に固定することができる。なお、固定手段としては、他の形状のもの(例えば、留め金、クランプ、ピン、穴、スナップ)も使用できる。
【0048】
ゲルには、プラスチック、金属、セラミクス、又は複合材料など、任意の適当な材料から形成されたマルチウェルテンプレート(130)で、複数のウェルを形成する。マルチウェルテンプレート(130)は、2枚の細長い側壁部(131a、131b)と、その末端に接合された2枚の末端壁部(133a、133b)を備えた細長い本体(132)から構成されている。本体(132)の長軸に沿って、端部が開放したチャンバー(134i〜n)が複数配置され、隣接チャンバー同士は、間に介在する壁部(135a〜135n−1)によって隔てられており、各壁部(135a〜135n−1)は、側壁部131aからもう一方の側壁部131bまで延在している。各チャンバー(134)は、円、楕円、多角形、正方形、長方形(図示)など、任意の形状とすることができる。
【0049】
マルチウェルテンプレート(130)の本体(132)は、フランジ(136)によって、第一部分(132a)と第二(132b)部分とに分かれており、第一部分(132a)は、トッププレート(140)の開口部(142)への挿入に適した形状、第二部分(132b)は、基部(138)に向かってテーパーがついており、ゲルに押しつけるのに適した形状となっている。図からも理解されるように、マルチウェルテンプレート(130)を下降させ、つまりゲル(110)に向かって押しつけて、テンプレート(130)が、ゲル(110)を担持しているシート(115)に接触又は近接すると、各チャンバー(134)はウェルを形成し、ゲル又はシートがウェルの底部に、チャンバーの壁部(図示せず)がウェルの壁部となる。こうして、ゲル上に、複数のウェルが形成される。マルチウェルテンプレート(130)は、ゲルに向かって下降させ、つまりゲルに押しつけて、ゲル上の複数のウェルを形成する前、又は後に、プラスチック又は金属(例えばステンレス)材料製のトッププレート(140)の開口部(142)に挿入することができる。図示した例では、テンプレート(130)は、フランジ(136)によって、トッププレート(140)の棚部(144)に保持されている。なお、テンプレートは、ゲルを切断するのではなく、押しつけることによって複数のウェルを形成することに注意されたい。ウェルは、トッププレート(140)をベースプレート(120)に対して固定手段(トッププレートに設けられた固定手段(146a〜d)及びベースプレートに設けられた固定手段(124a〜d))によって固定することによって、ベースプレート(120)及びトッププレート(140)に対して所定位置に保持される。図2の例では、ネジ(図示せず)を、トッププレートに設けられた開口部(146a〜d)を通して、ベースプレート(120)に設けられたネジ穴(124a〜d)まで到達させることによって、トッププレート(140)をベースプレート(120)に固定している。ゲルに形成された複数のウェルは、このようにして、トッププレートとベースプレートに対して所定位置に保持されている。
【0050】
図3は、本発明の方法を実施する際に使用することのできる別の装置の斜視図である。図3に示す装置は、等電点電気泳動のジェル、特にIPGストリップ、例えばImmobiline(登録商標)DryStripゲルとともに使用するのに適している。プラスチックの基材シートと、その上に担持されたポリアクリルアミドゲル(210)のコーティングからなるIPGストリップ(図示せず)を、リテーナ(250)に設けられた、電気泳動のマニホールドである凹部(252)に載置する。プラスチック材料製とするのが通例であるリテーナ(250)には、複数のIPGストリップを同時に処理できるよう、複数の凹部(252i〜n)を設けることができ、図3の例では、12個の凹部が示してある。IPGストリップで被分析物を電気泳動した後、リテーナ(250)とストリップとを、ベースプレート(220)上面の凹部(222)の所定位置に載置する。ベースプレートは、プラスチック又は金属材料製とすることができる。上述したのと似た構造をもつマルチウェルテンプレート(230)には、開放端チャンバー(234i〜n)が複数設けられており、このマルチウェルテンプレート(230)を、トッププレート(240)の開口部(242)に挿入して、マルチウェルテンプレート(230)のフランジ(236)が、開口部(242)の棚部(図示せず)によって担持されるようにする。マルチウェルテンプレート(230)とトッププレート(240)は、通常、プラスチック材料製とするが、金属等の他の材料から製造してもよい。トッププレート(240)には、上述のようにして複数のマルチウェルテンプレート(230)を載置することができ、例えば、図示した例では、トッププレート(240)に、マルチウェルテンプレート(230)12個を載置することができる。
【0051】
マルチウェルテンプレート(230)をトッププレート(240)に載置したら、マルチウェルテンプレート(230)を下降させ、つまりゲル(210)の表面まで移動させて、テンプレート本体のテーパー部分(232b)をゲル(210)に対して押しつけ、テンプレートの基部(238)が、ゲル(210)を担持しているプラスチックシートに近接するようにする。この位置では、ウェルが画成され、プラスチックシート又はゲルがウェルの底部に、テンプレートの壁部が、ウェルの壁部となっている。
【0052】
なお、マルチウェルテンプレート(230)をトッププレート(240)に挿入する前に、マルチウェルテンプレート(230)を下降させ、ゲル(210)まで移動させて複数のウェルをゲル上に形成することもできる。マルチウェルテンプレートは、この時点で、固定手段(トッププレートに設けられた固定手段(246a〜d)及びベースプレートに設けられた固定手段(224a〜d、dは図示せず))によって、トッププレート(240)及びベースプレート(220)に対して所定の位置に固定することができ、例えば図2では、ネジ(図示せず)を使用してプレート同士を固定することができる。
【0053】
マルチウェルテンプレート(230)を覆うように固定用ストリップ(260)を載置し、ストリップ(260)の開口部(264i〜n)と、テンプレート(230)の開放端チャンバー(234i〜n)の位置とが、重なり、対応するようにする。こうすると、ストリップに設けられた固定手段(266a〜b)とトッププレートに設けられた固定手段(248i〜n)を使用することで、マルチウェルテンプレート(230)がトッププレート(240)に固定されるので、固定用ストリップ(260)によって、マルチウェルテンプレート(230)が所定位置に固定される。この固定手段は、固定用ストリップ(266a〜b)の開口部、トッププレートに設けられたネジ穴(248i〜n)、及び孔径に合った1以上のネジからなるものとすることができる。別の形態では、固定用ストリップとマルチウェルテンプレートとを一体の部材として形成することもできる。
【0054】
図4は、図3の装置の斜視図で、各構成部品は、図3について記載したのと同様の特徴を備えている。したがって、この装置は、凹部(322)と固定手段(324a〜d、dは図示せず)が設けられたベースプレート(320)を備えている。リテーナ(350)である等電点電気泳動のマニホールドの一連の凹部(352i〜n)内には、プラスチックシートと、このプラスチックシートに担持されたポリアクリルアミドゲル(310)からなるIPGストリップ(図示せず)が保持されている。プラスチック材料製のトッププレート(340)には、複数の開口部(342i〜n)が、リテーナ(310)内のIPGストリップの位置に対応するよう設けられている。トッププレート(340)には、ベースプレートの固定手段(324a〜d)の固定手段に対応する固定手段(346a〜d、及び348i及びn)が設けられている。マルチウェルテンプレート(330)には、開放端チャンバー(334i〜n)が複数設けられ、固定用ストリップ(360)には、マルチウェルテンプレート(330)の開放端チャンバー(334i〜n)の位置に対応する数多くの開口部(364i〜n)と、固定手段(366a及びb)とが設けられている。
【0055】
図4の装置を、図3で説明したのと同様にして使用することによって、ゲル中の被分析物に試薬を加えることができる。
【0056】
図5aに、本発明の方法で使用されるマルチウェルテンプレート(430)の基部(438)を示す。マルチウェルテンプレート(430)の本体(432)の全長にわたって、一連の壁部(433)によって開放端チャンバー(434i〜n)が画成されている。マルチウェルテンプレート(430)の基部に設けられた凹部又はノッチ(437)を使用して、マルチウェルテンプレート(430)を、IPGストリップが担持されているリテーナ(図示せず)の凸部に載置し、マルチウェルテンプレート(430)を、IPGストリップに対して所定位置に位置決めする。
【0057】
図5bは、IPGストリップのプラスチックシート(415)が、マルチウェルテンプレート(430)の基部(438)に位置しているところを示す。図の斜視図では、ゲルは、シート(415)の裏側に位置しているので見えないが、マルチウェルテンプレート(430)の基部(438)と接触している。この位置では、各チャンバー(434)内に位置するシート(415)の基材が、ウェルの底部に、チャンバーの壁部が、ウェルの壁部になっている。
【0058】
図6は、トッププレート(540)の平面斜視図で、このトッププレート(540)は、鋼製である。図には、マルチウェルテンプレート(所定位置に載置)を格納する開口部(5542i〜n)を、ベースプレートに固定するための固定手段(546a〜d)及び固定用ストリップ固定用の固定手段(548i〜n)とともに示す。
【0059】
図7aは、本発明の方法で使用するトッププレート(640)の詳細を示す平面図で、固定用ストリップ(660)によって、マルチウェルテンプレート(図示せず)がトッププレート(640)に固定されている。固定手段(666)である開口部が、トッププレート内のリテーナ(図示せず)の開口部(図6の548i〜nを参照)と同位置に配置されている。
【0060】
図7bは、図7aの配置の詳細を図示した下面図である。マルチウェルテンプレートのテーパーのついた第二部分の基部(638)が、トッププレート(660)の下面から突出しているのが、この角度からははっきりと見える。この基部(638)によって、ゲルが押され、各開放端チャンバー(634i−n)が、ゲル又はゲルの基材シート(図示せず)とともにウェルを形成する。
【0061】
図8は、本発明の自動溶出システムを示す。ゲル、例えばIPGストリップでサンプルを電気泳動した後、上述した本発明の方法を使用して、複数のウェルを形成し、各ウェルにバッファーを加える。次に、各ウェル中のゲルをバッファーで溶出して、被分析物(例えばペプチド)を抽出し、得られた溶出液を、さらなる処理/分析に備えて反応容器に移す。図8は、本発明の装置のトッププレート(740)のウェルから、マイクロタイタープレート(780)のウェル(782i〜n)に溶出液を移動している過程の8チャネルの溶出プローブ(770)を示す。このシステムは、コンピュータ(図示せず)によって制御されている。IPGストリップに形成するウェルの数は、通常、マイクロタイタープレートの長さ又は幅方向のウェルの数(例えば、96ウェルのマイクロタイタープレートであれば、8又は12の倍数)又はこれらの番号の整数分の1(例えば、2、3、4、6)と対応している。
【実施例】
【0062】
等電点電気泳動、蛍光分析、ペプチドの抽出
0.5mgの酵母(Saccharomyces cerevisiae)(II型)のトリプシン処理サンプルを、各5μgのpIマーカー「3.73」、「4.25」、及び「4.54」と混合した。「pIマーカー」は、等電点が既知で、蛍光をスキャンすることによって検出が可能な蛍光標識ペプチドである。蛍光標識としては、Cy5(登録商標)(Amersham Biosciences AB(スウェーデン))を使用し、発光スペクトルは、約660nmで検出した(Ettan DIGE System、ユーザーマニュアル、Amersham Biosciences AB(スウェーデン))。24cmのIPGペプチドストリップ(pH3.4〜4.8)を、350μlの8M尿素とサンプル溶液で、一晩(約15時間、室温)再水和した。再水和したストリップを、Ettan(登録商標)IPGphor(登録商標)のマニホールドに移し、以下のプログラムで等電点電気泳動を行った。
【0063】
勾配500V(1分)、勾配4000V(1.5時間)、勾配6000V(1.5時間)、
勾配10000V(1.5時間)、ステップ10000V(12時間)(合計約150kV時間)。
【0064】
等電点電気泳動ユニットとしては、Ettan IPGphor IIを使用し、泳動は、20℃で行った。
【0065】
導電点電気泳動の後、IPGストリップを、蛍光スキャナー(Typhoon 9400スキャナー、Amersham Biosciences AB(スウェーデン)製)で、660nmにてスキャンして、蛍光pIマーカーの正確な位置を判定した。Typhoonで得られた図を、ImageQuantで評価し、蛍光強度のグラフを描いた。
【0066】
スキャン後、本発明のマルチウェルテンプレートを使用して、ストリップ中のペプチドを、ゲルから液体分画に抽出し、pH勾配を、ストリップに沿った一連の別々の分画に分割した。この方法によって、IPGストリップは、約3mm間隔の72の分画に分割された。72分画のそれぞれに、50μlの水を加え、室温で60分間インキュベートし、抽出されたペプチドを、自動で、マイクロタイタープレートに移動させた。この溶出過程を3回繰り返し、各ウェルから、すべてのペプチドを確実に抽出し、移動させた。抽出後は、マルチウェルテンプレートをIPGストリップから取り外せば、この器具は、清浄後に次の実験に再使用できる。この実験では、IPGペプチドストリップを再度Typhoonでスキャンし、画像をImageQuantで評価した。
【0067】
図9は、抽出前(図9a)と抽出後(図9b)のペプチドIPGストリップの蛍光強度を示す。図9cは、抽出したペプチドサンプルを含むマイクロタイタープレートと、抽出前と抽出後のストリップとを示すが、抽出前と抽出後のストリップには、それぞれ、高レベルと低レベルの蛍光が示されている。これらの図から、ペプチドが、IPGストリップから効果的に抽出され、この時点では、マイクロタイタープレートのウェルに存在していることが明らかである。
【0068】
図10は、IPGストリップの塩基側末端に位置する互いに隣接した7分画中に含まれるすべての識別済みペプチド配列を比較した結果である。比較した7分画中の全部で719個の識別済みペプチドのうち、ペプチドの82%は、1分画のみに存在しており、16%は、2分画に存在していた。この実験結果は、IPGストリップの高解像度を裏付けるばかりでなく、本発明のマルチウェルテンプレートを用いて形成したウェルの間で漏れの問題がなかったことを示すものでもある。
【図面の簡単な説明】
【0069】
【図1】図1は、本発明の方法を実施する際に使用することのできる装置を示す。
【図2】図2は、SDSゲル中に存在する被分析物に試薬を加える際に使用することのできる装置を示す。
【図3】図3は、等電点電気泳動用ゲルであるIPGストリップ中の被分析物に試薬を加える本発明の装置を示す。
【図4】図4は、図3の装置の平面斜視図である。
【図5】図5a及び5bは、本発明の方法で使用するマルチウェルテンプレートの各部を図示したものである。図5aは、テンプレートの基部を示す下面図で、複数の開放端チャンバーが図示されている。図5bは、図5aで、テンプレートの基部にIPGストリップを載置したところである。
【図6】図6は、図3及び4に図示した装置のトッププレートを示す。トッププレートには、マルチウェルテンプレートが挿入されている。
【図7】図7aは、本発明の方法で使用するトッププレートと固定用ストリップの詳細を示す平面図である。図6bは、マルチウェルテンプレートを載置したトッププレートの下面図である。
【図8】図8は、本発明の自動溶出システムを示す。
【図9】図9a及び9bは、蛍光標識ペプチドの分離に使用したIPGストリップの蛍光強度を、本発明の方法でゲルを溶出する前(図9a)と後(図9b)にスキャンしたものである。また、図9cに、IPGストリップの蛍光を、抽出の前後にスキャンした結果を、ストリップから溶出した分画を含むマイクロタイタープレートをスキャンした結果とともに示す。
【図10】図10は、識別されたペプチドが、本発明の方法を使用してゲルから抽出した分画1ないし数個のみに分布していることを示す図である。
【技術分野】
【0001】
本発明は、ゲル中の被分析物に試薬を加える方法及び装置に関するものであり、特に、生体分子、例えばペプチド、タンパク質、炭水化物、又は核酸の分離に使用したゲルに試薬を加える方法及び装置に関するものである。
【背景技術】
【0002】
生体分子、例えばタンパク質、ペプチド、核酸の識別及び定量を行う前に、或いは、そうした識別及び定量と並行して、それらの生体分子を分離するには、各種の方法を用いることができる。こうした生体分子をサイズ及び/又は帯電の有無によって分離する場合には、一般に、ゲル電気泳動が利用される。
【0003】
今日では、タンパク質やペプチドの種類や組成の判別は、質量分析を用いて行うことが多い。この場合、必要な情報を集めることができるように、まず第一の工程で、タンパク質を、酵素的手段又は化学的手段によってペプチドに切断する。最も一般的なアプローチは、タンパク質を特定のアミノ酸残基で切断する酵素を用いて消化を行う酵素消化法で、典型的な酵素としては、タンパク質をリジン又はアルギニン残基の後ろで加水分解するトリプシンを挙げることができる。極めて限られた数のタンパク質を含むサンプルでトリプシンによる消化を行う場合には、存在するタンパク質の種類を、消化によって得られたペプチドの質量から判定することが可能である。識別の目的で使用される第二のアプローチは、一次質量スペクトルで分離されたイオンから、衝突誘発二次質量スペクトルイオンを生成するアプローチである。二次質量スペクトルは、ペプチドを構成するアミノ酸残基の質量についての情報を含んでいるので、こうした質量を、一次スペクトルから選んだイオンの質量と組み合わせたものを、トリプシンペプチド並びにこのペプチドに対応するタンパク質の識別に使用することができる。MS/MSスペクトルは、酵素によって消化したペプチドの識別や特性解析ばかりでなく、生体サンプル中にもともと存在するペプチドにも利用できることはいうまでもない。プロテオームの研究では、MS又はMS/MSを、タンパク質の識別ばかりでなく、相対的定量化にも使用することが通例となっている(Aebersoldら; Nature, 2003, 422, 198−207)。
【0004】
MALDI−MSのターゲットに適用するサンプルは、限られた数のペプチドしか含有できず、同様に、ESI−MSの場合も時間単位あたり、限られた数のペプチドしか許容されない。サンプルは、通常、何千ものタンパク質を含む極めて複雑な混合物で、こうした数のタンパク質は、消化後は、10万以上〜百万以上のペプチドと対応することになる。したがって、質量分析による特性解析や定量化を行う前に、ペプチドをしっかりと分離しておく必要があり、その際には、電気泳動やクロマトグラフィーに基づいた方法をはじめとする様々な分離方法を使用することができ、通常、複数の分離工程が必要とされる。
【0005】
こうした分離は、トリプシンによる消化を行う前に、タンパク質のレベルでのみ行うこともできる。こうしたアプローチの典型例は、二次元(2−D)電気泳動である。或いは、第一工程で、タンパク質のレベルで分離しておいてから、消化を行い、最後に得られたペプチドを質量分析の前に分離することもできる。このアプローチの一例では、タンパク質のレベルで逆相クロマトグラフィー(RPC)を使用し、その後、消化を行ってから、得られたペプチドを、ESI MS/MSを行う前に逆相クロマトグラフィーで分離する。また、別のアプローチとしては、タンパク質のレベルでSDS−電気泳動を行っておいてから、消化を行い、さらにRPCを行う方法が記載されている(Breciら; Proteomics, 2005, 5, 2018−2028)。最後に、トリプシンによる消化を行ってから、ペプチドのレベルで多次元分離を行うことができる。こうしたタイプのアプローチとしては、MudPit(Washburnら、Nat Biotechnol., 2001, 19, 242−247)、より従来法的なイオン交換クロマトグラフィーを行っておいてからRPCを行う方法(Pengら、Journal of Proteome Research, 2003, 2, 43−50)、ペプチドの等電点電気泳動(IEF)を行ってからRPCを行う方法(Cargileら; Electrophoresis, 2004, 25, 936−945)を挙げることができる。
【0006】
トリプシンによる消化を第一工程として行う場合には、別のアプローチとして、ペプチドの小分画を選択しうるような方法を使用することによって、サンプルの複雑さを下げるようなアプローチを挙げることができる(例えば、iCAT [Aebersoldら、Proteomics, 2005, 5, 380−387] 又はCOFRADIC [Vandekerckhoveら、Nat Biotechnol., 2003, 21, 566−569])。
【0007】
一般に、IEFやSDS電気泳動のような電気泳動技術は、ゲル中でタンパク質のレベルで使用した場合には、クロマトグラフィーを利用した方法より、解像度及びタンパク質収量がはるかに高い。これらの2種の方法、すなわちIEFとSDSを組み合わせた二次元電気泳動も、極めて複雑なサンプルの分離を、タンパク質レベルで行う場合には、普通に使用されるアプローチである。しかし、電気泳動技術には、労働集約的で、熟練を要することが多く、自動化が困難だという欠点がある。
【0008】
また、被分析物をゲルから抽出する際にも、様々な問題がある。
【0009】
電気泳動のゲルを処理して、ペプチド、タンパク質、炭水化物、又は核酸を含むゲル分画を回収し、さらなる分離に備えたり、被分析物を分析できるようにしたりする過程では、操作者は様々な困難に遭遇する。ゲルがガラス又はプラスチックの板上に存在する場合には、個々のバンド又は分画をプレートからブロッティングしたり、スパチュラ又は鋭利なナイフなどを用いて掻き取ったりして、第二ゲル又は反応容器に注意深く移して、さらなる分析に備える必要がある。IPGストリップの場合のように、ゲルがプラスチックシートに担持されている場合には、ストリップを、はさみ又は鋭利な刃物で細かい断片に注意深く切断してから、この断片を別のゲル又は反応容器に移して、さらなる処理/分析に備えることになる。
【0010】
ゲルからバンド又はスポットを回収する自動サンプリングシステムは公知であり、例えば、国際公開第02/071072号に記載されている。実際、二次元電気泳動では、自動ピッカーが頻繁に用いられて、そうした場合には、ゲルは、タンパク質又はペプチドサンプルを検出する目的で染色されるのが通常である。しかし、こうしたシステムでは、大抵の場合、ゲルをピペットに吸引するので、ピペットの内外に吸着したゲルが失われる。さらに、こうしたシステムでは、タンパク質/ペプチドの染色が必要で、サンプルが失われたり汚染したりすることのないよう、装置を注意深く操作せねばならないので、作業が労働集約的で、多大な時間を要することになる。
【0011】
当業者であれば、ゲルのバンド又は分画を手動でプレート又はストリップから回収するプロセスというのは、ゲルを適切な数の分画に均等に分割して、ゲルから確実に被分析物を定量的に回収できるようにせねばならず、また、この移動の過程で使用する「汚染した」器具類によるクロスコンタミネーションを防止する必要があり、しかも入念に作業を進めねばならず、きわめて時間のかかる作業となることがあることがわかるはずである。このクロスコンタミネーションの問題は、IPGストリップを用いて被分析物を分離し、さらなる処理/分析に備えて、ストリップをはさみやメスを用いてバンドに切り離す場合には、特に重要である。というのも、こうした器具の刃は、ストリップからゲルの次のバンドを切り出す前に十分に清浄化しておく必要があるからである。また、こうしたプロセスは、一般に、ペプチド又はタンパク質を検出する目的でゲルを予め染色しておく工程をさらに含むので、システムが極度に労働集約的となる。
【0012】
当業者であれば、さらなる処理に備えて、ゲルのバンドをプレート又はIPGストリップから回収し、第二のゲル又は反応容器に移動する際に生じる上述のような問題が、バンド又は分画の数が増えるにつれて深刻になることもわかるはずである。したがって、例えば、IPGストリップを50個程度に分割し、その50個ほどの分割片のそれぞれを、別のゲル又は反応容器に移すような場合には、クロスコンタミネーションの可能性が増し、回収量が減る可能性が高まることになる。
【0013】
ゲルからのサンプル抽出に伴う問題を回避するために、等電点電気泳動による分離を、液相で実施することもできる(Zuoら; Methods Mol Biol., 2004, 244, 361−75)。Zuoらが使用した装置は、膜によって隔てられ、滴定によって特定のpHの値に保持された一連のチャンバーを備えている。しかし、このアプローチの不利な点として、ペプチドやタンパク質は、等電点付近では溶解度が低く、その結果、沈殿や凝集が生じて、等電点電気泳動の間のペプチドやタンパク質の解像度が低くなってしまうことを挙げることができる。
【0014】
Michelら(Electrophoresis, 2003, 24, 3−11)には、生体サンプルを等電点(pI)によって分画し、化合物を直接回収してさらなる分析に使用する方法が記載されている。この「オフ−ゲル(off−gel)IEF」と名づけられた方法では、IPGストリップを、両端が開放したマルチウェル器具を使用して、一連のウェルに分割し、タンパク質サンプルをIPGバッファーに加え、その後、電気泳動を実施して、タンパク質混合物を分離する。その後、各ウェルの内容物を取り出して、質量分析によるタンパク質の分析を行うのだが、この方法では解像度は0.1pH単位であった。しかし、上述のZuoらのアプローチと同じく、電気泳動の間にタンパク質は液相中に存在しており、その結果、沈殿や凝集の危険性が増大する。このMichelらのアプローチでは、タンパク質は、マルチウェル器具に溶液を加えることなく、ゲルのみで電気泳動を行った場合と比較して、電界のずっと低い領域に存在する形状となっている。そのため、従来のゲルでの電気泳動に比べて、この電気泳動では解像度が低く、電気泳動に要する時間も長くなる。
【0015】
同じグループ(Hellerら.; Electrophoresis, 2005, 26, 1174−1188)が、最近、タンパク質とそのアイソフォームの分離と識別に、「オフ−ゲルIEF」を利用することについて報告している。この方法は、二段階法で、第一段階で、タンパク質とそのアイソフォームをpIを利用して分離し、第二段階で、トリプシン処理したペプチド断片の分離と識別を行う。
【0016】
IEFは、分離したタンパク質を、膜で隔てられたチャンバーに入った溶液中に回収する形状でも実施できる(Righettiら; J. Biochem. Biophys. Meth., 1987, 15, 199−206)。このアプローチも、等電点に近いタンパク質は、凝集や沈殿を生じやすいという事実によって制限される。
【0017】
タンパク質を含むゲル断片をゲルから単離し、タンパク質分解性の消化を行い、その後、生成した切断ペプチドを識別するゲル中でのタンパク質処理方法を記載した他のシステムも開示されている。国際公開第02/071072号には、自動化されたシステムが記載されており、このシステムでは、単離したタンパク質−ゲル断片を、底部に疎水性フィルター膜が設けられた第一マイクロタイタープレートの対応する数の反応容器に、ロボットアーム装置で直接移動し、プロテアーゼとともにインキュベートする。加水分解の後、ペプチド生成物は、疎水性フィルター膜を通して第二マイクロタイタープレートへと濾過され、さらなる分析に備えて濃縮される。
【0018】
このように、ゲル中で電気泳動で分離を行うことによって卓越した解像度が得られるものの、上述したように、ゲルから液相にサンプルを移動する際には問題が生じることも多く、そのため、自動化が困難となっている。
【特許文献1】国際公開第02/071072号パンフレット
【非特許文献1】Aebersold et al; Nature, 2003, 422, 198-207
【非特許文献2】Breci et al; Proteomics, 2005, 5, 2018-2028
【非特許文献3】Washburn et al; Nat Biotechnol., 2001, 19, 242-247
【非特許文献4】Peng et al; Journal of Proteome Research, 2003, 2, 43-50
【非特許文献5】Cargile et al; Electrophoresis, 2004, 25, 936-945
【非特許文献6】Aebersold et al; Proteomics, 2005, 5, 380-387
【非特許文献7】Vandekerckhove et al; Nat Biotechnol., 2003, 21, 566-569
【非特許文献8】Zuo et al; Methods Mol Biol., 2004, 244, 361-75
【非特許文献9】Michel et al; Electrophoresis, 2003, 24, 3-11
【非特許文献10】Heller et al; Electrophoresis, 2005, 26, 1174-1188
【非特許文献11】Righetti et al; J. Biochem. Biophys. Meth., 1987, 15, 199-206
【発明の開示】
【発明が解決しようとする課題】
【0019】
したがって、本発明の目的は、先行技術の諸問題を軽減しつつ、ゲル分画を調製して、さらなる処理や操作を可能とする方法及びシステムを提供することにある。本発明の別の目的は、被分析物を検出するために、ゲルを予め染色しておく必要がない方法及びシステムを提供することにある。本発明のさらに別の目的は、化学的又は酵素的修飾の前又は後に、試薬をゲル分画に加えて、被分析物をゲルから溶出させる方法及びシステムを提供することにある。
【課題を解決するための手段】
【0020】
本発明の第一の態様では、ゲル中の被分析物に試薬を加える方法を提供する。この方法は、
i)端部が開放しており、それぞれ1以上の壁部で画成されたチャンバーが複数設けられた本体を備えるマルチウェルテンプレートを、ゲルに向かって移動させて、ゲルと1以上の壁部との間に複数のウェルを形成する工程と、
ii)必要に応じて、被分析物を、クロマトグラフィー又は電気泳動によってゲル中で分離する工程と、
iii)上記のウェルの1以上に試薬を加えて、液上の被分析物と試薬の混合物を生成する工程を含む方法であって、
試薬は、被分析物を溶解するか、被分析物又はその環境を修飾・変化しうるものである。
【0021】
試薬は、バッファーとするのが適当で、バッファーのpHは、との特定の被分析物に応じて変化させることができる。
【0022】
試薬を、酸又はアルカリとするのも適当で、この酸又はアルカリは、被分析物、又は、被分析物が存在している環境を変化させることができる。
【0023】
試薬を、酵素とするのも適当で、この酵素は、加水分解酵素であるのが好ましく、核酸分解酵素又はタンパク質分解酵素であるのがさらに好ましく、タンパク質分解酵素であるのが特に好ましい。
【0024】
試薬は、検出可能な成分とするのが適当であり、こうした検出可能なマーカーは、例えば、アイソトープ又は蛍光標識を含むものとすることができる。
【0025】
ゲルは、シート上に担持されているのが適当である。
【0026】
この方法は、ゲル又はシートをベースプレートに載置する工程をさらに含むものとするのが適当である。ベースプレートは、例えば、水平電気泳動装置の冷却プレートに対応するものとすることもできる。
【0027】
この方法は、ゲル又はシートをリテーナに載置する工程をさらに含むものとするのが適当である。
【0028】
この方法は、ゲル又はシート、或いはリテーナを、ベースプレートの所定の位置に位置決めする工程をさらに含むものとするのが適当であり、ベースプレートの一方の表面上には、この表面上で、ゲル又はシート、或いはゲル又はシートのリテーナを位置決めするための1以上の凹部及び/又は凸部がさらに設けられていることが好ましい。
【0029】
リテーナの一方の表面上には、ゲル又はシートを受け止めるための1以上の凹部又は凸部が設けられているのが適当である。このリテーナの1以上の凹部又は凸部には、シートを位置決めするための位置決め手段がさらに設けられていることが好ましい。
【0030】
この方法は、マルチウェルテンプレートを、トッププレートの開口部に挿入する工程をさらに含むのが適当である。
【0031】
この方法は、マルチウェルテンプレートに設けられた開放端チャンバーの位置に対応する複数の開口部が設けられた固定用ストリップを、トッププレート内に載置されたマルチウェルテンプレートの端部を覆うように装着する工程をさらに含むのが適当である。
【0032】
ベースプレート及び/又はトッププレート及び/又は固定用ストリップは、ゲルの所定位置に形成された複数のウェルを、ベースプレート及びトッププレートに対して位置決めするための固定手段をさらに備えていることが好ましいまた、この固定手段は、ベースプレートに設けられたネジ穴と、トッププレートに設けられたネジ用の開口部と、固定用ストリップとを含むものとするのが、さらに好ましい。
【0033】
ゲルは、好ましくは、ポリアクリルアミドゲルであり、より好ましくは、SDSゲル又は等電点電気泳動ゲルである。
【0034】
マルチウェルテンプレートの本体は、第一部分と第二部分とに分かれたものとし、第一部分は、トッププレートの開口部への挿入に適した形状、第二部分は、ゲルに向かって移動するのに適した基部に向かって傾斜のついた形状とすることが適当である。第一部分と第二部分とは、トッププレートの開口部内にマルチウェルテンプレートを担持するためのフランジによって隔てられていることが好ましい。
【0035】
被分析物は、ペプチド、タンパク質、核酸、又は炭水化物とするのが適当であり、ペプチド又はタンパク質とするのが好適である。
【0036】
マルチウェルテンプレートをゲルに向かって移動させるのは、クロマトグラフィー又は電気泳動によってゲル中で被分析物を分離した後とするのが好適である。しかし、状況によっては、クロマトグラフィー又は電気泳動によってゲル中で被分析物を分離する前に、マルチウェルテンプレートをゲルに向かって移動させることが好ましい場合もある。こうした場合には、マルチウェルテンプレートとゲルによって形成された1以上のウェルに、液状の試薬を加える前に、クロマトグラフィー又は電気泳動による分離を完了させておくものと理解されたい。
【0037】
液状の試薬は、手動で、例えばピペットを使用することによって加えるのが適当である。
【0038】
この方法は、液状の被分析物と試薬の混合物を、手動又は自動化された手段で第二容器に移す工程をさらに含むものとするのが適当である。手動の手段の例としては、手動で操作するピペットを挙げることができ、自動化手段の例としては、自動化又はプログラマブルな液体取扱い装置を挙げることができる。
【0039】
この第二容器は、マイクロタイタープレートのウェルとするのが好ましい。
【0040】
試薬を、自動液体取扱い装置で加えるか、及び/又は、液状の被分析物と試薬の混合物を、自動液体取扱い装置で移すのが適当である。自動液体取扱い装置は、コンピュータで制御するものとするのが好ましい。
【0041】
本発明の第二の態様では、上述の方法を実施するためのシステム提供する。このシステムは、
i)端部が開放しており、それぞれ1以上の壁部で画成されたチャンバーが複数設けられた本体を備えたマルチウェルテンプレートと、
ii)自動液体取扱い装置と
を備えている。
【0042】
このシステムは、コンピュータで制御するものとすることが好ましい。
【0043】
次に、本発明の方法及び装置を、図面を参照しつつ説明する。
【発明を実施するための最良の形態】
【0044】
試薬は、図1に示すマルチウェルテンプレート(30)を使用することによって、請求の範囲に記載した方法にしたがって、ゲル(10)中に存在する被分析物に加えることができる。図には、プラスチック又は金属など、適当な材料から形成されたマルチウェルテンプレート(30)を、プラスチック又はガラスなどで形成されたシート(15)で担持されたポリアクリルアミドゲル(10)に載置したところを示してある。ゲル(10)は、被分析物を含んでおり、この被分析物は、通常、電気泳動で分離ずみである。つまり、ゲルは、例えば、タンパク質又はペプチドを含むことができる。マルチウェルテンプレート(30)は、2枚の細長い側壁部(31a、31b)と、その末端に接合された2枚の末端壁部(33a、33b)を備えた細長い本体(32)から構成されている。本体(32)の長軸に沿って、端部が開放したチャンバー(34i〜n)が複数配置され、隣接チャンバー同士は、間に介在する壁部(35a〜35n−1)によって隔てられており、各壁部(35a〜35n−1)は、側壁部31aからもう一方の側壁部31bまで延在している。各チャンバー(34)の形状は、円、楕円、多角形、正方形、長方形(図示)など、各種のものとすることができる。
【0045】
マルチウェルテンプレート(30)をゲル(10)に向かって移動させ、マルチウェルテンプレートの本体のテーパー部分(32b)でゲル(10)を押して、マルチウェルテンプレートの基部(38)が、ゲル(10)を担持しているシートと近接するようにする。マルチウェルテンプレート(30)がこの位置に来ると、ウェルが画成され、ゲル又はプラスチックシートがウェルの底部を、テンプレートの壁部がウェルの壁部を画成することになる。
【0046】
液状の試薬、例えばバッファー又はタンパク質分解酵素の溶液を、1以上のウェル(34)に加え、液状の被分析物と試薬の混合物を形成する。試薬がバッファーなどの場合には、試薬によって被分析物が溶解され、(試薬がタンパク質分解酵素やタンパク質などの場合には、)試薬によって被分析物が修飾され、(試薬が酸などの場合には、)試薬によって被分析物が存在している環境が変化する。
【0047】
図2に、ゲル中の被分析物に試薬を加える際に使用することのできる別の装置の図を図2に示す。ゲル(110)、例えばSDSゲルが、シート(115)の表面に載置されている。シート(115)は、プラスチック又は金属材料製のベースプレート(120)に載置され、このベースプレート(120)には、シートをベースプレート(120)に対して所定位置に位置させるための凹部(122)が設けられている。ベースプレート(120)の四隅には、固定手段であるネジ穴(124a−c、124dは図示せず)が設けてあるので、ベースプレート(120)のネジ(図示せず)を、トッププレート(140)の所定位置に固定することができる。なお、固定手段としては、他の形状のもの(例えば、留め金、クランプ、ピン、穴、スナップ)も使用できる。
【0048】
ゲルには、プラスチック、金属、セラミクス、又は複合材料など、任意の適当な材料から形成されたマルチウェルテンプレート(130)で、複数のウェルを形成する。マルチウェルテンプレート(130)は、2枚の細長い側壁部(131a、131b)と、その末端に接合された2枚の末端壁部(133a、133b)を備えた細長い本体(132)から構成されている。本体(132)の長軸に沿って、端部が開放したチャンバー(134i〜n)が複数配置され、隣接チャンバー同士は、間に介在する壁部(135a〜135n−1)によって隔てられており、各壁部(135a〜135n−1)は、側壁部131aからもう一方の側壁部131bまで延在している。各チャンバー(134)は、円、楕円、多角形、正方形、長方形(図示)など、任意の形状とすることができる。
【0049】
マルチウェルテンプレート(130)の本体(132)は、フランジ(136)によって、第一部分(132a)と第二(132b)部分とに分かれており、第一部分(132a)は、トッププレート(140)の開口部(142)への挿入に適した形状、第二部分(132b)は、基部(138)に向かってテーパーがついており、ゲルに押しつけるのに適した形状となっている。図からも理解されるように、マルチウェルテンプレート(130)を下降させ、つまりゲル(110)に向かって押しつけて、テンプレート(130)が、ゲル(110)を担持しているシート(115)に接触又は近接すると、各チャンバー(134)はウェルを形成し、ゲル又はシートがウェルの底部に、チャンバーの壁部(図示せず)がウェルの壁部となる。こうして、ゲル上に、複数のウェルが形成される。マルチウェルテンプレート(130)は、ゲルに向かって下降させ、つまりゲルに押しつけて、ゲル上の複数のウェルを形成する前、又は後に、プラスチック又は金属(例えばステンレス)材料製のトッププレート(140)の開口部(142)に挿入することができる。図示した例では、テンプレート(130)は、フランジ(136)によって、トッププレート(140)の棚部(144)に保持されている。なお、テンプレートは、ゲルを切断するのではなく、押しつけることによって複数のウェルを形成することに注意されたい。ウェルは、トッププレート(140)をベースプレート(120)に対して固定手段(トッププレートに設けられた固定手段(146a〜d)及びベースプレートに設けられた固定手段(124a〜d))によって固定することによって、ベースプレート(120)及びトッププレート(140)に対して所定位置に保持される。図2の例では、ネジ(図示せず)を、トッププレートに設けられた開口部(146a〜d)を通して、ベースプレート(120)に設けられたネジ穴(124a〜d)まで到達させることによって、トッププレート(140)をベースプレート(120)に固定している。ゲルに形成された複数のウェルは、このようにして、トッププレートとベースプレートに対して所定位置に保持されている。
【0050】
図3は、本発明の方法を実施する際に使用することのできる別の装置の斜視図である。図3に示す装置は、等電点電気泳動のジェル、特にIPGストリップ、例えばImmobiline(登録商標)DryStripゲルとともに使用するのに適している。プラスチックの基材シートと、その上に担持されたポリアクリルアミドゲル(210)のコーティングからなるIPGストリップ(図示せず)を、リテーナ(250)に設けられた、電気泳動のマニホールドである凹部(252)に載置する。プラスチック材料製とするのが通例であるリテーナ(250)には、複数のIPGストリップを同時に処理できるよう、複数の凹部(252i〜n)を設けることができ、図3の例では、12個の凹部が示してある。IPGストリップで被分析物を電気泳動した後、リテーナ(250)とストリップとを、ベースプレート(220)上面の凹部(222)の所定位置に載置する。ベースプレートは、プラスチック又は金属材料製とすることができる。上述したのと似た構造をもつマルチウェルテンプレート(230)には、開放端チャンバー(234i〜n)が複数設けられており、このマルチウェルテンプレート(230)を、トッププレート(240)の開口部(242)に挿入して、マルチウェルテンプレート(230)のフランジ(236)が、開口部(242)の棚部(図示せず)によって担持されるようにする。マルチウェルテンプレート(230)とトッププレート(240)は、通常、プラスチック材料製とするが、金属等の他の材料から製造してもよい。トッププレート(240)には、上述のようにして複数のマルチウェルテンプレート(230)を載置することができ、例えば、図示した例では、トッププレート(240)に、マルチウェルテンプレート(230)12個を載置することができる。
【0051】
マルチウェルテンプレート(230)をトッププレート(240)に載置したら、マルチウェルテンプレート(230)を下降させ、つまりゲル(210)の表面まで移動させて、テンプレート本体のテーパー部分(232b)をゲル(210)に対して押しつけ、テンプレートの基部(238)が、ゲル(210)を担持しているプラスチックシートに近接するようにする。この位置では、ウェルが画成され、プラスチックシート又はゲルがウェルの底部に、テンプレートの壁部が、ウェルの壁部となっている。
【0052】
なお、マルチウェルテンプレート(230)をトッププレート(240)に挿入する前に、マルチウェルテンプレート(230)を下降させ、ゲル(210)まで移動させて複数のウェルをゲル上に形成することもできる。マルチウェルテンプレートは、この時点で、固定手段(トッププレートに設けられた固定手段(246a〜d)及びベースプレートに設けられた固定手段(224a〜d、dは図示せず))によって、トッププレート(240)及びベースプレート(220)に対して所定の位置に固定することができ、例えば図2では、ネジ(図示せず)を使用してプレート同士を固定することができる。
【0053】
マルチウェルテンプレート(230)を覆うように固定用ストリップ(260)を載置し、ストリップ(260)の開口部(264i〜n)と、テンプレート(230)の開放端チャンバー(234i〜n)の位置とが、重なり、対応するようにする。こうすると、ストリップに設けられた固定手段(266a〜b)とトッププレートに設けられた固定手段(248i〜n)を使用することで、マルチウェルテンプレート(230)がトッププレート(240)に固定されるので、固定用ストリップ(260)によって、マルチウェルテンプレート(230)が所定位置に固定される。この固定手段は、固定用ストリップ(266a〜b)の開口部、トッププレートに設けられたネジ穴(248i〜n)、及び孔径に合った1以上のネジからなるものとすることができる。別の形態では、固定用ストリップとマルチウェルテンプレートとを一体の部材として形成することもできる。
【0054】
図4は、図3の装置の斜視図で、各構成部品は、図3について記載したのと同様の特徴を備えている。したがって、この装置は、凹部(322)と固定手段(324a〜d、dは図示せず)が設けられたベースプレート(320)を備えている。リテーナ(350)である等電点電気泳動のマニホールドの一連の凹部(352i〜n)内には、プラスチックシートと、このプラスチックシートに担持されたポリアクリルアミドゲル(310)からなるIPGストリップ(図示せず)が保持されている。プラスチック材料製のトッププレート(340)には、複数の開口部(342i〜n)が、リテーナ(310)内のIPGストリップの位置に対応するよう設けられている。トッププレート(340)には、ベースプレートの固定手段(324a〜d)の固定手段に対応する固定手段(346a〜d、及び348i及びn)が設けられている。マルチウェルテンプレート(330)には、開放端チャンバー(334i〜n)が複数設けられ、固定用ストリップ(360)には、マルチウェルテンプレート(330)の開放端チャンバー(334i〜n)の位置に対応する数多くの開口部(364i〜n)と、固定手段(366a及びb)とが設けられている。
【0055】
図4の装置を、図3で説明したのと同様にして使用することによって、ゲル中の被分析物に試薬を加えることができる。
【0056】
図5aに、本発明の方法で使用されるマルチウェルテンプレート(430)の基部(438)を示す。マルチウェルテンプレート(430)の本体(432)の全長にわたって、一連の壁部(433)によって開放端チャンバー(434i〜n)が画成されている。マルチウェルテンプレート(430)の基部に設けられた凹部又はノッチ(437)を使用して、マルチウェルテンプレート(430)を、IPGストリップが担持されているリテーナ(図示せず)の凸部に載置し、マルチウェルテンプレート(430)を、IPGストリップに対して所定位置に位置決めする。
【0057】
図5bは、IPGストリップのプラスチックシート(415)が、マルチウェルテンプレート(430)の基部(438)に位置しているところを示す。図の斜視図では、ゲルは、シート(415)の裏側に位置しているので見えないが、マルチウェルテンプレート(430)の基部(438)と接触している。この位置では、各チャンバー(434)内に位置するシート(415)の基材が、ウェルの底部に、チャンバーの壁部が、ウェルの壁部になっている。
【0058】
図6は、トッププレート(540)の平面斜視図で、このトッププレート(540)は、鋼製である。図には、マルチウェルテンプレート(所定位置に載置)を格納する開口部(5542i〜n)を、ベースプレートに固定するための固定手段(546a〜d)及び固定用ストリップ固定用の固定手段(548i〜n)とともに示す。
【0059】
図7aは、本発明の方法で使用するトッププレート(640)の詳細を示す平面図で、固定用ストリップ(660)によって、マルチウェルテンプレート(図示せず)がトッププレート(640)に固定されている。固定手段(666)である開口部が、トッププレート内のリテーナ(図示せず)の開口部(図6の548i〜nを参照)と同位置に配置されている。
【0060】
図7bは、図7aの配置の詳細を図示した下面図である。マルチウェルテンプレートのテーパーのついた第二部分の基部(638)が、トッププレート(660)の下面から突出しているのが、この角度からははっきりと見える。この基部(638)によって、ゲルが押され、各開放端チャンバー(634i−n)が、ゲル又はゲルの基材シート(図示せず)とともにウェルを形成する。
【0061】
図8は、本発明の自動溶出システムを示す。ゲル、例えばIPGストリップでサンプルを電気泳動した後、上述した本発明の方法を使用して、複数のウェルを形成し、各ウェルにバッファーを加える。次に、各ウェル中のゲルをバッファーで溶出して、被分析物(例えばペプチド)を抽出し、得られた溶出液を、さらなる処理/分析に備えて反応容器に移す。図8は、本発明の装置のトッププレート(740)のウェルから、マイクロタイタープレート(780)のウェル(782i〜n)に溶出液を移動している過程の8チャネルの溶出プローブ(770)を示す。このシステムは、コンピュータ(図示せず)によって制御されている。IPGストリップに形成するウェルの数は、通常、マイクロタイタープレートの長さ又は幅方向のウェルの数(例えば、96ウェルのマイクロタイタープレートであれば、8又は12の倍数)又はこれらの番号の整数分の1(例えば、2、3、4、6)と対応している。
【実施例】
【0062】
等電点電気泳動、蛍光分析、ペプチドの抽出
0.5mgの酵母(Saccharomyces cerevisiae)(II型)のトリプシン処理サンプルを、各5μgのpIマーカー「3.73」、「4.25」、及び「4.54」と混合した。「pIマーカー」は、等電点が既知で、蛍光をスキャンすることによって検出が可能な蛍光標識ペプチドである。蛍光標識としては、Cy5(登録商標)(Amersham Biosciences AB(スウェーデン))を使用し、発光スペクトルは、約660nmで検出した(Ettan DIGE System、ユーザーマニュアル、Amersham Biosciences AB(スウェーデン))。24cmのIPGペプチドストリップ(pH3.4〜4.8)を、350μlの8M尿素とサンプル溶液で、一晩(約15時間、室温)再水和した。再水和したストリップを、Ettan(登録商標)IPGphor(登録商標)のマニホールドに移し、以下のプログラムで等電点電気泳動を行った。
【0063】
勾配500V(1分)、勾配4000V(1.5時間)、勾配6000V(1.5時間)、
勾配10000V(1.5時間)、ステップ10000V(12時間)(合計約150kV時間)。
【0064】
等電点電気泳動ユニットとしては、Ettan IPGphor IIを使用し、泳動は、20℃で行った。
【0065】
導電点電気泳動の後、IPGストリップを、蛍光スキャナー(Typhoon 9400スキャナー、Amersham Biosciences AB(スウェーデン)製)で、660nmにてスキャンして、蛍光pIマーカーの正確な位置を判定した。Typhoonで得られた図を、ImageQuantで評価し、蛍光強度のグラフを描いた。
【0066】
スキャン後、本発明のマルチウェルテンプレートを使用して、ストリップ中のペプチドを、ゲルから液体分画に抽出し、pH勾配を、ストリップに沿った一連の別々の分画に分割した。この方法によって、IPGストリップは、約3mm間隔の72の分画に分割された。72分画のそれぞれに、50μlの水を加え、室温で60分間インキュベートし、抽出されたペプチドを、自動で、マイクロタイタープレートに移動させた。この溶出過程を3回繰り返し、各ウェルから、すべてのペプチドを確実に抽出し、移動させた。抽出後は、マルチウェルテンプレートをIPGストリップから取り外せば、この器具は、清浄後に次の実験に再使用できる。この実験では、IPGペプチドストリップを再度Typhoonでスキャンし、画像をImageQuantで評価した。
【0067】
図9は、抽出前(図9a)と抽出後(図9b)のペプチドIPGストリップの蛍光強度を示す。図9cは、抽出したペプチドサンプルを含むマイクロタイタープレートと、抽出前と抽出後のストリップとを示すが、抽出前と抽出後のストリップには、それぞれ、高レベルと低レベルの蛍光が示されている。これらの図から、ペプチドが、IPGストリップから効果的に抽出され、この時点では、マイクロタイタープレートのウェルに存在していることが明らかである。
【0068】
図10は、IPGストリップの塩基側末端に位置する互いに隣接した7分画中に含まれるすべての識別済みペプチド配列を比較した結果である。比較した7分画中の全部で719個の識別済みペプチドのうち、ペプチドの82%は、1分画のみに存在しており、16%は、2分画に存在していた。この実験結果は、IPGストリップの高解像度を裏付けるばかりでなく、本発明のマルチウェルテンプレートを用いて形成したウェルの間で漏れの問題がなかったことを示すものでもある。
【図面の簡単な説明】
【0069】
【図1】図1は、本発明の方法を実施する際に使用することのできる装置を示す。
【図2】図2は、SDSゲル中に存在する被分析物に試薬を加える際に使用することのできる装置を示す。
【図3】図3は、等電点電気泳動用ゲルであるIPGストリップ中の被分析物に試薬を加える本発明の装置を示す。
【図4】図4は、図3の装置の平面斜視図である。
【図5】図5a及び5bは、本発明の方法で使用するマルチウェルテンプレートの各部を図示したものである。図5aは、テンプレートの基部を示す下面図で、複数の開放端チャンバーが図示されている。図5bは、図5aで、テンプレートの基部にIPGストリップを載置したところである。
【図6】図6は、図3及び4に図示した装置のトッププレートを示す。トッププレートには、マルチウェルテンプレートが挿入されている。
【図7】図7aは、本発明の方法で使用するトッププレートと固定用ストリップの詳細を示す平面図である。図6bは、マルチウェルテンプレートを載置したトッププレートの下面図である。
【図8】図8は、本発明の自動溶出システムを示す。
【図9】図9a及び9bは、蛍光標識ペプチドの分離に使用したIPGストリップの蛍光強度を、本発明の方法でゲルを溶出する前(図9a)と後(図9b)にスキャンしたものである。また、図9cに、IPGストリップの蛍光を、抽出の前後にスキャンした結果を、ストリップから溶出した分画を含むマイクロタイタープレートをスキャンした結果とともに示す。
【図10】図10は、識別されたペプチドが、本発明の方法を使用してゲルから抽出した分画1ないし数個のみに分布していることを示す図である。
【特許請求の範囲】
【請求項1】
ゲル中の被分析物に試薬を加える方法であって、
i)端部が開放しており、それぞれ1以上の壁部で画成されたチャンバーが複数設けられた本体を備えるマルチウェルテンプレートを、ゲルに向かって移動させて、ゲルと1以上の壁部との間に複数のウェルを形成する工程と、
ii)必要に応じて、被分析物を、クロマトグラフィー又は電気泳動によってゲル中で分離する工程と、
iii)上記のウェルの1以上に試薬を加えて、液上の被分析物と試薬の混合物を生成する工程を含む方法であって、
試薬が、被分析物を溶解するか、被分析物又はその環境を修飾・変化しうるものである方法。
【請求項2】
試薬がバッファーである、請求項1記載の方法。
【請求項3】
試薬が酸又はアルカリである、請求項1記載の方法。
【請求項4】
試薬が酵素である、請求項1記載の方法。
【請求項5】
酵素が加水分解酵素である、請求項4記載の方法。
【請求項6】
酵素が核酸分解酵素又はタンパク質分解酵素である、請求項4又は請求項5記載の方法。
【請求項7】
試薬が検出可能な成分である、請求項1乃至請求項6のいずれか1項記載の方法。
【請求項8】
ゲルがシート上に担持されている、請求項1乃至請求項7のいずれか1項記載の方法。
【請求項9】
ゲル又はシートをベースプレートに載置する工程をさらに含む、請求項1乃至請求項8のいずれか1項記載の方法。
【請求項10】
ゲル又はシートをリテーナに載置する工程をさらに含む、請求項9記載の方法。
【請求項11】
ゲル又はシート或いはリテーナを、ベースプレートの所定の位置に位置決めする工程をさらに含む、請求項9又は請求項10記載の方法。
【請求項12】
ベースプレートの一方の表面上に、該表面上で、ゲル又はシート、或いはゲル又はシートのリテーナを位置決めするための1以上の凹部及び/又は凸部がさらに設けられている、請求項9乃至請求項11のいずれか1項記載の方法。
【請求項13】
リテーナの一方の表面上に、ゲル又はシートを受け止めるための1以上の凹部又は凸部が設けられている、請求項10乃至請求項12のいずれか1項記載の方法。
【請求項14】
リテーナの1以上の凹部又は凸部にシートを位置決めするための位置決め手段がさらに設けられている、請求項13記載の方法。
【請求項15】
マルチウェルテンプレートをトッププレートの開口部に挿入する工程をさらに含む、請求項1乃至請求項14のいずれか1項記載の方法。
【請求項16】
マルチウェルテンプレートに設けられた開放端チャンバーの位置に対応する複数の開口部が設けられた固定用ストリップを、トッププレート内に載置されたマルチウェルテンプレートの端部を覆うように装着する工程をさらに含む、請求項15記載の方法。
【請求項17】
ベースプレート及び/又はトッププレート及び/又は固定用ストリップが、ゲルの所定位置に形成された複数のウェルを、ベースプレート及びトッププレートに対して位置決めするための固定手段をさらに備えている、請求項9乃至請求項16のいずれか1項記載の方法。
【請求項18】
固定手段が、ベースプレートに設けられたネジ穴と、トッププレートに設けられたネジ用の開口部と、固定用ストリップとを含む、請求項17記載の方法。
【請求項19】
ゲルがポリアクリルアミドゲルである、請求項1乃至請求項18のいずれか1項記載の方法。
【請求項20】
ゲルがSDSゲル又は等電点電気泳動ゲルである、請求項1乃至請求項19のいずれか1項記載の方法。
【請求項21】
マルチウェルテンプレートの本体が、第一部分と第二部分とに分かれ、第一部分が、トッププレートの開口部への挿入に適した形状、第二部分が、ゲルに向かって移動するのに適した基部に向かって傾斜のついた形状である、請求項1乃至請求項20のいずれか1項記載の方法。
【請求項22】
第一部分と第二部分とが、トッププレートの開口部内にマルチウェルテンプレートを担持するためのフランジによって隔てられている、請求項21記載の方法。
【請求項23】
被分析物がペプチド、タンパク質、核酸又は炭水化物である、請求項1乃至請求項22のいずれか1項記載の方法。
【請求項24】
被分析物が、タンパク質又はペプチドである、請求項1乃至請求項23のいずれか1項記載の方法。
【請求項25】
ゲル中の被分析物をクロマトグラフィー又は電気泳動で分離した後に、マルチウェルテンプレートをゲル上に移動させる、請求項1乃至請求項24のいずれか1項記載の方法。
【請求項26】
液状の試薬を、手動で加える、請求項1乃至請求項25のいずれか1項記載の方法。
【請求項27】
液状の被分析物と試薬の混合物を、手動又は自動化された手段で第二容器に移す工程をさらに含む、請求項1乃至請求項26のいずれか1項記載の方法。
【請求項28】
第二容器が、マイクロタイタープレートのウェルである、請求項27記載の方法。
【請求項29】
試薬を、自動液体取扱い装置で加えるか、及び/又は、液状の被分析物と試薬の混合物を、自動液体取扱い装置で移す、請求項1乃至請求項28のいずれか1項記載の方法。
【請求項30】
自動液体取扱い装置がコンピュータ制御される、請求項29記載の方法。
【請求項31】
i)端部が開放しており、それぞれ1以上の壁部で画成されたチャンバーが複数設けられた本体を備えたマルチウェルテンプレートと、
ii)自動液体取扱い装置と
を備える、請求項1乃至請求項30のいずれか1項記載の方法を実施するためのシステム。
【請求項32】
上記システムがコンピュータで御される、請求項31記載のシステム。
【請求項1】
ゲル中の被分析物に試薬を加える方法であって、
i)端部が開放しており、それぞれ1以上の壁部で画成されたチャンバーが複数設けられた本体を備えるマルチウェルテンプレートを、ゲルに向かって移動させて、ゲルと1以上の壁部との間に複数のウェルを形成する工程と、
ii)必要に応じて、被分析物を、クロマトグラフィー又は電気泳動によってゲル中で分離する工程と、
iii)上記のウェルの1以上に試薬を加えて、液上の被分析物と試薬の混合物を生成する工程を含む方法であって、
試薬が、被分析物を溶解するか、被分析物又はその環境を修飾・変化しうるものである方法。
【請求項2】
試薬がバッファーである、請求項1記載の方法。
【請求項3】
試薬が酸又はアルカリである、請求項1記載の方法。
【請求項4】
試薬が酵素である、請求項1記載の方法。
【請求項5】
酵素が加水分解酵素である、請求項4記載の方法。
【請求項6】
酵素が核酸分解酵素又はタンパク質分解酵素である、請求項4又は請求項5記載の方法。
【請求項7】
試薬が検出可能な成分である、請求項1乃至請求項6のいずれか1項記載の方法。
【請求項8】
ゲルがシート上に担持されている、請求項1乃至請求項7のいずれか1項記載の方法。
【請求項9】
ゲル又はシートをベースプレートに載置する工程をさらに含む、請求項1乃至請求項8のいずれか1項記載の方法。
【請求項10】
ゲル又はシートをリテーナに載置する工程をさらに含む、請求項9記載の方法。
【請求項11】
ゲル又はシート或いはリテーナを、ベースプレートの所定の位置に位置決めする工程をさらに含む、請求項9又は請求項10記載の方法。
【請求項12】
ベースプレートの一方の表面上に、該表面上で、ゲル又はシート、或いはゲル又はシートのリテーナを位置決めするための1以上の凹部及び/又は凸部がさらに設けられている、請求項9乃至請求項11のいずれか1項記載の方法。
【請求項13】
リテーナの一方の表面上に、ゲル又はシートを受け止めるための1以上の凹部又は凸部が設けられている、請求項10乃至請求項12のいずれか1項記載の方法。
【請求項14】
リテーナの1以上の凹部又は凸部にシートを位置決めするための位置決め手段がさらに設けられている、請求項13記載の方法。
【請求項15】
マルチウェルテンプレートをトッププレートの開口部に挿入する工程をさらに含む、請求項1乃至請求項14のいずれか1項記載の方法。
【請求項16】
マルチウェルテンプレートに設けられた開放端チャンバーの位置に対応する複数の開口部が設けられた固定用ストリップを、トッププレート内に載置されたマルチウェルテンプレートの端部を覆うように装着する工程をさらに含む、請求項15記載の方法。
【請求項17】
ベースプレート及び/又はトッププレート及び/又は固定用ストリップが、ゲルの所定位置に形成された複数のウェルを、ベースプレート及びトッププレートに対して位置決めするための固定手段をさらに備えている、請求項9乃至請求項16のいずれか1項記載の方法。
【請求項18】
固定手段が、ベースプレートに設けられたネジ穴と、トッププレートに設けられたネジ用の開口部と、固定用ストリップとを含む、請求項17記載の方法。
【請求項19】
ゲルがポリアクリルアミドゲルである、請求項1乃至請求項18のいずれか1項記載の方法。
【請求項20】
ゲルがSDSゲル又は等電点電気泳動ゲルである、請求項1乃至請求項19のいずれか1項記載の方法。
【請求項21】
マルチウェルテンプレートの本体が、第一部分と第二部分とに分かれ、第一部分が、トッププレートの開口部への挿入に適した形状、第二部分が、ゲルに向かって移動するのに適した基部に向かって傾斜のついた形状である、請求項1乃至請求項20のいずれか1項記載の方法。
【請求項22】
第一部分と第二部分とが、トッププレートの開口部内にマルチウェルテンプレートを担持するためのフランジによって隔てられている、請求項21記載の方法。
【請求項23】
被分析物がペプチド、タンパク質、核酸又は炭水化物である、請求項1乃至請求項22のいずれか1項記載の方法。
【請求項24】
被分析物が、タンパク質又はペプチドである、請求項1乃至請求項23のいずれか1項記載の方法。
【請求項25】
ゲル中の被分析物をクロマトグラフィー又は電気泳動で分離した後に、マルチウェルテンプレートをゲル上に移動させる、請求項1乃至請求項24のいずれか1項記載の方法。
【請求項26】
液状の試薬を、手動で加える、請求項1乃至請求項25のいずれか1項記載の方法。
【請求項27】
液状の被分析物と試薬の混合物を、手動又は自動化された手段で第二容器に移す工程をさらに含む、請求項1乃至請求項26のいずれか1項記載の方法。
【請求項28】
第二容器が、マイクロタイタープレートのウェルである、請求項27記載の方法。
【請求項29】
試薬を、自動液体取扱い装置で加えるか、及び/又は、液状の被分析物と試薬の混合物を、自動液体取扱い装置で移す、請求項1乃至請求項28のいずれか1項記載の方法。
【請求項30】
自動液体取扱い装置がコンピュータ制御される、請求項29記載の方法。
【請求項31】
i)端部が開放しており、それぞれ1以上の壁部で画成されたチャンバーが複数設けられた本体を備えたマルチウェルテンプレートと、
ii)自動液体取扱い装置と
を備える、請求項1乃至請求項30のいずれか1項記載の方法を実施するためのシステム。
【請求項32】
上記システムがコンピュータで御される、請求項31記載のシステム。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【公表番号】特表2008−544233(P2008−544233A)
【公表日】平成20年12月4日(2008.12.4)
【国際特許分類】
【出願番号】特願2008−516191(P2008−516191)
【出願日】平成18年6月9日(2006.6.9)
【国際出願番号】PCT/EP2006/005531
【国際公開番号】WO2006/136297
【国際公開日】平成18年12月28日(2006.12.28)
【出願人】(597064713)ジーイー・ヘルスケア・バイオサイエンス・アクチボラグ (109)
【Fターム(参考)】
【公表日】平成20年12月4日(2008.12.4)
【国際特許分類】
【出願日】平成18年6月9日(2006.6.9)
【国際出願番号】PCT/EP2006/005531
【国際公開番号】WO2006/136297
【国際公開日】平成18年12月28日(2006.12.28)
【出願人】(597064713)ジーイー・ヘルスケア・バイオサイエンス・アクチボラグ (109)
【Fターム(参考)】
[ Back to top ]

