ゲル組成物およびその製造方法、ならびに該ゲル組成物を用いたマイクロアレイ
【課題】解析の際には透明性を有し、温度を上げることにより、ゲル全体の収縮を抑制しつつ検体の拡散性を向上させることができるゲル組成物およびそれを用いたマイクロアレイを目的とする。
【解決手段】アクリルアミド系モノマーと架橋剤との共重合により得られる網目構造体からなる基盤ゲル10と、基盤ゲル10に一端が共有結合された感温性ポリマー14とを含むことを特徴とするゲル組成物1。基板を有し、該基板上に形成された区画に、前記ゲル組成物が配置されているマイクロアレイ。
【解決手段】アクリルアミド系モノマーと架橋剤との共重合により得られる網目構造体からなる基盤ゲル10と、基盤ゲル10に一端が共有結合された感温性ポリマー14とを含むことを特徴とするゲル組成物1。基板を有し、該基板上に形成された区画に、前記ゲル組成物が配置されているマイクロアレイ。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、ゲル組成物およびその製造方法、ならびに該ゲル組成物を用いたマイクロアレイに関する。
【背景技術】
【0002】
遺伝子の分析手段においては、特定のプローブを使用してDNA配列の解析、遺伝子発現解析などを一括して実施できるマイクロアレイが広く用いられている。このようなマイクロアレイの具体例としては、基板の2次元表面上でフォトリソグラフィーによりキャプチャープローブ(DNA(デオキシリボ核酸)、ペプチドなど)が逐次的に合成されたマイクロアレイ(特許文献1)、予め合成しておいたキャプチャープローブが基板の2次元表面上にスポッティングされたマイクロアレイ(特許文献2)、樹脂板などからなる基板に複数の溝または貫通孔(中空部)が形成され、それらの溝または貫通孔の内部にDNAなどを含有するゲルが保持されたマイクロアレイ(特許文献3)、平面基板上にDNAなどを含有するゲルのスポットが配置されたマイクロアレイ(特許文献4)などが知られている。また、中空繊維の中空部にゲルが保持された中空繊維配列体が、該中空繊維配列体の繊維軸と交叉する方向に切断されることにより得られるマイクロアレイ(特許文献5)が知られている。
【0003】
DNAマイクロアレイでは、基板に固定されたキャプチャーDNA(キャプチャープローブ)が前記基板に沿って倒れたような状態となることで、対象の遺伝子由来のDNA断片とのハイブリダイゼーション(二重螺旋形成反応)の効率が低くなることがある。
しかし、特許文献3〜5のようなゲルを用いたマイクロアレイでは、ゲル中の三次元反応場において、より生態環境に近いハイブリダイゼーションが可能となる。また、基板の2次元表面にキャプチャーDNAが固定されたマイクロアレイに比べて、一区画に固定化できるキャプチャーDNA量が多い。そのため、キャプチャーDNAと対象のDNA断片とのハイブリダイゼーション効率が高くなり、解析の精度および効率に優れる。
【0004】
また、このようなマイクロアレイでは、検査対象となるDNA断片などの試料(以下、「検体」という。)がゲル組成物の網目構造中で充分に拡散することで、ゲル組成物中のキャプチャーDNAとの高いハイブリダイゼーション効率が達成される。しかし、特許文献3〜5のようなマイクロアレイでは、ゲルの網目構造中で検体が充分に拡散せず、検査に使用できる領域がゲル表面に限定される場合もあった。
【0005】
このように、マイクロアレイに用いるゲル組成物は、キャプチャープローブと検体との反応時には検体の拡散性に優れていることが重要である。また、それと同時に蛍光分析などの解析時には透明性に優れていることも重要である。
そこで、ゲルの編目構造の有効細孔径を大きくし、検体の拡散性を向上させる特性を有するゲル組成物として、図3に示すように、モノマーと架橋剤とキャプチャープローブとを共重合させて得られる網目構造体からなる基盤ゲル110と、該基盤ゲル110の構成成分には共有結合されていない感温性ポリマー114とを含むゲル組成物101が示されている(特許文献6)。このゲル組成物101は、基盤ゲル110の網目構造中に、直鎖状の感温性ポリマー114が絡んだ構造を有している。また、感温性ポリマー114は、相転移温度以上になると疎水性相互作用により収縮する性質を有している。
【0006】
ゲル組成物101は、相転移温度よりも低温では、図3(A)に示すように、感温性ポリマー114が広がった状態であり、巨視的には均質で透明である。一方、相転移温度よりも高温では、図3(B)に示すように、感温性ポリマー114が疎水性相互作用により基盤ゲル110を巻き込みながら収縮し、該基盤ゲル110中の細孔112が崩壊して疎密構造を形成する。このとき、基盤ゲル110の網目構造が不均一な疎密構造となるためにゲル組成物101が白濁化する。
このようなゲル組成物101を基板に形成された区画に配置することにより、解析の際には透明性を有し、かつハイブリダイゼーション(40〜60℃程度)の際には検体の拡散性が向上するマイクロアレイを得ることができる。
【特許文献1】米国特許第5405783号明細書
【特許文献2】米国特許第5601980号明細書
【特許文献3】特開2000−60554号公報
【特許文献4】米国特許第6682893号明細書
【特許文献5】特開2000−270877号公報
【特許文献6】特開2008−13663号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
しかし、ゲル組成物101では、高温時に感温性ポリマー114が基盤ゲル110を巻き込みながら収縮することで疎密構造を形成するため、それに伴って基盤ゲル110が収縮し、ゲル組成物101自体の収縮が見られる。そのため、基盤ゲル110の収縮により、その基盤ゲル110中に作り出される疎な部分が充分に大きくならず、ハイブリダイゼーションの際の検体の拡散性が充分に向上しないことがあった。また、場合によっては、その収縮によりゲル組成物101が基板の区画から剥離してしまうおそれもあった。
以上のような理由から、解析の際には透明であり、ハイブリダイゼーション時などには検体の拡散性が向上するゲル組成物として、ゲル組成物自体の収縮を伴わないものが望まれている。
【0008】
そこで本発明では、解析の際に透明性を有し、温度を上げることにより、ゲル組成物自体の収縮を抑制しつつ検体の拡散性を向上させることができるゲル組成物およびその製造方法を目的とする。また、該ゲル組成物を用いたマイクロアレイを提供する。
【課題を解決するための手段】
【0009】
本発明のゲル組成物は、アクリルアミド系モノマーと架橋剤との共重合により得られる網目構造体からなる基盤ゲルと、該基盤ゲルに一端が共有結合された感温性ポリマーとを含むことを特徴とする組成物である。
また、本発明のゲル組成物は、前記感温性ポリマーが、ポリ(N−エチル(メタ)アクリルアミド)、ポリ(N−n−プロピル(メタ)アクリルアミド)、ポリ(N−イソプロピル(メタ)アクリルアミド)、ポリ(N−シクロプロピル(メタ)アクリルアミド)、ポリ(N−メチル−N−エチルアクリルアミド)、ポリ(N,N−ジエチルアクリルアミド)、ポリ(N−メチル−N−イソプロピルアクリルアミド)、ポリ(N−メチル−N−n−プロピルアクリルアミド)、ポリ(N−アクリロイルピロリドン)、ポリ(N−アクリロイルピペリジン)からなる群から選択される1種のポリマーまたは2種以上のポリマーの混合物であることが好ましい。
また、前記感温性ポリマーの共重合率が、0.01〜4mol%であることが好ましい。
また、前記感温性ポリマーの相転移温度が20〜50℃であることが好ましい。
また、前記感温性ポリマーの前記基盤ゲルへの共有結合が、前記感温性ポリマーの末端に不飽和結合が導入された感温性マクロモノマーを用いることにより形成されていることが好ましい。
また、さらに、前記基盤ゲルに共有結合された生体関連物質を含むことが好ましい。
【0010】
また、本発明のマイクロアレイは、基板を有し、該基板上に形成された区画に、前記いずれかのゲル組成物が配置されている。
また、本発明のマイクロアレイは、前記区画が、溝または貫通孔により形成されていることが好ましい。
【0011】
また、本発明のゲル組成物の製造方法は、アクリルアミド系モノマーと感温性マクロモノマーとの共重合反応により前記いずれかのゲル組成物を製造する方法である。
【発明の効果】
【0012】
本発明のゲル組成物は、解析時には透明性を有しており、温度を上げることにより、ゲル組成物自体の収縮を抑制しつつ検体の拡散性を向上させることができる。
また、本発明の製造方法によれば、解析時には透明性を有しており、温度を上げることにより、ゲル組成物自体の収縮を抑制しつつ検体の拡散性を向上させることができるゲル組成物を得ることができる。
また、本発明のマイクロアレイは、解析時には透明性を有しており、温度を上げることにより検体の拡散性が向上する。また、その際のゲル自体の収縮が抑制されているため、ゲル組成物が基板の区画から剥離することがなく、安定して高効率な解析を行うことができる。
【発明を実施するための最良の形態】
【0013】
<ゲル組成物>
以下、本発明のゲル組成物の実施形態の一例について、図1および2に基づいて説明する。図1は、第1実施形態のゲル組成物1を示した概念図である。また、図2は、第2実施形態のゲル組成物2を示した概念図である。
【0014】
[第1実施形態]
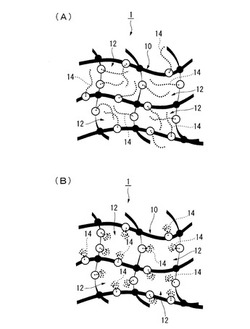
ゲル組成物1は、図1に示すように、アクリルアミド系モノマーと架橋剤との共重合により得られる網目構造体からなる基盤ゲル10と、該基盤ゲル10に一端が共有結合された感温性ポリマー14とを含む組成物である。ゲル組成物1は、基盤ゲル10により形成された細孔12内に感温性ポリマー14が配置される。
【0015】
基盤ゲル10は、アクリルアミド系モノマーと架橋剤との共重合により形成される網目構造体であり、ゲル組成物1の基盤となるゲルである。
アクリルアミド系モノマーとしては、例えば、アクリルアミド、メタクリルアミド、N−メチルアクリルアミド、N,N−ジメチルアクリルアミド(DMAA)、N−イソプロピルアクリルアミド(NIPAM)が挙げられる。
これらのアクリルアミド系モノマーは、1種のみを単独で使用してもよく、2種以上を併用してもよいが、1種のみの使用または2種の併用が好ましい。2種のアクリルアミド系モノマーを併用する場合は、DMAAとNIPAMの併用がより好ましい。
【0016】
架橋剤は、エチレン性不飽和結合を2個以上有する多官能性モノマーである。
架橋剤としては、例えば、N,N’−メチレンビスアクリルアミド、N,N’−ジアリル(1,2−ヒドロキシエチレン)−ビスアクリルアミド、N,N’−シスタミン−ビスアクリルアミド、N−アクリロイルトリス(ヒドロキシメチル)アミノメタン、ポリエチレングリコールジメタクリレートなどが挙げられる。なかでも、N,N’−メチレンビスアクリルアミドが好ましい。
これらの架橋剤は、1種のみを単独で使用してもよく、2種以上を併用してもよい。
【0017】
架橋剤の使用量は、主剤となるモノマー(アクリルアミド系モノマーおよび後述する感温性モノマー)のmol量と架橋剤のmol量とのmol比が、架橋剤1に対して、主剤となるモノマーが4〜500の範囲であることが好ましい。
前記mol比が、架橋剤1に対して主剤となるモノマーが4以上であれば、基盤ゲル10の網目構造が不均一になることで解析時(室温)などの低温環境においてゲル組成物1が白濁することを抑制しやすい。また、架橋剤1に対して主剤となるモノマーが500以下であれば、充分な架橋度を有する網目構造体からなる基盤ゲル10が得られやすい。
【0018】
また、ゲル組成物1においては、基盤ゲル10を形成するアクリルアミド系モノマーとして、後述する感温性ポリマー14の形成に用いる誘導体と同一のモノマー成分(例えば、NIPAMなど。以下、「モノマー成分(M1)」という。)を用いることもできるが、アクリルアミド系モノマーとしてそのような成分のみを用いると、基盤ゲル10自体の相転移により生じる収縮および白濁の影響が大きくなると考えられる。そのため、本発明においては、アクリルアミド系モノマーとしてモノマー成分(M1)とそれ以外のモノマー成分とを用いた共重合により得られる基盤ゲル10であることが好ましい。これらの共重合比は、全アクリルアミド系モノマー100mol%に対してモノマー成分(M1)が50mol%以下であることが好ましい。
【0019】
感温性ポリマー14は、相転移温度(以下、「Tc」という。)、すなわちLCST(Lower Critical Solution Temperature)を有するポリマーである。LCSTは下限臨界溶液温度とも呼ばれ、LCSTを有するポリマーはその温度以上で相分離を引き起こし、不溶化して白濁するか沈殿する。感温性ポリマー14は、前記Tcを超える温度になると、疎水性に転移して収縮する性質を有している。
【0020】
感温性ポリマー14を形成する誘導体としては、例えば、N−エチル(メタ)アクリルアミド、N−n−プロピル(メタ)アクリルアミド、N−イソプロピル(メタ)アクリルアミド、N−シクロプロピル(メタ)アクリルアミド、N−メチル−N−エチルアクリルアミド、N,N−ジエチルアクリルアミド、N−メチル−N−イソプロピルアクリルアミド、N−メチル−N−n−プロピルアクリルアミド、N−アクリロイルピロリドン、N−アクリロイルピペリジンが挙げられる。これらの誘導体は1種のみを単独で使用してもよく、2種以上を使用してもよい。
【0021】
感温性ポリマー14は、ポリ(N−エチルアクリルアミド)、ポリ(N−エチルメタクリルアミド)、ポリ(N−n−プロピルアクリルアミド)、ポリ(N−n−プロピルメタクリルアミド)、ポリ(N−イソプロピルアクリルアミド)(以下、「NIPAMポリマー」という。)、ポリ(N−イソプロピルメタクリルアミド)、ポリ(N−シクロプロピルアクリルアミド)、ポリ(N−シクロプロピルメタクリルアミド)、ポリ(N−メチル−N−エチルアクリルアミド)、ポリ(N,N−ジエチルアクリルアミド)、ポリ(N−メチル−N−イソプロピルアクリルアミド)、ポリ(N−メチル−N−n−プロピルアクリルアミド)、ポリ(N−アクリロイルピロリドン)、ポリ(N−アクリロイルピペリジン)からなる群から選択される1種以上の感温性ポリマーであることが好ましい。
【0022】
本発明における感温性ポリマー14は、例えばマイクロアレイに用いる場合、ゲル組成物内で生体関連物質(キャプチャープローブ)と検体とを反応させる際に検体の拡散性がより向上する点から、それらを反応させる温度よりもTcが低いものを用いることが好ましい。例えば、DNAマイクロアレイの場合には、通常ハイブリダイゼーションが行なわれる40〜60℃程度よりもTcが低い感温性ポリマー14を用いることが好ましい。一方、マイクロアレイによる解析時(室温)における透明性の点からは、ある程度Tcが高い感温性ポリマー14であることが好ましい。
感温性ポリマー14は、ハイブリダイゼーションバッファー(2×SSC、0.2%SDS)中でのTcが20〜50℃のものがより好ましく、ポリ(N−イソプロピルアクリルアミド)、ポリ(N,N−ジエチルアクリルアミド)であることが特に好ましい。
【0023】
また、感温性ポリマー14の誘導体として、両イオン性のポリマー(ベタインポリマー)を用いることもできる。
両イオン性のポリマーは、分子内に第4アンモニウム塩基、オキソニウム塩基、スルホニウム塩基などを有するポリマーであり、N,N−ジメチル(アクリルアミドプロピル)アンモニウムプロパンサルフォネイト(以下、「DMAAPS」という。)を用いたポリマーであることが好ましい。
【0024】
LSCTを有する感温性ポリマーは、用いる溶液の塩濃度などによってLSCTが大きく変化する。特に、本発明のゲル組成物を核酸検出などのマイクロアレイなどに用いる場合、ハイブリダイゼーション時のバッファー組成によって感温性ポリマー14を選定することが重要となる。NIPAMポリマーなどは高塩濃度領域ではLCSTが下がり、室温においても白濁するためにDNAマイクロアレイなどには適用し難くなる。しかし、低塩濃度領域では良好な相転移挙動を示す。
【0025】
これに対し、DMAAPSを用いたポリマーは、両イオン性ポリマーであるため高い塩濃度領域の溶液中では分子が溶解する。そのため、用いるバッファー組成に応じた感温性ポリマー14とすることができる。例えば、2×SSC以下の塩濃度(0.2%SDS添加)であればNIPAMポリマー、2×SSCより高い塩濃度(0.2%SDS添加)であればDMAAPSを用いた感温性ポリマー14であることが好ましい。
ただし、特にポリマー部分にDMAAPSを用いる場合には、単独では塩溶液中で分子が溶解し、温度を上げても相転移しなくなる。そのため、この場合は、DMAAPSと、塩溶液中で溶解せずにLCSTを有する感温性ポリマーを形成する誘導体(好ましくはNIPAM)とを共重合した感温性ポリマー14とすることが好ましい。これにより、相転移温度を調整することが可能となる。
【0026】
感温性ポリマー14にDMAAPSを用いる場合、DMAAPSの割合は、感温性ポリマー14の共重合に用いる誘導体の合計(100mol%)に対して、5〜15mol%であることが好ましい。
DMAAPSの割合が5mol%以上であれば、高い塩濃度条件への適用が容易になる。また、DMAAPSの割合が15mol%以下であれば、感温性ポリマー14が充分な相転移を起こしやすい。
【0027】
感温性ポリマー14の質量平均分子量は、感温性ポリマー14の全長が細孔12の大きさ(架橋点間の距離)よりも小さくなるようにすることが好ましく、細孔12の大きさによっても異なるが、2000〜20000であることが好ましく、2000〜10000であることがより好ましい。
感温性ポリマー14の質量平均分子量が2000以上であれば、強度に優れたゲル組成物1が得られやすい。また、感温性ポリマー14の質量平均分子量が20000以下であれば、感温性ポリマー14が基盤ゲル10を巻き込まずに収縮するため、ゲル組成物1自体が収縮することを抑制しやすい。
【0028】
本発明のゲル組成物は、このような感温性ポリマー14が、その一端で基盤ゲル10に共有結合されている。
感温性ポリマー14の基盤ゲル10への共有結合は、例えば、前述した感温性ポリマーの末端に不飽和結合が導入された感温性マクロモノマーを用いることにより形成することができる。具体的には、例えば感温性ポリマーの末端にビニル基などを導入して感温性マクロモノマーを製造し、それをアクリルアミド系モノマーおよび架橋剤と共重合させることにより、基盤ゲル10に一端が共有結合された感温性ポリマー14が得られる。前記不飽和結合を有する官能基(不飽和官能基)はビニル基には限定されず、アクリレートやメタクリレート骨格のものでもよい。
【0029】
感温性ポリマーの末端に不飽和結合を導入する方法は、その末端に所望の不飽和結合を導入することができれば特に限定されない。以下に具体例として、NIPAMポリマー(感温性ポリマー)の末端にビニル基を導入してNIPAMマクロモノマー(感温性マクロモノマー)を得る方法を示す。NIPAMマクロモノマーの合成スキームは以下の通りである。ただし、該合成スキーム中のnは繰り返し単位数を示す。
【0030】
【化1】

【0031】
工程(I)は、Kanekoらの方法(Macromolecules,28,7712(1995))を利用した反応であり、連鎖移動剤として2−アミノエタンチオール(AESH)を用い、NIPAMを重合したNIPAMポリマーの末端にアミノ基を導入することによりポリマー(1)が得られる。
溶媒としては、N,N-ジメチルホルムアミド(DMF)、ジメチルスルホキシド(DMSO)などの極性溶剤を用いることができる。
反応温度は、60〜100℃であることが好ましい。
重合開始剤としては、2,2’−アゾビスイソブチロニトリル(AIBN)、2,2’−アゾビス(2−メチルブチロニトリル)、2,2’−アゾビス(2,4−ジメチルバレロニトリル)などを用いることができる。
【0032】
工程(II)は、Liらの方法(Small,2,917(2006))を用いた方法であり、工程(I)で得られたポリマー(1)と塩化アクリロイルとを反応させ、末端のアミノ基部分にビニル基を導入することによりNIPAMマクロモノマー(2)が得られる。
溶媒としては、N,N−ジメチルホルムアミド(DMF)、ジメチルスルホキシド(DMSO)などの極性溶剤を用いることができる。
反応温度は、30〜50℃であることが好ましい。
【0033】
ゲル組成物の製造における共重合時の全モノマー濃度(アクリルアミド系モノマーおよび感温性マクロモノマーの合計)は、100〜700mol/m3であることが好ましい。
全モノマー濃度が100mol/m3以上であれば、より高強度のゲル組成物が得られやすい。また、全モノマー濃度が700mol/m3以下であれば、検体の拡散性がより向上したゲル組成物1が得られる。
【0034】
感温性マクロモノマーの共重合率は、アクリルアミド系モノマーおよび感温性マクロモノマーの合計(100mol%)に対して、0.01〜4mol%であることが好ましくい。
感温性マクロモノマーの共重合率が0.01mol%以上であれば、強度に優れたゲル組成物1が得られやすい。また、感温性マクロモノマーの共重合率が4mol%以下であれば、充分にゲル化が進行したゲル組成物1が得られやすく、ゲル組成物1内での検体の拡散性を向上させやすい。
【0035】
尚、感温性マクロモノマーを製造する方法は前述の方法には限定されず、導入する不飽和結合に応じた方法を用いることができる。
また、感温性ポリマー14の一端を基盤ゲル10に共有結合する方法は感温性マクロモノマーを用いる方法には限定されず、例えば、予め基盤ゲルのポリマー鎖中に反応性官能基を導入しておき、該官能基と反応する官能基を導入した感温性ポリマーと反応させる方法を用いてもよい。ここで利用できる反応としては、例えば、アルデヒド基とアミノ基とでシッフ塩基を形成させる反応やエチレンオキサイドとアミノ基との開環反応を利用する反応、または同じくエポキシとカルボン酸との反応などが挙げられる。
【0036】
[第2実施形態]
ゲル組成物2は、ゲル組成物1にさらに生体関連物質が含まれている組成物であり、図2に示すように、アクリルアミド系モノマーと架橋剤の共重合により得られる網目構造体からなる基盤ゲル10と、該基盤ゲル10に一端が共有結合された感温性ポリマー14と、基盤ゲル10に共有結合された生体関連物質16を含む組成物である。ゲル組成物2では、基盤ゲル10により形成された細孔12内に、感温性ポリマー14と生体関連物質16が配置される。
基盤ゲル10を形成するアクリルアミド系モノマーおよび架橋剤、感温性ポリマー14についてはゲル組成物1と同じであるので説明を省略する。
【0037】
生体関連物質16は、検出または測定の対象となる物質(検体)を捕獲するキャプチャープローブである。
生体関連物質16としては、DNA、RNA(リボ核酸)、蛋白質、脂質などが挙げられる。これらの生体関連物質は、市販品であってもよく、生細胞などから得ることもできる。生細胞からのDNAの抽出は、Blinらの方法(Nucleic Acids Res.,3,2303(1976))などを用いることができる。また、生細胞からのRNAの抽出は、Favaloroらの方法(Methods.Enzymol.,65,718(1980))などを用いることができる。
【0038】
また、DNAとしては、鎖状若しくは環状のプラスミドDNAまたは染色体DNAを用いることができる。さらには、制限酵素若しくは化学的に切断したDNA断片、試験管内で酵素などにより合成されたDNAまたは化学合成したオリゴヌクレオチドなどを用いることもできる。
【0039】
生体関連物質16は、アクリルアミド系モノマーおよび架橋剤との共重合反応により、基盤ゲル10の網目構造に固定することができる。すなわち、生体関連物質16は、感温性ポリマー14と同様に、共重合反応可能な不飽和官能基を導入し、アクリルアミド系モノマーおよび架橋剤と共重合させることにより、基盤ゲル10に共有結合させることができる。
不飽和官能基としては、ビニル基の他、アクリレート基や、メタクリレート基が挙げられる。不飽和官能基は、生体関連物質16の機能を損なわない限り、そのいずれの部位に導入されていてもよい。例えば、生体関連物質16が核酸の場合、不飽和官能基は核酸の末端、鎖中のいずれに導入されていてもよい。ただし、生体関連物質16と検体とのハイブリダイゼーション効率がより向上する点から、核酸の末端に導入されていることが好ましい。
前記不飽和官能基は、国際公開第02/062817号パンフレットに記載の方法などにより導入することができる。
【0040】
生体関連物質16の共重合率は、目的、用途に応じて調整することができ、アクリルアミド系モノマー、感温性ポリマー14および生体関連物質16の合計(100mol%)に対して、10〜100000μmol%であることが好ましく、100〜10000μmol%であることがより好ましい。
生体関連物質16の共重合率が10μmol%以上であれば、ゲル組成物2をマイクロアレイなどに用いた場合の検出、測定の効率および精度を向上させやすい。また、生体関連物質16の共重合率が100000μmol%以下であれば、ゲル組成物2内での検体の拡散性を向上させやすい。
【0041】
本発明のゲル組成物は、前記アクリルアミド系モノマー、架橋剤、感温性ポリマー、生体関連物質以外の他の成分を含んでいてもよい。
他の成分としては、例えば、グリセリンなどが挙げられる。
【0042】
[製造方法]
以下、本発明のゲル組成物の製造方法として、前述のゲル組成物1およびゲル組成物2の製造方法の一例について説明する。
ゲル組成物1は、アクリルアミド系モノマー、架橋剤、および感温性マクロモノマーを共重合させることにより得ることができる。また、ゲル組成物2は、アクリルアミド系モノマー、架橋剤、感温性マクロモノマー、および生体関連物質を共重合させることにより得ることができる。
【0043】
前記共重合の方法としては、例えば、重合開始剤を用いる方法が挙げられる。
重合開始剤は、重合反応の間に感温性マクロモノマーや生体関連物質が分解しない方法であれば特に限定されず、2,2’−アゾビス[2−(2−イミダゾリン−2−イル)プロパン]ジハイドロクロライド、APS(過硫酸アンモニウム)、KPS(過硫酸カリウム)などが挙げられる。
また、重合開始剤としてAPS、KPSを用いる場合は、重合促進剤としてTEMED(テトラメチルエチレンジアミン)を用いることが好ましい。
【0044】
重合に用いる溶媒としては、水、エタノールなどを用いることができる。
また、重合温度は、用いる感温性マクロモノマーのTcよりも低い温度となる範囲内で、アゾ系の重合開始剤を用いる場合には45℃以上、APS、KPSを単独で用いる場合は50℃以上、APS、KPSにTEMEDを併用する場合は20〜40℃の範囲内とすることが好ましい。
【0045】
以上説明した本発明のゲル組成物は、Tcより低い温度では、図1(A)および図2(A)に示すように、基盤ゲル10の細孔12内で感温性ポリマー14が広がって存在している。そのため、細孔12の有効細孔径が感温性ポリマー14により縮小された状態となっており、該感温性ポリマー14が障害となって検体の拡散性に劣る。ただし、この状態ではゲル組成物は巨視的に透明であるため解析には適している。ここで、本発明における「透明」とは、光透過率がゲルの厚さ2mmで80%程度以上であることを意味する。
【0046】
一方、Tcよりも高い温度になると、図1(B)および図2(B)に示すように、基盤ゲル10に一端が共有結合された感温性ポリマー14が収縮することで、細孔12の有効細孔径が、感温性ポリマー14がない場合とほぼ同等の状態となる。これにより、ゲル組成物中での検体の拡散性が向上する。感温性ポリマー14は温度を下げることで図1(A)および図2(A)に示したような拡がった状態に戻り、ゲル組成物は巨視的に透明になる。
以上のように、生体関連物質を有するゲル組成物を用いて検出や測定を行う場合に、該生体関連物質と検体との反応効率を向上させることができる。
【0047】
また、本発明のゲル組成物では、このような機構により検体の拡散性を向上させるため、基盤ゲル10が感温性ポリマー14の収縮に巻き込まれて収縮し、ゲル組成物自体が収縮することが抑制される。したがって、基盤ゲル10の収縮により細孔12の有効細孔径が縮小することを抑制することができ、検体の拡散性が充分に向上する。
【0048】
以上のように、本発明のゲル組成物は、生体関連物質と検体との反応の際には温度をTcよりも高くすることにより感温性マクロモノマーを収縮させて拡散性を向上させ、検体の検出時にはTcよりも低い温度にすることでゲル組成物を均一に戻して透明に変化させ、蛍光検出の際の励起光をゲル全体に透過させることができる。そのため、検出感度が極めて高くなる。
【0049】
本発明のゲル組成物は、例えば、生体関連物質(キャプチャープローブ)を保持するゲル(ゲル組成物2)を遺伝子解析に使用することができる。例えば、前述のゲル組成物2を管状体の中空部に充填することによりゲル保持管状体を作製することで、特開平3−47097号公報に記載のごとく、遺伝子変異を解析するためのツールとして使用できる。前記中空部へのゲル組成物の保持は、キャピラリーゲル電気泳動に使用されるキャピラリーカラムを作製するのと同様の方法で実施することができる。
【0050】
<マイクロアレイ>
以下、本発明のマイクロアレイについて説明する。本発明のマイクロアレイは、基板を有し、該基板に形成された区画に前述のゲル組成物が配置されている。以下、その実施形態の一例について説明する。
【0051】
本実施形態のマイクロアレイ20は、図4に示すように、基板22に複数の管状体24が固定されており、管状体24が有する中空部が貫通孔26(区画)を形成している。また、貫通孔26にはゲル組成物2が保持されている。
【0052】
基板22は、複数本の管状体24が束ねられたものを固定化する接着剤により形成される。
接着剤は、マイクロアレイの製造に通常用いられる樹脂を用いることができ、例えば、ニッポラン4276、コロネート4403(登録商標。日本ポリウレタン工業(株)製)などのポリウレタン樹脂接着剤が挙げられる。
【0053】
基板22の形状は、通常、貫通孔(管状体)を規則的に配列させて、正方形または長方形とされるが、これらに限定されるものではない。「規則的に」とは、一定の大きさの枠の中に含まれる管状体の本数が一定となるよう順序よく配列させることをいう。
また、基板22の厚さは、50μm〜1mmであることが好ましい。
【0054】
管状体24は、中空部を有する管状の形態であれば、ガラス管、ステンレス管、中空繊維、パルプなどいずれの形態であってもよい。加工性、取り扱いの容易さを考慮すると中空繊維を使用することが好ましい。なお、中空繊維としては、特に限定されるものではないが、例えば合成繊維、半合成繊維、再生繊維、天然繊維などが挙げられる。また、管状体24は、多孔質管状体、非多孔質管状体のいずれでもよいが、ゲル組成物の重合前の前駆体溶液の中空繊維外への拡散や、ゲル組成物の乾燥を抑制する点から、非多孔質管状体であることが好ましい。
【0055】
管状体24の材質は特に限定はなく、シリカ、ガラスなどの無機材料や、以下に示す有機材料などが挙げられる。
有機材料としては、例えば、ナイロン6、ナイロン66、芳香族ポリアミドなどのポリアミド系材料、ポリエチレンテレフタレート、ポリブチレンテレフタレート、ポリ乳酸、ポリグリコール酸、ポリカーボネートなどのポリエステル系材料、ポリアクリロニトリルなどのアクリル系材料、ポリエチレンやポリプロピレンなどのポリオレフィン系材料、ポリメタクリル酸メチルなどのポリメタクリレート系材料、ポリビニルアルコール系材料、ポリ塩化ビニリデン系材料、ポリ塩化ビニル系材料、ポリウレタン系材料、フェノール系材料、ポリフッ化ビニリデンやポリテトラフルオロエチレンなどのフッ素系材料、ポリアルキレンパラオキシベンゾエート系材料などが挙げられる。また、カーボンブラックなどの黒色顔料が含有されていてもよい。
【0056】
貫通孔26(管状体24の中空部)は、整列固定化されていることが好ましい。
貫通孔26の内径(管状体24の内径)は、特に限定されないが、1mm以下であることが好ましく、10μm〜300μmであることがより好ましい。
【0057】
貫通孔26の数(区画数)は、管状体24の本数により決定される。本発明のマイクロアレイの区画数は、マイクロアレイにおける通常の区画数とすることができ、10〜10000個/cm2であることが好ましい。
【0058】
[製造方法]
本発明のマイクロアレイは、以下の(i)〜(iii)の工程により製造することができる。
工程(i):複数本の管状体をそれらの長手方向が一致するように集束して集束物を得る工程。
工程(ii):前記集束物の各々の管状体の中空部に、アクリルアミド系モノマー、架橋剤および感温性マクロモノマーを含む前駆体溶液(本発明のゲル組成物の重合前の溶液)を充填し、中空部内で所定の重合温度(例えば40℃以下の重合温度)で共重合反応する工程。
工程(iii): 集束物を、該集束物の長手方向と交叉する方向に切断する工程。
工程(ii)では、中空部に本発明のゲル組成物2(生体関連物質を含むゲル組成物)を含むものを充填することが好ましい。
【0059】
以下、マイクロアレイの製造方法の一実施形態例として、図1に例示した、貫通孔26を100個有する、基板22の形状が正方形のマイクロアレイ20を製造する方法について説明する。
工程(i)では、10本の管状体を、1列に束ねて固定化して1層のシートとした後、各々の管状体の長手方向が一致するように、前記シートが10層になるように重ねて固定化することにより集束物を得る。工程(i)における管状体の固定化方法は、例えば、ポリウレタン樹脂接着剤などの接着剤により行う方法が挙げられる。
【0060】
ついで、工程(ii)において、集束物の各々の管状体の中空部に本発明のゲル組成物の前駆体溶液を充填する。前駆体溶液の充填方法は特に限定されず、例えば、集束物の一方の端部を前駆体溶液中に浸した状態で、もう一方の端部側から吸引する方法であってもよく、集束物の一方の端部側から前駆体溶液を押し込む方法であってもよい。
また、管状体の一方を封止し、減圧した後、開放端を前駆体溶液に浸し、その状態で常圧に戻すことにより吸引する方法であってもよい。
【0061】
工程(ii)における前駆体溶液の共重合の重合温度は、用いる感温性マクロモノマーのTc以下で行うことが好ましい。好ましい温度範囲は40℃以下である。重合温度が40℃より高い温度で行うと、重合中に感温性マクロモノマーが相転移し、白濁したゲル組成物になりやすくなる。このようなゲル組成物は、温度を低くしても透明にならないため、解析には不適切である。前述のような温度で重合を行うための開始剤としては、APSにTEMEDを添加したものや光分解型の開始剤などを用いることができる。
【0062】
工程(iii)では、得られた集束物を、該集束物の長手方向と交叉する方向に切断して薄片化する。これにより、100個の貫通孔26が形成された、所望の厚さの基板22を有するマイクロアレイ20が得られる。切断方法は、集束物を所望の厚さで切断できる方法であれば特に限定されず、例えば、ミクロトームにより切断する方法などが挙げられる。
【0063】
また、以上説明した工程(i)〜(iii)によりマイクロアレイ20を得ることができるが、工程(i)と工程(ii)の順序は特に限定されず、工程(ii)を行った後に工程(i)を行ってもよい。すなわち、各々の管状体の中空部に前駆体溶液を充填して重合反応した(工程(ii))後に、それらの管状体を集束して集束物を形成(工程(i))し、該集束物を薄片化してマイクロアレイを得る方法であってもよい(国際公開第00/5376号パンフレット参照)。
【0064】
以上説明した本発明のマイクロアレイは、本発明のゲル組成物を用いていることから、通常室温で行なわれる解析時には透明性を有しており、ハイブリダイゼーションなどの温度を上昇させた際には検体の拡散性を向上させることができるため、高効率かつ高精度な解析が可能となる。
尚、本発明のマイクロアレイは、図4に例示したマイクロアレイには限定されない。例えば、本発明のマイクロアレイの区画は、マイクロアレイ20のような貫通孔には限定されず、溝による区画であってもよい。ただし、前述の工程(i)〜(iii)による大量生産に適している点から、管状体を用いた貫通孔により区画を形成するマイクロアレイであることが好ましい。
【0065】
また、ゲル組成物2の代わりにゲル組成物1を配置したマイクロアレイであってもよい。
また、平面基板上に重合前または重合開始直後のキャプチャープローブを含む前駆体溶液を、予め定めた区画にスポッティングしたマイクロアレイであってもよい(特表平6−507486号公報、米国特許第5770721号明細書参照)。
【実施例】
【0066】
以下、実施例および比較例を示して本発明を詳細に説明する。ただし、本発明は以下の記載によっては限定されない。
<感温性マクロモノマー>
[製造例1]
前述の合成スキームを用いて感温性マクロモノマーであるNIPAMマクロモノマーを合成した。
工程(I)では、連鎖移動剤であるAESH(0.43446g)、NIPAM(11.5900g)、および溶媒であるDMFを、75℃のオイルバスに設置したコンデンサー付きのパラブルフラスコに仕込み、高純度窒素ガスを2時間パージした。次いで、予めDMFに溶解して室温にて高純度窒素ガスでパージしておいた重合開始剤のAIBN(0.1774g)を加え、高純度窒素ガス雰囲気下で15時間反応させた。反応に用いたDMFは45mLであった。
反応終了後、真空乾燥機を用いてDMFを除去し、感温性マクロモノマーの前駆体である末端にアミノ基を有するポリマー(1)を得た。次いで、ポリマー(1)を精製するために、得られた反応物をアセトンに再溶解させ、ジエチルエーテルに滴下し、ポリマー(1)を沈殿させた。その後、濾過を行い、再度ジエチルエーテルで精製した後、乾燥を行った。
【0067】
工程(II)では、得られたポリマー(1)(3.0g)、塩化アクリロイル(20mL)、およびDMF(5mL)をサンプル瓶に投入し、高純度窒素ガスをパージしながら室温で30分間攪拌した。これを温度40℃の恒温槽に移し、さらに2時間、高純度窒素ガス雰囲気下で攪拌し、反応を行った。反応終了後、得られた反応液をジエチルエーテルに滴下し、反応生成物のNIPAMマクロモノマーを沈殿させ、濾過した。更に、同様の操作を2回行って精製し、濾過回収したNIPAMマクロモノマーを真空乾燥した。
【0068】
[NMR分析]
製造例1で得られたNIPAMマクロモノマーを1H−NMRにより分析した結果を図5に示す。1H−NMRの測定溶媒には重水(D2O)を使用した。
図5(A)、(B)に示すように、NMRスペクトルの5.6〜6.5ppmの範囲に、ビニル基に特有のピーク(g)、(h)、(i)が見られ、末端にビニル基を有する目的のNIPAMマクロモノマーが得られていることが確認された。
【0069】
また、NMRスペクトルにおけるピーク積分比から、得られたNIPAMマクロモノマーの分子量を推算した。図6に示すように、末端のビニル基のピーク(H分1つのピーク)とNIPAMポリマー部分のイソプロピル基のピーク(H分6つのピーク)との積分比(1:125.7383)より、NIPAMポリマー部分の繰り返し単位数はn=21と推定した。これにより、NIPAMマクロモノマーの質量平均分子量は2500g/mol程度であると推定した。
【0070】
[相転移温度の測定]
また、製造例1で得られたNIPAMマクロモノマーの相転移温度(Tc)を、溶液の透過度(波長600nm)の温度依存性を測定することにより評価した。透過度の測定には、ペルチェ素子温度制御機能付き分光光度計(日本分光V530型)を用いた。水中、およびハイブリダイゼーションバッファー(2×SSC、0.2%SDS)中に、NIPAMマクロモノマーを5g/Lの割合で溶解し、透過度の温度依存性を求めた。その結果を図7に示す。
【0071】
図7に示すように、水中では、約34℃で著しい透過度の減少が起こっており、この温度がTcであるとみなすことができる。この製造例1で得られたNIPAMマクロモノマーのTcは、高分子量のNIPAMポリマー(ビニル基を導入していないもの)と同等の値であった。
また、ハイブリダイゼーションバッファー中では、Tcは水中の場合と比べて高温側に数℃シフトしていた。これは、塩であるSSCのTcを低下させる作用に比べ、界面活性剤であるSDSのTcを上昇させる作用がより大きいためであると考えられる。
【0072】
<ゲル組成物>
[実施例1]
アクリルアミド系モノマーであるN,N−ジメチルアクリルアミド(DMAA)、架橋剤であるN,N’−メチレンビスアクリルアミド(MBAA)、前記NIPAMマクロモノマーを、溶媒である水に溶解し、重合開始剤であるAPS、重合促進剤であるTEMEDを用いて、NIPAMマクロモノマーのTcより低い20℃で重合反応を行い、基盤ゲルと該基盤ゲルに一端が共有結合されたNIPAMポリマーとを有するゲル組成物を得た。尚、架橋剤の濃度は4mol/m3、TEMEDおよびAPSの濃度はそれぞれ10mol/m3および0.5mol/m3とした。また、全モノマー(DMAAとNIPAMマクロモノマーの合計)濃度を400mol/m3、NIPAMマクロモノマーの共重合率を5mol%とした。
全モノマー濃度を400mol/m3、架橋剤濃度を4mol/m3とした場合、架橋点間距離はDMAA単位100個程度(分子量10000程度)となると考えられ、NIPAMマクロモノマーよりも大きくなる。
【0073】
[実施例2〜13]
前記全モノマー濃度およびNIPAMマクロモノマーの共重合率を表1に示す通りに変更した以外は、実施例1と同様にしてゲル組成物を得た。
実施例1〜13で得られたゲル組成物のゲル化の状態を評価した結果を表1に示す。ゲル化の評価は、以下の基準に基づいて行なった。
◎:充分にゲル化した。
○:ゲル化が見られたが柔らかかった。
【0074】
【表1】

【0075】
表1に示すように、全モノマー濃度が400mol/m3の場合には、NIPAMマクロモノマーの共重合率が5mol%(実施例1)では得られたゲル組成物が柔らかかったが、3.5mol%以下(実施例2〜6)ではより強度に優れたゲル組成物が得られた。また、全モノマー濃度が300mol/m3の場合では、NIPAMマクロモノマーの共重合率が3.5mol%(実施例7)では得られたゲル組成物が柔らかかったが、3mol%以下(実施例8および9)ではより強度に優れたゲル組成物が得られた。
また、全モノマー濃度が267mol/m3の場合は、NIPAMマクロモノマーの共重合率が3mol%(実施例10)であっても1mol%(実施例11)であっても共に強度に優れたゲル組成物が得られ、全モノマー濃度が200mol/m3の場合(実施例12および13)に比べて強度に優れたゲル組成物が得られやすいことが分かった。
【0076】
[実施例14〜17]
全モノマー濃度を400mol/m3、NIPAMマクロモノマーの共重合率を0.5、1、2、3mol%とし、厚さ3mmのスペーサーを2枚のガラス板で挟んで形成した空間内で、APSおよびTEMEDを用いて20℃で重合反応を行い、厚さ3mmの板状ゲルを作製した。架橋剤の濃度は4mol/m3、TEMEDおよびAPSの濃度はそれぞれ10mol/m3および0.5mol/m3とした。それ以外は、実施例1〜13と同様に行った。
【0077】
[白濁化の評価]
光路長10mmの石英セルを用い、前記板状ゲルを該石英セルに入るように切断して挿入し、板状ゲルが光路に対して垂直になるようにペルチェ素子温度制御機能付き分光光度計(日本分光V530)に設置し、水中における透過度を測定した。測定結果を図8(A)に示す。
また、同様の方法でハイブリダイゼーションバッファー(2×SSC、0.2%SDS)中における透過度を測定した。測定結果を図8(B)に示す。
【0078】
図8(A)に示すように、水中の場合は、NIPAMマクロモノマーのTcである34℃を超えるとゲル(板状ゲル)が白濁した。また、この白濁の程度は、NIPAMマクロモノマーの共重合率が高くなるにつれて大きくなった。ただし、共重合率が3mol%になると白濁の程度が小さくなった。これは、共重合時のNIPAMマクロモノマーの割合が多くなることで、ゲル化の程度が低下するためであると考えられる。
また、ハイブリダイゼーションバッファー中では、図8(B)に示すように、NIPAMマクロモノマーの共重合率が2mol%の場合に70℃で若干の白濁化が見られたが、それ以外の共重合率の場合には白濁化が見られなかった。
【0079】
[実施例18]
NIPAMマクロモノマーの共重合率を1mol%とし、内径3.4mmのガラス管内で合成する以外は、実施例14〜17と同様にして円柱状ゲルを作製した。
【0080】
[参考例1]
NIPAMマクロモノマーを用いなかった以外は実施例18と同様の方法で円柱状ゲルを作製した。
【0081】
[膨潤度の温度依存性]
実施例18および参考例1で得られた円柱状ゲルについて、円柱状ゲルの膨潤径を、水中およびハイブリダイゼーションバッファー(2×SSC、0.2%SDS)中で各温度にて読み取り顕微鏡を用いて測定し、その温度依存性を評価した。水中での結果を図9(A)、ハイブリダイゼーションバッファー中での結果を図9(B)に示す。図9(A)、(B)における破線は、ゲルの合成に用いたガラス管の内径(3.4mm)を示している。
【0082】
実施例18の円柱状ゲルの膨潤径は、図9(A)に示すように、水中において基盤ゲル(DMAA)のみの参考例1と比較して多少収縮が見られたが、その温度依存性は小さかった。また、ハイブリダイゼーションバッファー中では、図9(B)に示すように、参考例1とほぼ同等の膨潤径であり、温度依存性が非常に小さかった。
水中に比べてハイブリダイゼーションバッファー中における温度依存性が小さいのは、界面活性剤であるSDSによりNIPAMポリマーの収縮がある程度低減されるためであると考えられる。
【0083】
次に、基盤ゲルに一端が共重合されたNIPAMポリマー(感温性ポリマー)の収縮による検体の拡散性の向上について評価するため、モデル物質として濃度測定が容易なローダミンBを用い、該ローダミンBの拡散係数の温度依存性を測定した。以下、拡散係数の温度依存性の測定について説明する。
【0084】
[実施例19]
全モノマー濃度を400mol/m3、NIPAMマクロモノマーの共重合率を1mol%として、図10に示すガラス製ゲルホルダー30内で重合反応を行なってゲル組成物からなるゲル膜1Aを得た。架橋剤の濃度は4mol/m3、TEMEDおよびAPSの濃度はそれぞれ10mol/m3および0.5mol/m3とした。
ガラス製ゲルホルダー30は、上部にゲル組成物の前駆体溶液を投入する開口を有するガラス板32が2枚のガラス板34で挟まれ、さらに金網38を有するガラス板36で挟まれた形態を有しており、ガラス板32、34および金網38で囲まれる空間内でゲル膜を製造することができる。そして、ゲル膜1Aを通過できる溶液などが、一方の側から金網38、ゲル膜、金網38を順に通って他方の側へと通過できるようになっている。
ガラス板32の上部に形成された開口は、接着剤40により封止した。
【0085】
次いで、2つのガラスセル52(容量500mL)を有し、各々のガラスセル52にそれぞれ300mLの水が入れられ、さらにそれらガラスセル52A、52Bが共に恒温槽54に入れられている拡散係数測定装置50(図11)の2つのガラスセル52A、52Bの間に、ゲル膜1Aを有するガラス製ゲルホルダー30を設置した。その後、ゲル膜1Aおよびガラスセル52A、52B内の水の温度を所定温度まで上げ、ガラスセル52Aの水中に前記所定温度のローダミンB水溶液(ローダミンB濃度:0.2g/L)100mLを注入し、ガラスセル52Bに水100mLを注入した。その後、ガラスセル52B側に拡散してきたローダミンBの濃度を経時的に測定し、拡散係数の温度依存性を評価した。ガラスセル52BにおけるローダミンBの濃度の測定は、分光光度計(日本分光V530型)を用いて波長533nmにて行なった。
【0086】
[比較例1]
NIPAMマクロモノマーを用いていないDMAAのみのゲル膜1Bを形成した以外は、実施例19と同様にしてガラスセル52BにおけるローダミンBの濃度を測定し、拡散係数の温度依存性を評価した。
【0087】
[拡散係数の測定および評価]
拡散係数は、以下に示す手順で算出することができる。
まず、時間tまでにゲル膜を透過したローダミンBの単位面積あたりの量Qは、下記式で表される。
【数1】

ここで、式中のC(t)、V、Xは以下の意味を示す。
C(t):時間tにおけるガラスセル52B側のローダミンBの濃度
V:ガラスセル52B内の溶液の容積
X:ゲル膜の面積
【0088】
上記式において、C(t)はガラスセル52A側のローダミンBの初期濃度C0に比べて非常に小さく、ローダミンBのゲル膜の透過速度が一定であると仮定し、拡散に関するFickの式を適用すると、次式が導かれる。
【数2】

ここで、式中、Dおよびdは以下の意味を示す。
D:ゲル膜中の拡散係数
d:ゲル膜の厚さ
これにより、拡散係数Dは次式のように表されるので、ガラスセル52B側のローダミンBの濃度の経時変化を測定することにより拡散係数を算出することができる。
【数3】

【0089】
測定については、ハイブリダイゼーションバッファー中では、バッファーとローダミンBとの間に相互作用が見られたため、水中での測定のみとした。
実施例19および比較例1における拡散係数の温度依存性の測定結果を図12に示す。また、実施例19における拡散係数のアレニウス(Arrhenius)プロットを図13に示す。
【0090】
図12に示すように、NIPAMマクロモノマーを共重合したNIPAMポリマーを有するゲル膜である実施例19では、温度上昇と共に拡散係数が大きく増加し、25℃の場合に比べて70℃では拡散係数が約4倍になっていた。また、水中でのNIPAMマクロモノマー(NIPAMポリマー)のTcである34℃の前後で拡散係数の増加傾向が異なっていた。一方、NIPAMマクロモノマーを用いていないDMAAのみの比較例1では、拡散係数が温度上昇と共に増加しているものの、低温領域において拡散係数が実施例19よりも大きかった。
このように、実施例19と比較例1は、低温領域では拡散係数に差が見られたが、温度上昇に伴ってその差が減少し、高温領域ではそれらの拡散係数がほぼ同等となった。
【0091】
この結果は、以下のように考えられる。実施例19のゲル膜1Aと比較例1のゲル膜1Bは、全モノマー量が共に400mol/m3であるため、より分子量が大きい長鎖のNIPAMポリマーを有する実施例19のゲル膜1Aの方が高密度である。そのため、Tcよりも低い温度では、NIPAMポリマーが拡がった構造で存在していることで、ゲル膜1Aの有効細孔径が小さくなっており、ローダミンBの拡散がゲル膜1Bに比べてより抑制されている。一方、Tcよりも高い温度では、NIPAMポリマーが収縮することによりゲル膜1Aの有効細孔径がゲル膜1Bの有効細孔径とほぼ同等となるために、拡散係数の温度依存性に対するNIPAMポリマーの影響が非常に小さくなり、拡散係数がほぼ同等になると考えられる。
【0092】
また、実施例19のゲル膜1Aでは、図13に示すように、Tc付近でアレニウスプロットの勾配(−Ea/RT、Ea:活性化エネルギー、R:気体定数)が大きく変化しており、Tcより低い温度に比べて高い温度で活性化エネルギーが小さくなっていた。この結果も、Tcを超えるとNIPAMポリマーの収縮が起こることで、ローダミンBの拡散性が向上することを示していると考えられる。
【産業上の利用可能性】
【0093】
本発明のゲル組成物は、解析の際には透明性を有し、温度を上昇させることで検体の拡散性を向上させることができる。そのため、高効率で高精度な検出または測定が行えるマイクロアレイなどとして好適に使用できる。
【図面の簡単な説明】
【0094】
【図1】本発明のゲル組成物の一実施形態例を示した概念図である。
【図2】本発明のゲル組成物の他の実施形態例を示した概念図である。
【図3】従来のゲル組成物の実施形態の一例を示した概念図である。
【図4】本発明のマイクロアレイの一実施形態例を示した斜視図である。
【図5】本実施例におけるNIPAMマクロモノマーのNMRスペクトルを示した図である。
【図6】本実施例におけるNIPAMマクロモノマーのNMRスペクトルを示した図である。
【図7】本実施例におけるNIPAMマクロモノマーの透過度の測定結果を示した図である。
【図8】実施例14〜17のNIPAMマクロモノマーの透過度の測定結果を示した図である。(A)水中、(B)ハイブリダイゼーションバッファー中。
【図9】実施例18および参考例1の膨潤径の測定結果を示した図である。(A)水中、(B)ハイブリダイゼーションバッファー中。
【図10】本実施例で用いたガラス製ゲルホルダーを示した図である。(A)ガラス製ゲルホルダーの中央部のガラス板積層部分の正面図、(B)縦分解断面図。
【図11】本実施例で用いた拡散係数測定装置を示した模式図である。
【図12】実施例19および比較例1の拡散係数の温度依存性を示した図である。
【図13】実施例19の拡散係数のアレニウスプロットを示した図である。
【符号の説明】
【0095】
1 ゲル組成物 2 ゲル組成物 10 基盤ゲル 12 細孔 14 感温性ポリマー 16 生体関連物質 20 マイクロアレイ 22 基板 24 管状体 26 貫通孔
【技術分野】
【0001】
本発明は、ゲル組成物およびその製造方法、ならびに該ゲル組成物を用いたマイクロアレイに関する。
【背景技術】
【0002】
遺伝子の分析手段においては、特定のプローブを使用してDNA配列の解析、遺伝子発現解析などを一括して実施できるマイクロアレイが広く用いられている。このようなマイクロアレイの具体例としては、基板の2次元表面上でフォトリソグラフィーによりキャプチャープローブ(DNA(デオキシリボ核酸)、ペプチドなど)が逐次的に合成されたマイクロアレイ(特許文献1)、予め合成しておいたキャプチャープローブが基板の2次元表面上にスポッティングされたマイクロアレイ(特許文献2)、樹脂板などからなる基板に複数の溝または貫通孔(中空部)が形成され、それらの溝または貫通孔の内部にDNAなどを含有するゲルが保持されたマイクロアレイ(特許文献3)、平面基板上にDNAなどを含有するゲルのスポットが配置されたマイクロアレイ(特許文献4)などが知られている。また、中空繊維の中空部にゲルが保持された中空繊維配列体が、該中空繊維配列体の繊維軸と交叉する方向に切断されることにより得られるマイクロアレイ(特許文献5)が知られている。
【0003】
DNAマイクロアレイでは、基板に固定されたキャプチャーDNA(キャプチャープローブ)が前記基板に沿って倒れたような状態となることで、対象の遺伝子由来のDNA断片とのハイブリダイゼーション(二重螺旋形成反応)の効率が低くなることがある。
しかし、特許文献3〜5のようなゲルを用いたマイクロアレイでは、ゲル中の三次元反応場において、より生態環境に近いハイブリダイゼーションが可能となる。また、基板の2次元表面にキャプチャーDNAが固定されたマイクロアレイに比べて、一区画に固定化できるキャプチャーDNA量が多い。そのため、キャプチャーDNAと対象のDNA断片とのハイブリダイゼーション効率が高くなり、解析の精度および効率に優れる。
【0004】
また、このようなマイクロアレイでは、検査対象となるDNA断片などの試料(以下、「検体」という。)がゲル組成物の網目構造中で充分に拡散することで、ゲル組成物中のキャプチャーDNAとの高いハイブリダイゼーション効率が達成される。しかし、特許文献3〜5のようなマイクロアレイでは、ゲルの網目構造中で検体が充分に拡散せず、検査に使用できる領域がゲル表面に限定される場合もあった。
【0005】
このように、マイクロアレイに用いるゲル組成物は、キャプチャープローブと検体との反応時には検体の拡散性に優れていることが重要である。また、それと同時に蛍光分析などの解析時には透明性に優れていることも重要である。
そこで、ゲルの編目構造の有効細孔径を大きくし、検体の拡散性を向上させる特性を有するゲル組成物として、図3に示すように、モノマーと架橋剤とキャプチャープローブとを共重合させて得られる網目構造体からなる基盤ゲル110と、該基盤ゲル110の構成成分には共有結合されていない感温性ポリマー114とを含むゲル組成物101が示されている(特許文献6)。このゲル組成物101は、基盤ゲル110の網目構造中に、直鎖状の感温性ポリマー114が絡んだ構造を有している。また、感温性ポリマー114は、相転移温度以上になると疎水性相互作用により収縮する性質を有している。
【0006】
ゲル組成物101は、相転移温度よりも低温では、図3(A)に示すように、感温性ポリマー114が広がった状態であり、巨視的には均質で透明である。一方、相転移温度よりも高温では、図3(B)に示すように、感温性ポリマー114が疎水性相互作用により基盤ゲル110を巻き込みながら収縮し、該基盤ゲル110中の細孔112が崩壊して疎密構造を形成する。このとき、基盤ゲル110の網目構造が不均一な疎密構造となるためにゲル組成物101が白濁化する。
このようなゲル組成物101を基板に形成された区画に配置することにより、解析の際には透明性を有し、かつハイブリダイゼーション(40〜60℃程度)の際には検体の拡散性が向上するマイクロアレイを得ることができる。
【特許文献1】米国特許第5405783号明細書
【特許文献2】米国特許第5601980号明細書
【特許文献3】特開2000−60554号公報
【特許文献4】米国特許第6682893号明細書
【特許文献5】特開2000−270877号公報
【特許文献6】特開2008−13663号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
しかし、ゲル組成物101では、高温時に感温性ポリマー114が基盤ゲル110を巻き込みながら収縮することで疎密構造を形成するため、それに伴って基盤ゲル110が収縮し、ゲル組成物101自体の収縮が見られる。そのため、基盤ゲル110の収縮により、その基盤ゲル110中に作り出される疎な部分が充分に大きくならず、ハイブリダイゼーションの際の検体の拡散性が充分に向上しないことがあった。また、場合によっては、その収縮によりゲル組成物101が基板の区画から剥離してしまうおそれもあった。
以上のような理由から、解析の際には透明であり、ハイブリダイゼーション時などには検体の拡散性が向上するゲル組成物として、ゲル組成物自体の収縮を伴わないものが望まれている。
【0008】
そこで本発明では、解析の際に透明性を有し、温度を上げることにより、ゲル組成物自体の収縮を抑制しつつ検体の拡散性を向上させることができるゲル組成物およびその製造方法を目的とする。また、該ゲル組成物を用いたマイクロアレイを提供する。
【課題を解決するための手段】
【0009】
本発明のゲル組成物は、アクリルアミド系モノマーと架橋剤との共重合により得られる網目構造体からなる基盤ゲルと、該基盤ゲルに一端が共有結合された感温性ポリマーとを含むことを特徴とする組成物である。
また、本発明のゲル組成物は、前記感温性ポリマーが、ポリ(N−エチル(メタ)アクリルアミド)、ポリ(N−n−プロピル(メタ)アクリルアミド)、ポリ(N−イソプロピル(メタ)アクリルアミド)、ポリ(N−シクロプロピル(メタ)アクリルアミド)、ポリ(N−メチル−N−エチルアクリルアミド)、ポリ(N,N−ジエチルアクリルアミド)、ポリ(N−メチル−N−イソプロピルアクリルアミド)、ポリ(N−メチル−N−n−プロピルアクリルアミド)、ポリ(N−アクリロイルピロリドン)、ポリ(N−アクリロイルピペリジン)からなる群から選択される1種のポリマーまたは2種以上のポリマーの混合物であることが好ましい。
また、前記感温性ポリマーの共重合率が、0.01〜4mol%であることが好ましい。
また、前記感温性ポリマーの相転移温度が20〜50℃であることが好ましい。
また、前記感温性ポリマーの前記基盤ゲルへの共有結合が、前記感温性ポリマーの末端に不飽和結合が導入された感温性マクロモノマーを用いることにより形成されていることが好ましい。
また、さらに、前記基盤ゲルに共有結合された生体関連物質を含むことが好ましい。
【0010】
また、本発明のマイクロアレイは、基板を有し、該基板上に形成された区画に、前記いずれかのゲル組成物が配置されている。
また、本発明のマイクロアレイは、前記区画が、溝または貫通孔により形成されていることが好ましい。
【0011】
また、本発明のゲル組成物の製造方法は、アクリルアミド系モノマーと感温性マクロモノマーとの共重合反応により前記いずれかのゲル組成物を製造する方法である。
【発明の効果】
【0012】
本発明のゲル組成物は、解析時には透明性を有しており、温度を上げることにより、ゲル組成物自体の収縮を抑制しつつ検体の拡散性を向上させることができる。
また、本発明の製造方法によれば、解析時には透明性を有しており、温度を上げることにより、ゲル組成物自体の収縮を抑制しつつ検体の拡散性を向上させることができるゲル組成物を得ることができる。
また、本発明のマイクロアレイは、解析時には透明性を有しており、温度を上げることにより検体の拡散性が向上する。また、その際のゲル自体の収縮が抑制されているため、ゲル組成物が基板の区画から剥離することがなく、安定して高効率な解析を行うことができる。
【発明を実施するための最良の形態】
【0013】
<ゲル組成物>
以下、本発明のゲル組成物の実施形態の一例について、図1および2に基づいて説明する。図1は、第1実施形態のゲル組成物1を示した概念図である。また、図2は、第2実施形態のゲル組成物2を示した概念図である。
【0014】
[第1実施形態]
ゲル組成物1は、図1に示すように、アクリルアミド系モノマーと架橋剤との共重合により得られる網目構造体からなる基盤ゲル10と、該基盤ゲル10に一端が共有結合された感温性ポリマー14とを含む組成物である。ゲル組成物1は、基盤ゲル10により形成された細孔12内に感温性ポリマー14が配置される。
【0015】
基盤ゲル10は、アクリルアミド系モノマーと架橋剤との共重合により形成される網目構造体であり、ゲル組成物1の基盤となるゲルである。
アクリルアミド系モノマーとしては、例えば、アクリルアミド、メタクリルアミド、N−メチルアクリルアミド、N,N−ジメチルアクリルアミド(DMAA)、N−イソプロピルアクリルアミド(NIPAM)が挙げられる。
これらのアクリルアミド系モノマーは、1種のみを単独で使用してもよく、2種以上を併用してもよいが、1種のみの使用または2種の併用が好ましい。2種のアクリルアミド系モノマーを併用する場合は、DMAAとNIPAMの併用がより好ましい。
【0016】
架橋剤は、エチレン性不飽和結合を2個以上有する多官能性モノマーである。
架橋剤としては、例えば、N,N’−メチレンビスアクリルアミド、N,N’−ジアリル(1,2−ヒドロキシエチレン)−ビスアクリルアミド、N,N’−シスタミン−ビスアクリルアミド、N−アクリロイルトリス(ヒドロキシメチル)アミノメタン、ポリエチレングリコールジメタクリレートなどが挙げられる。なかでも、N,N’−メチレンビスアクリルアミドが好ましい。
これらの架橋剤は、1種のみを単独で使用してもよく、2種以上を併用してもよい。
【0017】
架橋剤の使用量は、主剤となるモノマー(アクリルアミド系モノマーおよび後述する感温性モノマー)のmol量と架橋剤のmol量とのmol比が、架橋剤1に対して、主剤となるモノマーが4〜500の範囲であることが好ましい。
前記mol比が、架橋剤1に対して主剤となるモノマーが4以上であれば、基盤ゲル10の網目構造が不均一になることで解析時(室温)などの低温環境においてゲル組成物1が白濁することを抑制しやすい。また、架橋剤1に対して主剤となるモノマーが500以下であれば、充分な架橋度を有する網目構造体からなる基盤ゲル10が得られやすい。
【0018】
また、ゲル組成物1においては、基盤ゲル10を形成するアクリルアミド系モノマーとして、後述する感温性ポリマー14の形成に用いる誘導体と同一のモノマー成分(例えば、NIPAMなど。以下、「モノマー成分(M1)」という。)を用いることもできるが、アクリルアミド系モノマーとしてそのような成分のみを用いると、基盤ゲル10自体の相転移により生じる収縮および白濁の影響が大きくなると考えられる。そのため、本発明においては、アクリルアミド系モノマーとしてモノマー成分(M1)とそれ以外のモノマー成分とを用いた共重合により得られる基盤ゲル10であることが好ましい。これらの共重合比は、全アクリルアミド系モノマー100mol%に対してモノマー成分(M1)が50mol%以下であることが好ましい。
【0019】
感温性ポリマー14は、相転移温度(以下、「Tc」という。)、すなわちLCST(Lower Critical Solution Temperature)を有するポリマーである。LCSTは下限臨界溶液温度とも呼ばれ、LCSTを有するポリマーはその温度以上で相分離を引き起こし、不溶化して白濁するか沈殿する。感温性ポリマー14は、前記Tcを超える温度になると、疎水性に転移して収縮する性質を有している。
【0020】
感温性ポリマー14を形成する誘導体としては、例えば、N−エチル(メタ)アクリルアミド、N−n−プロピル(メタ)アクリルアミド、N−イソプロピル(メタ)アクリルアミド、N−シクロプロピル(メタ)アクリルアミド、N−メチル−N−エチルアクリルアミド、N,N−ジエチルアクリルアミド、N−メチル−N−イソプロピルアクリルアミド、N−メチル−N−n−プロピルアクリルアミド、N−アクリロイルピロリドン、N−アクリロイルピペリジンが挙げられる。これらの誘導体は1種のみを単独で使用してもよく、2種以上を使用してもよい。
【0021】
感温性ポリマー14は、ポリ(N−エチルアクリルアミド)、ポリ(N−エチルメタクリルアミド)、ポリ(N−n−プロピルアクリルアミド)、ポリ(N−n−プロピルメタクリルアミド)、ポリ(N−イソプロピルアクリルアミド)(以下、「NIPAMポリマー」という。)、ポリ(N−イソプロピルメタクリルアミド)、ポリ(N−シクロプロピルアクリルアミド)、ポリ(N−シクロプロピルメタクリルアミド)、ポリ(N−メチル−N−エチルアクリルアミド)、ポリ(N,N−ジエチルアクリルアミド)、ポリ(N−メチル−N−イソプロピルアクリルアミド)、ポリ(N−メチル−N−n−プロピルアクリルアミド)、ポリ(N−アクリロイルピロリドン)、ポリ(N−アクリロイルピペリジン)からなる群から選択される1種以上の感温性ポリマーであることが好ましい。
【0022】
本発明における感温性ポリマー14は、例えばマイクロアレイに用いる場合、ゲル組成物内で生体関連物質(キャプチャープローブ)と検体とを反応させる際に検体の拡散性がより向上する点から、それらを反応させる温度よりもTcが低いものを用いることが好ましい。例えば、DNAマイクロアレイの場合には、通常ハイブリダイゼーションが行なわれる40〜60℃程度よりもTcが低い感温性ポリマー14を用いることが好ましい。一方、マイクロアレイによる解析時(室温)における透明性の点からは、ある程度Tcが高い感温性ポリマー14であることが好ましい。
感温性ポリマー14は、ハイブリダイゼーションバッファー(2×SSC、0.2%SDS)中でのTcが20〜50℃のものがより好ましく、ポリ(N−イソプロピルアクリルアミド)、ポリ(N,N−ジエチルアクリルアミド)であることが特に好ましい。
【0023】
また、感温性ポリマー14の誘導体として、両イオン性のポリマー(ベタインポリマー)を用いることもできる。
両イオン性のポリマーは、分子内に第4アンモニウム塩基、オキソニウム塩基、スルホニウム塩基などを有するポリマーであり、N,N−ジメチル(アクリルアミドプロピル)アンモニウムプロパンサルフォネイト(以下、「DMAAPS」という。)を用いたポリマーであることが好ましい。
【0024】
LSCTを有する感温性ポリマーは、用いる溶液の塩濃度などによってLSCTが大きく変化する。特に、本発明のゲル組成物を核酸検出などのマイクロアレイなどに用いる場合、ハイブリダイゼーション時のバッファー組成によって感温性ポリマー14を選定することが重要となる。NIPAMポリマーなどは高塩濃度領域ではLCSTが下がり、室温においても白濁するためにDNAマイクロアレイなどには適用し難くなる。しかし、低塩濃度領域では良好な相転移挙動を示す。
【0025】
これに対し、DMAAPSを用いたポリマーは、両イオン性ポリマーであるため高い塩濃度領域の溶液中では分子が溶解する。そのため、用いるバッファー組成に応じた感温性ポリマー14とすることができる。例えば、2×SSC以下の塩濃度(0.2%SDS添加)であればNIPAMポリマー、2×SSCより高い塩濃度(0.2%SDS添加)であればDMAAPSを用いた感温性ポリマー14であることが好ましい。
ただし、特にポリマー部分にDMAAPSを用いる場合には、単独では塩溶液中で分子が溶解し、温度を上げても相転移しなくなる。そのため、この場合は、DMAAPSと、塩溶液中で溶解せずにLCSTを有する感温性ポリマーを形成する誘導体(好ましくはNIPAM)とを共重合した感温性ポリマー14とすることが好ましい。これにより、相転移温度を調整することが可能となる。
【0026】
感温性ポリマー14にDMAAPSを用いる場合、DMAAPSの割合は、感温性ポリマー14の共重合に用いる誘導体の合計(100mol%)に対して、5〜15mol%であることが好ましい。
DMAAPSの割合が5mol%以上であれば、高い塩濃度条件への適用が容易になる。また、DMAAPSの割合が15mol%以下であれば、感温性ポリマー14が充分な相転移を起こしやすい。
【0027】
感温性ポリマー14の質量平均分子量は、感温性ポリマー14の全長が細孔12の大きさ(架橋点間の距離)よりも小さくなるようにすることが好ましく、細孔12の大きさによっても異なるが、2000〜20000であることが好ましく、2000〜10000であることがより好ましい。
感温性ポリマー14の質量平均分子量が2000以上であれば、強度に優れたゲル組成物1が得られやすい。また、感温性ポリマー14の質量平均分子量が20000以下であれば、感温性ポリマー14が基盤ゲル10を巻き込まずに収縮するため、ゲル組成物1自体が収縮することを抑制しやすい。
【0028】
本発明のゲル組成物は、このような感温性ポリマー14が、その一端で基盤ゲル10に共有結合されている。
感温性ポリマー14の基盤ゲル10への共有結合は、例えば、前述した感温性ポリマーの末端に不飽和結合が導入された感温性マクロモノマーを用いることにより形成することができる。具体的には、例えば感温性ポリマーの末端にビニル基などを導入して感温性マクロモノマーを製造し、それをアクリルアミド系モノマーおよび架橋剤と共重合させることにより、基盤ゲル10に一端が共有結合された感温性ポリマー14が得られる。前記不飽和結合を有する官能基(不飽和官能基)はビニル基には限定されず、アクリレートやメタクリレート骨格のものでもよい。
【0029】
感温性ポリマーの末端に不飽和結合を導入する方法は、その末端に所望の不飽和結合を導入することができれば特に限定されない。以下に具体例として、NIPAMポリマー(感温性ポリマー)の末端にビニル基を導入してNIPAMマクロモノマー(感温性マクロモノマー)を得る方法を示す。NIPAMマクロモノマーの合成スキームは以下の通りである。ただし、該合成スキーム中のnは繰り返し単位数を示す。
【0030】
【化1】

【0031】
工程(I)は、Kanekoらの方法(Macromolecules,28,7712(1995))を利用した反応であり、連鎖移動剤として2−アミノエタンチオール(AESH)を用い、NIPAMを重合したNIPAMポリマーの末端にアミノ基を導入することによりポリマー(1)が得られる。
溶媒としては、N,N-ジメチルホルムアミド(DMF)、ジメチルスルホキシド(DMSO)などの極性溶剤を用いることができる。
反応温度は、60〜100℃であることが好ましい。
重合開始剤としては、2,2’−アゾビスイソブチロニトリル(AIBN)、2,2’−アゾビス(2−メチルブチロニトリル)、2,2’−アゾビス(2,4−ジメチルバレロニトリル)などを用いることができる。
【0032】
工程(II)は、Liらの方法(Small,2,917(2006))を用いた方法であり、工程(I)で得られたポリマー(1)と塩化アクリロイルとを反応させ、末端のアミノ基部分にビニル基を導入することによりNIPAMマクロモノマー(2)が得られる。
溶媒としては、N,N−ジメチルホルムアミド(DMF)、ジメチルスルホキシド(DMSO)などの極性溶剤を用いることができる。
反応温度は、30〜50℃であることが好ましい。
【0033】
ゲル組成物の製造における共重合時の全モノマー濃度(アクリルアミド系モノマーおよび感温性マクロモノマーの合計)は、100〜700mol/m3であることが好ましい。
全モノマー濃度が100mol/m3以上であれば、より高強度のゲル組成物が得られやすい。また、全モノマー濃度が700mol/m3以下であれば、検体の拡散性がより向上したゲル組成物1が得られる。
【0034】
感温性マクロモノマーの共重合率は、アクリルアミド系モノマーおよび感温性マクロモノマーの合計(100mol%)に対して、0.01〜4mol%であることが好ましくい。
感温性マクロモノマーの共重合率が0.01mol%以上であれば、強度に優れたゲル組成物1が得られやすい。また、感温性マクロモノマーの共重合率が4mol%以下であれば、充分にゲル化が進行したゲル組成物1が得られやすく、ゲル組成物1内での検体の拡散性を向上させやすい。
【0035】
尚、感温性マクロモノマーを製造する方法は前述の方法には限定されず、導入する不飽和結合に応じた方法を用いることができる。
また、感温性ポリマー14の一端を基盤ゲル10に共有結合する方法は感温性マクロモノマーを用いる方法には限定されず、例えば、予め基盤ゲルのポリマー鎖中に反応性官能基を導入しておき、該官能基と反応する官能基を導入した感温性ポリマーと反応させる方法を用いてもよい。ここで利用できる反応としては、例えば、アルデヒド基とアミノ基とでシッフ塩基を形成させる反応やエチレンオキサイドとアミノ基との開環反応を利用する反応、または同じくエポキシとカルボン酸との反応などが挙げられる。
【0036】
[第2実施形態]
ゲル組成物2は、ゲル組成物1にさらに生体関連物質が含まれている組成物であり、図2に示すように、アクリルアミド系モノマーと架橋剤の共重合により得られる網目構造体からなる基盤ゲル10と、該基盤ゲル10に一端が共有結合された感温性ポリマー14と、基盤ゲル10に共有結合された生体関連物質16を含む組成物である。ゲル組成物2では、基盤ゲル10により形成された細孔12内に、感温性ポリマー14と生体関連物質16が配置される。
基盤ゲル10を形成するアクリルアミド系モノマーおよび架橋剤、感温性ポリマー14についてはゲル組成物1と同じであるので説明を省略する。
【0037】
生体関連物質16は、検出または測定の対象となる物質(検体)を捕獲するキャプチャープローブである。
生体関連物質16としては、DNA、RNA(リボ核酸)、蛋白質、脂質などが挙げられる。これらの生体関連物質は、市販品であってもよく、生細胞などから得ることもできる。生細胞からのDNAの抽出は、Blinらの方法(Nucleic Acids Res.,3,2303(1976))などを用いることができる。また、生細胞からのRNAの抽出は、Favaloroらの方法(Methods.Enzymol.,65,718(1980))などを用いることができる。
【0038】
また、DNAとしては、鎖状若しくは環状のプラスミドDNAまたは染色体DNAを用いることができる。さらには、制限酵素若しくは化学的に切断したDNA断片、試験管内で酵素などにより合成されたDNAまたは化学合成したオリゴヌクレオチドなどを用いることもできる。
【0039】
生体関連物質16は、アクリルアミド系モノマーおよび架橋剤との共重合反応により、基盤ゲル10の網目構造に固定することができる。すなわち、生体関連物質16は、感温性ポリマー14と同様に、共重合反応可能な不飽和官能基を導入し、アクリルアミド系モノマーおよび架橋剤と共重合させることにより、基盤ゲル10に共有結合させることができる。
不飽和官能基としては、ビニル基の他、アクリレート基や、メタクリレート基が挙げられる。不飽和官能基は、生体関連物質16の機能を損なわない限り、そのいずれの部位に導入されていてもよい。例えば、生体関連物質16が核酸の場合、不飽和官能基は核酸の末端、鎖中のいずれに導入されていてもよい。ただし、生体関連物質16と検体とのハイブリダイゼーション効率がより向上する点から、核酸の末端に導入されていることが好ましい。
前記不飽和官能基は、国際公開第02/062817号パンフレットに記載の方法などにより導入することができる。
【0040】
生体関連物質16の共重合率は、目的、用途に応じて調整することができ、アクリルアミド系モノマー、感温性ポリマー14および生体関連物質16の合計(100mol%)に対して、10〜100000μmol%であることが好ましく、100〜10000μmol%であることがより好ましい。
生体関連物質16の共重合率が10μmol%以上であれば、ゲル組成物2をマイクロアレイなどに用いた場合の検出、測定の効率および精度を向上させやすい。また、生体関連物質16の共重合率が100000μmol%以下であれば、ゲル組成物2内での検体の拡散性を向上させやすい。
【0041】
本発明のゲル組成物は、前記アクリルアミド系モノマー、架橋剤、感温性ポリマー、生体関連物質以外の他の成分を含んでいてもよい。
他の成分としては、例えば、グリセリンなどが挙げられる。
【0042】
[製造方法]
以下、本発明のゲル組成物の製造方法として、前述のゲル組成物1およびゲル組成物2の製造方法の一例について説明する。
ゲル組成物1は、アクリルアミド系モノマー、架橋剤、および感温性マクロモノマーを共重合させることにより得ることができる。また、ゲル組成物2は、アクリルアミド系モノマー、架橋剤、感温性マクロモノマー、および生体関連物質を共重合させることにより得ることができる。
【0043】
前記共重合の方法としては、例えば、重合開始剤を用いる方法が挙げられる。
重合開始剤は、重合反応の間に感温性マクロモノマーや生体関連物質が分解しない方法であれば特に限定されず、2,2’−アゾビス[2−(2−イミダゾリン−2−イル)プロパン]ジハイドロクロライド、APS(過硫酸アンモニウム)、KPS(過硫酸カリウム)などが挙げられる。
また、重合開始剤としてAPS、KPSを用いる場合は、重合促進剤としてTEMED(テトラメチルエチレンジアミン)を用いることが好ましい。
【0044】
重合に用いる溶媒としては、水、エタノールなどを用いることができる。
また、重合温度は、用いる感温性マクロモノマーのTcよりも低い温度となる範囲内で、アゾ系の重合開始剤を用いる場合には45℃以上、APS、KPSを単独で用いる場合は50℃以上、APS、KPSにTEMEDを併用する場合は20〜40℃の範囲内とすることが好ましい。
【0045】
以上説明した本発明のゲル組成物は、Tcより低い温度では、図1(A)および図2(A)に示すように、基盤ゲル10の細孔12内で感温性ポリマー14が広がって存在している。そのため、細孔12の有効細孔径が感温性ポリマー14により縮小された状態となっており、該感温性ポリマー14が障害となって検体の拡散性に劣る。ただし、この状態ではゲル組成物は巨視的に透明であるため解析には適している。ここで、本発明における「透明」とは、光透過率がゲルの厚さ2mmで80%程度以上であることを意味する。
【0046】
一方、Tcよりも高い温度になると、図1(B)および図2(B)に示すように、基盤ゲル10に一端が共有結合された感温性ポリマー14が収縮することで、細孔12の有効細孔径が、感温性ポリマー14がない場合とほぼ同等の状態となる。これにより、ゲル組成物中での検体の拡散性が向上する。感温性ポリマー14は温度を下げることで図1(A)および図2(A)に示したような拡がった状態に戻り、ゲル組成物は巨視的に透明になる。
以上のように、生体関連物質を有するゲル組成物を用いて検出や測定を行う場合に、該生体関連物質と検体との反応効率を向上させることができる。
【0047】
また、本発明のゲル組成物では、このような機構により検体の拡散性を向上させるため、基盤ゲル10が感温性ポリマー14の収縮に巻き込まれて収縮し、ゲル組成物自体が収縮することが抑制される。したがって、基盤ゲル10の収縮により細孔12の有効細孔径が縮小することを抑制することができ、検体の拡散性が充分に向上する。
【0048】
以上のように、本発明のゲル組成物は、生体関連物質と検体との反応の際には温度をTcよりも高くすることにより感温性マクロモノマーを収縮させて拡散性を向上させ、検体の検出時にはTcよりも低い温度にすることでゲル組成物を均一に戻して透明に変化させ、蛍光検出の際の励起光をゲル全体に透過させることができる。そのため、検出感度が極めて高くなる。
【0049】
本発明のゲル組成物は、例えば、生体関連物質(キャプチャープローブ)を保持するゲル(ゲル組成物2)を遺伝子解析に使用することができる。例えば、前述のゲル組成物2を管状体の中空部に充填することによりゲル保持管状体を作製することで、特開平3−47097号公報に記載のごとく、遺伝子変異を解析するためのツールとして使用できる。前記中空部へのゲル組成物の保持は、キャピラリーゲル電気泳動に使用されるキャピラリーカラムを作製するのと同様の方法で実施することができる。
【0050】
<マイクロアレイ>
以下、本発明のマイクロアレイについて説明する。本発明のマイクロアレイは、基板を有し、該基板に形成された区画に前述のゲル組成物が配置されている。以下、その実施形態の一例について説明する。
【0051】
本実施形態のマイクロアレイ20は、図4に示すように、基板22に複数の管状体24が固定されており、管状体24が有する中空部が貫通孔26(区画)を形成している。また、貫通孔26にはゲル組成物2が保持されている。
【0052】
基板22は、複数本の管状体24が束ねられたものを固定化する接着剤により形成される。
接着剤は、マイクロアレイの製造に通常用いられる樹脂を用いることができ、例えば、ニッポラン4276、コロネート4403(登録商標。日本ポリウレタン工業(株)製)などのポリウレタン樹脂接着剤が挙げられる。
【0053】
基板22の形状は、通常、貫通孔(管状体)を規則的に配列させて、正方形または長方形とされるが、これらに限定されるものではない。「規則的に」とは、一定の大きさの枠の中に含まれる管状体の本数が一定となるよう順序よく配列させることをいう。
また、基板22の厚さは、50μm〜1mmであることが好ましい。
【0054】
管状体24は、中空部を有する管状の形態であれば、ガラス管、ステンレス管、中空繊維、パルプなどいずれの形態であってもよい。加工性、取り扱いの容易さを考慮すると中空繊維を使用することが好ましい。なお、中空繊維としては、特に限定されるものではないが、例えば合成繊維、半合成繊維、再生繊維、天然繊維などが挙げられる。また、管状体24は、多孔質管状体、非多孔質管状体のいずれでもよいが、ゲル組成物の重合前の前駆体溶液の中空繊維外への拡散や、ゲル組成物の乾燥を抑制する点から、非多孔質管状体であることが好ましい。
【0055】
管状体24の材質は特に限定はなく、シリカ、ガラスなどの無機材料や、以下に示す有機材料などが挙げられる。
有機材料としては、例えば、ナイロン6、ナイロン66、芳香族ポリアミドなどのポリアミド系材料、ポリエチレンテレフタレート、ポリブチレンテレフタレート、ポリ乳酸、ポリグリコール酸、ポリカーボネートなどのポリエステル系材料、ポリアクリロニトリルなどのアクリル系材料、ポリエチレンやポリプロピレンなどのポリオレフィン系材料、ポリメタクリル酸メチルなどのポリメタクリレート系材料、ポリビニルアルコール系材料、ポリ塩化ビニリデン系材料、ポリ塩化ビニル系材料、ポリウレタン系材料、フェノール系材料、ポリフッ化ビニリデンやポリテトラフルオロエチレンなどのフッ素系材料、ポリアルキレンパラオキシベンゾエート系材料などが挙げられる。また、カーボンブラックなどの黒色顔料が含有されていてもよい。
【0056】
貫通孔26(管状体24の中空部)は、整列固定化されていることが好ましい。
貫通孔26の内径(管状体24の内径)は、特に限定されないが、1mm以下であることが好ましく、10μm〜300μmであることがより好ましい。
【0057】
貫通孔26の数(区画数)は、管状体24の本数により決定される。本発明のマイクロアレイの区画数は、マイクロアレイにおける通常の区画数とすることができ、10〜10000個/cm2であることが好ましい。
【0058】
[製造方法]
本発明のマイクロアレイは、以下の(i)〜(iii)の工程により製造することができる。
工程(i):複数本の管状体をそれらの長手方向が一致するように集束して集束物を得る工程。
工程(ii):前記集束物の各々の管状体の中空部に、アクリルアミド系モノマー、架橋剤および感温性マクロモノマーを含む前駆体溶液(本発明のゲル組成物の重合前の溶液)を充填し、中空部内で所定の重合温度(例えば40℃以下の重合温度)で共重合反応する工程。
工程(iii): 集束物を、該集束物の長手方向と交叉する方向に切断する工程。
工程(ii)では、中空部に本発明のゲル組成物2(生体関連物質を含むゲル組成物)を含むものを充填することが好ましい。
【0059】
以下、マイクロアレイの製造方法の一実施形態例として、図1に例示した、貫通孔26を100個有する、基板22の形状が正方形のマイクロアレイ20を製造する方法について説明する。
工程(i)では、10本の管状体を、1列に束ねて固定化して1層のシートとした後、各々の管状体の長手方向が一致するように、前記シートが10層になるように重ねて固定化することにより集束物を得る。工程(i)における管状体の固定化方法は、例えば、ポリウレタン樹脂接着剤などの接着剤により行う方法が挙げられる。
【0060】
ついで、工程(ii)において、集束物の各々の管状体の中空部に本発明のゲル組成物の前駆体溶液を充填する。前駆体溶液の充填方法は特に限定されず、例えば、集束物の一方の端部を前駆体溶液中に浸した状態で、もう一方の端部側から吸引する方法であってもよく、集束物の一方の端部側から前駆体溶液を押し込む方法であってもよい。
また、管状体の一方を封止し、減圧した後、開放端を前駆体溶液に浸し、その状態で常圧に戻すことにより吸引する方法であってもよい。
【0061】
工程(ii)における前駆体溶液の共重合の重合温度は、用いる感温性マクロモノマーのTc以下で行うことが好ましい。好ましい温度範囲は40℃以下である。重合温度が40℃より高い温度で行うと、重合中に感温性マクロモノマーが相転移し、白濁したゲル組成物になりやすくなる。このようなゲル組成物は、温度を低くしても透明にならないため、解析には不適切である。前述のような温度で重合を行うための開始剤としては、APSにTEMEDを添加したものや光分解型の開始剤などを用いることができる。
【0062】
工程(iii)では、得られた集束物を、該集束物の長手方向と交叉する方向に切断して薄片化する。これにより、100個の貫通孔26が形成された、所望の厚さの基板22を有するマイクロアレイ20が得られる。切断方法は、集束物を所望の厚さで切断できる方法であれば特に限定されず、例えば、ミクロトームにより切断する方法などが挙げられる。
【0063】
また、以上説明した工程(i)〜(iii)によりマイクロアレイ20を得ることができるが、工程(i)と工程(ii)の順序は特に限定されず、工程(ii)を行った後に工程(i)を行ってもよい。すなわち、各々の管状体の中空部に前駆体溶液を充填して重合反応した(工程(ii))後に、それらの管状体を集束して集束物を形成(工程(i))し、該集束物を薄片化してマイクロアレイを得る方法であってもよい(国際公開第00/5376号パンフレット参照)。
【0064】
以上説明した本発明のマイクロアレイは、本発明のゲル組成物を用いていることから、通常室温で行なわれる解析時には透明性を有しており、ハイブリダイゼーションなどの温度を上昇させた際には検体の拡散性を向上させることができるため、高効率かつ高精度な解析が可能となる。
尚、本発明のマイクロアレイは、図4に例示したマイクロアレイには限定されない。例えば、本発明のマイクロアレイの区画は、マイクロアレイ20のような貫通孔には限定されず、溝による区画であってもよい。ただし、前述の工程(i)〜(iii)による大量生産に適している点から、管状体を用いた貫通孔により区画を形成するマイクロアレイであることが好ましい。
【0065】
また、ゲル組成物2の代わりにゲル組成物1を配置したマイクロアレイであってもよい。
また、平面基板上に重合前または重合開始直後のキャプチャープローブを含む前駆体溶液を、予め定めた区画にスポッティングしたマイクロアレイであってもよい(特表平6−507486号公報、米国特許第5770721号明細書参照)。
【実施例】
【0066】
以下、実施例および比較例を示して本発明を詳細に説明する。ただし、本発明は以下の記載によっては限定されない。
<感温性マクロモノマー>
[製造例1]
前述の合成スキームを用いて感温性マクロモノマーであるNIPAMマクロモノマーを合成した。
工程(I)では、連鎖移動剤であるAESH(0.43446g)、NIPAM(11.5900g)、および溶媒であるDMFを、75℃のオイルバスに設置したコンデンサー付きのパラブルフラスコに仕込み、高純度窒素ガスを2時間パージした。次いで、予めDMFに溶解して室温にて高純度窒素ガスでパージしておいた重合開始剤のAIBN(0.1774g)を加え、高純度窒素ガス雰囲気下で15時間反応させた。反応に用いたDMFは45mLであった。
反応終了後、真空乾燥機を用いてDMFを除去し、感温性マクロモノマーの前駆体である末端にアミノ基を有するポリマー(1)を得た。次いで、ポリマー(1)を精製するために、得られた反応物をアセトンに再溶解させ、ジエチルエーテルに滴下し、ポリマー(1)を沈殿させた。その後、濾過を行い、再度ジエチルエーテルで精製した後、乾燥を行った。
【0067】
工程(II)では、得られたポリマー(1)(3.0g)、塩化アクリロイル(20mL)、およびDMF(5mL)をサンプル瓶に投入し、高純度窒素ガスをパージしながら室温で30分間攪拌した。これを温度40℃の恒温槽に移し、さらに2時間、高純度窒素ガス雰囲気下で攪拌し、反応を行った。反応終了後、得られた反応液をジエチルエーテルに滴下し、反応生成物のNIPAMマクロモノマーを沈殿させ、濾過した。更に、同様の操作を2回行って精製し、濾過回収したNIPAMマクロモノマーを真空乾燥した。
【0068】
[NMR分析]
製造例1で得られたNIPAMマクロモノマーを1H−NMRにより分析した結果を図5に示す。1H−NMRの測定溶媒には重水(D2O)を使用した。
図5(A)、(B)に示すように、NMRスペクトルの5.6〜6.5ppmの範囲に、ビニル基に特有のピーク(g)、(h)、(i)が見られ、末端にビニル基を有する目的のNIPAMマクロモノマーが得られていることが確認された。
【0069】
また、NMRスペクトルにおけるピーク積分比から、得られたNIPAMマクロモノマーの分子量を推算した。図6に示すように、末端のビニル基のピーク(H分1つのピーク)とNIPAMポリマー部分のイソプロピル基のピーク(H分6つのピーク)との積分比(1:125.7383)より、NIPAMポリマー部分の繰り返し単位数はn=21と推定した。これにより、NIPAMマクロモノマーの質量平均分子量は2500g/mol程度であると推定した。
【0070】
[相転移温度の測定]
また、製造例1で得られたNIPAMマクロモノマーの相転移温度(Tc)を、溶液の透過度(波長600nm)の温度依存性を測定することにより評価した。透過度の測定には、ペルチェ素子温度制御機能付き分光光度計(日本分光V530型)を用いた。水中、およびハイブリダイゼーションバッファー(2×SSC、0.2%SDS)中に、NIPAMマクロモノマーを5g/Lの割合で溶解し、透過度の温度依存性を求めた。その結果を図7に示す。
【0071】
図7に示すように、水中では、約34℃で著しい透過度の減少が起こっており、この温度がTcであるとみなすことができる。この製造例1で得られたNIPAMマクロモノマーのTcは、高分子量のNIPAMポリマー(ビニル基を導入していないもの)と同等の値であった。
また、ハイブリダイゼーションバッファー中では、Tcは水中の場合と比べて高温側に数℃シフトしていた。これは、塩であるSSCのTcを低下させる作用に比べ、界面活性剤であるSDSのTcを上昇させる作用がより大きいためであると考えられる。
【0072】
<ゲル組成物>
[実施例1]
アクリルアミド系モノマーであるN,N−ジメチルアクリルアミド(DMAA)、架橋剤であるN,N’−メチレンビスアクリルアミド(MBAA)、前記NIPAMマクロモノマーを、溶媒である水に溶解し、重合開始剤であるAPS、重合促進剤であるTEMEDを用いて、NIPAMマクロモノマーのTcより低い20℃で重合反応を行い、基盤ゲルと該基盤ゲルに一端が共有結合されたNIPAMポリマーとを有するゲル組成物を得た。尚、架橋剤の濃度は4mol/m3、TEMEDおよびAPSの濃度はそれぞれ10mol/m3および0.5mol/m3とした。また、全モノマー(DMAAとNIPAMマクロモノマーの合計)濃度を400mol/m3、NIPAMマクロモノマーの共重合率を5mol%とした。
全モノマー濃度を400mol/m3、架橋剤濃度を4mol/m3とした場合、架橋点間距離はDMAA単位100個程度(分子量10000程度)となると考えられ、NIPAMマクロモノマーよりも大きくなる。
【0073】
[実施例2〜13]
前記全モノマー濃度およびNIPAMマクロモノマーの共重合率を表1に示す通りに変更した以外は、実施例1と同様にしてゲル組成物を得た。
実施例1〜13で得られたゲル組成物のゲル化の状態を評価した結果を表1に示す。ゲル化の評価は、以下の基準に基づいて行なった。
◎:充分にゲル化した。
○:ゲル化が見られたが柔らかかった。
【0074】
【表1】

【0075】
表1に示すように、全モノマー濃度が400mol/m3の場合には、NIPAMマクロモノマーの共重合率が5mol%(実施例1)では得られたゲル組成物が柔らかかったが、3.5mol%以下(実施例2〜6)ではより強度に優れたゲル組成物が得られた。また、全モノマー濃度が300mol/m3の場合では、NIPAMマクロモノマーの共重合率が3.5mol%(実施例7)では得られたゲル組成物が柔らかかったが、3mol%以下(実施例8および9)ではより強度に優れたゲル組成物が得られた。
また、全モノマー濃度が267mol/m3の場合は、NIPAMマクロモノマーの共重合率が3mol%(実施例10)であっても1mol%(実施例11)であっても共に強度に優れたゲル組成物が得られ、全モノマー濃度が200mol/m3の場合(実施例12および13)に比べて強度に優れたゲル組成物が得られやすいことが分かった。
【0076】
[実施例14〜17]
全モノマー濃度を400mol/m3、NIPAMマクロモノマーの共重合率を0.5、1、2、3mol%とし、厚さ3mmのスペーサーを2枚のガラス板で挟んで形成した空間内で、APSおよびTEMEDを用いて20℃で重合反応を行い、厚さ3mmの板状ゲルを作製した。架橋剤の濃度は4mol/m3、TEMEDおよびAPSの濃度はそれぞれ10mol/m3および0.5mol/m3とした。それ以外は、実施例1〜13と同様に行った。
【0077】
[白濁化の評価]
光路長10mmの石英セルを用い、前記板状ゲルを該石英セルに入るように切断して挿入し、板状ゲルが光路に対して垂直になるようにペルチェ素子温度制御機能付き分光光度計(日本分光V530)に設置し、水中における透過度を測定した。測定結果を図8(A)に示す。
また、同様の方法でハイブリダイゼーションバッファー(2×SSC、0.2%SDS)中における透過度を測定した。測定結果を図8(B)に示す。
【0078】
図8(A)に示すように、水中の場合は、NIPAMマクロモノマーのTcである34℃を超えるとゲル(板状ゲル)が白濁した。また、この白濁の程度は、NIPAMマクロモノマーの共重合率が高くなるにつれて大きくなった。ただし、共重合率が3mol%になると白濁の程度が小さくなった。これは、共重合時のNIPAMマクロモノマーの割合が多くなることで、ゲル化の程度が低下するためであると考えられる。
また、ハイブリダイゼーションバッファー中では、図8(B)に示すように、NIPAMマクロモノマーの共重合率が2mol%の場合に70℃で若干の白濁化が見られたが、それ以外の共重合率の場合には白濁化が見られなかった。
【0079】
[実施例18]
NIPAMマクロモノマーの共重合率を1mol%とし、内径3.4mmのガラス管内で合成する以外は、実施例14〜17と同様にして円柱状ゲルを作製した。
【0080】
[参考例1]
NIPAMマクロモノマーを用いなかった以外は実施例18と同様の方法で円柱状ゲルを作製した。
【0081】
[膨潤度の温度依存性]
実施例18および参考例1で得られた円柱状ゲルについて、円柱状ゲルの膨潤径を、水中およびハイブリダイゼーションバッファー(2×SSC、0.2%SDS)中で各温度にて読み取り顕微鏡を用いて測定し、その温度依存性を評価した。水中での結果を図9(A)、ハイブリダイゼーションバッファー中での結果を図9(B)に示す。図9(A)、(B)における破線は、ゲルの合成に用いたガラス管の内径(3.4mm)を示している。
【0082】
実施例18の円柱状ゲルの膨潤径は、図9(A)に示すように、水中において基盤ゲル(DMAA)のみの参考例1と比較して多少収縮が見られたが、その温度依存性は小さかった。また、ハイブリダイゼーションバッファー中では、図9(B)に示すように、参考例1とほぼ同等の膨潤径であり、温度依存性が非常に小さかった。
水中に比べてハイブリダイゼーションバッファー中における温度依存性が小さいのは、界面活性剤であるSDSによりNIPAMポリマーの収縮がある程度低減されるためであると考えられる。
【0083】
次に、基盤ゲルに一端が共重合されたNIPAMポリマー(感温性ポリマー)の収縮による検体の拡散性の向上について評価するため、モデル物質として濃度測定が容易なローダミンBを用い、該ローダミンBの拡散係数の温度依存性を測定した。以下、拡散係数の温度依存性の測定について説明する。
【0084】
[実施例19]
全モノマー濃度を400mol/m3、NIPAMマクロモノマーの共重合率を1mol%として、図10に示すガラス製ゲルホルダー30内で重合反応を行なってゲル組成物からなるゲル膜1Aを得た。架橋剤の濃度は4mol/m3、TEMEDおよびAPSの濃度はそれぞれ10mol/m3および0.5mol/m3とした。
ガラス製ゲルホルダー30は、上部にゲル組成物の前駆体溶液を投入する開口を有するガラス板32が2枚のガラス板34で挟まれ、さらに金網38を有するガラス板36で挟まれた形態を有しており、ガラス板32、34および金網38で囲まれる空間内でゲル膜を製造することができる。そして、ゲル膜1Aを通過できる溶液などが、一方の側から金網38、ゲル膜、金網38を順に通って他方の側へと通過できるようになっている。
ガラス板32の上部に形成された開口は、接着剤40により封止した。
【0085】
次いで、2つのガラスセル52(容量500mL)を有し、各々のガラスセル52にそれぞれ300mLの水が入れられ、さらにそれらガラスセル52A、52Bが共に恒温槽54に入れられている拡散係数測定装置50(図11)の2つのガラスセル52A、52Bの間に、ゲル膜1Aを有するガラス製ゲルホルダー30を設置した。その後、ゲル膜1Aおよびガラスセル52A、52B内の水の温度を所定温度まで上げ、ガラスセル52Aの水中に前記所定温度のローダミンB水溶液(ローダミンB濃度:0.2g/L)100mLを注入し、ガラスセル52Bに水100mLを注入した。その後、ガラスセル52B側に拡散してきたローダミンBの濃度を経時的に測定し、拡散係数の温度依存性を評価した。ガラスセル52BにおけるローダミンBの濃度の測定は、分光光度計(日本分光V530型)を用いて波長533nmにて行なった。
【0086】
[比較例1]
NIPAMマクロモノマーを用いていないDMAAのみのゲル膜1Bを形成した以外は、実施例19と同様にしてガラスセル52BにおけるローダミンBの濃度を測定し、拡散係数の温度依存性を評価した。
【0087】
[拡散係数の測定および評価]
拡散係数は、以下に示す手順で算出することができる。
まず、時間tまでにゲル膜を透過したローダミンBの単位面積あたりの量Qは、下記式で表される。
【数1】

ここで、式中のC(t)、V、Xは以下の意味を示す。
C(t):時間tにおけるガラスセル52B側のローダミンBの濃度
V:ガラスセル52B内の溶液の容積
X:ゲル膜の面積
【0088】
上記式において、C(t)はガラスセル52A側のローダミンBの初期濃度C0に比べて非常に小さく、ローダミンBのゲル膜の透過速度が一定であると仮定し、拡散に関するFickの式を適用すると、次式が導かれる。
【数2】

ここで、式中、Dおよびdは以下の意味を示す。
D:ゲル膜中の拡散係数
d:ゲル膜の厚さ
これにより、拡散係数Dは次式のように表されるので、ガラスセル52B側のローダミンBの濃度の経時変化を測定することにより拡散係数を算出することができる。
【数3】

【0089】
測定については、ハイブリダイゼーションバッファー中では、バッファーとローダミンBとの間に相互作用が見られたため、水中での測定のみとした。
実施例19および比較例1における拡散係数の温度依存性の測定結果を図12に示す。また、実施例19における拡散係数のアレニウス(Arrhenius)プロットを図13に示す。
【0090】
図12に示すように、NIPAMマクロモノマーを共重合したNIPAMポリマーを有するゲル膜である実施例19では、温度上昇と共に拡散係数が大きく増加し、25℃の場合に比べて70℃では拡散係数が約4倍になっていた。また、水中でのNIPAMマクロモノマー(NIPAMポリマー)のTcである34℃の前後で拡散係数の増加傾向が異なっていた。一方、NIPAMマクロモノマーを用いていないDMAAのみの比較例1では、拡散係数が温度上昇と共に増加しているものの、低温領域において拡散係数が実施例19よりも大きかった。
このように、実施例19と比較例1は、低温領域では拡散係数に差が見られたが、温度上昇に伴ってその差が減少し、高温領域ではそれらの拡散係数がほぼ同等となった。
【0091】
この結果は、以下のように考えられる。実施例19のゲル膜1Aと比較例1のゲル膜1Bは、全モノマー量が共に400mol/m3であるため、より分子量が大きい長鎖のNIPAMポリマーを有する実施例19のゲル膜1Aの方が高密度である。そのため、Tcよりも低い温度では、NIPAMポリマーが拡がった構造で存在していることで、ゲル膜1Aの有効細孔径が小さくなっており、ローダミンBの拡散がゲル膜1Bに比べてより抑制されている。一方、Tcよりも高い温度では、NIPAMポリマーが収縮することによりゲル膜1Aの有効細孔径がゲル膜1Bの有効細孔径とほぼ同等となるために、拡散係数の温度依存性に対するNIPAMポリマーの影響が非常に小さくなり、拡散係数がほぼ同等になると考えられる。
【0092】
また、実施例19のゲル膜1Aでは、図13に示すように、Tc付近でアレニウスプロットの勾配(−Ea/RT、Ea:活性化エネルギー、R:気体定数)が大きく変化しており、Tcより低い温度に比べて高い温度で活性化エネルギーが小さくなっていた。この結果も、Tcを超えるとNIPAMポリマーの収縮が起こることで、ローダミンBの拡散性が向上することを示していると考えられる。
【産業上の利用可能性】
【0093】
本発明のゲル組成物は、解析の際には透明性を有し、温度を上昇させることで検体の拡散性を向上させることができる。そのため、高効率で高精度な検出または測定が行えるマイクロアレイなどとして好適に使用できる。
【図面の簡単な説明】
【0094】
【図1】本発明のゲル組成物の一実施形態例を示した概念図である。
【図2】本発明のゲル組成物の他の実施形態例を示した概念図である。
【図3】従来のゲル組成物の実施形態の一例を示した概念図である。
【図4】本発明のマイクロアレイの一実施形態例を示した斜視図である。
【図5】本実施例におけるNIPAMマクロモノマーのNMRスペクトルを示した図である。
【図6】本実施例におけるNIPAMマクロモノマーのNMRスペクトルを示した図である。
【図7】本実施例におけるNIPAMマクロモノマーの透過度の測定結果を示した図である。
【図8】実施例14〜17のNIPAMマクロモノマーの透過度の測定結果を示した図である。(A)水中、(B)ハイブリダイゼーションバッファー中。
【図9】実施例18および参考例1の膨潤径の測定結果を示した図である。(A)水中、(B)ハイブリダイゼーションバッファー中。
【図10】本実施例で用いたガラス製ゲルホルダーを示した図である。(A)ガラス製ゲルホルダーの中央部のガラス板積層部分の正面図、(B)縦分解断面図。
【図11】本実施例で用いた拡散係数測定装置を示した模式図である。
【図12】実施例19および比較例1の拡散係数の温度依存性を示した図である。
【図13】実施例19の拡散係数のアレニウスプロットを示した図である。
【符号の説明】
【0095】
1 ゲル組成物 2 ゲル組成物 10 基盤ゲル 12 細孔 14 感温性ポリマー 16 生体関連物質 20 マイクロアレイ 22 基板 24 管状体 26 貫通孔
【特許請求の範囲】
【請求項1】
アクリルアミド系モノマーと架橋剤との共重合により得られる網目構造体からなる基盤ゲルと、該基盤ゲルに一端が共有結合された感温性ポリマーとを含むことを特徴とするゲル組成物。
【請求項2】
前記感温性ポリマーが、ポリ(N−エチル(メタ)アクリルアミド)、ポリ(N−n−プロピル(メタ)アクリルアミド)、ポリ(N−イソプロピル(メタ)アクリルアミド)、ポリ(N−シクロプロピル(メタ)アクリルアミド)、ポリ(N−メチル−N−エチルアクリルアミド)、ポリ(N,N−ジエチルアクリルアミド)、ポリ(N−メチル−N−イソプロピルアクリルアミド)、ポリ(N−メチル−N−n−プロピルアクリルアミド)、ポリ(N−アクリロイルピロリドン)、ポリ(N−アクリロイルピペリジン)からなる群から選択される1種のポリマーまたは2種以上のポリマーの混合物である、請求項1に記載のゲル組成物。
【請求項3】
前記感温性ポリマーの共重合率が、0.01〜4mol%である、請求項1または2に記載のゲル組成物。
【請求項4】
前記感温性ポリマーの相転移温度が20〜50℃である、請求項1〜3のいずれかに記載のゲル組成物。
【請求項5】
前記感温性ポリマーの前記基盤ゲルへの共有結合が、前記感温性ポリマーの末端に不飽和結合が導入された感温性マクロモノマーを用いることにより形成されている、請求項1〜4のいずれかに記載のゲル組成物。
【請求項6】
さらに、前記基盤ゲルに共有結合された生体関連物質を含む、請求項1〜5に記載のゲル組成物。
【請求項7】
基板を有し、該基板上に形成された区画に、請求項1〜6のいずれかに記載のゲル組成物が配置されているマイクロアレイ。
【請求項8】
前記区画が、溝または貫通孔により形成されている、請求項4に記載のマイクロアレイ。
【請求項9】
アクリルアミド系モノマーと感温性マクロモノマーとの共重合反応により請求項1〜6のいずれかに記載のゲル組成物を製造する、ゲル組成物の製造方法。
【請求項1】
アクリルアミド系モノマーと架橋剤との共重合により得られる網目構造体からなる基盤ゲルと、該基盤ゲルに一端が共有結合された感温性ポリマーとを含むことを特徴とするゲル組成物。
【請求項2】
前記感温性ポリマーが、ポリ(N−エチル(メタ)アクリルアミド)、ポリ(N−n−プロピル(メタ)アクリルアミド)、ポリ(N−イソプロピル(メタ)アクリルアミド)、ポリ(N−シクロプロピル(メタ)アクリルアミド)、ポリ(N−メチル−N−エチルアクリルアミド)、ポリ(N,N−ジエチルアクリルアミド)、ポリ(N−メチル−N−イソプロピルアクリルアミド)、ポリ(N−メチル−N−n−プロピルアクリルアミド)、ポリ(N−アクリロイルピロリドン)、ポリ(N−アクリロイルピペリジン)からなる群から選択される1種のポリマーまたは2種以上のポリマーの混合物である、請求項1に記載のゲル組成物。
【請求項3】
前記感温性ポリマーの共重合率が、0.01〜4mol%である、請求項1または2に記載のゲル組成物。
【請求項4】
前記感温性ポリマーの相転移温度が20〜50℃である、請求項1〜3のいずれかに記載のゲル組成物。
【請求項5】
前記感温性ポリマーの前記基盤ゲルへの共有結合が、前記感温性ポリマーの末端に不飽和結合が導入された感温性マクロモノマーを用いることにより形成されている、請求項1〜4のいずれかに記載のゲル組成物。
【請求項6】
さらに、前記基盤ゲルに共有結合された生体関連物質を含む、請求項1〜5に記載のゲル組成物。
【請求項7】
基板を有し、該基板上に形成された区画に、請求項1〜6のいずれかに記載のゲル組成物が配置されているマイクロアレイ。
【請求項8】
前記区画が、溝または貫通孔により形成されている、請求項4に記載のマイクロアレイ。
【請求項9】
アクリルアミド系モノマーと感温性マクロモノマーとの共重合反応により請求項1〜6のいずれかに記載のゲル組成物を製造する、ゲル組成物の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【公開番号】特開2010−77189(P2010−77189A)
【公開日】平成22年4月8日(2010.4.8)
【国際特許分類】
【出願番号】特願2008−244124(P2008−244124)
【出願日】平成20年9月24日(2008.9.24)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成20年8月24日 社団法人化学工学会発行の「化学工学会 第40回秋季大会 研究発表講演要旨集」に発表
【出願人】(000006035)三菱レイヨン株式会社 (2,875)
【出願人】(504136568)国立大学法人広島大学 (924)
【Fターム(参考)】
【公開日】平成22年4月8日(2010.4.8)
【国際特許分類】
【出願日】平成20年9月24日(2008.9.24)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成20年8月24日 社団法人化学工学会発行の「化学工学会 第40回秋季大会 研究発表講演要旨集」に発表
【出願人】(000006035)三菱レイヨン株式会社 (2,875)
【出願人】(504136568)国立大学法人広島大学 (924)
【Fターム(参考)】
[ Back to top ]

