コーヒー抽出物
本発明は、抗酸化及び抗炎症性特性を有するコーヒー抽出物を生成する方法、並びに本発明の抽出物の使用に関する。コーヒー抽出物は、コーヒー酸及び/又はフェルラ酸を含み、例えば微生物又は酵素で、コーヒー抽出物中に存在するクロロゲン酸を加水分解することによって生成できる。本発明のコーヒー抽出物は、例えば、食物又は飲料製品の成分として使用されてもよい。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、抗酸化及び抗炎症性特性を有する改良されたコーヒー抽出物を生成する方法、抽出物を生成する方法、並びに本発明の抽出物の使用に関する。
【背景技術】
【0002】
コーヒー並びにカフェイン及びジテルペン(例えば、カフェストール、カーウェオール)などのコーヒー活性化合物は、げっ歯動物において解毒酵素(例えば、グルタチオン−S−トランスフェラーゼGST)を誘導することが示された(Cavin C.ら、1998年、「コーヒーに特有のジテルペンであるカフェストール及びカーウェオールは、二重機構によってアフラトキシンB1に誘導される遺伝毒性を防ぐ(The coffee−specific diterpenes cafestol and kahweol protect against aflatoxin B1−induced genotoxicity trough a dual mechanism.)。」、Carcinogenesis、19巻、1369〜1375頁、Cavin,C.ら、2003年、「コーヒーのジテルペンは、ラット及びヒトの培養系において、ベンゾ[a]ピレンの遺伝毒性を妨げる(Coffee diterpenes prevent benzo[a]pyrene genotoxicity in rat and human culture systems.)。」、Biochemical Biophysical Research Communication、306巻、488〜495頁、Huber,W.ら、2002年a、「コーヒー成分であるカーウェオール及びカフェストールによる、ラットの特定の器官における化学的予防酵素であるグルクロニルトランスフェラーゼ及びグルタチオントランスフェラーゼの強化(Enhancement of the chemoprotective enzymes glucuronyl transferase and glutathione transferase in specific organs of the rat by the coffee components kahweol and cafestol.)。」、Archive of Toxicology、76巻、209〜217頁)。コーヒーにより増進したGST活性は、5日間でコーヒー800mlを摂取した後のヒトにおいて、さらに実証された(Steinkellner,H.ら、2005年、「コーヒー摂取は、血漿においてGSTPを誘導し、(+/−)−抗−ベンゾ[a]ピレン−7,8−ジヒドロジオール−9,10−エポキシドによって誘導されるDNA損傷からリンパ球を保護する:対照ヒト介入試験の結果(Coffee consumption induces GSTP in plasma and protects lymphocytes against (+/−)−anti−benzo[a]pyrene−7,8−dihydrodiol−9,10−epoxide induced DNA−damage:results of controlled human intervention trials.)。」、Mut.Res.591巻、264〜275頁)。さらに、Richelleら、J.Agric.Food Chem.、49巻、3438〜42頁、(2001年)は、生体外でのLDL酸化の遅延時間が、標準的な1杯分のコーヒーによって、実質的に増加することを示した。増進した全抗酸化能力は、コーヒー200mlを摂取した後、生体内でのヒト血漿においてもまた観察された(Natellaら、J.Agric.Food Chem.、50巻、6211〜16頁、2002年)。
【0003】
この種の抗酸化活性は、例えば癌、心臓病、退行性脳障害、及び老化に関与することがある損傷を与える遊離基を減少させることによって、「酸化ストレス」を防ぐことが知られている。
【0004】
食物及び飲料製品の健康上の利益を増進させるために、増進した抗酸化活性やその他の有益な生物活性を有する製品を製造すること、並びに、例えば化粧及び医薬品ばかりでなく、食物及び飲料製品の特性を強化するために使用できる、抗酸化剤及び有益な生物活性を有するその他の化合物の天然源を発見することが望まれている。抗酸化特性は、分子自体の性質に本来備わっている可能性があるか、又は酸化ストレスに対する自然防御の誘導によって仲介され得る。
【発明の概要】
【0005】
本発明者らは今、コーヒー酸の量が、乾燥物質1グラム当たり、少なくとも1ミリグラムであり、及び/又はフェルラ酸の量が、乾燥物質1グラム当たり、少なくとも0.5ミリグラムであるコーヒー抽出物を生成する方法、並びに、かかるコーヒー抽出物が、従来のコーヒー抽出物と比べて、抗酸化及び抗炎症性特性を向上させたことを見出した。したがって、本発明は、以下のステップ、a)水でコーヒー豆を抽出して、コーヒー抽出物を生成するステップ、及びb)クロロゲン酸を加水分解して、フェノール酸を生成するために、コーヒー抽出物を処理するステップを含む、コーヒー抽出物を生成する方法に関する。さらなる実施形態において、本発明は、本発明のコーヒー抽出物の使用、食物又は飲料製品を製造する方法、及び結果として生じる食物又は飲料製品に関する。
【図面の簡単な説明】
【0006】
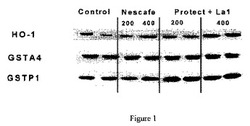
【図1】クロロゲン酸を加水分解する処理をしていないネスカフェレッドカップ(NESCAFE RED CUP)(登録商標)(焙煎したコーヒー豆の抽出物)200及び400ug/ml、及びラクトバチルス・ジョンソニイ(Lactobacillus johnsonii)で処理したネスカフェプロテクト(NESCAFE PROTECT)(登録商標)200及び400ug/mlで処理したラットの初代培養肝細胞、並びにコーヒー抽出物で処理していない対照試料におけるGSTのサブユニット(GSTA4、GSTP1)及びヘム−オキシゲナーゼ−1(HO−1)のタンパク質発現を示すウェスタンブロットゲルの図である。詳細については、実施例1を参照されたい。
【図2】クロロゲン酸を加水分解する処理をしていないネスカフェレッドカップ(登録商標)(焙煎したコーヒー豆の抽出物)(RN)、クロロゲン酸を加水分解する処理をしていないネスカフェプロテクト(登録商標)(生及び焙煎したコーヒー豆の共抽出物)(P)、及びラクトバチルス・ジョンソニイで処理したネスカフェプロテクト(登録商標)(La1−P)を5%含む食餌を2週間与えた雄性のラットの肝臓中での解毒酵素発現の誘導(GSTP1、NQO1)を示すウェスタンブロットの図である。詳細については、実施例1を参照されたい。
【発明を実施するための形態】
【0007】
本発明は、改良された抗酸化及び抗炎症性特性を有するコーヒー抽出物に関する。
【0008】
本発明の一実施形態において、コーヒー抽出物は、コーヒー酸を、乾燥物質1グラム当たり、少なくとも2、少なくとも5、少なくとも10、又は少なくとも25ミリグラムなど、乾燥物質1グラム当たり、少なくとも1ミリグラム含む。別の実施形態において、コーヒー抽出物は、フェルラ酸を、乾燥物質1グラム当たり、少なくとも1、少なくとも2、少なくとも5、又は少なくとも10ミリグラムなど、乾燥物質1グラム当たり、少なくとも0.5ミリグラム含む。さらなる実施形態において、コーヒー酸の量に対するカフェオイルキナ酸及びジエステルの量の割合は、50未満、10未満、又は1未満など、100未満(重量/重量)である。またさらなる実施形態において、フェルラ酸の量に対するフェルロイルキナ酸及びジエステルの量の割合は、10未満、5未満、又は1未満など、30未満(重量/重量)である。
【0009】
本発明のコーヒー抽出物は、生コーヒー豆及び/又は焙煎したコーヒー豆の抽出物であってもよい。コーヒー抽出物を生成する多数の方法は、当技術分野において知られている。
【0010】
本発明は、以下のステップ、a)水でコーヒー豆を抽出して、コーヒー抽出物を生成するステップ、及びb)クロロゲン酸をフェノール酸に加水分解するために、コーヒー抽出物を処理するステップを含む、コーヒー抽出物を生成する方法に、さらに関する。
【0011】
抽出されるコーヒー豆は、挽かれていなくても、又は挽かれていてもよい。本発明の一実施形態において、生コーヒー豆は、焙煎したコーヒー豆と一緒に共抽出される、すなわち生及び焙煎したコーヒー豆は、同一の抽出系において、同時に抽出されて、混合した抽出物を得る。最も揮発性の高い芳香成分は、例えば、抽出物が純粋な可溶性コーヒーの生成のために使用される予定の場合、抽出前に豆から剥離されてもよい。揮発性の芳香成分の剥離方法は、当技術分野において、例えばEP1078576から、よく知られている。
【0012】
水及び/又は蒸気でのコーヒー豆の抽出は、当技術分野において、例えばEP0916267から、よく知られている。抽出物は、濃縮ステップを経てもよく、クロロゲン酸を加水分解するための処理の前に、例えば、噴霧乾燥又は凍結乾燥によって、乾燥させてもよい。抽出物は、乾燥させた場合、クロロゲン酸を加水分解するための処理を達成するために、必要ならば、再懸濁してもよい。
【0013】
クロロゲン酸は、トランス桂皮酸とキナ酸の間に形成されるエステルのファミリーである。クロロゲン酸は、主にキナ酸と種々の位置に結合したフェノール基(例えばコーヒー基、フェルラ基、クマル基、メトキシ桂皮基)のモノ−及びジエステルとして、コーヒー中に本来存在する。本発明の方法により、コーヒー抽出物中のクロロゲン酸(キナ酸エステル)は、加水分解して、フェノール酸を生成でき、例えば、クロロゲン酸3−、4−、又は5−カフェオイルキナ酸及びジエステル、並びに3−、4−、又は5−フェルロイルキナ酸及びジエステルは、加水分解して、それぞれコーヒー酸及びフェルラ酸を生成できる。方法の好ましい実施形態において、カフェオイルキナ酸及び/又はジエステルは、加水分解して、コーヒー酸を生成し、及び/又はフェルロイルキナ酸及び/又はジエステルは、加水分解して、フェルラ酸を生成する。本発明の一実施形態において、クロロゲン酸を加水分解して、フェノール酸を生成するための処理は、処理された抽出物中のコーヒー酸の量が、乾燥物質1グラム当たり、少なくとも2、少なくとも5、又は少なくとも10ミリグラムなど、乾燥物質1グラム当たり、少なくとも1ミリグラムになるように実施される。本発明の別の実施形態において、クロロゲン酸を加水分解して、フェノール酸を生成するための処理は、処理されたコーヒー抽出物中のフェルラ酸の量が、乾燥物質1グラム当たり、少なくとも1、少なくとも2、又は少なくとも5ミリグラムなど、乾燥物質1グラム当たり、少なくとも0.5ミリグラムになるように実施される。さらなる実施形態において、コーヒー抽出物中に存在する、少なくとも30%、少なくとも50%、若しくは少なくとも75%など、少なくとも20%のカフェオイルキナ酸及びジエステル、及び/又はフェルロイルキナ酸及びジエステルは、クロロゲン酸を加水分解してフェノール酸を生成するための処理によって、加水分解される。
【0014】
クロロゲン酸をフェノール酸に加水分解するための、抽出物の処理は、抽出の後又は間に実施してもよい。抽出物は、クロロゲン酸を加水分解するための処理の前、間、又は後に抽出されたコーヒー豆から分離してもよい。一実施形態において、抽出物は、クロロゲン酸を加水分解するための処理の後で、抽出されたコーヒー豆から分離されたままである、すなわち、抽出物は、クロロゲン酸を加水分解するための処理の後に再び、抽出されたコーヒー豆と接触させない。抽出されたコーヒー豆からの抽出物の分離は、任意の適切な方法で、例えば濾過又は遠心分離によって、実施してもよい。分離は、現実的に及び経済的に実行可能な、並びに抽出物の所望の使用の観点から必要とされる程度まで実施してもよい。したがって、分離は100%完了していなくてもよく、例えば、豆からの溶解していない物質の微量部分が、分離の後に、抽出物と一緒に依然として存在していてもよい。
【0015】
クロロゲン酸の加水分解は、任意の適切な方法によって実施できる。本発明の一実施形態において、加水分解は、コーヒー抽出物中のクロロゲン酸を加水分解することができる微生物と共にコーヒー抽出物をインキュベート又は発酵することによって実施される。クロロゲン酸を加水分解することができる微生物は、例えば、本明細書の実施例において開示されている通り確認できる。適切な微生物は、酵母、真菌、又は細菌から選択されてもよい。適切な微生物は、例えば、例えばアスペルギルス・オリザエ(Aspergillus oryzae)などのアスペルギルス、例えばL.ジョンソニイ(L.johnsonii)(CNCM I−1225)などのラクトバチルス(Lactobacillus)、例えばB.ラクティス(B.lactis)(CNCM I−3446)などのビフィズス菌(Bifidobacterium)、又は、例えばサッカロミセス・セレビシエ(Saccharomyces cerevisiae)などの酵母であってもよい。インキュベーション又は発酵は、クロロゲン酸の必要とされる加水分解を達成するために必要な時間、特定の微生物の成長のために適切な条件下で、コーヒー抽出物に、クロロゲン酸を加水分解することができる微生物を接種することによって実施してもよい。特定の条件は、例えば本明細書中に含まれる実施例を参照して、当業者によって容易に決定できる。本発明の別の実施形態において、クロロゲン酸の加水分解は、非複製微生物、例えば溶解細胞の使用によって実施される。適切な条件下で、溶解細胞と共にコーヒー抽出物をインキュベートすることによって、細胞溶解物中に存在する酵素が、クロロゲン酸を加水分解して、フェノール酸を生成できる。適切な細胞は、例えば、上述の微生物の細胞であってもよい。細胞可溶化物を生成する適切な方法は、当技術分野において知られている。
【0016】
微生物の量及び発酵の条件は、クロロゲン酸の所望の加水分解を達成するのに適切であるべきであり、通例の方法により、例えば本明細書の実施例に開示された方法を使用して、当業者によって決定できる。
【0017】
別の実施形態において、クロロゲン酸の加水分解は、クロロゲン酸を加水分解することができる酵素の使用によって実施される。適切な酵素は、例えばエステラーゼ、例えばアスペルギルス・ジャポニクス(Aspergillus japonicus)(日本のキッコーマン株式会社から市販されている)に由来するクロロゲン酸エステラーゼ、アスペルギルス・オリザエ(EC3.1.1.20)(日本のキッコーマン株式会社から市販されている)からのタンナーゼ、パラターゼ(Palatase)20000L(EC3.1.1.3)(デンマークのNovozymes A/Sから市販されている)である。酵素加水分解は、酵素反応のための従来の方法によって、例えば、必要とされる酵素活性のために適切な条件下で、コーヒー抽出物中に酵素を溶解又は懸濁することによって実施してもよい。酵素は、加水分解が起きた後で、例えば加熱によって不活化してもよい。酵素は、例えば膜又は不活性担体上に固定化してもまたよく、処理されるコーヒー抽出物は、加水分解の所望の程度が達成されるまで、膜上で又は担体を通して循環させてもよい。
【0018】
使用される酵素の量及び条件は、クロロゲン酸の所望の加水分解を達成するのに適切であるべきであり、通例の方法により、例えば、クロロゲン酸の加水分解を決定するための本明細書の実施例に開示された方法を使用して、当業者によって決定することができる。
【0019】
本発明は、本発明のコーヒー抽出物が、食物又は飲料製品の成分として使用される、上記食物又は飲料製品を製造する方法にもまた関する。抽出物は、抽出されたコーヒー豆から分離して使用され、すなわち豆からの溶解していない物質は、本明細書中に記載されている通り、分離によって実質的に除去され、食物又は飲料製品の製造において使用されない。食物又は飲料製品は、当技術分野において既知の任意の食物又は飲料製品であってもよい。好ましい実施形態において、食物又は飲料製品は、コーヒー製品、例えば可溶性コーヒー製品又はすぐに飲めるコーヒー製品である。可溶性コーヒー製品は、本発明の抽出物を濃縮し、乾燥することによって、製造してもよい。乾燥の前に、抽出物を、クロロゲン酸を加水分解するための処理を行わなかったコーヒー抽出物、例えば焙煎したコーヒー豆、生コーヒー豆、又はその両方の抽出物と混合してもよい。コーヒー抽出物から可溶性コーヒー製品を製造する方法は、当技術分野においてよく知られている。抽出物をコーヒー製品の製造のために使用する場合、抽出される豆は、例えば欧州特許出願公開第1078576号に記載の通り、抽出の前に、揮発性の芳香成分を除去するためのストリッピングにかけた可能性がある。次に、揮発性の芳香成分は、クロロゲン酸を加水分解するための処理の後、例えば乾燥の後で、抽出物に添加して戻して、芳香付けをした可溶性コーヒー製品を製造してもよい。本発明のコーヒー抽出物から製造された可溶性コーヒー製品は、そのまま販売されてもよく、又は、例えば、クリーマー及び/又は甘味料と混合され、クリーマー及び/又は甘味料を含むコーヒー飲料、例えばカプチーノ若しくはカフェラテを調製するために販売されてもよい。
【0020】
本発明によるコーヒー抽出物は、食物又は飲料製品の成分として使用される場合、所望の効果を達成するために、上記食物又は飲料製品の製造工程における任意の適切なステップで添加してもよい。抽出物は、所望の効果、例えば抗酸化効果をもたらすのに適切ないずれの量でも添加されてもよい。本発明の方法によって製造された食物又は飲料製品は、例えば、コーヒーベースの飲料、茶ベースの飲料、ソフトドリンク、乳製品、菓子製品、又は栄養補助食品であってもよい。
【0021】
本発明は、抗酸化剤としての、例えば製品中の成分としての本発明のコーヒー抽出物の使用にもまた関するものであり、上記製品は、抗酸化特性が、例えば、貯蔵の間、製品の成分の酸化を防ぐために望まれる、例えば食物又は飲料製品である。抗酸化剤は、いくつかの製品において一般に使用されており、本発明のコーヒー抽出物は、従来の抗酸化剤と同様に使用されてもよい。
【0022】
本発明のコーヒー抽出物は、例えば、グルタチオン−S−トランスフェラーゼ(GST)などの解毒酵素を誘導することによって、及びNrf2−仲介遺伝子発現経路を増加させることによって、ヒト又は動物において、生体内で抗酸化能力を強化するために、また使用されてもよい。増加したNrf2活性関連遺伝子は、解毒作用を強化し、酸化ストレスに対する内因性防御を刺激することが報告された。これらの効果は、例えば、コーヒー抽出物の経口投与によって、又はヒト若しくは動物の肌への局所的適用によって達成してもよい。
【0023】
本発明の抽出物は、例えば、炎症促進剤(例えばインターロイキン1b、リポ多糖(LPS))によるプロスタグランジンE2レベルの上昇を阻止することによって、炎症を抑制するために使用してもよい。
【0024】
多くの健康問題及び障害は、酸化ストレス及び炎症に関連している。本発明のコーヒー抽出物は、かかる問題若しくは障害などを治療又は予防するために使用してもよい。関連する問題及び障害は、例えば、例えば紫外線放射によって引き起こされる光損傷、アトピー性皮膚炎、湿疹、落屑性、掻痒性、アレルギー性症状などの皮膚障害、脳障害、炎症、肥満、並びに、例えば皮膚癌及び肺癌などの癌である。
【0025】
本発明のコーヒー抽出物は、例えば血糖値を低下させる、及び/又は、レプチン、インシュリン、及び/又はc−ペプチドの血中濃度を上昇させることによる抗糖尿病薬として;例えば骨ミネラル密度を上昇させることによる、例えばエストロゲン及び/又はプロゲステロンの血清濃度、及び/又はアルカリホスファターゼ活性を上昇させることによる骨再構築剤として;例えば抗血管新生効果を有する抗転移薬としてさらに使用してもよい。
【0026】
本発明によるコーヒー抽出物は、皮膚障害、糖尿病、アレルギー、脳障害、炎症、肥満、及び/又は癌を、治療又は予防するための配合物の調製のために使用してもよい。配合物は、例えば経口投与又は皮膚への局所投与のためのいずれの適切な形態でも、例えば食物若しくは飲料製品、栄養補助食品、錠剤、外用水薬、又は化粧品の形態であってもよい。好ましい実施形態において、配合物は医薬である。
【実施例】
【0027】
実施例1
ラクトバチルス・ジョンソニイの新鮮細胞によるネスカフェプロテクト(登録商標)の処理
L.ジョンソニイ(CNCM I−1225)の細胞を成長させ(7.0E08cfu/ml)、遠心分離した(5000g、10分)。0.61g/mlの濃度で、リン酸緩衝液(50mM、pH7.0)中にペレットを再懸濁した。ネスカフェプロテクト(登録商標)(生及び焙煎したコーヒー豆の乾燥共抽出物)30mg/mlを添加し、混合物を37℃でインキュベートした。異なる反応時間で試料を抜き出し、遠心分離し(3000g、5分)、0.45μm孔径のシリンジフィルター(Millipore SLHA025BS)を通して濾過し、HPLCによって分析した。
【0028】
同一の反応条件下であるが細菌なしで、平行して反応対照を実施した。
【0029】
ラクトバチルス・ジョンソニイ抽出物(溶解細胞)によるネスカフェプロテクト(登録商標)の処理
L.ジョンソニイ(CNCM I−1225)の細胞を成長させ(7.0E08cfu/ml)、遠心分離した(5000g、10分)。0.61g/mlの濃度で、リン酸緩衝液(50mM、pH7.0)中にペレットを再懸濁した。次に、ガラスビーズ法を使用して、細胞を溶解させた。細胞調製物600μlをスクリューキャップチューブに入れ、0℃でガラスビーズ600μlを添加した。次に、チューブをミニビードビーター(Mini−Beadbeater)中に強振動下で1分間入れ、氷で冷却し、ミニビードビーター中に、さらに1分間入れた。次に、ネスカフェプロテクト(登録商標)(30mg/ml、リン酸緩衝液pH7.0)の溶液900μlに、粗細胞抽出物を添加し、混合物を37℃でインキュベートした。異なる反応時間で試料を抜き出し、遠心分離し(3000g、5分)、0.45μm孔径のシリンジフィルター(Millipore SLHA025BS)を通して濾過し、HPLCによって分析した。
【0030】
ラクトバチルス・ジョンソニイの噴霧乾燥調製物でのネスカフェプロテクト(登録商標)の処理
ネスカフェプロテクト(登録商標)30mgを、リン酸緩衝液(50mM、pH7.0)1ml又は水1mlに溶解した。この溶液に、ラクトバチルス・ジョンソニイ(CNCM I−1225)の噴霧乾燥調製物(3.3E9cfu/g)10mgを添加した。次に、混合物を37℃でインキュベートし、異なる反応時間で試料を抜き出した。遠心分離(3000g、5分)及び濾過(0.45μm孔径のシリンジフィルター、Millipore SLHA025BS)後、HPLCによって、試料を分析した。
【0031】
ラクトバチルス・ジョンソニイ(CNCM I−1225)の噴霧乾燥調製物での生コーヒー抽出物の処理
乾燥生コーヒー抽出物30mgを、リン酸緩衝液(50mM、pH7.0)1ml又は水1mlに溶解した。この溶液に、ラクトバチルス・ジョンソニイの噴霧乾燥調製物(3.3E9cfu/g)10mgを添加した。次に、混合物を37℃でインキュベートし、異なる反応時間で試料を抜き出した。遠心分離(3000g、5分)及び濾過(0.45μm孔径のシリンジフィルター、Millipore SLHA025BS)後、HPLCによって、試料を分析した。
【0032】
ラクトバチルス・ジョンソニイ(CNCM I−1225)の濃縮調製物でのネスカフェ(NESCAFE)(登録商標)の処理
ネスカフェスペシャルフィルター(NESCAFE SPECIAL FILTRE)(登録商標)(焙煎したコーヒー豆の乾燥抽出物)400mgを沸騰水1mlに溶解し、室温で37℃まで、この溶液を冷却した。このコーヒー溶液250μlに、ラクトバチルス・ジョンソニイの異なる量の濃縮調製物(50μl、100μl、350μl、750μl)を添加し、水で1mlになるまで量を調整した。次に、混合物を37℃で2時間及び4時間インキュベートした。遠心分離(3000g、5分)及び濾過後、HPLCによって、試料を分析した。
【0033】
HPLC分析
コーヒー試料を1%w/wに希釈し、CC250/4Nucleosil 100−5−C18カラム(Macherey−Nagel)でRP−HPLCによって分析した。溶離系は、流量1mL/分で、Millipore水、0.1%TFA、及びCH3CNであった。この方法により、外部標準検量線を使用して、カフェオイルキナ酸(CQA)、フェルロイルキナ酸(FQA)、ジカフェオイルキナ酸(diCQA)、フェルオイルキナ酸−ラクトン、コーヒー酸(CA)、及びフェルラ酸(FA)を同時に測定(325mmでの吸光度)できた。時間0(t0)での基準、又は細菌なしでの同時間の基準に対して結果を示した。
【0034】
抗酸化剤応答配列(ARE)ルシフェラーゼ分析
ネオマイシン選択可能マーカーを含むpcDNA3.1プラスミドと一緒に、ラットのグルタチオン−S−トランスフェラーゼA2(GSTA2)中に存在するARE8コピーを含むpGL−8xAREを、ヒトMCF7細胞に安定的に形質移入した(Wangら、Cancer Res.、66巻、10983〜10994頁、2006年)。ARE(抗酸化剤応答配列)は、解毒作用及び酸化ストレスに対する内因性防御に関与する遺伝子を制御する転写因子Nrf2の結合部位である。プラスミドpGL−8xAREは、Nrf2活性の監視を可能にする、8個のNrf2結合部位の下流にルシフェラーゼ遺伝子を含む。
【0035】
コーヒーでの処理のために、DMEM成長培地の96ウェルマイクロタイタープレートにAREc32細胞を播種した。異なるコーヒーで24時間処理した後、ホタルルシフェラーゼ活性を測定した。
【0036】
タンパク質発現
コラゲナーゼ溶液でのスプラーグドーリーラットの肝臓の灌流によって、初代培養肝細胞を得た(Sidhuら、Arch.Biochem.Biophys.301巻、103〜113頁、1993年)。トリパンブルー排除試験によって測定された細胞生存率は90〜95%の間の範囲であることがわかった。2mM L−グルタミン酸、10mMヘペスpH7.4を、ITS+、ペニシリン/ストレプトマイシン15000U、100nMデキサメタゾン、及び5%ウシ胎仔血清(ハイ−クローン)を補ったウィリアムス培地3mlで、60mmプラスチック組織培養皿上に、1.5×105細胞/cm2の密度で細胞を播種した。肝細胞を2時間付着させ、次に、EBSSで洗浄して、細胞片及び付着しなかった細胞を除去した。デキサメタゾン25nMを含む、新鮮な血清を含まない培地を添加し、次に、マトリゲルのオーバーレイ(233g/ml)を適用した。培地交換に続いて、2日に一度、新鮮なマトリゲルを培養物に添加した。解毒酵素及び抗酸化タンパク質発現についてのコーヒーの効果を研究するために、タンパク質抽出及びウェスタンブロット分析の前に、48時間の細胞播種の24時間後に、培地に試験材料を添加した(Cavinら、Food Chem Tox.、46巻、1239〜48頁、2008年)。
【0037】
プロスタグランジンE2の生成のアッセイ
ヒト結腸HT−29細胞を、異なるコーヒーで15時間処理し、続いて炎症誘発剤TNF−α(10ng/ml)と一緒に6時間共培養した。競合酵素免疫測定法(EIA)を使用して、HT−29細胞中のPGE2生成の分析を測定した(Cavinら、BBRC、327巻、742〜49頁、2005年)。
【0038】
結果
フェノール酸生成のためのクロロゲン酸の加水分解
実験1:様々な反応時間及び細胞調製物量による、L.ジョンソニイ新鮮細胞でのネスカフェプロテクト(登録商標)の処理。結果を表1に示す。
【0039】
【表1】

【0040】
実験2:様々な反応時間及び細胞調製物量による、L.ジョンソニイ抽出物(溶解細胞)によるネスカフェプロテクト(登録商標)の処理。結果を表2に示す。
【0041】
【表2】

【0042】
実験3:ラクトバチルス・ジョンソニイの噴霧乾燥調製物によるネスカフェプロテクト(登録商標)の処理。結果を表3に示す。
【0043】
【表3】

【0044】
実験4:ラクトバチルス・ジョンソニイの噴霧乾燥調製物での生コーヒー抽出物の処理。結果を表4に示す。
【0045】
【表4】

【0046】
実験5:ラクトバチルス・ジョンソニイの濃縮調製物でのネスカフェ(登録商標)の処理。結果を表5に示す。
【0047】
【表5】

【0048】
表6は、クロロゲン酸を加水分解するための処理をしなかった生コーヒー豆の抽出物(対照試料)の2つの異なる試料における、いくつかの化合物の絶対濃度を示す。
【0049】
【表6】

【0050】
タンパク質の発現
ラット初代培養肝細胞において、ネスカフェレッドカップ(登録商標)(焙煎したコーヒー豆の抽出物)200ug/mlは48時間の処理後、ウェスタンブロットにより、400ug/mlで、GSTサブユニット(GSTA4、GSTP1)及びヘム−オキシゲナーゼ−1(HO−1)のタンパク質発現の増加をもたらさず、GSTP1及びHO−1発現の弱い誘導をもたらした。対照的に、GSTA4、GSTP1、及びHO−1について、L.ジョンソニイで処理したネスカフェプロテクト(登録商標)200ug/ml及び400ug/mlの両方で、異なるタンパク質発現のより強い誘導を観察した。結果を、ウェスタンブロットゲルとして図1に示す。
【0051】
ネスカフェレッドカップ(登録商標)対ネスカフェプロテクト(登録商標)及びL.ジョンソニイで処理したネスカフェプロテクト(登録商標)を5%有する食餌を2週間与えたオスのラットの肝臓において得られたデータは、ラット初代培養肝細胞において観察された効果を確認した。未処理のネスカフェプロテクト(登録商標)(GSTP1、NQO1)及び未処理のネスカフェレッドカップ(登録商標)(GSTP1、NQO1)と比較して、解毒酵素発現の最強の誘導(GSTP1、NQO1)が、L.ジョンソニイで処理したネスカフェプロテクト(登録商標)について見られた。結果を、ウェスタンブロットゲルとして図2に示す。
【0052】
抗酸化剤応答配列(ARE)ルシフェラーゼ分析
ラットGSTA2−AREレポーター構築体の数コピーで、安定的に形質移入されたヒト乳癌細胞(AREc32)を使用して、コーヒーによるNrf2−ARE経路の活性化を実証した。クロロゲン酸を加水分解するための処理をしていない生コーヒー抽出物、及びL.ジョンソニイで24時間処理した異なる生コーヒー抽出物は、Nrf2−ルシフェラーゼレポーター活性における用量依存的上昇をもたらした(表7を参照されたい)。
【0053】
【表7】

【0054】
プロスタグランジンE2生成のアッセイ
ヒト結腸HT−29細胞で、L.ジョンソニイで処理した生コーヒー抽出物の潜在的な抗炎症性効果を分析した。炎症誘発剤TNF−αによる処理後、結腸細胞においてプロスタグランジンE2(PGE2)レベルが誘導される。この研究において、異なるコーヒー抽出物(クロロゲン酸を加水分解するための処理をしていない生コーヒー抽出物、及びL.ジョンソニイで24時間処理した異なる生コーヒー抽出物)で、細胞を24時間前処理した。実験の最後の6時間に、TNF−α(10ng/ml)を添加した。データ(表8を参照されたい)は、TNF−αで処理した対照細胞と比較した、PGE2生成のコーヒーによる明白な用量依存的減少を示した。
【0055】
【表8】

【0056】
実施例2
コーヒー試料
100%ロブスタ生豆からの生コーヒー抽出物
ネスカフェプロテクト(登録商標)、生及び焙煎したコーヒー豆の乾燥共抽出物
【0057】
酵素及び細胞
微生物 培地
ラクトバチルス・ジョンソニイ(CNCM I−1225) MRS
ビフィズス菌ラクティスBB12(CNCM I−3446) MRS+システイン
ビフィズス菌ロングム(Bifidobacterium longum)BB536(ATCC BAA−999) MRS+システイン
【0058】
アスペルギルス・ジャポニクス(日本のキッコーマン株式会社)由来のクロロゲン酸エステラーゼ(24U/g)。
アスペルギルス・オリザエ(日本のキッコーマン株式会社)からのタンナーゼ
【0059】
細菌細胞の調製
攪拌せずに、嫌気性環境で、37℃での培地における16時間の培養に対応する静止期に十分到達した後で、試験した菌株を採取した(5000gで10分間の遠心分離)。菌株の最初の活性化のために、凍結保存培養物を新鮮な培地中に植菌し、一晩成長させた。この前培養物を使用して、培養物を植菌した。
【0060】
細菌細胞でのコーヒー抽出物の処理
細菌の培養及び遠心分離の後で、0.61g/mlの濃度で、リン酸緩衝液(pH7.0)中にペレットを再懸濁した。この細胞調製物200μlに、コーヒー溶液(3%)800μlを添加し、37℃で、4時間、16時間、及び24時間、混合物をインキュベートした。
【0061】
クロロゲン酸エステラーゼでのコーヒー抽出物の培養
コーヒー溶液(3%)800μlに、リン酸緩衝液(pH7.0)200μl中のクロロゲン酸エステラーゼ(25mg)の溶液を添加した。次に、37℃で、4時間、16時間、及び24時間、混合物をインキュベートした。反応時間の後で、熱処理(3分、90℃)によって酵素活性を止め、分析の前に混合物を濾過した。
【0062】
AREルシフェラーゼ分析
実施例1の通り
【0063】
結果
ラットGSTA2−AREレポーター構築体の数コピーで、安定的に形質移入されたヒト乳癌細胞(AREc32)を使用して、コーヒーによる抗酸化Nrf2−ARE経路の活性化を実証した。クロロゲン酸を加水分解するための処理をしていない(未処理)生コーヒー抽出物、ラクトバチルス・ジョンソニイ(Lj)で24時間処理した生コーヒー抽出物、ビフィズス菌ラクティス(Bl)で24時間処理した生コーヒー抽出物、及びクロロゲン酸エステラーゼ(CE)で4時間処理した生コーヒー抽出物は全て、Nrf2−ルシフェラーゼレポーター活性における用量依存的上昇をもたらした(表9)。
【0064】
【表9】

【0065】
異なる微生物及びクロロゲン酸エステラーゼで、生コーヒー抽出物を処理して、クロロゲン酸を加水分解した。結果を表10に示す。
【0066】
【表10】

【0067】
異なる微生物及びクロロゲン酸エステラーゼで、ネスカフェプロテクト(登録商標)を処理し、クロロゲン酸を加水分解した。結果を表11に示す。
【0068】
【表11】

【技術分野】
【0001】
本発明は、抗酸化及び抗炎症性特性を有する改良されたコーヒー抽出物を生成する方法、抽出物を生成する方法、並びに本発明の抽出物の使用に関する。
【背景技術】
【0002】
コーヒー並びにカフェイン及びジテルペン(例えば、カフェストール、カーウェオール)などのコーヒー活性化合物は、げっ歯動物において解毒酵素(例えば、グルタチオン−S−トランスフェラーゼGST)を誘導することが示された(Cavin C.ら、1998年、「コーヒーに特有のジテルペンであるカフェストール及びカーウェオールは、二重機構によってアフラトキシンB1に誘導される遺伝毒性を防ぐ(The coffee−specific diterpenes cafestol and kahweol protect against aflatoxin B1−induced genotoxicity trough a dual mechanism.)。」、Carcinogenesis、19巻、1369〜1375頁、Cavin,C.ら、2003年、「コーヒーのジテルペンは、ラット及びヒトの培養系において、ベンゾ[a]ピレンの遺伝毒性を妨げる(Coffee diterpenes prevent benzo[a]pyrene genotoxicity in rat and human culture systems.)。」、Biochemical Biophysical Research Communication、306巻、488〜495頁、Huber,W.ら、2002年a、「コーヒー成分であるカーウェオール及びカフェストールによる、ラットの特定の器官における化学的予防酵素であるグルクロニルトランスフェラーゼ及びグルタチオントランスフェラーゼの強化(Enhancement of the chemoprotective enzymes glucuronyl transferase and glutathione transferase in specific organs of the rat by the coffee components kahweol and cafestol.)。」、Archive of Toxicology、76巻、209〜217頁)。コーヒーにより増進したGST活性は、5日間でコーヒー800mlを摂取した後のヒトにおいて、さらに実証された(Steinkellner,H.ら、2005年、「コーヒー摂取は、血漿においてGSTPを誘導し、(+/−)−抗−ベンゾ[a]ピレン−7,8−ジヒドロジオール−9,10−エポキシドによって誘導されるDNA損傷からリンパ球を保護する:対照ヒト介入試験の結果(Coffee consumption induces GSTP in plasma and protects lymphocytes against (+/−)−anti−benzo[a]pyrene−7,8−dihydrodiol−9,10−epoxide induced DNA−damage:results of controlled human intervention trials.)。」、Mut.Res.591巻、264〜275頁)。さらに、Richelleら、J.Agric.Food Chem.、49巻、3438〜42頁、(2001年)は、生体外でのLDL酸化の遅延時間が、標準的な1杯分のコーヒーによって、実質的に増加することを示した。増進した全抗酸化能力は、コーヒー200mlを摂取した後、生体内でのヒト血漿においてもまた観察された(Natellaら、J.Agric.Food Chem.、50巻、6211〜16頁、2002年)。
【0003】
この種の抗酸化活性は、例えば癌、心臓病、退行性脳障害、及び老化に関与することがある損傷を与える遊離基を減少させることによって、「酸化ストレス」を防ぐことが知られている。
【0004】
食物及び飲料製品の健康上の利益を増進させるために、増進した抗酸化活性やその他の有益な生物活性を有する製品を製造すること、並びに、例えば化粧及び医薬品ばかりでなく、食物及び飲料製品の特性を強化するために使用できる、抗酸化剤及び有益な生物活性を有するその他の化合物の天然源を発見することが望まれている。抗酸化特性は、分子自体の性質に本来備わっている可能性があるか、又は酸化ストレスに対する自然防御の誘導によって仲介され得る。
【発明の概要】
【0005】
本発明者らは今、コーヒー酸の量が、乾燥物質1グラム当たり、少なくとも1ミリグラムであり、及び/又はフェルラ酸の量が、乾燥物質1グラム当たり、少なくとも0.5ミリグラムであるコーヒー抽出物を生成する方法、並びに、かかるコーヒー抽出物が、従来のコーヒー抽出物と比べて、抗酸化及び抗炎症性特性を向上させたことを見出した。したがって、本発明は、以下のステップ、a)水でコーヒー豆を抽出して、コーヒー抽出物を生成するステップ、及びb)クロロゲン酸を加水分解して、フェノール酸を生成するために、コーヒー抽出物を処理するステップを含む、コーヒー抽出物を生成する方法に関する。さらなる実施形態において、本発明は、本発明のコーヒー抽出物の使用、食物又は飲料製品を製造する方法、及び結果として生じる食物又は飲料製品に関する。
【図面の簡単な説明】
【0006】
【図1】クロロゲン酸を加水分解する処理をしていないネスカフェレッドカップ(NESCAFE RED CUP)(登録商標)(焙煎したコーヒー豆の抽出物)200及び400ug/ml、及びラクトバチルス・ジョンソニイ(Lactobacillus johnsonii)で処理したネスカフェプロテクト(NESCAFE PROTECT)(登録商標)200及び400ug/mlで処理したラットの初代培養肝細胞、並びにコーヒー抽出物で処理していない対照試料におけるGSTのサブユニット(GSTA4、GSTP1)及びヘム−オキシゲナーゼ−1(HO−1)のタンパク質発現を示すウェスタンブロットゲルの図である。詳細については、実施例1を参照されたい。
【図2】クロロゲン酸を加水分解する処理をしていないネスカフェレッドカップ(登録商標)(焙煎したコーヒー豆の抽出物)(RN)、クロロゲン酸を加水分解する処理をしていないネスカフェプロテクト(登録商標)(生及び焙煎したコーヒー豆の共抽出物)(P)、及びラクトバチルス・ジョンソニイで処理したネスカフェプロテクト(登録商標)(La1−P)を5%含む食餌を2週間与えた雄性のラットの肝臓中での解毒酵素発現の誘導(GSTP1、NQO1)を示すウェスタンブロットの図である。詳細については、実施例1を参照されたい。
【発明を実施するための形態】
【0007】
本発明は、改良された抗酸化及び抗炎症性特性を有するコーヒー抽出物に関する。
【0008】
本発明の一実施形態において、コーヒー抽出物は、コーヒー酸を、乾燥物質1グラム当たり、少なくとも2、少なくとも5、少なくとも10、又は少なくとも25ミリグラムなど、乾燥物質1グラム当たり、少なくとも1ミリグラム含む。別の実施形態において、コーヒー抽出物は、フェルラ酸を、乾燥物質1グラム当たり、少なくとも1、少なくとも2、少なくとも5、又は少なくとも10ミリグラムなど、乾燥物質1グラム当たり、少なくとも0.5ミリグラム含む。さらなる実施形態において、コーヒー酸の量に対するカフェオイルキナ酸及びジエステルの量の割合は、50未満、10未満、又は1未満など、100未満(重量/重量)である。またさらなる実施形態において、フェルラ酸の量に対するフェルロイルキナ酸及びジエステルの量の割合は、10未満、5未満、又は1未満など、30未満(重量/重量)である。
【0009】
本発明のコーヒー抽出物は、生コーヒー豆及び/又は焙煎したコーヒー豆の抽出物であってもよい。コーヒー抽出物を生成する多数の方法は、当技術分野において知られている。
【0010】
本発明は、以下のステップ、a)水でコーヒー豆を抽出して、コーヒー抽出物を生成するステップ、及びb)クロロゲン酸をフェノール酸に加水分解するために、コーヒー抽出物を処理するステップを含む、コーヒー抽出物を生成する方法に、さらに関する。
【0011】
抽出されるコーヒー豆は、挽かれていなくても、又は挽かれていてもよい。本発明の一実施形態において、生コーヒー豆は、焙煎したコーヒー豆と一緒に共抽出される、すなわち生及び焙煎したコーヒー豆は、同一の抽出系において、同時に抽出されて、混合した抽出物を得る。最も揮発性の高い芳香成分は、例えば、抽出物が純粋な可溶性コーヒーの生成のために使用される予定の場合、抽出前に豆から剥離されてもよい。揮発性の芳香成分の剥離方法は、当技術分野において、例えばEP1078576から、よく知られている。
【0012】
水及び/又は蒸気でのコーヒー豆の抽出は、当技術分野において、例えばEP0916267から、よく知られている。抽出物は、濃縮ステップを経てもよく、クロロゲン酸を加水分解するための処理の前に、例えば、噴霧乾燥又は凍結乾燥によって、乾燥させてもよい。抽出物は、乾燥させた場合、クロロゲン酸を加水分解するための処理を達成するために、必要ならば、再懸濁してもよい。
【0013】
クロロゲン酸は、トランス桂皮酸とキナ酸の間に形成されるエステルのファミリーである。クロロゲン酸は、主にキナ酸と種々の位置に結合したフェノール基(例えばコーヒー基、フェルラ基、クマル基、メトキシ桂皮基)のモノ−及びジエステルとして、コーヒー中に本来存在する。本発明の方法により、コーヒー抽出物中のクロロゲン酸(キナ酸エステル)は、加水分解して、フェノール酸を生成でき、例えば、クロロゲン酸3−、4−、又は5−カフェオイルキナ酸及びジエステル、並びに3−、4−、又は5−フェルロイルキナ酸及びジエステルは、加水分解して、それぞれコーヒー酸及びフェルラ酸を生成できる。方法の好ましい実施形態において、カフェオイルキナ酸及び/又はジエステルは、加水分解して、コーヒー酸を生成し、及び/又はフェルロイルキナ酸及び/又はジエステルは、加水分解して、フェルラ酸を生成する。本発明の一実施形態において、クロロゲン酸を加水分解して、フェノール酸を生成するための処理は、処理された抽出物中のコーヒー酸の量が、乾燥物質1グラム当たり、少なくとも2、少なくとも5、又は少なくとも10ミリグラムなど、乾燥物質1グラム当たり、少なくとも1ミリグラムになるように実施される。本発明の別の実施形態において、クロロゲン酸を加水分解して、フェノール酸を生成するための処理は、処理されたコーヒー抽出物中のフェルラ酸の量が、乾燥物質1グラム当たり、少なくとも1、少なくとも2、又は少なくとも5ミリグラムなど、乾燥物質1グラム当たり、少なくとも0.5ミリグラムになるように実施される。さらなる実施形態において、コーヒー抽出物中に存在する、少なくとも30%、少なくとも50%、若しくは少なくとも75%など、少なくとも20%のカフェオイルキナ酸及びジエステル、及び/又はフェルロイルキナ酸及びジエステルは、クロロゲン酸を加水分解してフェノール酸を生成するための処理によって、加水分解される。
【0014】
クロロゲン酸をフェノール酸に加水分解するための、抽出物の処理は、抽出の後又は間に実施してもよい。抽出物は、クロロゲン酸を加水分解するための処理の前、間、又は後に抽出されたコーヒー豆から分離してもよい。一実施形態において、抽出物は、クロロゲン酸を加水分解するための処理の後で、抽出されたコーヒー豆から分離されたままである、すなわち、抽出物は、クロロゲン酸を加水分解するための処理の後に再び、抽出されたコーヒー豆と接触させない。抽出されたコーヒー豆からの抽出物の分離は、任意の適切な方法で、例えば濾過又は遠心分離によって、実施してもよい。分離は、現実的に及び経済的に実行可能な、並びに抽出物の所望の使用の観点から必要とされる程度まで実施してもよい。したがって、分離は100%完了していなくてもよく、例えば、豆からの溶解していない物質の微量部分が、分離の後に、抽出物と一緒に依然として存在していてもよい。
【0015】
クロロゲン酸の加水分解は、任意の適切な方法によって実施できる。本発明の一実施形態において、加水分解は、コーヒー抽出物中のクロロゲン酸を加水分解することができる微生物と共にコーヒー抽出物をインキュベート又は発酵することによって実施される。クロロゲン酸を加水分解することができる微生物は、例えば、本明細書の実施例において開示されている通り確認できる。適切な微生物は、酵母、真菌、又は細菌から選択されてもよい。適切な微生物は、例えば、例えばアスペルギルス・オリザエ(Aspergillus oryzae)などのアスペルギルス、例えばL.ジョンソニイ(L.johnsonii)(CNCM I−1225)などのラクトバチルス(Lactobacillus)、例えばB.ラクティス(B.lactis)(CNCM I−3446)などのビフィズス菌(Bifidobacterium)、又は、例えばサッカロミセス・セレビシエ(Saccharomyces cerevisiae)などの酵母であってもよい。インキュベーション又は発酵は、クロロゲン酸の必要とされる加水分解を達成するために必要な時間、特定の微生物の成長のために適切な条件下で、コーヒー抽出物に、クロロゲン酸を加水分解することができる微生物を接種することによって実施してもよい。特定の条件は、例えば本明細書中に含まれる実施例を参照して、当業者によって容易に決定できる。本発明の別の実施形態において、クロロゲン酸の加水分解は、非複製微生物、例えば溶解細胞の使用によって実施される。適切な条件下で、溶解細胞と共にコーヒー抽出物をインキュベートすることによって、細胞溶解物中に存在する酵素が、クロロゲン酸を加水分解して、フェノール酸を生成できる。適切な細胞は、例えば、上述の微生物の細胞であってもよい。細胞可溶化物を生成する適切な方法は、当技術分野において知られている。
【0016】
微生物の量及び発酵の条件は、クロロゲン酸の所望の加水分解を達成するのに適切であるべきであり、通例の方法により、例えば本明細書の実施例に開示された方法を使用して、当業者によって決定できる。
【0017】
別の実施形態において、クロロゲン酸の加水分解は、クロロゲン酸を加水分解することができる酵素の使用によって実施される。適切な酵素は、例えばエステラーゼ、例えばアスペルギルス・ジャポニクス(Aspergillus japonicus)(日本のキッコーマン株式会社から市販されている)に由来するクロロゲン酸エステラーゼ、アスペルギルス・オリザエ(EC3.1.1.20)(日本のキッコーマン株式会社から市販されている)からのタンナーゼ、パラターゼ(Palatase)20000L(EC3.1.1.3)(デンマークのNovozymes A/Sから市販されている)である。酵素加水分解は、酵素反応のための従来の方法によって、例えば、必要とされる酵素活性のために適切な条件下で、コーヒー抽出物中に酵素を溶解又は懸濁することによって実施してもよい。酵素は、加水分解が起きた後で、例えば加熱によって不活化してもよい。酵素は、例えば膜又は不活性担体上に固定化してもまたよく、処理されるコーヒー抽出物は、加水分解の所望の程度が達成されるまで、膜上で又は担体を通して循環させてもよい。
【0018】
使用される酵素の量及び条件は、クロロゲン酸の所望の加水分解を達成するのに適切であるべきであり、通例の方法により、例えば、クロロゲン酸の加水分解を決定するための本明細書の実施例に開示された方法を使用して、当業者によって決定することができる。
【0019】
本発明は、本発明のコーヒー抽出物が、食物又は飲料製品の成分として使用される、上記食物又は飲料製品を製造する方法にもまた関する。抽出物は、抽出されたコーヒー豆から分離して使用され、すなわち豆からの溶解していない物質は、本明細書中に記載されている通り、分離によって実質的に除去され、食物又は飲料製品の製造において使用されない。食物又は飲料製品は、当技術分野において既知の任意の食物又は飲料製品であってもよい。好ましい実施形態において、食物又は飲料製品は、コーヒー製品、例えば可溶性コーヒー製品又はすぐに飲めるコーヒー製品である。可溶性コーヒー製品は、本発明の抽出物を濃縮し、乾燥することによって、製造してもよい。乾燥の前に、抽出物を、クロロゲン酸を加水分解するための処理を行わなかったコーヒー抽出物、例えば焙煎したコーヒー豆、生コーヒー豆、又はその両方の抽出物と混合してもよい。コーヒー抽出物から可溶性コーヒー製品を製造する方法は、当技術分野においてよく知られている。抽出物をコーヒー製品の製造のために使用する場合、抽出される豆は、例えば欧州特許出願公開第1078576号に記載の通り、抽出の前に、揮発性の芳香成分を除去するためのストリッピングにかけた可能性がある。次に、揮発性の芳香成分は、クロロゲン酸を加水分解するための処理の後、例えば乾燥の後で、抽出物に添加して戻して、芳香付けをした可溶性コーヒー製品を製造してもよい。本発明のコーヒー抽出物から製造された可溶性コーヒー製品は、そのまま販売されてもよく、又は、例えば、クリーマー及び/又は甘味料と混合され、クリーマー及び/又は甘味料を含むコーヒー飲料、例えばカプチーノ若しくはカフェラテを調製するために販売されてもよい。
【0020】
本発明によるコーヒー抽出物は、食物又は飲料製品の成分として使用される場合、所望の効果を達成するために、上記食物又は飲料製品の製造工程における任意の適切なステップで添加してもよい。抽出物は、所望の効果、例えば抗酸化効果をもたらすのに適切ないずれの量でも添加されてもよい。本発明の方法によって製造された食物又は飲料製品は、例えば、コーヒーベースの飲料、茶ベースの飲料、ソフトドリンク、乳製品、菓子製品、又は栄養補助食品であってもよい。
【0021】
本発明は、抗酸化剤としての、例えば製品中の成分としての本発明のコーヒー抽出物の使用にもまた関するものであり、上記製品は、抗酸化特性が、例えば、貯蔵の間、製品の成分の酸化を防ぐために望まれる、例えば食物又は飲料製品である。抗酸化剤は、いくつかの製品において一般に使用されており、本発明のコーヒー抽出物は、従来の抗酸化剤と同様に使用されてもよい。
【0022】
本発明のコーヒー抽出物は、例えば、グルタチオン−S−トランスフェラーゼ(GST)などの解毒酵素を誘導することによって、及びNrf2−仲介遺伝子発現経路を増加させることによって、ヒト又は動物において、生体内で抗酸化能力を強化するために、また使用されてもよい。増加したNrf2活性関連遺伝子は、解毒作用を強化し、酸化ストレスに対する内因性防御を刺激することが報告された。これらの効果は、例えば、コーヒー抽出物の経口投与によって、又はヒト若しくは動物の肌への局所的適用によって達成してもよい。
【0023】
本発明の抽出物は、例えば、炎症促進剤(例えばインターロイキン1b、リポ多糖(LPS))によるプロスタグランジンE2レベルの上昇を阻止することによって、炎症を抑制するために使用してもよい。
【0024】
多くの健康問題及び障害は、酸化ストレス及び炎症に関連している。本発明のコーヒー抽出物は、かかる問題若しくは障害などを治療又は予防するために使用してもよい。関連する問題及び障害は、例えば、例えば紫外線放射によって引き起こされる光損傷、アトピー性皮膚炎、湿疹、落屑性、掻痒性、アレルギー性症状などの皮膚障害、脳障害、炎症、肥満、並びに、例えば皮膚癌及び肺癌などの癌である。
【0025】
本発明のコーヒー抽出物は、例えば血糖値を低下させる、及び/又は、レプチン、インシュリン、及び/又はc−ペプチドの血中濃度を上昇させることによる抗糖尿病薬として;例えば骨ミネラル密度を上昇させることによる、例えばエストロゲン及び/又はプロゲステロンの血清濃度、及び/又はアルカリホスファターゼ活性を上昇させることによる骨再構築剤として;例えば抗血管新生効果を有する抗転移薬としてさらに使用してもよい。
【0026】
本発明によるコーヒー抽出物は、皮膚障害、糖尿病、アレルギー、脳障害、炎症、肥満、及び/又は癌を、治療又は予防するための配合物の調製のために使用してもよい。配合物は、例えば経口投与又は皮膚への局所投与のためのいずれの適切な形態でも、例えば食物若しくは飲料製品、栄養補助食品、錠剤、外用水薬、又は化粧品の形態であってもよい。好ましい実施形態において、配合物は医薬である。
【実施例】
【0027】
実施例1
ラクトバチルス・ジョンソニイの新鮮細胞によるネスカフェプロテクト(登録商標)の処理
L.ジョンソニイ(CNCM I−1225)の細胞を成長させ(7.0E08cfu/ml)、遠心分離した(5000g、10分)。0.61g/mlの濃度で、リン酸緩衝液(50mM、pH7.0)中にペレットを再懸濁した。ネスカフェプロテクト(登録商標)(生及び焙煎したコーヒー豆の乾燥共抽出物)30mg/mlを添加し、混合物を37℃でインキュベートした。異なる反応時間で試料を抜き出し、遠心分離し(3000g、5分)、0.45μm孔径のシリンジフィルター(Millipore SLHA025BS)を通して濾過し、HPLCによって分析した。
【0028】
同一の反応条件下であるが細菌なしで、平行して反応対照を実施した。
【0029】
ラクトバチルス・ジョンソニイ抽出物(溶解細胞)によるネスカフェプロテクト(登録商標)の処理
L.ジョンソニイ(CNCM I−1225)の細胞を成長させ(7.0E08cfu/ml)、遠心分離した(5000g、10分)。0.61g/mlの濃度で、リン酸緩衝液(50mM、pH7.0)中にペレットを再懸濁した。次に、ガラスビーズ法を使用して、細胞を溶解させた。細胞調製物600μlをスクリューキャップチューブに入れ、0℃でガラスビーズ600μlを添加した。次に、チューブをミニビードビーター(Mini−Beadbeater)中に強振動下で1分間入れ、氷で冷却し、ミニビードビーター中に、さらに1分間入れた。次に、ネスカフェプロテクト(登録商標)(30mg/ml、リン酸緩衝液pH7.0)の溶液900μlに、粗細胞抽出物を添加し、混合物を37℃でインキュベートした。異なる反応時間で試料を抜き出し、遠心分離し(3000g、5分)、0.45μm孔径のシリンジフィルター(Millipore SLHA025BS)を通して濾過し、HPLCによって分析した。
【0030】
ラクトバチルス・ジョンソニイの噴霧乾燥調製物でのネスカフェプロテクト(登録商標)の処理
ネスカフェプロテクト(登録商標)30mgを、リン酸緩衝液(50mM、pH7.0)1ml又は水1mlに溶解した。この溶液に、ラクトバチルス・ジョンソニイ(CNCM I−1225)の噴霧乾燥調製物(3.3E9cfu/g)10mgを添加した。次に、混合物を37℃でインキュベートし、異なる反応時間で試料を抜き出した。遠心分離(3000g、5分)及び濾過(0.45μm孔径のシリンジフィルター、Millipore SLHA025BS)後、HPLCによって、試料を分析した。
【0031】
ラクトバチルス・ジョンソニイ(CNCM I−1225)の噴霧乾燥調製物での生コーヒー抽出物の処理
乾燥生コーヒー抽出物30mgを、リン酸緩衝液(50mM、pH7.0)1ml又は水1mlに溶解した。この溶液に、ラクトバチルス・ジョンソニイの噴霧乾燥調製物(3.3E9cfu/g)10mgを添加した。次に、混合物を37℃でインキュベートし、異なる反応時間で試料を抜き出した。遠心分離(3000g、5分)及び濾過(0.45μm孔径のシリンジフィルター、Millipore SLHA025BS)後、HPLCによって、試料を分析した。
【0032】
ラクトバチルス・ジョンソニイ(CNCM I−1225)の濃縮調製物でのネスカフェ(NESCAFE)(登録商標)の処理
ネスカフェスペシャルフィルター(NESCAFE SPECIAL FILTRE)(登録商標)(焙煎したコーヒー豆の乾燥抽出物)400mgを沸騰水1mlに溶解し、室温で37℃まで、この溶液を冷却した。このコーヒー溶液250μlに、ラクトバチルス・ジョンソニイの異なる量の濃縮調製物(50μl、100μl、350μl、750μl)を添加し、水で1mlになるまで量を調整した。次に、混合物を37℃で2時間及び4時間インキュベートした。遠心分離(3000g、5分)及び濾過後、HPLCによって、試料を分析した。
【0033】
HPLC分析
コーヒー試料を1%w/wに希釈し、CC250/4Nucleosil 100−5−C18カラム(Macherey−Nagel)でRP−HPLCによって分析した。溶離系は、流量1mL/分で、Millipore水、0.1%TFA、及びCH3CNであった。この方法により、外部標準検量線を使用して、カフェオイルキナ酸(CQA)、フェルロイルキナ酸(FQA)、ジカフェオイルキナ酸(diCQA)、フェルオイルキナ酸−ラクトン、コーヒー酸(CA)、及びフェルラ酸(FA)を同時に測定(325mmでの吸光度)できた。時間0(t0)での基準、又は細菌なしでの同時間の基準に対して結果を示した。
【0034】
抗酸化剤応答配列(ARE)ルシフェラーゼ分析
ネオマイシン選択可能マーカーを含むpcDNA3.1プラスミドと一緒に、ラットのグルタチオン−S−トランスフェラーゼA2(GSTA2)中に存在するARE8コピーを含むpGL−8xAREを、ヒトMCF7細胞に安定的に形質移入した(Wangら、Cancer Res.、66巻、10983〜10994頁、2006年)。ARE(抗酸化剤応答配列)は、解毒作用及び酸化ストレスに対する内因性防御に関与する遺伝子を制御する転写因子Nrf2の結合部位である。プラスミドpGL−8xAREは、Nrf2活性の監視を可能にする、8個のNrf2結合部位の下流にルシフェラーゼ遺伝子を含む。
【0035】
コーヒーでの処理のために、DMEM成長培地の96ウェルマイクロタイタープレートにAREc32細胞を播種した。異なるコーヒーで24時間処理した後、ホタルルシフェラーゼ活性を測定した。
【0036】
タンパク質発現
コラゲナーゼ溶液でのスプラーグドーリーラットの肝臓の灌流によって、初代培養肝細胞を得た(Sidhuら、Arch.Biochem.Biophys.301巻、103〜113頁、1993年)。トリパンブルー排除試験によって測定された細胞生存率は90〜95%の間の範囲であることがわかった。2mM L−グルタミン酸、10mMヘペスpH7.4を、ITS+、ペニシリン/ストレプトマイシン15000U、100nMデキサメタゾン、及び5%ウシ胎仔血清(ハイ−クローン)を補ったウィリアムス培地3mlで、60mmプラスチック組織培養皿上に、1.5×105細胞/cm2の密度で細胞を播種した。肝細胞を2時間付着させ、次に、EBSSで洗浄して、細胞片及び付着しなかった細胞を除去した。デキサメタゾン25nMを含む、新鮮な血清を含まない培地を添加し、次に、マトリゲルのオーバーレイ(233g/ml)を適用した。培地交換に続いて、2日に一度、新鮮なマトリゲルを培養物に添加した。解毒酵素及び抗酸化タンパク質発現についてのコーヒーの効果を研究するために、タンパク質抽出及びウェスタンブロット分析の前に、48時間の細胞播種の24時間後に、培地に試験材料を添加した(Cavinら、Food Chem Tox.、46巻、1239〜48頁、2008年)。
【0037】
プロスタグランジンE2の生成のアッセイ
ヒト結腸HT−29細胞を、異なるコーヒーで15時間処理し、続いて炎症誘発剤TNF−α(10ng/ml)と一緒に6時間共培養した。競合酵素免疫測定法(EIA)を使用して、HT−29細胞中のPGE2生成の分析を測定した(Cavinら、BBRC、327巻、742〜49頁、2005年)。
【0038】
結果
フェノール酸生成のためのクロロゲン酸の加水分解
実験1:様々な反応時間及び細胞調製物量による、L.ジョンソニイ新鮮細胞でのネスカフェプロテクト(登録商標)の処理。結果を表1に示す。
【0039】
【表1】

【0040】
実験2:様々な反応時間及び細胞調製物量による、L.ジョンソニイ抽出物(溶解細胞)によるネスカフェプロテクト(登録商標)の処理。結果を表2に示す。
【0041】
【表2】

【0042】
実験3:ラクトバチルス・ジョンソニイの噴霧乾燥調製物によるネスカフェプロテクト(登録商標)の処理。結果を表3に示す。
【0043】
【表3】

【0044】
実験4:ラクトバチルス・ジョンソニイの噴霧乾燥調製物での生コーヒー抽出物の処理。結果を表4に示す。
【0045】
【表4】

【0046】
実験5:ラクトバチルス・ジョンソニイの濃縮調製物でのネスカフェ(登録商標)の処理。結果を表5に示す。
【0047】
【表5】

【0048】
表6は、クロロゲン酸を加水分解するための処理をしなかった生コーヒー豆の抽出物(対照試料)の2つの異なる試料における、いくつかの化合物の絶対濃度を示す。
【0049】
【表6】

【0050】
タンパク質の発現
ラット初代培養肝細胞において、ネスカフェレッドカップ(登録商標)(焙煎したコーヒー豆の抽出物)200ug/mlは48時間の処理後、ウェスタンブロットにより、400ug/mlで、GSTサブユニット(GSTA4、GSTP1)及びヘム−オキシゲナーゼ−1(HO−1)のタンパク質発現の増加をもたらさず、GSTP1及びHO−1発現の弱い誘導をもたらした。対照的に、GSTA4、GSTP1、及びHO−1について、L.ジョンソニイで処理したネスカフェプロテクト(登録商標)200ug/ml及び400ug/mlの両方で、異なるタンパク質発現のより強い誘導を観察した。結果を、ウェスタンブロットゲルとして図1に示す。
【0051】
ネスカフェレッドカップ(登録商標)対ネスカフェプロテクト(登録商標)及びL.ジョンソニイで処理したネスカフェプロテクト(登録商標)を5%有する食餌を2週間与えたオスのラットの肝臓において得られたデータは、ラット初代培養肝細胞において観察された効果を確認した。未処理のネスカフェプロテクト(登録商標)(GSTP1、NQO1)及び未処理のネスカフェレッドカップ(登録商標)(GSTP1、NQO1)と比較して、解毒酵素発現の最強の誘導(GSTP1、NQO1)が、L.ジョンソニイで処理したネスカフェプロテクト(登録商標)について見られた。結果を、ウェスタンブロットゲルとして図2に示す。
【0052】
抗酸化剤応答配列(ARE)ルシフェラーゼ分析
ラットGSTA2−AREレポーター構築体の数コピーで、安定的に形質移入されたヒト乳癌細胞(AREc32)を使用して、コーヒーによるNrf2−ARE経路の活性化を実証した。クロロゲン酸を加水分解するための処理をしていない生コーヒー抽出物、及びL.ジョンソニイで24時間処理した異なる生コーヒー抽出物は、Nrf2−ルシフェラーゼレポーター活性における用量依存的上昇をもたらした(表7を参照されたい)。
【0053】
【表7】

【0054】
プロスタグランジンE2生成のアッセイ
ヒト結腸HT−29細胞で、L.ジョンソニイで処理した生コーヒー抽出物の潜在的な抗炎症性効果を分析した。炎症誘発剤TNF−αによる処理後、結腸細胞においてプロスタグランジンE2(PGE2)レベルが誘導される。この研究において、異なるコーヒー抽出物(クロロゲン酸を加水分解するための処理をしていない生コーヒー抽出物、及びL.ジョンソニイで24時間処理した異なる生コーヒー抽出物)で、細胞を24時間前処理した。実験の最後の6時間に、TNF−α(10ng/ml)を添加した。データ(表8を参照されたい)は、TNF−αで処理した対照細胞と比較した、PGE2生成のコーヒーによる明白な用量依存的減少を示した。
【0055】
【表8】

【0056】
実施例2
コーヒー試料
100%ロブスタ生豆からの生コーヒー抽出物
ネスカフェプロテクト(登録商標)、生及び焙煎したコーヒー豆の乾燥共抽出物
【0057】
酵素及び細胞
微生物 培地
ラクトバチルス・ジョンソニイ(CNCM I−1225) MRS
ビフィズス菌ラクティスBB12(CNCM I−3446) MRS+システイン
ビフィズス菌ロングム(Bifidobacterium longum)BB536(ATCC BAA−999) MRS+システイン
【0058】
アスペルギルス・ジャポニクス(日本のキッコーマン株式会社)由来のクロロゲン酸エステラーゼ(24U/g)。
アスペルギルス・オリザエ(日本のキッコーマン株式会社)からのタンナーゼ
【0059】
細菌細胞の調製
攪拌せずに、嫌気性環境で、37℃での培地における16時間の培養に対応する静止期に十分到達した後で、試験した菌株を採取した(5000gで10分間の遠心分離)。菌株の最初の活性化のために、凍結保存培養物を新鮮な培地中に植菌し、一晩成長させた。この前培養物を使用して、培養物を植菌した。
【0060】
細菌細胞でのコーヒー抽出物の処理
細菌の培養及び遠心分離の後で、0.61g/mlの濃度で、リン酸緩衝液(pH7.0)中にペレットを再懸濁した。この細胞調製物200μlに、コーヒー溶液(3%)800μlを添加し、37℃で、4時間、16時間、及び24時間、混合物をインキュベートした。
【0061】
クロロゲン酸エステラーゼでのコーヒー抽出物の培養
コーヒー溶液(3%)800μlに、リン酸緩衝液(pH7.0)200μl中のクロロゲン酸エステラーゼ(25mg)の溶液を添加した。次に、37℃で、4時間、16時間、及び24時間、混合物をインキュベートした。反応時間の後で、熱処理(3分、90℃)によって酵素活性を止め、分析の前に混合物を濾過した。
【0062】
AREルシフェラーゼ分析
実施例1の通り
【0063】
結果
ラットGSTA2−AREレポーター構築体の数コピーで、安定的に形質移入されたヒト乳癌細胞(AREc32)を使用して、コーヒーによる抗酸化Nrf2−ARE経路の活性化を実証した。クロロゲン酸を加水分解するための処理をしていない(未処理)生コーヒー抽出物、ラクトバチルス・ジョンソニイ(Lj)で24時間処理した生コーヒー抽出物、ビフィズス菌ラクティス(Bl)で24時間処理した生コーヒー抽出物、及びクロロゲン酸エステラーゼ(CE)で4時間処理した生コーヒー抽出物は全て、Nrf2−ルシフェラーゼレポーター活性における用量依存的上昇をもたらした(表9)。
【0064】
【表9】

【0065】
異なる微生物及びクロロゲン酸エステラーゼで、生コーヒー抽出物を処理して、クロロゲン酸を加水分解した。結果を表10に示す。
【0066】
【表10】

【0067】
異なる微生物及びクロロゲン酸エステラーゼで、ネスカフェプロテクト(登録商標)を処理し、クロロゲン酸を加水分解した。結果を表11に示す。
【0068】
【表11】

【特許請求の範囲】
【請求項1】
以下のステップ、
a)水でコーヒー豆を抽出して、コーヒー抽出物を生成するステップ、及び
b)クロロゲン酸を加水分解して、フェノール酸を生成するために、コーヒー抽出物を処理するステップ
を含む、コーヒー抽出物を生成する方法。
【請求項2】
抽出されるコーヒー豆が、挽かれていないコーヒー豆である、請求項1に記載の方法。
【請求項3】
ステップa)において抽出されるコーヒー豆が、生コーヒー豆である、請求項1又は2に記載の方法。
【請求項4】
ステップa)において生コーヒー豆が、焙煎したコーヒー豆と一緒に共抽出される、請求項3の方法。
【請求項5】
コーヒー抽出物が、ステップb)の処理の前、間、又は後に、抽出されたコーヒー豆から分離される、請求項1〜4のいずれか一項に記載の方法。
【請求項6】
コーヒー抽出物が、ステップb)の処理の後に、抽出されたコーヒー豆から分離されたままである、請求項5に記載の方法。
【請求項7】
ステップa)において得られた生コーヒー抽出物を、焙煎したコーヒー豆の抽出物と混合し、混合物を、ステップb)において処理する、請求項3に記載の方法。
【請求項8】
ステップb)におけるクロロゲン酸の加水分解が、クロロゲン酸を加水分解して、フェノール酸を生成することができる微生物での発酵によって実施される、請求項1〜7のいずれか一項に記載の方法。
【請求項9】
請求項1〜8のいずれか一項に記載の方法によって生成されたコーヒー抽出物が、食物又は飲料製品の成分として使用される、食物又は飲料製品を製造する方法。
【請求項10】
抗酸化剤としての、コーヒー酸の量が、乾燥物質1グラム当たり、少なくとも1ミリグラムであり、及び/又は、フェルラ酸の量が、乾燥物質1グラム当たり、少なくとも0.5ミリグラムである、コーヒー抽出物の使用。
【請求項11】
医薬の調製のための、コーヒー酸の量が、乾燥物質1グラム当たり、少なくとも1ミリグラムであり、及び/又はフェルラ酸の量が、乾燥物質1グラム当たり、少なくとも0.5ミリグラムである、コーヒー抽出物の使用。
【請求項12】
皮膚障害、糖尿病、脳障害、炎症、肥満、及び/又は癌を、治療又は予防する配合物の調製のための、コーヒー酸の量が、乾燥物質1グラム当たり、少なくとも1ミリグラムであり、及び/又はフェルラ酸の量が、乾燥物質1グラム当たり、少なくとも0.5ミリグラムである、コーヒー抽出物の使用。
【請求項13】
骨再構築を促進するための、コーヒー酸の量が、乾燥物質1グラム当たり、少なくとも1ミリグラムであり、及び/又はフェルラ酸の量が、乾燥物質1グラム当たり、少なくとも0.5ミリグラムである、コーヒー抽出物の使用。
【請求項14】
コーヒー抽出物中のコーヒー酸の量に対する、カフェオイルキナ酸及びジエステルの量の割合が、100未満(重量/重量)である、請求項10〜13のいずれか一項に記載の使用。
【請求項15】
コーヒー抽出物中のフェルラ酸の量に対する、フェルロイルキナ酸及びジエステルの量の割合が、30未満(重量/重量)である、請求項10〜13のいずれか一項に記載の使用。
【請求項1】
以下のステップ、
a)水でコーヒー豆を抽出して、コーヒー抽出物を生成するステップ、及び
b)クロロゲン酸を加水分解して、フェノール酸を生成するために、コーヒー抽出物を処理するステップ
を含む、コーヒー抽出物を生成する方法。
【請求項2】
抽出されるコーヒー豆が、挽かれていないコーヒー豆である、請求項1に記載の方法。
【請求項3】
ステップa)において抽出されるコーヒー豆が、生コーヒー豆である、請求項1又は2に記載の方法。
【請求項4】
ステップa)において生コーヒー豆が、焙煎したコーヒー豆と一緒に共抽出される、請求項3の方法。
【請求項5】
コーヒー抽出物が、ステップb)の処理の前、間、又は後に、抽出されたコーヒー豆から分離される、請求項1〜4のいずれか一項に記載の方法。
【請求項6】
コーヒー抽出物が、ステップb)の処理の後に、抽出されたコーヒー豆から分離されたままである、請求項5に記載の方法。
【請求項7】
ステップa)において得られた生コーヒー抽出物を、焙煎したコーヒー豆の抽出物と混合し、混合物を、ステップb)において処理する、請求項3に記載の方法。
【請求項8】
ステップb)におけるクロロゲン酸の加水分解が、クロロゲン酸を加水分解して、フェノール酸を生成することができる微生物での発酵によって実施される、請求項1〜7のいずれか一項に記載の方法。
【請求項9】
請求項1〜8のいずれか一項に記載の方法によって生成されたコーヒー抽出物が、食物又は飲料製品の成分として使用される、食物又は飲料製品を製造する方法。
【請求項10】
抗酸化剤としての、コーヒー酸の量が、乾燥物質1グラム当たり、少なくとも1ミリグラムであり、及び/又は、フェルラ酸の量が、乾燥物質1グラム当たり、少なくとも0.5ミリグラムである、コーヒー抽出物の使用。
【請求項11】
医薬の調製のための、コーヒー酸の量が、乾燥物質1グラム当たり、少なくとも1ミリグラムであり、及び/又はフェルラ酸の量が、乾燥物質1グラム当たり、少なくとも0.5ミリグラムである、コーヒー抽出物の使用。
【請求項12】
皮膚障害、糖尿病、脳障害、炎症、肥満、及び/又は癌を、治療又は予防する配合物の調製のための、コーヒー酸の量が、乾燥物質1グラム当たり、少なくとも1ミリグラムであり、及び/又はフェルラ酸の量が、乾燥物質1グラム当たり、少なくとも0.5ミリグラムである、コーヒー抽出物の使用。
【請求項13】
骨再構築を促進するための、コーヒー酸の量が、乾燥物質1グラム当たり、少なくとも1ミリグラムであり、及び/又はフェルラ酸の量が、乾燥物質1グラム当たり、少なくとも0.5ミリグラムである、コーヒー抽出物の使用。
【請求項14】
コーヒー抽出物中のコーヒー酸の量に対する、カフェオイルキナ酸及びジエステルの量の割合が、100未満(重量/重量)である、請求項10〜13のいずれか一項に記載の使用。
【請求項15】
コーヒー抽出物中のフェルラ酸の量に対する、フェルロイルキナ酸及びジエステルの量の割合が、30未満(重量/重量)である、請求項10〜13のいずれか一項に記載の使用。
【図1】


【図2】




【図2】


【公表番号】特表2011−520429(P2011−520429A)
【公表日】平成23年7月21日(2011.7.21)
【国際特許分類】
【出願番号】特願2011−506626(P2011−506626)
【出願日】平成21年3月12日(2009.3.12)
【国際出願番号】PCT/EP2009/052936
【国際公開番号】WO2009/132888
【国際公開日】平成21年11月5日(2009.11.5)
【出願人】(599132904)ネステク ソシエテ アノニム (637)
【Fターム(参考)】
【公表日】平成23年7月21日(2011.7.21)
【国際特許分類】
【出願日】平成21年3月12日(2009.3.12)
【国際出願番号】PCT/EP2009/052936
【国際公開番号】WO2009/132888
【国際公開日】平成21年11月5日(2009.11.5)
【出願人】(599132904)ネステク ソシエテ アノニム (637)
【Fターム(参考)】
[ Back to top ]

