サイトカインの検出方法、サイトカイン感受性細胞株及びサイトカイン産生細胞のスクリーニング方法
【課題】被検試料中の単数又は複数のサイトカインを効率よく確実に検出する。
【解決手段】DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株、好ましくは、受託番号FERM P−20652の細胞株を、被検試料中で培養する培養工程、前記細胞株の増殖に基づいて、サイトカインを検出する検出工程を含む方法によって、被検試料中のサイトカインを検出し、又はサイトカインを産生するサイトカイン産生細胞をスクリーニングする。
【解決手段】DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株、好ましくは、受託番号FERM P−20652の細胞株を、被検試料中で培養する培養工程、前記細胞株の増殖に基づいて、サイトカインを検出する検出工程を含む方法によって、被検試料中のサイトカインを検出し、又はサイトカインを産生するサイトカイン産生細胞をスクリーニングする。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、サイトカインの検出方法、サイトカイン感受性細胞株及びサイトカイン産生細胞のスクリーニング方法に関し、特に、被検試料中のサイトカインを検出するための検出方法及びこの検出方法に使用可能なサイトカイン感受性細胞株、並びにサイトカイン産生細胞のスクリーニング方法に関する。
【背景技術】
【0002】
各種細胞の分化及び増殖には、細胞が産生する各種サイトカインが大きく影響していることはよく知られている。このようなサイトカインには、インターフェロン(IFN)、各種インターロイキン(IL)、各種成長因子(GF)などを挙げることができる。
これらのサイトカインは、生体において多くの疾患とも関連性が深く、疾患の発症機序や治療剤の開発における研究ツール及び候補化合物としても注目されている。また、前述のように多くのサイトカインが見いだされているが、未知のサイトカインも多く存在していると思われ、これら未知のサイトカインの検出及び同定も、今後の研究、ひいては各種疾患の治療剤開発に重要である。
現在、サイトカインの検出には、例えば、細胞培養液を濃縮してタンパク質レベルで検出する方法や、既知のサイトカイン感受性細胞の増殖速度を比較する方法、既知のサイトカイン検出用抗体を利用する方法などによって行われている(例えば、特許文献1及び2)。
【特許文献1】特開平5−276986号公報
【特許文献2】特開2004−279429号公報
【発明の開示】
【発明が解決しようとする課題】
【0003】
しかしながら、特定のサイトカインのみを検出するには、そのサイトカインに対して感受性の高い細胞株等を用いて検出すればよいが、存在するサイトカインの種類が不明である場合や、複数種のサイトカインが混在していることもある。また、サイトカインがごく微量に存在している場合には、細胞自身の作用であるのかサイトカインによる影響なのかを正確に識別する必要がある。
従って、本発明の目的は、被検試料中の単数又は複数のサイトカインを効率よく確実に検出すること又は、そのようなサイトカインを産生する産生細胞を効率よくスクリーニングすることである。
【課題を解決するための手段】
【0004】
本発明のサイトカイン検出方法は、被検試料中のサイトカインを検出する方法において、DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株を、前記被検試料中で培養する培養工程、前記細胞株の増殖に基づいて、サイトカインを検出する検出工程を含むことを特徴としている。
本発明のサイトカイン産生細胞のスクリーニング方法は、被検細胞を培養して、被検培養上清を調製する調製工程、DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株を、前記被検培養上清を含有する培養液中で培養する培養工程、前記細胞株の増殖に基づいて、前記被検細胞からサイトカイン産生細胞を選定する選定工程、を含むことを特徴としている。
本発明の細胞株は、受託番号FERM P−20652の細胞株である。
本発明のサイトカインは、受託番号FERM P−20652の細胞株を用いて検出されたものである。
本発明のサイトカイン産生細胞は、受託番号FERM P−20652の細胞株用いて得られたものである。
【0005】
本発明では、DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株、特に受託番号FERM P−20652株を用いている。この細胞株は、複数種のサイトカインに対して感受性を有しているので、被検試料中に含有されるサイトカイン又は産生されるサイトカインの数や種類が不明であっても、広いレンジで被検試料中に含有されるサイトカインを検出することができ、又はサイトカイン産生細胞を効率よくスクリーニングすることができる。
【発明の効果】
【0006】
本発明によれば、被検試料中の単数又は複数のサイトカインを効率よく確実に検出することができ、又はそのようなサイトカインを産生する産生細胞を効率よくスクリーニングすることができる。
【発明を実施するための最良の形態】
【0007】
本発明のサイトカイン検出方法は、被検試料中のサイトカインを検出する方法において、DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株(以下、「単に好塩基球様ないしマスト細胞様細胞株」という)を、前記被検試料中で培養する培養工程、前記細胞株の増殖に基づいてサイトカインを検出する検出工程を含む。
【0008】
本発明にかかる好塩基球様ないしマスト細胞様細胞株は、複数種のサイトカインに対して感受性を有するものである。このような細胞株を用いることによって、被検試料中に含まれるサイトカインの数や種類が不明であっても、広いレンジで確実にサイトカインを検出することができる。
本発明にかかる好塩基球様ないしマスト細胞様細胞株は、DO11.10トランスジェニックマウスの脾臓細胞を卵白アルブミン(OVA抗原ペプチド)で刺激しながら誘導して得られた好塩基球様ないしマスト細胞様細胞株である。本好塩基球様ないしマスト細胞様細胞株を得るために用いられるOVA抗原ペプチドとしては、323番目−339番目のアミノ酸残基で構成されたものを挙げることができる。
これらの細胞株のうち、更に、R細胞(独立行政法人産業技術総合研究所特許生物寄託センター 受託番号 FERM P−20652、2005年9月1日付で受領)が感受性の高さ及び感受性を示すサイトカインの種類の観点から特に好ましい。
【0009】
本発明の好塩基球様ないしマスト細胞様細胞株は、好塩基球に特徴的な形態とマスト細胞に特徴的な形態との双方を兼ね備えた細胞株である。
例えばR細胞は、光学又は電子顕微鏡観察による形態観察では、顆粒密度の低い嚢胞状構造やトルイジンブルー(TB)染色では染まらない点で好塩基球様の形態を示し(図1参照)、細胞表面分子の解析では、c−kit、FcεRIαが共に陽性というマスト細胞様の形態を示すことが確認されている。このようにR細胞は、好塩基球に似た形態とマスト細胞に似た形態とを共に示しており、好塩基球様ないしマスト細胞様細胞株であると言える。
R細胞は、DO11.10 T細胞株の培養上清又はIL−3による刺激により維持することができるが、特徴的な活性を良好に維持できる観点からDO11.10細胞株の培養上清により維持することが好ましい。
【0010】
また、R細胞の維持条件としては、OVA抗原ペプチド刺激T細胞との共培養を挙げることができる。
共培養に用いられるT細胞は、表面マーカーCD4+CD8−のヘルパーT細胞であればよく、その起源としては、哺乳類、特に齧歯類を挙げることができ、好ましくはマウス、特に好ましくは、同一の遺伝的系統を有するマウスである。この用途に用いられるT細胞は、上記条件のものであればいずれのものであってもよいが、R細胞を確立するために使用した親細胞であり、DO11.10のTCRトランスジェニックマウスの脾臓細胞中のT細胞(以下、同系T細胞という)であることが特に好ましい。
共培養中でのOVA抗原ペプチドの濃度は、100nM〜1000nMとすることができ、100〜300nMであることが好ましい。
更に、ヘルパーT細胞のTCRの刺激を行うことによって得られたTCR刺激T細胞との共培養でも、同様にR細胞を維持及び増殖させることができる。
【0011】
R細胞の維持条件としては、細胞の操作及び単離の観点から、上記細胞の培養上清を含有する培養液を用いることが好ましい。
OVA抗原ペプチド刺激T細胞の培養上清又はTCR刺激T細胞の培養上清は、R細胞用培養液中に含有してあればよく、R細胞の状態に応じて適宜変更することができるが、好ましくは0.01容量%〜10容量%、特に0.01容量%〜0.5容量%とすることができる。
また、OVA抗原ペプチド刺激T細胞の培養上清の代わりにIL−3含有培地を用いる場合、培養液中に含まれるIL−3は、R細胞の状態に応じて適宜設定可能であるが、例えば約5ng/mlの濃度であればR細胞を維持・増殖させることができる。
【0012】
R細胞は、複数のサイトカインに対して高い感受性を有しており、中でもTh2型サイトカインを中心とするIL−3、IL−4、IL−5、IL−6、IL−9、IL−13、IL−15などのインターロイキンに対して増殖能を示し、このうち、IL−3、IL−4、IL−5、IL−6、IL−9、IL−13、特にIL−3、IL−4、IL−9に対して高い増殖能を示す。ただし、IL−2、IL−7、IL−10、GM−CFSやIFN−γに対しては感受性を示さない。
これらのサイトカインに対する感受性は、対応する周知のサイトカイン感受性細胞、例えばMC−9(IL−3)、CT.4S(IL−4)による感受性試験(それぞれ20pg/ml以上:ELISA)よりも高い。例えばIL−3に対しては1〜50pg/ml、IL−4に対しては10〜1000pg/mlの範囲でそれぞれ検出可能である。
【0013】
特に、R細胞は20〜200pg/mlのIL−9を確実に検出することができる。IL−9は、マスト細胞の増殖活性を増強する因子として知られ、アレルギー反応を促進する重要なサイトカインであるにも拘わらず、これまでIL−9を高い感度で検出可能な細胞株は得られてない。このため、IL−9を精度よく検出するにはELISAや抗体を用いなければならなかった。しかしながら、本発明のR細胞を用いることによって、細胞を用いた高い精度の検出が可能になった。
【0014】
本発明のサイトカイン検出方法における培養工程では、検出対象となる被検試料の存在下で上記細胞株の培養が行われる。サイトカインの含有が疑われる各種液体試料、例えば、緩衝液、培養液、培養上清等を挙げることができ、サイトカイン産生細胞の検出を行う場合には、被検細胞の培養上清(特定試薬による刺激実験後の上清を含む)であってもよい。
被検試料が被検細胞の培養上清であるので、被検試料のみを用いて上記細胞株を培養することができる。この場合には、被検試料を希釈せずに被検試料中のサイトカインを検出することができるため、好ましい。
【0015】
また、上述の培養上清は、マスト細胞及び好塩基球系細胞株の培養に通常用いられる培養液に添加して検出対象としてもよい。マスト細胞及び好塩基球系細胞株の培養に通常用いられる培養液には、例えば、ダルベッコ改変イーグル培地(DMEM)や、RPMI1640などを挙げることができる。これらの培養液に対しては、通常、血清、各種ビタミン、各種抗生物質等、通常の細胞培養に適用可能な各種添加剤を添加してもよい。
【0016】
培養温度及び湿度などの培養条件は、一般的なマスト細胞又は好塩基球系細胞株に対して用いられる培養条件をそのまま適用することができる。また、培養工程の前に細胞株に対して前培養を行ってもよい。
培養期間は、細胞株の種類や状態によって異なるが、一般に、2日〜7日、好ましくは3〜5日とすることができる。
【0017】
サイトカインの有無は、上記細胞株の増殖に基づいて検出される。
細胞株の増殖の速度は、通常、この目的のために用いられている各種の手段をそのまま適用することができ、例えば、目視又は顕微鏡による血球計算盤等を用いた細胞数の計測、放射性同位元素(例えば、3H−チミジン)の取り込み量などを挙げることができる。
【0018】
本発明のサイトカイン検出方法は、同時にサイトカイン産生細胞のスクリーニング方法としても利用することができる。この場合、被検細胞を培養して、被検試料を調製する調製工程、上記本発明の好塩基球様ないしマスト細胞様細胞株を、前記被検試料を含有する培養液中で培養する培養工程、前記細胞株の増殖に基づいて、前記被検細胞からサイトカイン産生細胞を選定する選定工程、を含むものであることが、効果的なスクリーニングを行うことができるため、好ましい。
本発明のスクリーニング方法におけるDO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株、培養工程などについては、前述した事項をそのまま適用することができる。
【0019】
調製工程では、被検細胞を培養して、上述の被検試料が調製される。被検細胞としては、サイトカインを産生する可能性がある細胞であればいずれであってもよく、例えばT細胞、マクロファージ、好塩基球細胞、好酸球細胞、単球、マスト細胞等を挙げることができる。
被検試料としては、上記被検細胞を培養して得られた培養上清の他、前述したものが挙げられる。
選定工程では、被検細胞の増殖に基づいてサイトカイン産生細胞を選択することができる。この増殖については前述した事項をそのまま適用することができる。
【0020】
また、本スクリーニング方法では、既知のサイトカイン、例えば、IL−3、IL−4、IL−5、IL−6、IL−9及びIL−13からなる群より選択された少なくとも1つのサイトカインを産生する細胞をスクリーニングするものであってもよいが、未知のサイトカインを産生する細胞をスクリーニングするものであってもよい。
未知のサイトカインを産生する細胞をスクリーニングする場合には、既知のサイトカインに感受性を有する感受性細胞株を用いる。これらの既知の感受性細胞株のいずれも増殖能を示さない被検試料を得る工程と、この被検試料を含有する培養液中で、本発明における好塩基球様ないしマスト細胞様細胞株、好ましくはR細胞を培養する工程と、細胞株の増殖に基づいて未知のサイトカインを含有する試験試料から、サイトカイン産生細胞を選定する工程とを含む。
これにより、未知のサイトカインを産生するサイトカイン産生細胞を容易にスクリーニングすることができる。
【0021】
本発明の好塩基球様ないしマスト細胞様細胞株が反応する既知のサイトカインについては、本細胞株を用いたスクリーニングの後に、被検試料を濃縮するなどした後にELISA法などの既知の方法を用いて定量及び/又は定性を行う。このような方法で、既知のサイトカインの存在が証明できない場合には、新たなサイトカインの存在の可能性が示唆される。このような可能性は、既知のサイトカイン中和抗体を、本発明の好塩基球様ないしマスト細胞様細胞株を用いた系に充分加えても試験試料中に本発明の好塩基球様ないしマスト細胞様細胞株の増殖性が認められる場合にも同様である。
【0022】
本発明によって検出可能なサイトカインは、天然由来のものであってもよく、リコンビナントによって得たものであってもよい。また、マウス由来のものであってもよく、ヒト由来のものであっても、感受性を示すことができる。
本発明では、本発明にかかる好塩基球様ないしマスト細胞様細胞株は複数のサイトカインに高い感受性を有するので、サイトカインの数及び量が不明な被検試料に対するサイトカインを効率よく検出する場合に好適に使用することができる。
【実施例】
【0023】
以下に本発明の実施例について説明するが、これに限定されるものではない。また実施例中の%は、特に断らない限り、重量(質量)基準である。
【0024】
[実施例1]
R細胞の作製
10週齢のメスDO11.10トランスジェニックマウス(米国ワシントン大学、Ken Murphy教授より供与)から脾臓細胞を摘出し、RPMI培地(10容量%FCS、ペニシリンGカリウム100U/ml、硫酸ストレプトマイシン100mg/ml添加:以下、単に10%血清含有培地という)にOVA抗原ペプチド(ニワトリOVA(cOVA)323−339 ペプチド:ISQAVHAAHAEINEAGR:配列番号1)を1000nM又は250mMの最終濃度となるように添加した培養条件下で培養した。
得られた培養物から、OVA抗原ペプチド反応性を示すT細胞を得た。このT細胞を抗CD3抗体で刺激しながら培養して、培養上清(R細胞増殖因子含有液:RCGF)を得た。以下、RCGFを培養に用いる際には、2日間培養して得たRCGFを0.5容量%の濃度で新規培地と混合して使用した。
【0025】
また、得られた培養物に、抗Thy1.2抗体(Pharmingen社製)と補体(ウサギ血清、Pel-Freeze社製)をそれぞれ1μg/ml及び最終10容量%の濃度で1×107個/100μLの細胞に対して添加して、約30分間反応させ、T細胞を除去し、上記RCGFを添加しながら培養を継続して、R細胞を得た。
R細胞は、0.5容量%のRCGFを含有する10容量%血清含有RPMI培地(又は5ng/mlのIL−3を含有するR細胞用培地)を用いて、37℃、5%CO2で培養し、維持した。R細胞は、培養環境からRCGF及びT細胞を除去すると、死滅した。
【0026】
[実施例2]
R細胞の特徴解析
上記のようにして得られたR細胞(受託番号FERM P−20652)に対して各種抗体を用いた表面抗原解析を行った。
蛍光色素(FITC)結合抗体として、抗マウスc−kit抗体(e-Bio社製)、抗マウスFcεRI抗体(e-Bio社製)、抗マウスB220抗体(e-Bio社製)、抗マウスCD3抗体(e-Bio社製)、抗マウスFcγRII/III抗体(Pharmingen社製)、抗ClassI抗体(Pharmingen社製)、抗マウスDX5抗体(e-Bio社製)、抗ClassII抗体(Pharmingen社製)を使用し、それぞれ約5〜10μgをR細胞1×106/100μL対して氷上で30分間反応させた。抗体の結合状態は、FACSを用いて解析した。
その結果、R細胞は、FcεRIα、FcγRII/III、c−kit、ClassIは陽性、CD3、B220、DX5、ClassIIは陰性であることがわかった。
【0027】
また光学顕微鏡及び電子顕微鏡を用いて形態観察を行った(図1及び2)。ヘマトキシリン・エオジン染色(HE染色)では、R細胞の細胞質はピンクに染色された。細胞質内には多数の顆粒が詰まっているが、その一部は空胞状顆粒構造を示している(図1(A)参照、矢印)。また、トルイジンブルー染色(TB染色)では、マスト細胞(図1(C)参照)と異なり染色されなかった(図1(B)参照。矢印は空胞構造を示す)。
また図2(A)に示されるように、電子顕微鏡像では、細胞質に多数の嚢胞状構造(矢印)をもち、その内部には、好塩基球(図2(B)参照)と同様に粒状構造物を含んでいた。また、粒状構造物はやや大型であるが、マスト細胞に見られるような指紋状・渦巻状構造(図2(C)参照。矢印)は認められなかった。細胞質内に多数の顆粒が詰まっているが、一部は空胞に抜けており(空胞状顆粒構造)、高密度の粒状構造を有するマスト細胞とは異なっていた。
これらのことから、R細胞は好塩基球様ないしマスト細胞様細胞株であることが示された。
【0028】
[実施例3]
R細胞のサイトカイン感受性実験
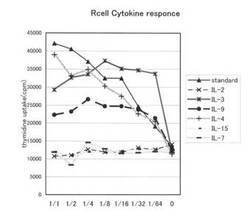
96ウェルマイクロプレートの各ウェルに、1×103個/ウェルの播種密度でR細胞を配置し、各種リコンビナントサイトカイン(IL−2[PeproTech社製]、IL−3[PeproTech社製]、IL−4[PeproTech社製]、IL−7[PeproTech社製]、IL−9[PeproTech社製]、IL−15[PeproTech社製])又は、スタンダードとしてRCGFをそれぞれ含有する培地(サイトカインの量は、50pg/mlからの1/2段階的希釈。RCGFは、0.5容量%含有培地からの1/2段階的希釈)を各ウェルに添加して、37℃、5%CO2の環境下で48時間培養した。培地には、3H−チミジンが含まれており、常法に従って、3Hの取り込み量を測定した。
【0029】
図3に示されるように、R細胞は、被検サイトカインのうち、IL−3、IL−4及びIL−9に対して反応を示した。このうちIL−4に対する反応性は濃度依存的であったが、IL−3及びIL−9に対する反応性は、極微量(64倍希釈)であって安定した反応性を示した。また、IL−3に対するR細胞の感受性が特に高いことが示された。
従って、R細胞を用いることによって、培養液中に存在するサイトカインを効率よく検出することができ、またIL−3の検出については、特に高い感度で検出できることは明らかであった。
なお、R細胞は、pgオーダーのIL−15に対しては上記のように反応性を示さなかったが、それよりも濃い場合、例えば100ng/mlの濃度のIL−15に対しては感受性を示した。
【0030】
[実施例4]
R細胞のIL−3に対する反応性
リコンビナントIL−3(カタログ#14−8031、eBioScience社製)を、0pg/ml、1pg/ml、5pg/ml、10pg/ml、20pg/ml、50pg/ml、200pg/ml及び500pg/mlの各濃度に調整した培地に20μCuの3H−チミジンを含有させて、1×104個/ウェルのR細胞を、37℃8〜12時間、インキュベートした。反応後3H−チミジンの取り込み量をMicroBeta TRILUX(WALLAC社製)を用いて測定した。結果を図4に示す。
図4に示されるように、R細胞は、1pg/mlからIL−3の刺激に応答して増殖能を示し、高い感度を有することが示された。
【0031】
[実施例5]
T細胞培養上清中のサイトカインの検出
反応性T細胞の培養上清中のサイトカインを、R細胞及びCTLL−2を用いて検出した。
反応性T細胞は、DO11.10の脾臓細胞を、抗原提示細胞と1000nMのOVA抗原ペプチドの存在下で1週間培養した後、培養細胞から死細胞を取り除いて調製した。抗原提示細胞としては、10週齢のBALB/cマウスから単離されると共に放射線照射により増殖不能化された脾細胞を使用した。
上記のようにして調製された反応性T細胞2×104個/ウェルを、上記と同様にして調製した抗原提示細胞5×105個/ウェルと、OVA抗原ペプチド(1000nM、250nM、62.5nM、12.5nM)とを含有する培地100μL中で37℃48時間培養し、培養上清を採取した。
この培養上清を、1×104個/ウェルのR細胞又は1×104個/ウェルのCTLL−2に、最終濃度10容量%で加えて36時間反応させた。それぞれ培地には3H−チミジンが0.5μCuの濃度で含有されており、反応後、常法に従って3H−チミジンの取り込み量を測定した。コントロールとして、培養上清後の上記反応性T細胞(2×104個/ウェル)に3H−チミジンを同量で添加して、反応性T細胞の増殖反応を同様に測定した。結果を図5にそれぞれ示す。
【0032】
その結果、T細胞培養上清中のサイトカインは、R細胞の増殖に基づいて精度よく容易に検出できることが示された(図5参照)。特に、10nMの抗原ペプチド濃度で刺激した培養上清であっても高い増殖能を示しているので、精度よく検出できることは明らかである。また、このT細胞培養上清には、どのようなサイトカインが存在しているか未確認であるが、R細胞が複数のサイトカインに対して感受性を有しているため、広いレンジで効率よく検出できることも明らかである。
一方、CTLL−2は、IL−2に対しては高い感受性を有しているが、IL−2以外のサイトカインにはほとんど反応しないため、IL−2が培養上清中になければ増殖することができない。このため、本実施例では、培養上清中に全くサイトカインが存在しないのか、IL−2のみが存在しないのか、を判断することができない。
また、反応性T細胞は、培養上清中のサイトカインに対して反応性を示していたが、250nM未満の濃度では増殖能が低く、精度よく検出することができない。
【0033】
このように本発明にかかるR細胞は、微量なサイトカインに対して高い感度を有すると共に複数のサイトカインに対して感受性を有するので、被検試料中のサイトカインに検出を効率よく行うことができる。
また、このようなR細胞による検出と、既存のサイトカイン検出用細胞株による検出を組み合わせることによって、より一層効率よく被検試料中のサイトカインを検出することができると共に、既存のサイトカイン検出用細胞株のいずれを用いても反応性を示さない被検試料に対してR細胞を反応させることによって、未知のサイトカインを検出することも可能である。
【図面の簡単な説明】
【0034】
【図1】(A)は本発明にかかるR細胞のHE染色像、(B)は本発明にかかるR細胞のTB染色像、(C)はマスト細胞のTB染色像である。
【図2】(A)は本発明にかかるR細胞の電子顕微鏡写真像、(B)は好塩基球の電子顕微鏡写真像、(C)はマスト細胞の電子顕微鏡写真像である。
【図3】本発明の実施例にかかるR細胞の各種サイトカインに対する反応性を示すグラフである。
【図4】本発明の実施例にかかるR細胞のIL−3に対する反応性を示すグラフである。
【図5】本発明の実施例にかかる抗原刺激T細胞培養上清に対するR細胞(白丸)、CTLL−2(黒丸)及び反応性T細胞(白三角)の反応性を示すグラフである。
【技術分野】
【0001】
本発明は、サイトカインの検出方法、サイトカイン感受性細胞株及びサイトカイン産生細胞のスクリーニング方法に関し、特に、被検試料中のサイトカインを検出するための検出方法及びこの検出方法に使用可能なサイトカイン感受性細胞株、並びにサイトカイン産生細胞のスクリーニング方法に関する。
【背景技術】
【0002】
各種細胞の分化及び増殖には、細胞が産生する各種サイトカインが大きく影響していることはよく知られている。このようなサイトカインには、インターフェロン(IFN)、各種インターロイキン(IL)、各種成長因子(GF)などを挙げることができる。
これらのサイトカインは、生体において多くの疾患とも関連性が深く、疾患の発症機序や治療剤の開発における研究ツール及び候補化合物としても注目されている。また、前述のように多くのサイトカインが見いだされているが、未知のサイトカインも多く存在していると思われ、これら未知のサイトカインの検出及び同定も、今後の研究、ひいては各種疾患の治療剤開発に重要である。
現在、サイトカインの検出には、例えば、細胞培養液を濃縮してタンパク質レベルで検出する方法や、既知のサイトカイン感受性細胞の増殖速度を比較する方法、既知のサイトカイン検出用抗体を利用する方法などによって行われている(例えば、特許文献1及び2)。
【特許文献1】特開平5−276986号公報
【特許文献2】特開2004−279429号公報
【発明の開示】
【発明が解決しようとする課題】
【0003】
しかしながら、特定のサイトカインのみを検出するには、そのサイトカインに対して感受性の高い細胞株等を用いて検出すればよいが、存在するサイトカインの種類が不明である場合や、複数種のサイトカインが混在していることもある。また、サイトカインがごく微量に存在している場合には、細胞自身の作用であるのかサイトカインによる影響なのかを正確に識別する必要がある。
従って、本発明の目的は、被検試料中の単数又は複数のサイトカインを効率よく確実に検出すること又は、そのようなサイトカインを産生する産生細胞を効率よくスクリーニングすることである。
【課題を解決するための手段】
【0004】
本発明のサイトカイン検出方法は、被検試料中のサイトカインを検出する方法において、DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株を、前記被検試料中で培養する培養工程、前記細胞株の増殖に基づいて、サイトカインを検出する検出工程を含むことを特徴としている。
本発明のサイトカイン産生細胞のスクリーニング方法は、被検細胞を培養して、被検培養上清を調製する調製工程、DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株を、前記被検培養上清を含有する培養液中で培養する培養工程、前記細胞株の増殖に基づいて、前記被検細胞からサイトカイン産生細胞を選定する選定工程、を含むことを特徴としている。
本発明の細胞株は、受託番号FERM P−20652の細胞株である。
本発明のサイトカインは、受託番号FERM P−20652の細胞株を用いて検出されたものである。
本発明のサイトカイン産生細胞は、受託番号FERM P−20652の細胞株用いて得られたものである。
【0005】
本発明では、DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株、特に受託番号FERM P−20652株を用いている。この細胞株は、複数種のサイトカインに対して感受性を有しているので、被検試料中に含有されるサイトカイン又は産生されるサイトカインの数や種類が不明であっても、広いレンジで被検試料中に含有されるサイトカインを検出することができ、又はサイトカイン産生細胞を効率よくスクリーニングすることができる。
【発明の効果】
【0006】
本発明によれば、被検試料中の単数又は複数のサイトカインを効率よく確実に検出することができ、又はそのようなサイトカインを産生する産生細胞を効率よくスクリーニングすることができる。
【発明を実施するための最良の形態】
【0007】
本発明のサイトカイン検出方法は、被検試料中のサイトカインを検出する方法において、DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株(以下、「単に好塩基球様ないしマスト細胞様細胞株」という)を、前記被検試料中で培養する培養工程、前記細胞株の増殖に基づいてサイトカインを検出する検出工程を含む。
【0008】
本発明にかかる好塩基球様ないしマスト細胞様細胞株は、複数種のサイトカインに対して感受性を有するものである。このような細胞株を用いることによって、被検試料中に含まれるサイトカインの数や種類が不明であっても、広いレンジで確実にサイトカインを検出することができる。
本発明にかかる好塩基球様ないしマスト細胞様細胞株は、DO11.10トランスジェニックマウスの脾臓細胞を卵白アルブミン(OVA抗原ペプチド)で刺激しながら誘導して得られた好塩基球様ないしマスト細胞様細胞株である。本好塩基球様ないしマスト細胞様細胞株を得るために用いられるOVA抗原ペプチドとしては、323番目−339番目のアミノ酸残基で構成されたものを挙げることができる。
これらの細胞株のうち、更に、R細胞(独立行政法人産業技術総合研究所特許生物寄託センター 受託番号 FERM P−20652、2005年9月1日付で受領)が感受性の高さ及び感受性を示すサイトカインの種類の観点から特に好ましい。
【0009】
本発明の好塩基球様ないしマスト細胞様細胞株は、好塩基球に特徴的な形態とマスト細胞に特徴的な形態との双方を兼ね備えた細胞株である。
例えばR細胞は、光学又は電子顕微鏡観察による形態観察では、顆粒密度の低い嚢胞状構造やトルイジンブルー(TB)染色では染まらない点で好塩基球様の形態を示し(図1参照)、細胞表面分子の解析では、c−kit、FcεRIαが共に陽性というマスト細胞様の形態を示すことが確認されている。このようにR細胞は、好塩基球に似た形態とマスト細胞に似た形態とを共に示しており、好塩基球様ないしマスト細胞様細胞株であると言える。
R細胞は、DO11.10 T細胞株の培養上清又はIL−3による刺激により維持することができるが、特徴的な活性を良好に維持できる観点からDO11.10細胞株の培養上清により維持することが好ましい。
【0010】
また、R細胞の維持条件としては、OVA抗原ペプチド刺激T細胞との共培養を挙げることができる。
共培養に用いられるT細胞は、表面マーカーCD4+CD8−のヘルパーT細胞であればよく、その起源としては、哺乳類、特に齧歯類を挙げることができ、好ましくはマウス、特に好ましくは、同一の遺伝的系統を有するマウスである。この用途に用いられるT細胞は、上記条件のものであればいずれのものであってもよいが、R細胞を確立するために使用した親細胞であり、DO11.10のTCRトランスジェニックマウスの脾臓細胞中のT細胞(以下、同系T細胞という)であることが特に好ましい。
共培養中でのOVA抗原ペプチドの濃度は、100nM〜1000nMとすることができ、100〜300nMであることが好ましい。
更に、ヘルパーT細胞のTCRの刺激を行うことによって得られたTCR刺激T細胞との共培養でも、同様にR細胞を維持及び増殖させることができる。
【0011】
R細胞の維持条件としては、細胞の操作及び単離の観点から、上記細胞の培養上清を含有する培養液を用いることが好ましい。
OVA抗原ペプチド刺激T細胞の培養上清又はTCR刺激T細胞の培養上清は、R細胞用培養液中に含有してあればよく、R細胞の状態に応じて適宜変更することができるが、好ましくは0.01容量%〜10容量%、特に0.01容量%〜0.5容量%とすることができる。
また、OVA抗原ペプチド刺激T細胞の培養上清の代わりにIL−3含有培地を用いる場合、培養液中に含まれるIL−3は、R細胞の状態に応じて適宜設定可能であるが、例えば約5ng/mlの濃度であればR細胞を維持・増殖させることができる。
【0012】
R細胞は、複数のサイトカインに対して高い感受性を有しており、中でもTh2型サイトカインを中心とするIL−3、IL−4、IL−5、IL−6、IL−9、IL−13、IL−15などのインターロイキンに対して増殖能を示し、このうち、IL−3、IL−4、IL−5、IL−6、IL−9、IL−13、特にIL−3、IL−4、IL−9に対して高い増殖能を示す。ただし、IL−2、IL−7、IL−10、GM−CFSやIFN−γに対しては感受性を示さない。
これらのサイトカインに対する感受性は、対応する周知のサイトカイン感受性細胞、例えばMC−9(IL−3)、CT.4S(IL−4)による感受性試験(それぞれ20pg/ml以上:ELISA)よりも高い。例えばIL−3に対しては1〜50pg/ml、IL−4に対しては10〜1000pg/mlの範囲でそれぞれ検出可能である。
【0013】
特に、R細胞は20〜200pg/mlのIL−9を確実に検出することができる。IL−9は、マスト細胞の増殖活性を増強する因子として知られ、アレルギー反応を促進する重要なサイトカインであるにも拘わらず、これまでIL−9を高い感度で検出可能な細胞株は得られてない。このため、IL−9を精度よく検出するにはELISAや抗体を用いなければならなかった。しかしながら、本発明のR細胞を用いることによって、細胞を用いた高い精度の検出が可能になった。
【0014】
本発明のサイトカイン検出方法における培養工程では、検出対象となる被検試料の存在下で上記細胞株の培養が行われる。サイトカインの含有が疑われる各種液体試料、例えば、緩衝液、培養液、培養上清等を挙げることができ、サイトカイン産生細胞の検出を行う場合には、被検細胞の培養上清(特定試薬による刺激実験後の上清を含む)であってもよい。
被検試料が被検細胞の培養上清であるので、被検試料のみを用いて上記細胞株を培養することができる。この場合には、被検試料を希釈せずに被検試料中のサイトカインを検出することができるため、好ましい。
【0015】
また、上述の培養上清は、マスト細胞及び好塩基球系細胞株の培養に通常用いられる培養液に添加して検出対象としてもよい。マスト細胞及び好塩基球系細胞株の培養に通常用いられる培養液には、例えば、ダルベッコ改変イーグル培地(DMEM)や、RPMI1640などを挙げることができる。これらの培養液に対しては、通常、血清、各種ビタミン、各種抗生物質等、通常の細胞培養に適用可能な各種添加剤を添加してもよい。
【0016】
培養温度及び湿度などの培養条件は、一般的なマスト細胞又は好塩基球系細胞株に対して用いられる培養条件をそのまま適用することができる。また、培養工程の前に細胞株に対して前培養を行ってもよい。
培養期間は、細胞株の種類や状態によって異なるが、一般に、2日〜7日、好ましくは3〜5日とすることができる。
【0017】
サイトカインの有無は、上記細胞株の増殖に基づいて検出される。
細胞株の増殖の速度は、通常、この目的のために用いられている各種の手段をそのまま適用することができ、例えば、目視又は顕微鏡による血球計算盤等を用いた細胞数の計測、放射性同位元素(例えば、3H−チミジン)の取り込み量などを挙げることができる。
【0018】
本発明のサイトカイン検出方法は、同時にサイトカイン産生細胞のスクリーニング方法としても利用することができる。この場合、被検細胞を培養して、被検試料を調製する調製工程、上記本発明の好塩基球様ないしマスト細胞様細胞株を、前記被検試料を含有する培養液中で培養する培養工程、前記細胞株の増殖に基づいて、前記被検細胞からサイトカイン産生細胞を選定する選定工程、を含むものであることが、効果的なスクリーニングを行うことができるため、好ましい。
本発明のスクリーニング方法におけるDO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株、培養工程などについては、前述した事項をそのまま適用することができる。
【0019】
調製工程では、被検細胞を培養して、上述の被検試料が調製される。被検細胞としては、サイトカインを産生する可能性がある細胞であればいずれであってもよく、例えばT細胞、マクロファージ、好塩基球細胞、好酸球細胞、単球、マスト細胞等を挙げることができる。
被検試料としては、上記被検細胞を培養して得られた培養上清の他、前述したものが挙げられる。
選定工程では、被検細胞の増殖に基づいてサイトカイン産生細胞を選択することができる。この増殖については前述した事項をそのまま適用することができる。
【0020】
また、本スクリーニング方法では、既知のサイトカイン、例えば、IL−3、IL−4、IL−5、IL−6、IL−9及びIL−13からなる群より選択された少なくとも1つのサイトカインを産生する細胞をスクリーニングするものであってもよいが、未知のサイトカインを産生する細胞をスクリーニングするものであってもよい。
未知のサイトカインを産生する細胞をスクリーニングする場合には、既知のサイトカインに感受性を有する感受性細胞株を用いる。これらの既知の感受性細胞株のいずれも増殖能を示さない被検試料を得る工程と、この被検試料を含有する培養液中で、本発明における好塩基球様ないしマスト細胞様細胞株、好ましくはR細胞を培養する工程と、細胞株の増殖に基づいて未知のサイトカインを含有する試験試料から、サイトカイン産生細胞を選定する工程とを含む。
これにより、未知のサイトカインを産生するサイトカイン産生細胞を容易にスクリーニングすることができる。
【0021】
本発明の好塩基球様ないしマスト細胞様細胞株が反応する既知のサイトカインについては、本細胞株を用いたスクリーニングの後に、被検試料を濃縮するなどした後にELISA法などの既知の方法を用いて定量及び/又は定性を行う。このような方法で、既知のサイトカインの存在が証明できない場合には、新たなサイトカインの存在の可能性が示唆される。このような可能性は、既知のサイトカイン中和抗体を、本発明の好塩基球様ないしマスト細胞様細胞株を用いた系に充分加えても試験試料中に本発明の好塩基球様ないしマスト細胞様細胞株の増殖性が認められる場合にも同様である。
【0022】
本発明によって検出可能なサイトカインは、天然由来のものであってもよく、リコンビナントによって得たものであってもよい。また、マウス由来のものであってもよく、ヒト由来のものであっても、感受性を示すことができる。
本発明では、本発明にかかる好塩基球様ないしマスト細胞様細胞株は複数のサイトカインに高い感受性を有するので、サイトカインの数及び量が不明な被検試料に対するサイトカインを効率よく検出する場合に好適に使用することができる。
【実施例】
【0023】
以下に本発明の実施例について説明するが、これに限定されるものではない。また実施例中の%は、特に断らない限り、重量(質量)基準である。
【0024】
[実施例1]
R細胞の作製
10週齢のメスDO11.10トランスジェニックマウス(米国ワシントン大学、Ken Murphy教授より供与)から脾臓細胞を摘出し、RPMI培地(10容量%FCS、ペニシリンGカリウム100U/ml、硫酸ストレプトマイシン100mg/ml添加:以下、単に10%血清含有培地という)にOVA抗原ペプチド(ニワトリOVA(cOVA)323−339 ペプチド:ISQAVHAAHAEINEAGR:配列番号1)を1000nM又は250mMの最終濃度となるように添加した培養条件下で培養した。
得られた培養物から、OVA抗原ペプチド反応性を示すT細胞を得た。このT細胞を抗CD3抗体で刺激しながら培養して、培養上清(R細胞増殖因子含有液:RCGF)を得た。以下、RCGFを培養に用いる際には、2日間培養して得たRCGFを0.5容量%の濃度で新規培地と混合して使用した。
【0025】
また、得られた培養物に、抗Thy1.2抗体(Pharmingen社製)と補体(ウサギ血清、Pel-Freeze社製)をそれぞれ1μg/ml及び最終10容量%の濃度で1×107個/100μLの細胞に対して添加して、約30分間反応させ、T細胞を除去し、上記RCGFを添加しながら培養を継続して、R細胞を得た。
R細胞は、0.5容量%のRCGFを含有する10容量%血清含有RPMI培地(又は5ng/mlのIL−3を含有するR細胞用培地)を用いて、37℃、5%CO2で培養し、維持した。R細胞は、培養環境からRCGF及びT細胞を除去すると、死滅した。
【0026】
[実施例2]
R細胞の特徴解析
上記のようにして得られたR細胞(受託番号FERM P−20652)に対して各種抗体を用いた表面抗原解析を行った。
蛍光色素(FITC)結合抗体として、抗マウスc−kit抗体(e-Bio社製)、抗マウスFcεRI抗体(e-Bio社製)、抗マウスB220抗体(e-Bio社製)、抗マウスCD3抗体(e-Bio社製)、抗マウスFcγRII/III抗体(Pharmingen社製)、抗ClassI抗体(Pharmingen社製)、抗マウスDX5抗体(e-Bio社製)、抗ClassII抗体(Pharmingen社製)を使用し、それぞれ約5〜10μgをR細胞1×106/100μL対して氷上で30分間反応させた。抗体の結合状態は、FACSを用いて解析した。
その結果、R細胞は、FcεRIα、FcγRII/III、c−kit、ClassIは陽性、CD3、B220、DX5、ClassIIは陰性であることがわかった。
【0027】
また光学顕微鏡及び電子顕微鏡を用いて形態観察を行った(図1及び2)。ヘマトキシリン・エオジン染色(HE染色)では、R細胞の細胞質はピンクに染色された。細胞質内には多数の顆粒が詰まっているが、その一部は空胞状顆粒構造を示している(図1(A)参照、矢印)。また、トルイジンブルー染色(TB染色)では、マスト細胞(図1(C)参照)と異なり染色されなかった(図1(B)参照。矢印は空胞構造を示す)。
また図2(A)に示されるように、電子顕微鏡像では、細胞質に多数の嚢胞状構造(矢印)をもち、その内部には、好塩基球(図2(B)参照)と同様に粒状構造物を含んでいた。また、粒状構造物はやや大型であるが、マスト細胞に見られるような指紋状・渦巻状構造(図2(C)参照。矢印)は認められなかった。細胞質内に多数の顆粒が詰まっているが、一部は空胞に抜けており(空胞状顆粒構造)、高密度の粒状構造を有するマスト細胞とは異なっていた。
これらのことから、R細胞は好塩基球様ないしマスト細胞様細胞株であることが示された。
【0028】
[実施例3]
R細胞のサイトカイン感受性実験
96ウェルマイクロプレートの各ウェルに、1×103個/ウェルの播種密度でR細胞を配置し、各種リコンビナントサイトカイン(IL−2[PeproTech社製]、IL−3[PeproTech社製]、IL−4[PeproTech社製]、IL−7[PeproTech社製]、IL−9[PeproTech社製]、IL−15[PeproTech社製])又は、スタンダードとしてRCGFをそれぞれ含有する培地(サイトカインの量は、50pg/mlからの1/2段階的希釈。RCGFは、0.5容量%含有培地からの1/2段階的希釈)を各ウェルに添加して、37℃、5%CO2の環境下で48時間培養した。培地には、3H−チミジンが含まれており、常法に従って、3Hの取り込み量を測定した。
【0029】
図3に示されるように、R細胞は、被検サイトカインのうち、IL−3、IL−4及びIL−9に対して反応を示した。このうちIL−4に対する反応性は濃度依存的であったが、IL−3及びIL−9に対する反応性は、極微量(64倍希釈)であって安定した反応性を示した。また、IL−3に対するR細胞の感受性が特に高いことが示された。
従って、R細胞を用いることによって、培養液中に存在するサイトカインを効率よく検出することができ、またIL−3の検出については、特に高い感度で検出できることは明らかであった。
なお、R細胞は、pgオーダーのIL−15に対しては上記のように反応性を示さなかったが、それよりも濃い場合、例えば100ng/mlの濃度のIL−15に対しては感受性を示した。
【0030】
[実施例4]
R細胞のIL−3に対する反応性
リコンビナントIL−3(カタログ#14−8031、eBioScience社製)を、0pg/ml、1pg/ml、5pg/ml、10pg/ml、20pg/ml、50pg/ml、200pg/ml及び500pg/mlの各濃度に調整した培地に20μCuの3H−チミジンを含有させて、1×104個/ウェルのR細胞を、37℃8〜12時間、インキュベートした。反応後3H−チミジンの取り込み量をMicroBeta TRILUX(WALLAC社製)を用いて測定した。結果を図4に示す。
図4に示されるように、R細胞は、1pg/mlからIL−3の刺激に応答して増殖能を示し、高い感度を有することが示された。
【0031】
[実施例5]
T細胞培養上清中のサイトカインの検出
反応性T細胞の培養上清中のサイトカインを、R細胞及びCTLL−2を用いて検出した。
反応性T細胞は、DO11.10の脾臓細胞を、抗原提示細胞と1000nMのOVA抗原ペプチドの存在下で1週間培養した後、培養細胞から死細胞を取り除いて調製した。抗原提示細胞としては、10週齢のBALB/cマウスから単離されると共に放射線照射により増殖不能化された脾細胞を使用した。
上記のようにして調製された反応性T細胞2×104個/ウェルを、上記と同様にして調製した抗原提示細胞5×105個/ウェルと、OVA抗原ペプチド(1000nM、250nM、62.5nM、12.5nM)とを含有する培地100μL中で37℃48時間培養し、培養上清を採取した。
この培養上清を、1×104個/ウェルのR細胞又は1×104個/ウェルのCTLL−2に、最終濃度10容量%で加えて36時間反応させた。それぞれ培地には3H−チミジンが0.5μCuの濃度で含有されており、反応後、常法に従って3H−チミジンの取り込み量を測定した。コントロールとして、培養上清後の上記反応性T細胞(2×104個/ウェル)に3H−チミジンを同量で添加して、反応性T細胞の増殖反応を同様に測定した。結果を図5にそれぞれ示す。
【0032】
その結果、T細胞培養上清中のサイトカインは、R細胞の増殖に基づいて精度よく容易に検出できることが示された(図5参照)。特に、10nMの抗原ペプチド濃度で刺激した培養上清であっても高い増殖能を示しているので、精度よく検出できることは明らかである。また、このT細胞培養上清には、どのようなサイトカインが存在しているか未確認であるが、R細胞が複数のサイトカインに対して感受性を有しているため、広いレンジで効率よく検出できることも明らかである。
一方、CTLL−2は、IL−2に対しては高い感受性を有しているが、IL−2以外のサイトカインにはほとんど反応しないため、IL−2が培養上清中になければ増殖することができない。このため、本実施例では、培養上清中に全くサイトカインが存在しないのか、IL−2のみが存在しないのか、を判断することができない。
また、反応性T細胞は、培養上清中のサイトカインに対して反応性を示していたが、250nM未満の濃度では増殖能が低く、精度よく検出することができない。
【0033】
このように本発明にかかるR細胞は、微量なサイトカインに対して高い感度を有すると共に複数のサイトカインに対して感受性を有するので、被検試料中のサイトカインに検出を効率よく行うことができる。
また、このようなR細胞による検出と、既存のサイトカイン検出用細胞株による検出を組み合わせることによって、より一層効率よく被検試料中のサイトカインを検出することができると共に、既存のサイトカイン検出用細胞株のいずれを用いても反応性を示さない被検試料に対してR細胞を反応させることによって、未知のサイトカインを検出することも可能である。
【図面の簡単な説明】
【0034】
【図1】(A)は本発明にかかるR細胞のHE染色像、(B)は本発明にかかるR細胞のTB染色像、(C)はマスト細胞のTB染色像である。
【図2】(A)は本発明にかかるR細胞の電子顕微鏡写真像、(B)は好塩基球の電子顕微鏡写真像、(C)はマスト細胞の電子顕微鏡写真像である。
【図3】本発明の実施例にかかるR細胞の各種サイトカインに対する反応性を示すグラフである。
【図4】本発明の実施例にかかるR細胞のIL−3に対する反応性を示すグラフである。
【図5】本発明の実施例にかかる抗原刺激T細胞培養上清に対するR細胞(白丸)、CTLL−2(黒丸)及び反応性T細胞(白三角)の反応性を示すグラフである。
【特許請求の範囲】
【請求項1】
被検試料中のサイトカインを検出する方法において、
DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株を、前記被検試料中で培養する培養工程、
前記細胞株の増殖に基づいて、サイトカインを検出する検出工程
を含むことを特徴とする当該検出方法。
【請求項2】
前記細胞株が、受託番号FERM P−20652の細胞株であることを特徴とする請求項1記載の検出方法。
【請求項3】
目的サイトカインがインターロイキンであることを特徴とする請求項1又は2記載の検出方法。
【請求項4】
前記サイトカインが、IL−3、IL−4、IL−5、IL−6、IL−9及びIL−13からなる群より選択された少なくとも1つであることを特徴とする請求項1乃至3のいずれか1項記載の検出方法。
【請求項5】
受託番号FERM P−20652の細胞株。
【請求項6】
サイトカイン産生細胞のスクリーニング方法であって、
被検細胞を培養して、被検培養上清を調製する調製工程、
DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株を、前記被検培養上清を含有する培養液中で培養する培養工程、
前記細胞株の増殖に基づいて、前記被検細胞からサイトカイン産生細胞を選定する選定工程、
を含むことを特徴とする当該スクリーニング方法。
【請求項7】
前記細胞株が、受託番号FERM P−20652の細胞株であることを特徴とする請求項6記載のスクリーニング方法。
【請求項8】
前記サイトカインがインターロイキンであることを特徴とする請求項6記載のスクリーニング方法。
【請求項9】
前記サイトカインが、IL−3、IL−4、IL−5、IL−6、IL−9及びIL−13からなる群より選択された少なくとも1つであることを特徴とする請求項6乃至8のいずれか1項記載のスクリーニング方法。
【請求項10】
受託番号FERM P−20652の細胞株を用いて検出されたサイトカイン。
【請求項11】
受託番号FERM P−20652の細胞株用いて得られたサイトカイン産生細胞。
【請求項1】
被検試料中のサイトカインを検出する方法において、
DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株を、前記被検試料中で培養する培養工程、
前記細胞株の増殖に基づいて、サイトカインを検出する検出工程
を含むことを特徴とする当該検出方法。
【請求項2】
前記細胞株が、受託番号FERM P−20652の細胞株であることを特徴とする請求項1記載の検出方法。
【請求項3】
目的サイトカインがインターロイキンであることを特徴とする請求項1又は2記載の検出方法。
【請求項4】
前記サイトカインが、IL−3、IL−4、IL−5、IL−6、IL−9及びIL−13からなる群より選択された少なくとも1つであることを特徴とする請求項1乃至3のいずれか1項記載の検出方法。
【請求項5】
受託番号FERM P−20652の細胞株。
【請求項6】
サイトカイン産生細胞のスクリーニング方法であって、
被検細胞を培養して、被検培養上清を調製する調製工程、
DO11.10トランスジェニックマウス脾臓細胞由来好塩基球様ないしマスト細胞様細胞株を、前記被検培養上清を含有する培養液中で培養する培養工程、
前記細胞株の増殖に基づいて、前記被検細胞からサイトカイン産生細胞を選定する選定工程、
を含むことを特徴とする当該スクリーニング方法。
【請求項7】
前記細胞株が、受託番号FERM P−20652の細胞株であることを特徴とする請求項6記載のスクリーニング方法。
【請求項8】
前記サイトカインがインターロイキンであることを特徴とする請求項6記載のスクリーニング方法。
【請求項9】
前記サイトカインが、IL−3、IL−4、IL−5、IL−6、IL−9及びIL−13からなる群より選択された少なくとも1つであることを特徴とする請求項6乃至8のいずれか1項記載のスクリーニング方法。
【請求項10】
受託番号FERM P−20652の細胞株を用いて検出されたサイトカイン。
【請求項11】
受託番号FERM P−20652の細胞株用いて得られたサイトカイン産生細胞。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2007−129941(P2007−129941A)
【公開日】平成19年5月31日(2007.5.31)
【国際特許分類】
【出願番号】特願2005−325392(P2005−325392)
【出願日】平成17年11月9日(2005.11.9)
【出願人】(803000115)学校法人東京理科大学 (545)
【Fターム(参考)】
【公開日】平成19年5月31日(2007.5.31)
【国際特許分類】
【出願日】平成17年11月9日(2005.11.9)
【出願人】(803000115)学校法人東京理科大学 (545)
【Fターム(参考)】
[ Back to top ]

