サンプリング装置、方法及びその使用
本発明は、免疫化学的サンプリング装置、その使用、サンプリング装置の製造方法、及びこのサンプリング装置を横方向流れ免疫アッセイにおいて使用する方法を提供する。サンプリング装置は、多孔質層によって近位端の一つで包囲された細長い支持体を含み、この多孔質層は不透過性保護層によって包囲されており、及び所望により保護層によって同時に細長い支持体に取り付けられている。多孔質層は標識化された特異的な結合試薬を含み、これは液体サンプルによって活性化され、サンプリング装置が多孔質担体を含む分析装置と接触されたときに制御された様式で可動化される。分析装置の多孔質担体は、少なくとも一つの特異的な結合試薬を検出領域に含む。分析装置は、一つのサンプルから幾つかの分析対象物を検出するために多数のチャネルを有する分析装置として用いられることができる。結果は、分析装置の検出領域から直接可視的に、又は結果を記録することができる好適な器具によって読みとられることができる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、免疫化学的サンプリング装置に関し、特に、家庭での使用、医師の診療所での使用及び/又は使用者から最小レベルの技術しか必要としない技術的に訓練されていないスタッフによる使用のために好適な装置に関する。
【背景技術】
【0002】
免疫拡散に基づく方法及び装置は、例えばUS4757002、US3990852、及びUS4562147から公知である。横方向の流れに基づく免疫クロマトグラフィー法は、EP0291194、EP0284232、EP0250137、US5250412、US5084245、US5760315、US6375896及びWO86/03839から公知である。
【0003】
US4562147は、ブタ及び他の動物における偽狂犬病抗体の検査のための半径方向免疫拡散酵素アッセイ方法を提供する。可溶化された非感染性ブタ偽狂犬病抗原の接着性被覆を下に含む寒天検査プレートが提供される。検査結果は、公式なウイルス中和検査によって得られる力価と相関する着色領域の直径から得られる。
【0004】
EP0291194は、特異的な結合が関与するアッセイ、特に免疫アッセイ及びそのための装置に関する。開示されている分析検査装置は、乾燥多孔質担体を含む中空のケーシングを含み、このケーシングは湿気を吸収しやすいサンプル受容部材を介してケーシングの外部と間接的に連通する。担体は、第一領域に標識化された特異的な結合試薬を、そして第一領域からは空間的に分離された第二領域(検査領域)に同じ分析対象物のための未標識の特異的な結合試薬を含む。使用にあたって、サンプル溶液は検査が行われるときに検査装置に直接適用され、これは検査領域をオーバーフローさせる危険性にさらす。
【0005】
EP0284232は、液体サンプル中の分析対象物の存在又は不存在を決定するための固相アッセイを提供する。この発明の検査ストリップは、第一部分に移動可能に支持されたトレーサーと、第二部分(検査領域)に固定された結合剤とを有する。使用にあたって、サンプル溶液は検査が行われるときに検査装置に直接適用され、これは検査領域をオーバーフローさせる危険性にさらす。
【0006】
EP0250137は、サンプル中のリガンドを検出するためのコロイド金を用いた免疫アッセイを記述し、そこでは膜ストリップはサンプルと接触させられ、同時に又は続いてリガンド結合パートナー又はコロイド金で標識化されたリガンドを含む液体試薬と接触させられる。検査を行うためには、使用者は標識化されたリガンドを含む液体試薬を膜ストリップに別個に適用しなければならない。
【0007】
US5250412は、分析対象物を収集して分析するための方法及びキットを記述する。サンプルは綿棒で収集され、この綿棒に対して、使用者は標識化された成分を含む別個の液体を適用して次に洗浄溶液を適用しなければならない。
【0008】
US5084245は、綿棒の吸収性先端に集められた標本を用いた免疫学的反応に基づく診断手順を行うための装置を提供する。使用されたとき、綿棒は、検査のための必要な試薬を含む感受性要素の方へ通路を通って押される。リブが通路に配置されており、先端を絞り、綿棒の流体を圧搾する。結果は、案内部材をベース成分から除去して感受性要素を露出することによって可視的に観察可能になる。
【0009】
US5760315は、吸収性パッドを用いるサンプルの収集のための装置を提供する。パッドは、対応する検査ストリップの検査領域に結合しない過剰の標識化された結合試薬を除去するための洗浄剤として機能するのに十分な体積のサンプル流体のための流体貯蔵所として機能する。様々な疎水性度及び多孔度の材料の複合体アレイは、装置中において、サンプル流体をその初期の収集中に、吸収パッド上に又は吸収パッドの近くに配置された標識化された試薬から離れる方向に向けるために利用される。
【0010】
US6375896は、物質の免疫化学的検出のための綿棒分析装置を記述する。綿棒分析装置の綿棒ペンは、サンプルの収集のために用いられる。サンプルは、別個の溶離液体を用いて装置から溶離されなければならない。
【0011】
WO86/03839は、固相拡散アッセイを例示し、そこではサンプルはまず標識化された結合物質と混合され、次に固定された吸収性分子を有する支持体の領域に適用され、そこで拡散させられる。拡散パターンは可視化され、測定される。
【0012】
背景技術の記載から、免疫アッセイを行うための多くの異なる検査キットが利用可能であることが明らかである。幅広い種類の検査キットが商業的に入手可能であり、それらの多くは家庭での使用を意図されている。それらの便利な形式にもかかわらず、それらが誤った様式で用いられると誤りが生ずる危険性が高い。この危険性は、検査装置がサンプリングのために用いられる場合、切迫しており、これは非実用的及び不便の両方でありうる。特に、検査装置がサンプリング装置として用いられる場合、又はサンプルを収集するために用いられる場合、感受性試薬及び分析装置の構造が破壊される又は妨害される危険性がある。
【0013】
本発明は、免疫化学的検査のための改良された検出システムを提供し、これは液体サンプルが収集されることを可能にしかつ標識化された特異的な結合試薬が制御された様式で移行されて可動化されることを可能にするサンプリング装置を含む。二部システムのため、分析装置は液体サンプルとは直接接触せず、それにより分析装置中の試薬及び分析装置の構造がサンプリング手順によって破壊されたり妨害される可能性が最小化される。
【0014】
二成分免疫アッセイ装置は、こぼれや汚染の危険性なしに使用者が液体サンプルを容易に収集してそれをアッセイの実行のために検査装置へ移行させることを可能にする。
【発明の開示】
【0015】
本発明は、免疫化学的サンプリング装置、キット及びこのサンプリング装置を横方向流れ免疫アッセイにおいて使用する方法を提供する。装置は、多孔質層によって近位端の一つで包囲された細長い支持体を含み、この多孔質層は所望により不透過性保護層を有し、前記多孔質層は標識化された特異的な結合試薬を含み、これは液体サンプルによって活性化され、サンプリング装置が多孔質担体を含む分析装置(結果装置)と接触されたときに制御された様式で可動化される。
【0016】
好ましい実施態様では、装置は細長い支持体(即ち、固体支持体)を含み、これに多孔質担体が部分的に巻きつけられ、次に実質的に不透過性の疎水性カバーで被覆される。遠位端で、多孔質担体は標識化された結合試薬(例えば抗体又は抗原)を含み、これはサンプリング装置が分析装置の検査ストリップ要素と接触状態にもたらされた(例えば検査ストリップ要素上に押された)ときに多孔質担体から液体サンプルと共に制御された流れの中へと解放される。
【0017】
別の好ましい実施態様では、免疫アッセイを行うための免疫化学的サンプリング装置は、(a)多孔質担体によって包囲された細長い支持体、(b)多孔質担体に解放可能なように結合された標識化された結合試薬、及び(c)多孔質層(即ち多孔質担体)上に配置された不透過性保護層(即ち疎水性カバー)を含む。不透過性保護層は、圧力平衡化手段をさらに含み、標識化された結合試薬は、液体サンプルと混合されたときに多孔質層が分析装置の検査ストリップと流体連通状態に置かれるまで多孔質内に保持される。
【0018】
また、液体サンプル中の分析対象物の存在又は不存在を決定する方法が本発明において提供される。この方法は、診断的サンプリング装置を液体サンプルと接触させ、診断的サンプリング装置を分析装置と接触させ、液体サンプルを標識化された特異的な結合試薬又はその反応生成物と共に診断的サンプリング装置から分析装置の多孔質担体へと移動又は流れさせるのに十分な時間放置し、そこで液体サンプルの反応生成物と標識化された結合試薬は分析装置の検出領域の方へ移動し、そして検出領域中の分析対象物の存在又は不存在を決定することによって結果を読み取るステップを含む。
【0019】
使用において、サンプルが多孔質層の近位端と接触するようにサンプリング装置の巻きつけられた部分は流体サンプルと接触状態にもたらされる(例えばサンプルの流れ中への浸漬又は導入によって)。この近位端は不透過性保護層の下に露出されている。多孔質層は、多孔質層中へのサンプルの流れ並びに分析装置と接触している多孔質層から外への標識化された結合試薬と混合されたサンプルの流れを最適化するように設計された様式で細長い支持体(これはその巻きつけられていない端でハンドルとして作用する)の周りに巻きつけられる。多孔質層を通るサンプルの流れの体積及び速度は、不透過性保護層中に与えられている圧力平衡化手段によって同様に制御される。
【0020】
特に、一旦サンプル流体がサンプリング装置(そこでサンプルは標識化された結合試薬と混合する)に収集されると、それはサンプリング装置の遠位端を分析装置の検査ストリップと接触状態にもたらすことによって分析装置中に解放されるまで保持される。サンプリング装置から外へのサンプル流体の流れは、検査ストリップとの接触によって媒介される毛管作用又は拡散を介して生じ、機械的に増大されることができる(例えばサンプリング装置に穏やかな圧力を適用することによって)。
【0021】
さらに、免疫化学的サンプリング装置の製造方法が提供される。この方法は、多孔質層の一以上の層を細長い支持体の周りに巻きつけてその状態で多孔質層を保持し、次に多孔質層に不透過性保護層を巻きつけてその状態で不透過性保護層を保持するステップを含む。多孔質材料は、上に標識化された結合試薬が解放可能なように結合された多孔質材料からなり、不透過性保護層は圧力平衡化手段を含む。
【0022】
免疫化学的分析で用いるためのキットは、免疫化学的サンプリング装置と少なくとも一つの結合試薬が配置されている分析装置とを含む。分析装置の多孔質担体は、点又は領域(検査線)として直接的に又は間接的に固定された少なくとも一つの特異的結合試薬を含む。さらに、多孔質担体上の一以上の点又は領域は制御領域として作用することができる。多孔質担体が検出領域を含む一以上の多孔質通路(これはサンプル溶液によって浸透されることができる)を含む分析装置との関連のみならず、多孔質担体が点又は領域として固定されたチャネル当たり少なくとも一つの特異的な結合試薬を含む好適な方法によって所望により作られた二以上のチャネルを含む分析装置との関連でもサンプリング装置は用いられることができることは当業者には自明である。
【0023】
好ましくは、分析装置は、結合試薬が結合する必要がないサンプル適用部位の下流の検査領域内に結合試薬が固定された検査ストリップを含む。最も好ましくは、分析装置は検査ストリップのための固体ハウジングをさらに含み、このハウジングはくぼみを有し、その中に検査ストリップのサンプル適用部位がサンプリング装置に適用された穏やかな圧力下で偏向され、多孔質層から外へのサンプルの流れを容易にする。
【0024】
免疫化学的サンプリング装置は、多孔質担体を含む分析装置における標識化された特異的な結合試薬の制御された可動化を可能にする。それにより、液体サンプル中の異なる分析対象物を検出するための一層感受性の方法が提供される。検出されるべき分析対象物は、細菌、ウイルス、真菌及び寄生生物の抗原又はこれらに対する抗体、又はそれらの成分及び生成物(疾患特異的抗体(例えばヘリコバクター・ピロリ、A型肝炎、HIV1,2、呼吸器疾患などに対する抗体)を含む);尿中に排出される抗原(黄体形成ホルモン(LH)、卵胞刺激ホルモン(FSH)及びヒト絨毛膜刺激ホルモン(hCG);又は流体サンプル中の麻薬又は麻薬代謝物の存在の指標である抗原)であることができる。
【0025】
本発明の装置及び方法は、妊娠、閉経、受胎能、甲状腺刺激ホルモン、トキソプラスマ症、癌抗原、呼吸器疾患、アレルギー、心筋梗塞、及び薬物検査などを含む多数の異なる検査のために用いられることができる。
【0026】
検査結果の増大された確実性以外の本発明のサンプリング装置及び検出システムの他の利点は;サンプリング装置及び分析装置の小さい形式(これは材料の節約に導く)、少ない廃棄生成物及び減少した運送費用であり、従って環境的に優しい製品を提供することができる。さらに、この検査システムは使用するのが容易であるので、それは家庭の使用を可能にする。分析装置は液体サンプルと直接接触しないので、オーバーフローは回避され、検査の増大された信頼性が得られる。サンプル流体は分析装置に直接適用されないので、検査ストリップの飽和及び/又は検査領域の汚染は回避される。さらに、本発明のサンプリング装置及び分析装置は、これらの装置が乾燥しているという事実のため、及びそれらが密封して貯蔵されることができるという事実のため、貯蔵しやすい。要するに、本発明は、使用及び製造が他に例を見ないほど簡単である、分析対象物の存在についてサンプル流体を収集して検査するための装置を提供する。
【0027】
図面の簡単な記述
図1は、本発明によるサンプリング装置の透視図である。
図2は、サンプリング装置を下側から見た図である。
図3は、本発明によるサンプリング装置の別の透視図である。
図4は、本発明による被覆された多孔質担体の拡大した透視図である。
図5は、サンプリング装置の別の実施態様を下側から見た図である。
図6は、サンプリング装置及び分析装置の側面図である。
図7は、分析装置を上側から見た図である。
図8は、分析装置の別の実施態様を上側から見た図である。
【発明を実施するための最良の形態】
【0028】
本発明は、横方向流れ検査のためのサンプルを収集するサンプリング装置を提供する。サンプリング装置は、細長い支持体(コアスティック)、及びコアスティックの一端の周りに適用された多孔質層を含む。多孔質層は、標識化された特異的な結合試薬を含み、かつ多孔質材料の反応性基がサンプル又は標識化された特異的な結合試薬と反応するのを防止するブロッキング溶液で処理されている。サンプリング装置は、検査されるべき液体と接触されることができ、続いて、点又は領域として固定された少なくとも一つの特異的な結合試薬を含む分析又は結果装置の多孔質担体と接触させられる。
【0029】
さらに、液体サンプル中の分析対象物の存在又は不存在を決定する免疫化学的方法が提供される。この方法は、サンプリング装置に液体サンプルを添加し、サンプリング装置を分析装置の検査ストリップのサンプル適用部位と流体連通接触状態に置き、そしてサンプル及び標識化された結合試薬がサンプリング装置から検査ストリップまで移動するのに十分な時間放置するステップを含む。検査結果は、分析対象物のための少なくとも一つの結合試薬がサンプル適用部位の下流の検査部位を形成するように検査ストリップ上に固定されている検査部位で観察される。液体サンプルは、分析装置の検査ストリップと流体連通接触状態にもたらされるまでサンプリング装置中に保持される。
【0030】
異なるタイプの分析装置が背景技術で記述されている。多数のチャネルを有する装置は、幾つかの分析対象物を同時に検査することを可能にする。異なる分析対象物に対して特異的なマーカーは、異なる生成物を形成するように一緒にグループ化されることができる。多数のチャネル装置は、検査されたサンプルが移動することができるチャネルの網状構造を生じさせるために撥水性処理などにより処理された多孔質担体を含む。異なる特異的結合試薬はそれぞれのチャネル中に結合されることができる。本発明の好ましい実施態様では、多数のチャネルを有する分析装置は、同一のサンプルを幾つかの分析対象物について同時に検出するために用いられる。この装置のそれぞれのチャネルは、そこに幾つかの検出領域及び/又はコントロール領域を有することができる。
【0031】
本発明の一実施態様では、分析装置は検出領域及び制御領域の両方を含む。さらなる検出領域は、定量的検査を行うために追加されてもよい。本発明の分析装置は、それが移動化可能な特異的試薬を欠くという点で従来技術とは異なる。
【0032】
本発明のサンプリング装置上の標識化された結合試薬の存在は、さらなる標識化された結合試薬が検査ストリップ又は分析装置内の他の構造(例えばサンプル適用パッド)上に配置された分析装置を用いる必要性を否定する。このように、本発明によって使用される好ましい分析装置は、少なくとも一つの検査領域(固定された結合試薬からなる)及び所望によりコントロール領域も有する検査ストリップを含むものである。
【0033】
当業者は、横方向流れ免疫アッセイで使用するための検査ストリップ並びに結合試薬及びコントロール試薬を固定する方法(サンドイッチ形式及び競合形式の両方での)をよく知っているだろう。これらは全て本発明のサンプリング装置で利用されることができ、そこから標識化された結合試薬及びサンプルが供給される。
【0034】
サンプリング装置の構築
サンプリング装置の構築は、多孔質材料をブロッキング溶液で処理し、乾燥させ、標識化された特異的な結合試薬を多孔質材料に添加し、乾燥させ、多孔質材料を細長い支持体の周りに取り付けて多孔質層を形成させ、不透過性材料層を多孔質層の周りに取り付けて最後に乾燥させて装置を包装するステップを含む。まず多孔質材料を支持体の周りに取り付け、その後ブロッキング溶液及び標識化された特異的な結合試薬をサンプリング装置の多孔質層に浸漬又は適用することも可能である。
【0035】
多孔質材料の不活性化
ブロッキング溶液は、アルブミン(BSA、ウシ血清アルブミン)及びカゼイン又はPEG(ポリエチレングリコール)、PVA(ポリビニルアルコール)及びPVP(ポリビニルピロリドン)の如き天然又は合成ポリマー、TWEEN20、HEXA(ヘキサンスルホン酸)、TRITON−X−100、SDS及びBRIJの如き非イオン性界面活性剤、及び糖(例えばグルコース、スクロース及びトレハロース又はそれらの誘導体)の如き保存剤を含む混合物であるが、このブロッキング溶液は、多孔質材料の反応性部位を不活性にするために多孔質層に添加される。ブロッキング溶液はポンプによって添加されてもよいし、又は多孔質材料はブロッキング溶液中に浸漬されてもよい。次のステップの前に、多孔質材料は乾燥される。
【0036】
特異的な標識化された試薬の添加
サンプリング装置の多孔質層は、特異的な標識化された試薬で含浸される。多孔質層の全体を含む多孔質材料の最外表面層の全て(及びいかなる下に横たわる層の一以上)は標識化された結合試薬で含浸されることができる。層全体が含浸されることができるが、好ましくは標識化された特異的な結合試薬は層の下端に含浸される。バックグラウンド干渉を最小化して検査時間を短縮するため、含浸は、多孔質層の最遠位端での多孔質材料の表面積の好ましくは半分未満、最も好ましくは約20〜40%に制限される。
【0037】
標識化された結合試薬は、当該技術分野で周知の方法、例えば当該技術分野で周知の方法を用いた特異的な結合試薬での標識粒子の被覆によって調製されることができる。特異的な及び非特異的な(好ましいのは前者である)抗体、抗体断片、組み換え抗体、組み換え抗体断片、抗原、レクチン、受容体及び/又はリガンドは好適な結合試薬であり、それらは着色されたラテックス、金、他の金属、染料、蛍光産生物質、又は超常磁性粒子の如きいかなる好適な標識にも取り付けられることができる。しかし、色素産生物質、特に蛍光色素産生物質及び酵素的標識をマーカーとして使用することも可能である。もしサンプルが異なる結合特異性の一以上の分析対象物について検出され、同じ特異的な結合試薬が全てについて用いられることができないなら、幾つかの異なる標識化された特異的な結合試薬の組合せを用いることが可能である。
【0038】
標識化された特異的な結合試薬は、針を通して正確な体積の試薬を送出するチューブポンプを用いて適用されることができ、又は多孔質材料は浸漬されることができる。多孔質材料は相対湿度が20%未満の乾燥室で乾燥され、さらに、相対湿度が8%未満の乾燥室で乾燥される。
【0039】
標識化された結合試薬組成物及び/又は多孔質材料は、サンプル流体を用いた結合試薬の多孔質材料から溶液中への(又は粒状の標識化された結合試薬の場合は懸濁液中への)解放を容易にするための薬剤で処理されることができる。当業者は、本発明で利用されることができる横方向流れアッセイで用いるのに好適な解放剤(糖、カゼイン及び界面活性剤の如き)に熟知しているであろう。
【0040】
材料の取り付け
多孔質材料の一以上の層は、例えば木材又はプラスチック(ポリプロピレン(PP)及びポリ塩化ビニル(PVC)の如き)製の細長い支持体(コアスティック)の周りに取り付けられる。一以上の層は一度に取り付けられることができ、又は多孔質材料のストリップは支持体スティックの周りに巻かれることができる。多孔質材料はテープによって取り付けられることができ、このテープはまず細長い支持体に取り付けられ、次に多孔質材料と共にスティックの周りに巻かれ、最後にテープはそれ自身に取り付けられる。当業者は多孔質材料を固体表面に取り付ける代替手段、例えば不活性な接着剤や熱結合に熟知しているであろう。ブロッキング溶液及び標識化された結合試薬は、多孔質層が細長い支持体に取り付けられる前又は後に多孔質層に適用されることができる。支持体スティックは細長い丸められた、平坦な又は平面状のスティックであることができ、これは中実又は中空であることができる。テープの如き不透過性材料の一以上の層は多孔質層の周りに取り付けられる。
【0041】
好ましくは、細長い支持体は、サンプリング装置から分析装置への標識化された結合試薬の流れを調整するために一以上の、好ましくは一〜五層のテープを含む不透過性層及び多孔質層によってその近位端で包囲される。サンプリング装置の多孔質層は、一以上の、好ましくは一〜五層の多孔質材料も含む。多孔質材料は、紙、ガラス繊維、ナイロン、ポリエステル又はセルロース及びそれらの誘導体からなる群の材料から選択され、最も好ましくはこれらの材料の湿気を吸収しやすい及び/又は親水性の形態である。
【0042】
別の好ましい実施態様では、不透過性保護層は、被覆されるべき多孔質層の部分の周りに巻きつけられ、その上に保持(例えば不活性な接着剤で)される。不透過性保護層はその遠位及び/又は近位端では親水性であることができるが、実質的に疎水性でありかつ不透過性である。好都合には、不透過性保護層は透明なポリエステルテープ、マイラーフィルム、又は他の不透過性材料からなることができる。所望により、例えばサンプルの収集についての指示及び標識化された結合試薬によって結合されることができる分析対象物の正体を表示する記号を有する疎水性の印刷紙(図示せず)が、不透過性保護層と多孔質層の間に配置されることができる。不透過性保護層は、複数の小さなベント8をさらに与えられることができ、これらはそれぞれ約0.1mm〜0.5mmの最大直径を有し、用いられるテープの25mm×51mmの片にわたって分布され、不透過性保護層を形成する。好ましくはベントは不透過性保護層の表面積の1〜50%にわたって与えられ、最も好ましくはベントは不透過性保護層の表面積の10〜25%にわたって与えられる。
【0043】
ベントは、多孔質層を通る流体の流れの体積及び速度を制御する役割を有する。本発明はベントがサンプリング装置中の流体の流れを制御する作用機構に制限されるものではないが、ベントは、サンプル流体が適用されたときの多孔質層内外の圧力を平衡化し、それにより圧力勾配(それに沿って流体の流れが標識化された結合試薬を洗い流してしまう危険性が高まる)の形成を回避する役割を有すると信じられる。実施において、ベントは、サンプリング装置が分析装置の検査ストリップ要素と流体連通接触状態におかれるまでサンプル流体を多孔質層中に保持する役割を有する。
【0044】
本発明の別の好ましい実施態様では、多孔質層は細長い支持体の周りにしっかりと巻きつけられているが、可能な最大限度では巻きつけられていない。材料が細長い支持体の周りに巻きつけられたときに材料中にいくらかのゆるみを残すことにより、サンプリング装置が好適な分析装置と接触状態にもたらされたときの多孔質層からのサンプル流体の測定される流れを促進する。
【0045】
例えば、全直径の観点から見ると、0.1Nmのトルク(好ましくは0.05〜0.5Nmの好適なトルクの範囲内)下で巻きつけられている本発明のこの実施態様による例示的なサンプリング装置は、存在する以下の成分と共に4.7mm±0.1mmの全直径を有するであろう:(a)51mmの幅及び0.03mmの厚さを有する不透過性保護層(ポリエステルテープ);(b)27mmの幅及び398μmの厚さを有する多孔質担体(不織布ポリエステル);及び(c)15mmの幅及び115μmの厚さを有する印刷された紙。これら全ては、(d)2mmの厚さを有する細長い支持体(プラスティックスティック)の周りに巻きつけられている。当業者はこれらの一般的な寸法を本発明によって構築された異なる寸法のサンプリング装置に容易に適合させることができるであろう。
【0046】
装置の乾燥及び包装
装置は8%以下の水分率まで乾燥され、好適な分析装置(結果記録検出装置)との組合せでキットで又は分離されて密封して包装される。
【0047】
分析装置の調製
本発明のサンプリング装置と共に使用するのに好適な分析装置であって検出システムの結果記録検出装置である分析装置は、ブロッキング前の装置の多孔質担体に直接的に又は間接的に一以上の特異的な結合試薬及び所望によりコントロール試薬を固定することによって調製されることができる。用いられるブロッキング溶液はサンプリング装置について用いられるものと同じものであることができる。多孔質担体は所望により不透過性裏打ち上に又はケーシングもしくはハウジング中に置かれることができる。
【0048】
多数のチャネルを有する装置は、異なる分析対象物(又はコントロール)の検査のための異なるチャネルを得るための好適な方法で多孔質材料を処理することによって調製されることができる。幾つかの分析対象物は一つの単一の検査によって同じサンプルから検出されることができる。
【0049】
好ましい実施態様では、八つのチャネルが多孔質担体上に好適な方法(例えばブロッキング、フォトリソグラフィー又はエッチング)によって作成される。チャネルは領域によって相互から分離されており、これらの領域のそれぞれはこれらの領域を通るサンプル流体の流れを防止するために疎水性に処理される。各チャネルは標識化されていない結合試薬からなる検査領域又は点を含む。また、サンプリング装置が多孔質担体と接触状態に置かれるサンプル適用部位も示される。
【0050】
分析装置の特異的な試薬は、抗体、抗体断片、組み換え抗体、組み換え抗体断片、抗原、レクチン、受容体及び/又はリガンドを含む。サンプリング装置に適用可能な標識は、着色されたラテックス、金、金属、染料、蛍光産生物質、特異的な結合剤で被覆された超常磁性粒子を含む。色素産生物質、特に蛍光色素産生物質及び酵素的標識もマーカーとして用いられることができる。
【0051】
分析装置の多孔質材料は、ニトロセルロース、紙、ガラス繊維、ナイロン、ポリエステル、ポリスルホネート、又はセルロース、及びこれらの誘導体からなる群から選択される。
【0052】
検出システムの使用
サンプリング装置は、尿の流れの下で装置を保持することによって、又は液体サンプルにサンプリング装置を浸漬することによって、又はサンプルをピペットで添加することによって使用されることができる。もしサンプリング装置が尿の流れの下に置かれるのなら、好ましい時間は2〜15秒間であり、さらに好ましくは5〜15秒間であり、最も好ましくは5〜10秒間である。もしサンプリング装置が液体サンプルに浸漬されるのなら、好ましい時間は2〜30秒間であり、さらに好ましくは10〜20秒間であり、最も好ましくは10〜12秒間である。もし液体サンプルがピペットによって添加されるのなら、好ましいサンプル量は2〜40滴であり、さらに好ましくは5〜20滴であり、最も好ましくは5〜15滴である。10滴は約0.5mlに等しい。乾燥及びサンプル適用後、サンプリング装置は装置の巻きつけられた部分を下に向けて実質的に垂直方向に維持されることが好ましい。
【0053】
一旦サンプルが収集されたなら、サンプリング装置の最遠位端は分析装置の検査ストリップと接触状態に置かれ(接触させられるか又は接触状態で放置される)、液体サンプルを標識化された特異的な結合試薬又はその反応生成物(複合体)と共に診断的サンプリング装置から分析装置の多孔質担体へと移動又は流れさせるのに十分な時間放置する。液体サンプル及び標識化された結合試薬は分析装置の検査領域に移動し(例えば拡散又は毛細管作用により)、そこでサンプル流体中の分析対象物の存在又は不存在が決定される。結果は直接可視的に(裸眼により)、又は結果の記録を可能にする好適な器具により読み取られることができる。
【0054】
液体サンプルは、尿、血液、血清、血漿、唾液、又はサンプル緩衝溶液であることができる。特に好ましい実施態様では、液体サンプルは尿である。
【0055】
サンプリング装置及び分析装置の構造
図1は、典型的なサンプリング装置を表す。細長い中空の支持体1は、その近位端の一つで多孔質材料2の多孔質層によって包囲されている。多孔質材料は、その下側端に標識化された特異的な結合試薬3を含む。
【0056】
図2は、下側から見たサンプリング装置を示す。多孔質材料2の四つの層が細長い支持体1の周りに巻かれている。多孔質層は不透過性保護層(疎水性被覆)4によって保護されている。
【0057】
図3は、不透過性保護層によって被覆された典型的なサンプリング装置を示す。多孔質層2は、細長い支持体1の遠位端の周りに配置されており、不透過性保護層4によって部分的に被覆されている。多孔質層2は不透過性保護層4によって軸的に被覆されており、その対向する近位端5及び遠位端6の表面のみが露出されている。
【0058】
図4は、不透過性保護層中のベントが示されたサンプリング装置を表す。不透過性保護層4は多数の小さいベント7を与えられている。
【0059】
図5は、サンプリング装置の下側から見た別の実施態様を示す。中空の支持体1は多孔質材料2の三つの層によって包囲されており、多孔質材料は不透過性保護層4の一以上の層によって包囲されている。
【0060】
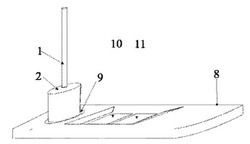
図6は、本発明の典型的な検出システムを表す。多孔質材料2によって包囲された支持体1を含むサンプリング装置は、サンプルウェル(サンプル適用口)9、検査窓10及びコントロール窓11を有するケーシング8を含む分析装置と接触させられている。
【0061】
図7は、上側から見た典型的な分析装置を示す。ケーシング8(例えば不透過性プラスチックハウジング)(その中に検査ストリップ(図示せず)が配置されている)はサンプルウェル9を含み、そこにサンプリング装置がそれが液体サンプルと接触させられたときに置かれる。多孔質層の検出領域は検査窓10中に置かれており、陽性の結果の場合には可視的な反応がそこで見られることができる。多孔質層のコントロール領域はコントロール窓11中に置かれており、そこでは検査が行われたときはいつでも可視的反応が見られるべきである。換言すれば、ハウジング8は、検査領域上に配置された窓9(それを通して検査結果が見られることができる)、及びコントロール領域上に配置された窓10(それを通してコントロールの結果が見られることができる)を含む。サンプル適用口11は、結合試薬が結合していない検査ストリップの一部分の上に配置されており、本発明のサンプリング装置のその中への挿入のために与えられている。
【0062】
図8は、分析装置の別の実施態様を示す。八つのチャネル12が好適な方法によって多孔質層上に作られている。装置のチャネルは処理領域13によって相互から分離されている。各チャネル12は検出領域又は点14を含む。また、サンプリング装置が接触されるべき場所15(サンプル又はサンプリング装置受入口、又はサンプル適用口)が示されている。
【0063】
図及び実施例で記述される実施態様は、本発明の範囲内にある実施態様の例としてのみ見られるべきものである。それらは特許請求の範囲によって規定される本発明の範囲を限定するものとみなされるべきではない。
【実施例】
【0064】
実施例1 妊娠検査
実施例1はhCG妊娠検査に関し、そこでは特異的な標識化された試薬を含む多孔質層に取り付けられてこれを保護するための保護不透過性層がサンプリング装置に追加される。コントロール領域は検査の適切な性能を確実にするために追加される。
【0065】
図1のサンプリング装置は、金コンジュゲートとhCG抗原の間の第一反応のためのプラットフォームとしての多孔質ポリエステルフィルター材料を用いることによって構築された。長さ100メートルで幅10mmのロールとして得ることができるポリエステル材料が用いられた。
【0066】
ポリエステル材料はまずBSA(0.1〜1.0%)、Tween20(0.01〜0.05%)及びトレハロース(0.5〜1.5%)を含むブロッキング溶液でブロッキングされた。乾燥後、hCG特異的な結合試薬を含む3μl/mmの金コンジュゲート溶液がブロッキングされたポリエステルに適用された。溶液はチューブポンプを用いて材料の端の5mm幅の領域に添加され、次に20%未満の相対湿度を有する乾燥室で乾燥させられた。乾燥は、8%未満の相対湿度を有する乾燥室で続けられた。
【0067】
ポリエステルフィルターは10mm×30mmの片に切られた。多孔質材料の四つの層は、ポリプロピレン製の丸い中空スティックの周りに巻かれ、テープで取り付けられた。テープはまずポリプロピレンスティックに取り付けられ、次にポリエステルでスティックの周りを巻かれ、最後にテープは自分自身に取り付けられた。含浸された標識化された特異的な結合試薬を有する端は、サンプリング装置の下側端に設定された。
【0068】
図7の分析装置はhCG特異的抗体を多孔質層の上に固定して検出領域を形成することによって構築された。標識化された特異的な結合試薬に対するモノクローナル抗体は担体上に固定されてコントロール領域を形成した。ニトロセルロースは次に、BSA(0.1〜5.0%)、TRITON−X−100、BRIJ及びサッカロースを含むブロッキング溶液でブロッキングされた。材料は乾燥させられた。多孔質担体はケーシング中に置かれた。
【0069】
サンプリング装置及び分析装置は8%の水分率まで乾燥され、密封ポーチ中に密封して包装された。
【0070】
サンプリングスティックの多孔質層を含む端は尿の流れの下に10秒間置かれた。その後、サンプリングスティックは分析装置のサンプルウェル中に置かれた。サンプルと標識化された特異的な結合試薬とから形成される複合体は5分間移動させられ、その後、結果は検査窓で読みとられた。赤い線が検査窓の検出領域及びコントロール窓のコントロール領域で見られ、これはサンプル中のhCGの存在を示した。
【0071】
実施例2 妊娠検査の構築
実施例2はhCG妊娠検査に関し、そこでは特異的な標識化された試薬を含む多孔質層に取り付けられてこれを保護するための保護不透過性層がサンプリング装置に追加される。コントロール領域は検査の適切な性能を確実にするために追加される。装置で利用された成分は以下の通りである:

【0072】
図3及び4のサンプリング装置は上述の材料を用いて構築された。ポリエステル材料はまずBSA(0.1〜1.0%)、Tween20(0.01〜0.05%)及びトレハロース(0.5〜1.5%)を含むブロッキング溶液でブロッキングされた。乾燥後、hCG特異的な結合試薬を含む3μl/cmの金コンジュゲート溶液がブロッキングされたポリエステルに適用された。溶液はチューブポンプを用いて材料の端の5mm幅の領域に添加され、次に20%未満の相対湿度を有する乾燥室で乾燥させられた。乾燥は、8%未満の相対湿度を有する乾燥室で続けられた。
【0073】
ポリエステル材料は25mm×27mmの片に切られた。多孔質材料の四つの層は、ポリプロピレン製の丸い中空スティックの周りに巻かれ、0.1Nmの巻きつけトルク下でテープで取り付けられた。テープはまずポリプロピレンスティックに取り付けられ、次にポリエステルでスティックの周りを巻かれ、最後にテープは自分自身に取り付けられて多孔質材料上に保護被覆を形成した。構築された各スティックの周りにテープ(25mm×51mm)が巻きつけられたとき、それは針で80〜120回穿孔され、その中にベントを形成した。各ベントは0.1〜0.5mmの間のベントの間で異なる直径を有していた。含浸された標識化された特異的な結合試薬を有する端は、サンプリング装置の下側端に設定された。
【0074】
図7の分析装置はhCG特異的抗体を多孔質担体の上に固定して検出領域を形成することによって構築された。標識化された特異的な結合試薬に対するモノクローナル抗体は担体上に固定されてコントロール領域を形成した。ニトロセルロースは次に、BSA(0.1〜5.0%)、TRITON−X−100、BRIJ及びサッカロースを含むブロッキング溶液でブロッキングされた。材料は乾燥させられた。多孔質担体はケーシング中に置かれた。
【0075】
サンプリング装置及び分析装置の検査ストリップは8%の水分率まで乾燥された。検査ストリップ(ケーシング内の)及びサンプリング装置は一緒に密封ポーチ中に密封して包装された。
【0076】
サンプリング装置の多孔質層を含む端は尿の流れの下に10秒間置かれた。その後、サンプリング装置は分析装置のサンプルウェル中に置かれた。サンプルと標識化された特異的な結合試薬とから形成される複合体は5分間移動させられ、その後、結果は検査窓で読みとられた。赤い線が検査窓の検出領域及びコントロール窓のコントロール領域で見られ、これはサンプル中のhCGの存在を示した。
【0077】
実施例3 妊娠検査
実施例3はhCG妊娠検査に関し、そこでは特異的な標識化された試薬を含む多孔質層が不透過性層なしで取り付けられている。コントロール領域は検査の適切な性能を確実にするために追加される。
【0078】
ポリエステルフィルターは実施例2に記述されたようにして前処理された。フィルターの一つの層は木製の中実スティックの周りに接着剤で接着され、テープで被覆されて実施例2に記述されたようにして形成される保護層を形成した。分析装置は実施例2と同様に作成され、最後に装置は乾燥されて実施例2に記述のように包装された。
【0079】
検査は、hCGを含む液体サンプルにサンプリング装置を10秒間浸漬することによって行われた。スティックは軽く振られ、その後、分析装置のサンプルウェル中に置かれた。hCGの存在は、実施例2に記述されたようにして検出された。
【0080】
実施例4 受胎能検査検出システム
実施例4は、本発明がどのようにして受胎能検査検出システムのために適用されることができるかを記述する。
【0081】
hCG、LH及びFSHについての三つの標識化された特異的な抗体を含む金コンジュゲート溶液3μl/cmがセルロースフィルターに適用された。溶液はチューブポンプを用いて材料の一端の3mm幅の領域に添加され、次に20%未満の相対湿度を有する乾燥室で乾燥させられた。セルロースフィルターは、BSA(0.1〜1.0%)、Tween20(0.01〜0.05%)及びトレハロース(0.5〜1.5%)を含むブロッキング溶液でブロッキングされた。
【0082】
セルロースフィルターは25mm×27mmの片に切られた。セルロースフィルターの一つの片は、ポリプロピレン製の丸い中空スティックの周りに四つの層として巻かれ、テープで取り付けられた。含浸された結合試薬を有する端はサンプリング装置の下側端に設定された。
【0083】
図7の分析装置は、BSA(0.1〜1.0%)、Tween20(0.01〜0.05%)及びトレハロース(0.5〜1.5%)を含むブロッキング溶液でニトロセルロースの多孔質担体をブロッキングすることによって構築された。材料は乾燥させられ、その後、1mg/mlのhCG、LH及びFSH特異的な抗体が多孔質担体上に固定されて三つの異なる検出領域を形成した。標識化された特異的な結合試薬に対するモノクローナル抗体1mg/mlが担体上に固定されてコントロール領域を形成した。多孔質担体は乾燥されてケーシング中に置かれた。
【0084】
検査は、尿の液体サンプル中にサンプリングスティックの多孔質層を含む端を10秒間浸漬することによって行われた。サンプリングスティックは次に分析装置のサンプルウェル中に置かれた。サンプルと標識化された特異的な結合試薬とから形成される複合体は5分間移動させられ、その後、結果は検査窓で読みとられた。赤い線が検査窓の検出領域及びコントロール窓のコントロール領域で見られ、これはサンプル中のhCG、LH又はFSHの全て又はこれらの一以上の存在を示した。
【0085】
実施例5 性病のための検出システム
実施例5はHIV1,2のための検出システムに関する。
【0086】
サンプリング装置の多孔質材料として用いられるポリエステルフィルターは、BSA(0.1〜5.0%)、TRITON−X−100、BRIJ及びサッカロースを含むブロッキング溶液でブロッキングされた。乾燥後、HIV1及びHIV2の両方を認識するポリペプチドを含む2μl/cmの着色されたラテックス溶液が、ブロッキングされた材料に適用された。溶液は4mmのフィルターに添加され、次に20%未満の相対湿度を有する乾燥室で乾燥された。
【0087】
ポリエステルフィルターは25mm×27mmの片に切られた。ポリエステルフィルターの一つの片は、木製の丸い中空スティックの周りに3回巻かれ、テープ(25mm×51mm)で取り付けられた。構築された各スティックの周りにテープが巻きつけられたとき、それは針で80〜120回穿孔され、その中にベントを形成した。各ベントは0.1〜0.5mmの間のベントの間で異なる直径を有していた。
【0088】
二つの検査窓及び一つのコントロール窓を有する分析装置は、0.5μlのHIV1組み換え抗原及び0.5μlのHIV2組み換え抗原を多孔質担体上に固定してニトロセルロースの多孔質担体上に検出領域を形成することによって構築された。材料は乾燥され、その後、ニトロセルロースは、BSA(0.1〜5.0%)、TRITON−X−100、BRIJ及びサッカロースを含むブロッキング溶液でブロッキングされた。標識化された特異的な結合試薬に対するモノクローナル抗体は、多孔質担体上に固定され、コントロール領域を形成した。多孔質担体は乾燥され、ケーシング中に置かれた。コントロール領域は、分析装置のサンプルウェルから最も離れた場所に置かれた。
【0089】
検査は、サンプリング装置の多孔質層を含む端を血清サンプル中に浸漬することによって行われた。サンプリング装置は分析装置のサンプルウェル中に置かれた。サンプルと標識化された特異的な結合試薬は5分間移動させられ、その後、結果は検査窓で読みとられた。結果は5分後及び10分後に読みとられた。その結果、赤い線が検査窓の検出領域及びコントロール窓のコントロール領域で見られ、これはサンプル中のHIV1,2の存在を示した。
【0090】
実施例6 アレルゲンのための多数のチャネル検査
実施例6はアレルゲン検査のための本発明の使用を記述する。同じサンプルは、多数のチャネルを有する分析装置を用いて幾つかのアレルゲンのために同時に検査される。
【0091】
サンプリング装置の多孔質材料として用いられるポリエステルフィルターは、BSA(0.1〜5.0%)、TRITON−X−100、BRIJ及びサッカロースを含むブロッキング溶液でブロッキングされた。乾燥後、IgE分子を特異的に認識する抗IgE抗体で被覆された着色されたラテックス粒子の水溶液10μlが、ブロッキングされた材料に適用された。溶液は全フィルターに添加され、次に20%未満の相対湿度を有する乾燥室で乾燥された。
【0092】
ポリエステルフィルターは10mm×20mmの片に切られた。ポリエステルフィルターの一つの片は、ポリプロピレン製の丸い中空スティックの周りに4回巻かれ、テープで取り付けられた。
【0093】
八つの分離されたチャネルを有する分析装置は、ニトロセルロースの多孔質担体中にチャネルを形成することによって構築され、八つの異なる特異的なアレルゲン0.5μlを含むマイラーフィルムが多孔質担体上に固定されて分析装置の各チャネル中に検出領域を形成した。材料は乾燥され、その後ニトロセルロースはBSA、HEXA及びトレハロースを含むブロッキング溶液でブロッキングされた。多孔質担体は乾燥された。
【0094】
検査は、サンプリングスティックの多孔質層を含む端を血清の液体サンプル中に浸漬することによって行われた。サンプリングスティックはサンプリング適用部位と接触させられ、サンプルと標識化された特異的な結合試薬は5分間移動させられ、その後、結果は検出領域中の可視的な点として読みとられ、これはサンプル中のアレルゲンの存在を示した。
【図面の簡単な説明】
【0095】
【図1】本発明によるサンプリング装置の透視図である。
【図2】サンプリング装置を下側から見た図である。
【図3】本発明によるサンプリング装置の別の透視図である。
【図4】本発明による被覆された多孔質担体の拡大した透視図である。
【図5】サンプリング装置の別の実施態様を下側から見た図である。
【図6】サンプリング装置及び分析装置の側面図である。
【図7】分析装置を上側から見た図である。
【図8】分析装置の別の実施態様を上側から見た図である。
【技術分野】
【0001】
本発明は、免疫化学的サンプリング装置に関し、特に、家庭での使用、医師の診療所での使用及び/又は使用者から最小レベルの技術しか必要としない技術的に訓練されていないスタッフによる使用のために好適な装置に関する。
【背景技術】
【0002】
免疫拡散に基づく方法及び装置は、例えばUS4757002、US3990852、及びUS4562147から公知である。横方向の流れに基づく免疫クロマトグラフィー法は、EP0291194、EP0284232、EP0250137、US5250412、US5084245、US5760315、US6375896及びWO86/03839から公知である。
【0003】
US4562147は、ブタ及び他の動物における偽狂犬病抗体の検査のための半径方向免疫拡散酵素アッセイ方法を提供する。可溶化された非感染性ブタ偽狂犬病抗原の接着性被覆を下に含む寒天検査プレートが提供される。検査結果は、公式なウイルス中和検査によって得られる力価と相関する着色領域の直径から得られる。
【0004】
EP0291194は、特異的な結合が関与するアッセイ、特に免疫アッセイ及びそのための装置に関する。開示されている分析検査装置は、乾燥多孔質担体を含む中空のケーシングを含み、このケーシングは湿気を吸収しやすいサンプル受容部材を介してケーシングの外部と間接的に連通する。担体は、第一領域に標識化された特異的な結合試薬を、そして第一領域からは空間的に分離された第二領域(検査領域)に同じ分析対象物のための未標識の特異的な結合試薬を含む。使用にあたって、サンプル溶液は検査が行われるときに検査装置に直接適用され、これは検査領域をオーバーフローさせる危険性にさらす。
【0005】
EP0284232は、液体サンプル中の分析対象物の存在又は不存在を決定するための固相アッセイを提供する。この発明の検査ストリップは、第一部分に移動可能に支持されたトレーサーと、第二部分(検査領域)に固定された結合剤とを有する。使用にあたって、サンプル溶液は検査が行われるときに検査装置に直接適用され、これは検査領域をオーバーフローさせる危険性にさらす。
【0006】
EP0250137は、サンプル中のリガンドを検出するためのコロイド金を用いた免疫アッセイを記述し、そこでは膜ストリップはサンプルと接触させられ、同時に又は続いてリガンド結合パートナー又はコロイド金で標識化されたリガンドを含む液体試薬と接触させられる。検査を行うためには、使用者は標識化されたリガンドを含む液体試薬を膜ストリップに別個に適用しなければならない。
【0007】
US5250412は、分析対象物を収集して分析するための方法及びキットを記述する。サンプルは綿棒で収集され、この綿棒に対して、使用者は標識化された成分を含む別個の液体を適用して次に洗浄溶液を適用しなければならない。
【0008】
US5084245は、綿棒の吸収性先端に集められた標本を用いた免疫学的反応に基づく診断手順を行うための装置を提供する。使用されたとき、綿棒は、検査のための必要な試薬を含む感受性要素の方へ通路を通って押される。リブが通路に配置されており、先端を絞り、綿棒の流体を圧搾する。結果は、案内部材をベース成分から除去して感受性要素を露出することによって可視的に観察可能になる。
【0009】
US5760315は、吸収性パッドを用いるサンプルの収集のための装置を提供する。パッドは、対応する検査ストリップの検査領域に結合しない過剰の標識化された結合試薬を除去するための洗浄剤として機能するのに十分な体積のサンプル流体のための流体貯蔵所として機能する。様々な疎水性度及び多孔度の材料の複合体アレイは、装置中において、サンプル流体をその初期の収集中に、吸収パッド上に又は吸収パッドの近くに配置された標識化された試薬から離れる方向に向けるために利用される。
【0010】
US6375896は、物質の免疫化学的検出のための綿棒分析装置を記述する。綿棒分析装置の綿棒ペンは、サンプルの収集のために用いられる。サンプルは、別個の溶離液体を用いて装置から溶離されなければならない。
【0011】
WO86/03839は、固相拡散アッセイを例示し、そこではサンプルはまず標識化された結合物質と混合され、次に固定された吸収性分子を有する支持体の領域に適用され、そこで拡散させられる。拡散パターンは可視化され、測定される。
【0012】
背景技術の記載から、免疫アッセイを行うための多くの異なる検査キットが利用可能であることが明らかである。幅広い種類の検査キットが商業的に入手可能であり、それらの多くは家庭での使用を意図されている。それらの便利な形式にもかかわらず、それらが誤った様式で用いられると誤りが生ずる危険性が高い。この危険性は、検査装置がサンプリングのために用いられる場合、切迫しており、これは非実用的及び不便の両方でありうる。特に、検査装置がサンプリング装置として用いられる場合、又はサンプルを収集するために用いられる場合、感受性試薬及び分析装置の構造が破壊される又は妨害される危険性がある。
【0013】
本発明は、免疫化学的検査のための改良された検出システムを提供し、これは液体サンプルが収集されることを可能にしかつ標識化された特異的な結合試薬が制御された様式で移行されて可動化されることを可能にするサンプリング装置を含む。二部システムのため、分析装置は液体サンプルとは直接接触せず、それにより分析装置中の試薬及び分析装置の構造がサンプリング手順によって破壊されたり妨害される可能性が最小化される。
【0014】
二成分免疫アッセイ装置は、こぼれや汚染の危険性なしに使用者が液体サンプルを容易に収集してそれをアッセイの実行のために検査装置へ移行させることを可能にする。
【発明の開示】
【0015】
本発明は、免疫化学的サンプリング装置、キット及びこのサンプリング装置を横方向流れ免疫アッセイにおいて使用する方法を提供する。装置は、多孔質層によって近位端の一つで包囲された細長い支持体を含み、この多孔質層は所望により不透過性保護層を有し、前記多孔質層は標識化された特異的な結合試薬を含み、これは液体サンプルによって活性化され、サンプリング装置が多孔質担体を含む分析装置(結果装置)と接触されたときに制御された様式で可動化される。
【0016】
好ましい実施態様では、装置は細長い支持体(即ち、固体支持体)を含み、これに多孔質担体が部分的に巻きつけられ、次に実質的に不透過性の疎水性カバーで被覆される。遠位端で、多孔質担体は標識化された結合試薬(例えば抗体又は抗原)を含み、これはサンプリング装置が分析装置の検査ストリップ要素と接触状態にもたらされた(例えば検査ストリップ要素上に押された)ときに多孔質担体から液体サンプルと共に制御された流れの中へと解放される。
【0017】
別の好ましい実施態様では、免疫アッセイを行うための免疫化学的サンプリング装置は、(a)多孔質担体によって包囲された細長い支持体、(b)多孔質担体に解放可能なように結合された標識化された結合試薬、及び(c)多孔質層(即ち多孔質担体)上に配置された不透過性保護層(即ち疎水性カバー)を含む。不透過性保護層は、圧力平衡化手段をさらに含み、標識化された結合試薬は、液体サンプルと混合されたときに多孔質層が分析装置の検査ストリップと流体連通状態に置かれるまで多孔質内に保持される。
【0018】
また、液体サンプル中の分析対象物の存在又は不存在を決定する方法が本発明において提供される。この方法は、診断的サンプリング装置を液体サンプルと接触させ、診断的サンプリング装置を分析装置と接触させ、液体サンプルを標識化された特異的な結合試薬又はその反応生成物と共に診断的サンプリング装置から分析装置の多孔質担体へと移動又は流れさせるのに十分な時間放置し、そこで液体サンプルの反応生成物と標識化された結合試薬は分析装置の検出領域の方へ移動し、そして検出領域中の分析対象物の存在又は不存在を決定することによって結果を読み取るステップを含む。
【0019】
使用において、サンプルが多孔質層の近位端と接触するようにサンプリング装置の巻きつけられた部分は流体サンプルと接触状態にもたらされる(例えばサンプルの流れ中への浸漬又は導入によって)。この近位端は不透過性保護層の下に露出されている。多孔質層は、多孔質層中へのサンプルの流れ並びに分析装置と接触している多孔質層から外への標識化された結合試薬と混合されたサンプルの流れを最適化するように設計された様式で細長い支持体(これはその巻きつけられていない端でハンドルとして作用する)の周りに巻きつけられる。多孔質層を通るサンプルの流れの体積及び速度は、不透過性保護層中に与えられている圧力平衡化手段によって同様に制御される。
【0020】
特に、一旦サンプル流体がサンプリング装置(そこでサンプルは標識化された結合試薬と混合する)に収集されると、それはサンプリング装置の遠位端を分析装置の検査ストリップと接触状態にもたらすことによって分析装置中に解放されるまで保持される。サンプリング装置から外へのサンプル流体の流れは、検査ストリップとの接触によって媒介される毛管作用又は拡散を介して生じ、機械的に増大されることができる(例えばサンプリング装置に穏やかな圧力を適用することによって)。
【0021】
さらに、免疫化学的サンプリング装置の製造方法が提供される。この方法は、多孔質層の一以上の層を細長い支持体の周りに巻きつけてその状態で多孔質層を保持し、次に多孔質層に不透過性保護層を巻きつけてその状態で不透過性保護層を保持するステップを含む。多孔質材料は、上に標識化された結合試薬が解放可能なように結合された多孔質材料からなり、不透過性保護層は圧力平衡化手段を含む。
【0022】
免疫化学的分析で用いるためのキットは、免疫化学的サンプリング装置と少なくとも一つの結合試薬が配置されている分析装置とを含む。分析装置の多孔質担体は、点又は領域(検査線)として直接的に又は間接的に固定された少なくとも一つの特異的結合試薬を含む。さらに、多孔質担体上の一以上の点又は領域は制御領域として作用することができる。多孔質担体が検出領域を含む一以上の多孔質通路(これはサンプル溶液によって浸透されることができる)を含む分析装置との関連のみならず、多孔質担体が点又は領域として固定されたチャネル当たり少なくとも一つの特異的な結合試薬を含む好適な方法によって所望により作られた二以上のチャネルを含む分析装置との関連でもサンプリング装置は用いられることができることは当業者には自明である。
【0023】
好ましくは、分析装置は、結合試薬が結合する必要がないサンプル適用部位の下流の検査領域内に結合試薬が固定された検査ストリップを含む。最も好ましくは、分析装置は検査ストリップのための固体ハウジングをさらに含み、このハウジングはくぼみを有し、その中に検査ストリップのサンプル適用部位がサンプリング装置に適用された穏やかな圧力下で偏向され、多孔質層から外へのサンプルの流れを容易にする。
【0024】
免疫化学的サンプリング装置は、多孔質担体を含む分析装置における標識化された特異的な結合試薬の制御された可動化を可能にする。それにより、液体サンプル中の異なる分析対象物を検出するための一層感受性の方法が提供される。検出されるべき分析対象物は、細菌、ウイルス、真菌及び寄生生物の抗原又はこれらに対する抗体、又はそれらの成分及び生成物(疾患特異的抗体(例えばヘリコバクター・ピロリ、A型肝炎、HIV1,2、呼吸器疾患などに対する抗体)を含む);尿中に排出される抗原(黄体形成ホルモン(LH)、卵胞刺激ホルモン(FSH)及びヒト絨毛膜刺激ホルモン(hCG);又は流体サンプル中の麻薬又は麻薬代謝物の存在の指標である抗原)であることができる。
【0025】
本発明の装置及び方法は、妊娠、閉経、受胎能、甲状腺刺激ホルモン、トキソプラスマ症、癌抗原、呼吸器疾患、アレルギー、心筋梗塞、及び薬物検査などを含む多数の異なる検査のために用いられることができる。
【0026】
検査結果の増大された確実性以外の本発明のサンプリング装置及び検出システムの他の利点は;サンプリング装置及び分析装置の小さい形式(これは材料の節約に導く)、少ない廃棄生成物及び減少した運送費用であり、従って環境的に優しい製品を提供することができる。さらに、この検査システムは使用するのが容易であるので、それは家庭の使用を可能にする。分析装置は液体サンプルと直接接触しないので、オーバーフローは回避され、検査の増大された信頼性が得られる。サンプル流体は分析装置に直接適用されないので、検査ストリップの飽和及び/又は検査領域の汚染は回避される。さらに、本発明のサンプリング装置及び分析装置は、これらの装置が乾燥しているという事実のため、及びそれらが密封して貯蔵されることができるという事実のため、貯蔵しやすい。要するに、本発明は、使用及び製造が他に例を見ないほど簡単である、分析対象物の存在についてサンプル流体を収集して検査するための装置を提供する。
【0027】
図面の簡単な記述
図1は、本発明によるサンプリング装置の透視図である。
図2は、サンプリング装置を下側から見た図である。
図3は、本発明によるサンプリング装置の別の透視図である。
図4は、本発明による被覆された多孔質担体の拡大した透視図である。
図5は、サンプリング装置の別の実施態様を下側から見た図である。
図6は、サンプリング装置及び分析装置の側面図である。
図7は、分析装置を上側から見た図である。
図8は、分析装置の別の実施態様を上側から見た図である。
【発明を実施するための最良の形態】
【0028】
本発明は、横方向流れ検査のためのサンプルを収集するサンプリング装置を提供する。サンプリング装置は、細長い支持体(コアスティック)、及びコアスティックの一端の周りに適用された多孔質層を含む。多孔質層は、標識化された特異的な結合試薬を含み、かつ多孔質材料の反応性基がサンプル又は標識化された特異的な結合試薬と反応するのを防止するブロッキング溶液で処理されている。サンプリング装置は、検査されるべき液体と接触されることができ、続いて、点又は領域として固定された少なくとも一つの特異的な結合試薬を含む分析又は結果装置の多孔質担体と接触させられる。
【0029】
さらに、液体サンプル中の分析対象物の存在又は不存在を決定する免疫化学的方法が提供される。この方法は、サンプリング装置に液体サンプルを添加し、サンプリング装置を分析装置の検査ストリップのサンプル適用部位と流体連通接触状態に置き、そしてサンプル及び標識化された結合試薬がサンプリング装置から検査ストリップまで移動するのに十分な時間放置するステップを含む。検査結果は、分析対象物のための少なくとも一つの結合試薬がサンプル適用部位の下流の検査部位を形成するように検査ストリップ上に固定されている検査部位で観察される。液体サンプルは、分析装置の検査ストリップと流体連通接触状態にもたらされるまでサンプリング装置中に保持される。
【0030】
異なるタイプの分析装置が背景技術で記述されている。多数のチャネルを有する装置は、幾つかの分析対象物を同時に検査することを可能にする。異なる分析対象物に対して特異的なマーカーは、異なる生成物を形成するように一緒にグループ化されることができる。多数のチャネル装置は、検査されたサンプルが移動することができるチャネルの網状構造を生じさせるために撥水性処理などにより処理された多孔質担体を含む。異なる特異的結合試薬はそれぞれのチャネル中に結合されることができる。本発明の好ましい実施態様では、多数のチャネルを有する分析装置は、同一のサンプルを幾つかの分析対象物について同時に検出するために用いられる。この装置のそれぞれのチャネルは、そこに幾つかの検出領域及び/又はコントロール領域を有することができる。
【0031】
本発明の一実施態様では、分析装置は検出領域及び制御領域の両方を含む。さらなる検出領域は、定量的検査を行うために追加されてもよい。本発明の分析装置は、それが移動化可能な特異的試薬を欠くという点で従来技術とは異なる。
【0032】
本発明のサンプリング装置上の標識化された結合試薬の存在は、さらなる標識化された結合試薬が検査ストリップ又は分析装置内の他の構造(例えばサンプル適用パッド)上に配置された分析装置を用いる必要性を否定する。このように、本発明によって使用される好ましい分析装置は、少なくとも一つの検査領域(固定された結合試薬からなる)及び所望によりコントロール領域も有する検査ストリップを含むものである。
【0033】
当業者は、横方向流れ免疫アッセイで使用するための検査ストリップ並びに結合試薬及びコントロール試薬を固定する方法(サンドイッチ形式及び競合形式の両方での)をよく知っているだろう。これらは全て本発明のサンプリング装置で利用されることができ、そこから標識化された結合試薬及びサンプルが供給される。
【0034】
サンプリング装置の構築
サンプリング装置の構築は、多孔質材料をブロッキング溶液で処理し、乾燥させ、標識化された特異的な結合試薬を多孔質材料に添加し、乾燥させ、多孔質材料を細長い支持体の周りに取り付けて多孔質層を形成させ、不透過性材料層を多孔質層の周りに取り付けて最後に乾燥させて装置を包装するステップを含む。まず多孔質材料を支持体の周りに取り付け、その後ブロッキング溶液及び標識化された特異的な結合試薬をサンプリング装置の多孔質層に浸漬又は適用することも可能である。
【0035】
多孔質材料の不活性化
ブロッキング溶液は、アルブミン(BSA、ウシ血清アルブミン)及びカゼイン又はPEG(ポリエチレングリコール)、PVA(ポリビニルアルコール)及びPVP(ポリビニルピロリドン)の如き天然又は合成ポリマー、TWEEN20、HEXA(ヘキサンスルホン酸)、TRITON−X−100、SDS及びBRIJの如き非イオン性界面活性剤、及び糖(例えばグルコース、スクロース及びトレハロース又はそれらの誘導体)の如き保存剤を含む混合物であるが、このブロッキング溶液は、多孔質材料の反応性部位を不活性にするために多孔質層に添加される。ブロッキング溶液はポンプによって添加されてもよいし、又は多孔質材料はブロッキング溶液中に浸漬されてもよい。次のステップの前に、多孔質材料は乾燥される。
【0036】
特異的な標識化された試薬の添加
サンプリング装置の多孔質層は、特異的な標識化された試薬で含浸される。多孔質層の全体を含む多孔質材料の最外表面層の全て(及びいかなる下に横たわる層の一以上)は標識化された結合試薬で含浸されることができる。層全体が含浸されることができるが、好ましくは標識化された特異的な結合試薬は層の下端に含浸される。バックグラウンド干渉を最小化して検査時間を短縮するため、含浸は、多孔質層の最遠位端での多孔質材料の表面積の好ましくは半分未満、最も好ましくは約20〜40%に制限される。
【0037】
標識化された結合試薬は、当該技術分野で周知の方法、例えば当該技術分野で周知の方法を用いた特異的な結合試薬での標識粒子の被覆によって調製されることができる。特異的な及び非特異的な(好ましいのは前者である)抗体、抗体断片、組み換え抗体、組み換え抗体断片、抗原、レクチン、受容体及び/又はリガンドは好適な結合試薬であり、それらは着色されたラテックス、金、他の金属、染料、蛍光産生物質、又は超常磁性粒子の如きいかなる好適な標識にも取り付けられることができる。しかし、色素産生物質、特に蛍光色素産生物質及び酵素的標識をマーカーとして使用することも可能である。もしサンプルが異なる結合特異性の一以上の分析対象物について検出され、同じ特異的な結合試薬が全てについて用いられることができないなら、幾つかの異なる標識化された特異的な結合試薬の組合せを用いることが可能である。
【0038】
標識化された特異的な結合試薬は、針を通して正確な体積の試薬を送出するチューブポンプを用いて適用されることができ、又は多孔質材料は浸漬されることができる。多孔質材料は相対湿度が20%未満の乾燥室で乾燥され、さらに、相対湿度が8%未満の乾燥室で乾燥される。
【0039】
標識化された結合試薬組成物及び/又は多孔質材料は、サンプル流体を用いた結合試薬の多孔質材料から溶液中への(又は粒状の標識化された結合試薬の場合は懸濁液中への)解放を容易にするための薬剤で処理されることができる。当業者は、本発明で利用されることができる横方向流れアッセイで用いるのに好適な解放剤(糖、カゼイン及び界面活性剤の如き)に熟知しているであろう。
【0040】
材料の取り付け
多孔質材料の一以上の層は、例えば木材又はプラスチック(ポリプロピレン(PP)及びポリ塩化ビニル(PVC)の如き)製の細長い支持体(コアスティック)の周りに取り付けられる。一以上の層は一度に取り付けられることができ、又は多孔質材料のストリップは支持体スティックの周りに巻かれることができる。多孔質材料はテープによって取り付けられることができ、このテープはまず細長い支持体に取り付けられ、次に多孔質材料と共にスティックの周りに巻かれ、最後にテープはそれ自身に取り付けられる。当業者は多孔質材料を固体表面に取り付ける代替手段、例えば不活性な接着剤や熱結合に熟知しているであろう。ブロッキング溶液及び標識化された結合試薬は、多孔質層が細長い支持体に取り付けられる前又は後に多孔質層に適用されることができる。支持体スティックは細長い丸められた、平坦な又は平面状のスティックであることができ、これは中実又は中空であることができる。テープの如き不透過性材料の一以上の層は多孔質層の周りに取り付けられる。
【0041】
好ましくは、細長い支持体は、サンプリング装置から分析装置への標識化された結合試薬の流れを調整するために一以上の、好ましくは一〜五層のテープを含む不透過性層及び多孔質層によってその近位端で包囲される。サンプリング装置の多孔質層は、一以上の、好ましくは一〜五層の多孔質材料も含む。多孔質材料は、紙、ガラス繊維、ナイロン、ポリエステル又はセルロース及びそれらの誘導体からなる群の材料から選択され、最も好ましくはこれらの材料の湿気を吸収しやすい及び/又は親水性の形態である。
【0042】
別の好ましい実施態様では、不透過性保護層は、被覆されるべき多孔質層の部分の周りに巻きつけられ、その上に保持(例えば不活性な接着剤で)される。不透過性保護層はその遠位及び/又は近位端では親水性であることができるが、実質的に疎水性でありかつ不透過性である。好都合には、不透過性保護層は透明なポリエステルテープ、マイラーフィルム、又は他の不透過性材料からなることができる。所望により、例えばサンプルの収集についての指示及び標識化された結合試薬によって結合されることができる分析対象物の正体を表示する記号を有する疎水性の印刷紙(図示せず)が、不透過性保護層と多孔質層の間に配置されることができる。不透過性保護層は、複数の小さなベント8をさらに与えられることができ、これらはそれぞれ約0.1mm〜0.5mmの最大直径を有し、用いられるテープの25mm×51mmの片にわたって分布され、不透過性保護層を形成する。好ましくはベントは不透過性保護層の表面積の1〜50%にわたって与えられ、最も好ましくはベントは不透過性保護層の表面積の10〜25%にわたって与えられる。
【0043】
ベントは、多孔質層を通る流体の流れの体積及び速度を制御する役割を有する。本発明はベントがサンプリング装置中の流体の流れを制御する作用機構に制限されるものではないが、ベントは、サンプル流体が適用されたときの多孔質層内外の圧力を平衡化し、それにより圧力勾配(それに沿って流体の流れが標識化された結合試薬を洗い流してしまう危険性が高まる)の形成を回避する役割を有すると信じられる。実施において、ベントは、サンプリング装置が分析装置の検査ストリップ要素と流体連通接触状態におかれるまでサンプル流体を多孔質層中に保持する役割を有する。
【0044】
本発明の別の好ましい実施態様では、多孔質層は細長い支持体の周りにしっかりと巻きつけられているが、可能な最大限度では巻きつけられていない。材料が細長い支持体の周りに巻きつけられたときに材料中にいくらかのゆるみを残すことにより、サンプリング装置が好適な分析装置と接触状態にもたらされたときの多孔質層からのサンプル流体の測定される流れを促進する。
【0045】
例えば、全直径の観点から見ると、0.1Nmのトルク(好ましくは0.05〜0.5Nmの好適なトルクの範囲内)下で巻きつけられている本発明のこの実施態様による例示的なサンプリング装置は、存在する以下の成分と共に4.7mm±0.1mmの全直径を有するであろう:(a)51mmの幅及び0.03mmの厚さを有する不透過性保護層(ポリエステルテープ);(b)27mmの幅及び398μmの厚さを有する多孔質担体(不織布ポリエステル);及び(c)15mmの幅及び115μmの厚さを有する印刷された紙。これら全ては、(d)2mmの厚さを有する細長い支持体(プラスティックスティック)の周りに巻きつけられている。当業者はこれらの一般的な寸法を本発明によって構築された異なる寸法のサンプリング装置に容易に適合させることができるであろう。
【0046】
装置の乾燥及び包装
装置は8%以下の水分率まで乾燥され、好適な分析装置(結果記録検出装置)との組合せでキットで又は分離されて密封して包装される。
【0047】
分析装置の調製
本発明のサンプリング装置と共に使用するのに好適な分析装置であって検出システムの結果記録検出装置である分析装置は、ブロッキング前の装置の多孔質担体に直接的に又は間接的に一以上の特異的な結合試薬及び所望によりコントロール試薬を固定することによって調製されることができる。用いられるブロッキング溶液はサンプリング装置について用いられるものと同じものであることができる。多孔質担体は所望により不透過性裏打ち上に又はケーシングもしくはハウジング中に置かれることができる。
【0048】
多数のチャネルを有する装置は、異なる分析対象物(又はコントロール)の検査のための異なるチャネルを得るための好適な方法で多孔質材料を処理することによって調製されることができる。幾つかの分析対象物は一つの単一の検査によって同じサンプルから検出されることができる。
【0049】
好ましい実施態様では、八つのチャネルが多孔質担体上に好適な方法(例えばブロッキング、フォトリソグラフィー又はエッチング)によって作成される。チャネルは領域によって相互から分離されており、これらの領域のそれぞれはこれらの領域を通るサンプル流体の流れを防止するために疎水性に処理される。各チャネルは標識化されていない結合試薬からなる検査領域又は点を含む。また、サンプリング装置が多孔質担体と接触状態に置かれるサンプル適用部位も示される。
【0050】
分析装置の特異的な試薬は、抗体、抗体断片、組み換え抗体、組み換え抗体断片、抗原、レクチン、受容体及び/又はリガンドを含む。サンプリング装置に適用可能な標識は、着色されたラテックス、金、金属、染料、蛍光産生物質、特異的な結合剤で被覆された超常磁性粒子を含む。色素産生物質、特に蛍光色素産生物質及び酵素的標識もマーカーとして用いられることができる。
【0051】
分析装置の多孔質材料は、ニトロセルロース、紙、ガラス繊維、ナイロン、ポリエステル、ポリスルホネート、又はセルロース、及びこれらの誘導体からなる群から選択される。
【0052】
検出システムの使用
サンプリング装置は、尿の流れの下で装置を保持することによって、又は液体サンプルにサンプリング装置を浸漬することによって、又はサンプルをピペットで添加することによって使用されることができる。もしサンプリング装置が尿の流れの下に置かれるのなら、好ましい時間は2〜15秒間であり、さらに好ましくは5〜15秒間であり、最も好ましくは5〜10秒間である。もしサンプリング装置が液体サンプルに浸漬されるのなら、好ましい時間は2〜30秒間であり、さらに好ましくは10〜20秒間であり、最も好ましくは10〜12秒間である。もし液体サンプルがピペットによって添加されるのなら、好ましいサンプル量は2〜40滴であり、さらに好ましくは5〜20滴であり、最も好ましくは5〜15滴である。10滴は約0.5mlに等しい。乾燥及びサンプル適用後、サンプリング装置は装置の巻きつけられた部分を下に向けて実質的に垂直方向に維持されることが好ましい。
【0053】
一旦サンプルが収集されたなら、サンプリング装置の最遠位端は分析装置の検査ストリップと接触状態に置かれ(接触させられるか又は接触状態で放置される)、液体サンプルを標識化された特異的な結合試薬又はその反応生成物(複合体)と共に診断的サンプリング装置から分析装置の多孔質担体へと移動又は流れさせるのに十分な時間放置する。液体サンプル及び標識化された結合試薬は分析装置の検査領域に移動し(例えば拡散又は毛細管作用により)、そこでサンプル流体中の分析対象物の存在又は不存在が決定される。結果は直接可視的に(裸眼により)、又は結果の記録を可能にする好適な器具により読み取られることができる。
【0054】
液体サンプルは、尿、血液、血清、血漿、唾液、又はサンプル緩衝溶液であることができる。特に好ましい実施態様では、液体サンプルは尿である。
【0055】
サンプリング装置及び分析装置の構造
図1は、典型的なサンプリング装置を表す。細長い中空の支持体1は、その近位端の一つで多孔質材料2の多孔質層によって包囲されている。多孔質材料は、その下側端に標識化された特異的な結合試薬3を含む。
【0056】
図2は、下側から見たサンプリング装置を示す。多孔質材料2の四つの層が細長い支持体1の周りに巻かれている。多孔質層は不透過性保護層(疎水性被覆)4によって保護されている。
【0057】
図3は、不透過性保護層によって被覆された典型的なサンプリング装置を示す。多孔質層2は、細長い支持体1の遠位端の周りに配置されており、不透過性保護層4によって部分的に被覆されている。多孔質層2は不透過性保護層4によって軸的に被覆されており、その対向する近位端5及び遠位端6の表面のみが露出されている。
【0058】
図4は、不透過性保護層中のベントが示されたサンプリング装置を表す。不透過性保護層4は多数の小さいベント7を与えられている。
【0059】
図5は、サンプリング装置の下側から見た別の実施態様を示す。中空の支持体1は多孔質材料2の三つの層によって包囲されており、多孔質材料は不透過性保護層4の一以上の層によって包囲されている。
【0060】
図6は、本発明の典型的な検出システムを表す。多孔質材料2によって包囲された支持体1を含むサンプリング装置は、サンプルウェル(サンプル適用口)9、検査窓10及びコントロール窓11を有するケーシング8を含む分析装置と接触させられている。
【0061】
図7は、上側から見た典型的な分析装置を示す。ケーシング8(例えば不透過性プラスチックハウジング)(その中に検査ストリップ(図示せず)が配置されている)はサンプルウェル9を含み、そこにサンプリング装置がそれが液体サンプルと接触させられたときに置かれる。多孔質層の検出領域は検査窓10中に置かれており、陽性の結果の場合には可視的な反応がそこで見られることができる。多孔質層のコントロール領域はコントロール窓11中に置かれており、そこでは検査が行われたときはいつでも可視的反応が見られるべきである。換言すれば、ハウジング8は、検査領域上に配置された窓9(それを通して検査結果が見られることができる)、及びコントロール領域上に配置された窓10(それを通してコントロールの結果が見られることができる)を含む。サンプル適用口11は、結合試薬が結合していない検査ストリップの一部分の上に配置されており、本発明のサンプリング装置のその中への挿入のために与えられている。
【0062】
図8は、分析装置の別の実施態様を示す。八つのチャネル12が好適な方法によって多孔質層上に作られている。装置のチャネルは処理領域13によって相互から分離されている。各チャネル12は検出領域又は点14を含む。また、サンプリング装置が接触されるべき場所15(サンプル又はサンプリング装置受入口、又はサンプル適用口)が示されている。
【0063】
図及び実施例で記述される実施態様は、本発明の範囲内にある実施態様の例としてのみ見られるべきものである。それらは特許請求の範囲によって規定される本発明の範囲を限定するものとみなされるべきではない。
【実施例】
【0064】
実施例1 妊娠検査
実施例1はhCG妊娠検査に関し、そこでは特異的な標識化された試薬を含む多孔質層に取り付けられてこれを保護するための保護不透過性層がサンプリング装置に追加される。コントロール領域は検査の適切な性能を確実にするために追加される。
【0065】
図1のサンプリング装置は、金コンジュゲートとhCG抗原の間の第一反応のためのプラットフォームとしての多孔質ポリエステルフィルター材料を用いることによって構築された。長さ100メートルで幅10mmのロールとして得ることができるポリエステル材料が用いられた。
【0066】
ポリエステル材料はまずBSA(0.1〜1.0%)、Tween20(0.01〜0.05%)及びトレハロース(0.5〜1.5%)を含むブロッキング溶液でブロッキングされた。乾燥後、hCG特異的な結合試薬を含む3μl/mmの金コンジュゲート溶液がブロッキングされたポリエステルに適用された。溶液はチューブポンプを用いて材料の端の5mm幅の領域に添加され、次に20%未満の相対湿度を有する乾燥室で乾燥させられた。乾燥は、8%未満の相対湿度を有する乾燥室で続けられた。
【0067】
ポリエステルフィルターは10mm×30mmの片に切られた。多孔質材料の四つの層は、ポリプロピレン製の丸い中空スティックの周りに巻かれ、テープで取り付けられた。テープはまずポリプロピレンスティックに取り付けられ、次にポリエステルでスティックの周りを巻かれ、最後にテープは自分自身に取り付けられた。含浸された標識化された特異的な結合試薬を有する端は、サンプリング装置の下側端に設定された。
【0068】
図7の分析装置はhCG特異的抗体を多孔質層の上に固定して検出領域を形成することによって構築された。標識化された特異的な結合試薬に対するモノクローナル抗体は担体上に固定されてコントロール領域を形成した。ニトロセルロースは次に、BSA(0.1〜5.0%)、TRITON−X−100、BRIJ及びサッカロースを含むブロッキング溶液でブロッキングされた。材料は乾燥させられた。多孔質担体はケーシング中に置かれた。
【0069】
サンプリング装置及び分析装置は8%の水分率まで乾燥され、密封ポーチ中に密封して包装された。
【0070】
サンプリングスティックの多孔質層を含む端は尿の流れの下に10秒間置かれた。その後、サンプリングスティックは分析装置のサンプルウェル中に置かれた。サンプルと標識化された特異的な結合試薬とから形成される複合体は5分間移動させられ、その後、結果は検査窓で読みとられた。赤い線が検査窓の検出領域及びコントロール窓のコントロール領域で見られ、これはサンプル中のhCGの存在を示した。
【0071】
実施例2 妊娠検査の構築
実施例2はhCG妊娠検査に関し、そこでは特異的な標識化された試薬を含む多孔質層に取り付けられてこれを保護するための保護不透過性層がサンプリング装置に追加される。コントロール領域は検査の適切な性能を確実にするために追加される。装置で利用された成分は以下の通りである:

【0072】
図3及び4のサンプリング装置は上述の材料を用いて構築された。ポリエステル材料はまずBSA(0.1〜1.0%)、Tween20(0.01〜0.05%)及びトレハロース(0.5〜1.5%)を含むブロッキング溶液でブロッキングされた。乾燥後、hCG特異的な結合試薬を含む3μl/cmの金コンジュゲート溶液がブロッキングされたポリエステルに適用された。溶液はチューブポンプを用いて材料の端の5mm幅の領域に添加され、次に20%未満の相対湿度を有する乾燥室で乾燥させられた。乾燥は、8%未満の相対湿度を有する乾燥室で続けられた。
【0073】
ポリエステル材料は25mm×27mmの片に切られた。多孔質材料の四つの層は、ポリプロピレン製の丸い中空スティックの周りに巻かれ、0.1Nmの巻きつけトルク下でテープで取り付けられた。テープはまずポリプロピレンスティックに取り付けられ、次にポリエステルでスティックの周りを巻かれ、最後にテープは自分自身に取り付けられて多孔質材料上に保護被覆を形成した。構築された各スティックの周りにテープ(25mm×51mm)が巻きつけられたとき、それは針で80〜120回穿孔され、その中にベントを形成した。各ベントは0.1〜0.5mmの間のベントの間で異なる直径を有していた。含浸された標識化された特異的な結合試薬を有する端は、サンプリング装置の下側端に設定された。
【0074】
図7の分析装置はhCG特異的抗体を多孔質担体の上に固定して検出領域を形成することによって構築された。標識化された特異的な結合試薬に対するモノクローナル抗体は担体上に固定されてコントロール領域を形成した。ニトロセルロースは次に、BSA(0.1〜5.0%)、TRITON−X−100、BRIJ及びサッカロースを含むブロッキング溶液でブロッキングされた。材料は乾燥させられた。多孔質担体はケーシング中に置かれた。
【0075】
サンプリング装置及び分析装置の検査ストリップは8%の水分率まで乾燥された。検査ストリップ(ケーシング内の)及びサンプリング装置は一緒に密封ポーチ中に密封して包装された。
【0076】
サンプリング装置の多孔質層を含む端は尿の流れの下に10秒間置かれた。その後、サンプリング装置は分析装置のサンプルウェル中に置かれた。サンプルと標識化された特異的な結合試薬とから形成される複合体は5分間移動させられ、その後、結果は検査窓で読みとられた。赤い線が検査窓の検出領域及びコントロール窓のコントロール領域で見られ、これはサンプル中のhCGの存在を示した。
【0077】
実施例3 妊娠検査
実施例3はhCG妊娠検査に関し、そこでは特異的な標識化された試薬を含む多孔質層が不透過性層なしで取り付けられている。コントロール領域は検査の適切な性能を確実にするために追加される。
【0078】
ポリエステルフィルターは実施例2に記述されたようにして前処理された。フィルターの一つの層は木製の中実スティックの周りに接着剤で接着され、テープで被覆されて実施例2に記述されたようにして形成される保護層を形成した。分析装置は実施例2と同様に作成され、最後に装置は乾燥されて実施例2に記述のように包装された。
【0079】
検査は、hCGを含む液体サンプルにサンプリング装置を10秒間浸漬することによって行われた。スティックは軽く振られ、その後、分析装置のサンプルウェル中に置かれた。hCGの存在は、実施例2に記述されたようにして検出された。
【0080】
実施例4 受胎能検査検出システム
実施例4は、本発明がどのようにして受胎能検査検出システムのために適用されることができるかを記述する。
【0081】
hCG、LH及びFSHについての三つの標識化された特異的な抗体を含む金コンジュゲート溶液3μl/cmがセルロースフィルターに適用された。溶液はチューブポンプを用いて材料の一端の3mm幅の領域に添加され、次に20%未満の相対湿度を有する乾燥室で乾燥させられた。セルロースフィルターは、BSA(0.1〜1.0%)、Tween20(0.01〜0.05%)及びトレハロース(0.5〜1.5%)を含むブロッキング溶液でブロッキングされた。
【0082】
セルロースフィルターは25mm×27mmの片に切られた。セルロースフィルターの一つの片は、ポリプロピレン製の丸い中空スティックの周りに四つの層として巻かれ、テープで取り付けられた。含浸された結合試薬を有する端はサンプリング装置の下側端に設定された。
【0083】
図7の分析装置は、BSA(0.1〜1.0%)、Tween20(0.01〜0.05%)及びトレハロース(0.5〜1.5%)を含むブロッキング溶液でニトロセルロースの多孔質担体をブロッキングすることによって構築された。材料は乾燥させられ、その後、1mg/mlのhCG、LH及びFSH特異的な抗体が多孔質担体上に固定されて三つの異なる検出領域を形成した。標識化された特異的な結合試薬に対するモノクローナル抗体1mg/mlが担体上に固定されてコントロール領域を形成した。多孔質担体は乾燥されてケーシング中に置かれた。
【0084】
検査は、尿の液体サンプル中にサンプリングスティックの多孔質層を含む端を10秒間浸漬することによって行われた。サンプリングスティックは次に分析装置のサンプルウェル中に置かれた。サンプルと標識化された特異的な結合試薬とから形成される複合体は5分間移動させられ、その後、結果は検査窓で読みとられた。赤い線が検査窓の検出領域及びコントロール窓のコントロール領域で見られ、これはサンプル中のhCG、LH又はFSHの全て又はこれらの一以上の存在を示した。
【0085】
実施例5 性病のための検出システム
実施例5はHIV1,2のための検出システムに関する。
【0086】
サンプリング装置の多孔質材料として用いられるポリエステルフィルターは、BSA(0.1〜5.0%)、TRITON−X−100、BRIJ及びサッカロースを含むブロッキング溶液でブロッキングされた。乾燥後、HIV1及びHIV2の両方を認識するポリペプチドを含む2μl/cmの着色されたラテックス溶液が、ブロッキングされた材料に適用された。溶液は4mmのフィルターに添加され、次に20%未満の相対湿度を有する乾燥室で乾燥された。
【0087】
ポリエステルフィルターは25mm×27mmの片に切られた。ポリエステルフィルターの一つの片は、木製の丸い中空スティックの周りに3回巻かれ、テープ(25mm×51mm)で取り付けられた。構築された各スティックの周りにテープが巻きつけられたとき、それは針で80〜120回穿孔され、その中にベントを形成した。各ベントは0.1〜0.5mmの間のベントの間で異なる直径を有していた。
【0088】
二つの検査窓及び一つのコントロール窓を有する分析装置は、0.5μlのHIV1組み換え抗原及び0.5μlのHIV2組み換え抗原を多孔質担体上に固定してニトロセルロースの多孔質担体上に検出領域を形成することによって構築された。材料は乾燥され、その後、ニトロセルロースは、BSA(0.1〜5.0%)、TRITON−X−100、BRIJ及びサッカロースを含むブロッキング溶液でブロッキングされた。標識化された特異的な結合試薬に対するモノクローナル抗体は、多孔質担体上に固定され、コントロール領域を形成した。多孔質担体は乾燥され、ケーシング中に置かれた。コントロール領域は、分析装置のサンプルウェルから最も離れた場所に置かれた。
【0089】
検査は、サンプリング装置の多孔質層を含む端を血清サンプル中に浸漬することによって行われた。サンプリング装置は分析装置のサンプルウェル中に置かれた。サンプルと標識化された特異的な結合試薬は5分間移動させられ、その後、結果は検査窓で読みとられた。結果は5分後及び10分後に読みとられた。その結果、赤い線が検査窓の検出領域及びコントロール窓のコントロール領域で見られ、これはサンプル中のHIV1,2の存在を示した。
【0090】
実施例6 アレルゲンのための多数のチャネル検査
実施例6はアレルゲン検査のための本発明の使用を記述する。同じサンプルは、多数のチャネルを有する分析装置を用いて幾つかのアレルゲンのために同時に検査される。
【0091】
サンプリング装置の多孔質材料として用いられるポリエステルフィルターは、BSA(0.1〜5.0%)、TRITON−X−100、BRIJ及びサッカロースを含むブロッキング溶液でブロッキングされた。乾燥後、IgE分子を特異的に認識する抗IgE抗体で被覆された着色されたラテックス粒子の水溶液10μlが、ブロッキングされた材料に適用された。溶液は全フィルターに添加され、次に20%未満の相対湿度を有する乾燥室で乾燥された。
【0092】
ポリエステルフィルターは10mm×20mmの片に切られた。ポリエステルフィルターの一つの片は、ポリプロピレン製の丸い中空スティックの周りに4回巻かれ、テープで取り付けられた。
【0093】
八つの分離されたチャネルを有する分析装置は、ニトロセルロースの多孔質担体中にチャネルを形成することによって構築され、八つの異なる特異的なアレルゲン0.5μlを含むマイラーフィルムが多孔質担体上に固定されて分析装置の各チャネル中に検出領域を形成した。材料は乾燥され、その後ニトロセルロースはBSA、HEXA及びトレハロースを含むブロッキング溶液でブロッキングされた。多孔質担体は乾燥された。
【0094】
検査は、サンプリングスティックの多孔質層を含む端を血清の液体サンプル中に浸漬することによって行われた。サンプリングスティックはサンプリング適用部位と接触させられ、サンプルと標識化された特異的な結合試薬は5分間移動させられ、その後、結果は検出領域中の可視的な点として読みとられ、これはサンプル中のアレルゲンの存在を示した。
【図面の簡単な説明】
【0095】
【図1】本発明によるサンプリング装置の透視図である。
【図2】サンプリング装置を下側から見た図である。
【図3】本発明によるサンプリング装置の別の透視図である。
【図4】本発明による被覆された多孔質担体の拡大した透視図である。
【図5】サンプリング装置の別の実施態様を下側から見た図である。
【図6】サンプリング装置及び分析装置の側面図である。
【図7】分析装置を上側から見た図である。
【図8】分析装置の別の実施態様を上側から見た図である。
【特許請求の範囲】
【請求項1】
多孔質層(2)によって近位端の一つで包囲された細長い支持体(1)を含む免疫アッセイを行うための免疫化学的サンプリング装置において、前記多孔質層(2)が多孔質層に解放可能なように結合された標識化された特異的な結合試薬(3)を含み、前記多孔質層が不透過性保護層(4)によって包囲されていること、及び液体サンプルと混合されたときに多孔質層(2)が分析装置と流体連通接触状態に置かれるまで標識化された結合試薬が多孔質層内に保持されることを特徴とする免疫化学的サンプリング装置。
【請求項2】
不透過性保護層が、圧力平衡化手段を含む不透過性保護層であることを特徴とする請求項1に記載の免疫化学的サンプリング装置。
【請求項3】
圧力平衡化手段が、不透過性保護層を通るベントを含むことを特徴とする請求項1又は2に記載の免疫化学的サンプリング装置。
【請求項4】
ベントが、不透過性保護層の表面積の10%〜50%にわたって分布されていることを特徴とする請求項1〜3のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項5】
ベントがそれぞれ0.1〜0.5mmの直径を有することを特徴とする請求項1〜4のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項6】
前記保護層がテープの一以上の層を含むことを特徴とする請求項1〜5のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項7】
前記多孔質層が多孔質材料の一以上の層を含むことを特徴とする請求項1〜6のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項8】
多孔質材料が、0.05〜0.5Nmの巻きつけトルク下で細長い支持体の周りに巻きつけられていることを特徴とする請求項1〜7のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項9】
多孔質材料が、0.1Nmの巻きつけトルク下で細長い支持体の周りに巻きつけられていることを特徴とする請求項1〜8のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項10】
多孔質層が、紙、ガラス繊維、ナイロン、ポリエステル又はセルロース及びそれらの誘導体からなる群から選択されることを特徴とする請求項1〜9のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項11】
サンプリング装置の前記多孔質材料が、天然又は合成のポリマー、非イオン性界面活性剤又は保存剤を含むブロッキング溶液でブロッキングされていることを特徴とする請求項1〜10のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項12】
前記特異的な結合試薬が、抗体、抗原、レクチン、受容体、リガンド、それらの断片又はそれらの組合せからなる群から選択されることを特徴とする請求項1〜11のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項13】
標識が、着色されたラテックス、金、金属、染料、蛍光産生物質、超常磁性物質、色素産生物質、蛍光色素産生物質、又は酵素的標識からなる群から選択されることを特徴とする請求項1〜12のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項14】
標識化された結合試薬が、多孔質層の最遠位端の表面積の20%〜40%に結合されていることを特徴とする請求項1〜13のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項15】
前記サンプリング装置が、前記分析装置との組合せで検出システムを形成することを特徴とする請求項1〜14のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項16】
前記装置が、8%以下の水分率まで乾燥され、前記分析装置と組み合わされるか又は分離されて密封して包装されていることを特徴とする請求項1〜15のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項17】
前記サンプリング装置が前記分析装置の多孔質担体と接触される請求項1〜16のいずれか一項に記載の免疫化学的サンプリング装置において、前記多孔質担体が、標識化された特異的な結合試薬を欠くことを特徴とする免疫化学的サンプリング装置。
【請求項18】
妊娠、閉経、受胎能、甲状腺刺激ホルモン、トキソプラスマ症、癌、呼吸器疾患、アレルギー、心筋梗塞、及び尿、血液、血清、血漿、唾液又はサンプル緩衝溶液中の薬物の検出のための請求項1〜17のいずれか一項に記載の免疫化学的サンプリング装置の使用。
【請求項19】
以下のステップを含む、免疫化学的サンプリング装置の製造方法:
a.多孔質担体(2)の一以上の層を細長い支持体(1)の周りに巻きつけてその状態で多孔質担体を保持する、但し多孔質担体は、標識化された結合試薬(3)が解放可能なように結合された多孔質材料からなる;
b.多孔質担体に不透過性保護層を巻きつけてその状態で不透過性保護層を保持する。
【請求項20】
不透過性保護層が圧力平衡化手段を含むことを特徴とする請求項19に記載の方法。
【請求項21】
圧力平衡化手段が、不透過性保護層を通るベントを含むことを特徴とする請求項19又は20に記載の方法。
【請求項22】
ベントが、不透過性保護層が多孔質担体の周りに巻きつけられているときに不透過性保護層を穿孔することによって形成されることを特徴とする請求項19〜21のいずれか一項に記載の方法。
【請求項23】
標識化された結合試薬が多孔質担体の最遠位端で多孔質材料の一以上の層の表面積の20%〜40%に結合されるようになるように標識化された結合試薬を多孔質材料上に配置するステップ(a)をさらに含むことを特徴とする請求項19〜22のいずれか一項に記載の方法。
【請求項24】
多孔質担体が、0.05〜0.5Nmの巻きつけトルク下で細長い支持体の周りに巻きつけられることを特徴とする請求項19〜23のいずれか一項に記載の方法。
【請求項25】
適用されるトルクが0.1Nmであることを特徴とする請求項19〜24のいずれか一項に記載の方法。
【請求項26】
以下のステップを含む、液体サンプル中の分析対象物の存在又は不存在を決定するための免疫化学的方法:
a.請求項1〜17のいずれか一項に記載のサンプリング装置に液体サンプルを添加する;
b.サンプリング装置を分析装置と接触させる;
c.サンプルと特異的な標識化された試薬との複合体がサンプリング装置から分析装置の多孔質担体まで移動するのに十分な時間放置する;そして
d.分析装置における前記分析対象物の存在又は不存在を検出することによって結果を観察する。
【請求項1】
多孔質層(2)によって近位端の一つで包囲された細長い支持体(1)を含む免疫アッセイを行うための免疫化学的サンプリング装置において、前記多孔質層(2)が多孔質層に解放可能なように結合された標識化された特異的な結合試薬(3)を含み、前記多孔質層が不透過性保護層(4)によって包囲されていること、及び液体サンプルと混合されたときに多孔質層(2)が分析装置と流体連通接触状態に置かれるまで標識化された結合試薬が多孔質層内に保持されることを特徴とする免疫化学的サンプリング装置。
【請求項2】
不透過性保護層が、圧力平衡化手段を含む不透過性保護層であることを特徴とする請求項1に記載の免疫化学的サンプリング装置。
【請求項3】
圧力平衡化手段が、不透過性保護層を通るベントを含むことを特徴とする請求項1又は2に記載の免疫化学的サンプリング装置。
【請求項4】
ベントが、不透過性保護層の表面積の10%〜50%にわたって分布されていることを特徴とする請求項1〜3のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項5】
ベントがそれぞれ0.1〜0.5mmの直径を有することを特徴とする請求項1〜4のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項6】
前記保護層がテープの一以上の層を含むことを特徴とする請求項1〜5のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項7】
前記多孔質層が多孔質材料の一以上の層を含むことを特徴とする請求項1〜6のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項8】
多孔質材料が、0.05〜0.5Nmの巻きつけトルク下で細長い支持体の周りに巻きつけられていることを特徴とする請求項1〜7のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項9】
多孔質材料が、0.1Nmの巻きつけトルク下で細長い支持体の周りに巻きつけられていることを特徴とする請求項1〜8のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項10】
多孔質層が、紙、ガラス繊維、ナイロン、ポリエステル又はセルロース及びそれらの誘導体からなる群から選択されることを特徴とする請求項1〜9のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項11】
サンプリング装置の前記多孔質材料が、天然又は合成のポリマー、非イオン性界面活性剤又は保存剤を含むブロッキング溶液でブロッキングされていることを特徴とする請求項1〜10のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項12】
前記特異的な結合試薬が、抗体、抗原、レクチン、受容体、リガンド、それらの断片又はそれらの組合せからなる群から選択されることを特徴とする請求項1〜11のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項13】
標識が、着色されたラテックス、金、金属、染料、蛍光産生物質、超常磁性物質、色素産生物質、蛍光色素産生物質、又は酵素的標識からなる群から選択されることを特徴とする請求項1〜12のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項14】
標識化された結合試薬が、多孔質層の最遠位端の表面積の20%〜40%に結合されていることを特徴とする請求項1〜13のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項15】
前記サンプリング装置が、前記分析装置との組合せで検出システムを形成することを特徴とする請求項1〜14のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項16】
前記装置が、8%以下の水分率まで乾燥され、前記分析装置と組み合わされるか又は分離されて密封して包装されていることを特徴とする請求項1〜15のいずれか一項に記載の免疫化学的サンプリング装置。
【請求項17】
前記サンプリング装置が前記分析装置の多孔質担体と接触される請求項1〜16のいずれか一項に記載の免疫化学的サンプリング装置において、前記多孔質担体が、標識化された特異的な結合試薬を欠くことを特徴とする免疫化学的サンプリング装置。
【請求項18】
妊娠、閉経、受胎能、甲状腺刺激ホルモン、トキソプラスマ症、癌、呼吸器疾患、アレルギー、心筋梗塞、及び尿、血液、血清、血漿、唾液又はサンプル緩衝溶液中の薬物の検出のための請求項1〜17のいずれか一項に記載の免疫化学的サンプリング装置の使用。
【請求項19】
以下のステップを含む、免疫化学的サンプリング装置の製造方法:
a.多孔質担体(2)の一以上の層を細長い支持体(1)の周りに巻きつけてその状態で多孔質担体を保持する、但し多孔質担体は、標識化された結合試薬(3)が解放可能なように結合された多孔質材料からなる;
b.多孔質担体に不透過性保護層を巻きつけてその状態で不透過性保護層を保持する。
【請求項20】
不透過性保護層が圧力平衡化手段を含むことを特徴とする請求項19に記載の方法。
【請求項21】
圧力平衡化手段が、不透過性保護層を通るベントを含むことを特徴とする請求項19又は20に記載の方法。
【請求項22】
ベントが、不透過性保護層が多孔質担体の周りに巻きつけられているときに不透過性保護層を穿孔することによって形成されることを特徴とする請求項19〜21のいずれか一項に記載の方法。
【請求項23】
標識化された結合試薬が多孔質担体の最遠位端で多孔質材料の一以上の層の表面積の20%〜40%に結合されるようになるように標識化された結合試薬を多孔質材料上に配置するステップ(a)をさらに含むことを特徴とする請求項19〜22のいずれか一項に記載の方法。
【請求項24】
多孔質担体が、0.05〜0.5Nmの巻きつけトルク下で細長い支持体の周りに巻きつけられることを特徴とする請求項19〜23のいずれか一項に記載の方法。
【請求項25】
適用されるトルクが0.1Nmであることを特徴とする請求項19〜24のいずれか一項に記載の方法。
【請求項26】
以下のステップを含む、液体サンプル中の分析対象物の存在又は不存在を決定するための免疫化学的方法:
a.請求項1〜17のいずれか一項に記載のサンプリング装置に液体サンプルを添加する;
b.サンプリング装置を分析装置と接触させる;
c.サンプルと特異的な標識化された試薬との複合体がサンプリング装置から分析装置の多孔質担体まで移動するのに十分な時間放置する;そして
d.分析装置における前記分析対象物の存在又は不存在を検出することによって結果を観察する。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【公表番号】特表2007−523337(P2007−523337A)
【公表日】平成19年8月16日(2007.8.16)
【国際特許分類】
【出願番号】特願2006−553607(P2006−553607)
【出願日】平成17年2月18日(2005.2.18)
【国際出願番号】PCT/FI2005/050041
【国際公開番号】WO2005/078441
【国際公開日】平成17年8月25日(2005.8.25)
【出願人】(506282458)
【Fターム(参考)】
【公表日】平成19年8月16日(2007.8.16)
【国際特許分類】
【出願日】平成17年2月18日(2005.2.18)
【国際出願番号】PCT/FI2005/050041
【国際公開番号】WO2005/078441
【国際公開日】平成17年8月25日(2005.8.25)
【出願人】(506282458)

【Fターム(参考)】
[ Back to top ]

