サーチュイン活性促進剤
【課題】生体細胞のサーチュイン活性をより強く促進し得る物質を解明し、各種疾患の予防や、アディポネクチンの血中濃度の低下、インスリン抵抗性の亢進等に起因する種々の疾患、例えばメタボリックシンドローム、糖尿病やその合併症、動脈硬化、消化器疾患等の種々の病態を治療・予防し得る医薬製剤や食品、飼料の開発に有効な物質を提供すること。
【解決手段】レスベラトロールの5倍以上の特に強いサーチュイン活性を有するε−ビニフェリン(viniferin)を有効成分とするサーチュイン活性促進剤。
【解決手段】レスベラトロールの5倍以上の特に強いサーチュイン活性を有するε−ビニフェリン(viniferin)を有効成分とするサーチュイン活性促進剤。
【発明の詳細な説明】
【技術分野】
【0001】
本発明はε−ビニフェリン(viniferin)を有効成分とする生体細胞サーチュイン活性促進剤に関する。本発明は食品、医薬製剤、飼料等に好適に適用される。
【背景技術】
【0002】
サーチュイン(sirtuin)は、NAD+依存型の脱アセチルか酵素群の総称であり、酵母(Sir2など5種類)、線虫(4種類)、ショウジョウバエ(5種類)及びヒト(SIRT1〜SIRT7)など、多様なサーチュインが同定されている。Sir2は、1992年に、ribosamal DNA(rDNA)領域のサイレンシングを保持するタンパク質として見出された(非特許文献1、Sirは silence information regulatorの略記)。脱アセチル化酵素であるSir2により、ヒストンからアセチル基が外れると、DNAのヒストンへの巻き付きが緊密になるため、環状rDNAが染色体の外に切り出されるときに作用する酵素が、DNAに接近できなくなり、ゲノムの安定性に寄与する。この脱アセチル型DNAは、“サイレント”と呼ばれる。染色体外に切り出された環状rDNAは、細胞分裂の際に母細胞の染色体と共に複製され、母細胞の核内に留まる。環状rDNAの蓄積により、最終的には、母細胞の細胞死がもたらされ、個体全体としては、「老化」が促進することとなる。
Sir2のNAD+依存型ヒストン脱アセチル活性が発見されたのは、2000年のことであり、この活性は、NADH、NADP、NADPHを補酵素としては発現されないため、NAD+にきわめて特異性の高い活性であるとされた(非特許文献2)。この酵母Sir2に高い相同性を示すSIRT1は、老化に関連しているp53タンパク質のリジン382を脱アセチル化することによって、p53の機能を制御することも認められている(非特許文献3)。2003年には、Sir2の活性を亢進させ、酵母の寿命を延長させる小分子化合物が見出され、初めてレスベラトロルの名前が、サーチュイン活性化物質として登場した(非特許文献4)。
カロリー制限をすることで、個体の寿命が延びることは、70年以上前に発見されていたが、カロリー制限により、サーチュインの活性が亢進すること(非特許文献5)が分かり、レスベラトロルは、このようなカロリー制限に伴うシグナル伝達経路を活性化し、寿命延長効果をもたらすことが判明した。現在では、レスベラトロルの持つ、このような寿命延長効果は、酵母のみならず、線虫、ショウジョウバエなどで認められており、マウスでは、高カロリー食の持つリスクを低減して、寿命延長をもたらすことが報告されており、ヒトにおいては、最近、SIRT1と癌との関連性が注目されている。SIRT2阻害剤は、パーキンソン病などの神経変性疾患治療に有用である可能性が報告されている。
現在、ヒト・サーチュインは、7種類が報告されている。いずれも、約275アミノ酸残基から構成されており、進化的な保存性の高い、触媒反応を担う領域を一時構造内に含んでいる。SIRT1、SIRT2、SIRT3、SIRT5は、タンパク質基質中の−アミノ基がアセチル化されたリジン残基から、NAD+依存的に脱アセチル化を触媒する。SIRT4とSIRT6は、NAD+を供与体として、タンパク質基質中のADP-リボシル化を触媒する。これらサーチュインは、細胞内局在も異なっており、SIRT1、SIRT3、SIRT6及びSIRT7は、核内タンパクであるが、SIRT2は、通常は、細胞質に局在し、細胞周期のG2/M期には、核内のクロマチンに結合している。SIRT3、SIRT4、SIRT5は、ミトコンドリアに局在が認められる。
上記のとおり、サーチュイン(Sirtuin)(サープロテイン(Sirprotein)ともいう)を活性化すると細胞死の予防、老化の予防、細胞死の治療、延命、寿命延長、癌発生の予防ができる(特許文献1)。例えば、サーチュインを活性化する成分として植物の感染抵抗性にかかわる成分であるレスベラトロールが知られている。そして動物実験によってコレステロールの減少、心臓病のリスク予防、早期ガンの予防及び進行抑制、血小板凝集予防などの効果が有名である。
【0003】
さらに最近、サーチュイン活性の上昇によってアディポネクチンが産生されることが明らかとなった(特許文献2)。
アディポネクチンはメタボリックシンドロームの発症・進展において中心的な役割を担っていること、血中アディポネクチン濃度の低下が非アルコール性脂肪性肝炎(NASH)、肝線維化の進展を促進すること、およびメタボリックシンドロームの病態として内臓脂肪蓄積、インスリン抵抗性、動脈硬化惹起性リポタンパク異常、血圧高値、高尿酸血症等が挙げられること、また、メタボリックシンドロームは軽度ではあるが全身性易炎症性状態、発癌や炎症性疾患の発症と関連づけられて注目されていること、等が報告されている。肥満・インスリン抵抗性に関連した発癌としては、子宮癌、閉経後乳癌、白血病、大腸癌、胃癌、前立腺癌などが挙げられ、これらが低アディポネクチン血症と密接に関連しているとの報告もされている。したがって低アディポネクチン血症の治療・予防、インスリン抵抗性の改善は、メタボリックシンドローム等の上記疾病の予防・治療にも有用である。またサーチュイン活性を促進することで種々の眼疾患の予防に効果があることが知られている(特許文献3)。
【0004】
このような状況下にあって、生体のサーチュイン活性を促進させる物質の探索が進められている。代表的な物質として前述のレスベラートルが上げられる(特許文献1特表2007−530417号公報)。このレスベラートルより強いサーチュイン活性を有する物質が求められている。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特表2007−530417号公報
【特許文献2】特開2008−255040号公報
【特許文献3】特開2006−298876号公報
【非特許文献】
【0006】
【非特許文献1】Transcriptional silencing in yeast is associated with reduced nucleosome acetylation. Braunstein M., Rose AB., Broach JR., et al., Genes Dev., 7: 592-604, 1993.
【非特許文献2】The silencing protein SIR2 and its homologs are NAD-dependent protein deacetylase. Landry J., Sutton A., Sternglanz R., et al., Proc. Natl. Acad. Sci. USA., 97: 5807-5811, 2000.
【非特許文献3】Human SIR2 deacetylates p53 and antagonizes PML/p53-induced cellular senescence. Langley E., Pearson M., Koundarides T., et al., EMBO J., 21: 2383-2396, 2002.
【非特許文献4】Small molecule activators or sirtuins extend Saccharomyces cerevisiae lifespan. Howitz KT., Bitterman KJ., Sinclair DA., et al., Nature, 425: 191-196, 2003.
【発明の概要】
【発明が解決しようとする課題】
【0007】
従来の技術情報から、生体細胞のサーチュイン活性をより強く促進し得る物質が解明できれば、各種疾患の予防や、アディポネクチンの血中濃度の低下、インスリン抵抗性の亢進等に起因する種々の疾患、例えばメタボリックシンドローム、糖尿病やその合併症、動脈硬化、消化器疾患等の種々の病態を治療・予防し得る医薬製剤や食品、飼料の開発に道が開かれることとなる。
【0008】
すなわち、本発明は、生体のサーチュイン活性を促進し得る物質を提供することを課題とする。
【課題を解決するための手段】
【0009】
上記課題を解決するために本発明者らは種々の化合物や天然物質の探索を鋭意進めた結果、ε−ビニフェリンが公知のレスベラトロールの5倍以上の特に強いサーチュイン活性を有することを見出し、本発明を完成するに至った。
【0010】
すなわち本発明は、ε−ビニフェリンを有効成分とするサーチュイン活性促進剤を提供する。
【0011】
また本発明は、健康食品である、上記サーチュイン活性促進剤を提供する。
【発明の効果】
【0012】
本発明はサーチュイン活性促進効果が高いため、それを利用した各種疾患治療剤や健康食品を提供することができ、サーチュイン活性の低下が関与するメタボリックメタボリックシンドローム、糖尿病やその合併症、動脈硬化、消化器疾患等の種々の病態の治療・予防に役立つ。
【図面の簡単な説明】
【0013】
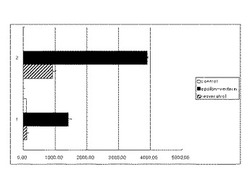
【図1】実施例1で測定したヒトサーチュイン酵素のうち、SIR1を測定した結果を示す。図中の1は各試験標品10マイクロモルを使用した試験群、2は各試験標品100マイクロモルを使用した試験群のサーチュイン酵素活性を示す。
【図2】実施例1で測定したヒトサーチュイン酵素のうち、SIR2を測定した結果である。
【図3】実施例1で測定したヒトサーチュイン酵素のうち、SIR3を測定した結果である。
【発明を実施するための形態】
【0014】
以下、本発明について詳述する。
【0015】
本発明で用いるε−ビニフェリンは、スチルベン系化合物であり、ブドウのファイトアレキシンの一種として知られている。ε−ビニフェリンを含有する植物体、好ましくはブドウ側枝より、各種抽出溶媒、好ましくは70%メタノールを用いてε−ビニフェリンを抽出することができる。抽出されたε−ビニフェリンは分取高速液体クロマトグラフィなどの分離精製手段によって分離、精製できる。
【0016】
ε−ビニフェリンは、レスベラートル類と総称されている。レスベラトロールは上述のとおり、ブドウの葉、新芽、果皮等に存在するポリフェノールの一種で、スチルベン系化合物であり、trans−レスベラトロール、cis−レスベラトロールが代表的な化合物であるが、これまで複合体や混合物としてしかサーチュイン活性を測定されていなかった。本発明者らが始めて、ε−ビニフェリン単独でサーチュイン活性を測定して、その活性の強さを発見した。
【0017】
ε―ビニフェリンは、有機化学的または微生物を用いて合成した高純度品の他、上述のブドウなどの植物体から抽出して用いることができ、その場合、抽出物を用いてもよく、またはその抽出物から単離したレスベラトロールを用いてもよい。天然物としては、ε−ビニフェリンの含有量がコントロールされているものであればよく、例えば、ブドウ、落花生、およびイタドリやツルドクダミ等のタデ科植物等が挙げられる。
【0018】
天然物としてはブドウが特に好ましい。ブドウの種類は、特に限定されるものではないが、デラウエア、巨峰、甲州、ピオーネ、マスカット、シュナンブラン、グレナッシュ、マタロ、ミュラーテュルガウ、トレッビアーノ、ベリーA、カベルネソービニオン、メルロー、ピノノアール、カベルネフラン、シラー、シャルドネ、ソービニヨンブラン、セミヨン、シラー、ガメイ、リースリング、アリゴテ等が好ましい。ブドウ抽出物とは、ブドウ果実、ブドウ葉またはブドウに由来する物からの抽出物を指す。ブドウに由来する物としては、ブドウジュース、ワイン、ワイン製造時の残渣、ワイン濃縮物等をいう。抽出は、例えば、レスベラトロール類はブドウの果皮や新芽、葉に多く含まれていることが知られているので、それらを必要により乾燥した後、抽出溶媒に一定期間浸漬するか、あるいは加熱還流している抽出溶媒と接触させ、次いで濾過し、濃縮し、さらに上述の分取クロマトによって分取することができる。抽出溶媒としては、通常抽出に用いられる溶媒であれば任意に用いることができ、例えば、水、メタノール、エタノール、プロピレングリコール、1,3−ブチレングリコール、グリセリン等のアルコール類、クロロホルム、ジクロルエタン、四塩化炭素、アセトン、酢酸エチル等の有機溶媒を、それぞれ単独あるいは組み合わせて用いることができる。上記溶媒で抽出して得た抽出液をそのまま、あるいは濃縮したエキスを用いるか、あるいはこれらエキスを吸着法、例えばイオン交換樹脂を用いて不純物を除去したものや、ポーラスポリマー(例えばアンバーライトXAD−2)のカラムにて吸着させた後、メタノールまたはエタノールで溶出し、濃縮したものも使用することができる。また分配法、例えば水/酢酸エチルで抽出した抽出物等も用いられる。また、ワイン、ワインの濃縮物または濃縮乾固した固形物中にも含まれているので、それらを用いることもできる。また、ワイン製造時に発生するブドウの残渣をそのまま用いるか、それから上記抽出方法と同様にして抽出することもできる。有機溶剤としてはエタノール等のアルコールが好ましく、特にエタノールが好ましい。
【0019】
本発明のサーチュイン活性促進剤は医薬製剤としてヒトおよび動物に投与することができる他、各種飲食品、飼料(ペットフード等)に配合しても摂取させることができる。
【0020】
医薬製剤は、経口的にあるいは非経口的(静脈投与、腹腔内投与、等)に適宜に使用される。剤型も任意で、例えば錠剤、顆粒剤、散剤、カプセル剤等の経口用固形製剤や、内服液剤、シロップ剤等の経口用液体製剤、または、注射剤などの非経口用液体製剤など、いずれの形態にも公知の方法により適宜調製することができる。これらの医薬製剤には、通常用いられる結合剤、崩壊剤、増粘剤、分散剤、再吸収促進剤、矯味剤、緩衝剤、界面活性剤、溶解補助剤、保存剤、乳化剤、等張化剤、安定化剤やpH調製剤などの賦形剤を適宜使用してもよい。
【0021】
本発明医薬製剤において、有効成分であるε−ビニフェリンの投与量は、その種類、その剤型、また患者の年令、体重、適応症状などによって異なるが、例えば経口投与の場合は、成人1日1回〜数回投与され、1日あたり1回約1mg〜200mg、好ましくは3mg〜20mg/人程度投与するのがよい。
【0022】
本発明のサーチュイン活性促進剤を飲食品、飼料等として用いる場合、一般の飲食品の他、低アディポネクチン血症の予防・治療、インスリン抵抗性改善、メタボリックシンドロームの予防・治療、糖尿病およびその合併症の予防・治療剤、癌(子宮内膜癌、閉経後乳癌、白血病、大腸癌、胃癌、前立腺癌等を含む)、非アルコール性脂肪性肝炎(NASH)およびそれに由来する肝疾患の予防・治療等の生理機能をコンセプトとし、その旨を表示した機能性飲食品、疾病者用食品、特定保険用食品等に応用することができる。
【0023】
飲食品の形態としては、例えば、顆粒状、粒状、ペースト状、ゲル状、固形状、または、液体状に任意に成形することができる。これらには、食品中に含有することが認められている公知の各種物質、例えば、結合剤、崩壊剤、増粘剤、分散剤、再吸収促進剤、矯味剤、緩衝剤、界面活性剤、溶解補助剤、保存剤、乳化剤、等張化剤、安定化剤やpH調製剤などの賦形剤を適宜含有させることができる。
【0024】
本発明の飲食品中に含まれる有効成分であるεニフェリンの含有量は、それらの種類、目的、形態、利用方法などに応じて、適宜決めることができ、例えば、1〜10質量%程度とすることができる。特に、保健用飲食品等として利用する場合には、本発明の有効成分を所定の効果が十分発揮されるような量で含有させることが好ましい。従ってこのような場合には、本発明の飲食品は、εビニフェリンを含有し、血中アディポネクチン量の増加、あるいはメタボリックシンドロームなどの種々の疾患の予防または改善等に用いられるものである旨の表示を付した飲食品とすることができる。
【実施例】
【0025】
以下、本発明を実施例に基づきさらに詳細に説明するが、本発明は以下の実施例に限定されるものではない。なお、配合量はすべて質量%で示す。
【0026】
ヒトサーチュイン活性促進効果の確認試験
1.試験系
ヒトサーチュインの測定は、SIRT1 Fluorimetirc Drug Discovery kit (AK-555, BIOMOL International, Plymouth Meeting, PA, USA [コスモ・バイオ株式会社、東京])を用いて、添付の冊子に従って行なった。試験方法の概略は、次のとおり。
【0027】
2.ヒトサーチュイン活性測定方法
測定用マイクロプレート(4℃保存)以外の試薬(-80℃保存)を氷上に静置し、SIRT1酵素(SE-239)及び5×Developer II(KI-286)を緩除に溶解した。SIRT1酵素を0.2 U/・Lとなるように、アッセイ緩衝液(KI-286)にて希釈した。使用時は、測定用プレートのウエル毎に、0.04 U/・L濃度で使用した。キットに付属している陽性対照薬としてのレスベラトロル(trans-resveratrol)は、99%エタノールを用いて溶解し、アッセイ緩衝液にて希釈(100・M、10・M)し、10・L/ウエルで使用した。SIRT1酵素反応時の体積は、50・Lであるため、陽性対照のレスベラトロル、検体物質であるε−ビニフェリンは、initial濃度5倍にて調製した。基質であるFluor de Lys-SIRT1(KI-177; 5mM) 及び補酵素NAD+(KI-282; 50mM)は、15・Lを用いるため、initial濃度を3.33倍にて調製した。酵素反応を行う前に、測定用マイクロプレートを37℃に加温しておき、被検試料とSIRT1酵素をプレートに添加して、37℃にて30分間インキュベート後、NAD+とFlor de Lys-SIRT1を加え、さらに37℃にて、60分間インキュベートした。その後、Flor de LysTM Developer IIにニコチンアミド(2mM)を加えた反応停止液を50μL加え、このDeveloper IIにより生ずる蛍光プローブを、励起波長360nm、蛍光波長460nmで、反応停止後60分以内に測定した(SPECTRA MAX Gemini EM; Molecular Device, Sunnyvale, CA, USA[日本モレキュラーデバイス株式会社、東京])。
ヒトSIR2、ヒトSIR3についても同様に市販のサーチュイン活性測定キット(SIRT2 Fluorescent Activity Assay/Drug Discovery Kit,HumanならびにSIRT3 Fluorescent Activity Assay/Drug Discovery Kit,Human、いずれもSIR1と同様にコスモバイオ社製品)を用いて測定した。
【0028】
3.試験結果
試験結果を図1、図2、図3に示す。
ε―ビニフェリンはレスベラトールの4〜5倍以上ヒトサーチュイン酵素の増強効果を有することが確認された。
【0029】
実施例2
ε−ビニフェリンの調製
ブドウ側枝(品種デラウエア)約5kgよりε−ビニフェリンを70%メタノール10lにより抽出し、分取HPLCにより分離・精製して約200mgのε−ビニフェリンを得た。HPLC分取時の移動相としてはアセトニトリル/水(7:13)を用い、1ml/分の流速で約8分後に検出される。検出は紫外吸収288nmで行った。このようにして得たビニフェリンを実施例1の試験例に用いた。またメタノール抽出後溶媒を留去して得た残渣を、粗精製ε−ビニフェリンとして、以下の処方例におけるビニフェリンとして用いた。
【0030】
処方例1:サプリメント
(配 合 成 分) (質量%)
乳糖 54.0
結晶セルロース 35.0
澱粉分解物 10.0
ε−ビネフェリン 1.0
【0031】
処方例2:ソフトカプセル
(配 合 成 分) (質量%)
食用大豆油 42.0
ε−ビネフリン 1.0
グリセリン脂肪酸エステル 12.0
ミツロウ 5.0
【0032】
実施例3:グミ
(配 合 成 分) (質量%)
還元水飴 40.0
グラニュー糖 20.0
ブドウ糖 20.0
ゼラチン 4.7
水 9.6
ε−ビネフリン 1.0
フレーバー 0.6
色素 0.1
【0033】
処方例3:清涼飲料
(配 合 成 分) (質量%)
果糖ブドウ糖液糖 30.0
ブドウ果汁 20.0
乳化剤 0.5
ε−ビネフリン 1.0
香料 適量
精製水 残余
【0034】
処方例4:錠菓
(配 合 成 分) (質量%)
砂糖 76.0
グルコース 19.0
ε−ビニフェリン 1.0
ショ糖脂肪酸エステル 0.2
精製水 3.8
【0035】
処方例5:キャンディー
(配 合 成 分) (質量%)
砂糖 50.0
水飴 33.0
水 14.0
有機酸 2.0
ε−ビニフェリン 0.5
香料 0.5
【技術分野】
【0001】
本発明はε−ビニフェリン(viniferin)を有効成分とする生体細胞サーチュイン活性促進剤に関する。本発明は食品、医薬製剤、飼料等に好適に適用される。
【背景技術】
【0002】
サーチュイン(sirtuin)は、NAD+依存型の脱アセチルか酵素群の総称であり、酵母(Sir2など5種類)、線虫(4種類)、ショウジョウバエ(5種類)及びヒト(SIRT1〜SIRT7)など、多様なサーチュインが同定されている。Sir2は、1992年に、ribosamal DNA(rDNA)領域のサイレンシングを保持するタンパク質として見出された(非特許文献1、Sirは silence information regulatorの略記)。脱アセチル化酵素であるSir2により、ヒストンからアセチル基が外れると、DNAのヒストンへの巻き付きが緊密になるため、環状rDNAが染色体の外に切り出されるときに作用する酵素が、DNAに接近できなくなり、ゲノムの安定性に寄与する。この脱アセチル型DNAは、“サイレント”と呼ばれる。染色体外に切り出された環状rDNAは、細胞分裂の際に母細胞の染色体と共に複製され、母細胞の核内に留まる。環状rDNAの蓄積により、最終的には、母細胞の細胞死がもたらされ、個体全体としては、「老化」が促進することとなる。
Sir2のNAD+依存型ヒストン脱アセチル活性が発見されたのは、2000年のことであり、この活性は、NADH、NADP、NADPHを補酵素としては発現されないため、NAD+にきわめて特異性の高い活性であるとされた(非特許文献2)。この酵母Sir2に高い相同性を示すSIRT1は、老化に関連しているp53タンパク質のリジン382を脱アセチル化することによって、p53の機能を制御することも認められている(非特許文献3)。2003年には、Sir2の活性を亢進させ、酵母の寿命を延長させる小分子化合物が見出され、初めてレスベラトロルの名前が、サーチュイン活性化物質として登場した(非特許文献4)。
カロリー制限をすることで、個体の寿命が延びることは、70年以上前に発見されていたが、カロリー制限により、サーチュインの活性が亢進すること(非特許文献5)が分かり、レスベラトロルは、このようなカロリー制限に伴うシグナル伝達経路を活性化し、寿命延長効果をもたらすことが判明した。現在では、レスベラトロルの持つ、このような寿命延長効果は、酵母のみならず、線虫、ショウジョウバエなどで認められており、マウスでは、高カロリー食の持つリスクを低減して、寿命延長をもたらすことが報告されており、ヒトにおいては、最近、SIRT1と癌との関連性が注目されている。SIRT2阻害剤は、パーキンソン病などの神経変性疾患治療に有用である可能性が報告されている。
現在、ヒト・サーチュインは、7種類が報告されている。いずれも、約275アミノ酸残基から構成されており、進化的な保存性の高い、触媒反応を担う領域を一時構造内に含んでいる。SIRT1、SIRT2、SIRT3、SIRT5は、タンパク質基質中の−アミノ基がアセチル化されたリジン残基から、NAD+依存的に脱アセチル化を触媒する。SIRT4とSIRT6は、NAD+を供与体として、タンパク質基質中のADP-リボシル化を触媒する。これらサーチュインは、細胞内局在も異なっており、SIRT1、SIRT3、SIRT6及びSIRT7は、核内タンパクであるが、SIRT2は、通常は、細胞質に局在し、細胞周期のG2/M期には、核内のクロマチンに結合している。SIRT3、SIRT4、SIRT5は、ミトコンドリアに局在が認められる。
上記のとおり、サーチュイン(Sirtuin)(サープロテイン(Sirprotein)ともいう)を活性化すると細胞死の予防、老化の予防、細胞死の治療、延命、寿命延長、癌発生の予防ができる(特許文献1)。例えば、サーチュインを活性化する成分として植物の感染抵抗性にかかわる成分であるレスベラトロールが知られている。そして動物実験によってコレステロールの減少、心臓病のリスク予防、早期ガンの予防及び進行抑制、血小板凝集予防などの効果が有名である。
【0003】
さらに最近、サーチュイン活性の上昇によってアディポネクチンが産生されることが明らかとなった(特許文献2)。
アディポネクチンはメタボリックシンドロームの発症・進展において中心的な役割を担っていること、血中アディポネクチン濃度の低下が非アルコール性脂肪性肝炎(NASH)、肝線維化の進展を促進すること、およびメタボリックシンドロームの病態として内臓脂肪蓄積、インスリン抵抗性、動脈硬化惹起性リポタンパク異常、血圧高値、高尿酸血症等が挙げられること、また、メタボリックシンドロームは軽度ではあるが全身性易炎症性状態、発癌や炎症性疾患の発症と関連づけられて注目されていること、等が報告されている。肥満・インスリン抵抗性に関連した発癌としては、子宮癌、閉経後乳癌、白血病、大腸癌、胃癌、前立腺癌などが挙げられ、これらが低アディポネクチン血症と密接に関連しているとの報告もされている。したがって低アディポネクチン血症の治療・予防、インスリン抵抗性の改善は、メタボリックシンドローム等の上記疾病の予防・治療にも有用である。またサーチュイン活性を促進することで種々の眼疾患の予防に効果があることが知られている(特許文献3)。
【0004】
このような状況下にあって、生体のサーチュイン活性を促進させる物質の探索が進められている。代表的な物質として前述のレスベラートルが上げられる(特許文献1特表2007−530417号公報)。このレスベラートルより強いサーチュイン活性を有する物質が求められている。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特表2007−530417号公報
【特許文献2】特開2008−255040号公報
【特許文献3】特開2006−298876号公報
【非特許文献】
【0006】
【非特許文献1】Transcriptional silencing in yeast is associated with reduced nucleosome acetylation. Braunstein M., Rose AB., Broach JR., et al., Genes Dev., 7: 592-604, 1993.
【非特許文献2】The silencing protein SIR2 and its homologs are NAD-dependent protein deacetylase. Landry J., Sutton A., Sternglanz R., et al., Proc. Natl. Acad. Sci. USA., 97: 5807-5811, 2000.
【非特許文献3】Human SIR2 deacetylates p53 and antagonizes PML/p53-induced cellular senescence. Langley E., Pearson M., Koundarides T., et al., EMBO J., 21: 2383-2396, 2002.
【非特許文献4】Small molecule activators or sirtuins extend Saccharomyces cerevisiae lifespan. Howitz KT., Bitterman KJ., Sinclair DA., et al., Nature, 425: 191-196, 2003.
【発明の概要】
【発明が解決しようとする課題】
【0007】
従来の技術情報から、生体細胞のサーチュイン活性をより強く促進し得る物質が解明できれば、各種疾患の予防や、アディポネクチンの血中濃度の低下、インスリン抵抗性の亢進等に起因する種々の疾患、例えばメタボリックシンドローム、糖尿病やその合併症、動脈硬化、消化器疾患等の種々の病態を治療・予防し得る医薬製剤や食品、飼料の開発に道が開かれることとなる。
【0008】
すなわち、本発明は、生体のサーチュイン活性を促進し得る物質を提供することを課題とする。
【課題を解決するための手段】
【0009】
上記課題を解決するために本発明者らは種々の化合物や天然物質の探索を鋭意進めた結果、ε−ビニフェリンが公知のレスベラトロールの5倍以上の特に強いサーチュイン活性を有することを見出し、本発明を完成するに至った。
【0010】
すなわち本発明は、ε−ビニフェリンを有効成分とするサーチュイン活性促進剤を提供する。
【0011】
また本発明は、健康食品である、上記サーチュイン活性促進剤を提供する。
【発明の効果】
【0012】
本発明はサーチュイン活性促進効果が高いため、それを利用した各種疾患治療剤や健康食品を提供することができ、サーチュイン活性の低下が関与するメタボリックメタボリックシンドローム、糖尿病やその合併症、動脈硬化、消化器疾患等の種々の病態の治療・予防に役立つ。
【図面の簡単な説明】
【0013】
【図1】実施例1で測定したヒトサーチュイン酵素のうち、SIR1を測定した結果を示す。図中の1は各試験標品10マイクロモルを使用した試験群、2は各試験標品100マイクロモルを使用した試験群のサーチュイン酵素活性を示す。
【図2】実施例1で測定したヒトサーチュイン酵素のうち、SIR2を測定した結果である。
【図3】実施例1で測定したヒトサーチュイン酵素のうち、SIR3を測定した結果である。
【発明を実施するための形態】
【0014】
以下、本発明について詳述する。
【0015】
本発明で用いるε−ビニフェリンは、スチルベン系化合物であり、ブドウのファイトアレキシンの一種として知られている。ε−ビニフェリンを含有する植物体、好ましくはブドウ側枝より、各種抽出溶媒、好ましくは70%メタノールを用いてε−ビニフェリンを抽出することができる。抽出されたε−ビニフェリンは分取高速液体クロマトグラフィなどの分離精製手段によって分離、精製できる。
【0016】
ε−ビニフェリンは、レスベラートル類と総称されている。レスベラトロールは上述のとおり、ブドウの葉、新芽、果皮等に存在するポリフェノールの一種で、スチルベン系化合物であり、trans−レスベラトロール、cis−レスベラトロールが代表的な化合物であるが、これまで複合体や混合物としてしかサーチュイン活性を測定されていなかった。本発明者らが始めて、ε−ビニフェリン単独でサーチュイン活性を測定して、その活性の強さを発見した。
【0017】
ε―ビニフェリンは、有機化学的または微生物を用いて合成した高純度品の他、上述のブドウなどの植物体から抽出して用いることができ、その場合、抽出物を用いてもよく、またはその抽出物から単離したレスベラトロールを用いてもよい。天然物としては、ε−ビニフェリンの含有量がコントロールされているものであればよく、例えば、ブドウ、落花生、およびイタドリやツルドクダミ等のタデ科植物等が挙げられる。
【0018】
天然物としてはブドウが特に好ましい。ブドウの種類は、特に限定されるものではないが、デラウエア、巨峰、甲州、ピオーネ、マスカット、シュナンブラン、グレナッシュ、マタロ、ミュラーテュルガウ、トレッビアーノ、ベリーA、カベルネソービニオン、メルロー、ピノノアール、カベルネフラン、シラー、シャルドネ、ソービニヨンブラン、セミヨン、シラー、ガメイ、リースリング、アリゴテ等が好ましい。ブドウ抽出物とは、ブドウ果実、ブドウ葉またはブドウに由来する物からの抽出物を指す。ブドウに由来する物としては、ブドウジュース、ワイン、ワイン製造時の残渣、ワイン濃縮物等をいう。抽出は、例えば、レスベラトロール類はブドウの果皮や新芽、葉に多く含まれていることが知られているので、それらを必要により乾燥した後、抽出溶媒に一定期間浸漬するか、あるいは加熱還流している抽出溶媒と接触させ、次いで濾過し、濃縮し、さらに上述の分取クロマトによって分取することができる。抽出溶媒としては、通常抽出に用いられる溶媒であれば任意に用いることができ、例えば、水、メタノール、エタノール、プロピレングリコール、1,3−ブチレングリコール、グリセリン等のアルコール類、クロロホルム、ジクロルエタン、四塩化炭素、アセトン、酢酸エチル等の有機溶媒を、それぞれ単独あるいは組み合わせて用いることができる。上記溶媒で抽出して得た抽出液をそのまま、あるいは濃縮したエキスを用いるか、あるいはこれらエキスを吸着法、例えばイオン交換樹脂を用いて不純物を除去したものや、ポーラスポリマー(例えばアンバーライトXAD−2)のカラムにて吸着させた後、メタノールまたはエタノールで溶出し、濃縮したものも使用することができる。また分配法、例えば水/酢酸エチルで抽出した抽出物等も用いられる。また、ワイン、ワインの濃縮物または濃縮乾固した固形物中にも含まれているので、それらを用いることもできる。また、ワイン製造時に発生するブドウの残渣をそのまま用いるか、それから上記抽出方法と同様にして抽出することもできる。有機溶剤としてはエタノール等のアルコールが好ましく、特にエタノールが好ましい。
【0019】
本発明のサーチュイン活性促進剤は医薬製剤としてヒトおよび動物に投与することができる他、各種飲食品、飼料(ペットフード等)に配合しても摂取させることができる。
【0020】
医薬製剤は、経口的にあるいは非経口的(静脈投与、腹腔内投与、等)に適宜に使用される。剤型も任意で、例えば錠剤、顆粒剤、散剤、カプセル剤等の経口用固形製剤や、内服液剤、シロップ剤等の経口用液体製剤、または、注射剤などの非経口用液体製剤など、いずれの形態にも公知の方法により適宜調製することができる。これらの医薬製剤には、通常用いられる結合剤、崩壊剤、増粘剤、分散剤、再吸収促進剤、矯味剤、緩衝剤、界面活性剤、溶解補助剤、保存剤、乳化剤、等張化剤、安定化剤やpH調製剤などの賦形剤を適宜使用してもよい。
【0021】
本発明医薬製剤において、有効成分であるε−ビニフェリンの投与量は、その種類、その剤型、また患者の年令、体重、適応症状などによって異なるが、例えば経口投与の場合は、成人1日1回〜数回投与され、1日あたり1回約1mg〜200mg、好ましくは3mg〜20mg/人程度投与するのがよい。
【0022】
本発明のサーチュイン活性促進剤を飲食品、飼料等として用いる場合、一般の飲食品の他、低アディポネクチン血症の予防・治療、インスリン抵抗性改善、メタボリックシンドロームの予防・治療、糖尿病およびその合併症の予防・治療剤、癌(子宮内膜癌、閉経後乳癌、白血病、大腸癌、胃癌、前立腺癌等を含む)、非アルコール性脂肪性肝炎(NASH)およびそれに由来する肝疾患の予防・治療等の生理機能をコンセプトとし、その旨を表示した機能性飲食品、疾病者用食品、特定保険用食品等に応用することができる。
【0023】
飲食品の形態としては、例えば、顆粒状、粒状、ペースト状、ゲル状、固形状、または、液体状に任意に成形することができる。これらには、食品中に含有することが認められている公知の各種物質、例えば、結合剤、崩壊剤、増粘剤、分散剤、再吸収促進剤、矯味剤、緩衝剤、界面活性剤、溶解補助剤、保存剤、乳化剤、等張化剤、安定化剤やpH調製剤などの賦形剤を適宜含有させることができる。
【0024】
本発明の飲食品中に含まれる有効成分であるεニフェリンの含有量は、それらの種類、目的、形態、利用方法などに応じて、適宜決めることができ、例えば、1〜10質量%程度とすることができる。特に、保健用飲食品等として利用する場合には、本発明の有効成分を所定の効果が十分発揮されるような量で含有させることが好ましい。従ってこのような場合には、本発明の飲食品は、εビニフェリンを含有し、血中アディポネクチン量の増加、あるいはメタボリックシンドロームなどの種々の疾患の予防または改善等に用いられるものである旨の表示を付した飲食品とすることができる。
【実施例】
【0025】
以下、本発明を実施例に基づきさらに詳細に説明するが、本発明は以下の実施例に限定されるものではない。なお、配合量はすべて質量%で示す。
【0026】
ヒトサーチュイン活性促進効果の確認試験
1.試験系
ヒトサーチュインの測定は、SIRT1 Fluorimetirc Drug Discovery kit (AK-555, BIOMOL International, Plymouth Meeting, PA, USA [コスモ・バイオ株式会社、東京])を用いて、添付の冊子に従って行なった。試験方法の概略は、次のとおり。
【0027】
2.ヒトサーチュイン活性測定方法
測定用マイクロプレート(4℃保存)以外の試薬(-80℃保存)を氷上に静置し、SIRT1酵素(SE-239)及び5×Developer II(KI-286)を緩除に溶解した。SIRT1酵素を0.2 U/・Lとなるように、アッセイ緩衝液(KI-286)にて希釈した。使用時は、測定用プレートのウエル毎に、0.04 U/・L濃度で使用した。キットに付属している陽性対照薬としてのレスベラトロル(trans-resveratrol)は、99%エタノールを用いて溶解し、アッセイ緩衝液にて希釈(100・M、10・M)し、10・L/ウエルで使用した。SIRT1酵素反応時の体積は、50・Lであるため、陽性対照のレスベラトロル、検体物質であるε−ビニフェリンは、initial濃度5倍にて調製した。基質であるFluor de Lys-SIRT1(KI-177; 5mM) 及び補酵素NAD+(KI-282; 50mM)は、15・Lを用いるため、initial濃度を3.33倍にて調製した。酵素反応を行う前に、測定用マイクロプレートを37℃に加温しておき、被検試料とSIRT1酵素をプレートに添加して、37℃にて30分間インキュベート後、NAD+とFlor de Lys-SIRT1を加え、さらに37℃にて、60分間インキュベートした。その後、Flor de LysTM Developer IIにニコチンアミド(2mM)を加えた反応停止液を50μL加え、このDeveloper IIにより生ずる蛍光プローブを、励起波長360nm、蛍光波長460nmで、反応停止後60分以内に測定した(SPECTRA MAX Gemini EM; Molecular Device, Sunnyvale, CA, USA[日本モレキュラーデバイス株式会社、東京])。
ヒトSIR2、ヒトSIR3についても同様に市販のサーチュイン活性測定キット(SIRT2 Fluorescent Activity Assay/Drug Discovery Kit,HumanならびにSIRT3 Fluorescent Activity Assay/Drug Discovery Kit,Human、いずれもSIR1と同様にコスモバイオ社製品)を用いて測定した。
【0028】
3.試験結果
試験結果を図1、図2、図3に示す。
ε―ビニフェリンはレスベラトールの4〜5倍以上ヒトサーチュイン酵素の増強効果を有することが確認された。
【0029】
実施例2
ε−ビニフェリンの調製
ブドウ側枝(品種デラウエア)約5kgよりε−ビニフェリンを70%メタノール10lにより抽出し、分取HPLCにより分離・精製して約200mgのε−ビニフェリンを得た。HPLC分取時の移動相としてはアセトニトリル/水(7:13)を用い、1ml/分の流速で約8分後に検出される。検出は紫外吸収288nmで行った。このようにして得たビニフェリンを実施例1の試験例に用いた。またメタノール抽出後溶媒を留去して得た残渣を、粗精製ε−ビニフェリンとして、以下の処方例におけるビニフェリンとして用いた。
【0030】
処方例1:サプリメント
(配 合 成 分) (質量%)
乳糖 54.0
結晶セルロース 35.0
澱粉分解物 10.0
ε−ビネフェリン 1.0
【0031】
処方例2:ソフトカプセル
(配 合 成 分) (質量%)
食用大豆油 42.0
ε−ビネフリン 1.0
グリセリン脂肪酸エステル 12.0
ミツロウ 5.0
【0032】
実施例3:グミ
(配 合 成 分) (質量%)
還元水飴 40.0
グラニュー糖 20.0
ブドウ糖 20.0
ゼラチン 4.7
水 9.6
ε−ビネフリン 1.0
フレーバー 0.6
色素 0.1
【0033】
処方例3:清涼飲料
(配 合 成 分) (質量%)
果糖ブドウ糖液糖 30.0
ブドウ果汁 20.0
乳化剤 0.5
ε−ビネフリン 1.0
香料 適量
精製水 残余
【0034】
処方例4:錠菓
(配 合 成 分) (質量%)
砂糖 76.0
グルコース 19.0
ε−ビニフェリン 1.0
ショ糖脂肪酸エステル 0.2
精製水 3.8
【0035】
処方例5:キャンディー
(配 合 成 分) (質量%)
砂糖 50.0
水飴 33.0
水 14.0
有機酸 2.0
ε−ビニフェリン 0.5
香料 0.5
【特許請求の範囲】
【請求項1】
ε−ビニフェリンを有効成分とするサーチュイン活性促進剤
【請求項2】
請求項1記載の剤を含有する健康食品
【請求項1】
ε−ビニフェリンを有効成分とするサーチュイン活性促進剤
【請求項2】
請求項1記載の剤を含有する健康食品
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2011−57580(P2011−57580A)
【公開日】平成23年3月24日(2011.3.24)
【国際特許分類】
【出願番号】特願2009−206649(P2009−206649)
【出願日】平成21年9月8日(2009.9.8)
【出願人】(593106918)株式会社ファンケル (310)
【Fターム(参考)】
【公開日】平成23年3月24日(2011.3.24)
【国際特許分類】
【出願日】平成21年9月8日(2009.9.8)
【出願人】(593106918)株式会社ファンケル (310)
【Fターム(参考)】
[ Back to top ]

