シクロプロパンカルボン酸エステルの遊離酸への加水分解方法
【課題】シクロプロパンカルボン酸エステルの遊離酸への加水分解方法を提供する。
【解決手段】シクロプロパンカルボン酸メチルまたはエチル1が、適切な場合1種もしくはそれ以上のアルコール2と、ならびにさらに水4および、適切な場合、塩化水素酸3と混合されて、または酸性固体の存在下で加水分解される。
【解決手段】シクロプロパンカルボン酸メチルまたはエチル1が、適切な場合1種もしくはそれ以上のアルコール2と、ならびにさらに水4および、適切な場合、塩化水素酸3と混合されて、または酸性固体の存在下で加水分解される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明はシクロプロパンカルボン酸およびアルコールの製造方法に関する。
【背景技術】
【0002】
メチルまたはエチルエステルの酸触媒加水分解によるシクロプロパンカルボン酸の製造は次の反応によって起こる。
【0003】
【化1】

【0004】
シクロプロパンカルボン酸は化学薬品、医薬品および作物保護剤の製造のための重要な中間体である。
【0005】
シクロプロパンカルボン酸エステルは公知の方法によって製造され、例えば、メチルエステルは、例えば、(特許文献1)に記載されているように、ナトリウムメトキシドを用いて4−クロロ酪酸メチルの環化によって得られる。
【0006】
シクロプロパンカルボン酸エステルは、例えば、(非特許文献1)に記載されているように、水性アルカリ金属水酸化物を用いて加水分解することができる。
【0007】
この手順の欠点は塩水溶液の避けられない形成であり、この水溶液から生成物が単離されなければならず、それは溶剤での抽出によってのみ達成することができるが、これはシクロプロパンカルボン酸の高い飽和濃度のために複雑となり、例えば、飽和硫酸ナトリウム溶液でさえまだ3%の濃度を有する。
【0008】
(非特許文献2)に記載されているように、塩化水素酸(3)などの酸がシクロプロパンカルボン酸およびその誘導体に付加して、例えば、4−クロロ酪酸誘導体を形成するので、シクロプロパンカルボン酸エステルの酸触媒加水分解は、触媒および選択性の損失を被る。
【0009】
(特許文献2)で、カウフホルド(Kaufhold)は、触媒としてトルエンスルホン酸の存在下に、シクロプロパンカルボン酸メチルまたはエチルを他のカルボン酸、好ましくはギ酸とエステル交換させ、次に、例えば、蒸留によって混合物からギ酸メチルを除去することによって収量損失および塩の形成を克服している。硫酸によって触媒される比較例では、わずかな収量損失がここでもまた起こる。この方法の欠点は、酸の必要性およびこの酸のエステルの避けられない形成である。
【0010】
シクロプロパンカルボン酸メチルまたはエチル(1)が水(4)によって加水分解され、シクロプロパンカルボン酸と概して純粋なアルコールとが唯一の生成物として形成される簡単な工業的方法は知られていないし、望ましい。
【0011】
それ故、エネルギーを節減する、先行技術と比較してより環境にやさしい、そして連続的に実施することができるシクロプロパンカルボン酸およびアルコールの製造方法であって、高純度を有するシクロプロパンカルボン酸およびアルコールを高収率で唯一の生成物として製造できる方法を提供することが本発明の目的であった。
【特許文献1】欧州特許出願公開第0 577 949 A1号明細書
【特許文献2】欧州特許出願公開第0 879 813 A1号明細書
【非特許文献1】スタンレー・ブルース(Stanley Bruce)およびロナルド・ケント(Ronald Kent)著、「有機製造および手順インターナショナル(Organic Preparations and Procedures International)」、6(4)(1974)、193−196ページ
【非特許文献2】ランバート(Lambert)、ナポリ(Napoli)、ジョンソン(Johnson)およびタバ(Taba)著、「有機化学雑誌(Journal of Organic Chemistry)」、50(8)(1985)、1291−1295ページ
【発明の開示】
【課題を解決するための手段】
【0012】
本目的は、シクロプロパンカルボン酸メチルまたはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて加水分解されることを特徴とするシクロプロパンカルボン酸(5)の製造方法であって、
a)アルコール(2)がカラム(A)の塔頂を通して取り出される状態で、自動撹拌機を備えていてもよく、かつ、凝縮器を備えた第1カラム(A)に連結されている容器(D)を含む装置中へ、シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、別々に、または一緒に供給され、そして、
1)シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、凝縮器を備えた第1カラム(A)中へ別々に、または一緒に導入されるか、または
2)シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、容器(D)中へ、別々にまたは一緒に供給されるか、または、
3)水(4)および、適切な場合、塩化水素酸(3)が容器(D)中へ、別々にまたは一緒に供給されながら、シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と混合されて、凝縮器を備えた第1カラム(A)中へ導入されるか
のいずれかであり、
b)直接にか、又はa)1)およびa)3)の場合は第1カラム(A)経由で全体的にまたは部分的に、容器(D)に入る反応混合物が、続いて凝縮器を備えた第2カラム(B)に供給され、シクロプロパンカルボン酸(5)がカラム(B)の塔底から取り出され、その間、残りの反応混合物は容器(D)に再循環され、そして塩化水素酸(3)が全く使用されない場合は、少なくとも1種の酸性固体(9)が容器(D)中に初めに配置されている、
方法によって達成される。
【0013】
【数1】

【0014】
【数2】

【0015】
【数3】

【発明を実施するための最良の形態】
【0016】
塩化水素酸(3)が使用される場合、容器(D)中に存在する反応混合物は、適切な場合冷却(F)後に、第2カラム(B)に供給される前に工程b)で相分離(E)にかけられて有機相と水相(7)とを形成し、水相(7)は容器(D)中へ導かれ、有機相(8)は凝縮器を備えた第2カラム(B)中へ導かれる。
【0017】
第2カラム(B)からの残液は好ましくは全凝縮もしくは部分凝縮させられるか、またはガス形態で容器(D)に再循環される。容器(D)は好ましくは加熱される。
【0018】
第1カラム(A)での還流比(R/R)は好ましくは10/1〜1/5、特に好ましくは5/1〜1/1である。
【0019】
第2カラム(B)での還流比(R/R)は好ましくは2/1〜1/100、特に好ましくは1/1〜1/50、非常に特に好ましくは1/2〜1/30である。
【0020】
有機相を排出するために、混合物は、相分離(E)の前に20〜90℃、好ましくは40〜70℃、非常に特に50〜60℃の範囲の温度に冷却されることが好ましい(F)。
【0021】
シクロプロパンカルボン酸メチルまたはエチル(1)とアルコール(2)との混合物は第1カラム(A)中へ、特に、第1カラム(A)においてシクロプロパンカルボン酸メチルまたはエチル(1)対アルコール(2)の比が出発原料の混合物の比に一致するポイントまたはその近くで計量供給されることが好ましい。
【0022】
シクロプロパンカルボン酸メチルまたはエチル(1)がアルコール(2)と共に計量供給される場合、導入のポイントは好ましくは重複第1カラム(A)の低い部分にある。
【0023】
第1カラム(A)は好ましくは40〜130℃、特に60〜110℃の温度で、そして0.1〜2.0バール、特に0.5〜1.2バールの圧力下で稼働する。
【0024】
第1カラム(A)は好ましくは2〜300、特に5〜50プレートを有する。
【0025】
第2カラム(B)は好ましくは40〜200℃、特に80〜180℃の温度で、そして0.01〜2.0バール、特に0.1〜1.2バールの圧力下で稼働する。
【0026】
第2カラム(B)は好ましくは1〜100、特に3〜30プレートを有する。
【0027】
〔第3カラム(C)による第1カラム(A)および第2カラム(B)の置換〕
第1カラム(A)および第2カラム(B)は好ましくは、容器(D)に連結されている第3カラム(C)によって置換される。
【0028】
第3カラム(C)は好ましくは、液体側で、そして適切な場合はガス側で容器(D)に連結される。
【0029】
第3カラム(C)は好ましくは40〜200℃、特に60〜180℃の温度で、そして0.01〜2.0バール、特に0.1〜1.2バールの圧力下で稼働する。
【0030】
第3カラム(C)は好ましくは5〜300、特に30〜60プレートを有する。
【0031】
第3カラム(C)での還流比(R/R)は好ましくは10/1〜1/1、特に好ましくは5/1〜2/1である。
【0032】
第3カラム(C)は好ましくは容器(D)として連結された反応器を有する。反応器の内容物(好ましくは有機相(8)のみ)は好ましくは第2〜第30番目プレート、特に好ましくは第3〜第15番目プレート、非常に特に好ましくは第6〜第10番目プレートに供給される。第3カラム(C)で下方に流れる液体は、好ましくは、反応混合物がカラム中へポンプ送液され且つ反応器中へ導入されるポイントの1〜10プレート上、特に好ましくは1〜5プレート上、非常に特に好ましくは1〜2プレート上にあるポイントで全体的にまたは部分的に取り出される。
【0033】
シクロプロパンカルボン酸エステル(1)は、適切な場合は、相当するアルコール(2)、塩化水素酸(3)および水(4)と混合されて、反応器、すなわち容器(D)中へ計量供給される。シクロプロパンカルボン酸エステル(1)がアルコール(2)と混合されて計量供給される場合、それは好ましくは反応器、すなわち容器(D)向けの取り出しポイントの上に配置された第3カラム(C)の部分へ導入される。
【0034】
蒸気(H)が形成され、そして排出される有機相と一緒に第3カラム(C)へ導入されるように、熱が容器(D)としての反応器中へ導入されることが好ましい。
【0035】
〔一般的情報〕
容器(D)からの混合物は、好ましくは、第2カラム(B)中へまたは第3カラム(C)中へ供給される前に追加の熱交換器を用いて加熱し、部分蒸発(G)させることができる。
【0036】
容器(D)は出発原料を92〜110℃、特に96〜100℃の温度に保持することが好ましい。
【0037】
水相中の塩化水素酸濃度(3)は、サンプルが室温まで冷却された後で、好ましくは4〜20%、特に好ましくは7〜14%、非常に特に好ましくは9〜12%である。
【0038】
塩化水素酸濃度(3)は、先行技術に記載されているように、センサーを用いて測定することができ、塩化水素酸(3)の導入をコントロールすることができる。容器(D)での第2の相(曇り点)の出現および消失は好ましくはコントロールのために利用される。濁りが消失した時、計量供給される量は濁りが再発するまで増やされ、次に、計量供給される量は濁りが再び消失するまで減らされる。
【0039】
塩化水素酸(3)が一定速度で計量供給されることも同様に可能であり、塩化水素酸濃度(3)は、濃度と共に増える塩化メチル形成によって確定される。
【0040】
水の計量供給添加は、冷却後の相の比によってコントロールされる。
【0041】
塩化水素酸(3)が除外される場合(これは混合物の腐食性の観点から利点を有する)、酸性固体(9)、特に好ましくはレワチット(Lewatit)(登録商標)またはナフィオン(Nafion)(登録商標)などのスルホン酸イオン交換樹脂を使用することが好ましい。これらの酸性固体(9)は容器(D)中へ導入され、スクリーンデバイスによってまたはパック材料(例えばモンツ(Montz)製のマルチパック(Multipack)(登録商標))としてそこに保持されるか、または容器(D)が固定床であるかのどちらかであり、それを通って混合物がポンプ送液される。
【0042】
本方法では、含水率は、第2の相が発生するほど高いものであるべきでなく、相分離(E)はそれ故必要ではない。水の計量供給添加はそれ故、例えば、混合物の沸点に応じて調節される。
【0043】
本方法は好ましくは連続的に、擬連続的にまたは回分式に実施される。
【0044】
シクロプロパンカルボン酸(5)の純度は、出発原料を基準にして、好ましくは>96%、特に>98%である。
【0045】
アルコール(2)の純度は、出発原料を基準にして、好ましくは>98.5%、特に>99.5%である。
【0046】
アルコール(2)は好ましくはメタノールおよび/またはエタノールである。
【0047】
装置は、複数の実施形態を示す図面を用いて以下に例示される。ここで、本発明のさらなる独創的な特徴および利点は、図面および本説明から導くことができる。
【0048】
本発明の独創的な範囲は、個々の請求項の主題によってだけでなく個々の請求項の互いの組み合わせによっても画定される。同じことは、本説明に開示されるすべてのパラメーターおよびそれらの任意の組み合わせに適用される。
【0049】
本発明は、それによって限定されることなく次の実施例によって例示される。
【0050】
[実施例]
測定方法
混合物の組成は、先行技術に相当するガスクロマトグラフ分析によって測定した。標準ガラスキャピラリーカラムのHP6890をクロマトグラフとして用いた。検出は水素炎イオン化検出器(FID)を用いて行った。検出限界は±0.1標準%(すなわち、重量%だが不検出成分なし)であった。
【0051】
塩化水素酸の濃度は滴定を用いて、極微量のケースでは蛍光X線を用いて測定した。検出限界は±10ppmであった。
【0052】
含水率はカール−フィッシャー(Karl−Fischer)法によって測定した。検出限界は±2相対%(すなわち、純水のケースでは2%、100ppmの含水率では2ppm)であった。
【0053】
〔実施例1(塩化水素酸(3)法)〕
装置を図1におけるように、しかしストリッピング・セクションの上流に部分蒸発(G)なしで構築した。それは、容器(D)として撹拌機付きのオイル加熱10Lフランジポットと、第1カラム(A)として約25プレートおよび凝縮器およびランバック・ディバイダーを有する重複カラムと、第2カラム(B)として約15プレートおよび凝縮器およびランバック・ディバイダーを有する重複カラムとを含んでいた。約550g/hのシクロプロパンカルボン酸メチル(1)および111g/hの10%強度の塩化水素酸(3)を、容器(D)としてのこのフランジポット中へ供給した。
【0054】
アルコール(2)としてメタノール、シクロプロパンカルボン酸メチル(1)、シクロプロパンカルボン酸(5)、塩化水素酸(3)および水(4)を含む約7Lの混合物は、容器(D)としてのフランジポット中で94〜95℃の沸点で沸騰する。第1カラム(A)の塔頂で、99%より高い純度を有し且つ0.17%の塩化メチル(6)および0.73%のシクロプロパンカルボン酸メチル(1)を含むメタノールを、64℃の温度およびR/R=2で取り出した。遊離の塩化水素酸(3)は10ppmの検出限界未満の濃度で蒸留液中に存在した。180g/hのメタノールは別として、15g/hの塩化メチル(6)が遊離したが、後者の主要部分は下流の冷トラップ中でのみ凝縮した。ランバック・ディバイダーは、76℃を超えた時にランバック・ディバイダーを全還流に設定する第1カラム(A)の中間での温度測定によってコントロールした。
【0055】
容器(D)からの混合物を相分離(E)にかけた。約1800g/hの有機相(8)を60℃に冷却し、分離し(E)、そして生成物としてシクロプロパンカルボン酸メチル(1)を集めるためにオーバーフロー付きのオイル加熱された10Lフランジポット上に配置された第2カラム(B)としての15プレートカラムの上方部へ供給した。フランジポットに182℃で沸騰する約6Lの液体を装入した。第2カラム(B)に、全て取り出す状態で稼働される還流ディバイダー付き凝縮器を重ねた。80℃で得られたオーバーヘッド生成物は2相よりなり、大部分はシクロプロパンカルボン酸メチル(1)および水(4)で構成され、約10%のメタノールおよび3.6%のシクロプロパンカルボン酸(5)を含有していた。2.1%のシクロプロパンカルボン酸無水物は別として他の成分が一切ない約480g/hのシクロプロパンカルボン酸(5)がフランジポットを出た。
【0056】
反応器の水相(7)は、滴定によれば約11%の(3)の含量を有していた。
【0057】
17%強度の塩化水素酸(3)をポンプ送入した時、塩化水素酸(3)の含量は12%に増加した。37%強度の塩化水素酸(3)は、14.5%の塩化水素酸(3)の含量をもたらした。この含量では、0.08%のブチロラクトンがシクロプロパンカルボン酸(5)中に検出され得た。水(4)と塩化水素ガス(3)とを混合することによって得られた50%強度の塩化水素酸(3)をポンプ送入した場合は、水相の塩化水素酸(3)含量は15%に上がり、0.14%のブチロラクトンがシクロプロパンカルボン酸(5)中に存在した。本方法を、曇り点で99.5℃で15%強度の塩化水素酸(3)および7%強度の塩化水素酸(3)の、または20%強度の塩化水素酸(3)および水(4)の交互導入によって実施した時、水相(7)は室温で約10%の塩化水素酸(3)を含有した。
【0058】
〔実施例2(酸性固体(9)−レワチット(登録商標)法)〕
装置を図2におけるように、しかしストリッピング・セクションの上流に部分蒸発(G)なしで構築した。容器(D)中の混合物を、反応器中にレワチットを残すためにスクリーンを通して反応器からポンプ送液した。第1および第2カラム(AおよびB)ならびにフランジポットは実施例1と同じものであった。酸性固体(9)として500gの市販の湿ったスルホン酸レワチット(K2431)が反応器中に存在した。280g/hのシクロプロパンカルボン酸メチル(1)および50g/hの水(4)を反応器中へポンプ送液した。99℃の沸点を水の導入によって維持した。温度が上った時には、導入される水の量もまた増やし、温度が低下した時には、導入される水の量もまた減らした。約0.2%のシクロプロパンカルボン酸メチル(1)を含有する約95g/hのメタノールが第1カラム(A)の塔頂で65℃で得られた。約700g/hの反応混合物をストリッピング・セクションへ供給した。ガスクロマトグラフィーによる分析によれば、3.5%のシクロプロパンカルボン酸無水物を含有する約240g/hのシクロプロパンカルボン酸(5)がストリッピング・セクションのフランジポットを出た。酸性固体(9)としてのレワチットは、1000時間後でさえ何の活性低下も示さなかった。
【図面の簡単な説明】
【0059】
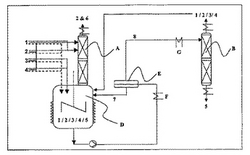
【図1】塩化水素酸(3)を用いてシクロプロパンカルボン酸(5)およびアルコール(2)を製造するための装置。ここで、容器(D)、第1カラム(A)、第2カラム(B)、相分離(E)、冷却(F)および部分蒸発(G)は互いに連結されている。
【図2】酸性固体(9)(レワチット(登録商標))を用いてシクロプロパンカルボン酸(5)およびアルコール(2)を製造するための装置。ここで、容器(D)、第1カラム(A)、第2カラム(B)および部分蒸発(G)は互いに連結されている。
【図3】塩化水素酸(3)を用いてシクロプロパンカルボン酸(5)およびアルコール(2)を製造するための装置。ここで、容器(D)、第3カラム(C)、相分離(E)、冷却(F)および部分蒸発(G)は互いに連結されている。
【図4】酸性固体(9)(レワチット(登録商標))を用いてシクロプロパンカルボン酸(5)およびアルコール(2)を製造するための装置。ここで、容器(D)、第3カラム(C)および部分蒸発(G)は互いに連結されている。
【符号の説明】
【0060】
1 シクロプロパンカルボン酸メチルまたはエチル
2 アルコール
3 塩化水素酸
4 水
5 シクロプロパンカルボン酸
6 塩化メチル
7 水相
8 有機相
9 酸性固体
A 第1カラム
B 第2カラム
C 第3カラム
D 容器
E 相分離
F 冷却
G 部分蒸発
H 蒸気
【技術分野】
【0001】
本発明はシクロプロパンカルボン酸およびアルコールの製造方法に関する。
【背景技術】
【0002】
メチルまたはエチルエステルの酸触媒加水分解によるシクロプロパンカルボン酸の製造は次の反応によって起こる。
【0003】
【化1】

【0004】
シクロプロパンカルボン酸は化学薬品、医薬品および作物保護剤の製造のための重要な中間体である。
【0005】
シクロプロパンカルボン酸エステルは公知の方法によって製造され、例えば、メチルエステルは、例えば、(特許文献1)に記載されているように、ナトリウムメトキシドを用いて4−クロロ酪酸メチルの環化によって得られる。
【0006】
シクロプロパンカルボン酸エステルは、例えば、(非特許文献1)に記載されているように、水性アルカリ金属水酸化物を用いて加水分解することができる。
【0007】
この手順の欠点は塩水溶液の避けられない形成であり、この水溶液から生成物が単離されなければならず、それは溶剤での抽出によってのみ達成することができるが、これはシクロプロパンカルボン酸の高い飽和濃度のために複雑となり、例えば、飽和硫酸ナトリウム溶液でさえまだ3%の濃度を有する。
【0008】
(非特許文献2)に記載されているように、塩化水素酸(3)などの酸がシクロプロパンカルボン酸およびその誘導体に付加して、例えば、4−クロロ酪酸誘導体を形成するので、シクロプロパンカルボン酸エステルの酸触媒加水分解は、触媒および選択性の損失を被る。
【0009】
(特許文献2)で、カウフホルド(Kaufhold)は、触媒としてトルエンスルホン酸の存在下に、シクロプロパンカルボン酸メチルまたはエチルを他のカルボン酸、好ましくはギ酸とエステル交換させ、次に、例えば、蒸留によって混合物からギ酸メチルを除去することによって収量損失および塩の形成を克服している。硫酸によって触媒される比較例では、わずかな収量損失がここでもまた起こる。この方法の欠点は、酸の必要性およびこの酸のエステルの避けられない形成である。
【0010】
シクロプロパンカルボン酸メチルまたはエチル(1)が水(4)によって加水分解され、シクロプロパンカルボン酸と概して純粋なアルコールとが唯一の生成物として形成される簡単な工業的方法は知られていないし、望ましい。
【0011】
それ故、エネルギーを節減する、先行技術と比較してより環境にやさしい、そして連続的に実施することができるシクロプロパンカルボン酸およびアルコールの製造方法であって、高純度を有するシクロプロパンカルボン酸およびアルコールを高収率で唯一の生成物として製造できる方法を提供することが本発明の目的であった。
【特許文献1】欧州特許出願公開第0 577 949 A1号明細書
【特許文献2】欧州特許出願公開第0 879 813 A1号明細書
【非特許文献1】スタンレー・ブルース(Stanley Bruce)およびロナルド・ケント(Ronald Kent)著、「有機製造および手順インターナショナル(Organic Preparations and Procedures International)」、6(4)(1974)、193−196ページ
【非特許文献2】ランバート(Lambert)、ナポリ(Napoli)、ジョンソン(Johnson)およびタバ(Taba)著、「有機化学雑誌(Journal of Organic Chemistry)」、50(8)(1985)、1291−1295ページ
【発明の開示】
【課題を解決するための手段】
【0012】
本目的は、シクロプロパンカルボン酸メチルまたはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて加水分解されることを特徴とするシクロプロパンカルボン酸(5)の製造方法であって、
a)アルコール(2)がカラム(A)の塔頂を通して取り出される状態で、自動撹拌機を備えていてもよく、かつ、凝縮器を備えた第1カラム(A)に連結されている容器(D)を含む装置中へ、シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、別々に、または一緒に供給され、そして、
1)シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、凝縮器を備えた第1カラム(A)中へ別々に、または一緒に導入されるか、または
2)シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、容器(D)中へ、別々にまたは一緒に供給されるか、または、
3)水(4)および、適切な場合、塩化水素酸(3)が容器(D)中へ、別々にまたは一緒に供給されながら、シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と混合されて、凝縮器を備えた第1カラム(A)中へ導入されるか
のいずれかであり、
b)直接にか、又はa)1)およびa)3)の場合は第1カラム(A)経由で全体的にまたは部分的に、容器(D)に入る反応混合物が、続いて凝縮器を備えた第2カラム(B)に供給され、シクロプロパンカルボン酸(5)がカラム(B)の塔底から取り出され、その間、残りの反応混合物は容器(D)に再循環され、そして塩化水素酸(3)が全く使用されない場合は、少なくとも1種の酸性固体(9)が容器(D)中に初めに配置されている、
方法によって達成される。
【0013】
【数1】

【0014】
【数2】

【0015】
【数3】

【発明を実施するための最良の形態】
【0016】
塩化水素酸(3)が使用される場合、容器(D)中に存在する反応混合物は、適切な場合冷却(F)後に、第2カラム(B)に供給される前に工程b)で相分離(E)にかけられて有機相と水相(7)とを形成し、水相(7)は容器(D)中へ導かれ、有機相(8)は凝縮器を備えた第2カラム(B)中へ導かれる。
【0017】
第2カラム(B)からの残液は好ましくは全凝縮もしくは部分凝縮させられるか、またはガス形態で容器(D)に再循環される。容器(D)は好ましくは加熱される。
【0018】
第1カラム(A)での還流比(R/R)は好ましくは10/1〜1/5、特に好ましくは5/1〜1/1である。
【0019】
第2カラム(B)での還流比(R/R)は好ましくは2/1〜1/100、特に好ましくは1/1〜1/50、非常に特に好ましくは1/2〜1/30である。
【0020】
有機相を排出するために、混合物は、相分離(E)の前に20〜90℃、好ましくは40〜70℃、非常に特に50〜60℃の範囲の温度に冷却されることが好ましい(F)。
【0021】
シクロプロパンカルボン酸メチルまたはエチル(1)とアルコール(2)との混合物は第1カラム(A)中へ、特に、第1カラム(A)においてシクロプロパンカルボン酸メチルまたはエチル(1)対アルコール(2)の比が出発原料の混合物の比に一致するポイントまたはその近くで計量供給されることが好ましい。
【0022】
シクロプロパンカルボン酸メチルまたはエチル(1)がアルコール(2)と共に計量供給される場合、導入のポイントは好ましくは重複第1カラム(A)の低い部分にある。
【0023】
第1カラム(A)は好ましくは40〜130℃、特に60〜110℃の温度で、そして0.1〜2.0バール、特に0.5〜1.2バールの圧力下で稼働する。
【0024】
第1カラム(A)は好ましくは2〜300、特に5〜50プレートを有する。
【0025】
第2カラム(B)は好ましくは40〜200℃、特に80〜180℃の温度で、そして0.01〜2.0バール、特に0.1〜1.2バールの圧力下で稼働する。
【0026】
第2カラム(B)は好ましくは1〜100、特に3〜30プレートを有する。
【0027】
〔第3カラム(C)による第1カラム(A)および第2カラム(B)の置換〕
第1カラム(A)および第2カラム(B)は好ましくは、容器(D)に連結されている第3カラム(C)によって置換される。
【0028】
第3カラム(C)は好ましくは、液体側で、そして適切な場合はガス側で容器(D)に連結される。
【0029】
第3カラム(C)は好ましくは40〜200℃、特に60〜180℃の温度で、そして0.01〜2.0バール、特に0.1〜1.2バールの圧力下で稼働する。
【0030】
第3カラム(C)は好ましくは5〜300、特に30〜60プレートを有する。
【0031】
第3カラム(C)での還流比(R/R)は好ましくは10/1〜1/1、特に好ましくは5/1〜2/1である。
【0032】
第3カラム(C)は好ましくは容器(D)として連結された反応器を有する。反応器の内容物(好ましくは有機相(8)のみ)は好ましくは第2〜第30番目プレート、特に好ましくは第3〜第15番目プレート、非常に特に好ましくは第6〜第10番目プレートに供給される。第3カラム(C)で下方に流れる液体は、好ましくは、反応混合物がカラム中へポンプ送液され且つ反応器中へ導入されるポイントの1〜10プレート上、特に好ましくは1〜5プレート上、非常に特に好ましくは1〜2プレート上にあるポイントで全体的にまたは部分的に取り出される。
【0033】
シクロプロパンカルボン酸エステル(1)は、適切な場合は、相当するアルコール(2)、塩化水素酸(3)および水(4)と混合されて、反応器、すなわち容器(D)中へ計量供給される。シクロプロパンカルボン酸エステル(1)がアルコール(2)と混合されて計量供給される場合、それは好ましくは反応器、すなわち容器(D)向けの取り出しポイントの上に配置された第3カラム(C)の部分へ導入される。
【0034】
蒸気(H)が形成され、そして排出される有機相と一緒に第3カラム(C)へ導入されるように、熱が容器(D)としての反応器中へ導入されることが好ましい。
【0035】
〔一般的情報〕
容器(D)からの混合物は、好ましくは、第2カラム(B)中へまたは第3カラム(C)中へ供給される前に追加の熱交換器を用いて加熱し、部分蒸発(G)させることができる。
【0036】
容器(D)は出発原料を92〜110℃、特に96〜100℃の温度に保持することが好ましい。
【0037】
水相中の塩化水素酸濃度(3)は、サンプルが室温まで冷却された後で、好ましくは4〜20%、特に好ましくは7〜14%、非常に特に好ましくは9〜12%である。
【0038】
塩化水素酸濃度(3)は、先行技術に記載されているように、センサーを用いて測定することができ、塩化水素酸(3)の導入をコントロールすることができる。容器(D)での第2の相(曇り点)の出現および消失は好ましくはコントロールのために利用される。濁りが消失した時、計量供給される量は濁りが再発するまで増やされ、次に、計量供給される量は濁りが再び消失するまで減らされる。
【0039】
塩化水素酸(3)が一定速度で計量供給されることも同様に可能であり、塩化水素酸濃度(3)は、濃度と共に増える塩化メチル形成によって確定される。
【0040】
水の計量供給添加は、冷却後の相の比によってコントロールされる。
【0041】
塩化水素酸(3)が除外される場合(これは混合物の腐食性の観点から利点を有する)、酸性固体(9)、特に好ましくはレワチット(Lewatit)(登録商標)またはナフィオン(Nafion)(登録商標)などのスルホン酸イオン交換樹脂を使用することが好ましい。これらの酸性固体(9)は容器(D)中へ導入され、スクリーンデバイスによってまたはパック材料(例えばモンツ(Montz)製のマルチパック(Multipack)(登録商標))としてそこに保持されるか、または容器(D)が固定床であるかのどちらかであり、それを通って混合物がポンプ送液される。
【0042】
本方法では、含水率は、第2の相が発生するほど高いものであるべきでなく、相分離(E)はそれ故必要ではない。水の計量供給添加はそれ故、例えば、混合物の沸点に応じて調節される。
【0043】
本方法は好ましくは連続的に、擬連続的にまたは回分式に実施される。
【0044】
シクロプロパンカルボン酸(5)の純度は、出発原料を基準にして、好ましくは>96%、特に>98%である。
【0045】
アルコール(2)の純度は、出発原料を基準にして、好ましくは>98.5%、特に>99.5%である。
【0046】
アルコール(2)は好ましくはメタノールおよび/またはエタノールである。
【0047】
装置は、複数の実施形態を示す図面を用いて以下に例示される。ここで、本発明のさらなる独創的な特徴および利点は、図面および本説明から導くことができる。
【0048】
本発明の独創的な範囲は、個々の請求項の主題によってだけでなく個々の請求項の互いの組み合わせによっても画定される。同じことは、本説明に開示されるすべてのパラメーターおよびそれらの任意の組み合わせに適用される。
【0049】
本発明は、それによって限定されることなく次の実施例によって例示される。
【0050】
[実施例]
測定方法
混合物の組成は、先行技術に相当するガスクロマトグラフ分析によって測定した。標準ガラスキャピラリーカラムのHP6890をクロマトグラフとして用いた。検出は水素炎イオン化検出器(FID)を用いて行った。検出限界は±0.1標準%(すなわち、重量%だが不検出成分なし)であった。
【0051】
塩化水素酸の濃度は滴定を用いて、極微量のケースでは蛍光X線を用いて測定した。検出限界は±10ppmであった。
【0052】
含水率はカール−フィッシャー(Karl−Fischer)法によって測定した。検出限界は±2相対%(すなわち、純水のケースでは2%、100ppmの含水率では2ppm)であった。
【0053】
〔実施例1(塩化水素酸(3)法)〕
装置を図1におけるように、しかしストリッピング・セクションの上流に部分蒸発(G)なしで構築した。それは、容器(D)として撹拌機付きのオイル加熱10Lフランジポットと、第1カラム(A)として約25プレートおよび凝縮器およびランバック・ディバイダーを有する重複カラムと、第2カラム(B)として約15プレートおよび凝縮器およびランバック・ディバイダーを有する重複カラムとを含んでいた。約550g/hのシクロプロパンカルボン酸メチル(1)および111g/hの10%強度の塩化水素酸(3)を、容器(D)としてのこのフランジポット中へ供給した。
【0054】
アルコール(2)としてメタノール、シクロプロパンカルボン酸メチル(1)、シクロプロパンカルボン酸(5)、塩化水素酸(3)および水(4)を含む約7Lの混合物は、容器(D)としてのフランジポット中で94〜95℃の沸点で沸騰する。第1カラム(A)の塔頂で、99%より高い純度を有し且つ0.17%の塩化メチル(6)および0.73%のシクロプロパンカルボン酸メチル(1)を含むメタノールを、64℃の温度およびR/R=2で取り出した。遊離の塩化水素酸(3)は10ppmの検出限界未満の濃度で蒸留液中に存在した。180g/hのメタノールは別として、15g/hの塩化メチル(6)が遊離したが、後者の主要部分は下流の冷トラップ中でのみ凝縮した。ランバック・ディバイダーは、76℃を超えた時にランバック・ディバイダーを全還流に設定する第1カラム(A)の中間での温度測定によってコントロールした。
【0055】
容器(D)からの混合物を相分離(E)にかけた。約1800g/hの有機相(8)を60℃に冷却し、分離し(E)、そして生成物としてシクロプロパンカルボン酸メチル(1)を集めるためにオーバーフロー付きのオイル加熱された10Lフランジポット上に配置された第2カラム(B)としての15プレートカラムの上方部へ供給した。フランジポットに182℃で沸騰する約6Lの液体を装入した。第2カラム(B)に、全て取り出す状態で稼働される還流ディバイダー付き凝縮器を重ねた。80℃で得られたオーバーヘッド生成物は2相よりなり、大部分はシクロプロパンカルボン酸メチル(1)および水(4)で構成され、約10%のメタノールおよび3.6%のシクロプロパンカルボン酸(5)を含有していた。2.1%のシクロプロパンカルボン酸無水物は別として他の成分が一切ない約480g/hのシクロプロパンカルボン酸(5)がフランジポットを出た。
【0056】
反応器の水相(7)は、滴定によれば約11%の(3)の含量を有していた。
【0057】
17%強度の塩化水素酸(3)をポンプ送入した時、塩化水素酸(3)の含量は12%に増加した。37%強度の塩化水素酸(3)は、14.5%の塩化水素酸(3)の含量をもたらした。この含量では、0.08%のブチロラクトンがシクロプロパンカルボン酸(5)中に検出され得た。水(4)と塩化水素ガス(3)とを混合することによって得られた50%強度の塩化水素酸(3)をポンプ送入した場合は、水相の塩化水素酸(3)含量は15%に上がり、0.14%のブチロラクトンがシクロプロパンカルボン酸(5)中に存在した。本方法を、曇り点で99.5℃で15%強度の塩化水素酸(3)および7%強度の塩化水素酸(3)の、または20%強度の塩化水素酸(3)および水(4)の交互導入によって実施した時、水相(7)は室温で約10%の塩化水素酸(3)を含有した。
【0058】
〔実施例2(酸性固体(9)−レワチット(登録商標)法)〕
装置を図2におけるように、しかしストリッピング・セクションの上流に部分蒸発(G)なしで構築した。容器(D)中の混合物を、反応器中にレワチットを残すためにスクリーンを通して反応器からポンプ送液した。第1および第2カラム(AおよびB)ならびにフランジポットは実施例1と同じものであった。酸性固体(9)として500gの市販の湿ったスルホン酸レワチット(K2431)が反応器中に存在した。280g/hのシクロプロパンカルボン酸メチル(1)および50g/hの水(4)を反応器中へポンプ送液した。99℃の沸点を水の導入によって維持した。温度が上った時には、導入される水の量もまた増やし、温度が低下した時には、導入される水の量もまた減らした。約0.2%のシクロプロパンカルボン酸メチル(1)を含有する約95g/hのメタノールが第1カラム(A)の塔頂で65℃で得られた。約700g/hの反応混合物をストリッピング・セクションへ供給した。ガスクロマトグラフィーによる分析によれば、3.5%のシクロプロパンカルボン酸無水物を含有する約240g/hのシクロプロパンカルボン酸(5)がストリッピング・セクションのフランジポットを出た。酸性固体(9)としてのレワチットは、1000時間後でさえ何の活性低下も示さなかった。
【図面の簡単な説明】
【0059】
【図1】塩化水素酸(3)を用いてシクロプロパンカルボン酸(5)およびアルコール(2)を製造するための装置。ここで、容器(D)、第1カラム(A)、第2カラム(B)、相分離(E)、冷却(F)および部分蒸発(G)は互いに連結されている。
【図2】酸性固体(9)(レワチット(登録商標))を用いてシクロプロパンカルボン酸(5)およびアルコール(2)を製造するための装置。ここで、容器(D)、第1カラム(A)、第2カラム(B)および部分蒸発(G)は互いに連結されている。
【図3】塩化水素酸(3)を用いてシクロプロパンカルボン酸(5)およびアルコール(2)を製造するための装置。ここで、容器(D)、第3カラム(C)、相分離(E)、冷却(F)および部分蒸発(G)は互いに連結されている。
【図4】酸性固体(9)(レワチット(登録商標))を用いてシクロプロパンカルボン酸(5)およびアルコール(2)を製造するための装置。ここで、容器(D)、第3カラム(C)および部分蒸発(G)は互いに連結されている。
【符号の説明】
【0060】
1 シクロプロパンカルボン酸メチルまたはエチル
2 アルコール
3 塩化水素酸
4 水
5 シクロプロパンカルボン酸
6 塩化メチル
7 水相
8 有機相
9 酸性固体
A 第1カラム
B 第2カラム
C 第3カラム
D 容器
E 相分離
F 冷却
G 部分蒸発
H 蒸気
【特許請求の範囲】
【請求項1】
シクロプロパンカルボン酸メチルまたはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて加水分解されることを特徴とするシクロプロパンカルボン酸(5)の製造方法であって、
a)アルコール(2)がカラム(A)の塔頂を通して取り出される状態で、自動撹拌機を備えていてもよく、かつ、凝縮器を備えた第1カラム(A)に連結されている容器(D)を含む装置中へ、シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、別々に、または一緒に供給され、そして、
1)シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、凝縮器を備えた第1カラム(A)中へ別々に、または一緒に導入されるか、または
2)シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、容器(D)中へ、別々にまたは一緒に供給されるか、または、
3)水(4)および、適切な場合、塩化水素酸(3)が容器(D)中へ、別々にまたは一緒に供給されながら、シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と混合されて、凝縮器を備えた第1カラム(A)中へ導入されるか
のいずれかであり、
b)直接にか、又はa)1)およびa)3)の場合は第1カラム(A)経由で全体的にまたは部分的に、容器(D)に入る反応混合物が、続いて凝縮器を備えた第2カラム(B)に供給され、シクロプロパンカルボン酸(5)がカラム(B)の塔底から取り出され、その間、残りの反応混合物は容器(D)に再循環され、そして塩化水素酸(3)が全く使用されない場合は、少なくとも1種の酸性固体(9)が容器(D)中に初めに配置されている、
製造方法。
【請求項2】
塩化水素酸(3)が使用される場合、容器(D)中に存在する反応混合物が、適切な場合冷却(F)後に、第2カラム(B)に供給される前に工程b)で相分離(E)にかけられて有機相と水相(7)とを形成し、水相(7)が容器(D)中へ導入され、そして有機相(8)が凝縮器を備えた第2カラム(B)中へ導入されることを特徴とする請求項1に記載の方法。
【請求項3】
シクロプロパンカルボン酸メチルまたはエチル(1)とアルコール(2)との混合物が、特に、第1カラム(A)においてシクロプロパンカルボン酸メチルまたはエチル(1)対アルコール(2)の比が出発原料の混合物における比に相当するポイントまたはその近くで、第1カラム(A)中へ計量供給されることを特徴とする請求項1または2に記載の方法。
【請求項4】
第1カラム(A)が40〜130℃、特に60〜110℃の温度で、および0.1〜2.0バール、特に0.5〜1.2バールの圧力下で稼働することを特徴とする請求項1〜3のいずれか一項に記載の方法。
【請求項5】
第1カラム(A)が2〜300、特に5〜50プレートを有することを特徴とする請求項1〜3のいずれか一項に記載の方法。
【請求項6】
第2カラム(B)が40〜200℃、特に80〜180℃の温度で、および0.01〜2.0バール、特に0.1〜1.2バールの圧力下で稼働することを特徴とする請求項1〜3のいずれか一項に記載の方法。
【請求項7】
第2カラム(B)が1〜100、特に3〜30プレートを有することを特徴とする請求項1〜3のいずれか一項に記載の方法。
【請求項8】
第1カラム(A)および第2カラム(B)が第3カラム(C)によって置き換えられ、かつ、この第3カラム(C)が容器(D)に連結されていることを特徴とする請求項1〜3のいずれか一項に記載の方法。
【請求項9】
第3カラム(C)が液体側でそして適切な場合ガス側で容器(D)に連結されていることを特徴とする請求項4に記載の方法。
【請求項10】
第3カラム(C)が40〜200℃、特に60〜180℃の温度で、および0.01〜2.0バール、特に0.1〜1.2バールの圧力下で稼働することを特徴とする請求項8または9に記載の方法。
【請求項11】
第3カラム(C)が5〜300、特に30〜60プレートを有することを特徴とする請求項8または9に記載の方法。
【請求項12】
容器(D)が出発原料を92〜110℃、特に96〜100℃の温度に保持することを特徴とする請求項1〜11のいずれか一項に記載の方法。
【請求項13】
レワチット(Lewatit)などのスルホン酸イオン交換樹脂が酸性固体(9)として使用されることを特徴とする請求項1〜12のいずれか一項に記載の方法。
【請求項14】
連続的に、擬連続的にまたは回分式で実施されることを特徴とする請求項1〜13のいずれか一項に記載の方法。
【請求項15】
シクロプロパンカルボン酸(5)の純度が出発原料を基準にして>96%、特に>98%であることを特徴とする請求項1〜14のいずれか一項に記載の方法。
【請求項16】
アルコール(2)の純度が出発原料を基準にして>98.5%、特に>99.5%であることを特徴とする請求項1〜15のいずれか一項に記載の方法。
【請求項17】
アルコール(2)がメタノールであることを特徴とする請求項1〜16のいずれか一項に記載の方法。
【請求項1】
シクロプロパンカルボン酸メチルまたはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて加水分解されることを特徴とするシクロプロパンカルボン酸(5)の製造方法であって、
a)アルコール(2)がカラム(A)の塔頂を通して取り出される状態で、自動撹拌機を備えていてもよく、かつ、凝縮器を備えた第1カラム(A)に連結されている容器(D)を含む装置中へ、シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、別々に、または一緒に供給され、そして、
1)シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、凝縮器を備えた第1カラム(A)中へ別々に、または一緒に導入されるか、または
2)シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と、ならびにさらに水(4)および、適切な場合、塩化水素酸(3)と混合されて、容器(D)中へ、別々にまたは一緒に供給されるか、または、
3)水(4)および、適切な場合、塩化水素酸(3)が容器(D)中へ、別々にまたは一緒に供給されながら、シクロプロパンカルボン酸メチルもしくはエチル(1)が、適切な場合1種もしくはそれ以上のアルコール(2)と混合されて、凝縮器を備えた第1カラム(A)中へ導入されるか
のいずれかであり、
b)直接にか、又はa)1)およびa)3)の場合は第1カラム(A)経由で全体的にまたは部分的に、容器(D)に入る反応混合物が、続いて凝縮器を備えた第2カラム(B)に供給され、シクロプロパンカルボン酸(5)がカラム(B)の塔底から取り出され、その間、残りの反応混合物は容器(D)に再循環され、そして塩化水素酸(3)が全く使用されない場合は、少なくとも1種の酸性固体(9)が容器(D)中に初めに配置されている、
製造方法。
【請求項2】
塩化水素酸(3)が使用される場合、容器(D)中に存在する反応混合物が、適切な場合冷却(F)後に、第2カラム(B)に供給される前に工程b)で相分離(E)にかけられて有機相と水相(7)とを形成し、水相(7)が容器(D)中へ導入され、そして有機相(8)が凝縮器を備えた第2カラム(B)中へ導入されることを特徴とする請求項1に記載の方法。
【請求項3】
シクロプロパンカルボン酸メチルまたはエチル(1)とアルコール(2)との混合物が、特に、第1カラム(A)においてシクロプロパンカルボン酸メチルまたはエチル(1)対アルコール(2)の比が出発原料の混合物における比に相当するポイントまたはその近くで、第1カラム(A)中へ計量供給されることを特徴とする請求項1または2に記載の方法。
【請求項4】
第1カラム(A)が40〜130℃、特に60〜110℃の温度で、および0.1〜2.0バール、特に0.5〜1.2バールの圧力下で稼働することを特徴とする請求項1〜3のいずれか一項に記載の方法。
【請求項5】
第1カラム(A)が2〜300、特に5〜50プレートを有することを特徴とする請求項1〜3のいずれか一項に記載の方法。
【請求項6】
第2カラム(B)が40〜200℃、特に80〜180℃の温度で、および0.01〜2.0バール、特に0.1〜1.2バールの圧力下で稼働することを特徴とする請求項1〜3のいずれか一項に記載の方法。
【請求項7】
第2カラム(B)が1〜100、特に3〜30プレートを有することを特徴とする請求項1〜3のいずれか一項に記載の方法。
【請求項8】
第1カラム(A)および第2カラム(B)が第3カラム(C)によって置き換えられ、かつ、この第3カラム(C)が容器(D)に連結されていることを特徴とする請求項1〜3のいずれか一項に記載の方法。
【請求項9】
第3カラム(C)が液体側でそして適切な場合ガス側で容器(D)に連結されていることを特徴とする請求項4に記載の方法。
【請求項10】
第3カラム(C)が40〜200℃、特に60〜180℃の温度で、および0.01〜2.0バール、特に0.1〜1.2バールの圧力下で稼働することを特徴とする請求項8または9に記載の方法。
【請求項11】
第3カラム(C)が5〜300、特に30〜60プレートを有することを特徴とする請求項8または9に記載の方法。
【請求項12】
容器(D)が出発原料を92〜110℃、特に96〜100℃の温度に保持することを特徴とする請求項1〜11のいずれか一項に記載の方法。
【請求項13】
レワチット(Lewatit)などのスルホン酸イオン交換樹脂が酸性固体(9)として使用されることを特徴とする請求項1〜12のいずれか一項に記載の方法。
【請求項14】
連続的に、擬連続的にまたは回分式で実施されることを特徴とする請求項1〜13のいずれか一項に記載の方法。
【請求項15】
シクロプロパンカルボン酸(5)の純度が出発原料を基準にして>96%、特に>98%であることを特徴とする請求項1〜14のいずれか一項に記載の方法。
【請求項16】
アルコール(2)の純度が出発原料を基準にして>98.5%、特に>99.5%であることを特徴とする請求項1〜15のいずれか一項に記載の方法。
【請求項17】
アルコール(2)がメタノールであることを特徴とする請求項1〜16のいずれか一項に記載の方法。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2006−282664(P2006−282664A)
【公開日】平成18年10月19日(2006.10.19)
【国際特許分類】
【出願番号】特願2006−86235(P2006−86235)
【出願日】平成18年3月27日(2006.3.27)
【出願人】(505422707)ランクセス・ドイチュランド・ゲーエムベーハー (220)
【Fターム(参考)】
【公開日】平成18年10月19日(2006.10.19)
【国際特許分類】
【出願日】平成18年3月27日(2006.3.27)
【出願人】(505422707)ランクセス・ドイチュランド・ゲーエムベーハー (220)
【Fターム(参考)】
[ Back to top ]

