シリビン配糖体含有皮膚外用組成物
【課題】シリビン配糖体を配合する皮膚外用組成物等を開発する
【解決手段】シリビン配糖体を含有する皮膚外用組成物
【解決手段】シリビン配糖体を含有する皮膚外用組成物
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、皮膚外用組成物に関する。
【背景技術】
【0002】
シリビンを主成分として含有するシリマリンは皮膚の老化を防ぐのに有用であり、紅斑、火傷、皮膚又は粘膜のジストロフィー状態、皮膚炎等の治療における治癒を促進し、外部環境からの刺激(放射線、風、太陽等)から皮膚を保護するのに有用であることが知られている(特許文献1:特開平1−100132号公報参照)。また、シリビンの表皮角化細胞の分化抑制効果(特許文献2:特開2004−91397号公報参照)、シリビンを主成分として含有するシリマリンのI型コラーゲン産生促進作用(特許文献3:WO2004/85429号公報参照)が知られている。
【0003】
一方、シリビンは、水、油にはほとんど溶解しないため、水系の組成物には配合し難いという課題点を有しており、シリマリンを分散させた飲料の技術(特許文献4:特開2002−34505号公報参照)、シリマリンをリン脂質錯体とすることにより生体適性を有利にする技術(特許文献1:特開平1−100132号公報参照)、マイクロエマルジョン組成物にして生体利用率を向上させる技術(特許文献5:特表2003−503441号公報参照)、シクロデキストリン誘導体を用いてシリビンの封入錯体を製造する技術(特許文献6:特開平3−206090号公報参照)が開示されている。
しかしながら、これらの技術を用いても必ずしもシリビンの析出を十分に抑制できない場合があり、シリビンの析出を抑制できたとしても、処方設計上の制約がある。
【0004】
シリビンのグルコース配糖体、ガラクトース配糖体、ラクトース配糖体、マルトース配糖体が抗酸化作用を有し、シリビンと比べて水溶性に優れることが知られているが(非特許文献1:Kosina P.et al.,Phytother. Res. 16,S33-S39(2002)参照) 、シリビン配糖体を含有する皮膚外用組成物、シリビン配糖体のシワ形成抑制効果、表皮角化細胞分化抑制効果、I型コラーゲン産生促進効果は知られていない。
【0005】
【特許文献1】特開平1−100132号公報
【特許文献2】特開2004−91397号公報
【特許文献3】WO2004/85429号公報
【特許文献4】特開2002−34505号公報
【特許文献5】特表2003−503441号公報
【特許文献6】特開平3−206090号公報
【非特許文献1】Kosina P.et al.,Phytother. Res. 16,S33-S39(2002)
【発明の開示】
【発明が解決しようとする課題】
【0006】
本発明は、シリビン配糖体を有効成分とする皮膚外用組成物等を開発することを課題とする。
【課題を解決するための手段】
【0007】
本発明者らは、シリビン配糖体を用いることにより本発明を完成した。
すなわち、本発明の主な構成は、次のとおりである。
【0008】
(1)シリビン配糖体を含有する皮膚外用組成物。
(2)シリビン配糖体が式(1)のシリビンラクトシドまたは式(2)のシリビンマルトシドであることを特徴とする(1)記載の皮膚外用組成物。
【化5】

式(1)
【化6】

式(2)
(3)シリビン配糖体を有効成分とするシワ形成抑制剤。
(4)シリビン配糖体を有効成分とする表皮角化細胞分化抑制剤。
(5)シリビン配糖体を有効成分とするI型コラーゲン産生促進剤。
(6)シリビン配糖体を有効成分とする日焼けによる肌荒れ改善剤。
(7)シリビン配糖体が式(1)のシリビンラクトシドまたは式(2)のシリビンマルトシドであることを特徴とする(3)〜(6)の何れかに記載の剤。
【化7】

式(1)
【化8】

式(2)
(8)水を溶媒として、シリビン配糖体を0.0008〜5.0重量%含有することを特徴とする(2)記載の皮膚外用組成物又は(7)記載の剤。
【発明の効果】
【0009】
1.溶解性の高いシリビン配糖体を用いることにより、シリビンの作用機序を向上させた皮膚外用組成物、シワ形成抑制剤、表皮角化細胞分化抑制剤、老化防止用皮膚外用組成物、I型コラーゲン産生促進剤、日焼けによる肌荒れ改善剤を提供することが可能となった。特に、水溶解性が高く、安全性、低刺激性、使用範囲が向上する。
2.特に、シリビン配糖体として、化学式(1)に示されるシリビンラクトシド又は化学式(2)に示されるシリビンマルトシドが有効である。
3.本発明で用いるシリビン配糖体は水溶性が高く、水溶液タイプの剤型として利用できる。化粧水、乳液、クリーム、パック等の皮膚外用組成物、メイクアップベースローション、メイクアップクリーム、乳液状又はクリーム状のファンデーションといったメイクアップ皮膚外用組成物、ハンドクリーム、レッグクリーム、ボディローション等の身体用皮膚外用組成物、入浴剤等とすることができる。
4.本発明で用いるシリビン配糖体は、0.0008〜5.0重量%を水に溶解させることができる。乳液などでも、水性部分に高配合することができる。
【図面の簡単な説明】
【0010】
【図1】表皮角化細胞分化抑制試験結果を示す図。
【図2】表皮角化細胞増殖維持試験結果を示すグラフ。
【図3】I型コラーゲン産生促進試験結果を示す図。
【図4】図3に示されるバンド強度をイメージ処理して数値化して示したグラフ。
【図5】紫外線照射試験を行ったマウスの水分蒸散量を測定した値を示すグラフ。
【図6】紫外線照射試験を行ったマウスの皮膚レプリカ表面のしわ体積率示すグラフ。
【発明を実施するための形態】
【0011】
シリビン(Silybin;CAS No.22888−70−6)は、キク科マリアアザミ(学名シリバム・マリアナムSilibum marianum Gaertn、別名オオアザミ、オオヒレアザミ、ミルクアザミ;CAS No.84604−20−6)から抽出されるフラボノリグナンの一種である。マリアアザミから抽出されるフラボノリグナンはシリマリン(Silymarin;CAS No.65666−07−1)の総称で呼ばれ、シリビン以外に、シリジアニン(Silydianin;CAS No.29782−68−1)、シリクリスチン(Silychristin;CAS No.33889−69−9)、イソシリビン(Isosilybin;CAS No.72581−71−6)などが含まれている。
シリビンはシリマリンからクロマトグラフィーを用いて単離することが可能であり、また、試薬を購入して入手することが可能である。
【0012】
シリビン配糖体は文献(Kren V. et al., J.Chem.Soc.,Perkin Trans 1,2467-2474(1997))に従って、ルイス酸を触媒として、シリビンにアセチル基で水酸基を保護した糖を結合し、脱アセチル化することにより調製できる。この反応系ではシリマリンの第一級アルコールの水酸基に糖が選択的にグリコシド結合する。
シリビンに、ルイス酸を触媒として、パーアセチルラクトースを反応させてグリコシド結合を生成し、脱アセチル化することにより、式(1)のシリビンラクトシドが得られる。
【化9】

式(1)
【0013】
シリビンに、ルイス酸を触媒として、パーアセチルマルトースを反応させてグリコシド結合を生成し、脱アセチル化することにより、式(2)のシリビンマルトシドが得られる。
【化10】

式(2)
【0014】
本発明に用いるシリビン配糖体は水溶性に優れ、シリビンラクトシド、シリビンマルトシドは水に約5%溶解することができる。従って、シリビンを配合することができなかった化粧水類にもシリビン配糖体であれば配合することができる。
【0015】
本発明の皮膚外用組成物には、本発明の効果を損なわない範囲内で、油剤、界面活性剤、防腐剤、多価アルコール、エタノール、糖類、金属イオン封鎖剤、水溶性高分子のような高分子、増粘剤、粉体成分、紫外線吸収剤、紫外線遮断剤、保湿剤、香料、pH調整剤等を含有させることができる。また、ビタミン類、皮膚賦活剤、血行促進剤、常在菌コントロール剤、活性酸素消去剤、抗炎症剤、美白剤、殺菌剤等の他の薬効成分、生理活性成分を含有させることもできる。
【0016】
本発明は、本発明に用いるシリビン配糖体は水溶性に優れており、シリビンラクトシド、シリビンマルトシドは水に約5%溶解することができる。従って、シリビンを配合することが困難であった化粧水類にもシリビン配糖体を配合することができる。
本発明のシリビン配糖体を有効成分とするシワ形成抑制剤としては、化粧水、乳液、クリーム、パック等のシワ改善用皮膚外用組成物、シワ改善用の医薬部外品、シワ改善用医薬が挙げられる。乳液であっても、水性部分にシリビン配糖体を高濃度で配合することができる。
【0017】
本発明のシリビン配糖体を有効成分とする表皮角化細胞分化抑制剤は、表皮角化細胞の分化を抑制し、増殖を維持し、ターンオーバーの遅延を予防、防止、改善し、加齢や紫外線照射により引き起こされる表皮の偏平化を防ぎ、老化した皮膚を再生する作用を有するので、老化防止用皮膚外用組成物として用いることができる。
本発明の、シリビン配糖体を有効成分とするI型コラーゲン産生促進剤は、皮膚のはりや弾力性を向上させ、しわやたるみを予防、防止、改善することが期待できるので、老化防止用皮膚外用組成物として用いることができる。
【0018】
〔シリビンラクトシドの合成〕
Helferichの方法に従ってシリビンラクトシドを合成した。
シリビン(3.0g、6.2mol)とオクタ-O-アセチル-D-ラクトース(6.3g、9.2mol)とを180 mlのジクロロメタン−アセトニトリル(1:1、v/v)の溶媒中で、三ふっ化ほう素ジメチルエーテル錯体(1.14ml、12.4mmol)を窒素存在下、室温で 19時間攪拌反応させた。反応終了後、氷冷しながら飽和炭酸水素ナトリウム水溶液を加え、150mlジクロロメタンで2回抽出処理し、無水硫酸ナトリウム処理後に抽出溶媒をエバポレーターにて除去した。
トリエチルアミン−メタノール−水(1:8:1)を35℃30時間反応させたのち、エバポレーターにより溶媒を除去した。BONDESIL-C18(Varian)を用いて精製を行い、シリビンラクトシド(1.0 g, 収率20%)を得た。得られたシリビンラクトシドをMSスペクトルで確認し、[M+H]+:807.5のピークを検出した。
【0019】
〔シリビンマルトシドの合成〕
Helferichの方法に従ってシリビンマルトシドを合成した。
シリビン(3.0g、6.2mol)とオクタ-O-アセチル-D-マルトース(6.3g、9.2mol)とを180mlのジクロロメタン−アセトニトリル(1:1、v/v)の溶媒中で、三ふっ化ほう素ジメチルエーテル錯体(1.14ml、12.4mmol)を窒素存在下、室温で 19時間攪拌反応させた。反応終了後、氷冷しながら飽和炭酸水素ナトリウム水溶液を加え、150mlジクロロメタンで2回抽出処理し、無水硫酸ナトリウム処理後に抽出溶媒をエバポレーターにて除去した。
トリエチルアミン−メタノール−水(1:8:1)を35℃30時間反応させたのち、エバポレーターにより溶媒を除去した。BONDESIL-C18(Varian)を用いて精製を行い、シリビンマルトシド(1.0g, 収率20%)を得た。得られたシリビンラクトシドをMSスペクトルで確認し、[M+H]+:807.5のピークを検出した。
【実施例1】
【0020】
水溶性試験
1.実験方法
シリビン、シリビンラクトシド、シリビンマルトシド(以下、シリビンをSB、シリビンラクトシドをSBL、シリビンマルトシドをSBMと記載することがある)を1.5mlチューブに適量はかりとり、そこに精製水を各濃度になるように加え、外観の透明性、また室温で遠心分離(15000rpm、5min)した際に沈殿として析出するかどうかを目視で判定した。またSBについては、非常に水溶性が悪いためビーカー内に少量はかりとり、水を加えてスターラーで約1時間かき混ぜ、混合操作を止めて1時間後に沈殿物が認められないものを溶解したと判定した。
【0021】
【表1】

【0022】
実験の結果、SBと比較してSBL、SBMの両者は劇的な水溶性の向上が認められ、約5000倍以上に水溶性が改善した。SBL、SBM間での溶解性の優劣は検出することはできなかった。SB濃度0.01mMは0.0005%(w/v)に相当する。SBL及びSBMの濃度50mM、60mMは、それぞれ4.1%(w/v)、4.9%(w/v)に相当する。従って、SBとSBL、SBMの溶解性を質量/容量%で比較すると、SBL、SBMの溶解性は、SBと比べて約10,000倍改善している。水溶性タイプの皮膚外用組成物などの剤では、SBでは、0.0005%(w/v)の濃度で含有させることも難しかったが、SBLでは、4.1%(w/v)の濃度で含有させることが可能であり、SBMでは、5.0%(w/v)の濃度で含有させることが可能である。尚、SBL、SBMの濃度0.01mMは0.0008%(w/v)に相当する。
【実施例2】
【0023】
表皮角化細胞分化抑制試験・増殖維持作用
1.実験材料
1.1 ヒト正常表皮角化細胞
ヒト正常表皮角化細胞NHEK(旭テクノグラス)を表皮角化細胞用培地:KGM(旭テクノグラス)で37℃-5%CO2インキュベーターにて培養した。本実験には経代数が3〜5代の細胞を利用した。
1.2 KGM(表皮角化細胞用培地)
KGMは表皮角化細胞基礎培地にヒト上皮細胞増殖因子(0.1ng/ml)、インシュリン(5.0μg/ml)、ハイドロコルチゾン(0.5μg/ml)、ゲンタマイシン(50μg/ml)、アンフォテリシンB(50μg/ml)、牛脳下垂体抽出液(2ml)を添加したものである。シリビン配糖体ははじめとするサンプルを細胞に添加する場合には、牛脳下垂体抽出液のみを除いた、KGM培地を用いて実験を行った。
1.3 添加サンプル
シリビン(SB)、シリビンマルトシド(SBM)、シリビンラクトシド(SBL)をDMSO(ジメチルスフフォキシド:和光純薬)に溶解し、各種濃度にて添加した。
【0024】
2.実験方法
2.1 表皮角化細胞分化抑制試験
NHEKをKGMで5×104/mlになるように懸濁し、4ml/ウエルで6穴プレートに播種し、24時間培養して、プレートに細胞を接着させた。各化合物を添加した牛脳下垂体抽出液を除いたKGMを4ml/ウエルで処理し、2日毎に培地交換しながら、8〜10日間培養した。毎日顕微鏡で形態観察を行い、DMSO処理したコントロール細胞が分化様の形態変化(扁平化)を示した時点で、写真撮影を行い、培養を終了した。
2.2 表皮角化細胞増殖維持試験
上記実験で得られた細胞をトリプシン処理によりプレートからはがした後に、KGM中で2.5×104/mlとなるように懸濁した。細胞懸濁液を2ml/ウエルで24穴プレートに播種し、2日ごとに培地交換しながら、8日間培養した。培養後、NHEKをトリプシン処理によりプレートからはがし、コールカウンター(ベックマン・コールター)により細胞数を測定した。
3.実験結果
3.1 表皮角化細胞分化抑制試験
得られた実験結果を図1に示す。この図は、細胞の顕微鏡写真である。
DMSOを処理した比較対照群であるControl並びにSB 3μM(シリビンを3μM添加した培地で培養)では、表皮角化細胞は扁平化し、分化様の形態変化を示した。それに対して、SBM3μM、SBL3μMでは分化様の形態は認められなかった。SB、SBL、SBMをそれぞれ10μM添加した培地で培養した場合には、全て、表皮角化細胞の分化が抑制された。SB、SBL、SBMは表皮角化細胞の分化抑制作用を有するが、SBM、SBLはSBに比べて表皮角化細胞分化抑制効果に優れている。
【0025】
3.2 表皮角化細胞増殖維持試験
上記の表皮角化細胞分化抑制試験において、分化が抑制されていれば細胞は増殖能を維持し、継代作業をすることで順次増殖するはずである。分化誘導された細胞は分化が付加逆的な反応であるため増殖することはできない。
そこで上記試験で得られた細胞を継代し、維持されている増殖能を増殖した細胞の数を測定することで調べた。
【0026】
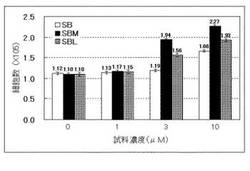
その結果を図2に示す。試料濃度3μMでは、SBを添加したものについて細胞増殖能は殆ど維持されていないが、SBMは試料無添加と比べて1.8倍、SBLは試料無添加と比べて1.4倍に細胞数が増加し、細胞増殖能の維持効果が認められた。試料濃度10μMでは、SB、SBM、SBLともに細胞数が増加し、SBは試料無添加と比べて1.5倍、SBMは試料無添加と比べて2.1倍、SBLは試料無添加と比べて1.8倍に細胞数が増加し、細胞増殖能の維持効果が認められた。SBと比べて、SBM、SBLの細胞増殖能の維持効果が高いことがわかる。
【実施例3】
【0027】
I型コラーゲン産生促進作用
1.実験材料
1.1 ヒト皮膚繊維芽細胞
ヒト皮膚繊維芽細胞CCD1074SK(大日本住友製薬)をD-MEM中で37℃-5% CO2インキュベーターにて培養した。本実験には経代数が10〜15代の細胞を利用した。
1.2 D-MEM
D-MEMは、D-MEM基礎培地(GIBCO)に牛胎児血清(Hyclone)を10%になるよう添加して用いた。またサンプルを処理する際には、牛胎児血清を入れないD-MEMを用いて実験を行った。
2.実験方法
ヒト皮膚繊維芽細胞CCD1074SKを10%牛胎児血清を含むD-MEM培地で3×105/mlになるように懸濁し、10cmシャーレに1ml播種し、24時間培養し、プレートに細胞を接着させた。培地をDMSOに溶解させた各サンプルを各濃度で添加した牛胎児血清を入れないD-MEM培地に交換した。培地交換48時間後に細胞培養液を回収し、限外ろ過装置を用いて培養液を濃縮した。約500ml以下に濃縮後、タンパク質定量を行い、タンパク質量をそろえた後に、細胞培養液濃縮サンプルとしてウエスタンブロティングに使用した。
1レーン当り10μgのタンパク質をアプライし、SDS-PAGEで分離後、ニトロセルロース膜に転写した。転写後のニトロセルロース膜をブロッキング溶液(スキムミルクを5%の濃度になるように0.1%のポリオキシエチレン(20)ソルビタンモノラウレートを含むPBSで溶解した溶液)に浸し、4℃で一昼夜ブロッキングした。洗浄液{0.1%のポリオキシエチレン(20)ソルビタンモノラウレートを含むPBS}で洗浄後、一次抗体{洗浄液で500ng/mlに調製したI型コラーゲンに対するポリクローナル抗体(ロックランド)}に浸し、室温で1時間反応させた。洗浄後、二次抗体(洗浄液で250ng/mlに調製したホースラディッシュパーオキシダーゼ標識化抗ウサギイムノグロブリンG)に浸し、室温で1時間反応させた。洗浄後、ECLプラスウエスタンプロッティング検出試薬(アマシャムバイオサイエンス社)を用いて検出した。
【0028】
実験結果
実験の結果、SBと同様にSBL、SBMの両者にもI型コラーゲン産生促進作用が認められた。実験結果を図3に示す。
【0029】
得られたバンドの強度をプログラムソフトImage Jにより数値化した結果を表2に示し、DMSO処理時のI型コラーゲンの産生量を1とした際の比較産生量を図4として示す。
【0030】
【表2】

【0031】
SB、SBM、SBLともにI型コラーゲン産生促進作用を示した。SBと比べて、SBM、SBLはI型コラーゲン産生促進効果が強い。特に、試料濃度10μMでは、SBM、SBLの作用効果が大きく、高濃度での顕著な作用効果が認められる。
【実施例4】
【0032】
紫外線照射による水分蒸散抑制作用シワ形成抑制作用
1.実験材料・器具
実験動物ヘアレスマウスHos;HR1 ♀ 5週齢 (星野実験材料)
1.2 紫外線照射装置
紫外線A波(FL32SBL/DMR:(株)クリニカルサプライ製)
紫外線B波(FL32SE/DMR:(株)クリニカルサプライ製)
1.3 経皮水分蒸散量測定装置
Vapometer(キーサイエンス社製)
1.4 レプリカ採取器具およびレプリカ解析システム
(有)アサヒバイオメッド製の反射型レプリカ採取キット及びレプリカ解析システムASA‐03RXD
【0033】
2.実験方法
2.1 飼育環境
25℃±2℃、湿度50%±5%、食餌は飼料MR、水道水をそれぞれ自由摂取できるコンベンショナルな飼育環境で飼育した。
一群につき5匹を群分けし同一ケージにて飼育した。
日照は午前7時〜午後7時までの12時間ごとに昼夜を設定した。
2.2 紫外線照射
へアレスマウスHos;HR1を1週間馴化したのち紫外線照射を開始した。紫外線照射時は、ヘアレスマウスを専用のケージに移し、1群ずつUVB20mJ/cm2およびUVA10J/cm2の紫外線を照射した。照射は月、水および金の週3日サイクルで10週間実施し、合計30回紫外線を照射した。
【0034】
2.3 群設定
紫外線照射後30分以内にSB、SBL、SBMメタノール溶液又は溶媒(メタノール)をマウス背部皮膚全面に100μL処理した。SB、SBL、SBM塗布の濃度設定をそれぞれ1.0%、0.3%、0.1%の3点設定し、これら全群については紫外線照射を行った。溶媒であるメタノールのみを塗布するものについて、紫外線未照射及び紫外線照射の群を設けた。溶媒にメタノールを用いたのはSBを溶解するためである。メタノール中において、SBM、SBLは1%濃度においても完全に溶解していたが、SBは0.1%のみが完全に溶解しているが、0.3%は若干析出が認められ、1%においては不溶物が認められた。SBメタノール溶液に不溶物が認められた場合も、そのまま実験に用いた。
【0035】
2.4 経皮水分蒸散量の測定
経皮水分蒸散量の測定は、VapoMeter(キーストン サイエンティフィック社製)を用い、背部の尾付け根より首に向かい2cm、腰椎から右側に0.5cm部位を3回測定して平均を求めた。測定端末の開口部はNailモード(開口部を狭くすることで、マウス皮膚の狭い範囲に対応した)を用い、1回ごとの測定時間に約19秒を要した。測定日は、紫外線照射10週間後に行った。
【0036】
2.5 レプリカ画像解析
シワの形成を正確に把握するためレプリカを採取した。レプリカ画像解析は反射用レプリカ解析システムASA‐03RXD((有)アサヒバイオメッド製)を使用して行った。ASA‐03RXDを用いて、採取したレプリカに角度27度からの平行光(LED光源)を照射する事により得られるシワの形状に応じた陰影画像をCCDカメラで撮像し、コンピュータに取り込み画像処理することでレプリカ表面のしわ体積率(μm3/mm2/100)を計測した。
【0037】
2.6 統計解析
試験結果は平均値±標準偏差(S.D.)で表し、有意差検定は等分散性の検定をバートレット検定により行った。等分散性の仮定が棄却されなかった時はDunnettの多重検定を行い、等分散性の仮定が棄却された時は参考データとしてDunnettの多重検定を行った。
【0038】
3.試験結果
3.1 体重変動、外観観察
10週間照射終了後、各群間で体重変遷に目立った違いは無かった。重篤な病変を示したマウスもいなかった。
マウス皮膚の外観を観察した結果、群2の紫外線照射メタノール処理群ではシワ形成が認められるのにたいし、群4の0.3%シリビン塗布群、群6〜群8の全てのSBM塗布群、群9〜群11の全てのSBL塗布群においてシワ抑制作用が認められた。
【0039】
3.2 経皮水分蒸散量
肌荒れの指標として、紫外線照射10週間後にVapoMeterを用いて各群の水分蒸散量を測定した。結果を表3と図5に示す。
群1紫外線未照射群に比べて群2の紫外線照射群では経皮水分蒸散量が高くなる。群3〜群11のシリビン(SB)、シリビン配糖体(SBM、SBL)塗布群では、危険率1%以下で有意に経皮水分蒸散量の上昇が抑制されていた。
【0040】
1群(紫外線非照射、メタノール塗布)の水分蒸散量を0%、2群(紫外線照射、メタノール塗布)の水分蒸散量を100%としたとき、3〜5群(紫外線照射、SB0.1〜1%塗布)の水分蒸散量は26〜76%、6〜8群(紫外線照射、SBM0.1〜1%塗布)の水分量は11〜21%、9〜11群(紫外線照射、SBL0.1〜1%塗布)の水分量は24〜27%となり、SB、SBM、SBLを添加することにより水分蒸散量の上昇が抑制された。特に、シリビン配糖体であるSBM、SBLの水分蒸散量の上昇抑制効果が高い。つまり日焼けによる肌荒れを改善する効果がある。
【0041】
【表3】

【0042】
3.3 シワ体積率
10週間照射終了後、シワの形成を正確に把握するためレプリカを採取し、画像解析によりレプリカ表面のしわ体積率(μm3/mm2/100)を計測した。結果を表4、図6に示す。
【0043】
Dunnettの有意差検定を実施した結果、群2(紫外線照射メタノール塗布)に対して、群1(紫外線未照射メタノール塗布)、群4(紫外線照射 SB0.3%塗布)、群7(紫外線照射 SBM0.3%塗布)、群11(紫外線照射 SBL1.0%塗布)は、それぞれ危険率5%以下で有意にシワ体積が抑制された。
【0044】
【表4】

【0045】
〔処方例1 化粧水〕
質量%
1.シリビンラクトシド 0.3
2.ジグリセリン 5.0
3.1,3−ブチレングリコール 2.0
4.ジプロピレングリコール 3.0
5.水酸化カリウム 適量
6.クエン酸 適量
7.精製水 残余
(製法)
7に1〜6を溶解した。
【0046】
〔処方例2 乳液〕
質量%
1.シリビンマルトシド 0.3
2.水素添加大豆リン脂質 0.7
3.ステアリン酸デカグリセリル(HLB12) 2.0
4.グリセリン 8.0
5.オリーブ油 8.0
6.ベヘニルアルコール 1.0
7.ジプロピレングリコール 8.0
8.カルボキシビニルポリマー 0.1
9.キサンタンガム 0.2
10.水酸化カリウム 適量
11.クエン酸 適量
12.精製水 残余
(製法)
1〜4及び7〜12を80℃で加温溶解する。これに、約80℃に加温した5、6を加え、ホモミキサーで攪拌混合し、30℃まで冷却し、乳液を得た。
【0047】
〔処方例3 モイスチャー美容液〕
質量%
1.シリビンラクトシド 0.2
2.水素添加大豆リン脂質 0.6
3.モノオレイン酸デカグリセリル(HLB12) 1.5
4.グリセリン 7.0
5.1,3−ブチレングリコール 5.0
6.ポリエチレングリコール4000 0.1
7.スクワラン 5.0
8.シリコーン 0.5
9.ラウロイルグルタミン酸ジ(フィトステリル/オクチルドデシル)
0.2
10.キサンタンガム 0.3
11.水酸化カリウム 適量
12.クエン酸 適量
13.精製水 残余
(製法)
1及び11〜13を攪拌溶解し、4〜6、10を添加後約80℃に加温溶解する。
これに、約80℃に加温した2、3、7〜9を加え、30℃まで冷却し、モイスチャー美容液を得た。
【0048】
〔処方例4 エモリエントクリーム〕
質量%
1.シリビンマルトシド 0.5
2.ジグリセリン 10.0
3.ジプロピレングリコール 8.0
4.1,2−ペンタンジオール 0.5
5.L−セリン 0.01
6.ジステアリン酸デカグリセリル(HLB9.5) 0.5
7.モノミリスチン酸デカグリセリル(HLB14) 1.5
8.オリーブ油 10.0
9.マカデミアナッツ油 1.0
10.ベヘニルアルコール 1.5
11.シリコーン 2.0
12.ホホバ油 3.0
13.トコフェロール 0.001
14.SIMULGEL NS(SEPPIC社製) 2.0
15.キサンタンガム 0.1
16.水酸化カリウム 適量
17.クエン酸 適量
18.精製水 残余
(製法)
1及び16〜18を攪拌溶解し、2〜5を添加後約80℃に加温溶解する。これに、約80℃に加温した6〜14を加え、30℃まで冷却し、エモリエントクリームを得た。
【0049】
〔処方例5 ボディ用乳液〕
質量%
1.シリビンラクトシド 0.2
2.PEG-60水添ヒマシ油(HLB14) 1.5
3.グリセリン 9.0
4.ジプロピレングリコール 7.0
5.ヒアルロン酸Na 0.001
6.流動パラフィン 10.0
7.シリコーン 3.0
8.オクチルドデカノール 4.0
9.(アクリル酸/アクリル酸アルキル(C10-30))コポリマー 0.2
10.水酸化カリウム 適量
11.クエン酸 適量
12.精製水 残余
13. エタノール 2.5
(製法)
1及び10〜12を攪拌溶解し、2〜5、9を添加後約80℃に加温溶解する。これに、約80℃に加温した6〜8を加え、30℃まで冷却、13を添加し、ボディ用乳液を得た。
【0050】
〔処方例6 マッサージクリーム〕
質量%
1.シリビンマルトシド 0.05
2.グリセリン 10.0
3.ジグリセリン 2.0
4.プロピレングリコール 7.0
5.モノステアリン酸デカグリセリル(HLB12) 1.0
6.エチルヘキサン酸セチル 12.0
7.ベヘニルアルコール 2.0
8.ステアリン酸 0.5
9.セピノブ EMT10(SEPPIC社製) 0.5
10.香料 適量
11.フェノキシエタノール 0.3
12.水酸化カリウム 適量
13.クエン酸 適量
14.精製水 残余
(製法)
1及び11〜14を攪拌溶解し、2〜4を添加後約80℃に加温溶解する。これに、約80℃に加温した5〜9を加え、30℃まで冷却、10を添加し、マッサージクリームを得た。
【0051】
〔処方例7 乳化型ファンデーション〕
質量%
1.シリビンラクトシド 0.1
2.グリセリン 10.0
3.ジプロピレングリコール 8.0
4.1,2−ペンタンジオール 1.0
5.キサンタンガム 0.3
6.トリイソステアリン酸ポリグリセリル-2 1.0
7.シクロメチコン 8.0
8.シリコーン 5.0
9.ネオペンタン酸イソステアリル 5.0
10.イソステアリン酸 1.5
11.ベヘニルアルコール 0.5
12.パルミチン酸デキストリン 1.0
13.タルク 3.0
14.二酸化チタン 5.0
15.ベンガラ 0.5
16.黄酸化鉄 1.4
17.黒酸化鉄 0.1
18.水酸化カリウム 適量
19.クエン酸 適量
20.精製水 残余
(製法)
1及び18〜20を攪拌溶解し、2〜5を添加後約70℃に加温溶解する。次に、よく粉砕した13〜17を添加し、攪拌混合する。これに、約80℃に加温した6〜12を加え、30℃まで冷却し、乳化型ファンデーションを得た。
【技術分野】
【0001】
本発明は、皮膚外用組成物に関する。
【背景技術】
【0002】
シリビンを主成分として含有するシリマリンは皮膚の老化を防ぐのに有用であり、紅斑、火傷、皮膚又は粘膜のジストロフィー状態、皮膚炎等の治療における治癒を促進し、外部環境からの刺激(放射線、風、太陽等)から皮膚を保護するのに有用であることが知られている(特許文献1:特開平1−100132号公報参照)。また、シリビンの表皮角化細胞の分化抑制効果(特許文献2:特開2004−91397号公報参照)、シリビンを主成分として含有するシリマリンのI型コラーゲン産生促進作用(特許文献3:WO2004/85429号公報参照)が知られている。
【0003】
一方、シリビンは、水、油にはほとんど溶解しないため、水系の組成物には配合し難いという課題点を有しており、シリマリンを分散させた飲料の技術(特許文献4:特開2002−34505号公報参照)、シリマリンをリン脂質錯体とすることにより生体適性を有利にする技術(特許文献1:特開平1−100132号公報参照)、マイクロエマルジョン組成物にして生体利用率を向上させる技術(特許文献5:特表2003−503441号公報参照)、シクロデキストリン誘導体を用いてシリビンの封入錯体を製造する技術(特許文献6:特開平3−206090号公報参照)が開示されている。
しかしながら、これらの技術を用いても必ずしもシリビンの析出を十分に抑制できない場合があり、シリビンの析出を抑制できたとしても、処方設計上の制約がある。
【0004】
シリビンのグルコース配糖体、ガラクトース配糖体、ラクトース配糖体、マルトース配糖体が抗酸化作用を有し、シリビンと比べて水溶性に優れることが知られているが(非特許文献1:Kosina P.et al.,Phytother. Res. 16,S33-S39(2002)参照) 、シリビン配糖体を含有する皮膚外用組成物、シリビン配糖体のシワ形成抑制効果、表皮角化細胞分化抑制効果、I型コラーゲン産生促進効果は知られていない。
【0005】
【特許文献1】特開平1−100132号公報
【特許文献2】特開2004−91397号公報
【特許文献3】WO2004/85429号公報
【特許文献4】特開2002−34505号公報
【特許文献5】特表2003−503441号公報
【特許文献6】特開平3−206090号公報
【非特許文献1】Kosina P.et al.,Phytother. Res. 16,S33-S39(2002)
【発明の開示】
【発明が解決しようとする課題】
【0006】
本発明は、シリビン配糖体を有効成分とする皮膚外用組成物等を開発することを課題とする。
【課題を解決するための手段】
【0007】
本発明者らは、シリビン配糖体を用いることにより本発明を完成した。
すなわち、本発明の主な構成は、次のとおりである。
【0008】
(1)シリビン配糖体を含有する皮膚外用組成物。
(2)シリビン配糖体が式(1)のシリビンラクトシドまたは式(2)のシリビンマルトシドであることを特徴とする(1)記載の皮膚外用組成物。
【化5】

式(1)
【化6】

式(2)
(3)シリビン配糖体を有効成分とするシワ形成抑制剤。
(4)シリビン配糖体を有効成分とする表皮角化細胞分化抑制剤。
(5)シリビン配糖体を有効成分とするI型コラーゲン産生促進剤。
(6)シリビン配糖体を有効成分とする日焼けによる肌荒れ改善剤。
(7)シリビン配糖体が式(1)のシリビンラクトシドまたは式(2)のシリビンマルトシドであることを特徴とする(3)〜(6)の何れかに記載の剤。
【化7】

式(1)
【化8】

式(2)
(8)水を溶媒として、シリビン配糖体を0.0008〜5.0重量%含有することを特徴とする(2)記載の皮膚外用組成物又は(7)記載の剤。
【発明の効果】
【0009】
1.溶解性の高いシリビン配糖体を用いることにより、シリビンの作用機序を向上させた皮膚外用組成物、シワ形成抑制剤、表皮角化細胞分化抑制剤、老化防止用皮膚外用組成物、I型コラーゲン産生促進剤、日焼けによる肌荒れ改善剤を提供することが可能となった。特に、水溶解性が高く、安全性、低刺激性、使用範囲が向上する。
2.特に、シリビン配糖体として、化学式(1)に示されるシリビンラクトシド又は化学式(2)に示されるシリビンマルトシドが有効である。
3.本発明で用いるシリビン配糖体は水溶性が高く、水溶液タイプの剤型として利用できる。化粧水、乳液、クリーム、パック等の皮膚外用組成物、メイクアップベースローション、メイクアップクリーム、乳液状又はクリーム状のファンデーションといったメイクアップ皮膚外用組成物、ハンドクリーム、レッグクリーム、ボディローション等の身体用皮膚外用組成物、入浴剤等とすることができる。
4.本発明で用いるシリビン配糖体は、0.0008〜5.0重量%を水に溶解させることができる。乳液などでも、水性部分に高配合することができる。
【図面の簡単な説明】
【0010】
【図1】表皮角化細胞分化抑制試験結果を示す図。
【図2】表皮角化細胞増殖維持試験結果を示すグラフ。
【図3】I型コラーゲン産生促進試験結果を示す図。
【図4】図3に示されるバンド強度をイメージ処理して数値化して示したグラフ。
【図5】紫外線照射試験を行ったマウスの水分蒸散量を測定した値を示すグラフ。
【図6】紫外線照射試験を行ったマウスの皮膚レプリカ表面のしわ体積率示すグラフ。
【発明を実施するための形態】
【0011】
シリビン(Silybin;CAS No.22888−70−6)は、キク科マリアアザミ(学名シリバム・マリアナムSilibum marianum Gaertn、別名オオアザミ、オオヒレアザミ、ミルクアザミ;CAS No.84604−20−6)から抽出されるフラボノリグナンの一種である。マリアアザミから抽出されるフラボノリグナンはシリマリン(Silymarin;CAS No.65666−07−1)の総称で呼ばれ、シリビン以外に、シリジアニン(Silydianin;CAS No.29782−68−1)、シリクリスチン(Silychristin;CAS No.33889−69−9)、イソシリビン(Isosilybin;CAS No.72581−71−6)などが含まれている。
シリビンはシリマリンからクロマトグラフィーを用いて単離することが可能であり、また、試薬を購入して入手することが可能である。
【0012】
シリビン配糖体は文献(Kren V. et al., J.Chem.Soc.,Perkin Trans 1,2467-2474(1997))に従って、ルイス酸を触媒として、シリビンにアセチル基で水酸基を保護した糖を結合し、脱アセチル化することにより調製できる。この反応系ではシリマリンの第一級アルコールの水酸基に糖が選択的にグリコシド結合する。
シリビンに、ルイス酸を触媒として、パーアセチルラクトースを反応させてグリコシド結合を生成し、脱アセチル化することにより、式(1)のシリビンラクトシドが得られる。
【化9】

式(1)
【0013】
シリビンに、ルイス酸を触媒として、パーアセチルマルトースを反応させてグリコシド結合を生成し、脱アセチル化することにより、式(2)のシリビンマルトシドが得られる。
【化10】

式(2)
【0014】
本発明に用いるシリビン配糖体は水溶性に優れ、シリビンラクトシド、シリビンマルトシドは水に約5%溶解することができる。従って、シリビンを配合することができなかった化粧水類にもシリビン配糖体であれば配合することができる。
【0015】
本発明の皮膚外用組成物には、本発明の効果を損なわない範囲内で、油剤、界面活性剤、防腐剤、多価アルコール、エタノール、糖類、金属イオン封鎖剤、水溶性高分子のような高分子、増粘剤、粉体成分、紫外線吸収剤、紫外線遮断剤、保湿剤、香料、pH調整剤等を含有させることができる。また、ビタミン類、皮膚賦活剤、血行促進剤、常在菌コントロール剤、活性酸素消去剤、抗炎症剤、美白剤、殺菌剤等の他の薬効成分、生理活性成分を含有させることもできる。
【0016】
本発明は、本発明に用いるシリビン配糖体は水溶性に優れており、シリビンラクトシド、シリビンマルトシドは水に約5%溶解することができる。従って、シリビンを配合することが困難であった化粧水類にもシリビン配糖体を配合することができる。
本発明のシリビン配糖体を有効成分とするシワ形成抑制剤としては、化粧水、乳液、クリーム、パック等のシワ改善用皮膚外用組成物、シワ改善用の医薬部外品、シワ改善用医薬が挙げられる。乳液であっても、水性部分にシリビン配糖体を高濃度で配合することができる。
【0017】
本発明のシリビン配糖体を有効成分とする表皮角化細胞分化抑制剤は、表皮角化細胞の分化を抑制し、増殖を維持し、ターンオーバーの遅延を予防、防止、改善し、加齢や紫外線照射により引き起こされる表皮の偏平化を防ぎ、老化した皮膚を再生する作用を有するので、老化防止用皮膚外用組成物として用いることができる。
本発明の、シリビン配糖体を有効成分とするI型コラーゲン産生促進剤は、皮膚のはりや弾力性を向上させ、しわやたるみを予防、防止、改善することが期待できるので、老化防止用皮膚外用組成物として用いることができる。
【0018】
〔シリビンラクトシドの合成〕
Helferichの方法に従ってシリビンラクトシドを合成した。
シリビン(3.0g、6.2mol)とオクタ-O-アセチル-D-ラクトース(6.3g、9.2mol)とを180 mlのジクロロメタン−アセトニトリル(1:1、v/v)の溶媒中で、三ふっ化ほう素ジメチルエーテル錯体(1.14ml、12.4mmol)を窒素存在下、室温で 19時間攪拌反応させた。反応終了後、氷冷しながら飽和炭酸水素ナトリウム水溶液を加え、150mlジクロロメタンで2回抽出処理し、無水硫酸ナトリウム処理後に抽出溶媒をエバポレーターにて除去した。
トリエチルアミン−メタノール−水(1:8:1)を35℃30時間反応させたのち、エバポレーターにより溶媒を除去した。BONDESIL-C18(Varian)を用いて精製を行い、シリビンラクトシド(1.0 g, 収率20%)を得た。得られたシリビンラクトシドをMSスペクトルで確認し、[M+H]+:807.5のピークを検出した。
【0019】
〔シリビンマルトシドの合成〕
Helferichの方法に従ってシリビンマルトシドを合成した。
シリビン(3.0g、6.2mol)とオクタ-O-アセチル-D-マルトース(6.3g、9.2mol)とを180mlのジクロロメタン−アセトニトリル(1:1、v/v)の溶媒中で、三ふっ化ほう素ジメチルエーテル錯体(1.14ml、12.4mmol)を窒素存在下、室温で 19時間攪拌反応させた。反応終了後、氷冷しながら飽和炭酸水素ナトリウム水溶液を加え、150mlジクロロメタンで2回抽出処理し、無水硫酸ナトリウム処理後に抽出溶媒をエバポレーターにて除去した。
トリエチルアミン−メタノール−水(1:8:1)を35℃30時間反応させたのち、エバポレーターにより溶媒を除去した。BONDESIL-C18(Varian)を用いて精製を行い、シリビンマルトシド(1.0g, 収率20%)を得た。得られたシリビンラクトシドをMSスペクトルで確認し、[M+H]+:807.5のピークを検出した。
【実施例1】
【0020】
水溶性試験
1.実験方法
シリビン、シリビンラクトシド、シリビンマルトシド(以下、シリビンをSB、シリビンラクトシドをSBL、シリビンマルトシドをSBMと記載することがある)を1.5mlチューブに適量はかりとり、そこに精製水を各濃度になるように加え、外観の透明性、また室温で遠心分離(15000rpm、5min)した際に沈殿として析出するかどうかを目視で判定した。またSBについては、非常に水溶性が悪いためビーカー内に少量はかりとり、水を加えてスターラーで約1時間かき混ぜ、混合操作を止めて1時間後に沈殿物が認められないものを溶解したと判定した。
【0021】
【表1】

【0022】
実験の結果、SBと比較してSBL、SBMの両者は劇的な水溶性の向上が認められ、約5000倍以上に水溶性が改善した。SBL、SBM間での溶解性の優劣は検出することはできなかった。SB濃度0.01mMは0.0005%(w/v)に相当する。SBL及びSBMの濃度50mM、60mMは、それぞれ4.1%(w/v)、4.9%(w/v)に相当する。従って、SBとSBL、SBMの溶解性を質量/容量%で比較すると、SBL、SBMの溶解性は、SBと比べて約10,000倍改善している。水溶性タイプの皮膚外用組成物などの剤では、SBでは、0.0005%(w/v)の濃度で含有させることも難しかったが、SBLでは、4.1%(w/v)の濃度で含有させることが可能であり、SBMでは、5.0%(w/v)の濃度で含有させることが可能である。尚、SBL、SBMの濃度0.01mMは0.0008%(w/v)に相当する。
【実施例2】
【0023】
表皮角化細胞分化抑制試験・増殖維持作用
1.実験材料
1.1 ヒト正常表皮角化細胞
ヒト正常表皮角化細胞NHEK(旭テクノグラス)を表皮角化細胞用培地:KGM(旭テクノグラス)で37℃-5%CO2インキュベーターにて培養した。本実験には経代数が3〜5代の細胞を利用した。
1.2 KGM(表皮角化細胞用培地)
KGMは表皮角化細胞基礎培地にヒト上皮細胞増殖因子(0.1ng/ml)、インシュリン(5.0μg/ml)、ハイドロコルチゾン(0.5μg/ml)、ゲンタマイシン(50μg/ml)、アンフォテリシンB(50μg/ml)、牛脳下垂体抽出液(2ml)を添加したものである。シリビン配糖体ははじめとするサンプルを細胞に添加する場合には、牛脳下垂体抽出液のみを除いた、KGM培地を用いて実験を行った。
1.3 添加サンプル
シリビン(SB)、シリビンマルトシド(SBM)、シリビンラクトシド(SBL)をDMSO(ジメチルスフフォキシド:和光純薬)に溶解し、各種濃度にて添加した。
【0024】
2.実験方法
2.1 表皮角化細胞分化抑制試験
NHEKをKGMで5×104/mlになるように懸濁し、4ml/ウエルで6穴プレートに播種し、24時間培養して、プレートに細胞を接着させた。各化合物を添加した牛脳下垂体抽出液を除いたKGMを4ml/ウエルで処理し、2日毎に培地交換しながら、8〜10日間培養した。毎日顕微鏡で形態観察を行い、DMSO処理したコントロール細胞が分化様の形態変化(扁平化)を示した時点で、写真撮影を行い、培養を終了した。
2.2 表皮角化細胞増殖維持試験
上記実験で得られた細胞をトリプシン処理によりプレートからはがした後に、KGM中で2.5×104/mlとなるように懸濁した。細胞懸濁液を2ml/ウエルで24穴プレートに播種し、2日ごとに培地交換しながら、8日間培養した。培養後、NHEKをトリプシン処理によりプレートからはがし、コールカウンター(ベックマン・コールター)により細胞数を測定した。
3.実験結果
3.1 表皮角化細胞分化抑制試験
得られた実験結果を図1に示す。この図は、細胞の顕微鏡写真である。
DMSOを処理した比較対照群であるControl並びにSB 3μM(シリビンを3μM添加した培地で培養)では、表皮角化細胞は扁平化し、分化様の形態変化を示した。それに対して、SBM3μM、SBL3μMでは分化様の形態は認められなかった。SB、SBL、SBMをそれぞれ10μM添加した培地で培養した場合には、全て、表皮角化細胞の分化が抑制された。SB、SBL、SBMは表皮角化細胞の分化抑制作用を有するが、SBM、SBLはSBに比べて表皮角化細胞分化抑制効果に優れている。
【0025】
3.2 表皮角化細胞増殖維持試験
上記の表皮角化細胞分化抑制試験において、分化が抑制されていれば細胞は増殖能を維持し、継代作業をすることで順次増殖するはずである。分化誘導された細胞は分化が付加逆的な反応であるため増殖することはできない。
そこで上記試験で得られた細胞を継代し、維持されている増殖能を増殖した細胞の数を測定することで調べた。
【0026】
その結果を図2に示す。試料濃度3μMでは、SBを添加したものについて細胞増殖能は殆ど維持されていないが、SBMは試料無添加と比べて1.8倍、SBLは試料無添加と比べて1.4倍に細胞数が増加し、細胞増殖能の維持効果が認められた。試料濃度10μMでは、SB、SBM、SBLともに細胞数が増加し、SBは試料無添加と比べて1.5倍、SBMは試料無添加と比べて2.1倍、SBLは試料無添加と比べて1.8倍に細胞数が増加し、細胞増殖能の維持効果が認められた。SBと比べて、SBM、SBLの細胞増殖能の維持効果が高いことがわかる。
【実施例3】
【0027】
I型コラーゲン産生促進作用
1.実験材料
1.1 ヒト皮膚繊維芽細胞
ヒト皮膚繊維芽細胞CCD1074SK(大日本住友製薬)をD-MEM中で37℃-5% CO2インキュベーターにて培養した。本実験には経代数が10〜15代の細胞を利用した。
1.2 D-MEM
D-MEMは、D-MEM基礎培地(GIBCO)に牛胎児血清(Hyclone)を10%になるよう添加して用いた。またサンプルを処理する際には、牛胎児血清を入れないD-MEMを用いて実験を行った。
2.実験方法
ヒト皮膚繊維芽細胞CCD1074SKを10%牛胎児血清を含むD-MEM培地で3×105/mlになるように懸濁し、10cmシャーレに1ml播種し、24時間培養し、プレートに細胞を接着させた。培地をDMSOに溶解させた各サンプルを各濃度で添加した牛胎児血清を入れないD-MEM培地に交換した。培地交換48時間後に細胞培養液を回収し、限外ろ過装置を用いて培養液を濃縮した。約500ml以下に濃縮後、タンパク質定量を行い、タンパク質量をそろえた後に、細胞培養液濃縮サンプルとしてウエスタンブロティングに使用した。
1レーン当り10μgのタンパク質をアプライし、SDS-PAGEで分離後、ニトロセルロース膜に転写した。転写後のニトロセルロース膜をブロッキング溶液(スキムミルクを5%の濃度になるように0.1%のポリオキシエチレン(20)ソルビタンモノラウレートを含むPBSで溶解した溶液)に浸し、4℃で一昼夜ブロッキングした。洗浄液{0.1%のポリオキシエチレン(20)ソルビタンモノラウレートを含むPBS}で洗浄後、一次抗体{洗浄液で500ng/mlに調製したI型コラーゲンに対するポリクローナル抗体(ロックランド)}に浸し、室温で1時間反応させた。洗浄後、二次抗体(洗浄液で250ng/mlに調製したホースラディッシュパーオキシダーゼ標識化抗ウサギイムノグロブリンG)に浸し、室温で1時間反応させた。洗浄後、ECLプラスウエスタンプロッティング検出試薬(アマシャムバイオサイエンス社)を用いて検出した。
【0028】
実験結果
実験の結果、SBと同様にSBL、SBMの両者にもI型コラーゲン産生促進作用が認められた。実験結果を図3に示す。
【0029】
得られたバンドの強度をプログラムソフトImage Jにより数値化した結果を表2に示し、DMSO処理時のI型コラーゲンの産生量を1とした際の比較産生量を図4として示す。
【0030】
【表2】

【0031】
SB、SBM、SBLともにI型コラーゲン産生促進作用を示した。SBと比べて、SBM、SBLはI型コラーゲン産生促進効果が強い。特に、試料濃度10μMでは、SBM、SBLの作用効果が大きく、高濃度での顕著な作用効果が認められる。
【実施例4】
【0032】
紫外線照射による水分蒸散抑制作用シワ形成抑制作用
1.実験材料・器具
実験動物ヘアレスマウスHos;HR1 ♀ 5週齢 (星野実験材料)
1.2 紫外線照射装置
紫外線A波(FL32SBL/DMR:(株)クリニカルサプライ製)
紫外線B波(FL32SE/DMR:(株)クリニカルサプライ製)
1.3 経皮水分蒸散量測定装置
Vapometer(キーサイエンス社製)
1.4 レプリカ採取器具およびレプリカ解析システム
(有)アサヒバイオメッド製の反射型レプリカ採取キット及びレプリカ解析システムASA‐03RXD
【0033】
2.実験方法
2.1 飼育環境
25℃±2℃、湿度50%±5%、食餌は飼料MR、水道水をそれぞれ自由摂取できるコンベンショナルな飼育環境で飼育した。
一群につき5匹を群分けし同一ケージにて飼育した。
日照は午前7時〜午後7時までの12時間ごとに昼夜を設定した。
2.2 紫外線照射
へアレスマウスHos;HR1を1週間馴化したのち紫外線照射を開始した。紫外線照射時は、ヘアレスマウスを専用のケージに移し、1群ずつUVB20mJ/cm2およびUVA10J/cm2の紫外線を照射した。照射は月、水および金の週3日サイクルで10週間実施し、合計30回紫外線を照射した。
【0034】
2.3 群設定
紫外線照射後30分以内にSB、SBL、SBMメタノール溶液又は溶媒(メタノール)をマウス背部皮膚全面に100μL処理した。SB、SBL、SBM塗布の濃度設定をそれぞれ1.0%、0.3%、0.1%の3点設定し、これら全群については紫外線照射を行った。溶媒であるメタノールのみを塗布するものについて、紫外線未照射及び紫外線照射の群を設けた。溶媒にメタノールを用いたのはSBを溶解するためである。メタノール中において、SBM、SBLは1%濃度においても完全に溶解していたが、SBは0.1%のみが完全に溶解しているが、0.3%は若干析出が認められ、1%においては不溶物が認められた。SBメタノール溶液に不溶物が認められた場合も、そのまま実験に用いた。
【0035】
2.4 経皮水分蒸散量の測定
経皮水分蒸散量の測定は、VapoMeter(キーストン サイエンティフィック社製)を用い、背部の尾付け根より首に向かい2cm、腰椎から右側に0.5cm部位を3回測定して平均を求めた。測定端末の開口部はNailモード(開口部を狭くすることで、マウス皮膚の狭い範囲に対応した)を用い、1回ごとの測定時間に約19秒を要した。測定日は、紫外線照射10週間後に行った。
【0036】
2.5 レプリカ画像解析
シワの形成を正確に把握するためレプリカを採取した。レプリカ画像解析は反射用レプリカ解析システムASA‐03RXD((有)アサヒバイオメッド製)を使用して行った。ASA‐03RXDを用いて、採取したレプリカに角度27度からの平行光(LED光源)を照射する事により得られるシワの形状に応じた陰影画像をCCDカメラで撮像し、コンピュータに取り込み画像処理することでレプリカ表面のしわ体積率(μm3/mm2/100)を計測した。
【0037】
2.6 統計解析
試験結果は平均値±標準偏差(S.D.)で表し、有意差検定は等分散性の検定をバートレット検定により行った。等分散性の仮定が棄却されなかった時はDunnettの多重検定を行い、等分散性の仮定が棄却された時は参考データとしてDunnettの多重検定を行った。
【0038】
3.試験結果
3.1 体重変動、外観観察
10週間照射終了後、各群間で体重変遷に目立った違いは無かった。重篤な病変を示したマウスもいなかった。
マウス皮膚の外観を観察した結果、群2の紫外線照射メタノール処理群ではシワ形成が認められるのにたいし、群4の0.3%シリビン塗布群、群6〜群8の全てのSBM塗布群、群9〜群11の全てのSBL塗布群においてシワ抑制作用が認められた。
【0039】
3.2 経皮水分蒸散量
肌荒れの指標として、紫外線照射10週間後にVapoMeterを用いて各群の水分蒸散量を測定した。結果を表3と図5に示す。
群1紫外線未照射群に比べて群2の紫外線照射群では経皮水分蒸散量が高くなる。群3〜群11のシリビン(SB)、シリビン配糖体(SBM、SBL)塗布群では、危険率1%以下で有意に経皮水分蒸散量の上昇が抑制されていた。
【0040】
1群(紫外線非照射、メタノール塗布)の水分蒸散量を0%、2群(紫外線照射、メタノール塗布)の水分蒸散量を100%としたとき、3〜5群(紫外線照射、SB0.1〜1%塗布)の水分蒸散量は26〜76%、6〜8群(紫外線照射、SBM0.1〜1%塗布)の水分量は11〜21%、9〜11群(紫外線照射、SBL0.1〜1%塗布)の水分量は24〜27%となり、SB、SBM、SBLを添加することにより水分蒸散量の上昇が抑制された。特に、シリビン配糖体であるSBM、SBLの水分蒸散量の上昇抑制効果が高い。つまり日焼けによる肌荒れを改善する効果がある。
【0041】
【表3】

【0042】
3.3 シワ体積率
10週間照射終了後、シワの形成を正確に把握するためレプリカを採取し、画像解析によりレプリカ表面のしわ体積率(μm3/mm2/100)を計測した。結果を表4、図6に示す。
【0043】
Dunnettの有意差検定を実施した結果、群2(紫外線照射メタノール塗布)に対して、群1(紫外線未照射メタノール塗布)、群4(紫外線照射 SB0.3%塗布)、群7(紫外線照射 SBM0.3%塗布)、群11(紫外線照射 SBL1.0%塗布)は、それぞれ危険率5%以下で有意にシワ体積が抑制された。
【0044】
【表4】

【0045】
〔処方例1 化粧水〕
質量%
1.シリビンラクトシド 0.3
2.ジグリセリン 5.0
3.1,3−ブチレングリコール 2.0
4.ジプロピレングリコール 3.0
5.水酸化カリウム 適量
6.クエン酸 適量
7.精製水 残余
(製法)
7に1〜6を溶解した。
【0046】
〔処方例2 乳液〕
質量%
1.シリビンマルトシド 0.3
2.水素添加大豆リン脂質 0.7
3.ステアリン酸デカグリセリル(HLB12) 2.0
4.グリセリン 8.0
5.オリーブ油 8.0
6.ベヘニルアルコール 1.0
7.ジプロピレングリコール 8.0
8.カルボキシビニルポリマー 0.1
9.キサンタンガム 0.2
10.水酸化カリウム 適量
11.クエン酸 適量
12.精製水 残余
(製法)
1〜4及び7〜12を80℃で加温溶解する。これに、約80℃に加温した5、6を加え、ホモミキサーで攪拌混合し、30℃まで冷却し、乳液を得た。
【0047】
〔処方例3 モイスチャー美容液〕
質量%
1.シリビンラクトシド 0.2
2.水素添加大豆リン脂質 0.6
3.モノオレイン酸デカグリセリル(HLB12) 1.5
4.グリセリン 7.0
5.1,3−ブチレングリコール 5.0
6.ポリエチレングリコール4000 0.1
7.スクワラン 5.0
8.シリコーン 0.5
9.ラウロイルグルタミン酸ジ(フィトステリル/オクチルドデシル)
0.2
10.キサンタンガム 0.3
11.水酸化カリウム 適量
12.クエン酸 適量
13.精製水 残余
(製法)
1及び11〜13を攪拌溶解し、4〜6、10を添加後約80℃に加温溶解する。
これに、約80℃に加温した2、3、7〜9を加え、30℃まで冷却し、モイスチャー美容液を得た。
【0048】
〔処方例4 エモリエントクリーム〕
質量%
1.シリビンマルトシド 0.5
2.ジグリセリン 10.0
3.ジプロピレングリコール 8.0
4.1,2−ペンタンジオール 0.5
5.L−セリン 0.01
6.ジステアリン酸デカグリセリル(HLB9.5) 0.5
7.モノミリスチン酸デカグリセリル(HLB14) 1.5
8.オリーブ油 10.0
9.マカデミアナッツ油 1.0
10.ベヘニルアルコール 1.5
11.シリコーン 2.0
12.ホホバ油 3.0
13.トコフェロール 0.001
14.SIMULGEL NS(SEPPIC社製) 2.0
15.キサンタンガム 0.1
16.水酸化カリウム 適量
17.クエン酸 適量
18.精製水 残余
(製法)
1及び16〜18を攪拌溶解し、2〜5を添加後約80℃に加温溶解する。これに、約80℃に加温した6〜14を加え、30℃まで冷却し、エモリエントクリームを得た。
【0049】
〔処方例5 ボディ用乳液〕
質量%
1.シリビンラクトシド 0.2
2.PEG-60水添ヒマシ油(HLB14) 1.5
3.グリセリン 9.0
4.ジプロピレングリコール 7.0
5.ヒアルロン酸Na 0.001
6.流動パラフィン 10.0
7.シリコーン 3.0
8.オクチルドデカノール 4.0
9.(アクリル酸/アクリル酸アルキル(C10-30))コポリマー 0.2
10.水酸化カリウム 適量
11.クエン酸 適量
12.精製水 残余
13. エタノール 2.5
(製法)
1及び10〜12を攪拌溶解し、2〜5、9を添加後約80℃に加温溶解する。これに、約80℃に加温した6〜8を加え、30℃まで冷却、13を添加し、ボディ用乳液を得た。
【0050】
〔処方例6 マッサージクリーム〕
質量%
1.シリビンマルトシド 0.05
2.グリセリン 10.0
3.ジグリセリン 2.0
4.プロピレングリコール 7.0
5.モノステアリン酸デカグリセリル(HLB12) 1.0
6.エチルヘキサン酸セチル 12.0
7.ベヘニルアルコール 2.0
8.ステアリン酸 0.5
9.セピノブ EMT10(SEPPIC社製) 0.5
10.香料 適量
11.フェノキシエタノール 0.3
12.水酸化カリウム 適量
13.クエン酸 適量
14.精製水 残余
(製法)
1及び11〜14を攪拌溶解し、2〜4を添加後約80℃に加温溶解する。これに、約80℃に加温した5〜9を加え、30℃まで冷却、10を添加し、マッサージクリームを得た。
【0051】
〔処方例7 乳化型ファンデーション〕
質量%
1.シリビンラクトシド 0.1
2.グリセリン 10.0
3.ジプロピレングリコール 8.0
4.1,2−ペンタンジオール 1.0
5.キサンタンガム 0.3
6.トリイソステアリン酸ポリグリセリル-2 1.0
7.シクロメチコン 8.0
8.シリコーン 5.0
9.ネオペンタン酸イソステアリル 5.0
10.イソステアリン酸 1.5
11.ベヘニルアルコール 0.5
12.パルミチン酸デキストリン 1.0
13.タルク 3.0
14.二酸化チタン 5.0
15.ベンガラ 0.5
16.黄酸化鉄 1.4
17.黒酸化鉄 0.1
18.水酸化カリウム 適量
19.クエン酸 適量
20.精製水 残余
(製法)
1及び18〜20を攪拌溶解し、2〜5を添加後約70℃に加温溶解する。次に、よく粉砕した13〜17を添加し、攪拌混合する。これに、約80℃に加温した6〜12を加え、30℃まで冷却し、乳化型ファンデーションを得た。
【特許請求の範囲】
【請求項1】
シリビン配糖体を含有する皮膚外用組成物。
【請求項2】
シリビン配糖体が式(1)のシリビンラクトシドまたは式(2)のシリビンマルトシドであることを特徴とする請求項1記載の皮膚外用組成物。
【化1】

式(1)
【化2】

式(2)
【請求項3】
シリビン配糖体を有効成分とするシワ形成抑制剤。
【請求項4】
シリビン配糖体を有効成分とする表皮角化細胞分化抑制剤。
【請求項5】
シリビン配糖体を有効成分とするI型コラーゲン産生促進剤。
【請求項6】
シリビン配糖体を有効成分とする日焼けによる肌荒れ改善剤。
【請求項7】
シリビン配糖体が式(1)のシリビンラクトシドまたは式(2)のシリビンマルトシドであることを特徴とする請求項3〜6の何れかに記載の剤。
【化3】

式(1)
【化4】

式(2)
【請求項8】
水を溶媒として、シリビン配糖体を0.0008〜5.0重量%含有することを特徴とする請求項2記載の皮膚外用組成物又は請求項7記載の剤。
【請求項1】
シリビン配糖体を含有する皮膚外用組成物。
【請求項2】
シリビン配糖体が式(1)のシリビンラクトシドまたは式(2)のシリビンマルトシドであることを特徴とする請求項1記載の皮膚外用組成物。
【化1】

式(1)
【化2】

式(2)
【請求項3】
シリビン配糖体を有効成分とするシワ形成抑制剤。
【請求項4】
シリビン配糖体を有効成分とする表皮角化細胞分化抑制剤。
【請求項5】
シリビン配糖体を有効成分とするI型コラーゲン産生促進剤。
【請求項6】
シリビン配糖体を有効成分とする日焼けによる肌荒れ改善剤。
【請求項7】
シリビン配糖体が式(1)のシリビンラクトシドまたは式(2)のシリビンマルトシドであることを特徴とする請求項3〜6の何れかに記載の剤。
【化3】

式(1)
【化4】

式(2)
【請求項8】
水を溶媒として、シリビン配糖体を0.0008〜5.0重量%含有することを特徴とする請求項2記載の皮膚外用組成物又は請求項7記載の剤。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】




【図2】


【図3】


【図4】


【図5】


【図6】


【公開番号】特開2013−40218(P2013−40218A)
【公開日】平成25年2月28日(2013.2.28)
【国際特許分類】
【出願番号】特願2012−262654(P2012−262654)
【出願日】平成24年11月30日(2012.11.30)
【分割の表示】特願2008−14361(P2008−14361)の分割
【原出願日】平成20年1月25日(2008.1.25)
【出願人】(593106918)株式会社ファンケル (310)
【出願人】(505380692)株式会社サイトパスファインダー (11)
【Fターム(参考)】
【公開日】平成25年2月28日(2013.2.28)
【国際特許分類】
【出願日】平成24年11月30日(2012.11.30)
【分割の表示】特願2008−14361(P2008−14361)の分割
【原出願日】平成20年1月25日(2008.1.25)
【出願人】(593106918)株式会社ファンケル (310)
【出願人】(505380692)株式会社サイトパスファインダー (11)
【Fターム(参考)】
[ Back to top ]

