セルロースナノ繊維の製造方法
【課題】酵素反応効率に優れると共に、アスペクト比及び結晶化度を容易に調節することができるセルロースナノ繊維の製造方法を提供すること。
【解決手段】本発明は、バイオマスを粉砕し、セルロースミクロフィブリルとする脆弱化工程S1と、該セルロースミクロフィブリルを耐熱性セルラーゼで加熱分解する加熱分解工程S2と、を備え、加熱分解工程S2における加熱温度が50℃よりも大きく、且つ加熱温度、加熱時間又は酵素濃度を調節することによってアスペクト比及び結晶化度の調節が可能となっているセルロースナノ繊維の製造方法である。
【解決手段】本発明は、バイオマスを粉砕し、セルロースミクロフィブリルとする脆弱化工程S1と、該セルロースミクロフィブリルを耐熱性セルラーゼで加熱分解する加熱分解工程S2と、を備え、加熱分解工程S2における加熱温度が50℃よりも大きく、且つ加熱温度、加熱時間又は酵素濃度を調節することによってアスペクト比及び結晶化度の調節が可能となっているセルロースナノ繊維の製造方法である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、セルロースナノ繊維の製造方法に関し、更に詳しくは、酵素反応効率に優れると共に、アスペクト比及び結晶化度を容易に調節することができるセルロースナノ繊維の製造方法に関する。
【背景技術】
【0002】
一般に、木質バイオマス資源から取り出されるセルロースナノ繊維は、セルロース分子が数十本集まってできる最少単位の集合体であるセルロースエレメンタリフィブリル、その集合体である直径15〜30nmのセルロースミクロフィブリル、及び、セルロースの硫酸加水分解等で得られる高結晶性セルロースナノクリスタルの3種類に大別できる。
これらのセルロースナノ繊維は、近年、高機能高分子複合材料の強化材、透明材料、メンブレインフィルター等の様々な分野で注目を浴びている。
【0003】
セルロースナノ繊維の製造方法としては、酵素作用促進処理と物理的破壊処理とを複合することによって、セルロースミクロフィブリルの凝集体又はセルロースミクロフィブリルそのものの非晶部分にエンドグルカナーゼを作用させ、セルロースナノ繊維を得る方法が知られている(例えば、特許文献1参照)。
【0004】
ところで、近年、セルロースナノ繊維の応用分野が拡大するに従って、様々なアスペクト比及び結晶化度を有するセルロースナノ繊維が求められている。なお、本明細書において、アスペクト比とは、「セルロースナノ繊維の断面の直径/セルロースナノ繊維の長さ」を意味する。
【0005】
例えば、繊維強化プラスチック(FRP)の製造において、繊維のマット(不織布)を作り熱硬化性樹脂を含沈させ、熱圧硬化させる方法では、アスペクト比が大きいセルロースナノ繊維を用いることで、繊維同士の物理的相互作用(例えば水素結合)を強くなり、物性を向上させることができる。
ところが、熱可塑性高分子にセルロースナノ繊維を複合する方法、特に、エクストルーダーやニーダーを用いる混練の際には、アスペクト比が大きいセルロースナノ繊維は、絡み合いや混練中の凝集が起こり、分散性が低下するので、アスペクト比が調節されたセルロースナノ繊維が求められている。
【0006】
ちなみに、木質バイオマスからなるセルロースナノクリスタルは、高い結晶性を示し、強い強度特性を示す利点があり、一般に、直径が4〜6nmで、長さが100〜300nmであるので、アスペクト比が非常に小さくなる。
ところが、セルロースナノクリスタルを製造する際には、強い酸触媒を必要とし、また用いた強酸の回収や除去に非常にコストがかかるという欠点もある。なお、酸触媒を使わないで酵素を使った方法は、環境に易しい方法といえる。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2008−150719号公報
【発明の概要】
【発明が解決しようとする課題】
【0008】
しかしながら、上記特許文献1記載のセルロースナノ繊維の製造方法を含む従来のセルロースナノ繊維の製造方法においては、アスペクト比及び結晶化度を調節することが困難である。
セルロースナノ繊維のアスペクト比及び結晶化度の調節は非常に重要な研究課題であり、そのアスペクト比及び結晶化度を調節されたセルロースナノ繊維の開発が要求されている。
【0009】
また、セルロース系バイオマスの分解反応は、主に糸状菌由来の常温性セルラーゼ群(最適反応温度50℃位)を用いた酵素が一般的であるが、産業的に使用している反応機の場合は、長時間の分解反応中の雑菌汚染及び酵素の大量消費等の問題があり、高効率分解反応が実現されていない。
【0010】
本発明は、上記事情に鑑みてなされたものであり、酵素反応効率に優れると共に、アスペクト比及び結晶化度を容易に調節することができるセルロースナノ繊維の製造方法を提供することを目的とする。
【課題を解決するための手段】
【0011】
本発明者等は、上記課題を解決するため鋭意検討したところ、通常行われる酵素反応は40〜50℃であるが、50℃よりも高温で酵素反応を行うことを考えた。そして、耐熱性セルラーゼを選定し、その耐熱性セルラーゼを用いて、セルロースミクロフィブリルを、高温で加熱分解し、さらに、その時の加熱温度、加熱時間及び酵素濃度を調節することによって、上記課題を解決できることを見出し、本発明を完成させるに至った。
【0012】
本発明は、(1)バイオマスを粉砕し、セルロースミクロフィブリルとする脆弱化工程と、該セルロースミクロフィブリルを耐熱性セルラーゼで加熱分解する加熱分解工程と、を備え、加熱分解工程における加熱温度が50℃よりも大きく、且つ加熱温度、加熱時間又は酵素濃度を調節することによってアスペクト比及び結晶化度の調節が可能となっているセルロースナノ繊維の製造方法に存する。
【0013】
本発明は、(2)加熱分解工程における加熱温度が80℃以上である上記(1)記載のセルロースナノ繊維の製造方法に存する。
【0014】
本発明は、(3)耐熱性セルラーゼが、80℃以上で熱処理した後、精製した耐熱性エンドグルカナーゼと、80℃以上で熱処理した後、精製した耐熱性ベターグルコシダーゼとからなるものである上記(1)又は(2)に記載のセルロースナノ繊維の製造方法に存する。
【0015】
本発明は、(4)耐熱性エンドグルカナーゼが、セルロースミクロフィブリルの非晶部分を選択的に分解する上記(3)記載のセルロースナノ繊維の製造方法に存する。
【0016】
本発明は、(5)耐熱性エンドグルカナーゼと、耐熱性ベターグルコシダーゼとの配合割合が、20:0.1〜1である上記(3)又は(4)に記載のセルロースナノ繊維の製造方法に存する。
【0017】
本発明は、(6)脆弱化工程が、バイオマスをミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である上記(1)〜(5)のいずれか1つに記載のセルロースナノ繊維の製造方法に存する。
【0018】
本発明は、(7)脆弱化工程が、バイオマスを酸化剤及び水熱処理により脆弱化した後、ミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である上記(1)〜(5)のいずれか1つに記載のセルロースナノ繊維の製造方法に存する。
【発明の効果】
【0019】
本発明のセルロースナノ繊維の製造方法によれば、バイオマスを、所定のアスペクト比及び結晶化度を有するセルロースナノ繊維とすることができる。すなわち、上記セルロースナノ繊維の製造方法においては、セルロースミクロフィブリルを、耐熱性セルラーゼで、50℃よりも高温で加熱分解する加熱分解工程を経ることにより、酵素反応効率を向上させることができる。
【0020】
また、加熱分解工程において、加熱温度、加熱時間及び酵素濃度を調節することによって、高い精度でアスペクト比及び結晶化度を調節することができる。ちなみに、機械的な粉砕では、セルロースナノ繊維の長さをミクロンレベルで調節することが限界であるが、本発明においては、セルロースナノ繊維の長さをナノレベルで調節することが可能となる。特に、加熱温度は、80℃以上とすることが好ましい。
【0021】
上記セルロースナノ繊維の製造方法においては、耐熱性セルラーゼが、80℃以上で熱処理した後、精製した耐熱性エンドグルカナーゼと、80℃以上で熱処理した後、精製した耐熱性ベターグルコシダーゼとからなるものである場合、耐熱性エンドグルカナーゼがセルロースミクロフィブリルの非晶部分を選択的に分解し、耐熱性ベターグルコシダーゼが耐熱性エンドグルカナーゼの活性を阻害する副生成物のセロビオースを分解するので、酵素反応効率が極めて向上する。
【0022】
上記セルロースナノ繊維の製造方法においては、耐熱性エンドグルカナーゼと、耐熱性ベターグルコシダーゼとの配合割合が、20:0.1〜1である場合、耐熱性ベターグルコシダーゼによる分解と、耐熱性エンドグルカナーゼによる分解とがバランス良く行われる。
【0023】
上記セルロースナノ繊維の製造方法においては、脆弱化工程が、バイオマスをミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である場合、又は、バイオマスを酸化剤及び水熱処理により脆弱化し、ミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である場合、天然のバイオマスから比較的簡単な工程でセルロースナノ繊維を製造することが可能となる。
【図面の簡単な説明】
【0024】
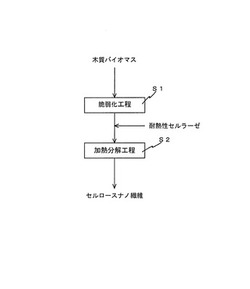
【図1】図1は、本実施形態に係るセルロースナノ繊維の製造方法における各工程を示すフローチャートである。
【図2】図2は、実施例1で得られたセルロースミクロフィブリルAの原子間力顕微鏡像の写真である。
【図3】図3は、実施例2で得られたセルロースミクロフィブリルBの原子間力顕微鏡像の写真である。
【図4】図4は、実施例3で得られたセルロースナノ繊維Cの原子間力顕微鏡像の写真である。
【図5】図5は、ブランクとして0時間経過のサンプルと、実施例の評価1で得られた1.0,2.7,17.5時間経過後のサンプル(セルロースナノ繊維)の原子間力顕微鏡像の写真である。
【発明を実施するための形態】
【0025】
以下、必要に応じて図面を参照しつつ、本発明の好適な実施形態について詳細に説明する。
図1は、本実施形態に係るセルロースナノ繊維の製造方法における各工程を示すフローチャートである。
図1に示すように、本実施形態に係るセルロースナノ繊維の製造方法は、バイオマスを粉砕し、セルロースミクロフィブリルとする脆弱化工程S1と、該セルロースミクロフィブリルを耐熱性セルラーゼで加熱分解する加熱分解工程S2と、を備える。
【0026】
本実施形態に係るセルロースナノ繊維の製造方法によれば、バイオマスから所定のアスペクト比及び結晶化度を有するセルロースナノ繊維を効率良く製造することができる。
以下、各工程について更に詳細に説明する。
【0027】
(脆弱化工程)
脆弱化工程S1は、バイオマスを機械的に粉砕する工程である。脆弱化工程S1により、バイオマスは、セルロースミクロフィブリルとなる。
【0028】
上記バイオマスは、セルロース、ヘミセルロース及びリグニンを含む天然物であり、セルロースがリグニン及びヘミセルロースに強固に結びついた三次元ネットワーク階層構造を有している。
かかるバイオマスとしては、一般に、木材、草木、農産物、綿花等の植物から得られる木質バイオマスや生物が産生するバクテリアセルロース等が挙げられる。
【0029】
バイオマスの大きさは、5cm角以下であることが好ましい。この場合、脆弱化工程S1において、粉砕しやすくなる。なお、バイオマスが5cmを超える場合は、予備的に機械粉砕する予備脆弱化工程を施すことが好ましい。
【0030】
脆弱化工程S1における粉砕の方法は、特に限定されず、媒体(以下便宜的に「粉砕用媒体」という。)を共存させてせん断力をバイオマスに印可できる方法が好ましい。
例えば、ボールミル(振動ボールミル、回転ボールミル、遊星型ボールミル)、ロッドミル、ビーズミル、ディスクミル、カッターミル、ハンマーミル、インペラーミル、エクストルーダー、ミキサー(高速回転羽根型ミキサー、ホモミキサー)、ホモジナイザー(高圧ホモジナイザー、機械式ホモジナイザー、超音波ホモジナイザー)等が挙げられる。
【0031】
これらの中でも、粉砕は、ボールミル、ロッドミル、ビーズミル、ディスクミル又はカッターミル等のミルにより施されることが好ましく、ボールミル又はディスクミルにより施されることが更に好ましい。特に、ボールミルを用いる場合、結晶性を低下させることができるので、得られるセルロースナノ繊維の結晶性が低くなり(非晶性が高くなり)、その結果、酵素分解効率が向上するという利点がある。
【0032】
脆弱化工程S1において用いられる粉砕用媒体としては、特に限定されないが、水、低分子化合物、高分子化合物又は脂肪酸類等が好適に用いられる。これらは1種類を単独で用いてもよく、2種類以上を混合して用いてもよい。
これらの中でも、粉砕用媒体は、水と、低分子化合物、高分子化合物又は脂肪酸類とを混合して用いることが好ましい。
【0033】
低分子化合物としては、アルコール類、エーテル類、ケトン類、スルホキシド類、アミド類、アミン類、芳香族類、モルフォリン類、イオン性液体等が挙げられ、高分子化合物としては、アルコール系高分子類、エーテル系高分子類、アミド系高分子類、アミン系高分子類、芳香族系高分子類等が挙げられ、脂肪酸類としては、飽和脂肪酸類、不飽和脂肪酸類等が挙げられる。なお、このとき上記低分子化合物、高分子化合物及び脂肪酸類は水溶性であることが好ましい。
【0034】
本実施形態に係るセルロースナノ繊維の製造方法においては、脆弱化工程S1を経ることにより後述する加熱分解工程S2において、天然のバイオマスから比較的簡単な工程でアスペクト比及び結晶化度を調節したセルロースナノ繊維を製造することが可能となる。
【0035】
(加熱分解工程)
加熱分解工程S2は、脆弱化工程S1で得られたセルロースミクロフィブリルを耐熱性セルラーゼで加熱分解する工程である。
【0036】
ここで、耐熱性セルラーゼは、耐熱性を有し、50℃よりも高温の反応条件で反応活性を示すセルラーゼであり、一般的なセルラーゼとは異なる性質を有する。
具体的には、耐熱性セルラーゼは、耐熱性エンドグルカナーゼ及び耐熱性ベターグルコシダーゼからなる。これらの酵素は、耐熱性であるので、50℃よりも高温で反応させることができる。これにより、酵素反応効率が向上する。
【0037】
上記耐熱性エンドグルカナーゼ(EGPh)は、エンドグルカナーゼを発現させた後、80℃以上で熱処理し、硫安分画、遠心分離、カラムクロマトグラフィー等で精製することにより得られる。
上記耐熱性ベターグルコシダーゼ(BGL)は、ベターグルコシダーゼを発現させた後、80℃以上で熱処理し、硫安分画、遠心分離、およびカラムクロマトグラフィー等で精製することにより得られる。
【0038】
耐熱性エンドグルカナーゼは、セルロースの非結晶の領域に活性があり、結晶の領域には活性が無いことが特徴である。すなわち、耐熱性エンドグルカナーゼは、セルロースミクロフィブリルの非晶部分を選択的に分解することができる。これにより、結晶性の高いセルロースナノ繊維を得ることが可能となる。
また、耐熱性エンドグルカナーゼは、耐熱性アーキアPyrococcus horikoshii 由来であり、セルロースをセロビオースに分解する。なお、エンドグルカナーゼの副生成物であるセロビオースは、耐熱性エンドグルカナーゼによる酵素反応を阻害する作用がある。
【0039】
耐熱性ベターグルコシダーゼは、2−7糖のセロオリゴ糖を基質として、グルコースを遊離するが、結晶性セルロースは反応しないことが特徴である。これにより、結晶性の高いセルロースナノ繊維を得ることが可能となる。
また、耐熱性ベターグルコシダーゼは、耐熱性アーキアPyrococcus furiosus由来であり、上記セロビオースを分解する。
したがって、セルロースナノ繊維の製造方法においては、耐熱性エンドグルカナーゼがセルロースミクロフィブリルの非晶部分を選択的に分解し、耐熱性ベターグルコシダーゼが耐熱性エンドグルカナーゼの活性を阻害する副生成物のセロビオースを分解するので、酵素反応効率が極めて向上することになる。
【0040】
耐熱性エンドグルカナーゼと、耐熱性ベターグルコシダーゼとの配合割合は、20:0.1〜1であることが好ましい。耐熱性エンドグルカナーゼ20質量部に対し、耐熱性ベターグルコシダーゼが0.1質量部未満であると、配合割合が上記範囲内にある場合と比較して、セロビオースを十分に分解できず、耐熱性エンドグルカナーゼの酵素反応効率が悪くなる場合があり、耐熱性エンドグルカナーゼ20質量部に対し、耐熱性ベターグルコシダーゼが1質量部を超えると、耐熱性エンドグルカナーゼの酵素反応効率は略一定となり、向上しなくなる。
【0041】
加熱分解工程S2における加熱温度は、50℃よりも大きく、80℃以上であることが好ましく、80〜105℃であることがより好ましい。加熱温度を80℃以上とすることにより、より耐熱性に優れるセルロースナノ繊維が得られる。
また、加熱温度が80〜105℃である場合、加熱時間は、0.1〜72時間であることが好ましい。
さらに、これらの場合の耐熱性エンドグルカナーゼの酵素濃度は、基質1Mに対して、0.01〜10mMであることが好ましい。
【0042】
また、セルロースナノ繊維の製造方法においては、加熱温度、加熱時間及び酵素濃度を調節することによってアスペクト比及び結晶化度の調節が可能となる。
例えば、加熱分解工程S2における加熱温度は、上述した加熱温度の範囲において、加熱温度を低くすることにより、セルロースナノ繊維の長さを大きくすることができ、加熱温度を高くすることにより、セルロースナノ繊維の長さを小さくすることができる。
加熱分解工程S2における加熱時間は、上述した加熱時間の範囲において、加熱時間を短くすることにより、セルロースナノ繊維の長さを大きくすることができ、加熱時間を長くすることにより、セルロースナノ繊維の長さを小さくすることができる。
加熱分解工程S2における耐熱性エンドグルカナーゼの酵素濃度は、上述した酵素濃度の範囲において、酵素濃度を低くすることにより、セルロースナノ繊維の長さを大きくすることができ、酵素濃度を高くすることにより、セルロースナノ繊維の長さを小さくすることができる。
【0043】
本実施形態に係るセルロースナノ繊維の製造方法においては、加熱分解工程S2を経ることにより、酵素反応効率を向上させることができる。
また、加熱温度、加熱時間及び酵素濃度を調節することによって、セルロースナノ繊維の長さをナノレベルで変えることができるので、高い精度でアスペクト比を調節することができる。
【0044】
得られるセルロースナノ繊維は、天然物であり、高分子からなる強化材、透明材料、メンブレインフィルター、コーティング剤等に利用できる。
また、これらの用途に用いられる場合、セルロースナノ繊維のアスペクト比は4〜1000であることが好ましく、結晶化度は5〜90%であることが好ましい。
【0045】
得られるセルロースナノ繊維は、無味、無臭、無毒性であり、且つ微細繊維状で舌触りに異物感を感じないので、食品に添加して用いることもできる。この場合、保水性、保油性、テクスチャー、形態安定性、又はダイエット性を付与することができる。
【0046】
以上、本発明の好適な実施形態について説明したが、本発明は上記実施形態に限定されるものではない。
【0047】
例えば、本実施形態に係るセルロースナノ繊維の製造方法においては、脆弱化工程S1が、バイオマスを機械的に粉砕する工程となっているが、予め、バイオマスを酸処理、アルカリ処理、水熱処理又は酸化剤処理等により脆弱化処理してもよい。すなわち、脆弱化工程は、バイオマスをこれらの処理により脆弱化した後、ミルにより機械的に粉砕して、セルロースミクロフィブリルとしてもよい。
【0048】
この場合、アルカリ触媒又は酸触媒存在下、バイオマスに酸化剤を加え、加熱撹拌することにより脆弱化され、バイオマスからリグニンが除去されたホロセルロースが得られる。該ホロセルロースが機械的に粉砕することにより、ホロセルロースミクロフィブリルが得られることになる。
アルカリ触媒としては、苛性ソーダー、炭酸ナトリウム等が好適に用いられる。
酸触媒としては、硫酸、各種有機酸等が好適に用いられる。
酸化剤としては、亜塩素酸ナトリウム、TEMPO酸化剤、オゾン等が好適に用いられる。
【0049】
本実施形態に係るセルロースナノ繊維の製造方法においては、加熱分解工程S2において、耐熱性エンドグルカナーゼ及び耐熱性ベターグルコシダーゼを用いているが、必要に応じて、セロビオヒドロラーゼを混合して用いてもよい。ちなみに、セロビオヒドロラーゼの場合は特に結晶性セルロースに高い活性を示す。
【実施例】
【0050】
以下、実施例及び比較例に基づいて本発明をより具体的に説明するが、本発明は以下の実施例に限定されるものではない。
【0051】
(耐熱性エンドグルカナーゼの製造)
エンドグルカナーゼの発現は、発現プラスミドベクターpET11と発現用大腸菌BL21(DE3)を用いた。そして、発現したエンドグルカナーゼを85℃で熱処理し、Hitrap Phenyl columnを用いて精製することにより、耐熱性エンドグルカナーゼ(酵素番号:EC 3.2.1.4、ファミリー5に属する)を得た。
【0052】
(耐熱性ベターグルコシダーゼの製造)
ベターグルコシダーゼの発現は、発現プラスミドベクターpET11と発現用大腸菌BL21(DE3)を用いた。そして、発現したベターグルコシダーゼを85℃で熱処理し、Hitrap Phenyl columnを用いて精製することにより、耐熱性ベターグルコシダーゼ(酵素番号:EC 3.2.1.21)を得た。
【0053】
(実施例1)
(セルロースミクロフィブリルAの製造)
木質バイオマスとして、5cm角のユーカリクラフトパルプを用いた。なお、広葉樹であるユーカリのクラフトパルプの成分分析をした結果、セルロース成分は0.2%、ヘミセルロースは22.3%、リグニンは10.3%であった。
ユーカリクラフトパルプを、ディスクミルを用いて機械的に粉砕した(脆弱化工程)。具体的には、ユーカリのクラフトパルプに水を加え、固形分濃度1%となるように水懸濁液とし、これに対してディスクミルを用いた機械的粉砕を10回行い、セルロースミクロフィブリルAとした。
【0054】
セルロースミクロフィブリルAの原子間力顕微鏡像を図2に示す。なお、原子間力顕微鏡観察においては、得られたセルロースミクロフィブリルAに固形分濃度0.05%となるように水を加え、これを、カチオン性ポリマーであるポリエチレンイミン(0.01
%水溶液)がコートされたゴルド表面にスピンコート(3000 rpm、1分)して薄膜を作り観察した。
セルロースミクロフィブリルAは、直径が5〜30nmであり、長さが1μm以上であったので、非常にアスペクト比が大きいことがわかった。
【0055】
(セルロースナノ繊維Aの製造)
セルロースミクロフィブリルAを、耐熱性セルラーゼで加熱分解した。具体的には、セルロースミクロフィブリルAに固形分濃度0.2%となるように水を加え、これに、0.1Mの酢酸緩衝液(pH5.5)を2mL加えた。そして、10μMの耐熱性エンドグルカナーゼと、0.2μMのベターグルコシダーゼとをそれぞれ0.2mL加え、加熱温度を85℃として攪拌することにより(加熱分解工程)、セルロースミクロフィブリルAを加熱分解したセルロースナノ繊維Aを得た。なお、0.5,1.0,2.7,17.5時間経過後にそれぞれサンプリングした。
【0056】
(実施例2)
(セルロースミクロフィブリルBの製造)
木質バイオマスとして、針葉樹であるヒノキ木粉(0.2mm)を用いた。
まず、ヒノキ木粉を、亜塩素酸アトリウムにより脱リグニン(脆弱化)した。具体的には、ヒノキ木粉25gに、蒸留水750ml、亜塩素酸ナトリウム(酸化剤)7.5g及び酢酸(酸触媒)1.5mlを加えて、80〜90℃の湯浴中で攪拌しながら1時間加温した。その後、さらに、亜塩素酸ナトリウム7.5g、酢酸1.5mlを加えて反応を行い、この操作を5回繰り返した後、蒸留水3Lで洗浄し、ホロセルロースを得た。
そして、得られたホロセルロースを、ディスクミルを用いて機械的に粉砕した(脆弱化工程)。具体的には、ヒノキ木粉に水を加え、固形分濃度1%となるように水懸濁液とし、これに対してディスクミルを用いた機械的粉砕を2回行い、セルロースミクロフィブリルBとした。
【0057】
セルロースミクロフィブリルBの原子間力顕微鏡像を図3に示す。なお、原子間力顕微鏡観察においては、得られたセルロースミクロフィブリルBに固形分濃度0.05%となるように水を加え、これを、カチオン性ポリマーであるポリエチレンイミン(0.01
%水溶液)がコートされたゴルド表面にスピンコート(3000 rpm、1分)して薄膜を作り観察した。
セルロースミクロフィブリルBは、セルロースミクロフィブリルAと同様に、非常にアスペクト比が大きいことがわかった。
【0058】
(セルロースナノ繊維Bの製造)
セルロースミクロフィブリルBを、耐熱性セルラーゼで加熱分解した。具体的には、セルロースミクロフィブリルBに固形分濃度0.2%となるように水を加え、これに、0.1Mの酢酸緩衝液(pH5.5)を2mL加えた。そして、10μMの耐熱性エンドグルカナーゼと、0.2μMのベターグルコシダーゼとをそれぞれ0.2mL加え、加熱温度を85℃として攪拌することにより(加熱分解工程)、セルロースミクロフィブリルBを加熱分解したセルロースナノ繊維Bを得た。なお、0.5,1.0,2.7,17.5時間経過後にそれぞれサンプリングした。
【0059】
(実施例3)
(セルロースミクロフィブリルCの製造)
木質バイオマスとして、サトウキビ残渣(バガス)1gを用いた。
まず、サトウキビ残渣を、遊星ボールミルを用いて機械的に粉砕した(脆弱化工程)。具体的には、サトウキビ残渣に水を加え、400rpmで2時間処理し、セルロースミクロフィブリルCとした。
【0060】
(セルロースナノ繊維Cの製造)
セルロースミクロフィブリルCを、耐熱性セルラーゼで加熱分解した。具体的には、セルロースミクロフィブリルC350mgに水を加え、これに、50mMのクエン酸緩衝液(citrate buffer、pH5.0)を加え、基質濃度を1%とした。そして、耐熱性エンドグルカナーゼ(345
UI/g of bagasse)を加え、加熱温度を85℃として72時間攪拌することにより(加熱分解工程)、セルロースミクロフィブリルCを加熱分解したセルロースナノ繊維Cを得た。なお、このときのグルコース生成量は33.42%であった。
セルロースナノ繊維Cの原子間力顕微鏡像を図4に示す。
図4に示すように、セルロースナノ繊維Cは、高結晶性セルロースナノクリスタルとなっていることが分かった。
【0061】
(評価1)
セルロースナノ繊維の製造において、ブランクとして0時間経過のサンプルと、セルロースミクロフィブリルAを加熱分解して得られた1.0,2.7,17.5時間経過後のサンプル(セルロースナノ繊維)について、原子間力顕微鏡で観察した。得られた原子間力顕微鏡像の写真を図5に示す。なお、原子間力顕微鏡観察においては、サンプルに固形分濃度0.05%となるように水を加え、これを、カチオン性ポリマーであるポリエチレンイミン(0.01
%水溶液)がコートされたゴルド表面にスピンコート(3000 rpm、1分)して薄膜を作り観察した。また、図5の上下の原子間力顕微鏡写真は、同じサンプルの異なる箇所を観察したものである。
【0062】
図5の1.0時間経過後の写真で認められるように、セルロースミクロフィブリルAの長い繊維が切断されている。また、2.7時間経過後では、大半の繊維の長さが1μm以下となっていることがわかった。さらに、17.5時間後には、殆どの繊維が、硫酸加水分解で得られる直径4〜10nm、長さ200nm前後のセルロースナノクリスタルまで分解が起こっていることがわかった。これらのことから、加熱温度、加熱時間又は酵素濃度を調節することによって、様々なアスペクト比を有するセルロースナノ繊維が調製可能であることが分かった。なお、図5の写真から、耐熱性エンドグルカナーゼは主に非晶領域を分解するが、セルロースナノ繊維からの高結晶性ナノクリスタルの調製も可能であることを示している。
【0063】
(評価2)
セルロースナノ繊維の製造において、セルロースミクロフィブリルA及びBをそれぞれ加熱分解して得られた0.5,1.0,2.7,17.5時間経過後のグルコースの定量を行った。その結果を表1に示す。
【0064】
(表1)

【0065】
表1の結果より、加熱時間の経過と共に、グルコース生成量が増加しているので、酵素反応が促進されていることがわかった。
【0066】
以上より、本発明のセルロースナノ繊維の製造方法によれば、酵素反応効率に優れると共に、アスペクト比及び結晶化度を容易に調節することができることが確認された。
【産業上の利用可能性】
【0067】
本発明のセルロースナノ繊維の製造方法により得られるセルロースナノ繊維は、高分子からなる強化材、透明材料、メンブレインフィルター等の様々な分野で用いることができる。
また、本発明のセルロースナノ繊維の製造方法によれば、用いられる分野のニーズにあわせたアスペクト比及び結晶化度を有するセルロースナノ繊維を提供することができる。
【符号の説明】
【0068】
S1・・・脆弱化工程
S2・・・加熱分解工程
【技術分野】
【0001】
本発明は、セルロースナノ繊維の製造方法に関し、更に詳しくは、酵素反応効率に優れると共に、アスペクト比及び結晶化度を容易に調節することができるセルロースナノ繊維の製造方法に関する。
【背景技術】
【0002】
一般に、木質バイオマス資源から取り出されるセルロースナノ繊維は、セルロース分子が数十本集まってできる最少単位の集合体であるセルロースエレメンタリフィブリル、その集合体である直径15〜30nmのセルロースミクロフィブリル、及び、セルロースの硫酸加水分解等で得られる高結晶性セルロースナノクリスタルの3種類に大別できる。
これらのセルロースナノ繊維は、近年、高機能高分子複合材料の強化材、透明材料、メンブレインフィルター等の様々な分野で注目を浴びている。
【0003】
セルロースナノ繊維の製造方法としては、酵素作用促進処理と物理的破壊処理とを複合することによって、セルロースミクロフィブリルの凝集体又はセルロースミクロフィブリルそのものの非晶部分にエンドグルカナーゼを作用させ、セルロースナノ繊維を得る方法が知られている(例えば、特許文献1参照)。
【0004】
ところで、近年、セルロースナノ繊維の応用分野が拡大するに従って、様々なアスペクト比及び結晶化度を有するセルロースナノ繊維が求められている。なお、本明細書において、アスペクト比とは、「セルロースナノ繊維の断面の直径/セルロースナノ繊維の長さ」を意味する。
【0005】
例えば、繊維強化プラスチック(FRP)の製造において、繊維のマット(不織布)を作り熱硬化性樹脂を含沈させ、熱圧硬化させる方法では、アスペクト比が大きいセルロースナノ繊維を用いることで、繊維同士の物理的相互作用(例えば水素結合)を強くなり、物性を向上させることができる。
ところが、熱可塑性高分子にセルロースナノ繊維を複合する方法、特に、エクストルーダーやニーダーを用いる混練の際には、アスペクト比が大きいセルロースナノ繊維は、絡み合いや混練中の凝集が起こり、分散性が低下するので、アスペクト比が調節されたセルロースナノ繊維が求められている。
【0006】
ちなみに、木質バイオマスからなるセルロースナノクリスタルは、高い結晶性を示し、強い強度特性を示す利点があり、一般に、直径が4〜6nmで、長さが100〜300nmであるので、アスペクト比が非常に小さくなる。
ところが、セルロースナノクリスタルを製造する際には、強い酸触媒を必要とし、また用いた強酸の回収や除去に非常にコストがかかるという欠点もある。なお、酸触媒を使わないで酵素を使った方法は、環境に易しい方法といえる。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2008−150719号公報
【発明の概要】
【発明が解決しようとする課題】
【0008】
しかしながら、上記特許文献1記載のセルロースナノ繊維の製造方法を含む従来のセルロースナノ繊維の製造方法においては、アスペクト比及び結晶化度を調節することが困難である。
セルロースナノ繊維のアスペクト比及び結晶化度の調節は非常に重要な研究課題であり、そのアスペクト比及び結晶化度を調節されたセルロースナノ繊維の開発が要求されている。
【0009】
また、セルロース系バイオマスの分解反応は、主に糸状菌由来の常温性セルラーゼ群(最適反応温度50℃位)を用いた酵素が一般的であるが、産業的に使用している反応機の場合は、長時間の分解反応中の雑菌汚染及び酵素の大量消費等の問題があり、高効率分解反応が実現されていない。
【0010】
本発明は、上記事情に鑑みてなされたものであり、酵素反応効率に優れると共に、アスペクト比及び結晶化度を容易に調節することができるセルロースナノ繊維の製造方法を提供することを目的とする。
【課題を解決するための手段】
【0011】
本発明者等は、上記課題を解決するため鋭意検討したところ、通常行われる酵素反応は40〜50℃であるが、50℃よりも高温で酵素反応を行うことを考えた。そして、耐熱性セルラーゼを選定し、その耐熱性セルラーゼを用いて、セルロースミクロフィブリルを、高温で加熱分解し、さらに、その時の加熱温度、加熱時間及び酵素濃度を調節することによって、上記課題を解決できることを見出し、本発明を完成させるに至った。
【0012】
本発明は、(1)バイオマスを粉砕し、セルロースミクロフィブリルとする脆弱化工程と、該セルロースミクロフィブリルを耐熱性セルラーゼで加熱分解する加熱分解工程と、を備え、加熱分解工程における加熱温度が50℃よりも大きく、且つ加熱温度、加熱時間又は酵素濃度を調節することによってアスペクト比及び結晶化度の調節が可能となっているセルロースナノ繊維の製造方法に存する。
【0013】
本発明は、(2)加熱分解工程における加熱温度が80℃以上である上記(1)記載のセルロースナノ繊維の製造方法に存する。
【0014】
本発明は、(3)耐熱性セルラーゼが、80℃以上で熱処理した後、精製した耐熱性エンドグルカナーゼと、80℃以上で熱処理した後、精製した耐熱性ベターグルコシダーゼとからなるものである上記(1)又は(2)に記載のセルロースナノ繊維の製造方法に存する。
【0015】
本発明は、(4)耐熱性エンドグルカナーゼが、セルロースミクロフィブリルの非晶部分を選択的に分解する上記(3)記載のセルロースナノ繊維の製造方法に存する。
【0016】
本発明は、(5)耐熱性エンドグルカナーゼと、耐熱性ベターグルコシダーゼとの配合割合が、20:0.1〜1である上記(3)又は(4)に記載のセルロースナノ繊維の製造方法に存する。
【0017】
本発明は、(6)脆弱化工程が、バイオマスをミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である上記(1)〜(5)のいずれか1つに記載のセルロースナノ繊維の製造方法に存する。
【0018】
本発明は、(7)脆弱化工程が、バイオマスを酸化剤及び水熱処理により脆弱化した後、ミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である上記(1)〜(5)のいずれか1つに記載のセルロースナノ繊維の製造方法に存する。
【発明の効果】
【0019】
本発明のセルロースナノ繊維の製造方法によれば、バイオマスを、所定のアスペクト比及び結晶化度を有するセルロースナノ繊維とすることができる。すなわち、上記セルロースナノ繊維の製造方法においては、セルロースミクロフィブリルを、耐熱性セルラーゼで、50℃よりも高温で加熱分解する加熱分解工程を経ることにより、酵素反応効率を向上させることができる。
【0020】
また、加熱分解工程において、加熱温度、加熱時間及び酵素濃度を調節することによって、高い精度でアスペクト比及び結晶化度を調節することができる。ちなみに、機械的な粉砕では、セルロースナノ繊維の長さをミクロンレベルで調節することが限界であるが、本発明においては、セルロースナノ繊維の長さをナノレベルで調節することが可能となる。特に、加熱温度は、80℃以上とすることが好ましい。
【0021】
上記セルロースナノ繊維の製造方法においては、耐熱性セルラーゼが、80℃以上で熱処理した後、精製した耐熱性エンドグルカナーゼと、80℃以上で熱処理した後、精製した耐熱性ベターグルコシダーゼとからなるものである場合、耐熱性エンドグルカナーゼがセルロースミクロフィブリルの非晶部分を選択的に分解し、耐熱性ベターグルコシダーゼが耐熱性エンドグルカナーゼの活性を阻害する副生成物のセロビオースを分解するので、酵素反応効率が極めて向上する。
【0022】
上記セルロースナノ繊維の製造方法においては、耐熱性エンドグルカナーゼと、耐熱性ベターグルコシダーゼとの配合割合が、20:0.1〜1である場合、耐熱性ベターグルコシダーゼによる分解と、耐熱性エンドグルカナーゼによる分解とがバランス良く行われる。
【0023】
上記セルロースナノ繊維の製造方法においては、脆弱化工程が、バイオマスをミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である場合、又は、バイオマスを酸化剤及び水熱処理により脆弱化し、ミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である場合、天然のバイオマスから比較的簡単な工程でセルロースナノ繊維を製造することが可能となる。
【図面の簡単な説明】
【0024】
【図1】図1は、本実施形態に係るセルロースナノ繊維の製造方法における各工程を示すフローチャートである。
【図2】図2は、実施例1で得られたセルロースミクロフィブリルAの原子間力顕微鏡像の写真である。
【図3】図3は、実施例2で得られたセルロースミクロフィブリルBの原子間力顕微鏡像の写真である。
【図4】図4は、実施例3で得られたセルロースナノ繊維Cの原子間力顕微鏡像の写真である。
【図5】図5は、ブランクとして0時間経過のサンプルと、実施例の評価1で得られた1.0,2.7,17.5時間経過後のサンプル(セルロースナノ繊維)の原子間力顕微鏡像の写真である。
【発明を実施するための形態】
【0025】
以下、必要に応じて図面を参照しつつ、本発明の好適な実施形態について詳細に説明する。
図1は、本実施形態に係るセルロースナノ繊維の製造方法における各工程を示すフローチャートである。
図1に示すように、本実施形態に係るセルロースナノ繊維の製造方法は、バイオマスを粉砕し、セルロースミクロフィブリルとする脆弱化工程S1と、該セルロースミクロフィブリルを耐熱性セルラーゼで加熱分解する加熱分解工程S2と、を備える。
【0026】
本実施形態に係るセルロースナノ繊維の製造方法によれば、バイオマスから所定のアスペクト比及び結晶化度を有するセルロースナノ繊維を効率良く製造することができる。
以下、各工程について更に詳細に説明する。
【0027】
(脆弱化工程)
脆弱化工程S1は、バイオマスを機械的に粉砕する工程である。脆弱化工程S1により、バイオマスは、セルロースミクロフィブリルとなる。
【0028】
上記バイオマスは、セルロース、ヘミセルロース及びリグニンを含む天然物であり、セルロースがリグニン及びヘミセルロースに強固に結びついた三次元ネットワーク階層構造を有している。
かかるバイオマスとしては、一般に、木材、草木、農産物、綿花等の植物から得られる木質バイオマスや生物が産生するバクテリアセルロース等が挙げられる。
【0029】
バイオマスの大きさは、5cm角以下であることが好ましい。この場合、脆弱化工程S1において、粉砕しやすくなる。なお、バイオマスが5cmを超える場合は、予備的に機械粉砕する予備脆弱化工程を施すことが好ましい。
【0030】
脆弱化工程S1における粉砕の方法は、特に限定されず、媒体(以下便宜的に「粉砕用媒体」という。)を共存させてせん断力をバイオマスに印可できる方法が好ましい。
例えば、ボールミル(振動ボールミル、回転ボールミル、遊星型ボールミル)、ロッドミル、ビーズミル、ディスクミル、カッターミル、ハンマーミル、インペラーミル、エクストルーダー、ミキサー(高速回転羽根型ミキサー、ホモミキサー)、ホモジナイザー(高圧ホモジナイザー、機械式ホモジナイザー、超音波ホモジナイザー)等が挙げられる。
【0031】
これらの中でも、粉砕は、ボールミル、ロッドミル、ビーズミル、ディスクミル又はカッターミル等のミルにより施されることが好ましく、ボールミル又はディスクミルにより施されることが更に好ましい。特に、ボールミルを用いる場合、結晶性を低下させることができるので、得られるセルロースナノ繊維の結晶性が低くなり(非晶性が高くなり)、その結果、酵素分解効率が向上するという利点がある。
【0032】
脆弱化工程S1において用いられる粉砕用媒体としては、特に限定されないが、水、低分子化合物、高分子化合物又は脂肪酸類等が好適に用いられる。これらは1種類を単独で用いてもよく、2種類以上を混合して用いてもよい。
これらの中でも、粉砕用媒体は、水と、低分子化合物、高分子化合物又は脂肪酸類とを混合して用いることが好ましい。
【0033】
低分子化合物としては、アルコール類、エーテル類、ケトン類、スルホキシド類、アミド類、アミン類、芳香族類、モルフォリン類、イオン性液体等が挙げられ、高分子化合物としては、アルコール系高分子類、エーテル系高分子類、アミド系高分子類、アミン系高分子類、芳香族系高分子類等が挙げられ、脂肪酸類としては、飽和脂肪酸類、不飽和脂肪酸類等が挙げられる。なお、このとき上記低分子化合物、高分子化合物及び脂肪酸類は水溶性であることが好ましい。
【0034】
本実施形態に係るセルロースナノ繊維の製造方法においては、脆弱化工程S1を経ることにより後述する加熱分解工程S2において、天然のバイオマスから比較的簡単な工程でアスペクト比及び結晶化度を調節したセルロースナノ繊維を製造することが可能となる。
【0035】
(加熱分解工程)
加熱分解工程S2は、脆弱化工程S1で得られたセルロースミクロフィブリルを耐熱性セルラーゼで加熱分解する工程である。
【0036】
ここで、耐熱性セルラーゼは、耐熱性を有し、50℃よりも高温の反応条件で反応活性を示すセルラーゼであり、一般的なセルラーゼとは異なる性質を有する。
具体的には、耐熱性セルラーゼは、耐熱性エンドグルカナーゼ及び耐熱性ベターグルコシダーゼからなる。これらの酵素は、耐熱性であるので、50℃よりも高温で反応させることができる。これにより、酵素反応効率が向上する。
【0037】
上記耐熱性エンドグルカナーゼ(EGPh)は、エンドグルカナーゼを発現させた後、80℃以上で熱処理し、硫安分画、遠心分離、カラムクロマトグラフィー等で精製することにより得られる。
上記耐熱性ベターグルコシダーゼ(BGL)は、ベターグルコシダーゼを発現させた後、80℃以上で熱処理し、硫安分画、遠心分離、およびカラムクロマトグラフィー等で精製することにより得られる。
【0038】
耐熱性エンドグルカナーゼは、セルロースの非結晶の領域に活性があり、結晶の領域には活性が無いことが特徴である。すなわち、耐熱性エンドグルカナーゼは、セルロースミクロフィブリルの非晶部分を選択的に分解することができる。これにより、結晶性の高いセルロースナノ繊維を得ることが可能となる。
また、耐熱性エンドグルカナーゼは、耐熱性アーキアPyrococcus horikoshii 由来であり、セルロースをセロビオースに分解する。なお、エンドグルカナーゼの副生成物であるセロビオースは、耐熱性エンドグルカナーゼによる酵素反応を阻害する作用がある。
【0039】
耐熱性ベターグルコシダーゼは、2−7糖のセロオリゴ糖を基質として、グルコースを遊離するが、結晶性セルロースは反応しないことが特徴である。これにより、結晶性の高いセルロースナノ繊維を得ることが可能となる。
また、耐熱性ベターグルコシダーゼは、耐熱性アーキアPyrococcus furiosus由来であり、上記セロビオースを分解する。
したがって、セルロースナノ繊維の製造方法においては、耐熱性エンドグルカナーゼがセルロースミクロフィブリルの非晶部分を選択的に分解し、耐熱性ベターグルコシダーゼが耐熱性エンドグルカナーゼの活性を阻害する副生成物のセロビオースを分解するので、酵素反応効率が極めて向上することになる。
【0040】
耐熱性エンドグルカナーゼと、耐熱性ベターグルコシダーゼとの配合割合は、20:0.1〜1であることが好ましい。耐熱性エンドグルカナーゼ20質量部に対し、耐熱性ベターグルコシダーゼが0.1質量部未満であると、配合割合が上記範囲内にある場合と比較して、セロビオースを十分に分解できず、耐熱性エンドグルカナーゼの酵素反応効率が悪くなる場合があり、耐熱性エンドグルカナーゼ20質量部に対し、耐熱性ベターグルコシダーゼが1質量部を超えると、耐熱性エンドグルカナーゼの酵素反応効率は略一定となり、向上しなくなる。
【0041】
加熱分解工程S2における加熱温度は、50℃よりも大きく、80℃以上であることが好ましく、80〜105℃であることがより好ましい。加熱温度を80℃以上とすることにより、より耐熱性に優れるセルロースナノ繊維が得られる。
また、加熱温度が80〜105℃である場合、加熱時間は、0.1〜72時間であることが好ましい。
さらに、これらの場合の耐熱性エンドグルカナーゼの酵素濃度は、基質1Mに対して、0.01〜10mMであることが好ましい。
【0042】
また、セルロースナノ繊維の製造方法においては、加熱温度、加熱時間及び酵素濃度を調節することによってアスペクト比及び結晶化度の調節が可能となる。
例えば、加熱分解工程S2における加熱温度は、上述した加熱温度の範囲において、加熱温度を低くすることにより、セルロースナノ繊維の長さを大きくすることができ、加熱温度を高くすることにより、セルロースナノ繊維の長さを小さくすることができる。
加熱分解工程S2における加熱時間は、上述した加熱時間の範囲において、加熱時間を短くすることにより、セルロースナノ繊維の長さを大きくすることができ、加熱時間を長くすることにより、セルロースナノ繊維の長さを小さくすることができる。
加熱分解工程S2における耐熱性エンドグルカナーゼの酵素濃度は、上述した酵素濃度の範囲において、酵素濃度を低くすることにより、セルロースナノ繊維の長さを大きくすることができ、酵素濃度を高くすることにより、セルロースナノ繊維の長さを小さくすることができる。
【0043】
本実施形態に係るセルロースナノ繊維の製造方法においては、加熱分解工程S2を経ることにより、酵素反応効率を向上させることができる。
また、加熱温度、加熱時間及び酵素濃度を調節することによって、セルロースナノ繊維の長さをナノレベルで変えることができるので、高い精度でアスペクト比を調節することができる。
【0044】
得られるセルロースナノ繊維は、天然物であり、高分子からなる強化材、透明材料、メンブレインフィルター、コーティング剤等に利用できる。
また、これらの用途に用いられる場合、セルロースナノ繊維のアスペクト比は4〜1000であることが好ましく、結晶化度は5〜90%であることが好ましい。
【0045】
得られるセルロースナノ繊維は、無味、無臭、無毒性であり、且つ微細繊維状で舌触りに異物感を感じないので、食品に添加して用いることもできる。この場合、保水性、保油性、テクスチャー、形態安定性、又はダイエット性を付与することができる。
【0046】
以上、本発明の好適な実施形態について説明したが、本発明は上記実施形態に限定されるものではない。
【0047】
例えば、本実施形態に係るセルロースナノ繊維の製造方法においては、脆弱化工程S1が、バイオマスを機械的に粉砕する工程となっているが、予め、バイオマスを酸処理、アルカリ処理、水熱処理又は酸化剤処理等により脆弱化処理してもよい。すなわち、脆弱化工程は、バイオマスをこれらの処理により脆弱化した後、ミルにより機械的に粉砕して、セルロースミクロフィブリルとしてもよい。
【0048】
この場合、アルカリ触媒又は酸触媒存在下、バイオマスに酸化剤を加え、加熱撹拌することにより脆弱化され、バイオマスからリグニンが除去されたホロセルロースが得られる。該ホロセルロースが機械的に粉砕することにより、ホロセルロースミクロフィブリルが得られることになる。
アルカリ触媒としては、苛性ソーダー、炭酸ナトリウム等が好適に用いられる。
酸触媒としては、硫酸、各種有機酸等が好適に用いられる。
酸化剤としては、亜塩素酸ナトリウム、TEMPO酸化剤、オゾン等が好適に用いられる。
【0049】
本実施形態に係るセルロースナノ繊維の製造方法においては、加熱分解工程S2において、耐熱性エンドグルカナーゼ及び耐熱性ベターグルコシダーゼを用いているが、必要に応じて、セロビオヒドロラーゼを混合して用いてもよい。ちなみに、セロビオヒドロラーゼの場合は特に結晶性セルロースに高い活性を示す。
【実施例】
【0050】
以下、実施例及び比較例に基づいて本発明をより具体的に説明するが、本発明は以下の実施例に限定されるものではない。
【0051】
(耐熱性エンドグルカナーゼの製造)
エンドグルカナーゼの発現は、発現プラスミドベクターpET11と発現用大腸菌BL21(DE3)を用いた。そして、発現したエンドグルカナーゼを85℃で熱処理し、Hitrap Phenyl columnを用いて精製することにより、耐熱性エンドグルカナーゼ(酵素番号:EC 3.2.1.4、ファミリー5に属する)を得た。
【0052】
(耐熱性ベターグルコシダーゼの製造)
ベターグルコシダーゼの発現は、発現プラスミドベクターpET11と発現用大腸菌BL21(DE3)を用いた。そして、発現したベターグルコシダーゼを85℃で熱処理し、Hitrap Phenyl columnを用いて精製することにより、耐熱性ベターグルコシダーゼ(酵素番号:EC 3.2.1.21)を得た。
【0053】
(実施例1)
(セルロースミクロフィブリルAの製造)
木質バイオマスとして、5cm角のユーカリクラフトパルプを用いた。なお、広葉樹であるユーカリのクラフトパルプの成分分析をした結果、セルロース成分は0.2%、ヘミセルロースは22.3%、リグニンは10.3%であった。
ユーカリクラフトパルプを、ディスクミルを用いて機械的に粉砕した(脆弱化工程)。具体的には、ユーカリのクラフトパルプに水を加え、固形分濃度1%となるように水懸濁液とし、これに対してディスクミルを用いた機械的粉砕を10回行い、セルロースミクロフィブリルAとした。
【0054】
セルロースミクロフィブリルAの原子間力顕微鏡像を図2に示す。なお、原子間力顕微鏡観察においては、得られたセルロースミクロフィブリルAに固形分濃度0.05%となるように水を加え、これを、カチオン性ポリマーであるポリエチレンイミン(0.01
%水溶液)がコートされたゴルド表面にスピンコート(3000 rpm、1分)して薄膜を作り観察した。
セルロースミクロフィブリルAは、直径が5〜30nmであり、長さが1μm以上であったので、非常にアスペクト比が大きいことがわかった。
【0055】
(セルロースナノ繊維Aの製造)
セルロースミクロフィブリルAを、耐熱性セルラーゼで加熱分解した。具体的には、セルロースミクロフィブリルAに固形分濃度0.2%となるように水を加え、これに、0.1Mの酢酸緩衝液(pH5.5)を2mL加えた。そして、10μMの耐熱性エンドグルカナーゼと、0.2μMのベターグルコシダーゼとをそれぞれ0.2mL加え、加熱温度を85℃として攪拌することにより(加熱分解工程)、セルロースミクロフィブリルAを加熱分解したセルロースナノ繊維Aを得た。なお、0.5,1.0,2.7,17.5時間経過後にそれぞれサンプリングした。
【0056】
(実施例2)
(セルロースミクロフィブリルBの製造)
木質バイオマスとして、針葉樹であるヒノキ木粉(0.2mm)を用いた。
まず、ヒノキ木粉を、亜塩素酸アトリウムにより脱リグニン(脆弱化)した。具体的には、ヒノキ木粉25gに、蒸留水750ml、亜塩素酸ナトリウム(酸化剤)7.5g及び酢酸(酸触媒)1.5mlを加えて、80〜90℃の湯浴中で攪拌しながら1時間加温した。その後、さらに、亜塩素酸ナトリウム7.5g、酢酸1.5mlを加えて反応を行い、この操作を5回繰り返した後、蒸留水3Lで洗浄し、ホロセルロースを得た。
そして、得られたホロセルロースを、ディスクミルを用いて機械的に粉砕した(脆弱化工程)。具体的には、ヒノキ木粉に水を加え、固形分濃度1%となるように水懸濁液とし、これに対してディスクミルを用いた機械的粉砕を2回行い、セルロースミクロフィブリルBとした。
【0057】
セルロースミクロフィブリルBの原子間力顕微鏡像を図3に示す。なお、原子間力顕微鏡観察においては、得られたセルロースミクロフィブリルBに固形分濃度0.05%となるように水を加え、これを、カチオン性ポリマーであるポリエチレンイミン(0.01
%水溶液)がコートされたゴルド表面にスピンコート(3000 rpm、1分)して薄膜を作り観察した。
セルロースミクロフィブリルBは、セルロースミクロフィブリルAと同様に、非常にアスペクト比が大きいことがわかった。
【0058】
(セルロースナノ繊維Bの製造)
セルロースミクロフィブリルBを、耐熱性セルラーゼで加熱分解した。具体的には、セルロースミクロフィブリルBに固形分濃度0.2%となるように水を加え、これに、0.1Mの酢酸緩衝液(pH5.5)を2mL加えた。そして、10μMの耐熱性エンドグルカナーゼと、0.2μMのベターグルコシダーゼとをそれぞれ0.2mL加え、加熱温度を85℃として攪拌することにより(加熱分解工程)、セルロースミクロフィブリルBを加熱分解したセルロースナノ繊維Bを得た。なお、0.5,1.0,2.7,17.5時間経過後にそれぞれサンプリングした。
【0059】
(実施例3)
(セルロースミクロフィブリルCの製造)
木質バイオマスとして、サトウキビ残渣(バガス)1gを用いた。
まず、サトウキビ残渣を、遊星ボールミルを用いて機械的に粉砕した(脆弱化工程)。具体的には、サトウキビ残渣に水を加え、400rpmで2時間処理し、セルロースミクロフィブリルCとした。
【0060】
(セルロースナノ繊維Cの製造)
セルロースミクロフィブリルCを、耐熱性セルラーゼで加熱分解した。具体的には、セルロースミクロフィブリルC350mgに水を加え、これに、50mMのクエン酸緩衝液(citrate buffer、pH5.0)を加え、基質濃度を1%とした。そして、耐熱性エンドグルカナーゼ(345
UI/g of bagasse)を加え、加熱温度を85℃として72時間攪拌することにより(加熱分解工程)、セルロースミクロフィブリルCを加熱分解したセルロースナノ繊維Cを得た。なお、このときのグルコース生成量は33.42%であった。
セルロースナノ繊維Cの原子間力顕微鏡像を図4に示す。
図4に示すように、セルロースナノ繊維Cは、高結晶性セルロースナノクリスタルとなっていることが分かった。
【0061】
(評価1)
セルロースナノ繊維の製造において、ブランクとして0時間経過のサンプルと、セルロースミクロフィブリルAを加熱分解して得られた1.0,2.7,17.5時間経過後のサンプル(セルロースナノ繊維)について、原子間力顕微鏡で観察した。得られた原子間力顕微鏡像の写真を図5に示す。なお、原子間力顕微鏡観察においては、サンプルに固形分濃度0.05%となるように水を加え、これを、カチオン性ポリマーであるポリエチレンイミン(0.01
%水溶液)がコートされたゴルド表面にスピンコート(3000 rpm、1分)して薄膜を作り観察した。また、図5の上下の原子間力顕微鏡写真は、同じサンプルの異なる箇所を観察したものである。
【0062】
図5の1.0時間経過後の写真で認められるように、セルロースミクロフィブリルAの長い繊維が切断されている。また、2.7時間経過後では、大半の繊維の長さが1μm以下となっていることがわかった。さらに、17.5時間後には、殆どの繊維が、硫酸加水分解で得られる直径4〜10nm、長さ200nm前後のセルロースナノクリスタルまで分解が起こっていることがわかった。これらのことから、加熱温度、加熱時間又は酵素濃度を調節することによって、様々なアスペクト比を有するセルロースナノ繊維が調製可能であることが分かった。なお、図5の写真から、耐熱性エンドグルカナーゼは主に非晶領域を分解するが、セルロースナノ繊維からの高結晶性ナノクリスタルの調製も可能であることを示している。
【0063】
(評価2)
セルロースナノ繊維の製造において、セルロースミクロフィブリルA及びBをそれぞれ加熱分解して得られた0.5,1.0,2.7,17.5時間経過後のグルコースの定量を行った。その結果を表1に示す。
【0064】
(表1)

【0065】
表1の結果より、加熱時間の経過と共に、グルコース生成量が増加しているので、酵素反応が促進されていることがわかった。
【0066】
以上より、本発明のセルロースナノ繊維の製造方法によれば、酵素反応効率に優れると共に、アスペクト比及び結晶化度を容易に調節することができることが確認された。
【産業上の利用可能性】
【0067】
本発明のセルロースナノ繊維の製造方法により得られるセルロースナノ繊維は、高分子からなる強化材、透明材料、メンブレインフィルター等の様々な分野で用いることができる。
また、本発明のセルロースナノ繊維の製造方法によれば、用いられる分野のニーズにあわせたアスペクト比及び結晶化度を有するセルロースナノ繊維を提供することができる。
【符号の説明】
【0068】
S1・・・脆弱化工程
S2・・・加熱分解工程
【特許請求の範囲】
【請求項1】
バイオマスを粉砕し、セルロースミクロフィブリルとする脆弱化工程と、
該セルロースミクロフィブリルを耐熱性セルラーゼで加熱分解する加熱分解工程と、
を備え、
前記加熱分解工程における加熱温度が50℃よりも大きく、且つ加熱温度、加熱時間又は酵素濃度を調節することによってアスペクト比及び結晶化度の調節が可能となっているセルロースナノ繊維の製造方法。
【請求項2】
前記加熱分解工程における加熱温度が80℃以上である請求項1記載のセルロースナノ繊維の製造方法。
【請求項3】
前記耐熱性セルラーゼが、80℃以上で熱処理した後、精製した耐熱性エンドグルカナーゼと、80℃以上で熱処理した後、精製した耐熱性ベターグルコシダーゼとからなるものである請求項1又は2に記載のセルロースナノ繊維の製造方法。
【請求項4】
前記耐熱性エンドグルカナーゼが、前記セルロースミクロフィブリルの非晶部分を選択的に分解する請求項3記載のセルロースナノ繊維の製造方法。
【請求項5】
前記耐熱性エンドグルカナーゼと、前記耐熱性ベターグルコシダーゼとの配合割合が、20:0.1〜1である請求項3又は4に記載のセルロースナノ繊維の製造方法。
【請求項6】
前記脆弱化工程が、バイオマスをミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である請求項1〜5のいずれか1項に記載のセルロースナノ繊維の製造方法。
【請求項7】
前記脆弱化工程が、バイオマスを酸化剤及び水熱処理により脆弱化した後、ミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である請求項1〜5のいずれか1項に記載のセルロースナノ繊維の製造方法。
【請求項1】
バイオマスを粉砕し、セルロースミクロフィブリルとする脆弱化工程と、
該セルロースミクロフィブリルを耐熱性セルラーゼで加熱分解する加熱分解工程と、
を備え、
前記加熱分解工程における加熱温度が50℃よりも大きく、且つ加熱温度、加熱時間又は酵素濃度を調節することによってアスペクト比及び結晶化度の調節が可能となっているセルロースナノ繊維の製造方法。
【請求項2】
前記加熱分解工程における加熱温度が80℃以上である請求項1記載のセルロースナノ繊維の製造方法。
【請求項3】
前記耐熱性セルラーゼが、80℃以上で熱処理した後、精製した耐熱性エンドグルカナーゼと、80℃以上で熱処理した後、精製した耐熱性ベターグルコシダーゼとからなるものである請求項1又は2に記載のセルロースナノ繊維の製造方法。
【請求項4】
前記耐熱性エンドグルカナーゼが、前記セルロースミクロフィブリルの非晶部分を選択的に分解する請求項3記載のセルロースナノ繊維の製造方法。
【請求項5】
前記耐熱性エンドグルカナーゼと、前記耐熱性ベターグルコシダーゼとの配合割合が、20:0.1〜1である請求項3又は4に記載のセルロースナノ繊維の製造方法。
【請求項6】
前記脆弱化工程が、バイオマスをミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である請求項1〜5のいずれか1項に記載のセルロースナノ繊維の製造方法。
【請求項7】
前記脆弱化工程が、バイオマスを酸化剤及び水熱処理により脆弱化した後、ミルにより機械的に粉砕して、セルロースミクロフィブリルとする工程である請求項1〜5のいずれか1項に記載のセルロースナノ繊維の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2013−110987(P2013−110987A)
【公開日】平成25年6月10日(2013.6.10)
【国際特許分類】
【出願番号】特願2011−258118(P2011−258118)
【出願日】平成23年11月25日(2011.11.25)
【出願人】(301021533)独立行政法人産業技術総合研究所 (6,529)
【Fターム(参考)】
【公開日】平成25年6月10日(2013.6.10)
【国際特許分類】
【出願日】平成23年11月25日(2011.11.25)
【出願人】(301021533)独立行政法人産業技術総合研究所 (6,529)
【Fターム(参考)】
[ Back to top ]

