センサーの分子密度依存シグナル増幅を利用した検出方法
【課題】原理的に如何なる種類の物質も検出対象とすることが可能で、且つ、簡便で効率的な検出方法等を提供すること。
【解決手段】本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域、及び被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子、及び、昆虫の体液から調製されたフェノール酸化酵素前駆体カスケード因子含有試薬を含む、メラニン化(黒化)反応により被検物質を検出するために組成物を用いる検出方法。
【解決手段】本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域、及び被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子、及び、昆虫の体液から調製されたフェノール酸化酵素前駆体カスケード因子含有試薬を含む、メラニン化(黒化)反応により被検物質を検出するために組成物を用いる検出方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、分子密度依存シグナル増幅を利用する各種物質の検出方法等に関するものである。
【背景技術】
【0002】
昆虫は地球上で繁栄を極めている。その理由には、変態や休眠といった生活環を取り入れて環境の変化に対応してきたことや、飛翔能力や微量なフェロモンを感知する優れた嗅覚なども含めた繁殖能力の高さが挙げられるが、効果的な感染防御機構を有していることも一因である。
【0003】
このような昆虫における感染防御機構の一つに、ペプチドグリカン及び(1→3)-β-D-グルカンがペプチドグルカン認識タンパク質(PGRP)又はβ-グルカン認識タンパク質(BGRP)等のセンサー物質と結合することによって開始されるプロテアーゼ系のカスケード反応により、最終的に呈色反応を誘導するフェノール酸化酵素が前駆体(proPO)から活性型に活性化され、メラニン色素を生成する経路(フェノール酸化酵素前駆体カスケード:ProPOカスケード)がある。
【0004】
この優れた感染防御反応を利用した例として、カイコの体液を無菌的に採取・調製して得られたProPOカスケードの因子を全て含んだ試薬「カイコプラズマ(SLP)試薬(和光純薬工業株式会社)」があり、該試薬は細菌の非特異的高感度検出法に使用される。SLP試薬はカイコ体液(プラズマ)に微生物が侵入すると即座にフェノール酸化酵素前駆体(proPO)系が活性化し、メラニン化(黒化)が誘導されることを利用している。
【0005】
一方、本発明者等はこれまでに、ショウジョウバエのproPO系を活性化する病原体認識タンパク質であり、グラム陽性菌の中では炭素菌等のバシラス属及びラクトバチルスが細胞壁に有するジアミノピメリン酸型ペプチドグリカンを特異的に認識する、ペプチドグリカン認識タンパク質(PGRP)-LEを同定している(非特許文献1、特許文献1)。更に、PGRP-LEによる病原体認識と感染シグナルの活性化機構を解析し、感染シグナルの活性化にはPGRP-LEの分子密度の上昇が重要であり、リガンドの結合には依存しないことを明らかにした(非特許文献2〜4)。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特許第3696578号
【非特許文献】
【0007】
【非特許文献1】Proc. Natl. Acad. Sci., USA (2002) 99:13705-13710
【非特許文献2】EMBO J. Vol.23., No.23 (2004) pp.4690-4700
【非特許文献3】J. Biol. Chem., vol.281, No.12 (2006), pp.8286-8295
【非特許文献4】Nature Immunology, Vol.7, No.7 (2006), pp.715-723
【発明の概要】
【発明が解決しようとする課題】
【0008】
本発明が解決しようとする課題は、原理的に如何なる種類の物質も検出対象とすることが可能で、且つ、簡便で効率的な検出方法を提供することである。
【課題を解決するための手段】
【0009】
本発明者は、上記のペプチドグリカン認識タンパク質(PGRP)-LEの特性に基づいた分子密度依存シグナル増幅(density-dependent signaling amplification: DDSA)を利用して各種物質を検出することが可能であることを初めて実証し、かかる機構を利用した検出技術によって本発明を完成して上記の課題が解決することに成功した。
【0010】
即ち、本発明は主に以下の各態様に係るものである。
[1]本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域、及び被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子、及び、昆虫の体液から調製されたフェノール酸化酵素前駆体カスケード因子含有試薬を含む、メラニン化(黒化)反応により被検物質を検出するために組成物。
[2]上記の組成物と被検物質を接触させ、PGRP-LEキメラ分子密度に依存するシグナル増幅によるメラニン化(黒化)による発色反応を測定することから成る、被検物質の存在を検出する方法。
[3]本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域と被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子を含む、上記の検出方法に使用する検出キット。
【発明の効果】
【0011】
DDSAを利用した本発明の検出方法によれば、ターゲットとする被検物質の種類に制約がない。又、非反応性試薬の洗浄工程が不要であり、ワンステップで被検物質の特異的な検出を簡便・効率的に行なうことが可能となる。
【図面の簡単な説明】
【0012】
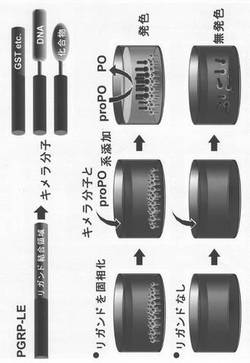
【図1】DDSAを利用した本発明方法における検出技術の概要を示す。
【図2】カイコ発現系を用いて作製したキメラ分子(LEAD-GST)の発現の様子を示す電気泳動の結果を示す写真である。
【図3】本発明の検出方法による測定結果を示す。
【図4】構造変換に伴い凝集化したタンパク質の特異的検出への本発明方法の応用を示す。
【発明を実施するための形態】
【0013】
本発明の第一の態様である組成物には、主成分の一つとして、本来のリガンド結合能、即ち、ジアミノピメリン酸型ペプチドグリカンに対する特異的結合能、を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域、及び被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子が含まれている。
【0014】
PGRP-LEはショウジョウバエの少なくとも12個のメンバーから成るペプチドグリカン認識タンパク質(PGRP)ファミリーのひとつであり、機能獲得遺伝的スクリーニングを用いて見出された(Werner, T., et al., (2000) Pro. Natl. Acad. Sci. U.S.A., 97, 13772-13777)。
【0015】
PGRP-LEは345個のアミノ酸からなるタンパク質であり、その遺伝子のコード領域の塩基配列及びアミノ酸配列は、夫々、配列番号1及び配列番号2に示される。ここで、C末端側の173〜345番目のアミノ酸から成る領域がリガンド結合領域(ドメイン)であることが知られている(非特許文献3)。
【0016】
上記のPGRP-LEキメラ分子において、PGRP-LE のリガンド結合能を喪失させるためには、当業者に公知の任意の方法・手段を用いることが出来る。例えば、PGRP-LEにおける上記のリガンド結合領域の少なくとも一部、又は全体をセンサー領域と置換することによって、ペプチドグリカン認識タンパク質(PGRP)-LE が本来有しているジアミノピメリン酸型ペプチドグリカンに対する特異的結合能を喪失させることが出来る。
【0017】
或いは、部位特異的突然変異等の当業者に公知の遺伝子工学的手法による遺伝子変異によってPGRP-LEにおけるリガンド結合領域の一部に、適当なアミノ酸による挿入、置換又は欠失等を起こさせることによって、PGRP-LEが本来有しているリガンド結合能を喪失させることも可能である。そのような場合には、特に、PGRP-LEにおけるリガンド結合領域の少なくとも一部をセンサー領域と置換する必要はない。
【0018】
センサー領域は被検物質(リガンド)を特異的に認識して結合する物質であり、被検物質の種類などに応じて、例えば、ポリペプチド、酵素及び抗体分子等のタンパク質、核酸、酵素基質、各種リガンド結合物質、及び低分子化合物から成る群から適宜選択される。
【0019】
尚、上記のPGRP-LEキメラ分子において上記PGRP-LE領域とセンサー領域とが直接に連結されていても良いし、或いは、例えば、ペプチドリンカーのような当業者に公知の任意のリンカーを介して両者を結合することも可能である。更に、FLAGタグ又はHisタグのような、当業者に公知の適当な検出用の標識物質を更にPGRP-LEキメラ分子の適当な位置(例えば、N末端)に付加することも出来る。
【0020】
このようなPGRP-LEキメラ分子は当業者に公知の任意の方法で作製することが出来る。例えば、センサー領域がポリペプチド又はタンパク質である場合には、本来のリガンド結合能を喪失させたPGRP-LE領域と該ポリペプチドとの融合タンパク質をコードするDNAを遺伝子組換え技術によって作製し、これを適当な発現系を利用して産生させることによって容易に調製することが出来る。或いは、まず、本来のリガンド結合能を喪失させたPGRP-LE領域を任意の方法で作製し、その後、適当な手段によって、該PGRP-LE領域とセンサー領域とを適当なリンカーを適宜使用することによって結合させることが出来る。
【0021】
本発明組成物のもう一つの主成分である昆虫の体液から調製されたフェノール酸化酵素前駆体カスケード因子含有試薬はメラニン化(黒化)反応を生起する試薬として当業者には公知であり、その一例として、カイコの体液を無菌的に採取・調製して得られたカイコプラズマ(SLP)試薬を挙げることが出来る。
【0022】
尚、本発明の組成物は、上記の2つの主成分の他に、適宜、緩衝剤、及び安定剤等の当業者に公知の任意の補助成分、並びに、水等の媒体を含み得るものである。
【0023】
本発明の検出方法は、上記の組成物と被検物質を接触させ、PGRP-LEキメラ分子密度に依存するシグナル増幅(DDSA)によるメラニン化(黒化)による発色反応を測定することによって、被検物質の存在を検出することを特徴とする。その概要を図1に示す。本発明の検出方法は分子密度依存シグナル増幅(DDSA)技術を利用するものである。即ち、PGRP-LEによるシグナルの活性化はリガンドと結合することによって該PGRP-LEの分子密度が上昇することによって生起する、という機構を利用するものであるので、本発明の検出方法は、特に、例えば、被検物質の多量体化等に因る存在状態(集合状態)の変化の検出、又は、被検物質として、例えば、様々な病態に関係するような、構造変換に伴い凝集化したタンパク質の特異的な検出に有利である。
【0024】
尚、本発明方法における検出対象である被検物質(リガンド)は、本発明のPGRP-LEキメラ分子のセンサー領域が特異的に認識して結合できる物質であれば、その種類に特に制限はなく、ポリペプチド並びに酵素及び抗体分子等のタンパク質、DNA又はRNA等の核酸分子、糖、若しくは脂質等の任意の種類の生体分子、又は、それらの断片又は一部の領域、酵素基質、及び低分子化合物等を例示することが出来る。尚、このような被検物質として、細胞、組織若しくは器官等の生体由来物質、又は、適当な材質からなる基板及びプレート等の適当な人工担体の表面上に固定又は結合等の任意の状態で存在しているものも含まれる。
【0025】
従って、本発明は更に、本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域と被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子を含む、上記の検出方法に使用する検出キットにも係る。該キットには、更に、カイコ等の昆虫の体液から調製されたフェノール酸化酵素前駆体カスケード因子含有試薬を含む本発明の組成物が含まれていることが好ましい。又、被検物質及び測定系の種類等に応じて、該キットには測定プレート等の適応な要素を更に含むことが出来る。
【0026】
以下、実施例に則して本発明を具体的に説明するが、本発明の技術的範囲はこれらの記載によって何等制限されるものではない。
【実施例1】
【0027】
PGRP-LEの2〜176アミノ酸からなる領域をコードするDNA配列とpAcG2T vector由来のGSTをコードする配列を制限酵素Bam HI認識配列で連結し、ペプチドグリカン認識タンパク質(PGRP)-LEのリガンド結合領域の一部(C末端側の177〜34番目のアミノ酸からなる領域)をGSTと置換することによって、本発明のPGRP-LEキメラ分子であるPGRP-LEとGSTとのキメラ分子(LEAD-GST)をコードする遺伝子を作製し、これをカイコ発現系vectorであるpM25 vectorあるいはpM07 vectorのクローニングサイトに挿入し、本遺伝子発現タンパク質をカイコ幼虫体液中に産生させることにより、本発明のキメラ分子を作製した。尚、これらのキメラ分子には検出用のタグ分子として、N末端にFLAGタグ又はHisタグが付加されている。”LEAD-“は、PGRP-LEのN末端側1〜176アミノ酸領域に相当する。その結果、産生されたキメラ分子の発現の様子を図2に示す。
【実施例2】
【0028】
次に、最終濃度100mM NaClとなる条件下、こうして調製したキメラ分子であるLEAD-GSTを発現させたカイコ体液と、発現させていないコントロール体液を、グルタチオンをプレート底面に固相化したプレート(グルタチオンプレート)、または通常のプレートに加え、これに等量のproPO系としてのSLP試薬(和光純薬工業株式会社)を加えて、30℃で75分反応させた後、proPO系の活性化を540nmにおける吸光度で測定した。その概要及び結果を図3に示す。この結果から、本発明の検出方法によって、プレート上で分子密度が上昇したLEAD-GSTの特異的な検出がワンステップで、簡便・効率的に行なうことが可能であることが示された。
【産業上の利用可能性】
【0029】
本発明の検出方法は、分子密度依存シグナル増幅(density-dependent signaling amplification: DDSA)を利用するものであり、このDDSA技術は、PCR又はELISA法等の従来の検出技術を補完する新たな増幅技術である。即ち、PCRはターゲットDNAの増幅に限定されるがDDSAはリガンド非特異的にシグナルの増幅が可能であるために、様々な種類のリガンド(被検物質)をターゲットにすることが可能となる。更に、分子密度依存的にシグナル増幅を行なうので、ELISA法のように非反応性の試薬を除去する必要がないワンステップの検出が可能である。
【0030】
従って、このようにDDSAに基づく本発明方法は、様々な対象を検出できる検出系として幅広い展開が期待できる。加えて、DDSA は、分子密度の上昇で活性化するため、検出する物質の集合状態などを識別できる可能性をも有している。例えば、異常型プリオンタンパク質、ポリグルタミン病での変異タンパク質、及びアミロイド等の、病態に関係して構造変換に伴い凝集化したタンパク質等の特異的検出への応用が期待できる(図4)。
【技術分野】
【0001】
本発明は、分子密度依存シグナル増幅を利用する各種物質の検出方法等に関するものである。
【背景技術】
【0002】
昆虫は地球上で繁栄を極めている。その理由には、変態や休眠といった生活環を取り入れて環境の変化に対応してきたことや、飛翔能力や微量なフェロモンを感知する優れた嗅覚なども含めた繁殖能力の高さが挙げられるが、効果的な感染防御機構を有していることも一因である。
【0003】
このような昆虫における感染防御機構の一つに、ペプチドグリカン及び(1→3)-β-D-グルカンがペプチドグルカン認識タンパク質(PGRP)又はβ-グルカン認識タンパク質(BGRP)等のセンサー物質と結合することによって開始されるプロテアーゼ系のカスケード反応により、最終的に呈色反応を誘導するフェノール酸化酵素が前駆体(proPO)から活性型に活性化され、メラニン色素を生成する経路(フェノール酸化酵素前駆体カスケード:ProPOカスケード)がある。
【0004】
この優れた感染防御反応を利用した例として、カイコの体液を無菌的に採取・調製して得られたProPOカスケードの因子を全て含んだ試薬「カイコプラズマ(SLP)試薬(和光純薬工業株式会社)」があり、該試薬は細菌の非特異的高感度検出法に使用される。SLP試薬はカイコ体液(プラズマ)に微生物が侵入すると即座にフェノール酸化酵素前駆体(proPO)系が活性化し、メラニン化(黒化)が誘導されることを利用している。
【0005】
一方、本発明者等はこれまでに、ショウジョウバエのproPO系を活性化する病原体認識タンパク質であり、グラム陽性菌の中では炭素菌等のバシラス属及びラクトバチルスが細胞壁に有するジアミノピメリン酸型ペプチドグリカンを特異的に認識する、ペプチドグリカン認識タンパク質(PGRP)-LEを同定している(非特許文献1、特許文献1)。更に、PGRP-LEによる病原体認識と感染シグナルの活性化機構を解析し、感染シグナルの活性化にはPGRP-LEの分子密度の上昇が重要であり、リガンドの結合には依存しないことを明らかにした(非特許文献2〜4)。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特許第3696578号
【非特許文献】
【0007】
【非特許文献1】Proc. Natl. Acad. Sci., USA (2002) 99:13705-13710
【非特許文献2】EMBO J. Vol.23., No.23 (2004) pp.4690-4700
【非特許文献3】J. Biol. Chem., vol.281, No.12 (2006), pp.8286-8295
【非特許文献4】Nature Immunology, Vol.7, No.7 (2006), pp.715-723
【発明の概要】
【発明が解決しようとする課題】
【0008】
本発明が解決しようとする課題は、原理的に如何なる種類の物質も検出対象とすることが可能で、且つ、簡便で効率的な検出方法を提供することである。
【課題を解決するための手段】
【0009】
本発明者は、上記のペプチドグリカン認識タンパク質(PGRP)-LEの特性に基づいた分子密度依存シグナル増幅(density-dependent signaling amplification: DDSA)を利用して各種物質を検出することが可能であることを初めて実証し、かかる機構を利用した検出技術によって本発明を完成して上記の課題が解決することに成功した。
【0010】
即ち、本発明は主に以下の各態様に係るものである。
[1]本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域、及び被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子、及び、昆虫の体液から調製されたフェノール酸化酵素前駆体カスケード因子含有試薬を含む、メラニン化(黒化)反応により被検物質を検出するために組成物。
[2]上記の組成物と被検物質を接触させ、PGRP-LEキメラ分子密度に依存するシグナル増幅によるメラニン化(黒化)による発色反応を測定することから成る、被検物質の存在を検出する方法。
[3]本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域と被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子を含む、上記の検出方法に使用する検出キット。
【発明の効果】
【0011】
DDSAを利用した本発明の検出方法によれば、ターゲットとする被検物質の種類に制約がない。又、非反応性試薬の洗浄工程が不要であり、ワンステップで被検物質の特異的な検出を簡便・効率的に行なうことが可能となる。
【図面の簡単な説明】
【0012】
【図1】DDSAを利用した本発明方法における検出技術の概要を示す。
【図2】カイコ発現系を用いて作製したキメラ分子(LEAD-GST)の発現の様子を示す電気泳動の結果を示す写真である。
【図3】本発明の検出方法による測定結果を示す。
【図4】構造変換に伴い凝集化したタンパク質の特異的検出への本発明方法の応用を示す。
【発明を実施するための形態】
【0013】
本発明の第一の態様である組成物には、主成分の一つとして、本来のリガンド結合能、即ち、ジアミノピメリン酸型ペプチドグリカンに対する特異的結合能、を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域、及び被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子が含まれている。
【0014】
PGRP-LEはショウジョウバエの少なくとも12個のメンバーから成るペプチドグリカン認識タンパク質(PGRP)ファミリーのひとつであり、機能獲得遺伝的スクリーニングを用いて見出された(Werner, T., et al., (2000) Pro. Natl. Acad. Sci. U.S.A., 97, 13772-13777)。
【0015】
PGRP-LEは345個のアミノ酸からなるタンパク質であり、その遺伝子のコード領域の塩基配列及びアミノ酸配列は、夫々、配列番号1及び配列番号2に示される。ここで、C末端側の173〜345番目のアミノ酸から成る領域がリガンド結合領域(ドメイン)であることが知られている(非特許文献3)。
【0016】
上記のPGRP-LEキメラ分子において、PGRP-LE のリガンド結合能を喪失させるためには、当業者に公知の任意の方法・手段を用いることが出来る。例えば、PGRP-LEにおける上記のリガンド結合領域の少なくとも一部、又は全体をセンサー領域と置換することによって、ペプチドグリカン認識タンパク質(PGRP)-LE が本来有しているジアミノピメリン酸型ペプチドグリカンに対する特異的結合能を喪失させることが出来る。
【0017】
或いは、部位特異的突然変異等の当業者に公知の遺伝子工学的手法による遺伝子変異によってPGRP-LEにおけるリガンド結合領域の一部に、適当なアミノ酸による挿入、置換又は欠失等を起こさせることによって、PGRP-LEが本来有しているリガンド結合能を喪失させることも可能である。そのような場合には、特に、PGRP-LEにおけるリガンド結合領域の少なくとも一部をセンサー領域と置換する必要はない。
【0018】
センサー領域は被検物質(リガンド)を特異的に認識して結合する物質であり、被検物質の種類などに応じて、例えば、ポリペプチド、酵素及び抗体分子等のタンパク質、核酸、酵素基質、各種リガンド結合物質、及び低分子化合物から成る群から適宜選択される。
【0019】
尚、上記のPGRP-LEキメラ分子において上記PGRP-LE領域とセンサー領域とが直接に連結されていても良いし、或いは、例えば、ペプチドリンカーのような当業者に公知の任意のリンカーを介して両者を結合することも可能である。更に、FLAGタグ又はHisタグのような、当業者に公知の適当な検出用の標識物質を更にPGRP-LEキメラ分子の適当な位置(例えば、N末端)に付加することも出来る。
【0020】
このようなPGRP-LEキメラ分子は当業者に公知の任意の方法で作製することが出来る。例えば、センサー領域がポリペプチド又はタンパク質である場合には、本来のリガンド結合能を喪失させたPGRP-LE領域と該ポリペプチドとの融合タンパク質をコードするDNAを遺伝子組換え技術によって作製し、これを適当な発現系を利用して産生させることによって容易に調製することが出来る。或いは、まず、本来のリガンド結合能を喪失させたPGRP-LE領域を任意の方法で作製し、その後、適当な手段によって、該PGRP-LE領域とセンサー領域とを適当なリンカーを適宜使用することによって結合させることが出来る。
【0021】
本発明組成物のもう一つの主成分である昆虫の体液から調製されたフェノール酸化酵素前駆体カスケード因子含有試薬はメラニン化(黒化)反応を生起する試薬として当業者には公知であり、その一例として、カイコの体液を無菌的に採取・調製して得られたカイコプラズマ(SLP)試薬を挙げることが出来る。
【0022】
尚、本発明の組成物は、上記の2つの主成分の他に、適宜、緩衝剤、及び安定剤等の当業者に公知の任意の補助成分、並びに、水等の媒体を含み得るものである。
【0023】
本発明の検出方法は、上記の組成物と被検物質を接触させ、PGRP-LEキメラ分子密度に依存するシグナル増幅(DDSA)によるメラニン化(黒化)による発色反応を測定することによって、被検物質の存在を検出することを特徴とする。その概要を図1に示す。本発明の検出方法は分子密度依存シグナル増幅(DDSA)技術を利用するものである。即ち、PGRP-LEによるシグナルの活性化はリガンドと結合することによって該PGRP-LEの分子密度が上昇することによって生起する、という機構を利用するものであるので、本発明の検出方法は、特に、例えば、被検物質の多量体化等に因る存在状態(集合状態)の変化の検出、又は、被検物質として、例えば、様々な病態に関係するような、構造変換に伴い凝集化したタンパク質の特異的な検出に有利である。
【0024】
尚、本発明方法における検出対象である被検物質(リガンド)は、本発明のPGRP-LEキメラ分子のセンサー領域が特異的に認識して結合できる物質であれば、その種類に特に制限はなく、ポリペプチド並びに酵素及び抗体分子等のタンパク質、DNA又はRNA等の核酸分子、糖、若しくは脂質等の任意の種類の生体分子、又は、それらの断片又は一部の領域、酵素基質、及び低分子化合物等を例示することが出来る。尚、このような被検物質として、細胞、組織若しくは器官等の生体由来物質、又は、適当な材質からなる基板及びプレート等の適当な人工担体の表面上に固定又は結合等の任意の状態で存在しているものも含まれる。
【0025】
従って、本発明は更に、本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域と被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子を含む、上記の検出方法に使用する検出キットにも係る。該キットには、更に、カイコ等の昆虫の体液から調製されたフェノール酸化酵素前駆体カスケード因子含有試薬を含む本発明の組成物が含まれていることが好ましい。又、被検物質及び測定系の種類等に応じて、該キットには測定プレート等の適応な要素を更に含むことが出来る。
【0026】
以下、実施例に則して本発明を具体的に説明するが、本発明の技術的範囲はこれらの記載によって何等制限されるものではない。
【実施例1】
【0027】
PGRP-LEの2〜176アミノ酸からなる領域をコードするDNA配列とpAcG2T vector由来のGSTをコードする配列を制限酵素Bam HI認識配列で連結し、ペプチドグリカン認識タンパク質(PGRP)-LEのリガンド結合領域の一部(C末端側の177〜34番目のアミノ酸からなる領域)をGSTと置換することによって、本発明のPGRP-LEキメラ分子であるPGRP-LEとGSTとのキメラ分子(LEAD-GST)をコードする遺伝子を作製し、これをカイコ発現系vectorであるpM25 vectorあるいはpM07 vectorのクローニングサイトに挿入し、本遺伝子発現タンパク質をカイコ幼虫体液中に産生させることにより、本発明のキメラ分子を作製した。尚、これらのキメラ分子には検出用のタグ分子として、N末端にFLAGタグ又はHisタグが付加されている。”LEAD-“は、PGRP-LEのN末端側1〜176アミノ酸領域に相当する。その結果、産生されたキメラ分子の発現の様子を図2に示す。
【実施例2】
【0028】
次に、最終濃度100mM NaClとなる条件下、こうして調製したキメラ分子であるLEAD-GSTを発現させたカイコ体液と、発現させていないコントロール体液を、グルタチオンをプレート底面に固相化したプレート(グルタチオンプレート)、または通常のプレートに加え、これに等量のproPO系としてのSLP試薬(和光純薬工業株式会社)を加えて、30℃で75分反応させた後、proPO系の活性化を540nmにおける吸光度で測定した。その概要及び結果を図3に示す。この結果から、本発明の検出方法によって、プレート上で分子密度が上昇したLEAD-GSTの特異的な検出がワンステップで、簡便・効率的に行なうことが可能であることが示された。
【産業上の利用可能性】
【0029】
本発明の検出方法は、分子密度依存シグナル増幅(density-dependent signaling amplification: DDSA)を利用するものであり、このDDSA技術は、PCR又はELISA法等の従来の検出技術を補完する新たな増幅技術である。即ち、PCRはターゲットDNAの増幅に限定されるがDDSAはリガンド非特異的にシグナルの増幅が可能であるために、様々な種類のリガンド(被検物質)をターゲットにすることが可能となる。更に、分子密度依存的にシグナル増幅を行なうので、ELISA法のように非反応性の試薬を除去する必要がないワンステップの検出が可能である。
【0030】
従って、このようにDDSAに基づく本発明方法は、様々な対象を検出できる検出系として幅広い展開が期待できる。加えて、DDSA は、分子密度の上昇で活性化するため、検出する物質の集合状態などを識別できる可能性をも有している。例えば、異常型プリオンタンパク質、ポリグルタミン病での変異タンパク質、及びアミロイド等の、病態に関係して構造変換に伴い凝集化したタンパク質等の特異的検出への応用が期待できる(図4)。
【特許請求の範囲】
【請求項1】
本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域、及び被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子、及び、昆虫の体液から調製されたフェノール酸化酵素前駆体カスケード因子含有試薬を含む、メラニン化(黒化)反応により被検物質を検出するために組成物。
【請求項2】
PGRP-LEキメラ分子がペプチドグリカン認識タンパク質(PGRP)-LEにおけるリガンド結合領域の少なくとも一部がセンサー領域と置換されて成る、請求項1記載の組成物。
【請求項3】
PGRP-LEキメラ分子がPGRP-LEにおけるリガンド結合領域全体がセンサー領域と置換されて成る、請求項2記載の組成物。
【請求項4】
リガンド結合領域が配列番号2に示されるアミノ酸配列の173〜345番目のアミノ酸から成る、請求項2又3記載の組成物。
【請求項5】
PGRP-LEとセンサー領域がリンカーを介して結合して成る、請求項2〜4のいずれか一項に記載の組成物。
【請求項6】
センサー領域がポリペプチド、核酸及び低分子化合物から成る群から選択される物質である、請求項1〜5のいずれか一項に記載の組成物。
【請求項7】
フェノール酸化酵素前駆体カスケード因子含有試薬が、カイコの体液を無菌的に採取・調製して得られたものである、請求項1〜6のいずれか一項に記載の組成物。
【請求項8】
請求項1〜7のいずれか一項に記載の組成物と被検物質を接触させ、PGRP-LEキメラ分子密度に依存するシグナル増幅によるメラニン化(黒化)による発色反応を測定することから成る、被検物質を検出する方法。
【請求項9】
請求項1〜7のいずれか一項に記載の組成物と被検物質を接触させ、PGRP-LEキメラ分子密度に依存するシグナル増幅によるメラニン化(黒化)による発色反応を測定することから成る、被検物質の存在状態(集合状態)の変化を検出する方法。
【請求項10】
被検物質の存在状態の変化が被検物質の多量体化に因るものである、請求項9記載の検出方法。
【請求項11】
被検物質が凝集化タンパク質である、請求項9記載の検出方法。
【請求項12】
本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域と被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子を含む、請求項8〜11のいずれか一項に記載の検出方法に使用する検出キット。
【請求項1】
本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域、及び被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子、及び、昆虫の体液から調製されたフェノール酸化酵素前駆体カスケード因子含有試薬を含む、メラニン化(黒化)反応により被検物質を検出するために組成物。
【請求項2】
PGRP-LEキメラ分子がペプチドグリカン認識タンパク質(PGRP)-LEにおけるリガンド結合領域の少なくとも一部がセンサー領域と置換されて成る、請求項1記載の組成物。
【請求項3】
PGRP-LEキメラ分子がPGRP-LEにおけるリガンド結合領域全体がセンサー領域と置換されて成る、請求項2記載の組成物。
【請求項4】
リガンド結合領域が配列番号2に示されるアミノ酸配列の173〜345番目のアミノ酸から成る、請求項2又3記載の組成物。
【請求項5】
PGRP-LEとセンサー領域がリンカーを介して結合して成る、請求項2〜4のいずれか一項に記載の組成物。
【請求項6】
センサー領域がポリペプチド、核酸及び低分子化合物から成る群から選択される物質である、請求項1〜5のいずれか一項に記載の組成物。
【請求項7】
フェノール酸化酵素前駆体カスケード因子含有試薬が、カイコの体液を無菌的に採取・調製して得られたものである、請求項1〜6のいずれか一項に記載の組成物。
【請求項8】
請求項1〜7のいずれか一項に記載の組成物と被検物質を接触させ、PGRP-LEキメラ分子密度に依存するシグナル増幅によるメラニン化(黒化)による発色反応を測定することから成る、被検物質を検出する方法。
【請求項9】
請求項1〜7のいずれか一項に記載の組成物と被検物質を接触させ、PGRP-LEキメラ分子密度に依存するシグナル増幅によるメラニン化(黒化)による発色反応を測定することから成る、被検物質の存在状態(集合状態)の変化を検出する方法。
【請求項10】
被検物質の存在状態の変化が被検物質の多量体化に因るものである、請求項9記載の検出方法。
【請求項11】
被検物質が凝集化タンパク質である、請求項9記載の検出方法。
【請求項12】
本来のリガンド結合能を喪失させたペプチドグリカン認識タンパク質(PGRP)-LE領域と被検物質と特異的に反応するセンサー領域が結合して成るPGRP-LEキメラ分子を含む、請求項8〜11のいずれか一項に記載の検出方法に使用する検出キット。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2011−10638(P2011−10638A)
【公開日】平成23年1月20日(2011.1.20)
【国際特許分類】
【出願番号】特願2009−160130(P2009−160130)
【出願日】平成21年7月6日(2009.7.6)
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成16年度生物系特定産業技術研究支援センター「新技術・新分野創出のための基礎研究推進事業」、産業活力再生特別措置法第30条の適用を受ける特許出願
【出願人】(504157024)国立大学法人東北大学 (2,297)
【Fターム(参考)】
【公開日】平成23年1月20日(2011.1.20)
【国際特許分類】
【出願日】平成21年7月6日(2009.7.6)
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成16年度生物系特定産業技術研究支援センター「新技術・新分野創出のための基礎研究推進事業」、産業活力再生特別措置法第30条の適用を受ける特許出願
【出願人】(504157024)国立大学法人東北大学 (2,297)
【Fターム(参考)】
[ Back to top ]

