センサ収納容器
【課題】
外部からセンサが確認可能な、センサ収納容器を提供する。
【解決手段】
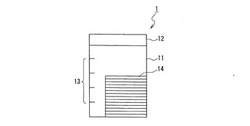
分析対象物を酸化若しくは還元させる酸化還元酵素と、酸化還元による電子の授受を媒介するメディエータと、前記酸化還元反応を検出する検出手段とを有するセンサ14を収納するための容器1であって、前記容器1の全部若しくは一部を透明若しくは半透明とし、前記容器外部から前記センサを確認可能にする。この容器1は、容器本体11と蓋12とから構成されていてもよく、容器本体11には目盛13があってもよい。前記センサとしては、ルテニウム金属錯体をメディエータとして使用したものが好ましい。
外部からセンサが確認可能な、センサ収納容器を提供する。
【解決手段】
分析対象物を酸化若しくは還元させる酸化還元酵素と、酸化還元による電子の授受を媒介するメディエータと、前記酸化還元反応を検出する検出手段とを有するセンサ14を収納するための容器1であって、前記容器1の全部若しくは一部を透明若しくは半透明とし、前記容器外部から前記センサを確認可能にする。この容器1は、容器本体11と蓋12とから構成されていてもよく、容器本体11には目盛13があってもよい。前記センサとしては、ルテニウム金属錯体をメディエータとして使用したものが好ましい。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、酸化還元反応により分析対象物を分析するためのセンサを収納するセンサ収納容器に関する。
【背景技術】
【0002】
従来、グルコース、コレステロール等の生体成分を分析するために、センサが汎用されている。例えば、グルコースセンサは、糖尿病患者の血糖値の自己管理に使用されている。グルコースセンサは、基板の上に作用極および参照極が形成され、この上にグルコースオキシダーゼおよびフェリシアン化カリウム等の試薬が配置された電極センサが一般的である。この電極センサを測定器にセットし、糖尿病患者が自己採血した血液を前記試薬部に付着させると、グルコースオキシダーゼによって、前記血液中のグルコースが酸化されることで電子の授受が起こり、これによる電流値の変化を前記一対の電極で捕らえ、その電流値の変化を前記測定器で測定して血糖値に換算して表示する。前記フェリシアン化カリウムは、酸化還元反応の電子の授受を媒介するものでメディエータと呼ばれ、この物質が電極との電子授受を行う。この電極とメディエータとの電子の授受の速度が速いため、その結果、測定速度も速まる。また、前記センサは、複数個で容器に収容されており、使用時に取り出される。
【0003】
しかしながら、前記センサの容器は、不透明であり、外からセンサの数量を把握できないため、センサの数量を確認するためには容器を開封しなければならず不便である。また確認のたびにセンサが外気に触れ、空気による酸化や湿気によりセンサが劣化するという問題があった。
【発明の概要】
【発明が解決しようとする課題】
【0004】
本発明は、このような事情に鑑みなされたもので、容器を開封することなくセンサの数量が外部から確認可能なセンサ収納容器の提供を、その目的とする。
【課題を解決するための手段】
【0005】
前記目的を達成するために、本発明の容器は、センサを収納するためのセンサ容器であって、その一部若しくは全部が透明若しくは半透明である容器である。
【発明の効果】
【0006】
本発明のセンサ収納容器によれば、外部からセンサの残量等を確認することができ便利であり、かつ、確認のたびに容器を開封することがないため、センサの劣化も抑制することができる。
【図面の簡単な説明】
【0007】
【図1】図1は、本発明の容器の一例の構成図である。
【図2】図2は、本発明の容器のその他の例の構成図である。
【図3】図3は、電極センサの構成の一例を示す断面図である。
【図4】図4は、比色センサの構成の一例を示す断面図である。
【図5A】図5Aは、それぞれ、本発明の容器のその他の構成の斜視図と断面図である。
【図5B】図5Bは、それぞれ、本発明の容器のその他の構成の斜視図と断面図である。
【発明を実施するための形態】
【0008】
本発明の容器において、収納されるセンサの種類は特に制限されず、耐光性があるものであっても、耐光性がないものであっても、いずれでもよい。耐光性があるセンサを収納する場合、透明若しくは半透明部分は、容器のどの部分に形成してもよい。
【0009】
なお、本発明において、透明若しくは半透明とは、外部からセンサを確認可能なものをいう。
【0010】
本発明の容器において、収納するセンサが、耐光性が無い場合、容器の底部のみが透明若しくは半透明であることが好ましい。このようにすれば、センサの確認のときのみ、底部からセンサを見ることができ、その他の時は、光の侵入を遮断できるため、センサの劣化をより防止できる。
【0011】
また、本発明の容器において、前記センサの数量を測定するための目盛を有することが好ましい。目盛があれば、センサの数量が、正確にわかるからである。なお、容器の底部のみが透明若しくは半透明である場合は、底部に目盛を有していることがより好ましい。本発明の容器は、容器本体と蓋とから構成されていてもよい。
【0012】
本発明の容器の材質は特に制限されないが、容器の半透明若しくは透明である部分には、半透明若しくは透明な材質を使用する。半透明の材質としては、例えば、ベークライト、フェノール樹脂、ポリエチレン、ポリスルホン、ポリカーボネート、ABS樹脂、ポリプロピレン、塩化ビニル、エポキシ樹脂等があり、このなかで、ポリエチレン、ポリプロピレン、塩化ビニルが好ましく、ポリエチレン、ポリプロピレンが特に好ましい。また、後述の透明材質に、例えば、顔料等の添加剤を加えることにより半透明に加工することもできる。前記透明材質としては、例えば、アクリル樹脂、ポリカーボネート、ポリスルホン、ABS樹脂、ポリエチレン、ポリプロピレン、塩化ビニル、エポキシ樹脂等があり、このなかで、ポリエチレン、ポリプロピレン、塩化ビニルが好ましく、特に好ましいのはポリプロピレンである。
【0013】
また、前記透明材質に、紫外線吸収剤を添加してもよい。前記紫外線吸収剤としては、例えば、2(2’−ヒドロキシ−5’−メチルフェニル)ベンゾトリアゾール、2(2’−ヒドロキシ−3’−t−ブチル−5’−メチルフェニル)5クロロベンゾトリアゾール、2(2’−ヒドロキシ−3’5−ジ−t−ブチルフェニル)5クロロベンゾトリアゾール、2−ヒドロキシ−4−n−オクトキシ−ベンゾフェノン、サリチル酸フェニル等があげられる。
【0014】
なお、本発明において、透明若しくは半透明の材質とは、その素材を通して外部からセンサを確認可能なものをいう。
【0015】
本発明の容器において、透明若しくは半透明の部分が着色されていてもよく、着色の色は、例えば、黒、グレー、ブラウン、青、緑、赤、黄、白があげられ、好ましくは黒、グレー、ブラウン、青、黄であり、より好ましくは黒、グレー、ブラウンである。このように着色することにより、耐光性に乏しいセンサの劣化を防止することが可能となる。
【0016】
本発明の容器において、透明若しくは半透明以外の部分の材質は、特に制限されず、例えば、上述の透明若しくは半透明の材質を使用でき、例えば、ベークライト、フェノール樹脂、ポリエチレン、アクリル樹脂、ポリカーボネート、ポリスルホン、ABS樹脂、ポリプロピレン、塩化ビニル、エポキシ樹脂等が使用できる。
【0017】
本発明の容器の形状は、特に制限されず、例えば、直方体形状、立方体形状、円柱形状、楕円柱形状等があり、センサの形状や大きさ等の諸条件により適宜決定される。本発明の容器のサイズも特に制限されず、センサの形状や大きさ等の諸条件により適宜決定される。例えば、容器の形状が直方体形状の場合、その大きさは、例えば、縦15mm〜50mm×横15mm〜50mm×高さ30mm〜100mmであり、好ましくは、縦20mm〜40mm×横20mm〜40mm×高さ40mm〜80mmであり、より好ましくは、縦30mm〜35mm×横30mm〜35mm×高さ45mm〜55mmである。
【0018】
本発明の容器の一例を、図1に示す。図示のように、このセンサ収納容器1は、容器本体11と蓋12とから構成され、前記容器本体11全体が半透明若しくは透明である。また、前記容器本体11側面には、高さ方向に目盛13がある。図中の14は、収納された複数のセンサを示す。また、目盛を容器底部につけた例を図2に示す。図示のように、このセンサ収納容器2は、容器本体21と蓋22とから構成され、前記容器本体21全体が透明若しくは半透明である。また、前記容器本体21の底部に目盛がある。この容器では、センサの数量を確認する場合は、容器を横にすればよい。図2において、24は、収納された複数のセンサを示す。
【0019】
本発明の容器のその他の例を、図5の斜視図(同図上)および断面図(同図下)に示す。図示のように、この容器5は、容器本体51(透明若しくは半透明)と、上蓋52と、底蓋54とから構成されている。容器本体51の上部には、円状開口53が設けられており、上蓋52の円環状突起部と嵌合可能となっている。また、容器本体51底部は、その全体が開口しており、底蓋54によって、閉口されている。この容器5においても、センサの数量を確認するための目盛を設けてもよい。このような形状の容器の大きさは、特に制限されず、例えば、幅15mm〜50mm×長さ15mm〜50mm×高さ30mm〜100mmであり、好ましくは、幅20mm〜40mm×長さ20mm〜40mm×高さ40mm〜80mmであり、より好ましくは、幅30mm〜35mm×長さ30mm〜35mm×高さ45mm〜55mmである。
【0020】
本発明の容器の製造方法は、特に制限されず、例えば、以下に示すように作製できる。例えば、底部のみが透明の容器を作製する方法としては、遮光性の顔料により着色した胴部と透明若しくは半透明の底部とを、それぞれ別部品として射出成形により作製し、それらを接着する方法、胴部と底部とを射出成形により2色成形し、その成形物を2軸延伸ブロー成形等により成形する方法、全体が透明若しくは半透明の容器を作製し、そして着色したシュリンクフィルムを底部以外に貼り付ける方法等があげられる。前記接着方法は、特に制限されないが、例えば、超音波溶着、熱溶着、接着剤、溶剤等により行うことができ、この中でも超音波溶着が好ましい。また、前記シュリンクフィルムの材質は、特に制限されず、例えば、ポリエチレン、ポリプロピレン、塩化ビニルが使用できる。
【0021】
つぎに、本発明に収納されるセンサの一例について説明する。
【0022】
本発明の容器に収納されるセンサは、例えば、酸化還元酵素と、酸化還元による電子の授受を媒介するメディエータと、前記酸化還元反応を検出する検出手段とを有する。
【0023】
前記センサは、光に対する耐性(耐光性)を有することが好ましい。このセンサに光に対する耐性を付与するための具体的手段としては、例えば、メディエータとして、耐光性遷移金属錯体を使用することや、センサの構成材料として遮光性材料を用いることがあげられる。前記耐光性遷移金属錯体としては、例えば、銅錯体、鉄錯体、ルテニウム錯体およびオスミウム錯体があるが、このなかでも、ルテニウム錯体が好ましい。以下、銅錯体、鉄錯体、ルテニウム錯体およびオスミウム錯体について、具体的に説明する。なお、以下の錯体は、市販品を使用できるし、従来公知の方法で自家調製してもよい。
【0024】
(銅錯体)
銅錯体は、酵素からの電子伝達により、例えば、青色(Cu2+)から赤褐色(Cu+)に色調が変化する。銅錯体の配位子としては、例えば、ビピリジン、イミダゾール、アミノ酸、フェナントロリン、エチレンジアミン等の含窒素配位子があげられる。前記ビピリジン、イミダゾール、アミノ酸、エチレンジアミン、フェナントロリンを組み合わせて混合配位子としてもよい。
【0025】
配位子がビピリジンの場合、その配位数は、4若しくは6であるが、安定性の見地から、ビピリジンは2個配位させることが好ましい。ビピリジンは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、4、4'位および5、5'位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などのハロゲン基がある。
【0026】
ビピリジン銅錯体の例としては、例えば、[Cu(bipyridine)2]、[Cu(4,4'−dimethyl−2,2'−bipyridine)2]、[Cu(4,4'−diphenyl−2,2'−bipyridine)2]、[Cu(4,4'−diamino−2,2'−bipyridine)2]、[Cu(4,4'−dihydroxy−2,2'−bipyridine)2]、[Cu(4,4'−dicarboxy−2,2'−bipyridine)2]、[Cu(4,4'−dibromo−2,2'−bipyridine)2]、[Cu(5,5'−dimethyl−2,2'−bipyridine)2]、[Cu(5,5'−diphenyl−2,2'−bipyridine)2]、[Cu(5,5'−diamino−2,2'−bipyridine)2]、[Cu(5,5'−dihydroxy−2,2'−bipyridine)2]、[Cu(5,5'−dicarboxy−2,2'−bipyridine)2]、[Cu(5,5'−dibromo−2,2'−bipyridine)2]、[Cu(bipyridine)3]、[Cu(4,4'−dimethyl−2,2'−bipyridine)3]、[Cu(4,4'−diphenyl−2,2'−bipyridine)3]、[Cu(4,4'−diamino−2,2'−bipyridine)3]、[Cu(4,4'−dihydroxy−2,2'−bipyridine)3]、[Cu(4,4'−dicarboxy−2,2'−bipyridine)3]、[Cu(4,4'−dibromo−2,2'−bipyridine)3]、[Cu(5,5'−dimethyl−2,2'−bipyridine)3]、[Cu(5,5'−diphenyl−2,2'−bipyridine)3]、[Cu(5,5'−diamino−2,2'−bipyridine)3]、[Cu(5,5'−dihydroxy−2,2'−bipyridine)3]、[Cu(5,5'−dicarboxy−2,2'−bipyridine)3]、[Cu(5,5'−dibromo−2,2'−bipyridine)3]等がある。
【0027】
配位子がイミダゾールの場合、その配位数は、4である。イミダゾールは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、2位、4位および5位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などのハロゲン基がある。
【0028】
イミダゾール銅錯体の例としては、例えば、[Cu(imidazole)4]、[Cu(4−methyl−imidazole)4]、[Cu(4−phenyl−imidazole)4]、[Cu(4−amino−imidazole)4]、[Cu(4−hydroxy−imidazole)4]、[Cu(4−carboxy−imidazole)4]、[Cu(4−bromo−imidazole)4]等がある。
【0029】
前記アミノ酸としては、例えば、アルギニン(L−Arg)がある。アルギニン銅錯体は、溶解性が高いという利点を持つ。また、混合配位子として、例えば、ビピリジンとイミダゾールとの組み合わせ、ビピリジンとアミノ酸との組み合わせがあり、具体例としては、[Cu(imidazole)2(bipyridine)]、[Cu(L−Arg)2(bipyridine)]がある。混合配位子を用いると銅錯体に様々な性質を付与でき、例えば、アルギニンを用いると錯体の溶解性が向上する。
【0030】
(鉄錯体)
鉄錯体は、酵素からの電子伝達により、例えば、黄色系(Fe3+)から赤色系(Fe2+)に色調が変化する。鉄錯体の配位子としては、例えば、ビピリジン、イミダゾール、アミノ酸、フェナントロリン、エチレンジアミン等の含窒素配位子があげられる。前記ビピリジン、イミダゾール、アミノ酸、フェナントロリン、エチレンジアミンを組み合わせて混合配位子としてもよい。
【0031】
配位子がビピリジンの場合、その配位数は、6である。ビピリジンは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、4、4'位および5、5'位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などハロゲン基がある。
【0032】
ビピリジン鉄錯体の例としては、例えば、[Fe(bipyridine)3]、[Fe(4,4'−dimethyl−2,2'−bipyridine)3]、[Fe(4,4'−diphenyl−2,2'−bipyridine)3]、[Fe(4,4'−diamino−2,2'−bipyridine)3]、[Fe(4,4'−dihydroxy−2,2'−bipyridine)3]、[Fe(4,4'−dicarboxy−2,2'−bipyridine)3]、[Fe(4,4'−dibromo−2,2'−bipyridine)3]、[Fe(5,5'−dimethyl−2,2'−bipyridine)3]、[Fe(5,5'−diphenyl−2,2'−bipyridine)3]、[Fe(5,5'−diamino−2,2'−bipyridine)3]、[Fe(5,5'−dihydroxy−2,2'−bipyridine)3]、[Fe(5,5'−dicarboxy−2,2'−bipyridine)3]、[Fe(5,5'−dibromo−2,2'−bipyridine)3]等がある。
【0033】
配位子がイミダゾールの場合、その配位数は、6である。イミダゾールは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、2位、4位および5位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などのハロゲン基がある。
【0034】
イミダゾール鉄錯体の例としては、例えば、[Fe(imidazole)6]、[Fe(4−methyl−imidazole)6]、[Fe(4−phenyl−imidazole)6]、[Fe(4−amino−imidazole)6]、[Fe(4−hydroxy−imidazole)6]、[Fe(4−carboxy−imidazole)6]、[Fe(4−bromo−imidazole)6]等がある。
【0035】
前記アミノ酸としては、例えば、アルギニン(L−Arg)がある。アルギニン鉄錯体は、溶解性が高いという利点を一般的に持つ。また、混合配位子として、例えば、ビピリジンとイミダゾールの組み合わせ、ビピリジンとアミノ酸の組み合わせがあり、具体例としては、[Fe(imidazole)2(bipyridine)2]、[Fe(L−Arg)2(bipyridine)2]がある。混合配位子を用いると錯体に様々な性質を付与でき、例えば、アルギニンを用いると錯体の溶解性が向上する。
【0036】
(ルテニウム錯体)
ルテニウム錯体の配位子としては、例えば、ビピリジン、イミダゾール、アミノ酸、フェナントロリン、エチレンジアミン等の含窒素配位子があげられる。前記ビピリジン、イミダゾール、アミノ酸、フェナントロリン,エチレンジアミンを組み合わせて混合配位子としてもよい。
【0037】
配位子がビピリジンの場合、配位数は、6である。ビピリジンは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、4、4’位および5、5’位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などハロゲン基がある。
【0038】
ビピリジンルテニウム錯体の例としては、例えば、[Ru(bipyridine)3]、[Ru(4,4'−dimethyl−2,2'−bipyridine)3]、[Ru(4,4'−diphenyl−2,2'−bipyridine)3]、[Ru(4,4'−diamino−2,2'−bipyridine)3]、[Ru(4,4'−dihydroxy−2,2'−bipyridine)3]、[Ru(4,4'−dicarboxy−2,2'−bipyridine)3]、[Ru(4,4'−dibromo−2,2'−bipyridine)3]、[Ru(5,5'−dimethyl−2,2'−bipyridine)3]、[Ru(5,5'−diphenyl−2,2'−bipyridine)3]、[Ru(5,5'−diamino−2,2'−bipyridine)3]、[Ru(5,5'−dihydroxy−2,2'−bipyridine)3]、[Ru(5,5'−dicarboxy−2,2'−bipyridine)3]、[Ru(5,5'−dibromo−2,2'−bipyridine)3]等がある。
【0039】
配位子がイミダゾールの場合、配位数は、6である。イミダゾールは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、2位、4位および5位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などハロゲン基がある。
【0040】
イミダゾールルテニウム錯体の例としては、例えば、[Ru(imidazole)6]、[Ru(4−methyl−imidazole)6]、[Ru(4−phenyl−imidazole)6]、[Ru(4−amino−imidazole)6]、[Ru(4−hydroxy−imidazole)6]、[Ru(4−carboxy−imidazole)6]、[Ru(4−bromo−imidazole)6]等がある。
【0041】
前記アミノ酸としては、例えば、アルギニン(L−Arg)がある。アルギニンルテニウム錯体は、溶解性が高いという利点を持つ。また、混合配位子として、例えば、ビピリジンとイミダゾールの組み合わせ、ビピリジンとアミノ酸の組み合わせがあり、具体例としては、[Ru(imidazole)2(bipyridine)2]、[Ru(L−Arg)2(bipyridine)2]がある。混合配位子を用いると錯体に様々な性質を付与でき、例えば、アルギニンを用いると錯体の溶解性が向上する。
【0042】
つぎに、前記センサに使用される酸化還元酵素は、特に制限されず、測定対象により適宜決定され、例えば、グルコースオキシダーゼ、グルコースデヒドロゲナーゼ、乳酸脱水素酵素、コレステロールオキシダーゼ等がある。
【0043】
つぎに、前記センサの前記酸化還元反応検出手段は、特に制限されず、例えば、電極センサの場合、前記酸化還元反応検出手段は、前記メディエータが酸化若しくは還元されることによりに生じる電流を検知する電極であり、比色センサの場合、前記酸化還元反応検出手段は、酸化若しくは還元により発色する色素である。
【0044】
前記センサの構成は、特に制限されず、一般的な構成が採用できる。
【0045】
まず、電極センサの基本的な構成例を、図3に示す。図示のように、この電極センサ3では、基板31の上に、一対の電極(作用極32と参照極33)が形成され、その上に、酸化還元酵素およびメディエータを含む試薬層が形成されている。この電極センサは、本発明の容器に収納されており、使用時に取り出して測定器にセットされる。そして、測定対象試料を前記試薬層34に付着させれば、前記酸化還元酵素によって酸化還元反応がおこり、これを電流値の変化として前記電極32,33でとらえ、前記測定器で所定の成分濃度に変換して表示する。
【0046】
図4に、比色センサの基本的な構成例を示す。図示のように、この比色センサ4では、基板41の上に、酸化還元酵素、発色剤(前記酵素の基質)およびメディエータを含む試薬層42が形成されている。この比色センサは、使用時に本発明の容器から取り出だされ、そして、測定対象試料を前記試薬層42に付着させれば、前記酸化還元酵素によって酸化還元反応がおこり、前記発色剤が発色する。この発色の程度を、分光光度計等の光学測定装置で測定して所定の成分濃度に換算する。
【0047】
前記センサにおいて、試薬層34、42は、その他の成分を含有していてもよく、例えば、親水性ポリマー、緩衝剤、安定剤等を含有していてもよい。
つぎに、本発明の実施例について説明する。
【実施例1】
【0048】
(透明容器)
図5に示す容器であって、全体が透明である容器を、材料としてポリプロピレンを用い、射出成型で作製した。この容器の全体大きさは、幅20mm×長さ40mm×高さ55mmであり、上部円形開口の内径は16mmである。
【0049】
(底部のみ透明の容器)
図5に示す容器であって、底部のみを透明とした容器を、材料としてポリプロピレンを用い、遮光性の胴部と透明の底部とを別部品として射出成形により作製し、それらを超音波溶着により接着することにより作製した。この容器の全体大きさは、幅20mm×長さ40mm×高さ55mmであり、上部円形開口の内径は16mmである。
【0050】
前記透明容器および底部のみ透明の容器に、メディエータとしてルテニウム錯体を使用したグルコース電極センサ若しくはフェリシアン化カリウムを使用したグルコース電極センサを入れて室内で4日間放置し、その後、グルコース溶液の濃度を測定した。さらに、容器の対照として、遮光ボトルに前記両センサを入れて、前記と同様にしてグルコース溶液の濃度を測定した。これらの結果を、下記の表2から表5に示す。なお、底部のみ透明の容器は、底部を下にして立てて放置した。前記両電極センサは、以下の方法で製造した。また、グルコース溶液の濃度の測定は、下記の条件で行った。
【0051】
(グルコース電極センサの作製)
グルコース電極センサとして、基板上に、第1電極、第2電極、試薬層、およびキャピラリが形成されたものを作製した。第1電極および第2電極は、基板上にカーボンインクをスクリーン印刷した後に乾燥させることにより形成した。キャピラリの容積は、0.3μLに設定した。試薬層は、電子伝達層(メディエータ層)および酵素含有層からなる2層構造とした。電子伝達層は、基板上に電子伝達物質(メディエータ:ルテニウム錯体若しくはフェリシアン化カリウム)を含む第1材料液0.4μLを塗布した後、これを送風乾燥(30℃、10%Rh)することにより形成した。酵素含有層は、電子伝達層上に、酸化還元酵素を含む第2材料液0.3μLを塗布した後、これを送風乾燥(30℃、10%Rh)することにより形成した。
【0052】
第1材料液は、下記表1の(1)〜(4)を番号通りの順序で混合した混合液を1から3日放置した後、この混合液に電子伝達物質を添加することにより調製した。第2材料液は、酸化還元酵素を0.1%CHAPSに溶解させることにより調製した。
【0053】
【表1】

【0054】
前記表1において、SWNはルーセントタイトであり、CHAPSは3−[(3−choamidopropyl)dimethylammonio]−1−propanesulfonateであり、ACESはN−(2−acetamido)−2−aminoetanesulfonic acidである。SWNは、コープケミカル(株)の製品番号「3150」を使用し、CHAPSは、同仁化学研究所の製品番号「KC062」を使用し、ACESは、同仁化学研究所の製品番号「ED067」を使用した。なお、ACES溶液はpHが7.5となるように調製した。
【0055】
ルテニウム(Ru)錯体としては、[Ru(NH3)6]Cl3(同仁化学研究所製「LM722」)を使用した。フェリシアン化カリウム(K3[Fe(III)(CN)6])としては、ナカライテスク(株)製「28637−75」)を使用した。酸化還元酵素としては、CyGDHを使用した。CyGDHは、αサブユニット、βサブユニットおよびγサブユニットからなるものである。
【0056】
(グルコース溶液濃度の測定)
測定器(テスター)に前記電極センサをセットし、0mg/dL(デシリットル)と600mg/dLとの二種類の濃度のグルコース溶液を測定した。なお、測定値は、電極に定電位(200mV)を印加10秒後の電流値(μA)である。
【0057】
【表2】

【0058】
【表3】

【0059】
【表4】

【0060】
【表5】

【0061】
前記表2から表5に示すように、フェリシアン化カリウム使用電極センサを透明容器に入れて室内で4日間放置すると、フェリシアン化カリウムが、光によってフェロシアン化カリウムに変化し、Back Ground電流(グルコース濃度0mg/dLの時の電流)の大幅な増加が確認された。これは、グルコース濃度換算で、+50%もの正誤差を生ずることを意味する。また、底部のみが透明の容器に入れて放置した場合、Back Ground電流の増加は見られず、正誤差を生ずることなく正確に測定でき、かつ、測定値のばらつきが少なかった。一方、ルテニウム錯体使用電極センサでは、透明容器に入れて放置しても、Back Ground電流の増加はなく、正誤差を生ずることなく正確に測定でき、かつ、測定値のばらつきが少なかった。
【実施例2】
【0062】
以下に示すようにして2種類の容器を作製し、それを用いて、実施例1と同様にしてグルコース溶液濃度の測定を行った。その結果を下記の表6から表9に示す。
【0063】
(底部のみ半透明)
図5に示す容器であって、底部のみを半透明とした容器を、材料としてポリプロピレンを用い、底部のみ透明の容器と同様にして作製した。なお、底部を作製するにあたって、まず、顔料(カーボンブラック)を用いて、濃い目の黒色に色調したカラーペレットを作製した(ペレット中の顔料の割合;20重量%)。センサ数が確認可能な限界点となるように、そのカラーペレットと無色のカラーペレットとを混合比5:100で混合し、それを用いて底部を作製した。この容器の全体大きさは、幅20mm×長さ40mm×高さ55mmであり、上部円形開口の内径は16mmである。
【0064】
(底部のみ透明(紫外線吸収剤添加))
図5に示す容器であって、底部のみ透明(紫外線吸収剤添加)とした容器を、材料としてポリプロピレンを用い、底部のみ透明の容器と同様にして作製した。なお、底部には、前記材料に2(2'−ヒドロキシ−5'−メチルフェニル)ベンゾトリアゾール(3重量%)を加えたものを使用した。この容器の全体大きさは、幅20mm×長さ40mm×高さ55mmであり、上部円形開口の内径は16mmである。
【0065】
【表6】

【0066】
【表7】

【0067】
【表8】

【0068】
【表9】

【0069】
前記表6から表9に示すように、どちらの容器を使用した場合でも、フェリシアン化カリウム使用センサ、ルテニウム錯体使用センサのBack Ground電流の増加は見られず、正誤差を生ずることなく正確に測定でき、かつ、測定値のばらつきが少なかった。
【産業上の利用可能性】
【0070】
本発明の容器によれば、外部からセンサの残量等を確認することができ、便利である。
【技術分野】
【0001】
本発明は、酸化還元反応により分析対象物を分析するためのセンサを収納するセンサ収納容器に関する。
【背景技術】
【0002】
従来、グルコース、コレステロール等の生体成分を分析するために、センサが汎用されている。例えば、グルコースセンサは、糖尿病患者の血糖値の自己管理に使用されている。グルコースセンサは、基板の上に作用極および参照極が形成され、この上にグルコースオキシダーゼおよびフェリシアン化カリウム等の試薬が配置された電極センサが一般的である。この電極センサを測定器にセットし、糖尿病患者が自己採血した血液を前記試薬部に付着させると、グルコースオキシダーゼによって、前記血液中のグルコースが酸化されることで電子の授受が起こり、これによる電流値の変化を前記一対の電極で捕らえ、その電流値の変化を前記測定器で測定して血糖値に換算して表示する。前記フェリシアン化カリウムは、酸化還元反応の電子の授受を媒介するものでメディエータと呼ばれ、この物質が電極との電子授受を行う。この電極とメディエータとの電子の授受の速度が速いため、その結果、測定速度も速まる。また、前記センサは、複数個で容器に収容されており、使用時に取り出される。
【0003】
しかしながら、前記センサの容器は、不透明であり、外からセンサの数量を把握できないため、センサの数量を確認するためには容器を開封しなければならず不便である。また確認のたびにセンサが外気に触れ、空気による酸化や湿気によりセンサが劣化するという問題があった。
【発明の概要】
【発明が解決しようとする課題】
【0004】
本発明は、このような事情に鑑みなされたもので、容器を開封することなくセンサの数量が外部から確認可能なセンサ収納容器の提供を、その目的とする。
【課題を解決するための手段】
【0005】
前記目的を達成するために、本発明の容器は、センサを収納するためのセンサ容器であって、その一部若しくは全部が透明若しくは半透明である容器である。
【発明の効果】
【0006】
本発明のセンサ収納容器によれば、外部からセンサの残量等を確認することができ便利であり、かつ、確認のたびに容器を開封することがないため、センサの劣化も抑制することができる。
【図面の簡単な説明】
【0007】
【図1】図1は、本発明の容器の一例の構成図である。
【図2】図2は、本発明の容器のその他の例の構成図である。
【図3】図3は、電極センサの構成の一例を示す断面図である。
【図4】図4は、比色センサの構成の一例を示す断面図である。
【図5A】図5Aは、それぞれ、本発明の容器のその他の構成の斜視図と断面図である。
【図5B】図5Bは、それぞれ、本発明の容器のその他の構成の斜視図と断面図である。
【発明を実施するための形態】
【0008】
本発明の容器において、収納されるセンサの種類は特に制限されず、耐光性があるものであっても、耐光性がないものであっても、いずれでもよい。耐光性があるセンサを収納する場合、透明若しくは半透明部分は、容器のどの部分に形成してもよい。
【0009】
なお、本発明において、透明若しくは半透明とは、外部からセンサを確認可能なものをいう。
【0010】
本発明の容器において、収納するセンサが、耐光性が無い場合、容器の底部のみが透明若しくは半透明であることが好ましい。このようにすれば、センサの確認のときのみ、底部からセンサを見ることができ、その他の時は、光の侵入を遮断できるため、センサの劣化をより防止できる。
【0011】
また、本発明の容器において、前記センサの数量を測定するための目盛を有することが好ましい。目盛があれば、センサの数量が、正確にわかるからである。なお、容器の底部のみが透明若しくは半透明である場合は、底部に目盛を有していることがより好ましい。本発明の容器は、容器本体と蓋とから構成されていてもよい。
【0012】
本発明の容器の材質は特に制限されないが、容器の半透明若しくは透明である部分には、半透明若しくは透明な材質を使用する。半透明の材質としては、例えば、ベークライト、フェノール樹脂、ポリエチレン、ポリスルホン、ポリカーボネート、ABS樹脂、ポリプロピレン、塩化ビニル、エポキシ樹脂等があり、このなかで、ポリエチレン、ポリプロピレン、塩化ビニルが好ましく、ポリエチレン、ポリプロピレンが特に好ましい。また、後述の透明材質に、例えば、顔料等の添加剤を加えることにより半透明に加工することもできる。前記透明材質としては、例えば、アクリル樹脂、ポリカーボネート、ポリスルホン、ABS樹脂、ポリエチレン、ポリプロピレン、塩化ビニル、エポキシ樹脂等があり、このなかで、ポリエチレン、ポリプロピレン、塩化ビニルが好ましく、特に好ましいのはポリプロピレンである。
【0013】
また、前記透明材質に、紫外線吸収剤を添加してもよい。前記紫外線吸収剤としては、例えば、2(2’−ヒドロキシ−5’−メチルフェニル)ベンゾトリアゾール、2(2’−ヒドロキシ−3’−t−ブチル−5’−メチルフェニル)5クロロベンゾトリアゾール、2(2’−ヒドロキシ−3’5−ジ−t−ブチルフェニル)5クロロベンゾトリアゾール、2−ヒドロキシ−4−n−オクトキシ−ベンゾフェノン、サリチル酸フェニル等があげられる。
【0014】
なお、本発明において、透明若しくは半透明の材質とは、その素材を通して外部からセンサを確認可能なものをいう。
【0015】
本発明の容器において、透明若しくは半透明の部分が着色されていてもよく、着色の色は、例えば、黒、グレー、ブラウン、青、緑、赤、黄、白があげられ、好ましくは黒、グレー、ブラウン、青、黄であり、より好ましくは黒、グレー、ブラウンである。このように着色することにより、耐光性に乏しいセンサの劣化を防止することが可能となる。
【0016】
本発明の容器において、透明若しくは半透明以外の部分の材質は、特に制限されず、例えば、上述の透明若しくは半透明の材質を使用でき、例えば、ベークライト、フェノール樹脂、ポリエチレン、アクリル樹脂、ポリカーボネート、ポリスルホン、ABS樹脂、ポリプロピレン、塩化ビニル、エポキシ樹脂等が使用できる。
【0017】
本発明の容器の形状は、特に制限されず、例えば、直方体形状、立方体形状、円柱形状、楕円柱形状等があり、センサの形状や大きさ等の諸条件により適宜決定される。本発明の容器のサイズも特に制限されず、センサの形状や大きさ等の諸条件により適宜決定される。例えば、容器の形状が直方体形状の場合、その大きさは、例えば、縦15mm〜50mm×横15mm〜50mm×高さ30mm〜100mmであり、好ましくは、縦20mm〜40mm×横20mm〜40mm×高さ40mm〜80mmであり、より好ましくは、縦30mm〜35mm×横30mm〜35mm×高さ45mm〜55mmである。
【0018】
本発明の容器の一例を、図1に示す。図示のように、このセンサ収納容器1は、容器本体11と蓋12とから構成され、前記容器本体11全体が半透明若しくは透明である。また、前記容器本体11側面には、高さ方向に目盛13がある。図中の14は、収納された複数のセンサを示す。また、目盛を容器底部につけた例を図2に示す。図示のように、このセンサ収納容器2は、容器本体21と蓋22とから構成され、前記容器本体21全体が透明若しくは半透明である。また、前記容器本体21の底部に目盛がある。この容器では、センサの数量を確認する場合は、容器を横にすればよい。図2において、24は、収納された複数のセンサを示す。
【0019】
本発明の容器のその他の例を、図5の斜視図(同図上)および断面図(同図下)に示す。図示のように、この容器5は、容器本体51(透明若しくは半透明)と、上蓋52と、底蓋54とから構成されている。容器本体51の上部には、円状開口53が設けられており、上蓋52の円環状突起部と嵌合可能となっている。また、容器本体51底部は、その全体が開口しており、底蓋54によって、閉口されている。この容器5においても、センサの数量を確認するための目盛を設けてもよい。このような形状の容器の大きさは、特に制限されず、例えば、幅15mm〜50mm×長さ15mm〜50mm×高さ30mm〜100mmであり、好ましくは、幅20mm〜40mm×長さ20mm〜40mm×高さ40mm〜80mmであり、より好ましくは、幅30mm〜35mm×長さ30mm〜35mm×高さ45mm〜55mmである。
【0020】
本発明の容器の製造方法は、特に制限されず、例えば、以下に示すように作製できる。例えば、底部のみが透明の容器を作製する方法としては、遮光性の顔料により着色した胴部と透明若しくは半透明の底部とを、それぞれ別部品として射出成形により作製し、それらを接着する方法、胴部と底部とを射出成形により2色成形し、その成形物を2軸延伸ブロー成形等により成形する方法、全体が透明若しくは半透明の容器を作製し、そして着色したシュリンクフィルムを底部以外に貼り付ける方法等があげられる。前記接着方法は、特に制限されないが、例えば、超音波溶着、熱溶着、接着剤、溶剤等により行うことができ、この中でも超音波溶着が好ましい。また、前記シュリンクフィルムの材質は、特に制限されず、例えば、ポリエチレン、ポリプロピレン、塩化ビニルが使用できる。
【0021】
つぎに、本発明に収納されるセンサの一例について説明する。
【0022】
本発明の容器に収納されるセンサは、例えば、酸化還元酵素と、酸化還元による電子の授受を媒介するメディエータと、前記酸化還元反応を検出する検出手段とを有する。
【0023】
前記センサは、光に対する耐性(耐光性)を有することが好ましい。このセンサに光に対する耐性を付与するための具体的手段としては、例えば、メディエータとして、耐光性遷移金属錯体を使用することや、センサの構成材料として遮光性材料を用いることがあげられる。前記耐光性遷移金属錯体としては、例えば、銅錯体、鉄錯体、ルテニウム錯体およびオスミウム錯体があるが、このなかでも、ルテニウム錯体が好ましい。以下、銅錯体、鉄錯体、ルテニウム錯体およびオスミウム錯体について、具体的に説明する。なお、以下の錯体は、市販品を使用できるし、従来公知の方法で自家調製してもよい。
【0024】
(銅錯体)
銅錯体は、酵素からの電子伝達により、例えば、青色(Cu2+)から赤褐色(Cu+)に色調が変化する。銅錯体の配位子としては、例えば、ビピリジン、イミダゾール、アミノ酸、フェナントロリン、エチレンジアミン等の含窒素配位子があげられる。前記ビピリジン、イミダゾール、アミノ酸、エチレンジアミン、フェナントロリンを組み合わせて混合配位子としてもよい。
【0025】
配位子がビピリジンの場合、その配位数は、4若しくは6であるが、安定性の見地から、ビピリジンは2個配位させることが好ましい。ビピリジンは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、4、4'位および5、5'位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などのハロゲン基がある。
【0026】
ビピリジン銅錯体の例としては、例えば、[Cu(bipyridine)2]、[Cu(4,4'−dimethyl−2,2'−bipyridine)2]、[Cu(4,4'−diphenyl−2,2'−bipyridine)2]、[Cu(4,4'−diamino−2,2'−bipyridine)2]、[Cu(4,4'−dihydroxy−2,2'−bipyridine)2]、[Cu(4,4'−dicarboxy−2,2'−bipyridine)2]、[Cu(4,4'−dibromo−2,2'−bipyridine)2]、[Cu(5,5'−dimethyl−2,2'−bipyridine)2]、[Cu(5,5'−diphenyl−2,2'−bipyridine)2]、[Cu(5,5'−diamino−2,2'−bipyridine)2]、[Cu(5,5'−dihydroxy−2,2'−bipyridine)2]、[Cu(5,5'−dicarboxy−2,2'−bipyridine)2]、[Cu(5,5'−dibromo−2,2'−bipyridine)2]、[Cu(bipyridine)3]、[Cu(4,4'−dimethyl−2,2'−bipyridine)3]、[Cu(4,4'−diphenyl−2,2'−bipyridine)3]、[Cu(4,4'−diamino−2,2'−bipyridine)3]、[Cu(4,4'−dihydroxy−2,2'−bipyridine)3]、[Cu(4,4'−dicarboxy−2,2'−bipyridine)3]、[Cu(4,4'−dibromo−2,2'−bipyridine)3]、[Cu(5,5'−dimethyl−2,2'−bipyridine)3]、[Cu(5,5'−diphenyl−2,2'−bipyridine)3]、[Cu(5,5'−diamino−2,2'−bipyridine)3]、[Cu(5,5'−dihydroxy−2,2'−bipyridine)3]、[Cu(5,5'−dicarboxy−2,2'−bipyridine)3]、[Cu(5,5'−dibromo−2,2'−bipyridine)3]等がある。
【0027】
配位子がイミダゾールの場合、その配位数は、4である。イミダゾールは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、2位、4位および5位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などのハロゲン基がある。
【0028】
イミダゾール銅錯体の例としては、例えば、[Cu(imidazole)4]、[Cu(4−methyl−imidazole)4]、[Cu(4−phenyl−imidazole)4]、[Cu(4−amino−imidazole)4]、[Cu(4−hydroxy−imidazole)4]、[Cu(4−carboxy−imidazole)4]、[Cu(4−bromo−imidazole)4]等がある。
【0029】
前記アミノ酸としては、例えば、アルギニン(L−Arg)がある。アルギニン銅錯体は、溶解性が高いという利点を持つ。また、混合配位子として、例えば、ビピリジンとイミダゾールとの組み合わせ、ビピリジンとアミノ酸との組み合わせがあり、具体例としては、[Cu(imidazole)2(bipyridine)]、[Cu(L−Arg)2(bipyridine)]がある。混合配位子を用いると銅錯体に様々な性質を付与でき、例えば、アルギニンを用いると錯体の溶解性が向上する。
【0030】
(鉄錯体)
鉄錯体は、酵素からの電子伝達により、例えば、黄色系(Fe3+)から赤色系(Fe2+)に色調が変化する。鉄錯体の配位子としては、例えば、ビピリジン、イミダゾール、アミノ酸、フェナントロリン、エチレンジアミン等の含窒素配位子があげられる。前記ビピリジン、イミダゾール、アミノ酸、フェナントロリン、エチレンジアミンを組み合わせて混合配位子としてもよい。
【0031】
配位子がビピリジンの場合、その配位数は、6である。ビピリジンは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、4、4'位および5、5'位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などハロゲン基がある。
【0032】
ビピリジン鉄錯体の例としては、例えば、[Fe(bipyridine)3]、[Fe(4,4'−dimethyl−2,2'−bipyridine)3]、[Fe(4,4'−diphenyl−2,2'−bipyridine)3]、[Fe(4,4'−diamino−2,2'−bipyridine)3]、[Fe(4,4'−dihydroxy−2,2'−bipyridine)3]、[Fe(4,4'−dicarboxy−2,2'−bipyridine)3]、[Fe(4,4'−dibromo−2,2'−bipyridine)3]、[Fe(5,5'−dimethyl−2,2'−bipyridine)3]、[Fe(5,5'−diphenyl−2,2'−bipyridine)3]、[Fe(5,5'−diamino−2,2'−bipyridine)3]、[Fe(5,5'−dihydroxy−2,2'−bipyridine)3]、[Fe(5,5'−dicarboxy−2,2'−bipyridine)3]、[Fe(5,5'−dibromo−2,2'−bipyridine)3]等がある。
【0033】
配位子がイミダゾールの場合、その配位数は、6である。イミダゾールは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、2位、4位および5位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などのハロゲン基がある。
【0034】
イミダゾール鉄錯体の例としては、例えば、[Fe(imidazole)6]、[Fe(4−methyl−imidazole)6]、[Fe(4−phenyl−imidazole)6]、[Fe(4−amino−imidazole)6]、[Fe(4−hydroxy−imidazole)6]、[Fe(4−carboxy−imidazole)6]、[Fe(4−bromo−imidazole)6]等がある。
【0035】
前記アミノ酸としては、例えば、アルギニン(L−Arg)がある。アルギニン鉄錯体は、溶解性が高いという利点を一般的に持つ。また、混合配位子として、例えば、ビピリジンとイミダゾールの組み合わせ、ビピリジンとアミノ酸の組み合わせがあり、具体例としては、[Fe(imidazole)2(bipyridine)2]、[Fe(L−Arg)2(bipyridine)2]がある。混合配位子を用いると錯体に様々な性質を付与でき、例えば、アルギニンを用いると錯体の溶解性が向上する。
【0036】
(ルテニウム錯体)
ルテニウム錯体の配位子としては、例えば、ビピリジン、イミダゾール、アミノ酸、フェナントロリン、エチレンジアミン等の含窒素配位子があげられる。前記ビピリジン、イミダゾール、アミノ酸、フェナントロリン,エチレンジアミンを組み合わせて混合配位子としてもよい。
【0037】
配位子がビピリジンの場合、配位数は、6である。ビピリジンは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、4、4’位および5、5’位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などハロゲン基がある。
【0038】
ビピリジンルテニウム錯体の例としては、例えば、[Ru(bipyridine)3]、[Ru(4,4'−dimethyl−2,2'−bipyridine)3]、[Ru(4,4'−diphenyl−2,2'−bipyridine)3]、[Ru(4,4'−diamino−2,2'−bipyridine)3]、[Ru(4,4'−dihydroxy−2,2'−bipyridine)3]、[Ru(4,4'−dicarboxy−2,2'−bipyridine)3]、[Ru(4,4'−dibromo−2,2'−bipyridine)3]、[Ru(5,5'−dimethyl−2,2'−bipyridine)3]、[Ru(5,5'−diphenyl−2,2'−bipyridine)3]、[Ru(5,5'−diamino−2,2'−bipyridine)3]、[Ru(5,5'−dihydroxy−2,2'−bipyridine)3]、[Ru(5,5'−dicarboxy−2,2'−bipyridine)3]、[Ru(5,5'−dibromo−2,2'−bipyridine)3]等がある。
【0039】
配位子がイミダゾールの場合、配位数は、6である。イミダゾールは、置換してなくても良いし、置換基を導入してもよい。置換基を導入することにより、例えば、溶解度や酸化還元電位等を調整することが可能となる。置換位置としては、2位、4位および5位がある。前記置換基は、例えば、メチル基、エチル基、プロピル基等のアルキル基、フェニル基、アミノ基等のアミン基、ヒドロキシ基、メトキシ基、エトキシ基等のアルコキシル基、カルボキシル基および臭素、塩素、ヨウ素などハロゲン基がある。
【0040】
イミダゾールルテニウム錯体の例としては、例えば、[Ru(imidazole)6]、[Ru(4−methyl−imidazole)6]、[Ru(4−phenyl−imidazole)6]、[Ru(4−amino−imidazole)6]、[Ru(4−hydroxy−imidazole)6]、[Ru(4−carboxy−imidazole)6]、[Ru(4−bromo−imidazole)6]等がある。
【0041】
前記アミノ酸としては、例えば、アルギニン(L−Arg)がある。アルギニンルテニウム錯体は、溶解性が高いという利点を持つ。また、混合配位子として、例えば、ビピリジンとイミダゾールの組み合わせ、ビピリジンとアミノ酸の組み合わせがあり、具体例としては、[Ru(imidazole)2(bipyridine)2]、[Ru(L−Arg)2(bipyridine)2]がある。混合配位子を用いると錯体に様々な性質を付与でき、例えば、アルギニンを用いると錯体の溶解性が向上する。
【0042】
つぎに、前記センサに使用される酸化還元酵素は、特に制限されず、測定対象により適宜決定され、例えば、グルコースオキシダーゼ、グルコースデヒドロゲナーゼ、乳酸脱水素酵素、コレステロールオキシダーゼ等がある。
【0043】
つぎに、前記センサの前記酸化還元反応検出手段は、特に制限されず、例えば、電極センサの場合、前記酸化還元反応検出手段は、前記メディエータが酸化若しくは還元されることによりに生じる電流を検知する電極であり、比色センサの場合、前記酸化還元反応検出手段は、酸化若しくは還元により発色する色素である。
【0044】
前記センサの構成は、特に制限されず、一般的な構成が採用できる。
【0045】
まず、電極センサの基本的な構成例を、図3に示す。図示のように、この電極センサ3では、基板31の上に、一対の電極(作用極32と参照極33)が形成され、その上に、酸化還元酵素およびメディエータを含む試薬層が形成されている。この電極センサは、本発明の容器に収納されており、使用時に取り出して測定器にセットされる。そして、測定対象試料を前記試薬層34に付着させれば、前記酸化還元酵素によって酸化還元反応がおこり、これを電流値の変化として前記電極32,33でとらえ、前記測定器で所定の成分濃度に変換して表示する。
【0046】
図4に、比色センサの基本的な構成例を示す。図示のように、この比色センサ4では、基板41の上に、酸化還元酵素、発色剤(前記酵素の基質)およびメディエータを含む試薬層42が形成されている。この比色センサは、使用時に本発明の容器から取り出だされ、そして、測定対象試料を前記試薬層42に付着させれば、前記酸化還元酵素によって酸化還元反応がおこり、前記発色剤が発色する。この発色の程度を、分光光度計等の光学測定装置で測定して所定の成分濃度に換算する。
【0047】
前記センサにおいて、試薬層34、42は、その他の成分を含有していてもよく、例えば、親水性ポリマー、緩衝剤、安定剤等を含有していてもよい。
つぎに、本発明の実施例について説明する。
【実施例1】
【0048】
(透明容器)
図5に示す容器であって、全体が透明である容器を、材料としてポリプロピレンを用い、射出成型で作製した。この容器の全体大きさは、幅20mm×長さ40mm×高さ55mmであり、上部円形開口の内径は16mmである。
【0049】
(底部のみ透明の容器)
図5に示す容器であって、底部のみを透明とした容器を、材料としてポリプロピレンを用い、遮光性の胴部と透明の底部とを別部品として射出成形により作製し、それらを超音波溶着により接着することにより作製した。この容器の全体大きさは、幅20mm×長さ40mm×高さ55mmであり、上部円形開口の内径は16mmである。
【0050】
前記透明容器および底部のみ透明の容器に、メディエータとしてルテニウム錯体を使用したグルコース電極センサ若しくはフェリシアン化カリウムを使用したグルコース電極センサを入れて室内で4日間放置し、その後、グルコース溶液の濃度を測定した。さらに、容器の対照として、遮光ボトルに前記両センサを入れて、前記と同様にしてグルコース溶液の濃度を測定した。これらの結果を、下記の表2から表5に示す。なお、底部のみ透明の容器は、底部を下にして立てて放置した。前記両電極センサは、以下の方法で製造した。また、グルコース溶液の濃度の測定は、下記の条件で行った。
【0051】
(グルコース電極センサの作製)
グルコース電極センサとして、基板上に、第1電極、第2電極、試薬層、およびキャピラリが形成されたものを作製した。第1電極および第2電極は、基板上にカーボンインクをスクリーン印刷した後に乾燥させることにより形成した。キャピラリの容積は、0.3μLに設定した。試薬層は、電子伝達層(メディエータ層)および酵素含有層からなる2層構造とした。電子伝達層は、基板上に電子伝達物質(メディエータ:ルテニウム錯体若しくはフェリシアン化カリウム)を含む第1材料液0.4μLを塗布した後、これを送風乾燥(30℃、10%Rh)することにより形成した。酵素含有層は、電子伝達層上に、酸化還元酵素を含む第2材料液0.3μLを塗布した後、これを送風乾燥(30℃、10%Rh)することにより形成した。
【0052】
第1材料液は、下記表1の(1)〜(4)を番号通りの順序で混合した混合液を1から3日放置した後、この混合液に電子伝達物質を添加することにより調製した。第2材料液は、酸化還元酵素を0.1%CHAPSに溶解させることにより調製した。
【0053】
【表1】

【0054】
前記表1において、SWNはルーセントタイトであり、CHAPSは3−[(3−choamidopropyl)dimethylammonio]−1−propanesulfonateであり、ACESはN−(2−acetamido)−2−aminoetanesulfonic acidである。SWNは、コープケミカル(株)の製品番号「3150」を使用し、CHAPSは、同仁化学研究所の製品番号「KC062」を使用し、ACESは、同仁化学研究所の製品番号「ED067」を使用した。なお、ACES溶液はpHが7.5となるように調製した。
【0055】
ルテニウム(Ru)錯体としては、[Ru(NH3)6]Cl3(同仁化学研究所製「LM722」)を使用した。フェリシアン化カリウム(K3[Fe(III)(CN)6])としては、ナカライテスク(株)製「28637−75」)を使用した。酸化還元酵素としては、CyGDHを使用した。CyGDHは、αサブユニット、βサブユニットおよびγサブユニットからなるものである。
【0056】
(グルコース溶液濃度の測定)
測定器(テスター)に前記電極センサをセットし、0mg/dL(デシリットル)と600mg/dLとの二種類の濃度のグルコース溶液を測定した。なお、測定値は、電極に定電位(200mV)を印加10秒後の電流値(μA)である。
【0057】
【表2】

【0058】
【表3】

【0059】
【表4】

【0060】
【表5】

【0061】
前記表2から表5に示すように、フェリシアン化カリウム使用電極センサを透明容器に入れて室内で4日間放置すると、フェリシアン化カリウムが、光によってフェロシアン化カリウムに変化し、Back Ground電流(グルコース濃度0mg/dLの時の電流)の大幅な増加が確認された。これは、グルコース濃度換算で、+50%もの正誤差を生ずることを意味する。また、底部のみが透明の容器に入れて放置した場合、Back Ground電流の増加は見られず、正誤差を生ずることなく正確に測定でき、かつ、測定値のばらつきが少なかった。一方、ルテニウム錯体使用電極センサでは、透明容器に入れて放置しても、Back Ground電流の増加はなく、正誤差を生ずることなく正確に測定でき、かつ、測定値のばらつきが少なかった。
【実施例2】
【0062】
以下に示すようにして2種類の容器を作製し、それを用いて、実施例1と同様にしてグルコース溶液濃度の測定を行った。その結果を下記の表6から表9に示す。
【0063】
(底部のみ半透明)
図5に示す容器であって、底部のみを半透明とした容器を、材料としてポリプロピレンを用い、底部のみ透明の容器と同様にして作製した。なお、底部を作製するにあたって、まず、顔料(カーボンブラック)を用いて、濃い目の黒色に色調したカラーペレットを作製した(ペレット中の顔料の割合;20重量%)。センサ数が確認可能な限界点となるように、そのカラーペレットと無色のカラーペレットとを混合比5:100で混合し、それを用いて底部を作製した。この容器の全体大きさは、幅20mm×長さ40mm×高さ55mmであり、上部円形開口の内径は16mmである。
【0064】
(底部のみ透明(紫外線吸収剤添加))
図5に示す容器であって、底部のみ透明(紫外線吸収剤添加)とした容器を、材料としてポリプロピレンを用い、底部のみ透明の容器と同様にして作製した。なお、底部には、前記材料に2(2'−ヒドロキシ−5'−メチルフェニル)ベンゾトリアゾール(3重量%)を加えたものを使用した。この容器の全体大きさは、幅20mm×長さ40mm×高さ55mmであり、上部円形開口の内径は16mmである。
【0065】
【表6】

【0066】
【表7】

【0067】
【表8】

【0068】
【表9】

【0069】
前記表6から表9に示すように、どちらの容器を使用した場合でも、フェリシアン化カリウム使用センサ、ルテニウム錯体使用センサのBack Ground電流の増加は見られず、正誤差を生ずることなく正確に測定でき、かつ、測定値のばらつきが少なかった。
【産業上の利用可能性】
【0070】
本発明の容器によれば、外部からセンサの残量等を確認することができ、便利である。
【特許請求の範囲】
【請求項1】
センサを収納するためのセンサ容器であって、その一部若しくは全部が透明若しくは半透明である容器。
【請求項2】
前記透明部に、前記センサの数量を測定するための目盛を有する請求項1記載の容器。
【請求項3】
容器本体と蓋とを含む請求項1記載の容器。
【請求項4】
前記センサが耐光性を有するセンサである請求項1記載の容器。
【請求項5】
前記耐光性を有するセンサが、酸化還元酵素と、酸化還元による電子の授受を媒介するメディエータと、前記酸化還元反応を検出する検出手段とを有し、前記メディエータが、耐光性遷移金属錯体である請求項4記載の容器。
【請求項6】
前記耐光性遷移金属錯体が、ルテニウム錯体である請求項5記載の容器。
【請求項7】
前記酸化還元反応検出手段が、前記メディエータが酸化若しくは還元されることによりに生じる電流を検知する電極であり、センサが電極センサである請求項5記載の容器。
【請求項8】
前記酸化還元反応検出手段が、酸化若しくは還元により発色する前記酸化還元酵素の基質であり、センサが比色センサである請求項5記載の容器。
【請求項9】
容器の底部のみが、透明若しくは半透明である請求項1記載の容器。
【請求項1】
センサを収納するためのセンサ容器であって、その一部若しくは全部が透明若しくは半透明である容器。
【請求項2】
前記透明部に、前記センサの数量を測定するための目盛を有する請求項1記載の容器。
【請求項3】
容器本体と蓋とを含む請求項1記載の容器。
【請求項4】
前記センサが耐光性を有するセンサである請求項1記載の容器。
【請求項5】
前記耐光性を有するセンサが、酸化還元酵素と、酸化還元による電子の授受を媒介するメディエータと、前記酸化還元反応を検出する検出手段とを有し、前記メディエータが、耐光性遷移金属錯体である請求項4記載の容器。
【請求項6】
前記耐光性遷移金属錯体が、ルテニウム錯体である請求項5記載の容器。
【請求項7】
前記酸化還元反応検出手段が、前記メディエータが酸化若しくは還元されることによりに生じる電流を検知する電極であり、センサが電極センサである請求項5記載の容器。
【請求項8】
前記酸化還元反応検出手段が、酸化若しくは還元により発色する前記酸化還元酵素の基質であり、センサが比色センサである請求項5記載の容器。
【請求項9】
容器の底部のみが、透明若しくは半透明である請求項1記載の容器。
【図1】


【図2】


【図3】


【図4】


【図5A】


【図5B】




【図2】


【図3】


【図4】


【図5A】


【図5B】


【公開番号】特開2012−141315(P2012−141315A)
【公開日】平成24年7月26日(2012.7.26)
【国際特許分類】
【出願番号】特願2012−49613(P2012−49613)
【出願日】平成24年3月6日(2012.3.6)
【分割の表示】特願2005−505350(P2005−505350)の分割
【原出願日】平成16年3月25日(2004.3.25)
【出願人】(000141897)アークレイ株式会社 (288)
【Fターム(参考)】
【公開日】平成24年7月26日(2012.7.26)
【国際特許分類】
【出願日】平成24年3月6日(2012.3.6)
【分割の表示】特願2005−505350(P2005−505350)の分割
【原出願日】平成16年3月25日(2004.3.25)
【出願人】(000141897)アークレイ株式会社 (288)
【Fターム(参考)】
[ Back to top ]

