タンパク質含有有機無機複合ヒドロゲル及びその製造方法、並びにタンパク質の安定化方法
【目的】
タンパク質の熱安定性をあげ、より高い温度でも機能を発揮できるようなタンパク質含有有機無機複合ヒドロゲル及びその製造方法、並びにタンパク質の安定化方法を提供する。
【構成】
複数のポリエチレングリコール鎖が化学的に架橋された分岐構造又は網目構造を有する高分子化合物と層状剥離した粘土鉱物とが複合化したヒドロゲル又はその分解物中にタンパク質を含有するタンパク質含有有機無機複合ヒドロゲルを用いることによりタンパク質の安定性が向上した。
タンパク質の熱安定性をあげ、より高い温度でも機能を発揮できるようなタンパク質含有有機無機複合ヒドロゲル及びその製造方法、並びにタンパク質の安定化方法を提供する。
【構成】
複数のポリエチレングリコール鎖が化学的に架橋された分岐構造又は網目構造を有する高分子化合物と層状剥離した粘土鉱物とが複合化したヒドロゲル又はその分解物中にタンパク質を含有するタンパク質含有有機無機複合ヒドロゲルを用いることによりタンパク質の安定性が向上した。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、タンパク質を安定的に用いる方法に関する。
【背景技術】
【0002】
タンパク質はアミノ酸が一次元的につながったひも状高分子であり、ひもは折れたたまれることにより特異的な立体構造をつくり、その結果、タンパク質は多彩な機能を発揮している。その代表例が酵素や抗体である。機能性タンパク質として、具体的には、アミラーゼ、プロテアーゼ、リパーゼ、セルラーゼ、オキシダーゼ、デヒドロゲナーゼ、ゼラチン、コラーゲン、フィブロネクチン、アルブミン、IgG、マクログロブリン、血液凝固因子、モノクロール抗体、ポリクローナル抗体などが例示される。
【0003】
このように、タンパク質の機能は疎水的相互作用、ファンデアワールス相互作用、水素結合など非共有結合により安定化された立体構造に基づき発現しているため、熱により立体構造が壊れやすく、加熱処理などにより、その機能を失活することが大きな課題となっている。
【0004】
これまで、タンパク質の耐熱性を向上させるために幾つかの方法が検討されている。例えば、タンパク質中のアミノ酸残基を置換して改良型タンパク質を得る方法(特許文献1)、突然変異酵素を取得して熱安定性タンパク質を得る方法(特許文献2)、カチオン界面活性剤によりタンパク質を熱安定化する方法(特許文献3)などが例示される。しかし、有効な耐熱性向上としては必ずしも十分な結果は得られていない。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2009−118749号
【特許文献2】特開2001−78786号
【特許文献3】特表2004−500005号
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明が解決しようとする課題は、タンパク質の熱安定性をあげ、より高い温度でも機能を発揮できるようなタンパク質含有有機無機複合ヒドロゲル及びその製造方法、並びにタンパク質の安定化方法を提供することにある。
【課題を解決するための手段】
【0007】
本発明者らは、上記課題を解決すべく鋭意研究に取り組んだ結果、架橋されたポリエチレングリコール中に、層状剥離した粘土鉱物を均一に微細分散し、それらが三次元網目を形成するように複合化させた有機無機複合ゲルの中にタンパク質を含有させたもの、及びそのゲルの分解物において、タンパク質の熱安定性が向上することを見出し、本発明を完成するに至った。
【0008】
即ち本発明は、複数のポリエチレングリコール鎖が化学的に架橋された分岐構造又は網目構造を有する高分子化合物(A)と層状剥離した粘土鉱物(B)とが複合化したヒドロゲル又はその分解物中にタンパク質(C)を含有していることを特徴とするタンパク質含有有機無機複合ヒドロゲルを提供する。
【0009】
また、本発明は、上記のタンパク質含有有機無機複合ヒドロゲルを用いた生体埋め込み材料を提供する。
【0010】
また、本発明は、粘土鉱物(B)を水媒体中で層状剥離させることにより該粘土鉱物(B)の水分散液を製造し、
その層状剥離した粘土鉱物及びタンパク質(C)の存在下で、
同一分子中にポリエチレングリコール鎖と複数の反応性官能基(Q1)とを有する化合物(a1)と、
該反応性官能基(Q1)と反応しうる複数の反応性官能基(Q2)を有する化合物(a2)とを反応させる工程を行なう、
ことを特徴とする上記のタンパク質含有有機無機複合ヒドロゲルの製造方法を提供する。
【0011】
更に、本発明は、複数のポリエチレングリコール鎖が化学的に架橋された分岐構造又は網目構造を有する高分子化合物(A)と層状剥離した粘土鉱物(B)とが複合化した有機無機複合ヒドロゲル又はその分解物中にタンパク質(C)を含有させることにより、該タンパク質(C)の安定性を向上させることを特徴とするタンパク質安定化方法を提供する。
【発明の効果】
【0012】
本発明により、タンパク質の熱安定性が向上し、例えば、酵素の酵素活性がより高温で、長時間継続する効果が得られる。
【図面の簡単な説明】
【0013】
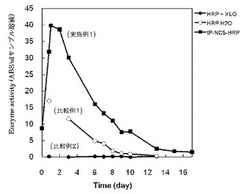
【図1】実施例1および比較例1、比較例2における酵素(Horse radish peroxidase)の活性の時間変化を示す図である。
【図2】実施例2および比較例3における酵素(Horse radish peroxidase)の活性の変化を示す図である。
【発明を実施するための形態】
【0014】
本発明で用いる高分子化合物(A)としては、複数のポリエチレングリコール鎖が化学的に架橋された分岐構造、又は網目構造を有する高分子化合物であり、複数の直鎖状ポリエチレングリコールが複数の架橋点、又は分岐点により結ばれた構造を有する。このような構造であれば、本発明の効果を損なわない限り特に限定なく使用可能である。特に、好ましくは、その高分子鎖の一部に、粘土鉱物との相互作用を生じる官能基、例えば、水酸基、カルボキシル基、アミノ基、スルホン酸基、アミド基、エステル基や、4級アンモニウムイオン基などのイオン性基の一種または複数種を導入したものが用いられる。
【0015】
中でも、高分子化合物(A)の化学的架橋がアミド結合によるものであり、分子鎖の一部にエステル基を有する構造の化合物は分解性に優れているため好ましい。より具体的には、少なくとも一部にエステル基を含むポリエチレングリコール鎖がアミド結合により化学的に架橋された分岐構造、又は網目構造を有する高分子化合物であり、複数の直鎖状ポリエチレングリコールが複数の架橋点、又は分岐点により結ばれた構造を有する化合物である。
【0016】
更に、本発明で用いる高分子化合物(A)としては、同一分子中にポリエチレングリコール鎖と複数の反応性官能基(Q1)とを有する化合物(a1)と、該反応性官能基(Q1)と反応しうる複数の反応性官能基(Q2)を有する化合物(a2)とを反応させることにより製造することができる。
【0017】
上記化合物(a1)又は化合物(a2)として、例えば、下記式(4)又は式(5)で表される化合物を用いることができる。
【0018】
【化1】

【0019】
【化2】

【0020】
上記式(4)及び式(5)中、Rは下記式(3)、式(6)〜式(11)で表される基であり、nは1以上の整数である。また、1分子中の4つのnの合計は、50〜1000が好ましく、100〜800がより好ましく、150〜500が特に好ましい。
【0021】
【化3】

【0022】
【化4】

【0023】
【化5】

【0024】
【化6】

【0025】
【化7】

【0026】
【化8】

【0027】
【化9】

【0028】
上記式(4)及び式(5)で表される化合物の重量平均分子量は1000〜100000であることが好ましく、5000〜50000であることがより好ましく、5000〜40000であることが特に好ましい。
【0029】
そのような化合物の市販品としては、
(1)Rが上記式(3)のタイプ
SUNBRIGHT PTE−050GS(重量平均分子量5000)、PTE−100GS(重量平均分子量10000)、PTE−150GS(重量平均分子量15000)、PTE−200GS(重量平均分子量20000)、PTE−400GS(重量平均分子量40000)
(2)Rが上記式(6)のタイプ
PTE−100HS(重量平均分子量10000)、PTE−200HS(重量平均分子量20000)、PTE−400HS(重量平均分子量40000)
(3)Rが上記式(8)のタイプ
PTE−100MA(重量平均分子量10000)、PTE−200MA(重量平均分子量20000)、PTE−400MA(重量平均分子量40000)
(4)Rが上記式(9)のタイプ
PTE−100PA(重量平均分子量10000)、PTE−150PA(重量平均分子量15000)、PTE−200PA(重量平均分子量20000)、PTE−400PA(重量平均分子量40000)
(5)Rが上記式(11)のタイプ
PTE−050SH(重量平均分子量5000)、PTE−100SH(重量平均分子量10000)、PTE−200SH(重量平均分子量20000)
等がある。
【0030】
上記式(3)、式(6)〜式(11)で表される基の中からいずれかの基を反応性官能基(Q1)として選択し、この反応性官能基(Q1)と反応可能な反応性官能基(Q2)を選択する。そして、これらの反応性官能基(Q1)及び(Q2)を有する化合物をそれぞれ化合物(a1)、化合物(a2)として反応させれば本発明で使用可能な高分子化合物(A)を製造することができる。
【0031】
また、上記式(4)及び式(5)で表される化合物の中から、いずれかの化合物を選択し、これを反応性官能基(Q1)を有する化合物(a1)として用い、上記式(4)及び式(5)で表される化合物以外であり、この反応性官能基(Q1)と反応可能な複数の反応性官能基(Q2)を有する公知の化合物(C)を化合物(a2)として用いても本発明で使用可能な高分子化合物(A)を製造することができる。
【0032】
このような化合物(C)としては、エチレンジアミン、ヘキサメチレンジアミン、ジエチレントリアミン、トリエチレンテトラミン、テトラエチレンペンタミン、フェニレンジアミン、ブタンジアミン、ペンタンジアミン、またアルギニン、アスパラギン、リジンなどのアミノ酸およびこれらを含有するタンパク質等が用いられる。
【0033】
本発明で使用する高分子化合物(A)としては、より好ましくは、架橋点間分子量が均一になるように化学架橋されているものが有効に用いられる。架橋点間分子量が均一になるように化学架橋されたポリエチレングリコールの例としては、例えば、非特許文献2、7に記載の2種の反応性4本鎖ポリエチレングリコール(末端にアミンを有するアミン末端4本鎖ポリエチレングリコール(TAPEG)および末端にN−ヒドロキシサクシイミドグルタレイト末端を有するポリエチレングリコール(TNPEG))を混合し反応させて得られるポリエチレングリコールがあげられる。この場合、ポリエチレングリコール鎖中には、アミド基やエステル基が存在する。また、化学架橋の架橋点間分子量は4本鎖ポリエチレングリコールの分子量の1/2となるが、その値は好ましくは1000〜50000、より好ましくは2000〜30000、特に好ましくは3000〜20000である。架橋点間分子量の値が1000より小さいと柔軟性が不足したり、延伸倍率が小さくなる。また、50000より大きいと、弾性率が低すぎたり、取り扱い性が悪くなったりする。
【0034】
本発明では、非特許文献2、7に記載のポリエチレングリコールの如く、化合物(a1)として下記式(1)で表される化合物であり、化合物(a2)として下記式(2)で表される化合物であり、共に重量平均分子量が1000〜100000である化合物を使用することが特に好ましい。
【0035】
【化10】

(式中、Xは下記式(3)
【0036】
【化11】

で表される基であり、nは整数である。)
【0037】
【化12】

(式中、Yは-CH2CH2CH2NH2で表される基であり、nは整数である。)
【0038】
上記式(1)で表される化合物と式(2)で表される化合物の架橋反応を下記の反応式で示した。
【0039】
【化13】

【0040】
本発明で用いられる粘土鉱物(B)としては、層状に剥離可能な膨潤性粘土鉱物が用いられ、特に好ましくは水中で分子状(単一層)又は1〜10層以内に層状剥離して均一分散可能な粘土鉱物が用いられる。例えば、水膨潤性スメクタイトや水膨潤性雲母などが用いられ、具体的には、ナトリウムを層間イオンとして含む水膨潤性ヘクトライト、水膨潤性モンモリロナイト、水膨潤性サポナイト、水膨潤性合成雲母などが挙げられる。
【0041】
本発明においては、層状剥離した粘土鉱物(B)と前記高分子化合物(A)が相互作用して三次元網目を形成していることが好ましい。粘土鉱物と高分子化合物(A)間の相互作用は、効果的な三次元網目を形成できれば、イオン結合、水素結合、疎水結合、配位結合、共有結合などのいずれか一つまたは複数であって良い。特に好ましくは、高分子化合物(A)の有するアミド基および/またはエステル基と粘土鉱物(B)が水素結合により三次元網目を形成しているものである。
【0042】
なお、かかる三次元網目形成を妨げない限り、または物性を向上させ、または制御する目的で、有機または無機の各種機能性分子や粒子を添加しておくことは可能である。例えば無機粒子としては、シリカ、チタニア、ジルコニア、パラジウム、銀、金、白金などのナノ粒子を共存させることは有効に用いられる。
【0043】
本発明における有機・無機複合ヒドロゲルは、高分子化合物(A)に対する粘土鉱物(B)の質量比(B/A)が0.03〜3であることが好ましく、より好ましくは0.04〜1.5、特に好ましくは0.05〜0.5である。質量比が0.03以下では機械的性質の向上が不十分となりやすく、3以上では粘土鉱物の均一微細分散が困難となってくる場合が多い。
【0044】
本発明で用いられるタンパク質(C)としては、オリゴペプチドやポリペプチドを含む単純タンパク質と、糖タンパク質、リポタンパク質、リン酸化タンパク質などの複合タンパク質のいずれもが使用できる。これらは生体由来の天然物、人工的な合成物、もしくはDNA組み替えによって細菌細胞等からの産出物のいずれであっても良い。さらに、これらは何らかの生理活性を有する機能性タンパク質であることが好ましく、例えば、血清タンパク質、酵素、免疫活性物質、抗血栓性物質、細胞接着性因子、ホルモン、サイトカイン、細菌、ウイルスなどが挙げられる。
【0045】
機能性タンパク質として、具体的には、アミラーゼ、プロテアーゼ、リパーゼ、セルラーゼ、ペルオキシダーゼ、オキシダーゼ、デヒドロゲナーゼ、ゼラチン、コラーゲン、フィブロネクチン、アルブミン、IgG、マクログロブリン、血液凝固因子、モノクロール抗体、ポリクローナル抗体などが例示される。これらの中から、一種または複数が選択して用いられる。
【0046】
本発明で用いられるタンパク質(C)の有機・無機複合ヒドロゲル中での含有量は均一分散が出来るは濃度範囲で目的に応じて設定できる。
【0047】
本発明のタンパク質含有有機・無機複合ヒドロゲルゲルの形成に用いる溶媒は、水であるが、タンパク質含有ゲルの形成が行われる限り、水と混和し、水溶性モノマーや粘土鉱物およびタンパク質と均一溶液を形成する水と混和する有機溶剤を含むことも可能である。また、均一溶液を形成する限り、塩などを含む水溶液も使用可能である。
【0048】
水と混和する有機溶剤としては、メタノール、エタノール、プロパノール、アセトン、メチルエチルケトン、メチルイソブチルケトン、テトラヒドロフラン、ジメチルアセトアミド、ジメチルホルムアミド、ジメチルスルホキシド及びそれらの混合溶媒が挙げられる。
【0049】
本発明のタンパク質含有有機・無機複合ゲルは、架橋されたポリエチレングリコール鎖と粘土鉱物とが複合化して形成された三次元網目中に水とタンパク質を含有するゲルである。即ち、架橋されたポリエチレングリコール鎖と粘土鉱物が水中で分子レベルで複合化することにより形成された三次元網目の中にタンパク質が各種相互作用(イオン性相互作用、水素結合、疎水相互作用、キレート形成、高分子絡み合いなど)の働きで微細に分散して旦持された特徴を有する。
【0050】
本発明におけるタンパク質含有有機・無機複合ヒドロゲルは、無機含有率によらず均一で、透明性を有し、粘土鉱物の凝集は観測されなかった。最終的な粘土鉱物の含有率は熱重量分析(TGA)により、また微細分散性は透過型電子顕微鏡(TEM)観察により測定される。本発明では、用いた粘土の全量が複合体に含まれていることがTGAにより確認され、且つ1層または2〜10層以内の層状剥離した粘土層が均一に分散しているのがTEMにより確認された。また、本発明で得られたタンパク質含有有機・無機複合ヒドロゲルは、優れた力学物性を示し、ほとんどの場合500%以上の破断伸びを示した。また、引っ張り強度や弾性率は広い範囲で制御が可能である。
【0051】
本発明において、タンパク質を有機・無機複合ゲルの中に担持させることにより、タンパク質の安定性が向上する。具体的には、例えば、タンパク質(酵素)含有有機・無機複合ゲルを37℃水中に保持して、周囲の液中における酵素活性を測定すると、単に酵素を37℃水中に入れておいたのに比較して高い酵素活性が長時間に渡って観測される。このことは、有機・無機複合ゲルの中に酵素を担持させておくことにより、また、その分解物の中に酵素を担持させておくことにより、酵素の安定化が図られたことを意味する。
【0052】
本発明におけるタンパク質含有有機・無機複合ヒドロゲルは、好ましくは、同一分子中にポリエチレングリコール鎖と複数の反応性官能基とを有する化合物の水溶液と層状剥離した粘土鉱物水分散液とタンパク質を予め混合し、次いで、該化合物の架橋反応を進める複合化手法が用いられる。より好ましくは、優れた均一性・機械的性質を有するタンパク質含有有機・無機複合ヒドロゲルを得るために、以下のことを行う。
(1)ピロリン酸ナトリウムに塩酸を添加してpHを調整した液をバッファーとして用いること。
(2)予め層状剥離させた粘土鉱物水分散液に上記の化合物(a1)及び化合物(a2)のいずれか片方を添加し、その後、他方の化合物を溶解させること。
(3)層状剥離した粘土鉱物を粘土鉱物の質量/化合物(a1)及び化合物(a2)の合計質量が0.03〜3となるようにすること。
更に好ましくは、
(4)タンパク質含有有機・無機複合ヒドロゲルを合成後に洗浄によりピロリン酸を除くことを行う。
【0053】
ポリエチレングリコールと層状剥離した粘土鉱物を複合化する手法としては、好ましくは高分子化合物(A)と層状剥離した粘土鉱物を予め混合して用いること、より好ましくは層状剥離した粘土鉱物がより安定に存在する片方の反応性4本鎖ポリエチレングリコールと混合させ、次いで、もう一種の反応性4本鎖ポリエチレングリコールを混合して、反応させることが用いられる。且つ、上記反応において、ピロリン酸をバッファーとすること、タンパク質を共存させておくこと、粘土鉱物/ポリエチレングリコールの質量比を0.03〜3とすることが併せて用いられ、優れた均一性と機械的性質を併せ持つタンパク質含有有機・無機複合ヒドロゲルが得られる。
【0054】
更に、本発明で得られる分解性を有するタンパク質含有有機・無機複合ゲルは、生体内における安全性、生体適合性を有するものが多く、分解性生体埋め込み材料やドラッグデリバリーシステムとして用いることが可能である。本発明における分解性を有するタンパク質含有有機・無機複合ゲルは、埋め込みに際して円柱状、棒状、フィルム状、糸状を初めとして目的に応じた種々の形状で用いることが可能であり、その埋め込み初期における力学物性もゲル組成(高分子化合物や粘土鉱物の濃度、含液率)によって広範囲に制御することが可能である。また、本発明で得られた分解性を有するタンパク質含有有機・無機複合ゲルは、単独で用いられるほか、一端、分解させて、水分散体としても用いることができる。
【実施例】
【0055】
次いで本発明を実施例により、より具体的に説明するが、もとより本発明は、以下に示す実施例にのみ限定されるものではない。
【0056】
(実施例1)
粘土鉱物には、[Mg5.34Li0.66Si8O20(OH)4]Na+0.66の組成を有する水膨潤性合成ヘクトライト(商標ラポナイトXLG、ロックウッド社製)を洗浄後、凍結乾燥して用いた。反応性4本鎖ポリエチレングリコールは、重量平均分子量20000の、SUNBRIGHT PTE200GS(以下、PTE200GSと略す)、およびSUNBRIGHT PTE200PA(重量平均分子量20000、以下、PTE200PAと略す)(共に日本油脂株式会社製)を用いた。100mMのピロリン酸ナトリウム(無水)(別名:二リン酸ナトリウム)に塩酸を添加することでpHを7.4に調整した水溶液3mlにラポナイトXLG0.16gを分散させた。次いで、PTE200PA240mgとHRP酵素(Horse radish peroxidase:hemeprotein:分子量44000、EC No. 1.11.1.7) 320μgを加え、均一に混合した。別途、100mMのピロリン酸ナトリウムに塩酸を添加し、pHを7.2に調整した水溶液1mlにPTE200GS240mgを溶解した。次いで、得られたPTE200PA/クレイ/HRP水溶液とPTE200GS水溶液を氷浴中で冷却後、混合し、15秒間強く攪拌した。混合した溶液を80mm×50mm×1mmのガラス容器に充填し、25℃で2時間反応させた。その結果、透明・均質なヒドロゲルが得られた。
【0057】
得られたゲルを1g切り出し、100mlの水中(37℃)に入れ、12日間保持した。12日の間の所定の時間毎に200μlずつ液を採取し、酵素活性を測定した。測定方法は、サンプリングした溶液を37℃にしておき、96ウェルプレートにSTEバッファー(組成:100mMTris−HCl、pH8.0、1MNaCl、10mMEDTA)5μl、溶液45μl、TMB(3,3',5,5'-tetramethylbenzidine)基質50μlを添加し、25℃で1分間反応させた後、1N−塩酸50μlを添加して酵素反応を停止させ、次いで、プレートリーダーで450nmの吸光度を測定し、サンプリングした溶液1μLあたりの吸光度(ABS/μL溶液)で、酵素活性を評価した。
【0058】
結果を図1に示す。比較例1(HRPを37℃水中で分散して保持)や比較例2(HRPを37℃のクレイ水溶液に分散して保持)と比べて高い活性を示し、有機・無機複合ゲルの分解物中に含まれた酵素は熱安定性が向上しているのがわかった。
【0059】
(比較例1)
HRP酵素を有機・無機複合ゲル中に担持させず、100mlの水中(37℃)に0.8μgのHRP(実施例1でのHRP担持量と一緒)を入れ、12日間保持し、その間の所定の時間で200μlずつ採取し、実施例1と同様の方法で酵素活性を評価した。その結果を図1に示す。低い酵素活性を示した。
【0060】
(比較例2)
HRP酵素を有機・無機複合ゲル中に担持させず、クレイ3.81gを含む100mlのクレイ水溶液中(37℃)に0.8μgのHRP(実施例1でのHRP担持量と一緒)を入れ、12日間保持し、その間の所定の時間で200μlずつ採取し、実施例1と同様の方法で酵素活性を評価した。その結果を図1に示す。酵素活性は殆ど示さなかった。
【0061】
(実施例2、比較例3)
実施例1で得られたHRP酵素含有有機・無機複合ゲルを密閉容器に移し、実施例2では37℃で4日間保存した。その後、ゲル1gを100gの水中(37℃)に浸漬して1日間保持し、水をサンプリングして実施例1と同様な方法により酵素活性を測定した。また比較例3ではHRPを37の℃水中にて4日間保持し、その後、更に、37℃の水中で1日間保持した後、水をサンプリングして同様に酵素活性を調べた。なお、実施例2および比較例3の酵素活性保持率は、37℃で保持する前に測定した値を100%として表示した。実施例2は比較例3と比べて高い活性を示した。
【技術分野】
【0001】
本発明は、タンパク質を安定的に用いる方法に関する。
【背景技術】
【0002】
タンパク質はアミノ酸が一次元的につながったひも状高分子であり、ひもは折れたたまれることにより特異的な立体構造をつくり、その結果、タンパク質は多彩な機能を発揮している。その代表例が酵素や抗体である。機能性タンパク質として、具体的には、アミラーゼ、プロテアーゼ、リパーゼ、セルラーゼ、オキシダーゼ、デヒドロゲナーゼ、ゼラチン、コラーゲン、フィブロネクチン、アルブミン、IgG、マクログロブリン、血液凝固因子、モノクロール抗体、ポリクローナル抗体などが例示される。
【0003】
このように、タンパク質の機能は疎水的相互作用、ファンデアワールス相互作用、水素結合など非共有結合により安定化された立体構造に基づき発現しているため、熱により立体構造が壊れやすく、加熱処理などにより、その機能を失活することが大きな課題となっている。
【0004】
これまで、タンパク質の耐熱性を向上させるために幾つかの方法が検討されている。例えば、タンパク質中のアミノ酸残基を置換して改良型タンパク質を得る方法(特許文献1)、突然変異酵素を取得して熱安定性タンパク質を得る方法(特許文献2)、カチオン界面活性剤によりタンパク質を熱安定化する方法(特許文献3)などが例示される。しかし、有効な耐熱性向上としては必ずしも十分な結果は得られていない。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2009−118749号
【特許文献2】特開2001−78786号
【特許文献3】特表2004−500005号
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明が解決しようとする課題は、タンパク質の熱安定性をあげ、より高い温度でも機能を発揮できるようなタンパク質含有有機無機複合ヒドロゲル及びその製造方法、並びにタンパク質の安定化方法を提供することにある。
【課題を解決するための手段】
【0007】
本発明者らは、上記課題を解決すべく鋭意研究に取り組んだ結果、架橋されたポリエチレングリコール中に、層状剥離した粘土鉱物を均一に微細分散し、それらが三次元網目を形成するように複合化させた有機無機複合ゲルの中にタンパク質を含有させたもの、及びそのゲルの分解物において、タンパク質の熱安定性が向上することを見出し、本発明を完成するに至った。
【0008】
即ち本発明は、複数のポリエチレングリコール鎖が化学的に架橋された分岐構造又は網目構造を有する高分子化合物(A)と層状剥離した粘土鉱物(B)とが複合化したヒドロゲル又はその分解物中にタンパク質(C)を含有していることを特徴とするタンパク質含有有機無機複合ヒドロゲルを提供する。
【0009】
また、本発明は、上記のタンパク質含有有機無機複合ヒドロゲルを用いた生体埋め込み材料を提供する。
【0010】
また、本発明は、粘土鉱物(B)を水媒体中で層状剥離させることにより該粘土鉱物(B)の水分散液を製造し、
その層状剥離した粘土鉱物及びタンパク質(C)の存在下で、
同一分子中にポリエチレングリコール鎖と複数の反応性官能基(Q1)とを有する化合物(a1)と、
該反応性官能基(Q1)と反応しうる複数の反応性官能基(Q2)を有する化合物(a2)とを反応させる工程を行なう、
ことを特徴とする上記のタンパク質含有有機無機複合ヒドロゲルの製造方法を提供する。
【0011】
更に、本発明は、複数のポリエチレングリコール鎖が化学的に架橋された分岐構造又は網目構造を有する高分子化合物(A)と層状剥離した粘土鉱物(B)とが複合化した有機無機複合ヒドロゲル又はその分解物中にタンパク質(C)を含有させることにより、該タンパク質(C)の安定性を向上させることを特徴とするタンパク質安定化方法を提供する。
【発明の効果】
【0012】
本発明により、タンパク質の熱安定性が向上し、例えば、酵素の酵素活性がより高温で、長時間継続する効果が得られる。
【図面の簡単な説明】
【0013】
【図1】実施例1および比較例1、比較例2における酵素(Horse radish peroxidase)の活性の時間変化を示す図である。
【図2】実施例2および比較例3における酵素(Horse radish peroxidase)の活性の変化を示す図である。
【発明を実施するための形態】
【0014】
本発明で用いる高分子化合物(A)としては、複数のポリエチレングリコール鎖が化学的に架橋された分岐構造、又は網目構造を有する高分子化合物であり、複数の直鎖状ポリエチレングリコールが複数の架橋点、又は分岐点により結ばれた構造を有する。このような構造であれば、本発明の効果を損なわない限り特に限定なく使用可能である。特に、好ましくは、その高分子鎖の一部に、粘土鉱物との相互作用を生じる官能基、例えば、水酸基、カルボキシル基、アミノ基、スルホン酸基、アミド基、エステル基や、4級アンモニウムイオン基などのイオン性基の一種または複数種を導入したものが用いられる。
【0015】
中でも、高分子化合物(A)の化学的架橋がアミド結合によるものであり、分子鎖の一部にエステル基を有する構造の化合物は分解性に優れているため好ましい。より具体的には、少なくとも一部にエステル基を含むポリエチレングリコール鎖がアミド結合により化学的に架橋された分岐構造、又は網目構造を有する高分子化合物であり、複数の直鎖状ポリエチレングリコールが複数の架橋点、又は分岐点により結ばれた構造を有する化合物である。
【0016】
更に、本発明で用いる高分子化合物(A)としては、同一分子中にポリエチレングリコール鎖と複数の反応性官能基(Q1)とを有する化合物(a1)と、該反応性官能基(Q1)と反応しうる複数の反応性官能基(Q2)を有する化合物(a2)とを反応させることにより製造することができる。
【0017】
上記化合物(a1)又は化合物(a2)として、例えば、下記式(4)又は式(5)で表される化合物を用いることができる。
【0018】
【化1】

【0019】
【化2】

【0020】
上記式(4)及び式(5)中、Rは下記式(3)、式(6)〜式(11)で表される基であり、nは1以上の整数である。また、1分子中の4つのnの合計は、50〜1000が好ましく、100〜800がより好ましく、150〜500が特に好ましい。
【0021】
【化3】

【0022】
【化4】

【0023】
【化5】

【0024】
【化6】

【0025】
【化7】

【0026】
【化8】

【0027】
【化9】

【0028】
上記式(4)及び式(5)で表される化合物の重量平均分子量は1000〜100000であることが好ましく、5000〜50000であることがより好ましく、5000〜40000であることが特に好ましい。
【0029】
そのような化合物の市販品としては、
(1)Rが上記式(3)のタイプ
SUNBRIGHT PTE−050GS(重量平均分子量5000)、PTE−100GS(重量平均分子量10000)、PTE−150GS(重量平均分子量15000)、PTE−200GS(重量平均分子量20000)、PTE−400GS(重量平均分子量40000)
(2)Rが上記式(6)のタイプ
PTE−100HS(重量平均分子量10000)、PTE−200HS(重量平均分子量20000)、PTE−400HS(重量平均分子量40000)
(3)Rが上記式(8)のタイプ
PTE−100MA(重量平均分子量10000)、PTE−200MA(重量平均分子量20000)、PTE−400MA(重量平均分子量40000)
(4)Rが上記式(9)のタイプ
PTE−100PA(重量平均分子量10000)、PTE−150PA(重量平均分子量15000)、PTE−200PA(重量平均分子量20000)、PTE−400PA(重量平均分子量40000)
(5)Rが上記式(11)のタイプ
PTE−050SH(重量平均分子量5000)、PTE−100SH(重量平均分子量10000)、PTE−200SH(重量平均分子量20000)
等がある。
【0030】
上記式(3)、式(6)〜式(11)で表される基の中からいずれかの基を反応性官能基(Q1)として選択し、この反応性官能基(Q1)と反応可能な反応性官能基(Q2)を選択する。そして、これらの反応性官能基(Q1)及び(Q2)を有する化合物をそれぞれ化合物(a1)、化合物(a2)として反応させれば本発明で使用可能な高分子化合物(A)を製造することができる。
【0031】
また、上記式(4)及び式(5)で表される化合物の中から、いずれかの化合物を選択し、これを反応性官能基(Q1)を有する化合物(a1)として用い、上記式(4)及び式(5)で表される化合物以外であり、この反応性官能基(Q1)と反応可能な複数の反応性官能基(Q2)を有する公知の化合物(C)を化合物(a2)として用いても本発明で使用可能な高分子化合物(A)を製造することができる。
【0032】
このような化合物(C)としては、エチレンジアミン、ヘキサメチレンジアミン、ジエチレントリアミン、トリエチレンテトラミン、テトラエチレンペンタミン、フェニレンジアミン、ブタンジアミン、ペンタンジアミン、またアルギニン、アスパラギン、リジンなどのアミノ酸およびこれらを含有するタンパク質等が用いられる。
【0033】
本発明で使用する高分子化合物(A)としては、より好ましくは、架橋点間分子量が均一になるように化学架橋されているものが有効に用いられる。架橋点間分子量が均一になるように化学架橋されたポリエチレングリコールの例としては、例えば、非特許文献2、7に記載の2種の反応性4本鎖ポリエチレングリコール(末端にアミンを有するアミン末端4本鎖ポリエチレングリコール(TAPEG)および末端にN−ヒドロキシサクシイミドグルタレイト末端を有するポリエチレングリコール(TNPEG))を混合し反応させて得られるポリエチレングリコールがあげられる。この場合、ポリエチレングリコール鎖中には、アミド基やエステル基が存在する。また、化学架橋の架橋点間分子量は4本鎖ポリエチレングリコールの分子量の1/2となるが、その値は好ましくは1000〜50000、より好ましくは2000〜30000、特に好ましくは3000〜20000である。架橋点間分子量の値が1000より小さいと柔軟性が不足したり、延伸倍率が小さくなる。また、50000より大きいと、弾性率が低すぎたり、取り扱い性が悪くなったりする。
【0034】
本発明では、非特許文献2、7に記載のポリエチレングリコールの如く、化合物(a1)として下記式(1)で表される化合物であり、化合物(a2)として下記式(2)で表される化合物であり、共に重量平均分子量が1000〜100000である化合物を使用することが特に好ましい。
【0035】
【化10】

(式中、Xは下記式(3)
【0036】
【化11】

で表される基であり、nは整数である。)
【0037】
【化12】

(式中、Yは-CH2CH2CH2NH2で表される基であり、nは整数である。)
【0038】
上記式(1)で表される化合物と式(2)で表される化合物の架橋反応を下記の反応式で示した。
【0039】
【化13】

【0040】
本発明で用いられる粘土鉱物(B)としては、層状に剥離可能な膨潤性粘土鉱物が用いられ、特に好ましくは水中で分子状(単一層)又は1〜10層以内に層状剥離して均一分散可能な粘土鉱物が用いられる。例えば、水膨潤性スメクタイトや水膨潤性雲母などが用いられ、具体的には、ナトリウムを層間イオンとして含む水膨潤性ヘクトライト、水膨潤性モンモリロナイト、水膨潤性サポナイト、水膨潤性合成雲母などが挙げられる。
【0041】
本発明においては、層状剥離した粘土鉱物(B)と前記高分子化合物(A)が相互作用して三次元網目を形成していることが好ましい。粘土鉱物と高分子化合物(A)間の相互作用は、効果的な三次元網目を形成できれば、イオン結合、水素結合、疎水結合、配位結合、共有結合などのいずれか一つまたは複数であって良い。特に好ましくは、高分子化合物(A)の有するアミド基および/またはエステル基と粘土鉱物(B)が水素結合により三次元網目を形成しているものである。
【0042】
なお、かかる三次元網目形成を妨げない限り、または物性を向上させ、または制御する目的で、有機または無機の各種機能性分子や粒子を添加しておくことは可能である。例えば無機粒子としては、シリカ、チタニア、ジルコニア、パラジウム、銀、金、白金などのナノ粒子を共存させることは有効に用いられる。
【0043】
本発明における有機・無機複合ヒドロゲルは、高分子化合物(A)に対する粘土鉱物(B)の質量比(B/A)が0.03〜3であることが好ましく、より好ましくは0.04〜1.5、特に好ましくは0.05〜0.5である。質量比が0.03以下では機械的性質の向上が不十分となりやすく、3以上では粘土鉱物の均一微細分散が困難となってくる場合が多い。
【0044】
本発明で用いられるタンパク質(C)としては、オリゴペプチドやポリペプチドを含む単純タンパク質と、糖タンパク質、リポタンパク質、リン酸化タンパク質などの複合タンパク質のいずれもが使用できる。これらは生体由来の天然物、人工的な合成物、もしくはDNA組み替えによって細菌細胞等からの産出物のいずれであっても良い。さらに、これらは何らかの生理活性を有する機能性タンパク質であることが好ましく、例えば、血清タンパク質、酵素、免疫活性物質、抗血栓性物質、細胞接着性因子、ホルモン、サイトカイン、細菌、ウイルスなどが挙げられる。
【0045】
機能性タンパク質として、具体的には、アミラーゼ、プロテアーゼ、リパーゼ、セルラーゼ、ペルオキシダーゼ、オキシダーゼ、デヒドロゲナーゼ、ゼラチン、コラーゲン、フィブロネクチン、アルブミン、IgG、マクログロブリン、血液凝固因子、モノクロール抗体、ポリクローナル抗体などが例示される。これらの中から、一種または複数が選択して用いられる。
【0046】
本発明で用いられるタンパク質(C)の有機・無機複合ヒドロゲル中での含有量は均一分散が出来るは濃度範囲で目的に応じて設定できる。
【0047】
本発明のタンパク質含有有機・無機複合ヒドロゲルゲルの形成に用いる溶媒は、水であるが、タンパク質含有ゲルの形成が行われる限り、水と混和し、水溶性モノマーや粘土鉱物およびタンパク質と均一溶液を形成する水と混和する有機溶剤を含むことも可能である。また、均一溶液を形成する限り、塩などを含む水溶液も使用可能である。
【0048】
水と混和する有機溶剤としては、メタノール、エタノール、プロパノール、アセトン、メチルエチルケトン、メチルイソブチルケトン、テトラヒドロフラン、ジメチルアセトアミド、ジメチルホルムアミド、ジメチルスルホキシド及びそれらの混合溶媒が挙げられる。
【0049】
本発明のタンパク質含有有機・無機複合ゲルは、架橋されたポリエチレングリコール鎖と粘土鉱物とが複合化して形成された三次元網目中に水とタンパク質を含有するゲルである。即ち、架橋されたポリエチレングリコール鎖と粘土鉱物が水中で分子レベルで複合化することにより形成された三次元網目の中にタンパク質が各種相互作用(イオン性相互作用、水素結合、疎水相互作用、キレート形成、高分子絡み合いなど)の働きで微細に分散して旦持された特徴を有する。
【0050】
本発明におけるタンパク質含有有機・無機複合ヒドロゲルは、無機含有率によらず均一で、透明性を有し、粘土鉱物の凝集は観測されなかった。最終的な粘土鉱物の含有率は熱重量分析(TGA)により、また微細分散性は透過型電子顕微鏡(TEM)観察により測定される。本発明では、用いた粘土の全量が複合体に含まれていることがTGAにより確認され、且つ1層または2〜10層以内の層状剥離した粘土層が均一に分散しているのがTEMにより確認された。また、本発明で得られたタンパク質含有有機・無機複合ヒドロゲルは、優れた力学物性を示し、ほとんどの場合500%以上の破断伸びを示した。また、引っ張り強度や弾性率は広い範囲で制御が可能である。
【0051】
本発明において、タンパク質を有機・無機複合ゲルの中に担持させることにより、タンパク質の安定性が向上する。具体的には、例えば、タンパク質(酵素)含有有機・無機複合ゲルを37℃水中に保持して、周囲の液中における酵素活性を測定すると、単に酵素を37℃水中に入れておいたのに比較して高い酵素活性が長時間に渡って観測される。このことは、有機・無機複合ゲルの中に酵素を担持させておくことにより、また、その分解物の中に酵素を担持させておくことにより、酵素の安定化が図られたことを意味する。
【0052】
本発明におけるタンパク質含有有機・無機複合ヒドロゲルは、好ましくは、同一分子中にポリエチレングリコール鎖と複数の反応性官能基とを有する化合物の水溶液と層状剥離した粘土鉱物水分散液とタンパク質を予め混合し、次いで、該化合物の架橋反応を進める複合化手法が用いられる。より好ましくは、優れた均一性・機械的性質を有するタンパク質含有有機・無機複合ヒドロゲルを得るために、以下のことを行う。
(1)ピロリン酸ナトリウムに塩酸を添加してpHを調整した液をバッファーとして用いること。
(2)予め層状剥離させた粘土鉱物水分散液に上記の化合物(a1)及び化合物(a2)のいずれか片方を添加し、その後、他方の化合物を溶解させること。
(3)層状剥離した粘土鉱物を粘土鉱物の質量/化合物(a1)及び化合物(a2)の合計質量が0.03〜3となるようにすること。
更に好ましくは、
(4)タンパク質含有有機・無機複合ヒドロゲルを合成後に洗浄によりピロリン酸を除くことを行う。
【0053】
ポリエチレングリコールと層状剥離した粘土鉱物を複合化する手法としては、好ましくは高分子化合物(A)と層状剥離した粘土鉱物を予め混合して用いること、より好ましくは層状剥離した粘土鉱物がより安定に存在する片方の反応性4本鎖ポリエチレングリコールと混合させ、次いで、もう一種の反応性4本鎖ポリエチレングリコールを混合して、反応させることが用いられる。且つ、上記反応において、ピロリン酸をバッファーとすること、タンパク質を共存させておくこと、粘土鉱物/ポリエチレングリコールの質量比を0.03〜3とすることが併せて用いられ、優れた均一性と機械的性質を併せ持つタンパク質含有有機・無機複合ヒドロゲルが得られる。
【0054】
更に、本発明で得られる分解性を有するタンパク質含有有機・無機複合ゲルは、生体内における安全性、生体適合性を有するものが多く、分解性生体埋め込み材料やドラッグデリバリーシステムとして用いることが可能である。本発明における分解性を有するタンパク質含有有機・無機複合ゲルは、埋め込みに際して円柱状、棒状、フィルム状、糸状を初めとして目的に応じた種々の形状で用いることが可能であり、その埋め込み初期における力学物性もゲル組成(高分子化合物や粘土鉱物の濃度、含液率)によって広範囲に制御することが可能である。また、本発明で得られた分解性を有するタンパク質含有有機・無機複合ゲルは、単独で用いられるほか、一端、分解させて、水分散体としても用いることができる。
【実施例】
【0055】
次いで本発明を実施例により、より具体的に説明するが、もとより本発明は、以下に示す実施例にのみ限定されるものではない。
【0056】
(実施例1)
粘土鉱物には、[Mg5.34Li0.66Si8O20(OH)4]Na+0.66の組成を有する水膨潤性合成ヘクトライト(商標ラポナイトXLG、ロックウッド社製)を洗浄後、凍結乾燥して用いた。反応性4本鎖ポリエチレングリコールは、重量平均分子量20000の、SUNBRIGHT PTE200GS(以下、PTE200GSと略す)、およびSUNBRIGHT PTE200PA(重量平均分子量20000、以下、PTE200PAと略す)(共に日本油脂株式会社製)を用いた。100mMのピロリン酸ナトリウム(無水)(別名:二リン酸ナトリウム)に塩酸を添加することでpHを7.4に調整した水溶液3mlにラポナイトXLG0.16gを分散させた。次いで、PTE200PA240mgとHRP酵素(Horse radish peroxidase:hemeprotein:分子量44000、EC No. 1.11.1.7) 320μgを加え、均一に混合した。別途、100mMのピロリン酸ナトリウムに塩酸を添加し、pHを7.2に調整した水溶液1mlにPTE200GS240mgを溶解した。次いで、得られたPTE200PA/クレイ/HRP水溶液とPTE200GS水溶液を氷浴中で冷却後、混合し、15秒間強く攪拌した。混合した溶液を80mm×50mm×1mmのガラス容器に充填し、25℃で2時間反応させた。その結果、透明・均質なヒドロゲルが得られた。
【0057】
得られたゲルを1g切り出し、100mlの水中(37℃)に入れ、12日間保持した。12日の間の所定の時間毎に200μlずつ液を採取し、酵素活性を測定した。測定方法は、サンプリングした溶液を37℃にしておき、96ウェルプレートにSTEバッファー(組成:100mMTris−HCl、pH8.0、1MNaCl、10mMEDTA)5μl、溶液45μl、TMB(3,3',5,5'-tetramethylbenzidine)基質50μlを添加し、25℃で1分間反応させた後、1N−塩酸50μlを添加して酵素反応を停止させ、次いで、プレートリーダーで450nmの吸光度を測定し、サンプリングした溶液1μLあたりの吸光度(ABS/μL溶液)で、酵素活性を評価した。
【0058】
結果を図1に示す。比較例1(HRPを37℃水中で分散して保持)や比較例2(HRPを37℃のクレイ水溶液に分散して保持)と比べて高い活性を示し、有機・無機複合ゲルの分解物中に含まれた酵素は熱安定性が向上しているのがわかった。
【0059】
(比較例1)
HRP酵素を有機・無機複合ゲル中に担持させず、100mlの水中(37℃)に0.8μgのHRP(実施例1でのHRP担持量と一緒)を入れ、12日間保持し、その間の所定の時間で200μlずつ採取し、実施例1と同様の方法で酵素活性を評価した。その結果を図1に示す。低い酵素活性を示した。
【0060】
(比較例2)
HRP酵素を有機・無機複合ゲル中に担持させず、クレイ3.81gを含む100mlのクレイ水溶液中(37℃)に0.8μgのHRP(実施例1でのHRP担持量と一緒)を入れ、12日間保持し、その間の所定の時間で200μlずつ採取し、実施例1と同様の方法で酵素活性を評価した。その結果を図1に示す。酵素活性は殆ど示さなかった。
【0061】
(実施例2、比較例3)
実施例1で得られたHRP酵素含有有機・無機複合ゲルを密閉容器に移し、実施例2では37℃で4日間保存した。その後、ゲル1gを100gの水中(37℃)に浸漬して1日間保持し、水をサンプリングして実施例1と同様な方法により酵素活性を測定した。また比較例3ではHRPを37の℃水中にて4日間保持し、その後、更に、37℃の水中で1日間保持した後、水をサンプリングして同様に酵素活性を調べた。なお、実施例2および比較例3の酵素活性保持率は、37℃で保持する前に測定した値を100%として表示した。実施例2は比較例3と比べて高い活性を示した。
【特許請求の範囲】
【請求項1】
複数のポリエチレングリコール鎖が化学的に架橋された分岐構造又は網目構造を有する高分子化合物(A)と層状剥離した粘土鉱物(B)とが複合化したヒドロゲル又はその分解物中にタンパク質(C)を含有していることを特徴とするタンパク質含有有機無機複合ヒドロゲル。
【請求項2】
前記高分子化合物(A)と層状剥離した粘土鉱物(B)の質量比((B)/(A))が0.03〜3である請求項1記載のタンパク質含有有機無機複合ヒドロゲル。
【請求項3】
前記層状剥離した粘土鉱物(B)が水膨潤性無機粘土鉱物である請求項1又は2に記載のタンパク質含有有機無機複合ヒドロゲル。
【請求項4】
前記高分子化合物(A)の化学的架橋がアミド結合によるものであり、且つ、(A)と(B)が三次元網目を形成している請求項1〜3のいずれかに記載のタンパク質含有有機無機複合ヒドロゲル。
【請求項5】
前記高分子化合物(A)がエステル基を有し、前記アミド結合に対するエステル基のモル比が、0.1〜2である請求項4記載のタンパク質含有有機無機複合ヒドロゲル。
【請求項6】
前記高分子化合物(A)が、同一分子中にポリエチレングリコール鎖と複数の反応性官能基(Q1)とを有する化合物(a1)と、該反応性官能基(Q1)と反応しうる複数の反応性官能基(Q2)を有する化合物(a2)とを反応させた化合物である請求項1、2又は3記載のタンパク質含有有機無機複合ヒドロゲル。
【請求項7】
前記化合物(a1)が下記式(1)で表される化合物であり、化合物(a2)が下記式(2)で表される化合物であり、共に重量平均分子量が1000〜100000である請求項6記載のタンパク質含有有機無機複合ヒドロゲル。
【化1】

(式中、Xは下記式(3)
【化2】

で表される基であり、nは整数である。)
【化3】

(式中、Yは-CH2CH2CH2NH2で表される基であり、nは整数である。)
【請求項8】
請求項1〜7のいずれかに記載のタンパク質含有有機無機複合ヒドロゲルを用いた生体埋め込み材料。
【請求項9】
粘土鉱物(B)を水媒体中で層状剥離させることにより該粘土鉱物(B)の水分散液を製造し、
その層状剥離した粘土鉱物及びタンパク質(C)の存在下で、
同一分子中にポリエチレングリコール鎖と複数の反応性官能基(Q1)とを有する化合物(a1)と、
該反応性官能基(Q1)と反応しうる複数の反応性官能基(Q2)を有する化合物(a2)とを反応させる工程を行なう、
ことを特徴とする請求項1〜7のいずれかに記載のタンパク質含有有機無機複合ヒドロゲルの製造方法。
【請求項10】
前記化合物(a1)と化合物(a2)の反応をピロリン酸の存在下で行なう請求項9記載のタンパク質含有有機無機複合ヒドロゲルの製造方法。
【請求項11】
前記粘土鉱物(B)及びタンパク質(C)の水分散液に前記化合物(a1)及び化合物(a2)のいずれか片方を添加し、その後、他方の化合物を添加して反応させる請求項9又は10記載のタンパク質含有有機無機複合ヒドロゲルの製造方法。
【請求項12】
複数のポリエチレングリコール鎖が化学的に架橋された分岐構造又は網目構造を有する高分子化合物(A)と層状剥離した粘土鉱物(B)とが複合化した有機無機複合ヒドロゲル又はその分解物中にタンパク質(C)を含有させることにより、該タンパク質(C)の安定性を向上させることを特徴とするタンパク質安定化方法。
【請求項1】
複数のポリエチレングリコール鎖が化学的に架橋された分岐構造又は網目構造を有する高分子化合物(A)と層状剥離した粘土鉱物(B)とが複合化したヒドロゲル又はその分解物中にタンパク質(C)を含有していることを特徴とするタンパク質含有有機無機複合ヒドロゲル。
【請求項2】
前記高分子化合物(A)と層状剥離した粘土鉱物(B)の質量比((B)/(A))が0.03〜3である請求項1記載のタンパク質含有有機無機複合ヒドロゲル。
【請求項3】
前記層状剥離した粘土鉱物(B)が水膨潤性無機粘土鉱物である請求項1又は2に記載のタンパク質含有有機無機複合ヒドロゲル。
【請求項4】
前記高分子化合物(A)の化学的架橋がアミド結合によるものであり、且つ、(A)と(B)が三次元網目を形成している請求項1〜3のいずれかに記載のタンパク質含有有機無機複合ヒドロゲル。
【請求項5】
前記高分子化合物(A)がエステル基を有し、前記アミド結合に対するエステル基のモル比が、0.1〜2である請求項4記載のタンパク質含有有機無機複合ヒドロゲル。
【請求項6】
前記高分子化合物(A)が、同一分子中にポリエチレングリコール鎖と複数の反応性官能基(Q1)とを有する化合物(a1)と、該反応性官能基(Q1)と反応しうる複数の反応性官能基(Q2)を有する化合物(a2)とを反応させた化合物である請求項1、2又は3記載のタンパク質含有有機無機複合ヒドロゲル。
【請求項7】
前記化合物(a1)が下記式(1)で表される化合物であり、化合物(a2)が下記式(2)で表される化合物であり、共に重量平均分子量が1000〜100000である請求項6記載のタンパク質含有有機無機複合ヒドロゲル。
【化1】

(式中、Xは下記式(3)
【化2】

で表される基であり、nは整数である。)
【化3】

(式中、Yは-CH2CH2CH2NH2で表される基であり、nは整数である。)
【請求項8】
請求項1〜7のいずれかに記載のタンパク質含有有機無機複合ヒドロゲルを用いた生体埋め込み材料。
【請求項9】
粘土鉱物(B)を水媒体中で層状剥離させることにより該粘土鉱物(B)の水分散液を製造し、
その層状剥離した粘土鉱物及びタンパク質(C)の存在下で、
同一分子中にポリエチレングリコール鎖と複数の反応性官能基(Q1)とを有する化合物(a1)と、
該反応性官能基(Q1)と反応しうる複数の反応性官能基(Q2)を有する化合物(a2)とを反応させる工程を行なう、
ことを特徴とする請求項1〜7のいずれかに記載のタンパク質含有有機無機複合ヒドロゲルの製造方法。
【請求項10】
前記化合物(a1)と化合物(a2)の反応をピロリン酸の存在下で行なう請求項9記載のタンパク質含有有機無機複合ヒドロゲルの製造方法。
【請求項11】
前記粘土鉱物(B)及びタンパク質(C)の水分散液に前記化合物(a1)及び化合物(a2)のいずれか片方を添加し、その後、他方の化合物を添加して反応させる請求項9又は10記載のタンパク質含有有機無機複合ヒドロゲルの製造方法。
【請求項12】
複数のポリエチレングリコール鎖が化学的に架橋された分岐構造又は網目構造を有する高分子化合物(A)と層状剥離した粘土鉱物(B)とが複合化した有機無機複合ヒドロゲル又はその分解物中にタンパク質(C)を含有させることにより、該タンパク質(C)の安定性を向上させることを特徴とするタンパク質安定化方法。
【図1】


【図2】




【図2】


【公開番号】特開2012−24050(P2012−24050A)
【公開日】平成24年2月9日(2012.2.9)
【国際特許分類】
【出願番号】特願2010−168035(P2010−168035)
【出願日】平成22年7月27日(2010.7.27)
【特許番号】特許第4704510号(P4704510)
【特許公報発行日】平成23年6月15日(2011.6.15)
【出願人】(000173751)一般財団法人川村理化学研究所 (206)
【Fターム(参考)】
【公開日】平成24年2月9日(2012.2.9)
【国際特許分類】
【出願日】平成22年7月27日(2010.7.27)
【特許番号】特許第4704510号(P4704510)
【特許公報発行日】平成23年6月15日(2011.6.15)
【出願人】(000173751)一般財団法人川村理化学研究所 (206)
【Fターム(参考)】
[ Back to top ]

