ダストの処理方法
【課題】本発明は、亜鉛を含むダストからフッ素イオン及び/又は塩素イオンを分離除去するための簡便で効率的な処理方法を提供する。
【解決手段】本発明は、亜鉛を含むダストを、多硫化物イオンを含むアルカリ水溶液に混合して、ダスト中の金属酸化物を金属硫化物に反応させると共に、ダスト中の塩素及び/又はフッ素をダスト中から浸出させ、金属硫化物を主体とする固形分と浸出廃液に分離することを特徴とするダストの処理方法である。
【解決手段】本発明は、亜鉛を含むダストを、多硫化物イオンを含むアルカリ水溶液に混合して、ダスト中の金属酸化物を金属硫化物に反応させると共に、ダスト中の塩素及び/又はフッ素をダスト中から浸出させ、金属硫化物を主体とする固形分と浸出廃液に分離することを特徴とするダストの処理方法である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、金属精錬炉や金属還元炉等から発生する亜鉛を含むダスト中のフッ素イオン及び/又は塩素イオンを分離除去し、亜鉛の精錬原料として、リサイクルする際の前処理技術である。
【背景技術】
【0002】
一般に、事業場や一般家庭から排出されるゴミ(「都市ゴミ」又は「一般廃棄物」と称されている。)は、都市ゴミ焼却場や産業廃棄物焼却工場等に集められ焼却処分されている。その際に焼却炉等から発生する焼却灰や飛灰(1次ダストともいう。)は、薬剤処理、又は、熔融炉、セメントキルン処理等の中間処理を施した後に最終処分場に堆積されている。
【0003】
また、製鉄精錬時に発生する鉄分主体の1次ダスト(例えば、転炉ダスト T−Fe:59%)は、回転炉床炉(回転炉床式還元炉、例えば、特許文献1や特許文献2を参照)や還元熔融ロータリーキルン炉(例えば、特許文献3を参照)等の還元炉で還元され、還元鉄を製造している。
【0004】
しかしながら、上記の熔融炉やセメントキルン処理等の中間処理や製鉄ダスト用の回転炉床等の還元炉では、蒸気圧の高い亜鉛、鉛、カドミウム等の重金属は炉内で揮発して排ガス中に入り、この排ガスに入った重金属は排ガス処理設備内で凝縮して再び飛灰(以降、2次ダストという。)となってしまうという問題があった。この再度の飛灰中には、塩素、フッ素、ナトリウム、カリウムと共に、亜鉛、鉛、カドミウム等の重金属が濃縮されて多量に含有されており、これらの回収を含めた安定した2次ダストの処理方法が求められていた。
【0005】
この2次ダスト中の亜鉛を回収する手段として、亜鉛精錬の原料として、主原料である亜鉛精鉱等と混合し、使用する方法がある。この場合、2次ダスト中の塩素やフッ素が塩化水素、フッ化水素のガスになり、耐火物を劣化させるという問題があり、配合率を抑制せねばならないという課題があった。
【0006】
これに対して、従来技術として、後述する水洗処理(比較例1)やアルカリ浸出処理(特許文献4、又は、比較例2)が開示されている。特許文献4では、アルカリ剤として好ましくは水酸化ナトリウムの溶液を飛灰に加えて重金属を浸出した後、このスラリーを希釈し、さらに鉱酸を添加してpH7〜13に調整した後、重金属含有殿物と塩素含有液とに分別することが開示されている。
【0007】
しかしながら、これらの処理(比較例1、比較例2)では、水洗処理後及びアルカリ浸出処理後の回収殿物中の塩素濃度は、それぞれ、2.0%、1.3%へ、フッ素濃度は、それぞれ、7.6%、0.7%へ低下したものの、十分に低い値ではない。水処理後の2次ダストとアルカリ浸出処理後の2次ダストをEPMA(Electron Probe Micro Analyzer、電子線マイクロアナライザ)を使用し、粒子断面を見ると、水洗処理やアルカリ浸出処理では、2次ダスト中の粒子内部まで水が到達することができないところがあり、そのため、塩素やフッ素成分は減少するものの、十分には低下しないためと推測している。
【0008】
また、亜鉛原料として主に使用されている亜鉛精鉱(例えば、主成分 Zn:52%、S:31%)中の硫黄成分は硫化物として存在し、亜鉛精錬段階にある燃焼工程で熱源として使用されている。この亜鉛精鉱と比較して、これらの飛灰は酸化物であり、還元硫黄を含まない。よって、亜鉛原料として、飛灰の混合比率を増加させていくと、熱源となる還元硫黄の含有比率が少なくなり、熱源が少なくなるという課題があった。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特公昭45−19569号公報
【特許文献2】特開平11−279611号公報
【特許文献3】特開2002−286209号公報
【特許文献4】特開2003−211122号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
このように、亜鉛濃度が高く、塩素、フッ素、ナトリウム、カリウムを含んだ2次ダストを亜鉛原料として利用する際に、主原料である亜鉛精鉱等に混合し利用した場合、飛灰中の塩素やフッ素が、塩化水素、ふっ化水素のガスになり、耐火物を傷める。そこで、塩素及び/又はフッ素を含み、かつ、亜鉛濃度が高いダストから、塩素、フッ素、ナトリウム、カリウムを分離することが課題である。
【0011】
そこで、本発明は、上記課題を解決し得る簡便で効率的なダストの処理方法を提供することを目的とする。
【課題を解決するための手段】
【0012】
前記の課題に対し、本発明者は、亜鉛濃度が高い2次ダストの主成分を酸化物から硫化物に変化させることにより、2次ダスト中のフッ素及び/又は塩素成分の殆ど全てが分離でき、かつ、ダスト中の酸化物を硫化物にすることで、亜鉛精錬における熱源を付加できることを見出した。これは、2次ダストの主成分(例えば、ZnO)を硫化物に変化させることで、粒子内に空隙が生じ、内部まで水が到達することができ、かつ、フッ素や塩素の化合物(ZnOHFやPbClF)が硫化物(ZnS、PbS)となり、フッ素や塩素は陰イオンとなり、殆ど全量浸出させることができるものと推測している。また、2次ダスト中の酸化物を硫化物にする硫黄源として、硫化物イオンを含む硫化ナトリウムや硫化カリウムや硫化マグネシウム等の硫化化合物や、多硫化物イオンを含む多硫化ナトリウム、多硫化カリウム、多硫化マグネシウム等の多硫化化合物が好ましいことを見出した。
【0013】
以下に課題を解決するための手段について詳細に説明する。
【0014】
まず、2次ダスト中の酸化物の硫化物への変化について、説明する。
【0015】
多硫化物イオンを含むアルカリ水溶液に、亜鉛を含む2次ダストを混合することで、2次ダスト中のフッ化ナトリウムや塩化ナトリウムは溶解し、酸化物やフッ化物や塩化物は硫化物となり、2次ダスト中の塩素及び/又はフッ素は分離される。これは、2次ダスト中の酸化物やフッ化物や塩化物が、より安定な硫化物に化学変化するために起こる現象であると考える。つまり、酸化亜鉛やフッ化亜鉛やフッ化塩素亜鉛は硫化亜鉛に、酸化鉛やフッ化鉛やフッ化塩素鉛は硫化鉛に、酸化カドミウムは硫化カドミウムになり、安定化する。その多硫化物イオンを含むアルカリ水溶液は、多硫化ナトリウム水溶液と、水酸化ナトリウム水溶液、水酸化カリウム水溶液、炭酸ナトリウム水溶液、炭酸水素ナトリウム水溶液、炭酸カリウム水溶液等のアルカリ水溶液を混合することによって作ることができる。但し、酸化カルシウムや水酸化カルシウム等のカルシウムを含むアルカリ水溶液を使用すると、後段の2次ダストからフッ素成分を浸出する際に、フッ化カルシウムを析出させてしまい、フッ素成分を分離できなくなる。また、アルカリ水溶液に元素硫黄を入れ、40℃以上100℃以下で、pH7.5〜14の領域で、0.5〜5時間熱することで、多硫化物イオンを含むアルカリ水溶液(黄水ともいう)を作ることができる。この際、(式1)に示すように、多硫化ナトリウムの他に亜硫酸ナトリウムやチオ硫酸ナトリウムが副生する。
NaOH、S ⇒ Na2S2〜4、Na2SO3、Na2S2O3 … (式1)
【0016】
投入した元素硫黄は、硫黄換算で、硫化物イオン、亜硫酸イオン、チオ硫酸イオン、硫酸イオンとして、それぞれ、約45〜50%、4〜6%、30〜35%、1〜3%に分解している。水温が高いほど、pHが高いほど、黄水の生成速度は大きくなる。硫黄としては、試薬の元素硫黄を使うこともできるが、撥水性が強く、黄水を生成するのに時間がかかるという欠点がある。これに対して、界面活性剤を少量混合することで硫黄の撥水性はほぼなくなり、硫黄と液の固液界面が多くなり、黄水の生成速度が大きくなる。また、コークスガスの脱硫時に発生する硫黄を使用すると、撥水性が殆どないため、黄水の生成時間を短くできる。また、黄水の生成領域はpH7.5〜14の領域であるため、黄水生成と同時にダストを入れても、ダスト中のフッ素や塩素を浸出することができる。この場合に使用するアルカリ成分として、水酸化ナトリウム、水酸化カリウム、炭酸ナトリウム、炭酸水素ナトリウム、炭酸カリウム等のアルカリ成分を混合するとよい。但し、酸化カルシウムや水酸化カルシウムなどのカルシウムを含むアルカリ成分を使用すると、後段の2次ダストからフッ素成分を浸出する際に、フッ化カルシウムを析出させてしまい、フッ素成分を分離できなくなる。
【0017】
また、黄水は、ダスト中の金属酸化物と反応すると、多硫化物イオンは、硫化物イオンを放出し、硫化亜鉛等の硫化金属となるため(式2)、多硫化物イオンは減少し、黄水は黄色から透明になり、ある波長に対する吸光度は減少する。その状況を示したのが、図1である。図1は、黄水の各吸収波長における吸光度と、黄水処理後で多硫化物イオンが殆どないときにおける各吸収波長における吸光度を示している。図1より、吸収波長270〜500nmにおける吸光度を測定することで、多硫化物イオンの未反応量を測定することができる。また、pH7.5〜14における反応であるため、硫化物イオン又は硫化水素イオン(HS−)として水溶液中に存在するため、硫化水素を形成し難く、硫化水素ガスとしても殆ど発生しない。
Sn2− + MeO → MeS + Sn−12− (但し、n=2〜4)
… (式2)
【0018】
また、アルカリ水溶液として、製鉄プロセスの圧延工程から廃棄される含油アルカリ廃液を使用することができる。含油アルカリ廃液は、様々な成分のものがあるが、pH12以上、油分は5%以下のものが好ましい。含油アルカリ廃液中のアルカリ成分は、主に水酸化ナトリウムであり、前述の黄水形成時のアルカリ成分として作用する。含油アルカリ廃液中の油分は、2次ダストの凝集剤となり、硫化物処理後の2次ダストと浸出液の固液分離性を向上させると同時に、油分が2次ダストに付着することにより、硫化処理後の2次ダストを亜鉛原料として精錬炉で利用する際の熱源となる。また、2次ダストに付着しなかった油分は、後述するCOD(化学酸素要求量)成分の生物酸化において、有機物成分となり、微生物フロックを形成し易い従属栄養性の微生物もしくは糸状菌を繁殖させる基質(餌ともいう)となる。しかしながら、油分を多く入れ過ぎると、硫化処理後の硫化物の脱水時において、脱水性を悪化させることになり、投入量については調整が必要となる。
【0019】
次に、黄水処理後に発生する浸出廃液の処理方法について、述べる。
【0020】
黄水処理後の浸出廃液中には、黄水生成時の反応において、副生した亜硫酸イオン、チオ硫酸イオン等と、反応しなかった少量の硫化物イオン、多硫化物イオンを含んでいる。これらのイオンは、CODとして測定されるため、黄水処理した浸出廃液を、無処理のまま一般水域への放出はできない。また、2次ダスト中のフッ素含有率にもよるが、黄水処理後の浸出廃液中には、2次ダストから浸出したフッ素イオンを1000〜30000mg/L含んでおり、やはり、未処理のまま一般水域への放出はできない。
【0021】
COD成分である、副生した亜硫酸イオン、チオ硫酸イオン等と、反応しなかった少量の硫化物イオン、多硫化物イオンは、次の方法により、酸化分解もしくは一部硫黄として回収することができる。
【0022】
酸化分解の方法としては、大きく分けて、微生物等の酸化力を利用した生物処理や、溶存酸素による酸化や塩素や6価クロム等の酸化剤による化学処理がある。
【0023】
生物処理としては、活性汚泥処理、硫黄酸化細菌によるCOD成分の酸化処理、硫黄酸化細菌による硫黄脱窒が考えられる。詳細は、後述する。
【0024】
化学処理について説明する。溶存酸素による酸化は、亜硫酸イオンは容易に常温で酸化されるが、チオ硫酸イオンは酸化され難い。次亜塩素酸や塩素、6価クロム等の酸化剤を使用すると、短時間で亜硫酸イオンやチオ硫酸イオンは酸化される。
【0025】
また、チオ硫酸イオンは、酸性領域(pH4以下、好ましくはpH3以下)で元素硫黄と亜硫酸イオンに自己分解する特性を有している。
【0026】
一方、フッ素成分を浸出廃液中から分離するためには、溶解度の小さいフッ化カルシウム、フッ化マグネシウム等として析出すればよい。マグネシウム源又はカルシウム源として、酸化マグネシウム、塩化マグネシウム、酸化カルシウム、水酸化カルシウム、塩化カルシウムを浸出液中に投入することで、フッ化カルシウム、フッ化マグネシウムの析出物を得ることができる。
【0027】
浸出廃液中にカルシウム源として酸化カルシウム、水酸化カルシウム、塩化カルシウムを投入した場合、浸出液中の硫酸濃度又は亜硫酸濃度が高いため、フッ化カルシウムの析出と同時に、硫酸カルシウムや亜硫酸カルシウムの析出物が生じることが多い。副生したフッ化カルシウムと硫酸カルシウムの混合物は、安定的で脱水後、最終処分することができる。
【0028】
浸出廃液中にマグネシウム源として、酸化マグネシウム、塩化マグネシウムを投入した場合、硫酸マグネシウムの溶解度は高く、また、亜硫酸マグネシウムの溶解度は低い。しかし、亜硫酸イオンは空気酸化し易く、硫酸マグネシウムとなるため溶解し易く、硫酸マグネシウムは析出し難い。そのため、フッ化マグネシウムを主体とする副産物が生成される。黄水処理後の浸出廃液中のチオ硫酸イオン及び亜硫酸イオンを次亜塩素酸ナトリウム溶液で酸化した浸出廃液(硫酸イオン濃度17,500mg/L、フッ素イオン濃度10,500mg/L)に塩化マグネシウムを投入した際のフッ素イオン及び硫酸イオンの析出状況を図2に示す。pH10以上では、投入した塩化マグネシウムの表面上にフッ化マグネシウムがコーテイングしてしまい、未反応分が生じ、浸出廃液中のフッ素濃度は低下しにくくなるが、pH9以下では、投入した塩化マグネシウムの表面上にフッ化マグネシウムのコーテイングが生じ難いため、殆ど反応し、浸出廃液中のフッ素イオン濃度を30〜40mg/Lまで低下させる。なお、フッ化マグネシウムは、フッ酸製造原料や、製鉄プロセスにおける精錬工程で使用する蛍石の代替として使用することができる。
【0029】
本発明は、上記知見に基づいてなされたものであり、その要旨は以下のとおりである。
(1) 亜鉛を含むダストを、多硫化物イオンを含みアルカリ土類金属を含まないアルカリ水溶液に混合して、ダスト中の金属酸化物を金属硫化物に反応させると共に、ダスト中の塩素及び/又はフッ素をダスト中から浸出させ、金属硫化物を主体とする固形分と浸出廃液とに分離することを特徴とする、ダストの処理方法。
(2) 亜鉛含むダストを硫黄と共にアルカリ土類金属を含まないアルカリ水溶液に混合して、40℃以上100℃以下の液温下で攪拌して、ダスト中の塩素及び/又はフッ素をダスト中から浸出させ、金属硫化物を主体とする固形分と浸出廃液とに分離することを特徴とする、ダストの処理方法。
(3) 前記アルカリ水溶液が、製鉄プロセスにおける圧延工程から排出される含油アルカリ廃液である、(1)又は(2)のいずれかに記載のダストの処理方法。
(4) 前記浸出廃液に対して、270〜500nmの領域の吸収波長を測定して前記硫化反応の進捗状況を把握する、(1)〜(3)のいずれかに記載のダストの処理方法。
(5) 前記浸出廃液に対して、マグネシウム化合物を含んだ水溶液又はスラリーを入れた後、又は、入れながら、pH5〜9に調整して、フッ素イオンをフッ化マグネシウムとして析出させ、固液分離する、(1)〜(4)のいずれかに記載のダストの処理方法。
(6) 前記浸出廃液に対して、カルシウム化合物を入れた後、又は、入れながら、pHを4〜10に調整することで、フッ素イオン及び/又は硫酸イオンをカルシウム塩として析出させ、固液分離する、(1)〜(5)のいずれかに記載のダストの処理方法。
(7) 前記浸出廃液中のCOD成分をさらに分解する、(1)〜(6)のいずれかに記載のダストの処理方法。
(8) (1)〜(4)のいずれかに記載の処理方法で分離された浸出廃液に対して、酸を投入しpHを4以下に調整して、硫黄を析出・分離してから、硫黄分離後の浸出廃液にマグネシウム化合物を入れた後、又は、入れながら、pH5.5〜6.5に調整することで、フッ素イオンをフッ化マグネシウムとして析出させ、分離することを特徴とする、ダストの処理方法。
(9) (1)〜(4)のいずれかに記載の処理方法で分離された浸出廃液に対して、酸を投入しpHを4以下に調整して、硫黄を析出・分離してから、硫黄分離後の浸出廃液にカルシウム化合物を入れた後、又は、入れながら、pH5.5〜8に調整することで、フッ素イオン及び/又は硫酸イオンをカルシウム塩として析出させ、分離することを特徴とする、ダストの処理方法。
【発明の効果】
【0030】
熔融炉やセメントキルン等の中間処理や製鉄ダスト用の回転炉床等の還元炉から発生する2次ダストは、本発明により、塩素及びフッ素含有率が著しく低下し、硫化亜鉛が主成分となる黄水処理ダストとなり、亜鉛精錬原料となる。また、脱塩素又は脱フッ素過程で生じる浸出廃液から、フッ化カルシウムやフッ化マグネシウムを回収することができる。
【図面の簡単な説明】
【0031】
【図1】吸収波長に対する吸光度の比較を示す図である。
【図2】浸出廃液に塩化マグネシウムを投入した際のフッ素イオン及び硫酸イオンの析出状況を示す図である。
【図3】本発明のダストの処理方法の一例を示す図である。
【図4】浸出廃液の微生物を用いた処理槽の構成例を示す図である。
【図5】浸出廃液の微生物を用いた処理槽の他の構成例を示す図である。
【図6】浸出廃液の微生物を用いた処理槽の別の構成例を示す図である。
【図7】本発明のダストの処理方法の他の例を示す図である。
【図8】硫黄析出工程における処理槽の構成例を示す図である。
【図9】MgF2析出・酸化工程における処理層の構成例を示す図である。
【図10】MgF2析出・酸化工程における処理層の他の構成例を示す図である。
【図11】比較例2におけるダスト処理方法を示す図である。
【図12】実施例1におけるダスト処理方法を示す図である。
【図13】実施例2におけるダスト処理方法を示す図である。
【図14】実施例3における浸出廃液の微生物を用いた処理槽の構成を示す図である。
【図15】実施例4における浸出廃液の微生物を用いた処理槽の構成を示す図である。
【発明を実施するための形態】
【0032】
以下に添付図面を参照しながら、本発明の好適な実施の形態について詳細に説明する。なお、本明細書及び図面において、実質的に同一の機能構成を有する構成要素については、同一の符号を付することにより重複説明を省略する。
【0033】
本発明について、以下に詳細に説明する。
【0034】
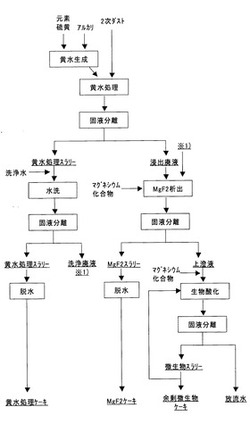
図3に本発明のダストの処理方法の一例(例1)を示す。図3では、『黄水生成』『黄水処理』『水洗』の工程からなる黄水処理プロセスと、『MgF2析出』『生物酸化』の工程からなる浸出廃液の処理プロセスとからなっている。
【0035】
それぞれの工程について、説明を行う。
【0036】
『黄水生成』工程では、アルカリ溶液に元素硫黄を入れ、40℃以上100℃以下で、pH7.5〜14の領域で、0.5〜5時間程度で、多硫化物イオンを含む溶液を作ることができる。より好ましくは、80℃以上100℃以下、pH10〜13の領域で1時間程度で、多硫化物イオンを含む溶液を作ることができる。この際、亜硫酸イオンやチオ硫酸イオンも副生する。
【0037】
『黄水処理』工程では、2次ダストと『黄水生成』工程で生成した黄水とを混合し、2次ダスト中の亜鉛、鉛、カドミウム等の重金属を硫化物にし、安定化する(式3)。この『黄水処理』工程では、40℃以上100℃以下で、pH7.5〜14の領域で、0.5〜5時間程度行うことが好ましい。より好ましくは、80℃以上100℃以下、pH10〜12の領域で1時間程度で行うことが好ましい。アルカリ領域では、黄水からの硫化水素の発生が抑制される。(式3)で生じたSn−12−イオンは、(式4)に示すように、元素硫黄と反応し、Sn2−イオンとなる。
Sn2− + MeO → MeS + Sn−12− (但し、n=2〜4)
… (式3)
Sn−12− + S → Sn2− … (式4)
【0038】
『水洗』工程では、『黄水処理』工程で生成した硫化亜鉛等を含む黄水処理スラリーを、水洗し、黄水処理スラリー中の液相(亜硫酸イオンやチオ硫酸イオンを含む)を洗い流す工程である。水洗された黄水処理スラリーは脱水し、硫化物(主に硫化亜鉛)を含む黄水処理ケーキとなり、それを亜鉛原料として利用することができる。
【0039】
『MgF2析出』工程では、『黄水処理』工程から発生した2次ダストの浸出廃液中のフッ素イオンをフッ化マグネシウムとして析出させ、フッ化マグネシウムのスラリーとして分離する。そのため、浸出廃液中には、マグネシウム化合物を投入するが、マグネシウム化合物(酸化マグネシウム又は水酸化マグネシウム又は塩化マグネシウム)はアルカリ領域では溶解し難く、マグネシウム化合物の未反応物が残り、酸性側(pH4以下)では、溶解性フッ素濃度は高くなる。よって、マグネシウム化合物投入後のpHを5〜9程度、好ましくは、pH5〜7にコントロールすることで、マグネシウム化合物の未反応物は殆どなく、析出したMgF2を分離した液相のフッ素濃度は30〜60mg/L程度になる。
【0040】
『生物酸化』工程では、独立栄養細菌である硫黄酸化細菌を利用したり、有機物を基質とする従属栄養細菌の集合体である活性汚泥を利用することができる。
【0041】
繁殖させる微生物の特徴を説明し、それに適当な処理方法を説明する。
【0042】
独立栄養細菌である硫黄酸化細菌の一部の微生物(例として、Thiobacillus thioparus、Thiobacillus neapolitanus等)は、好気条件、つまり溶存酸素がある場合には、溶存酸素を利用して、亜硫酸イオンやチオ硫酸イオンや元素硫黄等の還元性硫黄を硫酸イオンまで酸化し、エネルギーを得、水中に溶解した二酸化炭素を炭素源としてたんぱく質等を合成し、増殖している。生育pHは、4.5〜8.5、生育温度は8〜39℃である。この微生物自体では、活性汚泥処理法で見られるような生物フロックを作ることは難しいため、生物反応槽内に固定する必要があり、礫やスラグや素焼き物等の微生物担体を使用することで硫黄酸化細菌を固定することが望ましい。余剰汚泥が少ないことも特徴である。これらの微生物の特徴から、図4の処理システムで亜硫酸イオンやチオ硫酸イオン等のCOD成分を酸化分解することができる。生物反応槽3内に硫黄酸化細菌が付着する微生物担体2を設置し、亜硫酸イオンやチオ硫酸イオンを含む浸出廃液1は、硫黄酸化細菌が付着する微生物担体2を設置した生物反応槽3に投入し、生物反応槽3内にエアー5を吹き込むことで、酸化することができる。亜硫酸イオンやチオ硫酸イオン等のCOD成分が酸化分解された浸出廃液1は、処理水4として放流される。
【0043】
独立栄養細菌である硫黄酸化細菌の一部の種類(例として、Thiobacillus denitrificans)は、嫌気条件、つまり溶存酸素が全く存在しない場合で、硝酸イオンや亜硝酸イオンが存在している時、硝酸イオンや亜硝酸イオンの酸素を利用して、亜硫酸イオンやチオ硫酸イオンや元素硫黄等の還元性硫黄を硫酸イオンまで酸化し、エネルギーを得ながら、硝酸イオンや亜硝酸イオンは窒素ガスまで還元し、水中に溶解した二酸化炭素を炭素源としてたんぱく質等を合成し、増殖している。生育pHは、6〜9、生育水温は15〜35℃で、原水中のS/N比を3〜7(g/g)にすると良い。この場合も、活性汚泥処理法で見られるような生物フロックを作ることは難しいため、礫やスラグや素焼き物等の微生物担体を使用することで硫黄酸化細菌を固定することが望ましい。余剰汚泥が少ないことも特徴である。これらの特徴から、図5の処理システムで亜硫酸イオンやチオ硫酸イオン等のCOD成分を酸化しながら、硝酸イオンや亜硝酸イオンを還元していくことができる。脱窒槽15内に硫黄酸化細菌が付着する微生物担体2を設置し、脱窒槽15内を撹拌機13で撹拌させている。脱窒槽15の上部は蓋16をし、空気の混入を遮断している。亜硫酸イオンやチオ硫酸イオンを含む浸出廃液1と、硝酸イオンを含む硝酸廃液12を、硫黄酸化細菌が付着する微生物担体2を設置した脱窒槽15に投入することで、亜硫酸イオンやチオ硫酸イオン等のCOD成分を酸化しながら、硝酸イオンや亜硝酸イオンを還元していくことができる。亜硫酸イオンやチオ硫酸イオン等のCOD成分が酸化分解された浸出廃液1および硝酸イオンや亜硝酸イオンが還元された硝酸廃液12は、処理水4として放流される。
【0044】
従属栄養細菌の集合体である活性汚泥は、好気条件、つまり、溶存酸素が存在する場合で、有機物を基質としながら増殖する。活性汚泥中には、還元性硫黄を酸化できる、硫黄酸化細菌(例えば、Thiobacillus novellus、Thiobacillus versutus等)も生息している。なお、活性汚泥としては、下水処理場やコークス製造時に発生する安水の処理に使用されている。よって、有機物を含有した廃液22と共に、亜硫酸イオンやチオ硫酸イオンを含む浸出廃液1を、活性汚泥を入れた生物反応槽3に投入することで、有機物成分を酸化しながら、亜硫酸イオンやチオ硫酸イオンを酸化させることができる(図6)。生物反応槽3内には、エアー5を吹き込むことが必要である。活性汚泥はフロックを形成するため、図6のように、沈殿槽26で活性汚泥からなるフロックを沈降分離することができる。沈殿槽26で活性汚泥からなるフロックが沈降分離された浸出廃液1および有機物含有廃液22は、処理水4として放流される。
【0045】
図7に、本発明のプロセスの一例(例2)を示す。図7では、『黄水生成』『黄水処理』『水洗』の工程による硫化物回収プロセスと、『硫黄析出』『MgF2析出』の工程による浸出廃液の処理プロセスとからなっている。
【0046】
それぞれの工程について、説明を行う。
【0047】
『黄水生成』『黄水処理』『水洗』の工程による黄水処理プロセスは、図3と同じで、前記の説明のとおりである。
【0048】
『黄水処理』工程から排出された浸出廃液中には、亜硫酸イオン、チオ硫酸イオン、フッ素イオンを含むが、『硫黄析出』工程では、チオ硫酸イオンを酸性条件下(pH4以下、好ましくはpH3以下)で元素硫黄と亜硫酸イオンとに自己分解させる(図8)。硫黄析出槽32内に酸34を投入してpH4以下、好ましくは、pH3以下に維持しながら、撹拌機13で撹拌する。酸34としては、硫酸や塩酸が好ましい。次に、高分子凝集剤25を添加し、固液分離操作、例えば沈殿槽26で、元素硫黄を含む硫黄スラリー38と亜硫酸イオンを含む硫黄析出工程からの処理水40とに分離し、元素硫黄は、『黄水生成』工程に投入し、再度、黄水とする。硫黄析出工程からの処理水40中には、亜硫酸イオン、フッ素イオンを含むが、これらの成分は、次の『MgF2析出・酸化』工程で処理される。なお、『硫黄析出』工程では、pHを酸性側にするため、硫化水素ガスが少量発生する。発生する硫化水素ガスは排気ファン39で吸引し、『黄水処理』工程に投入することで、2次ダスト中の亜鉛成分を硫化物に変化させることができる。
【0049】
『硫黄析出』工程からの処理水40中には、フッ素イオンと亜硫酸イオンを含んでいる。『MgF2析出・酸化』工程では、塩化マグネシウム、酸化マグネシウム、水酸化マグネシウムのいずれかを投入し、フッ素イオンをフッ化マグネシウムとして析出させながら、亜硫酸イオンは、反応槽内に空気を吹き込み空気酸化したり、前述の微生物を用い酸化することができる。
【0050】
フッ化マグネシウムを析出するには、前述のように、マグネシウム化合物(酸化マグネシウム又は水酸化マグネシウム又は塩化マグネシウム)はアルカリ領域では溶解し難く、マグネシウム化合物の未反応物が残り、酸性側では、溶解性フッ素濃度は高くなる。よって、マグネシウム化合物投入後のpHを5〜9程度、好ましくは、pH5〜7にコントロールすることで、マグネシウム化合物の未反応物は殆どなく、MgF2を析出させることができる。一方、亜硫酸イオンを空気酸化させる場合、pHが高いとMgSO3の結晶が析出するため、pH5.5〜6.5に調整すること重要となる。よって、フッ素イオンを析出させながら、亜硫酸イオンを空気酸化するには、pH5.5〜6.5に調整することが好ましい。『MgF2析出・酸化』工程を図9に示す。『硫黄析出』工程から排出される処理水40中にマグネシウム化合物43を投入し、MgF2析出・酸化槽41内でフッ素イオンをフッ化マグネシウムとして析出させながら、MgF2析出・酸化槽41内に、pH調整剤44を添加してpH5.5〜6.5(pH計45により測定)に調整しながら、エアー5により酸素を供給し、亜硫酸イオンを酸化する。その後、高分子凝集剤25を投入し、沈殿槽26で固液分離を行い、MgF2スラリー48と処理水4とに分離される。処理水4は放流され、MgF2スラリー48は脱水機で脱水し、MgF2ケーキを得ることができる。
【0051】
また、『硫黄析出』工程からの処理水40中に、炭酸カルシウム、塩化カルシウム、酸化カルシウム、水酸化カルシウム(消石灰ともいう)のいずれかのカルシウム化合物53を投入し、フッ素イオンをフッ化カルシウムとして析出させながら、亜硫酸イオンは、CaF2析出・酸化槽51内にエアー5を吹き込み空気酸化したり、前述の微生物を用い酸化することができる。この工程を『CaF2析出・酸化』工程(図10)を説明する。『硫黄析出』工程から排出される処理水40は、CaF2析出・酸化槽51に投入され、pH調整剤44を添加してpH5.5〜8(pH計45により測定)に調整しながら、エアー5により酸素を供給し、亜硫酸イオンを硫酸イオンに酸化する。硫酸イオンは石膏となり、析出し、フッ素イオンはフッ化カルシウムとして析出する。その後、高分子凝集剤25を投入し、フロックを形成させ、沈殿槽26で固液分離を行い、フッ化カルシウムと石膏の混合スラリー58と処理水4とに分離される。処理水4は放流され、フッ化カルシウムと石膏の混合スラリー58は脱水機で脱水し、混合ケーキを得ることができる。
【実施例】
【0052】
(比較例1)
ビーカーに1Lの水道水を入れ、製鉄精錬時に発生する鉄分主体の1次ダストを回転炉床炉(回転炉床式還元炉)で還元した際に発生した2次ダスト50g入れ、pH調整はせずに、30分間攪拌した。その後、吸引ろ過を行い、固液分離を行い、浸出廃液と洗浄ダスト(29.1g)を得た。浸出廃液と洗浄ダストに対して、成分分析を行った。その結果を、表1及び表2に示す。洗浄により、洗浄ダスト中のF、Clは低下しているものの、その値は高く、亜鉛の精錬原料としては使用できないものであった。なお、F、Clの残存率は、それぞれ、39%、8%で高い値であった。
【0053】
【表1】

【0054】
【表2】

【0055】
(比較例2)
比較例1で用いたものと同じロットの2次ダストに対し、図11に示すように、アルカリ処理を実施した。ビーカーに、20%水酸化ナトリウム水溶液80mLと水道水170mLを入れ、40℃に保持した中に、2次ダストを50g入れ、10分間強攪拌した。その後、水道水125mLを加えて希釈し、中和剤として98%硫酸を添加して、pH12に調整し、30分間維持しながら、撹拌した。その後、ろ過し、浸出廃液を得た。また、水道水100mLを加え、ケーキ洗浄を行い、アルカリ処理ダスト(28.0g)を得た。
【0056】
浸出廃液とアルカリ処理ダストに対する分析結果を表3と表4に示す。アルカリ処理により、アルカリ処理ダスト中のF、Clは低下しているが、その値は、亜鉛の精錬原料として使用するには、若干高かった。なお、F、Clの残存率は、それぞれ、3.5%、4.9%であった。また、2次ダスト1g当りの薬剤使用量は、水酸化ナトリウムは、0.32gで、硫酸(100%換算)は、0.026gであった。また、浸出廃液中には、フッ素、鉛、6価クロムを含んでおり、一般水域に放出するには、これらの元素を浸出廃液中から分離する必要がある。
【0057】
【表3】

【0058】
【表4】

【0059】
(実施例1)
水道水10Lに20%水酸化ナトリウム水溶液0.78Lと元素硫黄250gを入れ、煮沸させ、浸出液(黄水)を作成した。浸出液中に比較例1で用いたものと同じロットの2次ダストを1000g投入した。pH10以上になるように、20%水酸化ナトリウム水溶液を投入し、30分間撹拌した(図12)。水温は、80℃に制御した。その後、ろ紙で濾過した後、黄水処理ケーキ(黄水処理ダストともいう)と、亜硫酸イオン、チオ硫酸イオン、フッ素イオンを含む浸出廃液とに分離した。その際、ケーキ洗浄水として1Lの水道水を使用した。
【0060】
浸出廃液と黄水処理ダストに対する分析結果を表5と表6に示す。黄水処理により、黄水処理ダスト中のF、Clは、比較例1又は2より低下し、亜鉛の精錬原料として十分使用できる濃度であった。なお、F、Clの残存率は、それぞれ、1.2%、0.4%であった。また、2次ダスト1g当りの薬剤使用量は、水酸化ナトリウムは、0.20gで、元素硫黄は、0.25gであった。また、浸出廃液中には、フッ素とCOD成分(亜硫酸イオン、チオ硫酸イオン等)を含んでおり、一般水域に放出するには、これらの元素を浸出廃液中から分離もしくは分解する必要があるが、比較例2で見られたような6価クロムは含有していない。また、亜硫酸イオンやチオ硫酸イオン濃度から計算されるCOD値は、6,500mg/lであるが、そのCOD値を大幅に上回っている。これは、反応していない多硫化物イオンが残存するためである。
【0061】
【表5】

【0062】
【表6】

【0063】
(実施例2)
水道水10Lに20%水酸化ナトリウム水溶液0.78Lと元素硫黄250gと比較例1で用いたものと同じロットの2次ダスト1100gを入れ、90℃にした。pH10以上になるように、20%水酸化ナトリウム水溶液を投入し、30分ゆっくり撹拌した。その後、ろ紙で濾過した後、黄水処理ケーキと、亜硫酸イオン、チオ硫酸イオン、フッ素イオンを含む浸出廃液とに分離した。その際、ケーキ洗浄水として1Lの水道水を使用した(図13)。
【0064】
浸出廃液と黄水処理ダストに対する分析結果を表7と表8に示す。黄水処理により、黄水処理ダスト中のF、Clは、比較例1又は2より低下し、亜鉛の精錬原料として十分使用できる濃度であった。なお、F、Clの残存率は、それぞれ、0.9%、0%であった。また、2次ダスト1g当りの薬剤使用量は、水酸化ナトリウムは、0.16gで、元素硫黄は、0.23gであった。また、浸出廃液中には、フッ素とCOD成分(亜硫酸イオン、チオ硫酸イオン等)を含んでおり、一般水域に放出するには、これらの元素を浸出廃液中から分離もしくは分解する必要がある。
【0065】
【表7】

【0066】
【表8】

【0067】
(実施例3)
水道水10Lに製鉄プロセスの圧延工程から発生する含油アルカリ排水(pH13.0で水酸化ナトリウムを含む、油分1.4%)1.5Lと元素硫黄250gと比較例1で用いたものと同じロットの2次ダスト1100gを入れ、90℃にした。pH10以上になるように、含油アルカリ排水を投入し、30分ゆっくり撹拌した。その後、ろ紙で濾過した後、黄水処理ケーキと、亜硫酸イオン、チオ硫酸イオン、フッ素イオンを含む浸出廃液とに分離した。その際、ケーキ洗浄水として1Lの水道水を使用した(図13)。
【0068】
浸出廃液と黄水処理ダストに対する分析結果を表9と表10に示す。黄水処理により、黄水処理ダスト中のF、Clは、比較例1又は2より低下し、亜鉛の精錬原料として十分使用できる濃度であった。なお、F、Clの残存率は、それぞれ、1.3%、0.6%であった。また、2次ダスト1g当りの含油アルカリ排水の使用量は、1.36mlで、元素硫黄は、0.23gであった。また、浸出廃液中には、フッ素とCOD成分(亜硫酸イオン、チオ硫酸イオン等)を含んでおり、一般水域に放出するには、これらの元素を浸出廃液中から分離もしくは分解する必要がある。
【0069】
【表9】

【0070】
【表10】

【0071】
(実施例4)
水道水10Lに20%水酸化ナトリウム水溶液0.78Lと元素硫黄250gを入れ、煮沸させ、浸出液(黄水)を作成した。波長400nmで、浸出液の吸光度を測定しながら、吸光度1.5以下になるまで、浸出液中に比較例1で用いたものと同じロットの2次ダストを投入した。pH10以上になるように、20%水酸化ナトリウム水溶液を投入し、30分間撹拌した(図12)。水温は、80℃に制御した。吸光度を測定する際には、浸出液を濾過し、その濾過液に対し、吸光度を測定した。2次ダスト投入量は総計で1100gであった。その後、ろ紙で濾過した後、黄水処理ケーキ(黄水処理ダストともいう)と、亜硫酸イオン、チオ硫酸イオン、フッ素イオンを含む浸出廃液とに分離した。その際、ケーキ洗浄水として1Lの水道水を使用した。
【0072】
浸出廃液と黄水処理ダストに対する分析結果を表11と表12に示す。黄水処理により、黄水処理ダスト中のF、Clは、比較例1又は2より低下し、亜鉛の精錬原料として十分使用できる濃度であった。なお、F、Clの残存率は、それぞれ、1.1%、0%であった。また、2次ダスト1g当りの薬剤使用量は、水酸化ナトリウムは、0.18gで、元素硫黄は、0.23gであった。また、浸出廃液中には、フッ素とCOD成分(亜硫酸イオン、チオ硫酸イオン等)を含んでおり、一般水域に放出するには、これらの元素を浸出廃液中から分離もしくは分解する必要がある。また、亜硫酸イオンやチオ硫酸イオン濃度から計算されるCOD値は、6,800mg/lであり、そのCOD値に近い。これは、反応していない多硫化物イオンが殆ど残存していないためであり、実施例1と比較して、多硫化物イオンをほぼ全量利用したと言える。
【0073】
【表11】

【0074】
【表12】

【0075】
(実施例5)
実施例2で生成した浸出廃液を水道水で4倍希釈した浸出廃液1を1mL/分で微生物担体2として礫岩(10mm以上50mm以下)を充填した生物反応槽3(2L)に連続投入した(図14)。生物反応槽3下部からは、エアー5を投入し、硫黄酸化細菌によるチオ硫酸イオンや亜硫酸イオンの酸化に必要な酸素を供給した。生物反応槽3のpHは5.5〜6.0になるように、1%水酸化ナトリウム水溶液を入れ、pH制御を行った。なお、生物反応槽5は、事前に回分状態にて、浸出廃液を入れ、硫黄酸化細菌を馴養させている。
【0076】
生物反応槽5から得た処理水40を、連続して、MgF2析出槽64(0.5L)に投入し、3%酸化マグネシウムスラリー66を投入し、pH調整剤44として1%水酸化ナトリウム水溶液を添加してpH6〜6.5(pH計45により測定)に調整した。生物反応槽3からの処理水中のフッ素イオンは、フッ化マグネシウムとして析出させた。その後、高分子凝集剤25を投入しフロックを形成させ、沈殿槽26で沈殿させ、処理水4を放流した。沈殿槽26で沈殿したMgF2スラリー71の一部は、MgF2析出槽64に戻し、残りは回収した。
【0077】
その際の、水質を、表13に示す。希釈浸出廃液1中のCOD成分である亜硫酸イオンやチオ硫酸イオンは、生物反応槽3内で、ほぼ全量、硫酸イオンまで分解されている。また、フッ素イオンはMgF2析出槽内で析出し、処理水4中のF濃度は56mg/Lまで低下している。回収したMgF2スラリー71中のMgF2濃度は、ドライ換算で、82%であった。
【0078】
【表13】

【0079】
(実施例6)
実施例2で生成した浸出廃液を水道水で4倍希釈した浸出廃液1を1mL/分で微生物担体2として礫岩(10mm以上50mm以下)を充填した生物反応槽3(2L)に連続投入した(図14)。生物反応槽3下部からは、エアー5を投入し、硫黄酸化細菌によるチオ硫酸イオンや亜硫酸イオンの酸化に必要な酸素を供給した。生物反応槽3のpHは5.5〜6.0になるように、pH調整剤44として1%水酸化ナトリウム水溶液を入れ、pH制御を行った。なお、生物反応槽3は、事前に回分状態にて、浸出廃液1を入れ、硫黄酸化細菌を馴養させている。
【0080】
生物反応槽3から得た処理水40を、連続して、CaF2析出槽64(0.5L)に投入し、3%水酸化カルシウムスラリー66を投入し、pH7〜7.5(pH計45により測定)に調整した。処理水中のフッ素イオンは、フッ化カルシウムとして析出させた。その後、高分子凝集剤25を投入しフロックを形成させ、沈殿槽26で沈殿させ、処理水4を放流した。沈殿槽26で沈殿したCaF2スラリー71の一部は、CaF2析出槽64に戻し、残りは回収した。
【0081】
その際の、水質を、表14に示す。希釈後の浸出廃液1中のCOD成分である亜硫酸イオンやチオ硫酸イオンは、生物反応槽3内で、ほぼ全量、硫酸イオンまで分解されている。また、フッ素イオンはCaF2析出槽64内で析出し、処理水4中のF濃度は12mg/Lまで低下している。回収したCaF2スラリー71中のCaF2濃度及びCaSO4濃度は、ドライ換算で、それぞれ、40%、48%であった。
【0082】
【表14】

【0083】
(実施例7)
実施例2で生成した浸出廃液を水道水で4倍希釈した浸出廃液1を1mL/分でMgF2析出・酸化槽41(2L)に連続投入した(図9)。MgF2析出・酸化槽41の下部からは、エアー5を投入し、硫黄酸化細菌によるチオ硫酸イオンや亜硫酸イオンの酸化に必要な酸素を供給した。MgF2析出・酸化槽41のpHは6.0〜6.5になるように、マグネシウム化合物43として、5%酸化マグネシウムスラリーを入れ、pH制御を行い、COD成分である亜硫酸イオンやチオ硫酸イオンを生物酸化させながら、浸出廃液1中のフッ素イオンを弗化マグネシウムとして析出させた。MgF2析出・酸化槽41から越流したスラリーに対して、高分子凝集剤25を投入して、フロックを作成し、沈澱槽26にて沈澱させた。沈澱させたMgF2スラリー48中には、硫黄酸化細菌が付着していることから、一部、MgF2析出・酸化槽41へ返送しながら、残りのMgF2スラリー48は沈澱槽26より回収した。なお、MgF2析出・酸化槽41内に投入した硫黄酸化細菌は、事前に回分状態にて、浸出廃液1を入れ、硫黄酸化細菌を馴養させている。
【0084】
その際の、水質を、表15に示す。希釈後の浸出廃液1中のCOD成分である亜硫酸イオンやチオ硫酸イオンは、MgF2析出・酸化槽41内で、ほぼ全量、硫酸イオンまで分解され、フッ素イオンは析出し、処理水中のF濃度は79mg/Lまで低下している。回収したMgF2スラリー中のMgF2濃度は、ドライ換算で、78%であった。
【0085】
【表15】

【0086】
(実施例8)
実施例2で生成した浸出廃液を水道水で4倍希釈した浸出廃液1を10ml/分で、硫黄析出槽32(0.6L)に連続投入し、攪拌機13で混合した。pH調整剤として5%硫酸85を添加し、硫黄析出槽32内のpHを2.5〜3.0に維持し、浸出廃液1中のチオ硫酸イオンを自己分解させ、硫黄を析出させ、亜硫酸イオンを生成させた。その後、高分子凝集剤25を加え、フロックを形成させた後、沈殿槽26で沈殿させ、硫黄を含む硫黄スラリー38を得た。沈殿槽26からの亜硫酸イオンを含む処理水40は、MgF2析出・酸化槽90に投入し、エアー5で撹拌した。MgF2析出・酸化槽90に3%酸化マグネシウムスラリー66を添加し、MgF2析出・酸化槽90内のpHを5.5〜6.0に維持しながら、亜硫酸イオンを空気酸化させた。その後、高分子凝集剤25を加え、フロックを形成させた後、沈殿槽26で沈殿させ、フッ化マグネシウム成分が主体のMgF2スラリー71を得た。硫黄析出槽32とその後段にある沈殿槽26の上部からは、硫化水素ガスが2〜5ppm程度検知されているが、そのガスは、排気ファン39で系外に排出した(図15)。
【0087】
その際の、水質を、表16に示す。希釈後の浸出廃液1中のチオ硫酸イオンは、ほぼ全量、硫黄析出槽32で硫黄と亜硫酸イオンに自己分解している。また、亜硫酸イオンは、MgF2析出・酸化槽90において、ほぼ全量エアー5により自然酸化され、それに伴い、COD値も低下している。また、フッ素イオンは、MgF2析出・酸化槽90内で析出し、処理水4中のF濃度は56mg/Lまで低下している。回収した硫黄スラリー38中の硫黄濃度は、86%であり、回収したMgF2スラリー71中のMgF2濃度は、ドライ換算で、75%であった。
【0088】
【表16】

【0089】
(実施例9)
実施例2で生成した浸出廃液を水道水で4倍希釈した浸出廃液1を10ml/分で、硫黄析出槽32(0.6L)に連続投入し、攪拌機13で混合した。pH調整剤として5%硫酸85を添加し、硫黄析出槽32内のpH2.5〜3.0に維持し、浸出廃液1中のチオ硫酸イオンを自己分解させ、硫黄を析出させ、亜硫酸イオンを生成させた。その後、高分子凝集剤25を加え、フロックを形成させた後、沈殿槽26で沈殿させ、硫黄を含む硫黄スラリー38を得た。沈殿槽26からの亜硫酸イオンを含む処理水40は、CaF2析出・酸化槽90に投入し、エアー5で撹拌した。CaF2析出・酸化槽90に3%水酸化カルシウムスラリー66を添加し、CaF2析出・酸化槽90内のpHを7.0〜7.5に維持しながら、亜硫酸イオンを空気酸化させた。その後、高分子凝集剤25を加え、フロックを形成させた後、沈殿槽26で沈殿させ、フッ化カルシウム成分が主体のCaF2スラリー71を得た。硫黄析出槽32とその後段にある沈殿槽26の上部からは、硫化水素ガスが2〜5ppm程度検知されているが、そのガスは、排気ファン39で系外に排出した(図15)。
【0090】
その際の、水質を、表17に示す。希釈後の浸出廃液1中のチオ硫酸イオンは、ほぼ全量、硫黄析出槽32で硫黄と亜硫酸イオンに自己分解している。また、亜硫酸イオンは、CaF2析出・酸化槽90において、ほぼ全量エアー5により自然酸化され、それに伴い、COD値も低下している。また、フッ素イオンは、CaF2析出・酸化槽90内で析出し、処理水4中のF濃度は12mg/Lまで低下している。回収した硫黄スラリー38中の硫黄濃度は、84%であり、回収したCaF2スラリー71中のCaF2濃度及びCaSO4濃度は、ドライ換算で、それぞれ、38%、47%であった。
【0091】
【表17】

【0092】
以上、添付図面を参照しながら本発明の好適な実施形態について説明したが、本発明はかかる例に限定されないことは言うまでもない。当業者であれば、特許請求の範囲に記載された範疇内において、各種の変更例または修正例に想到し得ることは明らかであり、それらについても当然に本発明の技術的範囲に属するものと了解される。
【符号の説明】
【0093】
1・・・浸出廃液
2・・・微生物担体
3・・・生物反応槽
4・・・処理水
5・・・エアー
12・・・硝酸廃液
13・・・撹拌機
15・・・脱窒槽
16・・・蓋
22・・・有機物含有廃液
25・・・高分子凝集剤
26・・・沈澱槽
32・・・硫黄析出槽
34・・・酸
38・・・硫黄スラリー
39・・・排気ファン
40・・・硫黄析出工程からの処理水
41・・・MgF2析出・酸化槽
43・・・マグネシウム化合物
44・・・pH調整剤
45・・・pH計
48・・・MgF2スラリー
51・・・CaF2析出・酸化槽
53・・・カルシウム化合物
58・・・CaF2・CaSO4スラリー(フッ化カルシウムと石膏の混合スラリー)
64・・・MgF2析出槽、または、CaF2析出槽
66・・・MgOスラリー、または、Ca(OH)2スラリー
71・・・MgF2スラリー、または、CaF2スラリー
85・・・硫酸
90・・・MgF2析出・酸化槽、または、CaF2析出・酸化槽
【技術分野】
【0001】
本発明は、金属精錬炉や金属還元炉等から発生する亜鉛を含むダスト中のフッ素イオン及び/又は塩素イオンを分離除去し、亜鉛の精錬原料として、リサイクルする際の前処理技術である。
【背景技術】
【0002】
一般に、事業場や一般家庭から排出されるゴミ(「都市ゴミ」又は「一般廃棄物」と称されている。)は、都市ゴミ焼却場や産業廃棄物焼却工場等に集められ焼却処分されている。その際に焼却炉等から発生する焼却灰や飛灰(1次ダストともいう。)は、薬剤処理、又は、熔融炉、セメントキルン処理等の中間処理を施した後に最終処分場に堆積されている。
【0003】
また、製鉄精錬時に発生する鉄分主体の1次ダスト(例えば、転炉ダスト T−Fe:59%)は、回転炉床炉(回転炉床式還元炉、例えば、特許文献1や特許文献2を参照)や還元熔融ロータリーキルン炉(例えば、特許文献3を参照)等の還元炉で還元され、還元鉄を製造している。
【0004】
しかしながら、上記の熔融炉やセメントキルン処理等の中間処理や製鉄ダスト用の回転炉床等の還元炉では、蒸気圧の高い亜鉛、鉛、カドミウム等の重金属は炉内で揮発して排ガス中に入り、この排ガスに入った重金属は排ガス処理設備内で凝縮して再び飛灰(以降、2次ダストという。)となってしまうという問題があった。この再度の飛灰中には、塩素、フッ素、ナトリウム、カリウムと共に、亜鉛、鉛、カドミウム等の重金属が濃縮されて多量に含有されており、これらの回収を含めた安定した2次ダストの処理方法が求められていた。
【0005】
この2次ダスト中の亜鉛を回収する手段として、亜鉛精錬の原料として、主原料である亜鉛精鉱等と混合し、使用する方法がある。この場合、2次ダスト中の塩素やフッ素が塩化水素、フッ化水素のガスになり、耐火物を劣化させるという問題があり、配合率を抑制せねばならないという課題があった。
【0006】
これに対して、従来技術として、後述する水洗処理(比較例1)やアルカリ浸出処理(特許文献4、又は、比較例2)が開示されている。特許文献4では、アルカリ剤として好ましくは水酸化ナトリウムの溶液を飛灰に加えて重金属を浸出した後、このスラリーを希釈し、さらに鉱酸を添加してpH7〜13に調整した後、重金属含有殿物と塩素含有液とに分別することが開示されている。
【0007】
しかしながら、これらの処理(比較例1、比較例2)では、水洗処理後及びアルカリ浸出処理後の回収殿物中の塩素濃度は、それぞれ、2.0%、1.3%へ、フッ素濃度は、それぞれ、7.6%、0.7%へ低下したものの、十分に低い値ではない。水処理後の2次ダストとアルカリ浸出処理後の2次ダストをEPMA(Electron Probe Micro Analyzer、電子線マイクロアナライザ)を使用し、粒子断面を見ると、水洗処理やアルカリ浸出処理では、2次ダスト中の粒子内部まで水が到達することができないところがあり、そのため、塩素やフッ素成分は減少するものの、十分には低下しないためと推測している。
【0008】
また、亜鉛原料として主に使用されている亜鉛精鉱(例えば、主成分 Zn:52%、S:31%)中の硫黄成分は硫化物として存在し、亜鉛精錬段階にある燃焼工程で熱源として使用されている。この亜鉛精鉱と比較して、これらの飛灰は酸化物であり、還元硫黄を含まない。よって、亜鉛原料として、飛灰の混合比率を増加させていくと、熱源となる還元硫黄の含有比率が少なくなり、熱源が少なくなるという課題があった。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特公昭45−19569号公報
【特許文献2】特開平11−279611号公報
【特許文献3】特開2002−286209号公報
【特許文献4】特開2003−211122号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
このように、亜鉛濃度が高く、塩素、フッ素、ナトリウム、カリウムを含んだ2次ダストを亜鉛原料として利用する際に、主原料である亜鉛精鉱等に混合し利用した場合、飛灰中の塩素やフッ素が、塩化水素、ふっ化水素のガスになり、耐火物を傷める。そこで、塩素及び/又はフッ素を含み、かつ、亜鉛濃度が高いダストから、塩素、フッ素、ナトリウム、カリウムを分離することが課題である。
【0011】
そこで、本発明は、上記課題を解決し得る簡便で効率的なダストの処理方法を提供することを目的とする。
【課題を解決するための手段】
【0012】
前記の課題に対し、本発明者は、亜鉛濃度が高い2次ダストの主成分を酸化物から硫化物に変化させることにより、2次ダスト中のフッ素及び/又は塩素成分の殆ど全てが分離でき、かつ、ダスト中の酸化物を硫化物にすることで、亜鉛精錬における熱源を付加できることを見出した。これは、2次ダストの主成分(例えば、ZnO)を硫化物に変化させることで、粒子内に空隙が生じ、内部まで水が到達することができ、かつ、フッ素や塩素の化合物(ZnOHFやPbClF)が硫化物(ZnS、PbS)となり、フッ素や塩素は陰イオンとなり、殆ど全量浸出させることができるものと推測している。また、2次ダスト中の酸化物を硫化物にする硫黄源として、硫化物イオンを含む硫化ナトリウムや硫化カリウムや硫化マグネシウム等の硫化化合物や、多硫化物イオンを含む多硫化ナトリウム、多硫化カリウム、多硫化マグネシウム等の多硫化化合物が好ましいことを見出した。
【0013】
以下に課題を解決するための手段について詳細に説明する。
【0014】
まず、2次ダスト中の酸化物の硫化物への変化について、説明する。
【0015】
多硫化物イオンを含むアルカリ水溶液に、亜鉛を含む2次ダストを混合することで、2次ダスト中のフッ化ナトリウムや塩化ナトリウムは溶解し、酸化物やフッ化物や塩化物は硫化物となり、2次ダスト中の塩素及び/又はフッ素は分離される。これは、2次ダスト中の酸化物やフッ化物や塩化物が、より安定な硫化物に化学変化するために起こる現象であると考える。つまり、酸化亜鉛やフッ化亜鉛やフッ化塩素亜鉛は硫化亜鉛に、酸化鉛やフッ化鉛やフッ化塩素鉛は硫化鉛に、酸化カドミウムは硫化カドミウムになり、安定化する。その多硫化物イオンを含むアルカリ水溶液は、多硫化ナトリウム水溶液と、水酸化ナトリウム水溶液、水酸化カリウム水溶液、炭酸ナトリウム水溶液、炭酸水素ナトリウム水溶液、炭酸カリウム水溶液等のアルカリ水溶液を混合することによって作ることができる。但し、酸化カルシウムや水酸化カルシウム等のカルシウムを含むアルカリ水溶液を使用すると、後段の2次ダストからフッ素成分を浸出する際に、フッ化カルシウムを析出させてしまい、フッ素成分を分離できなくなる。また、アルカリ水溶液に元素硫黄を入れ、40℃以上100℃以下で、pH7.5〜14の領域で、0.5〜5時間熱することで、多硫化物イオンを含むアルカリ水溶液(黄水ともいう)を作ることができる。この際、(式1)に示すように、多硫化ナトリウムの他に亜硫酸ナトリウムやチオ硫酸ナトリウムが副生する。
NaOH、S ⇒ Na2S2〜4、Na2SO3、Na2S2O3 … (式1)
【0016】
投入した元素硫黄は、硫黄換算で、硫化物イオン、亜硫酸イオン、チオ硫酸イオン、硫酸イオンとして、それぞれ、約45〜50%、4〜6%、30〜35%、1〜3%に分解している。水温が高いほど、pHが高いほど、黄水の生成速度は大きくなる。硫黄としては、試薬の元素硫黄を使うこともできるが、撥水性が強く、黄水を生成するのに時間がかかるという欠点がある。これに対して、界面活性剤を少量混合することで硫黄の撥水性はほぼなくなり、硫黄と液の固液界面が多くなり、黄水の生成速度が大きくなる。また、コークスガスの脱硫時に発生する硫黄を使用すると、撥水性が殆どないため、黄水の生成時間を短くできる。また、黄水の生成領域はpH7.5〜14の領域であるため、黄水生成と同時にダストを入れても、ダスト中のフッ素や塩素を浸出することができる。この場合に使用するアルカリ成分として、水酸化ナトリウム、水酸化カリウム、炭酸ナトリウム、炭酸水素ナトリウム、炭酸カリウム等のアルカリ成分を混合するとよい。但し、酸化カルシウムや水酸化カルシウムなどのカルシウムを含むアルカリ成分を使用すると、後段の2次ダストからフッ素成分を浸出する際に、フッ化カルシウムを析出させてしまい、フッ素成分を分離できなくなる。
【0017】
また、黄水は、ダスト中の金属酸化物と反応すると、多硫化物イオンは、硫化物イオンを放出し、硫化亜鉛等の硫化金属となるため(式2)、多硫化物イオンは減少し、黄水は黄色から透明になり、ある波長に対する吸光度は減少する。その状況を示したのが、図1である。図1は、黄水の各吸収波長における吸光度と、黄水処理後で多硫化物イオンが殆どないときにおける各吸収波長における吸光度を示している。図1より、吸収波長270〜500nmにおける吸光度を測定することで、多硫化物イオンの未反応量を測定することができる。また、pH7.5〜14における反応であるため、硫化物イオン又は硫化水素イオン(HS−)として水溶液中に存在するため、硫化水素を形成し難く、硫化水素ガスとしても殆ど発生しない。
Sn2− + MeO → MeS + Sn−12− (但し、n=2〜4)
… (式2)
【0018】
また、アルカリ水溶液として、製鉄プロセスの圧延工程から廃棄される含油アルカリ廃液を使用することができる。含油アルカリ廃液は、様々な成分のものがあるが、pH12以上、油分は5%以下のものが好ましい。含油アルカリ廃液中のアルカリ成分は、主に水酸化ナトリウムであり、前述の黄水形成時のアルカリ成分として作用する。含油アルカリ廃液中の油分は、2次ダストの凝集剤となり、硫化物処理後の2次ダストと浸出液の固液分離性を向上させると同時に、油分が2次ダストに付着することにより、硫化処理後の2次ダストを亜鉛原料として精錬炉で利用する際の熱源となる。また、2次ダストに付着しなかった油分は、後述するCOD(化学酸素要求量)成分の生物酸化において、有機物成分となり、微生物フロックを形成し易い従属栄養性の微生物もしくは糸状菌を繁殖させる基質(餌ともいう)となる。しかしながら、油分を多く入れ過ぎると、硫化処理後の硫化物の脱水時において、脱水性を悪化させることになり、投入量については調整が必要となる。
【0019】
次に、黄水処理後に発生する浸出廃液の処理方法について、述べる。
【0020】
黄水処理後の浸出廃液中には、黄水生成時の反応において、副生した亜硫酸イオン、チオ硫酸イオン等と、反応しなかった少量の硫化物イオン、多硫化物イオンを含んでいる。これらのイオンは、CODとして測定されるため、黄水処理した浸出廃液を、無処理のまま一般水域への放出はできない。また、2次ダスト中のフッ素含有率にもよるが、黄水処理後の浸出廃液中には、2次ダストから浸出したフッ素イオンを1000〜30000mg/L含んでおり、やはり、未処理のまま一般水域への放出はできない。
【0021】
COD成分である、副生した亜硫酸イオン、チオ硫酸イオン等と、反応しなかった少量の硫化物イオン、多硫化物イオンは、次の方法により、酸化分解もしくは一部硫黄として回収することができる。
【0022】
酸化分解の方法としては、大きく分けて、微生物等の酸化力を利用した生物処理や、溶存酸素による酸化や塩素や6価クロム等の酸化剤による化学処理がある。
【0023】
生物処理としては、活性汚泥処理、硫黄酸化細菌によるCOD成分の酸化処理、硫黄酸化細菌による硫黄脱窒が考えられる。詳細は、後述する。
【0024】
化学処理について説明する。溶存酸素による酸化は、亜硫酸イオンは容易に常温で酸化されるが、チオ硫酸イオンは酸化され難い。次亜塩素酸や塩素、6価クロム等の酸化剤を使用すると、短時間で亜硫酸イオンやチオ硫酸イオンは酸化される。
【0025】
また、チオ硫酸イオンは、酸性領域(pH4以下、好ましくはpH3以下)で元素硫黄と亜硫酸イオンに自己分解する特性を有している。
【0026】
一方、フッ素成分を浸出廃液中から分離するためには、溶解度の小さいフッ化カルシウム、フッ化マグネシウム等として析出すればよい。マグネシウム源又はカルシウム源として、酸化マグネシウム、塩化マグネシウム、酸化カルシウム、水酸化カルシウム、塩化カルシウムを浸出液中に投入することで、フッ化カルシウム、フッ化マグネシウムの析出物を得ることができる。
【0027】
浸出廃液中にカルシウム源として酸化カルシウム、水酸化カルシウム、塩化カルシウムを投入した場合、浸出液中の硫酸濃度又は亜硫酸濃度が高いため、フッ化カルシウムの析出と同時に、硫酸カルシウムや亜硫酸カルシウムの析出物が生じることが多い。副生したフッ化カルシウムと硫酸カルシウムの混合物は、安定的で脱水後、最終処分することができる。
【0028】
浸出廃液中にマグネシウム源として、酸化マグネシウム、塩化マグネシウムを投入した場合、硫酸マグネシウムの溶解度は高く、また、亜硫酸マグネシウムの溶解度は低い。しかし、亜硫酸イオンは空気酸化し易く、硫酸マグネシウムとなるため溶解し易く、硫酸マグネシウムは析出し難い。そのため、フッ化マグネシウムを主体とする副産物が生成される。黄水処理後の浸出廃液中のチオ硫酸イオン及び亜硫酸イオンを次亜塩素酸ナトリウム溶液で酸化した浸出廃液(硫酸イオン濃度17,500mg/L、フッ素イオン濃度10,500mg/L)に塩化マグネシウムを投入した際のフッ素イオン及び硫酸イオンの析出状況を図2に示す。pH10以上では、投入した塩化マグネシウムの表面上にフッ化マグネシウムがコーテイングしてしまい、未反応分が生じ、浸出廃液中のフッ素濃度は低下しにくくなるが、pH9以下では、投入した塩化マグネシウムの表面上にフッ化マグネシウムのコーテイングが生じ難いため、殆ど反応し、浸出廃液中のフッ素イオン濃度を30〜40mg/Lまで低下させる。なお、フッ化マグネシウムは、フッ酸製造原料や、製鉄プロセスにおける精錬工程で使用する蛍石の代替として使用することができる。
【0029】
本発明は、上記知見に基づいてなされたものであり、その要旨は以下のとおりである。
(1) 亜鉛を含むダストを、多硫化物イオンを含みアルカリ土類金属を含まないアルカリ水溶液に混合して、ダスト中の金属酸化物を金属硫化物に反応させると共に、ダスト中の塩素及び/又はフッ素をダスト中から浸出させ、金属硫化物を主体とする固形分と浸出廃液とに分離することを特徴とする、ダストの処理方法。
(2) 亜鉛含むダストを硫黄と共にアルカリ土類金属を含まないアルカリ水溶液に混合して、40℃以上100℃以下の液温下で攪拌して、ダスト中の塩素及び/又はフッ素をダスト中から浸出させ、金属硫化物を主体とする固形分と浸出廃液とに分離することを特徴とする、ダストの処理方法。
(3) 前記アルカリ水溶液が、製鉄プロセスにおける圧延工程から排出される含油アルカリ廃液である、(1)又は(2)のいずれかに記載のダストの処理方法。
(4) 前記浸出廃液に対して、270〜500nmの領域の吸収波長を測定して前記硫化反応の進捗状況を把握する、(1)〜(3)のいずれかに記載のダストの処理方法。
(5) 前記浸出廃液に対して、マグネシウム化合物を含んだ水溶液又はスラリーを入れた後、又は、入れながら、pH5〜9に調整して、フッ素イオンをフッ化マグネシウムとして析出させ、固液分離する、(1)〜(4)のいずれかに記載のダストの処理方法。
(6) 前記浸出廃液に対して、カルシウム化合物を入れた後、又は、入れながら、pHを4〜10に調整することで、フッ素イオン及び/又は硫酸イオンをカルシウム塩として析出させ、固液分離する、(1)〜(5)のいずれかに記載のダストの処理方法。
(7) 前記浸出廃液中のCOD成分をさらに分解する、(1)〜(6)のいずれかに記載のダストの処理方法。
(8) (1)〜(4)のいずれかに記載の処理方法で分離された浸出廃液に対して、酸を投入しpHを4以下に調整して、硫黄を析出・分離してから、硫黄分離後の浸出廃液にマグネシウム化合物を入れた後、又は、入れながら、pH5.5〜6.5に調整することで、フッ素イオンをフッ化マグネシウムとして析出させ、分離することを特徴とする、ダストの処理方法。
(9) (1)〜(4)のいずれかに記載の処理方法で分離された浸出廃液に対して、酸を投入しpHを4以下に調整して、硫黄を析出・分離してから、硫黄分離後の浸出廃液にカルシウム化合物を入れた後、又は、入れながら、pH5.5〜8に調整することで、フッ素イオン及び/又は硫酸イオンをカルシウム塩として析出させ、分離することを特徴とする、ダストの処理方法。
【発明の効果】
【0030】
熔融炉やセメントキルン等の中間処理や製鉄ダスト用の回転炉床等の還元炉から発生する2次ダストは、本発明により、塩素及びフッ素含有率が著しく低下し、硫化亜鉛が主成分となる黄水処理ダストとなり、亜鉛精錬原料となる。また、脱塩素又は脱フッ素過程で生じる浸出廃液から、フッ化カルシウムやフッ化マグネシウムを回収することができる。
【図面の簡単な説明】
【0031】
【図1】吸収波長に対する吸光度の比較を示す図である。
【図2】浸出廃液に塩化マグネシウムを投入した際のフッ素イオン及び硫酸イオンの析出状況を示す図である。
【図3】本発明のダストの処理方法の一例を示す図である。
【図4】浸出廃液の微生物を用いた処理槽の構成例を示す図である。
【図5】浸出廃液の微生物を用いた処理槽の他の構成例を示す図である。
【図6】浸出廃液の微生物を用いた処理槽の別の構成例を示す図である。
【図7】本発明のダストの処理方法の他の例を示す図である。
【図8】硫黄析出工程における処理槽の構成例を示す図である。
【図9】MgF2析出・酸化工程における処理層の構成例を示す図である。
【図10】MgF2析出・酸化工程における処理層の他の構成例を示す図である。
【図11】比較例2におけるダスト処理方法を示す図である。
【図12】実施例1におけるダスト処理方法を示す図である。
【図13】実施例2におけるダスト処理方法を示す図である。
【図14】実施例3における浸出廃液の微生物を用いた処理槽の構成を示す図である。
【図15】実施例4における浸出廃液の微生物を用いた処理槽の構成を示す図である。
【発明を実施するための形態】
【0032】
以下に添付図面を参照しながら、本発明の好適な実施の形態について詳細に説明する。なお、本明細書及び図面において、実質的に同一の機能構成を有する構成要素については、同一の符号を付することにより重複説明を省略する。
【0033】
本発明について、以下に詳細に説明する。
【0034】
図3に本発明のダストの処理方法の一例(例1)を示す。図3では、『黄水生成』『黄水処理』『水洗』の工程からなる黄水処理プロセスと、『MgF2析出』『生物酸化』の工程からなる浸出廃液の処理プロセスとからなっている。
【0035】
それぞれの工程について、説明を行う。
【0036】
『黄水生成』工程では、アルカリ溶液に元素硫黄を入れ、40℃以上100℃以下で、pH7.5〜14の領域で、0.5〜5時間程度で、多硫化物イオンを含む溶液を作ることができる。より好ましくは、80℃以上100℃以下、pH10〜13の領域で1時間程度で、多硫化物イオンを含む溶液を作ることができる。この際、亜硫酸イオンやチオ硫酸イオンも副生する。
【0037】
『黄水処理』工程では、2次ダストと『黄水生成』工程で生成した黄水とを混合し、2次ダスト中の亜鉛、鉛、カドミウム等の重金属を硫化物にし、安定化する(式3)。この『黄水処理』工程では、40℃以上100℃以下で、pH7.5〜14の領域で、0.5〜5時間程度行うことが好ましい。より好ましくは、80℃以上100℃以下、pH10〜12の領域で1時間程度で行うことが好ましい。アルカリ領域では、黄水からの硫化水素の発生が抑制される。(式3)で生じたSn−12−イオンは、(式4)に示すように、元素硫黄と反応し、Sn2−イオンとなる。
Sn2− + MeO → MeS + Sn−12− (但し、n=2〜4)
… (式3)
Sn−12− + S → Sn2− … (式4)
【0038】
『水洗』工程では、『黄水処理』工程で生成した硫化亜鉛等を含む黄水処理スラリーを、水洗し、黄水処理スラリー中の液相(亜硫酸イオンやチオ硫酸イオンを含む)を洗い流す工程である。水洗された黄水処理スラリーは脱水し、硫化物(主に硫化亜鉛)を含む黄水処理ケーキとなり、それを亜鉛原料として利用することができる。
【0039】
『MgF2析出』工程では、『黄水処理』工程から発生した2次ダストの浸出廃液中のフッ素イオンをフッ化マグネシウムとして析出させ、フッ化マグネシウムのスラリーとして分離する。そのため、浸出廃液中には、マグネシウム化合物を投入するが、マグネシウム化合物(酸化マグネシウム又は水酸化マグネシウム又は塩化マグネシウム)はアルカリ領域では溶解し難く、マグネシウム化合物の未反応物が残り、酸性側(pH4以下)では、溶解性フッ素濃度は高くなる。よって、マグネシウム化合物投入後のpHを5〜9程度、好ましくは、pH5〜7にコントロールすることで、マグネシウム化合物の未反応物は殆どなく、析出したMgF2を分離した液相のフッ素濃度は30〜60mg/L程度になる。
【0040】
『生物酸化』工程では、独立栄養細菌である硫黄酸化細菌を利用したり、有機物を基質とする従属栄養細菌の集合体である活性汚泥を利用することができる。
【0041】
繁殖させる微生物の特徴を説明し、それに適当な処理方法を説明する。
【0042】
独立栄養細菌である硫黄酸化細菌の一部の微生物(例として、Thiobacillus thioparus、Thiobacillus neapolitanus等)は、好気条件、つまり溶存酸素がある場合には、溶存酸素を利用して、亜硫酸イオンやチオ硫酸イオンや元素硫黄等の還元性硫黄を硫酸イオンまで酸化し、エネルギーを得、水中に溶解した二酸化炭素を炭素源としてたんぱく質等を合成し、増殖している。生育pHは、4.5〜8.5、生育温度は8〜39℃である。この微生物自体では、活性汚泥処理法で見られるような生物フロックを作ることは難しいため、生物反応槽内に固定する必要があり、礫やスラグや素焼き物等の微生物担体を使用することで硫黄酸化細菌を固定することが望ましい。余剰汚泥が少ないことも特徴である。これらの微生物の特徴から、図4の処理システムで亜硫酸イオンやチオ硫酸イオン等のCOD成分を酸化分解することができる。生物反応槽3内に硫黄酸化細菌が付着する微生物担体2を設置し、亜硫酸イオンやチオ硫酸イオンを含む浸出廃液1は、硫黄酸化細菌が付着する微生物担体2を設置した生物反応槽3に投入し、生物反応槽3内にエアー5を吹き込むことで、酸化することができる。亜硫酸イオンやチオ硫酸イオン等のCOD成分が酸化分解された浸出廃液1は、処理水4として放流される。
【0043】
独立栄養細菌である硫黄酸化細菌の一部の種類(例として、Thiobacillus denitrificans)は、嫌気条件、つまり溶存酸素が全く存在しない場合で、硝酸イオンや亜硝酸イオンが存在している時、硝酸イオンや亜硝酸イオンの酸素を利用して、亜硫酸イオンやチオ硫酸イオンや元素硫黄等の還元性硫黄を硫酸イオンまで酸化し、エネルギーを得ながら、硝酸イオンや亜硝酸イオンは窒素ガスまで還元し、水中に溶解した二酸化炭素を炭素源としてたんぱく質等を合成し、増殖している。生育pHは、6〜9、生育水温は15〜35℃で、原水中のS/N比を3〜7(g/g)にすると良い。この場合も、活性汚泥処理法で見られるような生物フロックを作ることは難しいため、礫やスラグや素焼き物等の微生物担体を使用することで硫黄酸化細菌を固定することが望ましい。余剰汚泥が少ないことも特徴である。これらの特徴から、図5の処理システムで亜硫酸イオンやチオ硫酸イオン等のCOD成分を酸化しながら、硝酸イオンや亜硝酸イオンを還元していくことができる。脱窒槽15内に硫黄酸化細菌が付着する微生物担体2を設置し、脱窒槽15内を撹拌機13で撹拌させている。脱窒槽15の上部は蓋16をし、空気の混入を遮断している。亜硫酸イオンやチオ硫酸イオンを含む浸出廃液1と、硝酸イオンを含む硝酸廃液12を、硫黄酸化細菌が付着する微生物担体2を設置した脱窒槽15に投入することで、亜硫酸イオンやチオ硫酸イオン等のCOD成分を酸化しながら、硝酸イオンや亜硝酸イオンを還元していくことができる。亜硫酸イオンやチオ硫酸イオン等のCOD成分が酸化分解された浸出廃液1および硝酸イオンや亜硝酸イオンが還元された硝酸廃液12は、処理水4として放流される。
【0044】
従属栄養細菌の集合体である活性汚泥は、好気条件、つまり、溶存酸素が存在する場合で、有機物を基質としながら増殖する。活性汚泥中には、還元性硫黄を酸化できる、硫黄酸化細菌(例えば、Thiobacillus novellus、Thiobacillus versutus等)も生息している。なお、活性汚泥としては、下水処理場やコークス製造時に発生する安水の処理に使用されている。よって、有機物を含有した廃液22と共に、亜硫酸イオンやチオ硫酸イオンを含む浸出廃液1を、活性汚泥を入れた生物反応槽3に投入することで、有機物成分を酸化しながら、亜硫酸イオンやチオ硫酸イオンを酸化させることができる(図6)。生物反応槽3内には、エアー5を吹き込むことが必要である。活性汚泥はフロックを形成するため、図6のように、沈殿槽26で活性汚泥からなるフロックを沈降分離することができる。沈殿槽26で活性汚泥からなるフロックが沈降分離された浸出廃液1および有機物含有廃液22は、処理水4として放流される。
【0045】
図7に、本発明のプロセスの一例(例2)を示す。図7では、『黄水生成』『黄水処理』『水洗』の工程による硫化物回収プロセスと、『硫黄析出』『MgF2析出』の工程による浸出廃液の処理プロセスとからなっている。
【0046】
それぞれの工程について、説明を行う。
【0047】
『黄水生成』『黄水処理』『水洗』の工程による黄水処理プロセスは、図3と同じで、前記の説明のとおりである。
【0048】
『黄水処理』工程から排出された浸出廃液中には、亜硫酸イオン、チオ硫酸イオン、フッ素イオンを含むが、『硫黄析出』工程では、チオ硫酸イオンを酸性条件下(pH4以下、好ましくはpH3以下)で元素硫黄と亜硫酸イオンとに自己分解させる(図8)。硫黄析出槽32内に酸34を投入してpH4以下、好ましくは、pH3以下に維持しながら、撹拌機13で撹拌する。酸34としては、硫酸や塩酸が好ましい。次に、高分子凝集剤25を添加し、固液分離操作、例えば沈殿槽26で、元素硫黄を含む硫黄スラリー38と亜硫酸イオンを含む硫黄析出工程からの処理水40とに分離し、元素硫黄は、『黄水生成』工程に投入し、再度、黄水とする。硫黄析出工程からの処理水40中には、亜硫酸イオン、フッ素イオンを含むが、これらの成分は、次の『MgF2析出・酸化』工程で処理される。なお、『硫黄析出』工程では、pHを酸性側にするため、硫化水素ガスが少量発生する。発生する硫化水素ガスは排気ファン39で吸引し、『黄水処理』工程に投入することで、2次ダスト中の亜鉛成分を硫化物に変化させることができる。
【0049】
『硫黄析出』工程からの処理水40中には、フッ素イオンと亜硫酸イオンを含んでいる。『MgF2析出・酸化』工程では、塩化マグネシウム、酸化マグネシウム、水酸化マグネシウムのいずれかを投入し、フッ素イオンをフッ化マグネシウムとして析出させながら、亜硫酸イオンは、反応槽内に空気を吹き込み空気酸化したり、前述の微生物を用い酸化することができる。
【0050】
フッ化マグネシウムを析出するには、前述のように、マグネシウム化合物(酸化マグネシウム又は水酸化マグネシウム又は塩化マグネシウム)はアルカリ領域では溶解し難く、マグネシウム化合物の未反応物が残り、酸性側では、溶解性フッ素濃度は高くなる。よって、マグネシウム化合物投入後のpHを5〜9程度、好ましくは、pH5〜7にコントロールすることで、マグネシウム化合物の未反応物は殆どなく、MgF2を析出させることができる。一方、亜硫酸イオンを空気酸化させる場合、pHが高いとMgSO3の結晶が析出するため、pH5.5〜6.5に調整すること重要となる。よって、フッ素イオンを析出させながら、亜硫酸イオンを空気酸化するには、pH5.5〜6.5に調整することが好ましい。『MgF2析出・酸化』工程を図9に示す。『硫黄析出』工程から排出される処理水40中にマグネシウム化合物43を投入し、MgF2析出・酸化槽41内でフッ素イオンをフッ化マグネシウムとして析出させながら、MgF2析出・酸化槽41内に、pH調整剤44を添加してpH5.5〜6.5(pH計45により測定)に調整しながら、エアー5により酸素を供給し、亜硫酸イオンを酸化する。その後、高分子凝集剤25を投入し、沈殿槽26で固液分離を行い、MgF2スラリー48と処理水4とに分離される。処理水4は放流され、MgF2スラリー48は脱水機で脱水し、MgF2ケーキを得ることができる。
【0051】
また、『硫黄析出』工程からの処理水40中に、炭酸カルシウム、塩化カルシウム、酸化カルシウム、水酸化カルシウム(消石灰ともいう)のいずれかのカルシウム化合物53を投入し、フッ素イオンをフッ化カルシウムとして析出させながら、亜硫酸イオンは、CaF2析出・酸化槽51内にエアー5を吹き込み空気酸化したり、前述の微生物を用い酸化することができる。この工程を『CaF2析出・酸化』工程(図10)を説明する。『硫黄析出』工程から排出される処理水40は、CaF2析出・酸化槽51に投入され、pH調整剤44を添加してpH5.5〜8(pH計45により測定)に調整しながら、エアー5により酸素を供給し、亜硫酸イオンを硫酸イオンに酸化する。硫酸イオンは石膏となり、析出し、フッ素イオンはフッ化カルシウムとして析出する。その後、高分子凝集剤25を投入し、フロックを形成させ、沈殿槽26で固液分離を行い、フッ化カルシウムと石膏の混合スラリー58と処理水4とに分離される。処理水4は放流され、フッ化カルシウムと石膏の混合スラリー58は脱水機で脱水し、混合ケーキを得ることができる。
【実施例】
【0052】
(比較例1)
ビーカーに1Lの水道水を入れ、製鉄精錬時に発生する鉄分主体の1次ダストを回転炉床炉(回転炉床式還元炉)で還元した際に発生した2次ダスト50g入れ、pH調整はせずに、30分間攪拌した。その後、吸引ろ過を行い、固液分離を行い、浸出廃液と洗浄ダスト(29.1g)を得た。浸出廃液と洗浄ダストに対して、成分分析を行った。その結果を、表1及び表2に示す。洗浄により、洗浄ダスト中のF、Clは低下しているものの、その値は高く、亜鉛の精錬原料としては使用できないものであった。なお、F、Clの残存率は、それぞれ、39%、8%で高い値であった。
【0053】
【表1】

【0054】
【表2】

【0055】
(比較例2)
比較例1で用いたものと同じロットの2次ダストに対し、図11に示すように、アルカリ処理を実施した。ビーカーに、20%水酸化ナトリウム水溶液80mLと水道水170mLを入れ、40℃に保持した中に、2次ダストを50g入れ、10分間強攪拌した。その後、水道水125mLを加えて希釈し、中和剤として98%硫酸を添加して、pH12に調整し、30分間維持しながら、撹拌した。その後、ろ過し、浸出廃液を得た。また、水道水100mLを加え、ケーキ洗浄を行い、アルカリ処理ダスト(28.0g)を得た。
【0056】
浸出廃液とアルカリ処理ダストに対する分析結果を表3と表4に示す。アルカリ処理により、アルカリ処理ダスト中のF、Clは低下しているが、その値は、亜鉛の精錬原料として使用するには、若干高かった。なお、F、Clの残存率は、それぞれ、3.5%、4.9%であった。また、2次ダスト1g当りの薬剤使用量は、水酸化ナトリウムは、0.32gで、硫酸(100%換算)は、0.026gであった。また、浸出廃液中には、フッ素、鉛、6価クロムを含んでおり、一般水域に放出するには、これらの元素を浸出廃液中から分離する必要がある。
【0057】
【表3】

【0058】
【表4】

【0059】
(実施例1)
水道水10Lに20%水酸化ナトリウム水溶液0.78Lと元素硫黄250gを入れ、煮沸させ、浸出液(黄水)を作成した。浸出液中に比較例1で用いたものと同じロットの2次ダストを1000g投入した。pH10以上になるように、20%水酸化ナトリウム水溶液を投入し、30分間撹拌した(図12)。水温は、80℃に制御した。その後、ろ紙で濾過した後、黄水処理ケーキ(黄水処理ダストともいう)と、亜硫酸イオン、チオ硫酸イオン、フッ素イオンを含む浸出廃液とに分離した。その際、ケーキ洗浄水として1Lの水道水を使用した。
【0060】
浸出廃液と黄水処理ダストに対する分析結果を表5と表6に示す。黄水処理により、黄水処理ダスト中のF、Clは、比較例1又は2より低下し、亜鉛の精錬原料として十分使用できる濃度であった。なお、F、Clの残存率は、それぞれ、1.2%、0.4%であった。また、2次ダスト1g当りの薬剤使用量は、水酸化ナトリウムは、0.20gで、元素硫黄は、0.25gであった。また、浸出廃液中には、フッ素とCOD成分(亜硫酸イオン、チオ硫酸イオン等)を含んでおり、一般水域に放出するには、これらの元素を浸出廃液中から分離もしくは分解する必要があるが、比較例2で見られたような6価クロムは含有していない。また、亜硫酸イオンやチオ硫酸イオン濃度から計算されるCOD値は、6,500mg/lであるが、そのCOD値を大幅に上回っている。これは、反応していない多硫化物イオンが残存するためである。
【0061】
【表5】

【0062】
【表6】

【0063】
(実施例2)
水道水10Lに20%水酸化ナトリウム水溶液0.78Lと元素硫黄250gと比較例1で用いたものと同じロットの2次ダスト1100gを入れ、90℃にした。pH10以上になるように、20%水酸化ナトリウム水溶液を投入し、30分ゆっくり撹拌した。その後、ろ紙で濾過した後、黄水処理ケーキと、亜硫酸イオン、チオ硫酸イオン、フッ素イオンを含む浸出廃液とに分離した。その際、ケーキ洗浄水として1Lの水道水を使用した(図13)。
【0064】
浸出廃液と黄水処理ダストに対する分析結果を表7と表8に示す。黄水処理により、黄水処理ダスト中のF、Clは、比較例1又は2より低下し、亜鉛の精錬原料として十分使用できる濃度であった。なお、F、Clの残存率は、それぞれ、0.9%、0%であった。また、2次ダスト1g当りの薬剤使用量は、水酸化ナトリウムは、0.16gで、元素硫黄は、0.23gであった。また、浸出廃液中には、フッ素とCOD成分(亜硫酸イオン、チオ硫酸イオン等)を含んでおり、一般水域に放出するには、これらの元素を浸出廃液中から分離もしくは分解する必要がある。
【0065】
【表7】

【0066】
【表8】

【0067】
(実施例3)
水道水10Lに製鉄プロセスの圧延工程から発生する含油アルカリ排水(pH13.0で水酸化ナトリウムを含む、油分1.4%)1.5Lと元素硫黄250gと比較例1で用いたものと同じロットの2次ダスト1100gを入れ、90℃にした。pH10以上になるように、含油アルカリ排水を投入し、30分ゆっくり撹拌した。その後、ろ紙で濾過した後、黄水処理ケーキと、亜硫酸イオン、チオ硫酸イオン、フッ素イオンを含む浸出廃液とに分離した。その際、ケーキ洗浄水として1Lの水道水を使用した(図13)。
【0068】
浸出廃液と黄水処理ダストに対する分析結果を表9と表10に示す。黄水処理により、黄水処理ダスト中のF、Clは、比較例1又は2より低下し、亜鉛の精錬原料として十分使用できる濃度であった。なお、F、Clの残存率は、それぞれ、1.3%、0.6%であった。また、2次ダスト1g当りの含油アルカリ排水の使用量は、1.36mlで、元素硫黄は、0.23gであった。また、浸出廃液中には、フッ素とCOD成分(亜硫酸イオン、チオ硫酸イオン等)を含んでおり、一般水域に放出するには、これらの元素を浸出廃液中から分離もしくは分解する必要がある。
【0069】
【表9】

【0070】
【表10】

【0071】
(実施例4)
水道水10Lに20%水酸化ナトリウム水溶液0.78Lと元素硫黄250gを入れ、煮沸させ、浸出液(黄水)を作成した。波長400nmで、浸出液の吸光度を測定しながら、吸光度1.5以下になるまで、浸出液中に比較例1で用いたものと同じロットの2次ダストを投入した。pH10以上になるように、20%水酸化ナトリウム水溶液を投入し、30分間撹拌した(図12)。水温は、80℃に制御した。吸光度を測定する際には、浸出液を濾過し、その濾過液に対し、吸光度を測定した。2次ダスト投入量は総計で1100gであった。その後、ろ紙で濾過した後、黄水処理ケーキ(黄水処理ダストともいう)と、亜硫酸イオン、チオ硫酸イオン、フッ素イオンを含む浸出廃液とに分離した。その際、ケーキ洗浄水として1Lの水道水を使用した。
【0072】
浸出廃液と黄水処理ダストに対する分析結果を表11と表12に示す。黄水処理により、黄水処理ダスト中のF、Clは、比較例1又は2より低下し、亜鉛の精錬原料として十分使用できる濃度であった。なお、F、Clの残存率は、それぞれ、1.1%、0%であった。また、2次ダスト1g当りの薬剤使用量は、水酸化ナトリウムは、0.18gで、元素硫黄は、0.23gであった。また、浸出廃液中には、フッ素とCOD成分(亜硫酸イオン、チオ硫酸イオン等)を含んでおり、一般水域に放出するには、これらの元素を浸出廃液中から分離もしくは分解する必要がある。また、亜硫酸イオンやチオ硫酸イオン濃度から計算されるCOD値は、6,800mg/lであり、そのCOD値に近い。これは、反応していない多硫化物イオンが殆ど残存していないためであり、実施例1と比較して、多硫化物イオンをほぼ全量利用したと言える。
【0073】
【表11】

【0074】
【表12】

【0075】
(実施例5)
実施例2で生成した浸出廃液を水道水で4倍希釈した浸出廃液1を1mL/分で微生物担体2として礫岩(10mm以上50mm以下)を充填した生物反応槽3(2L)に連続投入した(図14)。生物反応槽3下部からは、エアー5を投入し、硫黄酸化細菌によるチオ硫酸イオンや亜硫酸イオンの酸化に必要な酸素を供給した。生物反応槽3のpHは5.5〜6.0になるように、1%水酸化ナトリウム水溶液を入れ、pH制御を行った。なお、生物反応槽5は、事前に回分状態にて、浸出廃液を入れ、硫黄酸化細菌を馴養させている。
【0076】
生物反応槽5から得た処理水40を、連続して、MgF2析出槽64(0.5L)に投入し、3%酸化マグネシウムスラリー66を投入し、pH調整剤44として1%水酸化ナトリウム水溶液を添加してpH6〜6.5(pH計45により測定)に調整した。生物反応槽3からの処理水中のフッ素イオンは、フッ化マグネシウムとして析出させた。その後、高分子凝集剤25を投入しフロックを形成させ、沈殿槽26で沈殿させ、処理水4を放流した。沈殿槽26で沈殿したMgF2スラリー71の一部は、MgF2析出槽64に戻し、残りは回収した。
【0077】
その際の、水質を、表13に示す。希釈浸出廃液1中のCOD成分である亜硫酸イオンやチオ硫酸イオンは、生物反応槽3内で、ほぼ全量、硫酸イオンまで分解されている。また、フッ素イオンはMgF2析出槽内で析出し、処理水4中のF濃度は56mg/Lまで低下している。回収したMgF2スラリー71中のMgF2濃度は、ドライ換算で、82%であった。
【0078】
【表13】

【0079】
(実施例6)
実施例2で生成した浸出廃液を水道水で4倍希釈した浸出廃液1を1mL/分で微生物担体2として礫岩(10mm以上50mm以下)を充填した生物反応槽3(2L)に連続投入した(図14)。生物反応槽3下部からは、エアー5を投入し、硫黄酸化細菌によるチオ硫酸イオンや亜硫酸イオンの酸化に必要な酸素を供給した。生物反応槽3のpHは5.5〜6.0になるように、pH調整剤44として1%水酸化ナトリウム水溶液を入れ、pH制御を行った。なお、生物反応槽3は、事前に回分状態にて、浸出廃液1を入れ、硫黄酸化細菌を馴養させている。
【0080】
生物反応槽3から得た処理水40を、連続して、CaF2析出槽64(0.5L)に投入し、3%水酸化カルシウムスラリー66を投入し、pH7〜7.5(pH計45により測定)に調整した。処理水中のフッ素イオンは、フッ化カルシウムとして析出させた。その後、高分子凝集剤25を投入しフロックを形成させ、沈殿槽26で沈殿させ、処理水4を放流した。沈殿槽26で沈殿したCaF2スラリー71の一部は、CaF2析出槽64に戻し、残りは回収した。
【0081】
その際の、水質を、表14に示す。希釈後の浸出廃液1中のCOD成分である亜硫酸イオンやチオ硫酸イオンは、生物反応槽3内で、ほぼ全量、硫酸イオンまで分解されている。また、フッ素イオンはCaF2析出槽64内で析出し、処理水4中のF濃度は12mg/Lまで低下している。回収したCaF2スラリー71中のCaF2濃度及びCaSO4濃度は、ドライ換算で、それぞれ、40%、48%であった。
【0082】
【表14】

【0083】
(実施例7)
実施例2で生成した浸出廃液を水道水で4倍希釈した浸出廃液1を1mL/分でMgF2析出・酸化槽41(2L)に連続投入した(図9)。MgF2析出・酸化槽41の下部からは、エアー5を投入し、硫黄酸化細菌によるチオ硫酸イオンや亜硫酸イオンの酸化に必要な酸素を供給した。MgF2析出・酸化槽41のpHは6.0〜6.5になるように、マグネシウム化合物43として、5%酸化マグネシウムスラリーを入れ、pH制御を行い、COD成分である亜硫酸イオンやチオ硫酸イオンを生物酸化させながら、浸出廃液1中のフッ素イオンを弗化マグネシウムとして析出させた。MgF2析出・酸化槽41から越流したスラリーに対して、高分子凝集剤25を投入して、フロックを作成し、沈澱槽26にて沈澱させた。沈澱させたMgF2スラリー48中には、硫黄酸化細菌が付着していることから、一部、MgF2析出・酸化槽41へ返送しながら、残りのMgF2スラリー48は沈澱槽26より回収した。なお、MgF2析出・酸化槽41内に投入した硫黄酸化細菌は、事前に回分状態にて、浸出廃液1を入れ、硫黄酸化細菌を馴養させている。
【0084】
その際の、水質を、表15に示す。希釈後の浸出廃液1中のCOD成分である亜硫酸イオンやチオ硫酸イオンは、MgF2析出・酸化槽41内で、ほぼ全量、硫酸イオンまで分解され、フッ素イオンは析出し、処理水中のF濃度は79mg/Lまで低下している。回収したMgF2スラリー中のMgF2濃度は、ドライ換算で、78%であった。
【0085】
【表15】

【0086】
(実施例8)
実施例2で生成した浸出廃液を水道水で4倍希釈した浸出廃液1を10ml/分で、硫黄析出槽32(0.6L)に連続投入し、攪拌機13で混合した。pH調整剤として5%硫酸85を添加し、硫黄析出槽32内のpHを2.5〜3.0に維持し、浸出廃液1中のチオ硫酸イオンを自己分解させ、硫黄を析出させ、亜硫酸イオンを生成させた。その後、高分子凝集剤25を加え、フロックを形成させた後、沈殿槽26で沈殿させ、硫黄を含む硫黄スラリー38を得た。沈殿槽26からの亜硫酸イオンを含む処理水40は、MgF2析出・酸化槽90に投入し、エアー5で撹拌した。MgF2析出・酸化槽90に3%酸化マグネシウムスラリー66を添加し、MgF2析出・酸化槽90内のpHを5.5〜6.0に維持しながら、亜硫酸イオンを空気酸化させた。その後、高分子凝集剤25を加え、フロックを形成させた後、沈殿槽26で沈殿させ、フッ化マグネシウム成分が主体のMgF2スラリー71を得た。硫黄析出槽32とその後段にある沈殿槽26の上部からは、硫化水素ガスが2〜5ppm程度検知されているが、そのガスは、排気ファン39で系外に排出した(図15)。
【0087】
その際の、水質を、表16に示す。希釈後の浸出廃液1中のチオ硫酸イオンは、ほぼ全量、硫黄析出槽32で硫黄と亜硫酸イオンに自己分解している。また、亜硫酸イオンは、MgF2析出・酸化槽90において、ほぼ全量エアー5により自然酸化され、それに伴い、COD値も低下している。また、フッ素イオンは、MgF2析出・酸化槽90内で析出し、処理水4中のF濃度は56mg/Lまで低下している。回収した硫黄スラリー38中の硫黄濃度は、86%であり、回収したMgF2スラリー71中のMgF2濃度は、ドライ換算で、75%であった。
【0088】
【表16】

【0089】
(実施例9)
実施例2で生成した浸出廃液を水道水で4倍希釈した浸出廃液1を10ml/分で、硫黄析出槽32(0.6L)に連続投入し、攪拌機13で混合した。pH調整剤として5%硫酸85を添加し、硫黄析出槽32内のpH2.5〜3.0に維持し、浸出廃液1中のチオ硫酸イオンを自己分解させ、硫黄を析出させ、亜硫酸イオンを生成させた。その後、高分子凝集剤25を加え、フロックを形成させた後、沈殿槽26で沈殿させ、硫黄を含む硫黄スラリー38を得た。沈殿槽26からの亜硫酸イオンを含む処理水40は、CaF2析出・酸化槽90に投入し、エアー5で撹拌した。CaF2析出・酸化槽90に3%水酸化カルシウムスラリー66を添加し、CaF2析出・酸化槽90内のpHを7.0〜7.5に維持しながら、亜硫酸イオンを空気酸化させた。その後、高分子凝集剤25を加え、フロックを形成させた後、沈殿槽26で沈殿させ、フッ化カルシウム成分が主体のCaF2スラリー71を得た。硫黄析出槽32とその後段にある沈殿槽26の上部からは、硫化水素ガスが2〜5ppm程度検知されているが、そのガスは、排気ファン39で系外に排出した(図15)。
【0090】
その際の、水質を、表17に示す。希釈後の浸出廃液1中のチオ硫酸イオンは、ほぼ全量、硫黄析出槽32で硫黄と亜硫酸イオンに自己分解している。また、亜硫酸イオンは、CaF2析出・酸化槽90において、ほぼ全量エアー5により自然酸化され、それに伴い、COD値も低下している。また、フッ素イオンは、CaF2析出・酸化槽90内で析出し、処理水4中のF濃度は12mg/Lまで低下している。回収した硫黄スラリー38中の硫黄濃度は、84%であり、回収したCaF2スラリー71中のCaF2濃度及びCaSO4濃度は、ドライ換算で、それぞれ、38%、47%であった。
【0091】
【表17】

【0092】
以上、添付図面を参照しながら本発明の好適な実施形態について説明したが、本発明はかかる例に限定されないことは言うまでもない。当業者であれば、特許請求の範囲に記載された範疇内において、各種の変更例または修正例に想到し得ることは明らかであり、それらについても当然に本発明の技術的範囲に属するものと了解される。
【符号の説明】
【0093】
1・・・浸出廃液
2・・・微生物担体
3・・・生物反応槽
4・・・処理水
5・・・エアー
12・・・硝酸廃液
13・・・撹拌機
15・・・脱窒槽
16・・・蓋
22・・・有機物含有廃液
25・・・高分子凝集剤
26・・・沈澱槽
32・・・硫黄析出槽
34・・・酸
38・・・硫黄スラリー
39・・・排気ファン
40・・・硫黄析出工程からの処理水
41・・・MgF2析出・酸化槽
43・・・マグネシウム化合物
44・・・pH調整剤
45・・・pH計
48・・・MgF2スラリー
51・・・CaF2析出・酸化槽
53・・・カルシウム化合物
58・・・CaF2・CaSO4スラリー(フッ化カルシウムと石膏の混合スラリー)
64・・・MgF2析出槽、または、CaF2析出槽
66・・・MgOスラリー、または、Ca(OH)2スラリー
71・・・MgF2スラリー、または、CaF2スラリー
85・・・硫酸
90・・・MgF2析出・酸化槽、または、CaF2析出・酸化槽
【特許請求の範囲】
【請求項1】
亜鉛を含むダストを、多硫化物イオンを含みアルカリ土類金属を含まないアルカリ水溶液に混合して、ダスト中の金属酸化物を金属硫化物に反応させると共に、ダスト中の塩素及び/又はフッ素をダスト中から浸出させ、金属硫化物を主体とする固形分と浸出廃液とに分離することを特徴とする、ダストの処理方法。
【請求項2】
亜鉛含むダストを硫黄と共にアルカリ土類金属を含まないアルカリ水溶液に混合して、40℃以上100℃以下の液温下で攪拌して、ダスト中の塩素及び/又はフッ素をダスト中から浸出させ、金属硫化物を主体とする固形分と浸出廃液とに分離することを特徴とする、ダストの処理方法。
【請求項3】
前記アルカリ水溶液が、製鉄プロセスにおける圧延工程から排出される含油アルカリ廃液である、請求項1又は2のいずれか1項に記載のダストの処理方法。
【請求項4】
前記浸出廃液に対して、270〜500nmの領域の吸収波長を測定して前記硫化反応の進捗状況を把握する、請求項1〜3のいずれか1項に記載のダストの処理方法。
【請求項5】
前記浸出廃液に対して、マグネシウム化合物を含んだ水溶液又はスラリーを入れた後、又は、入れながら、pH5〜9に調整して、フッ素イオンをフッ化マグネシウムとして析出させ、固液分離する、請求項1〜4のいずれか1項に記載のダストの処理方法。
【請求項6】
前記浸出廃液に対して、カルシウム化合物を入れた後、又は、入れながら、pHを4〜10に調整することで、フッ素イオン及び/又は硫酸イオンをカルシウム塩として析出させ、固液分離する、請求項1〜5のいずれか1項に記載のダストの処理方法。
【請求項7】
前記浸出廃液中のCOD成分をさらに分解する、請求項1〜6のいずれか1項に記載のダストの処理方法。
【請求項8】
請求項1〜4のいずれか1項に記載の処理方法で分離された浸出廃液に対して、酸を投入しpHを4以下に調整して、硫黄を析出・分離してから、硫黄分離後の浸出廃液にマグネシウム化合物を入れた後、又は、入れながら、pH5.5〜6.5に調整することで、フッ素イオンをフッ化マグネシウムとして析出させ、分離することを特徴とする、ダストの処理方法。
【請求項9】
請求項1〜4のいずれか1項に記載の処理方法で分離された浸出廃液に対して、酸を投入しpHを4以下に調整して、硫黄を析出・分離してから、硫黄分離後の浸出廃液にカルシウム化合物を入れた後、又は、入れながら、pH5.5〜8に調整することで、フッ素イオン及び/又は硫酸イオンをカルシウム塩として析出させ、分離することを特徴とする、ダストの処理方法。
【請求項1】
亜鉛を含むダストを、多硫化物イオンを含みアルカリ土類金属を含まないアルカリ水溶液に混合して、ダスト中の金属酸化物を金属硫化物に反応させると共に、ダスト中の塩素及び/又はフッ素をダスト中から浸出させ、金属硫化物を主体とする固形分と浸出廃液とに分離することを特徴とする、ダストの処理方法。
【請求項2】
亜鉛含むダストを硫黄と共にアルカリ土類金属を含まないアルカリ水溶液に混合して、40℃以上100℃以下の液温下で攪拌して、ダスト中の塩素及び/又はフッ素をダスト中から浸出させ、金属硫化物を主体とする固形分と浸出廃液とに分離することを特徴とする、ダストの処理方法。
【請求項3】
前記アルカリ水溶液が、製鉄プロセスにおける圧延工程から排出される含油アルカリ廃液である、請求項1又は2のいずれか1項に記載のダストの処理方法。
【請求項4】
前記浸出廃液に対して、270〜500nmの領域の吸収波長を測定して前記硫化反応の進捗状況を把握する、請求項1〜3のいずれか1項に記載のダストの処理方法。
【請求項5】
前記浸出廃液に対して、マグネシウム化合物を含んだ水溶液又はスラリーを入れた後、又は、入れながら、pH5〜9に調整して、フッ素イオンをフッ化マグネシウムとして析出させ、固液分離する、請求項1〜4のいずれか1項に記載のダストの処理方法。
【請求項6】
前記浸出廃液に対して、カルシウム化合物を入れた後、又は、入れながら、pHを4〜10に調整することで、フッ素イオン及び/又は硫酸イオンをカルシウム塩として析出させ、固液分離する、請求項1〜5のいずれか1項に記載のダストの処理方法。
【請求項7】
前記浸出廃液中のCOD成分をさらに分解する、請求項1〜6のいずれか1項に記載のダストの処理方法。
【請求項8】
請求項1〜4のいずれか1項に記載の処理方法で分離された浸出廃液に対して、酸を投入しpHを4以下に調整して、硫黄を析出・分離してから、硫黄分離後の浸出廃液にマグネシウム化合物を入れた後、又は、入れながら、pH5.5〜6.5に調整することで、フッ素イオンをフッ化マグネシウムとして析出させ、分離することを特徴とする、ダストの処理方法。
【請求項9】
請求項1〜4のいずれか1項に記載の処理方法で分離された浸出廃液に対して、酸を投入しpHを4以下に調整して、硫黄を析出・分離してから、硫黄分離後の浸出廃液にカルシウム化合物を入れた後、又は、入れながら、pH5.5〜8に調整することで、フッ素イオン及び/又は硫酸イオンをカルシウム塩として析出させ、分離することを特徴とする、ダストの処理方法。
【図3】


【図5】


【図10】


【図12】


【図13】


【図14】


【図15】


【図1】


【図2】


【図4】


【図6】


【図7】


【図8】


【図9】


【図11】




【図5】


【図10】


【図12】


【図13】


【図14】


【図15】


【図1】


【図2】


【図4】


【図6】


【図7】


【図8】


【図9】


【図11】


【公開番号】特開2011−156473(P2011−156473A)
【公開日】平成23年8月18日(2011.8.18)
【国際特許分類】
【出願番号】特願2010−19658(P2010−19658)
【出願日】平成22年1月29日(2010.1.29)
【出願人】(000006655)新日本製鐵株式会社 (6,474)
【Fターム(参考)】
【公開日】平成23年8月18日(2011.8.18)
【国際特許分類】
【出願日】平成22年1月29日(2010.1.29)
【出願人】(000006655)新日本製鐵株式会社 (6,474)
【Fターム(参考)】
[ Back to top ]

