チエニル基包含ボロン−ジピリン化合物、その製造方法及び該化合物を備える化学センサー
【課題】本発明は、チエニル包含するボロン-ジピリン化合物、前記化合物の製造方法及び前記チエニルを包含するボロン-ジピリン化合物が包含された化学センサーを提供する。
【解決手段】本発明は、式(1)で表されるチエニルを包含するボロン-ジピリン化合物、この化合物の製造方法、及び式(1)の化合物が金属イオンと反応して色相変化と蛍光変化を表すことのできるチエニルを包含するボロン-ジピリン化合物が包含された化学センサーによって課題を達成する。式(1)の化合物:3-(R)-4,4-ジ(R)-8-(R)-4-ボラ-3a,4a-ジアザ-s-インダセン(式中、Rは、2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
【解決手段】本発明は、式(1)で表されるチエニルを包含するボロン-ジピリン化合物、この化合物の製造方法、及び式(1)の化合物が金属イオンと反応して色相変化と蛍光変化を表すことのできるチエニルを包含するボロン-ジピリン化合物が包含された化学センサーによって課題を達成する。式(1)の化合物:3-(R)-4,4-ジ(R)-8-(R)-4-ボラ-3a,4a-ジアザ-s-インダセン(式中、Rは、2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、チエニル基を包含するボロン-ジピリン化合物、その製造方法及び該化合物を備える化学センサーに関する。より詳細には、下記式(1)に表示されるチエニルを包含するボロン-ジピリン化合物、その製造方法及び該化合物が金属イオンと反応して色相変化と蛍光変化とを示すことを利用する該化合物を包含する化学センサーに関する。
【背景技術】
【0002】
本発明のチエニルを包含するボロン-ジピリン化合物において、ボロン-ジピリン化合物はBODIPY(Boron Dipyrrin)と知られている物質と構造的に類似である。
【0003】
BODIPYは、アントラセン、ローダミンなどのような有機染色物質として知られている。この物質の優れた蛍光特性が生物学的研究において多く使用されており、例えば、この物質を生体物質に標識させて生物学的反応過程を蛍光推移を通じて観察しようとする研究に応用されている。
【0004】
蛍光を表す染色物質は、主に化学的な反応によってその本来の染色物質が表す蛍光の程度が増加するか、減少又は消滅する性質を表し、これを化学センサー(Chemosensor)と称する。このような種類の多くの化学センサーが、近年、開発・報告されている。その一例として、銅イオン及び水銀イオンに対するセンサー、スイッチ、線量計(dosimeter)などがある。
【0005】
このような染色物質は、アントラセン、ピレン、シクロデキストリン、カリックスアレーン(calixarene)、フルオレセイン、キノリン、ローダミン、アズレン、ピリジン、チアゾール、チアジアゾール、チオフェン、シクラム(cyclam)、BODIPY、フェロセン、カーボハイドレイト、ペプチドのような物質などを母体として改変された構造を有する。
【0006】
金属イオンのうち、銅イオン(Cu2+)は、自然界で広範囲に発見されるとともに、生態系において様々な役割を果たしている。水銀(Hg)もやはり自然界で鉱物の形態で発見されている。しかし、これらが産業界で使用された時の水銀及び水銀イオン(Hg2+)は、生態環境の汚染源として注視されており、水層、土壌などの中に神経毒性を有するメチル水銀(CH3HgCl)の形態で蓄積される。
【0007】
このようなことから、銅イオン、水銀イオンの2つの陽イオンを検出することのできる新しいイオン検出計の開発が非常に重要な課題となっている。
【0008】
ボロン-ジピリンの形態で銅イオン及び水銀イオンを検出する特性を有する物質に対して報告されている(例えば、非特許文献1、2、3、4、5)。これらの物質は、金属イオン検出のための単位体としてピリジン又はクラウン(Crown)形態という典型的な配位単位を包含している。
【0009】
ボロン-ジピリンを大量的に合成することは困難であるが、5位の炭素が置換されたBF2-ジピリンの容易な合成法についてLindseyらによって発表されている(例えば、非特許文献6、7)。
【0010】
また、Keeは8位の炭素を種々の置換基に改変しながら、BF2-ジピリンが表す蛍光の強さを増加させる方法について報告している(例えば、(非特許文献8)。
【非特許文献1】Qi, X. et. al., Journal of Organic Chemistry 2006, 71, 2881-2884
【非特許文献2】Rurack, K. et. al., Journal of the American Chemical Society 2000, 122, 968-969
【非特許文献3】Coskun, A. et. al., Organic Letters 2007, 9, 607-609
【非特許文献4】Yuan, M. L. et. al., Organic Letters 2007, 9, 2313-2316
【非特許文献5】Moon, S. Y. et. al., Journal of Organic Chemistry 2004, 69, 181-183
【非特許文献6】Lee, C. H. et. al., Tetrahedron 1994, 50, 11427-11440
【非特許文献7】Littler, B. J. et. al., Journal of Organic Chemistry 1999, 64, 1391-1396
【非特許文献8】Kee, H. L. et. al., Journal of Physical Chemistry B 2005, 109, 20433-20443
【発明の開示】
【発明が解決しようとする課題】
【0011】
本発明は、新しい置換体を有するボロン-ジピリン化合物と、この化合物の製造方法を提供する。
また、このような新しい置換体を有するボロン-ジピリン化合物が包含されて分光学的特性の変化によって金属イオンを感知することのできる化学センサーを提供する。
【課題を解決するための手段】
【0012】
本発明は、チエニルを包含するボロン-ジピリン化合物を提供する。
また、前記チエニルを包含するボロン-ジピリン化合物の製造方法を提供する。
本発明は、前記チエニルを包含するボロン-ジピリン化合物、または前記チエニルを包含するボロン-ジピリン化合物の製造方法によって製造されたチエニルを包含するボロン-ジピリン化合物が包含された、化学センサーを提供する。
本発明は、前記チエニルを包含するボロン-ジピリン化合物、または前記チエニルを包含するボロン-ジピリン化合物の製造方法によって製造されたチエニルを包含するボロン-ジピリン化合物が包含された、金属イオン、特に銅イオンまたは水銀イオンを容易に検出することができる化学センサーを提供する。
【発明の効果】
【0013】
本発明のチエニルが包含されたボロン-ジピリン化合物は、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作って金属イオンを感知することのできる構造的特異性を有している。これら4つのチエニルのうち、3つのチエニルの置換された分子の模様がサソリ虫の形状と近似し、チエニルによって形成された空間が、金属イオンを受容することのできる配位子の役割を果たす。特に、銅イオンまたは水銀イオンを感知することによって配位子物質の色相変化と蛍光強度との変化を通じて目視によって確認することのできる。従って、本発明のチエニルが包含されたボロン-ジピリン化合物は、金属イオンの感知と、結合可逆性に対する特性を表すことによって、化学センサーの必要とする選択性、可逆性の双方を提供することができる。
【0014】
本発明のチエニルが包含されたボロン-ジピリン化合物は、金属イオン、特に、銅イオン及び/又は水銀イオンを検出することのできる新しい化学センサー物質としての応用性において、その潜在力が強く、本発明のチエニルが包含されたボロン-ジピリン化合物は、銅イオン、水銀イオンのような環境汚染の原因物質の除去に活用することができる。
【発明を実施するための最良の形態】
【0015】
以下、本発明を実施形態を通じてさらに詳細に説明する。
本発明は、チエニルを包含するボロン-ジピリン化合物である。
前記チエニルは、4つのチエニルを包含し、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物である。つまり、本発明のチエニルが包含されたボロン-ジピリン化合物は、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作って金属イオンを感知することができる構造的な特異性を有している。これら4つのチエニルのうち、3つのチエニルの置換された分子の模様がサソリ虫の模様とほぼ同様であり、チエニルによって形成された空間が、金属イオンを受容することのできる配位子の役割を果たす。
【0016】
本発明は、式(1)で表されるチエニルを包含するボロン-ジピリン化合物である。
3-(R)-4,4-di(R)-8-(R)-4-bora-3a,4a-diaza-s-indacene、つまり、
3-(R)-4,4-ジ(R)-8-(R)-4-ボラ-3a,4a-ジアザ-s-インダセン (1)
(式中、Rは2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
【0017】
本発明は、式(1)で表示される4つのチエニルを包含し、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物である。
【0018】
式(1)のチエニルを包含するボロン-ジピリン化合物は、化学式(2)の化合物のジフルオロと8位の炭素を2-チエニル及び3-チエニルの群から選択されるいずれか1つに置換させて得ることができる。
3-(R)-4,4-difluoro-4-bora-3a,4a-diaza-s-indacene、つまり、
3-(R)-4,4-ジフルオロ-4-ボラ-3a,4a-ジアザ-s-インダセン (2)
(式中、Rは上記と同義である。)
【0019】
また、本発明は、チエニルを包含するボロン-ジピリン化合物の製造方法を提供する。
つまり、4つのチエニルを包含し、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物の製造方法である。
【0020】
本発明は、上述した式(1)で表されるチエニルを包含するボロン-ジピリン化合物の製造方法である。
【0021】
また、本発明は、上述した式(1)で表示される4つのチエニルを包含し、4つのチエニルの中、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物の製造方法である。
【0022】
また、本発明は、上述した式(2)の化合物をチエニル基を有する物質と反応させて上述した式(1)に表されるチエニルを包含するボロン-ジピリン化合物を製造する方法である。
【0023】
前記において、チエニル基を有する物質は、2-チエニル及び3-チエニルの群から選択されるいずれか1つの作用基を有する物質である。
【0024】
前記チエニル基を有する物質は、例えば、2-チエニルリチウム、3-チエニルリチウムの群から選択されるいずれか1つを使用することができる。
前記において、式(2)の化合物とチエニル基を有する物質の反応は、式(2)の化合物1モルに対してチエニル基を有する物質1〜10モルを反応させて式(1)で表される、4つのチエニルを包含し、4つのチエニルのうち、3つのチエニルがサソリ虫模様のような空間を作る構造的な特異性、つまり、4つのチエニルの中、3つのチエニルが形成する分子の構造がサソリ虫模様とほぼ同様であり、このとき形成された空間に金属イオンを受容することのできる配位子を有するチエニルを包含するボロン-ジピリン化合物を製造することができる。
【0025】
前記において、式(2)の化合物とチエニル基を有する物質の反応は、式(2)の化合物1モルに対してチエニル基を有する物質1〜10モルを非活性気体の雰囲気下、−90℃〜0℃での攪拌によって実施することができる。
なお、式(2)の化合物とチエニル基を有する物質の反応において、前記の物質が全部反応するまで攪拌して反応を進行させる。
前記不活性ガスは、窒素(N)、ヘリウム(He)、ネオン(Ne)、アルゴン(Ar)の群から選択される種以上の気体である。
【0026】
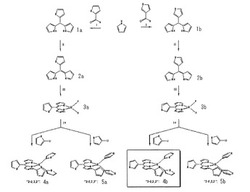
図1は、本発明の4つのチエニルを包含し、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有する、式(1)に表されるチエニルを包含するボロン-ジピリン化合物の製造方法を模式的に表す工程図である。
【0027】
図1には、化合物3a、3bを得ることのできる出発物質から出発して最終的に化合物4a、4b、5a、5bのチエニルを包含するボロン-ジピリン化合物の製造方法を示している。この工程によって後述する実施形態のように化合物3a、3bからチエニルを包含するボロン-ジピリン化合物である化合物4a、4b、5a、5bを得ることができる。
【0028】
また、本発明は、前記化学式(1)で表されるチエニルを包含するボロン-ジピリン化合物が特定のイオンと反応する時、色相の変化と蛍光変化を起す化学センサーを提供する。
より具体的には、前記化学式(1)で表される4つのチエニルを包含し、4つのチエニルの中、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物が特定のイオンと反応する時、色相変化と蛍光変化を起す化学センサーを提供する。
本発明は、前記の製造方法により製造された、化学式(1)で表されるチエニルを包含するボロン-ジピリン化合物が特定のイオンと反応する時、色相変化と蛍光変化を起す化学センサーである。
より詳細には、前記の製造方法によって製造された化学式(1)で表される4つのチエニルを包含し、その4つのチエニルの中、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物が特定のイオンと反応する時、色相変化と蛍光変化を起す化学センサーである。
【0029】
前記本発明の化学センサーは、式(1)で表されるチエニルを包含するボロン-ジピリン化合物が金属イオンに対して選択的に反応する。
前記化学センサーは、式(1)で表されるチエニルを包含するボロン-ジピリン化合物が金属イオンと反応することにより、色相変化と蛍光変化を表す。
【0030】
一例の実験によれば、先ず、式(1)で表される化合物を有機溶媒に溶解させてピンク色の溶液1を調製する。次いで、前記有機溶媒と同一の有機溶媒に金属イオンを投入して溶液2を得た後、前記溶液2を溶液1に添加する。このとき、溶液1の色相がピンク色から無色に変化する色相変化を起す特性と、蛍光の明るさが増加するか、または減少するような蛍光変化の反応が起る特性を示す。
【0031】
前記の有機溶媒は、テトラヒドロフラン(THF)、メチレンクロリド、エチルアルコール、n−ヘキサン、アセトン、アセテートの群から選択される1種以上を使用することができる。
【0032】
本発明の式(1)で表されるチエニルを包含するボロン-ジピリン化合物は、前記有機溶媒に対して高い溶解性があり、水に対しては比較的低い溶解性を有する。よって、アセテート溶媒と水との混合液を使用することによって溶解性を高めることができる。
【0033】
式(1)で表されるチエニルを包含するボロン−ジピリン化合物が前記の有機溶媒に溶解すると、溶液の色はピンク色を帯びる。
本発明の化学センサーは、式(1)で表示されるチエニルを包含するボロン-ジピリン化合物が銅イオンまたは水銀イオンのような金属イオンに対して選択的に反応する。
【0034】
より具体的には、本発明の化学センサーは、式(1)に表示されるチエニルを包含するボロン-ジピリン化合物が銅イオンまたは水銀イオンのような金属イオンと反応して色相変化と蛍光の変化とを示す特性を有する。例えば、前記化合物が溶解した溶液の色がピンク色から無色に変化する色相変化の特性と、蛍光の明るさが増加するか、または減少するような蛍光変化の反応を示す特性を示すことができる。
【0035】
以上、本発明のチエニルを包含するボロン-ジピリン化合物と、該化合物の製造方法、チエニルを包含するボロン-ジピリン化合物が包含された化学センサーは、本発明の目的を達成するためには前記のような条件を具備して提供されることが好ましい。
【0036】
以下、本発明の内容を実施例及び試験例を通じてより具体的に説明する。ただ、これらの実施例などは本発明をより詳細に説明するためであり、本発明がこれらの実施例に限定されるものではない。
【0037】
実施例1:3-(2-チエニル)-4,4-ジ(2-チエニル)-8-(2-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン(3-(2-thienyl)-4,4-di(2-thienyl)-8-(2-thienyl)-4-bora-3a,4a-diaza-s-indacene)[4a]の製造
下記反応式(1)のように化合物3aと2-チエニルリチウムを反応させて化合物4aを製造した。
【0038】
【化1】

【0039】
従来技術(Journal of Chemical Crystallography 2007、37、315)によって得られた化合物3a(1.35g、4.75mmol)を無水テトラヒドロフラン(THF)50mLに溶解させてアルゴン気体雰囲気下、−78℃で10分間攪拌した。この溶液に、THFによって1.0M濃度に希釈した2-チエニルリチウム30mLを1ml/secの速度で滴下した。その後、アルゴン気体の雰囲気下、-78℃で10分間さらに攪拌し、化合物3aと2-チエニルリチウムとの混合溶液の温度が常温になるまで放置した。
【0040】
TLC(thin layer chromatography)によって化合物3aがすべて反応したことを確認した後、20mLの蒸留水を混合溶液に投入して反応を終了させる。
【0041】
反応が終了した混合溶液の混合物をジクロロメタンで抽出して得た有機層を、マグネシウムスルフィドで乾燥し、ジクロロメタン溶媒を減圧乾燥により除去した後、残りの物質をシリカカラムを用いて精製した。この過程において、カラムに3回ほど通すが、このとき、へキサンとジクロロメタンが1:1の体積比で混合された混合液を流しながらカラムを展開させた。濃いピンク色を帯びる部分を集めてさらにPTLC(preparative thin layer column chromatography)と再結晶法とを利用して純粋な化合物4a(3-(2-チエニル)-4,4-ジ(2-チエニル)-8-(2-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン)を得た(0.7g、収率:31%)。
【0042】
溶融点:163 ℃。1H NMR(CD2Cl2:δ 5.32)7.72(dd,3JH−H=5.0,JH−H=0.8Hz,1Hb)、7.62(d,3JH−H=4.0Hz,1Hc)、7.58(s,1Hh)、7.48(d,3JH−H=4.6Hz,1Hd)、7.30(m,2Hn)、7.28(s,1Ha)、7.25(dd,3JH−H=0.6, 4JH−H=0.6Hz,1Hk)、7.21(dd,3JH−H=4.5,4JH−H=0.9Hz,1Hf)、7.04(d,3JH−H=3.3Hz,2Hl)、6.96(m,2Hm)、6.88(d,3JH−H=4.6Hz,1He)、6.87(s,1Hi)、6.74(dd,3JH−H=4.8,3JH−H=4.0Hz, 1Hj)、6.49(dd,3JH−H=4.0,JH−H=1.9Hz, 1Hg);13C NMR(CD2Cl2:δ 53.8)152.4(t,1JC−H=8.8Hz,1C5)、144.5(dt,1JC−H=185.0,3JC−H=9.0Hz,1Ch)、137.5(s,1C2)、136.8(t,2JC−H=9.0Hz,1C3)、135.4(p,2JC−H=5.6Hz,1C1)、134.5(m,JC−H=5.6Hz,1C6)、132.9(m,1C4)、132.8(ddd,1JC−H=169.9Hz,2JC−H=9.3Hz,3JC−H=6.1Hz,1Cc)、132.0(ddd,1JC−H=163.4Hz,3JC−H=9.2Hz,3JC−H=6.0Hz,1Ci)、131.0(dm,1JC−H=〜160Hz,1Cl)、(dm,1JC−H=〜160Hz,1Cd)、130.7(ddd,1JC−H=281.7,2JC−H=9.2,3JC−H=6.1Hz,1Cb)、129.0(dm,1JC−H=211.3Hz,1Ck)、128.5(m,1Cf)、128.2(dt,1JC−H=171.0,2JC−H=10.1Hz,1Ca)、127.6(dm,1JC−H=161.0Hz,1Cj)、127.5(dm,1JC−H=161.0Hz,2Cm)、127.1(dm,1JC−H=201.2Hz,2Cn)、122.3(dd,1JC−H=175.2,2JC−H=3.6Hz,1Ce)、118.4(ddd,1JC−H=174.8,3JC−H=8.9,3JC−H=3.5Hz,1Cg)。11B NMR(F3B・OEt2:δ 0.00)−3.59(s)、MALDITOF m/z(M+):484.04(calc.)483.99(obs.)、Anal.Calc.for C25H17BN2S4:C 61.98、H 3.54、and N 5.78、found:C 63.44、H 3.81、and N 6.00。
【0043】
実施例2:3-(2-チエニル)-4,4-ジ(2-チエニル)-8-(3-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン[4b]の製造
下記反応式2のように化合物3bと2-チエニルリチウムとを反応させて化合物4bを製造した。
【0044】
【化2】

【0045】
従来技術(Journal of Chemical Crystallography 2007、37、315)によって合成した化合物3b(0.18g、0.65mmol)を出発物質として使用し、2-チエニルリチウムを6.5mLを使用することを除いては実施例1と同様の方法によって化合物4bを製造した。
【0046】
反応終了の後に、TLCによってRfの値が0.8程度の濃い赤色蛍光を示す部分を認めることができた。それぞれ3回のシリカカラムとPTLCを通じて純粋な化合物4b(3-(2-チエニル)-4,4-ジ(2-チエニル)-8-(3-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン)を得た(0.12g、収率:35%)。
【0047】
溶融点:166 ℃。1H NMR(CD2Cl2:δ 5.32)7.79(dd,4JH−H=3.0,4JH−H=1.2Hz,1Hc)、7.57(d,J=3.0Hz,1Ha)、7.56(m,1Hh)、7.48(dd,3JH−H=5.0,4JH−H=1.2Hz,1Hb)、7.30(d,3JH−H=4.5Hz,1Hd)、7.29(dd,3JH−H=4.7,4JH−H=0.8Hz,2Hn)、7.24(dd,3JH−H=5.0,4JH−H=1.1Hz,1Hk)、7.03(d,3JH−H=obs,4JH−H=1.3Hz,1Hf)、7.02(dd,3JH−H=3.4,4JH−H=1.0Hz,2Hl)、6.95(m,2Hm)、6.85(d,3JH−H=4.5Hz,1He)、6.84(dd,3JH−H=3.7,4JH−H=1.1Hz, 1Hi)、6.73(dd,3JH−H=5.1,4JH−H=3.7Hz,1Hj)、6.47(dd,3J=4.2,1.9Hz,1Hg);13C NMR(CD2Cl2:δ 53.8)152.1(m,1C5)、144.3(dt,1JC−H=184.9,3JC−H=9.1Hz,1Ch)、139.7(s,1C2)、136.9(t,2JC−H=9.0Hz,1C3)、135.4(m,1C1)、134.6(m,1C6)、133.0(q,2JC−H=8.8Hz,1C4)、131.9(ddd,1JC−H=170.7,2JC−H=9.2,1Ci)、130.9(ddd,1JC−H=163.3,2JC−H=9.8,1Cl)、130.5(dm,1JC−H=171.9,1Cb)、130.4(dm,1JC−H=165.4Hz,1Cd)、129.6(dm,1JC−H=171.0Hz,1Cc)、128.9(dm,1JC−H=186.2Hz,1Ck)、127.9(dm,1JC−H=161.0,1Cf)、127.6(dm,1JC−H=170.8Hz,1Cj)、127.5(dm,1JC−H=168.7,2Cm)、127.0(ddd,1JC−H=184.2,2JC−H=10,3JC−H=7.8Hz,2Cn)、126.7(dt,1JC−H=186.8,3JC−H=6.9Hz,1Ca)、122.1(dd,1JC−H=175.1,3JC−H=3.7Hz,1Ce)、118.3(ddd,1JC−H=174.6,3JC−H=8.9,3JC−H=3.7Hz,1Cg)。11B NMR(BF3・OEt2:δ 0.00)−3.61(s)、MALDITOF m/z(M+):484.04(calc.)484.36(obs.)、Anal.Calc.for C25H17BN2S4:C 61.98、H 3.54、and N 5.78、found:C 62.63、H 4.21、and N 5.66
【0048】
実施例3:3-(3-チエニル)-4,4-ジ(3-チエニル)-8-(2-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン[5a]の製造
下記反応式3のように化合物3aと3-チエニルリチウムとを反応させて化合物5aを製造した。
【0049】
【化3】

【0050】
従来技術(Karlsson,L.et.al.,A Chemica Scripta 1974、6、214―221)によって3-チエニルリチウムを準備した。つまり、3-ブロモチオフェン(1.6mL、0.017mmol)を無水エーテル50mLに溶解させてアルゴン気体雰囲気下、−78℃を維持しながら10分程攪拌した。この溶液にヘキサンによって2.5Mに希釈したn-ブチルリチウム5.4mLを1ml/secの速度で滴下した。その後、10分程度さらに攪拌して3-チエニルリチウムを得た。
【0051】
化合物3a(0.46g、0.0017mol)を12mlの無水THFで溶解させて、室温状態に静置した。化合物3aが溶解した溶液を、上述した3-チエニルリチウム溶液が入っているフラスコによってカニューレ(cannula)を通じて移動させながら混合した。混合した後、アルゴン雰囲気下、−78℃を維持しながら攪拌する。10分後、TLCを通じて化合物3aが完全に反応して消耗されていることを確認し、その後、水を投入して反応を終了させた。実施例1の精製過程を経て最終的に純粋な化合物5a(3-(3-チエニル)-4,4-ジ(3-チエニル)-8-(2-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン)を得た(0.088g、収率:11%)。
【0052】
溶融点:184 ℃。1H NMR(CD2Cl2:δ 5.32)7.71(dd,3JH−H=5.1,4JH−H=1.2Hz,1Hb)、7.61(dd,3JH−H=3.7,4JH−H=1.2Hz,1Hc)、7.46(d,3JH−H=4.4Hz,1Hd)、7.41(m,1Hh)、7.28(m,1Ha)、7.19(dd,3JH−H=4.3,4JH−H=1.3Hz,1Hf)、7.15(dd,3JH−H=4.8,3JH−H=2.7Hz,2Hm)、7.01(m,1Hj)、6.97(m,1Hk)、6.94(dd,4JH−H=2.7,4JH−H=1.1Hz,2Hn)、6.89(dd,3JH−H=4.8,4JH−H=1.1Hz,2Hl)、6.81(dd,3JH−H=5.0,4JH−H=1.3Hz,2Hj)、6.74(d,3JH−H=4.4Hz, 1He)、6.46(dd,3JH−H=4.2,4JH−H=1.8Hz,1Hg);13C NMR(CD2Cl2:δ53.8)154.6(t,1JC−H=8.2Hz,1C5)143.6(dt、1JC−H=184.6,3JC−H=9.0Hz,1Ch)、138.0(s,1C2)、136.4(t,1JC−H=9.0Hz,1C3)、135.6(m,1C1)、133.4(m,1C6)、133.1(m,1C4)、132.8(ddd,1JC−H=170.0,2JC−H=9.3,3JC−H=5.8Hz,1Cc)、132.2(dm,1JC−H=152.1Hz,1Cl)、130.7(dm,1JC−H=169.6Hz,1Cd)、130.5(ddd,1JC−H=184.9,2JC−H=10.8,2JC−H=7.1Hz,1Cb)、129.2(ddd,1JC−H=171.1,3JC−H=10,3JC−H=3.6Hz,1Ci)、128.1(dm,1JC−H=180.9Hz,1Ca)、128.0(dm,1JC−H=〜170Hz,1Cf)、128.0(dm,1JC−H=〜170Hz,1Ck)、127.7(ddd,1JC−H=160.8,3JC−H=8.5,3JC−H=4.2Hz,1Cn)、124.6(ddd,1JC−H=183.2,JC−H=4.7Hz,1Cm)、124.1(ddd,1JC−H=187.6,3JC−H=6.2,3JC−H=4.7Hz,1Cj)、121.6(dd,1JC−H=174.4,3JC−H=3.5Hz,1Ce)、117.8(ddd,1JC−H=174.5,3JC−H=9.1,3JC−H=3.6Hz,1Cg)。11B NMR(BF3・OEt2:δ 0.00)−3.59(s)、MALDITOF m/z(M+):484.04(calc.)484.68(obs.)、Anal.Calc.for C25H17BN2S4:C 61.98、H 3.54、and N 5.78、found:C 63.68、H 3.82、and N 6.03。
【0053】
実施例4:3-(3-チエニル)-4,4-ジ(3-チエニル)-8-(3-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン[5b]の製造
下記反応式4のように化合物3bと3-チエニルリチウムとを反応させて化合物5bを製造した。
【0054】
【化4】

【0055】
化合物3aの代わりに化合物3b(1g、3.65mmol)を使用することの他は、実施例3と同様な方法によって化合物5bを製造した。
最終的に得られた化合物5bは、0.15gで略8.5%の収率を示した。
【0056】
溶融点:178 ℃。1H NMR(CD2Cl2:δ 5.32)7.78(dd,4JH−H=3.0,4JH−H=1.2Hz,1Hc)、7.55(m,1Ha)、7.47(dd,3JH−H=5.0,4JH−H=1.2Hz,1Hb)、7.43(m,1Hh)、7.30(d,3JH−H=4.5Hz,1Hd)、7.17(dd,3JH−H=4.7,4JH−H=2.7Hz,2Hm)、7.03(d,3JH−H=obs,4JH−H=1.2Hz,1Hf)、7.02(m,1Hj)、6.98(m,1Hk)、6.96(dd,J=2.7,1.1Hz,2Hn)、6.91(dd,J=4.8,1.1Hz,2H1)、6.83(dd,3JH−H=5.0,4JH−H=1.4Hz,1Hi)、6.73(d,3JH−H=4.5Hz, 1He)、6.46(dd,3JH−H=4.2,JH−H=1.8Hz,1Hg);13C NMR(CD2Cl2:δ 53.8)154.3(m,1C5)、152.4(br,1C7)、143.4(dt,1JC−H=184.4,3JC−H=9.0,1Ch)、140.1(s,1C2)、136.4(t,1JC−H=9.0Hz,1C3)、135.6(m,1C1)、133.5(m,1C6)、133.2(d,1JC−H=8.7Hz,1C4)、132.2(ddd,1JC−H=164.9,2JC−H=10.5,3JC−H=4.9Hz,Cl)、130.5(ddd,1JC−H=173.0,2JC−H=8.5,3JC−H=4.7Hz,1Cb)、130.2(dd,1JC−H=175.1,3JC−H=4.2Hz,1Cd)、129.4(dm,1JC−H=185.8Hz,1Cc)、129.2(ddd,1JC−H=170.5,2JC−H=8.5,3JC−H=4.1Hz,1Ci)、128.0(ddd,1JC−H=128.0,3JC−H=8.5,3JC−H=4.4Hz,1Ck)、127.6(dm,1JC−H=152.4Hz,Cn)、127.5(dm,1JC−H=195.4Hz,1Cf)、126.6(dm,1JC−H=188.8Hz,1Ca)、124.6(ddd,1JC−H=189.6,2JC−H=9.0,3JC−H=4.7Hz,2Cm)、124.1(dt,1JC−H=187.6Hz,3JC−H=6.3,1Cj)、121.4(dd,1JC−H=171.1,2JC−H=3.5Hz,1Ce)、117.7(ddd,1JC−H=174.3,3JC−H=9.0,3JC−H=3.7Hz,1Cg)。11B NMR(BF3・OEt2:δ 0.00)−3.35(s)、MALDITOF m/z(M+):484.04(calc.)484.41(obs.)、Anal.Calc.for C25H17BN2S4:C 61.98、H 3.54、and N 5.78、found:C 62.56、H 3.82、and N 5.88。
【0057】
実施例5:金属イオンに対する選択的反応に関する実験
紫外線-赤外線の吸収分光法と蛍光分光法とを利用するために、実施例1から実施例4で製造したそれぞれの化合物4a、4b、5a、5bの4つの物質をそれぞれCH3CNに溶解させて1×10−5モル濃度の溶液を調製した。
【0058】
使用した金属イオンは、全て金属-過塩素酸塩の形態で、やはりCH3CNに溶解させて1×10−3モル濃度に調製した。金属イオンとして、Zn2+、Pb2+、Mn2+、Hg2+、Cu2+、Cs+、Ca2+、Cd2+、Ag+を使用した。
化合物4a、4b、5a、5bの4つの物質をそれぞれ金属イオン間の化学量論比が1:1になるようにして、化合物4a-金属イオンの混合溶液、化合物4b-金属イオンの混合溶液、化合物5a-金属イオンの混合溶液、化合物5b-金属イオンの混合溶液の4つの化合物-金属イオンの混合溶液を調製し、紫外線-赤外線吸収分光器及び蛍光分光器を通じて観察した。
【0059】
化合物4bでは、Cu2+に対して懸隔なスペクトルの変化を示し、非常に微弱ではあるが、他の金属イオンなどと比較するとき、Hg2+に対する弱いスペクトル変化を示した。また、化合物4bに比べてはその変化が微々とはいえども、化合物4a、5a、5bもやはり銅と水銀イオンに対して紫外線-赤外線吸収分光スペクトルの変化を示した(図2a、図2b、図2c、図2d参照)。
【0060】
このような変化は、蛍光スペクトルでも確認され、これを図3a〜図3dに示す。
これによって、4つのチエニル基が置換されたサソリ虫模様のボロン-ジピリン化合物が銅及び水銀イオンに対して選択的に反応することが確認された。特に、化合物4bでは、投入した銅イオンの量に従ってピンク色の化合物4b溶液の色相が無色相に変化することが観察され、紫外線を照らすとき示す蛍光の強度も増加した。一方、水銀イオンに対してはこのような色相の変化及び蛍光の強度変化が少ないことが観察された(図4a、図4b参照)。
【0061】
実施例6:銅イオン及び水銀イオンに対する検出限界に対する実験
銅イオン及び水銀イオンの検出限界を測定するために、化合物4a、4b、5a、5bの4つの物質をそれぞれCH3CNに溶解し、1×10−5モル濃度の溶液をそれぞれ3mLずつ取って石英セルに分注し、銅イオン溶液をマイクロピペットで滴下しながら一定時間おきに紫外線-赤外線吸収分光スペクトルを測定した。
化合物4a、4b、5a、5bが溶解した溶液に1×10−3モル濃度の銅イオンを10μLだけ投入してもスペクトルの変化を示した。これは銅イオン濃度が略270ppbに該当する値である(図5a〜図5d参照)。
【0062】
上記と同様の方法によって、化合物4a、4b、5a、5bの4つの物質をそれぞれCH3CNに溶解し、1×10−5モル濃度の溶液を調製し、これに水銀イオンを添加しながらスペクトルの変化を観察した。水銀の場合には、投入する水銀イオンの量によって継続的な波長の変化とスペクトルの変化とを観察することができた。化合物4a、4b、5a、5bの水銀に対する検出限界は、1×10−3モル濃度の水銀イオン溶液20μLで、略1.7ppmに該当する。
【0063】
実施例7:銅イオン結合可逆性に対する実験
化合物4a、4b、5a、5bの4つの物質が銅イオンまたは水銀イオンと結合した後、さらに本来の配位子状態に戻る結合可逆性に対する実験を行うことによって本発明で提示する物質などのセンサーとしての特性を確認した。
代表的に化合物4b及び化合物5bを選択して結合可逆性に対する実験を紫外線-赤外線分光スペクトルを通じて実施した。
【0064】
化合物4bをCH3CNに溶解し、1×10−5モル濃度の溶液を調製した。銅イオンは5×10―3モルの濃度に調製した。Na4EDTAを蒸留水に溶解し、0.01モルの濃度に調製した。5つの試料瓶を準備し、それぞれの試料瓶に化合物4bが溶解し溶液を1mLずつ分注し、1番試料瓶は化合物4bが溶解した溶液のみに、2番試料瓶は化合物4bが溶解した溶液に対してモル比の15倍に該当する銅イオンを入れて、3番試料瓶は2番試料瓶に化合物4bが溶解した溶液に対してモル比で30倍ほどのNa4EDTAを入れた。4番試料瓶には順序を変えて化合物4bが溶解した溶液にモル比で30倍ほどのNa4EDTAを先ず投入し、よく混合した後、15倍のモルに該当する銅イオンを混合した。最後の5番試料瓶は化合物4bが溶解した溶液とNa4EDTAの約1:30の混合物である。また、5つの試料瓶は化合物4bの濃度をすべて一定に合わせるためにCH3CNを補充して全部2.5mLの体積を有するようにした。5つの試料の紫外線-赤外線吸収分光スペクトルを比較することによって、結合可逆性に対する結果を確認した。
【0065】
図6のように、化合物4bが銅と結合すると、本来の化合物4bが示す吸収分光スペクトルの模様が懸隔に変化することを確認することができる。ただし、2番試料に比べてEDTAが添加された3番試料の場合、本来と同じ程度ではないが、吸収分光スペクトルの模様がさらに変化していることが確認された。このような実験は化合物5bに対しても同一の条件下で行われたが(図7参照)、化合物4bと5b、2種類においてこの試料はEDTAが添加されることによって溶液が濁ることを確認した。吸収分光スペクトルがEDTA添加によって変化を示すが、その形態が本来の化合物4b及び5bのスペクトルに比べては不明瞭とする理由は、試料の濁度のためであると見える。
【0066】
実施例8:水銀イオン結合可逆性に対する実験
水銀イオンと結合した化合物4b及び5bの試料に対して結合可逆性に対する実験を、KIを利用して実施した。水銀イオンは、ヨウ化物アニオンと容易に結合することが知られている。
実施例7のように、5つの試料瓶にそれぞれ1mLずつの化合物4bを分注し、1番試料瓶は化合物4b、2番試料瓶は化合物4bと、モル比で15倍に該当する水銀イオン、3番試料瓶は2番試料瓶と同じ組成で約30倍のKIを入れた。4番試料瓶は化合物4bに約30倍のKIを先ず入れてよく混合した後、約15倍の水銀イオンを投入した。5番試料瓶は化合物4bの約30倍のKIを混合した。また、5つの試料は全て3mLの体積にしてCH3CNを補充することによって反応する化合物4bのモル濃度を全て同じ条件にした。同様に化合物5bに対しても試料を準備した。このとき、化合物4b及び5bは、CH3CNに溶解して5×10−5モル濃度、水銀イオンもCH3CNに溶かした状態で1×10−3モル濃度にして準備した。また、KIは蒸留水に溶解して1×10−3モル濃度に調製した。水銀イオンの場合には、準備した試料が全て清澄状態であり、図8及び図9のように、KIが投入されることによって、水銀イオンが結合した化合物4bまたは化合物5bから脱離し、本来の化合物4bまたは化合物5bが示す吸収分光スペクトルと同様の形態及び波長と一致したことから、水銀イオンとの結合可逆性に対する明白な結果が得られた。これは本発明において提示するチエニルを包含するボロン-ジピリン化合物が化学センサーとしての必要とする可逆性の特性をよく示す潜在的な結果としてその重要性を有する。
【0067】
上述のように、本発明の好ましい実施例を参照して説明したが、該当技術分野の熟練された当業者であれば特許請求範囲に記載の本発明の思想及び領域の範囲内で本発明を多様に修正または変更させることができる。
【産業上の利用可能性】
【0068】
本発明のチエニルが包含されたボロン-ジピリン化合物は、金属イオン、特に銅イオンまたは水銀イオンを検出することができ、化学センサーとして利用することができる、また、この化合物に、銅イオン、水銀イオンのように環境汚染をもたらす物質を包含させて、これらのイオンを除去するために利用することも可能である。
【図面の簡単な説明】
【0069】
【図1】4つのチエニルを包含するボロン-ジピリン化合物の製造工程の一例を示した工程図である。
【図2a】本発明の実施例1で製造した化合物4aの金属イオンに対する選択性を示す吸光スペクトルである。
【図2b】本発明の実施例2で製造した化合物4bの金属イオンに対する選択性を示す吸光スペクトルである。
【図2c】本発明の実施例3で製造した化合物5aの金属イオンに対する選択性を示す吸光スペクトルである。
【図2d】本発明の実施例4で製造した化合物5bの金属イオンに対する選択性を示す吸光スペクトルである。
【図3a】本発明の実施例1で製造した化合物4aの金属イオンに対する選択性を示す吸光スペクトルである。
【図3b】本発明の実施例2で製造した化合物4bの金属イオンに対する選択性を示す吸光スペクトルである。
【図3c】本発明の実施例3で製造した化合物5aの金属イオンに対する選択性を示す吸光スペクトルである。
【図3d】本発明の実施例4で製造した化合物5bの金属イオンに対する選択性を示す吸光スペクトルである。
【図4a】本発明の実施例1で製造した化合物4a及び実施例2で製造した化合物4bの銅イオン感知による色相変化及び蛍光変化を示した写真図である。
【図4b】本発明の実施例3で製造した化合物5a及び実施例3で製造した化合物5bの銅イオン感知による色相変化及び蛍光変化を示した写真図である。
【図5a】本発明の実施例1で製造した化合物4aの銅イオンの滴下による吸光スペクトルの変化を示したグラフである。
【図5b】本発明の実施例2で製造した化合物4bの銅イオンの滴下による吸光スペクトルの変化を示したグラフである。
【図5c】本発明の実施例3で製造した化合物5aの銅イオンの滴下による吸光スペクトルの変化を示したグラフである。
【図5d】本発明の実施例4で製造した化合物5bの銅イオンの滴下による吸光スペクトルの変化を示したグラフである。
【図6】EDTA添加による化合物4b-銅イオン化合物の結合可逆性を示す吸光スペクトルである。
【図7】EDTA添加による化合物5b-銅イオン化合物の結合可逆性を示す吸光スペクトルである。
【図8】KI添加による化合物4b-銅イオン化合物の結合可逆性を示す吸光スペクトルである。
【図9】KI添加による化合物5b-銅イオン化合物の結合可逆性を示す吸光スペクトルである。
【技術分野】
【0001】
本発明は、チエニル基を包含するボロン-ジピリン化合物、その製造方法及び該化合物を備える化学センサーに関する。より詳細には、下記式(1)に表示されるチエニルを包含するボロン-ジピリン化合物、その製造方法及び該化合物が金属イオンと反応して色相変化と蛍光変化とを示すことを利用する該化合物を包含する化学センサーに関する。
【背景技術】
【0002】
本発明のチエニルを包含するボロン-ジピリン化合物において、ボロン-ジピリン化合物はBODIPY(Boron Dipyrrin)と知られている物質と構造的に類似である。
【0003】
BODIPYは、アントラセン、ローダミンなどのような有機染色物質として知られている。この物質の優れた蛍光特性が生物学的研究において多く使用されており、例えば、この物質を生体物質に標識させて生物学的反応過程を蛍光推移を通じて観察しようとする研究に応用されている。
【0004】
蛍光を表す染色物質は、主に化学的な反応によってその本来の染色物質が表す蛍光の程度が増加するか、減少又は消滅する性質を表し、これを化学センサー(Chemosensor)と称する。このような種類の多くの化学センサーが、近年、開発・報告されている。その一例として、銅イオン及び水銀イオンに対するセンサー、スイッチ、線量計(dosimeter)などがある。
【0005】
このような染色物質は、アントラセン、ピレン、シクロデキストリン、カリックスアレーン(calixarene)、フルオレセイン、キノリン、ローダミン、アズレン、ピリジン、チアゾール、チアジアゾール、チオフェン、シクラム(cyclam)、BODIPY、フェロセン、カーボハイドレイト、ペプチドのような物質などを母体として改変された構造を有する。
【0006】
金属イオンのうち、銅イオン(Cu2+)は、自然界で広範囲に発見されるとともに、生態系において様々な役割を果たしている。水銀(Hg)もやはり自然界で鉱物の形態で発見されている。しかし、これらが産業界で使用された時の水銀及び水銀イオン(Hg2+)は、生態環境の汚染源として注視されており、水層、土壌などの中に神経毒性を有するメチル水銀(CH3HgCl)の形態で蓄積される。
【0007】
このようなことから、銅イオン、水銀イオンの2つの陽イオンを検出することのできる新しいイオン検出計の開発が非常に重要な課題となっている。
【0008】
ボロン-ジピリンの形態で銅イオン及び水銀イオンを検出する特性を有する物質に対して報告されている(例えば、非特許文献1、2、3、4、5)。これらの物質は、金属イオン検出のための単位体としてピリジン又はクラウン(Crown)形態という典型的な配位単位を包含している。
【0009】
ボロン-ジピリンを大量的に合成することは困難であるが、5位の炭素が置換されたBF2-ジピリンの容易な合成法についてLindseyらによって発表されている(例えば、非特許文献6、7)。
【0010】
また、Keeは8位の炭素を種々の置換基に改変しながら、BF2-ジピリンが表す蛍光の強さを増加させる方法について報告している(例えば、(非特許文献8)。
【非特許文献1】Qi, X. et. al., Journal of Organic Chemistry 2006, 71, 2881-2884
【非特許文献2】Rurack, K. et. al., Journal of the American Chemical Society 2000, 122, 968-969
【非特許文献3】Coskun, A. et. al., Organic Letters 2007, 9, 607-609
【非特許文献4】Yuan, M. L. et. al., Organic Letters 2007, 9, 2313-2316
【非特許文献5】Moon, S. Y. et. al., Journal of Organic Chemistry 2004, 69, 181-183
【非特許文献6】Lee, C. H. et. al., Tetrahedron 1994, 50, 11427-11440
【非特許文献7】Littler, B. J. et. al., Journal of Organic Chemistry 1999, 64, 1391-1396
【非特許文献8】Kee, H. L. et. al., Journal of Physical Chemistry B 2005, 109, 20433-20443
【発明の開示】
【発明が解決しようとする課題】
【0011】
本発明は、新しい置換体を有するボロン-ジピリン化合物と、この化合物の製造方法を提供する。
また、このような新しい置換体を有するボロン-ジピリン化合物が包含されて分光学的特性の変化によって金属イオンを感知することのできる化学センサーを提供する。
【課題を解決するための手段】
【0012】
本発明は、チエニルを包含するボロン-ジピリン化合物を提供する。
また、前記チエニルを包含するボロン-ジピリン化合物の製造方法を提供する。
本発明は、前記チエニルを包含するボロン-ジピリン化合物、または前記チエニルを包含するボロン-ジピリン化合物の製造方法によって製造されたチエニルを包含するボロン-ジピリン化合物が包含された、化学センサーを提供する。
本発明は、前記チエニルを包含するボロン-ジピリン化合物、または前記チエニルを包含するボロン-ジピリン化合物の製造方法によって製造されたチエニルを包含するボロン-ジピリン化合物が包含された、金属イオン、特に銅イオンまたは水銀イオンを容易に検出することができる化学センサーを提供する。
【発明の効果】
【0013】
本発明のチエニルが包含されたボロン-ジピリン化合物は、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作って金属イオンを感知することのできる構造的特異性を有している。これら4つのチエニルのうち、3つのチエニルの置換された分子の模様がサソリ虫の形状と近似し、チエニルによって形成された空間が、金属イオンを受容することのできる配位子の役割を果たす。特に、銅イオンまたは水銀イオンを感知することによって配位子物質の色相変化と蛍光強度との変化を通じて目視によって確認することのできる。従って、本発明のチエニルが包含されたボロン-ジピリン化合物は、金属イオンの感知と、結合可逆性に対する特性を表すことによって、化学センサーの必要とする選択性、可逆性の双方を提供することができる。
【0014】
本発明のチエニルが包含されたボロン-ジピリン化合物は、金属イオン、特に、銅イオン及び/又は水銀イオンを検出することのできる新しい化学センサー物質としての応用性において、その潜在力が強く、本発明のチエニルが包含されたボロン-ジピリン化合物は、銅イオン、水銀イオンのような環境汚染の原因物質の除去に活用することができる。
【発明を実施するための最良の形態】
【0015】
以下、本発明を実施形態を通じてさらに詳細に説明する。
本発明は、チエニルを包含するボロン-ジピリン化合物である。
前記チエニルは、4つのチエニルを包含し、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物である。つまり、本発明のチエニルが包含されたボロン-ジピリン化合物は、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作って金属イオンを感知することができる構造的な特異性を有している。これら4つのチエニルのうち、3つのチエニルの置換された分子の模様がサソリ虫の模様とほぼ同様であり、チエニルによって形成された空間が、金属イオンを受容することのできる配位子の役割を果たす。
【0016】
本発明は、式(1)で表されるチエニルを包含するボロン-ジピリン化合物である。
3-(R)-4,4-di(R)-8-(R)-4-bora-3a,4a-diaza-s-indacene、つまり、
3-(R)-4,4-ジ(R)-8-(R)-4-ボラ-3a,4a-ジアザ-s-インダセン (1)
(式中、Rは2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
【0017】
本発明は、式(1)で表示される4つのチエニルを包含し、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物である。
【0018】
式(1)のチエニルを包含するボロン-ジピリン化合物は、化学式(2)の化合物のジフルオロと8位の炭素を2-チエニル及び3-チエニルの群から選択されるいずれか1つに置換させて得ることができる。
3-(R)-4,4-difluoro-4-bora-3a,4a-diaza-s-indacene、つまり、
3-(R)-4,4-ジフルオロ-4-ボラ-3a,4a-ジアザ-s-インダセン (2)
(式中、Rは上記と同義である。)
【0019】
また、本発明は、チエニルを包含するボロン-ジピリン化合物の製造方法を提供する。
つまり、4つのチエニルを包含し、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物の製造方法である。
【0020】
本発明は、上述した式(1)で表されるチエニルを包含するボロン-ジピリン化合物の製造方法である。
【0021】
また、本発明は、上述した式(1)で表示される4つのチエニルを包含し、4つのチエニルの中、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物の製造方法である。
【0022】
また、本発明は、上述した式(2)の化合物をチエニル基を有する物質と反応させて上述した式(1)に表されるチエニルを包含するボロン-ジピリン化合物を製造する方法である。
【0023】
前記において、チエニル基を有する物質は、2-チエニル及び3-チエニルの群から選択されるいずれか1つの作用基を有する物質である。
【0024】
前記チエニル基を有する物質は、例えば、2-チエニルリチウム、3-チエニルリチウムの群から選択されるいずれか1つを使用することができる。
前記において、式(2)の化合物とチエニル基を有する物質の反応は、式(2)の化合物1モルに対してチエニル基を有する物質1〜10モルを反応させて式(1)で表される、4つのチエニルを包含し、4つのチエニルのうち、3つのチエニルがサソリ虫模様のような空間を作る構造的な特異性、つまり、4つのチエニルの中、3つのチエニルが形成する分子の構造がサソリ虫模様とほぼ同様であり、このとき形成された空間に金属イオンを受容することのできる配位子を有するチエニルを包含するボロン-ジピリン化合物を製造することができる。
【0025】
前記において、式(2)の化合物とチエニル基を有する物質の反応は、式(2)の化合物1モルに対してチエニル基を有する物質1〜10モルを非活性気体の雰囲気下、−90℃〜0℃での攪拌によって実施することができる。
なお、式(2)の化合物とチエニル基を有する物質の反応において、前記の物質が全部反応するまで攪拌して反応を進行させる。
前記不活性ガスは、窒素(N)、ヘリウム(He)、ネオン(Ne)、アルゴン(Ar)の群から選択される種以上の気体である。
【0026】
図1は、本発明の4つのチエニルを包含し、4つのチエニルのうち、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有する、式(1)に表されるチエニルを包含するボロン-ジピリン化合物の製造方法を模式的に表す工程図である。
【0027】
図1には、化合物3a、3bを得ることのできる出発物質から出発して最終的に化合物4a、4b、5a、5bのチエニルを包含するボロン-ジピリン化合物の製造方法を示している。この工程によって後述する実施形態のように化合物3a、3bからチエニルを包含するボロン-ジピリン化合物である化合物4a、4b、5a、5bを得ることができる。
【0028】
また、本発明は、前記化学式(1)で表されるチエニルを包含するボロン-ジピリン化合物が特定のイオンと反応する時、色相の変化と蛍光変化を起す化学センサーを提供する。
より具体的には、前記化学式(1)で表される4つのチエニルを包含し、4つのチエニルの中、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物が特定のイオンと反応する時、色相変化と蛍光変化を起す化学センサーを提供する。
本発明は、前記の製造方法により製造された、化学式(1)で表されるチエニルを包含するボロン-ジピリン化合物が特定のイオンと反応する時、色相変化と蛍光変化を起す化学センサーである。
より詳細には、前記の製造方法によって製造された化学式(1)で表される4つのチエニルを包含し、その4つのチエニルの中、3つのチエニルがサソリ虫模様の空間を作る構造的な特異性を有するチエニルを包含するボロン-ジピリン化合物が特定のイオンと反応する時、色相変化と蛍光変化を起す化学センサーである。
【0029】
前記本発明の化学センサーは、式(1)で表されるチエニルを包含するボロン-ジピリン化合物が金属イオンに対して選択的に反応する。
前記化学センサーは、式(1)で表されるチエニルを包含するボロン-ジピリン化合物が金属イオンと反応することにより、色相変化と蛍光変化を表す。
【0030】
一例の実験によれば、先ず、式(1)で表される化合物を有機溶媒に溶解させてピンク色の溶液1を調製する。次いで、前記有機溶媒と同一の有機溶媒に金属イオンを投入して溶液2を得た後、前記溶液2を溶液1に添加する。このとき、溶液1の色相がピンク色から無色に変化する色相変化を起す特性と、蛍光の明るさが増加するか、または減少するような蛍光変化の反応が起る特性を示す。
【0031】
前記の有機溶媒は、テトラヒドロフラン(THF)、メチレンクロリド、エチルアルコール、n−ヘキサン、アセトン、アセテートの群から選択される1種以上を使用することができる。
【0032】
本発明の式(1)で表されるチエニルを包含するボロン-ジピリン化合物は、前記有機溶媒に対して高い溶解性があり、水に対しては比較的低い溶解性を有する。よって、アセテート溶媒と水との混合液を使用することによって溶解性を高めることができる。
【0033】
式(1)で表されるチエニルを包含するボロン−ジピリン化合物が前記の有機溶媒に溶解すると、溶液の色はピンク色を帯びる。
本発明の化学センサーは、式(1)で表示されるチエニルを包含するボロン-ジピリン化合物が銅イオンまたは水銀イオンのような金属イオンに対して選択的に反応する。
【0034】
より具体的には、本発明の化学センサーは、式(1)に表示されるチエニルを包含するボロン-ジピリン化合物が銅イオンまたは水銀イオンのような金属イオンと反応して色相変化と蛍光の変化とを示す特性を有する。例えば、前記化合物が溶解した溶液の色がピンク色から無色に変化する色相変化の特性と、蛍光の明るさが増加するか、または減少するような蛍光変化の反応を示す特性を示すことができる。
【0035】
以上、本発明のチエニルを包含するボロン-ジピリン化合物と、該化合物の製造方法、チエニルを包含するボロン-ジピリン化合物が包含された化学センサーは、本発明の目的を達成するためには前記のような条件を具備して提供されることが好ましい。
【0036】
以下、本発明の内容を実施例及び試験例を通じてより具体的に説明する。ただ、これらの実施例などは本発明をより詳細に説明するためであり、本発明がこれらの実施例に限定されるものではない。
【0037】
実施例1:3-(2-チエニル)-4,4-ジ(2-チエニル)-8-(2-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン(3-(2-thienyl)-4,4-di(2-thienyl)-8-(2-thienyl)-4-bora-3a,4a-diaza-s-indacene)[4a]の製造
下記反応式(1)のように化合物3aと2-チエニルリチウムを反応させて化合物4aを製造した。
【0038】
【化1】

【0039】
従来技術(Journal of Chemical Crystallography 2007、37、315)によって得られた化合物3a(1.35g、4.75mmol)を無水テトラヒドロフラン(THF)50mLに溶解させてアルゴン気体雰囲気下、−78℃で10分間攪拌した。この溶液に、THFによって1.0M濃度に希釈した2-チエニルリチウム30mLを1ml/secの速度で滴下した。その後、アルゴン気体の雰囲気下、-78℃で10分間さらに攪拌し、化合物3aと2-チエニルリチウムとの混合溶液の温度が常温になるまで放置した。
【0040】
TLC(thin layer chromatography)によって化合物3aがすべて反応したことを確認した後、20mLの蒸留水を混合溶液に投入して反応を終了させる。
【0041】
反応が終了した混合溶液の混合物をジクロロメタンで抽出して得た有機層を、マグネシウムスルフィドで乾燥し、ジクロロメタン溶媒を減圧乾燥により除去した後、残りの物質をシリカカラムを用いて精製した。この過程において、カラムに3回ほど通すが、このとき、へキサンとジクロロメタンが1:1の体積比で混合された混合液を流しながらカラムを展開させた。濃いピンク色を帯びる部分を集めてさらにPTLC(preparative thin layer column chromatography)と再結晶法とを利用して純粋な化合物4a(3-(2-チエニル)-4,4-ジ(2-チエニル)-8-(2-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン)を得た(0.7g、収率:31%)。
【0042】
溶融点:163 ℃。1H NMR(CD2Cl2:δ 5.32)7.72(dd,3JH−H=5.0,JH−H=0.8Hz,1Hb)、7.62(d,3JH−H=4.0Hz,1Hc)、7.58(s,1Hh)、7.48(d,3JH−H=4.6Hz,1Hd)、7.30(m,2Hn)、7.28(s,1Ha)、7.25(dd,3JH−H=0.6, 4JH−H=0.6Hz,1Hk)、7.21(dd,3JH−H=4.5,4JH−H=0.9Hz,1Hf)、7.04(d,3JH−H=3.3Hz,2Hl)、6.96(m,2Hm)、6.88(d,3JH−H=4.6Hz,1He)、6.87(s,1Hi)、6.74(dd,3JH−H=4.8,3JH−H=4.0Hz, 1Hj)、6.49(dd,3JH−H=4.0,JH−H=1.9Hz, 1Hg);13C NMR(CD2Cl2:δ 53.8)152.4(t,1JC−H=8.8Hz,1C5)、144.5(dt,1JC−H=185.0,3JC−H=9.0Hz,1Ch)、137.5(s,1C2)、136.8(t,2JC−H=9.0Hz,1C3)、135.4(p,2JC−H=5.6Hz,1C1)、134.5(m,JC−H=5.6Hz,1C6)、132.9(m,1C4)、132.8(ddd,1JC−H=169.9Hz,2JC−H=9.3Hz,3JC−H=6.1Hz,1Cc)、132.0(ddd,1JC−H=163.4Hz,3JC−H=9.2Hz,3JC−H=6.0Hz,1Ci)、131.0(dm,1JC−H=〜160Hz,1Cl)、(dm,1JC−H=〜160Hz,1Cd)、130.7(ddd,1JC−H=281.7,2JC−H=9.2,3JC−H=6.1Hz,1Cb)、129.0(dm,1JC−H=211.3Hz,1Ck)、128.5(m,1Cf)、128.2(dt,1JC−H=171.0,2JC−H=10.1Hz,1Ca)、127.6(dm,1JC−H=161.0Hz,1Cj)、127.5(dm,1JC−H=161.0Hz,2Cm)、127.1(dm,1JC−H=201.2Hz,2Cn)、122.3(dd,1JC−H=175.2,2JC−H=3.6Hz,1Ce)、118.4(ddd,1JC−H=174.8,3JC−H=8.9,3JC−H=3.5Hz,1Cg)。11B NMR(F3B・OEt2:δ 0.00)−3.59(s)、MALDITOF m/z(M+):484.04(calc.)483.99(obs.)、Anal.Calc.for C25H17BN2S4:C 61.98、H 3.54、and N 5.78、found:C 63.44、H 3.81、and N 6.00。
【0043】
実施例2:3-(2-チエニル)-4,4-ジ(2-チエニル)-8-(3-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン[4b]の製造
下記反応式2のように化合物3bと2-チエニルリチウムとを反応させて化合物4bを製造した。
【0044】
【化2】

【0045】
従来技術(Journal of Chemical Crystallography 2007、37、315)によって合成した化合物3b(0.18g、0.65mmol)を出発物質として使用し、2-チエニルリチウムを6.5mLを使用することを除いては実施例1と同様の方法によって化合物4bを製造した。
【0046】
反応終了の後に、TLCによってRfの値が0.8程度の濃い赤色蛍光を示す部分を認めることができた。それぞれ3回のシリカカラムとPTLCを通じて純粋な化合物4b(3-(2-チエニル)-4,4-ジ(2-チエニル)-8-(3-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン)を得た(0.12g、収率:35%)。
【0047】
溶融点:166 ℃。1H NMR(CD2Cl2:δ 5.32)7.79(dd,4JH−H=3.0,4JH−H=1.2Hz,1Hc)、7.57(d,J=3.0Hz,1Ha)、7.56(m,1Hh)、7.48(dd,3JH−H=5.0,4JH−H=1.2Hz,1Hb)、7.30(d,3JH−H=4.5Hz,1Hd)、7.29(dd,3JH−H=4.7,4JH−H=0.8Hz,2Hn)、7.24(dd,3JH−H=5.0,4JH−H=1.1Hz,1Hk)、7.03(d,3JH−H=obs,4JH−H=1.3Hz,1Hf)、7.02(dd,3JH−H=3.4,4JH−H=1.0Hz,2Hl)、6.95(m,2Hm)、6.85(d,3JH−H=4.5Hz,1He)、6.84(dd,3JH−H=3.7,4JH−H=1.1Hz, 1Hi)、6.73(dd,3JH−H=5.1,4JH−H=3.7Hz,1Hj)、6.47(dd,3J=4.2,1.9Hz,1Hg);13C NMR(CD2Cl2:δ 53.8)152.1(m,1C5)、144.3(dt,1JC−H=184.9,3JC−H=9.1Hz,1Ch)、139.7(s,1C2)、136.9(t,2JC−H=9.0Hz,1C3)、135.4(m,1C1)、134.6(m,1C6)、133.0(q,2JC−H=8.8Hz,1C4)、131.9(ddd,1JC−H=170.7,2JC−H=9.2,1Ci)、130.9(ddd,1JC−H=163.3,2JC−H=9.8,1Cl)、130.5(dm,1JC−H=171.9,1Cb)、130.4(dm,1JC−H=165.4Hz,1Cd)、129.6(dm,1JC−H=171.0Hz,1Cc)、128.9(dm,1JC−H=186.2Hz,1Ck)、127.9(dm,1JC−H=161.0,1Cf)、127.6(dm,1JC−H=170.8Hz,1Cj)、127.5(dm,1JC−H=168.7,2Cm)、127.0(ddd,1JC−H=184.2,2JC−H=10,3JC−H=7.8Hz,2Cn)、126.7(dt,1JC−H=186.8,3JC−H=6.9Hz,1Ca)、122.1(dd,1JC−H=175.1,3JC−H=3.7Hz,1Ce)、118.3(ddd,1JC−H=174.6,3JC−H=8.9,3JC−H=3.7Hz,1Cg)。11B NMR(BF3・OEt2:δ 0.00)−3.61(s)、MALDITOF m/z(M+):484.04(calc.)484.36(obs.)、Anal.Calc.for C25H17BN2S4:C 61.98、H 3.54、and N 5.78、found:C 62.63、H 4.21、and N 5.66
【0048】
実施例3:3-(3-チエニル)-4,4-ジ(3-チエニル)-8-(2-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン[5a]の製造
下記反応式3のように化合物3aと3-チエニルリチウムとを反応させて化合物5aを製造した。
【0049】
【化3】

【0050】
従来技術(Karlsson,L.et.al.,A Chemica Scripta 1974、6、214―221)によって3-チエニルリチウムを準備した。つまり、3-ブロモチオフェン(1.6mL、0.017mmol)を無水エーテル50mLに溶解させてアルゴン気体雰囲気下、−78℃を維持しながら10分程攪拌した。この溶液にヘキサンによって2.5Mに希釈したn-ブチルリチウム5.4mLを1ml/secの速度で滴下した。その後、10分程度さらに攪拌して3-チエニルリチウムを得た。
【0051】
化合物3a(0.46g、0.0017mol)を12mlの無水THFで溶解させて、室温状態に静置した。化合物3aが溶解した溶液を、上述した3-チエニルリチウム溶液が入っているフラスコによってカニューレ(cannula)を通じて移動させながら混合した。混合した後、アルゴン雰囲気下、−78℃を維持しながら攪拌する。10分後、TLCを通じて化合物3aが完全に反応して消耗されていることを確認し、その後、水を投入して反応を終了させた。実施例1の精製過程を経て最終的に純粋な化合物5a(3-(3-チエニル)-4,4-ジ(3-チエニル)-8-(2-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン)を得た(0.088g、収率:11%)。
【0052】
溶融点:184 ℃。1H NMR(CD2Cl2:δ 5.32)7.71(dd,3JH−H=5.1,4JH−H=1.2Hz,1Hb)、7.61(dd,3JH−H=3.7,4JH−H=1.2Hz,1Hc)、7.46(d,3JH−H=4.4Hz,1Hd)、7.41(m,1Hh)、7.28(m,1Ha)、7.19(dd,3JH−H=4.3,4JH−H=1.3Hz,1Hf)、7.15(dd,3JH−H=4.8,3JH−H=2.7Hz,2Hm)、7.01(m,1Hj)、6.97(m,1Hk)、6.94(dd,4JH−H=2.7,4JH−H=1.1Hz,2Hn)、6.89(dd,3JH−H=4.8,4JH−H=1.1Hz,2Hl)、6.81(dd,3JH−H=5.0,4JH−H=1.3Hz,2Hj)、6.74(d,3JH−H=4.4Hz, 1He)、6.46(dd,3JH−H=4.2,4JH−H=1.8Hz,1Hg);13C NMR(CD2Cl2:δ53.8)154.6(t,1JC−H=8.2Hz,1C5)143.6(dt、1JC−H=184.6,3JC−H=9.0Hz,1Ch)、138.0(s,1C2)、136.4(t,1JC−H=9.0Hz,1C3)、135.6(m,1C1)、133.4(m,1C6)、133.1(m,1C4)、132.8(ddd,1JC−H=170.0,2JC−H=9.3,3JC−H=5.8Hz,1Cc)、132.2(dm,1JC−H=152.1Hz,1Cl)、130.7(dm,1JC−H=169.6Hz,1Cd)、130.5(ddd,1JC−H=184.9,2JC−H=10.8,2JC−H=7.1Hz,1Cb)、129.2(ddd,1JC−H=171.1,3JC−H=10,3JC−H=3.6Hz,1Ci)、128.1(dm,1JC−H=180.9Hz,1Ca)、128.0(dm,1JC−H=〜170Hz,1Cf)、128.0(dm,1JC−H=〜170Hz,1Ck)、127.7(ddd,1JC−H=160.8,3JC−H=8.5,3JC−H=4.2Hz,1Cn)、124.6(ddd,1JC−H=183.2,JC−H=4.7Hz,1Cm)、124.1(ddd,1JC−H=187.6,3JC−H=6.2,3JC−H=4.7Hz,1Cj)、121.6(dd,1JC−H=174.4,3JC−H=3.5Hz,1Ce)、117.8(ddd,1JC−H=174.5,3JC−H=9.1,3JC−H=3.6Hz,1Cg)。11B NMR(BF3・OEt2:δ 0.00)−3.59(s)、MALDITOF m/z(M+):484.04(calc.)484.68(obs.)、Anal.Calc.for C25H17BN2S4:C 61.98、H 3.54、and N 5.78、found:C 63.68、H 3.82、and N 6.03。
【0053】
実施例4:3-(3-チエニル)-4,4-ジ(3-チエニル)-8-(3-チエニル)-4-ボラ-3a,4a-ジアザ-s-インダセン[5b]の製造
下記反応式4のように化合物3bと3-チエニルリチウムとを反応させて化合物5bを製造した。
【0054】
【化4】

【0055】
化合物3aの代わりに化合物3b(1g、3.65mmol)を使用することの他は、実施例3と同様な方法によって化合物5bを製造した。
最終的に得られた化合物5bは、0.15gで略8.5%の収率を示した。
【0056】
溶融点:178 ℃。1H NMR(CD2Cl2:δ 5.32)7.78(dd,4JH−H=3.0,4JH−H=1.2Hz,1Hc)、7.55(m,1Ha)、7.47(dd,3JH−H=5.0,4JH−H=1.2Hz,1Hb)、7.43(m,1Hh)、7.30(d,3JH−H=4.5Hz,1Hd)、7.17(dd,3JH−H=4.7,4JH−H=2.7Hz,2Hm)、7.03(d,3JH−H=obs,4JH−H=1.2Hz,1Hf)、7.02(m,1Hj)、6.98(m,1Hk)、6.96(dd,J=2.7,1.1Hz,2Hn)、6.91(dd,J=4.8,1.1Hz,2H1)、6.83(dd,3JH−H=5.0,4JH−H=1.4Hz,1Hi)、6.73(d,3JH−H=4.5Hz, 1He)、6.46(dd,3JH−H=4.2,JH−H=1.8Hz,1Hg);13C NMR(CD2Cl2:δ 53.8)154.3(m,1C5)、152.4(br,1C7)、143.4(dt,1JC−H=184.4,3JC−H=9.0,1Ch)、140.1(s,1C2)、136.4(t,1JC−H=9.0Hz,1C3)、135.6(m,1C1)、133.5(m,1C6)、133.2(d,1JC−H=8.7Hz,1C4)、132.2(ddd,1JC−H=164.9,2JC−H=10.5,3JC−H=4.9Hz,Cl)、130.5(ddd,1JC−H=173.0,2JC−H=8.5,3JC−H=4.7Hz,1Cb)、130.2(dd,1JC−H=175.1,3JC−H=4.2Hz,1Cd)、129.4(dm,1JC−H=185.8Hz,1Cc)、129.2(ddd,1JC−H=170.5,2JC−H=8.5,3JC−H=4.1Hz,1Ci)、128.0(ddd,1JC−H=128.0,3JC−H=8.5,3JC−H=4.4Hz,1Ck)、127.6(dm,1JC−H=152.4Hz,Cn)、127.5(dm,1JC−H=195.4Hz,1Cf)、126.6(dm,1JC−H=188.8Hz,1Ca)、124.6(ddd,1JC−H=189.6,2JC−H=9.0,3JC−H=4.7Hz,2Cm)、124.1(dt,1JC−H=187.6Hz,3JC−H=6.3,1Cj)、121.4(dd,1JC−H=171.1,2JC−H=3.5Hz,1Ce)、117.7(ddd,1JC−H=174.3,3JC−H=9.0,3JC−H=3.7Hz,1Cg)。11B NMR(BF3・OEt2:δ 0.00)−3.35(s)、MALDITOF m/z(M+):484.04(calc.)484.41(obs.)、Anal.Calc.for C25H17BN2S4:C 61.98、H 3.54、and N 5.78、found:C 62.56、H 3.82、and N 5.88。
【0057】
実施例5:金属イオンに対する選択的反応に関する実験
紫外線-赤外線の吸収分光法と蛍光分光法とを利用するために、実施例1から実施例4で製造したそれぞれの化合物4a、4b、5a、5bの4つの物質をそれぞれCH3CNに溶解させて1×10−5モル濃度の溶液を調製した。
【0058】
使用した金属イオンは、全て金属-過塩素酸塩の形態で、やはりCH3CNに溶解させて1×10−3モル濃度に調製した。金属イオンとして、Zn2+、Pb2+、Mn2+、Hg2+、Cu2+、Cs+、Ca2+、Cd2+、Ag+を使用した。
化合物4a、4b、5a、5bの4つの物質をそれぞれ金属イオン間の化学量論比が1:1になるようにして、化合物4a-金属イオンの混合溶液、化合物4b-金属イオンの混合溶液、化合物5a-金属イオンの混合溶液、化合物5b-金属イオンの混合溶液の4つの化合物-金属イオンの混合溶液を調製し、紫外線-赤外線吸収分光器及び蛍光分光器を通じて観察した。
【0059】
化合物4bでは、Cu2+に対して懸隔なスペクトルの変化を示し、非常に微弱ではあるが、他の金属イオンなどと比較するとき、Hg2+に対する弱いスペクトル変化を示した。また、化合物4bに比べてはその変化が微々とはいえども、化合物4a、5a、5bもやはり銅と水銀イオンに対して紫外線-赤外線吸収分光スペクトルの変化を示した(図2a、図2b、図2c、図2d参照)。
【0060】
このような変化は、蛍光スペクトルでも確認され、これを図3a〜図3dに示す。
これによって、4つのチエニル基が置換されたサソリ虫模様のボロン-ジピリン化合物が銅及び水銀イオンに対して選択的に反応することが確認された。特に、化合物4bでは、投入した銅イオンの量に従ってピンク色の化合物4b溶液の色相が無色相に変化することが観察され、紫外線を照らすとき示す蛍光の強度も増加した。一方、水銀イオンに対してはこのような色相の変化及び蛍光の強度変化が少ないことが観察された(図4a、図4b参照)。
【0061】
実施例6:銅イオン及び水銀イオンに対する検出限界に対する実験
銅イオン及び水銀イオンの検出限界を測定するために、化合物4a、4b、5a、5bの4つの物質をそれぞれCH3CNに溶解し、1×10−5モル濃度の溶液をそれぞれ3mLずつ取って石英セルに分注し、銅イオン溶液をマイクロピペットで滴下しながら一定時間おきに紫外線-赤外線吸収分光スペクトルを測定した。
化合物4a、4b、5a、5bが溶解した溶液に1×10−3モル濃度の銅イオンを10μLだけ投入してもスペクトルの変化を示した。これは銅イオン濃度が略270ppbに該当する値である(図5a〜図5d参照)。
【0062】
上記と同様の方法によって、化合物4a、4b、5a、5bの4つの物質をそれぞれCH3CNに溶解し、1×10−5モル濃度の溶液を調製し、これに水銀イオンを添加しながらスペクトルの変化を観察した。水銀の場合には、投入する水銀イオンの量によって継続的な波長の変化とスペクトルの変化とを観察することができた。化合物4a、4b、5a、5bの水銀に対する検出限界は、1×10−3モル濃度の水銀イオン溶液20μLで、略1.7ppmに該当する。
【0063】
実施例7:銅イオン結合可逆性に対する実験
化合物4a、4b、5a、5bの4つの物質が銅イオンまたは水銀イオンと結合した後、さらに本来の配位子状態に戻る結合可逆性に対する実験を行うことによって本発明で提示する物質などのセンサーとしての特性を確認した。
代表的に化合物4b及び化合物5bを選択して結合可逆性に対する実験を紫外線-赤外線分光スペクトルを通じて実施した。
【0064】
化合物4bをCH3CNに溶解し、1×10−5モル濃度の溶液を調製した。銅イオンは5×10―3モルの濃度に調製した。Na4EDTAを蒸留水に溶解し、0.01モルの濃度に調製した。5つの試料瓶を準備し、それぞれの試料瓶に化合物4bが溶解し溶液を1mLずつ分注し、1番試料瓶は化合物4bが溶解した溶液のみに、2番試料瓶は化合物4bが溶解した溶液に対してモル比の15倍に該当する銅イオンを入れて、3番試料瓶は2番試料瓶に化合物4bが溶解した溶液に対してモル比で30倍ほどのNa4EDTAを入れた。4番試料瓶には順序を変えて化合物4bが溶解した溶液にモル比で30倍ほどのNa4EDTAを先ず投入し、よく混合した後、15倍のモルに該当する銅イオンを混合した。最後の5番試料瓶は化合物4bが溶解した溶液とNa4EDTAの約1:30の混合物である。また、5つの試料瓶は化合物4bの濃度をすべて一定に合わせるためにCH3CNを補充して全部2.5mLの体積を有するようにした。5つの試料の紫外線-赤外線吸収分光スペクトルを比較することによって、結合可逆性に対する結果を確認した。
【0065】
図6のように、化合物4bが銅と結合すると、本来の化合物4bが示す吸収分光スペクトルの模様が懸隔に変化することを確認することができる。ただし、2番試料に比べてEDTAが添加された3番試料の場合、本来と同じ程度ではないが、吸収分光スペクトルの模様がさらに変化していることが確認された。このような実験は化合物5bに対しても同一の条件下で行われたが(図7参照)、化合物4bと5b、2種類においてこの試料はEDTAが添加されることによって溶液が濁ることを確認した。吸収分光スペクトルがEDTA添加によって変化を示すが、その形態が本来の化合物4b及び5bのスペクトルに比べては不明瞭とする理由は、試料の濁度のためであると見える。
【0066】
実施例8:水銀イオン結合可逆性に対する実験
水銀イオンと結合した化合物4b及び5bの試料に対して結合可逆性に対する実験を、KIを利用して実施した。水銀イオンは、ヨウ化物アニオンと容易に結合することが知られている。
実施例7のように、5つの試料瓶にそれぞれ1mLずつの化合物4bを分注し、1番試料瓶は化合物4b、2番試料瓶は化合物4bと、モル比で15倍に該当する水銀イオン、3番試料瓶は2番試料瓶と同じ組成で約30倍のKIを入れた。4番試料瓶は化合物4bに約30倍のKIを先ず入れてよく混合した後、約15倍の水銀イオンを投入した。5番試料瓶は化合物4bの約30倍のKIを混合した。また、5つの試料は全て3mLの体積にしてCH3CNを補充することによって反応する化合物4bのモル濃度を全て同じ条件にした。同様に化合物5bに対しても試料を準備した。このとき、化合物4b及び5bは、CH3CNに溶解して5×10−5モル濃度、水銀イオンもCH3CNに溶かした状態で1×10−3モル濃度にして準備した。また、KIは蒸留水に溶解して1×10−3モル濃度に調製した。水銀イオンの場合には、準備した試料が全て清澄状態であり、図8及び図9のように、KIが投入されることによって、水銀イオンが結合した化合物4bまたは化合物5bから脱離し、本来の化合物4bまたは化合物5bが示す吸収分光スペクトルと同様の形態及び波長と一致したことから、水銀イオンとの結合可逆性に対する明白な結果が得られた。これは本発明において提示するチエニルを包含するボロン-ジピリン化合物が化学センサーとしての必要とする可逆性の特性をよく示す潜在的な結果としてその重要性を有する。
【0067】
上述のように、本発明の好ましい実施例を参照して説明したが、該当技術分野の熟練された当業者であれば特許請求範囲に記載の本発明の思想及び領域の範囲内で本発明を多様に修正または変更させることができる。
【産業上の利用可能性】
【0068】
本発明のチエニルが包含されたボロン-ジピリン化合物は、金属イオン、特に銅イオンまたは水銀イオンを検出することができ、化学センサーとして利用することができる、また、この化合物に、銅イオン、水銀イオンのように環境汚染をもたらす物質を包含させて、これらのイオンを除去するために利用することも可能である。
【図面の簡単な説明】
【0069】
【図1】4つのチエニルを包含するボロン-ジピリン化合物の製造工程の一例を示した工程図である。
【図2a】本発明の実施例1で製造した化合物4aの金属イオンに対する選択性を示す吸光スペクトルである。
【図2b】本発明の実施例2で製造した化合物4bの金属イオンに対する選択性を示す吸光スペクトルである。
【図2c】本発明の実施例3で製造した化合物5aの金属イオンに対する選択性を示す吸光スペクトルである。
【図2d】本発明の実施例4で製造した化合物5bの金属イオンに対する選択性を示す吸光スペクトルである。
【図3a】本発明の実施例1で製造した化合物4aの金属イオンに対する選択性を示す吸光スペクトルである。
【図3b】本発明の実施例2で製造した化合物4bの金属イオンに対する選択性を示す吸光スペクトルである。
【図3c】本発明の実施例3で製造した化合物5aの金属イオンに対する選択性を示す吸光スペクトルである。
【図3d】本発明の実施例4で製造した化合物5bの金属イオンに対する選択性を示す吸光スペクトルである。
【図4a】本発明の実施例1で製造した化合物4a及び実施例2で製造した化合物4bの銅イオン感知による色相変化及び蛍光変化を示した写真図である。
【図4b】本発明の実施例3で製造した化合物5a及び実施例3で製造した化合物5bの銅イオン感知による色相変化及び蛍光変化を示した写真図である。
【図5a】本発明の実施例1で製造した化合物4aの銅イオンの滴下による吸光スペクトルの変化を示したグラフである。
【図5b】本発明の実施例2で製造した化合物4bの銅イオンの滴下による吸光スペクトルの変化を示したグラフである。
【図5c】本発明の実施例3で製造した化合物5aの銅イオンの滴下による吸光スペクトルの変化を示したグラフである。
【図5d】本発明の実施例4で製造した化合物5bの銅イオンの滴下による吸光スペクトルの変化を示したグラフである。
【図6】EDTA添加による化合物4b-銅イオン化合物の結合可逆性を示す吸光スペクトルである。
【図7】EDTA添加による化合物5b-銅イオン化合物の結合可逆性を示す吸光スペクトルである。
【図8】KI添加による化合物4b-銅イオン化合物の結合可逆性を示す吸光スペクトルである。
【図9】KI添加による化合物5b-銅イオン化合物の結合可逆性を示す吸光スペクトルである。
【特許請求の範囲】
【請求項1】
式(1)
3-(R)-4,4-ジ(R)-8-(R)-4-ボラ-3a,4a-ジアザ-s-インダセン (1)
(式中、Rは2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
で表されるチエニルを包含するボロン-ジピリン化合物。
【請求項2】
式(1)の化合物は、式(2)
3-(R)-4,4-ジフルオロ-4-ボラ-3a,4a-ジアザ-s-インダセン (2)
(式中、Rは2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
の化合物におけるジフルオロと8位の炭素を2-チエニル及び3-チエニルの群から選択されるいずれか1つに置換させて得られる請求項1に記載のボロン-ジピリン化合物。
【請求項3】
式(2)
3-(R)-4,4-ジフルオロ-4-ボラ-3a,4a-ジアザ-s-インダセン (2)
(式中、Rは2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
の化合物を、チエニル基を有する物質と反応させて、式(2)の化合物であるジフルオロと8位の炭素をチエニル基によって置換させ、式(1)
3-(R)-4,4-ジ(R)-8-(R)-4-ボラ-3a,4a-ジアザ-s-インダセン (1)
(式中、Rは2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
で表されるチエニルを包含するボロン-ジピリン化合物の製造方法。
【請求項4】
式(2)の化合物と、チエニル基を有する物質との反応は、式(2)の化合物1モルに対してチエニル基を有する物質1〜10モルを反応させる請求項3に記載のボロン-ジピリン化合物の製造方法。
【請求項5】
式(2)の化合物と、チエニル基を有する物質の反応は、式(2)の化合物1モルに対してチエニル基を有する物質1〜10モルを不活性ガス雰囲気下、−90℃〜0℃で攪拌して反応させる請求項3又は4に記載のボロン-ジピリン化合物の製造方法。
【請求項6】
前記チエニル基を有する物質は、2-チエニル及び3-チエニルの群から選択されるいずれか1つの官能基を有する物質である請求項3〜5のいずれか1つに記載のボロン-ジピリン化合物の製造方法。
【請求項7】
前記チエニル基を有する物質は、2-チエニルリチウム及び3-チエニルリチウムの群から選択されるいずれか1つである請求項6に記載のボロン-ジピリン化合物の製造方法。
【請求項8】
請求項1又は2の式(1)で表されるチエニルを包含するボロン-ジピリン化合物が含有された化学センサー。
【請求項9】
式(1)で表されるチエニルを包含するボロン-ジピリン化合物を、金属イオンに対して選択的に反応させる請求項8に記載の化学センサー。
【請求項10】
式(1)で表されるチエニルを包含するボロン-ジピリン化合物を金属イオンと反応させて得られる色相変化と蛍光変化との選択性を利用する請求項8又は9に記載の化学センサー。
【請求項11】
金属イオンは、銅イオンまたは水銀イオンである請求項9又は10に記載の化学センサー。
【請求項1】
式(1)
3-(R)-4,4-ジ(R)-8-(R)-4-ボラ-3a,4a-ジアザ-s-インダセン (1)
(式中、Rは2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
で表されるチエニルを包含するボロン-ジピリン化合物。
【請求項2】
式(1)の化合物は、式(2)
3-(R)-4,4-ジフルオロ-4-ボラ-3a,4a-ジアザ-s-インダセン (2)
(式中、Rは2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
の化合物におけるジフルオロと8位の炭素を2-チエニル及び3-チエニルの群から選択されるいずれか1つに置換させて得られる請求項1に記載のボロン-ジピリン化合物。
【請求項3】
式(2)
3-(R)-4,4-ジフルオロ-4-ボラ-3a,4a-ジアザ-s-インダセン (2)
(式中、Rは2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
の化合物を、チエニル基を有する物質と反応させて、式(2)の化合物であるジフルオロと8位の炭素をチエニル基によって置換させ、式(1)
3-(R)-4,4-ジ(R)-8-(R)-4-ボラ-3a,4a-ジアザ-s-インダセン (1)
(式中、Rは2-チエニル及び3-チエニルの群から選択されるいずれか1つである。)
で表されるチエニルを包含するボロン-ジピリン化合物の製造方法。
【請求項4】
式(2)の化合物と、チエニル基を有する物質との反応は、式(2)の化合物1モルに対してチエニル基を有する物質1〜10モルを反応させる請求項3に記載のボロン-ジピリン化合物の製造方法。
【請求項5】
式(2)の化合物と、チエニル基を有する物質の反応は、式(2)の化合物1モルに対してチエニル基を有する物質1〜10モルを不活性ガス雰囲気下、−90℃〜0℃で攪拌して反応させる請求項3又は4に記載のボロン-ジピリン化合物の製造方法。
【請求項6】
前記チエニル基を有する物質は、2-チエニル及び3-チエニルの群から選択されるいずれか1つの官能基を有する物質である請求項3〜5のいずれか1つに記載のボロン-ジピリン化合物の製造方法。
【請求項7】
前記チエニル基を有する物質は、2-チエニルリチウム及び3-チエニルリチウムの群から選択されるいずれか1つである請求項6に記載のボロン-ジピリン化合物の製造方法。
【請求項8】
請求項1又は2の式(1)で表されるチエニルを包含するボロン-ジピリン化合物が含有された化学センサー。
【請求項9】
式(1)で表されるチエニルを包含するボロン-ジピリン化合物を、金属イオンに対して選択的に反応させる請求項8に記載の化学センサー。
【請求項10】
式(1)で表されるチエニルを包含するボロン-ジピリン化合物を金属イオンと反応させて得られる色相変化と蛍光変化との選択性を利用する請求項8又は9に記載の化学センサー。
【請求項11】
金属イオンは、銅イオンまたは水銀イオンである請求項9又は10に記載の化学センサー。
【図1】


【図2a】


【図2b】


【図2c】


【図2d】


【図3a】


【図3b】


【図3c】


【図3d】


【図4a】


【図4b】


【図5a】


【図5b】


【図5c】


【図5d】


【図6】


【図7】


【図8】


【図9】




【図2a】


【図2b】


【図2c】


【図2d】


【図3a】


【図3b】


【図3c】


【図3d】


【図4a】


【図4b】


【図5a】


【図5b】


【図5c】


【図5d】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2009−191060(P2009−191060A)
【公開日】平成21年8月27日(2009.8.27)
【国際特許分類】
【出願番号】特願2008−120920(P2008−120920)
【出願日】平成20年5月7日(2008.5.7)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 〔発行所〕 American Chemical Society Publications 〔刊行物名〕 「Inorganic Chemistry」 第46巻 第25号 〔発行日〕 2007年12月10日
【出願人】(592127149)韓国科学技術院 (129)
【氏名又は名称原語表記】KOREA ADVANCED INSTITUTE OF SCIENCE AND TECHNOLOGY
【住所又は居所原語表記】373−1,Gusung−dong,Yuseong−ku,Daejeon 305−701 KR
【Fターム(参考)】
【公開日】平成21年8月27日(2009.8.27)
【国際特許分類】
【出願日】平成20年5月7日(2008.5.7)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 〔発行所〕 American Chemical Society Publications 〔刊行物名〕 「Inorganic Chemistry」 第46巻 第25号 〔発行日〕 2007年12月10日
【出願人】(592127149)韓国科学技術院 (129)
【氏名又は名称原語表記】KOREA ADVANCED INSTITUTE OF SCIENCE AND TECHNOLOGY
【住所又は居所原語表記】373−1,Gusung−dong,Yuseong−ku,Daejeon 305−701 KR
【Fターム(参考)】
[ Back to top ]

