チタニアナノチューブアレイおよびチタニア電極の作成方法、チタニア電極、並びにこのチタニア電極を適用した色素増感太陽電池
【課題】理想的な幾何学形状を有し、高い電子伝導性を併せ持つチタニア電極の作製、およびこれを用いた高効率な色素増感太陽電池の提供。
【解決手段】電解後のアモルファス状態のチタニアナノチューブアレイをまず200〜300℃の低温で漸次昇温、焼成、降温し、整然と並んだチタニアナノチューブアレイの形状を固定した後、400〜650℃の高温で漸次昇温、焼成、降温することにより、アナターゼの{101}面の格子像がチューブの軸方向に走る単結晶チタニアナノチューブアレイを得た後、得られたチタニアナノチューブアレイ膜をTiO2の微粒子膜を塗布したITO基板上に接合する方法によってチタニア電極を作製するものとし、さらに、得られたチタニア電極を適用した色素増感太陽電池とする。
【解決手段】電解後のアモルファス状態のチタニアナノチューブアレイをまず200〜300℃の低温で漸次昇温、焼成、降温し、整然と並んだチタニアナノチューブアレイの形状を固定した後、400〜650℃の高温で漸次昇温、焼成、降温することにより、アナターゼの{101}面の格子像がチューブの軸方向に走る単結晶チタニアナノチューブアレイを得た後、得られたチタニアナノチューブアレイ膜をTiO2の微粒子膜を塗布したITO基板上に接合する方法によってチタニア電極を作製するものとし、さらに、得られたチタニア電極を適用した色素増感太陽電池とする。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、チタニアナノチューブアレイおよびチタニア電極の新規な作成方法、チタニア電極、並びにこのチタニア電極を適用した色素増感太陽電池に関する。
【背景技術】
【0002】
近年のグローバル化に伴い、発展途上国が急速に経済成長したことで、これまで先進国の経済成長によって消費されてきたエネルギー量をはるかに上回るエネルギー消費が起こっている。この膨大なエネルギー消費の増加を賄うために、石油エネルギー、化石燃料を中心としたエネルギー供給以外の、再生可能な環境負荷の少ない新規エネルギー開発が必須となっている。
【0003】
再生可能な新規エネルギー源として、最近注目されているのが太陽電池、風力発電、バイオ燃料であるが、最も有望な新規エネルギー源は太陽電池であると考えられている。
現在実用化されている太陽電池はシリコン太陽電池である。高い変換効率を獲得するためにはやはり、高純度単結晶シリコンを大量に使用しなければならないが、これには材料コストおよび精製に要する製造コストが高いといった問題点がある。
以上の点から、現在のシリコン太陽電池では、未だに化石燃料による発電コストに追いついていないのが現状といえる。
【0004】
この解決案として、有機系太陽電池である次世代型太陽電池の色素増感太陽電池(DSSC; Dye Sensitized Solar Cells)が挙げられる。
図18に色素増感太陽電池の基本セル構造を示す。増感色素には主として、太陽光の可視光領域まで吸収できるルテニウム(Ru)錯体が用いられ、光電極として導電性ガラス上にナノサイズの多孔質チタニア薄膜が形成されたものが使われている。その対極は、導電性ガラスに触媒として白金をコートしたもの、電解質には、酸化還元対を含む有機溶媒として、I−/I3−系が用いられる。
【0005】
色素増感太陽電池は従来の高純度単結晶シリコンよりも資源的な制約が少ない材料で構成されており、また製造プロセスが安価で低コストが期待されている上に形状や色を自由に変えられるといった特徴をもつことから、非常に魅力的な太陽電池として注目を集めている。
ところが、実用化に向けていくつかの課題を克服しなければならない。その一つとして、シリコン太陽電池と比較して光電変換効率が低い点が挙げられる。
【0006】
ここで、色素増感太陽電池の発電原理を含めて、変換効率の低い原因について説明する。色素増感太陽電池の発電原理は、従来のpn接合型太陽電池とは異なり、光合成の発電原理に類似する。
まず、図18に示す通り、太陽光を吸収した色素は光エネルギーによって励起された後、電子をチタニアへ与えて酸化状態になる。チタニアへ移動した電子は、チタニア電極の導電性ガラスにまで到達し、外部回路を通じて対極に移動する。一方、酸化状態になった色素は、電解質(I−)から電子を受け取って元の状態へと戻り、電解質は酸化状態となる(3I− →I3−+2e− )。酸化状態の電解質(I3−)は対極から電子を受け取り、還元状態に戻る。この一連のサイクルによって電池として機能する。
色素増感太陽電池の光電変換効率が低いのは、エネルギーロスが多いためである。例えば、可視光以上の波長領域をカバーできていない点、色素からチタニアへの注入効率、高エネルギー光からの高エネルギー電子を利用できていない点、チタニア間を移動する電子と電解質中のI3−イオンとの再結合反応による逆電子移動ロス、注入時および色素の再生時のエネルギー差によるロスその他が挙げられる。これらの問題点に対していくつか検討が行われてきたが、解決されていない問題もまだ数多く存在する。
【先行技術文献】
【非特許文献】
【0007】
【非特許文献1】Craig A. Grimes, et al., Nanotechnology, 17, 1446-1448 (2006)
【非特許文献2】P. Schmuki, et al., Nano Letters, 6, 215-218 (2006)
【非特許文献3】Craig A. Grimes, et al., Adv. Funct. Mater., 15, 1291-1296 (2005)
【非特許文献4】J. Jiu, et al., J.Electrocheml Soc, 151, A1653-A1658 (2004)
【発明の開示】
【発明が解決しようとする課題】
【0008】
ところで、図18に基本構造を示す色素増感太陽電池のチタニア電極に、結晶性の高い粒界の無いチタニア材料を利用すれば、発電効率の向上が見込まれるとされている。つまり、色素増感太陽電池の高効率化のためには、1次元形状の高結晶性チタニアナノ材料による高い電子伝導性に加え、規則配列を持ったチタニア電極構造の構築が求められている。
これに応え得る材料として、チタン金属薄片を定電位(定電圧)電解することで作製されるチタニアナノチューブアレイ(TNTA)がある。非特許文献1には、規則配列構造をもったチタニアナノチューブアレイが定電位電解法によってチタン金属の上に形成されることが開示されている。
【0009】
ここで、上記チタニアナノチューブアレイに関しては、定電位電解による作成直後はアモルファスであるナノチューブアレイを焼成することで結晶化を行い得るところ、従来法の下では結晶子径が20nm程度の多結晶となり、高い電子伝導性が望めないという問題点があった。
【0010】
さらに、上記の通りチタニアナノチューブアレイは定電位電解法によりチタン金属の上に形成されるところ、チタン金属は光を通さない性質があることから、チタニアナノチューブアレイを色素増感太陽電池に応用するには工夫が必要であった。
この問題については、これまでに種々創案がなされている。図19および図20にその一例を示す。
【0011】
図19に示す例は、チタニアナノチューブアレイを色素増感太陽電池に応用する手段として、白金電極の白金を薄く蒸着して透明性を持たせ、白金電極側から光を入射する手法を用いた例である。
しかしながら、この手法では白金電極の透明性の問題のほか、光を最も良く吸収して電子注入が最大となる位置が電子収集電極から最も遠い位置となると言う構造上の問題があり、高効率が望めない欠点があった。
【0012】
次に、図20に示す例は、透明導電膜或いは透明導電性ガラス(ITO基板)上にチタン金属を約500nm蒸着し、これを陽極酸化することで、透明導電膜に長さ約360nmのチタニアナノチューブアレイを作製したものである(非特許文献2参照)。非特許文献2では、チタニア層の厚みは通常の約1/30にも拘わらず、光電変換効率2.9%を達成していることから、規則配列を持った構造が理想的なチタニア電極構造であると考えられる。
さらに、図20上段に示すように、非特許文献3では、ITO基板上にチタンを蒸着後、定電位電解を実行してチタニアナノチューブアレイを作製したのち、焼成(450℃、3時間)を行うことによって透明導電性ガラス全体の透明度を上昇させる例が開示されている。
ところが、これら非特許文献2および3に開示された手法では経済的に大きな難点があり、実用的ではない。
【0013】
このように、チタン箔の陽極酸化によって得られるチタニアナノチューブアレイを色素増感太陽電池に応用して高効率化を実現した製品を実用化するには、上述したチタン蒸着法以外でチタニア電極側から太陽光を照射することが可能なチタニア電極を作製する方法を見出す必要があった。すなわち、チタニア電極構造を適用した色素増感太陽電池の更なる効率向上には、経済的にも十分リーズナブルな実用的手法でチタニアナノチューブアレイをチタン金属と分離させ、配列制御が維持された状態でITO基板に接合する手法を提供する必要があった。
【0014】
したがって本発明は、上記問題点を解決し、色素増感太陽電池のチタニア電極構造への適用を前提に、単結晶チタニアナノチューブアレイの作製を可能とする焼成法、並びにそれによって得られたチタニア電極構造およびこれを適用した色素増感太陽電池を提供することを課題とする。
【0015】
また本発明は、色素増感太陽電池のチタニア電極構造への適用を前提に、経済的にも十分リーズナブルな実用的手法でチタニアナノチューブアレイをチタン金属と分離させ、配列制御が維持された状態でITO基板に接合する手法、並びにそれによって得られたチタニア電極構造およびこれを適用した色素増感太陽電池を提供することを課題とする。
【課題を解決するための手段】
【0016】
上記課題を解決すべく種々検討を行った結果、本願発明者は、
i)電解後のアモルファス状態のチタニアナノチューブアレイをまず200〜300℃の低温で漸次昇温、焼成、降温し、整然と並んだチタニアナノチューブアレイの形状を固定した後、400〜650℃の高温で漸次昇温、焼成、降温することにより、アナターゼの{101}面の格子像がチューブの軸方向に走る単結晶チタニアナノチューブアレイを得た後、得られたチタニアナノチューブアレイ膜をTiO2の微粒子膜を塗布したITO基板上に接合する方法によってチタニア電極を作製するものとし、さらに、得られたチタニア電極を色素増感太陽電池に適用すること、また、
ii)チタン金属を溶解除去することをアプローチとしてチタン金属とチタニアナノチューブアレイを分離させ、配列状態を維持したままチタニアナノチューブアレイをITO基板上に接着する方法すなわち、定電位電解法によりチタン金属の上に形成されたチタニアナノチューブアレイについて、チタン金属を適宜溶解除去後、得られたチタニアナノチューブアレイ膜を、TiO2の微粒子膜が形成された透明導電性ガラス上に接合する方法によってチタニア電極を作製するものとし、さらに、得られたチタニア電極を色素増感太陽電池に適用すること、
で上記課題を解決可能なことを見い出し、本発明を完成させた。
【0017】
上記課題を解決可能な本発明のチタニアナノチューブアレイの作成方法は、(1)チタニアナノチューブアレイの作成方法であって、
定電位電解法により、作用電極とされた箔状または板状のチタンを電解し、前記チタン上にチタニアナノチューブアレイを作成するステップと、
前記電解後、アモルファス状態の前記チタニアナノチューブアレイを漸次200℃<t1≦300℃(t1:第1の焼成温度)まで昇温して焼成後、漸次室温まで降温し、前記チタニアナノチューブアレイの整列形状を固定する第1の焼成ステップと、
前記第1の焼成ステップを経た後の前記チタニアナノチューブアレイを漸次400℃<t2≦600℃(t2:第2の焼成温度)まで昇温して焼成後、漸次室温まで降温することにより、アナターゼの{101}面の格子像がチューブの軸方向に走る単結晶チタニアナノチューブアレイを得る第2の焼成ステップと、
からなることを特徴とするものである。
【0018】
又上記課題を解決可能な本発明のチタニア電極の作成方法は、(2)チタニア電極の作成方法であって、
本願請求項1に記載の方法で前記チタニアナノチューブアレイを作成した前記チタンをITO基板上に載置するステップと、
チタン溶解手段により前記ITO基板上の前記チタンを溶解除去するステップと、
前記チタニアナノチューブアレイを前記ITO基板に接合するステップと、
からなることを特徴とするものである。
【0019】
また、本願請求項3に記載のチタニア電極の作成方法は、(3)本願請求項2に記載のチタニア電極の作成方法であって、
前記チタン溶解手段が前記チタン上へ臭素メタノール溶液を滴下することからなることを特徴とするものである。
【0020】
また、本願請求項4に記載のチタニア電極の作成方法は、(4)本願請求項2または3に記載のチタニア電極の作成方法であって、
前記ITO基板の表面にはチタニア薄膜層が形成されており、前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合することを特徴とするものである。
【0021】
また、本願請求項5に記載のチタニア電極の作成方法は、(5)本願請求項4に記載のチタニア電極の作成方法であって、
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、TiO2微粒子を形成するための反応原液を前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とするものである。
【0022】
また、本願請求項6に記載のチタニア電極の作成方法は、(6)本願請求項5に記載のチタニア電極の作成方法であって、
前記反応原液が少なくともエチレンオキサイド/プロピレンオキサイド/エチレンオキサイドの骨格からなるトリブロック共重合体を含有したものからなることを特徴とするものである。
【0023】
また、本願請求項7に記載のチタニア電極の作成方法は、(7)本願請求項4に記載のチタニア電極の作成方法であって、
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、オルトチタン酸テトライソプロピル溶液を前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とするものである。
【0024】
また、本願請求項8に記載のチタニア電極の作成方法は、(8)本願請求項4に記載のチタニア電極の作成方法であって、
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、TiO2微粒子ゲルを前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とするものである。
【0025】
又上記課題を解決可能な本発明のチタニア電極は、(9)色素増感太陽電池に適用され、電解質を挟んで対極に対向配置されて使用されるチタニア電極であって、本願請求項2〜8のいずれか1項に記載の方法で作成されたものからなることを特徴とする
ものである。
【0026】
又上記課題を解決可能な本発明の色素増感太陽電池は、(10)電解質を挟んで互いに対向するチタニア電極と対極とからなる色素増感太陽電池であって、
前記チタニア電極が本願請求項9に記載のものからなっていることを特徴とするものである。
【0027】
また、本願請求項11に記載の色素増感太陽電池は、(11)本願請求項10に記載の色素増感太陽電池であって、
前記対極が、ITOガラスに白金が蒸着された白金電極からなることを特徴とするものである。
【0028】
[各試薬について]
本明細書で挙げた試薬の内、主要なものの詳細は次の通りである。
・グリセリン HO(CH2)CHOH(CH2)OH = 92.09 試薬特級(和光純薬工業社)、室温保存
・フッ化アンモニウム NH4F = 37.04 試薬特級(和光純薬工業社)、室温保存、吸湿性
・メタノール CH3OH = 32.04 試薬特級(和光純薬工業社)、遮光保存
・超純水: 18MΩ以上の抵抗値を示すElix(ミリポア社)を用いて精製し、更にメンブランフィルター(ADVANTEC、0.1μm、90mm)で減圧濾過した濾過済み超純水を使用。
・トリブロック共重合体(tri-block copolymer)F127
HO-(CH2 CH2O)106-(CH2 C(CH)3HO)70-(CH2 CH2O)106H 試薬(BASF)、遮光保存
【発明の効果】
【0029】
本発明により作成された単結晶のチタニアナノチューブアレイは、格段に高い電子伝導性が期待されることが明らかとなった。したがって本発明によれば、理想的な幾何学形状を有し、高い電子伝導性を併せ持つチタニア電極の作製が可能となり、これを色素増感太陽電池に適用することにより、色素増感太陽電池の効率向上を図ることができる。
【図面の簡単な説明】
【0030】
【図1】定電位電解装置の一例を示す図である。
【図2】定電位電解法により金属アルミニウムの陽極酸化を行うことを示す模式図である。
【図3】定電位電解によって得られるチタニアナノチューブアレイのSEM画像である。
【図4】定電位電解法によりチタン金属上にチタニアナノチューブアレイを形成する一例を示す図である。
【図5】定電位電解法によりチタン金属上にチタニアナノチューブアレイを形成する一例を示す図である。
【図6】焼成後に得られたチタニアナノチューブアレイの評価結果を示すSEM画像である。
【図7】焼成前後のTi−TNTA試料のXRD測定結果を示す図である。
【図8】焼成温度を変えてTi−TNTA試料を作成した場合のXRD測定結果を示す図である。
【図9】焼成後に得られたチタニアナノチューブアレイのHRTEM画像である。
【図10】本発明の色素増感太陽電池の概略構造を示す図である。
【図11】本発明による、チタニアナノチューブアレイをチタン金属と分離させる方法の一例を示す図である。
【図12】TIPT溶液を含んだF127ゲルから形成されるTiO2試料のXRD測定結果を示す図である。
【図13】TIPT溶液を含んだF127ゲルから形成されるTiO2試料のHRTEM画像である。
【図14】チタニアナノチューブアレイに、F127ゲルを用いてTiO2微粒子を析出させた場合のSEM画像およびHRTEM画像である。
【図15】実施例1および2につき説明する図である。
【図16】実施例1および2につき説明する図である。
【図17】実施例3につき説明する図である。
【図18】色素増感太陽電池の基本構造を示す図である。
【図19】従来例に付き説明する図である。
【図20】従来例に付き説明する図である。
【発明を実施するための形態】
【0031】
以下では、添付図面に基づき、本発明のチタニアナノチューブアレイおよびチタニア電極の作成方法、チタニア電極、並びにこのチタニア電極を適用した色素増感太陽電池の概要を説明する。
【0032】
[定電位電解法によるチタニアナノチューブの作成]
まずはじめに、本発明のチタニアナノチューブアレイの作成方法につき説明する。
図1に、本発明のチタニアナノチューブアレイを作成するために用いた定電位電解装置の一例を示す。
定電位電解法自体は種々の分野で用いられており、図2に示す通り、金属アルミニウムの陽極酸化の研究でも定電位電解法は用いられている。一例として図2左欄に、アルミニウムに規則的な配列パターンからなる多孔質層が形成される様子を、また図2右欄の(a)および(b)に、規則的な配列パターンが形成された多孔質構造からなるアルミナを上方から観た図および断面図を示す。
【0033】
本発明では、チタン金属の定電位電解によってチタニアナノチューブアレイが作成される知見に基づき種々検討の結果、1次元の高い電子伝導性に加えて、理想的なチタニア電極構造を構築可能なことを見い出した。以下、順を追って説明する。
【0034】
図1に示す定電位電解装置50は、電解槽51と、電解槽51内に満たされたグリセリン溶液からなる電解質52と、電解槽51の外に設けられたポテンショスタット53と、一端側がポテンショスタット53にそれぞれ接続される一方、他端側がそれぞれ電解槽51内の電解質52中に差し込まれた、チタン金属(金属板または金属箔)からなる作用電極54、白金箔からなる対極55および塩化銀からなる参照電極56と、電解質52の温度を測定する温度計57と、電解槽51の外部より電解質52中に窒素ガス58を供給する窒素タンク59と、から構成されている。この構成によって電気化学セルを構成し、10V〜40Vの定電位にて定電位電解を行うことにより、チタン金属上にチタニアナノチューブアレイ(Ti−TNTA試料)を作成することができる。なお、電解時間は15〜50時間程度であれば良く、好ましくは20〜40時間である。電解質温度は15〜45℃であれば良く、好ましくは20〜40℃であれば良い。
定電位電解を行っている期間中、電解質温度および電解電位は一定に保たれることが好ましい。
【0035】
図3上段に、上の条件下でのチタンのアノード酸化による過渡電流を示す。反応の初期段階で急激に電流密度は減少し、その後1時間以内に定常状態に達することが明らかとなった。
なお、電解質温度37℃の場合、22℃の時と比べて定常状態における電流密度がほぼ4倍上昇していることが確認できた。この結果は、以下のStokes-Einstein relationship(式1)
【数1】

(ここで、D;電解質の拡散係数、kB;ボルツマン定数、T;絶対温度、η;電解質の粘度、a;イオン半径)
が示すように、電解質の温度上昇によって電解質の粘度が低下することで、電解質中のイオンの拡散係数が増加していることに主に起因するものと考察される。また、37℃では定常状態における曲線の触れ幅が大きいことが確認できたが、これは、低粘度溶液では電極反応が振動的に進行するためと考察される。
【0036】
図3下段に、定電位電解によって得られるチタニアナノチューブアレイの断面走査型電子顕微鏡(SEM)画像、並びに表面に対して斜め垂直方向から観察した先端部分のSEM画像および末端部分のSEM画像を示す。また図4に、定電位電解によって得られるチタニアナノチューブアレイの形成過程の模式図を示す。チタニアナノチューブアレイの形成過程の初期段階はチタン金属側(アノード側)で以下の反応から進行する(式2)。
【数2】

また、白金箔側(カソード側)では以下の反応が起こっている(式3)。
【数3】

【0037】
(式3)の反応によって、チタン金属上に水酸化物チタンとチタニア層が急激に形成される。
ナノチューブの細孔の起源は、チタン金属上に形成されるBarrier Layerと呼ばれる水酸化物チタンとチタニア層との複合層の表面に存在するクラックであることが言われている。この酸化物の形成が起こると同時に酸化物の溶解が以下の反応式に従って生じる(式4)。
【数4】

この場合、定電位条件で反応を引き起こすことから、以下の(式5)、
【数5】

より、チタニア層がエッチングされると電場が増大し、水の分解が早く起きる。その結果、(式3)よりチタニアがさらに形成される。定電位条件で反応していることから、電解質と酸化物界面および水酸化物と金属界面ともに一定の電位が存在するので、電場の向きは常に界面に対して垂直方向であり、その結果電解質と酸化物界面および水酸化物と金属界面は半球状を形成する。
【0038】
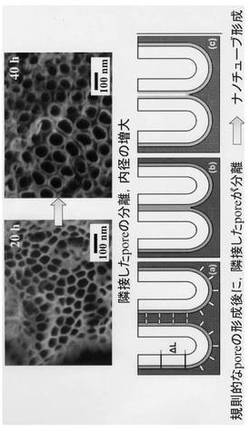
その後、チタニアの形成と溶解が同時に起こりながら、チューブの細孔が拡大し(図4(a)、図5(a))、隣接した二つのチューブが水酸化物の層同士で接触すると、拡大反応は停止し(図4(b)、図5(b))、チタニアを形成するために,水酸化物の層が分解される(図4(c)、図5(c))。つまり、隣接した二つのチューブが水酸化物の層同士で接触すると、チューブの内径は変化しない筈である。
【0039】
なお、電解時間についてみれば、一例では20時間の場合、隣接したチタニアナノチューブアレイが接合されているにも関わらず、20時間から40時間の間で穴径が増大している様子が観察された(図5上段参照)。
以上のことから、隣接した二つのチューブ間の水酸化物の層が分解されてからも、チューブ細孔の拡大反応が進行している。すなわちチューブの深さ方向だけでなく、横方向にもエッチング反応が進行することが推定される。これは、深さ方向にのみエッチング反応が進む、配向制御されたポーラスなアルミナの形成過程(図2参照)とは異なる形成過程を示している。
【0040】
[チタニアナノチューブの焼成について]
一例として、0.5wt%のフッ化アンモニウム(NH4F)を含んだエチレングリコールを電解質に用いて10V、20hで定電位電解を行った。得られたTi−TNTA試料を昇温速度2℃/minで250℃、2時間焼成(第1の焼成ステップ)し、一度冷却させた後、昇温速度2℃/minで500℃、2時間焼成(第2の焼成ステップ)した試料(二段階焼成)と、昇温速度2℃/minで500℃、2時間焼成した試料(一段階焼成)との構造評価を行った。
なお、第1の焼成ステップの焼成温度の範囲としては200℃<t1≦300℃(t1:第1の焼成温度)程度、第2の焼成ステップの焼成温度の範囲としては400℃<t2≦600℃(t2:第2の焼成温度)程度、好ましくは450℃≦t2≦550℃である。
【0041】
図6(a)および(b)に、一段階焼成と二段階焼成のチタニアナノチューブアレイの上から観察したSEM画像およびその拡大像を示す。図6(b)に示す二段階焼成の方が、図6(a)に示す一段階焼成に比べてチタニアナノチューブアレイ膜のクラッキングが少ない様子が観察された。この結果から、二段階焼成の方が色素増感太陽電池に応用するときに電子伝達性の向上が期待されることが明らかとなった。
また、チタニアナノチューブアレイ膜の表面をさらに拡大すると、チタニアナノチューブアレイの先端部分が破壊されている部分が存在するが、ナノチューブ自体の破壊は抑制されているように考察される。
【0042】
図7に、450℃で焼成前後のTi−TNTA試料のX線回折装置(XRD)測定結果を示す。また図8に、250℃、500℃、550℃、600℃の焼成によって得たTi−TNTA試料のXRD測定結果を示す。
図7のXRD測定結果から、電解直後のTi−TNTA試料はチタニアに関するピークを持たないことからアモルファスであることが分かった。ところが、450℃まで焼成を行うと、アナターゼ構造に特有なピークが得られたことから、アナターゼ結晶のチタニアが得られたことが明らかとなった。
なお、本明細書において「アナターゼ単結晶」或いは「アナターゼ結晶」とは、実質上アナターゼ単結晶と同一効果を発揮しており、同視し得るものまで包含するものとする。したがって例えば、極微量のルチルが含まれていても、実質上アナターゼ単結晶と同じ働きを持つものであれば、本明細書に言う「アナターゼ単結晶」或いは「アナターゼ結晶」に包含されるものとする。
【0043】
図9に、450℃まで焼成を行ったTi−TNTA試料にIPA中で5分間超音波照射を行い、チタニアナノチューブアレイを分散させたコロイド溶液をTEMグリッドに滴下して高分解能型電子顕微鏡(HRTEM)によって観察した結果を示す。この結果については下記実施例1においても言及する。
図9の結果から、ナノチューブの軸方向にアナターゼ結晶の(101)の格子像が確認でき、チタニアナノチューブアレイが高い結晶性をもつ単結晶構造であることが明らかとなった。
【0044】
[チタニアナノチューブアレイを用いた色素増感太陽電池の作成]
次に、上でその作成方法を説明した本発明のチタニアナノチューブアレイを備えたチタニア電極の作成方法、チタニア電極、並びにこのチタニア電極を適用した色素増感太陽電池の概要を説明する。
図10に、本発明の色素増感太陽電池の概略構造を示す。色素増感太陽電池セル100は、電解質2を挟んで互いに対向する白金電極1とチタニア電極10とからなっている。色素増感太陽電池セル100は、チタニア電極10側から光Lを受光し、光電変換作用によって外部に対しその発電電力を出力する。チタニア電極10の概略構造は、透明導電膜電極15と、透明導電膜電極15から白金電極1側に向かって実質的に垂直に伸びるチタニアナノチューブアレイ11とからなるものである。チタニア電極の10詳細については、図11に基づき説明する。
【0045】
図11に、本発明のチタニアナノチューブアレイを備えたチタニア電極構造において、チタニアナノチューブアレイをチタン金属と分離させる方法の一例を示す。
図11左側に示す通り、チタニアナノチューブアレイ11自体は、定電位電解装置50により金属チタン20上に作成されている。しかしながら、金属チタン20は光を通さないため、チタニア電極10側から光Lを受光させるためには、この金属チタン20を除去する必要がある。さらに、金属チタン20を除去したチタニアナノチューブアレイ11を、光Lの受光が可能で、かつ電極として機能し得る機械的に安定なものに接合し、チタニア電極として完成させる必要がある。
【0046】
本発明では、ITO膜13が表面に形成されたガラス14を透明導電膜電極15(ITO基板)とし、ITO膜13上にチタニア薄膜層(TiO2薄膜)12が形成(任意)されたITO基板15にチタニアナノチューブアレイ11が得られた金属チタン20を載置したのち、ITO基板15に向け臭素メタノール溶液を滴下することで金属チタン20を溶解除去している。
【0047】
このようにして得られた本発明のチタニア電極構造10は、図11右側に示す通り、必要に応じ表面にチタニア薄膜層(TiO2薄膜)12が形成されたITO基板15に、チタニアナノチューブアレイ11が、白金電極1側に向かって実質的に垂直に伸びる配列制御が維持された状態で接合されたものとなっている。
【0048】
以下、具体的なチタニア電極構造、並びにこのチタニア電極構造を適用した色素増感太陽電池の作成例については実施例を用いて順次説明する。
ここで、各実施例では、チタニアナノチューブアレイ11とチタニア薄膜層(TiO2薄膜)12との接合を強化するため、順に、図11下段に例示する通り、
i)TiO2微粒子を形成するための反応原液をチタニアナノチューブアレイとチタニア薄膜層の間に浸み込ませて接合する方法、すなわち、トリブロック共重合体F127ゲル反応原液を浸透させた後、重縮合反応によりチタニアナノチューブアレイ11とチタニア薄膜層12界面にF127ゲルを形成させて接合する方法(F127 liquid。第1の接合方法)、
ii)チタンのアルコキシドであるオルトチタン酸テトライソプロピル(Tetraisopropyl orthotitanate:TIPT)溶液を浸み込ませてチタニアナノチューブアレイ11とチタニア薄膜層12を接合する方法(第2の接合方法)、或いは、
iii)TiO2微粒子ゲルをチタニアナノチューブアレイ11とチタニア薄膜層12の間に浸み込ませて接合する方法、すなわち、既に形成済みのF127ゲルを浸透させて接合する方法(F127 gel。第3の接合方法)、
を用いている。
ここで、上記F127は、少なくともエチレンオキサイド/プロピレンオキサイド/エチレンオキサイドの骨格からなるトリブロック共重合体を含有したものの一例として列挙するものである。
【0049】
[F127ゲルによるTiO2微粒子の作製]
なお、下記の各実施例では、トリブロック共重合体F127 3.31gを29.801gの超純水で調製して10wt%のF127水溶液を調製した。この10wt%のF127水溶液に界面活性剤として臭化セチルトリメチルアンモニウム(Cetyltrimethylammonium bromide:CTAB)を0.606g加えてCTABが0.055Mになるように調製した。さらにこの溶液に、0.038M程度になるように塩酸を混合し、溶液が透明になるまで撹拌した。
【0050】
その後、TIPTとアセチルアセトンの0.4M、1.2M、2.4Mの等モル錯体溶液を加え、40℃で1日攪拌することによって淡黄色の透明な溶液を得た。この試料をトリブロック共重合体F127から合成した反応原液(F127原液)としている。
その後、80℃で重縮合反応させることによって溶液をゲル化させた。4日ほど80℃で放置した後、常温で保存した。この試料をトリブロック共重合体F127から合成したTiO2微粒子(F127ゲル。非特許文献4参照)としている。
【0051】
図12に0.4MのTIPT溶液を含んだF127ゲルから形成されるTiO2試料のXRD測定結果を示す。この測定結果より、F127ゲルから形成されるTiO2微粒子はアナターゼ結晶であることが明らかとなった。また、以下のシェラーの式を用いて、XRDの測定結果より(101)でのピークからナノ粒子の結晶子径を算出した(式6)。
【数6】

【0052】
図13(a)〜(c)に、0.4M、1.2M、2.4MのTIPT溶液を含んだF127ゲルから形成されるTiO2試料のHRTEM画像を示す。また下表1に、HRTEM観察から観察された0.4M、1.2M、2.4Mのチタニアナノ粒子の粒子径と結晶子径を示す。
【表1】

【0053】
図13(a)〜(c)から、0.4MのTIPTを含んだF127ゲルから形成されるTiO2試料は粒子径3〜5nmの球状粒子を有していることが明らかとなり、(式6)のシェラー式から得られた結晶子径とほぼ同じ値であった。さらに、得られた粒子はアナターゼ結晶の(101)の格子像が確認できたことから、F127ゲルから形成されるTiO2試料は高い結晶性をもつ単結晶構造であることが明らかとなった。1.2M、2.4MのTIPTを含んだF127ゲルから形成されるTiO2試料についても、図13(a)〜(c)から0.4Mの時と同様な(101)の格子像が確認でき、さらにHRTEM画像から得られる粒子径と(式6)のシェラー式から得られる結晶子径とほぼ同じ値であったことから、高い結晶性をもつ単結晶粒子が得られたことが明らかとなった。
【実施例1】
【0054】
[チタニアナノチューブアレイの作成]
本実施例では、0.5wt%のフッ化アンモニウムを含んだグリセリン溶液を電解質とし、作用電極にチタン金属(1cm×2cm、厚み0.2mm)を、対極に白金箔(1cm×2cm、厚み0.1mm)を、参照電極に塩化銀電極を用いて電気化学セルを構成し、10V〜40Vで定電位電解を行うことにより、チタン金属上にチタニアナノチューブアレイ(Ti−TNTA試料)を作製した。定電位電解装置は図1に示すものを使用した。得られた試料は、XRD、HRTEMおよびSEMを用いて構造評価を行った。
【0055】
[チタニアナノチューブアレイを用いた色素増感太陽電池の作成]
次に、本実施例における、チタニアナノチューブアレイを用いた色素増感太陽電池の作成要領につき、図10および図11、並びに図14〜図16を参照しながら説明する。
【0056】
本実施例では、上記Ti−TNTA試料を250℃で2時間焼成した後、さらに450℃で2時間焼成を行い、アナターゼ結晶構造を持つチタニアナノチューブアレイを得た。このチタニアナノチューブアレイをITO基板に接合するために、トリブロック共重合体F127より作製されるTiO2微粒子(F127ゲル)を用いた。なお、本実施例では、焼成には電気炉を使用した。以下同様である。
【0057】
より詳細に説明すると、準備段階としてまず、ITO基板にF127ゲルを塗布し、450℃で焼成してチタニア薄膜層を形成した。
【0058】
次に、図14に示す通り、250℃で2時間焼成した後の上記Ti−TNTA試料をエタノールに十分浸漬させ、F127ゲルを作製する反応原液(F127原液)をエタノールに混合し、40℃で1日浸漬後、80℃で重縮合反応を4日間進行させ、F127ゲルをチタニアナノチューブアレイのチューブ内、チューブの上部およびチューブの外壁に析出させて、450℃で2時間焼成を行った(S11,S12)。
【0059】
このTi−TNTA試料をITO基板上に載せ、臭素メタノール溶液を滴下することでチタン金属を溶解除去した(S13)。
チタニアナノチューブアレイとITO基板上のチタニア薄膜層との結合を強化するため、両者の間隙にF127原液を浸み込ませ、80℃で1時間反応させた後550℃で2時間焼成した(S14,S15)。この第1の接合方法による結合強化操作は2回行った。
【0060】
さらに、このITO基板上のチタニアナノチューブアレイを80mMのTiCl4水溶液に80℃で1.5時間浸漬後(S16)、550〜600℃で2時間焼成し、チタニア電極を作製した(S17)。
【0061】
その後、常法に従い、3×10−4MのN719ルテニウム色素溶液にチタニア電極を40℃で2日浸漬した。対極は白金電極を用い、ハイミラン(三井・デュポンポリケミカル)で両電極を接合した。また、白金電極の穴から電解質溶液を挿入して、色素増感太陽電池セルを完成させた。
【0062】
より具体的には、作製した色素増感チタニア電極と白金電極を接着させるために、横4mm× 縦9mmの穴をあけた熱可塑性接着シートである厚さ50μmのハイミランを色素増感チタニア電極の周りに重ならないように置き、ホットプレート(Model RCH−3、東京理科器械)上で、140℃程度で二つの電極を圧着した。次に、白金電極の片方の電解質注入口より、調製した電解質を注入した。この際、注入口を防ぐように滴を作り、真空を引くことで気泡を除去した。さらに、電解質が白金電極の界面にまで浸透するよう、電解質を注入後真空で数秒引き上げた。
【0063】
なお本実施例では、上記白金電極を、電解質の注入口が2箇所設けられた透明導電性ガラスであるITOガラス(2cm×2cm、シート抵抗2Ω/□、ジオマティク)にイオンコーター(IB3、Eiko)を用いて電流値5mAで5分間白金を蒸着させることで得ている。
【0064】
また本実施例では、上記電解質には、0.6M 1−ブチル−3−メチルイミダゾリウムヨージド(BMII)、0.03M I2、0.1M Guanidinium thiocyanate、0.5M 4-Tert-butylpyridine(TBP)を脱水アセトニトリルとn-Valeronitrileを85:15の体積比で構成される溶媒に溶解させたものを使用している。
【0065】
実験については、擬似太陽光でI−V測定を行ったほか、インピーダンス測定を実施した。
具体的には、I−V特性は、光源に100mW/cm2に調製したソーラーシュミレーター(YSS−E40、山下電装)を用いて擬似太陽光(AM 1.5 1sun)の条件でDSCセルに対して垂直に照射し、ポテンショスタット(R6423,ADVANTEST)を使い電圧を0.1V〜−0.88Vまでの順方向と−0.88V〜0.1Vまでの逆方向で積分時間を0.5V/min程度で走査させることで測定を行った。また、順方向と逆方向の測定値の平均値をそのDSCセルのI−V特性とした。
また、100mW/cm2の照射光の確認として財団法人電気安全環境研究所(JET)で校正された二次基準アモルファス太陽電池セル(43.4mA at AM1.5 100mW/cm2 25℃、適用規格JIS[8931-1995/IEC 60904-2])を用いて、測定前にソーラーシュミレーターの検定を行った。
【0066】
また、インピーダンス測定には,インピーダンスアナライザー(Solartron 1255B、ソーラートロン)を用い、交流電圧の振幅は10mVとして、1MHz〜0.01Hzの周波数で測定を行った。バイアス電圧はI−V測定で求めた開放電圧とした。
【0067】
[チタニアナノチューブアレイを用いたチタニア電極の評価]
図9に、450℃で2時間焼成を行ったチタニアナノチューブアレイのHRTEM画像を示す。XRD測定結果よりチタニアナノチューブアレイはアナターゼ結晶と同定でき、チタニアナノチューブアレイのチューブの軸方向にアナターゼ結晶の{101}面の格子像が、すべて同じ方向に揃ってまっすぐ伸びた単結晶であることが確認できる。したがって、このようなチタニアナノチューブアレイを太陽電池の電極に用いると、高い電子伝導性が期待されることが明らかとなった。
【0068】
また図14右欄に、焼成後のチタニアナノチューブアレイの内部、上部、外壁に、F127ゲルを用いてTiO2微粒子を析出させた場合のSEM画像、HRTEM画像を示す。図14(a)から、チタン金属に対して垂直にチタニアナノチューブアレイが立っている様子が観察できる。また、図14(d)に示すHRTEM画像から、F127ゲルから合成される3〜5nmのTiO2微粒子がチタニアナノチューブアレイの内部(白い矢印)に含まれている様子が観察できた。さらに、図14(b)に示すSEM画像から、チタニアナノチューブアレイの上部に析出している様子が観察できた。
【0069】
図14左欄に示す工程および図14右欄に示すHRTEM画像の結果から、Ti−TNTA試料をエタノールに十分浸漬させ、その後F127ゲルを作製する反応原液(F127原液)を混合し、40℃で1日浸漬させたことで、F127原液がチタニアナノチューブアレイ内部にまで浸透し、80℃の段階でチタニアナノチューブアレイ内部で粒子成長が起こったことが期待できる。
このように、図14右欄のSEM画像、HRTEM画像からは、F127ゲルから合成されるTiO2微粒子は、3〜5nmの高結晶性のアナターゼであり、このような微粒子がチタニアナノチューブアレイの内部、上部に析出している様子が観察できた。
【0070】
[実験結果]
図17右欄に、F127ゲル反応原液を浸透させた後、重縮合反応によりチタニアナノチューブアレイとチタニア薄膜層界面にF127ゲルを形成させて接合した場合(F127 liquid。第1の方法)と、既に形成済みのF127ゲルを浸透させて接合した場合(F127 gel。第3の接合方法)のI−V測定結果を示す。第3の接合方法については実施例3にて説明する。
I−V測定結果から、第1の接合方法であるF127 liquidでは3%以上の光電変換効率が得られた。一方、第3の接合方法であるF127 gelでは1.2%であった。
【実施例2】
【0071】
次に、上記第2の接合方法を用いた実施例2につき説明する。チタニアナノチューブアレイの作成要領は実施例1と同様である。
本実施例における、チタニアナノチューブアレイを用いた色素増感太陽電池の作成要領につき、図10および図11、並びに図15および図16を参照しながら説明すると、Ti−TNTA試料をITO基板上に載せ、臭素メタノール溶液を滴下することでチタン金属を溶解除去した(S13)後、チタニアナノチューブアレイとITO基板上のチタニア薄膜層との結合を強化するため、第1の接合方法に代え第2の接合方法が適用される。
具体的には、チタニアナノチューブアレイとITO基板上のチタニア薄膜層の間隙にTIPT溶液(水溶液或いはエタノール溶液)を浸み込ませ、80℃で1時間反応させた後550℃で2時間焼成される(S24,S15)。実施例2においても、上記結合強化操作は2回行われる。
この点を除き、実施例2に係る作成要領は実施例1と同様である。
【0072】
また、本実施例においては、チタニアナノチューブアレイとITO基板との接合に用いたTiO2微粒子について検討を行った。24時間40Vの定電位電解で作製したチタニアナノチューブアレイに、F127原液によって接合させた電極と、320mMのTIPTエタノール溶液によって接合させた電極を用いたセルを比較した。
【0073】
各電極試料の短絡電流Jsc、開放起電力Voc、フィルファクターFF、変換効率η、セルの全直列抵抗Rtotalおよび色素吸着量(Amount of Dye Adsorption)を図16下段の表に示す。図16下段の表から、F127原液の方が色素吸着量が多いことから短絡電流Jscが向上したと考えられる。これは、TIPTエタノール溶液より得られるTiO2微粒子よりも比表面積の大きなTiO2微粒子がF127原液から得られるため、色素吸着量が増大したものと考察される。
【0074】
また、F127原液の方がTIPTエタノール溶液よりもセルの全直列抵抗が小さく、FFの値も1.24倍大きくなっている。これは、TIPTエタノール溶液よりも、F127原液から得られるTiO2微粒子で接合する方が密着性の良いセルが得られることを示している。
【実施例3】
【0075】
次に、上記第3の接合方法を用いた実施例3につき説明する。チタニアナノチューブアレイの作成要領は実施例1と同様である。
本実施例における、チタニアナノチューブアレイを用いた色素増感太陽電池の作成要領につき、図10および図11、並びに図17左欄を参照しながら説明すると、まず、上記Ti−TNTA試料を250℃で2時間焼成した後(S31)、さらに450℃で2時間焼成を行い(S32)、アナターゼ結晶構造を持つチタニアナノチューブアレイを得た。また、ITO基板側の準備段階として、ITO基板にF127ゲルを塗布し、450℃で焼成してチタニア薄膜層を形成した。
【0076】
次に、Ti−TNTA試料をITO基板上に載せ、臭素メタノール溶液を滴下することでチタン金属を溶解除去した(S33)。
そして、チタニアナノチューブアレイとITO基板上のチタニア薄膜層との結合を強化するため、両者をF127ゲル中に十分浸漬させ、80℃で1時間放置、反応させた後550℃で2時間焼成した(S34、S35)。この第3の接合方法による結合強化操作は2回行った。
【0077】
さらに、このITO基板上のチタニアナノチューブアレイを80mMのTiCl4水溶液に80℃で1.5時間浸漬後(S36)、600℃で2時間焼成し(S37)、チタニア電極を作製した。
【0078】
この後は実施例1と同様で、常法に従い、3×10−4MのN719ルテニウム色素溶液にチタニア電極を40℃で2日浸漬した。対極は白金電極を用い、ハイミランで両電極を接合した。また、白金電極の穴から電解質溶液を挿入して、セルを完成させた。
【0079】
図17右欄に、上記第1の方法を用いて作成されたチタニア電極が適用された色素増感太陽電池と、第3の方法を用いて作成されたチタニア電極が適用された色素増感太陽電池のI−V測定結果を示す。
チタニアナノチューブアレイとITO基板上のチタニア薄膜層との接合に関して上記I−V測定結果から類推するに、TiO2ゲルはチタニアナノチューブアレイとITO基板上のチタニア薄膜層の間隙に浸透しにくいため、第3の接合方法では両者の接合が不十分となっている。一方、TiO2微粒子を形成する反応原液は奥深く浸透可能であり、反応によりTiO2微粒子を発生するので、第1の接合方法では両者の接合が良好に行われる。接合の良否が光電変換効率の差にも表れたものと考察される。
上記の結果から見ても、チタニアナノチューブアレイとチタニア薄膜層との接合方法の今後の改良次第で、更なる効率向上が期待されることが明らかとなった。
【0080】
以上、本発明により、電解質の温度や種類を変更し、電解質の粘度を制御することで、チタニアナノチューブアレイの形態を制御できることが明らかとなった。
また本発明により、一例として昇温速度2℃/minで250℃、2時間焼成し、一度冷却させた後、昇温速度2℃/minで500℃、2時間焼成することで、チタニアナノチューブアレイ膜のクラッキングを抑えられることが明らかとなった。
さらに本発明により、一例として450℃で焼成を行うと、チタニアナノチューブアレイはアモルファスからアナターゼ結晶に相転移し、ナノチューブの軸方向にアナターゼ結晶の(101)の格子像が観察される程、結晶性の高い単結晶構造を有することが明らかとなった。
さらに、本発明により得られたチタニアナノチューブアレイ電極においては、F127ゲルから合成される3〜5nmのTiO2微粒子がチタニアナノチューブアレイの内部に含まれている様子がHRTEM画像から観察された。
【0081】
その他、本発明のチタニアナノチューブアレイを利用することで、色素増感太陽電池におけるセル性能が改善されることが明らかとなった。また、チューブの内部にTiO2微粒子を十分に析出させる工夫を重ねることで、更なる高効率化を図ることが可能であることも明らかとなった。
【0082】
[変形例]
以上、一実施例を用いて本発明を詳細に説明したが、本発明は上記実施例記載の構成に限定されず、種々の変形実施をすることが可能である。
例えば、本実施例で説明したチタニアナノチューブアレイとチタニア薄膜層との接合を強化するための第1の接合方法〜第3の接合方法はあくまで一例に過ぎず、必要に応じ他の方法によってチタニアナノチューブアレイとチタニア薄膜層との接合を行っても構わない。
【0083】
また、本実施例ではチタン金属を溶解除去するのに臭素メタノール溶液を用いたが、これに限定されず、チタン金属を溶解除去可能な別の溶液その他を用いても構わない。
定電位電解装置50で用いた電解質52或いは本実施例の色素増感太陽電池セル100にて用いた電解質2についても、上記組成に何ら限定されず、同様の効果を発揮し得る他の構成を適宜採用して構わない。
定電位電解装置50についても、参照電極56は場合によっては省略して構わない。
【0084】
また、本実施例では、チタニア薄膜層を形成しておいたITO基板上にチタニアナノチューブアレイを接合する構成としたが、これに限定されず、チタン金属同様、チタニア薄膜層についても除去する構成としても構わない。
【0085】
以上に説明した通り、本発明により作成された単結晶のチタニアナノチューブアレイは、格段に高い電子伝導性が期待できる。したがって本発明は、理想的な幾何学形状を有し、高い電子伝導性を併せ持つチタニアナノチューブアレイの作成方法、それによって得られるチタニア電極構造、並びにこのチタニア電極構造を適用した色素増感太陽電池を提供することができる新規かつ有用なるものであることが明らかである。
【符号の説明】
【0086】
L 光
1 白金電極
2 電解質
10 チタニア電極
11 チタニアナノチューブアレイ
12 TiO2薄膜
13 ITO膜
14 ガラス
15 透明導電膜電極
20 Ti
50 定電位電解装置
51 電解槽
52 電解質
53 ポテンショスタット
54 作用電極
55 対極
56 参照電極
57 温度計
58 窒素ガス
59 窒素タンク
100 色素増感太陽電池セル
【技術分野】
【0001】
本発明は、チタニアナノチューブアレイおよびチタニア電極の新規な作成方法、チタニア電極、並びにこのチタニア電極を適用した色素増感太陽電池に関する。
【背景技術】
【0002】
近年のグローバル化に伴い、発展途上国が急速に経済成長したことで、これまで先進国の経済成長によって消費されてきたエネルギー量をはるかに上回るエネルギー消費が起こっている。この膨大なエネルギー消費の増加を賄うために、石油エネルギー、化石燃料を中心としたエネルギー供給以外の、再生可能な環境負荷の少ない新規エネルギー開発が必須となっている。
【0003】
再生可能な新規エネルギー源として、最近注目されているのが太陽電池、風力発電、バイオ燃料であるが、最も有望な新規エネルギー源は太陽電池であると考えられている。
現在実用化されている太陽電池はシリコン太陽電池である。高い変換効率を獲得するためにはやはり、高純度単結晶シリコンを大量に使用しなければならないが、これには材料コストおよび精製に要する製造コストが高いといった問題点がある。
以上の点から、現在のシリコン太陽電池では、未だに化石燃料による発電コストに追いついていないのが現状といえる。
【0004】
この解決案として、有機系太陽電池である次世代型太陽電池の色素増感太陽電池(DSSC; Dye Sensitized Solar Cells)が挙げられる。
図18に色素増感太陽電池の基本セル構造を示す。増感色素には主として、太陽光の可視光領域まで吸収できるルテニウム(Ru)錯体が用いられ、光電極として導電性ガラス上にナノサイズの多孔質チタニア薄膜が形成されたものが使われている。その対極は、導電性ガラスに触媒として白金をコートしたもの、電解質には、酸化還元対を含む有機溶媒として、I−/I3−系が用いられる。
【0005】
色素増感太陽電池は従来の高純度単結晶シリコンよりも資源的な制約が少ない材料で構成されており、また製造プロセスが安価で低コストが期待されている上に形状や色を自由に変えられるといった特徴をもつことから、非常に魅力的な太陽電池として注目を集めている。
ところが、実用化に向けていくつかの課題を克服しなければならない。その一つとして、シリコン太陽電池と比較して光電変換効率が低い点が挙げられる。
【0006】
ここで、色素増感太陽電池の発電原理を含めて、変換効率の低い原因について説明する。色素増感太陽電池の発電原理は、従来のpn接合型太陽電池とは異なり、光合成の発電原理に類似する。
まず、図18に示す通り、太陽光を吸収した色素は光エネルギーによって励起された後、電子をチタニアへ与えて酸化状態になる。チタニアへ移動した電子は、チタニア電極の導電性ガラスにまで到達し、外部回路を通じて対極に移動する。一方、酸化状態になった色素は、電解質(I−)から電子を受け取って元の状態へと戻り、電解質は酸化状態となる(3I− →I3−+2e− )。酸化状態の電解質(I3−)は対極から電子を受け取り、還元状態に戻る。この一連のサイクルによって電池として機能する。
色素増感太陽電池の光電変換効率が低いのは、エネルギーロスが多いためである。例えば、可視光以上の波長領域をカバーできていない点、色素からチタニアへの注入効率、高エネルギー光からの高エネルギー電子を利用できていない点、チタニア間を移動する電子と電解質中のI3−イオンとの再結合反応による逆電子移動ロス、注入時および色素の再生時のエネルギー差によるロスその他が挙げられる。これらの問題点に対していくつか検討が行われてきたが、解決されていない問題もまだ数多く存在する。
【先行技術文献】
【非特許文献】
【0007】
【非特許文献1】Craig A. Grimes, et al., Nanotechnology, 17, 1446-1448 (2006)
【非特許文献2】P. Schmuki, et al., Nano Letters, 6, 215-218 (2006)
【非特許文献3】Craig A. Grimes, et al., Adv. Funct. Mater., 15, 1291-1296 (2005)
【非特許文献4】J. Jiu, et al., J.Electrocheml Soc, 151, A1653-A1658 (2004)
【発明の開示】
【発明が解決しようとする課題】
【0008】
ところで、図18に基本構造を示す色素増感太陽電池のチタニア電極に、結晶性の高い粒界の無いチタニア材料を利用すれば、発電効率の向上が見込まれるとされている。つまり、色素増感太陽電池の高効率化のためには、1次元形状の高結晶性チタニアナノ材料による高い電子伝導性に加え、規則配列を持ったチタニア電極構造の構築が求められている。
これに応え得る材料として、チタン金属薄片を定電位(定電圧)電解することで作製されるチタニアナノチューブアレイ(TNTA)がある。非特許文献1には、規則配列構造をもったチタニアナノチューブアレイが定電位電解法によってチタン金属の上に形成されることが開示されている。
【0009】
ここで、上記チタニアナノチューブアレイに関しては、定電位電解による作成直後はアモルファスであるナノチューブアレイを焼成することで結晶化を行い得るところ、従来法の下では結晶子径が20nm程度の多結晶となり、高い電子伝導性が望めないという問題点があった。
【0010】
さらに、上記の通りチタニアナノチューブアレイは定電位電解法によりチタン金属の上に形成されるところ、チタン金属は光を通さない性質があることから、チタニアナノチューブアレイを色素増感太陽電池に応用するには工夫が必要であった。
この問題については、これまでに種々創案がなされている。図19および図20にその一例を示す。
【0011】
図19に示す例は、チタニアナノチューブアレイを色素増感太陽電池に応用する手段として、白金電極の白金を薄く蒸着して透明性を持たせ、白金電極側から光を入射する手法を用いた例である。
しかしながら、この手法では白金電極の透明性の問題のほか、光を最も良く吸収して電子注入が最大となる位置が電子収集電極から最も遠い位置となると言う構造上の問題があり、高効率が望めない欠点があった。
【0012】
次に、図20に示す例は、透明導電膜或いは透明導電性ガラス(ITO基板)上にチタン金属を約500nm蒸着し、これを陽極酸化することで、透明導電膜に長さ約360nmのチタニアナノチューブアレイを作製したものである(非特許文献2参照)。非特許文献2では、チタニア層の厚みは通常の約1/30にも拘わらず、光電変換効率2.9%を達成していることから、規則配列を持った構造が理想的なチタニア電極構造であると考えられる。
さらに、図20上段に示すように、非特許文献3では、ITO基板上にチタンを蒸着後、定電位電解を実行してチタニアナノチューブアレイを作製したのち、焼成(450℃、3時間)を行うことによって透明導電性ガラス全体の透明度を上昇させる例が開示されている。
ところが、これら非特許文献2および3に開示された手法では経済的に大きな難点があり、実用的ではない。
【0013】
このように、チタン箔の陽極酸化によって得られるチタニアナノチューブアレイを色素増感太陽電池に応用して高効率化を実現した製品を実用化するには、上述したチタン蒸着法以外でチタニア電極側から太陽光を照射することが可能なチタニア電極を作製する方法を見出す必要があった。すなわち、チタニア電極構造を適用した色素増感太陽電池の更なる効率向上には、経済的にも十分リーズナブルな実用的手法でチタニアナノチューブアレイをチタン金属と分離させ、配列制御が維持された状態でITO基板に接合する手法を提供する必要があった。
【0014】
したがって本発明は、上記問題点を解決し、色素増感太陽電池のチタニア電極構造への適用を前提に、単結晶チタニアナノチューブアレイの作製を可能とする焼成法、並びにそれによって得られたチタニア電極構造およびこれを適用した色素増感太陽電池を提供することを課題とする。
【0015】
また本発明は、色素増感太陽電池のチタニア電極構造への適用を前提に、経済的にも十分リーズナブルな実用的手法でチタニアナノチューブアレイをチタン金属と分離させ、配列制御が維持された状態でITO基板に接合する手法、並びにそれによって得られたチタニア電極構造およびこれを適用した色素増感太陽電池を提供することを課題とする。
【課題を解決するための手段】
【0016】
上記課題を解決すべく種々検討を行った結果、本願発明者は、
i)電解後のアモルファス状態のチタニアナノチューブアレイをまず200〜300℃の低温で漸次昇温、焼成、降温し、整然と並んだチタニアナノチューブアレイの形状を固定した後、400〜650℃の高温で漸次昇温、焼成、降温することにより、アナターゼの{101}面の格子像がチューブの軸方向に走る単結晶チタニアナノチューブアレイを得た後、得られたチタニアナノチューブアレイ膜をTiO2の微粒子膜を塗布したITO基板上に接合する方法によってチタニア電極を作製するものとし、さらに、得られたチタニア電極を色素増感太陽電池に適用すること、また、
ii)チタン金属を溶解除去することをアプローチとしてチタン金属とチタニアナノチューブアレイを分離させ、配列状態を維持したままチタニアナノチューブアレイをITO基板上に接着する方法すなわち、定電位電解法によりチタン金属の上に形成されたチタニアナノチューブアレイについて、チタン金属を適宜溶解除去後、得られたチタニアナノチューブアレイ膜を、TiO2の微粒子膜が形成された透明導電性ガラス上に接合する方法によってチタニア電極を作製するものとし、さらに、得られたチタニア電極を色素増感太陽電池に適用すること、
で上記課題を解決可能なことを見い出し、本発明を完成させた。
【0017】
上記課題を解決可能な本発明のチタニアナノチューブアレイの作成方法は、(1)チタニアナノチューブアレイの作成方法であって、
定電位電解法により、作用電極とされた箔状または板状のチタンを電解し、前記チタン上にチタニアナノチューブアレイを作成するステップと、
前記電解後、アモルファス状態の前記チタニアナノチューブアレイを漸次200℃<t1≦300℃(t1:第1の焼成温度)まで昇温して焼成後、漸次室温まで降温し、前記チタニアナノチューブアレイの整列形状を固定する第1の焼成ステップと、
前記第1の焼成ステップを経た後の前記チタニアナノチューブアレイを漸次400℃<t2≦600℃(t2:第2の焼成温度)まで昇温して焼成後、漸次室温まで降温することにより、アナターゼの{101}面の格子像がチューブの軸方向に走る単結晶チタニアナノチューブアレイを得る第2の焼成ステップと、
からなることを特徴とするものである。
【0018】
又上記課題を解決可能な本発明のチタニア電極の作成方法は、(2)チタニア電極の作成方法であって、
本願請求項1に記載の方法で前記チタニアナノチューブアレイを作成した前記チタンをITO基板上に載置するステップと、
チタン溶解手段により前記ITO基板上の前記チタンを溶解除去するステップと、
前記チタニアナノチューブアレイを前記ITO基板に接合するステップと、
からなることを特徴とするものである。
【0019】
また、本願請求項3に記載のチタニア電極の作成方法は、(3)本願請求項2に記載のチタニア電極の作成方法であって、
前記チタン溶解手段が前記チタン上へ臭素メタノール溶液を滴下することからなることを特徴とするものである。
【0020】
また、本願請求項4に記載のチタニア電極の作成方法は、(4)本願請求項2または3に記載のチタニア電極の作成方法であって、
前記ITO基板の表面にはチタニア薄膜層が形成されており、前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合することを特徴とするものである。
【0021】
また、本願請求項5に記載のチタニア電極の作成方法は、(5)本願請求項4に記載のチタニア電極の作成方法であって、
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、TiO2微粒子を形成するための反応原液を前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とするものである。
【0022】
また、本願請求項6に記載のチタニア電極の作成方法は、(6)本願請求項5に記載のチタニア電極の作成方法であって、
前記反応原液が少なくともエチレンオキサイド/プロピレンオキサイド/エチレンオキサイドの骨格からなるトリブロック共重合体を含有したものからなることを特徴とするものである。
【0023】
また、本願請求項7に記載のチタニア電極の作成方法は、(7)本願請求項4に記載のチタニア電極の作成方法であって、
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、オルトチタン酸テトライソプロピル溶液を前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とするものである。
【0024】
また、本願請求項8に記載のチタニア電極の作成方法は、(8)本願請求項4に記載のチタニア電極の作成方法であって、
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、TiO2微粒子ゲルを前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とするものである。
【0025】
又上記課題を解決可能な本発明のチタニア電極は、(9)色素増感太陽電池に適用され、電解質を挟んで対極に対向配置されて使用されるチタニア電極であって、本願請求項2〜8のいずれか1項に記載の方法で作成されたものからなることを特徴とする
ものである。
【0026】
又上記課題を解決可能な本発明の色素増感太陽電池は、(10)電解質を挟んで互いに対向するチタニア電極と対極とからなる色素増感太陽電池であって、
前記チタニア電極が本願請求項9に記載のものからなっていることを特徴とするものである。
【0027】
また、本願請求項11に記載の色素増感太陽電池は、(11)本願請求項10に記載の色素増感太陽電池であって、
前記対極が、ITOガラスに白金が蒸着された白金電極からなることを特徴とするものである。
【0028】
[各試薬について]
本明細書で挙げた試薬の内、主要なものの詳細は次の通りである。
・グリセリン HO(CH2)CHOH(CH2)OH = 92.09 試薬特級(和光純薬工業社)、室温保存
・フッ化アンモニウム NH4F = 37.04 試薬特級(和光純薬工業社)、室温保存、吸湿性
・メタノール CH3OH = 32.04 試薬特級(和光純薬工業社)、遮光保存
・超純水: 18MΩ以上の抵抗値を示すElix(ミリポア社)を用いて精製し、更にメンブランフィルター(ADVANTEC、0.1μm、90mm)で減圧濾過した濾過済み超純水を使用。
・トリブロック共重合体(tri-block copolymer)F127
HO-(CH2 CH2O)106-(CH2 C(CH)3HO)70-(CH2 CH2O)106H 試薬(BASF)、遮光保存
【発明の効果】
【0029】
本発明により作成された単結晶のチタニアナノチューブアレイは、格段に高い電子伝導性が期待されることが明らかとなった。したがって本発明によれば、理想的な幾何学形状を有し、高い電子伝導性を併せ持つチタニア電極の作製が可能となり、これを色素増感太陽電池に適用することにより、色素増感太陽電池の効率向上を図ることができる。
【図面の簡単な説明】
【0030】
【図1】定電位電解装置の一例を示す図である。
【図2】定電位電解法により金属アルミニウムの陽極酸化を行うことを示す模式図である。
【図3】定電位電解によって得られるチタニアナノチューブアレイのSEM画像である。
【図4】定電位電解法によりチタン金属上にチタニアナノチューブアレイを形成する一例を示す図である。
【図5】定電位電解法によりチタン金属上にチタニアナノチューブアレイを形成する一例を示す図である。
【図6】焼成後に得られたチタニアナノチューブアレイの評価結果を示すSEM画像である。
【図7】焼成前後のTi−TNTA試料のXRD測定結果を示す図である。
【図8】焼成温度を変えてTi−TNTA試料を作成した場合のXRD測定結果を示す図である。
【図9】焼成後に得られたチタニアナノチューブアレイのHRTEM画像である。
【図10】本発明の色素増感太陽電池の概略構造を示す図である。
【図11】本発明による、チタニアナノチューブアレイをチタン金属と分離させる方法の一例を示す図である。
【図12】TIPT溶液を含んだF127ゲルから形成されるTiO2試料のXRD測定結果を示す図である。
【図13】TIPT溶液を含んだF127ゲルから形成されるTiO2試料のHRTEM画像である。
【図14】チタニアナノチューブアレイに、F127ゲルを用いてTiO2微粒子を析出させた場合のSEM画像およびHRTEM画像である。
【図15】実施例1および2につき説明する図である。
【図16】実施例1および2につき説明する図である。
【図17】実施例3につき説明する図である。
【図18】色素増感太陽電池の基本構造を示す図である。
【図19】従来例に付き説明する図である。
【図20】従来例に付き説明する図である。
【発明を実施するための形態】
【0031】
以下では、添付図面に基づき、本発明のチタニアナノチューブアレイおよびチタニア電極の作成方法、チタニア電極、並びにこのチタニア電極を適用した色素増感太陽電池の概要を説明する。
【0032】
[定電位電解法によるチタニアナノチューブの作成]
まずはじめに、本発明のチタニアナノチューブアレイの作成方法につき説明する。
図1に、本発明のチタニアナノチューブアレイを作成するために用いた定電位電解装置の一例を示す。
定電位電解法自体は種々の分野で用いられており、図2に示す通り、金属アルミニウムの陽極酸化の研究でも定電位電解法は用いられている。一例として図2左欄に、アルミニウムに規則的な配列パターンからなる多孔質層が形成される様子を、また図2右欄の(a)および(b)に、規則的な配列パターンが形成された多孔質構造からなるアルミナを上方から観た図および断面図を示す。
【0033】
本発明では、チタン金属の定電位電解によってチタニアナノチューブアレイが作成される知見に基づき種々検討の結果、1次元の高い電子伝導性に加えて、理想的なチタニア電極構造を構築可能なことを見い出した。以下、順を追って説明する。
【0034】
図1に示す定電位電解装置50は、電解槽51と、電解槽51内に満たされたグリセリン溶液からなる電解質52と、電解槽51の外に設けられたポテンショスタット53と、一端側がポテンショスタット53にそれぞれ接続される一方、他端側がそれぞれ電解槽51内の電解質52中に差し込まれた、チタン金属(金属板または金属箔)からなる作用電極54、白金箔からなる対極55および塩化銀からなる参照電極56と、電解質52の温度を測定する温度計57と、電解槽51の外部より電解質52中に窒素ガス58を供給する窒素タンク59と、から構成されている。この構成によって電気化学セルを構成し、10V〜40Vの定電位にて定電位電解を行うことにより、チタン金属上にチタニアナノチューブアレイ(Ti−TNTA試料)を作成することができる。なお、電解時間は15〜50時間程度であれば良く、好ましくは20〜40時間である。電解質温度は15〜45℃であれば良く、好ましくは20〜40℃であれば良い。
定電位電解を行っている期間中、電解質温度および電解電位は一定に保たれることが好ましい。
【0035】
図3上段に、上の条件下でのチタンのアノード酸化による過渡電流を示す。反応の初期段階で急激に電流密度は減少し、その後1時間以内に定常状態に達することが明らかとなった。
なお、電解質温度37℃の場合、22℃の時と比べて定常状態における電流密度がほぼ4倍上昇していることが確認できた。この結果は、以下のStokes-Einstein relationship(式1)
【数1】

(ここで、D;電解質の拡散係数、kB;ボルツマン定数、T;絶対温度、η;電解質の粘度、a;イオン半径)
が示すように、電解質の温度上昇によって電解質の粘度が低下することで、電解質中のイオンの拡散係数が増加していることに主に起因するものと考察される。また、37℃では定常状態における曲線の触れ幅が大きいことが確認できたが、これは、低粘度溶液では電極反応が振動的に進行するためと考察される。
【0036】
図3下段に、定電位電解によって得られるチタニアナノチューブアレイの断面走査型電子顕微鏡(SEM)画像、並びに表面に対して斜め垂直方向から観察した先端部分のSEM画像および末端部分のSEM画像を示す。また図4に、定電位電解によって得られるチタニアナノチューブアレイの形成過程の模式図を示す。チタニアナノチューブアレイの形成過程の初期段階はチタン金属側(アノード側)で以下の反応から進行する(式2)。
【数2】

また、白金箔側(カソード側)では以下の反応が起こっている(式3)。
【数3】

【0037】
(式3)の反応によって、チタン金属上に水酸化物チタンとチタニア層が急激に形成される。
ナノチューブの細孔の起源は、チタン金属上に形成されるBarrier Layerと呼ばれる水酸化物チタンとチタニア層との複合層の表面に存在するクラックであることが言われている。この酸化物の形成が起こると同時に酸化物の溶解が以下の反応式に従って生じる(式4)。
【数4】

この場合、定電位条件で反応を引き起こすことから、以下の(式5)、
【数5】

より、チタニア層がエッチングされると電場が増大し、水の分解が早く起きる。その結果、(式3)よりチタニアがさらに形成される。定電位条件で反応していることから、電解質と酸化物界面および水酸化物と金属界面ともに一定の電位が存在するので、電場の向きは常に界面に対して垂直方向であり、その結果電解質と酸化物界面および水酸化物と金属界面は半球状を形成する。
【0038】
その後、チタニアの形成と溶解が同時に起こりながら、チューブの細孔が拡大し(図4(a)、図5(a))、隣接した二つのチューブが水酸化物の層同士で接触すると、拡大反応は停止し(図4(b)、図5(b))、チタニアを形成するために,水酸化物の層が分解される(図4(c)、図5(c))。つまり、隣接した二つのチューブが水酸化物の層同士で接触すると、チューブの内径は変化しない筈である。
【0039】
なお、電解時間についてみれば、一例では20時間の場合、隣接したチタニアナノチューブアレイが接合されているにも関わらず、20時間から40時間の間で穴径が増大している様子が観察された(図5上段参照)。
以上のことから、隣接した二つのチューブ間の水酸化物の層が分解されてからも、チューブ細孔の拡大反応が進行している。すなわちチューブの深さ方向だけでなく、横方向にもエッチング反応が進行することが推定される。これは、深さ方向にのみエッチング反応が進む、配向制御されたポーラスなアルミナの形成過程(図2参照)とは異なる形成過程を示している。
【0040】
[チタニアナノチューブの焼成について]
一例として、0.5wt%のフッ化アンモニウム(NH4F)を含んだエチレングリコールを電解質に用いて10V、20hで定電位電解を行った。得られたTi−TNTA試料を昇温速度2℃/minで250℃、2時間焼成(第1の焼成ステップ)し、一度冷却させた後、昇温速度2℃/minで500℃、2時間焼成(第2の焼成ステップ)した試料(二段階焼成)と、昇温速度2℃/minで500℃、2時間焼成した試料(一段階焼成)との構造評価を行った。
なお、第1の焼成ステップの焼成温度の範囲としては200℃<t1≦300℃(t1:第1の焼成温度)程度、第2の焼成ステップの焼成温度の範囲としては400℃<t2≦600℃(t2:第2の焼成温度)程度、好ましくは450℃≦t2≦550℃である。
【0041】
図6(a)および(b)に、一段階焼成と二段階焼成のチタニアナノチューブアレイの上から観察したSEM画像およびその拡大像を示す。図6(b)に示す二段階焼成の方が、図6(a)に示す一段階焼成に比べてチタニアナノチューブアレイ膜のクラッキングが少ない様子が観察された。この結果から、二段階焼成の方が色素増感太陽電池に応用するときに電子伝達性の向上が期待されることが明らかとなった。
また、チタニアナノチューブアレイ膜の表面をさらに拡大すると、チタニアナノチューブアレイの先端部分が破壊されている部分が存在するが、ナノチューブ自体の破壊は抑制されているように考察される。
【0042】
図7に、450℃で焼成前後のTi−TNTA試料のX線回折装置(XRD)測定結果を示す。また図8に、250℃、500℃、550℃、600℃の焼成によって得たTi−TNTA試料のXRD測定結果を示す。
図7のXRD測定結果から、電解直後のTi−TNTA試料はチタニアに関するピークを持たないことからアモルファスであることが分かった。ところが、450℃まで焼成を行うと、アナターゼ構造に特有なピークが得られたことから、アナターゼ結晶のチタニアが得られたことが明らかとなった。
なお、本明細書において「アナターゼ単結晶」或いは「アナターゼ結晶」とは、実質上アナターゼ単結晶と同一効果を発揮しており、同視し得るものまで包含するものとする。したがって例えば、極微量のルチルが含まれていても、実質上アナターゼ単結晶と同じ働きを持つものであれば、本明細書に言う「アナターゼ単結晶」或いは「アナターゼ結晶」に包含されるものとする。
【0043】
図9に、450℃まで焼成を行ったTi−TNTA試料にIPA中で5分間超音波照射を行い、チタニアナノチューブアレイを分散させたコロイド溶液をTEMグリッドに滴下して高分解能型電子顕微鏡(HRTEM)によって観察した結果を示す。この結果については下記実施例1においても言及する。
図9の結果から、ナノチューブの軸方向にアナターゼ結晶の(101)の格子像が確認でき、チタニアナノチューブアレイが高い結晶性をもつ単結晶構造であることが明らかとなった。
【0044】
[チタニアナノチューブアレイを用いた色素増感太陽電池の作成]
次に、上でその作成方法を説明した本発明のチタニアナノチューブアレイを備えたチタニア電極の作成方法、チタニア電極、並びにこのチタニア電極を適用した色素増感太陽電池の概要を説明する。
図10に、本発明の色素増感太陽電池の概略構造を示す。色素増感太陽電池セル100は、電解質2を挟んで互いに対向する白金電極1とチタニア電極10とからなっている。色素増感太陽電池セル100は、チタニア電極10側から光Lを受光し、光電変換作用によって外部に対しその発電電力を出力する。チタニア電極10の概略構造は、透明導電膜電極15と、透明導電膜電極15から白金電極1側に向かって実質的に垂直に伸びるチタニアナノチューブアレイ11とからなるものである。チタニア電極の10詳細については、図11に基づき説明する。
【0045】
図11に、本発明のチタニアナノチューブアレイを備えたチタニア電極構造において、チタニアナノチューブアレイをチタン金属と分離させる方法の一例を示す。
図11左側に示す通り、チタニアナノチューブアレイ11自体は、定電位電解装置50により金属チタン20上に作成されている。しかしながら、金属チタン20は光を通さないため、チタニア電極10側から光Lを受光させるためには、この金属チタン20を除去する必要がある。さらに、金属チタン20を除去したチタニアナノチューブアレイ11を、光Lの受光が可能で、かつ電極として機能し得る機械的に安定なものに接合し、チタニア電極として完成させる必要がある。
【0046】
本発明では、ITO膜13が表面に形成されたガラス14を透明導電膜電極15(ITO基板)とし、ITO膜13上にチタニア薄膜層(TiO2薄膜)12が形成(任意)されたITO基板15にチタニアナノチューブアレイ11が得られた金属チタン20を載置したのち、ITO基板15に向け臭素メタノール溶液を滴下することで金属チタン20を溶解除去している。
【0047】
このようにして得られた本発明のチタニア電極構造10は、図11右側に示す通り、必要に応じ表面にチタニア薄膜層(TiO2薄膜)12が形成されたITO基板15に、チタニアナノチューブアレイ11が、白金電極1側に向かって実質的に垂直に伸びる配列制御が維持された状態で接合されたものとなっている。
【0048】
以下、具体的なチタニア電極構造、並びにこのチタニア電極構造を適用した色素増感太陽電池の作成例については実施例を用いて順次説明する。
ここで、各実施例では、チタニアナノチューブアレイ11とチタニア薄膜層(TiO2薄膜)12との接合を強化するため、順に、図11下段に例示する通り、
i)TiO2微粒子を形成するための反応原液をチタニアナノチューブアレイとチタニア薄膜層の間に浸み込ませて接合する方法、すなわち、トリブロック共重合体F127ゲル反応原液を浸透させた後、重縮合反応によりチタニアナノチューブアレイ11とチタニア薄膜層12界面にF127ゲルを形成させて接合する方法(F127 liquid。第1の接合方法)、
ii)チタンのアルコキシドであるオルトチタン酸テトライソプロピル(Tetraisopropyl orthotitanate:TIPT)溶液を浸み込ませてチタニアナノチューブアレイ11とチタニア薄膜層12を接合する方法(第2の接合方法)、或いは、
iii)TiO2微粒子ゲルをチタニアナノチューブアレイ11とチタニア薄膜層12の間に浸み込ませて接合する方法、すなわち、既に形成済みのF127ゲルを浸透させて接合する方法(F127 gel。第3の接合方法)、
を用いている。
ここで、上記F127は、少なくともエチレンオキサイド/プロピレンオキサイド/エチレンオキサイドの骨格からなるトリブロック共重合体を含有したものの一例として列挙するものである。
【0049】
[F127ゲルによるTiO2微粒子の作製]
なお、下記の各実施例では、トリブロック共重合体F127 3.31gを29.801gの超純水で調製して10wt%のF127水溶液を調製した。この10wt%のF127水溶液に界面活性剤として臭化セチルトリメチルアンモニウム(Cetyltrimethylammonium bromide:CTAB)を0.606g加えてCTABが0.055Mになるように調製した。さらにこの溶液に、0.038M程度になるように塩酸を混合し、溶液が透明になるまで撹拌した。
【0050】
その後、TIPTとアセチルアセトンの0.4M、1.2M、2.4Mの等モル錯体溶液を加え、40℃で1日攪拌することによって淡黄色の透明な溶液を得た。この試料をトリブロック共重合体F127から合成した反応原液(F127原液)としている。
その後、80℃で重縮合反応させることによって溶液をゲル化させた。4日ほど80℃で放置した後、常温で保存した。この試料をトリブロック共重合体F127から合成したTiO2微粒子(F127ゲル。非特許文献4参照)としている。
【0051】
図12に0.4MのTIPT溶液を含んだF127ゲルから形成されるTiO2試料のXRD測定結果を示す。この測定結果より、F127ゲルから形成されるTiO2微粒子はアナターゼ結晶であることが明らかとなった。また、以下のシェラーの式を用いて、XRDの測定結果より(101)でのピークからナノ粒子の結晶子径を算出した(式6)。
【数6】

【0052】
図13(a)〜(c)に、0.4M、1.2M、2.4MのTIPT溶液を含んだF127ゲルから形成されるTiO2試料のHRTEM画像を示す。また下表1に、HRTEM観察から観察された0.4M、1.2M、2.4Mのチタニアナノ粒子の粒子径と結晶子径を示す。
【表1】

【0053】
図13(a)〜(c)から、0.4MのTIPTを含んだF127ゲルから形成されるTiO2試料は粒子径3〜5nmの球状粒子を有していることが明らかとなり、(式6)のシェラー式から得られた結晶子径とほぼ同じ値であった。さらに、得られた粒子はアナターゼ結晶の(101)の格子像が確認できたことから、F127ゲルから形成されるTiO2試料は高い結晶性をもつ単結晶構造であることが明らかとなった。1.2M、2.4MのTIPTを含んだF127ゲルから形成されるTiO2試料についても、図13(a)〜(c)から0.4Mの時と同様な(101)の格子像が確認でき、さらにHRTEM画像から得られる粒子径と(式6)のシェラー式から得られる結晶子径とほぼ同じ値であったことから、高い結晶性をもつ単結晶粒子が得られたことが明らかとなった。
【実施例1】
【0054】
[チタニアナノチューブアレイの作成]
本実施例では、0.5wt%のフッ化アンモニウムを含んだグリセリン溶液を電解質とし、作用電極にチタン金属(1cm×2cm、厚み0.2mm)を、対極に白金箔(1cm×2cm、厚み0.1mm)を、参照電極に塩化銀電極を用いて電気化学セルを構成し、10V〜40Vで定電位電解を行うことにより、チタン金属上にチタニアナノチューブアレイ(Ti−TNTA試料)を作製した。定電位電解装置は図1に示すものを使用した。得られた試料は、XRD、HRTEMおよびSEMを用いて構造評価を行った。
【0055】
[チタニアナノチューブアレイを用いた色素増感太陽電池の作成]
次に、本実施例における、チタニアナノチューブアレイを用いた色素増感太陽電池の作成要領につき、図10および図11、並びに図14〜図16を参照しながら説明する。
【0056】
本実施例では、上記Ti−TNTA試料を250℃で2時間焼成した後、さらに450℃で2時間焼成を行い、アナターゼ結晶構造を持つチタニアナノチューブアレイを得た。このチタニアナノチューブアレイをITO基板に接合するために、トリブロック共重合体F127より作製されるTiO2微粒子(F127ゲル)を用いた。なお、本実施例では、焼成には電気炉を使用した。以下同様である。
【0057】
より詳細に説明すると、準備段階としてまず、ITO基板にF127ゲルを塗布し、450℃で焼成してチタニア薄膜層を形成した。
【0058】
次に、図14に示す通り、250℃で2時間焼成した後の上記Ti−TNTA試料をエタノールに十分浸漬させ、F127ゲルを作製する反応原液(F127原液)をエタノールに混合し、40℃で1日浸漬後、80℃で重縮合反応を4日間進行させ、F127ゲルをチタニアナノチューブアレイのチューブ内、チューブの上部およびチューブの外壁に析出させて、450℃で2時間焼成を行った(S11,S12)。
【0059】
このTi−TNTA試料をITO基板上に載せ、臭素メタノール溶液を滴下することでチタン金属を溶解除去した(S13)。
チタニアナノチューブアレイとITO基板上のチタニア薄膜層との結合を強化するため、両者の間隙にF127原液を浸み込ませ、80℃で1時間反応させた後550℃で2時間焼成した(S14,S15)。この第1の接合方法による結合強化操作は2回行った。
【0060】
さらに、このITO基板上のチタニアナノチューブアレイを80mMのTiCl4水溶液に80℃で1.5時間浸漬後(S16)、550〜600℃で2時間焼成し、チタニア電極を作製した(S17)。
【0061】
その後、常法に従い、3×10−4MのN719ルテニウム色素溶液にチタニア電極を40℃で2日浸漬した。対極は白金電極を用い、ハイミラン(三井・デュポンポリケミカル)で両電極を接合した。また、白金電極の穴から電解質溶液を挿入して、色素増感太陽電池セルを完成させた。
【0062】
より具体的には、作製した色素増感チタニア電極と白金電極を接着させるために、横4mm× 縦9mmの穴をあけた熱可塑性接着シートである厚さ50μmのハイミランを色素増感チタニア電極の周りに重ならないように置き、ホットプレート(Model RCH−3、東京理科器械)上で、140℃程度で二つの電極を圧着した。次に、白金電極の片方の電解質注入口より、調製した電解質を注入した。この際、注入口を防ぐように滴を作り、真空を引くことで気泡を除去した。さらに、電解質が白金電極の界面にまで浸透するよう、電解質を注入後真空で数秒引き上げた。
【0063】
なお本実施例では、上記白金電極を、電解質の注入口が2箇所設けられた透明導電性ガラスであるITOガラス(2cm×2cm、シート抵抗2Ω/□、ジオマティク)にイオンコーター(IB3、Eiko)を用いて電流値5mAで5分間白金を蒸着させることで得ている。
【0064】
また本実施例では、上記電解質には、0.6M 1−ブチル−3−メチルイミダゾリウムヨージド(BMII)、0.03M I2、0.1M Guanidinium thiocyanate、0.5M 4-Tert-butylpyridine(TBP)を脱水アセトニトリルとn-Valeronitrileを85:15の体積比で構成される溶媒に溶解させたものを使用している。
【0065】
実験については、擬似太陽光でI−V測定を行ったほか、インピーダンス測定を実施した。
具体的には、I−V特性は、光源に100mW/cm2に調製したソーラーシュミレーター(YSS−E40、山下電装)を用いて擬似太陽光(AM 1.5 1sun)の条件でDSCセルに対して垂直に照射し、ポテンショスタット(R6423,ADVANTEST)を使い電圧を0.1V〜−0.88Vまでの順方向と−0.88V〜0.1Vまでの逆方向で積分時間を0.5V/min程度で走査させることで測定を行った。また、順方向と逆方向の測定値の平均値をそのDSCセルのI−V特性とした。
また、100mW/cm2の照射光の確認として財団法人電気安全環境研究所(JET)で校正された二次基準アモルファス太陽電池セル(43.4mA at AM1.5 100mW/cm2 25℃、適用規格JIS[8931-1995/IEC 60904-2])を用いて、測定前にソーラーシュミレーターの検定を行った。
【0066】
また、インピーダンス測定には,インピーダンスアナライザー(Solartron 1255B、ソーラートロン)を用い、交流電圧の振幅は10mVとして、1MHz〜0.01Hzの周波数で測定を行った。バイアス電圧はI−V測定で求めた開放電圧とした。
【0067】
[チタニアナノチューブアレイを用いたチタニア電極の評価]
図9に、450℃で2時間焼成を行ったチタニアナノチューブアレイのHRTEM画像を示す。XRD測定結果よりチタニアナノチューブアレイはアナターゼ結晶と同定でき、チタニアナノチューブアレイのチューブの軸方向にアナターゼ結晶の{101}面の格子像が、すべて同じ方向に揃ってまっすぐ伸びた単結晶であることが確認できる。したがって、このようなチタニアナノチューブアレイを太陽電池の電極に用いると、高い電子伝導性が期待されることが明らかとなった。
【0068】
また図14右欄に、焼成後のチタニアナノチューブアレイの内部、上部、外壁に、F127ゲルを用いてTiO2微粒子を析出させた場合のSEM画像、HRTEM画像を示す。図14(a)から、チタン金属に対して垂直にチタニアナノチューブアレイが立っている様子が観察できる。また、図14(d)に示すHRTEM画像から、F127ゲルから合成される3〜5nmのTiO2微粒子がチタニアナノチューブアレイの内部(白い矢印)に含まれている様子が観察できた。さらに、図14(b)に示すSEM画像から、チタニアナノチューブアレイの上部に析出している様子が観察できた。
【0069】
図14左欄に示す工程および図14右欄に示すHRTEM画像の結果から、Ti−TNTA試料をエタノールに十分浸漬させ、その後F127ゲルを作製する反応原液(F127原液)を混合し、40℃で1日浸漬させたことで、F127原液がチタニアナノチューブアレイ内部にまで浸透し、80℃の段階でチタニアナノチューブアレイ内部で粒子成長が起こったことが期待できる。
このように、図14右欄のSEM画像、HRTEM画像からは、F127ゲルから合成されるTiO2微粒子は、3〜5nmの高結晶性のアナターゼであり、このような微粒子がチタニアナノチューブアレイの内部、上部に析出している様子が観察できた。
【0070】
[実験結果]
図17右欄に、F127ゲル反応原液を浸透させた後、重縮合反応によりチタニアナノチューブアレイとチタニア薄膜層界面にF127ゲルを形成させて接合した場合(F127 liquid。第1の方法)と、既に形成済みのF127ゲルを浸透させて接合した場合(F127 gel。第3の接合方法)のI−V測定結果を示す。第3の接合方法については実施例3にて説明する。
I−V測定結果から、第1の接合方法であるF127 liquidでは3%以上の光電変換効率が得られた。一方、第3の接合方法であるF127 gelでは1.2%であった。
【実施例2】
【0071】
次に、上記第2の接合方法を用いた実施例2につき説明する。チタニアナノチューブアレイの作成要領は実施例1と同様である。
本実施例における、チタニアナノチューブアレイを用いた色素増感太陽電池の作成要領につき、図10および図11、並びに図15および図16を参照しながら説明すると、Ti−TNTA試料をITO基板上に載せ、臭素メタノール溶液を滴下することでチタン金属を溶解除去した(S13)後、チタニアナノチューブアレイとITO基板上のチタニア薄膜層との結合を強化するため、第1の接合方法に代え第2の接合方法が適用される。
具体的には、チタニアナノチューブアレイとITO基板上のチタニア薄膜層の間隙にTIPT溶液(水溶液或いはエタノール溶液)を浸み込ませ、80℃で1時間反応させた後550℃で2時間焼成される(S24,S15)。実施例2においても、上記結合強化操作は2回行われる。
この点を除き、実施例2に係る作成要領は実施例1と同様である。
【0072】
また、本実施例においては、チタニアナノチューブアレイとITO基板との接合に用いたTiO2微粒子について検討を行った。24時間40Vの定電位電解で作製したチタニアナノチューブアレイに、F127原液によって接合させた電極と、320mMのTIPTエタノール溶液によって接合させた電極を用いたセルを比較した。
【0073】
各電極試料の短絡電流Jsc、開放起電力Voc、フィルファクターFF、変換効率η、セルの全直列抵抗Rtotalおよび色素吸着量(Amount of Dye Adsorption)を図16下段の表に示す。図16下段の表から、F127原液の方が色素吸着量が多いことから短絡電流Jscが向上したと考えられる。これは、TIPTエタノール溶液より得られるTiO2微粒子よりも比表面積の大きなTiO2微粒子がF127原液から得られるため、色素吸着量が増大したものと考察される。
【0074】
また、F127原液の方がTIPTエタノール溶液よりもセルの全直列抵抗が小さく、FFの値も1.24倍大きくなっている。これは、TIPTエタノール溶液よりも、F127原液から得られるTiO2微粒子で接合する方が密着性の良いセルが得られることを示している。
【実施例3】
【0075】
次に、上記第3の接合方法を用いた実施例3につき説明する。チタニアナノチューブアレイの作成要領は実施例1と同様である。
本実施例における、チタニアナノチューブアレイを用いた色素増感太陽電池の作成要領につき、図10および図11、並びに図17左欄を参照しながら説明すると、まず、上記Ti−TNTA試料を250℃で2時間焼成した後(S31)、さらに450℃で2時間焼成を行い(S32)、アナターゼ結晶構造を持つチタニアナノチューブアレイを得た。また、ITO基板側の準備段階として、ITO基板にF127ゲルを塗布し、450℃で焼成してチタニア薄膜層を形成した。
【0076】
次に、Ti−TNTA試料をITO基板上に載せ、臭素メタノール溶液を滴下することでチタン金属を溶解除去した(S33)。
そして、チタニアナノチューブアレイとITO基板上のチタニア薄膜層との結合を強化するため、両者をF127ゲル中に十分浸漬させ、80℃で1時間放置、反応させた後550℃で2時間焼成した(S34、S35)。この第3の接合方法による結合強化操作は2回行った。
【0077】
さらに、このITO基板上のチタニアナノチューブアレイを80mMのTiCl4水溶液に80℃で1.5時間浸漬後(S36)、600℃で2時間焼成し(S37)、チタニア電極を作製した。
【0078】
この後は実施例1と同様で、常法に従い、3×10−4MのN719ルテニウム色素溶液にチタニア電極を40℃で2日浸漬した。対極は白金電極を用い、ハイミランで両電極を接合した。また、白金電極の穴から電解質溶液を挿入して、セルを完成させた。
【0079】
図17右欄に、上記第1の方法を用いて作成されたチタニア電極が適用された色素増感太陽電池と、第3の方法を用いて作成されたチタニア電極が適用された色素増感太陽電池のI−V測定結果を示す。
チタニアナノチューブアレイとITO基板上のチタニア薄膜層との接合に関して上記I−V測定結果から類推するに、TiO2ゲルはチタニアナノチューブアレイとITO基板上のチタニア薄膜層の間隙に浸透しにくいため、第3の接合方法では両者の接合が不十分となっている。一方、TiO2微粒子を形成する反応原液は奥深く浸透可能であり、反応によりTiO2微粒子を発生するので、第1の接合方法では両者の接合が良好に行われる。接合の良否が光電変換効率の差にも表れたものと考察される。
上記の結果から見ても、チタニアナノチューブアレイとチタニア薄膜層との接合方法の今後の改良次第で、更なる効率向上が期待されることが明らかとなった。
【0080】
以上、本発明により、電解質の温度や種類を変更し、電解質の粘度を制御することで、チタニアナノチューブアレイの形態を制御できることが明らかとなった。
また本発明により、一例として昇温速度2℃/minで250℃、2時間焼成し、一度冷却させた後、昇温速度2℃/minで500℃、2時間焼成することで、チタニアナノチューブアレイ膜のクラッキングを抑えられることが明らかとなった。
さらに本発明により、一例として450℃で焼成を行うと、チタニアナノチューブアレイはアモルファスからアナターゼ結晶に相転移し、ナノチューブの軸方向にアナターゼ結晶の(101)の格子像が観察される程、結晶性の高い単結晶構造を有することが明らかとなった。
さらに、本発明により得られたチタニアナノチューブアレイ電極においては、F127ゲルから合成される3〜5nmのTiO2微粒子がチタニアナノチューブアレイの内部に含まれている様子がHRTEM画像から観察された。
【0081】
その他、本発明のチタニアナノチューブアレイを利用することで、色素増感太陽電池におけるセル性能が改善されることが明らかとなった。また、チューブの内部にTiO2微粒子を十分に析出させる工夫を重ねることで、更なる高効率化を図ることが可能であることも明らかとなった。
【0082】
[変形例]
以上、一実施例を用いて本発明を詳細に説明したが、本発明は上記実施例記載の構成に限定されず、種々の変形実施をすることが可能である。
例えば、本実施例で説明したチタニアナノチューブアレイとチタニア薄膜層との接合を強化するための第1の接合方法〜第3の接合方法はあくまで一例に過ぎず、必要に応じ他の方法によってチタニアナノチューブアレイとチタニア薄膜層との接合を行っても構わない。
【0083】
また、本実施例ではチタン金属を溶解除去するのに臭素メタノール溶液を用いたが、これに限定されず、チタン金属を溶解除去可能な別の溶液その他を用いても構わない。
定電位電解装置50で用いた電解質52或いは本実施例の色素増感太陽電池セル100にて用いた電解質2についても、上記組成に何ら限定されず、同様の効果を発揮し得る他の構成を適宜採用して構わない。
定電位電解装置50についても、参照電極56は場合によっては省略して構わない。
【0084】
また、本実施例では、チタニア薄膜層を形成しておいたITO基板上にチタニアナノチューブアレイを接合する構成としたが、これに限定されず、チタン金属同様、チタニア薄膜層についても除去する構成としても構わない。
【0085】
以上に説明した通り、本発明により作成された単結晶のチタニアナノチューブアレイは、格段に高い電子伝導性が期待できる。したがって本発明は、理想的な幾何学形状を有し、高い電子伝導性を併せ持つチタニアナノチューブアレイの作成方法、それによって得られるチタニア電極構造、並びにこのチタニア電極構造を適用した色素増感太陽電池を提供することができる新規かつ有用なるものであることが明らかである。
【符号の説明】
【0086】
L 光
1 白金電極
2 電解質
10 チタニア電極
11 チタニアナノチューブアレイ
12 TiO2薄膜
13 ITO膜
14 ガラス
15 透明導電膜電極
20 Ti
50 定電位電解装置
51 電解槽
52 電解質
53 ポテンショスタット
54 作用電極
55 対極
56 参照電極
57 温度計
58 窒素ガス
59 窒素タンク
100 色素増感太陽電池セル
【特許請求の範囲】
【請求項1】
チタニアナノチューブアレイの作成方法であって、
定電位電解法により、作用電極とされた箔状または板状のチタンを電解し、前記チタン上にチタニアナノチューブアレイを作成するステップと、
前記電解後、アモルファス状態の前記チタニアナノチューブアレイを漸次200℃<t1≦300℃(t1:第1の焼成温度)まで昇温して焼成後、漸次室温まで降温し、前記チタニアナノチューブアレイの整列形状を固定する第1の焼成ステップと、
前記第1の焼成ステップを経た後の前記チタニアナノチューブアレイを漸次400℃<t2≦600℃(t2:第2の焼成温度)まで昇温して焼成後、漸次室温まで降温することにより、アナターゼの{101}面の格子像がチューブの軸方向に走る単結晶チタニアナノチューブアレイを得る第2の焼成ステップと、
からなることを特徴とする方法。
【請求項2】
チタニア電極の作成方法であって、
請求項1に記載の方法で前記チタニアナノチューブアレイを作成した前記チタンをITO基板上に載置するステップと、
チタン溶解手段により前記ITO基板上の前記チタンを溶解除去するステップと、
前記チタニアナノチューブアレイを前記ITO基板に接合するステップと、
からなることを特徴とする方法。
【請求項3】
前記チタン溶解手段が前記チタン上へ臭素メタノール溶液を滴下することからなることを特徴とする請求項2に記載の方法。
【請求項4】
前記ITO基板の表面にはチタニア薄膜層が形成されており、前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合することを特徴とする請求項2または3に記載の方法。
【請求項5】
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、TiO2微粒子を形成するための反応原液を前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とする請求項4に記載の方法。
【請求項6】
前記反応原液が少なくともエチレンオキサイド/プロピレンオキサイド/エチレンオキサイドの骨格からなるトリブロック共重合体を含有したものからなることを特徴とする請求項5に記載の方法。
【請求項7】
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、オルトチタン酸テトライソプロピル溶液を前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とする請求項4に記載の方法。
【請求項8】
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、TiO2微粒子ゲルを前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とする請求項4に記載の方法。
【請求項9】
色素増感太陽電池に適用され、電解質を挟んで対極に対向配置されて使用されるチタニア電極であって、請求項2〜8のいずれか1項に記載の方法で作成されたものからなることを特徴とするチタニア電極。
【請求項10】
電解質を挟んで互いに対向するチタニア電極と対極とからなる色素増感太陽電池であって、
前記チタニア電極が請求項9に記載のものからなっていることを特徴とする色素増感太陽電池。
【請求項11】
前記対極が、ITOガラスに白金が蒸着された白金電極からなることを特徴とする請求項10に記載の色素増感太陽電池。
【請求項1】
チタニアナノチューブアレイの作成方法であって、
定電位電解法により、作用電極とされた箔状または板状のチタンを電解し、前記チタン上にチタニアナノチューブアレイを作成するステップと、
前記電解後、アモルファス状態の前記チタニアナノチューブアレイを漸次200℃<t1≦300℃(t1:第1の焼成温度)まで昇温して焼成後、漸次室温まで降温し、前記チタニアナノチューブアレイの整列形状を固定する第1の焼成ステップと、
前記第1の焼成ステップを経た後の前記チタニアナノチューブアレイを漸次400℃<t2≦600℃(t2:第2の焼成温度)まで昇温して焼成後、漸次室温まで降温することにより、アナターゼの{101}面の格子像がチューブの軸方向に走る単結晶チタニアナノチューブアレイを得る第2の焼成ステップと、
からなることを特徴とする方法。
【請求項2】
チタニア電極の作成方法であって、
請求項1に記載の方法で前記チタニアナノチューブアレイを作成した前記チタンをITO基板上に載置するステップと、
チタン溶解手段により前記ITO基板上の前記チタンを溶解除去するステップと、
前記チタニアナノチューブアレイを前記ITO基板に接合するステップと、
からなることを特徴とする方法。
【請求項3】
前記チタン溶解手段が前記チタン上へ臭素メタノール溶液を滴下することからなることを特徴とする請求項2に記載の方法。
【請求項4】
前記ITO基板の表面にはチタニア薄膜層が形成されており、前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合することを特徴とする請求項2または3に記載の方法。
【請求項5】
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、TiO2微粒子を形成するための反応原液を前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とする請求項4に記載の方法。
【請求項6】
前記反応原液が少なくともエチレンオキサイド/プロピレンオキサイド/エチレンオキサイドの骨格からなるトリブロック共重合体を含有したものからなることを特徴とする請求項5に記載の方法。
【請求項7】
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、オルトチタン酸テトライソプロピル溶液を前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とする請求項4に記載の方法。
【請求項8】
前記チタニア薄膜層の上に前記チタニアナノチューブアレイを接合するに際し、さらに、TiO2微粒子ゲルを前記チタニアナノチューブアレイと前記チタニア薄膜層との間に浸み込ませることを特徴とする請求項4に記載の方法。
【請求項9】
色素増感太陽電池に適用され、電解質を挟んで対極に対向配置されて使用されるチタニア電極であって、請求項2〜8のいずれか1項に記載の方法で作成されたものからなることを特徴とするチタニア電極。
【請求項10】
電解質を挟んで互いに対向するチタニア電極と対極とからなる色素増感太陽電池であって、
前記チタニア電極が請求項9に記載のものからなっていることを特徴とする色素増感太陽電池。
【請求項11】
前記対極が、ITOガラスに白金が蒸着された白金電極からなることを特徴とする請求項10に記載の色素増感太陽電池。
【図7】


【図8】


【図12】


【図16】


【図17】


【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図9】


【図10】


【図11】


【図13】


【図14】


【図15】


【図18】


【図19】


【図20】




【図8】


【図12】


【図16】


【図17】


【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図9】


【図10】


【図11】


【図13】


【図14】


【図15】


【図18】


【図19】


【図20】


【公開番号】特開2012−38634(P2012−38634A)
【公開日】平成24年2月23日(2012.2.23)
【国際特許分類】
【出願番号】特願2010−179153(P2010−179153)
【出願日】平成22年8月10日(2010.8.10)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り (刊行物I)2010年2月13日 同志社大学大学院工学研究科工業化学専攻発行の「2009年度修士論文要旨集」に発表 (刊行物II)2010年2月18日 社団法人化学工学会発行の「化学工学会第75年会(2010)研究発表講演プログラム集」に発表 (刊行物III)2010年3月26日 電気化学会大会学術企画委員会発行の「電気化学会第77回大会講演要旨集」に発表 (刊行物IV)2010年4月30日 同志社大学界面現象研究センター発行の「同志社大学界面現象研究センター2009年度研究報告書」に発表
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成21年度、独立行政法人 科学技術振興機構、研究成果最適展開支援事業、産業技術力強化法第19条の適用を受ける特許出願
【出願人】(503027931)学校法人同志社 (346)
【出願人】(391003598)富士化学株式会社 (40)
【Fターム(参考)】
【公開日】平成24年2月23日(2012.2.23)
【国際特許分類】
【出願日】平成22年8月10日(2010.8.10)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り (刊行物I)2010年2月13日 同志社大学大学院工学研究科工業化学専攻発行の「2009年度修士論文要旨集」に発表 (刊行物II)2010年2月18日 社団法人化学工学会発行の「化学工学会第75年会(2010)研究発表講演プログラム集」に発表 (刊行物III)2010年3月26日 電気化学会大会学術企画委員会発行の「電気化学会第77回大会講演要旨集」に発表 (刊行物IV)2010年4月30日 同志社大学界面現象研究センター発行の「同志社大学界面現象研究センター2009年度研究報告書」に発表
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成21年度、独立行政法人 科学技術振興機構、研究成果最適展開支援事業、産業技術力強化法第19条の適用を受ける特許出願
【出願人】(503027931)学校法人同志社 (346)
【出願人】(391003598)富士化学株式会社 (40)
【Fターム(参考)】
[ Back to top ]

