チタン錯体、その製造方法、チタン含有薄膜及びその製法
【課題】高い蒸気圧及び高い熱安定性を持ち、チタン含有薄膜を製造するための優れた原料となる新規なチタン錯体、該錯体を用いた薄膜の製法を提供する。
【解決手段】一般式(1)

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体を製造し、それを用いてチタン含有薄膜を製造する。
【解決手段】一般式(1)

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体を製造し、それを用いてチタン含有薄膜を製造する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、半導体素子の製造原料として有用なチタン錯体、その製造方法、チタン含有薄膜及びその薄膜の製法に関するものである。
【背景技術】
【0002】
現在、ランダムアクセスメモリやフラッシュメモリなどの半導体装置の高性能化を促進するために、半導体素子を高集積化することが求められている。半導体素子の高集積化を達成するためには、微細な三次元構造体の表面に均一な厚みの薄膜を形成する手法の確立及び実用化が必須である。こうした手法の有力な候補として、気体の材料を基板上で分解して膜を堆積させるCVD法又は基板表面に吸着させた材料を分解して膜を堆積させる原子層蒸着法(ALD法)が注目されており、現在これらの実用化が検討されている。
【0003】
CVD法又はALD法により薄膜を形成するための材料には、高い蒸気圧と熱安定性を持つ物質が選択される。また、形成される薄膜の品質を一定に保つためには、薄膜形成時の材料濃度を正確に制御することが重要である。この観点から、液体材料は固体材料に比べて気化速度を制御しやすいため、薄膜形成用材料として好ましい。
【0004】
次世代以降のダイナミックランダムアクセスメモリ(DRAM)のキャパシタ誘電体膜の素材としては、酸化チタン及びチタン含有酸化物が候補に挙げられている。また、チタン含有酸化物は不揮発性メモリの強誘電体膜の素材などとしても候補に挙げられている。
【0005】
チタン含有薄膜をCVD法又はALD法によって形成するための材料として、これまでに四塩化チタンTiCl4やテトライソプロポキソチタンTi(OiPr)4などが検討されてきた。
【0006】
また、Ti(OiPr)4の水との反応性を制御するために、キレート配位子を導入する試みがいくつかなされている。例えば(ジイソプロポキソ)(ビス(2,2,6,6−テトラメチルヘプタンジオナト))チタン(Ti(OiPr)2(THD)2)、ジイソプロポキソビス(tert−ブチルアセトアセタト)チタン(Ti(OiPr)2(tbaoac)2)、ビス(ジメチルアミノエトキソ)ジイソプロポキソチタン(Ti(OiPr)2(dmae)2)、(ジメチルアミノエトキソ)トリイソプロポキソチタンTi(OiPr)3(dmae))などキレート配位子を持つチタン化合物が合成され、CVD法又はALD法の材料として検討されている。(非特許文献1、2、3及び4)。
【0007】
さらに、アミド配位子を有するチタン化合物もCVD法やALD法による薄膜形成材料として検討されている。例えば、テトラキス(ジメチルアミド)チタン(Ti(NMe2)4)を材料に用いたCVD法やALD法によって窒化チタン薄膜や酸化チタン薄膜などの形成が検討されている。(例えば非特許文献5及び6)。キレート配位子を有するアミドチタン錯体も薄膜形成用材料として検討されている。例えば特許文献1に記載されているチタン錯体を挙げることが出来る。
【0008】
また、エテン−1,2−ジイルジアミド配位子を有している点で本発明のチタン錯体と類似の構造を持つアリールオキソ錯体が知られている。(非特許文献7)
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開2007−153872号公報
【非特許文献】
【0010】
【非特許文献1】International Journal of Photoenergy、5巻、99ページ、(2003年)
【非特許文献2】Journal of Materials Chemistry、14巻、3231ページ、(2004年)
【非特許文献3】Bulletin of the Korean Chemical Society、25巻、475ページ、(2004年)
【非特許文献4】Journal of Materials Chemistry、8巻、1773ページ、(1998年)
【非特許文献5】Journal of Vacuum Science & Technology B、24巻、1535ページ、(2006年)
【非特許文献6】Journal of The Electrochemical Society、152巻、G29ページ(2005年)
【非特許文献7】Journal of The American Chemical Society、109巻、6068ページ(1987年)
【発明の概要】
【発明が解決しようとする課題】
【0011】
TiCl4には、成膜するために高い温度が必要とされる点や、それを用いて形成された薄膜の中に塩素が混入する点などの問題がある。Ti(OiPr)4は水との反応性が極めて高く、成膜に使用するキャリアガスや反応ガス中などに含まれる微量水分と容易に反応する。その結果として装置内の配管内部に形成された酸化チタンの微粉が装置を閉塞させて生産性を低下させる恐れがある。また、非特許文献1、2、3及び4に記載のキレート配位チタン錯体は蒸気圧が低いという欠点を有している。さらに、Ti(NMe2)4は、水に対して極度に反応性が高く、成膜に使用するキャリアガス、反応ガス中などに含まれる微量水分と反応し、Ti(OiPr)4の場合と同様に装置を閉塞させて生産性を低下させる恐れがある。
【0012】
非特許文献7に記載のアリールオキソ錯体は、複数の嵩高いアリール基を有する点で本発明のチタン錯体とは異なる。また、非特許文献7に記載されているアリールオキソ錯体の合成方法は、本発明の製造方法とは異なる。さらに、非特許文献7にはアリールオキソ錯体のチタン含有薄膜の材料としての使用に関する記述は一切無い。
特許文献1に記載されているチタン錯体は、CVD法またはALD法の材料として適した熱安定性と蒸気圧を併せ持っているが、近年、これらよりもさらに熱安定性が高い材料の開発が望まれている。
【0013】
本発明の目的は、高い蒸気圧及び高い熱安定性を持ち、CVD法又はALD法などの手法によってチタン含有薄膜を製造するための優れた材料となる新規なチタン錯体、それら錯体の製造方法、それら錯体を用いて作製したチタン含有薄膜及びそれら薄膜の製法を提供することである。
【課題を解決するための手段】
【0014】
本発明者らは上述の現状に鑑み、鋭意検討を重ねた結果、一般式(1)で表されるチタン錯体が上記課題を解決できる優れた化合物であることを見出し、本発明を完成するに至った。
【0015】
すなわち本発明は、一般式(1)
【0016】
【化1】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体である。
【0017】
また本発明は、一般式(2)
【0018】
【化2】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。)で表されるジイミン、アルカリ金属及び一般式(3)
【0019】
【化3】

(式中、R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるアルコキソ錯体を反応させることを特徴とする一般式(1)で表されるチタン錯体の製造方法である。
【0020】
さらに本発明は、一般式(4)
【0021】
【化4】

(式中、R1a及びR4aは各々独立に炭素数1から6のアルキル基を示す。R2a及びR3aは各々独立に水素原子又は炭素数1から3のアルキル基を示す。R7及びR8は各々独立にフッ素原子で置換されていても良い炭素数1から4のアルキル基を示す。)で表されるアミド錯体に、一般式(5)
【0022】
【化5】

(式中、R5aはフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるアルコールを反応させることを特徴とする一般式(1a)
【0023】
【化6】

(式中、R1a及びR4aは各々独立に炭素数1から6のアルキル基を示す。R2a及びR3aは各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5aはフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体の製造方法である。
【0024】
また本発明は、一般式(1)で表されるチタン錯体を材料として用いることにより製造されるチタン含有薄膜である。
【0025】
さらに本発明は、一般式(1)で表されるチタン錯体を材料として用いることを特徴とするチタン含有薄膜の製法である。
【0026】
また本発明は、上述のチタン含有薄膜を用いることを特徴とする半導体デバイスである。
【0027】
さらに本発明は、上述のチタン含有薄膜を用いることを特徴とする光触媒である。以下に本発明を更に詳細に説明する。
【0028】
R1及びR4で表される炭素数1から16のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基、ヘプチル基、シクロヘキシルメチル基、1,1−ジエチルプロピル基、2−メチルシクロヘキシル基、4−メチルシクロヘキシル基、オクチル基、1,1−ジエチル−2−メチルプロピル基、2,5−ジメチルシクロヘキシル基、3,5−ジメチルシクロヘキシル基、1,1,3,3−テトラメチルブチル基、1−メチル−1−プロピルブチル基、1,1,2,3,3−ペンタメチルブチル基、1,1−ジエチル−3,3−ジメチルブチル基、アダマンチル基、1,1−ジメチルオクチル基、1,1−ジプロピルブチル基、1,1−ジメチルデシル基、1,1−ジエチルオクチル基、1,1−ジブチルペンチル基、1,1−ジブチルヘキシル基、1,1−ジブチルヘプチル基又は1,1−ジペンチルヘキシル基などを例示することができる。
【0029】
R2及びR3で表される炭素数1から3のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基又はシクロプロピル基を例示することができる。
【0030】
R5で表される炭素数1から16のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基、ヘプチル基、シクロヘキシルメチル基、1,1−ジエチルプロピル基、2−メチルシクロヘキシル基、4−メチルシクロヘキシル基、オクチル基、1,1−ジエチル−2−メチルプロピル基、2,5−ジメチルシクロヘキシル基、3,5−ジメチルシクロヘキシル基、1,1,3,3−テトラメチルブチル基、1−メチル−1−プロピルブチル基、1,1,2,3,3−ペンタメチルブチル基、1,1−ジエチル−3,3−ジメチルブチル基、アダマンチル基、1,1−ジメチルオクチル基、1,1−ジプロピルブチル基、1,1−ジメチルデシル基、1,1−ジエチルオクチル基、1,1−ジブチルペンチル基、1,1−ジブチルヘキシル基、1,1−ジブチルヘプチル基又は1,1−ジペンチルヘキシル基などを例示することができる。
【0031】
これらのアルキル基はフッ素原子で置換されていても良く、例えばトリフルオロメチル基、2,2,2−トリフルオロエチル基、ペルフルオロエチル基、ペルフルオロプロピル基、ペルフルオロイソプロピル基、ペルフルオロブチル基、ペルフルオロ−sec−ブチル基、ペルフルオロ−tert−ブチル基、ペルフルオロヘキシル基、ペルフルオロヘプチル基、ペルフルオロオクチル基、ペルフルオロノニル基、ペルフルオロデシル基、ペルフルオロウンデシル基、ペルフルオロドデシル基、ペルフルオロトリデシル基、ペルフルオロテトラデシル基、ペルフルオロペンタデシル基又はペルフルオロヘキサデシル基などを例示することができる。
【0032】
良好な蒸気圧と優れた熱安定性を持つという点で、チタン錯体(1)におけるR1及びR4は各々独立に炭素数2から6のアルキル基が好ましく、例えばエチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基が好ましい。R1及びR4は各々独立に炭素数4又は5のアルキル基がさらに好ましく、例えばブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基又は1−エチルプロピル基が更に好ましい。
【0033】
また、R2及びR3は水素原子が好ましい。
【0034】
また、R5は炭素数1から8のアルキル基が好ましく、例えばメチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基、ヘプチル基、シクロヘキシルメチル基、1,1−ジエチルプロピル基、2−メチルシクロヘキシル基、4−メチルシクロヘキシル基、オクチル基、1,1−ジエチル−2−メチルプロピル基、2,5−ジメチルシクロヘキシル基、3,5−ジメチルシクロヘキシル基、1,1,3,3−テトラメチルブチル基又は1−メチル−1−プロピルブチル基が好ましい。R5は炭素数3から5のアルキル基がさらに好ましく、例えばプロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基又は1−エチルプロピル基が更に好ましい。
【0035】
一般式(1)で表されるチタン錯体としては、良好な蒸気圧と優れた熱安定性を持つという点でエテン−1,2−ジイルビス(イソプロピルアミド)ビス(tert−ペンチルオキソ)チタン(Ti(iPrNCHCHNiPr)(OtPe)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ジエトキソチタン(Ti(tBuNCHCHNtBu)(OEt)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ジイソプロポキソチタン(Ti(tBuNCHCHNtBu)(OiPr)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(tert−ペンチルオキソ)チタン(Ti(tBuNCHCHNtBu)(OtPe)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(1,1−ジエチルプロピルオキソ)チタン(Ti(tBuNCHCHNtBu)(OCEt3)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(1,1−ジエチル−2−メチルプロピルオキソ)チタン(Ti(tBuNCHCHNtBu)(OCEt2CHMe2)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(2,2,2−トリフルオロエトキソ)チタン(Ti(tBuNCHCHNtBu)(OCH2CF3)2)、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジメトキソチタン(Ti(tPeNCHCHNtPe)(OMe)2)、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジエトキソチタン(Ti(tPeNCHCHNtPe)(OEt)2)、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジイソプロポキソチタン(Ti(tPeNCHCHNtPe)(OiPr)2)、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジ(tert−ブトキソ)チタン(Ti(tPeNCHCHNtPe)(OtBu)2)、またはエテン−1,2−ジイルビス(1,1,3,3−テトラメチルブチルアミド)ジイソプロポキソチタン(Ti(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2)が好ましい。更に好ましくは、エテン−1,2−ジイルビス(tert−ブチルアミド)ジイソプロポキソチタン(Ti(tBuNCHCHNtBu)(OiPr)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(tert−ペンチルオキソ)チタン(Ti(tBuNCHCHNtBu)(OtPe)2)又はエテン−1,2−ジイルビス(tert−ペンチルアミド)ジイソプロポキソチタン(Ti(tPeNCHCHNtPe)(OiPr)2)を挙げることが出来る。
【0036】
次に本発明の製造方法について説明する。製法1はジイミン(2)にアルカリ金属及びアルコキソ錯体(3)を有機溶媒中で反応させることにより、本発明のチタン錯体(1)を製造する方法である。
【0037】
原料であるジイミン(2)は、既知の方法(例えばJournal of the American Chemical Society、120巻、12714ページ、(1998年))を参考にして合成することが出来る。アルコキソ錯体(3)は、市販の試薬又は工業原料として入手することが出来るほか、Journal of the American Chemical Society、46巻、256ページ、(1924年)、Inorganica Chimica Acta、52巻、79ページ、(1981年)、及びAlkoxo and Aryloxo Derivatives of Metals、Academic Press、(2001年)を参考にして合成することが出来る。
【0038】
ジイミン(2)とアルカリ金属を反応させることにより、ジイミンのアルカリ金属錯体が生成することが知られている(例えば例えばJournal of the American Chemical Society、120巻、12714ページ、(1998年))。本発明の製法1では、ジイミン(2)、アルカリ金属及びアルコキソ錯体(3)を反応させる順序に制限はなく、例えば別途に調製して単離したジイミンのアルカリ金属錯体にアルコキソ錯体(3)を反応させても良い。工程が少なくチタン錯体(1)の収率が良い点で、最初にジイミン(2)にアルカリ金属を反応させ、続いてアルコキソ錯体(3)を反応させるのが好ましい。
【0039】
製法1で用いるアルカリ金属の種類は、チタン錯体(1)の収率が良い点で、リチウム又はナトリウムが好ましい。用いるアルカリ金属の量は、チタン錯体(1)の収率が良い点で、ジイミンに対して2当量以上用いるのが好ましい。製法1で用いる有機溶媒は、アルカリ金属、ジイミン(2)、アルコキソ錯体(3)又はジイミン(2)のアルカリ金属錯体と反応しないものであれば良い。例えばペンタン、ヘキサン、ヘプタン、オクタン、シクロヘキサン、メチルシクロヘキサン、エチルシクロヘキサンなどのアルカン類、ベンゼン、トルエン、キシレンなどの芳香族炭化水素類、ジエチルエーテル、ジイソプロピルエーテル、ジブチルエーテル、テトラヒドロフラン、ジオキサン、エチレングリコールジメチルエーテル、ジグライム、トリグライム、シクロペンチルメチルエーテルなどのエーテル類などを挙げることが出来る。これらを単独で用いることも混合して用いることも出来る。
【0040】
製法1によって得られた本発明のチタン錯体(1)は、ろ過、抽出、蒸留、昇華、結晶化など一般的な錯体の精製方法を適宜選んで用いることにより単離することが出来る。
【0041】
製法2はアミド錯体(4)にアルコール(5)を有機溶媒中で反応させることにより、チタン錯体(1a)を製造する方法である。
【0042】
本発明において、R1a及びR4aで表される炭素数1から6のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基などを例示することができる。
【0043】
またR2a及びR3aで表される炭素数1から3のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基又はシクロプロピル基を例示することができる。
【0044】
R5aで表される炭素数1から16のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基、ヘプチル基、シクロヘキシルメチル基、1,1−ジエチルプロピル基、2−メチルシクロヘキシル基、4−メチルシクロヘキシル基、オクチル基、1,1−ジエチル−2−メチルプロピル基、2,5−ジメチルシクロヘキシル基、3,5−ジメチルシクロヘキシル基、1,1,3,3−テトラメチルブチル基、1−メチル−1−プロピルブチル基、1,1,2,3,3−ペンタメチルブチル基、1,1−ジエチル−3,3−ジメチルブチル基、アダマンチル基、1,1−ジメチルオクチル基、1,1−ジプロピルブチル基、1,1−ジメチルデシル基、1,1−ジエチルオクチル基、1,1−ジブチルペンチル基、1,1−ジブチルヘキシル基、1,1−ジブチルヘプチル基又は1,1−ジペンチルヘキシル基などを例示することができる。
【0045】
これらのアルキル基はフッ素原子で置換されていても良く、例えばトリフルオロメチル基、2,2,2−トリフルオロエチル基、ペルフルオロエチル基、ペルフルオロプロピル基、ペルフルオロイソプロピル基、ペルフルオロブチル基、ペルフルオロ−sec−ブチル基、ペルフルオロ−tert−ブチル基、ペルフルオロヘキシル基、ペルフルオロヘプチル基、ペルフルオロオクチル基、ペルフルオロノニル基、ペルフルオロデシル基、ペルフルオロウンデシル基、ペルフルオロドデシル基、ペルフルオロトリデシル基、ペルフルオロテトラデシル基、ペルフルオロペンタデシル基又はペルフルオロヘキサデシル基などを例示することができる。
【0046】
R7及びR8で表される炭素数1から4のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基などを例示することができる。これらのアルキル基はフッ素原子で置換されていても良く、例えばトリフルオロメチル基、2,2,2−トリフルオロエチル基、ペルフルオロエチル基、ペルフルオロプロピル基、ペルフルオロイソプロピル基、ペルフルオロブチル基、ペルフルオロ−sec−ブチル基、ペルフルオロ−tert−ブチル基等を例示することができる。
【0047】
これらの中でも、R1a及びR4aは炭素数2から6のアルキル基が好ましい。さらに好ましくは炭素数4または5のアルキル基であり、例えばブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基又は1−エチルプロピル基等が例示される。
【0048】
またR2a及びR3aは水素原子が好ましい。
【0049】
またR5aは炭素数1から8のアルキル基が好ましく、例えばメチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基、ヘプチル基、シクロヘキシルメチル基、1,1−ジエチルプロピル基、2−メチルシクロヘキシル基、4−メチルシクロヘキシル基、オクチル基、1,1−ジエチル−2−メチルプロピル基、2,5−ジメチルシクロヘキシル基、3,5−ジメチルシクロヘキシル基、1,1,3,3−テトラメチルブチル基又は1−メチル−1−プロピルブチル基が好ましい。R5aは炭素数3から5のアルキル基がさらに好ましく、例えばプロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基又は1−エチルプロピル基が更に好ましい。
【0050】
R7及びR8はメチル基またはエチル基が好ましく、メチル基がさらに好ましい。
【0051】
原料であるアミド錯体(4)は、既知の方法(特許文献1)を参考にして合成することが出来る。
【0052】
製法2で用いる有機溶媒は、アミド錯体(4)及びアルコール(5)と反応しないものであれば良い。例えばペンタン、ヘキサン、ヘプタン、オクタン、シクロヘキサン、メチルシクロヘキサン、エチルシクロヘキサンなどのアルカン類、ベンゼン、トルエン、キシレンなどの芳香族炭化水素類、ジエチルエーテル、ジイソプロピルエーテル、ジブチルエーテル、テトラヒドロフラン、ジオキサン、エチレングリコールジメチルエーテル、ジグライム、トリグライム、シクロペンチルメチルエーテルなどのエーテル類などを挙げることが出来る。これらを単独で用いることも混合して用いることも出来る。
【0053】
製法2によってチタン錯体(1a)を収率良く得るためには、アミド錯体(4)をあらかじめ有機溶媒に溶かした溶液にアルコール(5)を加えるのが好ましい。
【0054】
製法2では、チタン錯体(1a)の収率が良い点で、アミド錯体(4)に対して1.6から2.4当量のアルコール(5)を反応させるのが好ましく、アミド錯体(4)に対して2.0当量のアルコール(5)を作用させるのがさらに好ましい。
【0055】
製法2によって得られたチタン錯体(1a)は、蒸留、昇華、結晶化など一般的な錯体の精製方法を適宜選んで用いることにより単離することが出来る。
【0056】
本発明のチタン錯体(1)を材料に用いて、チタン含有薄膜を製造することが出来る。製造することが出来る薄膜としては、酸化チタン、窒化チタン及び炭化チタンなどの薄膜並びにチタン酸ストロンチウム、チタン酸バリウムなどチタンと他の金属を含む複合金属化合物の薄膜を例示することが出来る。チタン錯体(1)は分子内に酸素原子を含むため、酸化チタン又は複合酸化物の薄膜製造の材料に用いるのに適している。チタン含有薄膜の製造方法としては特に制限はないが、CVD法、ALD法、インクジェット法、スピンコート法、ディップコート法または溶液法などを例示することができる。CVD法又はALD法により薄膜を製造する場合、チタン錯体(1)を気化させ、気体として反応室に供給する。チタン錯体(1)を気化させる方法としては、例えばバブリング法やリキッドインジェクション法などを挙げることが出来る。バブリング法とは、一定の温度に温めた容器に納めたチタン錯体(1)の中に、ヘリウム、ネオン、アルゴン、クリプトン、キセノン又は窒素などのキャリアガスを吹き込むことによってチタン錯体(1)を気化させる方法である。リキッドインジェクション法とは、チタン錯体(1)を液体の状態で気化器に送りこみ、気化器内で加熱することによってチタン錯体(1)を気化させる方法である。リキッドインジェクション法では、チタン錯体(1)を溶媒に溶かして溶液として用いることが出来る。チタン錯体(1)を溶液として用いる場合の溶媒としては、1,2−ジメトキシエタン、ジグライム、トリグライム、ジオキサン、テトラヒドロフラン、シクロペンチルメチルエーテルなどのエーテル類、ヘキサン、シクロヘキサン、メチルシクロヘキサン、エチルシクロヘキサン、ヘプタン、オクタン、ノナン、デカンなどのアルカン類、ベンゼン、トルエン、エチルベンゼン、キシレン等の芳香族炭化水素類を例示することが出来る。これらの溶媒を単独で又は混合して用いることが出来る。
【0057】
気体として反応室に供給したチタン錯体(1)を分解することにより、基板上にチタン含有薄膜を形成することが出来る。チタン錯体(1)を分解する方法としては、熱による方法、プラズマや光などを使用する方法、反応室内に水、酸素、オゾン、過酸化水素、水素、アンモニアなどの反応ガスを送り込んで化学反応を起こさせる方法を挙げることが出来る。これらの方法を単独で又は併せて用いることによってチタン錯体(1)を分解し、チタン含有薄膜を形成することが出来る。
【0058】
本発明のチタン含有薄膜は、DRAM、SRAM、FeRAM、ReRAM、MRAM、PRAM、フラッシュメモリー等の半導体デバイスの構成素子や光触媒として使用することができる。
【発明の効果】
【0059】
本発明のチタン錯体(1)は、良好な気化特性及び優れた熱安定性を持ち、即ち高い蒸気圧及び高い熱安定性を持ち、これを材料として用いたCVD法又はALD法などの手法によってチタン含有薄膜を製造することが可能である。
【図面の簡単な説明】
【0060】
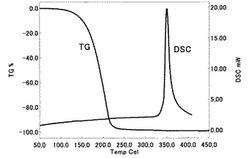
【図1】試験例1のTG及びDSC測定結果を示す図である。
【図2】試験例2のTG及びDSC測定結果を示す図である。
【図3】試験例3のTG及びDSC測定結果を示す図である。
【図4】試験例4のTG及びDSC測定結果を示す図である。
【図5】試験例5のTG及びDSC測定結果を示す図である。
【図6】試験例6のTG及びDSC測定結果を示す図である。
【図7】試験例7のTG及びDSC測定結果を示す図である。
【図8】試験例8のTG及びDSC測定結果を示す図である。
【図9】試験例9のTG及びDSC測定結果を示す図である。
【図10】試験例10のTG及びDSC測定結果を示す図である。
【図11】試験例11のTG及びDSC測定結果を示す図である。
【図12】試験例12のTG及びDSC測定結果を示す図である。
【図13】実施例16及び17で用いたCVD成膜装置の概略図である。
【図14】試験例13のTG及びDSC測定結果を示す図である。
【図15】実施例20、21、22及び23で用いたCVD成膜装置の概略図である。
【実施例】
【0061】
以下、本発明を実施例によりさらに詳細に説明する。ただし、本発明はこれら実施例に限定されるものではない。
【0062】
(実施例1)
アルゴン雰囲気下で、N,N’−ジイソプロピル−1,4−ジアザ−1,3−ブタジエン(iPrNCHCHNiPr)1.38g(9.83mmol)をヘキサン12mLとテトラヒドロフラン2mLの混合液に溶かし、リチウム143mg(20.6mmol)を加えて室温で12時間撹拌した。その反応液にテトラキス(tert−ペンチルオキソ)チタン(Ti(OtPe)4)3.90g(9.83mmol)をヘキサン10mLに溶かした溶液を加え、室温で14時間撹拌した。その反応液にさらにクロロトリメチルシラン2.14g(19.7mmol)を加えて室温で6時間撹拌した。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度95℃/0.07Torr)することにより、エテン−1,2−ジイルビス(イソプロピルアミド)ビス(tert−ペンチルオキソ)チタン(Ti(iPrNCHCHNiPr)(OtPe)2)を濃赤色の液体として得た(収量3.29g、収率92%)。
【0063】
(1H NMR(500MHz,C6D6,δ/ppm)
5.78(s,2H),3.55(sept,J=6Hz,2H),1.59(q,J=8Hz,4H),1.33(s,12H),1.25(br,12H),1.04(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
106.0,82.8,81.6(br),56.8,38.2,37.8,26.1,9.55,9.48。
【0064】
(試験例1)Ti(iPrNCHCHNiPr)(OtPe)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(iPrNCHCHNiPr)(OtPe)2のTG(熱重量測定)の結果及び密閉容器中で昇温速度10℃/minで測定したTi(iPrNCHCHNiPr)(OtPe)2のDSC(示差走査熱量測定)の結果を図1に示した。TGの結果からTi(iPrNCHCHNiPr)(OtPe)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(iPrNCHCHNiPr)(OtPe)2の熱安定性が良好なことが明らかである。
【0065】
(実施例2)
アルゴン雰囲気下で、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(ジメチルアミド)チタン(Ti(tBuNCHCHNtBu)(NMe2)2)2.01g(6.62mmol)をヘキサン8mLに溶かし、エタノール610mg(13.2mmol)を加えて室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度85℃/0.05Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ジエトキソチタン(Ti(tBuNCHCHNtBu)(OEt)2)を濃赤色の液体として得た(収量1.88g、収率93%)。
【0066】
1H NMR(500MHz,C6D6,δ/ppm)
5.98(s,2H),4.20(br,4H),1.29(s,18H),1.16−1.32(br,6H)
13C NMR(125MHz,C6D6,δ/ppm)
102.4,68−70(br),58.0,31.6,21.2。
【0067】
(試験例2)Ti(tBuNCHCHNtBu)(OEt)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OEt)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OEt)2のDSCの結果を図2に示した。TGの結果からTi(tBuNCHCHNtBu)(OEt)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OEt)2の熱安定性が良好なことが明らかである。
【0068】
(実施例3)
アルゴン雰囲気下で、N,N’−ジ(tert−ブチル)−1,4−ジアザ−1,3−ブタジエン(tBuNCHCHNtBu)2.22g(13.2mmol)をテトラヒドロフラン20mLに溶かし、ナトリウム606mg(26.4mmol)を加えて室温で12時間撹拌した。その反応液にテトライソプロポキソチタン(Ti(OiPr)4)3.56g(12.5mmol)をヘキサン10mLに溶かした溶液を加え、室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、残渣にヘキサン20mLを加えた。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度85℃/0.05Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ジイソプロポキソチタン(Ti(tBuNCHCHNtBu)(OiPr)2)を濃赤色の液体として得た(収量3.91g、収率93%)。
【0069】
1H NMR(500MHz,C6D6,δ/ppm)
5.96(s,2H),4.0−5.0(br,2H),1.30(s,18H),1.1−1.3(br,12H)
13C NMR(125MHz,C6D6,δ/ppm)
102.7,74.5(br),57.6,31.7,27.8。
【0070】
(試験例3)Ti(tBuNCHCHNtBu)(OiPr)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OiPr)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OiPr)2のDSCの結果を図3に示した。TGの結果からTi(tBuNCHCHNtBu)(OiPr)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OiPr)2の熱安定性が良好なことが明らかである。
【0071】
(実施例4)
アルゴン雰囲気下で、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(ジメチルアミド)チタン(Ti(tBuNCHCHNtBu)(NMe2)2)6.01g(19.7mmol)をトルエン20mLに溶かし、2−プロパノール2.37g(39.4mmol)を加えて室温で2時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度85℃/0.05Torr)することにより、Ti(tBuNCHCHNtBu)(OiPr)2を濃赤色の液体として得た(収量6.21g、収率94%)。このようにして得たTi(tBuNCHCHNtBu)(OiPr)2の1H及び13C NMRスペクトルを測定したところ、これらのスペクトルは実施例3で得たもののスペクトルと一致した。
【0072】
(実施例5)
アルゴン雰囲気下で、Ti(tBuNCHCHNtBu)(NMe2)21.76g(5.78mmol)をヘキサン7mLに溶かし、tert−ペンチルアルコール1.02g(11.6mmol)を加えて室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度97℃/0.05Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(tert−ペンチルオキソ)チタン(Ti(tBuNCHCHNtBu)(OtPe)2)を濃赤色の液体として得た(収量2.11g、収率93%)。
【0073】
1H NMR(500MHz,C6D6,δ/ppm)
5.93(s、2H),1.55(br、4H),1.30(s,18H),1.1−1.4(br,12H),0.99(br,6H)
13C NMR(125MHz,C6D6,δ/ppm)
103.1,81.4(br),57.4,38.3,31.9,31.1,9.8。
【0074】
(試験例4)Ti(tBuNCHCHNtBu)(OtPe)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OtPe)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OtPe)2のDSCの結果を図4に示した。TGの結果からTi(tBuNCHCHNtBu)(OtPe)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OtPe)2の熱安定性が良好なことが明らかである。
【0075】
(実施例6)
アルゴン雰囲気下で、Ti(tBuNCHCHNtBu)(NMe2)22.61g(8.58mmol)をヘキサン10mLに溶かし、3−エチル−3−ペンタノール2.00g(17.2mmol)を加えて室温で14時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度112℃/0.03Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(1,1−ジエチルプロピルオキソ)チタン(Ti(tBuNCHCHNtBu)(OCEt3)2)を濃赤色の液体として得た(収量1.93g、収率50%)。
【0076】
1H NMR(500MHz,C6D6,δ/ppm)
5.95(s,2H),1.55(br,12H),1.33(s,18H),0.96(br,18H)
13C NMR(125MHz,C6D6,δ/ppm)
103.0,86.0(br),57.5,32.3,31.5,8.8。
【0077】
(試験例5)Ti(tBuNCHCHNtBu)(OCEt3)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OCEt3)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OCEt3)2のDSCの結果を図5に示した。TGの結果からTi(tBuNCHCHNtBu)(OCEt3)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OCEt3)2の熱安定性が良好なことが明らかである。
【0078】
(実施例7)
アルゴン雰囲気下で、Ti(tBuNCHCHNtBu)(NMe2)23.09g(10.2mmol)をヘキサン10mLに溶かし、1,1−ジエチル−2−メチルプロピルアルコール2.64g(20.3mol)を加えて室温で4.5時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(油浴温度190℃/0.06Torr)することによりエテン−1,2−ジイルビス(tert−ブチルアミド)ビス(1,1−ジエチル−2−メチルプロピルオキソ)チタン(Ti(tBuNCHCHNtBu)(OCEt2CHMe2)2)を濃赤色の固体として得た(収量3.35g、収率69%)。
【0079】
1H NMR(500MHz,C6D6,δ/ppm)
5.97(s,2H),1.61(br,10H),1.34(s,18H),1.00(br,24H)
13C NMR(125MHz,C6D6,δ/ppm)
103.2,88.1(br),57.9,34.8,31.5,29.5,17.8,8.7。
【0080】
(試験例6)Ti(tBuNCHCHNtBu)(OCEt2CHMe2)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OCEt2CHMe2)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OCEt2CHMe2)2のDSCの結果を図6に示した。TGの結果からTi(tBuNCHCHNtBu)(OCEt2CHMe2)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OCEt2CHMe2)2の熱安定性が良好なことが明らかである。
【0081】
(実施例8)
アルゴン雰囲気下で、Ti(tBuNCHCHNtBu)(NMe2)24.11g(13.5mmol)をヘキサン20mLに溶かし、2,2,2−トリフルオロエタノール2.70g(27.0mmol)を加えて室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度90℃/0.10Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(2,2,2−トリフルオロエトキソ)チタン(Ti(tBuNCHCHNtBu)(OCH2CF3)2)を濃赤色の液体として得た(収量4.94g、収率88%)。
【0082】
1H NMR(500MHz,C6D6,δ/ppm)
5.90(s,2H),4.4(br,2H),3.8(br,2H),1.14(s,18H)
13C NMR(125MHz,C6D6,δ/ppm)
125.3(q,J=279Hz),101.4,70−72(br),68−70(br),59.7,31.0
19F NMR(470MHz,C6D6,δ/ppm)
−78.5(br),−79.2(br)。
【0083】
(試験例7)Ti(tBuNCHCHNtBu)(OCH2CF3)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OCH2CF3)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OCH2CF3)2のDSCの結果を図7に示した。TGの結果からTi(tBuNCHCHNtBu)(OCH2CF3)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OCH2CF3)2の熱安定性が良好なことが明らかである。
【0084】
(参考例1)
アルゴン雰囲気下で、N,N’−ジ(tert−ペンチル)−1,4−ジアザ−1,3−ブタジエン(tPeNCHCHNtPe)5.31g(27.0mmol)をテトラヒドロフラン50mLに溶かした溶液にリチウム379mg(54.6mmol)を加え、室温で14時間撹拌した。残ったリチウムをろ別し、ろ液から溶媒を減圧留去した。残った黄色固体をヘキサン30mLに懸濁させ、テトラキス(ジメチルアミド)チタン(Ti(NMe2)4)5.77g(25.7mmol)をヘキサン10mLに溶かした溶液を加えた。50℃で4時間攪拌した後、室温まで冷却し、不溶物をろ別した。ろ液から溶媒を減圧留去し、得られた残渣を減圧蒸留することにより、エテン−1,2−ジイルビス(tert−ペンチルアミド)ビス(ジメチルアミド)チタン(Ti(tPeNCHCHNtPe)(NMe2)2)を濃赤色の液体として得た(収量7.83g、収率91%)。
【0085】
1H NMR(500MHz,C6D6,δ/ppm)
5.77(s、2H),3.04(br,6H),1.51(q,J=8Hz,4H),1.24(s,12H),0.77(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
101.6,60.9,43.4,36.4,28.5,8.9。
【0086】
(実施例9)
アルゴン雰囲気下で、Ti(tPeNCHCHNtPe)(NMe2)23.43g(10.3mmol)をヘキサン15mLに溶かし、メタノール661mg(20.6mmol)を加えて室温で14時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度106℃/0.10Torr)することにより、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジメトキソチタン(Ti(tPeNCHCHNtPe)(OMe)2)を濃赤色の粘性液体として得た(収量2.92g、収率92%)。
【0087】
1H NMR(500MHz,C6D6,δ/ppm)
6.02(s,2H),3.99(br,6H),1.54(q,J=8Hz,4H),1.27(s,12H),0.78(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
103.0,61.4,61.2(br),37.0,28.5,9.3。
【0088】
(試験例8)Ti(tPeNCHCHNtPe)(OMe)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tPeNCHCHNtPe)(OMe)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tPeNCHCHNtPe)(OMe)2のDSCの結果を図8に示した。TGの結果からTi(tPeNCHCHNtPe)(OMe)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tPeNCHCHNtPe)(OMe)2の熱安定性が良好なことが明らかである。
【0089】
(実施例10)
アルゴン雰囲気下で、Ti(tPeNCHCHNtPe)(NMe2)22.21g(6.65mmol)をヘキサン10mLに溶かし、エタノール613mg(13.3mmol)を加えて室温で8時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度100℃/0.05Torr)することにより、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジエトキソチタン(Ti(tPeNCHCHNtPe)(OEt)2)を濃赤色の液体として得た(収量2.16g、収率97%)。
【0090】
1H NMR(500MHz,C6D6,δ/ppm)
5.91(s,2H),3.4−4.8(br,4H),1.55(q,J=8Hz,4H),1.25(12H),1.1−1.5(br,6H),0.80(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
102.3,71.0(br),60.7,36.6,29.1(br),21.1,9.2。
【0091】
(試験例9)Ti(tPeNCHCHNtPe)(OEt)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tPeNCHCHNtPe)(OEt)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tPeNCHCHNtPe)(OEt)2のDSCの結果を図9に示した。TGの結果からTi(tPeNCHCHNtPe)(OEt)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tPeNCHCHNtPe)(OEt)2の熱安定性が良好なことが明らかである。
【0092】
(実施例11)
アルゴン雰囲気下で、N,N’−ジ(tert−ペンチル)−1,4−ジアザ−1,3−ブタジエン(tPeNCHCHNtPe)3.09g(15.7mmol)をテトラヒドロフラン30mLに溶かし、ナトリウム758mg(33.0mmol)を加えて室温で12時間撹拌した。その反応液にテトライソプロポキソチタン(Ti(OiPr)4)4.25g(15.0mmol)をヘキサン10mLに溶かした溶液を加え、室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、残渣にヘキサン30mLを加えた。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度92℃/0.05Torr)することにより、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジイソプロポキソチタン(Ti(tPeNCHCHNtPe)(OiPr)2)を濃赤色の液体として得た(収量4.96g、収率92%)。
【0093】
1H NMR(500MHz,C6D6,δ/ppm)
5.90(s,2H),3.7−5.2(br,2H),1.56(q,J=8Hz,4H),1.26(s,12H),0.9−1.6(br,12H),0.81(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
102.6,74.4(br),60.3,36.8,29.2(br),27.8,9.3。
【0094】
(試験例10)Ti(tPeNCHCHNtPe)(OiPr)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tPeNCHCHNtPe)(OiPr)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tPeNCHCHNtPe)(OiPr)2のDSCの結果を図10に示した。TGの結果からTi(tPeNCHCHNtPe)(OiPr)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tPeNCHCHNtPe)(OiPr)2の熱安定性が良好なことが明らかである。
【0095】
(実施例12)
アルゴン雰囲気下で、エテン−1,2−ジイルビス(tert−ペンチルアミド)ビス(ジメチルアミド)チタン(Ti(tPeNCHCHNtPe)(NMe2)2)1.90g(5.71mmol)をヘキサン10mLに溶かし、2−プロパノール687mg(11.4mmol)を加えて室温で3時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度95℃/0.06Torr)することによりTi(tPeNCHCHNtPe)(OiPr)2を濃赤色の液体として得た(収量2.00g、収率96%)。このようにして得たTi(tPeNCHCHNtPe)(OiPr)2の1H及び13C NMRスペクトルを測定したところ、これらのスペクトルは実施例11で得たもののスペクトルと一致した。
【0096】
(実施例13)
アルゴン雰囲気下で、N,N’−ジ(tert−ペンチル)−1,4−ジアザ−1,3−ブタジエン(tPeNCHCHNtPe)2.38g(12.1mmol)をテトラヒドロフラン24mLに溶かし、ナトリウム584mg(25.4mmol)を加えて室温で12時間撹拌した。その反応液にテトラ(tert−ブトキソ)チタン(Ti(OtBu)4)3.93g(11.5mmol)をヘキサン12mLに溶かした溶液を加え、室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、残渣にヘキサン25mLを加えた。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度105℃/0.10Torr)することにより、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジ(tert−ブトキソ)チタン(Ti(tPeNCHCHNtPe)(OtBu)2)を濃赤色の液体として得た(収量4.28g、収率95%)。
【0097】
1H NMR(500MHz,C6D6,δ/ppm)
5.87(s,2H),1.58(q,J=8Hz,4H),1.27(s,12H),1.0−1.7(br,18H),0.81(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
103.1,79.3(br),60.0,37.0,33.4,29.4(br),9.4。
【0098】
(試験例11)Ti(tPeNCHCHNtPe)(OtBu)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tPeNCHCHNtPe)(OtBu)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tPeNCHCHNtPe)(OtBu)2のDSCの結果を図11に示した。TGの結果からTi(tPeNCHCHNtPe)(OtBu)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tPeNCHCHNtPe)(OtBu)2の熱安定性が良好なことが明らかである。
【0099】
(実施例14)
アルゴン雰囲気下で、Ti(tPeNCHCHNtPe)(NMe2)21.10g(3.32mmol)をヘキサン5mLに溶かし、tert−ブタノール493mg(6.65mmol)を加えて室温で14時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度105℃/0.10Torr)することにより、Ti(tPeNCHCHNtPe)(OtBu)2を濃赤色の液体として得た(収量1.24g、収率96%)。このようにして得たTi(tPeNCHCHNtPe)(OtBu)2の1H及び13C NMRスペクトルを測定したところ、これらのスペクトルは実施例13で得たもののスペクトルと一致した。
【0100】
(参考例2)
1,1,3,3−テトラメチルブチルアミン19.5g(151mmol)と水100mLの混合液に40%グリオキサル水溶液10.7g(73.5mmol)を加えて室温で1時間撹拌した。生成した固体をろ別し、水10mLで二回洗浄した後、減圧下で乾燥することにより、N,N’−ジ(1,1,3,3−テトラメチルブチル)−1,4−ジアザ−1,3−ブタジエン(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)を白色固体として得た(収量19.5g、収率95%)。
【0101】
1H NMR(500MHz,C6D6,δ/ppm)
8.09(s,2H),1.61(s,4H),1.14(s,12H),0.98(18H)
13C NMR(125MHz,C6D6,δ/ppm)
157.8,62.0,56.6,32.5,32.2,29.8。
【0102】
(実施例15)
アルゴン雰囲気下で、Me3CCH2CMe2NCHCHNCMe2CH2CMe32.98g(10.6mmol)をテトラヒドロフラン30mLに溶かし、ナトリウム538mg(23.4mmol)を加えて室温で16時間撹拌した。その反応液にTi(OiPr)43.02g(10.6mmol)をヘキサン15mLに溶かした溶液を加え、室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、残渣にヘキサン25mLを加えた。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度130℃/0.04Torr)することにより、エテン−1,2−ジイルビス(1,1,3,3−テトラメチルブチルアミド)ジイソプロポキソチタン(Ti(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2)を濃赤色の液体として得た(収量4.18g、収率88%)。
【0103】
1H NMR(500MHz,C6D6,δ/ppm)
5.93(s,2H),4.83(br,1H),4.11(br,1H),1.62(s,4H),1.2−1.7(br,18H),0.9−1.2(br,6H),0.94(s,18H)
13C NMR(125MHz,C6D6,δ/ppm)
102.3,76.0(br),73.1(br),61.5,56.9,32.1,32.0,31.9(br),27.9。
【0104】
(試験例12)Ti(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2のDSCの結果を図12に示した。TGの結果からTi(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2の熱安定性が良好なことが明らかである。
【0105】
(実施例16)
恒温槽を用いて61℃に保たれた材料容器内に納められたTi(tBuNCHCHNtBu)(OiPr)2にキャリアガスとしてアルゴンを流量30sccmで吹き込んでTi(tBuNCHCHNtBu)(OiPr)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量180sccmで、反応ガスとして酸素ガスを流量90sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を400℃に保ち、反応室内の圧力が4Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図13に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。また、この薄膜の組成をX線光電子分光法で分析したところ、酸化チタンであることが確認された。
【0106】
(実施例17)
恒温槽を用いて61℃に保たれた材料容器内に納められたTi(tBuNCHCHNtBu)(OiPr)2にキャリアガスとしてアルゴンを流量30sccmで吹き込んでTi(tBuNCHCHNtBu)(OiPr)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量180sccmで、反応ガスとして酸素ガスを流量90sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を240℃に保ち、反応室内の圧力が4Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図13に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。また、この薄膜の組成をX線光電子分光法で分析したところ、酸化チタンであることが確認された。
【0107】
(実施例18)
アルゴン雰囲気下で、Ti(tBuNCHCHNtBu)(NMe2)228.54g(93.8mmol)をヘキサン60mLに溶かし、sec−ブタノール13.90g(187.5mmol)を加えて室温で5時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度92−96℃/0.03Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(sec−ブトキソ)チタン(Ti(tBuNCHCHNtBu)(OsBu)2)を濃赤色の液体として得た(収量32.35g、収率95%)。なお、これはsec−ブチル基のキラリティーの違いに基づく異性体の混合物である。
【0108】
1H NMR(500MHz,C6D6,δ/ppm)
5.96(s,2H),4.25(br,2H),1.7−1.3(br,4H),1.30(s,18H),1.3−1.1(br,6H),1.1−0.9(br,6H).
13C NMR(125MHz,C6D6,δ/ppm)
102.73,102.71,102.70,80.0(br),57.8,57.74,57.71,34.3,31.7,25.7,11.1。
【0109】
(試験例13)Ti(tBuNCHCHNtBu)(OsBu)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OsBu)2のTGの結果及びアルゴン雰囲気下で密閉した容器の中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OEt)2のDSCの結果を図14に示した。TGの結果からTi(tBuNCHCHNtBu)(OsBu)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OsBu)2の熱安定性が良好なことが明らかである。
【0110】
(実施例19)
アルゴン雰囲気下で、N,N’−ジ(tert−ブチル)−1,4−ジアザ−1,3−ブタジエン(tBuNCHCHNtBu)14.85g(88.2mmol)をテトラヒドロフラン110mLに溶かし、ナトリウム4.18g(182mmol)を加えて室温で14時間撹拌した。その反応液をテトラ−sec−ブトキソチタン(Ti(OsBu)4)29.18g(85.7mmol)をヘキサン50mLに溶かした溶液に加え、室温で14時間撹拌した。その反応液から溶媒を減圧下で留去し、残渣にヘキサン120mLを加えた。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度92−96℃/0.03Torr)することにより、Ti(tBuNCHCHNtBu)(OsBu)2を濃赤色の液体として得た(収量28.81g、収率93%)。なお、これはsec−ブチル基のキラリティーの違いに基づく異性体の混合物である。このようにして得たTi(tBuNCHCHNtBu)(OsBu)2の1H及び13C NMRスペクトルを測定したところ、これらのスペクトルは実施例18で得たもののスペクトルと一致した。
【0111】
(実施例20)
恒温槽を用いて84℃に保たれた材料容器内に納められたTi(tBuNCHCHNtBu)(OEt)2にキャリアガスとしてアルゴンを流量10sccmで吹き込んでTi(tBuNCHCHNtBu)(OEt)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量230sccmで、反応ガスとして酸素ガスを流量60sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を400℃に保ち、反応室内の圧力が4Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図15に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。
【0112】
(実施例21)
恒温槽を用いて84℃に保たれた材料容器内に納められたTi(tBuNCHCHNtBu)(OtPe)2にキャリアガスとしてアルゴンを流量10sccmで吹き込んでTi(tBuNCHCHNtBu)(OtPe)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量230sccmで、反応ガスとして酸素ガスを流量60sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を400℃に保ち、反応室内の圧力が100Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図15に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。
【0113】
(実施例22)
恒温槽を用いて84℃に保たれた材料容器内に納められたTi(tPeNCHCHNtPe)(OiPr)2にキャリアガスとしてアルゴンを流量10sccmで吹き込んでTi(tPeNCHCHNtPe)(OiPr)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量230sccmで、反応ガスとして酸素ガスを流量60sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を400℃に保ち、反応室内の圧力が4Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図15に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。
【0114】
(実施例23)
恒温槽を用いて84℃に保たれた材料容器内に納められたTi(tBuNCHCHNtBu)(OsBu)2にキャリアガスとしてアルゴンを流量10sccmで吹き込んでTi(tBuNCHCHNtBu)(OsBu)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量230sccmで、反応ガスとして酸素ガスを流量60sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を400℃に保ち、反応室内の圧力が4Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図15に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。
【符号の説明】
【0115】
1.材料容器
2.恒温槽
3.反応室
4.基板
5.反応ガス
6.希釈ガス
7.キャリアガス
8.マスフローコントローラー
9.マスフローコントローラー
10.マスフローコントローラー
11.真空ポンプ
12.排気
13.材料容器
14.恒温槽
15.反応室
16.基板
17.反応ガス
18.希釈ガス
19.キャリアガス
20.マスフローコントローラー
21.マスフローコントローラー
22.マスフローコントローラー
23.真空ポンプ
24.排気
【技術分野】
【0001】
本発明は、半導体素子の製造原料として有用なチタン錯体、その製造方法、チタン含有薄膜及びその薄膜の製法に関するものである。
【背景技術】
【0002】
現在、ランダムアクセスメモリやフラッシュメモリなどの半導体装置の高性能化を促進するために、半導体素子を高集積化することが求められている。半導体素子の高集積化を達成するためには、微細な三次元構造体の表面に均一な厚みの薄膜を形成する手法の確立及び実用化が必須である。こうした手法の有力な候補として、気体の材料を基板上で分解して膜を堆積させるCVD法又は基板表面に吸着させた材料を分解して膜を堆積させる原子層蒸着法(ALD法)が注目されており、現在これらの実用化が検討されている。
【0003】
CVD法又はALD法により薄膜を形成するための材料には、高い蒸気圧と熱安定性を持つ物質が選択される。また、形成される薄膜の品質を一定に保つためには、薄膜形成時の材料濃度を正確に制御することが重要である。この観点から、液体材料は固体材料に比べて気化速度を制御しやすいため、薄膜形成用材料として好ましい。
【0004】
次世代以降のダイナミックランダムアクセスメモリ(DRAM)のキャパシタ誘電体膜の素材としては、酸化チタン及びチタン含有酸化物が候補に挙げられている。また、チタン含有酸化物は不揮発性メモリの強誘電体膜の素材などとしても候補に挙げられている。
【0005】
チタン含有薄膜をCVD法又はALD法によって形成するための材料として、これまでに四塩化チタンTiCl4やテトライソプロポキソチタンTi(OiPr)4などが検討されてきた。
【0006】
また、Ti(OiPr)4の水との反応性を制御するために、キレート配位子を導入する試みがいくつかなされている。例えば(ジイソプロポキソ)(ビス(2,2,6,6−テトラメチルヘプタンジオナト))チタン(Ti(OiPr)2(THD)2)、ジイソプロポキソビス(tert−ブチルアセトアセタト)チタン(Ti(OiPr)2(tbaoac)2)、ビス(ジメチルアミノエトキソ)ジイソプロポキソチタン(Ti(OiPr)2(dmae)2)、(ジメチルアミノエトキソ)トリイソプロポキソチタンTi(OiPr)3(dmae))などキレート配位子を持つチタン化合物が合成され、CVD法又はALD法の材料として検討されている。(非特許文献1、2、3及び4)。
【0007】
さらに、アミド配位子を有するチタン化合物もCVD法やALD法による薄膜形成材料として検討されている。例えば、テトラキス(ジメチルアミド)チタン(Ti(NMe2)4)を材料に用いたCVD法やALD法によって窒化チタン薄膜や酸化チタン薄膜などの形成が検討されている。(例えば非特許文献5及び6)。キレート配位子を有するアミドチタン錯体も薄膜形成用材料として検討されている。例えば特許文献1に記載されているチタン錯体を挙げることが出来る。
【0008】
また、エテン−1,2−ジイルジアミド配位子を有している点で本発明のチタン錯体と類似の構造を持つアリールオキソ錯体が知られている。(非特許文献7)
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開2007−153872号公報
【非特許文献】
【0010】
【非特許文献1】International Journal of Photoenergy、5巻、99ページ、(2003年)
【非特許文献2】Journal of Materials Chemistry、14巻、3231ページ、(2004年)
【非特許文献3】Bulletin of the Korean Chemical Society、25巻、475ページ、(2004年)
【非特許文献4】Journal of Materials Chemistry、8巻、1773ページ、(1998年)
【非特許文献5】Journal of Vacuum Science & Technology B、24巻、1535ページ、(2006年)
【非特許文献6】Journal of The Electrochemical Society、152巻、G29ページ(2005年)
【非特許文献7】Journal of The American Chemical Society、109巻、6068ページ(1987年)
【発明の概要】
【発明が解決しようとする課題】
【0011】
TiCl4には、成膜するために高い温度が必要とされる点や、それを用いて形成された薄膜の中に塩素が混入する点などの問題がある。Ti(OiPr)4は水との反応性が極めて高く、成膜に使用するキャリアガスや反応ガス中などに含まれる微量水分と容易に反応する。その結果として装置内の配管内部に形成された酸化チタンの微粉が装置を閉塞させて生産性を低下させる恐れがある。また、非特許文献1、2、3及び4に記載のキレート配位チタン錯体は蒸気圧が低いという欠点を有している。さらに、Ti(NMe2)4は、水に対して極度に反応性が高く、成膜に使用するキャリアガス、反応ガス中などに含まれる微量水分と反応し、Ti(OiPr)4の場合と同様に装置を閉塞させて生産性を低下させる恐れがある。
【0012】
非特許文献7に記載のアリールオキソ錯体は、複数の嵩高いアリール基を有する点で本発明のチタン錯体とは異なる。また、非特許文献7に記載されているアリールオキソ錯体の合成方法は、本発明の製造方法とは異なる。さらに、非特許文献7にはアリールオキソ錯体のチタン含有薄膜の材料としての使用に関する記述は一切無い。
特許文献1に記載されているチタン錯体は、CVD法またはALD法の材料として適した熱安定性と蒸気圧を併せ持っているが、近年、これらよりもさらに熱安定性が高い材料の開発が望まれている。
【0013】
本発明の目的は、高い蒸気圧及び高い熱安定性を持ち、CVD法又はALD法などの手法によってチタン含有薄膜を製造するための優れた材料となる新規なチタン錯体、それら錯体の製造方法、それら錯体を用いて作製したチタン含有薄膜及びそれら薄膜の製法を提供することである。
【課題を解決するための手段】
【0014】
本発明者らは上述の現状に鑑み、鋭意検討を重ねた結果、一般式(1)で表されるチタン錯体が上記課題を解決できる優れた化合物であることを見出し、本発明を完成するに至った。
【0015】
すなわち本発明は、一般式(1)
【0016】
【化1】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体である。
【0017】
また本発明は、一般式(2)
【0018】
【化2】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。)で表されるジイミン、アルカリ金属及び一般式(3)
【0019】
【化3】

(式中、R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるアルコキソ錯体を反応させることを特徴とする一般式(1)で表されるチタン錯体の製造方法である。
【0020】
さらに本発明は、一般式(4)
【0021】
【化4】

(式中、R1a及びR4aは各々独立に炭素数1から6のアルキル基を示す。R2a及びR3aは各々独立に水素原子又は炭素数1から3のアルキル基を示す。R7及びR8は各々独立にフッ素原子で置換されていても良い炭素数1から4のアルキル基を示す。)で表されるアミド錯体に、一般式(5)
【0022】
【化5】

(式中、R5aはフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるアルコールを反応させることを特徴とする一般式(1a)
【0023】
【化6】

(式中、R1a及びR4aは各々独立に炭素数1から6のアルキル基を示す。R2a及びR3aは各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5aはフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体の製造方法である。
【0024】
また本発明は、一般式(1)で表されるチタン錯体を材料として用いることにより製造されるチタン含有薄膜である。
【0025】
さらに本発明は、一般式(1)で表されるチタン錯体を材料として用いることを特徴とするチタン含有薄膜の製法である。
【0026】
また本発明は、上述のチタン含有薄膜を用いることを特徴とする半導体デバイスである。
【0027】
さらに本発明は、上述のチタン含有薄膜を用いることを特徴とする光触媒である。以下に本発明を更に詳細に説明する。
【0028】
R1及びR4で表される炭素数1から16のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基、ヘプチル基、シクロヘキシルメチル基、1,1−ジエチルプロピル基、2−メチルシクロヘキシル基、4−メチルシクロヘキシル基、オクチル基、1,1−ジエチル−2−メチルプロピル基、2,5−ジメチルシクロヘキシル基、3,5−ジメチルシクロヘキシル基、1,1,3,3−テトラメチルブチル基、1−メチル−1−プロピルブチル基、1,1,2,3,3−ペンタメチルブチル基、1,1−ジエチル−3,3−ジメチルブチル基、アダマンチル基、1,1−ジメチルオクチル基、1,1−ジプロピルブチル基、1,1−ジメチルデシル基、1,1−ジエチルオクチル基、1,1−ジブチルペンチル基、1,1−ジブチルヘキシル基、1,1−ジブチルヘプチル基又は1,1−ジペンチルヘキシル基などを例示することができる。
【0029】
R2及びR3で表される炭素数1から3のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基又はシクロプロピル基を例示することができる。
【0030】
R5で表される炭素数1から16のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基、ヘプチル基、シクロヘキシルメチル基、1,1−ジエチルプロピル基、2−メチルシクロヘキシル基、4−メチルシクロヘキシル基、オクチル基、1,1−ジエチル−2−メチルプロピル基、2,5−ジメチルシクロヘキシル基、3,5−ジメチルシクロヘキシル基、1,1,3,3−テトラメチルブチル基、1−メチル−1−プロピルブチル基、1,1,2,3,3−ペンタメチルブチル基、1,1−ジエチル−3,3−ジメチルブチル基、アダマンチル基、1,1−ジメチルオクチル基、1,1−ジプロピルブチル基、1,1−ジメチルデシル基、1,1−ジエチルオクチル基、1,1−ジブチルペンチル基、1,1−ジブチルヘキシル基、1,1−ジブチルヘプチル基又は1,1−ジペンチルヘキシル基などを例示することができる。
【0031】
これらのアルキル基はフッ素原子で置換されていても良く、例えばトリフルオロメチル基、2,2,2−トリフルオロエチル基、ペルフルオロエチル基、ペルフルオロプロピル基、ペルフルオロイソプロピル基、ペルフルオロブチル基、ペルフルオロ−sec−ブチル基、ペルフルオロ−tert−ブチル基、ペルフルオロヘキシル基、ペルフルオロヘプチル基、ペルフルオロオクチル基、ペルフルオロノニル基、ペルフルオロデシル基、ペルフルオロウンデシル基、ペルフルオロドデシル基、ペルフルオロトリデシル基、ペルフルオロテトラデシル基、ペルフルオロペンタデシル基又はペルフルオロヘキサデシル基などを例示することができる。
【0032】
良好な蒸気圧と優れた熱安定性を持つという点で、チタン錯体(1)におけるR1及びR4は各々独立に炭素数2から6のアルキル基が好ましく、例えばエチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基が好ましい。R1及びR4は各々独立に炭素数4又は5のアルキル基がさらに好ましく、例えばブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基又は1−エチルプロピル基が更に好ましい。
【0033】
また、R2及びR3は水素原子が好ましい。
【0034】
また、R5は炭素数1から8のアルキル基が好ましく、例えばメチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基、ヘプチル基、シクロヘキシルメチル基、1,1−ジエチルプロピル基、2−メチルシクロヘキシル基、4−メチルシクロヘキシル基、オクチル基、1,1−ジエチル−2−メチルプロピル基、2,5−ジメチルシクロヘキシル基、3,5−ジメチルシクロヘキシル基、1,1,3,3−テトラメチルブチル基又は1−メチル−1−プロピルブチル基が好ましい。R5は炭素数3から5のアルキル基がさらに好ましく、例えばプロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基又は1−エチルプロピル基が更に好ましい。
【0035】
一般式(1)で表されるチタン錯体としては、良好な蒸気圧と優れた熱安定性を持つという点でエテン−1,2−ジイルビス(イソプロピルアミド)ビス(tert−ペンチルオキソ)チタン(Ti(iPrNCHCHNiPr)(OtPe)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ジエトキソチタン(Ti(tBuNCHCHNtBu)(OEt)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ジイソプロポキソチタン(Ti(tBuNCHCHNtBu)(OiPr)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(tert−ペンチルオキソ)チタン(Ti(tBuNCHCHNtBu)(OtPe)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(1,1−ジエチルプロピルオキソ)チタン(Ti(tBuNCHCHNtBu)(OCEt3)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(1,1−ジエチル−2−メチルプロピルオキソ)チタン(Ti(tBuNCHCHNtBu)(OCEt2CHMe2)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(2,2,2−トリフルオロエトキソ)チタン(Ti(tBuNCHCHNtBu)(OCH2CF3)2)、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジメトキソチタン(Ti(tPeNCHCHNtPe)(OMe)2)、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジエトキソチタン(Ti(tPeNCHCHNtPe)(OEt)2)、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジイソプロポキソチタン(Ti(tPeNCHCHNtPe)(OiPr)2)、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジ(tert−ブトキソ)チタン(Ti(tPeNCHCHNtPe)(OtBu)2)、またはエテン−1,2−ジイルビス(1,1,3,3−テトラメチルブチルアミド)ジイソプロポキソチタン(Ti(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2)が好ましい。更に好ましくは、エテン−1,2−ジイルビス(tert−ブチルアミド)ジイソプロポキソチタン(Ti(tBuNCHCHNtBu)(OiPr)2)、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(tert−ペンチルオキソ)チタン(Ti(tBuNCHCHNtBu)(OtPe)2)又はエテン−1,2−ジイルビス(tert−ペンチルアミド)ジイソプロポキソチタン(Ti(tPeNCHCHNtPe)(OiPr)2)を挙げることが出来る。
【0036】
次に本発明の製造方法について説明する。製法1はジイミン(2)にアルカリ金属及びアルコキソ錯体(3)を有機溶媒中で反応させることにより、本発明のチタン錯体(1)を製造する方法である。
【0037】
原料であるジイミン(2)は、既知の方法(例えばJournal of the American Chemical Society、120巻、12714ページ、(1998年))を参考にして合成することが出来る。アルコキソ錯体(3)は、市販の試薬又は工業原料として入手することが出来るほか、Journal of the American Chemical Society、46巻、256ページ、(1924年)、Inorganica Chimica Acta、52巻、79ページ、(1981年)、及びAlkoxo and Aryloxo Derivatives of Metals、Academic Press、(2001年)を参考にして合成することが出来る。
【0038】
ジイミン(2)とアルカリ金属を反応させることにより、ジイミンのアルカリ金属錯体が生成することが知られている(例えば例えばJournal of the American Chemical Society、120巻、12714ページ、(1998年))。本発明の製法1では、ジイミン(2)、アルカリ金属及びアルコキソ錯体(3)を反応させる順序に制限はなく、例えば別途に調製して単離したジイミンのアルカリ金属錯体にアルコキソ錯体(3)を反応させても良い。工程が少なくチタン錯体(1)の収率が良い点で、最初にジイミン(2)にアルカリ金属を反応させ、続いてアルコキソ錯体(3)を反応させるのが好ましい。
【0039】
製法1で用いるアルカリ金属の種類は、チタン錯体(1)の収率が良い点で、リチウム又はナトリウムが好ましい。用いるアルカリ金属の量は、チタン錯体(1)の収率が良い点で、ジイミンに対して2当量以上用いるのが好ましい。製法1で用いる有機溶媒は、アルカリ金属、ジイミン(2)、アルコキソ錯体(3)又はジイミン(2)のアルカリ金属錯体と反応しないものであれば良い。例えばペンタン、ヘキサン、ヘプタン、オクタン、シクロヘキサン、メチルシクロヘキサン、エチルシクロヘキサンなどのアルカン類、ベンゼン、トルエン、キシレンなどの芳香族炭化水素類、ジエチルエーテル、ジイソプロピルエーテル、ジブチルエーテル、テトラヒドロフラン、ジオキサン、エチレングリコールジメチルエーテル、ジグライム、トリグライム、シクロペンチルメチルエーテルなどのエーテル類などを挙げることが出来る。これらを単独で用いることも混合して用いることも出来る。
【0040】
製法1によって得られた本発明のチタン錯体(1)は、ろ過、抽出、蒸留、昇華、結晶化など一般的な錯体の精製方法を適宜選んで用いることにより単離することが出来る。
【0041】
製法2はアミド錯体(4)にアルコール(5)を有機溶媒中で反応させることにより、チタン錯体(1a)を製造する方法である。
【0042】
本発明において、R1a及びR4aで表される炭素数1から6のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基などを例示することができる。
【0043】
またR2a及びR3aで表される炭素数1から3のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基又はシクロプロピル基を例示することができる。
【0044】
R5aで表される炭素数1から16のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基、ヘプチル基、シクロヘキシルメチル基、1,1−ジエチルプロピル基、2−メチルシクロヘキシル基、4−メチルシクロヘキシル基、オクチル基、1,1−ジエチル−2−メチルプロピル基、2,5−ジメチルシクロヘキシル基、3,5−ジメチルシクロヘキシル基、1,1,3,3−テトラメチルブチル基、1−メチル−1−プロピルブチル基、1,1,2,3,3−ペンタメチルブチル基、1,1−ジエチル−3,3−ジメチルブチル基、アダマンチル基、1,1−ジメチルオクチル基、1,1−ジプロピルブチル基、1,1−ジメチルデシル基、1,1−ジエチルオクチル基、1,1−ジブチルペンチル基、1,1−ジブチルヘキシル基、1,1−ジブチルヘプチル基又は1,1−ジペンチルヘキシル基などを例示することができる。
【0045】
これらのアルキル基はフッ素原子で置換されていても良く、例えばトリフルオロメチル基、2,2,2−トリフルオロエチル基、ペルフルオロエチル基、ペルフルオロプロピル基、ペルフルオロイソプロピル基、ペルフルオロブチル基、ペルフルオロ−sec−ブチル基、ペルフルオロ−tert−ブチル基、ペルフルオロヘキシル基、ペルフルオロヘプチル基、ペルフルオロオクチル基、ペルフルオロノニル基、ペルフルオロデシル基、ペルフルオロウンデシル基、ペルフルオロドデシル基、ペルフルオロトリデシル基、ペルフルオロテトラデシル基、ペルフルオロペンタデシル基又はペルフルオロヘキサデシル基などを例示することができる。
【0046】
R7及びR8で表される炭素数1から4のアルキル基としては、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基などを例示することができる。これらのアルキル基はフッ素原子で置換されていても良く、例えばトリフルオロメチル基、2,2,2−トリフルオロエチル基、ペルフルオロエチル基、ペルフルオロプロピル基、ペルフルオロイソプロピル基、ペルフルオロブチル基、ペルフルオロ−sec−ブチル基、ペルフルオロ−tert−ブチル基等を例示することができる。
【0047】
これらの中でも、R1a及びR4aは炭素数2から6のアルキル基が好ましい。さらに好ましくは炭素数4または5のアルキル基であり、例えばブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基又は1−エチルプロピル基等が例示される。
【0048】
またR2a及びR3aは水素原子が好ましい。
【0049】
またR5aは炭素数1から8のアルキル基が好ましく、例えばメチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基、1−エチルプロピル基、ヘキシル基、イソヘキシル基、1−メチルペンチル基、2−メチルペンチル基、3−メチルペンチル基、1,1−ジメチルブチル基、1,2−ジメチルブチル基、2,2−ジメチルブチル基、1,3−ジメチルブチル基、2,3−ジメチルブチル基、3,3−ジメチルブチル基、1−エチルブチル基、2−エチルブチル基、1,1,2−トリメチルプロピル基、1,2,2−トリメチルプロピル基、1−エチル−1−メチルプロピル基、1−エチル−2−メチルプロピル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロプロピルメチル基、シクロプロピルエチル基、シクロブチルメチル基、ヘプチル基、シクロヘキシルメチル基、1,1−ジエチルプロピル基、2−メチルシクロヘキシル基、4−メチルシクロヘキシル基、オクチル基、1,1−ジエチル−2−メチルプロピル基、2,5−ジメチルシクロヘキシル基、3,5−ジメチルシクロヘキシル基、1,1,3,3−テトラメチルブチル基又は1−メチル−1−プロピルブチル基が好ましい。R5aは炭素数3から5のアルキル基がさらに好ましく、例えばプロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルブチル基、2−メチルブチル基、1,2−ジメチルプロピル基又は1−エチルプロピル基が更に好ましい。
【0050】
R7及びR8はメチル基またはエチル基が好ましく、メチル基がさらに好ましい。
【0051】
原料であるアミド錯体(4)は、既知の方法(特許文献1)を参考にして合成することが出来る。
【0052】
製法2で用いる有機溶媒は、アミド錯体(4)及びアルコール(5)と反応しないものであれば良い。例えばペンタン、ヘキサン、ヘプタン、オクタン、シクロヘキサン、メチルシクロヘキサン、エチルシクロヘキサンなどのアルカン類、ベンゼン、トルエン、キシレンなどの芳香族炭化水素類、ジエチルエーテル、ジイソプロピルエーテル、ジブチルエーテル、テトラヒドロフラン、ジオキサン、エチレングリコールジメチルエーテル、ジグライム、トリグライム、シクロペンチルメチルエーテルなどのエーテル類などを挙げることが出来る。これらを単独で用いることも混合して用いることも出来る。
【0053】
製法2によってチタン錯体(1a)を収率良く得るためには、アミド錯体(4)をあらかじめ有機溶媒に溶かした溶液にアルコール(5)を加えるのが好ましい。
【0054】
製法2では、チタン錯体(1a)の収率が良い点で、アミド錯体(4)に対して1.6から2.4当量のアルコール(5)を反応させるのが好ましく、アミド錯体(4)に対して2.0当量のアルコール(5)を作用させるのがさらに好ましい。
【0055】
製法2によって得られたチタン錯体(1a)は、蒸留、昇華、結晶化など一般的な錯体の精製方法を適宜選んで用いることにより単離することが出来る。
【0056】
本発明のチタン錯体(1)を材料に用いて、チタン含有薄膜を製造することが出来る。製造することが出来る薄膜としては、酸化チタン、窒化チタン及び炭化チタンなどの薄膜並びにチタン酸ストロンチウム、チタン酸バリウムなどチタンと他の金属を含む複合金属化合物の薄膜を例示することが出来る。チタン錯体(1)は分子内に酸素原子を含むため、酸化チタン又は複合酸化物の薄膜製造の材料に用いるのに適している。チタン含有薄膜の製造方法としては特に制限はないが、CVD法、ALD法、インクジェット法、スピンコート法、ディップコート法または溶液法などを例示することができる。CVD法又はALD法により薄膜を製造する場合、チタン錯体(1)を気化させ、気体として反応室に供給する。チタン錯体(1)を気化させる方法としては、例えばバブリング法やリキッドインジェクション法などを挙げることが出来る。バブリング法とは、一定の温度に温めた容器に納めたチタン錯体(1)の中に、ヘリウム、ネオン、アルゴン、クリプトン、キセノン又は窒素などのキャリアガスを吹き込むことによってチタン錯体(1)を気化させる方法である。リキッドインジェクション法とは、チタン錯体(1)を液体の状態で気化器に送りこみ、気化器内で加熱することによってチタン錯体(1)を気化させる方法である。リキッドインジェクション法では、チタン錯体(1)を溶媒に溶かして溶液として用いることが出来る。チタン錯体(1)を溶液として用いる場合の溶媒としては、1,2−ジメトキシエタン、ジグライム、トリグライム、ジオキサン、テトラヒドロフラン、シクロペンチルメチルエーテルなどのエーテル類、ヘキサン、シクロヘキサン、メチルシクロヘキサン、エチルシクロヘキサン、ヘプタン、オクタン、ノナン、デカンなどのアルカン類、ベンゼン、トルエン、エチルベンゼン、キシレン等の芳香族炭化水素類を例示することが出来る。これらの溶媒を単独で又は混合して用いることが出来る。
【0057】
気体として反応室に供給したチタン錯体(1)を分解することにより、基板上にチタン含有薄膜を形成することが出来る。チタン錯体(1)を分解する方法としては、熱による方法、プラズマや光などを使用する方法、反応室内に水、酸素、オゾン、過酸化水素、水素、アンモニアなどの反応ガスを送り込んで化学反応を起こさせる方法を挙げることが出来る。これらの方法を単独で又は併せて用いることによってチタン錯体(1)を分解し、チタン含有薄膜を形成することが出来る。
【0058】
本発明のチタン含有薄膜は、DRAM、SRAM、FeRAM、ReRAM、MRAM、PRAM、フラッシュメモリー等の半導体デバイスの構成素子や光触媒として使用することができる。
【発明の効果】
【0059】
本発明のチタン錯体(1)は、良好な気化特性及び優れた熱安定性を持ち、即ち高い蒸気圧及び高い熱安定性を持ち、これを材料として用いたCVD法又はALD法などの手法によってチタン含有薄膜を製造することが可能である。
【図面の簡単な説明】
【0060】
【図1】試験例1のTG及びDSC測定結果を示す図である。
【図2】試験例2のTG及びDSC測定結果を示す図である。
【図3】試験例3のTG及びDSC測定結果を示す図である。
【図4】試験例4のTG及びDSC測定結果を示す図である。
【図5】試験例5のTG及びDSC測定結果を示す図である。
【図6】試験例6のTG及びDSC測定結果を示す図である。
【図7】試験例7のTG及びDSC測定結果を示す図である。
【図8】試験例8のTG及びDSC測定結果を示す図である。
【図9】試験例9のTG及びDSC測定結果を示す図である。
【図10】試験例10のTG及びDSC測定結果を示す図である。
【図11】試験例11のTG及びDSC測定結果を示す図である。
【図12】試験例12のTG及びDSC測定結果を示す図である。
【図13】実施例16及び17で用いたCVD成膜装置の概略図である。
【図14】試験例13のTG及びDSC測定結果を示す図である。
【図15】実施例20、21、22及び23で用いたCVD成膜装置の概略図である。
【実施例】
【0061】
以下、本発明を実施例によりさらに詳細に説明する。ただし、本発明はこれら実施例に限定されるものではない。
【0062】
(実施例1)
アルゴン雰囲気下で、N,N’−ジイソプロピル−1,4−ジアザ−1,3−ブタジエン(iPrNCHCHNiPr)1.38g(9.83mmol)をヘキサン12mLとテトラヒドロフラン2mLの混合液に溶かし、リチウム143mg(20.6mmol)を加えて室温で12時間撹拌した。その反応液にテトラキス(tert−ペンチルオキソ)チタン(Ti(OtPe)4)3.90g(9.83mmol)をヘキサン10mLに溶かした溶液を加え、室温で14時間撹拌した。その反応液にさらにクロロトリメチルシラン2.14g(19.7mmol)を加えて室温で6時間撹拌した。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度95℃/0.07Torr)することにより、エテン−1,2−ジイルビス(イソプロピルアミド)ビス(tert−ペンチルオキソ)チタン(Ti(iPrNCHCHNiPr)(OtPe)2)を濃赤色の液体として得た(収量3.29g、収率92%)。
【0063】
(1H NMR(500MHz,C6D6,δ/ppm)
5.78(s,2H),3.55(sept,J=6Hz,2H),1.59(q,J=8Hz,4H),1.33(s,12H),1.25(br,12H),1.04(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
106.0,82.8,81.6(br),56.8,38.2,37.8,26.1,9.55,9.48。
【0064】
(試験例1)Ti(iPrNCHCHNiPr)(OtPe)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(iPrNCHCHNiPr)(OtPe)2のTG(熱重量測定)の結果及び密閉容器中で昇温速度10℃/minで測定したTi(iPrNCHCHNiPr)(OtPe)2のDSC(示差走査熱量測定)の結果を図1に示した。TGの結果からTi(iPrNCHCHNiPr)(OtPe)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(iPrNCHCHNiPr)(OtPe)2の熱安定性が良好なことが明らかである。
【0065】
(実施例2)
アルゴン雰囲気下で、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(ジメチルアミド)チタン(Ti(tBuNCHCHNtBu)(NMe2)2)2.01g(6.62mmol)をヘキサン8mLに溶かし、エタノール610mg(13.2mmol)を加えて室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度85℃/0.05Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ジエトキソチタン(Ti(tBuNCHCHNtBu)(OEt)2)を濃赤色の液体として得た(収量1.88g、収率93%)。
【0066】
1H NMR(500MHz,C6D6,δ/ppm)
5.98(s,2H),4.20(br,4H),1.29(s,18H),1.16−1.32(br,6H)
13C NMR(125MHz,C6D6,δ/ppm)
102.4,68−70(br),58.0,31.6,21.2。
【0067】
(試験例2)Ti(tBuNCHCHNtBu)(OEt)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OEt)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OEt)2のDSCの結果を図2に示した。TGの結果からTi(tBuNCHCHNtBu)(OEt)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OEt)2の熱安定性が良好なことが明らかである。
【0068】
(実施例3)
アルゴン雰囲気下で、N,N’−ジ(tert−ブチル)−1,4−ジアザ−1,3−ブタジエン(tBuNCHCHNtBu)2.22g(13.2mmol)をテトラヒドロフラン20mLに溶かし、ナトリウム606mg(26.4mmol)を加えて室温で12時間撹拌した。その反応液にテトライソプロポキソチタン(Ti(OiPr)4)3.56g(12.5mmol)をヘキサン10mLに溶かした溶液を加え、室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、残渣にヘキサン20mLを加えた。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度85℃/0.05Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ジイソプロポキソチタン(Ti(tBuNCHCHNtBu)(OiPr)2)を濃赤色の液体として得た(収量3.91g、収率93%)。
【0069】
1H NMR(500MHz,C6D6,δ/ppm)
5.96(s,2H),4.0−5.0(br,2H),1.30(s,18H),1.1−1.3(br,12H)
13C NMR(125MHz,C6D6,δ/ppm)
102.7,74.5(br),57.6,31.7,27.8。
【0070】
(試験例3)Ti(tBuNCHCHNtBu)(OiPr)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OiPr)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OiPr)2のDSCの結果を図3に示した。TGの結果からTi(tBuNCHCHNtBu)(OiPr)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OiPr)2の熱安定性が良好なことが明らかである。
【0071】
(実施例4)
アルゴン雰囲気下で、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(ジメチルアミド)チタン(Ti(tBuNCHCHNtBu)(NMe2)2)6.01g(19.7mmol)をトルエン20mLに溶かし、2−プロパノール2.37g(39.4mmol)を加えて室温で2時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度85℃/0.05Torr)することにより、Ti(tBuNCHCHNtBu)(OiPr)2を濃赤色の液体として得た(収量6.21g、収率94%)。このようにして得たTi(tBuNCHCHNtBu)(OiPr)2の1H及び13C NMRスペクトルを測定したところ、これらのスペクトルは実施例3で得たもののスペクトルと一致した。
【0072】
(実施例5)
アルゴン雰囲気下で、Ti(tBuNCHCHNtBu)(NMe2)21.76g(5.78mmol)をヘキサン7mLに溶かし、tert−ペンチルアルコール1.02g(11.6mmol)を加えて室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度97℃/0.05Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(tert−ペンチルオキソ)チタン(Ti(tBuNCHCHNtBu)(OtPe)2)を濃赤色の液体として得た(収量2.11g、収率93%)。
【0073】
1H NMR(500MHz,C6D6,δ/ppm)
5.93(s、2H),1.55(br、4H),1.30(s,18H),1.1−1.4(br,12H),0.99(br,6H)
13C NMR(125MHz,C6D6,δ/ppm)
103.1,81.4(br),57.4,38.3,31.9,31.1,9.8。
【0074】
(試験例4)Ti(tBuNCHCHNtBu)(OtPe)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OtPe)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OtPe)2のDSCの結果を図4に示した。TGの結果からTi(tBuNCHCHNtBu)(OtPe)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OtPe)2の熱安定性が良好なことが明らかである。
【0075】
(実施例6)
アルゴン雰囲気下で、Ti(tBuNCHCHNtBu)(NMe2)22.61g(8.58mmol)をヘキサン10mLに溶かし、3−エチル−3−ペンタノール2.00g(17.2mmol)を加えて室温で14時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度112℃/0.03Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(1,1−ジエチルプロピルオキソ)チタン(Ti(tBuNCHCHNtBu)(OCEt3)2)を濃赤色の液体として得た(収量1.93g、収率50%)。
【0076】
1H NMR(500MHz,C6D6,δ/ppm)
5.95(s,2H),1.55(br,12H),1.33(s,18H),0.96(br,18H)
13C NMR(125MHz,C6D6,δ/ppm)
103.0,86.0(br),57.5,32.3,31.5,8.8。
【0077】
(試験例5)Ti(tBuNCHCHNtBu)(OCEt3)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OCEt3)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OCEt3)2のDSCの結果を図5に示した。TGの結果からTi(tBuNCHCHNtBu)(OCEt3)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OCEt3)2の熱安定性が良好なことが明らかである。
【0078】
(実施例7)
アルゴン雰囲気下で、Ti(tBuNCHCHNtBu)(NMe2)23.09g(10.2mmol)をヘキサン10mLに溶かし、1,1−ジエチル−2−メチルプロピルアルコール2.64g(20.3mol)を加えて室温で4.5時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(油浴温度190℃/0.06Torr)することによりエテン−1,2−ジイルビス(tert−ブチルアミド)ビス(1,1−ジエチル−2−メチルプロピルオキソ)チタン(Ti(tBuNCHCHNtBu)(OCEt2CHMe2)2)を濃赤色の固体として得た(収量3.35g、収率69%)。
【0079】
1H NMR(500MHz,C6D6,δ/ppm)
5.97(s,2H),1.61(br,10H),1.34(s,18H),1.00(br,24H)
13C NMR(125MHz,C6D6,δ/ppm)
103.2,88.1(br),57.9,34.8,31.5,29.5,17.8,8.7。
【0080】
(試験例6)Ti(tBuNCHCHNtBu)(OCEt2CHMe2)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OCEt2CHMe2)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OCEt2CHMe2)2のDSCの結果を図6に示した。TGの結果からTi(tBuNCHCHNtBu)(OCEt2CHMe2)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OCEt2CHMe2)2の熱安定性が良好なことが明らかである。
【0081】
(実施例8)
アルゴン雰囲気下で、Ti(tBuNCHCHNtBu)(NMe2)24.11g(13.5mmol)をヘキサン20mLに溶かし、2,2,2−トリフルオロエタノール2.70g(27.0mmol)を加えて室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度90℃/0.10Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(2,2,2−トリフルオロエトキソ)チタン(Ti(tBuNCHCHNtBu)(OCH2CF3)2)を濃赤色の液体として得た(収量4.94g、収率88%)。
【0082】
1H NMR(500MHz,C6D6,δ/ppm)
5.90(s,2H),4.4(br,2H),3.8(br,2H),1.14(s,18H)
13C NMR(125MHz,C6D6,δ/ppm)
125.3(q,J=279Hz),101.4,70−72(br),68−70(br),59.7,31.0
19F NMR(470MHz,C6D6,δ/ppm)
−78.5(br),−79.2(br)。
【0083】
(試験例7)Ti(tBuNCHCHNtBu)(OCH2CF3)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OCH2CF3)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OCH2CF3)2のDSCの結果を図7に示した。TGの結果からTi(tBuNCHCHNtBu)(OCH2CF3)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OCH2CF3)2の熱安定性が良好なことが明らかである。
【0084】
(参考例1)
アルゴン雰囲気下で、N,N’−ジ(tert−ペンチル)−1,4−ジアザ−1,3−ブタジエン(tPeNCHCHNtPe)5.31g(27.0mmol)をテトラヒドロフラン50mLに溶かした溶液にリチウム379mg(54.6mmol)を加え、室温で14時間撹拌した。残ったリチウムをろ別し、ろ液から溶媒を減圧留去した。残った黄色固体をヘキサン30mLに懸濁させ、テトラキス(ジメチルアミド)チタン(Ti(NMe2)4)5.77g(25.7mmol)をヘキサン10mLに溶かした溶液を加えた。50℃で4時間攪拌した後、室温まで冷却し、不溶物をろ別した。ろ液から溶媒を減圧留去し、得られた残渣を減圧蒸留することにより、エテン−1,2−ジイルビス(tert−ペンチルアミド)ビス(ジメチルアミド)チタン(Ti(tPeNCHCHNtPe)(NMe2)2)を濃赤色の液体として得た(収量7.83g、収率91%)。
【0085】
1H NMR(500MHz,C6D6,δ/ppm)
5.77(s、2H),3.04(br,6H),1.51(q,J=8Hz,4H),1.24(s,12H),0.77(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
101.6,60.9,43.4,36.4,28.5,8.9。
【0086】
(実施例9)
アルゴン雰囲気下で、Ti(tPeNCHCHNtPe)(NMe2)23.43g(10.3mmol)をヘキサン15mLに溶かし、メタノール661mg(20.6mmol)を加えて室温で14時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度106℃/0.10Torr)することにより、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジメトキソチタン(Ti(tPeNCHCHNtPe)(OMe)2)を濃赤色の粘性液体として得た(収量2.92g、収率92%)。
【0087】
1H NMR(500MHz,C6D6,δ/ppm)
6.02(s,2H),3.99(br,6H),1.54(q,J=8Hz,4H),1.27(s,12H),0.78(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
103.0,61.4,61.2(br),37.0,28.5,9.3。
【0088】
(試験例8)Ti(tPeNCHCHNtPe)(OMe)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tPeNCHCHNtPe)(OMe)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tPeNCHCHNtPe)(OMe)2のDSCの結果を図8に示した。TGの結果からTi(tPeNCHCHNtPe)(OMe)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tPeNCHCHNtPe)(OMe)2の熱安定性が良好なことが明らかである。
【0089】
(実施例10)
アルゴン雰囲気下で、Ti(tPeNCHCHNtPe)(NMe2)22.21g(6.65mmol)をヘキサン10mLに溶かし、エタノール613mg(13.3mmol)を加えて室温で8時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度100℃/0.05Torr)することにより、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジエトキソチタン(Ti(tPeNCHCHNtPe)(OEt)2)を濃赤色の液体として得た(収量2.16g、収率97%)。
【0090】
1H NMR(500MHz,C6D6,δ/ppm)
5.91(s,2H),3.4−4.8(br,4H),1.55(q,J=8Hz,4H),1.25(12H),1.1−1.5(br,6H),0.80(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
102.3,71.0(br),60.7,36.6,29.1(br),21.1,9.2。
【0091】
(試験例9)Ti(tPeNCHCHNtPe)(OEt)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tPeNCHCHNtPe)(OEt)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tPeNCHCHNtPe)(OEt)2のDSCの結果を図9に示した。TGの結果からTi(tPeNCHCHNtPe)(OEt)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tPeNCHCHNtPe)(OEt)2の熱安定性が良好なことが明らかである。
【0092】
(実施例11)
アルゴン雰囲気下で、N,N’−ジ(tert−ペンチル)−1,4−ジアザ−1,3−ブタジエン(tPeNCHCHNtPe)3.09g(15.7mmol)をテトラヒドロフラン30mLに溶かし、ナトリウム758mg(33.0mmol)を加えて室温で12時間撹拌した。その反応液にテトライソプロポキソチタン(Ti(OiPr)4)4.25g(15.0mmol)をヘキサン10mLに溶かした溶液を加え、室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、残渣にヘキサン30mLを加えた。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度92℃/0.05Torr)することにより、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジイソプロポキソチタン(Ti(tPeNCHCHNtPe)(OiPr)2)を濃赤色の液体として得た(収量4.96g、収率92%)。
【0093】
1H NMR(500MHz,C6D6,δ/ppm)
5.90(s,2H),3.7−5.2(br,2H),1.56(q,J=8Hz,4H),1.26(s,12H),0.9−1.6(br,12H),0.81(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
102.6,74.4(br),60.3,36.8,29.2(br),27.8,9.3。
【0094】
(試験例10)Ti(tPeNCHCHNtPe)(OiPr)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tPeNCHCHNtPe)(OiPr)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tPeNCHCHNtPe)(OiPr)2のDSCの結果を図10に示した。TGの結果からTi(tPeNCHCHNtPe)(OiPr)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tPeNCHCHNtPe)(OiPr)2の熱安定性が良好なことが明らかである。
【0095】
(実施例12)
アルゴン雰囲気下で、エテン−1,2−ジイルビス(tert−ペンチルアミド)ビス(ジメチルアミド)チタン(Ti(tPeNCHCHNtPe)(NMe2)2)1.90g(5.71mmol)をヘキサン10mLに溶かし、2−プロパノール687mg(11.4mmol)を加えて室温で3時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度95℃/0.06Torr)することによりTi(tPeNCHCHNtPe)(OiPr)2を濃赤色の液体として得た(収量2.00g、収率96%)。このようにして得たTi(tPeNCHCHNtPe)(OiPr)2の1H及び13C NMRスペクトルを測定したところ、これらのスペクトルは実施例11で得たもののスペクトルと一致した。
【0096】
(実施例13)
アルゴン雰囲気下で、N,N’−ジ(tert−ペンチル)−1,4−ジアザ−1,3−ブタジエン(tPeNCHCHNtPe)2.38g(12.1mmol)をテトラヒドロフラン24mLに溶かし、ナトリウム584mg(25.4mmol)を加えて室温で12時間撹拌した。その反応液にテトラ(tert−ブトキソ)チタン(Ti(OtBu)4)3.93g(11.5mmol)をヘキサン12mLに溶かした溶液を加え、室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、残渣にヘキサン25mLを加えた。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度105℃/0.10Torr)することにより、エテン−1,2−ジイルビス(tert−ペンチルアミド)ジ(tert−ブトキソ)チタン(Ti(tPeNCHCHNtPe)(OtBu)2)を濃赤色の液体として得た(収量4.28g、収率95%)。
【0097】
1H NMR(500MHz,C6D6,δ/ppm)
5.87(s,2H),1.58(q,J=8Hz,4H),1.27(s,12H),1.0−1.7(br,18H),0.81(t,J=8Hz,6H)
13C NMR(125MHz,C6D6,δ/ppm)
103.1,79.3(br),60.0,37.0,33.4,29.4(br),9.4。
【0098】
(試験例11)Ti(tPeNCHCHNtPe)(OtBu)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tPeNCHCHNtPe)(OtBu)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(tPeNCHCHNtPe)(OtBu)2のDSCの結果を図11に示した。TGの結果からTi(tPeNCHCHNtPe)(OtBu)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tPeNCHCHNtPe)(OtBu)2の熱安定性が良好なことが明らかである。
【0099】
(実施例14)
アルゴン雰囲気下で、Ti(tPeNCHCHNtPe)(NMe2)21.10g(3.32mmol)をヘキサン5mLに溶かし、tert−ブタノール493mg(6.65mmol)を加えて室温で14時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度105℃/0.10Torr)することにより、Ti(tPeNCHCHNtPe)(OtBu)2を濃赤色の液体として得た(収量1.24g、収率96%)。このようにして得たTi(tPeNCHCHNtPe)(OtBu)2の1H及び13C NMRスペクトルを測定したところ、これらのスペクトルは実施例13で得たもののスペクトルと一致した。
【0100】
(参考例2)
1,1,3,3−テトラメチルブチルアミン19.5g(151mmol)と水100mLの混合液に40%グリオキサル水溶液10.7g(73.5mmol)を加えて室温で1時間撹拌した。生成した固体をろ別し、水10mLで二回洗浄した後、減圧下で乾燥することにより、N,N’−ジ(1,1,3,3−テトラメチルブチル)−1,4−ジアザ−1,3−ブタジエン(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)を白色固体として得た(収量19.5g、収率95%)。
【0101】
1H NMR(500MHz,C6D6,δ/ppm)
8.09(s,2H),1.61(s,4H),1.14(s,12H),0.98(18H)
13C NMR(125MHz,C6D6,δ/ppm)
157.8,62.0,56.6,32.5,32.2,29.8。
【0102】
(実施例15)
アルゴン雰囲気下で、Me3CCH2CMe2NCHCHNCMe2CH2CMe32.98g(10.6mmol)をテトラヒドロフラン30mLに溶かし、ナトリウム538mg(23.4mmol)を加えて室温で16時間撹拌した。その反応液にTi(OiPr)43.02g(10.6mmol)をヘキサン15mLに溶かした溶液を加え、室温で12時間撹拌した。その反応液から溶媒を減圧下で留去し、残渣にヘキサン25mLを加えた。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度130℃/0.04Torr)することにより、エテン−1,2−ジイルビス(1,1,3,3−テトラメチルブチルアミド)ジイソプロポキソチタン(Ti(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2)を濃赤色の液体として得た(収量4.18g、収率88%)。
【0103】
1H NMR(500MHz,C6D6,δ/ppm)
5.93(s,2H),4.83(br,1H),4.11(br,1H),1.62(s,4H),1.2−1.7(br,18H),0.9−1.2(br,6H),0.94(s,18H)
13C NMR(125MHz,C6D6,δ/ppm)
102.3,76.0(br),73.1(br),61.5,56.9,32.1,32.0,31.9(br),27.9。
【0104】
(試験例12)Ti(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2のTGの結果及び密閉容器中で昇温速度10℃/minで測定したTi(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2のDSCの結果を図12に示した。TGの結果からTi(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(Me3CCH2CMe2NCHCHNCMe2CH2CMe3)(OiPr)2の熱安定性が良好なことが明らかである。
【0105】
(実施例16)
恒温槽を用いて61℃に保たれた材料容器内に納められたTi(tBuNCHCHNtBu)(OiPr)2にキャリアガスとしてアルゴンを流量30sccmで吹き込んでTi(tBuNCHCHNtBu)(OiPr)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量180sccmで、反応ガスとして酸素ガスを流量90sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を400℃に保ち、反応室内の圧力が4Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図13に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。また、この薄膜の組成をX線光電子分光法で分析したところ、酸化チタンであることが確認された。
【0106】
(実施例17)
恒温槽を用いて61℃に保たれた材料容器内に納められたTi(tBuNCHCHNtBu)(OiPr)2にキャリアガスとしてアルゴンを流量30sccmで吹き込んでTi(tBuNCHCHNtBu)(OiPr)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量180sccmで、反応ガスとして酸素ガスを流量90sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を240℃に保ち、反応室内の圧力が4Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図13に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。また、この薄膜の組成をX線光電子分光法で分析したところ、酸化チタンであることが確認された。
【0107】
(実施例18)
アルゴン雰囲気下で、Ti(tBuNCHCHNtBu)(NMe2)228.54g(93.8mmol)をヘキサン60mLに溶かし、sec−ブタノール13.90g(187.5mmol)を加えて室温で5時間撹拌した。その反応液から溶媒を減圧下で留去し、得られた残渣を減圧蒸留(留出温度92−96℃/0.03Torr)することにより、エテン−1,2−ジイルビス(tert−ブチルアミド)ビス(sec−ブトキソ)チタン(Ti(tBuNCHCHNtBu)(OsBu)2)を濃赤色の液体として得た(収量32.35g、収率95%)。なお、これはsec−ブチル基のキラリティーの違いに基づく異性体の混合物である。
【0108】
1H NMR(500MHz,C6D6,δ/ppm)
5.96(s,2H),4.25(br,2H),1.7−1.3(br,4H),1.30(s,18H),1.3−1.1(br,6H),1.1−0.9(br,6H).
13C NMR(125MHz,C6D6,δ/ppm)
102.73,102.71,102.70,80.0(br),57.8,57.74,57.71,34.3,31.7,25.7,11.1。
【0109】
(試験例13)Ti(tBuNCHCHNtBu)(OsBu)2の熱分析
アルゴンを400mL/minにて流通させている雰囲気下、昇温速度10℃/minの条件で測定したTi(tBuNCHCHNtBu)(OsBu)2のTGの結果及びアルゴン雰囲気下で密閉した容器の中で昇温速度10℃/minで測定したTi(tBuNCHCHNtBu)(OEt)2のDSCの結果を図14に示した。TGの結果からTi(tBuNCHCHNtBu)(OsBu)2はCVD法又はALD法などの材料として適した気化特性を有していることが明らかであり、DSCの結果からTi(tBuNCHCHNtBu)(OsBu)2の熱安定性が良好なことが明らかである。
【0110】
(実施例19)
アルゴン雰囲気下で、N,N’−ジ(tert−ブチル)−1,4−ジアザ−1,3−ブタジエン(tBuNCHCHNtBu)14.85g(88.2mmol)をテトラヒドロフラン110mLに溶かし、ナトリウム4.18g(182mmol)を加えて室温で14時間撹拌した。その反応液をテトラ−sec−ブトキソチタン(Ti(OsBu)4)29.18g(85.7mmol)をヘキサン50mLに溶かした溶液に加え、室温で14時間撹拌した。その反応液から溶媒を減圧下で留去し、残渣にヘキサン120mLを加えた。生成した不溶物をろ別し、ろ液から溶媒を減圧留去した。得られた残渣を減圧蒸留(留出温度92−96℃/0.03Torr)することにより、Ti(tBuNCHCHNtBu)(OsBu)2を濃赤色の液体として得た(収量28.81g、収率93%)。なお、これはsec−ブチル基のキラリティーの違いに基づく異性体の混合物である。このようにして得たTi(tBuNCHCHNtBu)(OsBu)2の1H及び13C NMRスペクトルを測定したところ、これらのスペクトルは実施例18で得たもののスペクトルと一致した。
【0111】
(実施例20)
恒温槽を用いて84℃に保たれた材料容器内に納められたTi(tBuNCHCHNtBu)(OEt)2にキャリアガスとしてアルゴンを流量10sccmで吹き込んでTi(tBuNCHCHNtBu)(OEt)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量230sccmで、反応ガスとして酸素ガスを流量60sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を400℃に保ち、反応室内の圧力が4Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図15に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。
【0112】
(実施例21)
恒温槽を用いて84℃に保たれた材料容器内に納められたTi(tBuNCHCHNtBu)(OtPe)2にキャリアガスとしてアルゴンを流量10sccmで吹き込んでTi(tBuNCHCHNtBu)(OtPe)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量230sccmで、反応ガスとして酸素ガスを流量60sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を400℃に保ち、反応室内の圧力が100Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図15に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。
【0113】
(実施例22)
恒温槽を用いて84℃に保たれた材料容器内に納められたTi(tPeNCHCHNtPe)(OiPr)2にキャリアガスとしてアルゴンを流量10sccmで吹き込んでTi(tPeNCHCHNtPe)(OiPr)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量230sccmで、反応ガスとして酸素ガスを流量60sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を400℃に保ち、反応室内の圧力が4Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図15に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。
【0114】
(実施例23)
恒温槽を用いて84℃に保たれた材料容器内に納められたTi(tBuNCHCHNtBu)(OsBu)2にキャリアガスとしてアルゴンを流量10sccmで吹き込んでTi(tBuNCHCHNtBu)(OsBu)2を気化させて反応室に送りこんだ。このときの原料容器の内圧は100Torrであった。同時に希釈ガスとしてアルゴンを流量230sccmで、反応ガスとして酸素ガスを流量60sccmでそれぞれ反応室に送りこんだ。反応室内に設置されたSiO2/Si基板の温度を400℃に保ち、反応室内の圧力が4Torrに保たれるように排気を行った。この条件で1時間かけて薄膜を形成した。CVD成膜装置の概略を図15に示す。得られた薄膜を蛍光X線装置を用いて分析したところ、Tiを含有していることが確認された。
【符号の説明】
【0115】
1.材料容器
2.恒温槽
3.反応室
4.基板
5.反応ガス
6.希釈ガス
7.キャリアガス
8.マスフローコントローラー
9.マスフローコントローラー
10.マスフローコントローラー
11.真空ポンプ
12.排気
13.材料容器
14.恒温槽
15.反応室
16.基板
17.反応ガス
18.希釈ガス
19.キャリアガス
20.マスフローコントローラー
21.マスフローコントローラー
22.マスフローコントローラー
23.真空ポンプ
24.排気
【特許請求の範囲】
【請求項1】
一般式(1)
【化1】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体。
【請求項2】
R1及びR4が各々独立に炭素数2から6のアルキル基であり、R2及びR3が水素原子であり、R5が炭素数1から8のアルキル基である請求項1に記載のチタン錯体。
【請求項3】
R1及びR4が各々独立に炭素数4又は5のアルキル基であり、R2及びR3が水素原子であり、R5が炭素数3から5のアルキル基である請求項1又は2に記載のチタン錯体。
【請求項4】
一般式(2)
【化2】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。)で表されるジイミン、アルカリ金属及び一般式(3)
【化3】

(式中、R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるアルコキソ錯体を反応させることを特徴とする一般式(1)
【化4】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体の製造方法。
【請求項5】
R1及びR4が各々独立に炭素数2から6のアルキル基であり、R2及びR3が水素原子であり、R5が炭素数1から8のアルキル基である請求項4に記載の製造方法。
【請求項6】
R1及びR4が各々独立に炭素数4又は5のアルキル基であり、R2及びR3が水素原子であり、R5が炭素数3から5のアルキル基である請求項4又は5に記載の製造方法。
【請求項7】
一般式(4)
【化5】

(式中、R1a及びR4aは各々独立に炭素数1から6のアルキル基を示す。R2a及びR3aは各々独立に水素原子又は炭素数1から3のアルキル基を示す。R7及びR8は各々独立にフッ素原子で置換されていても良い炭素数1から4のアルキル基を示す。)で表されるアミド錯体に、一般式(5)
【化6】

(式中、R5aはフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるアルコールを反応させることを特徴とする一般式(1a)
【化7】

(式中、R1a及びR4aは各々独立に炭素数1から6のアルキル基を示す。R2a及びR3aは各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5aはフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体の製造方法。
【請求項8】
R1a及びR4aが各々独立に炭素数2から6のアルキル基であり、R2a及びR3aが水素原子であり、R5aが炭素数1から8のアルキル基である請求項7に記載の製造方法。
【請求項9】
R1a及びR4aが各々独立に炭素数4又は5のアルキル基であり、R2a及びR3aが水素原子であり、R5aが炭素数3から5のアルキル基である請求項7又は8に記載の製造方法。
【請求項10】
一般式(1)
【化8】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体を材料として用いることにより製造されるチタン含有薄膜。
【請求項11】
一般式(1)
【化9】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体を材料として用いることを特徴とするチタン含有薄膜の製法。
【請求項12】
請求項10に記載のチタン含有薄膜を用いることを特徴とする半導体デバイス。
【請求項13】
請求項10に記載のチタン含有薄膜を用いることを特徴とする光触媒。
【請求項1】
一般式(1)
【化1】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体。
【請求項2】
R1及びR4が各々独立に炭素数2から6のアルキル基であり、R2及びR3が水素原子であり、R5が炭素数1から8のアルキル基である請求項1に記載のチタン錯体。
【請求項3】
R1及びR4が各々独立に炭素数4又は5のアルキル基であり、R2及びR3が水素原子であり、R5が炭素数3から5のアルキル基である請求項1又は2に記載のチタン錯体。
【請求項4】
一般式(2)
【化2】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。)で表されるジイミン、アルカリ金属及び一般式(3)
【化3】

(式中、R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるアルコキソ錯体を反応させることを特徴とする一般式(1)
【化4】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体の製造方法。
【請求項5】
R1及びR4が各々独立に炭素数2から6のアルキル基であり、R2及びR3が水素原子であり、R5が炭素数1から8のアルキル基である請求項4に記載の製造方法。
【請求項6】
R1及びR4が各々独立に炭素数4又は5のアルキル基であり、R2及びR3が水素原子であり、R5が炭素数3から5のアルキル基である請求項4又は5に記載の製造方法。
【請求項7】
一般式(4)
【化5】

(式中、R1a及びR4aは各々独立に炭素数1から6のアルキル基を示す。R2a及びR3aは各々独立に水素原子又は炭素数1から3のアルキル基を示す。R7及びR8は各々独立にフッ素原子で置換されていても良い炭素数1から4のアルキル基を示す。)で表されるアミド錯体に、一般式(5)
【化6】

(式中、R5aはフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるアルコールを反応させることを特徴とする一般式(1a)
【化7】

(式中、R1a及びR4aは各々独立に炭素数1から6のアルキル基を示す。R2a及びR3aは各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5aはフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体の製造方法。
【請求項8】
R1a及びR4aが各々独立に炭素数2から6のアルキル基であり、R2a及びR3aが水素原子であり、R5aが炭素数1から8のアルキル基である請求項7に記載の製造方法。
【請求項9】
R1a及びR4aが各々独立に炭素数4又は5のアルキル基であり、R2a及びR3aが水素原子であり、R5aが炭素数3から5のアルキル基である請求項7又は8に記載の製造方法。
【請求項10】
一般式(1)
【化8】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体を材料として用いることにより製造されるチタン含有薄膜。
【請求項11】
一般式(1)
【化9】

(式中、R1及びR4は各々独立に炭素数1から16のアルキル基を示す。R2及びR3は各々独立に水素原子又は炭素数1から3のアルキル基を示す。R5はフッ素原子で置換されていても良い炭素数1から16のアルキル基を示す。)で表されるチタン錯体を材料として用いることを特徴とするチタン含有薄膜の製法。
【請求項12】
請求項10に記載のチタン含有薄膜を用いることを特徴とする半導体デバイス。
【請求項13】
請求項10に記載のチタン含有薄膜を用いることを特徴とする光触媒。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【公開番号】特開2010−30986(P2010−30986A)
【公開日】平成22年2月12日(2010.2.12)
【国際特許分類】
【出願番号】特願2009−126417(P2009−126417)
【出願日】平成21年5月26日(2009.5.26)
【出願人】(000003300)東ソー株式会社 (1,901)
【出願人】(000173762)財団法人相模中央化学研究所 (151)
【Fターム(参考)】
【公開日】平成22年2月12日(2010.2.12)
【国際特許分類】
【出願日】平成21年5月26日(2009.5.26)
【出願人】(000003300)東ソー株式会社 (1,901)
【出願人】(000173762)財団法人相模中央化学研究所 (151)
【Fターム(参考)】
[ Back to top ]

