デクスメデトミジンの定量方法
【課題】 血液等の検体中のデクスメデトミジンを少量の検体で簡便かつ高感度で測定する方法を提供する。
【解決手段】 デクスメデトミジンを含む検体を固相抽出法に付して検体中のデクスメデトミジンを溶出成分として分離し、分離したデクスメデトミジンを、4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールを内部標準物質として使用して液体クロマトグラフィー/タンデム質量分析装置により検出、定量することを特徴とする検体中のデクスメデトミジンの定量方法。
【解決手段】 デクスメデトミジンを含む検体を固相抽出法に付して検体中のデクスメデトミジンを溶出成分として分離し、分離したデクスメデトミジンを、4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールを内部標準物質として使用して液体クロマトグラフィー/タンデム質量分析装置により検出、定量することを特徴とする検体中のデクスメデトミジンの定量方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、血液等の検体中のデクスメデトミジンを測定する方法に関する。
【背景技術】
【0002】
デクスメデトミジン((+)−(S)−4−[1−(2,3−ジメチルフェニル)エチル]−1H−イミダゾール)は以下の構造式:
【化1】

で表記される化合物であり、中枢性α2アドレナリン受容体を介して、大脳皮質等の上位中枢の興奮、覚醒レベル上昇を抑制することにより鎮静作用を発現する新しいクラスの鎮静剤である。特にデクスメデトミジンは、集中治療室において、静脈ライン(iv−line)やカテーテル等を設置された患者が興奮したり、不安や苦痛を感じるのを軽減させることができる。(特許文献1参照。)。
【0003】
デクスメデトミジンの用法用量として、通常、成人には、6μg/kg/時で10分間静脈内へ持続注入し(初期負荷投与)、続いて患者の状態に合わせて、至適鎮静レベルが得られる様、デクスメデトミジンの目標血漿中濃度が0.1〜1.25ng/mLとなるように維持量として通常0.2〜0.7μg/kg/時の範囲で静脈内へ持続注入される。しかし、前記デクスメデトミジンの維持量を静脈内へ持続注入しても、目標血漿中濃度を得ることができない患者や、逆に目標血漿中濃度を超える患者があり、デクスメデトミジンの血中濃度の管理が重要となっている。
デクスメデトミジンの血中濃度の測定法としては、ガスクロマトグラフィー/質量分析法(以下、GC/MS法)が知られている。前記GC/MS法によると、まずデクスメデトミジンを含む血漿にヘキサンとペンタフルオロベンゾイル・クロライドを加えると、デクスメデトミジンがペンタフルオロベンゾイル化され、その後ペンタフルオロベンゾイル化されたデクスメデトミジンを含む有機層を分取し、濃縮した後、該濃縮液をサンプルとして使用し、GC/MSによる定量分析に付する(非特許文献1参照)。しかし、この方法では、血液が2mL以上(血漿として1mL以上)必要で、かつデクスメデトミジンをペンタフルオロベンゾイル化しなければならない。このため、この方法は、集中治療室においてデクスメデトミジンが投与される患者の血中デクスメデトミジン濃度を迅速に管理、維持しなければならない方法としては、煩雑であり満足すべきものではなかった。
【特許文献1】特表2002−509880号公報
【非特許文献1】ジャーナル・オブ・クロマトグラフィー(Journal of chromatography)、1989年、第497巻、p.282−287
【発明の開示】
【発明が解決しようとする課題】
【0004】
本発明は、血液等の検体中のデクスメデトミジンを少量の検体で簡便かつ高感度で測定する方法を提供することを目的とする。
【課題を解決するための手段】
【0005】
本発明者らは、血液等の検体中に含まれるデクスメデトミジンを高感度で定量する方法について鋭意研究を行った結果、デクスメデトミジンを含む検体を前処理としての固相抽出法と、液体クロマトグラフィー/タンデム質量分析装置(以下、LC/MS/MSシステムと略記する。)による検出、定量法とを組み合わせて用いることにより、検体中のデクスメデトミジンを容易に高感度で検出できることを見出し、本発明を完成するに至った。
すなわち、本発明は、
(1) デクスメデトミジンを含む検体を固相抽出法に付して検体中のデクスメデトミジンを溶出成分として分離し、分離したデクスメデトミジンを、4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールを内部標準物質として使用してLC/MS/MSシステムにより検出、定量することを特徴とする検体中のデクスメデトミジンの定量方法、
(2) 固相抽出法における固相抽出用樹脂が、親水性と疎水性を兼ね備えたコンビネーションポリマー又はエンハンスドポリマーであることを特徴とする前記(1)記載の定量方法、
(3) 固相抽出法における溶出液が、水混和性の揮発し易い性質を持つ極性有機溶媒を60〜100V/V%含む溶液であることを特徴とする前記(1)又は(2)記載の定量方法、
(4) 極性有機溶媒が、メタノール又はアセトニトリルであることを特徴とする前記(3)記載の定量方法、
(5) LC/MS/MSシステムの高速液体クロマトグラフィーにおけるカラムが逆相クロマトグラフィーカラムであることを特徴とする前記(1)記載の定量方法、
(6) LC/MS/MSシステムの高速液体クロマトグラフィーにおける移動相が酢酸緩衝液/アセトニトリル混液であることを特徴とする前記(5)記載の定量方法、
(7) LC/MS/MSシステムにおいて、デクスメデトミジンのプリカーサーイオンとしてm/z201付近のイオンを選択し且つプロダクトイオンとしてm/z95付近のイオンを選択し、4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールのプリカーサーイオンとしてm/z187付近のイオンを選択し且つプロダクトイオンとしてm/z95付近のイオンを選択し、これらイオンをモニターする前記(1)記載の定量方法、
(8) 検体が動物の血漿、血清、血液又は尿である前記(1)記載の定量方法。
に関する。
【発明の効果】
【0006】
本発明に従えば、固相抽出法により前処理された検体を用いてLC/MS/MSシステムで分析定量を行うことにより、測定の対象であるデクスメデトミジンを簡便に高感度で定量することができる。
【発明を実施するための最良の形態】
【0007】
本発明において、デクスメデトミジンは遊離の塩基の状態のみならず、例えば塩酸塩等の塩の状態であってもよい。本発明において使用することのできる検体としては、特に制限はなく、デクスメデトミジンを含有するものであればいずれも使用可能であり、例えば、ヒトを含む動物の血液、血漿、血清、唾液、尿等の生体試料並びに動物における各種の臓器や組織等を挙げることができる。
【0008】
固相抽出法は、例えば固相抽出カートリッジを用いることが好ましい。固相抽出カートリッジとしては、生体試料中のデクスメデトミジンを高感度に抽出できる固相抽出カートリッジであればいずれも好ましく用いることができ、例えばオクチルシリカゲルを用いたIsolute C8(International sorbent technology社製)、Bond Elut C8(バリアン社製)、Sep−pak C8(ウォーターズ社製)等;オクタデシルシリカゲルを用いたIsolute C18(International sorbent technology社製)、Bond Elut C18(バリアン社製)、Sep−pak C18(ウォーターズ社製)等;親水性と疎水性を兼ね備えたコンビネーションポリマーを用いた固相抽出カートリッジ NEXUS(バリアン社製)、Oasis HLB(ウォーターズ社製);エンハンスドポリマーを用いた固相抽出カートリッジ Focus(バリアン社製)等が挙げられる。なかでも、親水性と疎水性を兼ね備えたコンビネーションポリマーを用いた固相抽出カートリッジ(NEXUS、Oasis HLB)又はエンハンスドポリマーを用いた固相抽出カートリッジ(Focus)がとりわけ好ましい。なお、固相抽出カラムはカートリッジタイプに限定されるものではなく、ディスクタイプ又はプレートタイプのもの等も適宜用いることができる。
【0009】
上記固相抽出における溶出液は、水混和性の揮発し易い性質を持つ極性有機溶媒を60〜100V/V%含む溶液が好ましい。当該溶液は、極性溶媒以外に水や非極性溶媒を含んでもよい。このような極性有機溶媒としては、例えば、メタノール、エタノール又はアセトニトリル等が挙げられる。前記極性溶媒は、1又は2種以上を適宜混合してもよい。前記極性溶媒は、さらに揮発性の酸、例えば酢酸又は塩酸(好ましくは約0.01〜1N塩酸)等で酸性としてもよい。酸は、極性溶媒に対して約0.01〜10V/V%、好ましくは約0.05〜5V/V%となるよう加えられるのがよい。溶出溶液を酸性とすることで、少量の溶出液(例えば、酸を加えない溶出液の体積の約1/2体積以下)でも、固相カートリッジに吸着されたデクスメデトミジンを溶出できる。また、溶出後の操作を考慮すると、溶出液は水を含まないか水を含んでも水の含量が40V/V%以下、好ましくは20V/V%以下、より好ましくは10V/V%以下がよい。
溶液は、通常はピペットや注射器等を用いて、カートリッジに注入される。
【0010】
LC/MS/MSシステムの高速液体クロマトグラフィー(LC)におけるカラムは、逆相クロマトグラフィーカラムが好ましい。逆相クロマトグラフィーカラムとしては、オクタデシルシリカゲル(ODS)系カラムが好ましく、例えばInertsil ODS(ジーエルサイエンス株式会社製)、L−column ODS (財団法人化学物質評価研究機構製)、Develosil ODS UG−5(野村化学株式会社製)、CAPCELL PAK C18 MGII(株式会社資生堂製)、ZORBAX XDB−C18(横河アナリティカルシステムズ株式会社製)、Symmetry C18(ウォーターズ社製)、Nucleosil C18(M.ナーゲル社製)等を挙げることができるが、ODS系カラムであればこれらに限定されない。
【0011】
上記高速液体クロマトグラフィーにおける移動相として、本発明においては酢酸緩衝液系移動相が好適に用いられる。酢酸緩衝液としては、酢酸溶液、酢酸アンモニウム溶液又は酢酸アンモニウム緩衝液が挙げられる。前記酢酸溶液中の酢酸濃度は、約0.1〜1V/V%、より好ましくは約0.4〜0.6V/V%の範囲とすることができる。また酢酸アンモニウム溶液における酢酸アンモニウムの濃度は、一般に約0.01〜100mM、好ましくは約1〜50mM、より好ましくは約1〜10mMの範囲内とすることができる。酢酸アンモニウム緩衝液は、前記酢酸アンモニウム溶液に酢酸を加えpHを約3〜5の範囲に調製されるのがよい。この酢酸緩衝液系移動相としては、例えば、酢酸溶液/メタノール混液、酢酸溶液/酢酸メタノール混液、酢酸溶液/アセトニトリル混液、酢酸溶液/酢酸アセトニトリル混液、酢酸溶液/メタノール/アセトニトリル混液、酢酸アンモニウム溶液又は酢酸アンモニウム緩衝液/メタノール混液、酢酸アンモニウム溶液又は酢酸アンモニウム緩衝液/アセトニトリル混液、あるいは酢酸アンモニウム溶液又は酢酸アンモニウム緩衝液/メタノール/アセトニトリル混液等が挙げられる。酢酸溶液及び酢酸アンモニウム溶液はそれぞれ酢酸水溶液及び酢酸アンモニウム水溶液であってもよい。メタノール又はアセトニトリルと酢酸溶液又は酢酸アンモニウム溶液もしくは酢酸アンモニウム緩衝液の混合割合は、容積比で一般に約1:99〜約99:1、好ましくは約20:80〜約80:20、さらに好ましくは、約30:70〜約70:30、もっとも好ましくは約35:65〜約60:40の範囲内である。
【0012】
LC/MS/MSシステムにおけるイオン化法としては、例えば、エレクトロスプレーイオン化(ESI)、大気圧化学イオン化(APCI)、サーモスプレーイオン化(TSP)又は高速原子衝撃(FAB)等が挙げられる。この中でもESIが好ましく、ESIターボイオンスプレイ法がより好適に用いられる。本発明において、MS/MSとはMS 1で得られたプリカーサーイオン(ここでは水素付加イオン)を選択し、MS 2でプリカーサーイオンを窒素ガスやアルゴンガス等により分解させ、生じるプロダクトイオンを検出する方法であり、この方法は、高選択性によりSN比が向上し高感度になる。
【0013】
生成したプロダクトイオンの検出方法としては、一般に、フルスキャン法、選択リアクションモニタリング(SRM)法又はマルチリアクションモニタリング(MRM)法等が挙げられるが、本発明においてはMRM法が好適に用いられる。このMRM法においては、例えば、デクスメデトミジンのプリカーサーイオンとして、m/z201付近のイオンのみを選択し、次に、このイオンを窒素ガスやアルゴンガス等の不活性ガスに衝突させ分解させた際に生じるプロダクトイオンのうちm/z10〜201の範囲内で最大のピークを示すイオン、好ましくはm/z95付近のイオンのみを選択してそのイオンの量をモニターすることにより、本発明が目的とする検体中のデクスメデトミジンを高感度で定量することができる。このとき、内部標準物質の4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールのプリカーサーイオンとして、m/z187付近のイオンを選択し、且つプロダクトイオンとして、m/z10〜187の範囲内で最大のピークを示すイオン、好ましくはm/z95付近のイオンが選択されるのがよい。
【0014】
本発明に用いられる内部標準物質として用いられる4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールは以下の構造;
【化2】

で表記される化合物(以下、内標化合物と略記する。)である。この内標化合物は、遊離の塩基の状態のみならず、例えば塩酸塩などの塩の状態であってもよい。前記内標化合物は、測定の対象であるデクスメデトミジンと比して分子量が約14小さいので、LC/MS/MSシステムでは、デクスメデトシミジン化合物の検出ピークと異なる位置にピークを得ることができ、かつそのピークは血漿等生体成分の検出ピークの位置とも異なる。また、上記内標化合物は、血漿等の生体成分中において安定で経時的変化が少なく、固相抽出法による処理を行っても回収率が良好で、取り扱い易い化合物である。このため上記内標化合物は、内部標準物質として使用することが可能となり、しかも、前記内標化合物を使用することにより検体中のデクスメデトミジンを驚くべき高感度で定量することができる。上記内標化合物は、例えば特公平3−72621号公報に記載の方法等に準じて製造することができる。
【0015】
以下に、 本発明の好ましい工程を例示する。例えば、
(a)検体を希釈して前処理する工程、
(b)前記(a)工程で得られた前処理物から固相抽出法でデクスメデトミジンを溶出成分として分離する工程、
(c)前記(b)工程で得られた溶出成分中のデクスメデトミジンをLC/MS/MSシステムを用いて測定する工程、及び
(e)前記(d)工程で得られた測定値から、検体中のデクスメデトミジンの濃度を算出する工程、
が挙げられる。
以下、上記した好ましい各工程についてより具体的に説明する。
【0016】
上記(a)工程では、例えばデクスメデトミジンを投与された患者から採血された血液から血漿を分離し、分離されたデクスメデトミジンを含有する血漿約100〜250μLに、内標化合物を加え、水、あるいは酸(1N塩酸)又は/及びアルカリ(1N水酸化ナトリウム)で最終的に約1.5〜10容量倍に血漿が希釈される。内標化合物を含む希釈された血漿は、約0℃〜室温、好ましくは約4〜10℃で、約10000〜20000rpm、約5〜10分間遠心分離され、その上清が使用されるのが好ましい。なお、遠心分離後、上記した最終的な容量倍に希釈してもよい。
【0017】
上記(b)工程は、前記(a)工程で得られた、希釈され又は所望により遠心分離された血漿は、常法によってあらかじめ極性有機溶媒及び水で活性化された上記した固相抽出カートリッジに注入される。前記極性有機溶媒としては、例えば、アルコール(例えばメタノール、エタノール等)又はアセトニトリル等が好ましい。血漿が注入された固相抽出カートリッジは、水約0.5〜2mL、次いで、約50V/V%以下(好ましくは約2〜40V/V%)のメタノール又はアセトニトリル水溶液で洗浄されるのが好ましい。これにより、デクスメデトミジン及び内標化合物が固相抽出カートリッジの固相に吸着し得る。次いで当該固相抽出カートリッジに溶出溶液約0.5〜2mLを注入し、固相抽出カートリッジからデクスメデトミジン及び内標化合物を溶出成分として溶出させる。溶出したデクスメデトミジン及び内標化合物を含む溶出液は窒素気流下、約20〜50℃で濃縮乾固される。
【0018】
上記(c)工程は、前記(b)工程で得られた濃縮乾固物が、LC/MS/MSシステムにおける高速液体クロマトグラフィーに用いられる移動相で溶解され、LC/MS/MSシステムに注入されデクスメデトミジンが測定される工程である。LC/MS/MSシステムとしては、例えばAPI4000 LC/MS/MSシステム(AB/MDS SCIEX製)、4000 Q TRAP LC/MS/MSシステム(AB/MDS SCIEX製)、Q TRAP LC/MS/MSシステム(AB/MDS SCIEX製)、API2000 LC/MS/MSシステム(AB/MDS SCIEX製)、TSQ QUANTUM LC/MS/MSシステム(サーモエレクトロン社製)又はTSQ7000 LC/MS/MSシステム(サーモエレクトロン社製)等が挙げられる。
【0019】
高速液体クロマトグラフィー(LC)は、上記したODS系カラムおよび移動相を用い、そのカラム温度は室温〜約50℃、好ましくは約35〜45℃とするのが好ましい。
ついで、高速液体クロマトグラフィーで分離・溶出された成分はタンデム質量分析装置(MS/MS)のイオン化室に導入されイオン化される。第一段目の質量分析計(MS)でプリカーサーイオンが選択され、ついでコリジョンセルと呼ばれる衝突室で窒素ガス等と衝突させてプリカーサーイオンを解離させ新しいイオン群を発生させる。この新しいイオン群のうち最大のピークを示すイオンがプロダクトイオンとして選択され、第2段目の質量分析計(MS)で分析される。
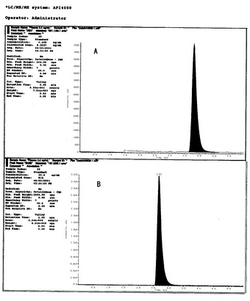
デクスメデトミジン0.2ng/mLと内標化合物10ng/mLを10μL注入時のマスクロマトグラムを図1に示す。この図では、デクスメデトミジンは約3.8分に、内標化合物は約2.7分に溶出される。
【0020】
上記(e)工程は、前記(d)工程で得られた測定値から、検体中のデクスメデトミジン及び内標化合物の濃度を算出できさえすれば特に限定されない。本工程に用いられる濃度の算出手段としては、例えばデクスメデトミジンの標準溶液を用いて作成した検量線を用いて行う手段等が挙げられる。具体的には、検量線はデクスメデトミジンの標準溶液に内標化合物を添加した検体を用いて、上記工程(a)〜工程(d)を実施して得られる測定値から作成される。
また、本工程において用いる検量線は、真度が定量下限濃度において±20%以内であり、その他の濃度において±15%以内であり、かつ相関係数が0.99以上である検量線を用いるのが好ましい。内標化合物を用いた場合には、たとえば、検体中のデクスメデトミジンのピーク面積値と内標化合物のピーク面積値との比を求め、この比をグラフ上にプロットすることにより信頼性の高い検量線を作成することができる。また、デクスメデトミジンを健常人の検体(例えば血漿)に溶解した標準溶液を用いることにより、例えば血漿に含まれる内因性要因の影響を除くことができる。すなわち、かかる検量線を用いることにより、患者におけるデクスメデトミジンの検体中の濃度を直接算出できるので、好都合である。上記定量下限濃度は、検量線作成のために用いるデクスメデトミジンを添加した検体のうち、検体中のデクスメデトミジンの濃度の一番薄い濃度を意味する。上記真度は、定量値の平均から添加濃度を減じた値を添加濃度で除することで算出される。上記相関係数は、例えば最小2乗法を用いて算出できる。
【0021】
本発明の定量方法を用いれば、例えば、検体として血漿を用いる場合、わずか約200μLの検体量で検体中のデクスメデトミジンの定量を行うことが可能となる
【0022】
以下に実施例を用いて本発明を説明するが、本発明はこれらに限定されるものではない。
なお、内標化合物としては、特公平3−72621号公報、実施例7に準じて製造した4−[1−(2−メチルフェニル)エチル]−1H−イミダゾール塩酸塩を使用した。
【実施例1】
【0023】
検量線の作成
以下の手順に従い、検量線を作成した。
(1)デクスメデトミジン標準溶液の調製:塩酸デクスメデトミジン11.8mg(デクスメデトミジンとして10mg)を精製水に溶解して10mLとし、デクスメデトミジン標準原液(1mg/mL)を調製した。前記標準原液を精製水で希釈し、デクスメデトミジン0.08、0.2、0.8、4.0、20.0、40.0、80.0ng/mLの標準溶液を調製した。
内部標準溶液の調製:内標化合物10.0mgを精密に量り取り、少量の精製水で溶解後、精製水で正確に10mLとして内部標準原液(1mg/mL))を調製した。この内部標準原液を精製水で正確に希釈し内部標準溶液(40ng/mL、100μg/mL又は5μg/mL)を調製した。
(2)ヒト血漿200μLに、デクスメデトミジン標準溶液各50μL(ヒト血漿1mL当たり、デクスメデトミジンが0.02、0.05、0.2、1.0、5.0、10.0、20.0ng添加されたこととなる。)、内部標準溶液50μL及び精製水700μLを加えて溶液を得た。
(3)前記(2)の溶液を、予めメタノール1mL及び水1mLを注入し活性化した固相抽出カートリッジ Oasis HLB(30mg/1mL;ウォーターズ社製)に注入した。次いでOasis HLBに精製水1mLを2回注入し、更に50V/V%メタノール水溶液1mLを注入し、Oasis HLBを洗浄した。
(4)洗浄された前記(3)のOasis HLBにメタノール1mLを注入し、Oasis HLBから溶出する溶出液を回収した。回収した溶出液を窒素気流下濃縮乾固した。濃縮乾固物に5mmol/L酢酸緩衝液(pH5.0)/アセトニトリル(70:30,V/V)75μLを加え、濃縮乾固物を溶解し、高速液体クロマトグラフィー用試料とした。
(5)前記(4)の高速液体クロマトグラフィー用試料10μLをLC/MS/MSシステム〔API4000 LC/MS/MSシステム(AB/MDS SCIEX製)〕に注入し、デクスメデトミジンを測定した。LC/MS/MSシステムは以下の条件で行った。
【0024】
LC(高速液体クロマトグラフィー):
分析カラム:CAPCELL PACK C18 MGII(2.0×75mm,3μm;株式会社資生堂製)
ガードカラム:GUARD CARTRIDGE CAPCELL C18 MGIIS−3(2.0×10mm,3μm;株式会社資生堂製)
移動相:5mmol/L酢酸緩衝液(pH5.0)/アセトニトリル(70:30,V/V)
ニードル洗浄液:メタノール/0.05V/V%酢酸溶液(90:10,V/V)
流速:0.2mL/min
カラム温度:40℃
オートサンプラー設定温度:4℃
試料注入量:10μL
MS/MS(タンデム質量分析装置)
イオン化法:Electrospray ionization(ESI)
(Turbo Ion Spray)
イオンスプレー電圧:5500V
ヒーターガス温度:700℃
マルチプライヤー電圧:1800V
ネブライザーガス(GS1):80psi(約552kPa)
ターボガス(GS2):70psi(約483kPa)
カーテンガス(Nitrogen):20psi(約138kPa)
コリジョンガス(Nitrogen):3psi(約21kPa)
検出モード:正イオン検出モード
Multiple reaction monitoring(MRM)
モニターイオン:
【表1】

【0025】
(6)得られた測定データは表2のとおりであった。
血漿中のデクスメデトミジン濃度0.02〜20ng/mLの範囲で、相関係数の高い検量線(r=0.9997)が得られることがわかった。また、血漿中のデクスメデトミジン濃度0.075〜40ng/mLの範囲についても、同様に検量線を作成したところ、直線性の高い検量線(r=0.9908)が得られることを確認した。このデクスメデトミジンの定量範囲は、投与されるデクスメデトミジンの目標血漿濃度0.1〜1.25ng/mLに合致し、デクスメデトミジンの血漿濃度の定量方法になり得ることが判明した。
【0026】
【表2】

【実施例2】
【0027】
ヒト血漿を用いたデクスメデトミジンの添加回収試験
ヒト血漿200μLに、実施例1(1)で調製したデクスメデトミジン標準溶液(0.08、4.0、80ng/mL)50μL(ヒト血漿1mL当たり、デクスメデトミジンが0.02、1.0、20.0ng添加されたこととなる。)及び内部標準溶液(40ng/mL)50μL及び精製水700μLを加え、ボルテックスミキサーで攪拌した。以後の操作は上記検量線の作成の手順(3)〜(5)と同様に行った。
結果を表3に示した。本結果は、デクスメデトミジンの目標血漿濃度0.1〜1.25ng/mLにおいて、回収率96%以上の精度で分析定量が可能であることを示すものである。
【表3】

【0028】
〔実施例3〜5〕
固相抽出法における固相抽出カートリッジの検討−ラット血漿を用いたデクスメデトミジンの添加回収試験−
ラット血漿200μLにデクスメデトミジン標準溶液50μL(ラット血漿1mL当たり、デクスメデトミジン100μg/mL添加)、実施例1(1)で調製した内部標準溶液(100μg/mL)50μL及び1N水酸化ナトリウム溶液400μLを添加し、ボルテックスミキサーで撹拌後、15000rpm、4℃、5分間遠心分離した。遠心分離後の上清を表4の固相抽出カートリッジ及び溶出液等を用い濃縮乾固物を調製した。対照として、デクスメデトミジン標準溶液50μL及び内部標準溶液50μLの代わりに精製水をそれぞれ50μL加えた血漿を使用した。
【0029】
【表4】

【0030】
得られた各乾固物に高速液体クロマトグラフィーに用いる下記する移動相200μLを加え、乾固物を溶解し、マイレックスHV 0.45μmフィルターでろ過し、高速液体クロマトグラフィー用試料を調製した。得られた各高速液体クロマトグラフィー用試料50μLを液体クロマトグラフィーに注入し、デクスメデトミジンを測定した。本実施例においては、デクスメデトミジンをUV検出器(波長220nm)で検出し、デクスメデトミジンのピーク面積値(Sampleピーク面積値)を算出した。前記ピーク面積値は高速液体クロマトグラフィーに接続されたコンピュータによって自動的に算出される。一方、デクスメデトミジン標準溶液(100μg/mL)50μL、内部標準溶液(100μg/mL)50μL及び下記する移動相100μLを混合し、スタンダード(STD)溶液を調製した。そのSTD溶液50μLを液体クロマトグラフィーに注入し、上記と同様にデクスメデトミジンを検出し、得られたデクスメデトミジンのピーク面積値をSTDピーク面積値とした。デクスメデトミジンの回収率は、以下に従い算出した。
回収率=(Sampleピーク面積値/STDピーク面積値)×100
なおUV検出器によるデクスメデトミジンの検出限界は0.125μg/mLであることを確認している。
【0031】
高速液体クロマトグラフィーの条件は以下の条件で行った。
分析カラム:Inertsil ODS−3(2.1×150mm,5μm;東ソー株式会社製)
ガードカラム:TSK GUARDGEL ODS−80Ts(1.5×20mm,5μm;東ソー株式会社製)
移動相:0.5V/V%酢酸/メタノール(65:35,V/V)
流速:0.3mL/min
カラム温度:40℃
試料注入量:50μL
【0032】
ラット血漿からのデクスメデトミジンの回収率は表5のとおりであった。親水性と疎水性を兼ね備えたコンビネーションポリマー又はエンハンスドポリマーのいずれの固相抽出カートリッジも本発明の定量に使用し得ることが判明した。
【表5】

【0033】
〔実施例6〜12〕
固相抽出法における溶出液の検討−ラット血漿を用いたデクスメデトミジンの添加回収試験−
ラット血漿200μLにデクスメデトミジン標準溶液50μL(ヒト血漿1mL当たり、デクスメデトミジン10μg/mL添加)、実施例1(1)で調製した内部標準溶液(5μg/mL)50μL及び1N塩酸溶液200μLを添加し、ボルテックスミキサーで撹拌後、15000rpm、4℃、5分間遠心分離した。遠心分離後の上清に1N水酸化ナトリウム溶液400μLを均一に混合した。前記混合液を、メタノール1mL及び精製水1mLで活性化した固相抽出カートリッジ Oasis HLB(10mg/1cc;ウォーターズ社製)又はFocus(バリアン社製)に注入し、精製水1mL、2回で、固相抽出カートリッジを洗浄した。表6、表7の溶出液等を用い、固相抽出カートリッジからデクスメデトミジン及び内標化合物を溶出し、溶出液を遠心乾固(120min,50℃)した。
【0034】
〔比較施例1〜3〕
表7の比較施例1〜3における溶出液を用いる以外は実施例6〜12と同様に操作し、固相抽出カートリッジからデクスメデトミジン塩酸塩及び内標化合物を溶出し、溶出液を遠心乾固(120min,50℃)した。
【0035】
【表6】

【0036】
【表7】

【0037】
実施例6〜7及び比較例1〜3で得られた各乾固物に、高速液体クロマトグラフィーに用いる下記する移動相200μLを加え、乾固物を溶解し、マイレックスHV 0.45μmフィルターでろ過し、高速液体クロマトグラフィー用試料を調製した。得られた各高速液体クロマトグラフィー用試料50μLを高速液体クロマトグラフィーに注入し、デクスメデトミジンを測定した。本実施例及び比較例においては、添加デクスメデトミジン量をUV検出器(波長220nm)で検出し、実施例3〜5と同様に回収率を算出した。
【0038】
高速液体クロマトグラフィーの条件は以下の条件で行った。
分析カラム:L−column ODS(2.1×150mm,3μm;財団法人化学物質評価研究機構製)
ガードカラム:TSK GUARDGEL ODS−80Ts(4.0×20mm;東ソー株式会社製)
移動相:5mM酢酸アンモニウム溶液:メタノール(40:60,V/V)
流速:0.25mL/min
カラム温度:40℃
試料注入量:100μL
【0039】
ラット血漿からのデクスメデトミジンの回収率は表8、9のとおりであった。血漿中のデクスメデトミジンの固相抽出法において、溶出液を60%以上のメタノール水溶液(極性溶媒溶液)とすることで、ラット血漿からのデクスメデトミジンの回収率が75%となり、定量に使用し得ることが判明した。
【0040】
【表8】

【0041】
【表9】

【産業上の利用可能性】
【0042】
本発明は、デクスメデトミジンの目標血漿中濃度0.1〜1.25ng/mLの範囲内でデクスメデトミジンの血漿中濃度の定量に有用である。また、デクスメデトミジンの血漿中濃度を簡便かつ高感度に定量できるので、デクスメデトミジンの血漿中濃度から至適鎮静レベルを維持するためのデクスメデトミジン持続投与量の決定に利用できる。
【図面の簡単な説明】
【0043】
【図1】図中Aは、デクスメデトミジン標準溶液(デクスメデトミジン0.2ng/mL)10μLをLC/MS/MSに注入時のマスクロマトグラムを示す図である。Bは内部標準溶液(内標化合物10ng/mL)10μLをLC/MS/MSに注入時のマスクロマトグラムを示す図である。
【技術分野】
【0001】
本発明は、血液等の検体中のデクスメデトミジンを測定する方法に関する。
【背景技術】
【0002】
デクスメデトミジン((+)−(S)−4−[1−(2,3−ジメチルフェニル)エチル]−1H−イミダゾール)は以下の構造式:
【化1】

で表記される化合物であり、中枢性α2アドレナリン受容体を介して、大脳皮質等の上位中枢の興奮、覚醒レベル上昇を抑制することにより鎮静作用を発現する新しいクラスの鎮静剤である。特にデクスメデトミジンは、集中治療室において、静脈ライン(iv−line)やカテーテル等を設置された患者が興奮したり、不安や苦痛を感じるのを軽減させることができる。(特許文献1参照。)。
【0003】
デクスメデトミジンの用法用量として、通常、成人には、6μg/kg/時で10分間静脈内へ持続注入し(初期負荷投与)、続いて患者の状態に合わせて、至適鎮静レベルが得られる様、デクスメデトミジンの目標血漿中濃度が0.1〜1.25ng/mLとなるように維持量として通常0.2〜0.7μg/kg/時の範囲で静脈内へ持続注入される。しかし、前記デクスメデトミジンの維持量を静脈内へ持続注入しても、目標血漿中濃度を得ることができない患者や、逆に目標血漿中濃度を超える患者があり、デクスメデトミジンの血中濃度の管理が重要となっている。
デクスメデトミジンの血中濃度の測定法としては、ガスクロマトグラフィー/質量分析法(以下、GC/MS法)が知られている。前記GC/MS法によると、まずデクスメデトミジンを含む血漿にヘキサンとペンタフルオロベンゾイル・クロライドを加えると、デクスメデトミジンがペンタフルオロベンゾイル化され、その後ペンタフルオロベンゾイル化されたデクスメデトミジンを含む有機層を分取し、濃縮した後、該濃縮液をサンプルとして使用し、GC/MSによる定量分析に付する(非特許文献1参照)。しかし、この方法では、血液が2mL以上(血漿として1mL以上)必要で、かつデクスメデトミジンをペンタフルオロベンゾイル化しなければならない。このため、この方法は、集中治療室においてデクスメデトミジンが投与される患者の血中デクスメデトミジン濃度を迅速に管理、維持しなければならない方法としては、煩雑であり満足すべきものではなかった。
【特許文献1】特表2002−509880号公報
【非特許文献1】ジャーナル・オブ・クロマトグラフィー(Journal of chromatography)、1989年、第497巻、p.282−287
【発明の開示】
【発明が解決しようとする課題】
【0004】
本発明は、血液等の検体中のデクスメデトミジンを少量の検体で簡便かつ高感度で測定する方法を提供することを目的とする。
【課題を解決するための手段】
【0005】
本発明者らは、血液等の検体中に含まれるデクスメデトミジンを高感度で定量する方法について鋭意研究を行った結果、デクスメデトミジンを含む検体を前処理としての固相抽出法と、液体クロマトグラフィー/タンデム質量分析装置(以下、LC/MS/MSシステムと略記する。)による検出、定量法とを組み合わせて用いることにより、検体中のデクスメデトミジンを容易に高感度で検出できることを見出し、本発明を完成するに至った。
すなわち、本発明は、
(1) デクスメデトミジンを含む検体を固相抽出法に付して検体中のデクスメデトミジンを溶出成分として分離し、分離したデクスメデトミジンを、4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールを内部標準物質として使用してLC/MS/MSシステムにより検出、定量することを特徴とする検体中のデクスメデトミジンの定量方法、
(2) 固相抽出法における固相抽出用樹脂が、親水性と疎水性を兼ね備えたコンビネーションポリマー又はエンハンスドポリマーであることを特徴とする前記(1)記載の定量方法、
(3) 固相抽出法における溶出液が、水混和性の揮発し易い性質を持つ極性有機溶媒を60〜100V/V%含む溶液であることを特徴とする前記(1)又は(2)記載の定量方法、
(4) 極性有機溶媒が、メタノール又はアセトニトリルであることを特徴とする前記(3)記載の定量方法、
(5) LC/MS/MSシステムの高速液体クロマトグラフィーにおけるカラムが逆相クロマトグラフィーカラムであることを特徴とする前記(1)記載の定量方法、
(6) LC/MS/MSシステムの高速液体クロマトグラフィーにおける移動相が酢酸緩衝液/アセトニトリル混液であることを特徴とする前記(5)記載の定量方法、
(7) LC/MS/MSシステムにおいて、デクスメデトミジンのプリカーサーイオンとしてm/z201付近のイオンを選択し且つプロダクトイオンとしてm/z95付近のイオンを選択し、4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールのプリカーサーイオンとしてm/z187付近のイオンを選択し且つプロダクトイオンとしてm/z95付近のイオンを選択し、これらイオンをモニターする前記(1)記載の定量方法、
(8) 検体が動物の血漿、血清、血液又は尿である前記(1)記載の定量方法。
に関する。
【発明の効果】
【0006】
本発明に従えば、固相抽出法により前処理された検体を用いてLC/MS/MSシステムで分析定量を行うことにより、測定の対象であるデクスメデトミジンを簡便に高感度で定量することができる。
【発明を実施するための最良の形態】
【0007】
本発明において、デクスメデトミジンは遊離の塩基の状態のみならず、例えば塩酸塩等の塩の状態であってもよい。本発明において使用することのできる検体としては、特に制限はなく、デクスメデトミジンを含有するものであればいずれも使用可能であり、例えば、ヒトを含む動物の血液、血漿、血清、唾液、尿等の生体試料並びに動物における各種の臓器や組織等を挙げることができる。
【0008】
固相抽出法は、例えば固相抽出カートリッジを用いることが好ましい。固相抽出カートリッジとしては、生体試料中のデクスメデトミジンを高感度に抽出できる固相抽出カートリッジであればいずれも好ましく用いることができ、例えばオクチルシリカゲルを用いたIsolute C8(International sorbent technology社製)、Bond Elut C8(バリアン社製)、Sep−pak C8(ウォーターズ社製)等;オクタデシルシリカゲルを用いたIsolute C18(International sorbent technology社製)、Bond Elut C18(バリアン社製)、Sep−pak C18(ウォーターズ社製)等;親水性と疎水性を兼ね備えたコンビネーションポリマーを用いた固相抽出カートリッジ NEXUS(バリアン社製)、Oasis HLB(ウォーターズ社製);エンハンスドポリマーを用いた固相抽出カートリッジ Focus(バリアン社製)等が挙げられる。なかでも、親水性と疎水性を兼ね備えたコンビネーションポリマーを用いた固相抽出カートリッジ(NEXUS、Oasis HLB)又はエンハンスドポリマーを用いた固相抽出カートリッジ(Focus)がとりわけ好ましい。なお、固相抽出カラムはカートリッジタイプに限定されるものではなく、ディスクタイプ又はプレートタイプのもの等も適宜用いることができる。
【0009】
上記固相抽出における溶出液は、水混和性の揮発し易い性質を持つ極性有機溶媒を60〜100V/V%含む溶液が好ましい。当該溶液は、極性溶媒以外に水や非極性溶媒を含んでもよい。このような極性有機溶媒としては、例えば、メタノール、エタノール又はアセトニトリル等が挙げられる。前記極性溶媒は、1又は2種以上を適宜混合してもよい。前記極性溶媒は、さらに揮発性の酸、例えば酢酸又は塩酸(好ましくは約0.01〜1N塩酸)等で酸性としてもよい。酸は、極性溶媒に対して約0.01〜10V/V%、好ましくは約0.05〜5V/V%となるよう加えられるのがよい。溶出溶液を酸性とすることで、少量の溶出液(例えば、酸を加えない溶出液の体積の約1/2体積以下)でも、固相カートリッジに吸着されたデクスメデトミジンを溶出できる。また、溶出後の操作を考慮すると、溶出液は水を含まないか水を含んでも水の含量が40V/V%以下、好ましくは20V/V%以下、より好ましくは10V/V%以下がよい。
溶液は、通常はピペットや注射器等を用いて、カートリッジに注入される。
【0010】
LC/MS/MSシステムの高速液体クロマトグラフィー(LC)におけるカラムは、逆相クロマトグラフィーカラムが好ましい。逆相クロマトグラフィーカラムとしては、オクタデシルシリカゲル(ODS)系カラムが好ましく、例えばInertsil ODS(ジーエルサイエンス株式会社製)、L−column ODS (財団法人化学物質評価研究機構製)、Develosil ODS UG−5(野村化学株式会社製)、CAPCELL PAK C18 MGII(株式会社資生堂製)、ZORBAX XDB−C18(横河アナリティカルシステムズ株式会社製)、Symmetry C18(ウォーターズ社製)、Nucleosil C18(M.ナーゲル社製)等を挙げることができるが、ODS系カラムであればこれらに限定されない。
【0011】
上記高速液体クロマトグラフィーにおける移動相として、本発明においては酢酸緩衝液系移動相が好適に用いられる。酢酸緩衝液としては、酢酸溶液、酢酸アンモニウム溶液又は酢酸アンモニウム緩衝液が挙げられる。前記酢酸溶液中の酢酸濃度は、約0.1〜1V/V%、より好ましくは約0.4〜0.6V/V%の範囲とすることができる。また酢酸アンモニウム溶液における酢酸アンモニウムの濃度は、一般に約0.01〜100mM、好ましくは約1〜50mM、より好ましくは約1〜10mMの範囲内とすることができる。酢酸アンモニウム緩衝液は、前記酢酸アンモニウム溶液に酢酸を加えpHを約3〜5の範囲に調製されるのがよい。この酢酸緩衝液系移動相としては、例えば、酢酸溶液/メタノール混液、酢酸溶液/酢酸メタノール混液、酢酸溶液/アセトニトリル混液、酢酸溶液/酢酸アセトニトリル混液、酢酸溶液/メタノール/アセトニトリル混液、酢酸アンモニウム溶液又は酢酸アンモニウム緩衝液/メタノール混液、酢酸アンモニウム溶液又は酢酸アンモニウム緩衝液/アセトニトリル混液、あるいは酢酸アンモニウム溶液又は酢酸アンモニウム緩衝液/メタノール/アセトニトリル混液等が挙げられる。酢酸溶液及び酢酸アンモニウム溶液はそれぞれ酢酸水溶液及び酢酸アンモニウム水溶液であってもよい。メタノール又はアセトニトリルと酢酸溶液又は酢酸アンモニウム溶液もしくは酢酸アンモニウム緩衝液の混合割合は、容積比で一般に約1:99〜約99:1、好ましくは約20:80〜約80:20、さらに好ましくは、約30:70〜約70:30、もっとも好ましくは約35:65〜約60:40の範囲内である。
【0012】
LC/MS/MSシステムにおけるイオン化法としては、例えば、エレクトロスプレーイオン化(ESI)、大気圧化学イオン化(APCI)、サーモスプレーイオン化(TSP)又は高速原子衝撃(FAB)等が挙げられる。この中でもESIが好ましく、ESIターボイオンスプレイ法がより好適に用いられる。本発明において、MS/MSとはMS 1で得られたプリカーサーイオン(ここでは水素付加イオン)を選択し、MS 2でプリカーサーイオンを窒素ガスやアルゴンガス等により分解させ、生じるプロダクトイオンを検出する方法であり、この方法は、高選択性によりSN比が向上し高感度になる。
【0013】
生成したプロダクトイオンの検出方法としては、一般に、フルスキャン法、選択リアクションモニタリング(SRM)法又はマルチリアクションモニタリング(MRM)法等が挙げられるが、本発明においてはMRM法が好適に用いられる。このMRM法においては、例えば、デクスメデトミジンのプリカーサーイオンとして、m/z201付近のイオンのみを選択し、次に、このイオンを窒素ガスやアルゴンガス等の不活性ガスに衝突させ分解させた際に生じるプロダクトイオンのうちm/z10〜201の範囲内で最大のピークを示すイオン、好ましくはm/z95付近のイオンのみを選択してそのイオンの量をモニターすることにより、本発明が目的とする検体中のデクスメデトミジンを高感度で定量することができる。このとき、内部標準物質の4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールのプリカーサーイオンとして、m/z187付近のイオンを選択し、且つプロダクトイオンとして、m/z10〜187の範囲内で最大のピークを示すイオン、好ましくはm/z95付近のイオンが選択されるのがよい。
【0014】
本発明に用いられる内部標準物質として用いられる4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールは以下の構造;
【化2】

で表記される化合物(以下、内標化合物と略記する。)である。この内標化合物は、遊離の塩基の状態のみならず、例えば塩酸塩などの塩の状態であってもよい。前記内標化合物は、測定の対象であるデクスメデトミジンと比して分子量が約14小さいので、LC/MS/MSシステムでは、デクスメデトシミジン化合物の検出ピークと異なる位置にピークを得ることができ、かつそのピークは血漿等生体成分の検出ピークの位置とも異なる。また、上記内標化合物は、血漿等の生体成分中において安定で経時的変化が少なく、固相抽出法による処理を行っても回収率が良好で、取り扱い易い化合物である。このため上記内標化合物は、内部標準物質として使用することが可能となり、しかも、前記内標化合物を使用することにより検体中のデクスメデトミジンを驚くべき高感度で定量することができる。上記内標化合物は、例えば特公平3−72621号公報に記載の方法等に準じて製造することができる。
【0015】
以下に、 本発明の好ましい工程を例示する。例えば、
(a)検体を希釈して前処理する工程、
(b)前記(a)工程で得られた前処理物から固相抽出法でデクスメデトミジンを溶出成分として分離する工程、
(c)前記(b)工程で得られた溶出成分中のデクスメデトミジンをLC/MS/MSシステムを用いて測定する工程、及び
(e)前記(d)工程で得られた測定値から、検体中のデクスメデトミジンの濃度を算出する工程、
が挙げられる。
以下、上記した好ましい各工程についてより具体的に説明する。
【0016】
上記(a)工程では、例えばデクスメデトミジンを投与された患者から採血された血液から血漿を分離し、分離されたデクスメデトミジンを含有する血漿約100〜250μLに、内標化合物を加え、水、あるいは酸(1N塩酸)又は/及びアルカリ(1N水酸化ナトリウム)で最終的に約1.5〜10容量倍に血漿が希釈される。内標化合物を含む希釈された血漿は、約0℃〜室温、好ましくは約4〜10℃で、約10000〜20000rpm、約5〜10分間遠心分離され、その上清が使用されるのが好ましい。なお、遠心分離後、上記した最終的な容量倍に希釈してもよい。
【0017】
上記(b)工程は、前記(a)工程で得られた、希釈され又は所望により遠心分離された血漿は、常法によってあらかじめ極性有機溶媒及び水で活性化された上記した固相抽出カートリッジに注入される。前記極性有機溶媒としては、例えば、アルコール(例えばメタノール、エタノール等)又はアセトニトリル等が好ましい。血漿が注入された固相抽出カートリッジは、水約0.5〜2mL、次いで、約50V/V%以下(好ましくは約2〜40V/V%)のメタノール又はアセトニトリル水溶液で洗浄されるのが好ましい。これにより、デクスメデトミジン及び内標化合物が固相抽出カートリッジの固相に吸着し得る。次いで当該固相抽出カートリッジに溶出溶液約0.5〜2mLを注入し、固相抽出カートリッジからデクスメデトミジン及び内標化合物を溶出成分として溶出させる。溶出したデクスメデトミジン及び内標化合物を含む溶出液は窒素気流下、約20〜50℃で濃縮乾固される。
【0018】
上記(c)工程は、前記(b)工程で得られた濃縮乾固物が、LC/MS/MSシステムにおける高速液体クロマトグラフィーに用いられる移動相で溶解され、LC/MS/MSシステムに注入されデクスメデトミジンが測定される工程である。LC/MS/MSシステムとしては、例えばAPI4000 LC/MS/MSシステム(AB/MDS SCIEX製)、4000 Q TRAP LC/MS/MSシステム(AB/MDS SCIEX製)、Q TRAP LC/MS/MSシステム(AB/MDS SCIEX製)、API2000 LC/MS/MSシステム(AB/MDS SCIEX製)、TSQ QUANTUM LC/MS/MSシステム(サーモエレクトロン社製)又はTSQ7000 LC/MS/MSシステム(サーモエレクトロン社製)等が挙げられる。
【0019】
高速液体クロマトグラフィー(LC)は、上記したODS系カラムおよび移動相を用い、そのカラム温度は室温〜約50℃、好ましくは約35〜45℃とするのが好ましい。
ついで、高速液体クロマトグラフィーで分離・溶出された成分はタンデム質量分析装置(MS/MS)のイオン化室に導入されイオン化される。第一段目の質量分析計(MS)でプリカーサーイオンが選択され、ついでコリジョンセルと呼ばれる衝突室で窒素ガス等と衝突させてプリカーサーイオンを解離させ新しいイオン群を発生させる。この新しいイオン群のうち最大のピークを示すイオンがプロダクトイオンとして選択され、第2段目の質量分析計(MS)で分析される。
デクスメデトミジン0.2ng/mLと内標化合物10ng/mLを10μL注入時のマスクロマトグラムを図1に示す。この図では、デクスメデトミジンは約3.8分に、内標化合物は約2.7分に溶出される。
【0020】
上記(e)工程は、前記(d)工程で得られた測定値から、検体中のデクスメデトミジン及び内標化合物の濃度を算出できさえすれば特に限定されない。本工程に用いられる濃度の算出手段としては、例えばデクスメデトミジンの標準溶液を用いて作成した検量線を用いて行う手段等が挙げられる。具体的には、検量線はデクスメデトミジンの標準溶液に内標化合物を添加した検体を用いて、上記工程(a)〜工程(d)を実施して得られる測定値から作成される。
また、本工程において用いる検量線は、真度が定量下限濃度において±20%以内であり、その他の濃度において±15%以内であり、かつ相関係数が0.99以上である検量線を用いるのが好ましい。内標化合物を用いた場合には、たとえば、検体中のデクスメデトミジンのピーク面積値と内標化合物のピーク面積値との比を求め、この比をグラフ上にプロットすることにより信頼性の高い検量線を作成することができる。また、デクスメデトミジンを健常人の検体(例えば血漿)に溶解した標準溶液を用いることにより、例えば血漿に含まれる内因性要因の影響を除くことができる。すなわち、かかる検量線を用いることにより、患者におけるデクスメデトミジンの検体中の濃度を直接算出できるので、好都合である。上記定量下限濃度は、検量線作成のために用いるデクスメデトミジンを添加した検体のうち、検体中のデクスメデトミジンの濃度の一番薄い濃度を意味する。上記真度は、定量値の平均から添加濃度を減じた値を添加濃度で除することで算出される。上記相関係数は、例えば最小2乗法を用いて算出できる。
【0021】
本発明の定量方法を用いれば、例えば、検体として血漿を用いる場合、わずか約200μLの検体量で検体中のデクスメデトミジンの定量を行うことが可能となる
【0022】
以下に実施例を用いて本発明を説明するが、本発明はこれらに限定されるものではない。
なお、内標化合物としては、特公平3−72621号公報、実施例7に準じて製造した4−[1−(2−メチルフェニル)エチル]−1H−イミダゾール塩酸塩を使用した。
【実施例1】
【0023】
検量線の作成
以下の手順に従い、検量線を作成した。
(1)デクスメデトミジン標準溶液の調製:塩酸デクスメデトミジン11.8mg(デクスメデトミジンとして10mg)を精製水に溶解して10mLとし、デクスメデトミジン標準原液(1mg/mL)を調製した。前記標準原液を精製水で希釈し、デクスメデトミジン0.08、0.2、0.8、4.0、20.0、40.0、80.0ng/mLの標準溶液を調製した。
内部標準溶液の調製:内標化合物10.0mgを精密に量り取り、少量の精製水で溶解後、精製水で正確に10mLとして内部標準原液(1mg/mL))を調製した。この内部標準原液を精製水で正確に希釈し内部標準溶液(40ng/mL、100μg/mL又は5μg/mL)を調製した。
(2)ヒト血漿200μLに、デクスメデトミジン標準溶液各50μL(ヒト血漿1mL当たり、デクスメデトミジンが0.02、0.05、0.2、1.0、5.0、10.0、20.0ng添加されたこととなる。)、内部標準溶液50μL及び精製水700μLを加えて溶液を得た。
(3)前記(2)の溶液を、予めメタノール1mL及び水1mLを注入し活性化した固相抽出カートリッジ Oasis HLB(30mg/1mL;ウォーターズ社製)に注入した。次いでOasis HLBに精製水1mLを2回注入し、更に50V/V%メタノール水溶液1mLを注入し、Oasis HLBを洗浄した。
(4)洗浄された前記(3)のOasis HLBにメタノール1mLを注入し、Oasis HLBから溶出する溶出液を回収した。回収した溶出液を窒素気流下濃縮乾固した。濃縮乾固物に5mmol/L酢酸緩衝液(pH5.0)/アセトニトリル(70:30,V/V)75μLを加え、濃縮乾固物を溶解し、高速液体クロマトグラフィー用試料とした。
(5)前記(4)の高速液体クロマトグラフィー用試料10μLをLC/MS/MSシステム〔API4000 LC/MS/MSシステム(AB/MDS SCIEX製)〕に注入し、デクスメデトミジンを測定した。LC/MS/MSシステムは以下の条件で行った。
【0024】
LC(高速液体クロマトグラフィー):
分析カラム:CAPCELL PACK C18 MGII(2.0×75mm,3μm;株式会社資生堂製)
ガードカラム:GUARD CARTRIDGE CAPCELL C18 MGIIS−3(2.0×10mm,3μm;株式会社資生堂製)
移動相:5mmol/L酢酸緩衝液(pH5.0)/アセトニトリル(70:30,V/V)
ニードル洗浄液:メタノール/0.05V/V%酢酸溶液(90:10,V/V)
流速:0.2mL/min
カラム温度:40℃
オートサンプラー設定温度:4℃
試料注入量:10μL
MS/MS(タンデム質量分析装置)
イオン化法:Electrospray ionization(ESI)
(Turbo Ion Spray)
イオンスプレー電圧:5500V
ヒーターガス温度:700℃
マルチプライヤー電圧:1800V
ネブライザーガス(GS1):80psi(約552kPa)
ターボガス(GS2):70psi(約483kPa)
カーテンガス(Nitrogen):20psi(約138kPa)
コリジョンガス(Nitrogen):3psi(約21kPa)
検出モード:正イオン検出モード
Multiple reaction monitoring(MRM)
モニターイオン:
【表1】

【0025】
(6)得られた測定データは表2のとおりであった。
血漿中のデクスメデトミジン濃度0.02〜20ng/mLの範囲で、相関係数の高い検量線(r=0.9997)が得られることがわかった。また、血漿中のデクスメデトミジン濃度0.075〜40ng/mLの範囲についても、同様に検量線を作成したところ、直線性の高い検量線(r=0.9908)が得られることを確認した。このデクスメデトミジンの定量範囲は、投与されるデクスメデトミジンの目標血漿濃度0.1〜1.25ng/mLに合致し、デクスメデトミジンの血漿濃度の定量方法になり得ることが判明した。
【0026】
【表2】

【実施例2】
【0027】
ヒト血漿を用いたデクスメデトミジンの添加回収試験
ヒト血漿200μLに、実施例1(1)で調製したデクスメデトミジン標準溶液(0.08、4.0、80ng/mL)50μL(ヒト血漿1mL当たり、デクスメデトミジンが0.02、1.0、20.0ng添加されたこととなる。)及び内部標準溶液(40ng/mL)50μL及び精製水700μLを加え、ボルテックスミキサーで攪拌した。以後の操作は上記検量線の作成の手順(3)〜(5)と同様に行った。
結果を表3に示した。本結果は、デクスメデトミジンの目標血漿濃度0.1〜1.25ng/mLにおいて、回収率96%以上の精度で分析定量が可能であることを示すものである。
【表3】

【0028】
〔実施例3〜5〕
固相抽出法における固相抽出カートリッジの検討−ラット血漿を用いたデクスメデトミジンの添加回収試験−
ラット血漿200μLにデクスメデトミジン標準溶液50μL(ラット血漿1mL当たり、デクスメデトミジン100μg/mL添加)、実施例1(1)で調製した内部標準溶液(100μg/mL)50μL及び1N水酸化ナトリウム溶液400μLを添加し、ボルテックスミキサーで撹拌後、15000rpm、4℃、5分間遠心分離した。遠心分離後の上清を表4の固相抽出カートリッジ及び溶出液等を用い濃縮乾固物を調製した。対照として、デクスメデトミジン標準溶液50μL及び内部標準溶液50μLの代わりに精製水をそれぞれ50μL加えた血漿を使用した。
【0029】
【表4】

【0030】
得られた各乾固物に高速液体クロマトグラフィーに用いる下記する移動相200μLを加え、乾固物を溶解し、マイレックスHV 0.45μmフィルターでろ過し、高速液体クロマトグラフィー用試料を調製した。得られた各高速液体クロマトグラフィー用試料50μLを液体クロマトグラフィーに注入し、デクスメデトミジンを測定した。本実施例においては、デクスメデトミジンをUV検出器(波長220nm)で検出し、デクスメデトミジンのピーク面積値(Sampleピーク面積値)を算出した。前記ピーク面積値は高速液体クロマトグラフィーに接続されたコンピュータによって自動的に算出される。一方、デクスメデトミジン標準溶液(100μg/mL)50μL、内部標準溶液(100μg/mL)50μL及び下記する移動相100μLを混合し、スタンダード(STD)溶液を調製した。そのSTD溶液50μLを液体クロマトグラフィーに注入し、上記と同様にデクスメデトミジンを検出し、得られたデクスメデトミジンのピーク面積値をSTDピーク面積値とした。デクスメデトミジンの回収率は、以下に従い算出した。
回収率=(Sampleピーク面積値/STDピーク面積値)×100
なおUV検出器によるデクスメデトミジンの検出限界は0.125μg/mLであることを確認している。
【0031】
高速液体クロマトグラフィーの条件は以下の条件で行った。
分析カラム:Inertsil ODS−3(2.1×150mm,5μm;東ソー株式会社製)
ガードカラム:TSK GUARDGEL ODS−80Ts(1.5×20mm,5μm;東ソー株式会社製)
移動相:0.5V/V%酢酸/メタノール(65:35,V/V)
流速:0.3mL/min
カラム温度:40℃
試料注入量:50μL
【0032】
ラット血漿からのデクスメデトミジンの回収率は表5のとおりであった。親水性と疎水性を兼ね備えたコンビネーションポリマー又はエンハンスドポリマーのいずれの固相抽出カートリッジも本発明の定量に使用し得ることが判明した。
【表5】

【0033】
〔実施例6〜12〕
固相抽出法における溶出液の検討−ラット血漿を用いたデクスメデトミジンの添加回収試験−
ラット血漿200μLにデクスメデトミジン標準溶液50μL(ヒト血漿1mL当たり、デクスメデトミジン10μg/mL添加)、実施例1(1)で調製した内部標準溶液(5μg/mL)50μL及び1N塩酸溶液200μLを添加し、ボルテックスミキサーで撹拌後、15000rpm、4℃、5分間遠心分離した。遠心分離後の上清に1N水酸化ナトリウム溶液400μLを均一に混合した。前記混合液を、メタノール1mL及び精製水1mLで活性化した固相抽出カートリッジ Oasis HLB(10mg/1cc;ウォーターズ社製)又はFocus(バリアン社製)に注入し、精製水1mL、2回で、固相抽出カートリッジを洗浄した。表6、表7の溶出液等を用い、固相抽出カートリッジからデクスメデトミジン及び内標化合物を溶出し、溶出液を遠心乾固(120min,50℃)した。
【0034】
〔比較施例1〜3〕
表7の比較施例1〜3における溶出液を用いる以外は実施例6〜12と同様に操作し、固相抽出カートリッジからデクスメデトミジン塩酸塩及び内標化合物を溶出し、溶出液を遠心乾固(120min,50℃)した。
【0035】
【表6】

【0036】
【表7】

【0037】
実施例6〜7及び比較例1〜3で得られた各乾固物に、高速液体クロマトグラフィーに用いる下記する移動相200μLを加え、乾固物を溶解し、マイレックスHV 0.45μmフィルターでろ過し、高速液体クロマトグラフィー用試料を調製した。得られた各高速液体クロマトグラフィー用試料50μLを高速液体クロマトグラフィーに注入し、デクスメデトミジンを測定した。本実施例及び比較例においては、添加デクスメデトミジン量をUV検出器(波長220nm)で検出し、実施例3〜5と同様に回収率を算出した。
【0038】
高速液体クロマトグラフィーの条件は以下の条件で行った。
分析カラム:L−column ODS(2.1×150mm,3μm;財団法人化学物質評価研究機構製)
ガードカラム:TSK GUARDGEL ODS−80Ts(4.0×20mm;東ソー株式会社製)
移動相:5mM酢酸アンモニウム溶液:メタノール(40:60,V/V)
流速:0.25mL/min
カラム温度:40℃
試料注入量:100μL
【0039】
ラット血漿からのデクスメデトミジンの回収率は表8、9のとおりであった。血漿中のデクスメデトミジンの固相抽出法において、溶出液を60%以上のメタノール水溶液(極性溶媒溶液)とすることで、ラット血漿からのデクスメデトミジンの回収率が75%となり、定量に使用し得ることが判明した。
【0040】
【表8】

【0041】
【表9】

【産業上の利用可能性】
【0042】
本発明は、デクスメデトミジンの目標血漿中濃度0.1〜1.25ng/mLの範囲内でデクスメデトミジンの血漿中濃度の定量に有用である。また、デクスメデトミジンの血漿中濃度を簡便かつ高感度に定量できるので、デクスメデトミジンの血漿中濃度から至適鎮静レベルを維持するためのデクスメデトミジン持続投与量の決定に利用できる。
【図面の簡単な説明】
【0043】
【図1】図中Aは、デクスメデトミジン標準溶液(デクスメデトミジン0.2ng/mL)10μLをLC/MS/MSに注入時のマスクロマトグラムを示す図である。Bは内部標準溶液(内標化合物10ng/mL)10μLをLC/MS/MSに注入時のマスクロマトグラムを示す図である。
【特許請求の範囲】
【請求項1】
デクスメデトミジンを含む検体を固相抽出法に付して検体中のデクスメデトミジンを溶出成分として分離し、分離したデクスメデトミジンを、4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールを内部標準物質として使用して液体クロマトグラフィー/タンデム質量分析装置により検出、定量することを特徴とする検体中のデクスメデトミジンの定量方法。
【請求項2】
固相抽出法における固相抽出用樹脂が、親水性と疎水性を兼ね備えたコンビネーションポリマー又はエンハンスドポリマーであることを特徴とする請求項1記載の定量方法。
【請求項3】
固相抽出法における溶出液が、水混和性の揮発し易い性質を持つ極性有機溶媒を60〜100V/V%含む溶液であることを特徴とする請求項1又は2記載の定量方法。
【請求項4】
極性有機溶媒が、メタノール、エタノール又はアセトニトリルであることを特徴とする請求項3記載の定量方法。
【請求項5】
液体クロマトグラフィー/タンデム質量分析装置の高速液体クロマトグラフィーにおけるカラムが逆相クロマトグラフィーカラムであることを特徴とする請求項1記載の定量方法。
【請求項6】
液体クロマトグラフィー/タンデム質量分析装置の高速液体クロマトグラフィーにおける移動相が酢酸緩衝液/アセトニトリル混液であることを特徴とする請求項5記載の定量方法。
【請求項7】
液体クロマトグラフィー/タンデム質量分析装置において、デクスメデトミジンのプリカーサーイオンとしてm/z201付近のイオンを選択し且つプロダクトイオンとしてm/z95付近のイオンを選択し、4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールのプリカーサーイオンとしてm/z187付近のイオンを選択し且つプロダクトイオンとしてm/z95付近のイオンを選択し、これらイオンをモニターする請求項1記載の定量方法。
【請求項8】
検体が動物の血漿、血清、血液又は尿である請求項1記載の定量方法。
【請求項1】
デクスメデトミジンを含む検体を固相抽出法に付して検体中のデクスメデトミジンを溶出成分として分離し、分離したデクスメデトミジンを、4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールを内部標準物質として使用して液体クロマトグラフィー/タンデム質量分析装置により検出、定量することを特徴とする検体中のデクスメデトミジンの定量方法。
【請求項2】
固相抽出法における固相抽出用樹脂が、親水性と疎水性を兼ね備えたコンビネーションポリマー又はエンハンスドポリマーであることを特徴とする請求項1記載の定量方法。
【請求項3】
固相抽出法における溶出液が、水混和性の揮発し易い性質を持つ極性有機溶媒を60〜100V/V%含む溶液であることを特徴とする請求項1又は2記載の定量方法。
【請求項4】
極性有機溶媒が、メタノール、エタノール又はアセトニトリルであることを特徴とする請求項3記載の定量方法。
【請求項5】
液体クロマトグラフィー/タンデム質量分析装置の高速液体クロマトグラフィーにおけるカラムが逆相クロマトグラフィーカラムであることを特徴とする請求項1記載の定量方法。
【請求項6】
液体クロマトグラフィー/タンデム質量分析装置の高速液体クロマトグラフィーにおける移動相が酢酸緩衝液/アセトニトリル混液であることを特徴とする請求項5記載の定量方法。
【請求項7】
液体クロマトグラフィー/タンデム質量分析装置において、デクスメデトミジンのプリカーサーイオンとしてm/z201付近のイオンを選択し且つプロダクトイオンとしてm/z95付近のイオンを選択し、4−[1−(2−メチルフェニル)エチル]−1H−イミダゾールのプリカーサーイオンとしてm/z187付近のイオンを選択し且つプロダクトイオンとしてm/z95付近のイオンを選択し、これらイオンをモニターする請求項1記載の定量方法。
【請求項8】
検体が動物の血漿、血清、血液又は尿である請求項1記載の定量方法。
【図1】




【公開番号】特開2006−112835(P2006−112835A)
【公開日】平成18年4月27日(2006.4.27)
【国際特許分類】
【出願番号】特願2004−298143(P2004−298143)
【出願日】平成16年10月12日(2004.10.12)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成16年9月15日 新井達潤発行の「日本臨床麻酔学会誌 Vol.24 No.8,2004」に発表
【出願人】(393028036)丸石製薬株式会社 (20)
【Fターム(参考)】
【公開日】平成18年4月27日(2006.4.27)
【国際特許分類】
【出願日】平成16年10月12日(2004.10.12)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成16年9月15日 新井達潤発行の「日本臨床麻酔学会誌 Vol.24 No.8,2004」に発表
【出願人】(393028036)丸石製薬株式会社 (20)
【Fターム(参考)】
[ Back to top ]

