ナノ秒時間ゲート分光診断装置
【課題】 レーザアブレーション(レーザ蒸散)によって生体組織表面から蒸散される発光プルームの分光スペクトルをもとに生体組織の成分を分析し、生体の病変・異常を診断する。
【解決手段】 光源1とレンズ12間に配置されるシャッター11と、前記発光プルーム14を検出する多チャンネル型分光器16と、レーザパルスの一部を検出する光検出器5と、ゲートトリガーパルスの遅延時間を測定するためのオシロスコープ6と、パルス発生器(PG)8と、ゲート制御器7と、CCDカメラ9と、このCCDカメラ9の一フレームの分光画像データを時系列アナログ信号として取込み、このアナログ信号をデジタル信号に変換してコンピュータ10に送り込むフレーム画像データ蓄積器10Aを含む。
【解決手段】 光源1とレンズ12間に配置されるシャッター11と、前記発光プルーム14を検出する多チャンネル型分光器16と、レーザパルスの一部を検出する光検出器5と、ゲートトリガーパルスの遅延時間を測定するためのオシロスコープ6と、パルス発生器(PG)8と、ゲート制御器7と、CCDカメラ9と、このCCDカメラ9の一フレームの分光画像データを時系列アナログ信号として取込み、このアナログ信号をデジタル信号に変換してコンピュータ10に送り込むフレーム画像データ蓄積器10Aを含む。
【発明の詳細な説明】
【0001】
【発明の属する技術分野】本発明は、ナノ秒時間ゲート分光診断装置に関するものである。
【0002】
【従来の技術】従来、このような分野における文献として、以下に示すようなものが開示されている。
(1)医療機器事典編集委員会偏:“1987−88 医療機器事典”pp.426−436 産業調査会(2)“ENCYCLOPEDIA OF MEDICAL SCIENCES”pp.46−50 講談社(3)佐藤卓蔵著:“レーザCDプレーヤからX線レーザまで,”pp.146−170 電気書院(1987)
(4)加藤治文、山本秀樹、日吉利光:“光感受性物質によるガン治療効果”O plus E,No.160,pp.83−88(1993)
(5)島岡優策、近江雅人、春名正光:“生体レーザアブレーションのナノ秒ストロボ顕微観測”、電子情報通信学会MEとバイオサイバネティックス研究会、信学技報 MBE96−93(1996)
(6)Yusaku Shimaoka,Mitsuo Nakamura,Masato Ohmi,Masamitsu Haruna:“Nanosecond stroboscopic microscope for laser ablation of biological tissue,”Conference on Laser & Electro Optics/Pacific Rim(CLEO/PR’97),Paper FF3,Technical Digest pp. 261−262,Makuhari,Chiba,1997従来、実際の医療現場では、赤外のCO2 レーザやNd:YAGレーザがレーザメスとして手術用の切開、凝固に用いられてきた〔上記文献(1)及び(2)参照〕。
【0003】また、レーザ励起蛍光分析〔上記文献(3)及び(4)参照〕は有力な診断法として継続して検討されている。今後、これらのレーザ励起生体反応を先端医療技術として進展、活用していくためには、レーザパルス照射時の生体表面近傍における反応形態の時間的推移、及び表面から飛散する物質の組成分析を含む詳細な実験データの蓄積が必要である。
【0004】
【発明が解決しようとする課題】生体におけるレーザアブレーション、蛍光発生等の物理現象は、一般の無機物と同様に〔上記文献(3)及び(4)参照〕ナノ秒あるいはそれ以下の反応速度を持つ。したがって、これらの分光分析を行うには、ナノ秒オーダーでの光測定技術を必要とする。ここで、生体レーザアブレーションとは、レーザパルス照射によって生体組織が熱的あるいは光化学的に分解し、瞬時に蒸散する現象である。
【0005】本発明者等は、既に、ナノ秒ストロボ観測システムを構築し、生体レーザアブレーションダイナミクス分析を行っている〔上記文献(5)及び(6)参照〕。その中で特にプルーム発光スペクトル分析を行うことによって、生体組織の組成分析あるいは正常部と病変部の識別を行える可能性がある。これは蛍光分析法と並んで、将来の光生体検査(optical biopsy)を支えるキーテクノロジーとなることが期待できる。
【0006】発光スペクトル分析法として、モノクロメータを用いたストロボ分光があるが〔上記文献(6)参照〕、これは単一レーザパルス照射では、特定の一波長しか測定できない。それ故、プルームの発光スペクトルを得るには、長い測定時間とそれに伴う試料の損傷という欠点があり、臨床への応用は難しいと考えられる。本発明は、上記問題点を解決するために、ナノ秒時間オーダーのゲート幅を持つ高速ゲートイメージインテンシファイアーを含む光マルチチャネルアナライザを用い、単一レーザパルス照射で発光プルームの分光分析を瞬時に行うことができるナノ秒時間ゲート分光診断装置を提供することを目的とする。
【0007】
【課題を解決するための手段】本発明は、上記目的を達成するために、〔1〕光源からのレーザパルスを生体組織に集光・照射し、レーザアブレーション(レーザ蒸散)によってこの生体組織表面から発生する発光プルーム(紡錘形発光体)をナノ秒の時間ゲートで分光し、この分光スペクトルをもとに前記生体組織の成分を分析し生体の病変・異常を診断するナノ秒時間ゲート分光診断装置であって、光源と生体組織に対向するレンズ間に配置されるシャッターと、前記発光プルームを検出する多チャンネル型分光器(ポリクロメータ)と、前記光源からのレーザパルスの一部を検出する光検出器と、この光検出器からの出力をモニターして高速ゲートイメージインテンシファイアーのゲートトリガーパルスの遅延時間を測定するためのオシロスコープと、レーザパルスに同期して二つの出力パルスの遅延時間を独立かつ任意に設定できるパルス発生器と、このパルス発生器およびオシロスコープに接続されるゲート制御器と、このゲート制御器によってゲートがナノ秒オーダーの時間間隔で開放され前記多チャンネル型分光器の出力光を増強・撮像する前記高速ゲートイメージインテンシファイアーと、この高速ゲートイメージインテンシファイアーの出力像を捕らえるCCDカメラと、このCCDカメラの一フレームの分光画像データを時系列アナログ信号として取込み、アナログ信号をデジタル信号に変換してコンピュータに送り込むフレーム画像データ蓄積器(フレームグラバー)を含むデータ処理装置とを設けるようにしたものである。
【0008】〔2〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、レーザアブレーションによって生体組織を蒸発・励起し、これによって発生する発光プルームの分光スペクトルをナノ秒オーダーの時間間隔で検出するようにしたものである。
〔3〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記光源は紫外光、可視光、赤外光領域におけるナノ秒レーザパルスを発生可能なレーザ光源である。
【0009】〔4〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記レーザ光源はフラッシュランプ励起あるいは半導体レーザ励起QスイッチNd:YAGレーザ又は半導体レーザ励起の全固体QスイッチNd:YAGレーザである。
〔5〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記光源のレーザ波長は検出される発光プルームの波長に比べて長い領域をも含むようにしたものである。
【0010】〔6〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記光源と生体組織の間にシャッターを配置して一個のレーザパルス照射によって極めて低侵襲な分光診断が可能である。
〔7〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記多チャンネル型分光器は、入射スリットから入射した光を複数のグレーティングで波長ごとに分散し、特定の範囲の波長成分がそれぞれ異なる出射角度で一度に出射口から出射される構成を有するようにしたものである。
【0011】〔8〕上記〔7〕記載のナノ秒時間ゲート分光診断装置において、前記複数のグレーティングは格子溝の密度が300本/mm、600本/mm、1200本/mmの何れかを設定可能であるようにしたものである。
〔9〕上記〔7〕記載のナノ秒時間ゲート分光診断装置において、前記多チャンネル型分光器の出射口から出射される特定の範囲の波長成分は前記CCDカメラの各画素に像を映し出すように構成したものである。
【0012】〔10〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記高速ゲートイメージインテンシファイアーとCCDカメラとを前記光源のトリガーパルスに同期させる手段とを具備するようにしたものである。
〔11〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記生体組織は毛髪、爪、歯牙等の生体硬組織である。
【0013】〔12〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記生体組織は血管壁、表皮下組織等の生体軟組織である。
【0014】
【発明の実施の形態】以下、本発明の実施の形態について詳細に説明する。本発明では、生体レーザアブレーションによるナノ秒時間ゲート分光システムを構築し、レーザ光源、パルス同期・遅延制御・発生系、時間ゲート分光系、分光画像処理系、それぞれの特性・機能について説明する。更に、実際にこの測定を行う際のゲート幅を決定した。
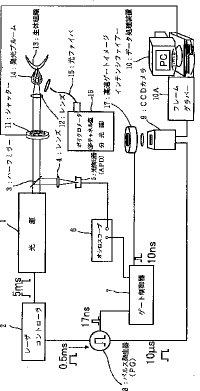
【0015】図1は本発明の実施例を示すナノ秒時間ゲート分光システムの構成図である。この図において、1は光源(例えば、フラッシュランプあるいは半導体レーザ励起QスイッチNd:YAGレーザ又は半導体レーザ励起の全固体QスイッチNd:YAGレーザ)、2はその光源1に接続されるレーザコントローラ、3はハーフミラー、4,12はレンズ、5は光検出器(アバランシェフォトダイオード:APD)、6はゲートパルス遅延時間測定/モニター用のオシロスコープ、7は高速ゲートイメージインテンシファイアーのゲート制御器、8はパルス発生器(PG)、9はCCDカメラ、10は画像演算処理機能をもつデータ処理装置(パーソナルコンピュータ:PC)、10Aはフレーム画像データ蓄積器(フレームグラバー)、11はシャッター、13は生体組織(ヒト指爪等)、14は発光プルーム、15は光ファイバ、16はポリクロメータ(多チャンネル型分光器)、17は高速ゲートイメージインテンシファイアーである。
【0016】以下、本発明の実施例を示すナノ秒時間ゲート分光システムの動作について、説明する。まず、光源(例えば、QスイッチNd:YAGレーザ)1からのレーザパルス(パルス幅10〜90ナノ秒)をシャッター11を通して一個だけ生体組織(ヒト指爪等)13に集光・照射すると、表面から微量の組織(約50ミクロン径で、深さ数ミクロン程度)が蒸散(アブレーション)されて励起状態になり発光プルーム(紡錘形の発光体)14が発生する。
【0017】また、レーザ照射直後に、主に生体組織(ヒト指爪)13表面近傍の水分が蒸散され、紡錘形の明るい発光プルーム(これを先行プルームと呼ぶ)が発生し成長する。さらに、レーザ照射後、約100ナノ秒経過すると、生体組織(ヒト指爪)表面が剥離されて、「後方プルーム」が発生する。これが対象とする生体組織の成分を含む蒸散・励起物質である。
【0018】したがって、上記の後方プルームの発光スペクトルを測定するために、光源1からのレーザパルスの一部を光検出器〔アバランシェフォトダイオード(APD〕5で検出し、この時刻を基準として、パルス発生器8から出力されるゲートトリガー用パルスの遅延時間をオシロスコープ6で所定の300〜400ナノ秒に測定・設定して、高速ゲートイメージインテンシファイアー17のゲート制御器7により、高速ゲートイメージインテンシファイアー17のゲートを10ナノ秒の時間間隔で開放する。これによって、光ファイバ15およびポリクロメータ16を用いて検出する後方プルームの発光スペクトルの10ナノ秒時間ゲート分光像を取り込む。
【0019】さらに、高速ゲートイメージインテンシファイアー17の出力像(分光イメージデータ)をCCDカメラ9で捕らえ、時系列の信号パルスに変換して、その信号データをフレームグラバー10A(フレーム画像データ蓄積器)を介して、パーソナルコンピュータを含むデータ処理装置10に取り込んで処理する。なお、フレームグラバーとは、CCDあるいはテレビの一画面(一フレーム)のデータを時系列信号として所定のメモリに蓄積/格納し、この時系列信号(アナログ信号)を8ビットあるいは10ビットのデジタル信号に変換してコンピュータに送り込む。メモリサイズによって異なるが、通常は10フレーム以上の画像データを同時に蓄積/格納でき、必要に応じて、所望のフレームデータをコンピュータに送り込む。
【0020】この装置では、光波長300〜900nmの範囲内(この範囲を四つのレンジに分けて測定)の光スペクトルを、波長分解能1nmで測定・表示することができる。このように、ナノ秒時間ゲート分光システムによれば、単一のレーザパルスを照射するだけで、蒸散物質の発光プルームの分光分析を行うことができ、ほぼ無侵襲の光診断を行うことができる。
【0021】特に、Ca、Na、Kなどのイオン化率の高い微量の金属イオンが効率良く検出できる。したがって、例えば、この装置で爪や毛髪のCa含有量を同定することによって、老年者の骨粗鬆症の診断が行える可能性を有している。上述のように、プローブ用のレーザパルスを用いて極微量の生体組織を蒸散させ、組織の病変を診断しようとする手法・装置は新規であり、従来の蛍光診断法と共に、光生体検査(光バイオプシ)のキーテクノロジー・装置として発展する可能性を充分に有するものである。
【0022】また、半導体レーザ(LD)励起の全固体Nd:YAGレーザを用いれば、診断装置の小型化が可能である。以下、ナノ秒時間ゲート分光システムの各部の詳細な説明を行う。照射レーザにはQスイッチNd:YAGレーザを用い、波長は基本波の1064nmである。レーザを焦点距離f=100mmレンズ12で集光して生体組織(ヒト指爪)13に照射し、生体組織をアブレーションする。
【0023】その場合、レンズ12の前にシャッタ11を挿入することによって、シャッタ11が開いた瞬間のみ1発だけ生体組織(ヒト指爪)13にレーザパルスを照射し、アブレーションが起こるようにした。発生したプルーム14の発光を光ファイバ15を通してポリクロメータ16に入射させた。入射した光はポリクロメータ16内に設けられたグレーティングで分光した後に出射される。この分光像は、高速ゲートイメージインテンシファイアー17で像増強され、その蛍光面に結像する。この蛍光像はCCDカメラ9によって分光画像として取り込まれる。さらに、CCDの画像データを時系列の信号としてフレームグラバー10Aに取り込み、アナログ信号をデジタル信号に変換してデータ処理する。
【0024】ポリクロメータ16から出射される分光像は横方向(光波長に対応する方向)に拡がり、これを10ナノ秒の時間ゲート(シャッター速度)で撮像するには、3〜6桁に及ぶ像信号の増強が必要である。このために用いる高速ゲートイメージインテンシファイアー17としては、例えば、浜松ホトニクス製C4078−01Xでゲート幅(シャッター速度に相当する量)は最小3ナノ秒である。ポリクロメータ(多チャンネル型分光器)16としては、アクトンリサーチ社のSpectra Pro−300i,Model SP−306を用いた。これには3種のグレーティングが内蔵されており、測定波長域300〜900nm、分解能1nmである。
【0025】図2は本発明に係るポリクロメータの構成を示す模式図である。この図に示すように、入射スリット16Aから入射した光は、グレーティング16D〜16Fで波長成分に分離(分光)される。なお、16B,16C,16Gは反射鏡である。ポリクロメータからは所定の波長範囲の分光スペクトル成分がそれぞれ異なる出射角度で一度に出射口16Hから出射され、これらはCCDカメラ上のそれぞれ異なる位置で検出される。
【0026】次に、分光画像処理系について説明する。ポリクロメータ16の中のグレーティング16D〜16Fで分散された光はCCDカメラ9に分光画像として映し出される。このときの分光画像は横軸が波長に対応したものである。この時系列のデータをパーソナルコンピュータに取り込み処理した。
【0027】図3は本発明に係る分光画像処理の流れを示す図であり、図3(a)はポリクロメータ16の中のグレーティング16D〜16Fによる光の分散を示す図、図3(b)はCCDカメラ9の分光画像を示す図、図3(c)は最終的に得られる分光スペクトルを示す図である。グレーティング16D〜16Fでは縦方向には分散されないので、縦軸は全て同じ波長成分のものである。よって縦軸方向に積分することにより、図3(c)に示すように、スペクトルを得ることができる。この処理はスペクトル解析ソフトウエアWin・Viewを用いて行った。
【0028】次に、波長スケールの較正について説明する。ポリクロメータ16からの出射光はCCDカメラ9の各画素に像を映し出すが、それがどの波長に対応するかを較正する必要がある。ここでは、水銀灯を用いて較正を行った。図4は本発明に係る波長の較正の方法を示す図であり、図4(a)は既知である水銀灯のスペクトルを示す図、図4(b)はその水銀灯の分光画像を示す図、図4(c)はその較正された分光画像を示す図である。
【0029】まず、図4(a)に示すように、水銀灯を分光させ、図4(b)に示すように、その分光像を取り込む。既に、知られている水銀の発光の輝線がこの波長範囲に2つ存在し、その波長は405nmと435nmである。分光像にも現れた2つの輝線に、この2点を割り当てることで、波長範囲内全ての波長の較正ができる。この処理には、スペクトル解析ソフトウエアWin・Specを用いた。
【0030】次に、同期パルス・遅延系について説明する。ナノ秒オーダーの分光分析を行う上では、同期系は極めて重要である。図1に示すように、出力レーザパルスの検出にはアバランシェフォトダイオード(APD)5を用い、その出力信号及び高速ゲートイメージインテンシファイアー17のゲート信号をオシロスコープ6で同期モニターして、パルス発生器8から出力されるゲート信号の遅延時間を測定した。
【0031】また、高速ゲートイメージインテンシファイアー17のゲート幅及び遅延時間(td )はパルス発生器(PG)8で制御する。高速ゲートイメージインテンシファイアー17と、CCDカメラ9はQスイッチNd:YAGレーザ1に同期して駆動する。次に、高速ゲートイメージインテンシファイアーのゲート幅の決定について、説明する。
【0032】プルームの発光スペクトルの分光分析を行う場合のゲート幅(tg )を決定するために、高速ゲートイメージインテンシファイアー17のゲート幅を変化させて測定した。図5はその高速ゲートイメージインテンシファイアーのゲート幅を変化させて測定した結果を示す図であり、図5(a)はそのゲート幅が50ns、遅延時間td が150nsの場合のヒト歯牙の発光スペクトを示す図、図5(b)はそのゲート幅が10nsで遅延時間を110ns、120ns、130ns、140ns、150nsとずらした場合のヒト歯牙の発光スペクトを示す図である。
【0033】図5(a)に示すように、ゲート幅が50nsの時はレーザ照射時からの遅延時間td =150nsであっても、実際はレーザパルス照射後100nsから150nsと分割された発光を取り込んでいることになる。図5(a)から明らかなように、この測定でもある程度輝線が見分けられる。しかし、図5(b)に示すように、ゲート幅を10nsにして同じレーザパルス照射後100nsから150nsまでを5分割し、測定してみると、この間でプルームのスペクトルは大きく変化していることが分かる。すなわち、ゲート幅が50nsでほかの輝線に埋もれて見にくかった390nm付近の輝線も、ゲート幅10ns、遅延時間td =150ns迄は、はっきりと確認できた。
【0034】その結果、ゲート幅が50nsでは時間分解が不十分であるといえる。ゲート幅は3nsまで短くできるが、光量が減ってしまうため、ゲート幅は10nsを採用した。次に、レーザ照射条件及び分光分析条件について説明する。レーザアブレーション及び本発明のナノ秒時間ゲート分光測定条件を表1に示す。
【0035】
【表1】

【0036】分光測定条件としては発光プルームのスペクトルの時間分解能を示すゲート幅や、グレーティングによって変わる測定波長範囲などがある。ゲート幅は10nsであり、測定波長範囲は格子溝が300本/mmのグレーティングを用いているので180nmであった。このように、本発明によれば、単一レーザパルス照射で発光プルームの分光分析を瞬時に行うことができる。
【0037】また、試料の前にシャッターを挿入することによって、単一レーザパルス照射を可能とした。さらに、QスイッチNd:YAGレーザのトリガーパルスで高速ゲートイメージインテンシファイアーとCCDカメラを同期させることによって、レーザアブレーションによる発光現象と、その分光画像の取り込みを同期させることができる。
【0038】以下、本発明の具体例について説明する。生体レーザアブレーションのナノ秒時間ゲート分光分析を行った。また、レーザアブレーション後の生体組織の変化を確認するために、顕微鏡写真を撮って考察した。
(1)発光プルームの時間的推移ストロボ顕微観測により、QスイッチNd:YAGレーザの基本波λ=1064nmをヒト歯牙に照射した際に、大気中で成長速度の違う2つのプルーム、先行および後方プルームが観測された。これらの2つのプルームを時間的に分離するために、まずヒト指爪を用いてプルームの発光スペクトルの時間的推移を測定した。
【0039】図6は本発明の第1の具体例を示すヒト指爪から発生する発光プルームの時間的推移の測定結果を示す図であり、図6(a)はその遅延時間td が200nsの場合の発光スペクトルの強度、図6(b)はその遅延時間td が300nsの場合の発光スペクトルの強度、図6(c)はその遅延時間td が400nsの場合の発光スペクトルの強度である。なお、どの場合にも、レーザパルス幅は35ns、高速ゲートイメージインテンシファイアーゲート幅は10ns、パルスエネルギーは17mJである。
【0040】この図を見ると、遅延時間td =200ns(レーザ照射後200ns)では波長500nm付近に強い輝線が見られる。しかし、この輝線は遅延時間td =300ns、400nsでは徐々に減衰していくのが見られる。これより、先行プルームの成分である窒素(N)の輝線であると考えられる。
【0041】一方、波長390nm付近に遅延時間td =300nsあたりから成長する輝線が見られる。これは後方プルームに含まれるカルシウム(Ca)の発光スペクトルである。このように、td =300ns以降では、先行プルームの影響が急激に減少し、生体組織の成分を反映する後方プルームの発光スペクトルが支配的となるので、時間ゲート分光の結果に基づいて生体組織の組成分析が可能になる。
【0042】(2)発光プルームの分光分析図7は本発明の第1の具体例を示すヒト指爪での発光プルーム分析結果を示す図である。なお、この図において、レーザパルス幅は35ns、高速ゲートイメージインテンシファイアーゲート幅は10ns、パルスエネルギーは17mJである。
【0043】図7に示すように、後方プルームの成分を分析するために遅延時間td =400nsで行った。単一パルス照射で測定できる範囲は180nmであるので、4回に分けて測定し、380nmから900nmまでのスペクトルを得た。これによれば、390nm付近に2本の強い輝線が見られる。これは上記したように、カルシウム(Ca)の輝線である。その他、589nmにナトリウム(Na)、658nmに炭素(C)と推定できる輝線が見られた。残りのピークについてはカルシウム(Ca)や酸素(O)及びリン酸(HPO)などと考えられるものがあるが、その付近に様々な組成元素の輝線があるために限定し難い。
【0044】また、400nmから500nmにかけて幅の広い吸収スペクトルが見られる。これも特定には至っていないが、有機化合物でこの様なスペクトルが見られると言われており、今後検討する必要がある。ヒト指爪におけるCaの含有量は0.1%程度である。それにも関わらず、爪の主成分であるケラチンを構成する炭素(C)の輝線よりも強いことが確認できた。この事実から、本測定システムではカルシウム(Ca)の感度が非常に高いことが分かった。このことより、カルシウムの輝線に注目し、様々な生体組織での分光分析を行った。
【0045】次に、様々な生体組織での分光分析結果について説明する。
(1)ヒトの毛髪での分析結果図8は本発明の第2の具体例を示すヒトの毛髪での発光プルーム分析結果を示す図である。なお、この図において、レーザパルス幅は35ns、高速ゲートイメージインテンシファイアーゲート幅は10ns、パルスエネルギーは17mJである。
【0046】図8に示すように、測定は遅延時間td =400nsで行った。毛髪においてもCaの含有量は約0.1%であるが、Caの輝線が顕著に見られた。この測定は、レーザのスポットサイズが直径50μmと小さいため、一本の毛髪で行うことができた。毛髪は重金属を排泄する役割を担っており、これに関しての医療への応用が期待できる。
【0047】(2)ヒト歯牙での分析結果図9は本発明の第3の具体例を示すヒトの歯牙での発光プルーム分析結果を示す図である。なお、この図において、レーザパルス幅は35ns、高速ゲートイメージインテンシファイアーゲート幅は10ns、パルスエネルギーは17mJである。
【0048】図9に示すように、測定は遅延時間td =400nsで行った。成分の36%がカルシウムであるヒト歯牙(エナメル質)では、Caの輝線は爪や毛髪と比べて、とても強いことが分かった。
(3)鶏の皮での分光分析結果図10は本発明の第4の具体例を示す鶏の皮の発光プルーム分析結果を示す図である。なお、この図において、レーザパルス幅は35ns、高速ゲートイメージインテンシファイアーゲート幅は10ns、パルスエネルギーは17mJである。
【0049】図10に示すように、測定は遅延時間td =400nsで行った。鶏の皮はCa成分をほとんど含まない表皮であるので、ほとんどCaのピークが見られなかった。一方、360nmから540nmの全範囲にわたって、幅の広い吸収スペクトルのようなものが見られた。これは上記した発光プルームの分光分析でも触れたように、有機化合物によるものと推定される。
【0050】このように、本発明のナノ秒時間ゲート分光システムにおいて、QスイッチNd:YAGレーザの基本波1064nmを用い、レーザアブレーションに伴う発光プルームで生体組織の分光分析を行った。その結果、高感度で生体組織のカルシウムの輝線を見出すことができた。またカルシウム輝線の強度とカルシウム含有量は対応していると見なすことができ、このことが臨床光診断の手がかりになると考えている。例えば、上記で顕著に見られたカルシウム(Ca)の輝線から骨粗鬆症の診断、及び老化の度合いの推定などに応用できる可能性がある。また、毛髪の分光分析により重金属中毒などの診断にも適用できると考えられる。
【0051】なお、本発明は上記実施例に限定されるものではなく、本発明の趣旨に基づいて種々の変形が可能であり、これらを本発明の範囲から排除するものではない。
【0052】
【発明の効果】上記したように、本発明によれば、以下のような効果を奏する。
(1)請求項1記載の発明によれば、単一のレーザパルスを照射するだけで、容易に、蒸散物質の発光プルームの分光分析を行うことができ、瞬時に無侵襲の光診断を行うことができる。
【0053】また、生体組織表面から発生する後方プルームの分光分析によりCa,Na,Kなどのイオン化率の高い微量の金属イオンを効率良く検出することができる。
(2)請求項2記載の発明によれば、蒸散物質の発光プルームの分光分析を迅速、かつ確実に行うことができる。
(3)請求項3記載の発明によれば、汎用性のある光源を用いて蒸散物質の発光プルームの分光分析を迅速、かつ確実に行うことができる。
【0054】(4)請求項4記載の発明によれば、診断装置の小型化が可能である(5)請求項5記載の発明によれば、従来の蛍光診断法と異なり、検出される発光プルームの波長に比べて、光源のレーザ波長は必ずしも短い必要はなくなる。
(6)請求項6記載の発明によれば、一個のレーザパルスの照射によって極めて低侵襲な分光診断を的確に行うことができる。
【0055】(7)請求項7記載の発明によれば、特定の範囲の波長成分がそれぞれ異なる出射角度で一度に出射され、波長ごとに分散を行うことができる。
(8)請求項8記載の発明によれば、格子溝の密度を変えることにより、分解能の調整を行うことができる。
(9)請求項9記載の発明によれば、高速ゲートイメージインテンシファイアーからの出射光は、CCDカメラの各画素に像を映し出すことができる。
【0056】(10)請求項10記載の発明によれば、高速ゲートイメージインテンシファイアーとCCDカメラとを前記光源のトリガーパルスに同期させ、確実な分光画像を得ることができる。
(11)請求項11記載の発明によれば、毛髪、爪、歯牙等の生体硬組織のレーザアブレーションにより、例えば、Ca含有量を同定することができ、骨粗鬆症の診断を行うことができる。
【0057】(12)請求項12記載の発明によれば、血管壁、表皮下組織等の生体軟組織のレーザアブレーションにより、例えば、有機化合物含有量を同定することができ、無侵襲の光診断を行うことができる。
【図面の簡単な説明】
【図1】本発明の実施例を示すナノ秒時間ゲート分光システムの構成図である。
【図2】本発明に係る多チャンネル型分光器(ポリクロメータ)の構成を示す模式図である。
【図3】本発明に係る分光画像処理の流れを示す図である。
【図4】本発明に係る波長の較正の方法を示す図である。
【図5】本発明に係る高速ゲートイメージインテンシファイアーのゲート幅を変化させて測定した結果を示す図である。
【図6】本発明の第1の具体例を示すヒト指爪から発生する発光プルームの時間的推移の測定結果を示す図である。
【図7】本発明の第1の具体例を示すヒト指爪での発光プルーム分析結果を示す図である。
【図8】本発明の第2の具体例を示すヒトの毛髪での発光プルーム分析結果を示す図である。
【図9】本発明の第3の具体例を示すヒトの歯牙での発光プルーム分析結果を示す図である。
【図10】本発明の第4の具体例を示す鶏の皮の発光プルーム分析結果を示す図である。
【符号の説明】
1 光源(フラッシュランプ励起あるいは半導体レーザ励起QスイッチNd:YAGレーザ又は半導体レーザ励起の全固体QスイッチNd:YAGレーザ)
2 レーザコントローラ
3 ハーフレンズ
4,12 集光レンズ
5 光検出器(アバランシェフォトダイオード:APD)
6 オシロスコープ
7 ゲート制御器
8 パルス発生器(PG)
9 CCDカメラ
10 データ処理装置(パーソナルコンピュータ:PC)
10A フレームグラバー(フレーム画像データ蓄積器)
11 シャッター
13 生体組織(ヒト指爪)
14 発光プルーム
15 光ファイバ
16 ポリクロメータ(多チャンネル型分光器)
16A 入射スリット
16B,16C,16G 反射鏡
16D〜16F グレーティング
16H 出射口
17 高速ゲートイメージインテンシファイアー
【0001】
【発明の属する技術分野】本発明は、ナノ秒時間ゲート分光診断装置に関するものである。
【0002】
【従来の技術】従来、このような分野における文献として、以下に示すようなものが開示されている。
(1)医療機器事典編集委員会偏:“1987−88 医療機器事典”pp.426−436 産業調査会(2)“ENCYCLOPEDIA OF MEDICAL SCIENCES”pp.46−50 講談社(3)佐藤卓蔵著:“レーザCDプレーヤからX線レーザまで,”pp.146−170 電気書院(1987)
(4)加藤治文、山本秀樹、日吉利光:“光感受性物質によるガン治療効果”O plus E,No.160,pp.83−88(1993)
(5)島岡優策、近江雅人、春名正光:“生体レーザアブレーションのナノ秒ストロボ顕微観測”、電子情報通信学会MEとバイオサイバネティックス研究会、信学技報 MBE96−93(1996)
(6)Yusaku Shimaoka,Mitsuo Nakamura,Masato Ohmi,Masamitsu Haruna:“Nanosecond stroboscopic microscope for laser ablation of biological tissue,”Conference on Laser & Electro Optics/Pacific Rim(CLEO/PR’97),Paper FF3,Technical Digest pp. 261−262,Makuhari,Chiba,1997従来、実際の医療現場では、赤外のCO2 レーザやNd:YAGレーザがレーザメスとして手術用の切開、凝固に用いられてきた〔上記文献(1)及び(2)参照〕。
【0003】また、レーザ励起蛍光分析〔上記文献(3)及び(4)参照〕は有力な診断法として継続して検討されている。今後、これらのレーザ励起生体反応を先端医療技術として進展、活用していくためには、レーザパルス照射時の生体表面近傍における反応形態の時間的推移、及び表面から飛散する物質の組成分析を含む詳細な実験データの蓄積が必要である。
【0004】
【発明が解決しようとする課題】生体におけるレーザアブレーション、蛍光発生等の物理現象は、一般の無機物と同様に〔上記文献(3)及び(4)参照〕ナノ秒あるいはそれ以下の反応速度を持つ。したがって、これらの分光分析を行うには、ナノ秒オーダーでの光測定技術を必要とする。ここで、生体レーザアブレーションとは、レーザパルス照射によって生体組織が熱的あるいは光化学的に分解し、瞬時に蒸散する現象である。
【0005】本発明者等は、既に、ナノ秒ストロボ観測システムを構築し、生体レーザアブレーションダイナミクス分析を行っている〔上記文献(5)及び(6)参照〕。その中で特にプルーム発光スペクトル分析を行うことによって、生体組織の組成分析あるいは正常部と病変部の識別を行える可能性がある。これは蛍光分析法と並んで、将来の光生体検査(optical biopsy)を支えるキーテクノロジーとなることが期待できる。
【0006】発光スペクトル分析法として、モノクロメータを用いたストロボ分光があるが〔上記文献(6)参照〕、これは単一レーザパルス照射では、特定の一波長しか測定できない。それ故、プルームの発光スペクトルを得るには、長い測定時間とそれに伴う試料の損傷という欠点があり、臨床への応用は難しいと考えられる。本発明は、上記問題点を解決するために、ナノ秒時間オーダーのゲート幅を持つ高速ゲートイメージインテンシファイアーを含む光マルチチャネルアナライザを用い、単一レーザパルス照射で発光プルームの分光分析を瞬時に行うことができるナノ秒時間ゲート分光診断装置を提供することを目的とする。
【0007】
【課題を解決するための手段】本発明は、上記目的を達成するために、〔1〕光源からのレーザパルスを生体組織に集光・照射し、レーザアブレーション(レーザ蒸散)によってこの生体組織表面から発生する発光プルーム(紡錘形発光体)をナノ秒の時間ゲートで分光し、この分光スペクトルをもとに前記生体組織の成分を分析し生体の病変・異常を診断するナノ秒時間ゲート分光診断装置であって、光源と生体組織に対向するレンズ間に配置されるシャッターと、前記発光プルームを検出する多チャンネル型分光器(ポリクロメータ)と、前記光源からのレーザパルスの一部を検出する光検出器と、この光検出器からの出力をモニターして高速ゲートイメージインテンシファイアーのゲートトリガーパルスの遅延時間を測定するためのオシロスコープと、レーザパルスに同期して二つの出力パルスの遅延時間を独立かつ任意に設定できるパルス発生器と、このパルス発生器およびオシロスコープに接続されるゲート制御器と、このゲート制御器によってゲートがナノ秒オーダーの時間間隔で開放され前記多チャンネル型分光器の出力光を増強・撮像する前記高速ゲートイメージインテンシファイアーと、この高速ゲートイメージインテンシファイアーの出力像を捕らえるCCDカメラと、このCCDカメラの一フレームの分光画像データを時系列アナログ信号として取込み、アナログ信号をデジタル信号に変換してコンピュータに送り込むフレーム画像データ蓄積器(フレームグラバー)を含むデータ処理装置とを設けるようにしたものである。
【0008】〔2〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、レーザアブレーションによって生体組織を蒸発・励起し、これによって発生する発光プルームの分光スペクトルをナノ秒オーダーの時間間隔で検出するようにしたものである。
〔3〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記光源は紫外光、可視光、赤外光領域におけるナノ秒レーザパルスを発生可能なレーザ光源である。
【0009】〔4〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記レーザ光源はフラッシュランプ励起あるいは半導体レーザ励起QスイッチNd:YAGレーザ又は半導体レーザ励起の全固体QスイッチNd:YAGレーザである。
〔5〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記光源のレーザ波長は検出される発光プルームの波長に比べて長い領域をも含むようにしたものである。
【0010】〔6〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記光源と生体組織の間にシャッターを配置して一個のレーザパルス照射によって極めて低侵襲な分光診断が可能である。
〔7〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記多チャンネル型分光器は、入射スリットから入射した光を複数のグレーティングで波長ごとに分散し、特定の範囲の波長成分がそれぞれ異なる出射角度で一度に出射口から出射される構成を有するようにしたものである。
【0011】〔8〕上記〔7〕記載のナノ秒時間ゲート分光診断装置において、前記複数のグレーティングは格子溝の密度が300本/mm、600本/mm、1200本/mmの何れかを設定可能であるようにしたものである。
〔9〕上記〔7〕記載のナノ秒時間ゲート分光診断装置において、前記多チャンネル型分光器の出射口から出射される特定の範囲の波長成分は前記CCDカメラの各画素に像を映し出すように構成したものである。
【0012】〔10〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記高速ゲートイメージインテンシファイアーとCCDカメラとを前記光源のトリガーパルスに同期させる手段とを具備するようにしたものである。
〔11〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記生体組織は毛髪、爪、歯牙等の生体硬組織である。
【0013】〔12〕上記〔1〕記載のナノ秒時間ゲート分光診断装置において、前記生体組織は血管壁、表皮下組織等の生体軟組織である。
【0014】
【発明の実施の形態】以下、本発明の実施の形態について詳細に説明する。本発明では、生体レーザアブレーションによるナノ秒時間ゲート分光システムを構築し、レーザ光源、パルス同期・遅延制御・発生系、時間ゲート分光系、分光画像処理系、それぞれの特性・機能について説明する。更に、実際にこの測定を行う際のゲート幅を決定した。
【0015】図1は本発明の実施例を示すナノ秒時間ゲート分光システムの構成図である。この図において、1は光源(例えば、フラッシュランプあるいは半導体レーザ励起QスイッチNd:YAGレーザ又は半導体レーザ励起の全固体QスイッチNd:YAGレーザ)、2はその光源1に接続されるレーザコントローラ、3はハーフミラー、4,12はレンズ、5は光検出器(アバランシェフォトダイオード:APD)、6はゲートパルス遅延時間測定/モニター用のオシロスコープ、7は高速ゲートイメージインテンシファイアーのゲート制御器、8はパルス発生器(PG)、9はCCDカメラ、10は画像演算処理機能をもつデータ処理装置(パーソナルコンピュータ:PC)、10Aはフレーム画像データ蓄積器(フレームグラバー)、11はシャッター、13は生体組織(ヒト指爪等)、14は発光プルーム、15は光ファイバ、16はポリクロメータ(多チャンネル型分光器)、17は高速ゲートイメージインテンシファイアーである。
【0016】以下、本発明の実施例を示すナノ秒時間ゲート分光システムの動作について、説明する。まず、光源(例えば、QスイッチNd:YAGレーザ)1からのレーザパルス(パルス幅10〜90ナノ秒)をシャッター11を通して一個だけ生体組織(ヒト指爪等)13に集光・照射すると、表面から微量の組織(約50ミクロン径で、深さ数ミクロン程度)が蒸散(アブレーション)されて励起状態になり発光プルーム(紡錘形の発光体)14が発生する。
【0017】また、レーザ照射直後に、主に生体組織(ヒト指爪)13表面近傍の水分が蒸散され、紡錘形の明るい発光プルーム(これを先行プルームと呼ぶ)が発生し成長する。さらに、レーザ照射後、約100ナノ秒経過すると、生体組織(ヒト指爪)表面が剥離されて、「後方プルーム」が発生する。これが対象とする生体組織の成分を含む蒸散・励起物質である。
【0018】したがって、上記の後方プルームの発光スペクトルを測定するために、光源1からのレーザパルスの一部を光検出器〔アバランシェフォトダイオード(APD〕5で検出し、この時刻を基準として、パルス発生器8から出力されるゲートトリガー用パルスの遅延時間をオシロスコープ6で所定の300〜400ナノ秒に測定・設定して、高速ゲートイメージインテンシファイアー17のゲート制御器7により、高速ゲートイメージインテンシファイアー17のゲートを10ナノ秒の時間間隔で開放する。これによって、光ファイバ15およびポリクロメータ16を用いて検出する後方プルームの発光スペクトルの10ナノ秒時間ゲート分光像を取り込む。
【0019】さらに、高速ゲートイメージインテンシファイアー17の出力像(分光イメージデータ)をCCDカメラ9で捕らえ、時系列の信号パルスに変換して、その信号データをフレームグラバー10A(フレーム画像データ蓄積器)を介して、パーソナルコンピュータを含むデータ処理装置10に取り込んで処理する。なお、フレームグラバーとは、CCDあるいはテレビの一画面(一フレーム)のデータを時系列信号として所定のメモリに蓄積/格納し、この時系列信号(アナログ信号)を8ビットあるいは10ビットのデジタル信号に変換してコンピュータに送り込む。メモリサイズによって異なるが、通常は10フレーム以上の画像データを同時に蓄積/格納でき、必要に応じて、所望のフレームデータをコンピュータに送り込む。
【0020】この装置では、光波長300〜900nmの範囲内(この範囲を四つのレンジに分けて測定)の光スペクトルを、波長分解能1nmで測定・表示することができる。このように、ナノ秒時間ゲート分光システムによれば、単一のレーザパルスを照射するだけで、蒸散物質の発光プルームの分光分析を行うことができ、ほぼ無侵襲の光診断を行うことができる。
【0021】特に、Ca、Na、Kなどのイオン化率の高い微量の金属イオンが効率良く検出できる。したがって、例えば、この装置で爪や毛髪のCa含有量を同定することによって、老年者の骨粗鬆症の診断が行える可能性を有している。上述のように、プローブ用のレーザパルスを用いて極微量の生体組織を蒸散させ、組織の病変を診断しようとする手法・装置は新規であり、従来の蛍光診断法と共に、光生体検査(光バイオプシ)のキーテクノロジー・装置として発展する可能性を充分に有するものである。
【0022】また、半導体レーザ(LD)励起の全固体Nd:YAGレーザを用いれば、診断装置の小型化が可能である。以下、ナノ秒時間ゲート分光システムの各部の詳細な説明を行う。照射レーザにはQスイッチNd:YAGレーザを用い、波長は基本波の1064nmである。レーザを焦点距離f=100mmレンズ12で集光して生体組織(ヒト指爪)13に照射し、生体組織をアブレーションする。
【0023】その場合、レンズ12の前にシャッタ11を挿入することによって、シャッタ11が開いた瞬間のみ1発だけ生体組織(ヒト指爪)13にレーザパルスを照射し、アブレーションが起こるようにした。発生したプルーム14の発光を光ファイバ15を通してポリクロメータ16に入射させた。入射した光はポリクロメータ16内に設けられたグレーティングで分光した後に出射される。この分光像は、高速ゲートイメージインテンシファイアー17で像増強され、その蛍光面に結像する。この蛍光像はCCDカメラ9によって分光画像として取り込まれる。さらに、CCDの画像データを時系列の信号としてフレームグラバー10Aに取り込み、アナログ信号をデジタル信号に変換してデータ処理する。
【0024】ポリクロメータ16から出射される分光像は横方向(光波長に対応する方向)に拡がり、これを10ナノ秒の時間ゲート(シャッター速度)で撮像するには、3〜6桁に及ぶ像信号の増強が必要である。このために用いる高速ゲートイメージインテンシファイアー17としては、例えば、浜松ホトニクス製C4078−01Xでゲート幅(シャッター速度に相当する量)は最小3ナノ秒である。ポリクロメータ(多チャンネル型分光器)16としては、アクトンリサーチ社のSpectra Pro−300i,Model SP−306を用いた。これには3種のグレーティングが内蔵されており、測定波長域300〜900nm、分解能1nmである。
【0025】図2は本発明に係るポリクロメータの構成を示す模式図である。この図に示すように、入射スリット16Aから入射した光は、グレーティング16D〜16Fで波長成分に分離(分光)される。なお、16B,16C,16Gは反射鏡である。ポリクロメータからは所定の波長範囲の分光スペクトル成分がそれぞれ異なる出射角度で一度に出射口16Hから出射され、これらはCCDカメラ上のそれぞれ異なる位置で検出される。
【0026】次に、分光画像処理系について説明する。ポリクロメータ16の中のグレーティング16D〜16Fで分散された光はCCDカメラ9に分光画像として映し出される。このときの分光画像は横軸が波長に対応したものである。この時系列のデータをパーソナルコンピュータに取り込み処理した。
【0027】図3は本発明に係る分光画像処理の流れを示す図であり、図3(a)はポリクロメータ16の中のグレーティング16D〜16Fによる光の分散を示す図、図3(b)はCCDカメラ9の分光画像を示す図、図3(c)は最終的に得られる分光スペクトルを示す図である。グレーティング16D〜16Fでは縦方向には分散されないので、縦軸は全て同じ波長成分のものである。よって縦軸方向に積分することにより、図3(c)に示すように、スペクトルを得ることができる。この処理はスペクトル解析ソフトウエアWin・Viewを用いて行った。
【0028】次に、波長スケールの較正について説明する。ポリクロメータ16からの出射光はCCDカメラ9の各画素に像を映し出すが、それがどの波長に対応するかを較正する必要がある。ここでは、水銀灯を用いて較正を行った。図4は本発明に係る波長の較正の方法を示す図であり、図4(a)は既知である水銀灯のスペクトルを示す図、図4(b)はその水銀灯の分光画像を示す図、図4(c)はその較正された分光画像を示す図である。
【0029】まず、図4(a)に示すように、水銀灯を分光させ、図4(b)に示すように、その分光像を取り込む。既に、知られている水銀の発光の輝線がこの波長範囲に2つ存在し、その波長は405nmと435nmである。分光像にも現れた2つの輝線に、この2点を割り当てることで、波長範囲内全ての波長の較正ができる。この処理には、スペクトル解析ソフトウエアWin・Specを用いた。
【0030】次に、同期パルス・遅延系について説明する。ナノ秒オーダーの分光分析を行う上では、同期系は極めて重要である。図1に示すように、出力レーザパルスの検出にはアバランシェフォトダイオード(APD)5を用い、その出力信号及び高速ゲートイメージインテンシファイアー17のゲート信号をオシロスコープ6で同期モニターして、パルス発生器8から出力されるゲート信号の遅延時間を測定した。
【0031】また、高速ゲートイメージインテンシファイアー17のゲート幅及び遅延時間(td )はパルス発生器(PG)8で制御する。高速ゲートイメージインテンシファイアー17と、CCDカメラ9はQスイッチNd:YAGレーザ1に同期して駆動する。次に、高速ゲートイメージインテンシファイアーのゲート幅の決定について、説明する。
【0032】プルームの発光スペクトルの分光分析を行う場合のゲート幅(tg )を決定するために、高速ゲートイメージインテンシファイアー17のゲート幅を変化させて測定した。図5はその高速ゲートイメージインテンシファイアーのゲート幅を変化させて測定した結果を示す図であり、図5(a)はそのゲート幅が50ns、遅延時間td が150nsの場合のヒト歯牙の発光スペクトを示す図、図5(b)はそのゲート幅が10nsで遅延時間を110ns、120ns、130ns、140ns、150nsとずらした場合のヒト歯牙の発光スペクトを示す図である。
【0033】図5(a)に示すように、ゲート幅が50nsの時はレーザ照射時からの遅延時間td =150nsであっても、実際はレーザパルス照射後100nsから150nsと分割された発光を取り込んでいることになる。図5(a)から明らかなように、この測定でもある程度輝線が見分けられる。しかし、図5(b)に示すように、ゲート幅を10nsにして同じレーザパルス照射後100nsから150nsまでを5分割し、測定してみると、この間でプルームのスペクトルは大きく変化していることが分かる。すなわち、ゲート幅が50nsでほかの輝線に埋もれて見にくかった390nm付近の輝線も、ゲート幅10ns、遅延時間td =150ns迄は、はっきりと確認できた。
【0034】その結果、ゲート幅が50nsでは時間分解が不十分であるといえる。ゲート幅は3nsまで短くできるが、光量が減ってしまうため、ゲート幅は10nsを採用した。次に、レーザ照射条件及び分光分析条件について説明する。レーザアブレーション及び本発明のナノ秒時間ゲート分光測定条件を表1に示す。
【0035】
【表1】

【0036】分光測定条件としては発光プルームのスペクトルの時間分解能を示すゲート幅や、グレーティングによって変わる測定波長範囲などがある。ゲート幅は10nsであり、測定波長範囲は格子溝が300本/mmのグレーティングを用いているので180nmであった。このように、本発明によれば、単一レーザパルス照射で発光プルームの分光分析を瞬時に行うことができる。
【0037】また、試料の前にシャッターを挿入することによって、単一レーザパルス照射を可能とした。さらに、QスイッチNd:YAGレーザのトリガーパルスで高速ゲートイメージインテンシファイアーとCCDカメラを同期させることによって、レーザアブレーションによる発光現象と、その分光画像の取り込みを同期させることができる。
【0038】以下、本発明の具体例について説明する。生体レーザアブレーションのナノ秒時間ゲート分光分析を行った。また、レーザアブレーション後の生体組織の変化を確認するために、顕微鏡写真を撮って考察した。
(1)発光プルームの時間的推移ストロボ顕微観測により、QスイッチNd:YAGレーザの基本波λ=1064nmをヒト歯牙に照射した際に、大気中で成長速度の違う2つのプルーム、先行および後方プルームが観測された。これらの2つのプルームを時間的に分離するために、まずヒト指爪を用いてプルームの発光スペクトルの時間的推移を測定した。
【0039】図6は本発明の第1の具体例を示すヒト指爪から発生する発光プルームの時間的推移の測定結果を示す図であり、図6(a)はその遅延時間td が200nsの場合の発光スペクトルの強度、図6(b)はその遅延時間td が300nsの場合の発光スペクトルの強度、図6(c)はその遅延時間td が400nsの場合の発光スペクトルの強度である。なお、どの場合にも、レーザパルス幅は35ns、高速ゲートイメージインテンシファイアーゲート幅は10ns、パルスエネルギーは17mJである。
【0040】この図を見ると、遅延時間td =200ns(レーザ照射後200ns)では波長500nm付近に強い輝線が見られる。しかし、この輝線は遅延時間td =300ns、400nsでは徐々に減衰していくのが見られる。これより、先行プルームの成分である窒素(N)の輝線であると考えられる。
【0041】一方、波長390nm付近に遅延時間td =300nsあたりから成長する輝線が見られる。これは後方プルームに含まれるカルシウム(Ca)の発光スペクトルである。このように、td =300ns以降では、先行プルームの影響が急激に減少し、生体組織の成分を反映する後方プルームの発光スペクトルが支配的となるので、時間ゲート分光の結果に基づいて生体組織の組成分析が可能になる。
【0042】(2)発光プルームの分光分析図7は本発明の第1の具体例を示すヒト指爪での発光プルーム分析結果を示す図である。なお、この図において、レーザパルス幅は35ns、高速ゲートイメージインテンシファイアーゲート幅は10ns、パルスエネルギーは17mJである。
【0043】図7に示すように、後方プルームの成分を分析するために遅延時間td =400nsで行った。単一パルス照射で測定できる範囲は180nmであるので、4回に分けて測定し、380nmから900nmまでのスペクトルを得た。これによれば、390nm付近に2本の強い輝線が見られる。これは上記したように、カルシウム(Ca)の輝線である。その他、589nmにナトリウム(Na)、658nmに炭素(C)と推定できる輝線が見られた。残りのピークについてはカルシウム(Ca)や酸素(O)及びリン酸(HPO)などと考えられるものがあるが、その付近に様々な組成元素の輝線があるために限定し難い。
【0044】また、400nmから500nmにかけて幅の広い吸収スペクトルが見られる。これも特定には至っていないが、有機化合物でこの様なスペクトルが見られると言われており、今後検討する必要がある。ヒト指爪におけるCaの含有量は0.1%程度である。それにも関わらず、爪の主成分であるケラチンを構成する炭素(C)の輝線よりも強いことが確認できた。この事実から、本測定システムではカルシウム(Ca)の感度が非常に高いことが分かった。このことより、カルシウムの輝線に注目し、様々な生体組織での分光分析を行った。
【0045】次に、様々な生体組織での分光分析結果について説明する。
(1)ヒトの毛髪での分析結果図8は本発明の第2の具体例を示すヒトの毛髪での発光プルーム分析結果を示す図である。なお、この図において、レーザパルス幅は35ns、高速ゲートイメージインテンシファイアーゲート幅は10ns、パルスエネルギーは17mJである。
【0046】図8に示すように、測定は遅延時間td =400nsで行った。毛髪においてもCaの含有量は約0.1%であるが、Caの輝線が顕著に見られた。この測定は、レーザのスポットサイズが直径50μmと小さいため、一本の毛髪で行うことができた。毛髪は重金属を排泄する役割を担っており、これに関しての医療への応用が期待できる。
【0047】(2)ヒト歯牙での分析結果図9は本発明の第3の具体例を示すヒトの歯牙での発光プルーム分析結果を示す図である。なお、この図において、レーザパルス幅は35ns、高速ゲートイメージインテンシファイアーゲート幅は10ns、パルスエネルギーは17mJである。
【0048】図9に示すように、測定は遅延時間td =400nsで行った。成分の36%がカルシウムであるヒト歯牙(エナメル質)では、Caの輝線は爪や毛髪と比べて、とても強いことが分かった。
(3)鶏の皮での分光分析結果図10は本発明の第4の具体例を示す鶏の皮の発光プルーム分析結果を示す図である。なお、この図において、レーザパルス幅は35ns、高速ゲートイメージインテンシファイアーゲート幅は10ns、パルスエネルギーは17mJである。
【0049】図10に示すように、測定は遅延時間td =400nsで行った。鶏の皮はCa成分をほとんど含まない表皮であるので、ほとんどCaのピークが見られなかった。一方、360nmから540nmの全範囲にわたって、幅の広い吸収スペクトルのようなものが見られた。これは上記した発光プルームの分光分析でも触れたように、有機化合物によるものと推定される。
【0050】このように、本発明のナノ秒時間ゲート分光システムにおいて、QスイッチNd:YAGレーザの基本波1064nmを用い、レーザアブレーションに伴う発光プルームで生体組織の分光分析を行った。その結果、高感度で生体組織のカルシウムの輝線を見出すことができた。またカルシウム輝線の強度とカルシウム含有量は対応していると見なすことができ、このことが臨床光診断の手がかりになると考えている。例えば、上記で顕著に見られたカルシウム(Ca)の輝線から骨粗鬆症の診断、及び老化の度合いの推定などに応用できる可能性がある。また、毛髪の分光分析により重金属中毒などの診断にも適用できると考えられる。
【0051】なお、本発明は上記実施例に限定されるものではなく、本発明の趣旨に基づいて種々の変形が可能であり、これらを本発明の範囲から排除するものではない。
【0052】
【発明の効果】上記したように、本発明によれば、以下のような効果を奏する。
(1)請求項1記載の発明によれば、単一のレーザパルスを照射するだけで、容易に、蒸散物質の発光プルームの分光分析を行うことができ、瞬時に無侵襲の光診断を行うことができる。
【0053】また、生体組織表面から発生する後方プルームの分光分析によりCa,Na,Kなどのイオン化率の高い微量の金属イオンを効率良く検出することができる。
(2)請求項2記載の発明によれば、蒸散物質の発光プルームの分光分析を迅速、かつ確実に行うことができる。
(3)請求項3記載の発明によれば、汎用性のある光源を用いて蒸散物質の発光プルームの分光分析を迅速、かつ確実に行うことができる。
【0054】(4)請求項4記載の発明によれば、診断装置の小型化が可能である(5)請求項5記載の発明によれば、従来の蛍光診断法と異なり、検出される発光プルームの波長に比べて、光源のレーザ波長は必ずしも短い必要はなくなる。
(6)請求項6記載の発明によれば、一個のレーザパルスの照射によって極めて低侵襲な分光診断を的確に行うことができる。
【0055】(7)請求項7記載の発明によれば、特定の範囲の波長成分がそれぞれ異なる出射角度で一度に出射され、波長ごとに分散を行うことができる。
(8)請求項8記載の発明によれば、格子溝の密度を変えることにより、分解能の調整を行うことができる。
(9)請求項9記載の発明によれば、高速ゲートイメージインテンシファイアーからの出射光は、CCDカメラの各画素に像を映し出すことができる。
【0056】(10)請求項10記載の発明によれば、高速ゲートイメージインテンシファイアーとCCDカメラとを前記光源のトリガーパルスに同期させ、確実な分光画像を得ることができる。
(11)請求項11記載の発明によれば、毛髪、爪、歯牙等の生体硬組織のレーザアブレーションにより、例えば、Ca含有量を同定することができ、骨粗鬆症の診断を行うことができる。
【0057】(12)請求項12記載の発明によれば、血管壁、表皮下組織等の生体軟組織のレーザアブレーションにより、例えば、有機化合物含有量を同定することができ、無侵襲の光診断を行うことができる。
【図面の簡単な説明】
【図1】本発明の実施例を示すナノ秒時間ゲート分光システムの構成図である。
【図2】本発明に係る多チャンネル型分光器(ポリクロメータ)の構成を示す模式図である。
【図3】本発明に係る分光画像処理の流れを示す図である。
【図4】本発明に係る波長の較正の方法を示す図である。
【図5】本発明に係る高速ゲートイメージインテンシファイアーのゲート幅を変化させて測定した結果を示す図である。
【図6】本発明の第1の具体例を示すヒト指爪から発生する発光プルームの時間的推移の測定結果を示す図である。
【図7】本発明の第1の具体例を示すヒト指爪での発光プルーム分析結果を示す図である。
【図8】本発明の第2の具体例を示すヒトの毛髪での発光プルーム分析結果を示す図である。
【図9】本発明の第3の具体例を示すヒトの歯牙での発光プルーム分析結果を示す図である。
【図10】本発明の第4の具体例を示す鶏の皮の発光プルーム分析結果を示す図である。
【符号の説明】
1 光源(フラッシュランプ励起あるいは半導体レーザ励起QスイッチNd:YAGレーザ又は半導体レーザ励起の全固体QスイッチNd:YAGレーザ)
2 レーザコントローラ
3 ハーフレンズ
4,12 集光レンズ
5 光検出器(アバランシェフォトダイオード:APD)
6 オシロスコープ
7 ゲート制御器
8 パルス発生器(PG)
9 CCDカメラ
10 データ処理装置(パーソナルコンピュータ:PC)
10A フレームグラバー(フレーム画像データ蓄積器)
11 シャッター
13 生体組織(ヒト指爪)
14 発光プルーム
15 光ファイバ
16 ポリクロメータ(多チャンネル型分光器)
16A 入射スリット
16B,16C,16G 反射鏡
16D〜16F グレーティング
16H 出射口
17 高速ゲートイメージインテンシファイアー
【特許請求の範囲】
【請求項1】 光源からのレーザパルスを生体組織に集光・照射し、レーザアブレーションによって該生体組織表面から発生する発光プルームをナノ秒の時間ゲートで分光し、この分光スペクトルをもとに前記生体組織の成分を分析し生体の病変・異常を診断するナノ秒時間ゲート分光診断装置であって、(a)光源と生体組織に対向するレンズ間に配置されるシャッターと、(b)前記発光プルームを検出する多チャンネル型分光器と、(c)前記光源からレーザパルスの一部を検出する光検出器と、(d)該光検出器からの出力をモニターして高速ゲートイメージインテンシファイアーのゲートトリガーパルスの遅延時間を測定するためのオシロスコープと、(e)レーザパルスに同期して二つの出力パルスの遅延時間を独立かつ任意に設定できるパルス発生器と、(f)該パルス発生器およびオシロスコープに接続されるゲート制御器と、(g)該ゲート制御器によってゲートがナノ秒オーダーの時間間隔で開放され前記多チャンネル型分光器の出力光を増強・撮像する前記高速ゲートイメージインテンシファイアーと、(h)該高速ゲートイメージインテンシファイアーの出力像を捕らえるCCDカメラと、(i)該CCDカメラの一フレームの分光画像データを時系列アナログ信号として取込み、アナログ信号をデジタル信号に変換してコンピュータに送り込むフレーム画像データ蓄積器を含むデータ処理装置とを具備することを特徴とするナノ秒時間ゲート分光診断装置。
【請求項2】 請求項1記載のナノ秒時間ゲート分光診断装置において、レーザアブレーションによって生体組織を蒸発・励起し、これによって発生する発光プルームの分光スペクトルをナノ秒オーダーの時間間隔で検出することを特徴とするナノ秒時間ゲート分光診断装置。
【請求項3】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記光源は紫外光、可視光、赤外光領域におけるナノ秒レーザパルスを発生可能なレーザ光源であることを特徴とするナノ秒時間ゲート分光診断装置。
【請求項4】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記レーザ光源はフラッシュランプ励起あるいは半導体レーザ励起QスイッチNd:YAGレーザ又は半導体レーザ励起の全固体QスイッチNd:YAGレーザであることを特徴とするナノ秒時間ゲート分光診断装置。
【請求項5】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記光源のレーザ波長は検出される発光プルームの波長に比べて長い領域をも含むことを特徴とするナノ秒時間ゲート分光診断装置。
【請求項6】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記光源と生体組織の間にシャッターを配置して一個のレーザパルス照射によって極めて低侵襲な分光診断が可能であることを特徴とするナノ秒時間ゲート分光診断装置。
【請求項7】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記多チャンネル型分光器は、入射スリットから入射した光を複数のグレーティングで波長ごとに分散し、特定の範囲の波長成分がそれぞれ異なる出射角度で一度に出射口から出射される構成を有することを特徴とするナノ秒時間ゲート分光診断装置。
【請求項8】 請求項7記載のナノ秒時間ゲート分光診断装置において、前記複数のグレーティングは格子溝の密度が300本/mm、600本/mm、1200本/mmの何れかを設定可能であることを特徴とするナノ秒時間ゲート分光診断装置。
【請求項9】 請求項7記載のナノ秒時間ゲート分光診断装置において、前記多チャンネル型分光器の出射口から出射される特定の範囲の波長成分は前記CCDカメラの各画素に像を映し出すように構成したことを特徴とするナノ秒時間ゲート分光診断装置。
【請求項10】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記高速ゲートイメージインテンシファイアーとCCDカメラとを前記光源のトリガーパルスに同期させる手段とを具備することを特徴とするナノ秒時間ゲート分光診断装置。
【請求項11】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記生体組織は毛髪、爪、歯牙等の生体硬組織であることを特徴とするナノ秒時間ゲート分光診断装置。
【請求項12】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記生体組織は血管壁、表皮下組織等の生体軟組織であることを特徴とするナノ秒時間ゲート分光診断装置。
【請求項1】 光源からのレーザパルスを生体組織に集光・照射し、レーザアブレーションによって該生体組織表面から発生する発光プルームをナノ秒の時間ゲートで分光し、この分光スペクトルをもとに前記生体組織の成分を分析し生体の病変・異常を診断するナノ秒時間ゲート分光診断装置であって、(a)光源と生体組織に対向するレンズ間に配置されるシャッターと、(b)前記発光プルームを検出する多チャンネル型分光器と、(c)前記光源からレーザパルスの一部を検出する光検出器と、(d)該光検出器からの出力をモニターして高速ゲートイメージインテンシファイアーのゲートトリガーパルスの遅延時間を測定するためのオシロスコープと、(e)レーザパルスに同期して二つの出力パルスの遅延時間を独立かつ任意に設定できるパルス発生器と、(f)該パルス発生器およびオシロスコープに接続されるゲート制御器と、(g)該ゲート制御器によってゲートがナノ秒オーダーの時間間隔で開放され前記多チャンネル型分光器の出力光を増強・撮像する前記高速ゲートイメージインテンシファイアーと、(h)該高速ゲートイメージインテンシファイアーの出力像を捕らえるCCDカメラと、(i)該CCDカメラの一フレームの分光画像データを時系列アナログ信号として取込み、アナログ信号をデジタル信号に変換してコンピュータに送り込むフレーム画像データ蓄積器を含むデータ処理装置とを具備することを特徴とするナノ秒時間ゲート分光診断装置。
【請求項2】 請求項1記載のナノ秒時間ゲート分光診断装置において、レーザアブレーションによって生体組織を蒸発・励起し、これによって発生する発光プルームの分光スペクトルをナノ秒オーダーの時間間隔で検出することを特徴とするナノ秒時間ゲート分光診断装置。
【請求項3】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記光源は紫外光、可視光、赤外光領域におけるナノ秒レーザパルスを発生可能なレーザ光源であることを特徴とするナノ秒時間ゲート分光診断装置。
【請求項4】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記レーザ光源はフラッシュランプ励起あるいは半導体レーザ励起QスイッチNd:YAGレーザ又は半導体レーザ励起の全固体QスイッチNd:YAGレーザであることを特徴とするナノ秒時間ゲート分光診断装置。
【請求項5】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記光源のレーザ波長は検出される発光プルームの波長に比べて長い領域をも含むことを特徴とするナノ秒時間ゲート分光診断装置。
【請求項6】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記光源と生体組織の間にシャッターを配置して一個のレーザパルス照射によって極めて低侵襲な分光診断が可能であることを特徴とするナノ秒時間ゲート分光診断装置。
【請求項7】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記多チャンネル型分光器は、入射スリットから入射した光を複数のグレーティングで波長ごとに分散し、特定の範囲の波長成分がそれぞれ異なる出射角度で一度に出射口から出射される構成を有することを特徴とするナノ秒時間ゲート分光診断装置。
【請求項8】 請求項7記載のナノ秒時間ゲート分光診断装置において、前記複数のグレーティングは格子溝の密度が300本/mm、600本/mm、1200本/mmの何れかを設定可能であることを特徴とするナノ秒時間ゲート分光診断装置。
【請求項9】 請求項7記載のナノ秒時間ゲート分光診断装置において、前記多チャンネル型分光器の出射口から出射される特定の範囲の波長成分は前記CCDカメラの各画素に像を映し出すように構成したことを特徴とするナノ秒時間ゲート分光診断装置。
【請求項10】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記高速ゲートイメージインテンシファイアーとCCDカメラとを前記光源のトリガーパルスに同期させる手段とを具備することを特徴とするナノ秒時間ゲート分光診断装置。
【請求項11】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記生体組織は毛髪、爪、歯牙等の生体硬組織であることを特徴とするナノ秒時間ゲート分光診断装置。
【請求項12】 請求項1記載のナノ秒時間ゲート分光診断装置において、前記生体組織は血管壁、表皮下組織等の生体軟組織であることを特徴とするナノ秒時間ゲート分光診断装置。
【図1】


【図2】


【図3】


【図8】


【図4】


【図6】


【図7】


【図5】


【図9】


【図10】




【図2】


【図3】


【図8】


【図4】


【図6】


【図7】


【図5】


【図9】


【図10】


【公開番号】特開平11−271226
【公開日】平成11年(1999)10月5日
【国際特許分類】
【出願番号】特願平10−75359
【出願日】平成10年(1998)3月24日
【出願人】(396020800)科学技術振興事業団 (35)
【公開日】平成11年(1999)10月5日
【国際特許分類】
【出願日】平成10年(1998)3月24日
【出願人】(396020800)科学技術振興事業団 (35)
[ Back to top ]

