ナノ粒子標識プローブ、その形成方法、及び核酸検出方法
【課題】遺伝子検査等において、より簡単で短時間に核酸検出を可能とするナノ粒子標識プローブ及びその形成方法を提供する。また、当該ナノ粒子標識プローブを用いた核酸検出方法を提供する。
【解決手段】核酸を認識し、ハイブリダイズすることが可能なプローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とするナノ粒子標識プローブ。
【解決手段】核酸を認識し、ハイブリダイズすることが可能なプローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とするナノ粒子標識プローブ。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は核酸を検出するためのナノ粒子標識プローブ及びその形成方法に関する。また本発明は当該ナノ粒子標識プローブを用いた核酸検出方法に関する。
【背景技術】
【0002】
遺伝子検査では検出に特異性を持たせるために、標的核酸に選択的にハイブリダイズすることが可能なプローブを用いるのが一般的である。プローブを用いた検出には様々な手法が存在し、蛍光分子を利用するもの、酵素を利用するもの、ナノ粒子を利用するもの、電気信号を検出するものなど、多種多様に及ぶ。その中でも、ナノ粒子を利用するものは、高い光学特性を有するため、検出が容易という利点がある。このようなナノ粒子を利用した核酸の検出は液相法(例えば特許文献1参照)及び固相法(例えば特許文献2参照)で行われている。
【0003】
しかしながら、ナノ粒子はサイズが1〜100nmとプローブに対して巨大であるため、固相法に適用したときに反応効率が低くなるという欠点があり、プローブにナノ粒子を直接標識したものを用いた検出は、溶液中でハイブリダイズが行われていた(特許文献1参照)。そして固相法に用いる場合は、核酸を固定化した後、ナノ粒子以外の標識がされたプローブを用いて一旦ハイブリダイズさせ、続いて、標識をナノ粒子で再度標識するという3段階のステップを取っていた(特許文献2及び図1参照)。しかし、このような複数のステップを経て検出する方法では、検出に時間と手間がかかるという問題があった。
【特許文献1】特開2004−275187号公報
【特許文献2】特開2006−21199号公報
【発明の開示】
【発明が解決しようとする課題】
【0004】
本発明は、上記問題に鑑みてなされたものであり、その解決課題は、遺伝子検査等において、より簡単で短時間に核酸検出を可能とするナノ粒子標識プローブ及びその形成方法を提供することである。また、当該ナノ粒子標識プローブを用いた核酸検出方法を提供することである。
【課題を解決するための手段】
【0005】
本発明に係る上記課題は下記の手段により解決される。
【0006】
1.核酸を認識し、ハイブリダイズすることが可能なプローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とするナノ粒子標識プローブ。
【0007】
2.前記ナノ粒子が金コロイド粒子であることを特徴とする前記1に記載のナノ粒子標識プローブ。
【0008】
3.前記1又は2に記載のナノ粒子標識プローブの形成方法であって、核酸を認識し、ハイブリダイズすることが可能なプローブに、抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させるステップ1と、前記ナノ粒子と結合しなかったプローブを除去するステップ2と、を有することを特徴とするナノ粒子標識プローブの形成方法。
【0009】
4.核酸を基盤に固定化するステップ1と、前記基盤に固定化されなかった核酸を除去するステップ2と、前記3に記載のナノ粒子標識プローブの形成方法で形成したナノ粒子標識プローブを加えて前記基盤に固定化した核酸にナノ粒子標識プローブをハイブリダイズさせるステップ3と、前記基盤に固定化した核酸にハイブリダイズしなかったナノ粒子標識プローブを除去するステップ4と、前記基盤に固定化した核酸にハイブリダイズしたナノ粒子標識プローブのナノ粒子が有する光学特性を検出することにより前記基盤に固定化した核酸を検出するステップ5と、を有することを特徴とする核酸検出方法。
【0010】
5.前記ナノ粒子標識プローブの分散液が、標識前と比べて、ナノ粒子の濃度換算で、3〜5倍に濃縮されていることを特徴とする前記4に記載の核酸検出方法。
【0011】
6.前記ナノ粒子が有する光学特性が吸光度であることを特徴とする前記4又は5に記載の核酸検出方法。
【発明の効果】
【0012】
本発明の上記手段により、遺伝子検査等において、より簡単で短時間に核酸検出を可能とするナノ粒子標識プローブ及びその形成方法を提供することができる。また、当該ナノ粒子標識プローブを用いた核酸検出方法を提供することができる。
【0013】
すなわち、本発明においては、ナノ粒子を予めプローブに反応させておくことで、従来よりも反応ステップが削減できる。これによって従来よりも検出時間の短縮が可能となる。また、従来のナノ粒子に直接プローブを結合させる方法と異なり、抗原・抗体又はアビジン・ビオチンを間に設けることによって、ナノ粒子−プローブ間の距離が広がり、固相法で反応効率が落ちるのを抑えることができるとともに、ナノ粒子−プローブ間の相互作用でナノ粒子やプローブの反応性が低下することを防ぐことができる。
【0014】
さらに、プローブをナノ粒子で標識する工程を最適な条件で予め行うことによって、反応効率が向上し、検出感度が向上する。加えて、ナノ粒子は遠心分離機によって容易に沈降させることが可能であるため、プローブと反応後、任意の濃度に濃縮することができ、濃度によって検出感度を調整することが可能となる。
【発明を実施するための最良の形態】
【0015】
本発明のナノ粒子標識プローブは、核酸を認識し、ハイブリダイズすることが可能なプローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とする。この特徴は、請求項1〜6に係る発明に共通する技術的特徴である。
【0016】
なお、本願において、「ナノ粒子」とは、1〜100nmの直径を持つ微粒子をいう。
【0017】
また、「ハイブリダイズする」とは、一本鎖核酸同士が、相補性をもつ塩基対間の水素結合により二本鎖核酸を形成することをいう。
【0018】
以下、本発明とその構成要素等について詳細な説明をする。
【0019】
(ナノ粒子標識プローブ)
本発明のナノ粒子標識プローブは、核酸を認識し、ハイブリダイズすることが可能なプローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とする。
【0020】
本発明に係る「ナノ粒子」とは、上述のように、本願では、1〜100nmの直径を持つ微粒子をいう。本発明においては、種々のナノ粒子を用いることが可能であるが、例えば金属ナノ粒子(Au,Ag,Cu,Pt)、半導体ナノ粒子(例えばCdS,CdSe,ZnS,ZnSe)などが挙げられる。
【0021】
本発明では、金属ナノ粒子、特に金コロイド粒子を用いることが好ましい。金コロイド粒子の直径は1〜100nmであることを要するが、10〜80nmの範囲にあることが好ましい。更には、当該直径を10〜40nmであること、特に、おおよそ20nmとすることが、検出感度、保存安定性等の観点から好ましい。
【0022】
なお、本発明において使用される金コロイド粒子は、種々の方法で調整することができるが、塩化金酸とクエン酸3ナトリウムを一定の比率、例えば、0.1mg/mlの塩化金酸水溶液100mlに対して1%クエン酸ナトリウムを1.1mlを混合することにより、極めて容易かつ安価に調製される(Geoghegan et al,J.Histochem.Cytochem.,25,1187−1200(1977),Goodmann et al,J.maicroscopy,123,201−213(1981),De Waele et al,J.Histochem.Cytochem.,31,376−381(1983),Roth et al.,J.Histochem.Cytochem.,30,691−696(1982))。
【0023】
本発明に係る「ハイブリダイズすることが可能なプローブ」とは、被検物質中の核酸を認識しハイブリダイズさせ得る相補的配列を有する核酸プローブをいう。ここで核酸とは、DNA、RNA、PNA、LNAのことを指す。
【0024】
なお、本発明では、当該プローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とする。
【0025】
なお、前記抗原及び前記抗体としては、例えばFITC(fluorescein isothiocyanate)と抗FITCの組み合わせを用いることができる。
【0026】
(ナノ粒子標識プローブの形成方法)
本発明のナノ粒子標識プローブの形成方法は、核酸を認識し、ハイブリダイズすることが可能なプローブに、抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させるステップ1と、前記ナノ粒子と結合しなかったプローブを除去するステップ2と、を有することを特徴とする。
【0027】
ナノ粒子を結合するステップ1では、抗原または抗体で標識されたプローブと、プローブの標識に対応する抗体または抗原で標識されたナノ粒子を混合し、抗原抗体反応に適した温度条件で反応が十分進行する時間反応させれば良い。
【0028】
又は、ビオチン若しくはビオチン親和性タンパク質(たとえばアビジン)で標識されたプローブと、プローブの標識と結合が可能なビオチン親和性タンパク質(たとえばアビジン)又はビオチンで標識されたナノ粒子を混合し、アビジン・ビオチン相互作用に適した温度条件で反応が十分進行する時間反応させれば良い。
【0029】
ステップ2では、ステップ1においてナノ粒子と結合しなかった未反応のプローブを除去する。ナノ粒子が遠心分離によって容易に沈降することを利用して、未反応のプローブを溶液とともに分離する方法を用いることができる。この際、遠心分離による沈降を利用することで、プローブ・ナノ粒子の反応物濃度を任意に調整することができる。
【0030】
なお、前記抗原および前記抗体には、種々の抗原抗体を用いることが可能であり、例えばFITC(fluorescein isothiocyanate)と抗FITCの組み合わせを用いることができる。
【0031】
(ナノ粒子標識プローブを用いた核酸検出法)
本発明に係る核酸検出方法は、核酸を基盤に固定化するステップ1と、前記基盤に固定化されなかった核酸を除去するステップ2と、上記のナノ粒子標識プローブの形成方法で形成したナノ粒子標識プローブを加えて前記基盤に固定化した核酸にナノ粒子標識プローブをハイブリダイズさせるステップ3と、前記基盤に固定化した核酸にハイブリダイズしなかったナノ粒子標識プローブを除去するステップ4と、前記基盤に固定化した核酸にハイブリダイズしたナノ粒子標識プローブのナノ粒子が有する光学特性を検出することにより前記基盤に固定化した核酸を検出するステップ5と、を有することを特徴とする。
【0032】
なお、前記ナノ粒子標識プローブの分散液が、標識前と比べて、ナノ粒子の濃度換算で、3〜5倍に濃縮されていることが好ましい。また、前記ナノ粒子が有する光学特性が吸光度であることが好ましい態様である。
【0033】
本発明に係る核酸検出法は、複数ステップを要する検出において、ナノ粒子の標識のステップ(図1参照;ステップ3)を予め行っておくことにより、ステップ数を減らし、検出時間の削減を図ったものである。
【0034】
前記抗原および前記抗体には、FITCと抗FITCの組み合わせを用いることができる。また前記ナノ粒子には、前述したように、種々のナノ粒子を用いることが可能であるが、特におおよそ20nmの金コロイドを用いることが好ましい。
【0035】
なお、前記核酸を基盤に固定化する方法として、ポリスチレンにストレプトアビジンを固定化した基盤を用い、末端にビオチンを導入した核酸を接触させて固定化する方法を用いることができる。
【0036】
また、ナノ粒子標識プローブの分散液が、標識前と比べて、ナノ粒子の濃度換算で、3〜5倍に濃縮しておくことで、検出感度を高めることができるのでより好ましい。濃縮は前述したように、遠心分離等を用いてナノ粒子の沈降を利用することにより、プローブ・ナノ粒子の反応物濃度を任意に調整することができる。
【0037】
以下、従来の核酸検出方法と本発明に係る核酸検出方法の相異点について図を参照して説明をする。
【0038】
図1は、従来の固相法における核酸検出方法を示す概念図である。
【0039】
図1において、ステップ1は、ビオチンとビオチン親和性タンパク質(例えばアビジンなど)の相互作用などを利用してビオチン親和性タンパク質が結合した基盤に核酸を固定化するステップである。
【0040】
ステップ2は、核酸とハイブリダイズ可能な、標識されたプローブを用いてハイブリダイゼーションを行うステップである。
【0041】
ステップ3は、プローブの標識を認識する抗体などで標識された金コロイドを用いてプローブをナノ粒子で標識するステップである。
【0042】
なお、各ステップのあとには未反応物を取り除くステップが入る(図には記載なし)。
【0043】
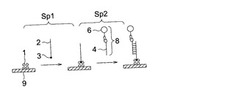
図2は、本発明の実施例を示した概念図である。
【0044】
ステップ1はビオチンとストレプトアビジンの相互作用を利用してビオチン親和性タンパク質が結合した基盤に核酸を固定化するステップである。
【0045】
ステップ2は核酸とハイブリダイズ可能な、抗原抗体反応を介して金コロイドが標識されたプローブを用いてハイブリダイゼーションを行うステップである。
【0046】
各ステップのあとには未反応物を取り除くステップが入る(図には記載なし)。
【実施例】
【0047】
以下、本発明の好ましい実施形態を説明する。なお本発明はかかる実施形態に限定されるものではなく、その他種々の形態で実施可能である。
【0048】
実施例1:抗FITC標識金コロイドの調製
金コロイド(シグマアルドリッチジャパン株式会社製、粒径20nm、A520(520nmの吸光度)=0.75)10mlに対して、抗FITC溶液(フナコシ株式会社製)1mlを混合し、10分間撹拌した後、メトキシ−PEG−SH(分子量5000、濃度0.3mM)1mlを加え、更に1時間撹拌した。その後遠心分離(8500rpm、20分、4℃)を3回繰り返して精製を行い、最後にSSC(Sodium Salt Citrate:0.75M NaCl、0.075M クエン酸バッファ)150ulに分散させた。(PEG:Polyethylene Glycol)
実施例2:プローブと抗FITC標識金コロイドの反応
プローブとして5′端にFITC標識がされたDNAプローブ(配列:CTAAGTTGTGACTCATA、50nM、バッファSSC)100ulと、実施例1で調製した、抗FITC標識金コロイド100ulを混合した。37℃において1時間反応させ、抗原抗体反応を進行させた。反応後遠心分離機を用いて(8500rpm、20分、4℃)金コロイドを沈降させ、上清とともに未反応のプローブを除去した。その後除去した液量と等量のSSCを加えて金コロイドを再懸濁させた。前記遠心、上清の除去、再懸濁を4回繰り返し、最後に加えるSSCの量を調整することで初期金コロイド濃度と比べて1〜5倍のプローブ・金コロイド反応液が得られた。
【0049】
実施例3:ストレプトアビジン標識金コロイドの調製
金コロイド(シグマアルドリッチジャパン株式会社製、粒径20nm、A520=0.75)10mlに対して、ストレプトアビジン溶液(シグマアルドリッチジャパン株式会社製、2uM)1mlを混合し、10分間撹拌した後、メトキシ−PEG−SH(分子量5000、濃度0.3mM)1mlを加え、更に1時間撹拌した。その後遠心分離(8500rpm、20分、4℃)を3回繰り返して精製を行い、最後にSSC150ulに分散させた。
【0050】
実施例4:プローブとストレプトアビジン標識金コロイドの調製
プローブとして5′端にビオチン標識がされたDNAプローブ(配列:CTAAGTTGTGACTCATA配列、50nM、バッファSSC)100ulと、実施例3で調整したストレプトアビジン標識金コロイド100ulを混合した。37℃において1時間反応させ、アビジン・ビオチン相互作用を進行させた。反応後遠心分離機を用いて(8500rpm、20分、4℃)金コロイドを沈降させ、上清とともに未反応のプローブを除去した。その後除去した液量と等量のSSCを加えて金コロイドを再懸濁させた。前記遠心、上清の除去、再懸濁を4回繰り返し、最後に加えるSSCの量を調整することで初期金コロイド濃度と比べて1〜5倍のプローブ・金コロイド反応液が得られた。
【0051】
実施例5
上記プローブを評価するために、ストレプトアビジンを固定化したポリスチレン上(検出部)で検出反応を行った。ポリスチレンにストレプトアビジンを固定化する方法は以下の通り。ポリスチレンシートをストレプトアビジン(シグマアルドリッチジャパン株式会社製、2uM)溶液に浸し、4℃で1日静置した。その後、37℃に昇温し2時間インキュベートした。次にポリスチレンシートを1%BSA(牛血清アルブミン、シグマアルドリッチジャパン株式会社製)溶液(0.1Mリン酸バッファ)に浸して37℃、2時間インキュベートした。このストレプトアビジン固定ポリスチレンを用いて検出反応を行った。
【0052】
まず、5′端にビオチンが導入されたDNA溶液(AGACTTGTGA CATGCTCGCC GAGTATGAGT CACAACTTAG CTATACGGAC CAGTTACTCA)を検出部に導入した。42℃、2分間反応させた後、DNA溶液を検出部から除去した。続いて、実施例2又は実施例4で調製したプローブ・金コロイド反応液を検出部に導入した。50℃、3分間反応させた後、プローブ・金コロイド反応液を除去し、SSCを用いて検出部の洗浄を行った。その後、吸光度変化を検出するために、反応を行ったポリスチレンに対し525nmの波長の光を照射し、透過光強度を測定した。SSC溶液の透過光を標準(blank)とし、吸光度を算出した。
【0053】
測定の結果、3倍濃縮液で従来の約1.5倍の、5倍濃縮液で従来の約2倍の感度が得られることが判明した。
【0054】
なお、上記実施例により、本発明に係る核酸検出方法は、従来法より検出に要するステップ数が少なく、より簡単で短時間に核酸検出が可能であることが分かる。
【図面の簡単な説明】
【0055】
【図1】従来の固相法における核酸検出方法を示す概念図
【図2】本発明の実施例を示した概念図
【符号の説明】
【0056】
Sp1 ステップ1:核酸固定化
Sp2 ステップ2:ハイブリダイゼーション
Sp3 ステップ3:ナノ粒子標識
1 ビオチン親和性タンパク質
2 核酸
3 ビオチン
4 プローブ
5 標識
6 ナノ粒子
7 標識認識抗体
8 ナノ粒子標識プローブ
9 基盤
【技術分野】
【0001】
本発明は核酸を検出するためのナノ粒子標識プローブ及びその形成方法に関する。また本発明は当該ナノ粒子標識プローブを用いた核酸検出方法に関する。
【背景技術】
【0002】
遺伝子検査では検出に特異性を持たせるために、標的核酸に選択的にハイブリダイズすることが可能なプローブを用いるのが一般的である。プローブを用いた検出には様々な手法が存在し、蛍光分子を利用するもの、酵素を利用するもの、ナノ粒子を利用するもの、電気信号を検出するものなど、多種多様に及ぶ。その中でも、ナノ粒子を利用するものは、高い光学特性を有するため、検出が容易という利点がある。このようなナノ粒子を利用した核酸の検出は液相法(例えば特許文献1参照)及び固相法(例えば特許文献2参照)で行われている。
【0003】
しかしながら、ナノ粒子はサイズが1〜100nmとプローブに対して巨大であるため、固相法に適用したときに反応効率が低くなるという欠点があり、プローブにナノ粒子を直接標識したものを用いた検出は、溶液中でハイブリダイズが行われていた(特許文献1参照)。そして固相法に用いる場合は、核酸を固定化した後、ナノ粒子以外の標識がされたプローブを用いて一旦ハイブリダイズさせ、続いて、標識をナノ粒子で再度標識するという3段階のステップを取っていた(特許文献2及び図1参照)。しかし、このような複数のステップを経て検出する方法では、検出に時間と手間がかかるという問題があった。
【特許文献1】特開2004−275187号公報
【特許文献2】特開2006−21199号公報
【発明の開示】
【発明が解決しようとする課題】
【0004】
本発明は、上記問題に鑑みてなされたものであり、その解決課題は、遺伝子検査等において、より簡単で短時間に核酸検出を可能とするナノ粒子標識プローブ及びその形成方法を提供することである。また、当該ナノ粒子標識プローブを用いた核酸検出方法を提供することである。
【課題を解決するための手段】
【0005】
本発明に係る上記課題は下記の手段により解決される。
【0006】
1.核酸を認識し、ハイブリダイズすることが可能なプローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とするナノ粒子標識プローブ。
【0007】
2.前記ナノ粒子が金コロイド粒子であることを特徴とする前記1に記載のナノ粒子標識プローブ。
【0008】
3.前記1又は2に記載のナノ粒子標識プローブの形成方法であって、核酸を認識し、ハイブリダイズすることが可能なプローブに、抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させるステップ1と、前記ナノ粒子と結合しなかったプローブを除去するステップ2と、を有することを特徴とするナノ粒子標識プローブの形成方法。
【0009】
4.核酸を基盤に固定化するステップ1と、前記基盤に固定化されなかった核酸を除去するステップ2と、前記3に記載のナノ粒子標識プローブの形成方法で形成したナノ粒子標識プローブを加えて前記基盤に固定化した核酸にナノ粒子標識プローブをハイブリダイズさせるステップ3と、前記基盤に固定化した核酸にハイブリダイズしなかったナノ粒子標識プローブを除去するステップ4と、前記基盤に固定化した核酸にハイブリダイズしたナノ粒子標識プローブのナノ粒子が有する光学特性を検出することにより前記基盤に固定化した核酸を検出するステップ5と、を有することを特徴とする核酸検出方法。
【0010】
5.前記ナノ粒子標識プローブの分散液が、標識前と比べて、ナノ粒子の濃度換算で、3〜5倍に濃縮されていることを特徴とする前記4に記載の核酸検出方法。
【0011】
6.前記ナノ粒子が有する光学特性が吸光度であることを特徴とする前記4又は5に記載の核酸検出方法。
【発明の効果】
【0012】
本発明の上記手段により、遺伝子検査等において、より簡単で短時間に核酸検出を可能とするナノ粒子標識プローブ及びその形成方法を提供することができる。また、当該ナノ粒子標識プローブを用いた核酸検出方法を提供することができる。
【0013】
すなわち、本発明においては、ナノ粒子を予めプローブに反応させておくことで、従来よりも反応ステップが削減できる。これによって従来よりも検出時間の短縮が可能となる。また、従来のナノ粒子に直接プローブを結合させる方法と異なり、抗原・抗体又はアビジン・ビオチンを間に設けることによって、ナノ粒子−プローブ間の距離が広がり、固相法で反応効率が落ちるのを抑えることができるとともに、ナノ粒子−プローブ間の相互作用でナノ粒子やプローブの反応性が低下することを防ぐことができる。
【0014】
さらに、プローブをナノ粒子で標識する工程を最適な条件で予め行うことによって、反応効率が向上し、検出感度が向上する。加えて、ナノ粒子は遠心分離機によって容易に沈降させることが可能であるため、プローブと反応後、任意の濃度に濃縮することができ、濃度によって検出感度を調整することが可能となる。
【発明を実施するための最良の形態】
【0015】
本発明のナノ粒子標識プローブは、核酸を認識し、ハイブリダイズすることが可能なプローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とする。この特徴は、請求項1〜6に係る発明に共通する技術的特徴である。
【0016】
なお、本願において、「ナノ粒子」とは、1〜100nmの直径を持つ微粒子をいう。
【0017】
また、「ハイブリダイズする」とは、一本鎖核酸同士が、相補性をもつ塩基対間の水素結合により二本鎖核酸を形成することをいう。
【0018】
以下、本発明とその構成要素等について詳細な説明をする。
【0019】
(ナノ粒子標識プローブ)
本発明のナノ粒子標識プローブは、核酸を認識し、ハイブリダイズすることが可能なプローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とする。
【0020】
本発明に係る「ナノ粒子」とは、上述のように、本願では、1〜100nmの直径を持つ微粒子をいう。本発明においては、種々のナノ粒子を用いることが可能であるが、例えば金属ナノ粒子(Au,Ag,Cu,Pt)、半導体ナノ粒子(例えばCdS,CdSe,ZnS,ZnSe)などが挙げられる。
【0021】
本発明では、金属ナノ粒子、特に金コロイド粒子を用いることが好ましい。金コロイド粒子の直径は1〜100nmであることを要するが、10〜80nmの範囲にあることが好ましい。更には、当該直径を10〜40nmであること、特に、おおよそ20nmとすることが、検出感度、保存安定性等の観点から好ましい。
【0022】
なお、本発明において使用される金コロイド粒子は、種々の方法で調整することができるが、塩化金酸とクエン酸3ナトリウムを一定の比率、例えば、0.1mg/mlの塩化金酸水溶液100mlに対して1%クエン酸ナトリウムを1.1mlを混合することにより、極めて容易かつ安価に調製される(Geoghegan et al,J.Histochem.Cytochem.,25,1187−1200(1977),Goodmann et al,J.maicroscopy,123,201−213(1981),De Waele et al,J.Histochem.Cytochem.,31,376−381(1983),Roth et al.,J.Histochem.Cytochem.,30,691−696(1982))。
【0023】
本発明に係る「ハイブリダイズすることが可能なプローブ」とは、被検物質中の核酸を認識しハイブリダイズさせ得る相補的配列を有する核酸プローブをいう。ここで核酸とは、DNA、RNA、PNA、LNAのことを指す。
【0024】
なお、本発明では、当該プローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とする。
【0025】
なお、前記抗原及び前記抗体としては、例えばFITC(fluorescein isothiocyanate)と抗FITCの組み合わせを用いることができる。
【0026】
(ナノ粒子標識プローブの形成方法)
本発明のナノ粒子標識プローブの形成方法は、核酸を認識し、ハイブリダイズすることが可能なプローブに、抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させるステップ1と、前記ナノ粒子と結合しなかったプローブを除去するステップ2と、を有することを特徴とする。
【0027】
ナノ粒子を結合するステップ1では、抗原または抗体で標識されたプローブと、プローブの標識に対応する抗体または抗原で標識されたナノ粒子を混合し、抗原抗体反応に適した温度条件で反応が十分進行する時間反応させれば良い。
【0028】
又は、ビオチン若しくはビオチン親和性タンパク質(たとえばアビジン)で標識されたプローブと、プローブの標識と結合が可能なビオチン親和性タンパク質(たとえばアビジン)又はビオチンで標識されたナノ粒子を混合し、アビジン・ビオチン相互作用に適した温度条件で反応が十分進行する時間反応させれば良い。
【0029】
ステップ2では、ステップ1においてナノ粒子と結合しなかった未反応のプローブを除去する。ナノ粒子が遠心分離によって容易に沈降することを利用して、未反応のプローブを溶液とともに分離する方法を用いることができる。この際、遠心分離による沈降を利用することで、プローブ・ナノ粒子の反応物濃度を任意に調整することができる。
【0030】
なお、前記抗原および前記抗体には、種々の抗原抗体を用いることが可能であり、例えばFITC(fluorescein isothiocyanate)と抗FITCの組み合わせを用いることができる。
【0031】
(ナノ粒子標識プローブを用いた核酸検出法)
本発明に係る核酸検出方法は、核酸を基盤に固定化するステップ1と、前記基盤に固定化されなかった核酸を除去するステップ2と、上記のナノ粒子標識プローブの形成方法で形成したナノ粒子標識プローブを加えて前記基盤に固定化した核酸にナノ粒子標識プローブをハイブリダイズさせるステップ3と、前記基盤に固定化した核酸にハイブリダイズしなかったナノ粒子標識プローブを除去するステップ4と、前記基盤に固定化した核酸にハイブリダイズしたナノ粒子標識プローブのナノ粒子が有する光学特性を検出することにより前記基盤に固定化した核酸を検出するステップ5と、を有することを特徴とする。
【0032】
なお、前記ナノ粒子標識プローブの分散液が、標識前と比べて、ナノ粒子の濃度換算で、3〜5倍に濃縮されていることが好ましい。また、前記ナノ粒子が有する光学特性が吸光度であることが好ましい態様である。
【0033】
本発明に係る核酸検出法は、複数ステップを要する検出において、ナノ粒子の標識のステップ(図1参照;ステップ3)を予め行っておくことにより、ステップ数を減らし、検出時間の削減を図ったものである。
【0034】
前記抗原および前記抗体には、FITCと抗FITCの組み合わせを用いることができる。また前記ナノ粒子には、前述したように、種々のナノ粒子を用いることが可能であるが、特におおよそ20nmの金コロイドを用いることが好ましい。
【0035】
なお、前記核酸を基盤に固定化する方法として、ポリスチレンにストレプトアビジンを固定化した基盤を用い、末端にビオチンを導入した核酸を接触させて固定化する方法を用いることができる。
【0036】
また、ナノ粒子標識プローブの分散液が、標識前と比べて、ナノ粒子の濃度換算で、3〜5倍に濃縮しておくことで、検出感度を高めることができるのでより好ましい。濃縮は前述したように、遠心分離等を用いてナノ粒子の沈降を利用することにより、プローブ・ナノ粒子の反応物濃度を任意に調整することができる。
【0037】
以下、従来の核酸検出方法と本発明に係る核酸検出方法の相異点について図を参照して説明をする。
【0038】
図1は、従来の固相法における核酸検出方法を示す概念図である。
【0039】
図1において、ステップ1は、ビオチンとビオチン親和性タンパク質(例えばアビジンなど)の相互作用などを利用してビオチン親和性タンパク質が結合した基盤に核酸を固定化するステップである。
【0040】
ステップ2は、核酸とハイブリダイズ可能な、標識されたプローブを用いてハイブリダイゼーションを行うステップである。
【0041】
ステップ3は、プローブの標識を認識する抗体などで標識された金コロイドを用いてプローブをナノ粒子で標識するステップである。
【0042】
なお、各ステップのあとには未反応物を取り除くステップが入る(図には記載なし)。
【0043】
図2は、本発明の実施例を示した概念図である。
【0044】
ステップ1はビオチンとストレプトアビジンの相互作用を利用してビオチン親和性タンパク質が結合した基盤に核酸を固定化するステップである。
【0045】
ステップ2は核酸とハイブリダイズ可能な、抗原抗体反応を介して金コロイドが標識されたプローブを用いてハイブリダイゼーションを行うステップである。
【0046】
各ステップのあとには未反応物を取り除くステップが入る(図には記載なし)。
【実施例】
【0047】
以下、本発明の好ましい実施形態を説明する。なお本発明はかかる実施形態に限定されるものではなく、その他種々の形態で実施可能である。
【0048】
実施例1:抗FITC標識金コロイドの調製
金コロイド(シグマアルドリッチジャパン株式会社製、粒径20nm、A520(520nmの吸光度)=0.75)10mlに対して、抗FITC溶液(フナコシ株式会社製)1mlを混合し、10分間撹拌した後、メトキシ−PEG−SH(分子量5000、濃度0.3mM)1mlを加え、更に1時間撹拌した。その後遠心分離(8500rpm、20分、4℃)を3回繰り返して精製を行い、最後にSSC(Sodium Salt Citrate:0.75M NaCl、0.075M クエン酸バッファ)150ulに分散させた。(PEG:Polyethylene Glycol)
実施例2:プローブと抗FITC標識金コロイドの反応
プローブとして5′端にFITC標識がされたDNAプローブ(配列:CTAAGTTGTGACTCATA、50nM、バッファSSC)100ulと、実施例1で調製した、抗FITC標識金コロイド100ulを混合した。37℃において1時間反応させ、抗原抗体反応を進行させた。反応後遠心分離機を用いて(8500rpm、20分、4℃)金コロイドを沈降させ、上清とともに未反応のプローブを除去した。その後除去した液量と等量のSSCを加えて金コロイドを再懸濁させた。前記遠心、上清の除去、再懸濁を4回繰り返し、最後に加えるSSCの量を調整することで初期金コロイド濃度と比べて1〜5倍のプローブ・金コロイド反応液が得られた。
【0049】
実施例3:ストレプトアビジン標識金コロイドの調製
金コロイド(シグマアルドリッチジャパン株式会社製、粒径20nm、A520=0.75)10mlに対して、ストレプトアビジン溶液(シグマアルドリッチジャパン株式会社製、2uM)1mlを混合し、10分間撹拌した後、メトキシ−PEG−SH(分子量5000、濃度0.3mM)1mlを加え、更に1時間撹拌した。その後遠心分離(8500rpm、20分、4℃)を3回繰り返して精製を行い、最後にSSC150ulに分散させた。
【0050】
実施例4:プローブとストレプトアビジン標識金コロイドの調製
プローブとして5′端にビオチン標識がされたDNAプローブ(配列:CTAAGTTGTGACTCATA配列、50nM、バッファSSC)100ulと、実施例3で調整したストレプトアビジン標識金コロイド100ulを混合した。37℃において1時間反応させ、アビジン・ビオチン相互作用を進行させた。反応後遠心分離機を用いて(8500rpm、20分、4℃)金コロイドを沈降させ、上清とともに未反応のプローブを除去した。その後除去した液量と等量のSSCを加えて金コロイドを再懸濁させた。前記遠心、上清の除去、再懸濁を4回繰り返し、最後に加えるSSCの量を調整することで初期金コロイド濃度と比べて1〜5倍のプローブ・金コロイド反応液が得られた。
【0051】
実施例5
上記プローブを評価するために、ストレプトアビジンを固定化したポリスチレン上(検出部)で検出反応を行った。ポリスチレンにストレプトアビジンを固定化する方法は以下の通り。ポリスチレンシートをストレプトアビジン(シグマアルドリッチジャパン株式会社製、2uM)溶液に浸し、4℃で1日静置した。その後、37℃に昇温し2時間インキュベートした。次にポリスチレンシートを1%BSA(牛血清アルブミン、シグマアルドリッチジャパン株式会社製)溶液(0.1Mリン酸バッファ)に浸して37℃、2時間インキュベートした。このストレプトアビジン固定ポリスチレンを用いて検出反応を行った。
【0052】
まず、5′端にビオチンが導入されたDNA溶液(AGACTTGTGA CATGCTCGCC GAGTATGAGT CACAACTTAG CTATACGGAC CAGTTACTCA)を検出部に導入した。42℃、2分間反応させた後、DNA溶液を検出部から除去した。続いて、実施例2又は実施例4で調製したプローブ・金コロイド反応液を検出部に導入した。50℃、3分間反応させた後、プローブ・金コロイド反応液を除去し、SSCを用いて検出部の洗浄を行った。その後、吸光度変化を検出するために、反応を行ったポリスチレンに対し525nmの波長の光を照射し、透過光強度を測定した。SSC溶液の透過光を標準(blank)とし、吸光度を算出した。
【0053】
測定の結果、3倍濃縮液で従来の約1.5倍の、5倍濃縮液で従来の約2倍の感度が得られることが判明した。
【0054】
なお、上記実施例により、本発明に係る核酸検出方法は、従来法より検出に要するステップ数が少なく、より簡単で短時間に核酸検出が可能であることが分かる。
【図面の簡単な説明】
【0055】
【図1】従来の固相法における核酸検出方法を示す概念図
【図2】本発明の実施例を示した概念図
【符号の説明】
【0056】
Sp1 ステップ1:核酸固定化
Sp2 ステップ2:ハイブリダイゼーション
Sp3 ステップ3:ナノ粒子標識
1 ビオチン親和性タンパク質
2 核酸
3 ビオチン
4 プローブ
5 標識
6 ナノ粒子
7 標識認識抗体
8 ナノ粒子標識プローブ
9 基盤
【特許請求の範囲】
【請求項1】
核酸を認識し、ハイブリダイズすることが可能なプローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とするナノ粒子標識プローブ。
【請求項2】
前記ナノ粒子が金コロイド粒子であることを特徴とする請求項1に記載のナノ粒子標識プローブ。
【請求項3】
請求項1又は2に記載のナノ粒子標識プローブの形成方法であって、核酸を認識し、ハイブリダイズすることが可能なプローブに、抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させるステップ1と、前記ナノ粒子と結合しなかったプローブを除去するステップ2と、を有することを特徴とするナノ粒子標識プローブの形成方法。
【請求項4】
核酸を基盤に固定化するステップ1と、前記基盤に固定化されなかった核酸を除去するステップ2と、請求項3に記載のナノ粒子標識プローブの形成方法で形成したナノ粒子標識プローブを加えて前記基盤に固定化した核酸にナノ粒子標識プローブをハイブリダイズさせるステップ3と、前記基盤に固定化した核酸にハイブリダイズしなかったナノ粒子標識プローブを除去するステップ4と、前記基盤に固定化した核酸にハイブリダイズしたナノ粒子標識プローブのナノ粒子が有する光学特性を検出することにより前記基盤に固定化した核酸を検出するステップ5と、を有することを特徴とする核酸検出方法。
【請求項5】
前記ナノ粒子標識プローブの分散液が、標識前と比べて、ナノ粒子の濃度換算で、3〜5倍に濃縮されていることを特徴とする請求項4に記載の核酸検出方法。
【請求項6】
前記ナノ粒子が有する光学特性が吸光度であることを特徴とする請求項4又は5に記載の核酸検出方法。
【請求項1】
核酸を認識し、ハイブリダイズすることが可能なプローブの一端に抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させたことを特徴とするナノ粒子標識プローブ。
【請求項2】
前記ナノ粒子が金コロイド粒子であることを特徴とする請求項1に記載のナノ粒子標識プローブ。
【請求項3】
請求項1又は2に記載のナノ粒子標識プローブの形成方法であって、核酸を認識し、ハイブリダイズすることが可能なプローブに、抗原抗体反応又はアビジン・ビオチン相互作用を介してナノ粒子を結合させるステップ1と、前記ナノ粒子と結合しなかったプローブを除去するステップ2と、を有することを特徴とするナノ粒子標識プローブの形成方法。
【請求項4】
核酸を基盤に固定化するステップ1と、前記基盤に固定化されなかった核酸を除去するステップ2と、請求項3に記載のナノ粒子標識プローブの形成方法で形成したナノ粒子標識プローブを加えて前記基盤に固定化した核酸にナノ粒子標識プローブをハイブリダイズさせるステップ3と、前記基盤に固定化した核酸にハイブリダイズしなかったナノ粒子標識プローブを除去するステップ4と、前記基盤に固定化した核酸にハイブリダイズしたナノ粒子標識プローブのナノ粒子が有する光学特性を検出することにより前記基盤に固定化した核酸を検出するステップ5と、を有することを特徴とする核酸検出方法。
【請求項5】
前記ナノ粒子標識プローブの分散液が、標識前と比べて、ナノ粒子の濃度換算で、3〜5倍に濃縮されていることを特徴とする請求項4に記載の核酸検出方法。
【請求項6】
前記ナノ粒子が有する光学特性が吸光度であることを特徴とする請求項4又は5に記載の核酸検出方法。
【図1】


【図2】




【図2】


【公開番号】特開2008−295326(P2008−295326A)
【公開日】平成20年12月11日(2008.12.11)
【国際特許分類】
【出願番号】特願2007−143066(P2007−143066)
【出願日】平成19年5月30日(2007.5.30)
【出願人】(303000420)コニカミノルタエムジー株式会社 (2,950)
【Fターム(参考)】
【公開日】平成20年12月11日(2008.12.11)
【国際特許分類】
【出願日】平成19年5月30日(2007.5.30)
【出願人】(303000420)コニカミノルタエムジー株式会社 (2,950)
【Fターム(参考)】
[ Back to top ]

