ハイレート特性に優れた二酸化マンガン
【課題】
アルカリマンガン乾電池の正極用活物質として使用されるハイレート特性に優れた二酸化マンガンを提供する。
【解決手段】
水酸化亜鉛を有してなる二酸化マンガン、特に二酸化マンガンのイオン交換サイトに水酸化亜鉛を有し、特に二酸化マンガン粒子の細孔内部のイオン交換サイトに水酸化亜鉛を有してなる二酸化マンガンを用いる。水酸化亜鉛の含有量が亜鉛換算で0.01wt%以上0.10wt%以下であることが好ましい。イオン交換サイトに水酸化亜鉛を含有する二酸化マンガンは、二酸化マンガンを亜鉛イオン含有水溶液でイオン交換し、洗浄後、さらにアルカリ水酸化物と反応させることによって製造できる。
アルカリマンガン乾電池の正極用活物質として使用されるハイレート特性に優れた二酸化マンガンを提供する。
【解決手段】
水酸化亜鉛を有してなる二酸化マンガン、特に二酸化マンガンのイオン交換サイトに水酸化亜鉛を有し、特に二酸化マンガン粒子の細孔内部のイオン交換サイトに水酸化亜鉛を有してなる二酸化マンガンを用いる。水酸化亜鉛の含有量が亜鉛換算で0.01wt%以上0.10wt%以下であることが好ましい。イオン交換サイトに水酸化亜鉛を含有する二酸化マンガンは、二酸化マンガンを亜鉛イオン含有水溶液でイオン交換し、洗浄後、さらにアルカリ水酸化物と反応させることによって製造できる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、たとえばマンガン乾電池、特にアルカリマンガン乾電池において、正極活物質として使用される二酸化マンガンおよびその製造方法、用途に関する。
【背景技術】
【0002】
二酸化マンガンは、たとえばマンガン乾電池またはアルカリマンガン乾電池の正極活物質として知られており、保存性に優れ、且つ安価であるという利点を有する。特に、二酸化マンガンを正極活物質として用いるアルカリマンガン乾電池は、重負荷での放電特性に優れていることから電子カメラ、携帯用テープレコーダー、携帯情報機器、さらにはゲーム機や玩具にまで幅広く使用され、近年急速にその需要が伸びてきている。
【0003】
しかし、アルカリマンガン乾電池は、放電電流が大きくなるに従い正極活物質である二酸化マンガンの利用される量が低下し、また放電電圧が低下するために放電容量が大きく損なわれるという課題があり、例えば大電流を使用(ハイレート放電)する機器にアルカリマンガン乾電池を用いると充填されている正極活物質である二酸化マンガンが十分に使用されず使用時間が短くなるという欠点を有していた。そこで短時間に大電流を取り出すハイレート放電条件においても、高容量、長寿命を発現できる優れた二酸化マンガン、所謂ハイレート特性に優れた二酸化マンガンが望まれていた。
【0004】
この様な課題に対する解決策として、二酸化マンガンに異種元素を添加したアルカリマンガン乾電池用正極活物質を利用する技術が知られている。前駆体に亜鉛を添加した正極活物質の利用として、二酸化マンガンを化学合成する際に、前駆体である天然二酸化マンガンに酸化亜鉛を添加した正極活物質の合成方法が報告されている(特許文献1)。しかし、化学合成された二酸化マンガン内部にヘテロライト(Mn2ZnO4)を生成させると、電池の正極活物質含有量が減少し、電池当りの放電容量低下を伴う。
【0005】
また、弱酸性(pH4.2)の電解二酸化マンガンに塩化亜鉛溶液で処理して塩化亜鉛型の二酸化マンガンを得る方法が提案されている(特許文献2)。この方法では正極合剤のpH変動に付随する特性のばらつきが抑制され、放電特性の改善がされるが、当該方法では中性雰囲気下のマンガン乾電池への効果は大きいが、強アルカリ性雰囲気下に置かれているアルカリマンガン乾電池においては十分な効果が得られていなかった。また、電解二酸化マンガンに対する塩化亜鉛溶液の濃度が高いために、過剰な亜鉛が付着しており、なおかつ不純物アニオンが含まれるためハイレート特性の改善が得られるものではなかった。
【0006】
さらに、酸化亜鉛を正極合剤中に添加する方法が提案されている(特許文献3)。この方法では二酸化マンガン表面に固定した酸化亜鉛が溶出することにより正極合剤の濡れ性が改善し、電池の安定化時間が短縮されるが、放電特性の改善効果は得られていなかった。
【0007】
他にも、アルカリマンガン乾電池における亜鉛の利用として、二酸化マンガンとオキシ水酸化ニッケルとを正極活物質としたアルカリマンガン乾電池において、オキシ水酸化ニッケルに亜鉛を固溶させる方法が提案されている(特許文献4、5)。この方法では亜鉛の固溶および酸化亜鉛の添加でオキシ水酸化ニッケルの自己放電が抑制されるが、当該方法では自己放電の大きいオキシ水酸化ニッケルへ効果はあるが、二酸化マンガンのみを正極活物質としたアルカリマンガン乾電池では効果が得られなかった。
【0008】
【特許文献1】特開昭58−161259号
【特許文献2】特開昭59−194357号
【特許文献3】特開平01−102852号
【特許文献4】特開2002−075354
【特許文献5】特開2006−179429
【発明の開示】
【発明が解決しようとする課題】
【0009】
異種元素、特に亜鉛を含む二酸化マンガンを正極活物質としたアルカリマンガン電池において、ハイレート特性に優れたものは得られていなかった。本発明の目的は、特にアルカリマンガン乾電池の正極活物質として使用される二酸化マンガンにおいて、大電流で放電時間が長い、所謂ハイレート特性に優れた二酸化マンガンを提供することである。
【課題を解決するための手段】
【0010】
本発明者等は、特にアルカリマンガン乾電池の正極活物質として使用される二酸化マンガンについて鋭意検討を重ねた結果、水酸化亜鉛を有してなる二酸化マンガン、特に二酸化マンガンのイオン交換サイトに水酸化亜鉛を有する二酸化マンガンでは、ハイレート特性に著しく優れることを見出し、本発明を完成するに至ったものである。
【0011】
以下、本発明の二酸化マンガンについて詳細に説明する。
【0012】
本発明の二酸化マンガンは、水酸化亜鉛を有してなる二酸化マンガンである。本発明の二酸化マンガンに含まれる亜鉛は水酸化亜鉛であるため、亜鉛をイオン状態(Zn2+)、酸化亜鉛、塩化亜鉛、硫酸亜鉛などの形態で含む従来のものとは異なるものである。
【0013】
本発明における二酸化マンガンは特に限定はないが、電解二酸化マンガン(EMD)であることが好ましい。
【0014】
本発明で二酸化マンガンに含まれる水酸化亜鉛は、イオン交換によって二酸化マンガンに導入した亜鉛イオンをアルカリ(水酸化ナトリウム、水酸化カリウム等)で水酸化亜鉛に転換したものが好ましい。
【0015】
本発明の二酸化マンガンに含まれる水酸化亜鉛は、二酸化マンガンのイオン交換サイトに存在することが好ましく、さらに、二酸化マンガン粒子の細孔内部(細孔内表面)のイオン交換サイトに存在することが好ましい。
【0016】
本発明における「イオン交換サイト」とは、二酸化マンガンのカチオン交換サイトのことである。二酸化マンガンは金属イオンなどのカチオン交換能を有している。これは、二酸化マンガン中にMn4+とMn3+が存在する場合に、Mn3+の電価不足を補償するために存在するH+と、金属イオンの交換により起こる場合や、二酸化マンガン表面の末端水酸基のH+が金属イオンと交換することで、カチオン交換が起こることが知られている。
【0017】
本発明における「イオン交換サイトに水酸化亜鉛を有してなる」とは、イオン交換サイトに直接に水酸化亜鉛が存在する場合や、イオン交換サイトの近傍に水酸化亜鉛が存在することを指す。前者の場合、イオン交換サイトの亜鉛イオンが、アルカリ性領域になったときに亜鉛イオンの移動を伴わずに、水酸化物化して水酸化亜鉛となる場合が考えられる。このときイオン交換サイトの電化補償はイオン交換サイト近傍のH+などの他のカチオンによりなされると考えられる。また、後者の場合、アルカリ性領域になったときに、イオン交換サイトの亜鉛イオンとアルカリ金属イオンとの間で交換が起こり、イオン交換サイトを外れた亜鉛イオンが、イオン交換サイト近傍で速やかに水酸化物化して水酸化亜鉛となる場合が考えられる。
【0018】
本発明の水酸化亜鉛の存在部位は、二酸化マンガン粒子全面を覆う被覆や、二酸化マンガンの結晶構造中、或いは一次粒子の内部に亜鉛が存在するものとは異なる。特に二酸化マンガン粒子の外表面を被覆する水酸化亜鉛では、本発明のハイレート特性の向上への寄与が小さいため、外表面の水酸化亜鉛は少ない方が好ましい。
【0019】
本発明の二酸化マンガンに対する水酸化亜鉛の含有量は、亜鉛換算で0.01wt%以上0.10wt%以下であることが好ましい。亜鉛の含有量が0.10wt%以上では水酸化亜鉛が二酸化マンガンの細孔を閉塞したり、二酸化マンガン粒子の表面を被覆し、電池反応を阻害し、ハイレート特性が低下する場合がある。一方、0.01wt%以下では、本発明のハイレート特性の改善効果が得られ難い。
【0020】
本発明において二酸化マンガンのハイレート特性が改善されるメカニズムは必ずしも明確にはなっていないが、以下のような機構によって改善されているものと考えられる。
【0021】
アルカリマンガン乾電池における二酸化マンガンの放電は(1)式によって進行することが知られている。
【0022】
MnO2 + H2O + e− → MnOOH + OH− (1)
従来、アルカリマンガン乾電池に含まれる二酸化マンガンは利用率が低く、(1)式に示した放電反応はアルカリマンガン乾電池に含まれる二酸化マンガンの30%程度しか関与してない。したがって、放電後のアルカリマンガン乾電池正極活物質は30%がMnOOHになっているが、残りの70%はMnO2のままで、電池として利用できていない。ここで(1)式から明らかなように、放電反応ではOH―が生成されるため、生成したOH−を効率的に除去することにより(1)式が進行し、放電反応が促進されると考えられる。
【0023】
アルカリマンガン乾電池は電解液に40%の水酸化カリウム溶液を使用しており、電池内部は強アルカリ雰囲気である。このようなアルカリ雰囲気下において、亜鉛は(2)式の平衡反応を起こすと考えられる。
【0024】
【数1】

即ち、(1)式の放電反応が起きる近傍で(2)式の反応が起こる環境を作り出せば放電反応で排出されるOH−が消費され、Zn(OH)42―が生成し、その結果として(1)式が促進され、結果的に放電反応が促進され、ハイレート特性が改善すると考えられる。
【0025】
従来、例えば塩化亜鉛で処理した場合にも電池の中で水酸化亜鉛は形成していると考えられるが、塩化物型の二酸化マンガンでは塩素などのアニオンを含有しているため、これら含有されたアニオンが副反応を引き起こすなどして、上記の反応を阻害するために十分なハイレート特性が得られないものと考えられる。よって本発明の水酸化物には塩素等の不純物アニオンを含まないものが好ましい。
【0026】
アルカリマンガン乾電池で使用される二酸化マンガンは通常は多孔質であり、電池反応は細孔内で多く進行するが、細孔内部では特に排出されたOH−が残存し易く、それが電池利用率の低下の原因となっている。本発明では、その様な細孔内部(細孔内表面)のOH−イオンを効率的に除去する様に、細孔内部に水酸化亜鉛を配置することにより優れたハイレート特性を達成するものである。
【0027】
二酸化マンガン粒子の外表面(細孔外)ではOH−イオンの除去は容易であるため、外表面に水酸化物を配置する効果は細孔内に比べて小さく、ハイレート特性向上に寄与しないため、外表面には水酸化亜鉛は付着していないことが好ましい。
【0028】
次に、本発明の二酸化マンガンの製造方法について説明する。
【0029】
本発明の二酸化マンガンは、二酸化マンガンを亜鉛イオン含有水溶液でイオン交換し、洗浄後、さらにアルカリ水酸化物と反応させることによって製造することができる。
【0030】
二酸化マンガンはイオン交換能を有するため、亜鉛塩の水溶液で処理することにより、容易にイオン交換することができる。
【0031】
二酸化マンガンに対する亜鉛イオンのイオン交換量は、亜鉛イオン含有溶液の濃度で制御できる。
【0032】
本発明で用いる亜鉛イオン含有溶液の原料亜鉛は特に限定されないが、亜鉛塩、例えば硫酸亜鉛、硝酸亜鉛等の無機塩、酢酸亜鉛、クエン酸亜鉛等の有機酸塩が用いることができる。さらに、亜鉛溶液の溶媒も限定されないが、水を用いることが好ましい。
【0033】
イオン交換の時間、温度は用いる二酸化マンガンの細孔量、亜鉛イオン含有溶液の濃度によって異なるため一概に決められないが、二酸化マンガンの細孔量、亜鉛イオン含有溶液の濃度によって水酸化亜鉛の含有量が亜鉛換算で0.01wt%以上0.10wt%以下となる様に適宜選択して用いればよい。
【0034】
先に説明した通り、亜鉛水酸化物は二酸化マンガンの細孔内部に局在することが好ましいため、イオン交換処理の後、十分に洗浄して粒子外表面の亜鉛、及び不純物アニオンは除去することが好ましい。
【0035】
細孔表面のイオン交換サイトにイオン交換された亜鉛イオンは洗浄によって除去され易い。そこで少なくとも細孔内のイオン交換サイトに水酸化亜鉛を配置するためには、イオン交換後の二酸化マンガンを洗浄して表面の亜鉛イオンを除去した後にアルカリと反応させることにより、細孔内に選択的に水酸化亜鉛が位置したものが得られる。
【0036】
イオン交換後、洗浄せずにアルカリ水酸化物と反応させた場合、本発明の効果が得られ難い場合があるが、これは過剰の亜鉛イオン、特に粒子表面(細孔外)に残存する亜鉛イオンが選択的に水酸化亜鉛に転換し、ハイレート特性を改善する細孔内の亜鉛が十分に水酸化亜鉛とならないことが原因と考えられる。
【0037】
洗浄後、アルカリ水酸化物で処理し、細孔表面及び/又は内部の亜鉛イオンを水酸化亜鉛に転換する。アルカリ水酸化物で処理する際には、イオン交換、洗浄処理した二酸化マンガンを純水中に分散してスラリーとし、そこにアルカリを含有する水溶液を添加してpHを調整して処理することが好ましい。
【0038】
スラリー溶液のpH調整はpH=7以上のアルカリ性、さらにpH=9以上にすることがより好ましい。前述の(2)式を効率よく起こすための水酸化亜鉛への転換が必要であり、イオン交換した亜鉛を確実に水酸化亜鉛に転換できる領域にする必要があるからである。
【0039】
以下、本発明を実施例及び比較例により詳細に説明するが、本発明はこれに限定されるものではない。
【0040】
(ハイレート連続放電評価)
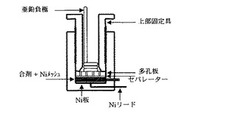
二酸化マンガン80wt%、導電剤としてカーボン5%、40%KOH水溶液15%で構成される混合物を調製し正極合材とした。当該正極合材を二酸化マンガン換算で0.09gとなるように秤量し、負極に亜鉛ワイヤーを使用して、図1に示した電池を作製した。当該電池を常温で1時間静置後、放電試験を行った。放電条件は100mA/cm2の電流密度で、終止電圧0.9Vとしたときの相対放電容量および相対放電エネルギーを評価した。なお、放電容量および放電エネルギーは比較例1(水酸化亜鉛を含まない市販の電解二酸化マンガン)の測定結果を100%とし、それに対する相対値で求めた。
【0041】
実施例1
電解二酸化マンガン(東ソー株式会社製;HH−TF)及び硫酸亜鉛水溶液(亜鉛濃度0.02wt%)を用い、二酸化マンガン10gに対して硫酸亜鉛水溶液50gとなるように混合し、1時間攪拌してイオン交換処理を行った。
【0042】
イオン交換処理後、ろ過し、20倍量の純水で十分に洗浄して二酸化マンガン粒子外表面の亜鉛を除去した。60℃で乾燥させた亜鉛イオン交換二酸化マンガンの亜鉛含有量は0.0154wt%であった。
【0043】
当該亜鉛イオン交換二酸化マンガンを純水に懸濁させスラリーとし、pH=9となるように水酸化ナトリウム水溶液でpH調整し、亜鉛イオンを水酸化亜鉛に転換し、ろ過、乾燥させて、水酸化亜鉛含有二酸化マンガンを得た。
【0044】
当該水酸化亜鉛含有二酸化マンガンのハイレート連続放電特性を評価した結果、放電容量は比較例1に対して109%であり、放電エネルギーは108%であった。結果を表1に示す。
【0045】
実施例2
硫酸亜鉛水溶液の亜鉛濃度を、二酸化マンガンの重量に対し0.2wt%とした以外は実施例1と同様の方法により二酸化マンガン粉末を得た。イオン交換後の亜鉛含有量は0.0406wt%であった。
【0046】
得られた二酸化マンガンのハイレート連続放電容量は103%であり、放電エネルギーは105%であった。結果を表1に示す。
【0047】
実施例3
硫酸亜鉛水溶液の亜鉛濃度を、二酸化マンガンの重量に対し2.0wt%とした以外は実施例1と同様の方法により二酸化マンガン粉末を得た。イオン交換後の亜鉛含有量は0.0854wt%であった。
【0048】
得られた二酸化マンガンのハイレート連続放電容量は106%であり、放電エネルギーは109%であった。結果を表1に示す。
【0049】
比較例1
水酸化亜鉛を含まない電解二酸化マンガン(東ソー株式会社製;HH−TF)をそのまま用い、ハイレート連続放電特性を測定した。得られた二酸化マンガンの測定結果を100%とした。結果を表1に示す。
【0050】
比較例2
二酸化マンガンを亜鉛イオン交換後、pH調整を施さなかった以外は実施例1と同様の方法により二酸化マンガン粉末を得た。
【0051】
得られた二酸化マンガンのハイレート連続放電容量は98%であり、放電エネルギーは95%であった。結果を表1に示す。
【0052】
比較例3
イオン交換後、ろ過・洗浄・乾燥を行わずにpH調製した以外は実施例1と同様の方法により二酸化マンガン粉末を得た。イオン交換後の亜鉛含有量は0.0254wt%であった。
【0053】
得られた二酸化マンガンは、ハイレート連続放電容量は98%であり、放電エネルギーは93%であった。結果を表1に示す。
【0054】
イオン交換後に洗浄を行わない不純物アニオンが含まれるものでは、ハイレート特性の向上は得られなかった。
【0055】
【表1】

【発明の効果】
【0056】
本発明の水酸化亜鉛含有二酸化マンガンは、アルカリマンガン乾電池の正極用活物質として用いて放電した際に二酸化マンガン内の水酸化物イオンを効率的に除去できるため、アルカリマンガン乾電池の正極用活物質に用いてハイレート放電をした場合に、従来にない高い放電容量及び放電エネルギーが達成される。
【図面の簡単な説明】
【0057】
【図1】ハイレート連続放電に用いた電池構造
【技術分野】
【0001】
本発明は、たとえばマンガン乾電池、特にアルカリマンガン乾電池において、正極活物質として使用される二酸化マンガンおよびその製造方法、用途に関する。
【背景技術】
【0002】
二酸化マンガンは、たとえばマンガン乾電池またはアルカリマンガン乾電池の正極活物質として知られており、保存性に優れ、且つ安価であるという利点を有する。特に、二酸化マンガンを正極活物質として用いるアルカリマンガン乾電池は、重負荷での放電特性に優れていることから電子カメラ、携帯用テープレコーダー、携帯情報機器、さらにはゲーム機や玩具にまで幅広く使用され、近年急速にその需要が伸びてきている。
【0003】
しかし、アルカリマンガン乾電池は、放電電流が大きくなるに従い正極活物質である二酸化マンガンの利用される量が低下し、また放電電圧が低下するために放電容量が大きく損なわれるという課題があり、例えば大電流を使用(ハイレート放電)する機器にアルカリマンガン乾電池を用いると充填されている正極活物質である二酸化マンガンが十分に使用されず使用時間が短くなるという欠点を有していた。そこで短時間に大電流を取り出すハイレート放電条件においても、高容量、長寿命を発現できる優れた二酸化マンガン、所謂ハイレート特性に優れた二酸化マンガンが望まれていた。
【0004】
この様な課題に対する解決策として、二酸化マンガンに異種元素を添加したアルカリマンガン乾電池用正極活物質を利用する技術が知られている。前駆体に亜鉛を添加した正極活物質の利用として、二酸化マンガンを化学合成する際に、前駆体である天然二酸化マンガンに酸化亜鉛を添加した正極活物質の合成方法が報告されている(特許文献1)。しかし、化学合成された二酸化マンガン内部にヘテロライト(Mn2ZnO4)を生成させると、電池の正極活物質含有量が減少し、電池当りの放電容量低下を伴う。
【0005】
また、弱酸性(pH4.2)の電解二酸化マンガンに塩化亜鉛溶液で処理して塩化亜鉛型の二酸化マンガンを得る方法が提案されている(特許文献2)。この方法では正極合剤のpH変動に付随する特性のばらつきが抑制され、放電特性の改善がされるが、当該方法では中性雰囲気下のマンガン乾電池への効果は大きいが、強アルカリ性雰囲気下に置かれているアルカリマンガン乾電池においては十分な効果が得られていなかった。また、電解二酸化マンガンに対する塩化亜鉛溶液の濃度が高いために、過剰な亜鉛が付着しており、なおかつ不純物アニオンが含まれるためハイレート特性の改善が得られるものではなかった。
【0006】
さらに、酸化亜鉛を正極合剤中に添加する方法が提案されている(特許文献3)。この方法では二酸化マンガン表面に固定した酸化亜鉛が溶出することにより正極合剤の濡れ性が改善し、電池の安定化時間が短縮されるが、放電特性の改善効果は得られていなかった。
【0007】
他にも、アルカリマンガン乾電池における亜鉛の利用として、二酸化マンガンとオキシ水酸化ニッケルとを正極活物質としたアルカリマンガン乾電池において、オキシ水酸化ニッケルに亜鉛を固溶させる方法が提案されている(特許文献4、5)。この方法では亜鉛の固溶および酸化亜鉛の添加でオキシ水酸化ニッケルの自己放電が抑制されるが、当該方法では自己放電の大きいオキシ水酸化ニッケルへ効果はあるが、二酸化マンガンのみを正極活物質としたアルカリマンガン乾電池では効果が得られなかった。
【0008】
【特許文献1】特開昭58−161259号
【特許文献2】特開昭59−194357号
【特許文献3】特開平01−102852号
【特許文献4】特開2002−075354
【特許文献5】特開2006−179429
【発明の開示】
【発明が解決しようとする課題】
【0009】
異種元素、特に亜鉛を含む二酸化マンガンを正極活物質としたアルカリマンガン電池において、ハイレート特性に優れたものは得られていなかった。本発明の目的は、特にアルカリマンガン乾電池の正極活物質として使用される二酸化マンガンにおいて、大電流で放電時間が長い、所謂ハイレート特性に優れた二酸化マンガンを提供することである。
【課題を解決するための手段】
【0010】
本発明者等は、特にアルカリマンガン乾電池の正極活物質として使用される二酸化マンガンについて鋭意検討を重ねた結果、水酸化亜鉛を有してなる二酸化マンガン、特に二酸化マンガンのイオン交換サイトに水酸化亜鉛を有する二酸化マンガンでは、ハイレート特性に著しく優れることを見出し、本発明を完成するに至ったものである。
【0011】
以下、本発明の二酸化マンガンについて詳細に説明する。
【0012】
本発明の二酸化マンガンは、水酸化亜鉛を有してなる二酸化マンガンである。本発明の二酸化マンガンに含まれる亜鉛は水酸化亜鉛であるため、亜鉛をイオン状態(Zn2+)、酸化亜鉛、塩化亜鉛、硫酸亜鉛などの形態で含む従来のものとは異なるものである。
【0013】
本発明における二酸化マンガンは特に限定はないが、電解二酸化マンガン(EMD)であることが好ましい。
【0014】
本発明で二酸化マンガンに含まれる水酸化亜鉛は、イオン交換によって二酸化マンガンに導入した亜鉛イオンをアルカリ(水酸化ナトリウム、水酸化カリウム等)で水酸化亜鉛に転換したものが好ましい。
【0015】
本発明の二酸化マンガンに含まれる水酸化亜鉛は、二酸化マンガンのイオン交換サイトに存在することが好ましく、さらに、二酸化マンガン粒子の細孔内部(細孔内表面)のイオン交換サイトに存在することが好ましい。
【0016】
本発明における「イオン交換サイト」とは、二酸化マンガンのカチオン交換サイトのことである。二酸化マンガンは金属イオンなどのカチオン交換能を有している。これは、二酸化マンガン中にMn4+とMn3+が存在する場合に、Mn3+の電価不足を補償するために存在するH+と、金属イオンの交換により起こる場合や、二酸化マンガン表面の末端水酸基のH+が金属イオンと交換することで、カチオン交換が起こることが知られている。
【0017】
本発明における「イオン交換サイトに水酸化亜鉛を有してなる」とは、イオン交換サイトに直接に水酸化亜鉛が存在する場合や、イオン交換サイトの近傍に水酸化亜鉛が存在することを指す。前者の場合、イオン交換サイトの亜鉛イオンが、アルカリ性領域になったときに亜鉛イオンの移動を伴わずに、水酸化物化して水酸化亜鉛となる場合が考えられる。このときイオン交換サイトの電化補償はイオン交換サイト近傍のH+などの他のカチオンによりなされると考えられる。また、後者の場合、アルカリ性領域になったときに、イオン交換サイトの亜鉛イオンとアルカリ金属イオンとの間で交換が起こり、イオン交換サイトを外れた亜鉛イオンが、イオン交換サイト近傍で速やかに水酸化物化して水酸化亜鉛となる場合が考えられる。
【0018】
本発明の水酸化亜鉛の存在部位は、二酸化マンガン粒子全面を覆う被覆や、二酸化マンガンの結晶構造中、或いは一次粒子の内部に亜鉛が存在するものとは異なる。特に二酸化マンガン粒子の外表面を被覆する水酸化亜鉛では、本発明のハイレート特性の向上への寄与が小さいため、外表面の水酸化亜鉛は少ない方が好ましい。
【0019】
本発明の二酸化マンガンに対する水酸化亜鉛の含有量は、亜鉛換算で0.01wt%以上0.10wt%以下であることが好ましい。亜鉛の含有量が0.10wt%以上では水酸化亜鉛が二酸化マンガンの細孔を閉塞したり、二酸化マンガン粒子の表面を被覆し、電池反応を阻害し、ハイレート特性が低下する場合がある。一方、0.01wt%以下では、本発明のハイレート特性の改善効果が得られ難い。
【0020】
本発明において二酸化マンガンのハイレート特性が改善されるメカニズムは必ずしも明確にはなっていないが、以下のような機構によって改善されているものと考えられる。
【0021】
アルカリマンガン乾電池における二酸化マンガンの放電は(1)式によって進行することが知られている。
【0022】
MnO2 + H2O + e− → MnOOH + OH− (1)
従来、アルカリマンガン乾電池に含まれる二酸化マンガンは利用率が低く、(1)式に示した放電反応はアルカリマンガン乾電池に含まれる二酸化マンガンの30%程度しか関与してない。したがって、放電後のアルカリマンガン乾電池正極活物質は30%がMnOOHになっているが、残りの70%はMnO2のままで、電池として利用できていない。ここで(1)式から明らかなように、放電反応ではOH―が生成されるため、生成したOH−を効率的に除去することにより(1)式が進行し、放電反応が促進されると考えられる。
【0023】
アルカリマンガン乾電池は電解液に40%の水酸化カリウム溶液を使用しており、電池内部は強アルカリ雰囲気である。このようなアルカリ雰囲気下において、亜鉛は(2)式の平衡反応を起こすと考えられる。
【0024】
【数1】

即ち、(1)式の放電反応が起きる近傍で(2)式の反応が起こる環境を作り出せば放電反応で排出されるOH−が消費され、Zn(OH)42―が生成し、その結果として(1)式が促進され、結果的に放電反応が促進され、ハイレート特性が改善すると考えられる。
【0025】
従来、例えば塩化亜鉛で処理した場合にも電池の中で水酸化亜鉛は形成していると考えられるが、塩化物型の二酸化マンガンでは塩素などのアニオンを含有しているため、これら含有されたアニオンが副反応を引き起こすなどして、上記の反応を阻害するために十分なハイレート特性が得られないものと考えられる。よって本発明の水酸化物には塩素等の不純物アニオンを含まないものが好ましい。
【0026】
アルカリマンガン乾電池で使用される二酸化マンガンは通常は多孔質であり、電池反応は細孔内で多く進行するが、細孔内部では特に排出されたOH−が残存し易く、それが電池利用率の低下の原因となっている。本発明では、その様な細孔内部(細孔内表面)のOH−イオンを効率的に除去する様に、細孔内部に水酸化亜鉛を配置することにより優れたハイレート特性を達成するものである。
【0027】
二酸化マンガン粒子の外表面(細孔外)ではOH−イオンの除去は容易であるため、外表面に水酸化物を配置する効果は細孔内に比べて小さく、ハイレート特性向上に寄与しないため、外表面には水酸化亜鉛は付着していないことが好ましい。
【0028】
次に、本発明の二酸化マンガンの製造方法について説明する。
【0029】
本発明の二酸化マンガンは、二酸化マンガンを亜鉛イオン含有水溶液でイオン交換し、洗浄後、さらにアルカリ水酸化物と反応させることによって製造することができる。
【0030】
二酸化マンガンはイオン交換能を有するため、亜鉛塩の水溶液で処理することにより、容易にイオン交換することができる。
【0031】
二酸化マンガンに対する亜鉛イオンのイオン交換量は、亜鉛イオン含有溶液の濃度で制御できる。
【0032】
本発明で用いる亜鉛イオン含有溶液の原料亜鉛は特に限定されないが、亜鉛塩、例えば硫酸亜鉛、硝酸亜鉛等の無機塩、酢酸亜鉛、クエン酸亜鉛等の有機酸塩が用いることができる。さらに、亜鉛溶液の溶媒も限定されないが、水を用いることが好ましい。
【0033】
イオン交換の時間、温度は用いる二酸化マンガンの細孔量、亜鉛イオン含有溶液の濃度によって異なるため一概に決められないが、二酸化マンガンの細孔量、亜鉛イオン含有溶液の濃度によって水酸化亜鉛の含有量が亜鉛換算で0.01wt%以上0.10wt%以下となる様に適宜選択して用いればよい。
【0034】
先に説明した通り、亜鉛水酸化物は二酸化マンガンの細孔内部に局在することが好ましいため、イオン交換処理の後、十分に洗浄して粒子外表面の亜鉛、及び不純物アニオンは除去することが好ましい。
【0035】
細孔表面のイオン交換サイトにイオン交換された亜鉛イオンは洗浄によって除去され易い。そこで少なくとも細孔内のイオン交換サイトに水酸化亜鉛を配置するためには、イオン交換後の二酸化マンガンを洗浄して表面の亜鉛イオンを除去した後にアルカリと反応させることにより、細孔内に選択的に水酸化亜鉛が位置したものが得られる。
【0036】
イオン交換後、洗浄せずにアルカリ水酸化物と反応させた場合、本発明の効果が得られ難い場合があるが、これは過剰の亜鉛イオン、特に粒子表面(細孔外)に残存する亜鉛イオンが選択的に水酸化亜鉛に転換し、ハイレート特性を改善する細孔内の亜鉛が十分に水酸化亜鉛とならないことが原因と考えられる。
【0037】
洗浄後、アルカリ水酸化物で処理し、細孔表面及び/又は内部の亜鉛イオンを水酸化亜鉛に転換する。アルカリ水酸化物で処理する際には、イオン交換、洗浄処理した二酸化マンガンを純水中に分散してスラリーとし、そこにアルカリを含有する水溶液を添加してpHを調整して処理することが好ましい。
【0038】
スラリー溶液のpH調整はpH=7以上のアルカリ性、さらにpH=9以上にすることがより好ましい。前述の(2)式を効率よく起こすための水酸化亜鉛への転換が必要であり、イオン交換した亜鉛を確実に水酸化亜鉛に転換できる領域にする必要があるからである。
【0039】
以下、本発明を実施例及び比較例により詳細に説明するが、本発明はこれに限定されるものではない。
【0040】
(ハイレート連続放電評価)
二酸化マンガン80wt%、導電剤としてカーボン5%、40%KOH水溶液15%で構成される混合物を調製し正極合材とした。当該正極合材を二酸化マンガン換算で0.09gとなるように秤量し、負極に亜鉛ワイヤーを使用して、図1に示した電池を作製した。当該電池を常温で1時間静置後、放電試験を行った。放電条件は100mA/cm2の電流密度で、終止電圧0.9Vとしたときの相対放電容量および相対放電エネルギーを評価した。なお、放電容量および放電エネルギーは比較例1(水酸化亜鉛を含まない市販の電解二酸化マンガン)の測定結果を100%とし、それに対する相対値で求めた。
【0041】
実施例1
電解二酸化マンガン(東ソー株式会社製;HH−TF)及び硫酸亜鉛水溶液(亜鉛濃度0.02wt%)を用い、二酸化マンガン10gに対して硫酸亜鉛水溶液50gとなるように混合し、1時間攪拌してイオン交換処理を行った。
【0042】
イオン交換処理後、ろ過し、20倍量の純水で十分に洗浄して二酸化マンガン粒子外表面の亜鉛を除去した。60℃で乾燥させた亜鉛イオン交換二酸化マンガンの亜鉛含有量は0.0154wt%であった。
【0043】
当該亜鉛イオン交換二酸化マンガンを純水に懸濁させスラリーとし、pH=9となるように水酸化ナトリウム水溶液でpH調整し、亜鉛イオンを水酸化亜鉛に転換し、ろ過、乾燥させて、水酸化亜鉛含有二酸化マンガンを得た。
【0044】
当該水酸化亜鉛含有二酸化マンガンのハイレート連続放電特性を評価した結果、放電容量は比較例1に対して109%であり、放電エネルギーは108%であった。結果を表1に示す。
【0045】
実施例2
硫酸亜鉛水溶液の亜鉛濃度を、二酸化マンガンの重量に対し0.2wt%とした以外は実施例1と同様の方法により二酸化マンガン粉末を得た。イオン交換後の亜鉛含有量は0.0406wt%であった。
【0046】
得られた二酸化マンガンのハイレート連続放電容量は103%であり、放電エネルギーは105%であった。結果を表1に示す。
【0047】
実施例3
硫酸亜鉛水溶液の亜鉛濃度を、二酸化マンガンの重量に対し2.0wt%とした以外は実施例1と同様の方法により二酸化マンガン粉末を得た。イオン交換後の亜鉛含有量は0.0854wt%であった。
【0048】
得られた二酸化マンガンのハイレート連続放電容量は106%であり、放電エネルギーは109%であった。結果を表1に示す。
【0049】
比較例1
水酸化亜鉛を含まない電解二酸化マンガン(東ソー株式会社製;HH−TF)をそのまま用い、ハイレート連続放電特性を測定した。得られた二酸化マンガンの測定結果を100%とした。結果を表1に示す。
【0050】
比較例2
二酸化マンガンを亜鉛イオン交換後、pH調整を施さなかった以外は実施例1と同様の方法により二酸化マンガン粉末を得た。
【0051】
得られた二酸化マンガンのハイレート連続放電容量は98%であり、放電エネルギーは95%であった。結果を表1に示す。
【0052】
比較例3
イオン交換後、ろ過・洗浄・乾燥を行わずにpH調製した以外は実施例1と同様の方法により二酸化マンガン粉末を得た。イオン交換後の亜鉛含有量は0.0254wt%であった。
【0053】
得られた二酸化マンガンは、ハイレート連続放電容量は98%であり、放電エネルギーは93%であった。結果を表1に示す。
【0054】
イオン交換後に洗浄を行わない不純物アニオンが含まれるものでは、ハイレート特性の向上は得られなかった。
【0055】
【表1】

【発明の効果】
【0056】
本発明の水酸化亜鉛含有二酸化マンガンは、アルカリマンガン乾電池の正極用活物質として用いて放電した際に二酸化マンガン内の水酸化物イオンを効率的に除去できるため、アルカリマンガン乾電池の正極用活物質に用いてハイレート放電をした場合に、従来にない高い放電容量及び放電エネルギーが達成される。
【図面の簡単な説明】
【0057】
【図1】ハイレート連続放電に用いた電池構造
【特許請求の範囲】
【請求項1】
水酸化亜鉛を有してなる二酸化マンガン。
【請求項2】
二酸化マンガンのイオン交換サイトに水酸化亜鉛を有してなる請求項1に記載の二酸化マンガン。
【請求項3】
少なくとも二酸化マンガンの細孔内部のイオン交換サイトに水酸化亜鉛を有してなる請求項1乃至2に記載の二酸化マンガン。
【請求項4】
二酸化マンガンに対する水酸化亜鉛の含有量が亜鉛換算で0.01wt%以上0.10wt%以下である請求項1乃至3に記載の二酸化マンガン。
【請求項5】
二酸化マンガンを亜鉛イオン含有水溶液でイオン交換し、洗浄後、さらにアルカリ水酸化物と反応させる請求項1乃至4に記載の二酸化マンガンの製造方法。
【請求項6】
請求項1乃至4に記載の二酸化マンガンを含んでなる電池用正極活物質。
【請求項7】
請求項6に記載の電池用正極活物質を用いてなる電池。
【請求項1】
水酸化亜鉛を有してなる二酸化マンガン。
【請求項2】
二酸化マンガンのイオン交換サイトに水酸化亜鉛を有してなる請求項1に記載の二酸化マンガン。
【請求項3】
少なくとも二酸化マンガンの細孔内部のイオン交換サイトに水酸化亜鉛を有してなる請求項1乃至2に記載の二酸化マンガン。
【請求項4】
二酸化マンガンに対する水酸化亜鉛の含有量が亜鉛換算で0.01wt%以上0.10wt%以下である請求項1乃至3に記載の二酸化マンガン。
【請求項5】
二酸化マンガンを亜鉛イオン含有水溶液でイオン交換し、洗浄後、さらにアルカリ水酸化物と反応させる請求項1乃至4に記載の二酸化マンガンの製造方法。
【請求項6】
請求項1乃至4に記載の二酸化マンガンを含んでなる電池用正極活物質。
【請求項7】
請求項6に記載の電池用正極活物質を用いてなる電池。
【図1】




【公開番号】特開2010−70389(P2010−70389A)
【公開日】平成22年4月2日(2010.4.2)
【国際特許分類】
【出願番号】特願2008−235970(P2008−235970)
【出願日】平成20年9月16日(2008.9.16)
【出願人】(000003300)東ソー株式会社 (1,901)
【Fターム(参考)】
【公開日】平成22年4月2日(2010.4.2)
【国際特許分類】
【出願日】平成20年9月16日(2008.9.16)
【出願人】(000003300)東ソー株式会社 (1,901)
【Fターム(参考)】
[ Back to top ]

