バイオセンサ
【課題】、簡易にターゲット物質を検知することができるバイオセンサ、および、バイオセンサの製造方法の提供。
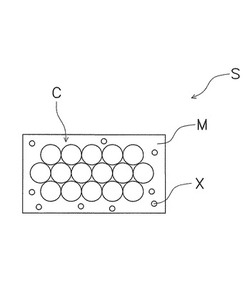
【解決手段】バイオセンサSは、フォトニック結晶Cと、刺激応答性高分子材料Mとを備えている。フォトニック結晶Cは、周期構造体から構成されている。刺激応答性高分子材料Mは、ターゲット物質と特異的に結合あるいは反応する特異的結合物質Xを含む。また、刺激応答性高分子材料Mは、ターゲット物質と特異的結合物質Xとが結合あるいは反応することによって、体積変化する。さらに、フォトニック結晶Cは、刺激応答性高分子材料Mに内包されている。
【解決手段】バイオセンサSは、フォトニック結晶Cと、刺激応答性高分子材料Mとを備えている。フォトニック結晶Cは、周期構造体から構成されている。刺激応答性高分子材料Mは、ターゲット物質と特異的に結合あるいは反応する特異的結合物質Xを含む。また、刺激応答性高分子材料Mは、ターゲット物質と特異的結合物質Xとが結合あるいは反応することによって、体積変化する。さらに、フォトニック結晶Cは、刺激応答性高分子材料Mに内包されている。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、バイオセンサならびにバイオセンサの製造方法に関する。
【背景技術】
【0002】
近年、研究機関や医療機関において遺伝子解析や臨床診断等の目的で使用される様々なバイオセンサが開発されている。
【0003】
例えば、特許文献1(特開2007−271609号公報)に開示されているバイオセンサは、特異的結合物質が三次元フォトニック結晶の表面に固定されている。
【0004】
三次元フォトニック結晶には、その周期的な屈折率分布によって、対応する波長の電磁波がブラッグ反射を受けて、電磁波に対するバンドギャップ(フォトニックバンドギャップ)が形成されるという特徴がある。また、フォトニックバンドギャップはフォトニック結晶の表面状態の変化に敏感に反応するため、フォトニック結晶の表面状態の変化に応じてフォトニックバンドギャップに由来する反射スペクトルのピーク波長が変化する。
【0005】
このため、特許文献1に開示されているバイオセンサでは、ターゲット物質と特異的結合物質とが結合する前後において、特定波長の電磁波をフォトニック結晶に照射して得られるフォトニックバンドギャップ由来の反射スペクトルのピーク波長を比較することで、ターゲット物質の有無を検知することができる。このように、このバイオセンサでは、フォトニック結晶の表面に生じる変化を検出することで、ターゲット物質を検知している。
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかしながら、特許文献1に開示されているバイオセンサでは、ターゲット物質の有無を検知するために、分光光度計等の測定機器を用いてフォトニック結晶の反射スペクトルの波長を検出する必要があり、操作が煩雑である。
【0007】
そこで、本発明の課題は、簡易にターゲット物質を検知することができるバイオセンサ、および、バイオセンサの製造方法を提供することにある。
【課題を解決するための手段】
【0008】
第1発明に係るバイオセンサは、フォトニック結晶と、刺激応答性高分子材料とを備えている。フォトニック結晶は、周期的に配置されている粒子から構成されている。刺激応答性高分子材料は、ターゲット物質と特異的に結合あるいは反応する特異的結合物質を含む。また、刺激応答性高分子材料は、ターゲット物質と特異的結合物質とが結合あるいは反応することによって、体積変化する。さらに、フォトニック結晶は、刺激応答性高分子材料に内包されている。
【0009】
第1発明に係るバイオセンサでは、フォトニック結晶が、刺激応答性高分子材料に内包されている。ここで、フォトニック結晶は、その粒子間距離に応じて異なる光学特性が観察されることが知られている。このため、例えば、刺激応答性高分子材料の体積変化に伴ってフォトニック結晶の粒子間距離が変化する場合には、フォトニック結晶の色調を変化させることができる。したがって、例えば、フォトニック結晶の色調が可視領域で変化する場合には、測定機器を用いなくても、目視でターゲット物質を検知することができる。
【0010】
これによって、簡易にターゲット物質を検知することができる。
【0011】
第2発明に係るバイオセンサは、第1発明のバイオセンサであって、フォトニック結晶の粒子の平均粒径は、50〜500nmの範囲内にある。このため、このバイオセンサでは、可視領域中でフォトニック結晶の色調を観察することができる。
【0012】
第3発明に係るバイオセンサは、第1発明または第2発明のバイオセンサであって、刺激応答性高分子材料の体積変化に伴ってフォトニック結晶の粒子間距離が変化する。また、フォトニック結晶の粒子間距離の変化に伴って、フォトニック結晶の色調が変化する。このため、このバイオセンサでは、色調の変化に基づいて、ターゲット物質を検知することができる。
【0013】
第4発明に係るバイオセンサの製造方法は、第1工程と、第2工程とを備える。第1工程は、周期的に配置されている粒子から構成されるフォトニック結晶と、体積変化可能な刺激応答性高分子材料とを混合し、刺激応答性高分子材料がフォトニック結晶を内包したフォトニック結晶内包刺激応答性高分子材料を得る工程である。第2工程は、第1工程で得られたフォトニック結晶内包刺激応答性高分子材料に、ターゲット物質と特異的に結合あるいは反応する特異的結合物質を固定する工程である。
【0014】
第4発明に係るバイオセンサの製造方法では、フォトニック結晶内包刺激応答性高分子材料に特異的結合物質が固定化されたバイオセンサが製造されている。このため、例えば、刺激応答性高分子材料がターゲット物質と特異的結合物質との結合あるいは反応によって体積変化し、刺激応答性高分子材料の体積変化に伴ってフォトニック結晶の粒子間距離が変化する場合には、フォトニック結晶の色調を変化させることができる。したがって、例えば、フォトニック結晶の色調が可視領域で変化する場合には、測定機器を用いなくても、目視でターゲット物質を検知することができる。
【0015】
これによって、この製造方法で製造されるバイオセンサでは、簡易にターゲット物質を検知することができる。
【0016】
第5発明に係るターゲット物質の検知方法は、第1検知工程と、第2検知工程とを備えている。第1検知工程は、第1発明から第3発明のいずれかのバイオセンサと、試料とを接触させる工程である。また、第2検知工程は、バイオセンサと試料との接触部分の色調を、所定方向から目視により観察する工程である。
【0017】
第5発明に係るターゲット物質の検知方法では、バイオセンサと試料との接触部分の色調が目視によって観察されている。このため、例えば、特異的結合物質と結合あるいは反応するターゲット物質が試料に含まれている場合であって、バイオセンサの備える刺激応答性高分子材料がターゲット物質と特異的結合物質との結合あるいは反応によって体積変化し、刺激応答性高分子材料の体積変化に伴ってバイオセンサの備えるフォトニック結晶の粒子間距離が変化する場合には、フォトニック結晶の色調を変化させることができる。したがって、例えば、フォトニック結晶の色調が可視領域で変化する場合には、測定機器を用いなくても、目視でターゲット物質を検知することができる。
【0018】
これによって、このターゲット物質の検知方法を適用可能なバイオセンサでは、簡易にターゲット物質を検知することができる。
【発明の効果】
【0019】
第1発明に係るバイオセンサでは、簡易にターゲット物質を検知することができる。
【0020】
第2発明に係るバイオセンサでは、可視領域中でフォトニック結晶の色調を観察することができる。
【0021】
第3発明に係るバイオセンサでは、色調の変化に基づいて、ターゲット物質を検知することができる。
【0022】
第4発明に係るバイオセンサの製造方法では、簡易にターゲット物質を検知することができる。
【0023】
第5発明に係るターゲット物質の検知方法では、簡易にターゲット物質を検知することができる。
【図面の簡単な説明】
【0024】
【図1】本発明のバイオセンサの概念図。
【図2】フォトニック結晶において(a)粒子間距離が変化する様子を示す概略図、(b)粒子間距離とピーク波長との関係を示す概略図。
【図3】実施例におけるピーク波長の経時的な変化を示す図。
【発明を実施するための形態】
【0025】
本発明のバイオセンサSは、周期的に配置されている粒子(周期構造体)から構成されるフォトニック結晶Cと、外部からの刺激によって体積変化する刺激応答性高分子材料Mとを備えている。また、刺激応答性高分子材料Mは、ターゲット物質と特異的に結合あるいは反応する特異的結合物質Xを含有している。さらに、このバイオセンサSでは、フォトニック結晶Cが、刺激応答性高分子材料Mに内包されている(図1参照)。なお、本発明の主旨を逸脱しない限り、本発明のバイオセンサSは、実施例に限定されるものではない。
【0026】
<フォトニック結晶>
本発明における周期構造体は、一定の規則性、即ち、周期性を有する構造体であって、その周期構造としては、結晶性無機固体と同様の結晶構造である六方最密充填構造、立方最密充填構造、体心立方充填構造、ログパイル構造、ダイヤモンド構造等が挙げられる。なお、これらの周期構造のうちでは、六方最密充填構造が好ましい。
【0027】
また、本発明におけるフォトニック結晶Cは、三次元的な屈折率分布をもつフォトニック結晶である。このような構造のフォトニック結晶Cには、半導体において原子核の周期ポテンシャルによって電子(電子波)がブラッグ反射を受けてバンドギャップが形成されるのと同様に、周期的な屈折率分布によって対応する波長の電磁波がブラッグ反射を受けて、電磁波に対するバンドギャップ(フォトニックバンドギャップ)が形成されるという特徴がある。さらに、フォトニック結晶Cは、材質元素が不変であっても、粒子間距離(周期構造の格子定数)や格子構造に敏感に左右される光学特性を有する。このため、フォトニック結晶Cの粒子間距離が変化することで、吸光度が最大となる波長(以下、ピーク波長という)が長波長側または短波長側にシフトする(図2参照)。したがって、フォトニック結晶Cに特定波長の光を照射すると、観測される反射光の色がフォトニック結晶Cの粒子間距離によって変化する。
【0028】
また、フォトニック結晶Cを構成するナノ粒子としては、例えば、シリカナノ粒子、ポリスチレンナノ粒子、TiO2、ITO、アガロースナノ粒子等の誘電体ナノ粒子が挙げられる。なお、可視領域中でフォトニック結晶Cの色調を観察するためには、ナノ粒子の平均粒子径が50〜500nmの範囲内であること好ましい。また、ナノ粒子の平均粒子径は、200nmであるものがより好ましい。
【0029】
<刺激応答性高分子材料>
本発明における刺激応答性高分子材料Mとしては、外部からの刺激、例えば、熱の付与、電界の付与、イオン強度の変化、磁界の付与、および、力学的刺激等の環境変化に応じて体積変化(膨潤および収縮)する性質を有する材料であればよく、例えば、アクリルアミド、ポリジメチルシロキサン、ポリビニルアルコール、ナフィオン、ポリアクリル酸アミド、N-イソプロピルアクリルアミド、アルギン酸ナトリウムおよびアクリル酸ナトリウム等が挙げられる。なお、刺激応答性高分子材料は、特異的結合物質Xに応じて最適な材料を適宜選択すればよい。
【0030】
熱の付与によって刺激応答する材料としては、例えば、N-イソプロピルアクリルアミド等が挙げられる。
【0031】
電界の付与によって刺激応答する材料としては、例えば、ナフィオン等が挙げられる。
【0032】
イオン強度の変化によって刺激応答する材料としては、例えば、アクリルアミドが挙げられる。
【0033】
磁界の付与によって刺激応答する材料としては、例えば、磁性ナノ粒子包含高分子等が挙げられる。
【0034】
力学的刺激の付与によって応答する材料としては、ポリマー材料であればよく、例えば、アガロース等が挙げられる。
【0035】
上記に挙げた刺激応答性高分子材料Mの中で特に好ましい材料としては、イオン強度の変化によって応答(膨潤および収縮)するアクリルアミド、溶媒の極性の変化によって応答(膨潤および収縮)するポリジメチルシロキサン、湿度の変化によって応答(膨潤および収縮)するポリアクリル酸アミド等が挙げられる。
【0036】
<特異的結合物質>
本発明における特異的結合物質Xとは、試料溶液中に含まれるターゲット物質と特異的に結合あるいは反応する物質(生体認識素子)であればよく、例えば、酵素、タンパク質、糖鎖、DNA、RNAおよびペプチド核酸等が挙げられる。
【0037】
また、試料溶液中に含まれるターゲット物質とは、特異的結合物質Xと特異的に結合あるいは反応する物質である。例えば、特異的結合物質Xが抗体の場合は、ターゲット物質はその抗体が認識する抗原である。また、例えば、特異的結合物質Xが遺伝子の場合には、ターゲット物質は相補的な遺伝子である。
【0038】
また、酵素としては、酸化還元酵素、加水分解酵素、異性化酵素、脱離酵素、合成酵素等を使用することができる。具体的には、グルコースオキシダーゼ、アルコールオキシダーゼ、アルデヒドデヒドロゲナーゼ等が挙げられる。このため、例えば、ターゲット物質がグルコースである場合には、特異的結合物質Xとしてグルコースオキシダーゼを使用することができる。また、例えば、ターゲット物質がアルコール類である場合には、特異的結合物質Xとしてアルコールオキシダーゼを使用することができる。
【0039】
また、タンパク質としては、抗体を使用することができる。具体的には、抗C反応性タンパク質抗体が挙げられる。このため、例えば、ターゲット物質がC反応性タンパク質である場合には、特異的結合物質Xとして抗C反応性タンパク質抗体を使用することができる。
【0040】
また、例えば、ターゲット物質がレクチンである場合には、特異的結合物質Xとして糖鎖を使用することができる。
【0041】
また、DNA、RNAおよびペプチド核酸としては、例えば、ターゲットとなる核酸と相補的にハイブリダイズするものを使用することができる。
【0042】
以上、説明したように、本発明のバイオセンサSは、ターゲット物質と特異的結合物質Xとの結合あるいは反応に基づく刺激により体積変化する刺激応答性高分子材料Mと、フォトニック結晶Cと、を備えており、フォトニック結晶Cが刺激応答性高分子材料Mに内包されている。また、刺激応答性高分子材料Mには、特異的結合物質Xが導入されて固定されている。このため、刺激応答性高分子材料Mに外部刺激を付与する(ターゲット物質を添加して特異的結合物質Xと結合あるいは反応させる)ことでイオン強度等の環境変化が生じ、前記環境変化によって刺激応答性高分子材料Mが体積変化(膨潤または収縮)し、刺激応答性高分子材料Mの体積変化に基づいてフォトニック結晶Cの粒子間距離が変化する。これによって、フォトニック結晶Cの色調を変化させることができる。なお、特異的結合物質Xは、刺激応答性高分子材料Mの内部に存在していてもよく、表面上に存在していてもよい。
【0043】
次に、本発明のバイオセンサSの製造方法について説明する。
【0044】
<バイオセンサの製造方法>
本発明のバイオセンサSの製造方法は第1工程と第2工程とを有しており、本発明のバイオセンサSは第1工程と第2工程とを経ることで製造することができる。第1工程とは、フォトニック結晶Cを内包した刺激応答性高分子材料Mを合成する工程である。また、第2工程とは、第1工程で得られたフォトニック結晶Cを内包した刺激応答性高分子材料Mに、特異的結合物質Xを固定化する工程である。
【0045】
次に、本実施形態におけるバイオセンサSの製造工程を記載する。
【0046】
第1工程では、フォトニック結晶Cを内包したポリアクリルアミドゲル(以下、フォトニック結晶内包型ポリアクリルアミドゲルという)が合成される。また、第2工程では、フォトニック結晶内包型ポリアクリルアミドゲルに特異的結合物質Xが固定化される。
【0047】
また、第1工程には、混合工程と、攪拌工程と、重合工程とが含まれる。さらに、第2工程には、洗浄工程と、加水分解処理工程と、COOH基活性化工程と、NHS基導入工程と、特異的結合物質浸漬工程とが含まれる。
【0048】
具体的には、混合工程では、9mlのシリカナノ粒子溶液(日本触媒社製のKE-W10)中に、0.9gのアクリルアミド(和光純薬工業社製のAcrylamide-HG)、0.1gのメチレンビスアクリルアミド(和光純薬工業社製のN,N'-methylenebis(acrylamide))、1.0gのイオン交換樹脂(BioRad社製のAG○R508-X8resin)、および、0.08gの重合開始剤(和光純薬工業社製社製の2,2'-Azobis[2-methyl-N-(2-hydroxyethyl)propion amide])を混合して混合溶液が作成される。なお、刺激応答性高分子材料を重合させるための重合開始剤は、非イオン性の重合開始剤であることが好ましい。
【0049】
攪拌工程では、混合工程で得られた混合溶液を、アズワン株式会社製のマイクロチューブローテーターを用いて1時間攪拌する。
【0050】
重合工程では、攪拌工程を経た混合溶液からイオン交換樹脂が取り除かれ、重合用容器内で光照射による光重合が行われる。具体的には、混合溶液を、6500rpmで10秒間遠心分離することで、攪拌工程を経た混合溶液からイオン交換樹脂が取り除かれる。なお、混合溶液からのイオン交換樹脂の除去方法は、遠心分離に限定されず、フォトニック結晶Cによる色調が観察可能な状態を維持することができる除去方法であればよい。また、重合用容器の形状やサイズは、フォトニック結晶Cの色調が観察可能なように重合させることができるものであればよい。さらに、光重合の方法としては、当業者に公知の手法が採用され得る。そして、重合に必要とされる時間は、使用される重合開始剤の種類や濃度に応じて最適な時間が採用され得る。これによって、フォトニック結晶内包型ポリアクリルアミドゲルを得ることができる。
【0051】
洗浄工程では、フォトニック結晶内包型ポリアクリルアミドゲルが重合用容器から取り出され、超純水中に浸漬される。これによって、フォトニック結晶内包型ポリアクリルアミドゲルから余剰の試薬が除去される。なお、ここでは、洗浄操作に使用する溶媒として、超純水が使用されているが、これに代えて、イオン交換水、または、蒸留水等が使用されてもよい。
【0052】
加水分解処理工程では、洗浄工程を経たフォトニック結晶内包型ポリアクリルアミドゲルが、1Nの水酸化ナトリウム(NaOH)(和光純薬工業社製のNaOH)溶液中に浸漬された状態で、1時間静置される。これによって、フォトニック結晶内包型ポリアクリルアミドゲルに加水分解処理が施される。なお、NaOH溶液の濃度および静置する時間(加水分解処理を施す時間)については、これに限定されず、バイオセンサSとして使用可能なように刺激応答性高分子材料Mが体積変化するために必要な所定量以上の特異的結合物質Xの固定化が可能であればよい。
【0053】
COOH基活性化工程では、加水分解工程を経て加水分解処理が施されたフォトニック結晶内包型ポリアクリルアミドゲルが超純水で洗浄された後、1mol/lの1-ethyl-3-(3-dimethylaminopropyl)carbodiimidehydrochloride(EDC)(DOJINDO社製)溶液中に浸漬された状態で、1時間静置される。これによって、フォトニック結晶内包型ポリアクリルアミドゲルにおいて、加水分解処理によって生成されたCOOH基の活性化処理が施される。なお、EDC溶液の濃度、および、静置する時間(活性化処理を施す時間)は、これに限定されず、バイオセンサSとして使用可能なように刺激応答性高分子材料Mが体積変化するために必要な所定量以上の特異的結合物質Xの固定化が可能であればよい。
【0054】
NHS基導入工程では、COOH基活性化工程においてCOOH基の活性化処理が施されたフォトニック結晶内包型ポリアクリルアミドゲルが超純水で洗浄された後、1mol/lのN-hydroxysuccinimide(NHS)(和光純薬工業社製)溶液中に浸漬された状態で、1時間静置される。これによって、NHS基がフォトニック結晶内包型ポリアクリルアミドゲル中に導入される。なお、NHS溶液の濃度、および、静置する時間については、これに限定されず、バイオセンサSとして使用可能なように刺激応答性高分子材料Mが体積変化するために必要な所定量以上の特異的結合物質Xの固定化が可能であればよい。
【0055】
特異的結合物質浸漬工程では、NHS基導入工程においてNHS基が導入されたフォトニック結晶内包型ポリアクリルアミドゲルが超純水で洗浄された後、100U/mlのグルコースオキシダーゼ(オリエンタル酵母社製)溶液中に浸漬されて、4℃の温度で12時間静置される。なお、特異的結合物質Xの濃度、および、温度や静置時間等を含む固定化条件は、これに限定されず、刺激応答性高分子材料の体積変化を生じさせることができればよい。
【0056】
これによって、グルコースオキシダーゼがフォトニック結晶内包型ポリアクリルアミドゲルに固定される。なお、ターゲット物質を含む試料溶液中に混入している夾雑物によるノイズを防ぐため、フォトニック結晶内包型ポリアクリルアミドゲルに特異的結合物質Xが固定された後に、非特異的吸着の除去操作が行われることが好ましい。
【0057】
次に、本発明のバイオセンサSを用いたターゲット物質の検知方法を説明する。
【0058】
<ターゲット物質の検知方法>
本発明のバイオセンサSを用いたターゲット物質の検知方法は第1検知工程と第2検知工程とを有しており、第1検知工程と第2検知工程とを経ることで、ターゲット物質を検知することができる。第1検知工程は、本発明のバイオセンサSと、試料とを接触させる工程である。また、第2検知工程は、バイオセンサSと試料との接触部分の色調を所定方向から目視により観察する工程である。なお、バイオセンサSと接触させる試料は、液体状態であってもよく、固体状態であってもよく、気体状態であってもよい。
【0059】
ここで、特異的結合物質Xと特異的に結合あるいは反応するターゲット物質が試料に含まれている場合には、特異的結合物質Xとターゲット物質との結合あるいは反応によって刺激応答性高分子材料Mの体積変化が生じる。また、刺激応答性高分子材料Mの体積変化に基づいて、フォトニック結晶Cの粒子間距離が変化する。このため、フォトニック結晶Cの色調が変化する。したがって、試料にターゲット物質が含まれている場合には前記接触部分の色調変化を観察することができ、試料中にターゲット物質が含まれていない場合には前記接触部分の色調変化を観察することができない。
【0060】
このようにして、バイオセンサSと試料との接触部分の色調を、所定方向から目視により観察することで、ターゲット物質を検知することができる。
【実施例】
【0061】
以下に、本発明の実施形態に係るバイオセンサSの評価試験およびその結果を示す。
【0062】
バイオセンサSの評価試験は、グルコースオキシダーゼを固定化したフォトニック結晶内包型ポリアクリルアミドゲル上に試料溶液を1000μl滴下して、試料溶液を滴下した直後および試料溶液を滴下してから5分後の滴下部分の色調を目視により観察することで行った。なお、バイオセンサSは観察する角度に応じて色調が異なるため、ここでは、観察する方向を、静置しているバイオセンサSに対して垂直な方向(鉛直方向)とした。
【0063】
<試料溶液の調整>
グルコース(和光純薬工業社製)と20mMのリン酸緩衝液(pH 7.4)とを混合して150mMのグルコース溶液を調整し、これを試料溶液とした。上記試料溶液を用いて、色調の評価試験を行ったところ、緑色から黄色への色調の変化が観察された。また、グルコースオキシダーゼを固定化したフォトニック結晶内包型ポリアクリルアミドゲルを測定用容器に配置し、上記試料溶液を滴下して、Beckman Coulter社製のDU○R800を用いて滴下部分の所定時間毎のピーク波長を測定した結果、ピーク波長は経時的に変化していた(図3参照)。
【0064】
また、比較例として、マンニトールと上記と同様のリン酸緩衝液とを混合して150mMのマンニトール溶液を調整し、これを試料溶液として、上述と同様の方法で目視により評価試験を行った結果、色調の変化は観察されなかった。
【0065】
なお、バイオセンサにおけるターゲット物質と特異的結合物質Xとの反応時間(目視による評価試験が実行される時間)は、これに限定されず、ターゲット物質および固定化した特異的結合物質Xの濃度に応じて適宜決定すればよい。また、測定機器としては、光透過型および光反射型のいずれの測定系であってもよく、分光光度計(Beckman Coulter社製、DU○R800)の他に、マルチチャンネル分光器(Ocean Optics社製、USB4000)あるいは色度計等の測定機器を使用することができる。さらに、あらかじめターゲット物質の濃度に対するフォトニック結晶Cの粒子間距離の変化に伴う色調の変化を評価(数値化)しておくことで、ターゲット物質の濃度を定量することができる。
【0066】
<特徴>
上記実施形態では、フォトニック結晶Cが、ターゲット物質と特異的結合物質Xとの結合あるいは反応に基づく刺激により体積変化する刺激応答性高分子材料Mに内包されている。また、フォトニック結晶Cを構成するナノ粒子の平均粒子径が50〜500nmの範囲内である場合には、可視領域中でフォトニック結晶の色調を観察することができる。さらに、刺激応答性高分子材料Mには、特異的結合物質Xが導入されて固定されている。このため、刺激応答性高分子材料Mに外部刺激を付与(ターゲット物質を添加して特異的結合物質Xと結合あるいは反応させる)することで環境変化が生じ、前記環境変化によって刺激応答性高分子材料Mが膨潤または収縮し、刺激応答性高分子材料Mの膨潤または収縮に基づいてフォトニック結晶Cの粒子間距離が変化する。したがって、フォトニック結晶Cの色調を変化させることができる。言い換えると、刺激応答性高分子材料Mが特異的結合物質Xを含有していることで検知したいターゲット物質(化学物質等)に応答して膨潤度を変化させる刺激応答性高分子材料Mを得ることができ、刺激応答性高分子材料Mの膨潤度が変化することで内包されているフォトニック結晶Cの粒子間距離が変化するため、ターゲット物質の種類や濃度に依存して色調が変化するバイオセンサSを得ることができる。すなわち、本発明のバイオセンサSでは、フォトニック結晶Cのナノ粒子間距離の変化に伴う色調の変化を目視で観察することができる。
【0067】
これによって、測定機器を用いなくても目視でターゲット物質を検知することができるため、簡易にターゲット物質を検知することができている。
【産業上の利用可能性】
【0068】
本発明のバイオセンサは、簡易にターゲット物質を検知することができるバイオセンサとして、様々な用途、特に、研究用途や医療用途への適用が有効である。
【符号の説明】
【0069】
C フォトニック結晶
M アクリルアミド/刺激応答性高分子材料(刺激応答性高分子材料)
S バイオセンサ
X グルコースオキシダーゼ/特異的結合物質(特異的結合物質)
【先行技術文献】
【特許文献】
【0070】
【特許文献1】特開2007−271609号公報
【技術分野】
【0001】
本発明は、バイオセンサならびにバイオセンサの製造方法に関する。
【背景技術】
【0002】
近年、研究機関や医療機関において遺伝子解析や臨床診断等の目的で使用される様々なバイオセンサが開発されている。
【0003】
例えば、特許文献1(特開2007−271609号公報)に開示されているバイオセンサは、特異的結合物質が三次元フォトニック結晶の表面に固定されている。
【0004】
三次元フォトニック結晶には、その周期的な屈折率分布によって、対応する波長の電磁波がブラッグ反射を受けて、電磁波に対するバンドギャップ(フォトニックバンドギャップ)が形成されるという特徴がある。また、フォトニックバンドギャップはフォトニック結晶の表面状態の変化に敏感に反応するため、フォトニック結晶の表面状態の変化に応じてフォトニックバンドギャップに由来する反射スペクトルのピーク波長が変化する。
【0005】
このため、特許文献1に開示されているバイオセンサでは、ターゲット物質と特異的結合物質とが結合する前後において、特定波長の電磁波をフォトニック結晶に照射して得られるフォトニックバンドギャップ由来の反射スペクトルのピーク波長を比較することで、ターゲット物質の有無を検知することができる。このように、このバイオセンサでは、フォトニック結晶の表面に生じる変化を検出することで、ターゲット物質を検知している。
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかしながら、特許文献1に開示されているバイオセンサでは、ターゲット物質の有無を検知するために、分光光度計等の測定機器を用いてフォトニック結晶の反射スペクトルの波長を検出する必要があり、操作が煩雑である。
【0007】
そこで、本発明の課題は、簡易にターゲット物質を検知することができるバイオセンサ、および、バイオセンサの製造方法を提供することにある。
【課題を解決するための手段】
【0008】
第1発明に係るバイオセンサは、フォトニック結晶と、刺激応答性高分子材料とを備えている。フォトニック結晶は、周期的に配置されている粒子から構成されている。刺激応答性高分子材料は、ターゲット物質と特異的に結合あるいは反応する特異的結合物質を含む。また、刺激応答性高分子材料は、ターゲット物質と特異的結合物質とが結合あるいは反応することによって、体積変化する。さらに、フォトニック結晶は、刺激応答性高分子材料に内包されている。
【0009】
第1発明に係るバイオセンサでは、フォトニック結晶が、刺激応答性高分子材料に内包されている。ここで、フォトニック結晶は、その粒子間距離に応じて異なる光学特性が観察されることが知られている。このため、例えば、刺激応答性高分子材料の体積変化に伴ってフォトニック結晶の粒子間距離が変化する場合には、フォトニック結晶の色調を変化させることができる。したがって、例えば、フォトニック結晶の色調が可視領域で変化する場合には、測定機器を用いなくても、目視でターゲット物質を検知することができる。
【0010】
これによって、簡易にターゲット物質を検知することができる。
【0011】
第2発明に係るバイオセンサは、第1発明のバイオセンサであって、フォトニック結晶の粒子の平均粒径は、50〜500nmの範囲内にある。このため、このバイオセンサでは、可視領域中でフォトニック結晶の色調を観察することができる。
【0012】
第3発明に係るバイオセンサは、第1発明または第2発明のバイオセンサであって、刺激応答性高分子材料の体積変化に伴ってフォトニック結晶の粒子間距離が変化する。また、フォトニック結晶の粒子間距離の変化に伴って、フォトニック結晶の色調が変化する。このため、このバイオセンサでは、色調の変化に基づいて、ターゲット物質を検知することができる。
【0013】
第4発明に係るバイオセンサの製造方法は、第1工程と、第2工程とを備える。第1工程は、周期的に配置されている粒子から構成されるフォトニック結晶と、体積変化可能な刺激応答性高分子材料とを混合し、刺激応答性高分子材料がフォトニック結晶を内包したフォトニック結晶内包刺激応答性高分子材料を得る工程である。第2工程は、第1工程で得られたフォトニック結晶内包刺激応答性高分子材料に、ターゲット物質と特異的に結合あるいは反応する特異的結合物質を固定する工程である。
【0014】
第4発明に係るバイオセンサの製造方法では、フォトニック結晶内包刺激応答性高分子材料に特異的結合物質が固定化されたバイオセンサが製造されている。このため、例えば、刺激応答性高分子材料がターゲット物質と特異的結合物質との結合あるいは反応によって体積変化し、刺激応答性高分子材料の体積変化に伴ってフォトニック結晶の粒子間距離が変化する場合には、フォトニック結晶の色調を変化させることができる。したがって、例えば、フォトニック結晶の色調が可視領域で変化する場合には、測定機器を用いなくても、目視でターゲット物質を検知することができる。
【0015】
これによって、この製造方法で製造されるバイオセンサでは、簡易にターゲット物質を検知することができる。
【0016】
第5発明に係るターゲット物質の検知方法は、第1検知工程と、第2検知工程とを備えている。第1検知工程は、第1発明から第3発明のいずれかのバイオセンサと、試料とを接触させる工程である。また、第2検知工程は、バイオセンサと試料との接触部分の色調を、所定方向から目視により観察する工程である。
【0017】
第5発明に係るターゲット物質の検知方法では、バイオセンサと試料との接触部分の色調が目視によって観察されている。このため、例えば、特異的結合物質と結合あるいは反応するターゲット物質が試料に含まれている場合であって、バイオセンサの備える刺激応答性高分子材料がターゲット物質と特異的結合物質との結合あるいは反応によって体積変化し、刺激応答性高分子材料の体積変化に伴ってバイオセンサの備えるフォトニック結晶の粒子間距離が変化する場合には、フォトニック結晶の色調を変化させることができる。したがって、例えば、フォトニック結晶の色調が可視領域で変化する場合には、測定機器を用いなくても、目視でターゲット物質を検知することができる。
【0018】
これによって、このターゲット物質の検知方法を適用可能なバイオセンサでは、簡易にターゲット物質を検知することができる。
【発明の効果】
【0019】
第1発明に係るバイオセンサでは、簡易にターゲット物質を検知することができる。
【0020】
第2発明に係るバイオセンサでは、可視領域中でフォトニック結晶の色調を観察することができる。
【0021】
第3発明に係るバイオセンサでは、色調の変化に基づいて、ターゲット物質を検知することができる。
【0022】
第4発明に係るバイオセンサの製造方法では、簡易にターゲット物質を検知することができる。
【0023】
第5発明に係るターゲット物質の検知方法では、簡易にターゲット物質を検知することができる。
【図面の簡単な説明】
【0024】
【図1】本発明のバイオセンサの概念図。
【図2】フォトニック結晶において(a)粒子間距離が変化する様子を示す概略図、(b)粒子間距離とピーク波長との関係を示す概略図。
【図3】実施例におけるピーク波長の経時的な変化を示す図。
【発明を実施するための形態】
【0025】
本発明のバイオセンサSは、周期的に配置されている粒子(周期構造体)から構成されるフォトニック結晶Cと、外部からの刺激によって体積変化する刺激応答性高分子材料Mとを備えている。また、刺激応答性高分子材料Mは、ターゲット物質と特異的に結合あるいは反応する特異的結合物質Xを含有している。さらに、このバイオセンサSでは、フォトニック結晶Cが、刺激応答性高分子材料Mに内包されている(図1参照)。なお、本発明の主旨を逸脱しない限り、本発明のバイオセンサSは、実施例に限定されるものではない。
【0026】
<フォトニック結晶>
本発明における周期構造体は、一定の規則性、即ち、周期性を有する構造体であって、その周期構造としては、結晶性無機固体と同様の結晶構造である六方最密充填構造、立方最密充填構造、体心立方充填構造、ログパイル構造、ダイヤモンド構造等が挙げられる。なお、これらの周期構造のうちでは、六方最密充填構造が好ましい。
【0027】
また、本発明におけるフォトニック結晶Cは、三次元的な屈折率分布をもつフォトニック結晶である。このような構造のフォトニック結晶Cには、半導体において原子核の周期ポテンシャルによって電子(電子波)がブラッグ反射を受けてバンドギャップが形成されるのと同様に、周期的な屈折率分布によって対応する波長の電磁波がブラッグ反射を受けて、電磁波に対するバンドギャップ(フォトニックバンドギャップ)が形成されるという特徴がある。さらに、フォトニック結晶Cは、材質元素が不変であっても、粒子間距離(周期構造の格子定数)や格子構造に敏感に左右される光学特性を有する。このため、フォトニック結晶Cの粒子間距離が変化することで、吸光度が最大となる波長(以下、ピーク波長という)が長波長側または短波長側にシフトする(図2参照)。したがって、フォトニック結晶Cに特定波長の光を照射すると、観測される反射光の色がフォトニック結晶Cの粒子間距離によって変化する。
【0028】
また、フォトニック結晶Cを構成するナノ粒子としては、例えば、シリカナノ粒子、ポリスチレンナノ粒子、TiO2、ITO、アガロースナノ粒子等の誘電体ナノ粒子が挙げられる。なお、可視領域中でフォトニック結晶Cの色調を観察するためには、ナノ粒子の平均粒子径が50〜500nmの範囲内であること好ましい。また、ナノ粒子の平均粒子径は、200nmであるものがより好ましい。
【0029】
<刺激応答性高分子材料>
本発明における刺激応答性高分子材料Mとしては、外部からの刺激、例えば、熱の付与、電界の付与、イオン強度の変化、磁界の付与、および、力学的刺激等の環境変化に応じて体積変化(膨潤および収縮)する性質を有する材料であればよく、例えば、アクリルアミド、ポリジメチルシロキサン、ポリビニルアルコール、ナフィオン、ポリアクリル酸アミド、N-イソプロピルアクリルアミド、アルギン酸ナトリウムおよびアクリル酸ナトリウム等が挙げられる。なお、刺激応答性高分子材料は、特異的結合物質Xに応じて最適な材料を適宜選択すればよい。
【0030】
熱の付与によって刺激応答する材料としては、例えば、N-イソプロピルアクリルアミド等が挙げられる。
【0031】
電界の付与によって刺激応答する材料としては、例えば、ナフィオン等が挙げられる。
【0032】
イオン強度の変化によって刺激応答する材料としては、例えば、アクリルアミドが挙げられる。
【0033】
磁界の付与によって刺激応答する材料としては、例えば、磁性ナノ粒子包含高分子等が挙げられる。
【0034】
力学的刺激の付与によって応答する材料としては、ポリマー材料であればよく、例えば、アガロース等が挙げられる。
【0035】
上記に挙げた刺激応答性高分子材料Mの中で特に好ましい材料としては、イオン強度の変化によって応答(膨潤および収縮)するアクリルアミド、溶媒の極性の変化によって応答(膨潤および収縮)するポリジメチルシロキサン、湿度の変化によって応答(膨潤および収縮)するポリアクリル酸アミド等が挙げられる。
【0036】
<特異的結合物質>
本発明における特異的結合物質Xとは、試料溶液中に含まれるターゲット物質と特異的に結合あるいは反応する物質(生体認識素子)であればよく、例えば、酵素、タンパク質、糖鎖、DNA、RNAおよびペプチド核酸等が挙げられる。
【0037】
また、試料溶液中に含まれるターゲット物質とは、特異的結合物質Xと特異的に結合あるいは反応する物質である。例えば、特異的結合物質Xが抗体の場合は、ターゲット物質はその抗体が認識する抗原である。また、例えば、特異的結合物質Xが遺伝子の場合には、ターゲット物質は相補的な遺伝子である。
【0038】
また、酵素としては、酸化還元酵素、加水分解酵素、異性化酵素、脱離酵素、合成酵素等を使用することができる。具体的には、グルコースオキシダーゼ、アルコールオキシダーゼ、アルデヒドデヒドロゲナーゼ等が挙げられる。このため、例えば、ターゲット物質がグルコースである場合には、特異的結合物質Xとしてグルコースオキシダーゼを使用することができる。また、例えば、ターゲット物質がアルコール類である場合には、特異的結合物質Xとしてアルコールオキシダーゼを使用することができる。
【0039】
また、タンパク質としては、抗体を使用することができる。具体的には、抗C反応性タンパク質抗体が挙げられる。このため、例えば、ターゲット物質がC反応性タンパク質である場合には、特異的結合物質Xとして抗C反応性タンパク質抗体を使用することができる。
【0040】
また、例えば、ターゲット物質がレクチンである場合には、特異的結合物質Xとして糖鎖を使用することができる。
【0041】
また、DNA、RNAおよびペプチド核酸としては、例えば、ターゲットとなる核酸と相補的にハイブリダイズするものを使用することができる。
【0042】
以上、説明したように、本発明のバイオセンサSは、ターゲット物質と特異的結合物質Xとの結合あるいは反応に基づく刺激により体積変化する刺激応答性高分子材料Mと、フォトニック結晶Cと、を備えており、フォトニック結晶Cが刺激応答性高分子材料Mに内包されている。また、刺激応答性高分子材料Mには、特異的結合物質Xが導入されて固定されている。このため、刺激応答性高分子材料Mに外部刺激を付与する(ターゲット物質を添加して特異的結合物質Xと結合あるいは反応させる)ことでイオン強度等の環境変化が生じ、前記環境変化によって刺激応答性高分子材料Mが体積変化(膨潤または収縮)し、刺激応答性高分子材料Mの体積変化に基づいてフォトニック結晶Cの粒子間距離が変化する。これによって、フォトニック結晶Cの色調を変化させることができる。なお、特異的結合物質Xは、刺激応答性高分子材料Mの内部に存在していてもよく、表面上に存在していてもよい。
【0043】
次に、本発明のバイオセンサSの製造方法について説明する。
【0044】
<バイオセンサの製造方法>
本発明のバイオセンサSの製造方法は第1工程と第2工程とを有しており、本発明のバイオセンサSは第1工程と第2工程とを経ることで製造することができる。第1工程とは、フォトニック結晶Cを内包した刺激応答性高分子材料Mを合成する工程である。また、第2工程とは、第1工程で得られたフォトニック結晶Cを内包した刺激応答性高分子材料Mに、特異的結合物質Xを固定化する工程である。
【0045】
次に、本実施形態におけるバイオセンサSの製造工程を記載する。
【0046】
第1工程では、フォトニック結晶Cを内包したポリアクリルアミドゲル(以下、フォトニック結晶内包型ポリアクリルアミドゲルという)が合成される。また、第2工程では、フォトニック結晶内包型ポリアクリルアミドゲルに特異的結合物質Xが固定化される。
【0047】
また、第1工程には、混合工程と、攪拌工程と、重合工程とが含まれる。さらに、第2工程には、洗浄工程と、加水分解処理工程と、COOH基活性化工程と、NHS基導入工程と、特異的結合物質浸漬工程とが含まれる。
【0048】
具体的には、混合工程では、9mlのシリカナノ粒子溶液(日本触媒社製のKE-W10)中に、0.9gのアクリルアミド(和光純薬工業社製のAcrylamide-HG)、0.1gのメチレンビスアクリルアミド(和光純薬工業社製のN,N'-methylenebis(acrylamide))、1.0gのイオン交換樹脂(BioRad社製のAG○R508-X8resin)、および、0.08gの重合開始剤(和光純薬工業社製社製の2,2'-Azobis[2-methyl-N-(2-hydroxyethyl)propion amide])を混合して混合溶液が作成される。なお、刺激応答性高分子材料を重合させるための重合開始剤は、非イオン性の重合開始剤であることが好ましい。
【0049】
攪拌工程では、混合工程で得られた混合溶液を、アズワン株式会社製のマイクロチューブローテーターを用いて1時間攪拌する。
【0050】
重合工程では、攪拌工程を経た混合溶液からイオン交換樹脂が取り除かれ、重合用容器内で光照射による光重合が行われる。具体的には、混合溶液を、6500rpmで10秒間遠心分離することで、攪拌工程を経た混合溶液からイオン交換樹脂が取り除かれる。なお、混合溶液からのイオン交換樹脂の除去方法は、遠心分離に限定されず、フォトニック結晶Cによる色調が観察可能な状態を維持することができる除去方法であればよい。また、重合用容器の形状やサイズは、フォトニック結晶Cの色調が観察可能なように重合させることができるものであればよい。さらに、光重合の方法としては、当業者に公知の手法が採用され得る。そして、重合に必要とされる時間は、使用される重合開始剤の種類や濃度に応じて最適な時間が採用され得る。これによって、フォトニック結晶内包型ポリアクリルアミドゲルを得ることができる。
【0051】
洗浄工程では、フォトニック結晶内包型ポリアクリルアミドゲルが重合用容器から取り出され、超純水中に浸漬される。これによって、フォトニック結晶内包型ポリアクリルアミドゲルから余剰の試薬が除去される。なお、ここでは、洗浄操作に使用する溶媒として、超純水が使用されているが、これに代えて、イオン交換水、または、蒸留水等が使用されてもよい。
【0052】
加水分解処理工程では、洗浄工程を経たフォトニック結晶内包型ポリアクリルアミドゲルが、1Nの水酸化ナトリウム(NaOH)(和光純薬工業社製のNaOH)溶液中に浸漬された状態で、1時間静置される。これによって、フォトニック結晶内包型ポリアクリルアミドゲルに加水分解処理が施される。なお、NaOH溶液の濃度および静置する時間(加水分解処理を施す時間)については、これに限定されず、バイオセンサSとして使用可能なように刺激応答性高分子材料Mが体積変化するために必要な所定量以上の特異的結合物質Xの固定化が可能であればよい。
【0053】
COOH基活性化工程では、加水分解工程を経て加水分解処理が施されたフォトニック結晶内包型ポリアクリルアミドゲルが超純水で洗浄された後、1mol/lの1-ethyl-3-(3-dimethylaminopropyl)carbodiimidehydrochloride(EDC)(DOJINDO社製)溶液中に浸漬された状態で、1時間静置される。これによって、フォトニック結晶内包型ポリアクリルアミドゲルにおいて、加水分解処理によって生成されたCOOH基の活性化処理が施される。なお、EDC溶液の濃度、および、静置する時間(活性化処理を施す時間)は、これに限定されず、バイオセンサSとして使用可能なように刺激応答性高分子材料Mが体積変化するために必要な所定量以上の特異的結合物質Xの固定化が可能であればよい。
【0054】
NHS基導入工程では、COOH基活性化工程においてCOOH基の活性化処理が施されたフォトニック結晶内包型ポリアクリルアミドゲルが超純水で洗浄された後、1mol/lのN-hydroxysuccinimide(NHS)(和光純薬工業社製)溶液中に浸漬された状態で、1時間静置される。これによって、NHS基がフォトニック結晶内包型ポリアクリルアミドゲル中に導入される。なお、NHS溶液の濃度、および、静置する時間については、これに限定されず、バイオセンサSとして使用可能なように刺激応答性高分子材料Mが体積変化するために必要な所定量以上の特異的結合物質Xの固定化が可能であればよい。
【0055】
特異的結合物質浸漬工程では、NHS基導入工程においてNHS基が導入されたフォトニック結晶内包型ポリアクリルアミドゲルが超純水で洗浄された後、100U/mlのグルコースオキシダーゼ(オリエンタル酵母社製)溶液中に浸漬されて、4℃の温度で12時間静置される。なお、特異的結合物質Xの濃度、および、温度や静置時間等を含む固定化条件は、これに限定されず、刺激応答性高分子材料の体積変化を生じさせることができればよい。
【0056】
これによって、グルコースオキシダーゼがフォトニック結晶内包型ポリアクリルアミドゲルに固定される。なお、ターゲット物質を含む試料溶液中に混入している夾雑物によるノイズを防ぐため、フォトニック結晶内包型ポリアクリルアミドゲルに特異的結合物質Xが固定された後に、非特異的吸着の除去操作が行われることが好ましい。
【0057】
次に、本発明のバイオセンサSを用いたターゲット物質の検知方法を説明する。
【0058】
<ターゲット物質の検知方法>
本発明のバイオセンサSを用いたターゲット物質の検知方法は第1検知工程と第2検知工程とを有しており、第1検知工程と第2検知工程とを経ることで、ターゲット物質を検知することができる。第1検知工程は、本発明のバイオセンサSと、試料とを接触させる工程である。また、第2検知工程は、バイオセンサSと試料との接触部分の色調を所定方向から目視により観察する工程である。なお、バイオセンサSと接触させる試料は、液体状態であってもよく、固体状態であってもよく、気体状態であってもよい。
【0059】
ここで、特異的結合物質Xと特異的に結合あるいは反応するターゲット物質が試料に含まれている場合には、特異的結合物質Xとターゲット物質との結合あるいは反応によって刺激応答性高分子材料Mの体積変化が生じる。また、刺激応答性高分子材料Mの体積変化に基づいて、フォトニック結晶Cの粒子間距離が変化する。このため、フォトニック結晶Cの色調が変化する。したがって、試料にターゲット物質が含まれている場合には前記接触部分の色調変化を観察することができ、試料中にターゲット物質が含まれていない場合には前記接触部分の色調変化を観察することができない。
【0060】
このようにして、バイオセンサSと試料との接触部分の色調を、所定方向から目視により観察することで、ターゲット物質を検知することができる。
【実施例】
【0061】
以下に、本発明の実施形態に係るバイオセンサSの評価試験およびその結果を示す。
【0062】
バイオセンサSの評価試験は、グルコースオキシダーゼを固定化したフォトニック結晶内包型ポリアクリルアミドゲル上に試料溶液を1000μl滴下して、試料溶液を滴下した直後および試料溶液を滴下してから5分後の滴下部分の色調を目視により観察することで行った。なお、バイオセンサSは観察する角度に応じて色調が異なるため、ここでは、観察する方向を、静置しているバイオセンサSに対して垂直な方向(鉛直方向)とした。
【0063】
<試料溶液の調整>
グルコース(和光純薬工業社製)と20mMのリン酸緩衝液(pH 7.4)とを混合して150mMのグルコース溶液を調整し、これを試料溶液とした。上記試料溶液を用いて、色調の評価試験を行ったところ、緑色から黄色への色調の変化が観察された。また、グルコースオキシダーゼを固定化したフォトニック結晶内包型ポリアクリルアミドゲルを測定用容器に配置し、上記試料溶液を滴下して、Beckman Coulter社製のDU○R800を用いて滴下部分の所定時間毎のピーク波長を測定した結果、ピーク波長は経時的に変化していた(図3参照)。
【0064】
また、比較例として、マンニトールと上記と同様のリン酸緩衝液とを混合して150mMのマンニトール溶液を調整し、これを試料溶液として、上述と同様の方法で目視により評価試験を行った結果、色調の変化は観察されなかった。
【0065】
なお、バイオセンサにおけるターゲット物質と特異的結合物質Xとの反応時間(目視による評価試験が実行される時間)は、これに限定されず、ターゲット物質および固定化した特異的結合物質Xの濃度に応じて適宜決定すればよい。また、測定機器としては、光透過型および光反射型のいずれの測定系であってもよく、分光光度計(Beckman Coulter社製、DU○R800)の他に、マルチチャンネル分光器(Ocean Optics社製、USB4000)あるいは色度計等の測定機器を使用することができる。さらに、あらかじめターゲット物質の濃度に対するフォトニック結晶Cの粒子間距離の変化に伴う色調の変化を評価(数値化)しておくことで、ターゲット物質の濃度を定量することができる。
【0066】
<特徴>
上記実施形態では、フォトニック結晶Cが、ターゲット物質と特異的結合物質Xとの結合あるいは反応に基づく刺激により体積変化する刺激応答性高分子材料Mに内包されている。また、フォトニック結晶Cを構成するナノ粒子の平均粒子径が50〜500nmの範囲内である場合には、可視領域中でフォトニック結晶の色調を観察することができる。さらに、刺激応答性高分子材料Mには、特異的結合物質Xが導入されて固定されている。このため、刺激応答性高分子材料Mに外部刺激を付与(ターゲット物質を添加して特異的結合物質Xと結合あるいは反応させる)することで環境変化が生じ、前記環境変化によって刺激応答性高分子材料Mが膨潤または収縮し、刺激応答性高分子材料Mの膨潤または収縮に基づいてフォトニック結晶Cの粒子間距離が変化する。したがって、フォトニック結晶Cの色調を変化させることができる。言い換えると、刺激応答性高分子材料Mが特異的結合物質Xを含有していることで検知したいターゲット物質(化学物質等)に応答して膨潤度を変化させる刺激応答性高分子材料Mを得ることができ、刺激応答性高分子材料Mの膨潤度が変化することで内包されているフォトニック結晶Cの粒子間距離が変化するため、ターゲット物質の種類や濃度に依存して色調が変化するバイオセンサSを得ることができる。すなわち、本発明のバイオセンサSでは、フォトニック結晶Cのナノ粒子間距離の変化に伴う色調の変化を目視で観察することができる。
【0067】
これによって、測定機器を用いなくても目視でターゲット物質を検知することができるため、簡易にターゲット物質を検知することができている。
【産業上の利用可能性】
【0068】
本発明のバイオセンサは、簡易にターゲット物質を検知することができるバイオセンサとして、様々な用途、特に、研究用途や医療用途への適用が有効である。
【符号の説明】
【0069】
C フォトニック結晶
M アクリルアミド/刺激応答性高分子材料(刺激応答性高分子材料)
S バイオセンサ
X グルコースオキシダーゼ/特異的結合物質(特異的結合物質)
【先行技術文献】
【特許文献】
【0070】
【特許文献1】特開2007−271609号公報
【特許請求の範囲】
【請求項1】
周期的に配置されている粒子から構成されるフォトニック結晶(C)と、
ターゲット物質と特異的に結合あるいは反応する特異的結合物質(X)を含み、前記ターゲット物質と前記特異的結合物質とが結合あるいは反応することによって体積変化する刺激応答性高分子材料(M)と、を備え、
前記フォトニック結晶は、前記刺激応答性高分子材料に内包されている、
バイオセンサ(S)。
【請求項2】
前記フォトニック結晶の粒子の平均粒径は、50〜500nmの範囲内にある、
請求項1に記載のバイオセンサ。
【請求項3】
前記刺激応答性高分子材料の体積変化に伴って前記フォトニック結晶の粒子間距離が変化し、前記フォトニック結晶の粒子間距離の変化によって、前記フォトニック結晶の色調が変化する、
請求項1または2に記載のバイオセンサ。
【請求項4】
周期的に配置されている粒子から構成されるフォトニック結晶(C)と体積変化可能な刺激応答性高分子材料(M)とを混合し、前記刺激応答性高分子材料が前記フォトニック結晶を内包したフォトニック結晶内包刺激応答性高分子材料を得る第1工程と、
前記第1工程で得られた前記フォトニック結晶内包刺激応答性高分子材料に、ターゲット物質と特異的に結合あるいは反応する特異的結合物質(X)を固定する第2工程と、
を備えるバイオセンサ(S)の製造方法。
【請求項5】
請求項1から3のいずれかに記載のバイオセンサ(S)と、試料とを接触させる第1検知工程と、
前記バイオセンサと前記試料との接触部分の色調を、所定方向から目視により観察する第2検知工程と、
を備えるターゲット物質の検知方法。
【請求項1】
周期的に配置されている粒子から構成されるフォトニック結晶(C)と、
ターゲット物質と特異的に結合あるいは反応する特異的結合物質(X)を含み、前記ターゲット物質と前記特異的結合物質とが結合あるいは反応することによって体積変化する刺激応答性高分子材料(M)と、を備え、
前記フォトニック結晶は、前記刺激応答性高分子材料に内包されている、
バイオセンサ(S)。
【請求項2】
前記フォトニック結晶の粒子の平均粒径は、50〜500nmの範囲内にある、
請求項1に記載のバイオセンサ。
【請求項3】
前記刺激応答性高分子材料の体積変化に伴って前記フォトニック結晶の粒子間距離が変化し、前記フォトニック結晶の粒子間距離の変化によって、前記フォトニック結晶の色調が変化する、
請求項1または2に記載のバイオセンサ。
【請求項4】
周期的に配置されている粒子から構成されるフォトニック結晶(C)と体積変化可能な刺激応答性高分子材料(M)とを混合し、前記刺激応答性高分子材料が前記フォトニック結晶を内包したフォトニック結晶内包刺激応答性高分子材料を得る第1工程と、
前記第1工程で得られた前記フォトニック結晶内包刺激応答性高分子材料に、ターゲット物質と特異的に結合あるいは反応する特異的結合物質(X)を固定する第2工程と、
を備えるバイオセンサ(S)の製造方法。
【請求項5】
請求項1から3のいずれかに記載のバイオセンサ(S)と、試料とを接触させる第1検知工程と、
前記バイオセンサと前記試料との接触部分の色調を、所定方向から目視により観察する第2検知工程と、
を備えるターゲット物質の検知方法。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2011−80848(P2011−80848A)
【公開日】平成23年4月21日(2011.4.21)
【国際特許分類】
【出願番号】特願2009−232984(P2009−232984)
【出願日】平成21年10月7日(2009.10.7)
【出願人】(000002853)ダイキン工業株式会社 (7,604)
【出願人】(304021417)国立大学法人東京工業大学 (1,821)
【Fターム(参考)】
【公開日】平成23年4月21日(2011.4.21)
【国際特許分類】
【出願日】平成21年10月7日(2009.10.7)
【出願人】(000002853)ダイキン工業株式会社 (7,604)
【出願人】(304021417)国立大学法人東京工業大学 (1,821)
【Fターム(参考)】
[ Back to top ]

