バイオチップ用基板及びその製造方法
【課題】タンパク質や核酸等の生体関連物質から成るプローブを固定化するためのバイオチップ用基板として使用する際に、プローブ固定化率が高く、且つ固定化密度が均一であり、さらに、タンパク質の非特異吸着を防止することにより検出感度が高く且つ再現性が高くなるバイオチップ用基板を提供すること。
【解決手段】基板の表面にアミノ基含有ポリマーを共有結合で固定化することにより、基板表面上にアミノ基を均一に、高密度に、かつ安定に結合することができ、このアミノ基を利用してタンパク質や核酸等の生体関連物質から成るプローブを固定化することにより、プローブ固定化率が高く、且つ固定化密度が均一であり、さらに、タンパク質の非特異吸着を防止することにより検出感度が高く且つ再現性が高くなる。
【解決手段】基板の表面にアミノ基含有ポリマーを共有結合で固定化することにより、基板表面上にアミノ基を均一に、高密度に、かつ安定に結合することができ、このアミノ基を利用してタンパク質や核酸等の生体関連物質から成るプローブを固定化することにより、プローブ固定化率が高く、且つ固定化密度が均一であり、さらに、タンパク質の非特異吸着を防止することにより検出感度が高く且つ再現性が高くなる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、タンパク質、核酸、ペプチド誘導体、糖鎖とその誘導体、天然物、小分子化合物等の生体関連物質をプローブとして固定化するためのバイオチップ用基板、その製造方法及びそれを用いたバイオチップに関する。
【背景技術】
【0002】
平板状の基板表面に核酸、タンパク質を固定化させたバイオチップには、フォトリソグラフィを用いて基板表面でオリゴヌクレオチドを合成するAffymetrix法と、予め準備したプローブ核酸、プローブタンパク質をスポットして基板表面に固定化するStanford法があり、いずれの場合もターゲットとの生化学的な反応後に蛍光を検出し、その強度変化やパターンから分子識別や診断を行うことは良く知られている。上記2法の内、Affymetrix法は基板表面で合成するため、安定的な固定化や長いオリゴヌクレオチドの合成が困難であり、コストも高いという欠点があった。また、Stanford法はプローブ核酸、プローブタンパク質などの微少なスポットを基板表面に載せ、吸着や共有結合で被認識分子を固定化するために、基板表面に非共有結合型のポリリジンあるいは共有結合型のアミノ基、アルデヒド基、シラノ基、エポキシ基を付与しておくが、非共有結合型では安定性が悪く保存期間が短く、時間経過と共にプローブ固定化量が減少するという課題がある。
【0003】
共有結合型では官能基の量が面内で均一でなく、プローブ密度が不均一になるために面内で均一なSN比が得られない。また、官能基の密度も十分でなく特にタンパク質の固定化密度が再現性を得るには十分でない。さらに、生体物質、特にタンパク質の非特異吸着が多く、SN比が減少するため検出感度、再現性において全てを満足する基板は得られなかった。
【0004】
【特許文献1】特開2001-128683号公報
【特許文献2】特表2005-510440号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
本発明の目的は、タンパク質や核酸等の生体関連物質から成るプローブを固定化するためのバイオチップ用基板として使用する際に、プローブ固定化率が高く、且つ固定化密度が均一であり、さらに、タンパク質の非特異吸着を防止することにより検出感度が高く且つ再現性が高くなるバイオチップ用基板を提供することにある。
【課題を解決するための手段】
【0006】
本願発明者らは、鋭意研究の結果、基板の表面にアミノ基含有ポリマーを共有結合で固定化することにより、基板表面上にアミノ基を均一に、高密度に、かつ安定に結合することができ、このアミノ基を利用してタンパク質や核酸等の生体関連物質から成るプローブを固定化することにより、プローブ固定化率が高く、且つ固定化密度が均一であり、さらに、タンパク質の非特異吸着を防止することにより検出感度が高く且つ再現性が高くなることを見出し本発明を完成した。
【0007】
すなわち、本発明は、基板表面に、アミノ基含有ポリマーが共有結合により固定化されたバイオチップ用基板を提供する。また、本発明は、バイオチップ用基板の前記アミノ基に、直接又はリンカーを介して生体関連物質が固定化されたバイオチップを提供する。さらに、本発明は、基板表面に、前記アミノ基含有ポリマーの溶液を塗布した後、減圧雰囲気下又は不活性ガス雰囲気下で該基板表面を光照射することを含む上記本発明のバイオチップ用基板の製造方法を提供する。さらに、本発明は、基板表面を、プラズマ照射又は光照射し、直後に該基板を前記アミノ基含有ポリマーの溶液に浸漬することを含む上記本発明のバイオチップ用基板の製造方法を提供する。
【発明の効果】
【0008】
本発明のバイオチップ用基板では、基板表面上にアミノ基が均一に、高密度に、かつ安定に結合され、このアミノ基を利用してタンパク質や核酸等の生体関連物質から成るプローブを固定化することにより、プローブ固定化率が高く、且つ固定化密度が均一であり、さらに、タンパク質の非特異吸着を防止することにより検出感度が高く且つ再現性が高くなる。
【発明を実施するための最良の形態】
【0009】
本発明のバイオチップ用基板(以下、単に「基板」と略すことがある)では、基板表面にアミノ基含有ポリマーが共有結合により固定化されている点に特徴がある。ここで、「アミノ基」は、一級アミノ基、すなわち、-NH2を意味する。アミノ基含有ポリマーとしては、好ましくは、基板表面に固定化される前の状態で、前記アミノ基含有ポリマーを構成する構成単位の50%以上、さらに好ましくは90%以上、さらに好ましくは99%以上が、それぞれアミノ基を少なくとも1個有するものである。このようなアミノ基含有ポリマーは、1分子中に多数のアミノ基を有するので、基板表面上にアミノ基が均一かつ高密度に結合される。アミノ基含有ポリマーは、アミノ基を有するビニル系モノマーが付加重合することにより形成されたものであることが好ましく、特にポリアリルアミン(PAA)が好ましい。なお、アミノ基含有ポリマーが共有結合している場合には、下記実施例に具体的に記載される通り、純水中で1時間振とう洗浄してもアミノ基含有ポリマーが離脱せず、また、下記実施例に記載する、アミノ基をブロモアセチル化処理した後、メルカプトエタノールで処理することで遊離した臭化物イオンをイオンクロマトグラフィーで定量する方法によりアミノ基の定量が可能である。また、X線光電分光(XPS)により直接確認することも可能である。
【0010】
アミノ基含有ポリマーの平均分子量(重量平均分子量)は、本発明の効果をより良く達成する観点からPAA換算で1000以上が好ましく、さらに好ましくは2000以上である。ここで、「PAA換算」は、1分子中のアミノ基の数を基準として換算することを意味する(以下同じ)。一方、アミノ基含有ポリマーの分子量の上限は、特に限定されず、溶解性及び塗布液の安定性等の取扱い性に問題がない範囲であればよく、6万以下が好ましく、さらには6000以下が好ましい。
【0011】
アミノ基含有ポリマーの基板表面への固定化量は、ポリアリルアミン換算で4μg/cm2以上が好ましい。固定化量がこれより少ない場合も基板表面のアミノ基量が少なくなり、検体やプローブの固定化量が不十分となる。一方、アミノ基含有ポリマーの基板表面への固定化量は、40μg/cm2以下が好ましい。固定化量がこれより多いとポリマー層が剥がれやすくなり、検体やプローブの固定化が損なわれることがある。
【0012】
下記実施例で具体的に示されるように、アミノ基含有ポリマーのみを固定化した基板にプローブを固定化したものであってもタンパク質の非特異吸着はほとんど起きないが、疎水結合等によるタンパク質等の非特異吸着をさらに防止することが望まれる場合には、アミノ基含有ポリマーに加え、親水性ポリマーを基板表面に共有結合で固定化することができる。親水性ポリマーとしては、アミノ基との反応性の低いものを使用する。親水性ポリマーの例として、ポリエーテル類、ポリアクリルアミド、アガロース等を挙げることができる。特にポリエーテル類の中でもポリエチレングリコール(以下、「PEG」と略すことがある)は分子量分布を制御したものが使用可能であり、安定性も高く、生体物質を不活性化しないため好ましい。親水性ポリマーの平均分子量はアミノ基含有ポリマーのリンカーまたはプローブとの反応性を阻害しない分子量が好ましく、1,000〜10,000であり、より好ましくは1,000である。
【0013】
親水性ポリマーを固定化する場合には、アミノ基の均一な分布を確保するために、アミノ基含有ポリマーと親水性ポリマーは均一に混合されていることが好ましい。すなわち、アミノ基含有ポリマーと親水性ポリマーの均一な混合物を後述する方法で基板表面上に固定化することが好ましい。
【0014】
親水性ポリマーは、任意成分であるので、固定化しなくてもよいが、固定化する場合には、その固定化量は、アミノ基含有ポリマーの固定化量以下にすることが、十分な数のアミノ基を基板表面上に結合する上で好ましい。また、アミノ基含有ポリマーと親水性ポリマーの両方を固定化する場合でも、アミノ基含有ポリマーの基板表面への固定化量は、上記の通りポリアリルアミン換算で4μg/cm2以上であることが好ましい。一方、アミノ基含有ポリマーと親水性ポリマーの合計固定化量は、アミノ基含有ポリマー単独の場合と同様、40μg/cm2以下であることが好ましい。親水性ポリマーの固定化量により、基板の親水性を調節することができる。
【0015】
基板表面は、上記したポリマー(単にポリマーという場合には、特に断りがない限り、アミノ基含有ポリマー、又はアミノ基含有ポリマーと親水性ポリマーの混合物を意味する)を共有結合できるものであればよいが、後述するように、光照射やプラズマ照射によりラジカルが生じ易い材質から成ることが好ましい。C−C、C−O、C−Hのように、炭素原子が少なくとも一方である結合は、光照射やプラズマ照射によりラジカルが生じ易いので、少なくとも基板表面は、カーボン又はプラスチックから成ることが好ましい。カーボンとしては、アモルファスカーボンやダイヤモンドライクカーボンが好ましい。また、プラスチックとしては、炭素を含むプラスチックであればいずれのプラスチックでも使用可能であり、好ましいプラスチックの例としては強度や加工性の点からアクリル樹脂、ポリスチレン、ポリエチレンテレフタレート等を挙げることができる。なお、バイオチップとして用いる際の測定の精度を高くするため、基板表面はできるだけ平坦であることが好ましく、必要に応じ表面を研磨することができる。表面粗さRaは、2nm以下が好ましく、1nm程度がさらに好ましい。
【0016】
少なくとも基板表面が上記のような材料で形成されていれば、基板本体の材質は何ら限定されない。基板全体を、アモルファスカーボンやプラスチック等の、基板表面を形成する上記した材料で構成することもできるし、基板本体上にダイヤモンドカーボン等をコーティングすることもできる。基板本体は、例えば、カーボン、金属、ガラス、セラミックス、プラスチック、の何れか1種、またはこれらの複合体等で形成することができ、カーボン及びプラスチック以外の場合には、その表面にカーボン層を設ける処理を行った後、上記ポリマーを固定化することができる。これらのうち、基板全体をカーボンで形成することは、耐薬品性、耐熱性、自家発光が無いことから特に好ましい。また、金属は、アルミニウム、ステンレス鋼、鉄鋼、銅等の単体、またはこれらの合金の表面にポリマーとの共有結合を確保するために、スパッタリング、CVD、PVD等の処理方法により、カーボンまたはダイヤモンドライクカーボンの層を設けたものを基板材料として使用することができる。アルミニウムは耐食性、表面硬度を改善するためにニッケル−リンめっきなどの表面処理を施した後、さらに上記カーボン層を表面に設けた後に基板材料に供することも可能である。ガラス、セラミックスはバイオチップ基板の素材として一般的に用いられる材料である。ポリマーとの共有結合を確保する目的と、タンパク質検体の余分な吸着を防止する目的のために、さらに表面にスパッタリング、CVD、PVD等の処理方法により、カーボンまたはダイヤモンドライクカーボンの層を設けて基板材料とすることができる。
【0017】
基板表面のカーボン又はプラスチックとポリマーと共有結合させるためには、基板表面にポリマーを塗布後、光照射によりカーボン表面とポリマーにラジカルを生成させて共有結合させる第1の方法と、カーボン表面にプラズマ処理または光照射によりラジカルを生成させ、これにポリマーを反応させて結合させる第2の方法とがある。
【0018】
第1の方法は、ポリマー溶液を基板表面に塗布後、光照射によって生成するラジカルにより結合させるもので、照射する光としては、波長150nm〜260nm程度、例えば波長184nmや254nm等の紫外線を使用することができる。この波長の光によりC−C、C−O、C−H結合が切断され、ラジカルが発生する。このとき空気中の酸素分子、水分子も分解されて酸素ラジカル、オゾンが発生し基板材料カーボンとポリマーの酸化分解も同時に起こり共有結合生成阻害の原因となる。これを防止するため本製造方法は減圧下または、不活性ガス雰囲気下で光照射を実施することが好ましい。減圧は大気圧を基準(0MPa)として−0.05MPa以下、より好ましくは−0.08MPa以下の真空度で実施する。不活性ガスはアルゴン、ヘリウム等の光照射を受けてもラジカル化しにくい希ガス元素を使用する。光の照射量は、ポリマーを共有結合するのに必要な量であればよく、エネルギー量として、基板表面1cm2当たり通常、約1〜6ジュール、好ましくは約2〜4ジュール程度である。例えば、基板表面1cm2当たり18.5mWの紫外線を通常1〜5分、好ましくは2〜4分照射する。また、ポリマーの塗布量は、上記したポリマーの固定化量を達成する量である。ポリマー溶液の濃度は、必要なポリマー塗布量を達成でき、均一に塗布できる濃度であればよく、0.5〜3質量%程度が好ましい。
【0019】
第2の方法は、カーボン表面にプラズマ照射または光照射によりラジカルを発生させ、直ちにポリマー溶液を接触させて、基板表面に生じたラジカルとポリマーを反応させる。プラズマは減圧下または大気圧下で実施することができるが、アルゴンガス、炭酸ガス、アンモニアガス、水蒸気等を適宜導入して反応性プラズマとしても実施可能である。プラズマの照射量は、高周波出力1〜100W、反応ガス流量5〜20cm3/min、照射時間10〜120秒、より好ましくは、1〜10W、反応ガス流量5〜15cm3/min、照射時間20〜90秒である。光の照射量は、ポリマーを共有結合するのに必要な量であればよく、エネルギー量として、基板表面1cm2当たり通常、約3〜35ジュール、好ましくは約5〜16ジュール程度である。例えば、基板表面1cm2当たり18.5mWの紫外線を通常3〜30分、好ましくは5〜15分照射する。光照射は、大気圧下で行なうことができる。第2の方法のみによりポリマーを固定化する場合には、生じたラジカルが消失する前に速やかにポリマー溶液を接触させる必要があり、速やかに十分な量のポリマー溶液と接触させる観点から、ロールコート、スプレーコート、ディップコーティング(浸漬)が好ましい。
【0020】
なお、ポリマーの固定化のためには、上記した第1の方法と第2の方法のいずれかを行なえばよいが、これらを組合せて、第2の方法を実施した後、第1の方法を行うことも可能である。すなわち、基板表面にプラズマ照射又は光照射を行なった後、ポリマー溶液を塗布し、さらに、光照射を行なってもよく、好ましい方法である。この場合には、第2の方法により生じたラジカルが減少又は消滅しても、ポリマー溶液塗布後にさらに光照射が行なわれるので問題はない。この場合でも、先に行われる第2の方法により少なくともポリマー溶液の濡れ性が改善されるという効果がもたらされ、ポリマー溶液塗布の前処理と位置づけることができる。
【0021】
ポリマーの基板表面への塗布は、一般的な手法を用いることができ、ポリマーの塗布量を制御できる手法であれば、特にその方法を限定するものではない。例えば、ロールコート、スプレーコート、スピンコート、ディップコート等から選択し実施可能である。
【0022】
上記のようにして得られる本発明の基板は、表面に均一かつ高密度にアミノ基を有する。このアミノ基を利用して、生体関連物質を共有結合により固定化することによりバイオチップを構成することができる。生体関連物質としては、バイオチップにおいてプローブとして用いられているいずれの物質であってもよく、任意のポリペプチド(天然又は合成のタンパク質、オリゴペプチドを包含)、核酸(DNA及びRNA並びに人工核酸を包含)、糖、脂質、これらの複合体(糖タンパク質等)並びに誘導体(修飾タンパク質や核酸等)が挙げられる。
【0023】
生体関連物質は、アミノ基に直接共有結合することもできるし、所望のリンカーを介して結合することもできる。表面にアミノ基を有するバイオチップ用基板自体は広く市販されているので、生体関連物質のアミノ基への共有結合は、周知の常法により容易に行なうことができる。生体関連物質がタンパク質のように、アミノ基と結合するカルボキシル基等を有している場合には直接結合することができ、このような官能基を有していない場合、あるいは所望により、リンカーを介して結合することも可能である。リンカーも周知であり、例えば、一端にカルボキシル基、他端に例えばマレイミド基等を有するものが広く用いられている。
【実施例】
【0024】
以下、本発明を実施例及び比較例に基づきより具体的に説明する。もっとも、本発明は下記実施例に限定されるものではない。各例の説明に先立ち、作製した基板の評価方法について説明する。
【0025】
[基板表面のアミノ基量の均一性評価]
基板表面のアミノ基の均一性は、基板表面全面をアミノ基と反応性を有するように活性化した蛍光分子(TAMRA)溶液でアミノ基に蛍光分子を結合させ、蛍光スキャナーでスキャンすることで評価した。具体的には10mM N,N,N',N'-テトラメチル-(5又は6)-カルボキシローダミン(TAMRA)、10mM HBTU(2−1H[ベンゾトリアゾルー1−イル]―1,1,3,3,テトラメチルウロニウムーヘキサフルオロホスフェート)、20mM DIEA(ジイソプロピルエチルアミン)/DMF(ジメチルホルムアミド)溶液に基板を浸漬し室温で1時間振とうさせてアミノ基にTAMRAを結合させた。続いてメタノール洗浄で過剰なTAMRAを洗い流した後、基板を減圧乾燥した。これを蛍光スキャナー(日立ソフトウェア、CRBIO IIe)でスキャン(Power 40%、Resolution 30μm、PMT 65%、励起光532 nm、発光573 nm)し、得られた画像および輝度の分布ヒストグラムで均一性を評価した。
【0026】
[基板表面のアミノ基量の評価]
基板表面のアミノ基量は基板表面をブロモアセチル化したのち、メルカプトエタノールで処理することで遊離した臭化物イオンをイオンクロマトグラフィー(島津製作所)で定量する方法で測定した。具体的には、10mM無水ブロモ酢酸(ブロモ酢酸とDCC[ジシクロヘキシルカルボジイミド]をジオキサン中で混合することで調製)、10mMピリジンのジオキサン溶液中に基板を浸漬し1時間振とうさせアミノ基をブロモ化アセチルした。続いて過剰なブロモ酢酸をメタノールで洗浄後、減圧乾燥させた。さらに、10mMメルカプトエタノール水溶液に基板を浸漬し1時間振とうさせ臭化物イオンを遊離させた。この臭化物イオンを含有する溶液を10 μL分取しイオンクロマトグラフィーに供して臭化物イオン濃度を定量し、基板の表面積から単位面積当たりのアミノ基量を算出した。
【0027】
[プローブ固定化の評価]
プローブと基板とのリンカーとしてEMCA(6-マレイミドカプロン酸)を導入した。EMCAをDCCにより対称無水物としたのち、ピリジンを加え10mMに調整した溶液にPAA固定化したアモルファスカーボン基板を1時間浸漬した。これにプローブとして、α−ヘリックス構造の合成ペプチド(アミノ酸配列GLQQLARALRRLAQAGC)に蛍光分子TAMRAを標識したペプチドを1%酢酸水溶液に濃度10μMになるように調整した溶液を上記基板表面にスポット(アレイ化)した。さらに、過剰なEMCAをキャッピングするため、10mMメルカプトエタノール液に当該基板を浸漬し、メタノールで洗浄後、スピン乾燥させたのち、蛍光スキャナーで蛍光を測定しプローブの存在を確認した。さらに、50%イソプロパノール水溶液で洗浄後、真空乾燥し再度蛍光スキャナーで蛍光を測定し、プローブの残存(すなわち固定化されている)を確認した。
【0028】
[タンパク質の吸着性の評価]
タンパク質として牛血清アルブミン(BSA)を蛍光分子TAMRAで標識したものを、リン酸バッファーに溶解して濃度0.01%に調整した溶液を基板表面にスポットして1時間静置した。これを、50%イソプロパノール水溶液で洗浄後、スピン乾燥した基板を蛍光スキャナーで測定した。発光画像によりタンパク質吸着状態を評価した。
【0029】
実施例1
1. バイオチップ用基板の作製
(1) 基板及び紫外線処理
表面粗さRaが1nmになるように研磨したアモルファスカーボン板(25.0×75.0mm 公差±0.1mm 板厚1.000mm 公差±0.025mm)を基板材料とし、紫外線照射装置(セン特殊光源株式会社,フォト・サーフェイス・プロセッサーPL16-110)で15分間紫外線照射(18.5 mW/cm2、254nm)を行った。
【0030】
(2) ポリマー溶液の塗布およびポリマーの固定化
PAA(平均分子量3,000)をエタノールで1質量%となるように濃度調整したものをコーティング液とした。PAAコーティング液を適量ピペットで分取し、基板材料表面に滴下した後、PAA塗布量が20μg/cm2になるように塗工厚さを3mil(約0.076mm)に設定したベーカー式アプリケーターにより基板材料表面全体にコーティング液を塗り広げた。溶媒が揮発してからさらに1時間真空乾燥した(真空度-0.098MPa)のち、そのまま真空下で3分間紫外線を照射(18.5mW/cm2,254nm)しPAAを固定化した。さらに超純水で1時間振とう洗浄して未反応のPAAを除去してからスピン乾燥させ本発明のバイオチップ用基板を得た。
【0031】
2. 評価
作製された基板の2枚について上記方法によりアミノ基の均一性評価した(図1a,b)。また、画像データのドット強度のヒストグラムによりアミノ基の分布を評価した(図2a,b)。PAAコーティングカーボン基板は市販のアミノ化ガラス基板(後述の比較例2)に比べて均一にアミノ基が分布している。さらに、アミノ基量を遊離臭化物イオン濃度から算出したところ、PAAコーティングしたカーボン基板は基板表面に5.6±0.4nmol/cm2のアミノ基量を有しており、後述する比較例2のアミノ化ガラス基板よりも高密度であった。また、上記方法により固定化したプローブは洗浄2回繰り返しても固定化されたままであった(図5)。さらに、上記方法によりタンパク質の吸着性を評価したところ、タンパク質の吸着(図7)は比較例2のガラス基板(図8)に比べて少なかった。さらに、
XPSによる解析を行なったところ、表面アミノ基をブロモアセチル化した後XPSでC-Br結合が観察された(図9)。このことによりPAAが共有結合で基板表面に結合していることが確認された。
【0032】
実施例2
アルミニウム合金(5000系合金)の圧延板(75×25mm厚さ1mm)をPVA砥石で厚さ0.98mmまで研削し、表面粗さをRa30nmとした後、全面をアルカリ脱脂、硝酸デスマット、亜鉛ジンケート処理を行い、ニッケル−リン無電解めっきを片面あたり厚さ13μmつけた。さらに、両面をアルミナスラリーにより片面あたり3μm研磨し表面粗さRaを1nmとした。続いて、表面にイオン化蒸着装置を用いて、ヘキサメチルシロキサンガス中SiCを20nm成膜した後、メタンガス中でDLCを200nm成膜して表面にカーボンをコーティングしたものを基板材料に供した。以後は、実施例1と同様にしてポリマーを固定化し、バイオチップ用基板を得た。
【0033】
実施例3
信越化学工業製の合成石英スライドガラス(75×25mm板厚1mm)をフッ化水素酸で洗浄後、真空乾燥した。続いて、表面にカーボンを実施例2と同じ方法で200nmコーティングしたものを基板材料に供した。以後は、実施例1と同様にしてポリマーを固定化し、バイオチップ用基板を得た。
【0034】
実施例4
ポリメタクリル酸メチル板(75×25mm板厚1mm)をメタノールで洗浄し基板材料に供した。以後は、実施例1と同様にしてポリマーを固定化し、バイオチップ用基板を得た。
【0035】
実施例5
ポリマー溶液としてPAA1%エタノール溶液に親水性ポリマーとしてPEGが濃度0.3%になるように調整した溶液をコーティング液とし、モルファスカーボン表面に塗布方法に従って塗布した。以後は、実施例1と同様にしてポリマーを固定化し、バイオチップ用基板を得た。
【0036】
比較例1
アモルファスカーボンを実施例1と同様に紫外線処理(PAA溶液塗布前の紫外線処理)した後、アミノ基の均一性を評価した(図1c)。また、画像データのドット強度のヒストグラムによりアミノ基の分布を評価した(図2c)。アミノ基含有ポリマーを固定化していないため、アミノ基は検出されなかった。
【0037】
比較例2
2種類の市販のアミノ化ガラス基板についてアミノ基の均一性評価した(図3)。また、画像データのドット強度のヒストグラムによりアミノ基の分布を評価した(図4)。実施例に比べてアミノ基の量は不均一であり、画像の輝度のムラおよびヒストグラムの幅が大きくなっている。さらに、アミノ基量を遊離臭化物イオン濃度から算出したところ、臭化物イオンは検出されなかった。これはガラス表面には共有結合での固定化が難しいことを意味する。プローブは図6のように残るが色素の吸着が激しくかつ共有結合できないためにじむ。タンパク質の吸着は、(図8)のように激しい。
【図面の簡単な説明】
【0038】
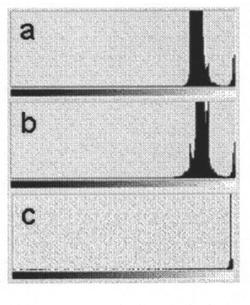
【図1】実施例1で作製した基板の表面を、アミノ基に結合する蛍光標識で修飾した表面像(a,b)及び比較例1で作製した基板の表面を、アミノ基に結合する蛍光標識で修飾した表面像(c)である。
【図2】図1に示す表面像の輝度の分布ヒストグラムである。
【図3】比較例2の基板の表面を、アミノ基に結合する蛍光標識で修飾した表面像(a,b)及び蛍光標識前の表面像(c)を示す。
【図4】図3に示す表面像の輝度の分布ヒストグラムである。
【図5】実施例1で作製した基板にプローブを固定化し、2回洗浄した後の各洗浄後のプローブからの蛍光を、蛍光スキャナーで蛍光を測定した結果を示す図である。
【図6】比較例2の基板にプローブを固定化し、2回洗浄した後の各洗浄後のプローブからの蛍光を、蛍光スキャナーで蛍光を測定した結果を示す図である。
【図7】実施例1で作製した基板へタンパク質を吸着させ、2回洗浄した後の各洗浄後のプローブからの蛍光を、蛍光スキャナーで蛍光を測定した結果を示す図である。
【図8】比較例2で作製した基板へタンパク質を吸着させ、2回洗浄した後の各洗浄後のプローブからの蛍光を、蛍光スキャナーで蛍光を測定した結果を示す図である。
【図9】実施例1で作製した基板のX線光電分光の結果を示す図である。
【技術分野】
【0001】
本発明は、タンパク質、核酸、ペプチド誘導体、糖鎖とその誘導体、天然物、小分子化合物等の生体関連物質をプローブとして固定化するためのバイオチップ用基板、その製造方法及びそれを用いたバイオチップに関する。
【背景技術】
【0002】
平板状の基板表面に核酸、タンパク質を固定化させたバイオチップには、フォトリソグラフィを用いて基板表面でオリゴヌクレオチドを合成するAffymetrix法と、予め準備したプローブ核酸、プローブタンパク質をスポットして基板表面に固定化するStanford法があり、いずれの場合もターゲットとの生化学的な反応後に蛍光を検出し、その強度変化やパターンから分子識別や診断を行うことは良く知られている。上記2法の内、Affymetrix法は基板表面で合成するため、安定的な固定化や長いオリゴヌクレオチドの合成が困難であり、コストも高いという欠点があった。また、Stanford法はプローブ核酸、プローブタンパク質などの微少なスポットを基板表面に載せ、吸着や共有結合で被認識分子を固定化するために、基板表面に非共有結合型のポリリジンあるいは共有結合型のアミノ基、アルデヒド基、シラノ基、エポキシ基を付与しておくが、非共有結合型では安定性が悪く保存期間が短く、時間経過と共にプローブ固定化量が減少するという課題がある。
【0003】
共有結合型では官能基の量が面内で均一でなく、プローブ密度が不均一になるために面内で均一なSN比が得られない。また、官能基の密度も十分でなく特にタンパク質の固定化密度が再現性を得るには十分でない。さらに、生体物質、特にタンパク質の非特異吸着が多く、SN比が減少するため検出感度、再現性において全てを満足する基板は得られなかった。
【0004】
【特許文献1】特開2001-128683号公報
【特許文献2】特表2005-510440号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
本発明の目的は、タンパク質や核酸等の生体関連物質から成るプローブを固定化するためのバイオチップ用基板として使用する際に、プローブ固定化率が高く、且つ固定化密度が均一であり、さらに、タンパク質の非特異吸着を防止することにより検出感度が高く且つ再現性が高くなるバイオチップ用基板を提供することにある。
【課題を解決するための手段】
【0006】
本願発明者らは、鋭意研究の結果、基板の表面にアミノ基含有ポリマーを共有結合で固定化することにより、基板表面上にアミノ基を均一に、高密度に、かつ安定に結合することができ、このアミノ基を利用してタンパク質や核酸等の生体関連物質から成るプローブを固定化することにより、プローブ固定化率が高く、且つ固定化密度が均一であり、さらに、タンパク質の非特異吸着を防止することにより検出感度が高く且つ再現性が高くなることを見出し本発明を完成した。
【0007】
すなわち、本発明は、基板表面に、アミノ基含有ポリマーが共有結合により固定化されたバイオチップ用基板を提供する。また、本発明は、バイオチップ用基板の前記アミノ基に、直接又はリンカーを介して生体関連物質が固定化されたバイオチップを提供する。さらに、本発明は、基板表面に、前記アミノ基含有ポリマーの溶液を塗布した後、減圧雰囲気下又は不活性ガス雰囲気下で該基板表面を光照射することを含む上記本発明のバイオチップ用基板の製造方法を提供する。さらに、本発明は、基板表面を、プラズマ照射又は光照射し、直後に該基板を前記アミノ基含有ポリマーの溶液に浸漬することを含む上記本発明のバイオチップ用基板の製造方法を提供する。
【発明の効果】
【0008】
本発明のバイオチップ用基板では、基板表面上にアミノ基が均一に、高密度に、かつ安定に結合され、このアミノ基を利用してタンパク質や核酸等の生体関連物質から成るプローブを固定化することにより、プローブ固定化率が高く、且つ固定化密度が均一であり、さらに、タンパク質の非特異吸着を防止することにより検出感度が高く且つ再現性が高くなる。
【発明を実施するための最良の形態】
【0009】
本発明のバイオチップ用基板(以下、単に「基板」と略すことがある)では、基板表面にアミノ基含有ポリマーが共有結合により固定化されている点に特徴がある。ここで、「アミノ基」は、一級アミノ基、すなわち、-NH2を意味する。アミノ基含有ポリマーとしては、好ましくは、基板表面に固定化される前の状態で、前記アミノ基含有ポリマーを構成する構成単位の50%以上、さらに好ましくは90%以上、さらに好ましくは99%以上が、それぞれアミノ基を少なくとも1個有するものである。このようなアミノ基含有ポリマーは、1分子中に多数のアミノ基を有するので、基板表面上にアミノ基が均一かつ高密度に結合される。アミノ基含有ポリマーは、アミノ基を有するビニル系モノマーが付加重合することにより形成されたものであることが好ましく、特にポリアリルアミン(PAA)が好ましい。なお、アミノ基含有ポリマーが共有結合している場合には、下記実施例に具体的に記載される通り、純水中で1時間振とう洗浄してもアミノ基含有ポリマーが離脱せず、また、下記実施例に記載する、アミノ基をブロモアセチル化処理した後、メルカプトエタノールで処理することで遊離した臭化物イオンをイオンクロマトグラフィーで定量する方法によりアミノ基の定量が可能である。また、X線光電分光(XPS)により直接確認することも可能である。
【0010】
アミノ基含有ポリマーの平均分子量(重量平均分子量)は、本発明の効果をより良く達成する観点からPAA換算で1000以上が好ましく、さらに好ましくは2000以上である。ここで、「PAA換算」は、1分子中のアミノ基の数を基準として換算することを意味する(以下同じ)。一方、アミノ基含有ポリマーの分子量の上限は、特に限定されず、溶解性及び塗布液の安定性等の取扱い性に問題がない範囲であればよく、6万以下が好ましく、さらには6000以下が好ましい。
【0011】
アミノ基含有ポリマーの基板表面への固定化量は、ポリアリルアミン換算で4μg/cm2以上が好ましい。固定化量がこれより少ない場合も基板表面のアミノ基量が少なくなり、検体やプローブの固定化量が不十分となる。一方、アミノ基含有ポリマーの基板表面への固定化量は、40μg/cm2以下が好ましい。固定化量がこれより多いとポリマー層が剥がれやすくなり、検体やプローブの固定化が損なわれることがある。
【0012】
下記実施例で具体的に示されるように、アミノ基含有ポリマーのみを固定化した基板にプローブを固定化したものであってもタンパク質の非特異吸着はほとんど起きないが、疎水結合等によるタンパク質等の非特異吸着をさらに防止することが望まれる場合には、アミノ基含有ポリマーに加え、親水性ポリマーを基板表面に共有結合で固定化することができる。親水性ポリマーとしては、アミノ基との反応性の低いものを使用する。親水性ポリマーの例として、ポリエーテル類、ポリアクリルアミド、アガロース等を挙げることができる。特にポリエーテル類の中でもポリエチレングリコール(以下、「PEG」と略すことがある)は分子量分布を制御したものが使用可能であり、安定性も高く、生体物質を不活性化しないため好ましい。親水性ポリマーの平均分子量はアミノ基含有ポリマーのリンカーまたはプローブとの反応性を阻害しない分子量が好ましく、1,000〜10,000であり、より好ましくは1,000である。
【0013】
親水性ポリマーを固定化する場合には、アミノ基の均一な分布を確保するために、アミノ基含有ポリマーと親水性ポリマーは均一に混合されていることが好ましい。すなわち、アミノ基含有ポリマーと親水性ポリマーの均一な混合物を後述する方法で基板表面上に固定化することが好ましい。
【0014】
親水性ポリマーは、任意成分であるので、固定化しなくてもよいが、固定化する場合には、その固定化量は、アミノ基含有ポリマーの固定化量以下にすることが、十分な数のアミノ基を基板表面上に結合する上で好ましい。また、アミノ基含有ポリマーと親水性ポリマーの両方を固定化する場合でも、アミノ基含有ポリマーの基板表面への固定化量は、上記の通りポリアリルアミン換算で4μg/cm2以上であることが好ましい。一方、アミノ基含有ポリマーと親水性ポリマーの合計固定化量は、アミノ基含有ポリマー単独の場合と同様、40μg/cm2以下であることが好ましい。親水性ポリマーの固定化量により、基板の親水性を調節することができる。
【0015】
基板表面は、上記したポリマー(単にポリマーという場合には、特に断りがない限り、アミノ基含有ポリマー、又はアミノ基含有ポリマーと親水性ポリマーの混合物を意味する)を共有結合できるものであればよいが、後述するように、光照射やプラズマ照射によりラジカルが生じ易い材質から成ることが好ましい。C−C、C−O、C−Hのように、炭素原子が少なくとも一方である結合は、光照射やプラズマ照射によりラジカルが生じ易いので、少なくとも基板表面は、カーボン又はプラスチックから成ることが好ましい。カーボンとしては、アモルファスカーボンやダイヤモンドライクカーボンが好ましい。また、プラスチックとしては、炭素を含むプラスチックであればいずれのプラスチックでも使用可能であり、好ましいプラスチックの例としては強度や加工性の点からアクリル樹脂、ポリスチレン、ポリエチレンテレフタレート等を挙げることができる。なお、バイオチップとして用いる際の測定の精度を高くするため、基板表面はできるだけ平坦であることが好ましく、必要に応じ表面を研磨することができる。表面粗さRaは、2nm以下が好ましく、1nm程度がさらに好ましい。
【0016】
少なくとも基板表面が上記のような材料で形成されていれば、基板本体の材質は何ら限定されない。基板全体を、アモルファスカーボンやプラスチック等の、基板表面を形成する上記した材料で構成することもできるし、基板本体上にダイヤモンドカーボン等をコーティングすることもできる。基板本体は、例えば、カーボン、金属、ガラス、セラミックス、プラスチック、の何れか1種、またはこれらの複合体等で形成することができ、カーボン及びプラスチック以外の場合には、その表面にカーボン層を設ける処理を行った後、上記ポリマーを固定化することができる。これらのうち、基板全体をカーボンで形成することは、耐薬品性、耐熱性、自家発光が無いことから特に好ましい。また、金属は、アルミニウム、ステンレス鋼、鉄鋼、銅等の単体、またはこれらの合金の表面にポリマーとの共有結合を確保するために、スパッタリング、CVD、PVD等の処理方法により、カーボンまたはダイヤモンドライクカーボンの層を設けたものを基板材料として使用することができる。アルミニウムは耐食性、表面硬度を改善するためにニッケル−リンめっきなどの表面処理を施した後、さらに上記カーボン層を表面に設けた後に基板材料に供することも可能である。ガラス、セラミックスはバイオチップ基板の素材として一般的に用いられる材料である。ポリマーとの共有結合を確保する目的と、タンパク質検体の余分な吸着を防止する目的のために、さらに表面にスパッタリング、CVD、PVD等の処理方法により、カーボンまたはダイヤモンドライクカーボンの層を設けて基板材料とすることができる。
【0017】
基板表面のカーボン又はプラスチックとポリマーと共有結合させるためには、基板表面にポリマーを塗布後、光照射によりカーボン表面とポリマーにラジカルを生成させて共有結合させる第1の方法と、カーボン表面にプラズマ処理または光照射によりラジカルを生成させ、これにポリマーを反応させて結合させる第2の方法とがある。
【0018】
第1の方法は、ポリマー溶液を基板表面に塗布後、光照射によって生成するラジカルにより結合させるもので、照射する光としては、波長150nm〜260nm程度、例えば波長184nmや254nm等の紫外線を使用することができる。この波長の光によりC−C、C−O、C−H結合が切断され、ラジカルが発生する。このとき空気中の酸素分子、水分子も分解されて酸素ラジカル、オゾンが発生し基板材料カーボンとポリマーの酸化分解も同時に起こり共有結合生成阻害の原因となる。これを防止するため本製造方法は減圧下または、不活性ガス雰囲気下で光照射を実施することが好ましい。減圧は大気圧を基準(0MPa)として−0.05MPa以下、より好ましくは−0.08MPa以下の真空度で実施する。不活性ガスはアルゴン、ヘリウム等の光照射を受けてもラジカル化しにくい希ガス元素を使用する。光の照射量は、ポリマーを共有結合するのに必要な量であればよく、エネルギー量として、基板表面1cm2当たり通常、約1〜6ジュール、好ましくは約2〜4ジュール程度である。例えば、基板表面1cm2当たり18.5mWの紫外線を通常1〜5分、好ましくは2〜4分照射する。また、ポリマーの塗布量は、上記したポリマーの固定化量を達成する量である。ポリマー溶液の濃度は、必要なポリマー塗布量を達成でき、均一に塗布できる濃度であればよく、0.5〜3質量%程度が好ましい。
【0019】
第2の方法は、カーボン表面にプラズマ照射または光照射によりラジカルを発生させ、直ちにポリマー溶液を接触させて、基板表面に生じたラジカルとポリマーを反応させる。プラズマは減圧下または大気圧下で実施することができるが、アルゴンガス、炭酸ガス、アンモニアガス、水蒸気等を適宜導入して反応性プラズマとしても実施可能である。プラズマの照射量は、高周波出力1〜100W、反応ガス流量5〜20cm3/min、照射時間10〜120秒、より好ましくは、1〜10W、反応ガス流量5〜15cm3/min、照射時間20〜90秒である。光の照射量は、ポリマーを共有結合するのに必要な量であればよく、エネルギー量として、基板表面1cm2当たり通常、約3〜35ジュール、好ましくは約5〜16ジュール程度である。例えば、基板表面1cm2当たり18.5mWの紫外線を通常3〜30分、好ましくは5〜15分照射する。光照射は、大気圧下で行なうことができる。第2の方法のみによりポリマーを固定化する場合には、生じたラジカルが消失する前に速やかにポリマー溶液を接触させる必要があり、速やかに十分な量のポリマー溶液と接触させる観点から、ロールコート、スプレーコート、ディップコーティング(浸漬)が好ましい。
【0020】
なお、ポリマーの固定化のためには、上記した第1の方法と第2の方法のいずれかを行なえばよいが、これらを組合せて、第2の方法を実施した後、第1の方法を行うことも可能である。すなわち、基板表面にプラズマ照射又は光照射を行なった後、ポリマー溶液を塗布し、さらに、光照射を行なってもよく、好ましい方法である。この場合には、第2の方法により生じたラジカルが減少又は消滅しても、ポリマー溶液塗布後にさらに光照射が行なわれるので問題はない。この場合でも、先に行われる第2の方法により少なくともポリマー溶液の濡れ性が改善されるという効果がもたらされ、ポリマー溶液塗布の前処理と位置づけることができる。
【0021】
ポリマーの基板表面への塗布は、一般的な手法を用いることができ、ポリマーの塗布量を制御できる手法であれば、特にその方法を限定するものではない。例えば、ロールコート、スプレーコート、スピンコート、ディップコート等から選択し実施可能である。
【0022】
上記のようにして得られる本発明の基板は、表面に均一かつ高密度にアミノ基を有する。このアミノ基を利用して、生体関連物質を共有結合により固定化することによりバイオチップを構成することができる。生体関連物質としては、バイオチップにおいてプローブとして用いられているいずれの物質であってもよく、任意のポリペプチド(天然又は合成のタンパク質、オリゴペプチドを包含)、核酸(DNA及びRNA並びに人工核酸を包含)、糖、脂質、これらの複合体(糖タンパク質等)並びに誘導体(修飾タンパク質や核酸等)が挙げられる。
【0023】
生体関連物質は、アミノ基に直接共有結合することもできるし、所望のリンカーを介して結合することもできる。表面にアミノ基を有するバイオチップ用基板自体は広く市販されているので、生体関連物質のアミノ基への共有結合は、周知の常法により容易に行なうことができる。生体関連物質がタンパク質のように、アミノ基と結合するカルボキシル基等を有している場合には直接結合することができ、このような官能基を有していない場合、あるいは所望により、リンカーを介して結合することも可能である。リンカーも周知であり、例えば、一端にカルボキシル基、他端に例えばマレイミド基等を有するものが広く用いられている。
【実施例】
【0024】
以下、本発明を実施例及び比較例に基づきより具体的に説明する。もっとも、本発明は下記実施例に限定されるものではない。各例の説明に先立ち、作製した基板の評価方法について説明する。
【0025】
[基板表面のアミノ基量の均一性評価]
基板表面のアミノ基の均一性は、基板表面全面をアミノ基と反応性を有するように活性化した蛍光分子(TAMRA)溶液でアミノ基に蛍光分子を結合させ、蛍光スキャナーでスキャンすることで評価した。具体的には10mM N,N,N',N'-テトラメチル-(5又は6)-カルボキシローダミン(TAMRA)、10mM HBTU(2−1H[ベンゾトリアゾルー1−イル]―1,1,3,3,テトラメチルウロニウムーヘキサフルオロホスフェート)、20mM DIEA(ジイソプロピルエチルアミン)/DMF(ジメチルホルムアミド)溶液に基板を浸漬し室温で1時間振とうさせてアミノ基にTAMRAを結合させた。続いてメタノール洗浄で過剰なTAMRAを洗い流した後、基板を減圧乾燥した。これを蛍光スキャナー(日立ソフトウェア、CRBIO IIe)でスキャン(Power 40%、Resolution 30μm、PMT 65%、励起光532 nm、発光573 nm)し、得られた画像および輝度の分布ヒストグラムで均一性を評価した。
【0026】
[基板表面のアミノ基量の評価]
基板表面のアミノ基量は基板表面をブロモアセチル化したのち、メルカプトエタノールで処理することで遊離した臭化物イオンをイオンクロマトグラフィー(島津製作所)で定量する方法で測定した。具体的には、10mM無水ブロモ酢酸(ブロモ酢酸とDCC[ジシクロヘキシルカルボジイミド]をジオキサン中で混合することで調製)、10mMピリジンのジオキサン溶液中に基板を浸漬し1時間振とうさせアミノ基をブロモ化アセチルした。続いて過剰なブロモ酢酸をメタノールで洗浄後、減圧乾燥させた。さらに、10mMメルカプトエタノール水溶液に基板を浸漬し1時間振とうさせ臭化物イオンを遊離させた。この臭化物イオンを含有する溶液を10 μL分取しイオンクロマトグラフィーに供して臭化物イオン濃度を定量し、基板の表面積から単位面積当たりのアミノ基量を算出した。
【0027】
[プローブ固定化の評価]
プローブと基板とのリンカーとしてEMCA(6-マレイミドカプロン酸)を導入した。EMCAをDCCにより対称無水物としたのち、ピリジンを加え10mMに調整した溶液にPAA固定化したアモルファスカーボン基板を1時間浸漬した。これにプローブとして、α−ヘリックス構造の合成ペプチド(アミノ酸配列GLQQLARALRRLAQAGC)に蛍光分子TAMRAを標識したペプチドを1%酢酸水溶液に濃度10μMになるように調整した溶液を上記基板表面にスポット(アレイ化)した。さらに、過剰なEMCAをキャッピングするため、10mMメルカプトエタノール液に当該基板を浸漬し、メタノールで洗浄後、スピン乾燥させたのち、蛍光スキャナーで蛍光を測定しプローブの存在を確認した。さらに、50%イソプロパノール水溶液で洗浄後、真空乾燥し再度蛍光スキャナーで蛍光を測定し、プローブの残存(すなわち固定化されている)を確認した。
【0028】
[タンパク質の吸着性の評価]
タンパク質として牛血清アルブミン(BSA)を蛍光分子TAMRAで標識したものを、リン酸バッファーに溶解して濃度0.01%に調整した溶液を基板表面にスポットして1時間静置した。これを、50%イソプロパノール水溶液で洗浄後、スピン乾燥した基板を蛍光スキャナーで測定した。発光画像によりタンパク質吸着状態を評価した。
【0029】
実施例1
1. バイオチップ用基板の作製
(1) 基板及び紫外線処理
表面粗さRaが1nmになるように研磨したアモルファスカーボン板(25.0×75.0mm 公差±0.1mm 板厚1.000mm 公差±0.025mm)を基板材料とし、紫外線照射装置(セン特殊光源株式会社,フォト・サーフェイス・プロセッサーPL16-110)で15分間紫外線照射(18.5 mW/cm2、254nm)を行った。
【0030】
(2) ポリマー溶液の塗布およびポリマーの固定化
PAA(平均分子量3,000)をエタノールで1質量%となるように濃度調整したものをコーティング液とした。PAAコーティング液を適量ピペットで分取し、基板材料表面に滴下した後、PAA塗布量が20μg/cm2になるように塗工厚さを3mil(約0.076mm)に設定したベーカー式アプリケーターにより基板材料表面全体にコーティング液を塗り広げた。溶媒が揮発してからさらに1時間真空乾燥した(真空度-0.098MPa)のち、そのまま真空下で3分間紫外線を照射(18.5mW/cm2,254nm)しPAAを固定化した。さらに超純水で1時間振とう洗浄して未反応のPAAを除去してからスピン乾燥させ本発明のバイオチップ用基板を得た。
【0031】
2. 評価
作製された基板の2枚について上記方法によりアミノ基の均一性評価した(図1a,b)。また、画像データのドット強度のヒストグラムによりアミノ基の分布を評価した(図2a,b)。PAAコーティングカーボン基板は市販のアミノ化ガラス基板(後述の比較例2)に比べて均一にアミノ基が分布している。さらに、アミノ基量を遊離臭化物イオン濃度から算出したところ、PAAコーティングしたカーボン基板は基板表面に5.6±0.4nmol/cm2のアミノ基量を有しており、後述する比較例2のアミノ化ガラス基板よりも高密度であった。また、上記方法により固定化したプローブは洗浄2回繰り返しても固定化されたままであった(図5)。さらに、上記方法によりタンパク質の吸着性を評価したところ、タンパク質の吸着(図7)は比較例2のガラス基板(図8)に比べて少なかった。さらに、
XPSによる解析を行なったところ、表面アミノ基をブロモアセチル化した後XPSでC-Br結合が観察された(図9)。このことによりPAAが共有結合で基板表面に結合していることが確認された。
【0032】
実施例2
アルミニウム合金(5000系合金)の圧延板(75×25mm厚さ1mm)をPVA砥石で厚さ0.98mmまで研削し、表面粗さをRa30nmとした後、全面をアルカリ脱脂、硝酸デスマット、亜鉛ジンケート処理を行い、ニッケル−リン無電解めっきを片面あたり厚さ13μmつけた。さらに、両面をアルミナスラリーにより片面あたり3μm研磨し表面粗さRaを1nmとした。続いて、表面にイオン化蒸着装置を用いて、ヘキサメチルシロキサンガス中SiCを20nm成膜した後、メタンガス中でDLCを200nm成膜して表面にカーボンをコーティングしたものを基板材料に供した。以後は、実施例1と同様にしてポリマーを固定化し、バイオチップ用基板を得た。
【0033】
実施例3
信越化学工業製の合成石英スライドガラス(75×25mm板厚1mm)をフッ化水素酸で洗浄後、真空乾燥した。続いて、表面にカーボンを実施例2と同じ方法で200nmコーティングしたものを基板材料に供した。以後は、実施例1と同様にしてポリマーを固定化し、バイオチップ用基板を得た。
【0034】
実施例4
ポリメタクリル酸メチル板(75×25mm板厚1mm)をメタノールで洗浄し基板材料に供した。以後は、実施例1と同様にしてポリマーを固定化し、バイオチップ用基板を得た。
【0035】
実施例5
ポリマー溶液としてPAA1%エタノール溶液に親水性ポリマーとしてPEGが濃度0.3%になるように調整した溶液をコーティング液とし、モルファスカーボン表面に塗布方法に従って塗布した。以後は、実施例1と同様にしてポリマーを固定化し、バイオチップ用基板を得た。
【0036】
比較例1
アモルファスカーボンを実施例1と同様に紫外線処理(PAA溶液塗布前の紫外線処理)した後、アミノ基の均一性を評価した(図1c)。また、画像データのドット強度のヒストグラムによりアミノ基の分布を評価した(図2c)。アミノ基含有ポリマーを固定化していないため、アミノ基は検出されなかった。
【0037】
比較例2
2種類の市販のアミノ化ガラス基板についてアミノ基の均一性評価した(図3)。また、画像データのドット強度のヒストグラムによりアミノ基の分布を評価した(図4)。実施例に比べてアミノ基の量は不均一であり、画像の輝度のムラおよびヒストグラムの幅が大きくなっている。さらに、アミノ基量を遊離臭化物イオン濃度から算出したところ、臭化物イオンは検出されなかった。これはガラス表面には共有結合での固定化が難しいことを意味する。プローブは図6のように残るが色素の吸着が激しくかつ共有結合できないためにじむ。タンパク質の吸着は、(図8)のように激しい。
【図面の簡単な説明】
【0038】
【図1】実施例1で作製した基板の表面を、アミノ基に結合する蛍光標識で修飾した表面像(a,b)及び比較例1で作製した基板の表面を、アミノ基に結合する蛍光標識で修飾した表面像(c)である。
【図2】図1に示す表面像の輝度の分布ヒストグラムである。
【図3】比較例2の基板の表面を、アミノ基に結合する蛍光標識で修飾した表面像(a,b)及び蛍光標識前の表面像(c)を示す。
【図4】図3に示す表面像の輝度の分布ヒストグラムである。
【図5】実施例1で作製した基板にプローブを固定化し、2回洗浄した後の各洗浄後のプローブからの蛍光を、蛍光スキャナーで蛍光を測定した結果を示す図である。
【図6】比較例2の基板にプローブを固定化し、2回洗浄した後の各洗浄後のプローブからの蛍光を、蛍光スキャナーで蛍光を測定した結果を示す図である。
【図7】実施例1で作製した基板へタンパク質を吸着させ、2回洗浄した後の各洗浄後のプローブからの蛍光を、蛍光スキャナーで蛍光を測定した結果を示す図である。
【図8】比較例2で作製した基板へタンパク質を吸着させ、2回洗浄した後の各洗浄後のプローブからの蛍光を、蛍光スキャナーで蛍光を測定した結果を示す図である。
【図9】実施例1で作製した基板のX線光電分光の結果を示す図である。
【特許請求の範囲】
【請求項1】
基板表面に、アミノ基含有ポリマーが共有結合により固定化されたバイオチップ用基板。
【請求項2】
前記基板表面に固定化される前の状態で、前記アミノ基含有ポリマーを構成する構成単位の50%以上が、それぞれアミノ基を少なくとも1個有する請求項1記載の基板。
【請求項3】
前記アミノ基含有ポリマーを構成する構成単位の90%以上が、それぞれアミノ基を少なくとも1個有する請求項2記載の基板。
【請求項4】
前記アミノ基含有ポリマーがポリアリルアミンである請求項3記載の基板。
【請求項5】
前記アミノ基含有ポリマーの固定化量が、ポリアリルアミン換算で4μg/cm2以上である請求項1〜4のいずれか1項に記載の基板。
【請求項6】
前記アミノ基含有ポリマーの固定化量が、40μg/cm2以下である請求項5記載の基板。
【請求項7】
前記アミノ基含有ポリマーの重量平均分子量が、ポリアリルアミン換算で1000以上である請求項1〜6のいずれか1項に記載の基板。
【請求項8】
前記アミノ基含有ポリマーの重量平均分子量が6万以下である請求項7記載の基板。
【請求項9】
基板表面に、前記アミノ基含有ポリマーと均一に混合された親水性ポリマーが共有結合によりさらに固定化された請求項1ないし8のいずれか1項に記載の基板。
【請求項10】
前記親水性ポリマーが、ポリエチレングリコール、ポリアクリルアミド及びアガロースから成る群より選ばれる少なくとも1種である請求項9記載の基板。
【請求項11】
前記アミノ基含有ポリマーの固定化量が、ポリアリルアミン換算で4μg/cm2以上であり、前記アミノ基含有ポリマー及び前記親水性ポリマーの固定化量の合計が40μg/cm2以下である請求項9又は10記載の基板。
【請求項12】
前記基板表面が、カーボン又はプラスチックから成る請求項1ないし11のいずれか1項に記載の基板。
【請求項13】
前記基板表面が、カーボンから成る請求項12記載の基板。
【請求項14】
請求項1ないし13のいずれか1項に記載のバイオチップ用基板の前記アミノ基に、直接又はリンカーを介して生体関連物質が共有結合されたバイオチップ。
【請求項15】
前記基板表面に、前記アミノ基含有ポリマーを塗布した後、減圧雰囲気下又は不活性ガス雰囲気下で該基板表面を光照射することを含む請求項1記載のバイオチップ用基板の製造方法。
【請求項16】
前記基板表面を、プラズマ照射又は光照射し、次いで該基板を前記アミノ基含有ポリマーと接触させることを含む請求項1記載のバイオチップ用基板の製造方法。
【請求項17】
アミノ基含有ポリマーと接触させた後、さらに減圧雰囲気下又は不活性ガス雰囲気下で該基板表面を光照射することを含む請求項16記載の方法。
【請求項18】
前記基板表面が、カーボン又はプラスチックから成る請求項16又は17記載の方法。
【請求項19】
前記基板表面が、カーボンから成る請求項18記載の方法。
【請求項1】
基板表面に、アミノ基含有ポリマーが共有結合により固定化されたバイオチップ用基板。
【請求項2】
前記基板表面に固定化される前の状態で、前記アミノ基含有ポリマーを構成する構成単位の50%以上が、それぞれアミノ基を少なくとも1個有する請求項1記載の基板。
【請求項3】
前記アミノ基含有ポリマーを構成する構成単位の90%以上が、それぞれアミノ基を少なくとも1個有する請求項2記載の基板。
【請求項4】
前記アミノ基含有ポリマーがポリアリルアミンである請求項3記載の基板。
【請求項5】
前記アミノ基含有ポリマーの固定化量が、ポリアリルアミン換算で4μg/cm2以上である請求項1〜4のいずれか1項に記載の基板。
【請求項6】
前記アミノ基含有ポリマーの固定化量が、40μg/cm2以下である請求項5記載の基板。
【請求項7】
前記アミノ基含有ポリマーの重量平均分子量が、ポリアリルアミン換算で1000以上である請求項1〜6のいずれか1項に記載の基板。
【請求項8】
前記アミノ基含有ポリマーの重量平均分子量が6万以下である請求項7記載の基板。
【請求項9】
基板表面に、前記アミノ基含有ポリマーと均一に混合された親水性ポリマーが共有結合によりさらに固定化された請求項1ないし8のいずれか1項に記載の基板。
【請求項10】
前記親水性ポリマーが、ポリエチレングリコール、ポリアクリルアミド及びアガロースから成る群より選ばれる少なくとも1種である請求項9記載の基板。
【請求項11】
前記アミノ基含有ポリマーの固定化量が、ポリアリルアミン換算で4μg/cm2以上であり、前記アミノ基含有ポリマー及び前記親水性ポリマーの固定化量の合計が40μg/cm2以下である請求項9又は10記載の基板。
【請求項12】
前記基板表面が、カーボン又はプラスチックから成る請求項1ないし11のいずれか1項に記載の基板。
【請求項13】
前記基板表面が、カーボンから成る請求項12記載の基板。
【請求項14】
請求項1ないし13のいずれか1項に記載のバイオチップ用基板の前記アミノ基に、直接又はリンカーを介して生体関連物質が共有結合されたバイオチップ。
【請求項15】
前記基板表面に、前記アミノ基含有ポリマーを塗布した後、減圧雰囲気下又は不活性ガス雰囲気下で該基板表面を光照射することを含む請求項1記載のバイオチップ用基板の製造方法。
【請求項16】
前記基板表面を、プラズマ照射又は光照射し、次いで該基板を前記アミノ基含有ポリマーと接触させることを含む請求項1記載のバイオチップ用基板の製造方法。
【請求項17】
アミノ基含有ポリマーと接触させた後、さらに減圧雰囲気下又は不活性ガス雰囲気下で該基板表面を光照射することを含む請求項16記載の方法。
【請求項18】
前記基板表面が、カーボン又はプラスチックから成る請求項16又は17記載の方法。
【請求項19】
前記基板表面が、カーボンから成る請求項18記載の方法。
【図9】


【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】




【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【公開番号】特開2010−8378(P2010−8378A)
【公開日】平成22年1月14日(2010.1.14)
【国際特許分類】
【出願番号】特願2008−171322(P2008−171322)
【出願日】平成20年6月30日(2008.6.30)
【出願人】(502249851)株式会社ハイペップ研究所 (11)
【出願人】(000004743)日本軽金属株式会社 (627)
【公開日】平成22年1月14日(2010.1.14)
【国際特許分類】
【出願日】平成20年6月30日(2008.6.30)
【出願人】(502249851)株式会社ハイペップ研究所 (11)
【出願人】(000004743)日本軽金属株式会社 (627)
[ Back to top ]

