ヒト免疫不全ウイルス除去或いは不活性化用高分子基材
【課題】 目詰まりを起こすことなく血液等の体液を流すことができ、効率的に体液中のウイルスを除去或いは不活性化することが可能な基材、器具を提供すること。
【解決手段】 (メタ)アクリル酸を、ポリオレフィンを基質とする中空糸にグラフト重合させてなるヒト免疫不全ウイルスを除去或いは不活性化する高分子基材、該高分子基材を備えたヒト免疫不全ウイルス除去或いは不活性化用器具、及び該器具を用いたヒト免疫不全ウイルスの除去或いは不活性化方法を提供することによる。
【解決手段】 (メタ)アクリル酸を、ポリオレフィンを基質とする中空糸にグラフト重合させてなるヒト免疫不全ウイルスを除去或いは不活性化する高分子基材、該高分子基材を備えたヒト免疫不全ウイルス除去或いは不活性化用器具、及び該器具を用いたヒト免疫不全ウイルスの除去或いは不活性化方法を提供することによる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、(メタ)アクリル酸を、ポリオレフィンを基質とする中空糸にグラフト重合させてなるヒト免疫不全ウイルス除去或いは不活性化用高分子基材、及び当該高分子基材を用いたヒト免疫不全ウイルス除去或いは不活性化用器具に関する。
本発明は、「平成18年度、新エネルギー・産業技術総合開発機構委託研究、産業技術力強化法第19条の適用を受ける特許出願」(旧「平成18年度、新エネルギー・産業技術総合開発機構委託研究、産業活力再生特別措置法第30条の適用を受ける特許出願」)である。
【背景技術】
【0002】
ヒト免疫不全ウイルス(HIV)は後天性免疫不全症候群(AIDS)の原因ウイルスであり、分類学上は、エンベロープを有し、プラス鎖の一本鎖RNAをゲノムとするレトロウイルス科レンチウイルス属に属する。形状は直径約100nmの球状で、膜の内側にはRNAとGAGタンパク質から成る核様体がある。HIVはヒトの免疫機能の発現誘導に重要なCD4陽性T細胞に感染し、比較的長い潜伏期間を経て活性化し、該細胞を破壊する。CD4陽性T細胞が破壊されその数が低減すると免疫力が低下し、その結果、日和見感染症や日和見腫瘍が発生しやすくなりAIDSを発症する。現在、日本におけるHIV感染患者数はおよそ1万人、全世界では4000万人程度と言われている。
【0003】
1987年に最初のAIDS薬としてアジドチミジンがアメリカで認可されて以来、現在に至るまで約30種類の薬剤が開発されている。これらはHIV生活環のどの段階に作用するかで大きく6種類(ヌクレオシド系逆転写酵素阻害剤、非ヌクレオシド系逆転写酵素阻害剤、プロテアーゼ阻害剤、融合阻害剤、コレセプター阻害剤、インテグラーゼ阻害剤)に分類することができる。
【0004】
今日標準的に用いられている抗HIV/AIDS治療法は、薬剤を3〜4種類の組み合わせ(ヌクレオシド系逆転写酵素阻害剤2剤+プロテアーゼ阻害剤1〜2剤、またはヌクレオシド系逆転写酵素阻害剤2剤+非ヌクレオシド系逆転写酵素阻害剤1剤)で使用するHAARTと呼ばれる多剤併用療法である。これによりHIV感染者の生命予後は著しく改善された。しかしその一方で、AIDSを根治することは未だ困難であり、また薬剤の使用には様々な薬物有害副反応を引き起こしたり、薬剤耐性株の出現を誘導してしまったりという問題もある。HIVは非常に変異しやすいウイルスであるため、通常よりも容易に薬剤耐性を獲得しやすく、また同じ理由から持続的に効果を発揮しうるワクチンを作製することも難しい。
【0005】
そこで、血液浄化療法の採用が提案されている。前記HAARTを開始する時期の判断基準として、例えば血中HIV濃度が105コピー/mL以上などといったものがあるが、血液浄化療法を採用することで血中からHIVを除去し、その濃度を下げられればHAART開始時期を遅らすことができる、即ち、薬を飲み始めたら生涯服薬し続けなくてはならないという患者負担が軽減されたり、耐性株の出現を遅らせたりすることができると期待されている。また、感染初期段階から薬剤と血液浄化療法とを併用すれば、より有害副反応の少ない薬剤で効果を得ることができるなど薬剤選択の幅が広がる、あるいは抗ウイルス作用に相乗効果が現れるなどといったことが期待される。
【0006】
従来、血液浄化によるHIV除去用吸着材として、例えばCOOH型の弱酸性固体物質などが知られていた(特許文献1)。しかし、これは主に粒状などの形態をとった前記物質をカラムに充填し、そこにHIV感染患者の血液等を通過させてウイルスを除去するといった装置を想定したものであり、乏しい線速とやがて血栓等による目詰まりを起こして閉塞するという問題があった。
【0007】
また、HIVを含めた生体高分子物質の細胞外体液からの捕獲を目的とした、カルボン酸など荷電可能な側鎖を有する吸着性粒子とそれにより構成される流動床についても開示(特許文献2)されているが、流動床を効果的に機能させるためには吸着性粒子を安定して上昇させるのに十分な細胞外体液の流速が必要であり、カラムの大きさによっては実施困難となる場合がある。
【0008】
更に、特許文献3には、特定の配列を有する抗体、核酸が吸着分子として表面に固定化された中空糸が記載されている。該中空糸は、血液中のHIVを減少させるために使用することが可能であるという。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特許第2635365号公報
【特許文献2】特開2009−536号公報
【特許文献3】WO00/12103号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明が解決しようとする課題は、従来技術を鑑み、目詰まりを起こすことなく血液等の体液を流すことができ、効率的に体液中のウイルスを除去或いは不活性化することが可能な基材、器具、及びウイルスを除去或いは不活性化する方法を提供することにある。
【課題を解決するための手段】
【0011】
即ち、本発明は、ウイルスを除去或いは不活性化するための材料に関し、更に詳しくは、(メタ)アクリル酸を、ポリオレフィンを基質とする中空糸にグラフト重合させてなるヒト免疫不全ウイルス除去或いは不活性化用高分子基材、当該高分子基材を用いたヒト免疫不全ウイルス除去或いは不活性化用器具、及びウイルスを除去或いは不活性化する方法に関する。
【発明の効果】
【0012】
目詰まりを起こすことなく血液等の体液を流すことができ、効率的に体液中のウイルスを除去或いは不活性化することが可能な基材、当該基材を用いたヒト免疫不全ウイルス除去或いは不活性化用器具、及びウイルスを除去或いは不活性化する方法を提供することができる。
【図面の簡単な説明】
【0013】
【図1】本発明の高分子基材を備えてなる医療器具の一例を示す概略断面図である。
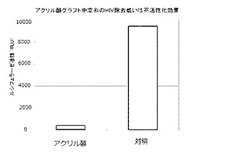
【図2】実施例1におけるHIV除去或いは不活性化の効果を示すグラフである。
【発明を実施するための形態】
【0014】
即ち、本発明は、
1.(メタ)アクリル酸を、ポリオレフィンを基質とする中空糸にグラフト重合反応により固定化させてなる、ヒト免疫不全ウイルス除去或いは不活性化用高分子基材、
2.ポリオレフィンが、ポリ−4−メチルペンテン−1、ポリエチレン、又はポリプロピレンである、1.に記載のヒト免疫不全ウイルス除去或いは不活性化用高分子基材、
3.1.又は2.に記載のヒト免疫不全ウイルス除去或いは不活性化用高分子基材を備えた、ヒト免疫不全ウイルス除去或いは不活性化用器具、
4.3.に記載のヒト免疫不全ウイルス除去或いは不活性化用器具を用いた、ヒト免疫不全ウイルスを除去或いは不活性化する方法、
に関する。
【0015】
・中空糸
本発明に用いる(メタ)アクリル酸を固定化させる中空糸は、電離放射線照射によってラジカルを生成することから主鎖にメチレン基を有するような高分子化合物であれば良い。このような高分子化合物としては血液適合性の高いものであれば種々のものを用いることができるが、例えば、オレフィン系樹脂、スチレン系樹脂、スルホン系樹脂、アクリル系樹脂、ウレタン系樹脂、エステル系樹脂、エーテル系樹脂又はセルロースアセテートが挙げられ、より具体的にはポリエチレンテレフタレート、エチレンビニルアルコール共重合体、ポリメチルメタクリレート、ポリスルホン、ポリエーテルスルホン、ポリアクリロニトリル、ポリエチレン、ポリプロピレン又はポリ−4−メチルペンテン−1等を例示できる。
【0016】
体外循環への適用時には血液が滞留する構造を持つビーズや不織布として用いることも可能であるが、ビーズや不織布は滞留部において血栓の発生が多くなることから、このような用途を目的とする場合は中空糸が特に好ましい。
【0017】
・グラフト重合
本発明では、前記中空糸に電離放射線を照射して発生させたラジカルにより、(メタ)アクリル酸が有するエチレン性不飽和基を高分子支持体にグラフト重合させる。グラフト重合に際して用いる電離放射線源としては、公知慣用のα線、β線、γ線、加速電子線、X線等があげられ、実用的にはγ線、加速電子線が望ましい。
【0018】
グラフト重合法は前記中空糸と(メタ)アクリル酸とを接触させて電離放射線を照射する同時照射グラフト重合法と、中空糸を予め照射した後(メタ)アクリル酸と接触させる前照射グラフト重合法のいずれでも可能であり、目的に合わせて選択できる。
【0019】
本発明に用いる電離放射線を用いたグラフト重合法において、照射線量や加速電圧は中空糸によって異なるため一概には範囲を決めることができず、中空糸の素材、形態、厚みなどを考慮し適宜調整することが必要である。例えば、照射量が多いと帯電による絶縁破壊が発生し、照射量が少ないと重合反応が進行しない。このため、中空糸の材質や形態などを考慮し、帯電による絶縁破壊が発生せず、かつ重合反応が充分に進む照射量を適宜調整すればよい。また、加速電圧は透過性に関係し、中空糸の厚みによって異なる。フィルムなどの薄い形態の場合、加速電圧は一般には小さくて済み、高分子支持体の形態によって選択すればよい。
【0020】
例えば、中空糸がポリ−4−メチルペンテン−1からなる厚さ10(μm)〜100(μm)の中空糸の場合においては、10(kGy)以上、300(kGy)以下であり、さらに望ましくは90(kGy)以下であればよく、加速電圧は適宜選択することができる。
【0021】
前記接触工程と前記電離放射線照射工程の順に特に限定はない。
例えば、前記中空糸に(メタ)アクリル酸を接触させた後、この状態で電離放射線を照射する工程をこの順で行っても良いし、逆に、前記中空糸に電離放射線を先に照射し、その後該中空糸に(メタ)アクリル酸を接触させる工程をこの順で行ってもよい。
【0022】
前記照射グラフト重合において、照射後の基材中のラジカルは温度の上昇、酸素との接触によって速やかに不活化される。従って、照射後は十分に酸素を除いた状態で低温にて貯蔵し、速やかに固定化を行うことが好ましい。また前記の理由から、固定化においては脱酸素下、又は不活性ガス下で実施することが望ましい。
【0023】
グラフト重合反応後の中空糸は、溶媒による洗浄など種々の方法で未反応の(メタ)アクリル酸を除去すればよい。
【0024】
なお、該中空糸へ前記(メタ)アクリル酸を固定化する場合には、実施形態に応じて糸の内面、外面のどちらか、又は両方に固定化することができる。例えば中空糸内部に血液を灌流させる時は中空糸内部に、前記(メタ)アクリル酸を固定化すればよく、逆に、外部灌流時には中空糸外部に前記(メタ)アクリル酸を接触すれば良い。
【0025】
・器具
本発明で得られるヒト免疫不全ウイルス除去或いは不活性化用高分子基材を備えてなるウイルス除去或いは不活性化用器具の形態としては、前記用途に適用可能な形状であれば特に限定されるものではないが、例えば中空糸モジュールや濾過カラム、フィルターなどが挙げられる。中空糸モジュールや濾過カラムにおいて、容器の形状及び材質は特に限定されないが、体液(血液)の体外循環に適用する場合、内部容量が10〜400mLで外径が2〜10cm程度の筒状容器とすることが好ましく、内部容量が20〜200mLで外径が2.5〜4cm程度の筒状容器とすることがより好ましい。図1にその一例を挙げる。
【0026】
ヒト免疫不全ウイルスを含む液(例えば、ウイルスを含む水溶液や血液、血漿、血清等の体液)などの感染力価は該ウイルスを除去或いは不活性化することで低減させることが可能であり、本発明の高分子基材および器具はこうした性能を有するという特長を持つ。
ここで例えば、該ウイルスの除去による感染力価低減の作用機構として、本発明の基材(器具)がウイルス粒子を非特異的に捕捉して液中に存在するウイルス数を大きく減じる、あるいは、数としてはそれ程減らさないものの、感染性の高いウイルス粒子を特異的に認識して捕捉することで感染力価を低減するという可能性が考えられる。また例えば、該ウイルスの不活性化による感染力価低減の作用機構として、本発明の基材(器具)が該ウイルス粒子と接触した際、粒子の一部を捕捉・変性・破壊することで感染力価を低減するという可能性が考えられる。
【0027】
・除去或いは不活性化方法
本発明のヒト免疫不全ウイルス除去或いは不活性化用器具の使用方法としては、ウイルスを含む液と接触させて該液中のウイルスを除去或いは不活性化することができればいずれの方法でもよい。このような方法として、例えば以下の方法を挙げることができる。
(1)本発明の高分子基材を有するモジュールを用意し、該モジュールにウイルスを含む液を通過させる方法
(2)流出口に液は通過できるが本発明の高分子基材は通過できないフィルターを装着し、内部に該基材を充填したカラム様容器を用意し、これにウイルスを含む液を通過させる方法
(3)貯留バッグ等の容器を用意し、これにウイルスを含む液と本発明の高分子基材を加えて混合した後、上澄み液を回収する方法
(1)や(2)の方法は操作が簡便である点で好ましく、体外循環回路に組み込むことにより患者の体液や血液から効率よくインラインでウイルスを除去することが可能である。このうち、さらに好ましい方法として(1)の方法が挙げられる。(2)や(3)の方法では、例えば血液を扱う場合、その凝固を防止するため血液を血球と血漿に分離した上で血漿のみを処理する必要があるが、(1)の方法ではこのような工程を必要とせず、操作が最も簡便でかつ患者への負担が少なくて済む。
【実施例】
【0028】
以下の実施例により本発明を更に詳細に説明する。
【0029】
(実施例1)
<アクリル酸グラフト中空糸の作製>
アクリル酸モノマー1gをイオン交換水100gに溶解して1質量%水溶液とし、撹拌しながら減圧することで水溶液中の溶存酸素を除去した。
【0030】
一方、ポリ−4−メチルペンテン−1製の中空糸束(中空糸表面積:200cm2、DIC(株)製)をガラス製試験管に入れ、ゴム栓にて密閉し、試験管内部を窒素置換した。その後、4.8MeVの加速エネルギーで90kGyの電子線を照射した。
【0031】
次に、電子線を照射した中空糸束入り試験管内を真空にし、23℃条件下、脱酸素したアクリル酸モノマー水溶液を加えてグラフト重合を開始した。4時間静置後、中空糸束を取り出し、未反応のモノマー等がGPC測定で検出限界(1μg/mL。以下同様。)以下になるまで水洗を繰り返した。こうして、得られたアクリル酸ポリマー結合中空糸の性状は、アクリル酸ポリマー結合量約25mg、結合密度(モノマー換算)約1.7μmol/cm2であった。
【0032】
<HIVの調製>
定法に従いプラスミドpNL4−3で293T細胞に形質移入し、48時間培養した。培養上清からウイルス(HIV)を回収し、その量をコアタンパク質p24を指標に測定したところ、2837ng/mLであった。該ウイルス液をPBS100倍希釈して希釈ウイルス液を調製した。
【0033】
<HIV除去或いは不活性化バッチ式試験>
前記アクリル酸グラフト中空糸5cm2を切り出し、PBS中に2時間浸漬してよくなじませた。これを15mL容量試験管に移し、前記希釈ウイルス液1mLを加えて室温で2時間往復振盪した。比較対照として、中空糸を入れていない試験区も用意した。それぞれ上清を回収し、培地(DMEM+10%FBS)で4倍希釈した。
【0034】
96穴プレートに播種したTZM−bl細胞に前記希釈上清それぞれ100μLずつを添加し、37℃で3時間インキュベートした。更に培地を100μLずつ加え、続けて3日間培養した。
【0035】
各試験区の培養上清を除去し、市販のSteady−Go基質を使用して細胞を溶解後、ルシフェラーゼ活性を測定した(図2)。対照試験区に対するアクリル酸グラフト中空糸試験区のルシフェラーゼ活性、即ちHIV除去或いは不活性化率を求めたところ96%であった。
【0036】
(実施例2)バッチ式試験 ポリエチレン製中空糸
基本的に実施例1と同様の操作により、アクリル酸グラフト中空糸の作製及びHIV除去或いは不活性化試験を行った。但し、前記ポリ−4−メチルペンテン−1製の代わりにポリエチレン製中空糸を用いた。このときのアクリル酸ポリマー結合量は約28mg、結合密度(モノマー換算)は約1.9μmol/cm2であった。また、アクリル酸グラフト中空糸試験区のHIV除去或いは不活性化率は95%であった。
【0037】
(実施例3)バッチ式試験 ポリプロピレン製中空糸
基本的に実施例1と同様の操作により、アクリル酸グラフト中空糸の作製及びHIV除去或いは不活性化試験を行った。但し、前記ポリ−4−メチルペンテン−1製の代わりにポリプロピレン製中空糸を用いた。このときのアクリル酸ポリマー結合量は約20mg、結合密度(モノマー換算)は約1.4μmol/cm2であった。また、アクリル酸グラフト中空糸試験区のHIV除去或いは不活性化率は88%であった。
【0038】
(実施例4)循環式試験
<アクリル酸グラフト中空糸の作製>
アクリル酸モノマー5gをメタノール100mLに溶解して5g/dLメタノール溶液とし、窒素ガスを溶液中に導入してメタノール溶液中の溶存酸素を除去した。次にポリ−4−メチルペンテン−1製の中空糸束(中空糸表面積:240cm2、DIC(株)製)をガラス製試験管に入れ、ゴム栓にて密閉し、試験管内部を窒素置換した。その後、4.8MeVの加速エネルギーで90kGyの電子線を照射した。
【0039】
次に、23℃で、電子線を照射した中空糸束入り試験管内を真空にしてから、脱酸素したアクリル酸モノマーのメタノール溶液を加えて電子線グラフト重合を行った。23℃で4時間静置した後、中空糸束を取り出し、メタノールで数回洗浄して未反応のモノマー等を除去し、未反応のモノマー等がGPC測定で検出限界以下になったことを確認した。こうして、アクリル酸ポリマーを固定化した中空糸を得た。中空糸に固定化されたポリアクリル酸の量は重量増加から確認した。アクリル酸ポリマー固定化量29mg、結合密度(モノマー換算)1.6μmol/cm2であった。
【0040】
<中空糸モジュールの作製>
次に、得られたアクリル酸ポリマーを固定化した中空糸を束ねて両端部をホットメルト接着剤(エスダイン8512XS 積水化学(株)製)で目止めした。その後、中空糸モジュール用ハウジングパイプ(内径18mm×外径22mm、全長60mm)に挿入し、両端部に治具を取付けて遠心機にセットし、350rpmで回転させてから、ハウジングパイプに設けたポッティング剤注入口よりポッティング剤を注入した。なお、ポッティング剤にはポリウレタン樹脂(主剤:コロネート4421、硬化剤:ニッポラン4221、日本ポリウレタン工業(株)製)を用いた。
【0041】
ポッティング剤が硬化してから、遠心機の回転を止め、ハウジングパイプを遠心機から取り出し、ハウジングパイプ両端部から突出したアクリル酸固定化中空糸束および硬化したポッティング剤の不要部分を切断して除去し、流体流出入ポートをハウジングパイプの両端に接着してアクリル酸固定化中空糸モジュールを得た。
【0042】
<HIV除去或いは不活性化の確認試験>
該モジュール(中空糸100cm2)に対し、室温で前記希釈ウイルス液6mLを流速0.2mL/minで4時間還流させた。経時的(1、2、4時間)に灌流液の一部をサンプリングし、前記同様TZM−bl細胞を用いた感染実験により除去或いは不活性化率を算出した(表1)。その結果、本発明の中空糸モジュールはHIVに対して高い除去或いは不活性化能を有していることが示された。
【0043】
【表1】

【0044】
(比較例1)循環式試験
<中空糸モジュールの作製>
実施例4と同様の操作により中空糸モジュールを作製した。但し、アクリル酸グラフト中空糸の代わりに未処理の中空糸を用いた。
<HIV除去或いは不活性化の確認試験>
前記調製中空糸モジュールを用い、実施例4と同様の操作により除去或いは不活性化率を求めた(表2)。その結果、HIVに対する除去或いは不活性化能はほとんどないことが示された。
【0045】
【表2】

【産業上の利用可能性】
【0046】
本発明の高分子基材及び当該高分子基材を用いた器具は、ヒト免疫不全ウイルスの除去或いは不活性化する方法への利用が可能である。
【符号の説明】
【0047】
1 流出口
2 流入口
3 アクリル酸
4 中空糸
5 容器
6 隔壁
【技術分野】
【0001】
本発明は、(メタ)アクリル酸を、ポリオレフィンを基質とする中空糸にグラフト重合させてなるヒト免疫不全ウイルス除去或いは不活性化用高分子基材、及び当該高分子基材を用いたヒト免疫不全ウイルス除去或いは不活性化用器具に関する。
本発明は、「平成18年度、新エネルギー・産業技術総合開発機構委託研究、産業技術力強化法第19条の適用を受ける特許出願」(旧「平成18年度、新エネルギー・産業技術総合開発機構委託研究、産業活力再生特別措置法第30条の適用を受ける特許出願」)である。
【背景技術】
【0002】
ヒト免疫不全ウイルス(HIV)は後天性免疫不全症候群(AIDS)の原因ウイルスであり、分類学上は、エンベロープを有し、プラス鎖の一本鎖RNAをゲノムとするレトロウイルス科レンチウイルス属に属する。形状は直径約100nmの球状で、膜の内側にはRNAとGAGタンパク質から成る核様体がある。HIVはヒトの免疫機能の発現誘導に重要なCD4陽性T細胞に感染し、比較的長い潜伏期間を経て活性化し、該細胞を破壊する。CD4陽性T細胞が破壊されその数が低減すると免疫力が低下し、その結果、日和見感染症や日和見腫瘍が発生しやすくなりAIDSを発症する。現在、日本におけるHIV感染患者数はおよそ1万人、全世界では4000万人程度と言われている。
【0003】
1987年に最初のAIDS薬としてアジドチミジンがアメリカで認可されて以来、現在に至るまで約30種類の薬剤が開発されている。これらはHIV生活環のどの段階に作用するかで大きく6種類(ヌクレオシド系逆転写酵素阻害剤、非ヌクレオシド系逆転写酵素阻害剤、プロテアーゼ阻害剤、融合阻害剤、コレセプター阻害剤、インテグラーゼ阻害剤)に分類することができる。
【0004】
今日標準的に用いられている抗HIV/AIDS治療法は、薬剤を3〜4種類の組み合わせ(ヌクレオシド系逆転写酵素阻害剤2剤+プロテアーゼ阻害剤1〜2剤、またはヌクレオシド系逆転写酵素阻害剤2剤+非ヌクレオシド系逆転写酵素阻害剤1剤)で使用するHAARTと呼ばれる多剤併用療法である。これによりHIV感染者の生命予後は著しく改善された。しかしその一方で、AIDSを根治することは未だ困難であり、また薬剤の使用には様々な薬物有害副反応を引き起こしたり、薬剤耐性株の出現を誘導してしまったりという問題もある。HIVは非常に変異しやすいウイルスであるため、通常よりも容易に薬剤耐性を獲得しやすく、また同じ理由から持続的に効果を発揮しうるワクチンを作製することも難しい。
【0005】
そこで、血液浄化療法の採用が提案されている。前記HAARTを開始する時期の判断基準として、例えば血中HIV濃度が105コピー/mL以上などといったものがあるが、血液浄化療法を採用することで血中からHIVを除去し、その濃度を下げられればHAART開始時期を遅らすことができる、即ち、薬を飲み始めたら生涯服薬し続けなくてはならないという患者負担が軽減されたり、耐性株の出現を遅らせたりすることができると期待されている。また、感染初期段階から薬剤と血液浄化療法とを併用すれば、より有害副反応の少ない薬剤で効果を得ることができるなど薬剤選択の幅が広がる、あるいは抗ウイルス作用に相乗効果が現れるなどといったことが期待される。
【0006】
従来、血液浄化によるHIV除去用吸着材として、例えばCOOH型の弱酸性固体物質などが知られていた(特許文献1)。しかし、これは主に粒状などの形態をとった前記物質をカラムに充填し、そこにHIV感染患者の血液等を通過させてウイルスを除去するといった装置を想定したものであり、乏しい線速とやがて血栓等による目詰まりを起こして閉塞するという問題があった。
【0007】
また、HIVを含めた生体高分子物質の細胞外体液からの捕獲を目的とした、カルボン酸など荷電可能な側鎖を有する吸着性粒子とそれにより構成される流動床についても開示(特許文献2)されているが、流動床を効果的に機能させるためには吸着性粒子を安定して上昇させるのに十分な細胞外体液の流速が必要であり、カラムの大きさによっては実施困難となる場合がある。
【0008】
更に、特許文献3には、特定の配列を有する抗体、核酸が吸着分子として表面に固定化された中空糸が記載されている。該中空糸は、血液中のHIVを減少させるために使用することが可能であるという。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特許第2635365号公報
【特許文献2】特開2009−536号公報
【特許文献3】WO00/12103号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明が解決しようとする課題は、従来技術を鑑み、目詰まりを起こすことなく血液等の体液を流すことができ、効率的に体液中のウイルスを除去或いは不活性化することが可能な基材、器具、及びウイルスを除去或いは不活性化する方法を提供することにある。
【課題を解決するための手段】
【0011】
即ち、本発明は、ウイルスを除去或いは不活性化するための材料に関し、更に詳しくは、(メタ)アクリル酸を、ポリオレフィンを基質とする中空糸にグラフト重合させてなるヒト免疫不全ウイルス除去或いは不活性化用高分子基材、当該高分子基材を用いたヒト免疫不全ウイルス除去或いは不活性化用器具、及びウイルスを除去或いは不活性化する方法に関する。
【発明の効果】
【0012】
目詰まりを起こすことなく血液等の体液を流すことができ、効率的に体液中のウイルスを除去或いは不活性化することが可能な基材、当該基材を用いたヒト免疫不全ウイルス除去或いは不活性化用器具、及びウイルスを除去或いは不活性化する方法を提供することができる。
【図面の簡単な説明】
【0013】
【図1】本発明の高分子基材を備えてなる医療器具の一例を示す概略断面図である。
【図2】実施例1におけるHIV除去或いは不活性化の効果を示すグラフである。
【発明を実施するための形態】
【0014】
即ち、本発明は、
1.(メタ)アクリル酸を、ポリオレフィンを基質とする中空糸にグラフト重合反応により固定化させてなる、ヒト免疫不全ウイルス除去或いは不活性化用高分子基材、
2.ポリオレフィンが、ポリ−4−メチルペンテン−1、ポリエチレン、又はポリプロピレンである、1.に記載のヒト免疫不全ウイルス除去或いは不活性化用高分子基材、
3.1.又は2.に記載のヒト免疫不全ウイルス除去或いは不活性化用高分子基材を備えた、ヒト免疫不全ウイルス除去或いは不活性化用器具、
4.3.に記載のヒト免疫不全ウイルス除去或いは不活性化用器具を用いた、ヒト免疫不全ウイルスを除去或いは不活性化する方法、
に関する。
【0015】
・中空糸
本発明に用いる(メタ)アクリル酸を固定化させる中空糸は、電離放射線照射によってラジカルを生成することから主鎖にメチレン基を有するような高分子化合物であれば良い。このような高分子化合物としては血液適合性の高いものであれば種々のものを用いることができるが、例えば、オレフィン系樹脂、スチレン系樹脂、スルホン系樹脂、アクリル系樹脂、ウレタン系樹脂、エステル系樹脂、エーテル系樹脂又はセルロースアセテートが挙げられ、より具体的にはポリエチレンテレフタレート、エチレンビニルアルコール共重合体、ポリメチルメタクリレート、ポリスルホン、ポリエーテルスルホン、ポリアクリロニトリル、ポリエチレン、ポリプロピレン又はポリ−4−メチルペンテン−1等を例示できる。
【0016】
体外循環への適用時には血液が滞留する構造を持つビーズや不織布として用いることも可能であるが、ビーズや不織布は滞留部において血栓の発生が多くなることから、このような用途を目的とする場合は中空糸が特に好ましい。
【0017】
・グラフト重合
本発明では、前記中空糸に電離放射線を照射して発生させたラジカルにより、(メタ)アクリル酸が有するエチレン性不飽和基を高分子支持体にグラフト重合させる。グラフト重合に際して用いる電離放射線源としては、公知慣用のα線、β線、γ線、加速電子線、X線等があげられ、実用的にはγ線、加速電子線が望ましい。
【0018】
グラフト重合法は前記中空糸と(メタ)アクリル酸とを接触させて電離放射線を照射する同時照射グラフト重合法と、中空糸を予め照射した後(メタ)アクリル酸と接触させる前照射グラフト重合法のいずれでも可能であり、目的に合わせて選択できる。
【0019】
本発明に用いる電離放射線を用いたグラフト重合法において、照射線量や加速電圧は中空糸によって異なるため一概には範囲を決めることができず、中空糸の素材、形態、厚みなどを考慮し適宜調整することが必要である。例えば、照射量が多いと帯電による絶縁破壊が発生し、照射量が少ないと重合反応が進行しない。このため、中空糸の材質や形態などを考慮し、帯電による絶縁破壊が発生せず、かつ重合反応が充分に進む照射量を適宜調整すればよい。また、加速電圧は透過性に関係し、中空糸の厚みによって異なる。フィルムなどの薄い形態の場合、加速電圧は一般には小さくて済み、高分子支持体の形態によって選択すればよい。
【0020】
例えば、中空糸がポリ−4−メチルペンテン−1からなる厚さ10(μm)〜100(μm)の中空糸の場合においては、10(kGy)以上、300(kGy)以下であり、さらに望ましくは90(kGy)以下であればよく、加速電圧は適宜選択することができる。
【0021】
前記接触工程と前記電離放射線照射工程の順に特に限定はない。
例えば、前記中空糸に(メタ)アクリル酸を接触させた後、この状態で電離放射線を照射する工程をこの順で行っても良いし、逆に、前記中空糸に電離放射線を先に照射し、その後該中空糸に(メタ)アクリル酸を接触させる工程をこの順で行ってもよい。
【0022】
前記照射グラフト重合において、照射後の基材中のラジカルは温度の上昇、酸素との接触によって速やかに不活化される。従って、照射後は十分に酸素を除いた状態で低温にて貯蔵し、速やかに固定化を行うことが好ましい。また前記の理由から、固定化においては脱酸素下、又は不活性ガス下で実施することが望ましい。
【0023】
グラフト重合反応後の中空糸は、溶媒による洗浄など種々の方法で未反応の(メタ)アクリル酸を除去すればよい。
【0024】
なお、該中空糸へ前記(メタ)アクリル酸を固定化する場合には、実施形態に応じて糸の内面、外面のどちらか、又は両方に固定化することができる。例えば中空糸内部に血液を灌流させる時は中空糸内部に、前記(メタ)アクリル酸を固定化すればよく、逆に、外部灌流時には中空糸外部に前記(メタ)アクリル酸を接触すれば良い。
【0025】
・器具
本発明で得られるヒト免疫不全ウイルス除去或いは不活性化用高分子基材を備えてなるウイルス除去或いは不活性化用器具の形態としては、前記用途に適用可能な形状であれば特に限定されるものではないが、例えば中空糸モジュールや濾過カラム、フィルターなどが挙げられる。中空糸モジュールや濾過カラムにおいて、容器の形状及び材質は特に限定されないが、体液(血液)の体外循環に適用する場合、内部容量が10〜400mLで外径が2〜10cm程度の筒状容器とすることが好ましく、内部容量が20〜200mLで外径が2.5〜4cm程度の筒状容器とすることがより好ましい。図1にその一例を挙げる。
【0026】
ヒト免疫不全ウイルスを含む液(例えば、ウイルスを含む水溶液や血液、血漿、血清等の体液)などの感染力価は該ウイルスを除去或いは不活性化することで低減させることが可能であり、本発明の高分子基材および器具はこうした性能を有するという特長を持つ。
ここで例えば、該ウイルスの除去による感染力価低減の作用機構として、本発明の基材(器具)がウイルス粒子を非特異的に捕捉して液中に存在するウイルス数を大きく減じる、あるいは、数としてはそれ程減らさないものの、感染性の高いウイルス粒子を特異的に認識して捕捉することで感染力価を低減するという可能性が考えられる。また例えば、該ウイルスの不活性化による感染力価低減の作用機構として、本発明の基材(器具)が該ウイルス粒子と接触した際、粒子の一部を捕捉・変性・破壊することで感染力価を低減するという可能性が考えられる。
【0027】
・除去或いは不活性化方法
本発明のヒト免疫不全ウイルス除去或いは不活性化用器具の使用方法としては、ウイルスを含む液と接触させて該液中のウイルスを除去或いは不活性化することができればいずれの方法でもよい。このような方法として、例えば以下の方法を挙げることができる。
(1)本発明の高分子基材を有するモジュールを用意し、該モジュールにウイルスを含む液を通過させる方法
(2)流出口に液は通過できるが本発明の高分子基材は通過できないフィルターを装着し、内部に該基材を充填したカラム様容器を用意し、これにウイルスを含む液を通過させる方法
(3)貯留バッグ等の容器を用意し、これにウイルスを含む液と本発明の高分子基材を加えて混合した後、上澄み液を回収する方法
(1)や(2)の方法は操作が簡便である点で好ましく、体外循環回路に組み込むことにより患者の体液や血液から効率よくインラインでウイルスを除去することが可能である。このうち、さらに好ましい方法として(1)の方法が挙げられる。(2)や(3)の方法では、例えば血液を扱う場合、その凝固を防止するため血液を血球と血漿に分離した上で血漿のみを処理する必要があるが、(1)の方法ではこのような工程を必要とせず、操作が最も簡便でかつ患者への負担が少なくて済む。
【実施例】
【0028】
以下の実施例により本発明を更に詳細に説明する。
【0029】
(実施例1)
<アクリル酸グラフト中空糸の作製>
アクリル酸モノマー1gをイオン交換水100gに溶解して1質量%水溶液とし、撹拌しながら減圧することで水溶液中の溶存酸素を除去した。
【0030】
一方、ポリ−4−メチルペンテン−1製の中空糸束(中空糸表面積:200cm2、DIC(株)製)をガラス製試験管に入れ、ゴム栓にて密閉し、試験管内部を窒素置換した。その後、4.8MeVの加速エネルギーで90kGyの電子線を照射した。
【0031】
次に、電子線を照射した中空糸束入り試験管内を真空にし、23℃条件下、脱酸素したアクリル酸モノマー水溶液を加えてグラフト重合を開始した。4時間静置後、中空糸束を取り出し、未反応のモノマー等がGPC測定で検出限界(1μg/mL。以下同様。)以下になるまで水洗を繰り返した。こうして、得られたアクリル酸ポリマー結合中空糸の性状は、アクリル酸ポリマー結合量約25mg、結合密度(モノマー換算)約1.7μmol/cm2であった。
【0032】
<HIVの調製>
定法に従いプラスミドpNL4−3で293T細胞に形質移入し、48時間培養した。培養上清からウイルス(HIV)を回収し、その量をコアタンパク質p24を指標に測定したところ、2837ng/mLであった。該ウイルス液をPBS100倍希釈して希釈ウイルス液を調製した。
【0033】
<HIV除去或いは不活性化バッチ式試験>
前記アクリル酸グラフト中空糸5cm2を切り出し、PBS中に2時間浸漬してよくなじませた。これを15mL容量試験管に移し、前記希釈ウイルス液1mLを加えて室温で2時間往復振盪した。比較対照として、中空糸を入れていない試験区も用意した。それぞれ上清を回収し、培地(DMEM+10%FBS)で4倍希釈した。
【0034】
96穴プレートに播種したTZM−bl細胞に前記希釈上清それぞれ100μLずつを添加し、37℃で3時間インキュベートした。更に培地を100μLずつ加え、続けて3日間培養した。
【0035】
各試験区の培養上清を除去し、市販のSteady−Go基質を使用して細胞を溶解後、ルシフェラーゼ活性を測定した(図2)。対照試験区に対するアクリル酸グラフト中空糸試験区のルシフェラーゼ活性、即ちHIV除去或いは不活性化率を求めたところ96%であった。
【0036】
(実施例2)バッチ式試験 ポリエチレン製中空糸
基本的に実施例1と同様の操作により、アクリル酸グラフト中空糸の作製及びHIV除去或いは不活性化試験を行った。但し、前記ポリ−4−メチルペンテン−1製の代わりにポリエチレン製中空糸を用いた。このときのアクリル酸ポリマー結合量は約28mg、結合密度(モノマー換算)は約1.9μmol/cm2であった。また、アクリル酸グラフト中空糸試験区のHIV除去或いは不活性化率は95%であった。
【0037】
(実施例3)バッチ式試験 ポリプロピレン製中空糸
基本的に実施例1と同様の操作により、アクリル酸グラフト中空糸の作製及びHIV除去或いは不活性化試験を行った。但し、前記ポリ−4−メチルペンテン−1製の代わりにポリプロピレン製中空糸を用いた。このときのアクリル酸ポリマー結合量は約20mg、結合密度(モノマー換算)は約1.4μmol/cm2であった。また、アクリル酸グラフト中空糸試験区のHIV除去或いは不活性化率は88%であった。
【0038】
(実施例4)循環式試験
<アクリル酸グラフト中空糸の作製>
アクリル酸モノマー5gをメタノール100mLに溶解して5g/dLメタノール溶液とし、窒素ガスを溶液中に導入してメタノール溶液中の溶存酸素を除去した。次にポリ−4−メチルペンテン−1製の中空糸束(中空糸表面積:240cm2、DIC(株)製)をガラス製試験管に入れ、ゴム栓にて密閉し、試験管内部を窒素置換した。その後、4.8MeVの加速エネルギーで90kGyの電子線を照射した。
【0039】
次に、23℃で、電子線を照射した中空糸束入り試験管内を真空にしてから、脱酸素したアクリル酸モノマーのメタノール溶液を加えて電子線グラフト重合を行った。23℃で4時間静置した後、中空糸束を取り出し、メタノールで数回洗浄して未反応のモノマー等を除去し、未反応のモノマー等がGPC測定で検出限界以下になったことを確認した。こうして、アクリル酸ポリマーを固定化した中空糸を得た。中空糸に固定化されたポリアクリル酸の量は重量増加から確認した。アクリル酸ポリマー固定化量29mg、結合密度(モノマー換算)1.6μmol/cm2であった。
【0040】
<中空糸モジュールの作製>
次に、得られたアクリル酸ポリマーを固定化した中空糸を束ねて両端部をホットメルト接着剤(エスダイン8512XS 積水化学(株)製)で目止めした。その後、中空糸モジュール用ハウジングパイプ(内径18mm×外径22mm、全長60mm)に挿入し、両端部に治具を取付けて遠心機にセットし、350rpmで回転させてから、ハウジングパイプに設けたポッティング剤注入口よりポッティング剤を注入した。なお、ポッティング剤にはポリウレタン樹脂(主剤:コロネート4421、硬化剤:ニッポラン4221、日本ポリウレタン工業(株)製)を用いた。
【0041】
ポッティング剤が硬化してから、遠心機の回転を止め、ハウジングパイプを遠心機から取り出し、ハウジングパイプ両端部から突出したアクリル酸固定化中空糸束および硬化したポッティング剤の不要部分を切断して除去し、流体流出入ポートをハウジングパイプの両端に接着してアクリル酸固定化中空糸モジュールを得た。
【0042】
<HIV除去或いは不活性化の確認試験>
該モジュール(中空糸100cm2)に対し、室温で前記希釈ウイルス液6mLを流速0.2mL/minで4時間還流させた。経時的(1、2、4時間)に灌流液の一部をサンプリングし、前記同様TZM−bl細胞を用いた感染実験により除去或いは不活性化率を算出した(表1)。その結果、本発明の中空糸モジュールはHIVに対して高い除去或いは不活性化能を有していることが示された。
【0043】
【表1】

【0044】
(比較例1)循環式試験
<中空糸モジュールの作製>
実施例4と同様の操作により中空糸モジュールを作製した。但し、アクリル酸グラフト中空糸の代わりに未処理の中空糸を用いた。
<HIV除去或いは不活性化の確認試験>
前記調製中空糸モジュールを用い、実施例4と同様の操作により除去或いは不活性化率を求めた(表2)。その結果、HIVに対する除去或いは不活性化能はほとんどないことが示された。
【0045】
【表2】

【産業上の利用可能性】
【0046】
本発明の高分子基材及び当該高分子基材を用いた器具は、ヒト免疫不全ウイルスの除去或いは不活性化する方法への利用が可能である。
【符号の説明】
【0047】
1 流出口
2 流入口
3 アクリル酸
4 中空糸
5 容器
6 隔壁
【特許請求の範囲】
【請求項1】
(メタ)アクリル酸を、ポリオレフィンを基質とする中空糸にグラフト重合反応により固定化させてなる、ヒト免疫不全ウイルス除去或いは不活性化用高分子基材。
【請求項2】
ポリオレフィンが、ポリ−4−メチルペンテン−1、ポリエチレン、又はポリプロピレンである、請求項1に記載のヒト免疫不全ウイルス除去或いは不活性化用高分子基材。
【請求項3】
請求項1又は2に記載のヒト免疫不全ウイルス除去或いは不活性化用高分子基材を備えた、ヒト免疫不全ウイルス除去或いは不活性化用器具。
【請求項4】
請求項3に記載のヒト免疫不全ウイルス除去或いは不活性化用器具を用いた、ヒト免疫不全ウイルスを除去或いは不活性化する方法。
【請求項1】
(メタ)アクリル酸を、ポリオレフィンを基質とする中空糸にグラフト重合反応により固定化させてなる、ヒト免疫不全ウイルス除去或いは不活性化用高分子基材。
【請求項2】
ポリオレフィンが、ポリ−4−メチルペンテン−1、ポリエチレン、又はポリプロピレンである、請求項1に記載のヒト免疫不全ウイルス除去或いは不活性化用高分子基材。
【請求項3】
請求項1又は2に記載のヒト免疫不全ウイルス除去或いは不活性化用高分子基材を備えた、ヒト免疫不全ウイルス除去或いは不活性化用器具。
【請求項4】
請求項3に記載のヒト免疫不全ウイルス除去或いは不活性化用器具を用いた、ヒト免疫不全ウイルスを除去或いは不活性化する方法。
【図1】


【図2】




【図2】


【公開番号】特開2012−125556(P2012−125556A)
【公開日】平成24年7月5日(2012.7.5)
【国際特許分類】
【出願番号】特願2011−254977(P2011−254977)
【出願日】平成23年11月22日(2011.11.22)
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成18年度、新エネルギー・産業技術総合開発機構委託研究、産業技術力強化法第19条の適用を受ける特許出願
【出願人】(000002886)DIC株式会社 (2,597)
【出願人】(591222245)国立感染症研究所長 (48)
【Fターム(参考)】
【公開日】平成24年7月5日(2012.7.5)
【国際特許分類】
【出願日】平成23年11月22日(2011.11.22)
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成18年度、新エネルギー・産業技術総合開発機構委託研究、産業技術力強化法第19条の適用を受ける特許出願
【出願人】(000002886)DIC株式会社 (2,597)
【出願人】(591222245)国立感染症研究所長 (48)
【Fターム(参考)】
[ Back to top ]

