ビームスキャニングによる上皮性管腔器官の光学的撮像方法およびシステム
【課題】光学的収差を補正するように構成された装置を提供すること。
【解決手段】管腔又は中空サンプル内部の一以上の部分のデータを取得する方法、装置、及びシステムを提供する。本方法、システム又は装置は、患者の口又は鼻を介して挿入可能である。例えば、第1の光学構成部は、該部分に電磁放射を放射し、受け取ることができる。第1の光学構成部を少なくとも部分的に囲繞する第2の構成部を設けてもよい。さらに、第3の構成部を、第1の光学構成部が管腔又は中空サンプル内部の所定の部位に位置するように作動可能に構成できる。第1の光学構成部は、第2の構成部又は第3の構成部によって生じる収差(例えば、非点収差)を補正するように構成してもよい。第2の構成部は、ガイド構成部を挿入することができる、一以上の部分を含むことができる。一以上の部分の内部の圧力を測定するように構成した他の装置も提供できる。
【解決手段】管腔又は中空サンプル内部の一以上の部分のデータを取得する方法、装置、及びシステムを提供する。本方法、システム又は装置は、患者の口又は鼻を介して挿入可能である。例えば、第1の光学構成部は、該部分に電磁放射を放射し、受け取ることができる。第1の光学構成部を少なくとも部分的に囲繞する第2の構成部を設けてもよい。さらに、第3の構成部を、第1の光学構成部が管腔又は中空サンプル内部の所定の部位に位置するように作動可能に構成できる。第1の光学構成部は、第2の構成部又は第3の構成部によって生じる収差(例えば、非点収差)を補正するように構成してもよい。第2の構成部は、ガイド構成部を挿入することができる、一以上の部分を含むことができる。一以上の部分の内部の圧力を測定するように構成した他の装置も提供できる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は光学的撮像のための方法およびシステムに関するものであり、具体的には、ビームスキャニングを用いた上皮性管腔器官(epithelial luminal organ)の光学的撮像に関わる。
【背景技術】
【0002】
(関連出願の相互参照)
【0003】
本出願は、2006年1月19日出願の米国特許出願第60/761,004号に基づき優先度の利益を主張するものであり、この全ての開示内容を本明細書の一部として援用する。
(連邦政府により支援された研究に関する声明)
【0004】
本発明は、米国政府助成契約第RO1CA103769号として国立衛生研究所によりの支援を受けた。それ故、米国連邦政府は本発明に一定の権利を有するものである。
【0005】
疾病のスクリーニングは、1以上の可能性のある疾病を有しているか不明な個人が、そのような疾病を有しているか否かを判定するために受けるテストの一過程である。スクリーニングはしばしば大きな集団に対して行われるものであり、それ故廉価であり侵襲は最小となると見込まれる。特定の疾病を有する患者のサーベイランスとして、その疾病の過程において、疾病の重篤性を決定するテスト、例えば前癌状態が知られている患者では異形性の程度を決定するためのテストを行う。上皮性管腔器管、例えば消化管、尿管、胆嚢腺、婦人科関連器官管腔、中咽頭・肺系統などの疾病(例えば異形成症、癌など)に対する効果的なスクリーニング及びサーベイランスには、広範囲にわたる粘膜の総合的な評価を用いる。これまでに、時間領域光コヒーレンストモグラフィー(OCT)、スペクトル領域光コヒーレンストモグラフィー(SD−OCT)、光周波数領域撮像(OFDI)、ラマン分光法、反射分光法、共焦点顕微鏡検査法、光散乱分光法などの技術を含む、ビームスキャニング光学技術は、異形成症、初期癌などの粘膜性疾病の診断に利用可能な決定的な情報を提供することが実証されている。しかしながら、これらの技術は一般的に一度に一箇所の画像データのみを取得することができる、点スキャン方法であると考えられる。大きな管腔性器官を全体的にスクリーニングする場合、目的とする器官の領域、例えば、広い領域にわたって、集光ビームで高速にスキャンし、光学的な測定値を得る。それ故、カテーテル、プローブおよびこのビームスキャニング機能を実行できる機器は、これらの光学技術およびその他の光学技術を広い粘膜領域のスクリーニングに適切に応用して利用されている。
【0006】
また、上述のスクリーニングは、多くの人々が検診を受けられるよう廉価であるべきである。スクリーニングの費用を下げるためには、スタンドアローンの撮像モードで動作することができる機器あるいはシステムを提供することが好ましい。このようなスタンドアローン撮像は、患者が鎮静化されていなくても実行することができるものであり、ビデオ内視鏡検査に比べて検査手順のコストならびに複雑さが大幅に改善されている。サーベイランスでは、最も重篤な疾病を含む部位に対しては総合的な撮像手順を実行して直接的な組織検査を行うことができる。撮像と診療行為の両方を同一の撮像のセッションで行うことができるため、この総合的な撮像および大量のボリュームデータの判読は短時間に完了させる必要がある。
【発明の概要】
【発明が解決しようとする課題】
【0007】
管腔器官の総合的な画像生成にスキャニング収束光を用いる場合、幾つかの課題が存在する。収束光のスポットは通常、プローブから組織表面までのある距離範囲で収束した状態にある。ある種の器官用撮像システムでは、この焦点距離(例えば、その一測定基準はレイリー距離である)は、管腔径に比べて著しく小さなものである。この結果、管腔器官粘膜のスクリーニングでは、通常、ビームがその総合スキャン中収束するように器官管腔内の撮像用プローブの遠端/集光光学系のセンタリングが行われる。センタリングバルーンを用いた従来の食道OCT撮像用のシステムについて幾つか報告されている。(G.Tearney、「バレット氏病患者のスクリーニングおよび検査の改善」、NIH 助成No.R01−CA103769、およびBappart et al、「光コヒーレンストモグラフィー;バレット氏食道の内視鏡撮像の先端技術」、Endoscopy 2000;32(12)、pp.921−930を参照)
【0008】
これまでの臨床研究は、大概、食道の離散的な指定区域からのみ画像を取得していることが知られている。このような従来型装置の使用に際しては、食道壁に沿って関心領域を特定し、これらの部位に撮像用プローブを誘導するために内視鏡誘導装置を使用した。この装置は、集光ビームを高解像度でスキャンするためのある種の部品を検討する必要がある。各器官用システムでは、手術時の侵襲を軽減するためのカテーテル/プローブの種類および患者への挿入様式が望まれる。種々のセンタリング機構が可能であり、設計はその生態組織に特有なものである。ビームスキャニングプローブ用光学素子は、費用が嵩む、あるいは診療行為を複雑にすることなく、撮像の実行に先立って関心領域に配置する必要がある。このビーム集光機構は、プローブ被覆/センタリング機構により生じる収差を補正する構成を含む必要がある。当該器官の広い領域にわたる2次元または3次元画像を正確に取得するため、各データ取得位置に対してビーム位置を正確に知る必要がある。
【0009】
従って、上述の課題を解決する必要がある。
【課題を解決するための手段】
【0010】
上述の課題および/または課題を解決するため、ビームスキャニングによって上皮性管腔器官の光学的撮像を行う、代表的な実施の形態の装置および方法を提供することができる。これらの代表的な実施の形態の装置および方法は、プローブおよび/またはプローブの使い捨て部分、またはビームスキャニングによって上皮性管腔器官の光学的撮像を行う以下の要素および/または部品を使用可能なその他の機器を利用できる。特に、これらの代表的な実施の形態は、一以上の光学導波管、ビームを集光する遠端の一以上の光学部材、ビームを再誘導する遠端の一以上の光学部材、光沢的収差を補正するための遠端の一以上の光学部材、管腔器官表面を介したスキャニングビーム用の一以上の構成、センタリング機構、およびガイドワイヤ装置を利用できる。
【0011】
このため、本発明の代表的な実施の形態によると、少なくとも一つの管腔または中空サンプルの内部の少なくとも一つの部分のデータを取得する少なくとも一つの方法、装置、システムを提供する。方法、システムまたは装置は、患者の口または鼻の少なくとも一つを介して挿入できる。例えば、第1の光学構成部は、部分に少なくとも一つの電磁(例えば、可視)放射を放射し、受け取るように構成できる。第1の光学構成部を少なくとも部分的に囲繞する第2の構成部を設けてもよい。さらに、第3の構成部は、第1の光学構成部を少なくとも一つの管腔又は中空サンプルの内部の所定の部位に配置するように作動するように構成することができる。第1の光学構成部は、第2の構成部および/または第3の構成部の少なくとも一つによって生じる少なくとも一つの収差(例えば、非点収差)を補正するように構成してもよい。第2の構成部は、ガイド構成部を挿入することができる少なくとも一つの部分を含むことができる。
【0012】
本発明の他の代表的な実施の形態によると、少なくとも一つの部分の内部の圧力を測定するように構成された他の構成部を設けてもよい。データは、第1の光学構成部の管腔または中空サンプルに対する位置および/または方向性の少なくとも一つを含んでもよい。さらなる構成部は、スキャニング構成部を含み、少なくとも一つのサンプルを少なくとも一回スキャンする間にスキャニング構成部から取得したエンコーダ信号をデジタルにカウントして、位置および回転角度を検出するようにできる。位置および回転角度を受け、この位置および回転角度を用いて少なくとも一つの部分に関連する少なくとも一つの画像を生成するように構成されたさらなる構成部を備えることができる。さらなる構成部は、さらに、少なくとも一つの画像の少なくとも一つの空間歪みを補正するように構成してもよい。
【0013】
本発明の他の代表的な実施の形態では、第1の光学構成部がサンプルに対して少なくとも二軸並進の間、サンプルの複数の画像を受信するように制御可能な処理構成部をさらに備えてもよい。二軸並進の各々は回転角度で行ってもよい。データは、少なくとも一つのサンプルに関連する干渉データでもよい。干渉データは、スペクトル領域光コヒーレンストモグラフィーデータ、時間領域光コヒーレンストモグラフィーデータまたは光周波数領域撮像データの少なくとも一つでもよい。
【0014】
本発明のこれらの目的、機能、長所、またはその他の目的、機能、長所は、添付の特許請求の範囲とともに、以下の本発明の実施の形態の詳細な説明から明らかになる。
【発明の効果】
【0015】
本発明によれば、上述の課題を解決することができる。
【図面の簡単な説明】
【0016】
【図1】図1は、センタリング機構を内蔵可能な、本発明の代表的な実施の形態のマイクロモータカテーテルの概略分離図である。
【図2】図2は、生体組織構造の標的領域の限定された広域の撮像を行うことができる線形プッシュプルカテーテルの可視画像である。
【図3】図3は、ガイドワイヤ、収差補正光学部材、センタリング機構、およびフィードバック機能を具備した高速ビームスキャニング機構を含むことができる、本発明の代表的な実施の形態の構成の基本概略図である。
【図4】図4は、生体組織構造の標的領域で使用する場合の、図3に示した構成の代表的な実施の形態の撮像用カテーテルの概略図である。
【図5】図5は、図4に示した本発明の代表的な構成の、データ収集及び制御ユニット、撮像データ、プローブスキャナモータ制御部、およびプローブスキャナモータを含む、制御及びデータ記録機構の部品の間の代表的な電気的接続及びデータ接続のブロック及びフロー図である。
【図6】図6は、図5に示したデータ収集ユニットによりデータを収集し、また測定したa―ライン毎にプローブ位置を提供することができる、本発明の代表的な実施の形態の処理を説明する概略図である。
【図7A】図7Aは、ビームが加速して回転し、軸方向に低速度で移動して螺旋形撮像パターンを生成する、本発明の代表的な実施の形態のプローブスキャニング方法を説明する図である。
【図7B】図7Bは、ビームがスキャンを加速して軸方向に行い、続いて、回転して再び位置決め行うことを繰り返す、本発明の他の代表的な実施の形態のプローブスキャニング方法を説明する図である。
【図8A】図8Aは、先端部に設けたガイドワイヤを含む、本発明の第1の代表的な実施の形態の高速交換バルーンカテーテルの概略/動作図である。
【図8B】図8Bは、先端部に第2の経路として設けたガイドワイヤを含む、本発明の第2の代表的な実施の形態の高速交換バルーンカテーテルの概略/動作図である。
【図8C】図8Cは、バルーンの前方に第2の経路として設けたガイドワイヤを含む、本発明の第3の代表的な実施の形態の高速交換バルーンカテーテルの概略/動作図である。
【図9A】図9Aは、ガイドワイヤを挿入する際の、本発明の代表的な実施の形態のワイヤをまたがるバルーンカテーテルの使用の立体分解図である。
【図9B】図9Bは、ガイドワイヤを介してバルーンカテーテルを配置する際の、本発明の代表的な実施の形態のワイヤをまたがるバルーンカテーテルの使用の立体分解図である。
【図9C】図9Cは、ガイドワイヤを除去する際の、本発明の代表的な実施の形態のワイヤをまたがるバルーンカテーテルの使用の立体分解図である。
【図9D】図9Dは、光学部材をバルーンに配置する際の、本発明の代表的な実施の形態のワイヤをまたがるバルーンカテーテルの使用の立体分解図である。
【図10】図10は、二つの被覆を用いて、膨張物質(例えば、空気、食塩水)を遠端部分の膨張経路からこれらの被覆の間のバルーンに誘導する、代表的な実施の形体のバルーン構成の概略図である。
【図11】図11は、撮像インドウが単一被覆を含むことができるようにする、代表的な実施の形態のバルーンカテーテルの概略図である。
【図12】図12は、収差補正光学部材(例えば、マイクロ円筒型レンズ)を含む、本発明の代表的な実施の形態のプローブ光学部材の概略側面図および概略正面図である。
【図13】図13は、撮像ビームを回転する、後方を向いた(backward facing in−)カテーテルモータを用いる、本発明の他の代表的な実施の形態のバルーンカテーテルの概略側面図である。
【図14】図14は、撮像ビームを回転する、前方を向いた(forward facing in−)カテーテルモータを用いた、本発明のさらに他の代表的な実施の形態のバルーンカテーテルの概略側面図である。
【図15】図15は、モータ位置測定(例えば、エンコーダ)信号を生成できるように改変した、図14に示したバルーンカテーテルの代表的な変形態様の概略側面図である。
【図16A】図16Aは、システムの撮像領域における組織を保持するために測定したバルーン位置に対する基準アームの応答遅延を調節するように構成された、本発明の代表的な実施の形態のシステムのブロック図である。
【図16B】図16Bは、図16Aのシステムから出力される反射率と深度との関係のグラフである。
【図17A】図17Aは、撮像ユニットが患者によって嚥下され、撮像ユニットとを結ぶ光ファイバーおよび/または電気的接続を含む「紐」によって接続された、本発明の代表的な実施の形態の「紐付き玉」の一般図である。
【図17B】図17Bは、患者によって嚥下されている間の図17Aに示した構成部の動作を示す図である。
【図17C】図17Cは、図17Aに示した構成部の概要詳細図である。
【図18A】図18Aは、本発明の代表的な実施の形態のカテーテルの経口配置を示す図である。
【図18B】図18Bは、本発明の代表的な実施の形態の経口カテーテルの経鼻配置を示す図である。
【図19A】図19Aは、クローズドモードの、本発明の代表的なワイヤケージセンタリング構成の概略図である。
【図19B】図19Bは、その遠端部分から開始するオープニング時における、本発明の代表的なワイヤケージセンタリング構成の概略図である。
【図20】図20は、第2の波長帯で動作するさらなる光学的撮像構成と組み合わせた、本発明の代表的な実施の形態の光コヒーレンストモグラフィースクリーニング機器のブロック図である。
【図21】図21は、アブレーションビームをサンプルアームの撮像ビームと結合するように構成された、本発明のさらなる代表的な実施の形態の光コヒーレンストモグラフィー撮像システムのブロック図である。
【図22】図22は、オンザフライアブレーションを行うことができるように構成された、本発明のさらなる代表的な実施の形態の光コヒーレンストモグラフィー撮像システムのブロック図である。
【図23A】図23Aは、オンザフライアブレーションを行なう、本発明の代表的な実施の形態のアブレーションマーキング用処理のフロー図である。
【図23B】図23Bは、停止およびアブレーションを行う、本発明の代表的な実施の形態のアブレーションマーキング処理のフロー図を示す。
【図24】図24は、本発明の代表的な実施の形態の構成および処理による撮像で、豚の食道のアブレーションマークの可視性を示す内視鏡画像である。
【図25A】図25Aは、マルチプレクサ(MUX)の後に光学スイッチを設け、光学スイッチをシャッターとしてともに多重化する、波長が1400nmから1499nmの範囲の多重化レーザを用いる、アブレーション用レーザ源を含む、本発明の代表的な実施の形態の構成のブロック図である。
【図25B】図25Bは、マルチプレクサ(MUX)の前に位置するレーザ毎に独立して光学スイッチを設け、光学スイッチをシャッターとしてともに多重化する、波長が1400nmから1499nmの範囲の多重化レーザを用いる、アブレーション用レーザ源を含む、本発明の代表的な実施の形態の構成のブロック図である。
【図26】図26は、完結した撮像セッションで特定された関心領域をマーキングする、本発明の撮像システムが実行する代表的な処理のフロー図である。
【図27】図27は、本発明の代表的な実施の形態のワイヤをまたがるカテーテルまたは高速交換カテーテルの配置の代表的な手順のフロー図である。
【図28A】図28Aは、本発明の代表的な実施の形態の様々な段階の、プローブの撮像インドウの領域より大きい領域の撮像を実行する複数のプローブ配置を表す図である。
【図28B】図28Bは、本発明の代表的な実施の形態の様々な段階の、プローブの撮像インドウの領域より大きい領域の撮像を実行する複数のプローブ配置を表す図である。
【図28C】図28Cは、本発明の代表的な実施の形態の様々な段階の、プローブの撮像インドウの領域より大きい領域の撮像を実行する複数のプローブ配置を表す図である。
【図29】図29は、バルーンを胃の中で膨張させて、抵抗を感じるまで引き戻すことによって、バルーンの近端部を胃食道の接合部に配置する、本発明の代表的な配置手順のフロー図である。
【図30A】図30Aは、図29の代表的な方法を用いた代表的な構成によって実行される代表的なステップである。
【図30B】図30Bは、図29の代表的な方法を用いた代表的な構成によって実行される代表的なステップである。
【図30C】図30Cは、図29の代表的な方法を用いた代表的な構成によって実行される代表的なステップである。
【発明を実施するための形態】
【0017】
特に説明のない限り、図面を通して同様の参照番号および文字は、例示された実施の形態における同様の機能、要素、部品または部分を意味する。これらの図面を参照して、例示的な実施の形態の説明をしながら、本発明について詳細に説明する。なお、記載した実施の形態に対する変更及び改変については、添付の特許請求の範囲によって画定される本発明の真の範囲及び趣旨から逸脱することなく行うことができる。
【0018】
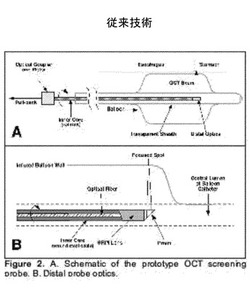
本発明による代表的な実施の形態として、食道下部の全体の画像の取得可能性を調査するためのプロトタイプの食道用プローブ1を作成した。図1にこの代表的なプローブの概略図を示す。この代表的なプロトタイプの食道スクリーニング用プローブ1は、スタンドアローンモードで、内視鏡検査とは独立して動作しながら食道下部の全体の画像の取得ができるように設計されている。しかしながら、食道下部の全体の撮像は、カテーテルと食道壁との距離が著しく変化することがあるため、最適な条件の下であっても困難である。画像が収束するレイリー領域は約1mm(スポット径〜35μm)であるため、食道管腔は可能な限り円形として、プローブは概ね食道管腔の中心に配置する必要がある。
【0019】
このような代表的なプロトタイプのスクリーニング用プローブ1において、食道バルーンセンタリングカテーテル(例えば、Eclipse 18x8、Wilson−Cook Medical,Inc.社製)を用いて、これらの課題を達成した。このプローブは、光ファイバーを包含する内部コアを内蔵している。図1に示すように、このファイバーは内部コアの遠端で終端し、光はGRIN(miniature gradient index)レンズで集光され、マイクロプリズムによって食道表面上に導かれる。内部コアはバルーンカテーテルの中央管腔に挿入した(図1に例示)。このプローブを用いて、内部コアを高速回転し、円周断面画像を取得しながら内部コアを長手方向に並進させて、食道下部の三次元画像を取得した。プロトタイププローブを用いて、生体外で、豚の2cm径の食道の三次元データを長手方向に長さ3cmにわたって取得した。3次元データセットの一つの長手断面および横断面は、本機器が体積全体にわたり高解像度画像を取得できる可能性を実証している。プルバック速度毎秒100μm、毎秒4フレーム、画像を取得することにより、三次元データセット全体を5分間で取得した(図2参照)。本発明のこの代表的なプロトタイプにより、小径OCTプローブを構成して、食道下部全体の高品質で高解像度画像を取得できることが実証された。
【0020】
本発明のビームスキャニングによる上皮性管腔器官の大領域撮像を実行する代表的な実施の形態の装置を提供することができる。このような代表的な実施の形態の装置は、撮像システム、撮像用カテーテルおよびカテーテルスキャナーを含むことができる。撮像システムは、光を撮像用カテーテルへ伝達し、カテーテルから戻る光を回収して、画像を生成する。撮像用カテーテルは、撮像システムで生成した光を管腔器官へ導き、この光をビームとして集光させて器官の管腔表面へ導く。カテーテルスキャナーを用いて、このビームによって管腔表面の広い領域を横断してスキャニングする。
【0021】
図3に、撮像システムを含むことができる、本発明の代表的な実施の形態の構成の基本概略図を示す。撮像システムは、(例えば、2004年9月8日出願の国際特許出願第PCT/US2004/029148号に記載の)光周波数領域撮像(OFDI)システム100を具備することができ、カテーテルスキャナーは、(例えば、2005年11月2日出願の米国特許出願第11/266,779号に記載の)プルバック型回転式光ファイバーカップラー110であり、撮像用カテーテルはバルーンカテーテルプローブ120である。OFDIは、光コヒーレントトモグラフィー(OCT)に類似した高速撮像技術である。図3に示す撮像システム100は、(例えば、2004年7月9日出願の米国特許出願第10/501,276号に記載の)スペクトル領域光コヒーレンストモグラフィー(SD−OCT)システムあるいは時間領域光コヒーレンストモグラフィー(TD−OCT)システムであってもよい。撮像システム100からの光は、バルーン撮像用カテーテル120の一部として構成可能なカテーテルスキャナー110へ導くことができる。
【0022】
図4は、解剖学的構造の標的領域で使用する場合の、図3に示した構成の代表的な実施の形態のバルーン撮像用カテーテル120の概略図を示す。例えば、カテーテルスキャナー110は、光(またはその他の電磁放射)を内部コア125へ供給してもよい。内部コア125は、光学的透過性被覆130で被覆することができる。内部コア125の遠端では、集光光学部材140が撮像する管腔器官145の表面に光を導き、焦点合わせする。バルーン135は、内部コア125が器官145の内部の中心に位置するように膨張させることができる。この内部コア125は、カテーテルスキャナー110を介して回転し、かつ軸方向に並進させるように構成できる。これにより、器官145の広い領域にわたり撮像ビームでスキャンすることが可能となる。内部コア125は、内部コア125の遠端へこの光を誘導する光ファイバーケーブルを含むことができる。ビームでスキャンしながら信号(例えばOFDI信号)を記録することにより、管腔器官145の広い領域を撮像することができる。
【0023】
図5は、図4に示した本発明の代表的な構成の、制御及びデータ記録機構の部品の間の代表的な電気的接続及びデータ接続のブロック及びフロー図である。図5に示すデータ、信号及び/又は情報のフローは、撮像データの記録とほぼ同時にビーム位置を記録することができるので、例えば、撮像データをほぼ正確に空間登録することができる。図5に示すように、OFDIシステムが取得した撮像データは、データ収集及び制御ユニット210により収集することができる。カテーテルスキャナー110は、回転機能を備えたモータ240とプルバック機能を備えたモータ250とを用いてビームスキャニングを行うことができる。モータ240とモータ250とはそれぞれモータ制御ユニット220、230によって閉ループ動作で制御できる。データ収集及び制御ユニット210は、モータ制御ユニット220、230に所要のモータ速度、及び/又は位置を達成するように指示することができる。モータ240、250とから送出されるエンコーダ信号は、モータ制御ユニット220、230、データ収集及び制御ユニット210の両方に利用できるように構成できる。このようにして撮像データ入力で深度スキャンを行う都度、モータ240、250の各々に対しエンコーダ信号を記録することができるので、その深度スキャンに対する正確なビーム位置を記録することができる。
【0024】
図6は、図5に示したデータ収集ユニット210によりデータを収集し、また測定したa―ライン毎にプローブ位置を提供することができる、本発明の代表的な実施の形態の処理を説明する概略図である。例えば、トリガ信号300を、アナログ−デジタル(A−D)変換器311で深度スキャン一回毎のトリガと、また、それぞれ回転モータエンコーダ信号320を受けることができるデジタルカウンタ321と、プルバックモータエンコーダ信号330を受けることができるデジタルカウンタ331の値を記録するために使用できる。エンコーダ信号320、330は、TTLパルス列であってもよく、TTLパルス列は、モータの1回転当り所定のレートで切り替わってもよい。このように、デジタルカウンタを用いてこれらの切り替えをカウントすることにより、モータの現在位置を測定できる。A−D変換器311とデジタルカウンタ321、331はデータ収集ユニット340に内蔵できる。
【0025】
図7Aは、ビームが加速して回転し、軸方向に低速度で移動して螺旋形撮像パターンを生成する、本発明の代表的な実施の形態のプローブスキャニング方法350を説明する図である。例えば回転スキャニングを、第1の優先度で行い、軸方向(例えばプルバック)スキャニングを第2の優先度で行なうことができる。これによって螺旋状データセットを得ることができる。
【0026】
図7Bは、ビームがスキャンを加速して軸方向に行い、続いて、回転して再び位置決め行うことを繰り返す、本発明の他の代表的な実施の形態のプローブスキャニング方法360を説明する図である。(B)では、軸方向(プルバック)スキャニングを第1の優先度で行い、回転スキャニングを第2の優先度で行なう。撮像品質は第1のスキャニング優先度に沿った時が最も優れていると考えられるため、スキャニングの優先度は横方向(回転方向)画像が必要なのか又は軸方向画像が必要なのかに応じて選択できる。
【0027】
図8Aは、先端部に設けたガイドワイヤを含む、図3を参照して説明した代表的な実施の形態の変形態様の高速交換バルーンカテーテル120の概略/動作図である。この代表的な実施の形態では、ガイドワイヤ全体にわたりその高速交換配置が可能である。具体的には、高速交換配置の場合、ガイドワイヤ400を最初に撮像を行う器官に配置し、次いでこのガイドワイヤ400に沿ってカテーテルを挿入することができる。本発明によるこの代表的な技術は、多くの使用例でカテーテルを大幅に配置しやすくするものである。例えば、図8Aに示すように、ガイドワイヤはバルーンカテーテル120の被覆の遠端に貫通孔410を設けて取り付けることができる。図8Bは、バルーンカテーテル120の遠端に第2のチューブ420を取り付けて設けたガイドワイヤを含む、本発明の代表的な実施の形態の他の変形態様の高速交換バルーンカテーテル120の概略/動作図である。図8Cは、チューブ430をバルーンの近端側に配置した、本発明の代表的な実施の形態の更に他の変形態様の高速交換バルーンカテーテル120の概略/動作図である。
【0028】
図9A−9Dは、ガイドワイヤ510の挿入時に中央管腔内のガイドワイヤ510を用いる、本発明の代表的な実施の形態のワイヤをまたがるバルーンカテーテルの使用の立体分解図である。図9Aにおいて、前記ガイドワイヤ510は器官500の中に配置されている。次いで、図9Bにおいて、ガイドワイヤ510がカテーテルの中央管腔520内に囲繞されるように、カテーテルをガイドワイヤ510をまたがって挿入する。次に、図9Cにおいてこのガイドワイヤ510を除去する。さらに、図9Dにおいて、内部光学コア530をカテーテル中央管腔520内に挿入し、撮像を開始する。
【0029】
図10は、バルーンを膨張させるために用いることができる機器600を含む、代表的な実施の形体のバルーンカテーテルの概略側面図である。例えば、バルーン650の気圧をマノメータ620を用いてモニタしてもよい。この気圧に基づいて、バルーン630の膨張を最適にすることができ、また、器官の圧力をモニタすることによって、カテーテルの配置を判定することもできる。
【0030】
図11は、撮像インドウが単一被覆を含むことができるようにする、代表的な実施の形態のバルーンカテーテルの一部分の概略図を示す。例えば、この図には、バルーン700と、カテーテル内部被覆705へ取り付けるためのその近端側アタッチメント720、および遠端側アタッチメント710が示されている。(既に説明し、さらに図8A〜図8Cに示したように)、断面図Bに詳細に示すように、遠端側アタッチメント710では、高速交換カテーテルで使用するためのガイドワイヤを受けるために被覆715に小孔が設けられている。このバルーン700は、バルーンの長さまで伸びた内側被覆722に取り付けることができる。バルーン700の近端側アタッチメント720の詳細を断面図Cに示す。バルーン720は、バルーン700内に入った直後に終端する外側被覆721に取り付けられている。この外側被覆721は内側被覆722に接着することができる。外側被覆721と内側被覆722とにより形成された経路(channel)を通してバルーンを膨張させることができるように、2つの小孔724、725を外側被覆721に設けてもよい。この代表的な設計のバルーンカテーテルの代表的な長所の一つは、バルーン720に沿って、バルーン720のその大部分に伸びた単一の被覆を用いる点にある。これらの被覆は撮像ビームに収差を惹起し撮像品質を劣化させる可能性があるため、バルーン中に2組に代えて1組の被覆を使用できれば画像品質を改善できるものである。
【0031】
図12は、本発明の代表的な実施の形態のカテーテルの内側コアの遠端における集光光学部材の側面断面図および正面断面図である。光ファイバー830経由で供給された光あるいはそれ以外の電磁放射は、GRINレンズ840により拡大され、次いで集光される。このレンズ840の焦点特性は、器官管腔近傍にビームの焦点が位置するように選択してもよい。マイクロプリズム850は、ビームを略90度反射することができる。被覆800および810により惹起されたビームの非点収差を補正するためにマイクロプリズム850に小型の円筒型レンズ860を取り付けてもよい。あるいは、マイクロプリズム850そのものを研磨して、一端が円筒型曲率を持つようにして、この非点収差の補正を行なってもよい。
【0032】
図13は、本発明による装置の代表的な実施法およびその他の代表的な実施の形態の、例えば、代表的なバルーンカテーテル中のビームスキャニングの概略図である。特に、カテーテルそのものの内部にマイクロモータ930を配置することにより回転スキャニングを行えるようにしている。図13に示すように、モータ930はカテーテルの遠端に配置することが可能であり、光ファイバー950はモータシャフト965に取り付けたプリズム960に導いてもよい。モータ940への代表的な電気的接続は、モータ930への撮像経路を通して取り回すことができるが、撮像ビームを若干妨害する可能性がある。バルーンを用いてこの光学コアを管腔器官内でセンタリングすることができる。円筒型レンズあるいはその他の非点収差補正用光学部材970を、プリズム上あるいはプリズムに設置して、透明被覆900を通過することにより生じる非点収差を補正してもよい。軸方向のスキャニングは、透明被覆カテーテル900内を、集光部材とモータ930を含む光学コア部分全体を並進させることによって行うことができる。この並進は、カテーテルの遠端のプルバック装置の影響を受ける可能性もある。
【0033】
図14に、図13と類似しているが、モータ電気接続部による撮像ビームの妨害を回避するように改変した、本発明の代表的な実施の形態のカテーテルを示す。この代表的な実施の形態では、光ファイバー1000をモータ1010の先へ導くことができ、ビームを反射キャップ1080によりモータシャフト1055上に取り付けたマイクロプリズム1050に反射する。収差補正光学部材1060を、プリズム1050の上またはこのプリズムに設けることができる。機器全体は、軸方向のスキャニングを行うために並進することができる。
【0034】
図15は、図14に類似しているが、モータエンコーダ信号として用いることができる光信号をさらに使用できるように改変した、他の代表的な実施の形態のカテーテルの側面図である。この代表的な実施の形態では、第2の光ファイバー1100は光またはその他の電磁放射をモータ1010の先まで誘導する。この光/放射は光学部材1110により集光され、モータのドライブシャフト1111に配置した反射エンコーダ1120へ反射される。この反射エンコーダ1120は高反射率、低反射率の領域を交互に含むことができる。モータシャフト1111が回転すると、このファイバーに反射投入される光はエンコーダ1120が提供する情報に従って変化してもよい。反射光学パワーを検出することにより、モータ1010回転の位置、速度および方向を測定することができる。この情報は、モータ1010の制御および/または画像とそのビーム位置の登録に用いることができる。
【0035】
図16Aは、システムの撮像領域における組織を保持するために測定したバルーン位置に対する基準アームの応答遅延を調節するように構成された、本発明の代表的な一実施の形態のシステム(例えばOCTシステム)のブロック図である。この代表的なOCT撮像システムは、自動照準合わせを実行することができる。例えば、OCT、OFDIまたはSD−OCTシステムでは、限定された深度領域にわたり反射率を測定できる。もし、サンプルがこの深度領域内に存在しなければ、このサンプルは通常、測定することができない。バルーンカテーテルはその管腔内でこの光プローブのセンタリングを行うことができるため、器官の管腔表面をプローブから概ね一定の深度(バルーン半径)に保持することができる。しかしながら、もしバルーンの形状が歪みその圧力のため上述の一定の深度を保持することが不完全であるならば、その器官は撮像する領域の外に外すことができる。図16Aに示す代表的な実施の形態では、管腔器官の位置を追跡するために撮像深度領域を調節する自動照準を用いることができる。これは、サンプル表面(例えばバルーン表面)の位置1210を(図16Bに示すように)その大きな反射信号により決定し、基準アーム遅延1220を調節して撮像領域の再位置決めを行うことにより実現できる。この基準アーム調節は、基準アーム光路遅延の修正を含むことができる。
【0036】
図17Aおよび図17Cは、本発明の代表的な実施の形態の「紐付き玉(pill−on−a−string)」構成を示しており、撮像ユニットは患者に嚥下され、光ファイバーおよび/または電気的接続系を含む「紐(string)」1310により撮像プローブ1300に接続されている。例えば、この撮像プローブ1300(例えば、「玉(pill)」)はマイクロモータ1320を含むものであって、患者に嚥下される(図17B参照)。図14に示す代表的なマイクロモータはモータ1320として用いることができる。プローブ1300は、光ファイバーと電気接続系を含む「紐」1310によりシステムに接続できる。この「紐」1310を用いることにより、プローブ1300の位置を制御することができ、また、プローブ1300を、例えば患者の食道中に配置することができる。撮像完了後、この「紐」を用いてプローブを回収することができる。
【0037】
図18Aと図18Bは、それぞれ本発明の代表的な実施の形態のカテーテルの経口ならびに経鼻配置、例えば、上部胃―腸管撮像の概略図である。図18Bにおいて、カテーテル1410は口1400を経由して、すなわち、経口により配置できる。図18Bで、カテーテル1410は鼻孔1420を経由して、すなわち経鼻により配置することができる。経鼻設計は患者の鎮痛処置を必要としないという長所を有するが、直径を小さくするべきである。本発明の代表的な実施の形態の光ファイバー撮像コアは比較的小型であるため、経鼻配置が可能である。
【0038】
図19Aおよび図19Bは、それぞれクローズドモードおよびその遠端部分から開始するオープニング時における、本発明の代表的な実施の形態の、代表的なカテーテルのワイヤケージセンタリング構成の概略図である。例えば、管腔器官内で内側の光学コアを伸張させ、センタリングをするために、バルーンに代えてワイヤ撚り線を使用してもよい。このカテーテルは、外側被覆1510、一組の伸張可能なワイヤステント1500および内部コア1530を含むことができる。このカテーテルを配置した後、ワイヤステント1500が器官を拡張することができるように、他の被覆を縮小してもよい。撮像の後、外側被覆1510は拡張してワイヤステントを折り畳むと、カテーテルは除去できる。
【0039】
図20は、第2の波長帯をカテーテル内に多重化して第2の撮像モダリティを達成できる、本発明の代表的な実施の形態の撮像システムのブロック図である。このモダリティは、例えば、可視光反射撮像または蛍光撮像であってよい。この代表的な構成において、可視光源1600は、第2の波長帯を第一の撮像波長帯、例えば、代表的には赤外と結合させる波長分割マルチプレクサ1630経由で、(一例として、図3に示されたような)撮像用カテーテルへ結合することができる。サンプルからの反射された可視光は、この波長分割マルチプレクサ1630により一次撮像波長帯から分離されて、スプリッタ1610により光レシーバ1620へ誘導される。
【0040】
上皮管腔器官撮像システムにとって有利な更なる機能性として、撮像データセットで同定された関心領域を直接に続けて精密に検査することができる点にある。例えば、食道領域内に異形成部分を検出した場合、その診断を確かめるために直接内視鏡によってその部分の組織生検を要望する場合がある。方法及びシステムを用いて画像データセットで同定した関心部位の組織に可視マークを付すことができる。さらに、図21に、アブレーション用レーザ1700を光ファイバー波長分割マルチプレクサ1710を介して撮像用カテーテルに結合してこれを実現する、本発明の他の代表的な実施の形態の構成のブロック図を示す。アブレーション用レーザ1700は、管腔器官上に表面変異を生じるに十分な光学パワーと波長を有するように構成することができる。これらの変異は内視鏡検査で見ることができ、さらなる検査、例えば生体検査用のマーカとして使用してよい。図21に示すように、このカテーテルはマーキングを付すべき領域に向けて固定できる。次いで、可視の変異を生じるに十分な時間このアブレーション用レーザを作動する。
【0041】
図22に、カテーテルスキャナーを停止せずアブレーションを動的(オンザフライ)に行なう、本発明の代替の代表的な実施の形態の構成を示す。データ収集ユニット1720は、カテーテルが関心領域を指差す場合に光学シャッター1730を開くようにプログラムされている。この光学シャッター1730は、開いているときにはアブレーション光を伝達し、閉じているときには遮断する。例えば、このカテーテルは動作し続けることができる。
【0042】
図23Aに、関心領域にオンザフライアブレーションを行なうための、本発明の代表的な実施の形態のアブレーションマーキング用処理のフロー図を示す。特に、ステップ1810において、アブレーションを行うポイント(溶発点)を特定する。ステップ1820において、シャッターがこのポイントで開くように設定する。ステップ1830において、このシャッターおよびアブレーションレーザを作動可能とし、次いでステップ1840でシャッターおよび/又はアブレーションレーザを作動不能とする。
【0043】
図23Bに、関心領域で停止およびアブレーション実施を行う、本発明の代表的な実施の形態のアブレーションマーキング処理のフロー図を示す。特に、ステップ1850においてアブレーションを行うべきポイント(溶発点)を特定する。ステップ1860において、カテーテルがそのポイントで停止するように命令する。ステップ1870において、シャッターおよび/またはアブレーションレーザを作動可能とし、ステップ1880において、これらのシャッターおよび/またはアブレーションレーザを作動不能とする。カテーテルはステップ1890において再び回転を開始する。
【0044】
図24に、関心領域のアブレーションマーキングを含む(本発明の代表的な実施の形態を用いて生成した)代表的な画像を示す。一例として、波長が1440nmから1480nmおよび光学パワーが約1秒間にわたり約300mWである一連のレーザを用いて食道に形成されたアブレーションマーク1900を例示する。
【0045】
図25Aおよび図25Bに、代表的な構成の多重アブレーション用レーザと光学スイッチ(シャッター)とを組み合わせることができる、本発明の代表的な実施の形態の構成と本発明の代表的な実施方法の実施の相互関連のフロー図およびブロック図を示す。図25Aにおいて、多重化レーザ2000、2010および2020は、マルチプレクサ(MUX)2030を用いて結合することができる。このマルチプレクサ2030は、波長分割マルチプレクサ、偏光マルチプレクサ、および/または両者の結合型であってもよく、これらのあとに単一のシャッター2040が続く。図25Bにおいて、各レーザ2000、2010、2020は独立したシャッター2050、2060、2070を用いており、これらのシャッターは次いでMUX2080を用いて結合される。
【0046】
図26に、管腔器官の検査および後続の関心領域のマーキングを行う、代表的な実施の形態の方法のブロック図を表す。ステップ2100において、管腔領域全体を画像化する。次いで、ステップ2110において、関心領域を自動アルゴリズムまたはオペレータの点検により識別する。ステップ2120において、カテーテルを第1の関心領域の部位へ導く。またステップ2130において、必要に応じて撮像を開始し、関心領域を再探索してカテーテル位置をインターラクティブに調節する。この再探索手順で、例えば食道の蠕動によるカテーテルの位置ずれを補正することができる。次いで、ステップ2140において、一つあるいは一連のアブレーションマークを関心領域の隣接領域あるいは周辺に形成することができる。この手順は各関心領域に対して繰り返し行う(ステップ2150、2130、2140等)。次いでステップ2160においてカテーテルを除去し、ステップ2170で更なる検査即ち生検をこれらのマークが付された領域に対して行なう。
【0047】
図27に、ガイドワイヤの内視鏡配置を用いた撮像用カテーテルの配置の本発明の代表的な実施の形態の手順を示す。特に、ステップ2200により、ガイドワイヤを内視鏡経路を通して挿入する。次いでステップ2210においてガイドワイヤを残してこの内視鏡を除去する。ステップ2220において、本発明のさまざまな代表的な実施の形態を参照して説明したように、カテーテルをガイドワイヤを覆うように配置する。次いで、ステップ2230において、このガイドワイヤを除去する。さらに、ステップ2240において、バルーンを膨張させ、次いでステップ2250で撮像を開始する。
【0048】
図28A〜図28Cに、バルーンの複数配置によりバルーン長よりも大きな領域の撮像を実施する、本発明の代表的な構成を用いた代表的な動作ステップを表す。図28A〜図28Cに示す位置のバルーンで取得された撮像情報は、組み合わせて広い範囲にわたる撮像画像を生成することができる。
【0049】
図29に、管状の食道と胃との間の接合部に撮像プローブを配置する代表的な実施の形態の方法を示す。図30A〜図30Cに、図29の方法を用いた本発明の代表的な構成により実行される代表的なステップを示す。ステップ2400において、バルーンは収縮した状態で挿入され胃に配置される。ステップ2410において、バルーンを膨張させ(図30A)、ステップ2420で抵抗を感じるまで引き戻す。これにより、バルーンの近端側が胃食道接合部(胃と食道との間の接合部)に配置される。次いで、ステップ2430において、バルーンを部分的に縮小させ(図30B)、カテーテルをあらかじめ定められた量、例えばバルーンの長さ分引き戻す。さらに、ステップ2440において、バルーンを膨張させ、胃食道接合部に配置されたカテーテルを用いて撮像処理を行う。
【0050】
本発明の更なる実施の形態では、カテーテルがその器官に適切に配置されているか判断するために、撮像システムを簡略モード(例えばスカウト撮像)で操作することができる。全体的な総合撮像は、カテーテルが適切に配置されていることが確認された後に開始することができる。さらに、本発明の他の代表的な実施の形態では、バルーンセンタリングカテーテルは空気以外の光学的に透明な物質、例えば、これらに限定するものではないが、水、重水(D2O)或いは油を用いて膨張させることができる。本発明のさらに他の代表的な実施の形態においては、レーザマーキングに、マーキングレーザの吸収を齎すように器官に事前投与した外因性作用物質を用いてもよい。本発明のさらなる代表的な実施の形態では、カテーテルの挿入を補助するために潤滑剤を使用することができる。本発明の他の代表的な実施の形態では、撮像品質を劣化させる可能性のある器官の粘膜を除去するために撮像に先立ち当該器官に粘膜除去剤を使用することができる。
【0051】
以上、単に本発明の原理を例示して説明した。本明細書に記載の技術を考慮して、記載の実施の形態にさまざまな修正や変更を行なうことは当業者には明かである。実際、本発明の代表的な実施の形態の装置、システム及び方法は、任意のOCTシステム、OFDIシステム、SD−OCTシステム或いはその他の撮像システムとともに用いる、および/またはこれらを実装することが可能であり、例えば、その全ての開示内容を本明細書の一部として援用する、2004年9月8日出願の国際特許出願第PCT/US2004/029148号、2005年11月2日出願の米国特許出願第11/266,779号、および2004年7月9日出願の米国特許出願第10/501,276号に記載のシステム等とともに使用することができる。従って、当業者にとっては、本明細書に明確に提示又は説明されていなくとも、本発明の原理を具現化する数多くのシステム、装置、及び方法に工夫を凝らすことが可能であり、これは本発明の趣旨と範囲内に含まれることが理解されるであろう。さらに、上述の明細書に前記の先行技術の知識が明示的に援用されていない範囲においても、その全体を明示的に本明細書に援用する。本明細書で引用した上述の全ての文献は、その全体を本明細書の一部として援用する。
【0052】
本発明のさらなる目的、機能、および長所は、詳細な説明と、例示的な本発明の実施の形態を示す以下の添付の図面から明らかになる。
【符号の説明】
【0053】
100 撮像システム
110 カテーテルスキャナー
125 内部コア
120 バルーン撮像用カテーテル
130 光学的透過性被覆
145 管腔器官
【技術分野】
【0001】
本発明は光学的撮像のための方法およびシステムに関するものであり、具体的には、ビームスキャニングを用いた上皮性管腔器官(epithelial luminal organ)の光学的撮像に関わる。
【背景技術】
【0002】
(関連出願の相互参照)
【0003】
本出願は、2006年1月19日出願の米国特許出願第60/761,004号に基づき優先度の利益を主張するものであり、この全ての開示内容を本明細書の一部として援用する。
(連邦政府により支援された研究に関する声明)
【0004】
本発明は、米国政府助成契約第RO1CA103769号として国立衛生研究所によりの支援を受けた。それ故、米国連邦政府は本発明に一定の権利を有するものである。
【0005】
疾病のスクリーニングは、1以上の可能性のある疾病を有しているか不明な個人が、そのような疾病を有しているか否かを判定するために受けるテストの一過程である。スクリーニングはしばしば大きな集団に対して行われるものであり、それ故廉価であり侵襲は最小となると見込まれる。特定の疾病を有する患者のサーベイランスとして、その疾病の過程において、疾病の重篤性を決定するテスト、例えば前癌状態が知られている患者では異形性の程度を決定するためのテストを行う。上皮性管腔器管、例えば消化管、尿管、胆嚢腺、婦人科関連器官管腔、中咽頭・肺系統などの疾病(例えば異形成症、癌など)に対する効果的なスクリーニング及びサーベイランスには、広範囲にわたる粘膜の総合的な評価を用いる。これまでに、時間領域光コヒーレンストモグラフィー(OCT)、スペクトル領域光コヒーレンストモグラフィー(SD−OCT)、光周波数領域撮像(OFDI)、ラマン分光法、反射分光法、共焦点顕微鏡検査法、光散乱分光法などの技術を含む、ビームスキャニング光学技術は、異形成症、初期癌などの粘膜性疾病の診断に利用可能な決定的な情報を提供することが実証されている。しかしながら、これらの技術は一般的に一度に一箇所の画像データのみを取得することができる、点スキャン方法であると考えられる。大きな管腔性器官を全体的にスクリーニングする場合、目的とする器官の領域、例えば、広い領域にわたって、集光ビームで高速にスキャンし、光学的な測定値を得る。それ故、カテーテル、プローブおよびこのビームスキャニング機能を実行できる機器は、これらの光学技術およびその他の光学技術を広い粘膜領域のスクリーニングに適切に応用して利用されている。
【0006】
また、上述のスクリーニングは、多くの人々が検診を受けられるよう廉価であるべきである。スクリーニングの費用を下げるためには、スタンドアローンの撮像モードで動作することができる機器あるいはシステムを提供することが好ましい。このようなスタンドアローン撮像は、患者が鎮静化されていなくても実行することができるものであり、ビデオ内視鏡検査に比べて検査手順のコストならびに複雑さが大幅に改善されている。サーベイランスでは、最も重篤な疾病を含む部位に対しては総合的な撮像手順を実行して直接的な組織検査を行うことができる。撮像と診療行為の両方を同一の撮像のセッションで行うことができるため、この総合的な撮像および大量のボリュームデータの判読は短時間に完了させる必要がある。
【発明の概要】
【発明が解決しようとする課題】
【0007】
管腔器官の総合的な画像生成にスキャニング収束光を用いる場合、幾つかの課題が存在する。収束光のスポットは通常、プローブから組織表面までのある距離範囲で収束した状態にある。ある種の器官用撮像システムでは、この焦点距離(例えば、その一測定基準はレイリー距離である)は、管腔径に比べて著しく小さなものである。この結果、管腔器官粘膜のスクリーニングでは、通常、ビームがその総合スキャン中収束するように器官管腔内の撮像用プローブの遠端/集光光学系のセンタリングが行われる。センタリングバルーンを用いた従来の食道OCT撮像用のシステムについて幾つか報告されている。(G.Tearney、「バレット氏病患者のスクリーニングおよび検査の改善」、NIH 助成No.R01−CA103769、およびBappart et al、「光コヒーレンストモグラフィー;バレット氏食道の内視鏡撮像の先端技術」、Endoscopy 2000;32(12)、pp.921−930を参照)
【0008】
これまでの臨床研究は、大概、食道の離散的な指定区域からのみ画像を取得していることが知られている。このような従来型装置の使用に際しては、食道壁に沿って関心領域を特定し、これらの部位に撮像用プローブを誘導するために内視鏡誘導装置を使用した。この装置は、集光ビームを高解像度でスキャンするためのある種の部品を検討する必要がある。各器官用システムでは、手術時の侵襲を軽減するためのカテーテル/プローブの種類および患者への挿入様式が望まれる。種々のセンタリング機構が可能であり、設計はその生態組織に特有なものである。ビームスキャニングプローブ用光学素子は、費用が嵩む、あるいは診療行為を複雑にすることなく、撮像の実行に先立って関心領域に配置する必要がある。このビーム集光機構は、プローブ被覆/センタリング機構により生じる収差を補正する構成を含む必要がある。当該器官の広い領域にわたる2次元または3次元画像を正確に取得するため、各データ取得位置に対してビーム位置を正確に知る必要がある。
【0009】
従って、上述の課題を解決する必要がある。
【課題を解決するための手段】
【0010】
上述の課題および/または課題を解決するため、ビームスキャニングによって上皮性管腔器官の光学的撮像を行う、代表的な実施の形態の装置および方法を提供することができる。これらの代表的な実施の形態の装置および方法は、プローブおよび/またはプローブの使い捨て部分、またはビームスキャニングによって上皮性管腔器官の光学的撮像を行う以下の要素および/または部品を使用可能なその他の機器を利用できる。特に、これらの代表的な実施の形態は、一以上の光学導波管、ビームを集光する遠端の一以上の光学部材、ビームを再誘導する遠端の一以上の光学部材、光沢的収差を補正するための遠端の一以上の光学部材、管腔器官表面を介したスキャニングビーム用の一以上の構成、センタリング機構、およびガイドワイヤ装置を利用できる。
【0011】
このため、本発明の代表的な実施の形態によると、少なくとも一つの管腔または中空サンプルの内部の少なくとも一つの部分のデータを取得する少なくとも一つの方法、装置、システムを提供する。方法、システムまたは装置は、患者の口または鼻の少なくとも一つを介して挿入できる。例えば、第1の光学構成部は、部分に少なくとも一つの電磁(例えば、可視)放射を放射し、受け取るように構成できる。第1の光学構成部を少なくとも部分的に囲繞する第2の構成部を設けてもよい。さらに、第3の構成部は、第1の光学構成部を少なくとも一つの管腔又は中空サンプルの内部の所定の部位に配置するように作動するように構成することができる。第1の光学構成部は、第2の構成部および/または第3の構成部の少なくとも一つによって生じる少なくとも一つの収差(例えば、非点収差)を補正するように構成してもよい。第2の構成部は、ガイド構成部を挿入することができる少なくとも一つの部分を含むことができる。
【0012】
本発明の他の代表的な実施の形態によると、少なくとも一つの部分の内部の圧力を測定するように構成された他の構成部を設けてもよい。データは、第1の光学構成部の管腔または中空サンプルに対する位置および/または方向性の少なくとも一つを含んでもよい。さらなる構成部は、スキャニング構成部を含み、少なくとも一つのサンプルを少なくとも一回スキャンする間にスキャニング構成部から取得したエンコーダ信号をデジタルにカウントして、位置および回転角度を検出するようにできる。位置および回転角度を受け、この位置および回転角度を用いて少なくとも一つの部分に関連する少なくとも一つの画像を生成するように構成されたさらなる構成部を備えることができる。さらなる構成部は、さらに、少なくとも一つの画像の少なくとも一つの空間歪みを補正するように構成してもよい。
【0013】
本発明の他の代表的な実施の形態では、第1の光学構成部がサンプルに対して少なくとも二軸並進の間、サンプルの複数の画像を受信するように制御可能な処理構成部をさらに備えてもよい。二軸並進の各々は回転角度で行ってもよい。データは、少なくとも一つのサンプルに関連する干渉データでもよい。干渉データは、スペクトル領域光コヒーレンストモグラフィーデータ、時間領域光コヒーレンストモグラフィーデータまたは光周波数領域撮像データの少なくとも一つでもよい。
【0014】
本発明のこれらの目的、機能、長所、またはその他の目的、機能、長所は、添付の特許請求の範囲とともに、以下の本発明の実施の形態の詳細な説明から明らかになる。
【発明の効果】
【0015】
本発明によれば、上述の課題を解決することができる。
【図面の簡単な説明】
【0016】
【図1】図1は、センタリング機構を内蔵可能な、本発明の代表的な実施の形態のマイクロモータカテーテルの概略分離図である。
【図2】図2は、生体組織構造の標的領域の限定された広域の撮像を行うことができる線形プッシュプルカテーテルの可視画像である。
【図3】図3は、ガイドワイヤ、収差補正光学部材、センタリング機構、およびフィードバック機能を具備した高速ビームスキャニング機構を含むことができる、本発明の代表的な実施の形態の構成の基本概略図である。
【図4】図4は、生体組織構造の標的領域で使用する場合の、図3に示した構成の代表的な実施の形態の撮像用カテーテルの概略図である。
【図5】図5は、図4に示した本発明の代表的な構成の、データ収集及び制御ユニット、撮像データ、プローブスキャナモータ制御部、およびプローブスキャナモータを含む、制御及びデータ記録機構の部品の間の代表的な電気的接続及びデータ接続のブロック及びフロー図である。
【図6】図6は、図5に示したデータ収集ユニットによりデータを収集し、また測定したa―ライン毎にプローブ位置を提供することができる、本発明の代表的な実施の形態の処理を説明する概略図である。
【図7A】図7Aは、ビームが加速して回転し、軸方向に低速度で移動して螺旋形撮像パターンを生成する、本発明の代表的な実施の形態のプローブスキャニング方法を説明する図である。
【図7B】図7Bは、ビームがスキャンを加速して軸方向に行い、続いて、回転して再び位置決め行うことを繰り返す、本発明の他の代表的な実施の形態のプローブスキャニング方法を説明する図である。
【図8A】図8Aは、先端部に設けたガイドワイヤを含む、本発明の第1の代表的な実施の形態の高速交換バルーンカテーテルの概略/動作図である。
【図8B】図8Bは、先端部に第2の経路として設けたガイドワイヤを含む、本発明の第2の代表的な実施の形態の高速交換バルーンカテーテルの概略/動作図である。
【図8C】図8Cは、バルーンの前方に第2の経路として設けたガイドワイヤを含む、本発明の第3の代表的な実施の形態の高速交換バルーンカテーテルの概略/動作図である。
【図9A】図9Aは、ガイドワイヤを挿入する際の、本発明の代表的な実施の形態のワイヤをまたがるバルーンカテーテルの使用の立体分解図である。
【図9B】図9Bは、ガイドワイヤを介してバルーンカテーテルを配置する際の、本発明の代表的な実施の形態のワイヤをまたがるバルーンカテーテルの使用の立体分解図である。
【図9C】図9Cは、ガイドワイヤを除去する際の、本発明の代表的な実施の形態のワイヤをまたがるバルーンカテーテルの使用の立体分解図である。
【図9D】図9Dは、光学部材をバルーンに配置する際の、本発明の代表的な実施の形態のワイヤをまたがるバルーンカテーテルの使用の立体分解図である。
【図10】図10は、二つの被覆を用いて、膨張物質(例えば、空気、食塩水)を遠端部分の膨張経路からこれらの被覆の間のバルーンに誘導する、代表的な実施の形体のバルーン構成の概略図である。
【図11】図11は、撮像インドウが単一被覆を含むことができるようにする、代表的な実施の形態のバルーンカテーテルの概略図である。
【図12】図12は、収差補正光学部材(例えば、マイクロ円筒型レンズ)を含む、本発明の代表的な実施の形態のプローブ光学部材の概略側面図および概略正面図である。
【図13】図13は、撮像ビームを回転する、後方を向いた(backward facing in−)カテーテルモータを用いる、本発明の他の代表的な実施の形態のバルーンカテーテルの概略側面図である。
【図14】図14は、撮像ビームを回転する、前方を向いた(forward facing in−)カテーテルモータを用いた、本発明のさらに他の代表的な実施の形態のバルーンカテーテルの概略側面図である。
【図15】図15は、モータ位置測定(例えば、エンコーダ)信号を生成できるように改変した、図14に示したバルーンカテーテルの代表的な変形態様の概略側面図である。
【図16A】図16Aは、システムの撮像領域における組織を保持するために測定したバルーン位置に対する基準アームの応答遅延を調節するように構成された、本発明の代表的な実施の形態のシステムのブロック図である。
【図16B】図16Bは、図16Aのシステムから出力される反射率と深度との関係のグラフである。
【図17A】図17Aは、撮像ユニットが患者によって嚥下され、撮像ユニットとを結ぶ光ファイバーおよび/または電気的接続を含む「紐」によって接続された、本発明の代表的な実施の形態の「紐付き玉」の一般図である。
【図17B】図17Bは、患者によって嚥下されている間の図17Aに示した構成部の動作を示す図である。
【図17C】図17Cは、図17Aに示した構成部の概要詳細図である。
【図18A】図18Aは、本発明の代表的な実施の形態のカテーテルの経口配置を示す図である。
【図18B】図18Bは、本発明の代表的な実施の形態の経口カテーテルの経鼻配置を示す図である。
【図19A】図19Aは、クローズドモードの、本発明の代表的なワイヤケージセンタリング構成の概略図である。
【図19B】図19Bは、その遠端部分から開始するオープニング時における、本発明の代表的なワイヤケージセンタリング構成の概略図である。
【図20】図20は、第2の波長帯で動作するさらなる光学的撮像構成と組み合わせた、本発明の代表的な実施の形態の光コヒーレンストモグラフィースクリーニング機器のブロック図である。
【図21】図21は、アブレーションビームをサンプルアームの撮像ビームと結合するように構成された、本発明のさらなる代表的な実施の形態の光コヒーレンストモグラフィー撮像システムのブロック図である。
【図22】図22は、オンザフライアブレーションを行うことができるように構成された、本発明のさらなる代表的な実施の形態の光コヒーレンストモグラフィー撮像システムのブロック図である。
【図23A】図23Aは、オンザフライアブレーションを行なう、本発明の代表的な実施の形態のアブレーションマーキング用処理のフロー図である。
【図23B】図23Bは、停止およびアブレーションを行う、本発明の代表的な実施の形態のアブレーションマーキング処理のフロー図を示す。
【図24】図24は、本発明の代表的な実施の形態の構成および処理による撮像で、豚の食道のアブレーションマークの可視性を示す内視鏡画像である。
【図25A】図25Aは、マルチプレクサ(MUX)の後に光学スイッチを設け、光学スイッチをシャッターとしてともに多重化する、波長が1400nmから1499nmの範囲の多重化レーザを用いる、アブレーション用レーザ源を含む、本発明の代表的な実施の形態の構成のブロック図である。
【図25B】図25Bは、マルチプレクサ(MUX)の前に位置するレーザ毎に独立して光学スイッチを設け、光学スイッチをシャッターとしてともに多重化する、波長が1400nmから1499nmの範囲の多重化レーザを用いる、アブレーション用レーザ源を含む、本発明の代表的な実施の形態の構成のブロック図である。
【図26】図26は、完結した撮像セッションで特定された関心領域をマーキングする、本発明の撮像システムが実行する代表的な処理のフロー図である。
【図27】図27は、本発明の代表的な実施の形態のワイヤをまたがるカテーテルまたは高速交換カテーテルの配置の代表的な手順のフロー図である。
【図28A】図28Aは、本発明の代表的な実施の形態の様々な段階の、プローブの撮像インドウの領域より大きい領域の撮像を実行する複数のプローブ配置を表す図である。
【図28B】図28Bは、本発明の代表的な実施の形態の様々な段階の、プローブの撮像インドウの領域より大きい領域の撮像を実行する複数のプローブ配置を表す図である。
【図28C】図28Cは、本発明の代表的な実施の形態の様々な段階の、プローブの撮像インドウの領域より大きい領域の撮像を実行する複数のプローブ配置を表す図である。
【図29】図29は、バルーンを胃の中で膨張させて、抵抗を感じるまで引き戻すことによって、バルーンの近端部を胃食道の接合部に配置する、本発明の代表的な配置手順のフロー図である。
【図30A】図30Aは、図29の代表的な方法を用いた代表的な構成によって実行される代表的なステップである。
【図30B】図30Bは、図29の代表的な方法を用いた代表的な構成によって実行される代表的なステップである。
【図30C】図30Cは、図29の代表的な方法を用いた代表的な構成によって実行される代表的なステップである。
【発明を実施するための形態】
【0017】
特に説明のない限り、図面を通して同様の参照番号および文字は、例示された実施の形態における同様の機能、要素、部品または部分を意味する。これらの図面を参照して、例示的な実施の形態の説明をしながら、本発明について詳細に説明する。なお、記載した実施の形態に対する変更及び改変については、添付の特許請求の範囲によって画定される本発明の真の範囲及び趣旨から逸脱することなく行うことができる。
【0018】
本発明による代表的な実施の形態として、食道下部の全体の画像の取得可能性を調査するためのプロトタイプの食道用プローブ1を作成した。図1にこの代表的なプローブの概略図を示す。この代表的なプロトタイプの食道スクリーニング用プローブ1は、スタンドアローンモードで、内視鏡検査とは独立して動作しながら食道下部の全体の画像の取得ができるように設計されている。しかしながら、食道下部の全体の撮像は、カテーテルと食道壁との距離が著しく変化することがあるため、最適な条件の下であっても困難である。画像が収束するレイリー領域は約1mm(スポット径〜35μm)であるため、食道管腔は可能な限り円形として、プローブは概ね食道管腔の中心に配置する必要がある。
【0019】
このような代表的なプロトタイプのスクリーニング用プローブ1において、食道バルーンセンタリングカテーテル(例えば、Eclipse 18x8、Wilson−Cook Medical,Inc.社製)を用いて、これらの課題を達成した。このプローブは、光ファイバーを包含する内部コアを内蔵している。図1に示すように、このファイバーは内部コアの遠端で終端し、光はGRIN(miniature gradient index)レンズで集光され、マイクロプリズムによって食道表面上に導かれる。内部コアはバルーンカテーテルの中央管腔に挿入した(図1に例示)。このプローブを用いて、内部コアを高速回転し、円周断面画像を取得しながら内部コアを長手方向に並進させて、食道下部の三次元画像を取得した。プロトタイププローブを用いて、生体外で、豚の2cm径の食道の三次元データを長手方向に長さ3cmにわたって取得した。3次元データセットの一つの長手断面および横断面は、本機器が体積全体にわたり高解像度画像を取得できる可能性を実証している。プルバック速度毎秒100μm、毎秒4フレーム、画像を取得することにより、三次元データセット全体を5分間で取得した(図2参照)。本発明のこの代表的なプロトタイプにより、小径OCTプローブを構成して、食道下部全体の高品質で高解像度画像を取得できることが実証された。
【0020】
本発明のビームスキャニングによる上皮性管腔器官の大領域撮像を実行する代表的な実施の形態の装置を提供することができる。このような代表的な実施の形態の装置は、撮像システム、撮像用カテーテルおよびカテーテルスキャナーを含むことができる。撮像システムは、光を撮像用カテーテルへ伝達し、カテーテルから戻る光を回収して、画像を生成する。撮像用カテーテルは、撮像システムで生成した光を管腔器官へ導き、この光をビームとして集光させて器官の管腔表面へ導く。カテーテルスキャナーを用いて、このビームによって管腔表面の広い領域を横断してスキャニングする。
【0021】
図3に、撮像システムを含むことができる、本発明の代表的な実施の形態の構成の基本概略図を示す。撮像システムは、(例えば、2004年9月8日出願の国際特許出願第PCT/US2004/029148号に記載の)光周波数領域撮像(OFDI)システム100を具備することができ、カテーテルスキャナーは、(例えば、2005年11月2日出願の米国特許出願第11/266,779号に記載の)プルバック型回転式光ファイバーカップラー110であり、撮像用カテーテルはバルーンカテーテルプローブ120である。OFDIは、光コヒーレントトモグラフィー(OCT)に類似した高速撮像技術である。図3に示す撮像システム100は、(例えば、2004年7月9日出願の米国特許出願第10/501,276号に記載の)スペクトル領域光コヒーレンストモグラフィー(SD−OCT)システムあるいは時間領域光コヒーレンストモグラフィー(TD−OCT)システムであってもよい。撮像システム100からの光は、バルーン撮像用カテーテル120の一部として構成可能なカテーテルスキャナー110へ導くことができる。
【0022】
図4は、解剖学的構造の標的領域で使用する場合の、図3に示した構成の代表的な実施の形態のバルーン撮像用カテーテル120の概略図を示す。例えば、カテーテルスキャナー110は、光(またはその他の電磁放射)を内部コア125へ供給してもよい。内部コア125は、光学的透過性被覆130で被覆することができる。内部コア125の遠端では、集光光学部材140が撮像する管腔器官145の表面に光を導き、焦点合わせする。バルーン135は、内部コア125が器官145の内部の中心に位置するように膨張させることができる。この内部コア125は、カテーテルスキャナー110を介して回転し、かつ軸方向に並進させるように構成できる。これにより、器官145の広い領域にわたり撮像ビームでスキャンすることが可能となる。内部コア125は、内部コア125の遠端へこの光を誘導する光ファイバーケーブルを含むことができる。ビームでスキャンしながら信号(例えばOFDI信号)を記録することにより、管腔器官145の広い領域を撮像することができる。
【0023】
図5は、図4に示した本発明の代表的な構成の、制御及びデータ記録機構の部品の間の代表的な電気的接続及びデータ接続のブロック及びフロー図である。図5に示すデータ、信号及び/又は情報のフローは、撮像データの記録とほぼ同時にビーム位置を記録することができるので、例えば、撮像データをほぼ正確に空間登録することができる。図5に示すように、OFDIシステムが取得した撮像データは、データ収集及び制御ユニット210により収集することができる。カテーテルスキャナー110は、回転機能を備えたモータ240とプルバック機能を備えたモータ250とを用いてビームスキャニングを行うことができる。モータ240とモータ250とはそれぞれモータ制御ユニット220、230によって閉ループ動作で制御できる。データ収集及び制御ユニット210は、モータ制御ユニット220、230に所要のモータ速度、及び/又は位置を達成するように指示することができる。モータ240、250とから送出されるエンコーダ信号は、モータ制御ユニット220、230、データ収集及び制御ユニット210の両方に利用できるように構成できる。このようにして撮像データ入力で深度スキャンを行う都度、モータ240、250の各々に対しエンコーダ信号を記録することができるので、その深度スキャンに対する正確なビーム位置を記録することができる。
【0024】
図6は、図5に示したデータ収集ユニット210によりデータを収集し、また測定したa―ライン毎にプローブ位置を提供することができる、本発明の代表的な実施の形態の処理を説明する概略図である。例えば、トリガ信号300を、アナログ−デジタル(A−D)変換器311で深度スキャン一回毎のトリガと、また、それぞれ回転モータエンコーダ信号320を受けることができるデジタルカウンタ321と、プルバックモータエンコーダ信号330を受けることができるデジタルカウンタ331の値を記録するために使用できる。エンコーダ信号320、330は、TTLパルス列であってもよく、TTLパルス列は、モータの1回転当り所定のレートで切り替わってもよい。このように、デジタルカウンタを用いてこれらの切り替えをカウントすることにより、モータの現在位置を測定できる。A−D変換器311とデジタルカウンタ321、331はデータ収集ユニット340に内蔵できる。
【0025】
図7Aは、ビームが加速して回転し、軸方向に低速度で移動して螺旋形撮像パターンを生成する、本発明の代表的な実施の形態のプローブスキャニング方法350を説明する図である。例えば回転スキャニングを、第1の優先度で行い、軸方向(例えばプルバック)スキャニングを第2の優先度で行なうことができる。これによって螺旋状データセットを得ることができる。
【0026】
図7Bは、ビームがスキャンを加速して軸方向に行い、続いて、回転して再び位置決め行うことを繰り返す、本発明の他の代表的な実施の形態のプローブスキャニング方法360を説明する図である。(B)では、軸方向(プルバック)スキャニングを第1の優先度で行い、回転スキャニングを第2の優先度で行なう。撮像品質は第1のスキャニング優先度に沿った時が最も優れていると考えられるため、スキャニングの優先度は横方向(回転方向)画像が必要なのか又は軸方向画像が必要なのかに応じて選択できる。
【0027】
図8Aは、先端部に設けたガイドワイヤを含む、図3を参照して説明した代表的な実施の形態の変形態様の高速交換バルーンカテーテル120の概略/動作図である。この代表的な実施の形態では、ガイドワイヤ全体にわたりその高速交換配置が可能である。具体的には、高速交換配置の場合、ガイドワイヤ400を最初に撮像を行う器官に配置し、次いでこのガイドワイヤ400に沿ってカテーテルを挿入することができる。本発明によるこの代表的な技術は、多くの使用例でカテーテルを大幅に配置しやすくするものである。例えば、図8Aに示すように、ガイドワイヤはバルーンカテーテル120の被覆の遠端に貫通孔410を設けて取り付けることができる。図8Bは、バルーンカテーテル120の遠端に第2のチューブ420を取り付けて設けたガイドワイヤを含む、本発明の代表的な実施の形態の他の変形態様の高速交換バルーンカテーテル120の概略/動作図である。図8Cは、チューブ430をバルーンの近端側に配置した、本発明の代表的な実施の形態の更に他の変形態様の高速交換バルーンカテーテル120の概略/動作図である。
【0028】
図9A−9Dは、ガイドワイヤ510の挿入時に中央管腔内のガイドワイヤ510を用いる、本発明の代表的な実施の形態のワイヤをまたがるバルーンカテーテルの使用の立体分解図である。図9Aにおいて、前記ガイドワイヤ510は器官500の中に配置されている。次いで、図9Bにおいて、ガイドワイヤ510がカテーテルの中央管腔520内に囲繞されるように、カテーテルをガイドワイヤ510をまたがって挿入する。次に、図9Cにおいてこのガイドワイヤ510を除去する。さらに、図9Dにおいて、内部光学コア530をカテーテル中央管腔520内に挿入し、撮像を開始する。
【0029】
図10は、バルーンを膨張させるために用いることができる機器600を含む、代表的な実施の形体のバルーンカテーテルの概略側面図である。例えば、バルーン650の気圧をマノメータ620を用いてモニタしてもよい。この気圧に基づいて、バルーン630の膨張を最適にすることができ、また、器官の圧力をモニタすることによって、カテーテルの配置を判定することもできる。
【0030】
図11は、撮像インドウが単一被覆を含むことができるようにする、代表的な実施の形態のバルーンカテーテルの一部分の概略図を示す。例えば、この図には、バルーン700と、カテーテル内部被覆705へ取り付けるためのその近端側アタッチメント720、および遠端側アタッチメント710が示されている。(既に説明し、さらに図8A〜図8Cに示したように)、断面図Bに詳細に示すように、遠端側アタッチメント710では、高速交換カテーテルで使用するためのガイドワイヤを受けるために被覆715に小孔が設けられている。このバルーン700は、バルーンの長さまで伸びた内側被覆722に取り付けることができる。バルーン700の近端側アタッチメント720の詳細を断面図Cに示す。バルーン720は、バルーン700内に入った直後に終端する外側被覆721に取り付けられている。この外側被覆721は内側被覆722に接着することができる。外側被覆721と内側被覆722とにより形成された経路(channel)を通してバルーンを膨張させることができるように、2つの小孔724、725を外側被覆721に設けてもよい。この代表的な設計のバルーンカテーテルの代表的な長所の一つは、バルーン720に沿って、バルーン720のその大部分に伸びた単一の被覆を用いる点にある。これらの被覆は撮像ビームに収差を惹起し撮像品質を劣化させる可能性があるため、バルーン中に2組に代えて1組の被覆を使用できれば画像品質を改善できるものである。
【0031】
図12は、本発明の代表的な実施の形態のカテーテルの内側コアの遠端における集光光学部材の側面断面図および正面断面図である。光ファイバー830経由で供給された光あるいはそれ以外の電磁放射は、GRINレンズ840により拡大され、次いで集光される。このレンズ840の焦点特性は、器官管腔近傍にビームの焦点が位置するように選択してもよい。マイクロプリズム850は、ビームを略90度反射することができる。被覆800および810により惹起されたビームの非点収差を補正するためにマイクロプリズム850に小型の円筒型レンズ860を取り付けてもよい。あるいは、マイクロプリズム850そのものを研磨して、一端が円筒型曲率を持つようにして、この非点収差の補正を行なってもよい。
【0032】
図13は、本発明による装置の代表的な実施法およびその他の代表的な実施の形態の、例えば、代表的なバルーンカテーテル中のビームスキャニングの概略図である。特に、カテーテルそのものの内部にマイクロモータ930を配置することにより回転スキャニングを行えるようにしている。図13に示すように、モータ930はカテーテルの遠端に配置することが可能であり、光ファイバー950はモータシャフト965に取り付けたプリズム960に導いてもよい。モータ940への代表的な電気的接続は、モータ930への撮像経路を通して取り回すことができるが、撮像ビームを若干妨害する可能性がある。バルーンを用いてこの光学コアを管腔器官内でセンタリングすることができる。円筒型レンズあるいはその他の非点収差補正用光学部材970を、プリズム上あるいはプリズムに設置して、透明被覆900を通過することにより生じる非点収差を補正してもよい。軸方向のスキャニングは、透明被覆カテーテル900内を、集光部材とモータ930を含む光学コア部分全体を並進させることによって行うことができる。この並進は、カテーテルの遠端のプルバック装置の影響を受ける可能性もある。
【0033】
図14に、図13と類似しているが、モータ電気接続部による撮像ビームの妨害を回避するように改変した、本発明の代表的な実施の形態のカテーテルを示す。この代表的な実施の形態では、光ファイバー1000をモータ1010の先へ導くことができ、ビームを反射キャップ1080によりモータシャフト1055上に取り付けたマイクロプリズム1050に反射する。収差補正光学部材1060を、プリズム1050の上またはこのプリズムに設けることができる。機器全体は、軸方向のスキャニングを行うために並進することができる。
【0034】
図15は、図14に類似しているが、モータエンコーダ信号として用いることができる光信号をさらに使用できるように改変した、他の代表的な実施の形態のカテーテルの側面図である。この代表的な実施の形態では、第2の光ファイバー1100は光またはその他の電磁放射をモータ1010の先まで誘導する。この光/放射は光学部材1110により集光され、モータのドライブシャフト1111に配置した反射エンコーダ1120へ反射される。この反射エンコーダ1120は高反射率、低反射率の領域を交互に含むことができる。モータシャフト1111が回転すると、このファイバーに反射投入される光はエンコーダ1120が提供する情報に従って変化してもよい。反射光学パワーを検出することにより、モータ1010回転の位置、速度および方向を測定することができる。この情報は、モータ1010の制御および/または画像とそのビーム位置の登録に用いることができる。
【0035】
図16Aは、システムの撮像領域における組織を保持するために測定したバルーン位置に対する基準アームの応答遅延を調節するように構成された、本発明の代表的な一実施の形態のシステム(例えばOCTシステム)のブロック図である。この代表的なOCT撮像システムは、自動照準合わせを実行することができる。例えば、OCT、OFDIまたはSD−OCTシステムでは、限定された深度領域にわたり反射率を測定できる。もし、サンプルがこの深度領域内に存在しなければ、このサンプルは通常、測定することができない。バルーンカテーテルはその管腔内でこの光プローブのセンタリングを行うことができるため、器官の管腔表面をプローブから概ね一定の深度(バルーン半径)に保持することができる。しかしながら、もしバルーンの形状が歪みその圧力のため上述の一定の深度を保持することが不完全であるならば、その器官は撮像する領域の外に外すことができる。図16Aに示す代表的な実施の形態では、管腔器官の位置を追跡するために撮像深度領域を調節する自動照準を用いることができる。これは、サンプル表面(例えばバルーン表面)の位置1210を(図16Bに示すように)その大きな反射信号により決定し、基準アーム遅延1220を調節して撮像領域の再位置決めを行うことにより実現できる。この基準アーム調節は、基準アーム光路遅延の修正を含むことができる。
【0036】
図17Aおよび図17Cは、本発明の代表的な実施の形態の「紐付き玉(pill−on−a−string)」構成を示しており、撮像ユニットは患者に嚥下され、光ファイバーおよび/または電気的接続系を含む「紐(string)」1310により撮像プローブ1300に接続されている。例えば、この撮像プローブ1300(例えば、「玉(pill)」)はマイクロモータ1320を含むものであって、患者に嚥下される(図17B参照)。図14に示す代表的なマイクロモータはモータ1320として用いることができる。プローブ1300は、光ファイバーと電気接続系を含む「紐」1310によりシステムに接続できる。この「紐」1310を用いることにより、プローブ1300の位置を制御することができ、また、プローブ1300を、例えば患者の食道中に配置することができる。撮像完了後、この「紐」を用いてプローブを回収することができる。
【0037】
図18Aと図18Bは、それぞれ本発明の代表的な実施の形態のカテーテルの経口ならびに経鼻配置、例えば、上部胃―腸管撮像の概略図である。図18Bにおいて、カテーテル1410は口1400を経由して、すなわち、経口により配置できる。図18Bで、カテーテル1410は鼻孔1420を経由して、すなわち経鼻により配置することができる。経鼻設計は患者の鎮痛処置を必要としないという長所を有するが、直径を小さくするべきである。本発明の代表的な実施の形態の光ファイバー撮像コアは比較的小型であるため、経鼻配置が可能である。
【0038】
図19Aおよび図19Bは、それぞれクローズドモードおよびその遠端部分から開始するオープニング時における、本発明の代表的な実施の形態の、代表的なカテーテルのワイヤケージセンタリング構成の概略図である。例えば、管腔器官内で内側の光学コアを伸張させ、センタリングをするために、バルーンに代えてワイヤ撚り線を使用してもよい。このカテーテルは、外側被覆1510、一組の伸張可能なワイヤステント1500および内部コア1530を含むことができる。このカテーテルを配置した後、ワイヤステント1500が器官を拡張することができるように、他の被覆を縮小してもよい。撮像の後、外側被覆1510は拡張してワイヤステントを折り畳むと、カテーテルは除去できる。
【0039】
図20は、第2の波長帯をカテーテル内に多重化して第2の撮像モダリティを達成できる、本発明の代表的な実施の形態の撮像システムのブロック図である。このモダリティは、例えば、可視光反射撮像または蛍光撮像であってよい。この代表的な構成において、可視光源1600は、第2の波長帯を第一の撮像波長帯、例えば、代表的には赤外と結合させる波長分割マルチプレクサ1630経由で、(一例として、図3に示されたような)撮像用カテーテルへ結合することができる。サンプルからの反射された可視光は、この波長分割マルチプレクサ1630により一次撮像波長帯から分離されて、スプリッタ1610により光レシーバ1620へ誘導される。
【0040】
上皮管腔器官撮像システムにとって有利な更なる機能性として、撮像データセットで同定された関心領域を直接に続けて精密に検査することができる点にある。例えば、食道領域内に異形成部分を検出した場合、その診断を確かめるために直接内視鏡によってその部分の組織生検を要望する場合がある。方法及びシステムを用いて画像データセットで同定した関心部位の組織に可視マークを付すことができる。さらに、図21に、アブレーション用レーザ1700を光ファイバー波長分割マルチプレクサ1710を介して撮像用カテーテルに結合してこれを実現する、本発明の他の代表的な実施の形態の構成のブロック図を示す。アブレーション用レーザ1700は、管腔器官上に表面変異を生じるに十分な光学パワーと波長を有するように構成することができる。これらの変異は内視鏡検査で見ることができ、さらなる検査、例えば生体検査用のマーカとして使用してよい。図21に示すように、このカテーテルはマーキングを付すべき領域に向けて固定できる。次いで、可視の変異を生じるに十分な時間このアブレーション用レーザを作動する。
【0041】
図22に、カテーテルスキャナーを停止せずアブレーションを動的(オンザフライ)に行なう、本発明の代替の代表的な実施の形態の構成を示す。データ収集ユニット1720は、カテーテルが関心領域を指差す場合に光学シャッター1730を開くようにプログラムされている。この光学シャッター1730は、開いているときにはアブレーション光を伝達し、閉じているときには遮断する。例えば、このカテーテルは動作し続けることができる。
【0042】
図23Aに、関心領域にオンザフライアブレーションを行なうための、本発明の代表的な実施の形態のアブレーションマーキング用処理のフロー図を示す。特に、ステップ1810において、アブレーションを行うポイント(溶発点)を特定する。ステップ1820において、シャッターがこのポイントで開くように設定する。ステップ1830において、このシャッターおよびアブレーションレーザを作動可能とし、次いでステップ1840でシャッターおよび/又はアブレーションレーザを作動不能とする。
【0043】
図23Bに、関心領域で停止およびアブレーション実施を行う、本発明の代表的な実施の形態のアブレーションマーキング処理のフロー図を示す。特に、ステップ1850においてアブレーションを行うべきポイント(溶発点)を特定する。ステップ1860において、カテーテルがそのポイントで停止するように命令する。ステップ1870において、シャッターおよび/またはアブレーションレーザを作動可能とし、ステップ1880において、これらのシャッターおよび/またはアブレーションレーザを作動不能とする。カテーテルはステップ1890において再び回転を開始する。
【0044】
図24に、関心領域のアブレーションマーキングを含む(本発明の代表的な実施の形態を用いて生成した)代表的な画像を示す。一例として、波長が1440nmから1480nmおよび光学パワーが約1秒間にわたり約300mWである一連のレーザを用いて食道に形成されたアブレーションマーク1900を例示する。
【0045】
図25Aおよび図25Bに、代表的な構成の多重アブレーション用レーザと光学スイッチ(シャッター)とを組み合わせることができる、本発明の代表的な実施の形態の構成と本発明の代表的な実施方法の実施の相互関連のフロー図およびブロック図を示す。図25Aにおいて、多重化レーザ2000、2010および2020は、マルチプレクサ(MUX)2030を用いて結合することができる。このマルチプレクサ2030は、波長分割マルチプレクサ、偏光マルチプレクサ、および/または両者の結合型であってもよく、これらのあとに単一のシャッター2040が続く。図25Bにおいて、各レーザ2000、2010、2020は独立したシャッター2050、2060、2070を用いており、これらのシャッターは次いでMUX2080を用いて結合される。
【0046】
図26に、管腔器官の検査および後続の関心領域のマーキングを行う、代表的な実施の形態の方法のブロック図を表す。ステップ2100において、管腔領域全体を画像化する。次いで、ステップ2110において、関心領域を自動アルゴリズムまたはオペレータの点検により識別する。ステップ2120において、カテーテルを第1の関心領域の部位へ導く。またステップ2130において、必要に応じて撮像を開始し、関心領域を再探索してカテーテル位置をインターラクティブに調節する。この再探索手順で、例えば食道の蠕動によるカテーテルの位置ずれを補正することができる。次いで、ステップ2140において、一つあるいは一連のアブレーションマークを関心領域の隣接領域あるいは周辺に形成することができる。この手順は各関心領域に対して繰り返し行う(ステップ2150、2130、2140等)。次いでステップ2160においてカテーテルを除去し、ステップ2170で更なる検査即ち生検をこれらのマークが付された領域に対して行なう。
【0047】
図27に、ガイドワイヤの内視鏡配置を用いた撮像用カテーテルの配置の本発明の代表的な実施の形態の手順を示す。特に、ステップ2200により、ガイドワイヤを内視鏡経路を通して挿入する。次いでステップ2210においてガイドワイヤを残してこの内視鏡を除去する。ステップ2220において、本発明のさまざまな代表的な実施の形態を参照して説明したように、カテーテルをガイドワイヤを覆うように配置する。次いで、ステップ2230において、このガイドワイヤを除去する。さらに、ステップ2240において、バルーンを膨張させ、次いでステップ2250で撮像を開始する。
【0048】
図28A〜図28Cに、バルーンの複数配置によりバルーン長よりも大きな領域の撮像を実施する、本発明の代表的な構成を用いた代表的な動作ステップを表す。図28A〜図28Cに示す位置のバルーンで取得された撮像情報は、組み合わせて広い範囲にわたる撮像画像を生成することができる。
【0049】
図29に、管状の食道と胃との間の接合部に撮像プローブを配置する代表的な実施の形態の方法を示す。図30A〜図30Cに、図29の方法を用いた本発明の代表的な構成により実行される代表的なステップを示す。ステップ2400において、バルーンは収縮した状態で挿入され胃に配置される。ステップ2410において、バルーンを膨張させ(図30A)、ステップ2420で抵抗を感じるまで引き戻す。これにより、バルーンの近端側が胃食道接合部(胃と食道との間の接合部)に配置される。次いで、ステップ2430において、バルーンを部分的に縮小させ(図30B)、カテーテルをあらかじめ定められた量、例えばバルーンの長さ分引き戻す。さらに、ステップ2440において、バルーンを膨張させ、胃食道接合部に配置されたカテーテルを用いて撮像処理を行う。
【0050】
本発明の更なる実施の形態では、カテーテルがその器官に適切に配置されているか判断するために、撮像システムを簡略モード(例えばスカウト撮像)で操作することができる。全体的な総合撮像は、カテーテルが適切に配置されていることが確認された後に開始することができる。さらに、本発明の他の代表的な実施の形態では、バルーンセンタリングカテーテルは空気以外の光学的に透明な物質、例えば、これらに限定するものではないが、水、重水(D2O)或いは油を用いて膨張させることができる。本発明のさらに他の代表的な実施の形態においては、レーザマーキングに、マーキングレーザの吸収を齎すように器官に事前投与した外因性作用物質を用いてもよい。本発明のさらなる代表的な実施の形態では、カテーテルの挿入を補助するために潤滑剤を使用することができる。本発明の他の代表的な実施の形態では、撮像品質を劣化させる可能性のある器官の粘膜を除去するために撮像に先立ち当該器官に粘膜除去剤を使用することができる。
【0051】
以上、単に本発明の原理を例示して説明した。本明細書に記載の技術を考慮して、記載の実施の形態にさまざまな修正や変更を行なうことは当業者には明かである。実際、本発明の代表的な実施の形態の装置、システム及び方法は、任意のOCTシステム、OFDIシステム、SD−OCTシステム或いはその他の撮像システムとともに用いる、および/またはこれらを実装することが可能であり、例えば、その全ての開示内容を本明細書の一部として援用する、2004年9月8日出願の国際特許出願第PCT/US2004/029148号、2005年11月2日出願の米国特許出願第11/266,779号、および2004年7月9日出願の米国特許出願第10/501,276号に記載のシステム等とともに使用することができる。従って、当業者にとっては、本明細書に明確に提示又は説明されていなくとも、本発明の原理を具現化する数多くのシステム、装置、及び方法に工夫を凝らすことが可能であり、これは本発明の趣旨と範囲内に含まれることが理解されるであろう。さらに、上述の明細書に前記の先行技術の知識が明示的に援用されていない範囲においても、その全体を明示的に本明細書に援用する。本明細書で引用した上述の全ての文献は、その全体を本明細書の一部として援用する。
【0052】
本発明のさらなる目的、機能、および長所は、詳細な説明と、例示的な本発明の実施の形態を示す以下の添付の図面から明らかになる。
【符号の説明】
【0053】
100 撮像システム
110 カテーテルスキャナー
125 内部コア
120 バルーン撮像用カテーテル
130 光学的透過性被覆
145 管腔器官
【特許請求の範囲】
【請求項1】
少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置であって、
少なくとも一つの電磁放射を前記少なくとも一つの部分に送受するように構成された光学的第1の構成部と、
前記光学的第1の構成部を少なくとも部分的に囲繞する第2の構成部と、
前記光学的第1の構成部が前記少なくとも一つの管腔又は中空サンプルの内部の所定の部位に位置するように作動するように構成された第3の構成部と、を備え、
前記光学的第1の構成部は、前記第2の構成部または前記第3の構成部の少なくとも一つによって生じる少なくとも一つの光学的収差を補正するように構成された装置。
【請求項2】
前記少なくとも一つの補正された収差は非点収差である、請求項1記載の装置。
【請求項3】
患者の口または鼻の少なくとも一つを介して挿入可能に小型化されて構成された、請求項1記載の装置。
【請求項4】
前記光学的第1の構成部は、前記少なくとも一つの収差を補正するように構成された少なくとも一つの円筒形表面を含む、請求項1記載の装置。
【請求項5】
前記光学的第1の構成部は、前記少なくとも一つの収差を補正するように構成された少なくとも一つの楕円形ボールレンズを含む、請求項1記載の装置。
【請求項6】
前記第3の構成部は、バルーンを含む、請求項1記載の装置。
【請求項7】
前記バルーンは、ガスまたは液体の少なくとも一つで充填できる、請求項6記載の装置。
【請求項8】
前記第2の構成部は、ガイド構成部を挿入することができる、少なくとも一つの部材を含む、請求項1記載の装置。
【請求項9】
前記少なくとも一つの部分の内部の圧力を測定するように構成されたさらなる構成部を備える、請求項1記載の装置。
【請求項10】
前記データは、前記光学的第1の構成部の前記少なくとも一つの管腔または中空サンプルに対する位置または方向性の少なくとも一つを含む、請求項1記載の装置。
【請求項11】
前記少なくとも一つの電磁放射は可視である、請求項1記載の装置。
【請求項12】
前記光学的第1の構成部は、前記少なくとも一つの電磁放射を前記少なくとも一つの部分に導いて、前記データを取得する部位を含む、請求項1記載の装置。
【請求項13】
嚥下することが可能に小型化されて構成された、請求項1記載の装置。
【請求項14】
前記光学的第1の構成部が、前記少なくとも一つの部分に少なくとも一つの第1の電磁放射を送受し、前記少なくとも一つの部分の熱による損傷、又は熱による損傷による構造的変化を生成するために少なくとも一つの第2の電磁放射を送信する、請求項1記載の装置。
【請求項15】
前記第2の構成部を少なくとも部分的に囲繞し、前記光学的第1の構成部の部分周辺の空間的に外側の周辺の位置まで延伸することができる、さらなる構成部を備える、請求項14記載の装置。
【請求項16】
前記データ、および前記光学的第1の構成部の前記少なくとも一つのサンプルに対する位置および回転角度を受けて記憶するように構成されたさらなる構成部を備える、請求項1記載の装置。
【請求項17】
前記さらなる構成部はスキャニング構成部を含み、前記少なくとも一つのサンプルを少なくとも一回スキャンする間に前記スキャニング構成部から取得したエンコーダ信号をデジタルにカウントして、前記位置および前記回転角度を検出する、請求項16記載の装置。
【請求項18】
前記位置および前記回転角度を受け、前記位置および前記回転角度を用いて前記少なくとも一つの部分に関連する少なくとも一つの画像を生成するように構成されたさらなる構成部を備える、請求項16記載の装置。
【請求項19】
前記さらなる構成部は、さらに、前記少なくとも一つの画像の少なくとも一つの空間歪みを補正するように構成されている、請求項18記載の装置。
【請求項20】
前記光学的第1の構成部が前記少なくとも一つのサンプルに対して少なくとも二軸並進の間、前記少なくとも一つのサンプルの複数の画像を受信するように制御可能な処理構成部をさらに備え、前記二軸並進の各々は回転角度で行われる、請求項1記載の装置。
【請求項21】
前記データは、前記少なくとも一つのサンプルに関連する干渉データである、請求項1記載の装置。
【請求項22】
前記干渉データは、スペクトル領域光コヒーレンストモグラフィーデータ、または光周波数領域画像データの少なくとも一つである、請求項21記載の装置。
【請求項23】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
前記光学的第1の構成部を少なくとも部分的に囲繞して、ガイド構成部を挿入することができる少なくとも一つの部分を含む、第2の構成部と、
データの生成を容易とするために、前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部においてセンタリングされるように作動するように構成された第3の構成部と、を備えた、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項24】
患者の口または鼻の少なくとも一つを介して挿入可能に小型化されて構成された、請求項23記載の装置。
【請求項25】
前記データ、および前記光学的第1の構成部の前記少なくとも一つのサンプルに対する位置および回転角度を受けて記憶するように構成されたさらなる構成部を備える、請求項23記載の装置。
【請求項26】
前記さらなる構成部はスキャニング構成部を含み、前記少なくとも一つのサンプルを少なくとも一回スキャンする間に前記スキャニング構成部から取得したエンコーダ信号をデジタルにカウントして、前記位置および前記回転角度を検出する、請求項25記載の装置。
【請求項27】
前記位置および前記回転角度を受け、前記位置および前記回転角度を用いて前記少なくとも一つの部分に関連する少なくとも一つの画像を生成するように構成されたさらなる構成部を備える、請求項25記載の装置。
【請求項28】
前記さらなる構成部は、さらに、前記少なくとも一つの画像の少なくとも一つの空間歪みを補正するように構成されている、請求項27記載の装置。
【請求項29】
前記光学的第1の構成部が前記少なくとも一つのサンプルに対して少なくとも二軸並進の間、前記少なくとも一つのサンプルの複数の画像を受信するように制御可能な処理構成部をさらに備え、前記二軸並進の各々は回転角度で行われる、請求項23記載の装置。
【請求項30】
前記データは、前記少なくとも一つのサンプルに関連する干渉データである、請求項23記載の装置。
【請求項31】
前記干渉データは、スペクトル領域光コヒーレンストモグラフィーデータ、時間領域光コヒーレンストモグラフィーデータまたは光周波数領域画像データの少なくとも一つである、請求項30記載の装置。
【請求項32】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
データの生成を容易とするために、前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部においてセンタリングされるように作動するように構成された、少なくとも一つの非膨張部分を含む第2の構成部と、を備えた、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項33】
患者の口または鼻の少なくとも一つを介して挿入可能に小型化されて構成された、請求項32記載の装置。
【請求項34】
前記少なくとも一つの非膨張部分は、伸張可能で折り畳み可能なバスケットである、請求項32記載の装置。
【請求項35】
前記データ、および前記光学的第1の構成部の前記少なくとも一つのサンプルに対する位置および回転角度を受けて記憶するように構成されたさらなる構成部を備える、請求項32記載の装置。
【請求項36】
前記さらなる構成部はスキャニング構成部を含み、前記少なくとも一つのサンプルを少なくとも一回スキャンする間に前記スキャニング構成部から取得したエンコーダ信号をデジタルにカウントして、前記位置および前記回転角度を検出する、請求項35記載の装置。
【請求項37】
前記位置および前記回転角度を受け、前記位置および前記回転角度を用いて前記少なくとも一つの部分に関連する少なくとも一つの画像を生成するように構成されたさらなる構成部を備える、請求項35記載の装置。
【請求項38】
前記さらなる構成部は、さらに、前記少なくとも一つの画像の少なくとも一つの空間歪みを補正するように構成されている、請求項37記載の装置。
【請求項39】
前記光学的第1の構成部が前記少なくとも一つのサンプルに対して少なくとも二軸並進の間、前記少なくとも一つのサンプルの複数の画像を受信するように制御可能な処理構成部をさらに備え、前記二軸並進の各々は回転角度で行われる、請求項32記載の装置。
【請求項40】
前記データは、前記少なくとも一つのサンプルに関連する干渉データである、請求項32記載の装置。
【請求項41】
前記干渉データは、スペクトル領域光コヒーレンストモグラフィーデータ、時間領域光コヒーレンストモグラフィーデータまたは光周波数領域画像データの少なくとも一つである、請求項40記載の装置。
【請求項42】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
前記少なくとも一つの部分の圧力を測定するように構成された第2の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの少なくとも一つの部分のデータを取得する装置。
【請求項43】
前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部の所定の部位に位置するように作動するように構成された第2の構成部をさらに備える、請求項42記載の装置。
【請求項44】
患者の口または鼻の少なくとも一つを介して挿入可能に小型化されて構成された、請求項42記載の装置。
【請求項45】
前記第2の構成部がマノメータを含む、請求項42記載の装置。
【請求項46】
前記データ、および前記光学的第1の構成部の前記少なくとも一つのサンプルに対する位置および回転角度を受けて記憶するように構成されたさらなる構成部を備える、請求項42記載の装置。
【請求項47】
前記さらなる構成部はスキャニング構成部を含み、前記少なくとも一つのサンプルを少なくとも一回スキャンする間に前記スキャニング構成部から取得したエンコーダ信号をデジタルにカウントして、前記位置および前記回転角度を検出する、請求項46記載の装置。
【請求項48】
前記位置および前記回転角度を受け、前記位置および前記回転角度を用いて前記少なくとも一つの部分に関連する少なくとも一つの画像を生成するように構成されたさらなる構成部を備える、請求項46記載の装置。
【請求項49】
前記さらなる構成部は、さらに、前記少なくとも一つの画像の少なくとも一つの空間歪みを補正するように構成されている、請求項48記載の装置。
【請求項50】
前記光学的第1の構成部が前記少なくとも一つのサンプルに対して少なくとも二軸並進の間、前記少なくとも一つのサンプルの複数の画像を受信するように制御可能な処理構成部をさらに備え、前記二軸並進の各々は回転角度で行われる、請求項43記載の装置。
【請求項51】
前記データは、前記少なくとも一つのサンプルに関連する干渉データである、請求項43記載の装置。
【請求項52】
前記干渉データは、スペクトル領域光コヒーレンストモグラフィーデータ、時間領域光コヒーレンストモグラフィーデータまたは光周波数領域画像データの少なくとも一つである、請求項51記載の装置。
【請求項53】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
データの生成を容易とするために、前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部においてセンタリングされるように作動するように構成された第2の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置であって、
前記データは、前記光学的第1の構成部の前記少なくとも一つの管腔または中空サンプルに対する位置または方向性の少なくとも一つを含む、装置。
【請求項54】
患者の口または鼻の少なくとも一つを介して挿入可能に小型化されて構成された、請求項53記載の装置。
【請求項55】
少なくとも一つの部分に少なくとも一つの可視の電磁放射を送受するように構成された光学的第1の構成部と、
前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部の所定の部位に位置するように作動するように構成された第2の構成部と、を備え、
前記第2の構成部は、バルーンを有し、
前記光学的第1の構成部は、前記バルーンを通して少なくとも一つの電磁放射を送受する、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項56】
少なくとも一つの部分に少なくとも一つの第1の電磁放射を送受し、前記少なくとも一つの部分の構造的変化を生成するために少なくとも一つの第2の電磁放射を送信する光学的第1の構成部と、
前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部においてセンタリングされるように作動するように構成された第2の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項57】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
少なくとも玉(pill)の形状を有する器具の一部であり、前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部の所定の部位に位置するように作動するように構成された第2の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項58】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
器具の外表面の少なくとも一部が玉(pill)の形状を有し、少なくとも一つの管腔又は中空サンプルからの少なくとも一つの戻り放射を光コヒーレンストモグラフィーシステムに伝送するように構成された第2の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項59】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成され、前記少なくとも一つの電磁放射を前記少なくとも一つの部分に導き、データを取得する部位を含む、光学的第1の構成部と、
前記光学的第1の構成部を少なくとも部分的に囲繞する第2の構成部と、
前記第2の構成部を少なくとも部分的に囲繞し、前記光学的第1の構成部の前記部位の周辺の空間的に外側の位置まで延伸することができる、第3の構成部と、
前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部においてセンタリングされるように作動するように構成された第4の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項60】
第4の構成部が、前記第2の構成部および前記第3の構成部の間を延伸する経路(channel)を介して膨張するように構成されたバルーンを含む、請求項11記載の装置。
【請求項61】
少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置であって、該装置は、
前記少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成され、前記少なくとも一つの電磁放射を前記少なくとも一つの部分に導き、前記データを取得する部位を含む光学構成部と、
前記光学構成部の前記部位の長手方向の並進を制御する作動構成部と、を備え、
前記作動構成部は、前記部位の近傍に配設され、前記少なくとも一つの管腔または中空サンプルの内部または近傍に位置する、装置。
【請求項62】
さらに、前記光学構成部を少なくとも部分的に囲繞する第2の構成部と、
前記光学構成部を前記少なくとも一つの管腔又は中空サンプルの内部の所定の部位に配置するように作動するように構成された第3の構成部と、を備える、請求項61記載の装置。
【請求項63】
前記少なくとも一つの部分の方向に向けられた前記少なくとも一つの電磁放射の、前記少なくとも一つの部分に対する回転角度または位置の少なくとも一つを決定するように構成された少なくとも一つの第4の構成部をさらに備える、請求項62記載の装置。
【請求項64】
前記作動構成部がモータである、請求項62記載の装置。
【請求項65】
前記少なくとも一つの部分は、生体組織の一部である、請求項42に記載の装置。
【請求項1】
少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置であって、
少なくとも一つの電磁放射を前記少なくとも一つの部分に送受するように構成された光学的第1の構成部と、
前記光学的第1の構成部を少なくとも部分的に囲繞する第2の構成部と、
前記光学的第1の構成部が前記少なくとも一つの管腔又は中空サンプルの内部の所定の部位に位置するように作動するように構成された第3の構成部と、を備え、
前記光学的第1の構成部は、前記第2の構成部または前記第3の構成部の少なくとも一つによって生じる少なくとも一つの光学的収差を補正するように構成された装置。
【請求項2】
前記少なくとも一つの補正された収差は非点収差である、請求項1記載の装置。
【請求項3】
患者の口または鼻の少なくとも一つを介して挿入可能に小型化されて構成された、請求項1記載の装置。
【請求項4】
前記光学的第1の構成部は、前記少なくとも一つの収差を補正するように構成された少なくとも一つの円筒形表面を含む、請求項1記載の装置。
【請求項5】
前記光学的第1の構成部は、前記少なくとも一つの収差を補正するように構成された少なくとも一つの楕円形ボールレンズを含む、請求項1記載の装置。
【請求項6】
前記第3の構成部は、バルーンを含む、請求項1記載の装置。
【請求項7】
前記バルーンは、ガスまたは液体の少なくとも一つで充填できる、請求項6記載の装置。
【請求項8】
前記第2の構成部は、ガイド構成部を挿入することができる、少なくとも一つの部材を含む、請求項1記載の装置。
【請求項9】
前記少なくとも一つの部分の内部の圧力を測定するように構成されたさらなる構成部を備える、請求項1記載の装置。
【請求項10】
前記データは、前記光学的第1の構成部の前記少なくとも一つの管腔または中空サンプルに対する位置または方向性の少なくとも一つを含む、請求項1記載の装置。
【請求項11】
前記少なくとも一つの電磁放射は可視である、請求項1記載の装置。
【請求項12】
前記光学的第1の構成部は、前記少なくとも一つの電磁放射を前記少なくとも一つの部分に導いて、前記データを取得する部位を含む、請求項1記載の装置。
【請求項13】
嚥下することが可能に小型化されて構成された、請求項1記載の装置。
【請求項14】
前記光学的第1の構成部が、前記少なくとも一つの部分に少なくとも一つの第1の電磁放射を送受し、前記少なくとも一つの部分の熱による損傷、又は熱による損傷による構造的変化を生成するために少なくとも一つの第2の電磁放射を送信する、請求項1記載の装置。
【請求項15】
前記第2の構成部を少なくとも部分的に囲繞し、前記光学的第1の構成部の部分周辺の空間的に外側の周辺の位置まで延伸することができる、さらなる構成部を備える、請求項14記載の装置。
【請求項16】
前記データ、および前記光学的第1の構成部の前記少なくとも一つのサンプルに対する位置および回転角度を受けて記憶するように構成されたさらなる構成部を備える、請求項1記載の装置。
【請求項17】
前記さらなる構成部はスキャニング構成部を含み、前記少なくとも一つのサンプルを少なくとも一回スキャンする間に前記スキャニング構成部から取得したエンコーダ信号をデジタルにカウントして、前記位置および前記回転角度を検出する、請求項16記載の装置。
【請求項18】
前記位置および前記回転角度を受け、前記位置および前記回転角度を用いて前記少なくとも一つの部分に関連する少なくとも一つの画像を生成するように構成されたさらなる構成部を備える、請求項16記載の装置。
【請求項19】
前記さらなる構成部は、さらに、前記少なくとも一つの画像の少なくとも一つの空間歪みを補正するように構成されている、請求項18記載の装置。
【請求項20】
前記光学的第1の構成部が前記少なくとも一つのサンプルに対して少なくとも二軸並進の間、前記少なくとも一つのサンプルの複数の画像を受信するように制御可能な処理構成部をさらに備え、前記二軸並進の各々は回転角度で行われる、請求項1記載の装置。
【請求項21】
前記データは、前記少なくとも一つのサンプルに関連する干渉データである、請求項1記載の装置。
【請求項22】
前記干渉データは、スペクトル領域光コヒーレンストモグラフィーデータ、または光周波数領域画像データの少なくとも一つである、請求項21記載の装置。
【請求項23】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
前記光学的第1の構成部を少なくとも部分的に囲繞して、ガイド構成部を挿入することができる少なくとも一つの部分を含む、第2の構成部と、
データの生成を容易とするために、前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部においてセンタリングされるように作動するように構成された第3の構成部と、を備えた、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項24】
患者の口または鼻の少なくとも一つを介して挿入可能に小型化されて構成された、請求項23記載の装置。
【請求項25】
前記データ、および前記光学的第1の構成部の前記少なくとも一つのサンプルに対する位置および回転角度を受けて記憶するように構成されたさらなる構成部を備える、請求項23記載の装置。
【請求項26】
前記さらなる構成部はスキャニング構成部を含み、前記少なくとも一つのサンプルを少なくとも一回スキャンする間に前記スキャニング構成部から取得したエンコーダ信号をデジタルにカウントして、前記位置および前記回転角度を検出する、請求項25記載の装置。
【請求項27】
前記位置および前記回転角度を受け、前記位置および前記回転角度を用いて前記少なくとも一つの部分に関連する少なくとも一つの画像を生成するように構成されたさらなる構成部を備える、請求項25記載の装置。
【請求項28】
前記さらなる構成部は、さらに、前記少なくとも一つの画像の少なくとも一つの空間歪みを補正するように構成されている、請求項27記載の装置。
【請求項29】
前記光学的第1の構成部が前記少なくとも一つのサンプルに対して少なくとも二軸並進の間、前記少なくとも一つのサンプルの複数の画像を受信するように制御可能な処理構成部をさらに備え、前記二軸並進の各々は回転角度で行われる、請求項23記載の装置。
【請求項30】
前記データは、前記少なくとも一つのサンプルに関連する干渉データである、請求項23記載の装置。
【請求項31】
前記干渉データは、スペクトル領域光コヒーレンストモグラフィーデータ、時間領域光コヒーレンストモグラフィーデータまたは光周波数領域画像データの少なくとも一つである、請求項30記載の装置。
【請求項32】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
データの生成を容易とするために、前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部においてセンタリングされるように作動するように構成された、少なくとも一つの非膨張部分を含む第2の構成部と、を備えた、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項33】
患者の口または鼻の少なくとも一つを介して挿入可能に小型化されて構成された、請求項32記載の装置。
【請求項34】
前記少なくとも一つの非膨張部分は、伸張可能で折り畳み可能なバスケットである、請求項32記載の装置。
【請求項35】
前記データ、および前記光学的第1の構成部の前記少なくとも一つのサンプルに対する位置および回転角度を受けて記憶するように構成されたさらなる構成部を備える、請求項32記載の装置。
【請求項36】
前記さらなる構成部はスキャニング構成部を含み、前記少なくとも一つのサンプルを少なくとも一回スキャンする間に前記スキャニング構成部から取得したエンコーダ信号をデジタルにカウントして、前記位置および前記回転角度を検出する、請求項35記載の装置。
【請求項37】
前記位置および前記回転角度を受け、前記位置および前記回転角度を用いて前記少なくとも一つの部分に関連する少なくとも一つの画像を生成するように構成されたさらなる構成部を備える、請求項35記載の装置。
【請求項38】
前記さらなる構成部は、さらに、前記少なくとも一つの画像の少なくとも一つの空間歪みを補正するように構成されている、請求項37記載の装置。
【請求項39】
前記光学的第1の構成部が前記少なくとも一つのサンプルに対して少なくとも二軸並進の間、前記少なくとも一つのサンプルの複数の画像を受信するように制御可能な処理構成部をさらに備え、前記二軸並進の各々は回転角度で行われる、請求項32記載の装置。
【請求項40】
前記データは、前記少なくとも一つのサンプルに関連する干渉データである、請求項32記載の装置。
【請求項41】
前記干渉データは、スペクトル領域光コヒーレンストモグラフィーデータ、時間領域光コヒーレンストモグラフィーデータまたは光周波数領域画像データの少なくとも一つである、請求項40記載の装置。
【請求項42】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
前記少なくとも一つの部分の圧力を測定するように構成された第2の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの少なくとも一つの部分のデータを取得する装置。
【請求項43】
前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部の所定の部位に位置するように作動するように構成された第2の構成部をさらに備える、請求項42記載の装置。
【請求項44】
患者の口または鼻の少なくとも一つを介して挿入可能に小型化されて構成された、請求項42記載の装置。
【請求項45】
前記第2の構成部がマノメータを含む、請求項42記載の装置。
【請求項46】
前記データ、および前記光学的第1の構成部の前記少なくとも一つのサンプルに対する位置および回転角度を受けて記憶するように構成されたさらなる構成部を備える、請求項42記載の装置。
【請求項47】
前記さらなる構成部はスキャニング構成部を含み、前記少なくとも一つのサンプルを少なくとも一回スキャンする間に前記スキャニング構成部から取得したエンコーダ信号をデジタルにカウントして、前記位置および前記回転角度を検出する、請求項46記載の装置。
【請求項48】
前記位置および前記回転角度を受け、前記位置および前記回転角度を用いて前記少なくとも一つの部分に関連する少なくとも一つの画像を生成するように構成されたさらなる構成部を備える、請求項46記載の装置。
【請求項49】
前記さらなる構成部は、さらに、前記少なくとも一つの画像の少なくとも一つの空間歪みを補正するように構成されている、請求項48記載の装置。
【請求項50】
前記光学的第1の構成部が前記少なくとも一つのサンプルに対して少なくとも二軸並進の間、前記少なくとも一つのサンプルの複数の画像を受信するように制御可能な処理構成部をさらに備え、前記二軸並進の各々は回転角度で行われる、請求項43記載の装置。
【請求項51】
前記データは、前記少なくとも一つのサンプルに関連する干渉データである、請求項43記載の装置。
【請求項52】
前記干渉データは、スペクトル領域光コヒーレンストモグラフィーデータ、時間領域光コヒーレンストモグラフィーデータまたは光周波数領域画像データの少なくとも一つである、請求項51記載の装置。
【請求項53】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
データの生成を容易とするために、前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部においてセンタリングされるように作動するように構成された第2の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置であって、
前記データは、前記光学的第1の構成部の前記少なくとも一つの管腔または中空サンプルに対する位置または方向性の少なくとも一つを含む、装置。
【請求項54】
患者の口または鼻の少なくとも一つを介して挿入可能に小型化されて構成された、請求項53記載の装置。
【請求項55】
少なくとも一つの部分に少なくとも一つの可視の電磁放射を送受するように構成された光学的第1の構成部と、
前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部の所定の部位に位置するように作動するように構成された第2の構成部と、を備え、
前記第2の構成部は、バルーンを有し、
前記光学的第1の構成部は、前記バルーンを通して少なくとも一つの電磁放射を送受する、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項56】
少なくとも一つの部分に少なくとも一つの第1の電磁放射を送受し、前記少なくとも一つの部分の構造的変化を生成するために少なくとも一つの第2の電磁放射を送信する光学的第1の構成部と、
前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部においてセンタリングされるように作動するように構成された第2の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項57】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
少なくとも玉(pill)の形状を有する器具の一部であり、前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部の所定の部位に位置するように作動するように構成された第2の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項58】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成された光学的第1の構成部と、
器具の外表面の少なくとも一部が玉(pill)の形状を有し、少なくとも一つの管腔又は中空サンプルからの少なくとも一つの戻り放射を光コヒーレンストモグラフィーシステムに伝送するように構成された第2の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項59】
少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成され、前記少なくとも一つの電磁放射を前記少なくとも一つの部分に導き、データを取得する部位を含む、光学的第1の構成部と、
前記光学的第1の構成部を少なくとも部分的に囲繞する第2の構成部と、
前記第2の構成部を少なくとも部分的に囲繞し、前記光学的第1の構成部の前記部位の周辺の空間的に外側の位置まで延伸することができる、第3の構成部と、
前記光学的第1の構成部が少なくとも一つの管腔又は中空サンプルの内部においてセンタリングされるように作動するように構成された第4の構成部と、を備える、少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置。
【請求項60】
第4の構成部が、前記第2の構成部および前記第3の構成部の間を延伸する経路(channel)を介して膨張するように構成されたバルーンを含む、請求項11記載の装置。
【請求項61】
少なくとも一つの管腔又は中空サンプルの内部の少なくとも一つの部分のデータを取得する装置であって、該装置は、
前記少なくとも一つの部分に少なくとも一つの電磁放射を送受するように構成され、前記少なくとも一つの電磁放射を前記少なくとも一つの部分に導き、前記データを取得する部位を含む光学構成部と、
前記光学構成部の前記部位の長手方向の並進を制御する作動構成部と、を備え、
前記作動構成部は、前記部位の近傍に配設され、前記少なくとも一つの管腔または中空サンプルの内部または近傍に位置する、装置。
【請求項62】
さらに、前記光学構成部を少なくとも部分的に囲繞する第2の構成部と、
前記光学構成部を前記少なくとも一つの管腔又は中空サンプルの内部の所定の部位に配置するように作動するように構成された第3の構成部と、を備える、請求項61記載の装置。
【請求項63】
前記少なくとも一つの部分の方向に向けられた前記少なくとも一つの電磁放射の、前記少なくとも一つの部分に対する回転角度または位置の少なくとも一つを決定するように構成された少なくとも一つの第4の構成部をさらに備える、請求項62記載の装置。
【請求項64】
前記作動構成部がモータである、請求項62記載の装置。
【請求項65】
前記少なくとも一つの部分は、生体組織の一部である、請求項42に記載の装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7A】


【図7B】


【図8A】


【図8B】


【図8C】


【図9A】


【図9B】


【図9C】


【図9D】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16A】


【図16B】


【図17A】


【図17B】


【図17C】


【図18A】


【図18B】


【図19A】


【図19B】


【図20】


【図21】


【図22】


【図23A】


【図23B】


【図24】


【図25A】


【図25B】


【図26】


【図27】


【図28A】


【図28B】


【図28C】


【図29】


【図30A】


【図30B】


【図30C】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7A】


【図7B】


【図8A】


【図8B】


【図8C】


【図9A】


【図9B】


【図9C】


【図9D】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16A】


【図16B】


【図17A】


【図17B】


【図17C】


【図18A】


【図18B】


【図19A】


【図19B】


【図20】


【図21】


【図22】


【図23A】


【図23B】


【図24】


【図25A】


【図25B】


【図26】


【図27】


【図28A】


【図28B】


【図28C】


【図29】


【図30A】


【図30B】


【図30C】


【公開番号】特開2013−106970(P2013−106970A)
【公開日】平成25年6月6日(2013.6.6)
【国際特許分類】
【出願番号】特願2013−22740(P2013−22740)
【出願日】平成25年2月7日(2013.2.7)
【分割の表示】特願2008−551555(P2008−551555)の分割
【原出願日】平成19年1月19日(2007.1.19)
【出願人】(592017633)ザ ジェネラル ホスピタル コーポレイション (177)
【Fターム(参考)】
【公開日】平成25年6月6日(2013.6.6)
【国際特許分類】
【出願日】平成25年2月7日(2013.2.7)
【分割の表示】特願2008−551555(P2008−551555)の分割
【原出願日】平成19年1月19日(2007.1.19)
【出願人】(592017633)ザ ジェネラル ホスピタル コーポレイション (177)
【Fターム(参考)】
[ Back to top ]

