フェキソフェナジン多形体
【課題】 フェキソフェナジン塩酸塩無水I形を、簡単で直接的な方法でアセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物から調製する。
【解決手段】 結晶性フェキソフェナジン塩酸塩無水I形を調製するためのプロセスであって、a)アセトニトリルと水の混合物にアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物を分散するステップ、b)結晶性フェキソフェナジン塩酸塩無水I形をシード添加するステップ、c)反応混合物を還流するステップ、d)混合物を冷却するステップ、e)沈殿を分離して回収するステップを含むプロセス。
【解決手段】 結晶性フェキソフェナジン塩酸塩無水I形を調製するためのプロセスであって、a)アセトニトリルと水の混合物にアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物を分散するステップ、b)結晶性フェキソフェナジン塩酸塩無水I形をシード添加するステップ、c)反応混合物を還流するステップ、d)混合物を冷却するステップ、e)沈殿を分離して回収するステップを含むプロセス。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、国際公開第95/31437号パンフレットで知られているフェキソフェナジン無水塩酸塩の多形性I形を調製するためのプロセス(process)に関する。
【背景技術】
【0002】
式
【0003】
【化1】

【0004】
のフェキソフェナジン塩酸塩(4−[4−[4−(ヒドロキシジフェニルメチル)−1−ピペリジニル]−1−ヒドロキシブチル]−α,α−ジメチルベンゼン酢酸塩酸塩)は、商標Allegra(登録商標)の下に米国で販売されている抗ヒスタミンおよび抗アレルギー薬である。
【0005】
国際公開第02/066429号パンフレット(特許文献1)は、フェキソフェナジン塩酸塩の非水和多形性形(A形)を開示している。
【0006】
欧州特許第1614681号明細書(特許文献2)は、アセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物の結晶性形(C形)の形成およびA形へのその変換を含むプロセスによるそのようなA形の調製を開示している。前記方法によれば、フェキソフェナジン塩酸塩C形は、アセトニトリル中でのフェキソフェナジン塩酸塩水和物(B形)の分散液の調製と、続く、約1時間にわたって約70℃から還流温度の範囲の温度における加熱を含むプロセスにより得られる。次いで、アセトニトリル分散液は、−5℃未満の温度まで冷却される。
【0007】
次いで、得られるフェキソフェナジン塩酸塩一溶媒和物C形の沈殿は、周知の技法で単離される。次いで、無水A形を得るための前記一溶媒和物C形からのアセトニトリル溶媒の除去は、アセトニトリルを除去するのに適している任意の物理的手段で、好ましくは約18〜30時間にわたって、約80〜110℃にて真空下で加熱することにより行うことができる。
【0008】
国際公開第95/31437号パンフレット(特許文献3)は、フェキソフェナジン塩酸塩の水和物および無水形態について記載しており、とりわけ、共沸蒸留または水最少化再結晶による水和II形からの無水I形の調製を開示している。特に、前記再結晶は、無水溶媒中で水和形の溶液をまず形成し、溶液を還流下で加熱し、次いで、溶液を得るために使用されたさらなる量の同じ溶媒か第二の適当な無水逆溶媒のどちらかを加えて無水形の沈澱を開始し、次いで、反応混合物を冷却して行われる。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】国際公開第02/066429号パンフレット
【特許文献2】欧州特許第1614681号明細書
【特許文献2】国際公開第95/31437号パンフレット
【発明の概要】
【課題を解決するための手段】
【0010】
今回、フェキソフェナジン塩酸塩無水I形を、共沸蒸留、水最少化再結晶、噴霧乾燥および凍結乾燥などの操作を必要とせず、したがって、普通なら再結晶による変換プロセスにより必要とされる濾過および濾液の洗浄の操作を避けて、簡単で直接的な方法でアセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物から調製することができることが判明した。
【0011】
結晶性無水I形を、周知のXRPD(X線粉末回折)技法により特徴付けた。X線粉末回折(XRPD)スペクトルは、下記の操作条件:CuKα放射(λ=1.5418Å)、1秒間にわたって0.03°の角度ステップでの走査の下に、粉末および液体用のAPD 2000 θ/2θ自動回折計(Ital−Structures)を使用して記録した。水含有量は、カールフィッシャー技法で滴定により決定した。
【図面の簡単な説明】
【0012】
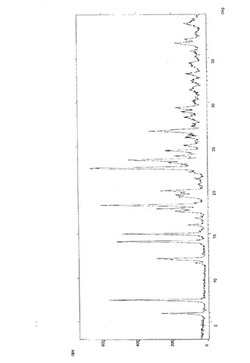
【図1】最も強い回折ピークが、5.9;7.5;12.2;14.1;15.0;17.9;18.3;22.5;23.5;および26.7゜(2θ)にあるフェキソフェナジン塩酸塩無水I形のXRPD(X線粉末回折)スペクトル。
【発明を実施するための形態】
【0013】
本発明によれば、「おおよそ一溶媒和物」とは、結晶性固体が、フェキソフェナジン塩酸塩1モル当たり溶媒約0.8〜1.2mol、好ましくは、約0.9〜1.1molのアセトニトリル溶媒の含有量を有することを意味する。
【0014】
本発明によれば、「沈澱形成」(または「沈澱」)および結晶化(または「結晶」)という表現は、区別せずに使用することができ、固体形態の取得に関する。
【0015】
第一の態様によれば、本発明は、国際公開第95/31437号パンフレットで定義されているように、結晶性フェキソフェナジン塩酸塩無水I形を調製するためのプロセスであって、
a)アセトニトリルと水の混合物にアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物を分散するステップ、
b)結晶性フェキソフェナジン塩酸塩無水I形をシード添加(seeding)するステップ、
c)反応混合物を還流するステップ、
d)混合物を冷却するステップ、
e)沈殿を分離して回収するステップ、
を含むプロセスを提供する。
【0016】
好ましくは、出発材料として使用されるアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物は、欧州特許第1614681号明細書に従って得られるC形である。
【0017】
アセトニトリル混合物中に存在する水の量は、フェキソフェナジン塩酸塩一溶媒和物の約0.5モル〜1.5モルの範囲であり、特に、フェキソフェナジン塩酸塩一溶媒和物1モル当たり水約1モルである。
【0018】
アセトニトリルと水の混合物中でのアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物の分散液の形成は、約1/8〜1/15重量/体積比の範囲、好ましくは約1/10の重量/体積比で、室温から約50℃の範囲の温度にて、特に約25〜40℃にて、前記混合物に前記化合物を注ぎ入れるか前記化合物に前記混合物を注ぎ入れることにより得ることができる。
【0019】
結晶性フェキソフェナジン塩酸塩無水I形のシード添加は、反応混合物の還流を開始する前に行われることが好ましい。いかなる場合でも、シード添加は、加熱を始めた後のどの時点でも行うことができる。
【0020】
結晶性フェキソフェナジン塩酸塩無水I形を反応混合物にシード添加すると、フェキソフェナジン塩酸塩無水I形の結晶の形成および沈殿が開始する。
【0021】
反応混合物は、約1時間半〜5時間、好ましくは約3〜4時間にわたって還流温度下に保たれる。
【0022】
続く混合物の冷却は、典型的には約−20〜−5℃、好ましくは約−15〜−10℃の温度にて、約15分〜8時間、好ましくは約4〜5時間にわたってゆっくりと行われ、フェキソフェナジン塩酸塩無水I形の完全な沈殿形成を得るのに十分な時間にわたってこの温度に分散液を保つことが好ましい。
【0023】
次いで、沈殿は、周知の技法、例えば濾過または溶媒のデカンテーションにより、好ましくは濾過により、分離および回収される。次いで、生成物は、約60℃以下の温度にて、好ましくは10時間にわたって約50℃にて真空下で乾燥される。
【0024】
本発明の好ましい態様によれば、アセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物(例えば、欧州特許第1614681号明細書に従って結晶性フェキソフェナジン塩酸塩水和物から得られる)は、欧州特許第1614681号明細書に開示されているように単離も回収もされないが、そのアセトニトリル中の分散液は、上に報告されているプロセスのステップb)においてそのようなものとして使用される。
【0025】
本発明は、アセトニトリル中でのフェキソフェナジン塩酸塩結晶性水和物の分散液の形成およびアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物への変換を含むプロセスによる、アセトニトリル中でのアセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物の分散液の形成をさらに含む。
【0026】
したがって、本発明は、国際公開第95/31437号パンフレットで定義されているように、結晶性フェキソフェナジン塩酸塩無水I形を調製するためのプロセスであって、
a)アセトニトリルにフェキソフェナジン塩酸塩結晶性水和物を分散し、それをアセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物に変換するステップ、
b)分散液に結晶性フェキソフェナジン塩酸塩無水I形をシード添加するステップ、
c)反応混合物を還流するステップ、
d)混合物を冷却するステップ、
e)沈殿を分離して回収するステップ、
を含むプロセスを提供する。
【0027】
出発材料として使用されるフェキソフェナジン塩酸塩結晶性水和物は、欧州特許第1614681号明細書に従って得られる結晶性一水和物B形であることが好ましい。
【0028】
アセトニトリル中でのフェキソフェナジン塩酸塩結晶性水和物の分散液の形成は、約1/8〜1/15重量/体積比の範囲、好ましくは約1/10重量/体積比で、約35〜60℃、好ましくは約40〜55℃、特に約45℃にて、温アセトニトリルに前記生成物を注ぎ入れることにより得ることができる。アセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物が得られる。
【0029】
プロセスの続くステップは、ステップb)〜e)について上に報告されているように行うことができる。
【0030】
結晶性フェキソフェナジン塩酸塩無水I形の調製は、大きな操作利点を有し、フェキソフェナジン塩酸塩水和物からすぐに出発して、すなわち同じ反応器中で行うことができる。さらに、出発フェキソフェナジンを完全に溶かすこと、濾過することおよび濾液を洗浄することなどの複雑な操作は、国際公開第95/31437号パンフレットとは違って、もはや必要とされない。
【実施例】
【0031】
下記の例は、本発明を例示している。
【0032】
例1:フェキソフェナジン塩酸塩B形の調製
4−[4−[4−(ヒドロキシジフェニルメチル)−1−ピペリジニル)−1−オキソブチル]−α,α−ジメチルベンゼン酢酸278g、水355ml、メタノール765mlおよび水酸化ナトリウムスケール22.6gを、3リットルの四つ口フラスコに入れる。得られる混合物を40℃にて加熱し、次いで、水47ml中の水素化ホウ素ナトリウム(9.8g)の溶液を加える。還元反応の終了後、アセトン40mlを加え、36%w/w塩酸でpHを2.5〜3の範囲の値に調整する。40℃に温度を保ちながら、メタノール140mlと、次いで、水450mlを加える。得られる混合物を−15℃までゆっくりと冷却し、形成した沈澱を濾過し、1/1比の水とメタノールの混合物で洗浄する。得られる生成物を、一定重量まで40℃にて真空下で乾燥する。最も強い回折ピークが、23.6;10.1;7.9;5.2;4.7および4.4゜(2θ)にある欧州特許第1614681号明細書の図1に図示されているXRPDスペクトルを有し、一水和物と定義することができるようにカール−フィッシャーによる水含有量が4.1%のフェキソフェナジン塩酸塩265gが得られる。
【0033】
例2:フェキソフェナジン塩酸塩C形の調製
アセトニトリル2650mlを、3リットルの四つ口フラスコに入れ、45℃にて加熱する。次いで、例1から得ることができるフェキソフェナジン塩酸塩水和物265gを撹拌下で入れ、懸濁液を還流し(80〜82℃)、約1時間にわたって前記条件を保つ。懸濁液を、約4時間で約−15〜−10℃まで冷却する。固体を濾過し、アセトニトリル(2×80ml)で洗浄する。湿った生成物285gが得られ、これを10時間にわたって50℃にて真空下で乾燥した後、最も強い回折ピークが、7.0;11.6;15.4;17.3;18.0および20.5゜(2θ)にある欧州特許第1614681号明細書の図3に図示されているXRPDスペクトルを有し、カール−フィッシャーによる水含有量が0.25%のアセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物262gが得られる。
【0034】
例3:フェキソフェナジン塩酸塩I形の調製(アセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物から)
アセトニトリル2650ml、水13gおよび例2から得ることができるアセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物262gを、3リットルの四つ口フラスコに入れる。フェキソフェナジン塩酸塩I形100mgを加え、懸濁液を還流し(80〜82℃)、約3時間にわたって前記条件を保つ。懸濁液を、約4時間で約−15〜−10℃まで冷却する。固体を濾過し、アセトニトリル(2×80ml)で洗浄する。湿った生成物267gが得られ、これを10時間にわたって50℃にて真空下で乾燥した後、最も強い回折ピークが、5.9;7.5;12.2;14.1;15.0;17.9;18.3;22.5;23.5;および26.7゜(2θ)にある図に図示されているXRPDスペクトルを有し、カール−フィッシャーによる水含有量が0.12%のフェキソフェナジン塩酸塩I形236gが得られる。
【0035】
例4:フェキソフェナジン塩酸塩I形の調製(フェキソフェナジン水和形から)
アセトニトリル1325mlを3リットルの四つ口フラスコに入れ、45℃にて加熱する。次いで、例1から得ることができるフェキソフェナジン塩酸塩水和物133gを撹拌下で入れ、フェキソフェナジン塩酸塩I形100mgを加え、懸濁液を還流し(80〜82℃)、約3時間にわたって前記条件を保つ。懸濁液を、約4時間で約−15〜−10℃まで冷却する。固体を濾過し、アセトニトリル(2×40ml)で洗浄する。湿った生成物140gが得られ、これを10時間にわたって50℃にて真空下で乾燥した後、最も強い回折ピークが、2θで5.9;7.5;12.2;14.1;15.0;17.9;18.3;22.5;23.5;および26.7゜にある図に図示されているXRPDスペクトルを有し、カール−フィッシャーによる水含有量が0.11%のフェキソフェナジン塩酸塩I形120gが得られる。
【技術分野】
【0001】
本発明は、国際公開第95/31437号パンフレットで知られているフェキソフェナジン無水塩酸塩の多形性I形を調製するためのプロセス(process)に関する。
【背景技術】
【0002】
式
【0003】
【化1】

【0004】
のフェキソフェナジン塩酸塩(4−[4−[4−(ヒドロキシジフェニルメチル)−1−ピペリジニル]−1−ヒドロキシブチル]−α,α−ジメチルベンゼン酢酸塩酸塩)は、商標Allegra(登録商標)の下に米国で販売されている抗ヒスタミンおよび抗アレルギー薬である。
【0005】
国際公開第02/066429号パンフレット(特許文献1)は、フェキソフェナジン塩酸塩の非水和多形性形(A形)を開示している。
【0006】
欧州特許第1614681号明細書(特許文献2)は、アセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物の結晶性形(C形)の形成およびA形へのその変換を含むプロセスによるそのようなA形の調製を開示している。前記方法によれば、フェキソフェナジン塩酸塩C形は、アセトニトリル中でのフェキソフェナジン塩酸塩水和物(B形)の分散液の調製と、続く、約1時間にわたって約70℃から還流温度の範囲の温度における加熱を含むプロセスにより得られる。次いで、アセトニトリル分散液は、−5℃未満の温度まで冷却される。
【0007】
次いで、得られるフェキソフェナジン塩酸塩一溶媒和物C形の沈殿は、周知の技法で単離される。次いで、無水A形を得るための前記一溶媒和物C形からのアセトニトリル溶媒の除去は、アセトニトリルを除去するのに適している任意の物理的手段で、好ましくは約18〜30時間にわたって、約80〜110℃にて真空下で加熱することにより行うことができる。
【0008】
国際公開第95/31437号パンフレット(特許文献3)は、フェキソフェナジン塩酸塩の水和物および無水形態について記載しており、とりわけ、共沸蒸留または水最少化再結晶による水和II形からの無水I形の調製を開示している。特に、前記再結晶は、無水溶媒中で水和形の溶液をまず形成し、溶液を還流下で加熱し、次いで、溶液を得るために使用されたさらなる量の同じ溶媒か第二の適当な無水逆溶媒のどちらかを加えて無水形の沈澱を開始し、次いで、反応混合物を冷却して行われる。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】国際公開第02/066429号パンフレット
【特許文献2】欧州特許第1614681号明細書
【特許文献2】国際公開第95/31437号パンフレット
【発明の概要】
【課題を解決するための手段】
【0010】
今回、フェキソフェナジン塩酸塩無水I形を、共沸蒸留、水最少化再結晶、噴霧乾燥および凍結乾燥などの操作を必要とせず、したがって、普通なら再結晶による変換プロセスにより必要とされる濾過および濾液の洗浄の操作を避けて、簡単で直接的な方法でアセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物から調製することができることが判明した。
【0011】
結晶性無水I形を、周知のXRPD(X線粉末回折)技法により特徴付けた。X線粉末回折(XRPD)スペクトルは、下記の操作条件:CuKα放射(λ=1.5418Å)、1秒間にわたって0.03°の角度ステップでの走査の下に、粉末および液体用のAPD 2000 θ/2θ自動回折計(Ital−Structures)を使用して記録した。水含有量は、カールフィッシャー技法で滴定により決定した。
【図面の簡単な説明】
【0012】
【図1】最も強い回折ピークが、5.9;7.5;12.2;14.1;15.0;17.9;18.3;22.5;23.5;および26.7゜(2θ)にあるフェキソフェナジン塩酸塩無水I形のXRPD(X線粉末回折)スペクトル。
【発明を実施するための形態】
【0013】
本発明によれば、「おおよそ一溶媒和物」とは、結晶性固体が、フェキソフェナジン塩酸塩1モル当たり溶媒約0.8〜1.2mol、好ましくは、約0.9〜1.1molのアセトニトリル溶媒の含有量を有することを意味する。
【0014】
本発明によれば、「沈澱形成」(または「沈澱」)および結晶化(または「結晶」)という表現は、区別せずに使用することができ、固体形態の取得に関する。
【0015】
第一の態様によれば、本発明は、国際公開第95/31437号パンフレットで定義されているように、結晶性フェキソフェナジン塩酸塩無水I形を調製するためのプロセスであって、
a)アセトニトリルと水の混合物にアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物を分散するステップ、
b)結晶性フェキソフェナジン塩酸塩無水I形をシード添加(seeding)するステップ、
c)反応混合物を還流するステップ、
d)混合物を冷却するステップ、
e)沈殿を分離して回収するステップ、
を含むプロセスを提供する。
【0016】
好ましくは、出発材料として使用されるアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物は、欧州特許第1614681号明細書に従って得られるC形である。
【0017】
アセトニトリル混合物中に存在する水の量は、フェキソフェナジン塩酸塩一溶媒和物の約0.5モル〜1.5モルの範囲であり、特に、フェキソフェナジン塩酸塩一溶媒和物1モル当たり水約1モルである。
【0018】
アセトニトリルと水の混合物中でのアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物の分散液の形成は、約1/8〜1/15重量/体積比の範囲、好ましくは約1/10の重量/体積比で、室温から約50℃の範囲の温度にて、特に約25〜40℃にて、前記混合物に前記化合物を注ぎ入れるか前記化合物に前記混合物を注ぎ入れることにより得ることができる。
【0019】
結晶性フェキソフェナジン塩酸塩無水I形のシード添加は、反応混合物の還流を開始する前に行われることが好ましい。いかなる場合でも、シード添加は、加熱を始めた後のどの時点でも行うことができる。
【0020】
結晶性フェキソフェナジン塩酸塩無水I形を反応混合物にシード添加すると、フェキソフェナジン塩酸塩無水I形の結晶の形成および沈殿が開始する。
【0021】
反応混合物は、約1時間半〜5時間、好ましくは約3〜4時間にわたって還流温度下に保たれる。
【0022】
続く混合物の冷却は、典型的には約−20〜−5℃、好ましくは約−15〜−10℃の温度にて、約15分〜8時間、好ましくは約4〜5時間にわたってゆっくりと行われ、フェキソフェナジン塩酸塩無水I形の完全な沈殿形成を得るのに十分な時間にわたってこの温度に分散液を保つことが好ましい。
【0023】
次いで、沈殿は、周知の技法、例えば濾過または溶媒のデカンテーションにより、好ましくは濾過により、分離および回収される。次いで、生成物は、約60℃以下の温度にて、好ましくは10時間にわたって約50℃にて真空下で乾燥される。
【0024】
本発明の好ましい態様によれば、アセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物(例えば、欧州特許第1614681号明細書に従って結晶性フェキソフェナジン塩酸塩水和物から得られる)は、欧州特許第1614681号明細書に開示されているように単離も回収もされないが、そのアセトニトリル中の分散液は、上に報告されているプロセスのステップb)においてそのようなものとして使用される。
【0025】
本発明は、アセトニトリル中でのフェキソフェナジン塩酸塩結晶性水和物の分散液の形成およびアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物への変換を含むプロセスによる、アセトニトリル中でのアセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物の分散液の形成をさらに含む。
【0026】
したがって、本発明は、国際公開第95/31437号パンフレットで定義されているように、結晶性フェキソフェナジン塩酸塩無水I形を調製するためのプロセスであって、
a)アセトニトリルにフェキソフェナジン塩酸塩結晶性水和物を分散し、それをアセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物に変換するステップ、
b)分散液に結晶性フェキソフェナジン塩酸塩無水I形をシード添加するステップ、
c)反応混合物を還流するステップ、
d)混合物を冷却するステップ、
e)沈殿を分離して回収するステップ、
を含むプロセスを提供する。
【0027】
出発材料として使用されるフェキソフェナジン塩酸塩結晶性水和物は、欧州特許第1614681号明細書に従って得られる結晶性一水和物B形であることが好ましい。
【0028】
アセトニトリル中でのフェキソフェナジン塩酸塩結晶性水和物の分散液の形成は、約1/8〜1/15重量/体積比の範囲、好ましくは約1/10重量/体積比で、約35〜60℃、好ましくは約40〜55℃、特に約45℃にて、温アセトニトリルに前記生成物を注ぎ入れることにより得ることができる。アセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物が得られる。
【0029】
プロセスの続くステップは、ステップb)〜e)について上に報告されているように行うことができる。
【0030】
結晶性フェキソフェナジン塩酸塩無水I形の調製は、大きな操作利点を有し、フェキソフェナジン塩酸塩水和物からすぐに出発して、すなわち同じ反応器中で行うことができる。さらに、出発フェキソフェナジンを完全に溶かすこと、濾過することおよび濾液を洗浄することなどの複雑な操作は、国際公開第95/31437号パンフレットとは違って、もはや必要とされない。
【実施例】
【0031】
下記の例は、本発明を例示している。
【0032】
例1:フェキソフェナジン塩酸塩B形の調製
4−[4−[4−(ヒドロキシジフェニルメチル)−1−ピペリジニル)−1−オキソブチル]−α,α−ジメチルベンゼン酢酸278g、水355ml、メタノール765mlおよび水酸化ナトリウムスケール22.6gを、3リットルの四つ口フラスコに入れる。得られる混合物を40℃にて加熱し、次いで、水47ml中の水素化ホウ素ナトリウム(9.8g)の溶液を加える。還元反応の終了後、アセトン40mlを加え、36%w/w塩酸でpHを2.5〜3の範囲の値に調整する。40℃に温度を保ちながら、メタノール140mlと、次いで、水450mlを加える。得られる混合物を−15℃までゆっくりと冷却し、形成した沈澱を濾過し、1/1比の水とメタノールの混合物で洗浄する。得られる生成物を、一定重量まで40℃にて真空下で乾燥する。最も強い回折ピークが、23.6;10.1;7.9;5.2;4.7および4.4゜(2θ)にある欧州特許第1614681号明細書の図1に図示されているXRPDスペクトルを有し、一水和物と定義することができるようにカール−フィッシャーによる水含有量が4.1%のフェキソフェナジン塩酸塩265gが得られる。
【0033】
例2:フェキソフェナジン塩酸塩C形の調製
アセトニトリル2650mlを、3リットルの四つ口フラスコに入れ、45℃にて加熱する。次いで、例1から得ることができるフェキソフェナジン塩酸塩水和物265gを撹拌下で入れ、懸濁液を還流し(80〜82℃)、約1時間にわたって前記条件を保つ。懸濁液を、約4時間で約−15〜−10℃まで冷却する。固体を濾過し、アセトニトリル(2×80ml)で洗浄する。湿った生成物285gが得られ、これを10時間にわたって50℃にて真空下で乾燥した後、最も強い回折ピークが、7.0;11.6;15.4;17.3;18.0および20.5゜(2θ)にある欧州特許第1614681号明細書の図3に図示されているXRPDスペクトルを有し、カール−フィッシャーによる水含有量が0.25%のアセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物262gが得られる。
【0034】
例3:フェキソフェナジン塩酸塩I形の調製(アセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物から)
アセトニトリル2650ml、水13gおよび例2から得ることができるアセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物262gを、3リットルの四つ口フラスコに入れる。フェキソフェナジン塩酸塩I形100mgを加え、懸濁液を還流し(80〜82℃)、約3時間にわたって前記条件を保つ。懸濁液を、約4時間で約−15〜−10℃まで冷却する。固体を濾過し、アセトニトリル(2×80ml)で洗浄する。湿った生成物267gが得られ、これを10時間にわたって50℃にて真空下で乾燥した後、最も強い回折ピークが、5.9;7.5;12.2;14.1;15.0;17.9;18.3;22.5;23.5;および26.7゜(2θ)にある図に図示されているXRPDスペクトルを有し、カール−フィッシャーによる水含有量が0.12%のフェキソフェナジン塩酸塩I形236gが得られる。
【0035】
例4:フェキソフェナジン塩酸塩I形の調製(フェキソフェナジン水和形から)
アセトニトリル1325mlを3リットルの四つ口フラスコに入れ、45℃にて加熱する。次いで、例1から得ることができるフェキソフェナジン塩酸塩水和物133gを撹拌下で入れ、フェキソフェナジン塩酸塩I形100mgを加え、懸濁液を還流し(80〜82℃)、約3時間にわたって前記条件を保つ。懸濁液を、約4時間で約−15〜−10℃まで冷却する。固体を濾過し、アセトニトリル(2×40ml)で洗浄する。湿った生成物140gが得られ、これを10時間にわたって50℃にて真空下で乾燥した後、最も強い回折ピークが、2θで5.9;7.5;12.2;14.1;15.0;17.9;18.3;22.5;23.5;および26.7゜にある図に図示されているXRPDスペクトルを有し、カール−フィッシャーによる水含有量が0.11%のフェキソフェナジン塩酸塩I形120gが得られる。
【特許請求の範囲】
【請求項1】
最も強い回折ピークが、5.9;7.5;12.2;14.1;15.0;17.9;18.3;22.5;23.5;および26.7゜(2θ)にある結晶性フェキソフェナジン塩酸塩無水I形を調製するためのプロセスであって、
a)アセトニトリルと水の混合物にアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物を分散するステップ、
b)結晶性フェキソフェナジン塩酸塩無水I形をシード添加するステップ、
c)反応混合物を還流するステップ、
d)混合物を冷却するステップ、
e)沈殿を分離して回収するステップ
を含むプロセス。
【請求項2】
アセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物が、最も強い回折ピークが、7.0;11.6;15.4;17.3;18.0および20.5゜(2θ)にあるC形である、請求項1に記載のプロセス。
【請求項3】
アセトニトリルとの混合物中の水の量が、フェキソフェナジン塩酸塩1モル当たり約0.5モル〜1.5モルの範囲、好ましくは、アセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物1モル当たり水約1モルである、請求項1に記載のプロセス。
【請求項4】
アセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物とアセトニトリルと水の混合物の間の重量/体積比が、約1/8〜1/15、好ましくは約1/10である、請求項1に記載のプロセス。
【請求項5】
結晶性フェキソフェナジン塩酸塩無水I形のシード添加が、還流温度まで反応混合物を加熱する前に行われる、請求項1に記載のプロセス。
【請求項6】
反応混合物が、約1.5〜5時間、好ましくは約3〜4時間の範囲の時間にわたって還流される、請求項1に記載のプロセス。
【請求項7】
混合物が、好ましくは約15分〜8時間、好ましくは約4〜5時間でゆっくりと冷却される、請求項1に記載のプロセス。
【請求項8】
混合物が、約−20〜−5℃、好ましくは約−15〜−10℃の温度にて冷却される、請求項1に記載のプロセス。
【請求項9】
アセトニトリルに水和物結晶性フェキソフェナジン塩酸塩を分散するステップおよびそれをアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物に変換するステップを含むプロセスにより、アセトニトリルと水の混合物にアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物を分散するステップをさらに含む、請求項1に記載のプロセス。
【請求項10】
アセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物が、7.0;11.6;15.4;17.3;18.0および20.5゜(2θ)にある最も強い回折ピークを有するC形であり、水和物結晶性フェキソフェナジン塩酸塩が、2θで23.6;10.1;7.9;5.2;4.7および4.4゜にある最も強い回折ピークを有するB形である、請求項9に記載のプロセス。
【請求項11】
最も強い回折ピークが、5.9;7.5;12.2;14.1;15.0;17.9;18.3;22.5;23.5;および26.7゜(2θ)にある無水結晶性フェキソフェナジン塩酸塩I形を調製するためのプロセスであって、
a)アセトニトリル中の水和物結晶性フェキソフェナジン塩酸塩の分散液を提供するステップおよびそのアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物への変換、
b)結晶性フェキソフェナジン塩酸塩無水I形をシード添加するステップ、
c)反応混合物を還流するステップ、
d)混合物を冷却するステップ、
e)沈殿を分離して回収するステップを含むプロセス。
【請求項12】
アセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物が、7.0;11.6;15.4;17.3;18.0および20.5゜(2θ)にある最も強い回折ピークを有するC形であり、水和物結晶性フェキソフェナジン塩酸塩が、23.6;10.1;7.9;5.2;4.7および4.4(2θ)にある最も強い回折ピークを有するB形である、請求項11に記載のプロセス。
【請求項1】
最も強い回折ピークが、5.9;7.5;12.2;14.1;15.0;17.9;18.3;22.5;23.5;および26.7゜(2θ)にある結晶性フェキソフェナジン塩酸塩無水I形を調製するためのプロセスであって、
a)アセトニトリルと水の混合物にアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物を分散するステップ、
b)結晶性フェキソフェナジン塩酸塩無水I形をシード添加するステップ、
c)反応混合物を還流するステップ、
d)混合物を冷却するステップ、
e)沈殿を分離して回収するステップ
を含むプロセス。
【請求項2】
アセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物が、最も強い回折ピークが、7.0;11.6;15.4;17.3;18.0および20.5゜(2θ)にあるC形である、請求項1に記載のプロセス。
【請求項3】
アセトニトリルとの混合物中の水の量が、フェキソフェナジン塩酸塩1モル当たり約0.5モル〜1.5モルの範囲、好ましくは、アセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物1モル当たり水約1モルである、請求項1に記載のプロセス。
【請求項4】
アセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物とアセトニトリルと水の混合物の間の重量/体積比が、約1/8〜1/15、好ましくは約1/10である、請求項1に記載のプロセス。
【請求項5】
結晶性フェキソフェナジン塩酸塩無水I形のシード添加が、還流温度まで反応混合物を加熱する前に行われる、請求項1に記載のプロセス。
【請求項6】
反応混合物が、約1.5〜5時間、好ましくは約3〜4時間の範囲の時間にわたって還流される、請求項1に記載のプロセス。
【請求項7】
混合物が、好ましくは約15分〜8時間、好ましくは約4〜5時間でゆっくりと冷却される、請求項1に記載のプロセス。
【請求項8】
混合物が、約−20〜−5℃、好ましくは約−15〜−10℃の温度にて冷却される、請求項1に記載のプロセス。
【請求項9】
アセトニトリルに水和物結晶性フェキソフェナジン塩酸塩を分散するステップおよびそれをアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物に変換するステップを含むプロセスにより、アセトニトリルと水の混合物にアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物を分散するステップをさらに含む、請求項1に記載のプロセス。
【請求項10】
アセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物が、7.0;11.6;15.4;17.3;18.0および20.5゜(2θ)にある最も強い回折ピークを有するC形であり、水和物結晶性フェキソフェナジン塩酸塩が、2θで23.6;10.1;7.9;5.2;4.7および4.4゜にある最も強い回折ピークを有するB形である、請求項9に記載のプロセス。
【請求項11】
最も強い回折ピークが、5.9;7.5;12.2;14.1;15.0;17.9;18.3;22.5;23.5;および26.7゜(2θ)にある無水結晶性フェキソフェナジン塩酸塩I形を調製するためのプロセスであって、
a)アセトニトリル中の水和物結晶性フェキソフェナジン塩酸塩の分散液を提供するステップおよびそのアセトニトリルとの結晶性フェキソフェナジン塩酸塩一溶媒和物への変換、
b)結晶性フェキソフェナジン塩酸塩無水I形をシード添加するステップ、
c)反応混合物を還流するステップ、
d)混合物を冷却するステップ、
e)沈殿を分離して回収するステップを含むプロセス。
【請求項12】
アセトニトリルとのフェキソフェナジン塩酸塩一溶媒和物が、7.0;11.6;15.4;17.3;18.0および20.5゜(2θ)にある最も強い回折ピークを有するC形であり、水和物結晶性フェキソフェナジン塩酸塩が、23.6;10.1;7.9;5.2;4.7および4.4(2θ)にある最も強い回折ピークを有するB形である、請求項11に記載のプロセス。
【図1】




【公開番号】特開2012−1544(P2012−1544A)
【公開日】平成24年1月5日(2012.1.5)
【国際特許分類】
【出願番号】特願2011−132282(P2011−132282)
【出願日】平成23年6月14日(2011.6.14)
【出願人】(507161569)ディフアルマ フランチス ソシエタ ア レスポンサビリタ リミタータ (11)
【氏名又は名称原語表記】DIPHARMA FRANCIS S.R.L.
【Fターム(参考)】
【公開日】平成24年1月5日(2012.1.5)
【国際特許分類】
【出願日】平成23年6月14日(2011.6.14)
【出願人】(507161569)ディフアルマ フランチス ソシエタ ア レスポンサビリタ リミタータ (11)
【氏名又は名称原語表記】DIPHARMA FRANCIS S.R.L.
【Fターム(参考)】
[ Back to top ]

