フコシル化程度の変更により改良されたエフェクター機能を示すFc領域含有ポリペプチドおよびその使用法
本発明は、フコシル化程度の変更により改良されたエフェクター機能を示すFc領域含有ポリペプチド、ならびに癌および他の疾患を治療または予防するためにこのようなポリペプチドを使用する方法に関する。本発明のFc領域含有ポリペプチドは、好ましくは、Fc領域が野生型Fc領域の対応するアミノ酸配列に対して少なくとも1つのアミノ酸置換を含み、かつ、翻訳後フコシル化を減衰させ、活性化型Fc受容体との結合の改良および阻害型Fc受容体との結合の低減を媒介するのに十分な免疫グロブリン(例えば、抗体)である。本発明の方法は、FcγRにより媒介されるエフェクター細胞機能の効力の増強が望まれる(例えば、癌、感染性疾患)かまたはFcγRにより媒介されるエフェクター細胞応答の阻害が望まれる(例えば、炎症、自己免疫疾患)疾患、障害または感染に関連する1以上の症状の予防、治療または改善に特に有用である。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
ヒトIgG Fc領域の翻訳後フコシル化を減衰させる方法であって、前記Fc領域をL234位、L235位、F243位、R292位、Y300位、V305位またはP396位にアミノ酸置換を含むように改変すること、および前記Fc領域を正常なグリコシル化を媒介することができる宿主細胞において発現させることを含む、方法。
【請求項2】
前記Fc領域がF243、R292、Y300またはP396位にアミノ酸置換を含む、請求項1に記載の方法。
【請求項3】
(a)前記F243位での置換がF243C、F243LまたはF243Rであり;
(b)前記R292位での置換がR292G、R292L、R292M、R292P、R292SまたはR292Yであり;
(c)前記Y300位での置換がY300Lであり;
(d)前記P396位での置換がP396Lである、
請求項2に記載の方法。
【請求項4】
前記Fc領域が、CD16A受容体、CD16B受容体またはCD32A受容体に対する変更された親和性を示す、請求項1に記載の方法。
【請求項5】
前記Fc領域が、CD32B受容体に対する低下した親和性を示す、請求項4に記載の方法。
【請求項6】
前記Fc領域が、CD16A受容体に対する増大した親和性を示す、請求項4に記載の方法。
【請求項7】
前記Fc領域がモノクローナル抗体、キメラ抗体、ヒト化抗体、ヒト抗体、または重鎖および軽鎖を含む一本鎖抗体のFc領域である、請求項1に記載の方法。
【請求項8】
前記抗体がCD16A、CD32B、HER2/neu、A33、CD5、CD11c、CD19、CD20、CD22、CD23、CD27、CD40、CD45、CD79a、CD79b、CD103、CTLA4、ErbB1、ErbB3、ErbB4、VEGF受容体、TNF−α受容体、TNF−β受容体またはTNF−γ受容体CD16Aと特異的に結合する、請求項7に記載の方法。
【請求項9】
前記抗体が癌抗原と特異的に結合する、請求項7に記載の方法。
【請求項10】
前記癌が乳癌、卵巣癌、前立腺癌、子宮頸癌、肺癌または膵癌である、請求項9に記載の方法。
【請求項11】
前記癌が乳癌であり、前記抗原がHER2/neuである、請求項9に記載の方法。
【請求項12】
請求項1に記載の方法によって作出されたFc領域を含み、乳癌、卵巣癌、前立腺癌、子宮頸癌、肺癌または膵癌からなる群から選択される癌に特徴的な癌抗原と特異的に結合する抗体。
【請求項13】
変異型ヒトIgG Fc領域を含み、
(A)前記Fc領域がL234、L235、F243、R292、Y300、V305またはP396位にアミノ酸置換を含み、
(B)前記Fc領域の、高マンノース型オリゴ糖グリコシル化と複合型オリゴ糖グリコシル化との比が0.2より大きい、
ポリペプチド。
【請求項14】
前記Fc領域がF243、R292、Y300またはP396位にアミノ酸置換を含む、請求項13に記載のポリペプチド。
【請求項15】
(a)前記F243位での置換がF243C、F243LまたはF243Rであり;
(b)前記R292位での置換がR292G、R292L、R292M、R292P、R292SまたはR292Yであり;
(c)前記Y300位での置換がY300Lであり;
(d)前記P396位での置換がP396Lである、
請求項14に記載のポリペプチド。
【請求項16】
前記Fc領域が、CD16A受容体、CD16B受容体またはCD32A受容体に対する変更された親和性を示す、請求項13に記載のポリペプチド。
【請求項17】
前記Fc領域が、CD32B受容体に対する低下した親和性を示す、請求項16に記載のポリペプチド。
【請求項18】
前記Fc領域が、CD16A受容体に対する増大した親和性を示す、請求項16に記載のポリペプチド。
【請求項19】
前記Fc領域がモノクローナル抗体、キメラ抗体、ヒト化抗体、ヒト抗体、または重鎖および軽鎖を含む一本鎖抗体のFc領域である、請求項13に記載のポリペプチド。
【請求項20】
前記抗体がCD16A、CD32B、HER2/neu、A33、CD5、CD11c、CD19、CD20、CD22、CD23、CD27、CD40、CD45、CD79a、CD79b、CD103、CTLA4、ErbB1、ErbB3、ErbB4、VEGF受容体、TNF−α受容体、TNF−β受容体またはTNF−γ受容体CD16Aと特異的に結合する、請求項19に記載のポリペプチド。
【請求項21】
前記抗体が癌抗原と特異的に結合する、請求項19に記載のポリペプチド。
【請求項22】
前記癌が乳癌、卵巣癌、前立腺癌、子宮頸癌、肺癌または膵癌である、請求項21に記載のポリペプチド。
【請求項23】
前記癌が乳癌であり、前記抗原がHER2/neuである、請求項21に記載のポリペプチド。
【請求項24】
治療上有効な量の請求項20に記載のポリペプチドを患者に投与することを含む、それを必要とする対象における疾患を処置する方法。
【請求項25】
治療上有効な量の請求項21に記載のポリペプチドを患者に投与することを含む、それを必要とする対象における癌を処置する方法。
【請求項26】
前記癌が乳癌であり、前記抗原がHER−2/neuである、請求項25に記載の方法。
【請求項27】
治療上有効な量の請求項20に記載の抗体と薬学上許容される担体とを含む、医薬組成物。
【請求項28】
治療上有効な量の請求項21に記載の抗体と薬学上許容される担体とを含む、医薬組成物。
【請求項1】
ヒトIgG Fc領域の翻訳後フコシル化を減衰させる方法であって、前記Fc領域をL234位、L235位、F243位、R292位、Y300位、V305位またはP396位にアミノ酸置換を含むように改変すること、および前記Fc領域を正常なグリコシル化を媒介することができる宿主細胞において発現させることを含む、方法。
【請求項2】
前記Fc領域がF243、R292、Y300またはP396位にアミノ酸置換を含む、請求項1に記載の方法。
【請求項3】
(a)前記F243位での置換がF243C、F243LまたはF243Rであり;
(b)前記R292位での置換がR292G、R292L、R292M、R292P、R292SまたはR292Yであり;
(c)前記Y300位での置換がY300Lであり;
(d)前記P396位での置換がP396Lである、
請求項2に記載の方法。
【請求項4】
前記Fc領域が、CD16A受容体、CD16B受容体またはCD32A受容体に対する変更された親和性を示す、請求項1に記載の方法。
【請求項5】
前記Fc領域が、CD32B受容体に対する低下した親和性を示す、請求項4に記載の方法。
【請求項6】
前記Fc領域が、CD16A受容体に対する増大した親和性を示す、請求項4に記載の方法。
【請求項7】
前記Fc領域がモノクローナル抗体、キメラ抗体、ヒト化抗体、ヒト抗体、または重鎖および軽鎖を含む一本鎖抗体のFc領域である、請求項1に記載の方法。
【請求項8】
前記抗体がCD16A、CD32B、HER2/neu、A33、CD5、CD11c、CD19、CD20、CD22、CD23、CD27、CD40、CD45、CD79a、CD79b、CD103、CTLA4、ErbB1、ErbB3、ErbB4、VEGF受容体、TNF−α受容体、TNF−β受容体またはTNF−γ受容体CD16Aと特異的に結合する、請求項7に記載の方法。
【請求項9】
前記抗体が癌抗原と特異的に結合する、請求項7に記載の方法。
【請求項10】
前記癌が乳癌、卵巣癌、前立腺癌、子宮頸癌、肺癌または膵癌である、請求項9に記載の方法。
【請求項11】
前記癌が乳癌であり、前記抗原がHER2/neuである、請求項9に記載の方法。
【請求項12】
請求項1に記載の方法によって作出されたFc領域を含み、乳癌、卵巣癌、前立腺癌、子宮頸癌、肺癌または膵癌からなる群から選択される癌に特徴的な癌抗原と特異的に結合する抗体。
【請求項13】
変異型ヒトIgG Fc領域を含み、
(A)前記Fc領域がL234、L235、F243、R292、Y300、V305またはP396位にアミノ酸置換を含み、
(B)前記Fc領域の、高マンノース型オリゴ糖グリコシル化と複合型オリゴ糖グリコシル化との比が0.2より大きい、
ポリペプチド。
【請求項14】
前記Fc領域がF243、R292、Y300またはP396位にアミノ酸置換を含む、請求項13に記載のポリペプチド。
【請求項15】
(a)前記F243位での置換がF243C、F243LまたはF243Rであり;
(b)前記R292位での置換がR292G、R292L、R292M、R292P、R292SまたはR292Yであり;
(c)前記Y300位での置換がY300Lであり;
(d)前記P396位での置換がP396Lである、
請求項14に記載のポリペプチド。
【請求項16】
前記Fc領域が、CD16A受容体、CD16B受容体またはCD32A受容体に対する変更された親和性を示す、請求項13に記載のポリペプチド。
【請求項17】
前記Fc領域が、CD32B受容体に対する低下した親和性を示す、請求項16に記載のポリペプチド。
【請求項18】
前記Fc領域が、CD16A受容体に対する増大した親和性を示す、請求項16に記載のポリペプチド。
【請求項19】
前記Fc領域がモノクローナル抗体、キメラ抗体、ヒト化抗体、ヒト抗体、または重鎖および軽鎖を含む一本鎖抗体のFc領域である、請求項13に記載のポリペプチド。
【請求項20】
前記抗体がCD16A、CD32B、HER2/neu、A33、CD5、CD11c、CD19、CD20、CD22、CD23、CD27、CD40、CD45、CD79a、CD79b、CD103、CTLA4、ErbB1、ErbB3、ErbB4、VEGF受容体、TNF−α受容体、TNF−β受容体またはTNF−γ受容体CD16Aと特異的に結合する、請求項19に記載のポリペプチド。
【請求項21】
前記抗体が癌抗原と特異的に結合する、請求項19に記載のポリペプチド。
【請求項22】
前記癌が乳癌、卵巣癌、前立腺癌、子宮頸癌、肺癌または膵癌である、請求項21に記載のポリペプチド。
【請求項23】
前記癌が乳癌であり、前記抗原がHER2/neuである、請求項21に記載のポリペプチド。
【請求項24】
治療上有効な量の請求項20に記載のポリペプチドを患者に投与することを含む、それを必要とする対象における疾患を処置する方法。
【請求項25】
治療上有効な量の請求項21に記載のポリペプチドを患者に投与することを含む、それを必要とする対象における癌を処置する方法。
【請求項26】
前記癌が乳癌であり、前記抗原がHER−2/neuである、請求項25に記載の方法。
【請求項27】
治療上有効な量の請求項20に記載の抗体と薬学上許容される担体とを含む、医薬組成物。
【請求項28】
治療上有効な量の請求項21に記載の抗体と薬学上許容される担体とを含む、医薬組成物。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6A】


【図6B】


【図6C】


【図6D】


【図6E】


【図6F】


【図6G】


【図6H】


【図7】


【図8A】


【図8B】


【図8C】


【図9】


【図10】


【図11】


【図12A1】


【図12A2】


【図12B1】


【図12B2】


【図13】


【図14】


【図15A】


【図15B】


【図15C】


【図15D】


【図15E】


【図16】


【図17】


【図18】


【図19A】


【図19B】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


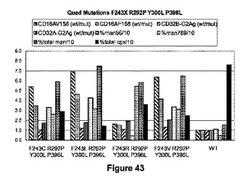
【図43】


【図44】


【図45】


【図46】


【図47】


【図48】




【図2】


【図3】


【図4】


【図5】


【図6A】


【図6B】


【図6C】


【図6D】


【図6E】


【図6F】


【図6G】


【図6H】


【図7】


【図8A】


【図8B】


【図8C】


【図9】


【図10】


【図11】


【図12A1】


【図12A2】


【図12B1】


【図12B2】


【図13】


【図14】


【図15A】


【図15B】


【図15C】


【図15D】


【図15E】


【図16】


【図17】


【図18】


【図19A】


【図19B】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【図45】


【図46】


【図47】


【図48】


【公表番号】特表2013−507128(P2013−507128A)
【公表日】平成25年3月4日(2013.3.4)
【国際特許分類】
【出願番号】特願2012−533318(P2012−533318)
【出願日】平成22年10月7日(2010.10.7)
【国際出願番号】PCT/US2010/051831
【国際公開番号】WO2011/044368
【国際公開日】平成23年4月14日(2011.4.14)
【出願人】(504438727)マクロジェニクス,インコーポレーテッド (23)
【Fターム(参考)】
【公表日】平成25年3月4日(2013.3.4)
【国際特許分類】
【出願日】平成22年10月7日(2010.10.7)
【国際出願番号】PCT/US2010/051831
【国際公開番号】WO2011/044368
【国際公開日】平成23年4月14日(2011.4.14)
【出願人】(504438727)マクロジェニクス,インコーポレーテッド (23)
【Fターム(参考)】
[ Back to top ]

